EKSTRAK AIR BUAH BELIMBING WULUH (
Averrhoa bilimbi
)
SEBAGAI REDUKTOR DALAM PEMBUATAN
NANOMAGNETIT
IIS ISMAWATI
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM INSTITUT PERTANIAN BOGOR
PERNYATAAN MENGENAI SKRIPSI DAN
SUMBER INFORMASI SERTA PELIMPAHAN HAK CIPTA
Dengan ini saya menyatakan bahwa skripsi berjudul Ekstrak Air Buah Belimbing Wuluh (Averrhoa bilimbi) sebagai Reduktor dalam Pembuatan Nanomagnetit adalah benar karya saya dengan arahan dari komisi pembimbing dan belum diajukan dalam bentuk apa pun kepada perguruan tinggi mana pun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir skripsi ini.
Dengan ini saya melimpahkan hak cipta dari karya tulis saya kepada Institut Pertanian Bogor.
ABSTRAK
IIS ISMAWATI. Ekstrak Air Buah Belimbing Wuluh (Averrhoa bilimbi) sebagai Reduktor dalam Pembuatan Nanomagnetit. Dibimbing oleh DEDEN SAPRUDIN dan ZULHAN ARIF.
Kandungan sitrat dalam buah belimbing wuluh (Averrhoa bilimbi) berpotensi sebagai pereduksi Fe3+ dalam sintesis nanomagnetit secara hidrotermal. Tujuan penelitian ini adalah menyintesis nanomagnetit menggunakan FeCl3, urea, dan ekstrak air dari buah secara hidrotermal. Sampel dihaluskan dengan penghancur buah sehingga diperoleh suspensi dan filtrat ekstrak air. Suspensi ekstrak air yang direaksikan dengan FeCl3 dan urea dengan metode hidrotermal pada suhu 200 oC selama 12 jam tidak menghasilkan nanomagnetit, sedangkan filtrat ekstrak yang diberi perlakuan yang sama menghasilkan nanomagnetit. Filtrat ekstrak air menghasilkan kristal nanomagnetit yang berukuran 27.06 nm lebih kecil daripada kristal sintesis menggunakan natrium sitrat sebagai pereduksi. Nanomagnetit hasil sintesis mengandung kobalt sebesar 7 ppm dengan cairan hasil sintesis mengandung amonium sebesar 52% menunjukkan jumlah urea yang terdekomposisi dalam sintesis. Berdasarkan penelitian ini, ekstrak air buah belimbing wuluh dapat dimanfaatkan dalam pembuatan nanomagnetit.
Kata kunci: buah belimbing wuluh, hidrotermal, nanomagnetit, sitrat.
ABSTRACT
IIS ISMAWATI. Water Extract of Bilimbi Fruit (Averrhoa bilimbi) as a Reductor in Nanomagnetite Synthesis. Supervised by DEDEN SAPRUDIN and ZULHAN ARIF.
Citrate content of bilimbi fruit (Averrhoa bilimbi) is potential as a Fe3+ reductor in nanomagnetite synthesis through hydrothermal method. The purpose of this experiment was to synthesis nanomagnetite using FeCl3, urea, and water extract of the fruit by hydrothermal method. Some fruit samples were smashed using blender to give suspension and water extract. The suspension reacted with FeCl3 and urea by hydrothermal method at 200 oC for 12 hours did not formed nanomagnetite, while those reacted under the same treatment formed nanomagnetite. The filtrate gave crystal size of 27.06 nm, which was smaller than that synthesized using sodium citrate as a reducing agent. The synthesized nanomagnetite contained 7 ppm cobalt and the liquid of the synthesized magnetite contained 52% ammonium showing the decomposed urea during the synthesis. Based on the experiment, water extract of bilimbi fruit can be used in nanomagnetite synthesis.
Skripsi
sebagai salah satu syarat untuk memperoleh gelar Sarjana Sains pada
Program Studi S1 Departemen Kimia
EKSTRAK AIR BUAH BELIMBING WULUH (
Averrhoa bilimbi
)
SEBAGAI REDUKTOR DALAM PEMBUATAN
NANOMAGNETIT
IIS ISMAWATI
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM INSTITUT PERTANIAN BOGOR
Judul Skripsi : Ekstrak Air Buah Belimbing Wuluh (Averrhoa bilimbi) sebagai Reduktor dalam Pembuatan Nanomagnetit
Nama : Iis Ismawati NIM : G44090009
Disetujui oleh
Dr Deden Saprudin, MSi Pembimbing I
Zulhan Arif, SSi MSi Pembimbing II
Diketahui oleh
Prof Dr Dra Purwantiningsih Sugita, MS Ketua Departemen
PRAKATA
Puji dan syukur penulis panjatkan kepada Allah SWT karena atas limpahan rahmat dan hidayah-Nya penulis dapat menyelesaikan skripsi yang berjudul Ekstrak Air Buah Belimbing Wuluh (Averrhoa bilimbi) sebagai Reduktor
dalam Pembuatan Nanomagnetit. Penelitian ini dilakukan pada bulan Maret sampai Agustus 2013 di Laboratorium Kimia Analitik dan Laboratorium Bersama Departemen Kimia, Institut Pertanian Bogor.
Penulis mengucapkan terima kasih kepada Bapak Dr Deden Saprudin, MSi dan Bapak Zulhan Arif, SSi MSi yang telah memberikan arahan dan bimbingan selama penelitian. Ucapan terima kasih diberikan kepada seluruh staf Laboratorium Kimia Analitik (Pak Eman, Pak Dede, dan Bu Nunung) dan staf Laboratorium Bersama (Pak Wawan) yang telah memberikan bantuan dan masukan kepada penulis. Terima kasih juga kepada Yesi, Nur, Dwi, Indri, dan teman-teman Analitik yang telah memberikan semangat dan bantuan selama penelitian. Terima kasih tak terhingga penulis ucapkan kepada Ibu, Ayah, dan kakak-kakak tercinta atas doa, dukungan, dan kasih sayang yang selalu diberikan.
Semoga skripsi ini dapat bermanfaat. Terima kasih.
Bogor, Oktober 2013
DAFTAR ISI
DAFTAR TABEL vi
DAFTAR GAMBAR vi
DAFTAR LAMPIRAN vi
PENDAHULUAN 1
Latar Belakang 1
Tujuan Penelitian 2
METODE 2
Alat dan Bahan 2
Prosedur 2
HASIL DAN PEMBAHASAN 4
Ekstrak Air Buah Belimbing Wuluh 4
Sintesis Nanomagnetit 5
Karakterisasi Hasil 7
SIMPULAN DAN SARAN 11
Simpulan 11
Saran 12
DAFTAR PUSTAKA 12
LAMPIRAN 14
DAFTAR TABEL
1 Kandungan asam organik buah belimbing wuluh 1
2 Variasi komposisi sintesis magnetit 6
3 Puncak 2θ standar magnetit dan padatan hasil sintesis 8
4 Derajat kristalinitas hasil sintesis 9
5 Komposisi unsur padatan hasil sintesis 10
6 Kandungan Fe dalam hasil sintesis 10
7 Kadar ammonium dalam cairan hasil sintesis 11
DAFTAR GAMBAR
1 Buah belimbing wuluh 4
2 Struktur asam sitrat 5
3 Larutan suspensi dan filtrat ekstrak air belimbing wuluh 5 4 Respon magnet terhadap hasil sintesis menggunakan filtrat ekstrak air
buah belimbing wuluh (C2) 7
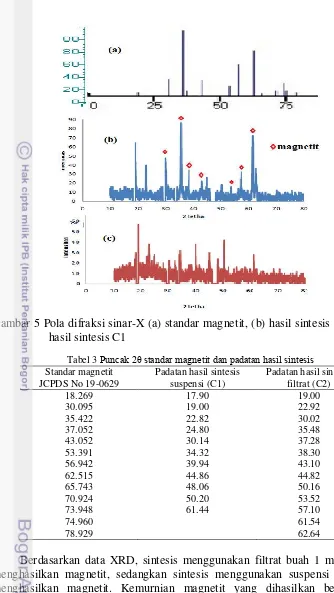
5 Pola difraksi sinar-X (a) standar magnetit, (b) hasil sintesis C2, dan (c)
hasil sintesis C1 8
DAFTAR LAMPIRAN
1 Bagan alir penelitian 14
2 Pembuatan larutan standar dan pereaksi pada penentuan ammonium 15
3 Penentuan kadar air dan kadar abu 16
4 Perhitungan kadar asam 17
5 Sudut difraksi standar magnetit dan padatan hasil sintesis 18
6 Penentuan ukuran kristal 19
7 Perhitungan kadar Fe dan Co hasil sintesis 20
PENDAHULUAN
Latar Belakang
Nanomagnetit (Fe3O4) merupakan molekul oksida besi yang banyak digunakan untuk kepentingan penelitian, biosensor glukosa dan urea, serta aplikasi kedokteran, seperti antikanker dan pengantar obat (Loh et al. 2008). Fauziah (2012) dan Sari (2012) menggunakan magnetit sebagai pemodifikasi elektrode pasta karbon pada teknik voltametri siklik. Hal ini karena nanomagnetit memiliki beberapa kelengkapan sifat diantaranya sifat kemagnetan, katalitik, konduktivitas, dan luas permukaannya yang besar. Magnetit terdiri atas dua bentuk Fe, yaitu Fe2+ dan Fe3+. Atom Fe2+ dan sebagian Fe3+ berikatan oktahedral, sedangkan Fe3+ lainnya berikatan tetrahedral membentuk kristal spinel kubus bepusat muka (Roonasi 2007). Nanomagnetit bersifat paramagnetik dan stabil pada suhu tinggi (Márquez et al. 2011).
Metode yang sudah dikembangkan dalam sintesis nanomagnetit diantaranya metode sol-gel, kopresipitasi, teknik mikroemulsi, dan teknik pemanasan hidrotermal (Fernandez 2011). Menurut Byrappa dan Adschiri (2007), pemanasan hidrotermal banyak digunakan karena mampu menghasilkan partikel murni dengan homogenitas yang sangat tinggi. Sintesis nanomagnetit dilakukan Cheng et al. (2010) dengan menggunakan prekursor FeCl3, natrium sitrat, poliakrilamida, dan urea. Magnetit yang dihasilkan berukuran 20 nm, berbentuk bulat dan terdispersi dalam air. Cara ini dianggap lebih murah dan tidak beracun. Selanjutnya Pradana (2013) juga berhasil mensintesis magnetit dari FeCl3, natrium sitrat, dan urea tanpa penambahan poliakrilamida. Magnetit yang dihasilkan berukuran 46.66 nm, berbentuk bulat, dan teraglomersi.
Magnetit terbentuk dari reaksi reduksi FeCl3 oleh sitrat. Ion sitrat dapat mengkompleks Fe dan menghasilkan reaksi lambat yang baik untuk pembentukan kristal. Sitrat akan mereduksi sebagian Fe3+ menjadi Fe2+ yang selanjutnya berubah menjadi magnetit (Fe3O4). Selain itu, sitrat juga berperan dalam pembentukan fase murni Fe3O4 dan menunjang keberhasilan produk magnetit yang dihasilkan. Kristal yang terbentuk tanpa penambahan sitrat adalah α-Fe2O3 (Cheng et al. 2010). Sumber sitrat banyak ditemukan pada berbagai buah dan sayuran, namun ditemukan dengan konsentrasi tinggi pada jeruk lemon, limau, markisa, nanas, dan buah belimbing wuluh (Lancashire 2004). Menurut Manggung (2008), rasa asam pada buah belimbing wuluh berasal dari asam sitrat dan asam oksalat, sesuai penelitian Hertanto (2012) buah belimbing wuluh mengandung asam-asam organik yang didominasi asam sitrat. Asam-asam organik tersebut selengkapnya disajikan dalam Tabel 1.
Tabel 1 Kandungan asam organik buah belimbing wuluh
Asam Organik Jumlah (meq/100 g bahan segar)
Asam Sitrat 92.6-133.8
Asam Oksalat 5.5-8.9
Asam Asetat 1.6-1.9
Asam Format 0.4-0.9
2
Pemanfaatan buah belimbing wuluh masih jarang dilakukan. Buahnya dimanfaatkan sebatas untuk keperluan memasak dan manisan. Tanaman belimbing wuluh menghasilkan buah sepanjang tahun. Selain itu, tanaman ini juga mudah ditanam dan diperbanyak sehingga buahnya melimpah (Hidayati 2007). Oleh karena itu, dalam penelitian ini ekstrak air buah belimbing wuluh akan dijadikan sumber sitrat yang sangat potensial dalam sintesis magnetit. Hasil penelitian ini diharapkan dapat meningkatkan nilai guna dalam pemanfaatan buah belimbing wuluh dan dapat menghasilkan partikel magnetit yang memiliki banyak kegunaan.
Tujuan Penelitian
Penelitian bertujuan mensintesis nanomagnetit menggunakan prekursor FeCl3, urea, dan ekstrak air buah belimbing wuluh sebagai sumber sitrat secara hidrotermal.
METODE
Alat dan Bahan
Alat yang digunakan pada penelitian ini adalah neraca analitik, alat penggiling (blender), alat gelas, cawan porselin, oven, Bunsen, tanur, eksikator, pH meter, buret, bejana hidrotermal, Difraktometer sinar-X (XRD Shimadzu 7000 Maxima), Penganalisis Dispersif Energi (EDX), Spektrofotometer UV-Vis, dan Spektrofotometer Serapan Atom (AAS). Bahan yang digunakan adalah buah belimbing wuluh, FeCl3.6H2O (Nacalai Tesque), urea (Merck), akuades, larutan etanol, asam oksalat (Merck), NaOH (Merck), kalium-natrium tartrat (Merck), fenol (Merck), (NH4)2SO4 (Merck), NaOCl 12%, dan HNO3 pekat.
Prosedur
Penelitian terdiri dari empat tahapan utama mengikuti diagram alir pada Lampiran 1, meliputi (1) pembuatan ekstrak air buah belimbing wuluh (suspensi dan filtrat buah belimbing wuluh), (2) penentuan kadar asam ekstrak air buah belimbing wuluh menggunakan metode titrasi, (3) sintesis nanomagnetit dengan variasi komposisi FeCl3 dan urea menggunakan metode hidrotermal, dan (4) karakterisasi hasil sintesis. Karakterisasi dilakukan menggunakan Difraktometer sinar-X (XRD), Penganalisis Dispersif Energi (EDX), penentuan kadar Fe menggunakan Spektrofotometer Serapan Atom (AAS), dan penentuan kadar ammonium.
Penentuan Kadar Air Belimbing Wuluh (AOAC 2007)
3 Penentuan Kadar Abu (AOAC 2007)
Cawan porselen dikeringkan dalam tanur bersuhu 600oC selama 30 menit. Cawan kemudian didinginkan dalam eksikator selama 30 menit dan bobot kosong cawan ditimbang. Sebanyak 2 g simplisia buah belimbing wuluh dimasukkan ke dalam cawan lalu dipijarkan di atas nyala api pembakar bunsen sampai tidak berasap. Cawan dimasukkan ke dalam tanur pada suhu 600oC selama 2 jam hingga diperoleh abu. Cawan berisi abu didinginkan dalam eksikator selama 30 menit dan ditimbang. Prosedur dilakukan sebanyak tiga kali ulangan.
Pembuatan Ekstrak Air buah belimbing wuluh
Buah belimbing wuluh terlebih dahulu dicuci bersih, dipotong kecil-kecil lalu digiling dengan menggunakan blender sampai halus. Hasil penggilingan disaring dan diambil airnya sebagai suspensi ekstrak buah. Ekstrak air buah sebagian disimpan selama 1 minggu pada suhu 4oC. Ekstrak hasil penyimpanan yang telah membentuk endapan diambil filtratnya. Suspensi dan filtrat 1 minggu dianalisis kadar asamnya menggunakan metode titrasi dan dijadikan bahan pembuatan nanomagnetit.
Penentuan Kadar Asam Ekstrak Air Buah Belimbing Wuluh
Standardisasi NaOH dilakukan dengan menimbang sebanyak 0.3150 g asam oksalat dan dilarutkan dalam labu takar 50 mL lalu ditera menggunakan akuades. Larutan asam oksalat 10 mL dipipet ke dalam Erlenmeyer lalu ditambah 2-3 tetes indikator fenolftalein. Larutan dititrasi menggunakan NaOH sampai berubah warna menjadi merah muda seulas. Titrasi dilakukan sebanyak 3 kali ulangan. Selanjutnya, sebanyak 1 mL suspensi dan filtrat 1 minggu buah belimbing wuluh diencerkan menggunakan akuades hingga volumenya 10 mL. Sampel ditambah indikator fenolftalein 2-3 tetes lalu dititrasi menggunakan NaOH yang telah distandardisasi. Titrasi dihentikan ketika terjadi perubahan warna menjadi merah muda seulas.
Sintesis Nanomagnetit (modifikasi Cheng et al. (2010))
Sintesis dilakukan dengan 3 variasi komposisi. Komposisi Campuran A terdiri dari 2 mmol FeCl3, 6 mmol urea, dan 12 mmol asam. Komposisi campuran B terdiri dari 3 mmol FeCl3, 9 mmol urea, dan 12 mmol asam, sedangkan campuran C terdiri dari 4 mmol FeCl3, 12 mmol urea, dan 12 mmol asam dari ekstrak air buah belimbing wuluh. Ekstrak yang digunakan berupa suspensi dan filtrat 1 minggu. Campuran dimasukkan ke dalam gelas piala lalu dimasukkan ke dalam alat teflon-hidrotemal dan ditutup rapat selama 12 jam dengan suhu 200oC. Selanjutnya alat hidrotemal didinginkan dan hasil sintesis yang terbentuk dipisahkan antara bagian padatan dan cairannya. Padatan yang terbentuk kemudian dicuci dengan akuades dan etanol. Selanjutnya endapan dikeringkan pada suhu 70oC.
Karakterisasi Hasil Sintesis
4
Penentuan Kadar Fe Hasil Sintesis
Penentuan kadar Fe dilakukan terhadap serbuk dan cairan hasil sintesis. Serbuk hasil sintesis ditimbang sebanyak 0.5 g dan ditambah 5 ml HNO3 lalu dipanaskan. Filtrat disaring dan diencerkan dalam labu takar 50 mL menggunakan akuades selanjutnya diukur menggunakan AAS. Pengukuran Fe dalam cairan dilakukan dengan mencampurkan 7 mL cairan hasil sintesis ditambah 0.7 mL HNO3, kemudian dikocok hingga homogen. Selanjutnya larutan dianalisis menggunakan AAS.
Penentuan Kadar Ammonium dalam Cairan Hasil Sintesis (Pradana 2013) Sebanyak 1 mL cairan hasil sintesis dimasukkan ke dalam tabung reaksi kemudian ditambahkan larutan sangga tartrat dan Na-fenat masing-masing sebanyak 2 mL. Larutan dikocok dan dibiarkan selama 10 menit. Selanjutnya larutan ditambah 2 mL NaOCl 5% dan diukur serapannya menggunakan spektrofotometer UV-Vis pada panjang gelombang 615 nm. Pembuatan pereaksi diperlihatkan pada Lampiran 2.
HASIL DAN PEMBAHASAN
Ekstrak Air Buah Belimbing Wuluh
Buah belimbing wuluh (A. bilimbi) merupakan buah yang dikenal sangat asam. Keasaman yang tinggi dihubungkan dengan kadar asam sitrat yang terkandung di dalamnya. Asam sitrat merupakan asam organik lemah yang ditemukan pada daun dan buah tumbuhan. Keasaman sitrat didapatkan dari tiga gugus karboksil COOH yang dapat melepas proton dalam larutan. Asam sitrat akan mengion menjadi ion sitrat yang baik digunakan dalam larutan penyangga untuk mengendalikan pH larutan (Kasmiyatun dan Jos 2008).
Gambar 1 Buah belimbing wuluh
5 asam-asam organik, terutama asam sitrat yang dapat melepaskan proton dalam larutan (Gambar 2) (Kasmiyatun dan Jos 2008).
Gambar 2 Struktur asam sitrat
Buah belimbing wuluh memiliki kadar abu sebesar 6.51% berdasarkan bobot kering. Kadar abu tersebut menunjukkan kandungan mineral yang terdapat dalam buah belimbing wuluh. Menurut Roy et al. (2011) mineral yang terdapat dalam buah belimbing wuluh meliputi fosfor, kalium, kalsium, dan besi.
Berdasarkan hasil titrasi, konsentrasi asam dalam suspensi ekstrak buah belimbing wuluh dan filtrat buah yang disimpan 1 minggu tidak jauh berbeda. Suspensi ekstrak buah memiliki konsentrasi asam sebesar 0.2928 N sedangkan konsentrasi asam dalam filtrat buah 1 minggu sebesar 0.2865 N. Proses penyimpanan ekstrak buah tidak menyebabkan penurunan kadar asam, tetapi hanya menyebabkan padatan-padatan terlarut di dalam suspensi ekstrak buah mengendap sehingga filtrat yang dihasilkan lebih jernih. Konsentrasi asam ini menunjukkan total asam yang terdapat dalam buah, tidak hanya asam sitrat saja Dengan konsentrasi asam tersebut, jumlah filtrat yang perlu ditambahkan dalam sintesis ialah sebanyak 41.9 mL sebanding dengan 12 mmol asam (Lampiran 4).
Sintesis Nanomagnetit
Sintesis dilakukan dengan mencampurkan FeCl3, urea dan ekstrak air buah belimbing wuluh. Ekstrak yang digunakan berupa suspensi ekstrak segar dan filtrat ekstrak yang disimpan selama 1 minggu. Suspensi ekstrak segar lebih banyak mengandung padatan terlarut dibandingkan filtrat yang disimpan selama 1 minggu. Filtrat 1 minggu mengandung padatan terlarut yang telah mengendap akibat penyimpanan sehingga cairannya lebih homogen dan lebih jernih.
Gambar 3 Larutan suspensi dan filtrat ekstrak air belimbing wuluh
6
Dekarboksilasi ini menyebabkan sitrat teroksidasi dan Fe3+ tereduksi menjadi Fe2+. Selain itu, CO2 akan dihasilkan sebagai produk samping proses dekarboksilasi ion sitrat (Reaksi 1) (Yang et al. 2010). Reduksi besi terjadi dengan metode hidrotermal yang memanfaatkan suhu tinggi mencapai 200oC selama 12 jam. Suhu yang tinggi dalam sistem tertutup akan menghasilkan tekanan diatas 1 atm (Rizal dan Ismunandar 2007). Menurut Fernandez (2011) tekanan yang dihasilkan sistem hidrotermal bisa mencapai 100 barr (setara 98.69 atm). Metode ini dapat memaksimalkan reaksi kimia yang terjadi karena tekanan yang tinggi akan menyebabkan peningkatan daya larut padatan dan meningkatnya kecepatan reaksi yang mendorong minimalisasi energi permukaan sehingga partikel akan mulai mengkristal (Cheng et al. 2010). Tekanan tinggi juga dapat mencegah pembentukan kristal sehingga derajat kristalinitas akan meningkat (Abdullah et al. 2008).
Suhu yang tinggi menyebabkan urea terdekomposisi menjadi NH3 yang akan membuat suasana menjadi basa (Reaksi 2) (Lv et al. (2009). Suasana basa akan menyebabkan terbentuknya Fe(OH)3 dan Fe(OH)2 (Reaksi 3 dan 4) yang selanjutnya berubah menjadi magnetit dan menghasilkan air (Reaksi 5). Menurut Cheng et al. (2010) reaksi pembentukan magnetit dituliskan sebagai berikut:
C6H5O73- + 2Fe3+ C5H4O52- + H+ + CO2 + 2Fe2+ ... (1)
(NH2)2CO + 3H2O 2NH3.H2O + CO2 ... (2)
Fe2+ + 2NH3.H2O Fe(OH)2 + 2NH4+ ... (3)
Fe3+ + 3NH3.H2O Fe(OH)3 + 3NH4+ ... (4)
Fe(OH)2 + 2Fe(OH)3 Fe3O4 + 4H2O ... (5) Hasil sintesis dengan beberapa komposisi ditampilkan dalam Tabel 2.
Tabel 2 Variasi komposisi sintesis magnetit FeCl3
7 lemah. Menurut Liang et al. (2006), pembentukan magnetit membutuhkan basa dengan konsentrasi yang tinggi, sedangkan penambahan basa dengan konsentrasi rendah akan menghasilkan geotit.
Magnetit merupakan mineral yang bersifat paramagnetik. Hal ini akan terlihat jika magnetit didekatkan dengan medan magnet maka akan merespon medan magnet (Paul 2010). Sintesis menggunakan suspensi (C1) menghasilkan serbuk hitam yang tidak merespon medan magnet sedangkan sintesis menggunakan filtrat 1 minggu (C2) menghasilkan serbuk hitam yang merespon medan magnet. Serbuk hasil sintesis menggunakan filtrat 1 minggu (C2) diduga merupakan magnetit, sedangkan serbuk hasil sintesis menggunakan suspensi (C1) bukan magnetit, kemungkinan oksida besi lainnya. Hal ini terlihat ketika serbuk hasil sintesis C2 didekatkan dengan medan magnet maka serbuk akan menempel pada medan magnet menunjukkan bahwa serbuk bersifat paramagnetik (Gambar 4). Sifat magnetik tersebut karena ukuran kristal hasil sintesis menggunakan filtrat 1 minggu lebih kecil dibandingkan ukuran kristal hasil sintesis suspensi ekstrak segar. Menurut Lu et al. (2007) dan Cheng et al. (2010) bahwa partikel yang memiliki ukuran 10-30 nm akan memiliki sifat paramagnetik. Sifat paramagnetik Fe3O4 juga disebabkan oleh adanya transfer elektron antara Fe3+ dan Fe2+ dalam kisi oktahedral dan adanya spin elektron yang tak berpasangan pada kisi kristal (Lu et al. 2007). Serbuk hasil sintesis C1 dan C2 tersebut selanjutnya dikarakterisasi untuk membuktikan telah terbentuknya magnetit.
Gambar 4 Respon magnet terhadap hasil sintesis menggunakan filtrat ekstrak air buah belimbing wuluh (C2)
Karakterisasi Hasil
8
Gambar 5 Pola difraksi sinar-X (a) standar magnetit, (b) hasil sintesis C2, dan (c) hasil sintesis C1
Tabel 3 Puncak 2θ standar magnetit dan padatan hasil sintesis Standar magnetit
JCPDS No 19-0629
Padatan hasil sintesis suspensi (C1)
Padatan hasil sintesis filtrat (C2)
18.269 17.90 19.00
30.095 19.00 22.92
35.422 22.82 30.02
37.052 24.80 35.48
43.052 30.14 37.28
53.391 34.32 38.30
56.942 39.94 43.10
62.515 44.86 44.82
65.743 48.06 50.16
70.924 50.20 53.52
73.948 61.44 57.10
74.960 61.54
78.929 62.64
9 sintesis filtrat 1 minggu (C2) memiliki puncak dengan intensitas yang lebih tinggi dibandingkan dengan puncak padatan hasil sintesis menggunakan suspensi (C1). Puncak hasil sintesis filtrat 1 minggu membentuk luas daerah kristalin yang lebih banyak dibandingkan luas daerah amorf membuktikan padatan hasil sintesis filtrat 1 minggu terbentuk lebih baik dengan derajat kristalinitas yang lebih tinggi. Hasil perhitungan derajat kristalinitas hasil sintesis ditampilkan dalam Tabel 4.
Tabel 4 Derajat kristalinitas hasil sintesis
Padatan hasil sintesis Luas daerah kristalin
(kcps*deg)
Derajat kristalinitas diperoleh berdasarkan perbandingan antara luas daerah kristalin dengan luas daerah total (kristalin dan amorf) yang dihasilkan oleh sampel. Padatan hasil sintesis menggunakan filtrat 1 minggu (C2) memiliki derajat kristalinitas lebih tinggi sebesar 95.36% dibandingkan padatan hasil sintesis suspensi segar (C1) sebesar 84.08%. Hal ini karena jumlah padatan terlarut dalam filtrat 1 minggu menjadi lebih sedikit akibat proses penyimpanan. Proses penyimpanan ekstrak air buah menyebabkan terbentuk endapan pada ekstrak buah dan filtrat menjadi lebih jernih sehingga tidak banyak komponen yang ikut bereaksi selama sintesis. Menurut De Lima (2001), jumlah padatan terlarut yang terkandung dalam buah belimbing wuluh berkisar antara 3.94 sampai 5.06%. Selama proses sintesis, tekanan yang tinggi akan mengakibatkan terjadinya peningkatan daya larut padatan sehingga mendorong kecepatan reaksi yang meningkatkan kristalinitas bahan (Fernandez 2011). Selain itu, waktu sintesis juga akan mempengaruhi derajat kristalinitas. Waktu sintesis selama 12 jam memungkinkan reaksi telah berjalan sempurna sehingga derajat kristalinitasnya tinggi.
Hasil analisis XRD juga diketahui ukuran kristal. Ukuran kristal diperoleh dengan menggunakan persamaan Debye Scherrer (Zakaria et al. 2009). Hasil perhitungan ditampilkan dalam Lampiran 6. Kristal hasil sintesis menggunakan filtrat 1 minggu (C2) memilki ukuran rata-rata 27.06 nm sedangkan kristal hasil sintesis menggunakan suspensi (C1) memiliki ukuran rata-rata 67.37 nm. Sintesis magnetit dalam larutan berair dapat menghasilkan kristal dengan ukuran kurang dari 1 μm. Menurut Laurent et al. (2008), jika ukuran kristal yang diperoleh lebih kecil dari 100 nm maka dapat dikatakan sampel tersebut adalah nanokristal. Dengan demikian, kedua kristal hasil sintesis tersebut dapat dikategorikan sebagai nanokristal karena ukurannya kurang dari 100 nm.
10
kemurnian kristal cukup rendah karena masih adanya komponen lain dalam kristal.
Tabel 5 Komposisi unsur padatan hasil sintesis
Unsur Komposisi padatan (%)
Filtrat 1 minggu (C2) Suspensi segar (C1)
Besi 48.60 20.95 ditambahkan, sedangkan fosfor dan kobalt dihasilkan dari ekstrak air buah belimbing wuluh. Berdasarkan Tabel 5, diketahui padatan hasil sintesis menggunakan filtrat buah 1 minggu mengandung besi dan oksigen sebagai penyusun utama magnetit dengan komposisi besi sebesar 48.60% dan oksigen sebesar 31.79%. Padatan hasil sintesis menggunakan suspensi buah mengandung lebih banyak oksigen (52.05%) dan karbon (25.87%) sehingga proporsi besi di dalamnya menjadi lebih sedikit (20.95%). Karbon dan oksigen dalam suspensi tersebut diduga berasal dari serat-serat, karbohidrat, dan padatan terlarut lainnya yang ada dalam ekstrak air buah belimbing wuluh. Hasil EDX menunjukkan magnetit tidak mengandung nitrogen. Hal ini disebabkan karena analisis menggunakan EDX hanya dapat mendeteksi unsur-unsur di permukaan partikel tertentu saja.
Adanya logam kobalt dalam padatan hasil sintesis diukur dengan menggunakan spektrofotometer serapan atom (AAS). Hasil AAS diperoleh bahwa padatan hasil sintesis menggunakan suspensi (C1) mengandung 1.7229 ppm kobalt sedangkan hasil sintesis menggunakan filtrat buah 1 minggu (C2) mengandung kobalt sebanyak 7.0277 ppm (Lampiran 7). Jumlah Co yang terdapat dalam padatan hasil sintesis menggunakan suspensi (C1) sebanyak 0.0017 mg sedangkan jumlah Co yang terdapat dalam padatan hasil sintesis menggunakan filtrate (C2) sebanyak 0.0044 mg. Logam Co ini berasal dari ekstrak air buah belimbing wuluh yang ikut bereaksi selama proses sintesis.
Pengukuran logam menggunakan AAS juga dilakukan untuk mengetahui kadar Fe dalam hasil sintesis. Analisis kandungan Fe dilakukan untuk mengetahui jumlah Fe awal yang berubah menjadi produk. Hasil AAS menunjukkan lebih dari 96% Fe telah terkonversi menjadi padatan (Lampiran 7), namun padatan yang terbentuk belum dipastikan membentuk magnetit.
Tabel 6 Kandungan Fe dalam hasil sintesis
Ekstrak air Bobot Fe (mg) dalam Fe dalam padatan
11 dalam padatan sintesis menggunakan suspensi buah sebesar 21.50% dan persen Fe dalam padatan hasil sintesis menggunakan filtrat 1 minggu sebesar 34.14%.
Sintesis menggunakan suspensi (C1) menghasilkan padatan sebanyak 990 mg lebih banyak dibandingkan sintesis menggunakan filtrat 1 minggu (C2) yang menghasilkan padatan sebanyak 630 mg. Hal ini karena suspensi buah banyak mengandung padatan terlarut di dalamnya sehingga lebih banyak komponen yang terbawa selama reaksi. Namun demikian, jumlah padatan tersebut lebih sedikit dari jumlah serbuk secara teori, yaitu 1008.4 mg untuk sintesis menggunakan suspensi dan 637.1 mg untuk sintesis menggunakan filtrat buah 1 minggu. Perbedaan ini disebabkan karena masih adanya serbuk sisa yang masih menempel dalam permukaan Teflon hidrotermal yang digunakan sehingga bobot hasil sintesis yang didapatkan lebih sedikit dari bobot sebenarnya.
Penentuan kadar ammonium dalam cairan hasil sintesis dilakukan untuk mengetahui jumlah urea yang terdekomposisi menjadi amonia. Amonia dalam air berbentuk ammonium. Amonium dalam cairan sebagai produk samping dari hasil sintesis. Pengukuran dilakukan menggunakan spektrofotometer UV-Vis pada panjang gelombang maksimum 615 nm (Lampiran 8).
Tabel 7 Kadar ammonium dalam cairan hasil sintesis
Cairan sintesis Masa ammonium (g) Ammonium (%b/v)
Filtrat 1 minggu (C2) 0.2243 0.6231
Suspensi (C1) 0.2107 0.5852
Berdasarkan Tabel 7, kadar ammonium dalam cairan hasil sintesis menggunakan suspensi (C1) sebesar 0.5852%, sedangkan kadar ammonium dalam cairan sintesis menggunakan filtrat 1 minggu (C2) sebesar 0.6231%. Masa ammonium yang terbentuk dalam 36 ml cairan hasil sintesis menggunakan suspensi buah didapatkan sebesar 0.2107 g, sedangkan cairan sintesis menggunakan filtrat buah 1 minggu mengandung ammonium sebesar 0.2243 g. Masa ammonium kedua cairan sintesis lebih sedikit dibandingkan masa ammonium yang seharusnya, yaitu sebesar 0.432 g sehingga didapat persentase hasil sintesis menggunakan suspensi (C1) dan filtrat (C2) berturut-turut sebesar 48.77% dan 51.92%. Hal ini disebabkan pemanasan urea tidak hanya akan menghasilkan amonia tetapi juga menghasilkan produk samping berupa NH2CONHCONH2 sehingga jumlah amonia yang dihasilkan akan berkurang (Winarso 2004). Selain itu, dengan semakin tingginya derajat kristalinitas akan membuat urea terabsorpsi dalam kristal sehingga kadar ammonium dalam cairan menjadi lebih sedikit.
SIMPULAN DAN SARAN
Simpulan
12
difraksi dengan standar magnetit, yaitu pada sudut 2θ 30.02; 35.48; 37.28; 43.10; 53.52; 57.10; dan 62.64o. Ukuran kristal magnetit hasil sintesis C2 sebesar 27.06 nm. Hasil EDX menunjukkan Fe dan O sebagai komponen utama padatan magnetit yang dihasilkan. Pengukuran kadar Fe diketahui lebih dari 96% Fe berhasil diubah menjadi padatan.
Saran
Analisis terhadap kandungan kimia yang terdapat dalam ekstrak air buah belimbing wuluh perlu dilakukan untuk mengetahui pengaruhnya terhadap kemurnian hasil sintesis. Perlu dilakukan analisis lanjutan terhadap oksida besi hasil sintesis yang tidak membentuk magnetit.
DAFTAR PUSTAKA
Abdullah M, Virgus Y, Nirmin, Khairurrijal. 2008. Sintesis Nanomaterial. J Nano Saintek 1(2):33-57.
[AOAC] Association Official Agriculture Chemist. 2007. Official Methods of Analysis of AOAC International. Maryland: AOAC International.
Byrappa K, Adschiri T. 2007. Hydrothermal technology for nanotechnology. Progress in Crystal Growth and Characterization of Materials53 : 117-166. doi:10.1016/j.pcrysgrow.2007.04.001.
Cheng W, Tang K, Qi Y, Sheng J, Liu Z. 2010. One-step synthesis of superparamagnetic monodisperse porous Fe3O4 hollow and core-shell spheres. J Mater Chem. 20:1799-1805.doi:10.1039/b919164j.
De Lima VLAG, Melo EDA, Lima LS. 2001. Physicochemical characteristics of bilimbi (Averrhoa bilimbi L.). Rev.Bras. Frutic 23(2):421-423.
Fauziah H. 2012. Nanomagnetit sebagai peningkat sensitivitas elektrode pasta karbon dalam analisis iodida secara voltametri siklik [skripsi]. Bogor (ID): Institut Pertanian Bogor.
Fernandez BR. 2011. Sintesis nanopartikel [tesis]. Padang (ID): Pascasarjana Universitas Andalas.
Hertanto B. 2012. Penggunaan belimbing wuluh untuk mengahambat oksidasi dan mempertahankan mutu organoleptik pada dendeng sapi selama penyimpanan [skripsi]. Bogor (ID): Institut Pertanian Bogor.
Hidayati IL. 2007. Formulasi tablet effervescent dari ekstrak daun belimbing wuluh (Averrhoa bilimbi L.) sebagai anti hipertensi [skripsi]. Bogor (ID): Institut Pertanian Bogor.
Kasmiyatun M, Jos B. 2008. Ekstraksi asam sitrat dan asam oksalat: pengaruh trioctylamine sebagai extracting power dalam berbagai solven campuran terhadap koefisien distribusi. Reaktor 12 (2):107-116.
Lancashire RJ. 2004. The chemistry of passion fruit. [Internet]. [diunduh 2013
Sep 14]. Tersedia pada:
http://www.chem.uwimona.edu.jm/lectures/psnfruit.html.
13 physicochemical characterizations, and biological applications. Chem Rev 108 (16): 2069-2070.doi:10.1021/cr068445e.
Liang X, Wang X, Zhuang J, Chen Y, Wang D, Li Y. 2006. Synthesis of nearly monodisperse iron oxide and oxyhydroxide nanocrystals. Adv. Funct. Mater.16:1805-1813.doi:10.1002/adfm.200500884.
Loh KS. Lee YH, Musa A, Salmah AA, Zamri I. 2008. Use of Fe3O4 nanoparticle for enhancement of biosensor respons the herbiside 2,4-dichlorophenoxyacetic acid. Sensor 8:5775-5791. doi:10.3390/s8095775. Lu A H, Salabas El, dan Scutch F. 2007. Magnetic nanoparticles: synthesis,
protection, functionalization, and application. Wiley-VCH Verlag GmbH & Co 46:1222 – 1244.doi: 10.1002/anie.200602866.
Lv Y, Wang H, Wang X, Bai J. 2009. Synthesis, characterization and growing mechanism of monodisperse Fe3O4 microspheres. J Crystal Growth 311: 3445-3450.doi:10.1016/j.jcrysgro.2009.03.046.
Manggung RER. 2008. Pengujian toksisitas akut lethal dose 50 (LD50) ekstrak etanol buah belimbing wuluh (Averrhoa bilimbi L.) pada mencit (Mus musculus albinus) [skripsi]. Bogor (ID): Institut Pertanian Bogor.
Márquez F, Campo T, Cotto M, Polanco R, Roque R, Fierro P, Sanz JM, Elizalde E, Morant C. 2011. Synthesis and characterization of monodisperse magnetite hollow microspheres. Soft Nanoscience Letters 1: 25-32. doi:10.4236/snl.2011.12005.
Paul MC. 2010. Molecular beam epitaxy and properties of magnetite thin films on semiconducting substrates [disertasi]. Wurzburg (DE): Universitas Julius Maximilians.
Pradana VM. 2013. Keragaan nitrogen-ammonium dalam magnetit sintetik (Fe3O4) [skripsi]. Bogor (ID): Institut Pertanian Bogor.
Rizal M, Ismunandar. 2007. Sintesis dengan metode hidrotermal dan karakterisasi senyawa berstruktur Aurivillius Bi4Ti3O12. J Mat Sains 12:44-48.
Roonasi P. 2007. Adsorption and surface reaction properties of synthesized magnetite nano-particles [tesis]. Luleå (SE): Luleå University of Technology.
Roy A, Geetha RV, Lakshmi T. 2011. Averrhoa bilimbi Linn –nature’s drug store- a pharmacological. International Journal of Drug Development & Research 3 (3): 101-106.
Sari EO. 2012. Kinerja elektrode pasta karbon termodifikasi nanomagnetit pada teknik voltametri siklik [skripsi]. Bogor (ID): Institut Pertanian Bogor. Winarso L. 2004. Optimasi alat pengolah limbah cair 2nd stage hydrolizer dan
pemanfaatannya sebagai air umpan boiler [tesis]. Semarang: Program Pascasarjana, Universitas Dipenegoro.
Yang Z, Qian H, Chen H, Anker JN. 2010. One-pot hydrothermal synthesis of silver nanowires via citrate reduction. J Colloid Interface Sc. 352: 285-281. doi:10.1016/j.jcis.2010.08.072.
14
Lampiran 1 Bagan alir penelitian
Buah belimbing wuluh
Ekstrak air buah ampas
Penentuan kadar asam
Filtrat 1 minggu Suspensi segar
Sintesis nanomagnetit
pemisahan
cairan padatan
Karakterisasi XRD dan EDS Penentuan
kadar amonium
Penentuan kadar Fe
15 Lampiran 2 Pembuatan larutan standar dan pereaksi pada penentuan ammonium
Standar pokok 1000 ppm N
Sebanyak 0.4174 g serbuk (NH4)2SO4 p.a ditimbang dan dilarutkan menggunakan air bebas ion dalam labu takar hingga volumenya tepat 100 mL. larutan dikocok hingga homogen.
Standar 20 ppm N
Sebanyak 2 mL larutan standar pokok 1000 ppm N dipipet ke dalam labu takar 100 mL dan diencerkan menggunakan akuades hingga tepat 100 mL.
Deret standar
Deret larutan standar 0, 1, 2, 4, 6, 8, dan 10 ppm dibuat dengan memipet larutan standar 20 ppm N sebanyak 0; 0.5; 1; 2; 3; 4; dan 5 mL berturut-turut ke dalam tabung reaksi. Kemudian ditambahkan akuades hingga semua volumenya menjadi 10 mL.
Larutan Na-fenat
Sebanyak 5 g serbuk NaOH p.a ditimbang dan dilarukan dalam labu takar 50 mL menggunakan sekitar 25 mL air bebas ion. Setelah dingin, larutan ditambah 6.25 gram fenol dan diaduk hingga larut. Selanjutnya larutan diencerkan dengan air bebas ion hingga volumenya tepat 50 mL.
Larutan sangga tartrat
16
Lampiran 3 Penentuan kadar air dan kadar abu Penentuan kadar air buah belimbing wuluh
Ulangan Bobot wadah Penentuan kadar abu buah belimbing wuluh
17 Lampiran 4 Perhitungan kadar asam
Data standardisasi NaOH oleh asam oksalat ulangan Volume asam
oksalat (mL)
Volume NaOH (mL) Konsentrasi NaOH (N)
Volume NaOH (mL) Total asam (N)
18
Lampiran 5 Sudut difraksi standar magnetit dan padatan hasil sintesis Standar Magnetit
(JCPDS No 19-0629)
Padatan hasil sintesis suspensi segar
Padatan hasil sintesis filtrat 1 minggu
2θ Intensitas 2θ Intensitas 2θ Intensitas
18.269 4 17.90 30 19.00 64
30.095 26 19.00 56 22.92 40
35.422 100 22.82 38 30.02 48
37.052 8 24.80 28 35.48 86
43.052 24 30.14 22 37.28 16
53.391 15 34.32 32 38.30 34
56.942 47 39.94 38 43.10 22
62.515 68 44.86 30 44.82 26
65.743 4 48.06 24 50.16 18
70.924 8 50.20 42 53.52 16
73.948 20 61.44 28 57.10 32
74.960 8 61.54 72
19 Lampiran 6 Penentuan ukuran kristal
Padatan hasil sintesis suspensi segar 2θ (deg) a θ (deg) cos θ
Padatan hasil sintesis filtrat 1 minggu 2θ (deg) a θ (deg) cos θ
Ukuran kristal berdasarkan hukum Debye Scherrer: D =
20
Lampiran 7 Perhitungan kadar Fe dan Co hasil sintesis Kadar Fe Cairan Hasil Sintesis
Cairan Sintesis [Fe]
Contoh perhitungan cairan sintesis menggunakan suspensi: 1. Bobot Fe awal yang ditimbang = 4 mmol x 56 mg/mmol
= 224 mg 2. Bobot Fe yang terkonversi menjadi cairan
=
3. Fe yang terkonversi menjadi padatan (teori)
= bobot Fe awal – bobot Fe yang terkonversi menjadi cairan = 224 mg – 4.8
= 219.2 mg
Kadar Fe Padatan Hasil Sintesis Padatan
Contoh perhitungan (padatan sintesis menggunakan suspensi): 1. Bobot Fe awal yang ditimbang = 4 mmol x 56 mg/mmol
= 224 mg 2. Bobot Fe yang terkonversi menjadi padatan
=
21 % Fe dalam padatan =
x 100% = 21.50%
% Hasil sintesis =
x 100% =
x 100% = 98.17%
b) Filtrat 1 minggu
Bobot padatan (teori) =
x 100% = 637.1 mg
% Fe dalam padatan =
x 100% = 34.14%
% Hasil sintesis =
x 100% =
x 100% = 98.89%
Penentuan kadar Co padatan hasil sintesis Padatan
sintesis [Co] (%)
Bobot hasil sintesis (mg)
Bobot Co dalam
padatan (mg) Kadar Co (ppm)
Suspensi 1.7229 x 10-4 990 0.0017 1.7229
Filtrat 7.0277 x 10-4 630 0.0044 7.0277
Contoh perhitungan (suspensi):
Bobot Co dalam padatan =
22
23
24
Rerata % (b/v)
6230.8712 mg/L x
x
= 0.6231g/100 mL
Ammonium (g)
x 36 mL = 0.2243g
Reaksi dekomposisi urea menjadi ammonium CO(NH2)2 + H2O CO2 + 2NH3
Konversi urea menjadi ammonium secara teoritis: Jumlah mmol urea = 12 mmol
Jumlah mmol ammonium = 2 x 12 mmol = 24 mmol
Bobot ammonium yang terbentuk secara teoritis = 24 mmol x Mr ammonium = 24 mmol x 18 g/mol = 0.432 g
Bobot ammonium pada cairan hasil sintesis menggunakan suspensi = 0.2107 g Persentase urea yang terdekomposisi menjadi ammonium pada cairan hasil sintesis menggunakan suspensi:
=
=
x 100% = 48.77%
Bobot ammonium pada cairan hasil sintesis menggunakan filtrat = 0.2243 g Persentase urea yang terdekomposisi menjadi ammonium pada cairan hasil sintesis menggunakan filtrat:
=
=
25
RIWAYAT HIDUP
Penulis dilahirkan di Sukabumi pada tanggal 1 Januari 1990 dari pasangan Ayah Pudin dan Ibu Patimah. Penulis merupakan anak keempat dari empat bersaudara. Pada tahun 2006 penulis lulus dari MTs. Al-Qurthubiyyah, kemudian melanjutkan pendidikan di SMA Negeri 1 Cibadak dan lulus tahun 2009. Selanjutnya pada tahun yang sama penulis diterima di Departemen Kimia Institut Pertanian Bogor melalui jalur Undangan Seleksi Masuk IPB (USMI).