REZANA FALACHI
DEPARTEMEN BIOKIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
ABSTRAK
REZANA FALACHI. Toksisitas Subkronis Ekstrak Etanol 70% Daun Wungu
(
Graptophyllum Pictum (L.) Griff
) pada mencit. Dibimbing oleh EMAN
KUSTAMAN dan DIMAS ANDRIANTO.
Daun wungu (
Graptophyllum pictum
(L.) Griff) merupakan salah satu
tanaman dari famili
Acanthaceae
. Tanaman ini mengandung senyawa alkaloid,
flavonoid, saponin, tanin, dan steroid, serta memiliki aktivitas antidiabetes.
Namun keamanan pengonsumsian tanaman ini belum diuji, sehingga perlu
dilakukan uji toksisitas subkronis secara
in vivo
dan pengamatan histopatologi.
Toksisitas subkronis daun wungu dilakukan selama 3 bulan. Selama perlakuan
mencit dicekok ekstrak daun wungu tiap hari dengan dosis 100 mg/kg, 500 mg/kg,
dan 1000 mg/kg, serta akuades sebagai normal. Pengukuran berat badan mencit
dan pengamatan kematian dilakukan selama penelitian. Bobot badan mencit
selama perlakuan mengalami kenaikan. Ekstrak daun wungu pelarut etanol 70%
tidak diperoleh nilai LD
50toksisitas subkronis. Jumlah kematian kelompok normal
sebanyak 4 ekor, kelompok 100 mg/kg 3 ekor, kelompok 500 mg/kg 2 ekor, dan
kelompok 1000 mg/kg 1 ekor. Pemberian ekstrak daun wungu pelarut etanol 70%
dosis 100 mg/kg dan 500 mg/kg memberikan kerusakan yang cukup parah pada
organ ginjal, jantung, dan paru-paru, serta dosis 1000 mg/kg memberikan
kerusakan pada organ ginjal. Pemberian ekstrak daun wungu pelarut etanol 70%
memberikan efek kerusakan pada beberapa organ.
ABSTRACT
REZANA FALACHI. Subchronic Toxicity of 70% Ethanol Extracts
(Graptophyllum Pictum (L.) Griff) leaf in mice. Under the direction of EMAN
KUSTAMAN dan DIMAS ANDRIANTO.
Graptophyllum pictum
(L.) Griff is one of the family
Acanthaceae
. This
plant contains alkaloid compounds, flavonoids, saponins, tannins, and steroids, as
well as having antidiabetic activity. But consume this plant safely has not been
test, so it needs subchronics toxicity test and histopathological observations. The
subchronics toxicity of
Graptophyllum pictum
(L.) Griff leaf will do for 3 months.
During the treatment of mice give peroral
Graptophyllum pictum
(L.) Griff
extract daily and divide into 4 doses, they are 100 mg/kg, 500 mg/kg, 1000
mg/kg, and distilled water as control. Measurements of mice body weight and
mortality observations made during the study. Mice body weight has increase
during the study.
Graptophyllum pictum
(L.) Griff leaf ethanol extract
doesn’t
give number of LD
50subchronic toxicity. Number of death mice in normal groups
is 4 mice, 100 mg/kg groups is 3 mice, 500 mg/kg group is 2 mice, and 1000
mg/kg is one mice.
Graptophyllum pictum
(L.) Griff leaf ethanol extract for dose
100 mg/kg and 500 mg/kg give damage in histopathology of kidney, heart, and
lung, for dose 1000 mg/kg give damage in histopathology of kidney.
Graptophyllum pictum
(L.) Griff leaf ethanol extract give damage effect in organs.
TOKSISITAS SUBKRONIS EKSTRAK ETANOL 70% DAUN
WUNGU (
Graptophyllum pictum
(L.) Griff) PADA MENCIT
REZANA FALACHI
Skripsi
sebagai salah satu syarat memperoleh gelar
Sarjana Sains pada
Departemen Biokimia
DEPARTEMEN BIOKIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
Judul : Toksisitas Subkronis Ekstrak Etanol 70% Daun Wungu (
Graptophyllum
Pictum
(Linn) Griff) pada Mencit.
Nama : Rezana Falachi
NIM : G84070069
Disetujui
Komisi Pembimbing,
Ir. Eman Kustaman
Dimas Andrianto, M.Si
Ketua
Anggota
Diketahui,
Dr. I Made Artika, M. App. Sc
Ketua Departemen Biokimia
PRAKATA
Puja puji serta syukur penulis ucapkan pada Allah SWT yang telah menjadi
motivasi terbesar penulis untuk menyelesaikan usulan penelitian ini dengan
menciptakan dunia dan semesta alam yang melimpah akan ilmu pengetahuan ini.
Tak lupa pula shalawat serta salam kepada Nabi Muhammad SAW yang telah
menjadi panutan serta pemimpin di dunia ini sehingga penulis dapat termotivasi
dan lancar dalam penyelesaian usulan penelitian ini.
Terima kasih juga penulis ucapkan pada Ir. Eman Kustaman dan Dimas
Andrianto, M.Si atas bantuan dan bimbingannya sehingga penulis dapat
menyelesaikan usulan penelitian ini sebaik mungkin. Penulis juga mengucapkan
terima kasih yang sangat besar pada kedua orang tua penulis yaitu Bapak
Muhammad Tauchid dan Ibu Sofiatul Hanani atas doa dan motivasinya untuk
kelancaran serta kesuksesan penulis. Penulis juga mengucapkan terimakasih
sebesar-besarnya kepada Rama Andhita, Muhammad Taufan, Rezsa Berri, Ganep,
Fitri, Fajri, Ayu dan seluruh sahabat yang telah mendukung dan mendoakan
penelitian penulis, serta Pak Nana, Pak Yadi, Pak Arya, Bu Tini, Bu Tuti, Bu
Merry dan seluruh staf Biokimia IPB yang setia membantu dan memberikan
semangat kepada penulis.
Bogor, Juni 2012
RIWAYAT HIDUP
Penulis dilahirkan di Kota Sidoarjo, Provinsi Jawa Timur pada tanggal 12
Juni 1989 sebagai anak sulung dari 3 bersaudara, pasangan Muhammad Tauchid
dan Sofiatul Hanani.
Penulis lulus dari SMA Negeri 6 kota Bogor tahun 2007 dan pada tahun
yang sama lulus seleksi masuk IPB lewat jalur Seleksi Penerimaan Mahasiswa
Baru (SPMB). Penulis kemudian memilih Mayor Biokimia, FMIPA IPB pada
tahun berikutnya.
Selama perkuliahan, penulis pernah aktif dalam organisasi kemahasiswaan
sebagai staff komisi 3 Dewan Perwakilan Mahasiswa (DPM) FMIPA periode
2008-2009 dan staff departemen sosial dan lingkungan Badan Eksekutif
Mahasiswa (BEM) FMIPA periode 2009-2010. Penulis pernah pula melakukan
praktik lapangan
di Balai Besar Penelitian dan Pengembangan Bioteknologi dan
Sumber Daya Genetik Pertanian Jl. Tentara Pelajar No. 3A Bogor. Praktik lapang
dilakukan mulai bulan Juli hingga Agustus 2010 dan membuat karya ilmiah yang
diberi judul Penapisan Padi Transgenik Penanda Aktivasi Varietas Taipei 309
DAFTAR ISI
Halaman
DAFTAR TABEL ... iv
DAFTAR GAMBAR ... iv
DAFTAR LAMPIRAN ... v
PENDAHULUAN ... 1
TINJAUAN PUSTAKA
Daun Wungu ... 2
Metode Ekstraksi dan Pelarut ... 2
Uji Toksisitas ... 3
Hati ... 3
Ginjal ... 4
Histopatologi ... 4
BAHAN DAN METODE
Bahan dan alat ... 5
Metode ... 5
HASIL DAN PEMBAHASAN
Keadaan Hewan Coba ... 6
Potensi toksisitas subkronis (LD
50) ... 7
Gambaran Histopatologi Ginjal ... 8
Gambaran Histopatologi Hati ... 9
Pengamatan Histopatologi Organ Pendukung ... 10
SIMPULAN DAN SARAN ... 14
DAFTAR PUSTAKA ... 14
DAFTAR TABEL
Halaman
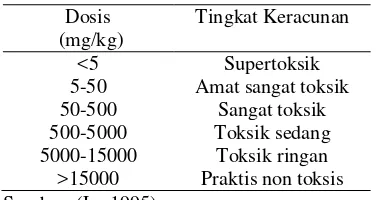
1 Klasifikasi toksisitas ... 3
2 Bobot badan, konsumsi pakan, dan efisiensi ... 6
3 Hasil pengamatan histopatologi ginjal ... 8
4 Hasil pengamatan histopatologi hati ... 10
5 Hasil Pengamatan histopatologi otak ... 11
6 Hasil pengamatan histopatologi usus ... 11
7 Hasil pengamatan histopatologi limpa ... 13
8 Hasil pengamatan histopatologi jantung ... 12
9 Hasil pengamatan histopatologi paru-paru ... 13
DAFTAR GAMBAR
Halaman
1 Daun wungu (
Graptophyllum pictum
(L) Griff) ... 2
2 Bobot badan mencit selama penelitian ... 7
3 Jumlah kematian mencit selama perlakuan ... 7
4 Histopatologi ginjal mencit bulan pertama ... 9
5 Histopatologi hati mencit bulan pertama ... 10
6 Histopatologi otak bulan pertama ... 11
7 Histopatologi usus bulan pertama ... 11
8 Histopatologi jantung bulan pertama ... 12
DAFTAR LAMPIRAN
Halaman
1 Gambaran umum penelitian ... 19
2 Diagram alir uji toksisitas subkronis ... 20
3 Diagram alir histopatologi organ ... 21
4 Redemen ekstrak daun wungu pelarut etanol 70% ... 22
5 Nilai LD
50toksisitas subkronis ... 22
6 Bobot badan mencit selama perlakuan ... 23
PENDAHULUAN
Pengobatan secara modern dirasa sangat mahal, efek samping cukup tinggi dan hasilnya pun belum tentu memuaskan. Keadaan semacam ini memacu pemanfaatan bahan alami untuk memperoleh bahan obat alternatif, salah satunya obat tradisional
(Soedibyo 1998). Tanaman merupakan
sumber utama dalam penemuan obat baru dan alam Indonesia menyediakan sumber alamiah yang belum dimanfaatkan. Penggunaan obat tradisional yang dapat diperoleh dari alam menjadi alternatif penting dalam mencapai kualitas kesehatan masyarakat yang lebih baik (Wahyono 2003). Masyarakat di Indonesia telah lama mengenal dan menggunakan tanaman berkhasiat obat sebagai salah satu upaya menanggulangi masalah kesehatan. Pengetahuan tentang tanaman berkhasiat obat
berdasarkan pada pengalaman dan
keterampilan yang secara turun temurun telah diwariskan dari satu generasi ke generasi berikutnya (Kumalasari 2006). Indonesia memiliki sekurang-kurangnya 9600 spesies tumbuhan berkhasiat sebagai obat dan kurang lebih 300 spesies telah digunakan sebagai bahan obat tradisional oleh industri obat tradisional (Depkes 2007). Menurut Badan POM (2006), 283 spesies tanaman telah
diregistrasi untuk penggunaan obat
tradisional/jamu. Kelebihan dari pengobatan
dengan menggunakan ramuan secara
tradisional tersebut ialah mempunyai efek
samping kecil dibandingkan dengan
pengobatan kimiawi, mudah diperoleh, dan harganya relatif lebih murah (Thomas 1989). Penyembuhan penyakit menggunakan ramuan tradisional membutuhkan waktu yang lama,
tetapi efek yang diberikan bersifat
perlindungan, membangun dan berimplikasi positif terhadap organ lain yang lemah atau
yang kuat. Hal ini berbeda dengan
penyembuhan menggunakan obat kimia, proses kerja lebih cepat sehingga bersifat merusak terhadap organ-organ yang sakit maupun normal (Soenanto 2005).
Salah satu tanaman yang dapat digunakan sebagai obat tradisional adalah tanaman
wungu (Graptophyllum pictum (L.) Griff).
Tumbuhan wungu merupakan salah satu tanaman asli Papua. Tumbuhan wungu sering ditemukan tumbuh liar di pedesaan atau ditanam sebagai tanaman hias dan tanaman pagar. Tumbuh baik pada tempat-tempat terbuka yang terkena sinar matahari, dengan iklim kering atau lembab. Tumbuhan wungu pada bagian daun berkhasiat sebagai peluruh
kencing, mempercepat pemasakan bisul, pencahar ringan, dan pelembut kulit. Hal ini
dikarenakan daun wungu mengandung
senyawa alkaloid yang tidak beracun,
glikosida, steroid, dan saponin (Dalimartha 1999). Ekstrak daun wungu pelarut etanol 70% memiliki inhibisi α-glukosidase sebesar 66,11%, serta mengandung senyawa alkaloid, flavonoid, saponin, tanin, dan steroid (Irwan 2011).
Keamanan daun wungu jika digunakan sebagai pengobatan belum banyak diteliti, sehingga diperlukan uji toksisitas yang dibedakan menjadi uji toksisitas akut, subkronis, dan kronis. Tujuan uji toksisitas adalah untuk mengetahui spektrum efek toksik serta hubungan dosis dan toksisitas pada pemberian berulang dalam jangka waktu tertentu. Umumnya pengukuran toksisitas
dapat dilakukan secara in vivo yang
menggunakan hewan percobaan. Ekstrapolasi hasil uji dari hewan percobaan ke manusia sulit dilakukan namun penggunaan hewan percobaan mempunyai beberapa keuntungan antara lain mudah dilakukan, harganya murah, dan dapat dikontrol (dosis dan lama percobaan), serta pengamatan lebih rinci terhadap semua jaringan (melalui operasi).
Pengamatan dapat dilakukan terhadap
kerusakan hati dan ginjal (Ganong 2003). Pengujian toksisitas akut ekstrak daun wungu tidak memberikan efek yang berbahaya hingga dosis 4000 mg/kg (Olagbende-Dada et al. 2011). Namun pengujian toksisitas subkronis ekstrak daun wungu belum pernah dilakukan. Pemeriksaan toksisitas subkronis
penting dilakukan terutama terhadap
pemakaian obat tradisional atau tanaman obat yang sering digunakan dalam jangka waktu lama (Wahjoedi et al. 1996).
Evaluasi tidak hanya melalui LD50, tetapi
juga dilengkapi dengan pemeriksaan
laboratorium klinik dan pembuatan preparat histopatologi dari organ yang dianggap memperlihatkan kelainan (Darmansjah 1995). Hati dan ginjal merupakan organ yang rentan terhadap pengaruh zat kimia. Kerentanan ini terjadi karena erat fungsinya dalam proses
sirkulasi darah. Hati dapat mudah
berhubungan dengan zat yang diserap dari saluran pencernaan dan ginjal melalui vena porta (Koeman 1987).
Penelitian ini bertujuan untuk menguji
toksisitas subkronik serta mengamati
Gambar 1 Daun wungu (Graptophyllum pictum (L) Griff)
pelarut etanol 70% aman dikonsumsi setelah melewati uji toksisitas subronik. Hal ini diharapkan sebagai informasi awal mengenai keamanan pengonsumsian daun wungu untuk obat yang berkhasiat.
TINJAUAN PUSTAKA
Daun Wungu
Tanaman wungu memiliki sistematika taksonomi yang terdiri dari kingdom Plantae, divisi Spermatophyta, kelas Dicotyledonae, ordo Tubiflorae, famili Acanthaceae, genus Graptophyllum, spesies Graptophyllum pictum (Linn) Griff (Syamsuhidayat dan Hutapea 1991). Tanaman wungu berasal dari Irian dan Polynesia, dapat ditemukan dari dataran rendah sampai pegunungan dengan ketinggian 1250 meter di atas permukaan laut (Heyne 1987). Tanaman wungu sering ditemukan tumbuh liar di pedesaan atau ditanam sebagai tanaman hias dan tanaman pagar. Tumbuh baik pada tempat-tempat terbuka yang terkena sinar matahari, dengan iklim kering atau lembab. Tanaman wungu merupakan tanaman perdu atau pohon kecil, dengan tinggi 1.5-3 m, batang berkayu. Kulit dan daun berlendir dan baunya kurang enak.
Wungu memiliki daun yang letaknya
berhadap-hadapan. Perbungaan majemuk dan tersusun dalam rangkaian berupa tandan yang berwarna merah tua. Tanaman ini memliki 3 varietas, yaitu yang berdaun ungu, hijau, dan belang-belang putih. Namun yang digunakan sebagai obat adalah varietas yang berdaun ungu (Wijayakusuma et al. 1996).
Secara tradisional daun wungu telah
dimanfaatkan sebagai obat luar untuk
mengobati borok, bisul dan kudis. Air rebusan daunnya dapat diminum untuk mengobati penyakit wasir, batu empedu dan penyakit hati. Bunganya bermanfaat sebagai pelancar
haid (Wijayakusuma et al. 1996). Daun
tumbuhan ini mengandung alkaloida yang tidak beracun, glikosida, steroida, dan saponin. Batang daun tumbuhan wungu mengandung kalsium oksalat, asam format, dan lemak (Dalimartha 1999).
Metode Ekstraksi dan Pelarut Ekstraksi merupakan proses pemisahan senyawa campuran dengan menggunakan pelarut yang sesuai. Ekstraksi digunakan untuk mengisolasi produk alam dari jaringan asli kering tumbuh-tumbuhan. Produk alam volatil diisolasi dengan cara distilasi uap, sedangkan produk non volatil diisolasi dengan cara perendaman atau maserasi dalam satu pelarut (Kusnaeni 2008). Secara umum
ekstraksi senyawa metabolit sekunder
menggunakan metode maserasi dengan
pelarut polar atau nonpolar.
Maserasi merupakan proses perendaman sampel pelarut organik yang digunakan pada
temperatur ruangan. Proses ini sangat
menguntungkan dalam isolasi senyawa bahan alam karena dengan perendaman sampel tumbuhan akan terjadi pemecahan dinding dan membran sel akibat perbedaan tekanan antara di dalam dan di luar sel sehingga metabolit sekunder yang ada dalam sitoplasma akan terlarut dalam pelarut organik dan ekstrak senyawa akan sempurna karena dapat diatur lama perendaman yang dilakukan. Pemilihan
pelarut untuk proses maserasi akan
memberikan efektivitas yang tinggi dengan memperhatikan kelarutan senyawa bahan alam pelarut tersebut. Prinsip dari ekstraksi maserasi adalah penyarian zat aktif yang dilakukan dengan cara merendam serbuk dalam cairan penyari yang sesuai selama sehari atau beberapa hari pada suhu kamar dan terlindung dari cahaya (Sudjadi 1986).
Keuntungan dari metode ini adalah
peralatannya yang sederhana, sedang
kerugiannya antara lain, waktu yang
diperlukan untuk mengekstrak sampel cukup lama, cairan penyari yang digunakan lebih banyak, tidak dapat digunakan untuk bahan-bahan yang mempunyai tekstur keras seperti benzoin, tiraks, dan lilin (Taofik 2010).
Kepolaran suatu pelarut menunjukkan tingkat kelarutan pelarut air ataupun pelarut organik terhadap suatu bahan. Kepolaran ini timbul dari perbedaan dua kutub kelarutan. Kecenderungan suatu bahan yang lebih larut dalam air disebut memiliki sifat yang polar dan sebaliknya yang cenderung lebih larut dalam pelarut organik disebut nonpolar (Sudarmadji et al. 2003). Pemilihan pelarut merupakan salah satu faktor yang dapat menentukan kesempurnaan proses ekstraksi. Pelarut yang digunakan pada proses ekstraksi harus dapat menarik komponen aktif dari campuran dalam sampel (Gamse 2002).
Faktor-faktor yang harus diperhatikan
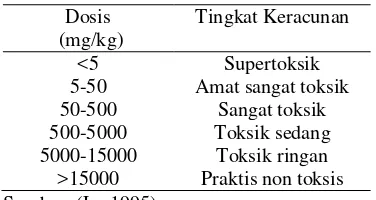
Tabel 1 Klasifikasi toksisitas Dosis
(mg/kg)
Tingkat Keracunan
<5 Supertoksik
5-50 Amat sangat toksik
50-500 Sangat toksik
500-5000 Toksik sedang
5000-15000 Toksik ringan
>15000 Praktis non toksis
Sumber: (Lu 1995) selektivitas, sifat pelarut dan kemampuan
pelarut untuk mengekstraksi, tidak bersifat racun, mudah diuapkan, dan relatif murah (Gamse 2002). Pelarut yang digunakan dalam proses ekstraksi dapat menembus pori-pori bahan padat sehingga bahan yang ingin diekstrak dapat dengan mudah tertarik. Pelarut yang umum digunakan diantaranya, etil asetat, heksana, eter, benzena, toluena, etanol, isopropanol, aseton dan air (Simpen 2008).
Uji Toksisitas
Toksisitas merupakan suatu sifat relatif dari zat kimia dan sejauh menyangkut diri manusia secara langsung atau tidak langsung, mungkin diperlukan atau tidak diperlukan. Namun, toksisitas selalu menunjuk ke suatu efek berbahaya atas mekanisme biologi tertentu (Loomis 1978).
Menurut Loomis (1978), pada umumnya uji toksisitas dapat dibagi menjadi dua golongan yaitu uji toksisitas umum dan toksisitas spesifik. Uji toksisitas umum
meliputi uji toksisitas akut, toksisitas
subkronis, serta toksisitas kronis. Uji
tokisisitas spesifik meliputi uji potensi, teratogenik, reproduksi, mutagenik, dan uji prilaku. Sedangkan Lu (1995) menggolongkan uji toksisitas menjadi tiga jenis berdasarkan lama masa pajanan dengan toksikan, yakni toksisitas akut, toksisitas jangka pendek, dan toksisitas jangka panjang.
Toksisitas subkronik adalah pengaruh yang merugikan pada hewan percobaan yang timbul sebagai akibat pemberian takaran harian berulang dari bahan kimia atau bahan lain, dengan periode pemaparan selama 3 bulan (Deptan 2007). Sekurang-kurangnya digunakan tiga kelompok dosis dan satu kelompok kontrol. Batas uji dosis toksisitas subkronis sebesar 1000 mg/kg bobot badan
(Harmita & Radji 2008). Menurut
Environmental Protection Agency (EPA 1998), LD50 digunakan untuk mengetahui kematian 50% hewan percobaan dalam 24-96
jam. Pengaruh LD50 secara umum diukur
menggunakan dosis bertingkat. Kisaran
tingkat dosis yang digunakan yaitu dosis terendah yang hampir tidak mematikan seluruh hewan percobaan dan dosis tertinggi yang dapat menyebabkan kematian seluruh atau hampir seluruh hewan percobaan. Setiap hewan percobaan akan memberikan reaksi yang berbeda pada dosis tertentu. Perbedaan reaksi akibat pemberian suatu zat diakibatkan oleh perbedaan tingkat kepekaan setiap hewan (Guyton dan Hall 1997). Faktor-faktor
yang berpengaruh terhadap LD50 adalah
spesies, strain, jenis kelamin, umur, berat badan, cara pemberian, faktor lingkungan, kesehatan hewan, dan diet (Balls et al. 1991)
Tingkat keracunan senyawa kimia
berdasarkan nilai LD50 dapat diklasifikasikan seperti pada tabel 1.
Hati
Hati merupakan kelenjar terbesar dan
mempunyai fungsi yang penting bagi
kehidupan. Hati terletak di dalam rongga abdomen sebelah kanan atas di bawah diafragma. (Dyce et al. 2002). Organ ini diselubungi oleh kapsula fibrosa yang dilindungi peritoneum visceral (Martini 1992). Hati mencit terdiri dari 4 lobus yang menyatu pada bagian dorsal, yaitu lobus median yang dibagi menjadi kiri dan kanan oleh bifukatio, lobus lateral kiri, lobus lateral kanan yang dibagi secara horisontal menjadi anterior dan posterior dan lobus kaudal yang terdiri dari bagian dorsal dan ventral (Harada et al. 1999). Secara garis besar, fungsi hati dapat digolongkan menjadi lima besar, yaitu detoksifikasi, sekresi, penyimpanan cadangan makanan, hematologis, proteksi, dan juga
berperan dalam proses metabolisme
biomolekul (karbohidrat, lipid, asam amino, hormon, dan bilirubin) (Kaplan & Pesce 1998). Hati dapat mensintesis lebih dari 1000 protein plasma, seperti albumin dan globulin secara de novo dari asam amino esensial dan non esensial. Hati juga dapat mensintesis
asam lemak, trigliserida, kolesterol,
apolipoprotein, lipoprotein, dan kolesterol ester dalam fosfolipid. Beberapa bahan hasil metabolisme ini dapat tersimpan dalam hati, seperti glikogen, trigliserida, Fe, dan Cu (Stockham & Scott 2002).
Hati merupakan salah satu organ yang terlibat dalam metabolisme zat makanan serta sebagian besar obat dan toksikan. Hepatosit merupakan sel utama yang bertanggung jawab
terhadap peran sentral hati dalam
metabolisme. Organ ini paling umum
saluran pencernaan (Maclachlan & Cullen 1995). Sebagian besar toksikan memasuki tubuh melalui sistem gastrointestinal, dan setelah diserap toksikan dibawa oleh vena porta ke hati. Hati memiliki enzim yang mampu memetabolisme xenobiotik (terutama sitokrom P-450). Hal ini menyebabkan sebagian besar toksikan menjadi kurang toksik dan mudah larut air, sehingga lebih mudah diekskresikan. Toksikan dapat menyebabkan berbagai perubahan pada berbagai organel sel hati, sehingga mengakibatkan perlemakan hati, nekrosis hati, kolestasis, dan sirosis (Lu 1995).
Nekrosis hati adalah kematian sel hati.
Nekrosis dapat bersifat fokal (sentral,
pertengahan, dan perifer) atau masif. Pada
umumnya nekrosa toksopatik hanya
memerlukan waktu singkat untuk
menimbulkan gejala klinis. Biasanya secara histopatologi terlihat nekrosa berkelompok, teratur, dan tersebar di seluruh hati, akan tetapi bila racun sangat kuat maka akan terlihat gambaran nekrosa terpencar. Sirosis
hati adalah suatu keadaan yang
menggambarkan pengerasan hati. Sirosis dapat disebabkan oleh berbagai hal tetapi penyebabnya belum diketahui secara pasti. Pada umumnya bahan-bahan toksik dan parasit dapat menyebabkan sirosis hati (Ressang 1984, Price & Wilson 1995).
Ginjal
Ginjal merupakan organ utama yang berperan terhadap homeostatis air dan elektrolit. Ginjal juga merupakan organ utama yang terkena efek toksisitas jika tubuh terpapar zat toksik. Fungsi utama ginjal adalah
mengeluarkan limbah metabolisme,
memusnahkan bahan toksik, mengatur cairan, garam, keseimbangan asam basa, serta mengatur tekanan darah (Dellmann & Brown 1992). Selain itu ginjal berfungsi memekatkan toksikan pada filtrat dan membawa toksikan melalui tubulus. Ginjal juga memiliki fungsi sebagai penyingkir buangan metabolisme normal dan mengekskresikan xenobiotik dan metabolitnya (Lu 1995). Ginjal juga memiliki fungsi sebagai organ endokrin yang dapat menghasilkan hormon-hormon eritropoetin,
renin, dan prostaglandin (Huminto et al.
1995). Ginjal terletak di retroperitoneum vertebralis lumbalis, dibungkus oleh kapsula yang normalnya dapat bergerak bebas pada permukaannya (Maxie 1993), berpasangan dan berwarna merah kecoklatan. Pada umumnya ginjal berbentuk seperti kacang dengan hillus renalis yaitu tempat masuknya
pembuluh darah dan keluarnya ureter
(Hartono 1992). Ginjal terbagi menjadi dua bagian, yaitu korteks dan medula, dengan perbandingan rata-rata 1 banding 2 atau 1 banding 3 (Maxie 1993), dan ukuran ginjal dalam berbagai spesies sangat ditentukan oleh jumlah nefron (Ganong 2003). Ginjal mencit
bertekstur lembut, berwarna coklat
kemerahan, berada di dorsal dinding tubuh, dikelilingi jaringan lemak dan termasuk unilobular dengan papilla tunggal. Ginjal kanan normalnya berada lebih anterior daripada ginjal kiri dan pada kelamin jantan lebih berat dibandingkan pada kelamin betina (Seely 1999).
Kerusakan yang terjadi pada ginjal dapat bersifat akut atau kronis karena kerusakan permanen (Huminto et al. 1995). Gangguan pada ginjal seperti infeksi ginjal atau masuknya bahan-bahan racun, polutan, dan obat-obatan yang merusak ginjal dapat
menyebabkan terhambatnya proses
pembentukan urin. Gangguan yang paling jelas pada kasus gagal fungsi ginjal adalah kemampuan filtrasi glomerulus menurun. Akibatnya, jumlah urin berkurang, tekanan
darah meningkat dan timbul racun
metabolisme dalam darah, terutama limbah metabolisme nitrogen seperti urea dan kreatinin.
Histopatologi
Histopatologi adalah pemeriksaan
morfologi sel atau jaringan pada sediaan mikroskopik dengan proses pewarnaan untuk menetapkan diagnosis kelainan degenerasi, radang atau infeksi dan neoplasma (Rahayu et al. 2006). Histopatologi merupakan cara utama untuk diagnosis tumor dan juga memberikan informasi tentang prognosisnya dengan cara penilaian tingkat dan stadium
spesimen hasil pembedahan. Diagnosis
histopatologi sebagian besar dilakukan dari potongan jaringan blok parafin dengan
pewarnaan hematoksilin dan eosin
(Underwood 1999).
spesifik dari jaringan. Pewarnaan yang
digunakan pada histopatologi seperti
pewarnaan hematoksilin dan eosin untuk pewarnaan rutin untuk histologi, Masson’s trikhrom untuk jaringan ikat, Perls’ untuk hemosiderin, Ziehl-Neelsen untuk basil tahan asam, Grocott’s silver untuk jamur, dan sebagainya (Underwood 1999).
BAHAN DAN METODE
Bahan dan alat
Bahan-bahan yang digunakan dalam penelitian ini adalah daun wungu yang diperoleh dari Pusat Studi Biofarmaka (PSB)-IPB Bogor, akuades, etanol 70%, Buffer Neutral Formaline (BNF) 10%, etanol 80%, etanol 95%, etanol absolut, xilol, Mayer’s Haematoxylin, LiCl, pewarna Eosin, dan permounting medium.
Alat-alat yang dipakai adalah corong kaca, kertas saring, labu Erlenmeyer, gelas piala, pipet mikro, pipet volumetrik, pipet tetes, rotavapour, Tissue Tec, oven, preparat, mikroskop cahaya, dan kamera.
Metode
Ekstraksi Daun Wungu (BPOM 2005) Daun wungu yang telah didapat, diproses dengan dua tahapan, preparasi dan ekstraksi. Daun wungu (Graptophyllum pictum (L.) Griff) dikeringkan dalam oven dengan suhu 40-50°C selama 5 hari. Simplisia daun wungu yang sudah kering kemudian digiling hingga berukuran 100 mesh dan berbentuk serbuk (dengan kadar air ≤ 10 %). Sampel yang berbentuk serbuk dilanjutkan dengan metode
ekstraksi yang mengacu pada Badan
Pengawas Obat dan Makanan atau BPOM (2005) yaitu maserasi. Maserasi sampel dilakukan dengan merendam sampel dalam etanol 70% dengan perbandingan 1:10, proses ini dilakukan dalam maserator selama 6 jam dan sesekali diaduk. Kemudian sampel tersebut didiamkan selama 24 jam, maserat yang didapat, dipisahkan. Keseluruhan sampel
dihilangkan pelarutnya dalam rotavapour
pada suhu 40°C dan dihasilkan ekstrak kering. Ekstraksi maserasi penelitian ini (lampiran 4) diperoleh rendemen rata-rata ekstrak kering daun wungu pelarut etanol 70% sebesar 5,14% ± 1,31.
Uji Toksisitas Subkronik (Gad 2007) Toksisitas subkronis dilakukan dengan menggunakan mencit galur ddY dengan umur 2 bulan, selama 3 bulan yang terdiri dari 4 kelompok. Mencit dikelompokkan secara acak
dengan mempertimbangkan keseragaman
bobot badan. Jumlah ulangan uji toksisitas subkronik setiap kelompok terdiri atas 10 mencit jantan (Gad 2007). Kelompok normal yaitu tanpa menerima ekstrak daun wungu dan hanya diberi akuades. Kelompok perlakuan memperoleh cekokan ekstrak daun wungu pelarut etanol 70% dengan dosis 100 mg/kg, dosis 500 mg/kg, dan dosis 1000 mg/kg (lampiran 7). Perlakuan tersebut dilakukan setiap hari. Kerusakan hati, ginjal dan organ-organ pendukung akan diuji setiap bulan terhadap kerusakan secara histopatologi. Air
minum diberikan secara ad libitum dan
dilakukan pengukuran bobot badan dan konsumsi pakan selama perlakuan diberikan.
Pembuatan Preparat Histopatologi Hati, Ginjal, Jantung, Otak, Limpa, Paru-paru, dan Usus (Humason 1972; Kiernan 1990)
Metode yang digunakan adalah metode Humason (1972) dan Kiernan (1990) yang terdiri atas 4 tahap, yaitu fiksasi, dehidrasi, pencetakan (embedding), dan pewarnaan (staining). Tahap fiksasi dilakukan dengan memotong organ hati dan ginjal dengan ukuran 2x2x1 cm, dimasukkan ke dalam buffer neutral formalin (BNF) 10% selama 3x24 jam, kemudian dipotong lagi dengan ukuran lebih tipis. Potongan-potongan hati tersebut dilanjutkan ke tahap dehidrasi, yaitu dengan perendaman menggunakan etanol bertingkat (etanol 70%, 80%, 96%, absolut I, absolut II). Kemudian etanol dihilangkan dengan xilol I, II, dan III masing-masing selama 40 menit. Infiltrasi menggunakan parafin cair dilakukan pada suhu 60°C selama 4 kali masing-masing selama 30 menit. Sebelum pencetakan cetakan dicuci dengan campuran etanol 96%, xilol, dan air.
Pencetakan dilakukan dengan penuangan parafin panas dalam blok cetakan sebanyak setengah cetakan dengan alat Tissue Tec. Potongan hati dan ginjal dimasukan ke dalamnya perlahan agar tidak menyentuh dasar cetakan lalu ditutup lagi dengan parafin cair. Setelah beku organ dalam parafin tersebut dipotong dengan alat mikrotom setebal 4-5 um. Potongan yang diperoleh dimasukkan ke dalam air hangat (40°C) untuk melelehkan parafin, kemudian diletakkan dalam kaca objek. Potongan tadi dikeringkan dalam oven inkubator bersuhu 56°C selama satu malam.
Tahap pewarnaan Haematoxylin Eosin
Tabel 2 Bobot badan, konsumsi pakan, dan efisiensi
Kelompok Pertambahan bobot
badan (gram/har)i
Konsumsi pakan (gram/hari)
Efisiensi (%)
Normal 0,15 3,59 4,17
100 mg/kg 0,09 3,66 2,45
500 mg/kg 0,14 3,69 3,8
1000 mg/kg 0,16 3,81 4,2
dengan etanol absolut selama 2 menit, kemudian dengan etanol 95% dan 80% masing-masing selama 1 menit, dan dicuci dengan air mengalir. Kemudian preparat
direndam dalam pewarnaan Mayer’s
Haemotoxylin selama 8 menit, dicuci dengan air mengalir, dimasukkan ke dalam LiCl selama 30 detik, dan dicuci kembali dengan air mengalir. Kemudian irisan preparat diberi pewarna eosin selama 2-3 menit, lalu dicuci. Setelah itu, irisan hati dicelupkan dalam etanol 95% dan absolut I masing-masing sebanyak 10 kali dan diteruskan dengan etanol absolut II selama 2 menit, xilol I selama 1 menit dan xilol II selama 2 menit. Setelah diangin-anginkan beberapa saat, preparat yang telah diwarnai tersebut kemudian diberi permounting medium dan ditutup dengan kaca penutup. Setelah terbentuk sediaan histologi, kemudian dilakukan analisis dan pengamatan terhadap perubahan yang terjadi pada sel-sel hati dengan menggunakan mikroskop cahaya dan difoto hasil pengamatannya. Pembuatan
dan pengamatan histopatologi organ
dilakukan oleh BALITVET.
HASIL DAN PEMBAHASAN
Keadaan Hewan Coba
Selama perlakuan secara in vivo, salah satu syarat pada perlakuan hewan coba adalah kondisi hewan harus dalam keadaan sehat. Beberapa parameter yang mudah diamati untuk mengetahui kesehatan hewan coba adalah dengan mengamati peningkatan bobot badan dan konsumsi pakan (Lu 1995). Kondisi tikus yang sehat ini menjadi faktor yang penting karena dapat memperkecil nilai galat percobaan yang terukur ketika memasuki tahap percobaan. Gambar 2 menunjukkan grafik bobot badan hewan coba pada masa adaptasi dan masa perlakuan. Selama masa adaptasi, hewan coba memiliki bobot badan 18 gram hingga 20 gram. Memasuki masa perlakuan terjadi kenaikan bobot badan mencit seluruh kelompok. Pada kelompok 500 mg/kg dan 1000 mg/kg mengalami kenaikan yang signifikan pada bulan kedua. Kenaikan bobot badan mencit seluruh kelompok selama
masa perlakuan merupakan respon
pertumbuhan, khususnya kelompok perlakuan yang mengalami kenaikan lebih tinggi dibandingkan kelompok normal. Hal ini dipengaruhi pula pada konsumsi pakan dan air minum. Tabel 2 menunjukkan pertambahan bobot badan seluruh kelompok mencit per hari selama masa perlakuan, kelompok dosis 500
mg/kg dan 1000 mg/kg mengalami
pertambahan bobot badan sebesar 0,14 gram/ hari dan 0,16 gram/ hari, hal ini tidak berbeda nyata dengan kelompok normal yang memiliki pertambahan bobot badan sebesar 0,15 gram/ hari. Namun kelompok 100 mg/kg mengalami pertambahan bobot badan paling kecil, hal ini dapat dipengaruhi oleh faktor lingkungan dan kondisi mencit tersebut yang menyebabkan naik turunnya bobot mencit per hari. Menurut Smith dan Mangkoewidjojo (1988), bahwa rata-rata pertumbuhan bobot mencit sebesar 1 gram/hari. Hasil penelitian Hadian (2004) menunjukkan rata-rata pertambahan bobot badan mencit umur 3-8 minggu sebesar 0,49 g/hari.
Kenaikan bobot badan mencit dipengaruhi oleh konsumsi pakan yang meningkat tiap bulannya. Pakan yang digunakan adalah pakan standar tikus berasal dari perusahaan Indofeed Bogor. Menurut Priambodo (1995), kebutuhan pakan bagi seekor tikus putih setiap harinya kurang lebih sebanyak 10% dari bobot tubuhnya, jika pakan tersebut merupakan pakan kering. Konsumsi pakan mencit perhari berdasarkan tabel 2 sebesar 3,8 gram. Menurut Smith dan Mangkoewidjojo (1988), bahwa seekor mencit dewasa dapat mengkonsumsi pakan 3-5 gram/hari. Malole dan Pramono (1989) menyatakan bahwa tingkat konsumsi makanan dan minuman pada seekor mencit akan bervariasi menurut suhu kandang, kelembaban, kualitas makanan, kesehatan dan kadar air dalam makanan.
Efisiensi penggunaan pakan merupakan
Gambar 2 Bobot badan mencit selama penelitian, (----) normal, (----) 100 mg/kg, (----) 500 mg/kg, (----) 1000 mg/kg, (A) masa adaptasi, (B) masa perlakuan
0 5 10 15 20 25 30 35 40
-2 -1 0 1 2 3 4 5 6 7 8 9 10 11 12 13 14
B o b o t B ad an (g) Minggu
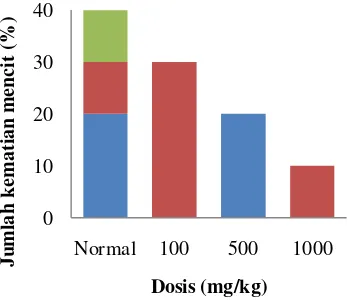
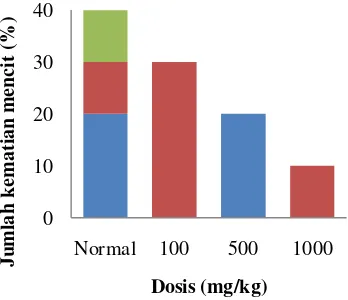
Ke-Gambar 3 Jumlah kematian mencit selama perlakuan, ■ bulan ke-1, ■ bulan ke-2,
■ bulan ke-3 0
10 20 30 40
Normal 100 500 1000
Ju m lah k e m ati an m e n c it (% ) Dosis (mg/kg) yang sedikit akan dihasilkan pertambahan
bobot badan yang tinggi. Keefisienan pakan mencit berdasarkan tabel 2, kelompok normal sebesar 4,17%, kelompok 100 mg/kg memiliki
efisiensi terendah sebesar 2,45% dan
kelompok 1000 mg/kg memiliki efisiensi tertinggi sebesar 4,2%. Keefisienan pakan dipengaruhi oleh kondisi mencit, pakan, dan lingkungan.
Potensi toksisitas subkronis (LD50) Ekstrak daun wungu pelarut etanol 70%
memiliki kandungan senyawa alkaloid,
flavonoid, saponin, tanin, dan steroid (Irwan 2011). Uji toksisitas akut ekstrak daun wungu tidak memberikan efek racun hingga dosis 4000 mg/kg. Nilai LD50 toksisitas akut tidak dapat dihitung, hal ini dikarenakan tidak
adanya kematian hewan coba seluruh
kelompok selama masa perlakuan
(Olagbende-Dada et al. 2011). Sehingga
diperlukan uji toksisitas subkronis untuk mengetahui efek racun yang terdapat pada tanaman obat dalam jangka waktu lama. Gambar 3 menunjukkan jumlah kematian mencit selama masa perlakuan, kelompok normal memiliki jumlah kematian lebih banyak dibandingkan dengan kelompok perlakuan. Kondisi beberapa organ mencit kelompok normal pada masa perlakuan berdasarkan hasil histopatologi mengalami gangguan yaitu pada organ ginjal, jantung, dan paru-paru. Organ ginjal mengalami gangguan kongesti dan nekrosis tubulus.
Organ jantung mengalami gangguan
degenerasi serabut otot dan kongesti. Dan
organ paru-paru mengalami gangguan
bronkopneumonia dan infiltrasi sel
mononuklear. Gangguan yang terjadi pada organ ginjal dan jantung disebabkan oleh zat toksik (Lu 1995), sedangkan gangguan pada organ paru-paru disebabkan oleh virus (Hunter 2006). Kematian kelompok normal dapat disebabkan oleh kerusakan yang terjadi pada organ jantung dan paru-paru. Kerusakan yang terjadi dapat diakibatkan oleh faktor lingkungan. Menurut Malole dan Pramono (1989) bahwa temperatur kandang yang ideal untuk mencit adalah 18-29oC dengan rataan
22oC dan kelembaban relatif 30-70%.
Kandang tidak boleh ditempatkan pada area B
Tabel 3 Hasil pengamatan histopatologi ginjal untuk berbagai kelompok
Kelompok Bulan Ke-
1 2 3
Normal Kongesti Nekrosis
tubulus Kongesti
100 mg/kg TAKS TAKS Kongesti
500 mg/kg Kongesti Nekrosis
tubulus Kongesti
1000
mg/kg Kongesti
Nekrosis
tubulus Kongesti
TAKS: Tak ada kelainan spesifik yang bising dan harus memiliki pertukaran
udara yang baik, kelembaban yang baik serta bebas dari debu. Mencit lebih menyukai tempat yang gelap (Rakhmadi 2008). Alas kandang berupa serbuk kayu merupakan salah satu faktor berkembang baiknya mencit selama penelitian karena alas kandang harus non alergi, bebas debu, nontoksik dan kering untuk mencegah timbulnya gangguan berupa bau dan iritasi selaput lendir. Alas kandang pada mencit berfungsi sebagai tempat untuk melakukan aktivitas sehari-hari seperti tempat tidur, tempat beranak dan tempat membuang kotoran (Malole dan Pramono 1989). Menurut Rakhmadi (2008), bahwa penyediaan sekat alas kandang atau roda kawat pada kandang dapat melatih mencit untuk lebih aktif bergerak dan bermain. Sebaliknya, kondisi mencit pada kandang tanpa sekat terlihat tidak terlalu aktif. Kegiatan mencit lebih banyak digunakan untuk makan dan tidur. Bulu terlihat agak kusam karena bersentuhan langsung dengan alas yang sudah kotor bahkan ada beberapa mencit yang menjadi rontok bulu. Menurut Blackley dan David (1991), kondisi lingkungan yang baik dan sesuai dengan kebutuhan ternak dapat menurunkan angka mortalilas. Mortalitas mencit dipengaruhi oleh kualitas pakan,
kepekaan terhadap penyakit, suhu,
kelembaban, dan manajemen pemeliharaan mencit.
Gambar 3 juga menunjukkan bahwa jumlah kematian kelompok dosis 100 mg/kg lebih banyak dibandingkan dengan kelompok dosis 1000 mg/kg. Hal ini tidak sesuai dengan pernyataan Guyton dan Hall (1997) bahwa kisaran tingkat dosis yang digunakan yaitu dosis terendah yang hampir tidak mematikan seluruh hewan percobaan dan dosis tertinggi yang dapat menyebabkan kematian seluruh atau hampir seluruh hewan percobaan. Hasil histopatologi menunjukkan bahwa terdapat kerusakan pada organ ginjal, paru-paru, dan jantung khususnya pada kelompok 100 mg/kg dan 500 mg\/kg, yang menyebabkan jumlah kematiannya lebih banyak dibandingkan
kelompok 1000 mg/kg. Perhitungan LD50
berdasarkan persamaan garis diperoleh nilai LD50 toksisitas subkronis ekstrak daun wungu pelarut etanol 70% sebesar 0,04 mg/kg (lampiran 5), namun hasil perhitungan ini tidak dapat dijadikan acuan. Hal ini dikarenakan jumlah kematian pada kelompok 100 mg/kg lebih banyak dibandingkan dengan kelompok 1000 mg/kg, serta kelompok normal yang memiliki jumlah kematian lebih banyak dibandingkan kelompok perlakuan.
Sehingga nilai LD50 toksisitas subkronis ekstrak daun wungu pelarut etanol 70% tidak dapat diperoleh.
Gambaran Histopatologi Ginjal Ginjal merupakan organ utama yang terkena efek toksisitas jika tubuh terpapar zat
toksik. Fungsi utama ginjal adalah
mengeluarkan limbah metabolisme,
memusnahkan bahan toksik, mengatur cairan garam, keseimbangan asam basa, serta mengatur tekanan darah (Dellmann & Brown 1992). Hasil pengamatan histopatologi ginjal mencit selama masa perlakuan berdasarkan tabel 3 menunjukkan bahwa kondisi ginjal pada kelompok normal mengalami kongesti dan nekrosis tubulus. Kongesti adalah suatu keadaan adanya darah yang berlebihan di dalam pembuluh pada daerah tertentu.
Kongesti pada pembuluh darah dapat
berlangsung sesaat atau kongesti akut, atau dapat berlangsung lama atau kongesti kronis. Jika kongesti berlangsung sesaat, maka tidak ada pengaruh pada jaringan tersebut. Kongesti kronis, terdapat perubahan-perubahan yang permanen dalam jaringan. Keadaan tersebut memungkinkan terjadinya hipoksia jaringan yang dapat mengakibatkan penyusutan atau hilangnya sel-sel dari jaringan (Price and Wilson 1988). Masuknya suatu substansi toksik ke dalam tubuh dalam waktu yang lama akan menyebabkan nekrosis tubulus ginjal (Runnels et al. 1965). Tubulus proksimal merupakan bagian yang paling mudah mengalami perlukaan akibat iskemia dan zat toksik. Hal ini dikarenakan pada tubulus proksimal terjadi proses absorbsi dan sekresi (Lu 1995).
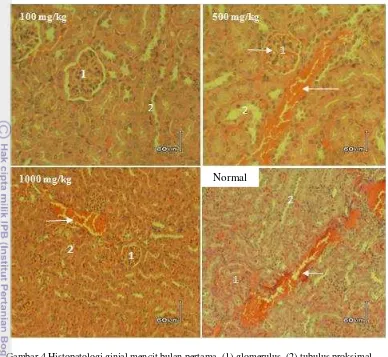
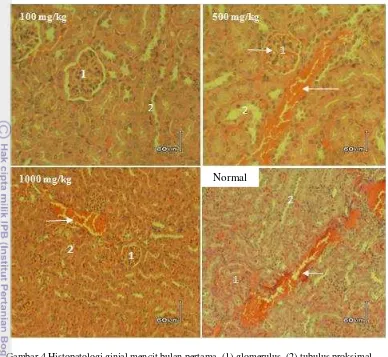
Kondisi ginjal pada kelompok perlakuan tidak berbeda nyata dengan kondisi ginjal kelompok normal (Gambar 4), terjadi kongesti dan nekrosis tubulus selama perlakuan.
Kongesti dan nekrosis tubulus dapat
Gambar 4 Histopatologi ginjal mencit bulan pertama, (1) glomerulus, (2) tubulus proksimal, () kongesti
masa perlakuan, pada bulan ketiga terjadi kongesti. Kelompok 500 mg/kg dan 1000 mg/kg mengalami kongesti dan nekrosis
tubulus, nekrosis tubulus organ ginjal
diindikasikan sebagai salah satu faktor
penyebab kematian mencit, hal ini
ditunjukkan pada gambar 3 bahwa jumlah kematian terbanyak terjadi pada bulan kedua masa perlakuan. Pada kerusakan sel epitel tubuli terjadi akibat masuknya toksin yang menyebabkan kerusakan membran sel, yang ditandai dengan penurunan ATP untuk penyediaan energi. Dalam hal ini ATP dibutuhkan untuk proses reabsorpsi zat-zat dan cairan dalam tubulus. Kerusakan pada membran sel akan menurunkan produksi ATP
yang dihasilkan di mitokondria dan
pengurangan pompa sodium, sehingga
keseimbangan pengaturan ion
sodium-potasium intraselular terganggu (Cheville
2006). Kegagalan dalam mengatur
keseimbangan ion sodium intraselular
mengakibatkan masuknya sejumlah cairan secara berlebih ke dalam sel. Peningkatan cairan intraselular tersebut menyebabkan
kebengkakan pada sel, termasuk mitokondria dan retikulum endoplasmik kasar (Jones et al. 2006). Pada sel yang mengalami kerusakan tersebut dinamakan degenerasi hidropis epitel
tubuli. Adanya gangguan pada tubuli
mengakibatkan daya selektifitas tubuli
menurun sehingga mempengaruhi
homeostasis tubuh (Hatzios 2005). Sehingga, semakin lama pemberian ekstrak daun wungu dan semakin besar dosis yang digunakan, akan memberikan efek kerusakan pada organ ginjal.
Gambaran Histopatologi Hati Hati merupakan salah satu organ yang terlibat dalam metabolisme zat makanan serta sebagian besar obat dan toksikan. Organ ini paling umum mengalami kerusakan karena racun. Hal ini disebabkan hati menerima suplai darah dari vena porta sekitar 80% yang mengalir dari saluran pencernaan (Maclachlan & Cullen 1995). Hasil uji histopatologi hati mencit selama perlakuan berdasarkan tabel 4 menunjukkan bahwa kondisi hati kelompok normal tidak mengalami kelainan spesifik
Tabel 4 Hasil pengamatan histopatologi hati untuk berbagai kelompok
Kelompok Bulan ke-
1 2 3
Normal TAKS TAKS TAKS
100 mg/kg PMN TAKS PMN
500 mg/kg PMN TAKS TAKS
1000 mg/kg PMN TAKS TAKS
TAKS : Tak ada kelainan spesifik PMN : Polimorfonuklear
Gambar 5 Histopatologi hati mencit bulan pertama, (1) polimorfonuklear, (2) vena centralis, (3) portal tract
selama perlakuan. Kondisi hati pada
kelompok perlakuan tidak memberikan
kerusakan yang berarti terhadap organ, namun terjadi efek yang diakibatkan pemberian ekstrak daun wungu, yaitu terdapatnya sel polimorfonuklear (Gambar 5). Bulan pertama perlakuan pada seluruh kelompok perlakuan terdapat sel polimorfonuklear. Sel ini timbul diakibatkan oleh masuknya zat asing ke dalam tubuh seperti ekstrak daun wungu yang menyebabkan terjadinya radang akut hingga
terjadinya luka pada organ hati. Sel
polimorfonuklear termasuk sel neutrofil, yaitu sel pertahanan pertama terhadap kontaminasi mikroba pada peradangan. Fungsi neutrofil adalah membersihkan daerah luka dari benda asing, bakteri (Singer dan Clark 1999) fungi, protozoa, virus dan sel-sel yang rusak atau mati (McGavin dan Zachary 2007). Neutrofil dibentuk di dalam sumsum tulang belakang (Tizard 1988). Bulan kedua dan ketiga seluruh kelompok perlakuan tidak ada kelainan spesifik pada organ hati. Pemberian ekstrak daun wungu pelarut etanol 70% tidak memberikan kerusakan yang berarti pada organ hati, hal ini didukung dengan kondisi
organ hati kelompok normal yang tidak mengalami kelainan spesifik.
Pengamatan Histopatologi Organ Pendukung
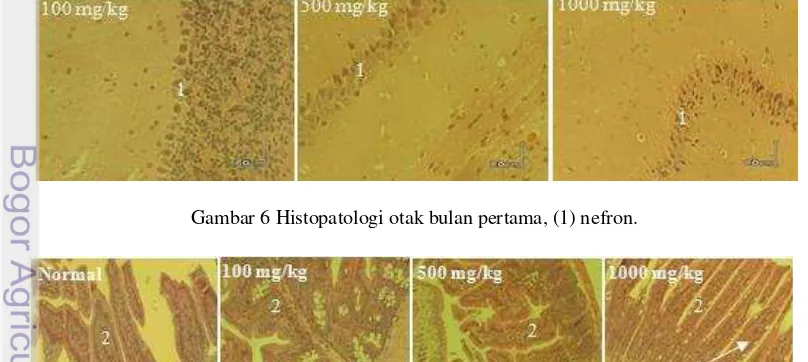
Gambar 6 Histopatologi otak bulan pertama, (1) nefron.
Gambar 7 Histopatologi usus bulan pertama, (1) sel goblet, (2) vili mukosa Tabel 6 Hasil pengamatan histopatologi
usus untuk berbagai kelompok
Kelompok Bulan ke-
1 2 3
Normal Sel
goblet TAKS (-)
100 mg/kg Sel
goblet
Payer
patches TAKS
500 mg/kg Sel
goblet TAKS (-)
1000 mg/kg Sel
goblet TAKS
Payer patches
TAKS: Tak ada kelainan spesifik (-): Tidak dilakukan
Tabel 5 Hasil Pengamatan histopatologi otak untuk berbagai kelompok
Kelompok Bulan ke-
1 2 3
Normal TAKS TAKS TAKS
100 mg/kg TAKS TAKS TAKS
500 mg/kg TAKS TAKS TAKS
1000 mg/kg TAKS TAKS TAKS
TAKS: Tak ada kelainan spesifik
tidak mengalami kelainan spesifik selama perlakuan. Kondisi otak pada kelompok perlakuan tidak berbeda nyata dengan kelompok normal (gambar 6). Pemberian ekstrak daun wungu pelarut etanol 70% tidak memberikan kerusakan yang berarti terhadap organ otak.
Usus halus merupakan bagian dari sistem pencernaan yang berfungsi mencerna dan menyerap zat-zat makanan seperti asam amino, lipid dan monosakarida (Banks 1993). Fungsi utama usus halus adalah absorbsi mikronutrien, mineral dan vitamin. Beda lokasi usus halus, berbeda pula jenis mikronutrien yang diabsorbsi (Kandi 2008). Pengamatan histopatologi organ usus mencit
kelompok normal selama perlakuan
berdasarkan tabel 6, timbulnya sel goblet pada bulan pertama, dan tidak ada kelainan spesifik pada bulan kedua dan ketiga.
Kondisi usus pada kelompok perlakuan tidak mengalami kerusakan yang berarti, namun terjadi beberapa efek yang diakibatkan pemberian ekstrak daun wungu pelarut etanol 70% (gambar 7). Efek yang ditimbulkan
seperti terjadinya sel goblet dan payer
patches. Kelompok perlakuan di bulan pertama terdapat banyak sel goblet. Sel goblet timbul akibat dari pemberian ekstrak daun wungu pelarut etanol 70%. Salah satu komponen pertahanan usus halus dan usus besar adalah sel goblet, yang menghasilkan mukus dan berfungsi untuk mengeluarkan benda atau zat asing yang masuk (Ardyanti 2006). Bulan kedua pada kelompok 100 mg/kg terdapat payer patches. Payer patches adalah sekelompok sel goblet yang berada pada folikel getah bening dan membentuk daun payer (Murray et al. 1999). Bulan ketiga pada kelompok 100 mg/kg tidak ada kelainan
spesifik. Sel Goblet dan payer patches
Tabel 7 Hasil pengamatan histopatologi jantung mencit untuk berbagai kelompok
Kelompok Bulan ke-
1 2 3
Normal De-generasi serabut otot Kongesti De-generasi serabut otot 100
mg/kg TAKS
De-generasi serabut otot De-generasi serabut otot 500 mg/kg De-generasi serabut otot De-generasi serabut otot De-generasi serabut otot 1000
mg/kg TAKS TAKS TAKS
TAKS: Tak ada kelainan spesifik
Gambar 8 Histopatologi jantung bulan pertama, (1) degenerasi serabut otot, (2) serabut otot payer patches. Bulan kedua dan ketiga
kelompok 500 mg/kg tidak mengalami kelainan spesifik pada organ usus. Kelompok 1000 mg/kg tidak mengalami kelainan spesifik pada bulan kedua dan pada bulan ketiga terjadi payer patches di organ usus. Pemberian ekstrak daun wungu pelarut etanol 70% berbagai dosis tidak memberikan kerusakan yang berarti pada usus namun memberikan efek dari pemberian ekstrak, hal ini mengakibatkan munculnya sel goblet dan payer patches yang sifatnya sementara.
Jantung adalah sebuah organ berotot dengan empat ruang yang terletak di rongga dada, dibawah perlindungan tulang iga, sedikit ke posisi kiri sternum. Jantung terdapat di dalam sebuah kantong longgar berisi cairan yang disebut perikardium. Keempat ruang jantung adalah atrium kiri dan kanan serta ventrikel kiri dan kanan (Corwin 2001). Pengamatan histopatologi jantung mencit berdasarkan tabel 7 menunjukkan bahwa kondisi jantung kelompok normal mengalami degenerasi serabut otot dan kongesti (gambar
8). Degenerasi merupakan perubahan
morfologi tidak berakibat fatal dan masih
dapat pulih. Degenerasi menyebabkan
gangguan pada metabolisme karbohidrat, protein, dan lemak pada sel (MacKenzie & Alison 1990). Kongesti adalah keadaan di mana terdapat darah secara berlebihan di dalam pembuluh darah pada daerah tertentu (Ressang 1984).
Kondisi jantung pada kelompok 100 mg/kg dan 500 mg/kg mengalami degenerasi serabut otot selama perlakuan, namun kelompok 1000 mg/kg tidak mengalami
kelainan spesifik pada organ jantung.
Pemberian ekstrak daun wungu pelarut etanol 70% dapat menyebabkan terjadinya kerusakan pada organ jantung. Jantung yang mengalami kelemahan karena degenerasi otot tidak dapat
berkontraksi secara normal sehingga
menyebabkan pemompaan darah tidak
sempurna. Akibatnya, pembuluh darah
jantung tidak terisi cukup darah sehingga tekanan darah turun. Penurunan tekanan darah secara cepat mengakibatkan berkurangnya
suplai darah sehingga menimbulkan kondisi hipoksia, yang akhirnya menyebabkan daya kerja jantung semakin melemah (Carlton & McGavin 1995). Menurut Lu (1995), jantung mudah dirusak oleh berbagai jenis zat kimia karena merupakan salah satu organ sasaran. Zat kimia bekerja secara langsung atau tidak langsung pada otot jantung melalui susunan saraf atau pembuluh darah. Suatu toksikan dapat mempengaruhi salah satu dari pembuluh darah dan akibat yang ditimbulkan tergantung dari seberapa penting organ yang disuplai darah oleh pembuluh darah yang terkena.
Gambar 9 Histopatologi paru-paru bulan pertama, (1) alveol, (2) pneumonia dan infiltrasi sel mononuklear, (3) infiltrasi sel mononuklear
Tabel 9 Hasil pengamatan histopatologi paru-paru mencit untuk berbagai kelompok
Kelompok Bulan ke-
1 2 3
Normal TAKS
Bronko pneumonia dan infiltrasi sel
mononuklear
TAKS
100 mg/kg
Pneumonia dan infiltrasi sel mononuklear
Pneumonia dan infiltrasi sel mononuklear
Edema, hiperemia, dan infiltrasi sel
mononuklear
500 mg/kg Infiltrasi sel
mononuklear Edema pulmonum
Edema pulmonum dan infiltrasi sel
mononuklear
1000 mg/kg TAKS TAKS Edema
TAKS: Tak ada kelainan spesifik
Tabel 8 Hasil pengamatan histopatologi limpa mencit untuk berbagai kelompok
Kelompok Bulan ke-
1 2 3
Normal TAKS TAKS TAKS
100 mg/kg (-) TAKS TAKS
500 mg/kg (-) TAKS
Deplesia pulpa merah 1000
mg/kg (-) TAKS TAKS
TAKS : Tak ada kelainan spesifik (-) : Tidak dilakukan
perlakuan tidak berbeda nyata dengan kelompok normal yang tidak ada kelainan spesifik. Pemberian ekstrak daun wungu pelarut etanol 70% tidak memberikan efek kerusakan yang berarti terhadap organ limpa.
Pengamatan histopatologi organ paru-paru mencit berdasarkan tabel 9 menunjukkan bahwa kondisi paru-paru kelompok normal mengalami bronkopneumonia dan infiltrasi sel
mononuklear. Bronkopneumonia adalah
terjadinya pneumonia pada bagian
bronkiolitis. Pneumonia terjadi akibat respon inflamasi terhadap mikroorganisme pada parenkim paru normal (Hunter 2006).
Infiltrasi sel mononuklear merupakan salah satu sistem pertahanan dari zat asing yang dimiliki organ paru-paru. Infiltrasi sel
mononuklear muncul akibat adanya
bronkopneumonia.
Kondisi paru-paru kelompok perlakuan
mengalami pneumonia, infiltrasi sel
(Ressang 1984). Adanya edema dan hiperemia
menyebabkan terjadinya infiltrasi sel
mononuklear, sel ini merupakan sel
pertahanan paru-paru untuk membersihkan luka yang diakibatkan oleh zat asing. Kelompok 500 mg/kg mengalami edema selama masa perlakuan. Edema terjadi akibat dari kongesti yang berkelanjutan, saat kondisi vena yang terbendung (kongesti), maka terjadi peningkatan tekanan hidrostatik intravaskular yang menimbulkan perembesan cairan plasma ke dalam ruang interstitium. Cairan plasma ini akan mengisi pada sela-sela jaringan ikat longgar dan rongga badan, sehingga terjadi edema (Marchelinda 2011). Pemberian ekstrak daun wungu pelarut 70% menyebabkan kongesti hingga terjadi edema. Edema juga terjadi pada kelompok 1000 mg/kg pada bulan ketiga. Pemberian ekstrak daun wungu pelarut etanol 70% dalam waktu lama akan memberikan efek kerusakan pada organ paru-paru.
Pemberian ekstrak daun wungu pelarut etanol 70% memberikan efek kerusakan pada beberapa organ pendukung. Kelompok 100 mg/kg dan 500 mg/kg mengalami kerusakan pada organ jantung dan paru-paru. Sedangkan kelompok 1000 mg/kg tidak memberikan efek kerusakan yang berarti terhadap histopatologi beberapa organ pendukung.
SIMPULAN DAN SARAN
Simpulan
Ekstrak daun wungu pelarut etanol 70% tidak diperoleh nilai LD50 toksisitas subkronis. Pemberian ekstrak daun wungu pelarut etanol 70% dosis 100 mg/kg dan 500 mg/kg memberikan kerusakan pada organ ginjal, jantung, dan paru-paru, serta dosis 1000 mg/kg hanya memberikan kerusakan pada organ ginjal. Pemberian ekstrak daun wungu pelarut etanol 70% memberikan kerusakan pada beberapa organ.
Saran
Perlu dilakukan penelitian lanjutan untuk mengetahui tingkah laku, berat organ, nilai
LD50, dan menggunakan hewan coba
terstandar, serta fasilitas kandang yang lebih baik.
DAFTAR PUSTAKA
[BPOM RI] Badan Pengawas Obat dan Makanan Republik Indonesia. 2005.
Gerakan Nasional Minum Temulawak. Jakarta : BPOM RI.
[BPOM RI] Badan Pengawasan Obat dan Makanan Republik Indonesia. 2006. Monograf Ekstrak Tanaman Obat Indonesia. Jakarta: BPOM RI.
[Depkes] Departemen Kesehatan Republik Indonesia. 2007. Keputusan Menteri Kesehatan Republik Indonesia nomor
381/Menkes/SK/III/2007 tentang
Kebijakan Obat Tradisional Nasional tahun 2007. Jakarta: Depkes.
[Deptan] Departemen Pertanian Republik Indonesia. 2007. Peraturan Menteri
Pertanian Nomor
07/Permentan/SR.140/2/2007 tentang
Syarat dan Tatacara Pendaftaran
Pestisida. Jakarta: Deptan
Ardyanti FJ. 2006. Perbandingan gambaran histopatologi, gambaran darah dan kimia darah kambing pasca pemberian daun lamtoro merah (Acacia villosa) dan kalliandra (Calliandra calothyrsus) [skripsi]. Bogor: Fakultas Kedokteran Hewan Institut Pertanian Bogor.
Balls, James M, Jacqueline B. 1991. Animals and Alternatives in Toxicology. Cambridge: Great Britain at the University Press.
Banks WJ. 1993. Applied Veterinary
Histology. 3rd Edition. Philadelphia: Mosby.
Blackley J dan HB David. 1991. Ilmu
Peternakan. Edisi ke-4. Yogyakarta: Gadjah Mada University Press.
Carlton WW, McGavin MD. 1996. Thomson's Spesial Veterinary Pathology ed ke-2. St Louis: Mosby.
Cheville NF. 2006. Cell Death and Cell
Recovery. In: Introduction to
Veterinary Pathology Edisi 3. USA: Blackwell Publishing.
Dalimartha. 1999. Ramuan Tradisional untuk Pengobatan Hepatitis. Jakarta: Penebar Swadaya.
Darmansjah I. 1995. Toksikologi. Di dalam:
Ganiswarna SG, editor. Farmakologi
dan Terapi. Jakarta: Bagian
Farmakologi Fakultas Kedokteran
Universitas Indonesia.
Dellmann HD, dan Brown EM. 1992. Buku teks Histologi Veteriner. Ed ke-3. Hartono R, penerjemah. Jakarta: UI Press. Terjemahan dari: Textbook of veterinary histology.
Dyce KM, Sack WO, Wensing CJG. 2002. Textbook of Veterinary Anatomy. Ed ke-3. Philadelphia: Elsevier.
Environmental Protection Agency (EPA). 1998. Health effect Test Guidlines. OPPTS 870.1100. Acute Toxicity Testing- Acute Oral Toxicity. EPA 712-C-98-190.
Gad S.C. 2007. Animal Models in Toxicology. Ed ke-2. Taylor & Francais: Boca Raton.
Gamse T. 2002. Liquid-liquid Extraction and Solid-Liquid Extraction. New York: Graz Pr.
Ganong WF. 2003. Buku Ajar Fisiologi
Kedokteran. Jakarta: EGC.
Guyton AC, Hall JE. 1997. Buku Ajar Fisiologi Kedokteran. Ed ke-9. Setiawan I, Tengadi KA, Santoso A,
penerjemah; Setiawan I, editor.
Jakarta: Penerbit Buku Kedokteran, EGC.
Hadian S. 2004. Performa Hasil Silangan Mencit Agouti dan Mencit Putih pada Penambahan Tepung Kunyit (Curcuma Domestica) dalam Ransum [skripsi]. Bogor: Fakultas Peternakan Institut Pertanian Bogor
Harada T, Akiko E, Gary AB, Robert RM. 1999. Liver and Gallblader. Di dalam: Maronpot RR, Gary AB, Beth WG, editor. Pathology of The mouse. USA: Cache River Press.
Harmita & Radji M. 2008. Buku Ajar Analisis Hayati Ed. 3. Jakarta: EGC.
Hartono. 1992. Histologi Veteriner. Bogor: FKH-IPB.
Hatzios KK. 2005. Metabolism and
Elimination of Toxicants. Di dalam:
Hock B dan Elstner EF. Plant
Toxicology. Edisi ke-4. Marce Dekker. New York.
Heyne K. 1987. Tumbuhan Berguna
Indonesia. Jilid III. Badan Litbang Kehutanan. Departemen Kehutanan, Jakarta.
Humason GL. 1972. Animal Tissue
Techniques. Ed ke-3. San Fransisco: WH Freeman.
Huminto H, Bahagia S, Estuningsih S, Koesharto FX. 1995. Patologi Gizi. Jakarta: Departemen Pendidikan dan
Kebudayaan Direktorat Jendral
Pendidikan Dasar dan Menengah
Kejuruan. Proyek Peningkatan
pendidikan dan Kejuruan Non Teknik II.
Hunter JD. 2006. Ventilator associated pneumonia. Postgrad Med J 82: 172-8
Irwan F. 2011. Aktivitas Antidiabetes dan Analisis Fitokimia Ekstrak Air Dan Etanol Daun Wungu (Graptophyllum pictum (L.) Griff) [skripsi]. Bogor:
Fakultas Matematika dan Ilmu
Pengetahuan Alam Institut Pertanian Bogor.
Jones TC, Ronald DH, Norval WK. 2006. Veterinary Pathology. Edisi ke-6. USA: Blackwell Publishing.
Kandi MM. 2008. Gambaran Histologis Usus Tikus Putih (Rattus norvegicus) yang
Diberi Ransum Daging Hasil
Fermentasi dengan Lactobacillus
plantarum 1B1 [skripsi]. Bogor:
Fakultas Peternakan Institut Pertanian Bogor.
Kaplan LA & Pesce JA. 1998. Clinical Chemistry: Theory Analysis and Correlation. Ed ke-3. New York: Mosby Year Book.
Kiernan JA. 1990. Histological and
Departement of Anatomy The University of Western Ontario.
Koeman JH. 1987. Pengantar Umum
Toksikologi (terjemahan).Yogyakarta : Gajah Mada University Press.
Kumalasari. LOR. 2006. Pemanfaatan Obat
Tradisional dengan Pertimbangan
Manfaat dan Keamanannya. Majalah
Ilmu Kefarmasian, Vol. III, No. 1, April 2006, 01-07
Kusnaeni V. 2008. Isolasi dan Karakterisasi Senyawa Fraksi n-Heksana dari ekstrak kulit batang Angsret (Spathoda campanulata Beauv) [skripsi]. Malang: Jurusan Kimia. Fakultas MIPA. Universitas Brawijaya.
Loomis TA. 1978. Essential Of Toxicology. 3rd ed. Philadelphia: Lea & Febiger.
Lu FC. 1995. Toksikologi Dasar : Asas, Organ, Sasaran, dan Penilaian Resiko. Ed 2. Jakarta: UI Press.
Maclachlan NJ, Cullen JM. 1995. Liver,
Billiary System, and Exocrine
Pancreas. Di dalam: Carlton WW,
McGavin MD, editor. Thomson’s
Special Veterinary Pathology. Ed ke-2. New York: Mosby Yearbook.
MacKenzie WF, Alison R. 1990. Heart. Di dalam: Pathology of the Fischer Rat
Reference and Atlas. Australia:
Academic Press
Malole MBM dan Pramono CS. 1989. Penggunaan Hewan-hewan Percobaan Laboratorium. Departemen Pendidikan dan Kebudayaan. Direktorat Jendral
Pendidikan Tinggi Pusat Antar
Universitas Bioteknologi. Institut
Pertanian Bogor, Bogor.
Marchelinda C. 2011. Kajian Histopatologi Paru-Paru Ayam Broiler yang Diuji Tantang Virus Avian Infulenza (H5N1) setelah Pemberian Ekstrak Tanaman
Sirih Merah (Piper Crocatum)
[skripsi]. Bogor: Fakultas Kedokteran Hewan Institut Pertanian Bogor
Mardiati R. 1996. Buku Kuliah Sistem Otak Manusia. Edisi ke-1. Jakarta: CV Agung Seto
Martini F. 1992. Fundamental of Anatomy
and Physiology. Ed ke-2. USA : A Simon and Schuster Company.
Maxie MG. 1993. The Urinary System. Di dalam: Jubb KVF, Peter CK and Nigel
P, editor. Pathology of Domestic
Animal. Ed ke-4. Volume ke-2. London: Academic Press.
McGavin D dan Zachary J. 2007. Pathologic Basic Veterinary Disease . Philadelpia: Elsevier Inc.
Murray RK, Daryl KG, Peter AM, Viktor WR. 1999. Biokimia Harper, ed 24. Jakarta: EKG
Olagbende-Dada SO, Ukpo GE, Coker HAB, Adesina SA. 2011. Blood glucose lowering effect of aqueous
extract of Graptophyllum pictum
(Linn) Griff. on alloxan-induced
diabetic rats and its acute toxicity in mice. African Journal of Biotechnology 10(6), pp. 1039-1043
Priambodo S. 1995. Pengendalian Tikus
Terpadu. Seri PHT. Jakarta: Penebar Swadaya.
Price SA and Wilson LM. 1988.
Pathophysiology Clinical Concepts of Diseases Processes Ed 2. Jakarta: EGC.
Price SA, Wilson LM. 1995. Fisiologi Proses-proses Penyakit. Alih bahasa: Anugerah P. Edisi empat . Jakarta.
Rahayu L, Damayanti R, Wikanta T. 2006. Gambaran histopatologi pankreas tikus hiperglikemia setelah mengkomsumsi k-karagenan dan i-karagenan. Jurnal Ilmu Kefarmasian Indonesia 4(2): 96-101.
Rakhmadi I. 2008. Performa Mencit Jantan (Mus Musculus) Umur 28-63 hari pada Kandang tanpa Sekat dan Bersekat dengan Alas Kandang yang Berbeda [skripsi]. Bogor: Fakultas Peternakan IPB
Ressang AA. 1984. Patologi khusus veteriner. Ed ke-2. Bali: Percetakan Bali.
Runnels RA, WS Monlux & AW Monlux.
Pathology. Ed 7. Iowa: The Iowa State University Press.
Seely JC. 1999. Kidney. Di dalam: Maronpot RR, Gary AB, Beth WG, editor. Pathology of The mouse. USA: Cache River Press.
Simpen I. 2008. Isolasi cashew nut shell liquid dari kulit jambu mete (Anarcadium occidentalle L) dan kajian beberapa sifat fisiko-kimianya. J Kimia 2:71-76.
Singer AJ dan Clark RAF. 1999. Cutaneus
Wond Healing. N England J Med.
341:738-154.
Smith JB dan Mangkoewidjojo. 1988.
Pemeliharaan Pembiakan dan
Penggunaan Hewan Percobaan di Daerah Tropis. Jakarta: UI press.
Soedibyo M. 1998. Alam Sumber Kesehatan, Manfaat dan Kegunaan. Jakarta: Balai Pustaka.
Soenanto H. 2005. Musnahkan Penyakit dengan Tanaman Obat. Jakarta: Puspa Swara.
Spector WG, Spector TD. 1993. Pengantar Patologi Umum. ED ke 3. Soetjipto
NS,Harsoyo,Hana A,Astuti P,
penerjemah: Moelyono MPE, editor. Yogyakarta: Gajah Mada University
Press. Terjemahan dari: An
Introduction to General Pathology. 3th Edition.
Stockham SL, Scott MA. 2002. Fundamentals of Veterinary Clinical Pathology. Ed
ke-1. Iowa state Pr. Blackwell
Publishing Co.
Sudarmadji S, Haryono B dan Suhardi. 2003. Prosedur Analisa Bahan Makanan dan Pertanian. Yogyakarta: Liberty.
Sudjadi 1986. Metode Pemisahan.
Yogyakarta: UGM-Press.
Sudono A. 1981. Pengaruh Interaksi antara Genotipe dan Lingkungan terhadap Pertumbuhan, Keefisienan Makanan, Daya Reproduksi, dan Produksi Susu Mencit [Desertasi]. Bogor: Pasca Sarjana Institut Pertanian Bogor.
Syamsuhidayat SS dan Hutapea R. 1991. Inventaris Tanaman Obat Indonesia (I). Badan Penelitian dan Pengembangan Kesehatan. Departemen Kesehatan RI.
Taofik M. 2010. Isolasi dan Identifikasi Senyawa Aktif Ekstrak Air Duan Paitan (Thitonia diversifolia) sebagai
Bahan Insektisida Botani Untuk
Pengendalian Hama Tungau
Eriohyidae [skripsi]. Malang: Fakultas Sains dan Teknologi Universitas Islam Negeri Malang
Thomas ANS. 1989. Tanaman Obat
Tradisional I. Yogyakarta: Kanisius.
Tizard I. 1988. Pengantar Imunologi
Veteriner. Surabaya: Airlangga University Press.
Underwood JCE. 1999. Patologi Umum dan
Sistematik. Sarjadi, penerjemah.
Jakarta: EGC. Terjemahan dari:
General and systematic pathology.
Wahjoedi B, Astuti YN, Winarno W,
Pudjiastuti, Nuratmi B. 1996.
Penelitian Toksisitas Subkronik Infus Daun Johar (Cassia Slamea Lamk.)
pada Tikus Putih. Bul. Penelitian
Kesehatan vol 24(4)
Wahyono, Hakim L, Wahyuono, S, Mursyidi A, Verpoorte R., Timmerman H. 2003.
Isolation of Tracheospasmolytic
Compounds From Piper cubeba
Fruits. Ind. J. of Pharm., 14 (3), 119-23
Lampiran 1 Gambaran umum penelitian
Preparasi sampel
Ekstraksi etanol 70%
Uji Toksisitas Subkronis
Simplisia
Ekstrak kasar
Histopatologi Hati, Ginjal, dan Organ
pendukung
Daun Wungu
Lampiran 2 Diagram alir uji toksisitas subkronis
Ekstrak Etanol 70%
Dosis 100
mg/kg
Dosis 1000
mg/kg
Dosis 500
mg/kg
Pencekokan
mencit
kelompok II
Pencekokan
mencit kelompok
III
Pencekokan
Mencit kelompok
IV
Pencekokan
mencit
kelompok I
Selama 3 bulan
Pengamatan LD
50Lampiran 3 Diagram alir histopatologi organ
Sampling Organ
Fiksasi
Dalam BNF 10% selama 6-48 jam
Dehidrasi
(Penghilangan air dengan etanol 70%, 80%, 90%, 95% etanol absolut I
dan etanol absolut II masing-masing selama 2 jam)
Clearing
(Pembersihan dengan Xilol I dan Xilol II)
Embedding
(Penanaman jaringan dalam parafin)
Sectioning
(Pengirisan dengan menggunakan mikrotom setebal 5μm)
Mounting
(Penempelan sediaan pada gelas obyek)
Staining