KARAKTERISASI SIMPLISIA DAN
STANDARDISASI EKSTRAK ETANOL HERBA
KEMANGI
(Ocimum americanum L.)
SKRIPSI
NUR KHOIRANI
NIM : 109102000066
FAKULTAS KEDOKTERAN DAN ILMU KESEHATAN PROGRAM STUDI FARMASI
KARAKTERISASI SIMPLISIA DAN STANDARDISASI
EKSTRAK ETANOL HERBA KEMANGI
(
Ocimum americanum L
.)
SKRIPSI
Diajukan sebagai salah satu syarat memperoleh gelar Sarjana Farmasi
NUR KHOIRANI
NIM : 109102000066
FAKULTAS KEDOKTERAN DAN ILMU KESEHATAN PROGRAM STUDI FARMASI
Nama : Nur Khoirani
Program Studi : Farmasi
Judul : Karakterisasi Simplisia dan Standardisasi Ekstrak Etanol Herba Kemangi (Ocimum americanum L.)
Karakterisasi simplisia dan standardisasi ekstrak etanol herba kemangi (Ocimum americanum L.) sebagai obat herbal telah dilakukan. Karakterisasi simplisia meliputi uji makroskopik pada tanaman segar dan uji mikroskopik pada serbuk simplisia. Standardisasi ekstrak etanol herba kemangi dilakukan berdasarkan parameter standar umum ekstrak tumbuhan obat. Hasil pengujian parameter spesifik menunjukkan organoleptik ekstrak kental, berwarna coklat kehitaman, bau aromatis dan memiliki rasa kelat, dan agak sedikit pahit), dengan kandungan senyawa larut dalam air 11,30% ± 2,92% dan senyawa larut dalam etanol 69% ± 0,70%, dan hasil kandungan senyawa eugenol sebagai senyawa marker didalam ekstrak sejumlah 0,0215%. Hasil pengujian parameter non spesifik ektrak etanol herba kemangi menunjukkan kadar abu total 20,445% ± 0,233% dan kadar abu tidak larut asam 2,485% ± 0,07%, susut pengeringan 19,201% ± 0,0027%, kadar air 17,345% ± 0,488%, bobot jenis ekstrak 5% adalah 0,9312 ± 0,0025, total cemaran bakteri 44,670 x 102 koloni/g, total cemaran kapang 10* koloni/g, dan pada pengujian aflatoksin didalam ekstrak hasilnya negatif. Pada pengujian logam berat didapatkan logam timbal 0,007733 x 10-4 mg/kg, cadmium 0,00477x 10
-4
mg/kg, arsen 0,002396 µg/kg. Dari data yang dihasilkan, ekstrak memenuhi persyaratan secara umum sebagai bahan baku obat yang berasal dari bahan alam.
Name : Nur Khoirani
Program Study
: Pharmacy
Tittle : Characterization of Simplicia and Standardization of Ethanol Extract Kemangi Herb (Ocimum americanum L.)
Characterization of simplicia and standardization of ethanol extract kemangi herb (Ocimum americanum L.) as medicine have been done. Characterization of simplicia was based on general literature of kemangi plants. Result of characterization simplicia includes macroscopic test of plants and microscopic test of simplicia powder. The standardization of ethanol extract kemangi herb based on common standards parameters of medicinal plant extract. Result of standardization specific parameters showed organoleptic extract thick, brown, aromatic ordor, and brace teste slightly bitter, which compound contents dissolved in water of 11.30% ± 2.92% and compound contents dissolved in ethanol of 69% ± 0.70%, and result of eugenol countent as marker compound in the extract was 0.0215%. Result of standardization non specific parameters tests showed total ash content of extract 20.419% ± 0.249% and ash content insoluble in acid was 2.485% ± 0.07%, the loss on drying 19.201% ± 0.0027%, the density of extract 5% was 0.9312 ± 0.0025, the total bacteria contamination 44.670 x 102 koloni/g, total mold and yeasts contamination 10* koloni/g, and the aflatoxin test in the extract was negative. The heavy metal tests resulted lead metal of 0.007733 x 10-4 mg/kg, cadmium 0.00477x 10-4mg/kg, and arsenic 0.002396 µg/kg. The result showed that extract fulfill the general requirements of medicine made by nature material.
Assalamu’alaikum warahmatullahi wabarakatu
Alhamdulillah, puji dan syukur kehadirat Allah SWT yang telah
melimpahkan rahmat dan karunia-Nya serta shalawat dan salam selalu tercurah
kepada junjungan kita Nabi Muhammad SAW karena dengan segala rahmat dan
karunia-Nya penulis dapat menyelesaikan penelitian dan penulisan skripsi dengan
judul “KARAKTERISASI SIMPLISIA DAN STANDARDISASI EKSTRAK
ETANOL HERBA KEMANGI (Ocimum americanum L.)”. Skripsi ini disusun
untuk memenuhi tugas akhir sebagai salah satu syarat untuk memperoleh gelar
Sarjana Farmasi pada Fakultas Kedokteran dan Ilmu Kesehatan Program Studi
Farmasi UIN Syarif Hidayatullah, Jakarta.
Pada kesempatan ini perkenankanlah penulis menyampaikan ucapan
terima kasih yang sebesar-besarnya kepada:
1. Allah SWT atas segala nikmat yang telah diberikan-Nya kepada penulis dan
Nabi Muhammad SAW sebagai teladan dalam menjalani kehidupan
2. Bapak Prof. Dr. Komarudin Hidayat, selaku Rektor Universitas Islam Negri
Syarif Hidayatullah Jakarta
3. Bapak Prof. Dr. (hc) dr. M.K Tajudin Sp.And, selaku Dekan Fakultas
Kedokteran dan Ilmu Kesehatan UIN Syarif Hidayatullah Jakarta.
4. Bapak Drs. Umar Mansur, M.Sc selaku Ketua Jurusan Farmasi
5. Ibu Eka Putri, M.Si, Apt, dan ibu Sabrina, M.Farm, Apt, selaku pembimbing
yang telah memberikan banyak ilmu, bimbingan, pengarahan dan dukungan
selama penulisan skripsi ini.
6. Kepala Dinas Pendidikan Nasional Provinsi Sumatra Selatan, dan staf pengurus program beasiswa “Santri Jadi Dokter Provinsi Sumatra Selatan” yang telah memberikan kesempatan kepada saya untuk memperoleh ilmu dan
pendidikan sehingga dapat saya pergunakan untuk pengabdian kepada
Kiki Chairani Saputri, Tika Widya Sari, Nurul Komariah, Vita Fitriah, Ira
Sukaina, Susilowati, Fitri Nurmayanti, Maharani, Seila Inayatullah, Rafita
Oktavia, Etika Rahmawati, Midun, Ani Oktavia, Inti Fikriah Salsabilah, yang
selalu memberikan doa, dukungan dan motivasi untuk bisa lulus bareng, serta
trimakasih juga kepada adik-adik beasiswa SJD-Semsel atas doa dan
dukungannya.
8. Kedua orang tua, Ayah dan Ibu tercinta yaitu Bapak Daharudin Dahamid dan
Ibu Nyayu Adawiyah yang selalu memberikan kasih sayang dan doa yang
tiada henti senantiasa mengiringi perjalan hidup ananda, serta dukungan
kapada ananda baik moril maupun material. Tiada apapun di dunian ini yang
dapat membalas semua kebaikan, cinta dan kasih sayang yang telah engkau
berikan. Kepada adik-adik ku yang paling aku sayangi Nova Dewi Yanti,
Taufik Hidayat, dan Dina Arwani yang telah banyak mengibur dan
memberikan doa dan semangat sehingga penulis dapat memyelesaikan skripsi
ini.
9. Bapak dan ibu dosen yang telah memberikan ilmu dan pengetahuan hingga
penulis dapat menyelesaikan studi di jurusan Frmasi FKIK UIN Syarif
Hidayatullah Jakarta.
10. Para staf dan karyawan program studi Farmasi. Staf Administrasi Farmasi,
kak pia dan Pak Rizal yang telah banyak membantu selama penelitian dan
penyelesaian skripsi ini.
11. Seluruh laboran, Kak Lisna, Kak Tiwi, Kak Rani, Kak Eris, Kak Liken dan
Kak Ramamdi yang telah banyak mmembantu dalam penelitian ini.
12. Sahabat SUMSEL Program Stantri Jadi Dokter Angakatan Pertama yang
selama 4 tahun telah menjadi sahabat-sahabat yang paling baik. Rudi dan Aan
yang telah bersedia menemani ke BPPT dan LIPI. Ira, Vita, Nurul, Susi, dan
Maya sebagai teman-teman sperjuangan Farmasi. Kiki dan Tika teman kamar
yang selalu memberikan semangat.
13. Teman-teman seperjuangan penelitian kemangi Alfrida, Ira, Nurul, Zil, terima
15. Kepada teman-teman Rangers A4, terima kasih atas semangat, doa dan
kebersamaan, hiburan serta motivasi kepada penulis.
16. Buat yang terkasih, terima kasih atas do’a, dukungan, dan perhatiannya.
17. Kepada teman-teman Edta-C dan teman-teman Farmasi 2009, terimakasih
atas dukungan, semangat, doa, dan kerjasamanya selama ini.
18. Kepada adik-adik kelas atas dukungan dan doa tulus yang diberikan kepada
penulis. Serta semua pihak yang tidak dapat disebutkan satu persatu yang
turut membantu menyelesaikan skripsi ini.
Penulis menyadari dalam penyusunan skripsi ini masih banyak kekurangan
dan masih jauh dari kesempurnaan.Penulis hanya bisa berdoa semoga amal baik
dari semua pihak yang telah membantu penulis dalam menyelesaikan Studi di
UIN Sarif Hidayatullah Jakarta ini mendapat balasan terindah dari Allah SWT.
Akhir kata kesempurnaan hanya milik Allah SWT dan kesalahan datangnya dari
penulis selaku manusia biasa, dengan penuh rasa hormat dan kerendahan hati,
penulis berharap semoga skripsi ini dapat memberikan manfaat bagi penulis
maupun bagi kita semua.
Jakarta, September 2013
DAFTAR ISI
Halaman
HALAMAN JUDUL………. ii
HALAM PERNYATAAN ORISINALITAS……….. iii
HALAMAN PERSETUJUAN PEMBIMBING………. iv
HALAMAN PENGESAHAN SKRIPSI………. v
ABSTRAK………. vi
ABSTRACT………... vii
KATA PENGANTAR………... viii
HALAMAN PERSETUJUAN PUBLIKASI KARYA ILMIAH……….. xi
DAFTAR ISI……….. xii
BAB 2 TINJAUAN PUSTAKA... 5
2.1 Deskripsi Tanaman Kemangi (Ocimum americanumL.)…………. 5
2.1.1 Taksonomi ……… 5
2.8 Parameter-parameter Standar Ekstrak………... 13
2.8.1 Parameter Spesifik Ekstrak………. 13
2.8.2 Parameter Non Spesifik Ekstrak………. 14
2.9 Uraian Instrumen……….. 16
BAB 3 METODE PENELITIAN………. 19
3.3.3 Pemeriksaan Karakterisasi Simplisia……… 20
3.3.3.1 Uji Makrokopik……… 20
BAB 4 HASIL DAN PEMBAHASAN... 30
4.1 Hasil Penelitian……….. 30
4.1.5.2 Analisis Komponen Senyawa Kimia dengan GCMS……….. 34 4.1.5.3 Penentuan Kadar Senyawa Marker (Eugenol) dalam Ekstrak Etanol Herba Kemangi (Ocimum americanum L.)………... 36
4.1.6 Hasil Pengujian Parameter Non Spesifik……….. 37
4.2 Pembahasan……… 38
BAB 5 KESIMPULAN DAN SARAN………. 47
DAFTAR TABEL
Halaman
Tabel 4.1. Hasil Uji Makroskopik Herba Kemangi (Ocimum
americanumL.)………... 29
Tabel 4.2. Uji Mikroskopik pada Serbuk Herba Kemangi (Ocimum
americanumL.)………... 31
Tabel 4.3. Hasil Pengujian Identitas Ekstrak, Organoleptik Ekstrak dan Kadar Senyawa yang Terlarut dalam Pelarut
Tertentu... 32
Tabel 4.4. Hasil Pengujian Kandungan Kimia dengan Penapisan
Fitokimia………... 33
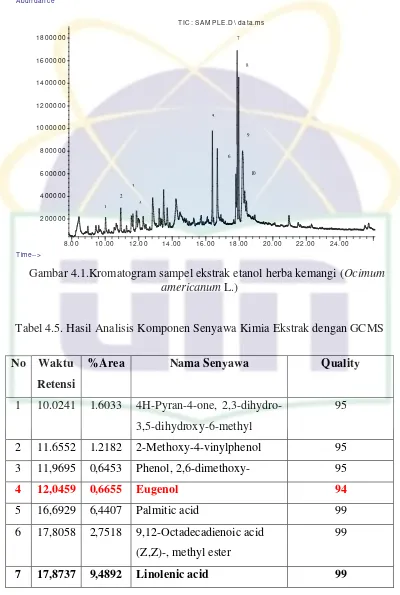
Tabel 4.5. Hasil Analisis Komponen Senyawa Kimia Ekstrak
dengan GCMS………... 33
DAFTAR GAMBAR
Halaman
Gambar 2.1. Tanaman Kemangi (Ocimum americanumL.)……… 6 Gambar 4.1. Kromatogram Sampel Ekstrak Etanol Herba
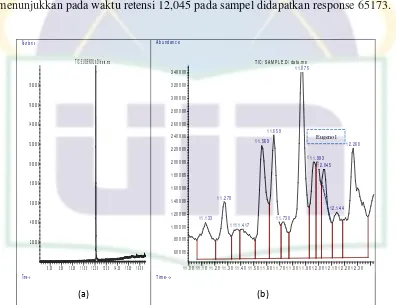
Kemangi (Ocimum americanum L)... 35 Gambar 4.2. Perbandingan Kromatogram Standar Eugenol dan
Kromatogram Sampel Ekstrak Etanol Herba
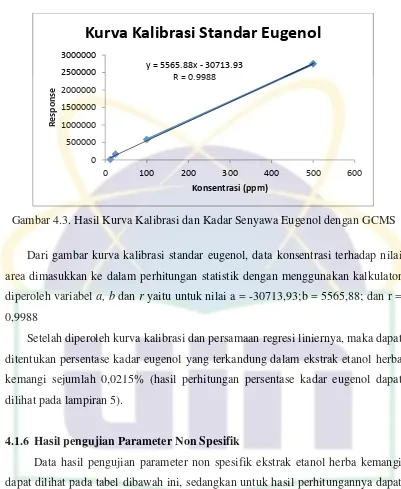
Kemangi (Ocimum americanumL.)…...……….. 36 Gambar 4.3. Hasil Kurva Kalibrasi dan Kadar Senyawa Eugenol
dengan GCMS…………..……… 37
DAFTAR LAMPIRAN
Halaman
Lampiran 1. Skema Prosedur Penelitian……….. 53 Lampiran 2. Hasil Determinasi Tanaman Herba Kemangi (Ocimum
americanumL.)………... 54
Lampiran 3. Kemangi (Ocimum americanum L.)……… 55 Lampiran 4. Perhitungan Rendemen Ekstrak Etanol 70% Herba
Kemangi (Ocimum americanumL.)………...……. 56 Lampiran 5. Perhitungan Parameter Spesifik Ekstrak Etanol Herba
Kemangi (Ocimum americanumL.)………...……. 57 Lampiran 6. Penapisan Fitokimia Ekstrak Etanol Herba Kemangi
(Ocimum americanumL.)…...……….... 61
Lampiran 7. Hasil data GCMS Komponen Senyawa Kimia Ekstrak
Etanol Herba Kemangi (Ocimum americanum L.)…… 63 Lampiran 8. Perhitungan Parameter Non Spesifik Ekstrak Etanol
Herba Kemangi (Ocimum americanumL.)………...….. 65 Lampiran 9. Hasil Uji Cemaran Mikroba dengan ALT…...……... 76 Lampiran 10. Hasil Uji Cemaran Kapang dan Khamir……...……... 77 Lampiran 11. Sertifikasi Hasil Pengujian Aflatoksin pada Ekstrak
Etanol Herba Kemangi (Ocimum americanumL.)…….. 78 Lampiran 12. Hasil LCMS Ekstrak Etanol Herba Kemangi dan
Standar Aflatoksin B1………. 79
BAB 1
Ocimum memiliki banyak kegunaan untuk pengobatan dan sebagai tanaman
aromatik di banyak negara, antara lain Mesir, India, Yunani, Itali, Maroko, dan
negara-negara lainnya (Shadia, Aziz, Omer, & Sabra, 2007).
Di Indonesia genus Ocimum yang di kenal ada empat, yaitu; O. gratissimum
(O. viridiflorum. Roth), O. canum Sims (O. africanum Lour, O. americanum L.,
O. branchiatum Blume), O. basilicum, dan O. tenuiflorum (Oyen & Dung, 1999
dalam Hadipoentyanti & Wahyuni, 2008).
Ocimum americanum merupakan spesies dari ocimum famili lamiaceae
(labiatae). Ocimum americanum L. tumbuh liar dan menyebar di seluruh wilayah
tropis Asia dan Afrika (Siemonsma, J.S & Piluek, K., 1994; Shadia, Aziz, Omer,
& Sabra, 2007). Ocimum americanum L. di Indonesia dikenal dengan kemangi.
Kemangi sering digunakan sebagai sayuran (lalapan) karena dapat meningkatkan
selera makan (Pitojo, 1996; Hadipoentyanti & Wahyuni, 2008). Menurut catatan
Sudarman Mardi Siswoyo (1975), tanaman kemangi dapat dimanfaatkan sebagai
obat tradisional untuk mengobati berbagai kelainan tubuh, daun kemangi
digunakan untuk mengobati demam, peluruh air susu kurang lancar, dan rasa
mual. Sedangkan biji kemangi digunakan untuk mengobati sembelit (Pitojo,
1996).
Ocimum americanum L. mengandung senyawa kimia alami antara lain,
minyak atsiri, karbohidrat, alkaloid, senyawa fenolik, fitosterol, tanin, lignin, pati,
saponin, flavonoid, terpenoid dan antrakuinon (Dhale, Birari, & Dhulgande, 2010;
Sarma and Babu, 2011). Minyak atsiri merupakan komponen utama pada Ocimum
americanum L (Sarma and Babu, 2011). Mutu minyak atsiri dipengaruhi oleh
penyinaran) (Hadipoentyanti & Wahyuni, 2008). Senyawa minyak atsiri yang
paling utama pada Ocimum americanum adalah kamfor, metil sinamat, dan sitral
(Siemonsma, J.S & Piluek, K., 1994, Verma & Kotyal, 2012).
Banyak penelitian-penelitian tentang aktivitas farmakologi dari tanaman
kemangi (Ocimum americanum L.). Ekstrak hidroalkoholik dari daun Ocimum
americanum diteliti memiliki aktivitas antioksidan yang dapat mencegah ischemia
(Behera, Panigrahi, Babu, & Ramani, 2012). Pada penelitian lain juga mengatakan
ekstrak petroleum eter, metanol, dan air dari tanaman kemangi (Ocimum
americanum L.)memiliki aktivitas analgetik-antinflamasi (Behera, Baidya, Satish,
Bilal, & Panda, 2011; Verma & Kothiyal, 2012). Selain itu, pada penelitian lain
juga mengatakan bahwa ekstrak air dari Ocimum americanum dapat digunakan
sebagai anti diabetes melitus (Verma & Kothiyal, 2012). Sedangkan minyak
atsirinya dapat memperlihatkan aktivitas melawan fungi yang bersifat patogen
pada manusia, melawan mikroorganisme oral, agrotis ipsilon (Lepidoptera :
Noctuide) (Ntezurubanza, L., 1986 dalam Shadia, Aziz, Omer, & Sabra, 2007;
Thaweboon, S & Thaweboon, B., 2009; Shadia, El-Aziz, Omer, & Sabra, 2007;
Verma & Kotyal, 2012).
Melihat besarnya potensi tanaman Ocimum americanum L. sebagai tanaman
obat, maka perlu dilakukan karakterisasi simplisia dan standardisasi ekstrak herba
kemangi sehingga dapat menetapkan mutu dan keamanan bahan bahan baku
ekstrak yang digunakan dalam menunjang kesehatan. Dampak positif
standardisasi sebenarnya menguntungkan semua pihak yakni konsumen,
pemerintah, bahkan produsen sendiri. Tujuan dari standardisasi sendiri adalah
menjaga konsistensi dan keseragaman khasiat dari obat herbal, menjaga
senyawa-senyawa aktif selalu konsisten terukur antara perlakuan, menjaga keamanan dan
stabilitas ekstrak/bentuk sedian terkait dengan efikasi dan keamanan pada
konsumen, dan meningkatkan nilai ekonomi (Saifudin, Rahayu, & Teruna, 2011).
Dalam proses standardisasi herba kemangi (Ocimum americanum L.), di
perlukan bahan baku atau simplisia yang memenuhi syarat dalam monografi
terbitan resmi Departemen Kesehatan (Materia Medika Indonesia) dan ekstrak
yang memenuhi persyaratan dalam buku khusus monografi ekstrak tumbuhan
(Ocimum amerianum) belum tercantum dalam monografi terbitan resmi
Departemen Kesehatan (Materia Medika Indonesia & Monografi ekstrak
tumbuhan obat). Oleh karena itu, diharapkan dengan dilakukannya karakterisasi
simplisia dan standardisasi ekstrak etanol herba kemangi (Ocimum americanum
L.) ini dapat dijadikan acuan sebagai parameter standar mutu ekstrak.
Pada pengujian standardisasi ini dilakukan ekstraksi herba kemangi
(Ocimum americanum L.) dengan menggunakan pelarut etanol. Etanol merupakan
pelarut serba guna yang baik untuk ekstraksi pendahuluan (J.B. Harbone, 1987).
Pelarut organik selain etanol memiliki potensi toksisitas yang lebih tinggi
(Saifudin, Rahayu, & Teruna, 2011). Selain itu, etanol juga memiliki kemampuan
menyari dengan polaritas yang lebar mulai dari senyawa nonpolar sampai dengan
polar (Saifudin, Rahayu, & Teruna, 2011).
1.2 Rumusan Masalah
Berdasarkan latar belakang di atas, dan belum adanya laporan penelitian
mengenai karakterisasi simplisia dan standardisasi ekstrak etanol herba kemangi
(Ocimum americanum L.), maka dilakukan penelitian ini untuk mendapatkan
informasi sebagai berikut:
1. Bagaimana hasil data karakterisasi simplisia dari herba kemangi (Ocimum
americanum L.) ?
2. Bagaimana hasil data standardisasi ekstrak etanol herba kemangi Ocimum
americanum L.) ?
1.3 Tujuan Penelitian
Tujuan dalam penelitian ini adalah :
1. Mendapatkan data karakterisasi simplisia tanaman herba kemangi (Ocimum
americanum L.).
2. Mendapatkan data parameter standardisasi ekstrak etanol herba kemangi
1.4 Manfaat Penelitian
Hasil penelitian ini diharapkan dapat memberikan ilustrasi tentang
karakterisasi simplisia dan standardisasi herba kemangi (Ocimum americanum L.)
yang akan di gunakan sebagai bahan baku obat fitofarmaka atau minimal obat
herbal terstandar.
1.5 Batasan Penelitian
Batasan penelitan adalah penentuan makroskopis dan mikroskopis simplisia
herba kemangi (Ocimum americanum L.) yang mengacu kepada literatur secara
umum. Sedangkan untuk penentuan parameter spesifik dan non spesifik pada
ekstrak etanol herba kemangi (Ocimum americanum L.) mengacu kepada
Parameter Standar Umum Ekstrak Tumbuhan Obat Depkes 2000 dan buku
BAB 2
TINJAUAN PUSTAKA
2.1 Deskripsi Tanaman Kemangi (Ocimum americanum L.)
Ocimum americanum L. merupakan nama latin dari tanaman kemangi
(Siemonsma, J.S & Piluek, K., 1994; Pitojo, 1996; Hadipoentyanti dan Wahyuni,
2008). Ocimum americanum L. tumbuh liar dan menyebar di seluruh wilayah
tropis Asia dan Afrika (Siemonsma, J.S & Piluek, K., 1994; Shadia, Aziz, Omer,
& Sabra, 2007).
Ocimum americanum termasuk kedalam genus ocimum famili lamiaceae
(Labiatae) telah digunakan sejak lama sebagai obat dan tumbuhan aromatik di
banyak negara, antara lain Mesir, India, Yunani, Itali, Marocco dan negara lainnya
(Shadia, Aziz, Omer, & Sabra, 2007; Hadipoentyanti dan Wahyuni, 2008).
Lamiaceae adalah famili yang menghasilkan sejumlah besar taksa tanaman obat,
terutama karena kaya akan kandungan minyak atsirinya (Heinrich, Barnes,
Gibbons, & Wiliamson, 2010). Umumnya minyak atsiri terdapat di dalam kelenjar
epidermis. Sebagian besar kelompok famili lamiaceae ini berupa herba atau
semak pendek dengan batang muda sering bersudut empat (Heinrich, Barnes,
Gibbons, & Wiliamson, 2010).
2.1.1 Taksonomi
Menurut ilmu tumbuh-tumbuhan tanaman kemangi termasuk dalam
sistematika sebagai berikut:
a. Divisi : Spermatophyta
b. Sub-divisi : Angiospermae
c. Kelas : Dicotyledonae
d. Ordo : Amaranthaceae
e. Family : Lamiaceae atau Labiatae
f. Genus : Ocimum
g. Species : Ocimum americanum L.
Gambar 2.1. Tanaman Kemangi (Ocimum americanum L.)
Sumber : Koleksi pribadi
2.1.2 Sinonim
Ocimum americanum L. memiliki sinonim yaitu : Ocimum canum Sims,
Ocimum affricanum Lour, Ocimum brachiatum Blume (Siemonsma, J.S & Piluek,
K., 1994; Hadipoentyanti dan Wahyuni, 2008).
2.1.3 Nama Daerah
Ocimum americanum di kenal dengan hoary basil, wild basil, dan lemon
basil. Indonesia: kemangi, serawung, selasih putih. Malaysia: selaseh, kemangi,
ruku-ruku. Thailand: Maenglak. Vietnam: rau h[us]ng (Siemonsma, J.S & Piluek,
K., 1994; Pitojo, 1996).
2.1.4 Ekologi dan Penyebaran
Ocimum americanum L. tumbuh liar dan menyebar di seluruh wilayah
tropis Asia dan Afrika. Tanaman asal dari Ocimum americanum L. belum
diketahui. Tanaman ini tersebar di wilayah Asia Tenggara di belahan benua, di
Indonesia dan Papua Nugini. Tanaman ini juga terkenal di wilayah tropis Amerika
dan beberapa pulau diwilayah Hindia Barat. Tumbuh kurang dari 300 m di atas
permukaan laut (Siemonsma, J.S & Piluek, K., 1994; Pitojo, 1996; Shadia, Aziz,
2.1.5 Morfologi
Ocimum americanum L. merupakan tanaman berbatang tegak, tinggi
tanaman antara 0,3-0,6 m. Batang muda berwarna hijau dan setelah tua berwarna
kecokelatan; tangkai daun berwarna hijau dan panjangnya antara 0,5-2 cm (Pitojo,
1996), bentuk batang mudanya persegi (Simoemonsma, J.S & Piluek, K., 1994).
Pada batang terdapat bulu terutama pada tanaman muda (Hadipoentyanti &
Wahyuni, 2008).
Daun Ocimum americanum berwarna hijau terang (Hadipoentyanti &
Wahyuni, 2008), helaian daun berbentuk bulat telur, ujungnya meruncing, tampak
menggelombang; pada sebelah menyebelah ibu tulang daun terdapat 3-6 tulang
cabang; tepi daun sedikit bergerigi (Pitojo, 1994); terdapat bintik-bintik serupa
kelenjar (Pitojo, 1996; Hadipoentyanti & Wahyuni, 2008).
Ocimum americanum berbunga semu terdiri dari 1-6 karangan bunga,
berkumpul menjadi tandan; terletak di bagian ujung batang, cabang, atau ranting
tanaman; panjang karangan bunga mencapai 25 cm dengan 20 kelompok bunga.
Daun pelindung elips atau bulat telur, panjang antara 0,5-1 cm. Kelopak bunga
hijau, berambut, di sebelah dalam lebih rapat dan bergigi tak beraturan. Daun
mahkota berwarna putih, berbibir dua. Bibir atas bertaju 4, bibir bawah utuh
(Pitojo, 1994). Tangkai kepala putik berwarna ungu, sedangkan tangkai kepala
sari dan tepung sari berwarna putih (Pitojo, 1996), jumlah putik 1, sedangkan
jumlah benang sari 4 (2 pendek, 2 panjang) (Martono, Hadipoentyanti, & Udamo,
2004; Hadipoentyanti & Wahyuni, 2008). Tangakai dan kelopak buah letaknya
tegak, melekat pada sumbu dari karangan bunga. Biji buah Ocimum americanum
kecil, keras, berwarna kehitaman. Secara keseluruhan tandan bunga dan buah,
tanpak hijau keputihan dan tidak mencolok (Pitojo, 1996).
2.1.6 Kandungan Kimia
Kandungan kimia pada Ocimum americanum L. antara lain, minyak atsiri,
karbohidrat, alkaloid, senyawa fenolik, tanin, fitosterol, lignin, pati, saponin,
flavonoid, terpenoid dan antrakuinon (Dhale., et al, 2010; Sarma dan Babu, 2011).
Minyak atsiri pada Ocimum americanum L. mengandung komponen campor,
2004; Hadipoentyanti dan Wahyuni, 2008). Senyawa minyak atsiri yang paling
utama pada O. americanum adalah kamfor, metil sinamat, dan sitral (Siemonsma,
J.S & Piluek, K., 1994, Verma & Kotyal, 2012).
Menurut buku “Glossaary of indian medicinal Plants” kandungan kimia
utama dalam Ocimum americanum adalah minyak atsiri, flavonoid, dan
polisakarida. Senyawa penyusun minyak atsiri yaitu metil sinamat, metilheptenon,
metilnonilketon, d-camphor, citral, ocimin, metilchavicol, linalool, nevadensin,
slavigenin, beta-sitosterol, betulinat, ursolat, asam oleonolat. Sedangkan
flavonoids tersusun atas pectolinarigenin-7-metileter dan nevadensin. Polisakarida
tersusun atas xylosa, arabinosa, rhamnosa, dan asam galakturonat (Sarma dan
Babu, 2011).
2.1.7 Khasiat dan Kegunaan
Didalam pengobatan tradisional, O. americanum digunakan untuk
pengobatan penyakit ringan dimasyarakat. Jamu-jamuan O. americanum yang
direbus digunakan untuk obat batuk, daun yang dimemarkan kemudian di tempel
diatas dahi dapat meringankan radang selaput lendir di hidung dan tenggorokan,
sedangkan di tempel diatas dada dapat meringankan masalah pernapasan.
Tanaman keseluruhan (herba) dapat digunakan pada saat mandi yang berkhasiat
untuk pengobatan rematik, selain itu herba juga berhasiat untuk pengobatan batu
ginjal (Siemonsma, J.S & Piluek, K., 1994).
Secara tradisional, biji kemangi dapat dimanfaatkan untuk membuat
ramuan minuman penyegar dapat dimanfaatkan untuk menekan dahaga dan
pendingin rasa perut, selain itu juga dapat digunakan untuk mengobati sembelit
(Pitojo, 1996). Daun kemangi digunakan untuk mengobati demam, peluruh air
susu kurang lancar, dan rasa mual. Biji kemangi di gunakan untuk mengobati
sembelit (Pitojo, 1996).
Penelitian tentang aktivitas biologi herba kemangi (Ocimum
americanum/canum) juga banyak di laporkan. Pada ekstrak Ocimum americanum
memiliki aktivitas sebagai analgesik dan anti-inflamasi (Behera, Baidya, Satish,
Panigrahi, Babu, & Ramani, 2012), dan dapat melawan bakteri gram negatif dan
gram positif (Dhale, Birari, & Dhulgande, 2010).
Pada minyak atsiri Ocimum americanum, di teliti memiliki memiliki
aktivitas dapat melawan mikroorganisme oral (S. Thaweboon & B. Thaweboon),
Agrotis ipsilon (Lepidoptera : Noctuide) (Shadia, El-Aziz, Omer, & Sabra, 2007),
dapat digunakan sebagai insektisida nabati yang dapat melawan hama padi, dan
dapat digunakan sebagai alat antifungi yang aman yang dapat berfungsi sebagai
parameter indikasi percobaan fungi yang bersifat patogen (Verma & Kothiyal,
2012).
2.2 Simplisia
Simplisia adalah bahan alamiah yang dipergunakan sebagai obat yang
belum mengalami pengolahan apapun juga dan kecuali dikatakan lain, berupa
bahan yang telah dikeringkan (Depkes RI, 1995).
Menurut “Materia Medika Indonesia” simplisia dibedakan menjadi tiga, yaitu; simplisia nabati, simplisia hewani, dan simplisia pelican (mineral).
Simplisia nabati adalah simplisia yang berupa tumbuhan utuh, bagian tumbuhan
atau eksudat tumbuhan. Eksudat tumbuhan ialah isi sel yang secara spontan keluar
dari tumbuhan atau isi sel yang dengan cara tertentu dikeluarkan dari selnya, atau
senyawa nabati lainnya yang dengan cara tertentu dipisahkan dari tumbuhannya
dan belum berupa senyawa kimia murni (Depkes RI, 1995 dalam Saifudin,
Rahayu, & Teruna, 2011).
2.3 Karakterisasi Simplisia
Simplisia sebagai produk hasil pertanian atau pengumpulan dari tumbuhan
liar (wild crop) memiliki kandungan kimia yang tidak terjamin selalu konstan
karena adanya variabel bibit, tempat tumbuh, iklim, kondisi (umur dan cara)
panen, serta proses pasca panen dan preparasi akhir. Variasi kandungan senyawa
dalam produk hasil panen tumbuhan obat disebabkan oleh beberapa aspek sebagai
berikut (Depkes RI, 2000) :
1) Genetik (bibit)
3) Rekayasa agronomi (fertilizer, perlakuan selama masa tumbuh)
4) Panen (waktu dan pasca panen)
Besarnya variasi senyawa kandungan meliputi baik jenis ataupun kadarnya,
sehingga timbul jenis (species) lain yang disebut kultivar (Depkes RI, 2000).
Proses pemanenan dan preparasi simplisia merupakan proses yang dapat
menentukan mutu simplisia dalam artian, yaitu komposisi senyawa kandungan,
kontaminasi dan stabilitas bahan (Depkes RI, 2000).
Karakterisasi suatu simplisia mempunyai pengertian bahwa simplisia yang
akan digunakan untuk obat sebagai bahan baku harus memenuhi persyaratan yang
tercantum dalam monografi terbitan resmi Departemen Kesehatan (Materia Media
Indonesia). Sedangkan sebagai produk yang langsung dikonsumsi (serbuk jamu
dsb.) masih harus memenuhi persyaratan produk kefarmasian sesuai dengan
peraturan yang berlaku (Depkes RI, 2000). Karakterisasi simplisia meliputi uji
makroskopik, uji mikroskopik dan identifikasi simplisia (Depkes RI, 1995).
2.4 Ekstraksi
Ekstraksi suatu tanaman obat adalah pemisahan secara kimia atau fisika
suatu bahan padat atau bahan cair dari suatu padatan, yaitu tanaman obat (Depkes
RI, 2000). Metode ekstraksi dengan menggunakan pelarut dibedakan menjadi dua
cara yaitu ; cara dingin dan cara panas. Cara dingin terbagi menjadi dua yaitu;
maserasi dan perkolasi, sedangkan cara panas terbagi menjadi empat jenis yaitu;
refluks, soxhlet, digesti, infus, dan dekok (Depkes RI, 2000).
Maserasi adalah proses pengekstrakan simplisia dengan menggunakan
pelarut dengan beberapa kali pengocokan atau pengadukan pada temperatur
ruangan (kamar) (Depkes RI, 2000). Maserasi berasal dari bahasa latin macerase
berarti mengairi dan melunakkan. Maserasi merupakan cara ekstraksi yang paling
sederhana. Dasar dari maserasi adalah melarutnya bahan kandungan simplisia dari
sel yang rusak, yang terbentuk pada saat penghalusan, ekstraksi (difusi) bahan
kandungan dari sel yang masih utuh. Setelah selesai waktu maserasi, artinya
keseimbangan antara bahan yang diekstraksi pada bagian dalam sel dengan yang
masuk kedalam cairan, telah tercapai maka proses difusi segera berakhir (Voigt,
Selama maserasi atau proses perendaman dilakukan pengocokan
berulang-ulang, upaya pengocokan ini dapat menjamin keseimbangan konsentrasi bahan
ekstraksi yang lebih cepat didalam cairan. Sedangkan keadaan diam selama
maserasi menyebabkan turunnya perpindahan bahan aktif. Secara teoritis pada
suatu maserasi tidak memungkinkan terjadinya ekstraksi absolut. Semakin besar
perbandingan simplisia terhadap cairan pengekstraksi, akan semakin banyak hasil
yang diperoleh (Voigt, 1994).
Secara teknologi maserasi termasuk ekstraksi dengan prinsip metode
pencapaian konsentrasi pada keseimbangan. Maserasi kinetik berarti dilakukan
pengadukan yang kontinu (terus-menerus). Remaserasi berarti dilakukan
pengulangan penambahan pelarut setelah dilakukan penyaringan maserat pertama,
dan seterusnya (Depkes RI, 2000).
2.5 Ekstrak
Ekstrak adalah sediaan pekat yang diperoleh dengan mengekstraksi zat aktif
dari simplisia nabati atau simplisia hewani menggunakan pelarut yang sesuai,
kemudian semua atau hampir semua pelarut diuapkan dan massa atau serbuk yang
tersisa diperlakukan sedemikian hingga memenuhi baku yang telah ditetapkan
(Depkes RI, 1995). Ada beberapa jenis ekstrak yakni: ekstrak cair, ekstrak kental
dan ekstrak kering. Ekstrak cair jika hasil ekstraksi masih bisa dituang, biasanya
kadar air lebih dari 30%. Ekstrak kental jika memiliki kadar air antara 5-30%.
Ekstrak kering jika mengandung kadar air kurang dari 5% (Voigt, 1994).
Faktor yang mempengaruhi ekstrak yaitu faktor biologi dan faktor kimia.
Faktor biologi meliputi: spesies tumbuhan, lokasi tumbuh, waktu pemanenan,
penyimpanan bahan tumbuhan, umur tumbuhan dan bagian yang digunakan.
Sedangkan faktor kimia yaitu: faktor internal (Jenis senyawa aktif dalam bahan,
komposisi kualitatif senyawa aktif, komposisi kuantitatif senyawa aktif, kadar
total rata-rata senyawa aktif) dan faktor eksternal (metode ekstraksi, perbandingan
ukuran alat ekstraksi, ukuran, kekerasan dan kekeringan bahan, pelarut yang
digunakan dalam ekstraksi, kandungan logam berat, kandungan pestisida)
Selain faktor yang mempengaruhi ekstrak, ada faktor penentu mutu ekstrak
yang terdiri dari beberapa aspek, yaitu; kesahihan tanaman, genetik, lingkungan
tempat tumbuh, penambahan bahan pendukung pertumbuhan, waktu panen,
penangan pasca panen, teknologi ekstraksi, teknologi pengentalan dan
pengeringan ekstrak, dan penyimpanan ekstrak (Saifudin, Rahayu, & Teruna,
2011).
2.6 Standardisasi
Standardisasi adalah rangkaian proses yang melibatkan berbagai metode
analisis kimiawi berdasarkan data farmakologis, melibatkan analisis fisik dan
mikrobiologi berdasarkan kriteria umum keamanan (toksikologi) terhadap suatu
ekstrak alam (Saefudin et al., 2011).
Standardisasi secara normatif ditujukan untuk memberikan efikasi yang
terukur secara farmakologis dan menjamin keamanan konsumen. Standardisasi
obat herbal meliputi dua aspek :
1. Aspek parameter spesifik: berfokus pada senyawa atau golongan senyawa
yang bertanggung jawab terhadap aktivitas farmakologis. Analisis kimia yang
dilibatkan ditujukan untuk analisa kualitatif dan kuantitatif terhadap senyawa
aktif.
2. Aspek parameter non spesifik: berfokus pada aspek kimia, mikrobiologi dan
fisis yang akan mempengaruhi keamanan konsumen dan stabilitas missal
kadar logam berat, aflatoksin, kadar air dan lain-lain.
2.7 Standardisasi Obat Herbal
Standardisasi obat herbal merupakan rangkaian proses melibatkan berbagai
metode analisis kimiawi berdasarkan data farmakologis, melibatkan analisis fisik
dan mikrobiologi bersadarkan kriteria umum keamanan (toksikologi) terhadap
suatu ekstrak alam atau tumbuhan obat herbal (Saifudin, Rahayu, & Teruna,
2011).
Standardisasi dalam kefarmasian tidak lain adalah serangkaian parameter,
prosedur dan cara pengukuran yang hasilnya merupakan unsur-unsur terkait
biologi dan farmasi), termasuk jaminan (batas-batas) stabilitas sebagai produk
kefarmasian umumnya. Dengan kata lain, pengertian standardisasi juga berarti
proses menjamin bahwa produk akhir obat (obat, ekstrak atau produk ekstrak)
mempunyai nilai parameter tertentu yang konstan dan ditetapkan terlebih dahulu.
Terdapat dua faktor yang mempengaruhi mutu ekstrak yaitu faktor biologi dari
bahan asal tumbuhan obat dan faktor kandungan kimia bahan obat tersebut.
Standardisasi ekstrak terdiri dari parameter standar spesifik dan parameter standar
non spesifik (Depkes RI, 2000).
2.8 Parameter-parameter Standar Ekstrak
Parameter- parameter standar ekstrak terdiri dari parameter spesifik dan
parameter non spesifik
2.8.1 Parameter Spesifik Ekstrak (Depkes RI, 2000)
Penentuan parameter spesifik adalah aspek kandungan kimia kualitatif dan
aspek kuantitatif kadar senyawa kima yang bertanggung jawab langsung terhadap
aktivitas farmakologis tertentu. Parameter spesifik ekstrak meliputi :
1. Identitas (parameter identitas ekstrak) meliputi : deskripsi tata nama, nama
ekstrak (generik, dagang, paten), nama lain tumbuhan (sistematika botani),
bagian tumbuhan yang digunakan (rimpang, daun dsb) dan nama Indonesia
tumbuhan.
2. Organoleptis : Parameter organoleptik ekstrak meliputi penggunaan panca
indera mendeskripsikan bentuk, warna, bau, rasa guna pengenalan awal yang
sederhana se-objektif mungkin
3. Senyawa terlarut dalam pelarut tertentu : melarutkan ekstrak dengan pelarut
(alkohol/air) untuk ditentukan jumlah larutan yang identik dengan jumlah
senyawa kandungan secara gravimetrik. Dalam hal tertentu dapat diukur
senyawa terlarut dalam pelarut lain misalnya heksana, diklorometan, metanol.
4. Uji kandungan kimia ekstrak :
a. Pola kromatogram
Pola kromatogram dilakukan sebagai analisis kromatografi sehingga
memberikan pola kromatogram yang khas. Bertujuan untuk memberikan
gambaran awal komposisi kandungan kimia berdasarkan pola
kromatogram (KLT, KCKT). (Depkes, 2000)
b. Kadar kandungan kimia tertentu
Suatu kandungan kimia yang berupa senyawa identitas atau senyawa
kimia utama ataupun kandungan kimia lainnya, maka secara kromatografi
instrumental dapat dilakukan penetapan kadar kandungan kimia tersebut.
Instrumen yang dapat digunakan adalah densitometri, kromatografi gas,
KCKT atau instrumen yang sesuai. Tujuannya memberikan data kadar
kandungan kimia tertentu sebagai senyawa identitas atau senyawa yang
diduga bertanggung jawab pada efek farmakologi. (Depkes, 2000)
2.8.2 Parameter Non Spesifik Ekstrak (DEPKES RI,2000)
Penentuan parameter non spesifik ekstrak yaitu penentuan aspek kimia,
mikrobiologi dan fisis yang akan mempengaruhi keamanan konsumen dan
stabilitas (Saifudin, Rahayu, & Teruna, 2011).
Parameter non spesifik ekstrak menurut buku “Parameter Standar Umum
Ekstrak Tumbuhan Obat” (Depkes RI, 2000), meliputi :
1. Bobot jenis
Parameter bobot jenis adalah masa per satuan volume yang diukur pada
suhu kamar tertentu (250C) yang menggunakan alat khusus piknometer atau
alat lainnya. Tujuannya adalah memberikan batasan tentang besarnya masa
persatuan volume yang merupakan parameter khusus ekstrak cair sampai
ekstrak pekat (kental) yang masih dapat dituang, bobot jenis juga terkait
dengan kemurnian dari ekstrak dan kontaminasi (Depkes RI, 2000).
2. Kadar air
Parameter kadar air adalah pengukuran kandungan air yang berada
didalam bahan, yang bertujuan untuk memberikan batasan minimal atau
3. Kadar abu
Parameter kadar abu adalah bahan dipanaskan pada temperatur dimana
senyawa organik dan turunanya terdestruksi dan menguap. Sehingga tingga
unsur mineral dan anorganik, yang memberikan gambaran kandungan mineral
internal dan eksternal yang berasal dari proses awal sampai terbentuknya
ekstrak. Parameter kadar abu ini terkait dengan kemurnian dan kontaminasi
suatu ekstrak (Depkes RI, 2000).
4. Sisa pelarut
Parameter sisa pelarut adalah penentuan kandungan sisa pelarut tertentu
yang mungkin terdapat dalam ekstrak. Tujuannya adalah memberikan jaminan
bahwa selama proses tidak meninggalkan sisa pelarut yang memang
seharusnya tidak boleh ada (Depkes RI, 2000). Pengujian sisa pelarut berguna
dalam penyimpanan ekstrak dan kelayakan ekstrak untuk formulasi (Putri, E.,
anggraeni, & Khairina, 2012).
5. Cemaran mikroba
Parameter cemaran mikroba adalah penentuan adanya mikroba yang
patogen secara secara analisis mikrobiologis. Tujuannya adalah memberikan
jaminan bahwa ekstrak tidak boleh mengandung mikroba patogen dan tidak
mengandung mikroba non patogen melebihi batas yang ditetapkan karena
berpengaruh pada stabilitas ekstrak dan berbahaya (toksik) bagi kesehatan
(Depkes RI, 2000).
6. Cemaran aflatoksin
Aflatoksin merupakan metabolit sekunder yang dihasilkan oleh jamur.
Aflatoksik sangat berbahaya karena dapat menyebabkan toksigenik
(menimbulkan keracunan), mutagenik (mutasi gen), tertogenik (penghambatan
pada pertumbuhan janin) dan karsinogenik (menimbulkan kanker pada
jaringan) (Rustian, 1993 dalam Arifini, H., Anggraini, Handayani, & Rasyid).
Jika ekstrak positif mengandung aflatoksin maka pada media pertumbuhan
akan menghasilkan koloni berwarna hijau kekuningan sangat cerah (Saifudin,
7. Cemaran logam berat
Parameter cemaran logam berat adalah penetuan kandungan logam berat
dalam suatu ekstrak, sehingga dapat memberikan jaminan bahwa ekstrak tidak
mengandung logam berat tertentu (Hg, Pb, Cd, dll) melebihi batas yang telah
ditetapkan karena berbahaya bagi kesehatan (Depkes RI, 2000).
2.9 Uraian Instrumen
2.9.1 Spektroskopi Serapan Atom
Spektrometri merupakan suatu metode analisis kuantitatif yang
pengukurannya berdasarkan banyaknya radiasi yang dihasilkan atau yang diserap
oleh spesi atom atau molekul analit. Salah satu bagian dari spektrometri ialah
Spektrometri Serapan Atom (SSA), merupakan metode analisis unsur secara
kuantitatif yang pengukurannya berdasarkan penyerapan cahaya dengan panjang
gelombang tertentu oleh atom logam dalam keadaan bebas (Skoog et al., 2004
dalam Arifiani, 2012).
Apabila cahaya dengan panjang gelombang tertentu dilewatkan pada suatu
sel yang mengandung atom-atom bebas yang bersangkutan maka sebagian cahaya
tersebut akan diserap dan intensitas penyerapan akan berbanding lurus dengan
banyaknya atom bebas logam yang berada dalam sel (Underwood & Day, 2002).
Pada alat SSA terdapat dua bagian utama yaitu suatu sel atom yang
menghasilkan atom-atom gas bebas dalam keadaaan dasarnya dan suatu sistem
optik untuk pengukuran sinyal (Willard, Merritt, Dean, & Settle, 1988).
Pada prinsipnya mekanisme kerja dari SSA ini adalah atom-atom suatu
logam diuapkan dalam suatu nyala dan serapannya pada suatu pita radiasi sempit
yang dihasilkan oleh suatu lampu katode rongga. Kemudian, dilapisi dengan
logam tertentu yang sedang ditentukan, setelah itu diukur (Watson, DG., 2010).
Dalam metode SSA, sebagaimana dalam metode spektrometri atomik yang
lain, contoh harus diubah ke dalam bentuk uap atom. Proses pengubahan ini
dikenal dengan istilah atomisasi, pada proses ini sampel diuapkan dan
didekomposisi untuk membentuk atom dalam bentuk uap. Secara umum
pembentukan atom bebas dalam keadaan gas melalui tahapan-tahapan sebagai
a. Pengisatan pelarut, pada tahap ini pelarut akan teruapkan dan meninggalkan
residu padat.
b. Penguapan zat padat, zat padat ini terdisosiasi menjadi atom- atom
penyusunnya yang mula-mula akan berada dalam keadaan dasar.
Beberapa atom akan mengalami eksitasi ke tingkatan energi yang lebih
tinggi dan akan mencapai kondisi dimana atom-atom tersebut mampu
memancarkan energy (Basset et al. 1994).
Aplikasi dalam penetapan kadar dengan menggunakan SSA ini, terutama
sering digunakan dalam uji batas untuk logam-logam didalam obat sebelum
dimasukan kedalam formulasi. Sampel biasanya dilarutkan dalam asam nitrat 0,1
M untuk menghindari pembentukan hidroksida logam dari logam berat, yang
relative non-volatil dan menekan hasil bacaan SSA (Watson, DG., 2010).
2.9.2 Gas Chromatography Mass Spectrophotometry (GCMS)
Gas Chromatopraphy Mass Spectrophotometry atau kromatografi gas
spektroskopi masa merupakan suatu kesatuan instrumen kromatografi gas dan
spektroskopi masa (Willard, Merritt, Dean, & Settle, 1988).
Kromatografi adalah suatu metode pemisahan fisik, dimana
komponen-komponen yang dipisahkan didistribusikan diantara dua fasa, salah satu fasa
tersebut adalah suatu lapisan stasioner dengan permukaan yang luas, yang
mengalir lembut di sepanjang landasan stasioner (Underwood & Day, 2002).
Kromatografi gas adalah metode pemisahan dan deteksi yang dinamis pada
senyawa volatil organik dan beberapa senyawa anorganik. Kromatografi gas dapat
memisahkan senyawa volatil dan semi volatil dengan resolusi yang baik, tetapi
tidak dapat mengidentifikasi. Sedangkan spektroskopi massa dapat memberikan
informasi struktural yang rinci pada berbagai senyawa sehingga mampu
diidentifikasi dengan tepat. Prinsip kerja kromatografi gas melibatkan partisi dari
gas terlarut antara gas mulia sebagai fase gerak dan cairan atau padatan sebagai
fase diam, sedangkan spektrometri massa diperoleh dengan mengukur puncak dan
massa yang tepat dari ion yang membentuk spektrum massa (Arifiani, 2012).
Penggunaan secara umum kromatografi gas spektrometri massa adalah
kompleks, penentuan berat molekul dan terkadang komposisi unsur senyawa
organik yang belum diketahui dalam campuran yang kompleks, penentuan
struktur senyawa organik yang belum diketahui dengan pemcocokan spektrum
yang terdapat pada spektroskopi massa. Kromatografi gas spektrometri massa
dapat digunakan untuk identifikasi secara kualitatif dan secara kuantitatif untuk
memastikan komponen senyawa dalam campuran yang kompleks. Untuk
pengukuran kuantitatif didasarkan pada luas puncak dari kromatografi massa atau
BAB 3
METODE PENELITIAN
3.1.Tempat dan Waktu
Penelitian ini dilakukan selama ± 5 bulan, terhitung mulai dari bulan Maret –
Juli tahun 2013 di Laboratorium Penelitian I, Laboratorium Farmakognosi dan
Fitokimia, Laboratorium Kimia Obat, Laboratorium Formulasi Sediaan
SterilFakultas Kedokeran dan Ilmu Kesehatan program studi Farmasi UIN Syarif
Hidayatullah Jakarta, BPPT PUSLIT-Serpong, Balitro-Cimanggu Bogor,Pusat
Laboratorium Terpadu, LIPI Kimia-Serpong, dan Lab. Forensik Mabes
Polri-Jakarta.
3.2.Alat dan Bahan
3.2.1. Alat
Alat-alat yang digunakan dalam penelitian ini adalah tabung reaksi, rak
tabung reaksi, cawan penguap, batang pengaduk, piknometer, timbangan analitik
(Wiggen Hauser), labu destilasi (alat destilasi), oven (memmert), hot plate
(Wiggen Hauser®), cawan petri, pipet tetes, gelas piala, gelas ukur, kapas, kertas
saring, kertas saring bebas abu, erlemmeyer, corong, mikropipet, termometer,
vortex, Spektrofotometri UV (Hitachi Type U2910), Gas Chromatography-Mass
Spectrometry (Agilent), mikroskop(Olympus IX71), Atomic Absorption
Spechtrophotometer (Hitachi Z-2000 Polarized Zeeman®), Atomic Absorption
Spechtrophotometer (Spektra AA-880).
3.2.2. Bahan
Ekstrak etanol 70% herba kemangi (Ocimum americanum L.)yang
berumur 3 bulan diperoleh dari kebun kemangi di daerah Grogol, Kecamatan
Limo, Depok yang telah dideterminasi.Kloroform, aseton, n-heksan, amoniak
10%, petroleum eter, alcohol (etanol 96%), FeCl3 1%, , HCl 1%, HCl 10%, HCl
pekat, amoniak 25%, HNO3 pekat, NaOH 5%, H2SO4 pekat, H2SO4 encer, H2SO4
lempengan Mg, pewarna Anisaldehid, standar eugenol,Nutrien Agar (NA) dan
Potato Dextrose Agar (PDA)
3.3.Prosedur Penelitian
3.3.1. Determinasi Tanaman
Pemeriksaan atau determinasi tanaman dilakukan di Herbarium
Bogoriense, Pusat Penelitian Biologi LIPI, Bogor, Jawa Barat.
3.3.2. Penyiapan Simplisia
Tanaman kemangi yang diperoleh dari kebun kemangi di daerah Grogol,
Kecamatan Limo, Depok yang telah dideterminasi, kemudian disortasi dari
bahan-bahan pengotor. Lalu dilakukan pencucian dengan air mengalir hingga bersih,
setelah itu dikeringkan dengan cara diangin-anginkan hingga kering (selama ± 2
minggu). Kemudian dihaluskan dengan menggunakan blender hingga menjadi
serbuk dengan ukuran derajat kehalusan serbuk simplisia yang sesuai.Setelah itu
disimpan dalam wadah kering tertutup rapat dalam ruangan terlindung dari cahaya
matahari.
3.3.3. Pemeriksaan Karakterisasi Simplisia (Depkes RI, 1979)
3.3.3.1. Uji Makroskopik
Uji makroskopik bertujuan untuk menentukan ciri khas simplisia dengan
pengamatan secara langsung berdasarkan bentuk simplisia dan ciri-ciri
organoleptik herba kemangi (Ocimum americanum L.) menurut literatur secara
umum.
3.3.3.2. Uji Mikroskopik
Uji mikroskopik mencakup pengamatan terhadap bagian simplisia dan
fragmen pengenal dalam bentuk sel, isi sel atau jaringan tanaman serbuk simplisia
herba kemangi (Ocimum americanum L) secara umum yang dilakukan
3.3.4. Penyiapan Ekstrak
Serbuk simplisia herba kemangi dimaserasi dengan menggunakan etanol
70% selama 24 jam dan pada 6 jam pertama sekali-sekali dilakukan pengadukan.
Hasil maserasi disaring dengan kapas dan kertas saring.Selanjutnya, residu
dimaserasi kembali hingga warna coklat bening.Filtrat herba kemangi yang
diperoleh disatukan dan dipekatkan dengan menggunakan rotary evaporator pada
suhu 400C - 500C sampai diperoleh ekstrak kental. Rendemen dari ekstrak
kemudian dihitung dengan rumus :
3.3.5. Pengujian Parameter Spesifik
3.3.5.1. Identitas (Depkes RI, 2000)
Pendiskripsian tata nama, yaitu nama ekstrak, nama latin tumbuhan,
bagian tumbuhan yang digunakan, dan nama Indonesia tumbuhan.
3.3.5.2. Organoleptik (Depkes RI, 2000)
Penetapan organoleptik yaitu dengan pengenalan secara fisik dengan
menggunakan panca indera dalam mendiskripsikan bentuk, warna, bau, dan rasa.
3.3.5.3. Senyawa Terlarut Dalam Pelarut Tertentu
Pengujian senyawa terlarut dalam pelarut tertentu dalam ekstrak terdiri
dari kadar senyawa yang terlarut dalam air dan kadar senyawa yang terlarut dalam
etanol(Depkes RI, 2000; Saifudin, Rahayu, & Teruna, 2011).
(i) Kadar Senyawa yang Larut dalam Air
Sejumlah 1 g ekstrak (W1) dimaserasi dengan 25 mL kloroform selama 24
jam, menggunakan labu ukur sambil berkali-kali dikocok selama 6 jam pertama.
Kemudian didiamkan selama 18 jam dan disaring. Filtrat sebanyak 5 mL
diuapkandalam cawan dangkal berdasar rata yang telah ditara (W0) dengan cara
residu pada suhu 105oC hingga bobot tetap (W2)(Saifudin, Rahayu, & Teruna,
2011).
Keterangan :
W0 = bobot cawan kosong
W1 = bobot ekstrak awal
W2 = bobot cawan + residu yang dioven
(ii) Kadar Senyawa yang Larut dalam Etanol
Sejumlah 1 g ekstrak (W1) dimaserasi dengan 25 mL etanol 96%, selama 24
jam dengan menggunakan labu bersumbat sambil berkali-kali dikocok selama 6
jam pertama. Kemudian didiamkan selama 18 jam dan disaring cepat untuk
menghindarkan penguapan etanol. Filtrat sebanyak 5 mL diuapkan dalam cawan
dangkal berdasar rata yang telah ditara (W0) dengan cara didiamkan sampai
pelarutnya menguap dan tersisa residunya, panaskan residu pada suhu 105oC
hingga bobot tetap (W2)(Saifudin, Rahayu, & Teruna, 2011).
Keterangan :
W0 = bobot cawan kosong
W1 = bobot ekstrak awal
W2 = bobot cawan + residu yang dioven
3.3.5.4. Uji Kandungan Kimia Ekstrak
(i) Uji Penapisan Fitokimia
(a) Identifikasi Alkaloid
Ekstrak 0,5 gram dalam tabung reaksi ditambahkan 2 mL etanol 70%
kemudian diaduk, ditambahkan 5 ml HCl 2 N, dipanaskan pada penangas air.
Setelah dingin, campuran disaring dan filtrat ditambahkan beberapa tetes reagen
Mayer. Sampel kemudian diamati hingga keruh atau ada endapan (Mojab,
(b) Identifikasi Flavonoid
Ekstrak 0,5 gram dalam cawan ditambahkan 2 mL etanol 70% kemudian
diaduk, ditambahkan serbuk magnesium 0,5 g dan 3 tetes HCl pekat.
Terbentuknya warna jingga sampai merah menunjukkan adanya flavon, merah
sampai merah padam menunjukkan flavanol, merah padam sampai merah
keunguan menunjukkan flavanon (Mojab, Kamalinejad, Ghaderi, & Vahidipour,
2003).
(c) Identifikasi Saponin
Ekstrak 0,5 gram dalam tabung reaksi ditambahkan 2 mL etanol 70%
kemudian diaduk, ditambahkan dengan 20 mL aquabides dan dikocok kemudian
didiamkan selama 15-20 menit.Jika tidak ada busa = negatif; busa lebih dari 1 cm
= positif lemah; busa dengan tinggi 1,2 cm = positif; dan busa lebih besar dari 2
cm = positif kuat (Mojab, Kamalinejad, Ghaderi, & Vahidipour, 2003; Sarma &
Babu, 2011).
(d) Identifikasi Triterpenoid
Ekstrak 0,5 gram dalam tabung reaksi ditambahkan 2 mL etanol 70%
kemudian diaduk, ditambahkan 1 mL kloroform dan 1 mL asetat anhidrida lalu
didinginkan. Setelah dingin, ditambahkan H2SO4. Jika terjadi warna kemerahan,
menunjukkan adanya triterpenoid (Mandal dan Ghasal, 2012).
(e) Identifikasi Steroid
Ekstrak 0,5 gram dalam tabung reaksi ditambahkan 2 mL etanol 70%
kemudian diaduk, ditambahkan 2 mL kloroform, kemudian ditambahkan 2 mL
H2SO4 pekat dengan cara diteteskan pelan-pelan dari sisi dinding tabung reaksi.
Pembentukan cincin warna merah menunjukkan adanya steroid (Mandal dan
Ghasal, 2012).
(f) Identifikasi Tanin
Ekstrak 0,5 gram dalam cawan ditambahkan 2 mL etanol 70% kemudian
biru-hitam, hijau atau biru-hijau dan endapan (Mojab, Kamalinejad, Ghaderi, &
Vahidipour, 2003).
(g) Identifikasi Minyak Atsiri
Ekstrak 2 gram dalam tabung reaksi (volume 20 mL) ditambahkan 10 mL
pelarut petroleum eter dan dipasang corong (yang diberi lapisan kapas yang telah
dibasahi dengan air) pada mulut tabung, dipanaskan selama 10 menit diatas
penangas air dan didinginkan lalu disaring dengan kertas saring. Filtrat yang
diperoleh diuapkan dengan cawan penguap hingga diperoleh residu. Residu
dilarutkan dengan pelarut alkohol sebanyak 5 mL lalu disaring dengan kertas
saring. Filtratnya diuapkan dalam cawan penguap, jika residu berbau
aromatik/menyenangkan maka hal itu menunjukkan adanya senyawa golongan
minyak atsiri (Farnsworth, 1966).
(ii) Analisis Komponen Senyawa Kimia dengan GCMS (Agilent MSD ChemStation G1701EA E.02.02.1431)
Analisis komponen senyawa kimia ekstrak dilakukan dengan menggunakan
Gas Chromatography-Mass Spectrometrydengan model number Agilent
19091S-433E yang disuntikkan sebanyak 1,0 mikroliter, dengan kondisi kolom HP-5MS
dan temperatur maksimum 3500C dengan aliran awal kolom 1,00 ml/min, gas
pembawa adalah Helium dengan tekanan kolom 8,57 psi, split rasio 50:1, split
aliran 49,0 ml/menit dengan total aliran 52,9 ml/min dan suhu awal 290oC ditahan
selama selama 2 menit dengan aliran 20,0 ml/min sampai seluruh komponen
selesai dielusi. Komponen diidentifikasi dengan mencocokkan spektrum massa
pada Library seperti Wiley dan Nasional Institute of Standards and Technology
(NIST).
(iii) Penentuan Kadar Senyawa Marker (Eugenol) dalam Ekstrak Etanol Herba Kemangi (Ocimum americanum L.)
Penentuan kadar senyawa marker dengan menggunakan senyawa
pembanding yaitu eugenol standar. Penetapan ini dilakukan dengan membuat
standar yaitu 12,5 ppm, 25 ppm, 50 ppm, 100 ppm, dan 500 ppm.Kemudian lima
seri konsentrasi ini disuntikkan ke alat GCMS sebanyak 1,0 mikroliter dengan
spesifikasi alat sama seperti point (ii)), sehingga didapatkan nilai response (luas
area) dari berbagai seri konsentrasi. Setelah itu data yang didapat diplot, sehingga
didapatkan kurva kalibrasi dan persamaan regresi liniernya.Untuk penetapan
kadar senyawa marker (eugenol), data response (luas area) yang didapat untuk
eugenol dalam sampel ekstrak yang disuntikan ke alat GCMS sebanyak 1,0
mikroliter kemudian dimasukkan kedalam persamaan regresi linier dan ditetapkan
kadar senyawa marker (eugenol) didalam ekstrak.
3.3.6. Pengujian Parameter Non Spesifik
3.3.6.1. Kadar Abu
(i) Penetapan Kadar Abu Total
Sebanyak 1 gram ekstrak ditimbang seksama (W1) dimasukkan dalam krus
silikat yang sebelumnya telah telah dipijarkan dan ditimbang (W0). Setelah itu
ekstrak dipijar dengan menggunakan tanur secara perlahan-lahan (dengan suhu
dinaikkan secara bertahap hingga 600 ± 250C (Depkes RI, 1980 dalam Arifin, H.,
Anggraini, Handayani, & Rasyid, 2006) hingga arang habis.Kemudian ditimbang
hingga bobot tetap (W2).
Keterangan :
W0 = bobot cawan kosong (gram)
W1 = bobot ekstrak awal (gram)
W2 = bobot cawan + ekstrak setelah diabukan (gram)
(ii) Penetapan Kadar Abu yang Tidak Larut dalam Asam
Abu yang diperoleh pada penetapan kadar abu dididihkan dengan 25 ml
asam sulfat encer selama 5 menit, kumpulkan bagian yang tidak larut asam.
Kemudian disaring dengan kertas saring bebas abu dan residunya dibilas dengan
krus silikat yang sama. Setelah itu ekstrak dipijar dengan menggunakan tanur
secara perlahan-lahan (dengan suhu dinaikan secara bertahap hingga 600 ± 250C
(Depkes RI, 1980 dalam Arifin, H., Anggraini, Handayani, & Rasyid, 2006))
hingga arang habis.Kemudian ditimbang hingga bobot tetap (W3).
Keterangan :
W0 = bobot cawan kosong (gram)
C = bobot kertas saring (gram)
W1 = bobot ekstrak awal (gram)
W2 = bobot cawan + abu yang tidak larut asam (gram)
3.3.6.2. Bobot Jenis
Piknometer yang bersih, kering ditimbang.Kemudian dikalibrasi dengan
menetapkan bobot piknometer dan bobot air yang baru dididihkan pada suhu 25oC
kemudian ditimbang (W1). Ekstrak cair diatur suhunya kurang lebih 20oC lalu
dimasukkan ke dalam piknometer kosong, buang kelebihan ekstrak, atur suhu
piknometer yang telah diisi hingga suhu 25oC kemudian ditimbang (W2) (Depkes
RI, 2000).
Keterangan :
d = bobot jenis
W0 = bobot piknometer kosong
W1 = bobot piknometer + air
3.3.6.3. Kadar Air
Penetapan kadar air dilakukan dengan cara destilasi toluena. Toluena
yang digunakan dijenuhkan dengan air terlebih dahulu, setelah dikocok
didiamkan, kedua lapisan air dan toluena akan memisah, lapisan air dibuang.
Sebanyak 10 g ekstrak yang ditimbang dengan seksama dimasukkan kedalam labu
alas bulat dan ditambahkan toluena yang telah dijenuhkan dengan air. Labu
dipanaskan hati-hati selama 100 menit, setelah toluena mulai mendidih,
penyulingan diatur 2 tetes/detik, lalu 4 tetes/detik.Setelah semua toluena
mendidih,dilanjutkan pemanasan selama 5 menit. Kemudian, dibiarkan tabung
menerima dingin sampai temperatur kamar. Setelah lapisan air dan toluena
memisah sempurna, volume air dibaca dan dihitung kadar air dalam persen
terhadap berat ekstrak semula. Pekerjaan diulang tiga kali.(Saifudin, Rahayu, &
Teruna, 2011).
Keterangan :
V = Volume air (ml)
W = Bobot ekstrak (gr)
3.3.6.4. Sisa Pelarut
Ektrak mengandung etanol 30% atau kurang. Timbang sejumlah 2,0
gram ekstrak kental dilarutkan dalam air sampai 25,0 ml kemudian dimasukkan
kedalam labu destilasi. Atur suhu destilat pada 78,5oC.Catat destilasi hingga
diperoleh destilat lebih kurang 2 ml lebih kecil dari volume cairan uji (destilasi
selama 2 jam atau tidak menetes lagi). Tambahkan air sampai 25,0 ml. Tetapkan
bobot jenis cairan pada suhu 25oC seperti yang tetera pada Penetapan Bobot Jenis.
Hitung persentase dalam volume dari etanol dalam cairan menggunakan Tabel
Bobot Jenis dan Kadar Etanol pada Farmakope Indonesia Edisi IV (Depkes RI,
3.3.6.5. Cemaran Mikroba
Pada penyiapan sampel ditimbang 1 gram ekstrak. Sampel dimasukkan
ke dalam labu ukur 10 ml ditambah aquadest sampai 10,0 mL sehingga diperoleh
pengenceran 10-1, dan dikocok hingga larut atau dengan bantuan vortex.
Dilanjutkan dengan pengenceran 10-2 dan 10-3(Depkes RI, 2000; Saifudin,
Rahayu, & Teruna, 2011).
(i) Angka Lempengan Total (ALT)
Dipipet 1 ml dari tiap pengenceran ke dalam cawan petri yang steril (duplo),
dengan menggunakan pipet yang berbeda dan steril untuk tiap pengenceran.Ke
dalam tiap cawan petri dituangkan 5 ml media Nutrient Agar yang telah dicairkan
bersuhu kurang lebih 45oC. Cawan petri digoyangkan dengan hati-hati (putar dan
goyangkan ke depan dan ke belakang serta ke kanan ke kiri) hingga sampel
bercampur rata dengan pembenihan. Kemudian dibiarkan hingga campuran dalam
cawan petri membeku.Cawan petri dengan posisi terbalik dimasukkan kedalam
lemari inkubator suhu 35oC selama 24 jam.Catat pertumbuhan koloni pada
masing-masing cawan yang mengandung 30-300 koloni setelah 24 jam.Hitung
ALT dalam koloni/g sampel dengan mengalikan jumlah rata-rata koloni pada
cawan dengan faktor pengenceran yang sesuai (Depkes RI, 2000; Saifudin,
Rahayu, & Teruna, 2011).
(ii) Kapang dan Khamir
Kedalam cawan petri yang steril (duplo) tuangkan 5 ml media Potato
dextros Agar yang telah dicairkan bersuhu 45oC, biarkan membeku pada cawan.
Pipet 0,5 ml dari tiap pengenceran kedalam cawan petri yang steril (metode
semai), dengan menggunakan pipet yang berbeda dan steril untuk tiap
pengenceran. Cawan petri digoyangkan dengan hati-hati hingga sampel tersemai
secara merata pada media. Kemudian diinkubasikan pada suhu kamar atau 25oC
selama 7 hari. Dicatat hasil sebagai jumlah kapang dan khamir/g sampel
3.3.6.6. Cemaran Aflatoksin
Untuk uji kualitatif metode yang dipersyaratkan adalah dengan
menggunakan Kromatografi Lapis Tipis (KLT).Ekstrak di KLT dengan
menggunakan pembanding campuran aflatoksin B1. Eluen yang digunakan adalah
campuran kloroform: aseton: n heksan (83:15:20) dengan jarak rambat 8 cm.
Kemudian hasil dilihat pada sinar uv 366 nm, jika terlihat adanya bercak dan
warna yang sama (biru atau hijau kebiruan) menandakan positif adanya aflatoksin.
Selanjutnya analisa secara kuantitatif dilakukan jika analisa kualitatif positif.
Analisa kuantitatif dengan menggunakan High Performance Liquid
Chromatography (HPLC) (Saifudin, Rahayu, & Teruna, 2011).
3.3.6.7. Cemaran Logam Berat
Penetapan kadar Arsen (As), Timbal (Pb) dan Kadmium (Cd) dengan
menggunakan alat Atomic Absorption Spechtrophotometer. Penetapan kadar
ketiga logam berat dilakukan dengan cara digesti basah. Ditimbang 1 gram
ekstrak dan ditambahkan 10 ml HNO3 pekat, kemudian dipanaskan dengan
heating mantel hingga kental atau kering. Ekstrak yang kental dan dingin
ditambahkan aquadest 10 ml dan asam perkolat 5 ml, kemudian dipanaskan
hingga kental lalu disaring ke labu ukur 50 ml. Sampel diukur dengan alat Atomic
BAB 4
HASIL DAN PEMBAHASAN
4.1Hasil Penelitian
4.1.1 Hasil Determinasi Tanaman
Determinasi tanaman dilakukan di Herbarium Bogoriense Pusat Penelitian
Biologi LIPI, Bogor, Jawa Barat. Hasil determinasi menunjukkan bahwa sampel
yang digunakan adalah tanaman kemangi (Ocimum americanum L.) famili
Lamiaceae. Hasil determinasi dapat dilihat pada lampiran 2.
4.1.2 Hasil Karakterisasi Simplisia
4.1.2.1. Uji Makroskopik
Pada uji makroskopik dilakukan pengamatan secara langsung terhadap
bentuk fisik dari herbakemangi (Ocimum americanum L.). Pengamatan yang telah
dilakukan diperoleh data sebagai berikut:
Tabel 4.1. Hasil Uji Makroskopik Herba Kemangi (Ocimum americanum L.)
No Sampel uji Literatur
1 Kemangi secara umum
Tanaman mempunyai batang
tegak, yang tingginya sekitar 60
cm atau 0,6 meter.
Tanaman berbatang tegak, tinggi
tanaman antara 0,3 – 1 meter
(Siemonsma, J.S & Piluek, 1994).
2 Batang
Batang muda tanaman berwarna
hijau, setelah tua berwarna
kecoklatan. Bentuk batang muda
persegi terdapat bulu-bulu halus.
Batang muda berwarna hijau,
setelah tua berwarna kecoklatan;
bentuk batang muda persegi; pada
batang terdapat bulu terutama pada
tanaman muda (Martono,