PEMBUATAN BIOPLASTIK POLI-
β
-HIDROKSIALKANOAT
(PHA) YANG DIHASILKAN OLEH Rastonia eutropha PADA
SUBSTRAT HIDROLISAT PATI SAGU DENGAN
PEMLASTIS ISOPROPIL PALMITAT
Oleh
JUMMI WALDI
F34102017
2007
Hidup akan terasa indah jikalau kita mau menikmati
setiap episode-episode yang kita jalani. Hidup bukanlah
untuk menyesali kondisi yang ada, sebab kita bisa
mengambil hikmah dari setiap kejadian yang kita rasakan
dan alami. Memang hidup itu penuh dengan ‘jalan yang
berliku’; selalu dihadapkan dengan masalah, baik besar
maupun kecil. Kita perlu menyadari bahwa setiap masalah
yang kita hadapi adalah sebuah tahapan untuk menuju
kedewasaan dalam menjalani serta mengarungi kehidupan
ini.
JUMMI WALDI. F34102017. Pembuatan Bioplastik Poli-β-Hidroksialkanoat (PHA) yang Dihasilkan oleh Rastonia Eutropha pada Substrat Hidrolisat Pati Sagu dengan Pemlastis Isopropil Palmitat. Dibawah bimbingan Chilwan Pandji dan Khaswar Syamsu. 2007.
RINGKASAN
Penggunaan bahan dasar plastik yang dapat didegradasi secara biologis oleh mikroorganisme alami sebagai substitusi plastik berbasis petrokimia merupakan salah satu alternatif untuk mengatasi permasalahan lingkungan yang ditimbulkan oleh sampah-sampah non-organik. Salah satu bahan bioplastik yang cukup penting dan masih terus diteliti serta dikembangkan sampai saat ini adalah Poli-β-Hidroksialkanoat (PHA). Poli-β-hidroksialkanoat (PHA) merupakan poliester hidroksialkanoat yang disintesa oleh sejumlah bakteri sebagai komponen simpanan energi dan karbon intraseluler, diakumulasi sebagai granula dalam sitoplasma sel (Lee, 1996). Pada penelitian ini PHA diperoleh dari hasil kultivasi
Ralstonia eutropha secara fed-batch selama 96 jam pada substrat hidrolisat pati sagu.
Pemlastis adalah cairan aditif yang digunakan untuk melembutkan polimer plastik sehingga dapat merubah sifat kaku menjadi lebih fleksibel. Berdasarkan komposisi asam lemak minyak sawit yang unik dengan kadungan asam lemak utama, yaitu asam oleat dan palmitat atau fraksi olein dan stearin, kedua fraksi tersebut dapat dikonversi menjadi pemlastis. Salah satu ester asam lemak minyak sawit yang dapat dimanfaatkan sebagai pemlastis adalah isopropil palmitat (Sadi dan Purboyo, 1996). Isopropil palmitat merupakan ester dari isopropil alkohol dan asam palmitat, mempunyai nama resmi 1-metil etil heksadekanoat (Anonim1, 2006).
Pembuatan bioplastik dilakukan dengan metode solution casting dan menggunakan klorofom sebagai pelarut. Konsentrasi isopropil palmitat (IPP) yang dipakai adalah 0% (b/b) (kontrol), 10% (b/b), 15% (b/b), dan 20% (b/b). Untuk melihat pengaruh penambahan IPP sebagai pemlastis maka dilakukan karakterisasi sifat mekanis, gugus fungsi, sifat termal, dan derajat kristalinitas dari bioplastik yang dihasilkan.
Berdasarkan hasil penelitian diperoleh kesimpulan bahwa kuat tarik bioplastik PHA yang dibuat dengan menggunakan pemlastis IPP semakin turun sejalan dengan peningkatan konsentrasi IPP sebagai pemlastis. Nilai kuat tarik bioplastik dengan konsentrasi IPP 0% (b/b), 10% (b/b), 15% (b/b), dan 20% (b/b) adalah berturut-turut sebesar 10.923 MPa, 6.1371 MPa, 4.6219 MPa, dan 2.6160 MPa. Nilai perpanjangan putus bioplastik dengan konsentrasi IPP 0% (b/b), 10% (b/b), 15% (b/b), dan 20% (b/b) adalah berturut-turut sebesar 2.7262%, 2.8534%, 2.8649%, dan 1.7147%. Dan nilai elastic modulus bioplastik dengan konsentrasi IPP 0% (b/b), 10% (b/b), 15% (b/b), dan 20% (b/b) adalah berturut-turut sebesar 500.99 MPa, 298.18 MPa, 208.81 MPa, dan 182.64 MPa.
mekanik tersebut dapat dinyatakan bahwa bioplastik yang dibuat dengan konsentrasi IPP 15% (b/b) adalah yang terbaik.
Analisa gugus fungsi bioplastik tanpa pemlastis (Juari, 2006) menunjukkan peak dominan untuk gugus fungsi PHA yaitu adanya gugus C = O ester, gugus C – O – C polimer, gugus OH, gugus CH2, gugus C – C, dan gugus
CH3. Sedangkan analisa gugus fungsi untuk bioplastik dengan konsentrasi IPP
15% (b/b) menunjukan C = O ester pada bilangan panjang gelombang 1724.2. Sifat termal polimer meliputi pengujian suhu peralihan kaca Tg (glass transition) dan suhu pelelehan Tm (melting point). Hasil analisa DSC PHA tanpa
pemlastis (Juari, 2006) dan bioplastik dengan konsentrasi IPP 15% (b/b) tidak dapat dibandingkan secara nyata karena terdapat beberapa perbedaan diantaranya kemurnian bahan baku (PHA) yang digunakan dan keakuratan alat pengujian. Tm
untuk PHA tanpa pemlastis adalah sebesar 168,72 oC sedangkan Tm untuk
bioplastik dengan konsentrasi IPP 15% (b/b) adalah sebesar 168.8 oC.
PHA dengan derajat kristalinitas 100% mempunyai perubahan entalpi sebesar 146 J/g (Hahn et al.,1995). Dengan metode perbandingan langsung antara perubahan entalpi bioplastik sampel dan PHA 100% kristalin, maka dapat diketahui nilai derajat kristalinitas bioplastik PHA tanpa pemlastis adalah sebesar 50,52% dan bioplastik dengan konsentrasi IPP 15% (b/b) adalah sebesar 53.97%.
JUMMI WALDI. F34102017. Production of Bioplastic Poly-ß-Hydroxyalkanoate (PHA) Produced by Rastonia eutropha Using Hydrolyzed Sago Starch Substrate with Isopropyl Palmitate as Plasticizer. Supervised by Chilwan Pandji and Khaswar Syamsu. 2007.
SUMMARY
Biodegradable polymer as a substitute for petrochemical based plastics is an alternative in solving environmental problem caused by non-organic wastes. One of the potential biodegradable polymers is Poly-ß-Hydroxyalkanoate (PHA). Poly-ß-Hydroxyalkanoate is polyester synthesized by various types of bacteria and accumulated as reserve energy and carbon in the form of granules in cytoplasm (Lee, 1996). In this research, PHA is produced by Ralstonia eutropha
fed batch cultivation for 96 hours using hydrolyzed sago starch substrate.
Plasticizer is a liquid additive which is used to soften a polymer and can change its characteristic into a more flexible shape. Based on an unique fatty acid composition of palm oil with especial content fatty acid, that is oleic acid and palmitate or fraction olein and stearin, both the fraction can be converted into plasticizers. One of fatty acid esters of palm oil that is able to be exploited as plasticizer is isopropyl palmitate (Sadi and Purboyo, 1996). Isopropyl palmitate is ester from isopropyl alcohol and palmitic acid that has the formal name of 1-metyl ethyl hexadecanoate (Anonim1, 2006).
Bioplastic was made by solution casting method and use cloroform as solvent and isopropyl palmitate as plasticizer. The concentration of isopropyl palmitate (IPP) that is used in this research were 0% (w/w) (as control), 10% (w/w), 15% (w/w), and 20% (w/w). Mechanic, functional groups, thermal and crystalline analyses were used to observe the effects of IPP addition as plasticizer.
The research results showed that bioplastic tensile strength progressively decrease with the increasing of IPP concentration. The tensile strength’s values for 0%, 10%, 15%, and 20% (w/w) IPP bioplastics are 10.923 MPa, 6.1371 MPa, 4.6219 MPa, and 2.6160 MPa. The elongation at break’s values for 0%, 10%, 15%, and 20% (w/w) IPP bioplastics are 2.7262%, 2.8534%, 2.8649%, and 1.7147%. And the values of elastic modulus for 0%, 10%, 15%, and 20% (w/w) IPP bioplastics are 500.99 MPa, 298.18 MPa, 208.81 MPa, and 182.84 MPa.
The tensile strength result for 15% (w/w) IPP bioplastic showed a yield point, which means that this bioplastic has a high value of elongation at break. Based on its mechanical characteristics, bioplastic with an addition of 15% (w/w) IPP is the best bioplastic result.
Functional groups analysis of bioplastic without plazticizer addition (Juari, 2006) showed a dominant peak for PHA’s functional groups, which is groups of C=O ester, groups of C–O–C polymer, groups of OH, groups of CH2, groups of
C–C, and groups CH3. Functional groups analysis of bioplastic with 15% (w/w)
IPP concentration could not be compared directly because there were some differences between those bioplastics, such as the purity level of raw material (PHA) that was used and the accuracy of instrument test. Tm for PHA without
plasticizer addition is 168.72 oC, while Tm of bioplastic with 15% (w/w) IPP
concentration is 168.8oC.
PHA with 100% crystalinity degree has a changing enthalpy for about 146 J/g (Hahn et al., 1995). By direct comparison method based on the changes of enthalpy bioplastics sample and PHA with 100% crystalinity degree, the crystalinity degree for bioplastic PHA without plasticizer addition is 50.52% and bioplastic PHA with 15% (w/w) IPP concentration is 53.97%.
PEMBUATAN BIOPLASTIK POLI-β-HIDROKSIALKANOAT (PHA) YANG DIHASILKAN OLEH Rastonia eutropha PADA SUBSTRAT
HIDROLISAT PATI SAGU DENGAN PEMLASTIS ISOPROPIL PALMITAT
SKRIPSI
Sebagai salah satu syarat untuk memperoleh gelar
SARJANA TEKNOLOGI PERTANIAN (STP)
Pada Departemen Teknologi Industri Pertanian Fakultas Teknologi Pertanian
Institut Pertanian Bogor
Oleh JUMMI WALDI
F34102017
2007
DEPARTEMEN TEKNOLOGI INDUSTRI PERTANIAN FAKULTAS TEKNOLOGI PERTANIAN
INSTITUT PERTANIAN BOGOR
PEMBUATAN BIOPLASTIK POLI-β-HIDROKSIALKANOAT (PHA) YANG DIHASILKAN OLEH Rastonia eutropha PADA SUBSTRAT
HIDROLISAT PATI SAGU DENGAN PEMLASTIS ISOPROPIL PALMITAT
SKRIPSI
Sebagai salah satu syarat untuk memperoleh gelar
SARJANA TEKNOLOGI PERTANIAN (STP)
Pada Departemen Teknologi Industri Pertanian Fakultas Teknologi Pertanian
Institut Pertanian Bogor
Oleh JUMMI WALDI
F34102017
Dilahirkan di Bukittinggi Tanggal 4 Mei 1984
Tanggal Lulus : 24 Januari 2007
Disetujui, Bogor, 29 Januari 2007
Drs. Chilwan Pandji, APT. MSc. Dr. Ir. Khaswar Syamsu, MSc.St.
SURAT PERNYATAAN
Saya yang bertanda tangan di bawah ini, menyatakan dengan
sebenar-benarnya bahwa skripsi yang berjudul “Pembuatan Bioplastik Poli-β
-Hidroksialkanoat (PHA) yang Dihasilkan Oleh Ralstonia eutropha pada Substrat Hidrolisat Pati Sagu dengan Pemlastis Isopropil Palmitat” adalah hasil karya sendiri dengan arahan dari dosen pembimbing, kecuali rujukan yang dengan jelas disebutkan sumbernya.
Bogor, Januari 2007 Yang bertanda tangan
RIWAYAT HIDUP
JUMMI WALDI dilahirkan di Bukittinggi, 04 Mei 1984. Penulis merupakan anak keempat dari lima bersaudara, putra dari pasangan Hasan Basri dan Rosminar. Penulis menyelesaikan pendidikan dasar hingga SLTA di kampung halaman Sumatera Barat. Penulis menyelesaikan sekolah dasar pada SD Negeri 01 Baso pada tahun 1996 dan melanjutkan ke SLTP Negeri II IV Angkat Candung pada tahun yang sama. Tahun 1999, Penulis menyelesaikan pendidikan SLTP dan melanjutkan ke SMU Negeri I IV Angkat Candung dan lulus pada tahun 2002. Pada tahun 2002, Penulis diterima di Institut Pertanian Bogor melalui jalur USMI. Penulis diterima pada Departemen Teknologi Industri Pertanian, Fakultas Teknologi Pertanian, Institut Pertanian Bogor.
Selama masa kuliah, Penulis aktif dalam berbagai organisasi dan kegiatan didalam dan luar kampus. Penulis bergabung dalam kepengurusan Himpunan Mahasiswa Teknologi Industri (HIMALOGIN) pada tahun 2003 dan memprioritaskan diri pada bidang Human Resource Development HIMALOGIN. Pada tahun yang sama, Penulis juga menjabat sebagai Ketua Ikatan Pelajar dan Mahasiswa Minang (IPMM) Bogor. Penulis menjabat sebagai ketua umum IPMM Bogor selama 2 periode kepengurusan (2003-2004).
Penulis menyelesaikan masa kuliah (insyaallah) pada Departemen Teknologi Industri Pertanian, Fakultas Teknologi Pertanian, Institut Pertanian Bogor pada tahun 2007 dengan menyelesaikan tugas akhir / skripsi dengan
berjudul “Pembuatan Bioplastik Poli-β-Hidroksialkanoat (PHA) yang
PEMBUATAN BIOPLASTIK POLI-
β
-HIDROKSIALKANOAT
(PHA) YANG DIHASILKAN OLEH Rastonia eutropha PADA
SUBSTRAT HIDROLISAT PATI SAGU DENGAN
PEMLASTIS ISOPROPIL PALMITAT
Oleh
JUMMI WALDI
F34102017
2007
Hidup akan terasa indah jikalau kita mau menikmati
setiap episode-episode yang kita jalani. Hidup bukanlah
untuk menyesali kondisi yang ada, sebab kita bisa
mengambil hikmah dari setiap kejadian yang kita rasakan
dan alami. Memang hidup itu penuh dengan ‘jalan yang
berliku’; selalu dihadapkan dengan masalah, baik besar
maupun kecil. Kita perlu menyadari bahwa setiap masalah
yang kita hadapi adalah sebuah tahapan untuk menuju
kedewasaan dalam menjalani serta mengarungi kehidupan
ini.
JUMMI WALDI. F34102017. Pembuatan Bioplastik Poli-β-Hidroksialkanoat (PHA) yang Dihasilkan oleh Rastonia Eutropha pada Substrat Hidrolisat Pati Sagu dengan Pemlastis Isopropil Palmitat. Dibawah bimbingan Chilwan Pandji dan Khaswar Syamsu. 2007.
RINGKASAN
Penggunaan bahan dasar plastik yang dapat didegradasi secara biologis oleh mikroorganisme alami sebagai substitusi plastik berbasis petrokimia merupakan salah satu alternatif untuk mengatasi permasalahan lingkungan yang ditimbulkan oleh sampah-sampah non-organik. Salah satu bahan bioplastik yang cukup penting dan masih terus diteliti serta dikembangkan sampai saat ini adalah Poli-β-Hidroksialkanoat (PHA). Poli-β-hidroksialkanoat (PHA) merupakan poliester hidroksialkanoat yang disintesa oleh sejumlah bakteri sebagai komponen simpanan energi dan karbon intraseluler, diakumulasi sebagai granula dalam sitoplasma sel (Lee, 1996). Pada penelitian ini PHA diperoleh dari hasil kultivasi
Ralstonia eutropha secara fed-batch selama 96 jam pada substrat hidrolisat pati sagu.
Pemlastis adalah cairan aditif yang digunakan untuk melembutkan polimer plastik sehingga dapat merubah sifat kaku menjadi lebih fleksibel. Berdasarkan komposisi asam lemak minyak sawit yang unik dengan kadungan asam lemak utama, yaitu asam oleat dan palmitat atau fraksi olein dan stearin, kedua fraksi tersebut dapat dikonversi menjadi pemlastis. Salah satu ester asam lemak minyak sawit yang dapat dimanfaatkan sebagai pemlastis adalah isopropil palmitat (Sadi dan Purboyo, 1996). Isopropil palmitat merupakan ester dari isopropil alkohol dan asam palmitat, mempunyai nama resmi 1-metil etil heksadekanoat (Anonim1, 2006).
Pembuatan bioplastik dilakukan dengan metode solution casting dan menggunakan klorofom sebagai pelarut. Konsentrasi isopropil palmitat (IPP) yang dipakai adalah 0% (b/b) (kontrol), 10% (b/b), 15% (b/b), dan 20% (b/b). Untuk melihat pengaruh penambahan IPP sebagai pemlastis maka dilakukan karakterisasi sifat mekanis, gugus fungsi, sifat termal, dan derajat kristalinitas dari bioplastik yang dihasilkan.
Berdasarkan hasil penelitian diperoleh kesimpulan bahwa kuat tarik bioplastik PHA yang dibuat dengan menggunakan pemlastis IPP semakin turun sejalan dengan peningkatan konsentrasi IPP sebagai pemlastis. Nilai kuat tarik bioplastik dengan konsentrasi IPP 0% (b/b), 10% (b/b), 15% (b/b), dan 20% (b/b) adalah berturut-turut sebesar 10.923 MPa, 6.1371 MPa, 4.6219 MPa, dan 2.6160 MPa. Nilai perpanjangan putus bioplastik dengan konsentrasi IPP 0% (b/b), 10% (b/b), 15% (b/b), dan 20% (b/b) adalah berturut-turut sebesar 2.7262%, 2.8534%, 2.8649%, dan 1.7147%. Dan nilai elastic modulus bioplastik dengan konsentrasi IPP 0% (b/b), 10% (b/b), 15% (b/b), dan 20% (b/b) adalah berturut-turut sebesar 500.99 MPa, 298.18 MPa, 208.81 MPa, dan 182.64 MPa.
mekanik tersebut dapat dinyatakan bahwa bioplastik yang dibuat dengan konsentrasi IPP 15% (b/b) adalah yang terbaik.
Analisa gugus fungsi bioplastik tanpa pemlastis (Juari, 2006) menunjukkan peak dominan untuk gugus fungsi PHA yaitu adanya gugus C = O ester, gugus C – O – C polimer, gugus OH, gugus CH2, gugus C – C, dan gugus
CH3. Sedangkan analisa gugus fungsi untuk bioplastik dengan konsentrasi IPP
15% (b/b) menunjukan C = O ester pada bilangan panjang gelombang 1724.2. Sifat termal polimer meliputi pengujian suhu peralihan kaca Tg (glass transition) dan suhu pelelehan Tm (melting point). Hasil analisa DSC PHA tanpa
pemlastis (Juari, 2006) dan bioplastik dengan konsentrasi IPP 15% (b/b) tidak dapat dibandingkan secara nyata karena terdapat beberapa perbedaan diantaranya kemurnian bahan baku (PHA) yang digunakan dan keakuratan alat pengujian. Tm
untuk PHA tanpa pemlastis adalah sebesar 168,72 oC sedangkan Tm untuk
bioplastik dengan konsentrasi IPP 15% (b/b) adalah sebesar 168.8 oC.
PHA dengan derajat kristalinitas 100% mempunyai perubahan entalpi sebesar 146 J/g (Hahn et al.,1995). Dengan metode perbandingan langsung antara perubahan entalpi bioplastik sampel dan PHA 100% kristalin, maka dapat diketahui nilai derajat kristalinitas bioplastik PHA tanpa pemlastis adalah sebesar 50,52% dan bioplastik dengan konsentrasi IPP 15% (b/b) adalah sebesar 53.97%.
JUMMI WALDI. F34102017. Production of Bioplastic Poly-ß-Hydroxyalkanoate (PHA) Produced by Rastonia eutropha Using Hydrolyzed Sago Starch Substrate with Isopropyl Palmitate as Plasticizer. Supervised by Chilwan Pandji and Khaswar Syamsu. 2007.
SUMMARY
Biodegradable polymer as a substitute for petrochemical based plastics is an alternative in solving environmental problem caused by non-organic wastes. One of the potential biodegradable polymers is Poly-ß-Hydroxyalkanoate (PHA). Poly-ß-Hydroxyalkanoate is polyester synthesized by various types of bacteria and accumulated as reserve energy and carbon in the form of granules in cytoplasm (Lee, 1996). In this research, PHA is produced by Ralstonia eutropha
fed batch cultivation for 96 hours using hydrolyzed sago starch substrate.
Plasticizer is a liquid additive which is used to soften a polymer and can change its characteristic into a more flexible shape. Based on an unique fatty acid composition of palm oil with especial content fatty acid, that is oleic acid and palmitate or fraction olein and stearin, both the fraction can be converted into plasticizers. One of fatty acid esters of palm oil that is able to be exploited as plasticizer is isopropyl palmitate (Sadi and Purboyo, 1996). Isopropyl palmitate is ester from isopropyl alcohol and palmitic acid that has the formal name of 1-metyl ethyl hexadecanoate (Anonim1, 2006).
Bioplastic was made by solution casting method and use cloroform as solvent and isopropyl palmitate as plasticizer. The concentration of isopropyl palmitate (IPP) that is used in this research were 0% (w/w) (as control), 10% (w/w), 15% (w/w), and 20% (w/w). Mechanic, functional groups, thermal and crystalline analyses were used to observe the effects of IPP addition as plasticizer.
The research results showed that bioplastic tensile strength progressively decrease with the increasing of IPP concentration. The tensile strength’s values for 0%, 10%, 15%, and 20% (w/w) IPP bioplastics are 10.923 MPa, 6.1371 MPa, 4.6219 MPa, and 2.6160 MPa. The elongation at break’s values for 0%, 10%, 15%, and 20% (w/w) IPP bioplastics are 2.7262%, 2.8534%, 2.8649%, and 1.7147%. And the values of elastic modulus for 0%, 10%, 15%, and 20% (w/w) IPP bioplastics are 500.99 MPa, 298.18 MPa, 208.81 MPa, and 182.84 MPa.
The tensile strength result for 15% (w/w) IPP bioplastic showed a yield point, which means that this bioplastic has a high value of elongation at break. Based on its mechanical characteristics, bioplastic with an addition of 15% (w/w) IPP is the best bioplastic result.
Functional groups analysis of bioplastic without plazticizer addition (Juari, 2006) showed a dominant peak for PHA’s functional groups, which is groups of C=O ester, groups of C–O–C polymer, groups of OH, groups of CH2, groups of
C–C, and groups CH3. Functional groups analysis of bioplastic with 15% (w/w)
IPP concentration could not be compared directly because there were some differences between those bioplastics, such as the purity level of raw material (PHA) that was used and the accuracy of instrument test. Tm for PHA without
plasticizer addition is 168.72 oC, while Tm of bioplastic with 15% (w/w) IPP
concentration is 168.8oC.
PHA with 100% crystalinity degree has a changing enthalpy for about 146 J/g (Hahn et al., 1995). By direct comparison method based on the changes of enthalpy bioplastics sample and PHA with 100% crystalinity degree, the crystalinity degree for bioplastic PHA without plasticizer addition is 50.52% and bioplastic PHA with 15% (w/w) IPP concentration is 53.97%.
PEMBUATAN BIOPLASTIK POLI-β-HIDROKSIALKANOAT (PHA) YANG DIHASILKAN OLEH Rastonia eutropha PADA SUBSTRAT
HIDROLISAT PATI SAGU DENGAN PEMLASTIS ISOPROPIL PALMITAT
SKRIPSI
Sebagai salah satu syarat untuk memperoleh gelar
SARJANA TEKNOLOGI PERTANIAN (STP)
Pada Departemen Teknologi Industri Pertanian Fakultas Teknologi Pertanian
Institut Pertanian Bogor
Oleh JUMMI WALDI
F34102017
2007
DEPARTEMEN TEKNOLOGI INDUSTRI PERTANIAN FAKULTAS TEKNOLOGI PERTANIAN
INSTITUT PERTANIAN BOGOR
PEMBUATAN BIOPLASTIK POLI-β-HIDROKSIALKANOAT (PHA) YANG DIHASILKAN OLEH Rastonia eutropha PADA SUBSTRAT
HIDROLISAT PATI SAGU DENGAN PEMLASTIS ISOPROPIL PALMITAT
SKRIPSI
Sebagai salah satu syarat untuk memperoleh gelar
SARJANA TEKNOLOGI PERTANIAN (STP)
Pada Departemen Teknologi Industri Pertanian Fakultas Teknologi Pertanian
Institut Pertanian Bogor
Oleh JUMMI WALDI
F34102017
Dilahirkan di Bukittinggi Tanggal 4 Mei 1984
Tanggal Lulus : 24 Januari 2007
Disetujui, Bogor, 29 Januari 2007
Drs. Chilwan Pandji, APT. MSc. Dr. Ir. Khaswar Syamsu, MSc.St.
SURAT PERNYATAAN
Saya yang bertanda tangan di bawah ini, menyatakan dengan
sebenar-benarnya bahwa skripsi yang berjudul “Pembuatan Bioplastik Poli-β
-Hidroksialkanoat (PHA) yang Dihasilkan Oleh Ralstonia eutropha pada Substrat Hidrolisat Pati Sagu dengan Pemlastis Isopropil Palmitat” adalah hasil karya sendiri dengan arahan dari dosen pembimbing, kecuali rujukan yang dengan jelas disebutkan sumbernya.
Bogor, Januari 2007 Yang bertanda tangan
RIWAYAT HIDUP
JUMMI WALDI dilahirkan di Bukittinggi, 04 Mei 1984. Penulis merupakan anak keempat dari lima bersaudara, putra dari pasangan Hasan Basri dan Rosminar. Penulis menyelesaikan pendidikan dasar hingga SLTA di kampung halaman Sumatera Barat. Penulis menyelesaikan sekolah dasar pada SD Negeri 01 Baso pada tahun 1996 dan melanjutkan ke SLTP Negeri II IV Angkat Candung pada tahun yang sama. Tahun 1999, Penulis menyelesaikan pendidikan SLTP dan melanjutkan ke SMU Negeri I IV Angkat Candung dan lulus pada tahun 2002. Pada tahun 2002, Penulis diterima di Institut Pertanian Bogor melalui jalur USMI. Penulis diterima pada Departemen Teknologi Industri Pertanian, Fakultas Teknologi Pertanian, Institut Pertanian Bogor.
Selama masa kuliah, Penulis aktif dalam berbagai organisasi dan kegiatan didalam dan luar kampus. Penulis bergabung dalam kepengurusan Himpunan Mahasiswa Teknologi Industri (HIMALOGIN) pada tahun 2003 dan memprioritaskan diri pada bidang Human Resource Development HIMALOGIN. Pada tahun yang sama, Penulis juga menjabat sebagai Ketua Ikatan Pelajar dan Mahasiswa Minang (IPMM) Bogor. Penulis menjabat sebagai ketua umum IPMM Bogor selama 2 periode kepengurusan (2003-2004).
Penulis menyelesaikan masa kuliah (insyaallah) pada Departemen Teknologi Industri Pertanian, Fakultas Teknologi Pertanian, Institut Pertanian Bogor pada tahun 2007 dengan menyelesaikan tugas akhir / skripsi dengan
berjudul “Pembuatan Bioplastik Poli-β-Hidroksialkanoat (PHA) yang
KATA PENGANTAR
Dengan menyebut asma Allah Subhanahuwata’ala, disertai syukur Alhamdulillah atas segala rahmat dan hidayah-Nya, sehingga penulis dapat
menyelesaikan skripsi ini, dengan judul “Pembuatan Bioplastik Poli-β
-Hidroksialkanoat (PHA) yang Dihasilkan oleh Rastonia Eutropha pada Substrat Hidrolisat Pati Sagu dengan Pemlastis Isopropil Palmitat”. Dalam menyusun skripsi ini, penulis dibantu oleh banyak pihak. Untuk itu, penulis mengucapkan terima kasih kepada:
1. Drs. Chilwan Pandji, Apt, MSc., selaku Pembimbing I, Dr. Ir. Khaswar Syamsu, MSc. St., selaku Pembimbing II, atas segala bimbingan dan arahannya, khususnya selama pelaksanaan penelitian dan selama menyusun skripsi.
2. Ir. Dwi Setyaningsih, MSi., selaku Dosen Penguji Wakil Departemen, atas segala masukkan, arahan dan perbaikkan yang telah diberikan.
3. Keluarga besar “VG-3 Sandaran” tercinta, Bapak, Mama, Uda Andi, Uni Tiwi, Uni Emma, dan si bungsu Eka, yang senantiasa memberikan dukungan dan kasih sayang tulus pada penulis.
4. Bapak Rahmat Satoto, Bapak Anung, dan Ibu Tuti atas semua masukannya yang sangat berharga bagi penulis.
5. Rekan-rekan bioplastik; Juari, Vico, Dede, Dossi, Eva, Evi, MU, dan Arban.
6. Mbak Pepi, Mbak Emi, Pak Mulya, serta Bapak, Ibu, Mas dan Mbak yang ada di Laboratorium Biorin, Genetika, Kultur Jaringan, dan Mikrobiologi PAU-IPB atas semua bantuan yang telah diberikan kepada penulis selama penulis melakukan penelitian.
ii yang telah diberikan kepada penulis selama penulis melakukan penelitian dan selama penyusunan tulisan ini.
9. Keluarga besar Pondok Islah (Bpk. dan Ibu Inan, Arief, Fitro, Rama, Joko, Heri, Lenggo, dan Mega), atas do’a, dukungan dan semangat yang telah diberikan kepada penulis.
10.Keluarga besar Core.net (Mas Puji, D’Zoel, Andra-Ujang, Akhyar-Botak), atas dukungan dan semangat yang telah diberikan kepada penulis.
11.TIN-ers 39 dan seluruh teman-teman seperjuangan (Ferri, Wahyu,
Thomas, Fifi, Sesar, Gibol, dll.
12.Pihak-pihak yang turut membantu terlaksananya penelitian dan
penyusunan skripsi yang tidak dapat penulis sebutkan satu persatu.
Dalam pelaksanaan penelitian maupun penyajian skripsi ini, penulis menyadari bahwa masih banyak terdapat kekurangan. Penulis akan menerima segala masukan yang bermanfaat untuk penyempurnaan.
Demikianlah skripsi ini penulis susun, semoga bermanfaat, dan dapat digunakan sebagai mana mestinya. Wabillahi taufiq wal hidayah.
Bogor, Januari 2007
DAFTAR ISI
KATA PENGANTAR ... i DAFTAR ISI ... iii DAFTAR TABEL ... v DAFTAR GAMBAR ... vi DAFTAR LAMPIRAN ... vii I. PENDAHULUAN ... 1
A. Latar Belakang ... 1 B. Tujuan Penelitian ... 3 C. Ruang Lingkup Penelitian ... 3
II. TINJAUAN PUSTAKA ... 4
A. Ralstonia eutropha ... 4 B. Poli-β-Hidroksialkanoat (PHA) ... 5 C. Isopropil Palmitat ... 8 D. Kloroform ... 10 E. Pembuatan Bioplastik ... 11 F. Karakteristik Bioplastik ... 12 1. Kuat Tarik dan Perpanjangan Putus ... 12 2. Gugus Fungsi ... 12 3. Sifat Termal ... 13 4. Derajat Kristalinitas ... 14
III.METODOLOGI ... 15
A. Bahan dan Alat ... 15 B. Metode Penelitian ... 16 C. Analisis Data ... 21 D. Waktu dan Tempat Penelitian ... 21
IV.HASIL DAN PEMBAHASAN ... 22
iv B. Pembuatan dan Karakterisasi Bioplastik ... 26 1. Pembuatan Bioplastik ... 26 2. Karakteristik Bioplastik ... 29 a. Sifat Mekanis ... 30 b. Analisa Gugus Fungsi ... 34 c. Sifat Termal ... 37 d. Derajat Kristalinitas ... 40 e. Densitas ... 41
V. KESIMPULAN DAN SARAN ... 43
A. Kesimpulan ... 43 B. Saran ... 44
DAFTAR TABEL
Tabel 1. Perbandingan karakteristik PHB dan PHB/HV dengan plastik
vi
DAFTAR GAMBAR
Gambar 1. Hasil scanning electron microscope granula PHB pada Ralstonia eutropha ... 5 Gambar 2. Struktur umum poli-β-hidroksialkanoat ... 5 Gambar 3. Struktur molekul poli-β-hidroksibutirat ... 6 Gambar 4. Struktur molekul isopropil palmitat ... 10 Gambar 5. Bioreaktor skala 13 liter dengan kapasitas kerja 10 liter ... 16 Gambar 6. PHA kering hasil digest dengan NaOCl 0.2% dan sentrifugasi ... 24 Gambar 7. Proses pemurnian bubuk PHA dengan ekstraksi pelarut (reflux) ... 25 Gambar 8. PHA murni hasil pemurnian dengan kloroform ... 25 Gambar 9. (a) Reaksi antara polimer dan pelarut, (b) Reaksi penambahan
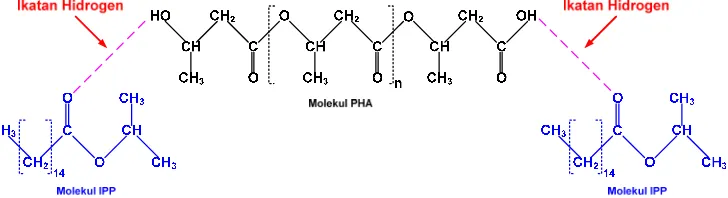
pemlastis pada polimer ... 28 Gambar 10. Pendugaan mekanisme ikatan hidrogen yang terjadi antara molekul
PHA dengan molekul IPP ... 28 Gambar 11. Ikatan hidrogen asam etanoat (asam cuka) ... 29 Gambar 12. Lembaran bioplastik yang terbentuk pada semua selang
konsentrasi ... 30 Gambar 13. Perbandingan nilai kuat tarik (a), perpanjangan putus (b), dan
elastic modulus (c) bioplastik pada berbagai selang konsentrasi .... 31 Gambar 14. Grafik hubungan kuat tarik dengan perpanjangan putus pada
konsentrasi IPP 15% ... 34 Gambar 15. Hasil spektrum FTIR PHA pati sagu tanpa pemlastis (a), dan
bioplastik dengan konsentrasi IPP 15% (b) ... 37 Gambar 16. Hasil analisa sifat termal bioplastik PHA tanpa pemlastis (a),
bioplastik PHA dengan konsentrasi IPP 15% ... 40 Gambar 17. Grafik perbandingan densitas bioplastik pada berbagai selang
DAFTAR LAMPIRAN
Lampiran 1. Diagram alir pembuatan bioplastik ... 49 Lampiran 2. Perhitungan formulasi bioplastik ... 50 Lampiran 3. a. Hasil pengukuran kuat tarik, perpanjangan putus, dan elastic
modulus bioplastik dari PHA pati sagu (konsentrasi IPP 0 %) 51 b. Hasil pengukuran kuat tarik, perpanjangan putus, dan elastic
modulus bioplastik dari PHA pati sagu (konsentrasi IPP 10%) 53 c. Hasil pengukuran kuat tarik, perpanjangan putus, dan elastic
modulus bioplastik dari PHA pati sagu (konsentrasi IPP 15%) 55 d. Hasil pengukuran kuat tarik, perpanjangan putus, dan elastic
BAB I
PENDAHULUAN
A. Latar Belakang
Penggunaan polimer sebagai material teknik terus meningkat dewasa ini, salah satu contoh penggunaannya adalah plastik. Ketidakmampuan mikroorganisme alami untuk menguraikan material ini telah menimbulkan masalah sampah non-organik, yang jika tidak ditangani dengan baik akan menimbulkan masalah yang sangat serius di masa yang akan datang. Proses
recycle yang dilakukan guna mengurangi dampak negatif yang ditimbulkan oleh sampah non-organik ini pun masih menghasilkan produk baru dengan kualitas yang rendah.
Penggunaan bahan dasar plastik yang dapat didegradasi secara biologis oleh mikroorganisme alami terus dikembangkan dalam rangka mengurangi permasalahan lingkungan yang ditimbulkan oleh sampah-sampah non-organik, terutama sampah plastik. Keuntungan lain dari penggunaan bahan baku alami dalam pembuatan plastik adalah sifatnya yang merupakan sumber daya alam yang dapat diperbaharui, sehingga keberadaannya dapat terus dilestarikan.
Beberapa contoh plastik biodegradable yang telah banyak dikomersilkan antara lain terdiri dari bahan hasil sintesis kimia seperti poli asam glikolat, poli asam laktat, poli kaprolakton, dan poli vinil alkohol; hasil kultivasi mikroba seperti golongan poliester dan polisakarida; dan yang terakhir adalah dari hasil modifikasi kimia bahan-bahan alami seperti pati, selulosa, kitin, dan protein kedelai (Huang dan Edelman dalam Scott dan Gilead, 1995)
Salah satu bahan bioplastik yang cukup penting dan masih terus diteliti serta dikembangkan sampai saat ini adalah Poli-β-Hidroksialkanoat (PHA).
Poli-β-hidroksialkanoat (PHA) merupakan poliester hidroksialkanoat yang disintesa oleh sejumlah bakteri sebagai komponen simpanan energi dan karbon intraseluler, diakumulasi sebagai granula dalam sitoplasma sel (Lee, 1996).
dasarnya atau dapat memunculkan sifat baru yang tidak ada dalam bahan dasarnya (Spink dan Waychoff dalam Frados, 1958).
Berdasarkan komposisi asam lemak minyak sawit yang unik dengan kadungan asam lemak utama, yaitu asam oleat dan palmitat atau fraksi olein dan stearin, kedua fraksi tersebut dapat dikonversi menjadi pemlastis Salah satu ester asam lemak minyak sawit yang dapat dimanfaatkan sebagai pemlastis adalah isopropil palmitat. (Sadi dan Purboyo, 1996).
Isopropil palmitat biasanya digunakan dalam pembuatan kosmetik sebagai pengental (thickening agent) dan emollient. Isopropil palmitat bersifat edible atau aman jika dikonsumsi karena isopropil palmitat dapat dihasilkan dari asam palmitat minyak sawit. Isopropil palmitat merupakan ester dari isopropil alkohol dan asam palmitat, mempunyai nama resmi 1-metil etil heksadekanoat. (Anonim1, 2006). Secara umum isopropil palmitat merupakan materi tidak beracun dan tidak menyebabkan iritasi. Toksikologi isopropil palmitat diketahui berdasarkan sifat sebagai berikut: LD50 (tikus, IP) sebesar 0,1 g/kg, LD50 (kelinci, kulit) lebih dari 5 g/kg, dan LD50 (mencit, oral) lebih dari 5 g/kg. (Anonim1, 2006)
Penggunaan pemlastis sintetis seperti dimetil ftalat (DMF) (Juari, 2006) dalam pembuatan bioplastik menggunakan PHA masih menghasilkan karakteristik bioplastik yang masih rendah. Nilai kuat tarik dan perpanjangan putus bioplastik dengan menggunakan pemlastis DMF berturut-turut adalah 3.382 MPa dan 23.88%. Selain menghasilkan karakteristik yang masih rendah, pemakaian pemlastis sintetis dalam pembuatan bioplastik dengan PHA akan menghasilkan bioplastik yang bersifat non-edible terutama jika digunakan sebagai bahan kemasan produk-produk pangan.
3
B. Tujuan Penelitian
Tujuan dari penelitian ini antara lain :
a) Mendapatkan konsentrasi pemlastis isopropil palmitat yang terbaik dalam pembuatan bioplastik PHA.
b) Mengetahui karakteristik bioplastik PHA yang dihasilkan dengan
menggunakan pemlastis isopropil palmitat.
C. Ruang Lingkup Penelitian
Ruang lingkup penelitian ini adalah:
a) Pembuatan bioplastik dengan menggunakan Poli-β-Hidroksialkanoat (PHA), isopropil palmitat sebagai pemlastis, dan kloroform sebagai pelarut.
BAB II
TINJAUAN PUSTAKA
A. Rastonia eutropha
R. eutropha termasuk bakteri gram negatif, aerob obligat, motil, suhu optimum 20 – 37 oC, koloni pada NA (Nutrient Agar) tidak berwarna, termasuk oksidase positif dan katalase positif, tidak memproduksi indol, kemoorganotrofik atau dapat menggunakan berbagai macam asam organik dan asam amino sebagai sumber karbon, dapat mereduksi NO3- menjadi NO2- dan dapat tumbuh secara
anaerobik dengan adanya NO3-. Habitat alaminya adalah tanah dan air tapi juga
dapat ditemukan pada usus vertebrata (John et al.,1994).
Lafferty et al. dalam Rehm dan Reed (1988) mengatakan bahwa PHA
dapat diproduksi oleh mikroorganisme pada kondisi pertumbuhan yang tidak seimbang, seperti ketika terbatasnya jumlah nutrien seperti nitrogen, pospat atau sulfat, konsentrasi oksigen yang rendah, atau pada kondisi rasio C:N dalam substrat tinggi.
Lee dan Choi dalam Babel dan Steinbuchel (2001) meyatakan bahwa R. eutropha dapat tumbuh baik pada media minimal yang relatif murah dan mengakumulasi PHB pada kondisi pertumbuhan yang tidak seimbang. Sumber karbon yang dapat digunakan untuk pertumbuhannya adalah D-glukosa (mutan), D-fruktosa, D-glukonat, asetat, adipat, itakonat (John et al. 1994). R. eutropha
menghasilkan PHB pada kondisi terbatasnya nitrogen, oksigen dan fosfor (Klem
dalam Robinson et al., 1999). Kim dan Lenz dalam Scheper (2001) menyatakan
bahwa ammonium merupakan nutrisi pembatas bagi R. eutropha. Polimer
5
Gambar 1. Hasil scanning electron microscopegranula PHA pada R. eutropha
(Sumber : http://che.kaist.ac.kr/~biosyst/research/pha/pha.html)
B. Poli-β-Hidroksialkanoat (PHA)
Poli-β-hidroksialkanoat (PHA) merupakan poliester hidroksialkanoat yang disintesa oleh sejumlah bakteri sebagai komponen simpanan energi dan karbon intraseluler, diakumulasi sebagai granula dalam sitoplasma sel (Lee, 1996).PHA disintesis jika salah satu elemen nutrisi seperti N, P, S, O atau Mg ada dalam jumlah terbatas namun sumber karbon ada dalam jumlah berlebih (Lee dan Choi 2001).
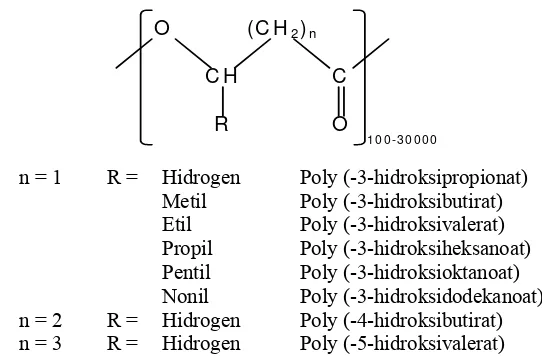
Poli-β-hidroksialkanoat (PHA) adalah poliester dari hidroksialkanoat dengan struktur umum seperti pada Gambar 2. (Ojumu et al., 2003)
O
C H
(C H2)n
C
R O
1 0 0 -3 0 0 0 0
n = 1 R = Hidrogen Poly (-3-hidroksipropionat) Metil Poly (-3-hidroksibutirat) Etil Poly (-3-hidroksivalerat) Propil Poly (-3-hidroksiheksanoat) Pentil Poly (-3-hidroksioktanoat) Nonil Poly (-3-hidroksidodekanoat) n = 2 R = Hidrogen Poly (-4-hidroksibutirat)
n = 3 R = Hidrogen Poly (-5-hidroksivalerat) Gambar 2. Struktur Umum Poli-β-hidroksialkanoat
[image:32.612.178.449.410.588.2](180oC) mendekati suhu degradasi termalnya (200oC). Kelemahan ini dapat diperbaiki dengan kopolimerisasi 3HB (hidroksibutirat) dan 3HV (hidroksivalerat) menjadi kopolimer poli-(3HB-co-3HV)yang lebih fleksibel dan rendah suhu prosesnya (Kim dan Lenz dalam Scheper, 2001). Suatu galur mutan
Ralstonia eutropha yang ditumbuhkan dengan glukosa dan asam propionat dapat menghasilkan kopolimer dari monomer 3HB dan 3HV. Kerapuhan kopolimer HB-HV lebih rendah daripada PHB, sifat termomekanisnya lebih bervariasi tergantung dari kadar unit 3-HV penyusunnya sehingga aplikasinya lebih luas (Lefebvre et al. 1997, Klem dalam Robinson et al., 1999).
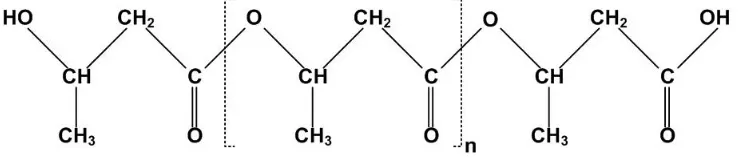
[image:33.612.137.506.399.478.2]Asam poli-β-hidroksibutirat (poli-HB) adalah polimer dengan sifat optik aktif asam D(-)-3-hidroksibutirat (3-hidroksibutanoat) dengan struktur molekul seperti pada Gambar 3. Jumlah unit berulang (n) dipengaruhi oleh beberapa faktor dan dapat mencapai nilai n = 35.000. Contoh poli-HB dengan bobot molekul mencapai 3,39 x 106 telah ditemukan pada bakteri Azotobacter vinelandii dengan menggunakan klorofom atau diklorometan pada proses ekstraksi dari massa sel (Lafferty et al. dalam Rehm dan Reed, 1988).
Gambar 3. Struktur molekul Poli-β-Hidroksibutirat (Lafferty et al. dalam Rehm dan Reed, 1988)
Menurut Poirer et al. (1995), PHB sering dibandingkan dengan
7
Tabel 1. Perbandingan Karakteristik PHB dan PHB/HV dengan Plastik Konvensional
Karakteristik Fisik
Satuan PHB PHB/HV
10% HV
PHB/HV 20% HV
PP PET HDPE PS
Melting point oC 177 150 135 170 262 135 110 Tensile strength MPa 40 25 20 34.5 56 29 50 Flexual modulus GPa 3.5 1.2 0.8 1.72 2.2 0.94 3.1 Extension to break % 3.0 20 100 400 7300 - -
Notched Izod J/m 35 100 300 45 3400 32 21
Keterangan : PP = polipropilen, PET = polietilenterephathalat, HDPE = high density polietilen, PS = polistiren. Sumber : Bryom, 1994
Menurut Atifah (2006), pengumpanan sumber karbon dilakukan pada saat bakteri memasuki fase pertumbuhan stasioner dari daur hidupnya. Bakteri
Ralstonia eutropha mengalami fase pertumbuhan logaritmik hingga jam ke 36 dan memasuki fase pertumbuhan stasioner mulai jam ke 48. Pada fase stasioner konsentrasi residu gula mendekati titik nol (<1 g/L) seiring dengan laju
pertumbuhan spesifik (μ) yang menunjukkan angka nol. Pada saat laju
pertumbuhan spesifik mendekati nol, bakteri sebagian besar tidak lagi memperbanyak diri, sehingga sumber karbon pada media digunakan untuk pembentukan PHA di dalam sitoplasmanya.
Aplikasi PHA difokuskan pada 3 hal yaitu kesehatan dan farmasi, pertanian, dan kemasan produk (Lafferty et al. di dalam Rehm dan Reid, 1988; Lee, 1996). Meskipun bidang aplikasinya luas, namun pemanfaatan PHA masih terbatas karena harganya mahal. Berbagai penelitian akhir-akhir ini diarahkan untuk menurunkan biaya produksi, meliputi penelitian tentang (1) galur bakteri baru yang dapat mensintesis PHA, (2) substrat yang murah, (3) strategi kultivasi yang baru, (4) penggunaan mikroba rekombinan, (5) pengembangan tanaman transgenik yang dapat mensintesis PHA dan (6) penggunaan kultur sel serangga (insekta) untuk memproduksi PHB (Lefebvre et al. 1997). Beberapa aplikasi
poli-β-hidroksialkanoat disajikan pada Tabel 2.
Tabel 2. Aplikasi poli-β-hidroksialkanoat
Medis dan farmasi
1 Keperluan operasi bedah: benang jahit, pin, penyeka 2 Pembalut luka
3 Pemasangan pembuluh darah dan jaringan tubuh (karena kemampuan depolimerisasi PHB menjadi monomer asam D(-)-3-hidroksibutirat 4 Pemasangan tulang dan lempeng tulang
[image:34.612.134.501.600.705.2]Pertanian
1 Pembawa (biodegradable carrier) bahan aktif pada herbisida, fungisida, insektisida atau pupuk (karena kemampuan degradasi di dalam tanah) 2 Kontainer semaian bibit
3 Matrik (biodegradable matrix) untuk obat pada bidang veteriner
Kemasan dan komoditas lain
1 Kemasan kontainer, botol, pembungkus, kantong, dan film 2 Bahan-bahan sekali pakai seperti popok bayi dan pembalut wanita Sumber : Brandl et al. dalam Babel dan Steinbuchel, 2001; Punrattanasin, 2001
C. Isopropil Palmitat
Pemlastis adalah zat aditif dengan titik didih tinggi yang dapat berupa cairan, padatan, gum sintetis atau murni alami. Penambahan pemlastis baik sintetis maupun alami bertujuan untuk memperbaiki sifat bahan selama pembuatan plastik, memperluas atau memodifikasi sifat dasarnya atau dapat memunculkan sifat baru yang tidak ada dalam bahan dasarnya (Spink dan Waychoff dalam Frados, 1958).
Perbedaan utama antara pemlastis dengan pelarut adalah kemampuan penguapan kedua bahan tersebut. Pelarut lebih mudah menguap sedangkan pemlastis tidak mudah menguap. Persyaratan ideal yang harus dimiliki suatu pemlastis meliputi kecocokan (compatibilitas), permanen atau tidaknya pemlastis tersebut berada dalam polimer, dan efisiensi penggunaannya. Pemlastis umumnya memiliki sifat-sifat tidak berbau, tidak berasa, tidak beracun dan tidak mudah terbakar (Beeler dan Finney dalam Frados, 1958).
Menurut Sadi dan Purboyo (1996), ester asam lemak epoksi atau trigliserida dapat digunakan sebagai bahan pemlastis dan stabilizer dalam industri polimer dan plastik. Berdasarkan komposisi asam lemak minyak sawit yang unik dengan kandungan asam lemak utama, yaitu asam oleat dan palmitat atau fraksi olein dan stearin, kedua fraksi tersebut dapat dikonversi menjadi pemlastis.
9 Isopropil palmitat biasanya tidak berwarna seperti ester-ester turunan oleat. Ester ini larut dalam aseton, castrol oil, kloroform, minyak biji kapas, etil asetat, etanol dan minterol oil. Ester ini tidak larut dalam air, gliserol dan propilen glikol (Sadi dan Purboyo, 1996).
Isopropil palmitat merupakan ester dari isopropil alkohol dan asam palmitat, mempunyai nama resmi 1-metil etil heksadekanoat. Rumus empiris isopropil palmitat C19H38O2 dengan rumus struktur CH3(CH2)14COOCH(CH3)2.
Struktur molekul isopropil palmitat dapat dilihat pada Gambar 4. Bobot molekul isopropil palmitat sesuai dengan rumus kimianya adalah 298,51. Pada suhu ruang isopropil palmitat merupakan cairan jernih tidak berwarna sampai berwarna kekuningan, tidak berbau, dan bersifat kental. Viskositas yang terukur adalah antara 5 sampai 10 mPa.s (5-10 cP) pada 25°C. Suhu didih isopropil palmitat adalah 160°C pada 266 Pa (2 mm Hg). Titik beku terukur antara 13 sampai 15 °C,
dan umumnya isopropil palmitat ini memadat pada suhu di bawah 16 °C.
Isopropil palmitat mudah larut dalam pelarut non polar. Isopropil palmitat larut dalam aseton, kloroform, etanol etil asetat, minyak mineral, propan-2-ol, minyak sayur, serta hidrokarbon aromatik dan alifatik. Pada prinsipnya isopropil palmitat tidak larut dalam gliserin, glikol, dan air. (Anonim1, 2006)
Gambar 4. Struktur Molekul Isopropil Palmitat
(Modifikasi www.chemicalland21.com/lifescience/foco/ISOPROPYL_PALMITATE)
Penyimpanan isopropil palmitat menuntut kondisi yang gelap, karena meteri ini memang sensitif terhadap cahaya. Isopropil palmitat menuntut resistan terhadap oksidasi dan hidrolisis, dan tidak dapat berubah menjadi tengik, namun demikian disarankan tempat penyimpanannya tertutup dengan baik. Suhu penyimpanan disarankan di atas 16°C (Anonim1, 2006).
D. Kloroform
Kloroform merupakan cairan dengan berat molekul tinggi, tidak berwarna, berbau harum, dan sangat toksik. Kloroform merupakan cairan stabil dengan titik didih rendah (Mellan, 1950).
[image:37.612.136.410.460.583.2]Karena bersifat narkotik dan toksik, kloroform tidak digunakan secara luas sebagai pelarut (Durran dan Davies, 1988). Tetapi menurut Mellan (1950) kloroform memiliki daya larut yang sangat tinggi dan telah dimanfaatkan untuk tujuan-tujuan khusus seperti untuk lemak, minyak, lilin, alkanoid, asam asetat, resin, tar, selulosa asetat, nitrat, dan berbagai kepentingan lainnya. Kloroform dapat larut dengan semua hidrokarbon terhalogenasi dan dengan sebagian besar pelarut umum lainnya. Sifat-sifat fisika dan kimia kloroform dapat dilihat pada Tabel 3.
Tabel 3. Sifat Fisik dan Kimia Kloroform
Sifat Fisik dan Kimia Nilai
Berat molekul 119.38 Gravitasi spesifik 1.499 (15 oC) Titik didih 60 – 62 oC Titik beku – 63.5 oC Panas laten penguapan 59.1 cal/g
106.4 B.t.u/lb
Panas spesifik 0.233 cal/g/oC atau B.t.u/lb/oF
Viskositas 5.63 millipoise (20 oC) 5.10 millipoise (30 oC)
Sumber : Mellan, 1950
Penggunaan pelarut (solvent) pada saat proses pembuatan plastik
11 Poli-β-hidroksialkanoat (PHA) dapat larut pada berbagai pelarut seperti kloroform, metilen klorida, etilen klorida, piridin atau campuran diklorometan/etanol (Atkinson dan Mavituna, 1991).
E. Pembuatan Bioplastik
Menurut Cowd (1991) proses terbentuknya suatu polimer dikenal dengan istilah polimerisasi. Polimerisasi ini merupakan pembentukan molekul raksasa (polimer) melalui penggabungan molekul-molekul kecil dan sederhana yang disebut monomer. Pembentukan ikatan polimer menghasilkan ikatan kunci antar monomer yang disebut sebagai ikatan tulang punggung (backbone).
Menurut Ramsay et al. (1993), terdapat dua macam cara pembuatan film PHB. Solvent-cast film dibuat dengan cara menuangkan larutan kloroform-PHB 5% (w/v) pada sebuah plat kaca atau teflon. Pelarut kemudian diuapkan dan film yang terbentuk dibiarkan selama dua minggu pada suhu ruang untuk mencapai keseimbangan kristalinitas. Heat-pressed film dibuat dengan cara menuangkan larutan 25% PHB (b/v) pada plat kaca, lalu dikeringkan semalam pada suhu ruang dan kemudian ditempatkan diantara dua lembar lempengan yang dibungkus
aluminium foil. PHB dalam cetakan lalu di-press pada suhu 155-160OC pada tekanan 5000 lb/in2 selama satu menit.
Spink dan Waychoff di dalam Frados (1958) menjelaskan teori mengenai reaksi yang terjadi antara pemlastis dengan suatu polimer. Pemlastis yang ditambahkan pada suatu bahan polimer resin akan tersisip secara fisika di antara rantai-rantai polimer tersebut. Penambahan pemlastis dapat mengakibatkan terbentuknya ‘ikatan yang hilang’. Ikatan baru yang terbentuk biasanya ikatan jembatan hidrogen antara polimer resin dan pemlastis tersebut.
F. Karakteristik Bioplastik
1. Kuat Tarik dan Perpanjangan Putus
Kuat tarik adalah gaya tarik maksimum yang dapat ditahan oleh film sampai film tersebut putus. Kuat tarik dipengaruhi oleh bahan pemlastis yang ditambahkan dalam proses pembuatan film. Persen pemanjangan merupakan perubahan panjang maksimum film sebelum terputus. Elastisitas akan menurun seiring dengan meningkatnya jumlah bahan pemlastis dalam film. Elastisitas merupakan ukuran dari kekuatan film yang dihasilkan (Latief, 2001).
Pengujian kuat tarik akan menghasilkan kurva tegangan-regangan (stress-strain). Informasi yang diperoleh dari kurva tegangan-regangan untuk polimer adalah kekuatan tarik saat putus (ultimate strength) dan perpanjangan saat putus (elongation at break, ε) dari bahan (Billmayer, 1971).
Elastisitas akan menurun seiring dengan meningkatnya jumlah bahan pemlastis dalam film. Elastisitas adalah sifat benda yang mengalami perubahan bentuk atau deformasi secara tidak permanen (Dede, 2006). Benda
dapat dikatakan elastis sempurna artinya jika gaya penyebab perubahan
bentuk hilang maka benda akan kembali ke bentuk semula. Banyak benda yang bersifat elastis sempurna yaitu mempunyai batas-batas deformasi yang disebut limit elastis sehingga jika melebihi dari limit elastik maka benda tidak akan kembali ke bentuk semula. Sifat yang lain adalah sifat plastis atau sifat tidak elastis dan perubahan cenderung tidak kembali ke bentuk semula, misalnya lilin.Perbedaan antara sifat elastis dan plastis adalah pada tingkatan dalam besar atau kecilnya deformasi yang terjadi (Dede, 2006).
Allcock dan Lampe (1981) mengatakan bahwa sifat tegangan dan regangan dari sebagian besar bahan sangat tergantung pada waktu, sehingga pada saat pengukuran harus diukur kecepatan awal tegangannya.
2. Gugus Fungsi
13 organik maupun senyawa anorganik (Fessenden dan Fessenden, 1986). Infra merah merupakan gelombang elektromagnetik dengan panjang gelombang diatas daerah sinar tampak yaitu pada 700-3000 μm atau 0.7-3 μm (Mohsenin, 1984).
Menurut Murray dan Williams dalam Williams, (1990), informasi dari spektrum pantulan ini didapat karena radiasi infra merah dekat yang dipancarkan oleh sumber radiasi berkorespondensi dengan frekuensi vibrasi dari molekul-molekul yang ada di dalam bahan organik karena setiap ikatan kimia CH, NH dan OH memiliki frekuensi vibrasi tertentu sedangkan yang tidak berkorespondensi dengan molekul yang ada dalam bahan tersebut akan dipantulkan.
Spektrum pantulan yang dihasilkan berisi basil pengukuran
parameter-parameter yang dijelaskan oleh panjang gelombang dalam nanometer,
amplitudo dengan tinggi puncak gelombang dan lebar gelombang yang menjelaskan intensitasnya sehingga dengan parameter-parameter ini seluruh informasi penyerapan dari suatu bahan dapat dijelaskan (Murray dan Williams, 1990).
3. Sifat Termal
Menurut Jandali dan Widmann (1995) analisa sifat termal merupakan suatu teknik untuk mengetahui karakteristik suatu bahan berdasarkan fungsi suhu dan waktu. Pada teknik ini, sampel dipanaskan atau didinginkan pada laju konstan. Salah satu teknik analisis sifat termal adalah DSC (Diffrential Scanning Calorimetry). Perubahan entalpi maupun suhu yang terjadi pada sampel dimonitor oleh sensor yang terpasang pada DSC, sehingga dapat
memberikan informasi tentang suhu transisi kaca (transition glass
temperature, Tg) dan suhu pelelehan (melting temperature, Tm). Informasi mengenai sifat termal suatu polimer berguna untuk menentukan aplikasi yang sesuai serta bagaimana kondisi proses terutama suhu dari polimer tersebut.
menggunakan metode ini adalah pengukuran aliran panas berdasarkan kompensasi tenaga (Rabek 1983).
4. Derajat Kristalinitas
Pengukuran derajat kristalinitas dilakukan dengan pendekatan hasil uji DSC berdasarkan perubahan entalpi yang terjadi saat tercapai suhu pelelehan. Menurut Hahn et al. (1995), PHA dengan derajat kristalinitas 100% akan mempunyai perubahan entalphi sebesar 146 J/g.
BAB III
METODOLOGI PENELITIAN
A. Bahan dan Alat 1. Bahan
Bahan-bahan yang digunakan dalam pembuatan bioplastik ini antara lain; (1) Poli-β-Hidroksialkanoat (PHA) sebagai biji plastik; (2) kloroform sebagai pelarut; (3) isopropil palmitat sebagai pemlastis. Poli-β -Hidroksialkanoat (PHA) yang digunakan dalam penelitian ini adalah PHA hasil kultivasi secara fed-batch oleh bakteri Ralstonia eutropha IAM 12368 yang diperoleh dari IAM Culture Collection, Institute of Molecular and Celular Bioscience, The University of Tokyo. Sumber karbon yang digunakan dalam substrat kultivasi adalah hidrolisat pati sagu yang dibuat dengan hidrolisis enzimatis pati sagu dengan enzim α–amilase dan amiloglukosidase.
Bahan-bahan lain yang dibutuhkan untuk kultivasi bakteri dan isolasi PHA adalah nutrient broth, (NH4)2HPO4, K2HPO4, KH2PO4,
MgSO4 0.1 m, FeSO4.7H2O, MnCl2.4H2O, CoSO4.7H2O, CaCl2.7H2O,
CuCl2.2H2O, ZnSO4.7H2O, buffer tris-hidroklorida, NaOH, NaOCl dan
NH4OH.
2. Alat
Alat-alat yang digunakan untuk kultivasi PHA adalah bioreaktor skala 13 liter dengan volume kerja 10 liter, autoklaf, pH meter, waterbath sheker, rotary shaking inkubator, sentrifuse, penyaring vakum, termometer, oven, desikator, freezer, neraca analitik, clean bench, pipet mikro, ose bunsen, pendingin tegak, hotplet, lemari asap, plat kaca, dan alat-alat gelas.
Gambar 5. Bioreaktor skala 13 liter dengan kapasitas kerja 10 liter. Laboratorium Rekayasa Bioproses – Pusat Penelitian Sumberdaya Hayati dan Bioteknologi IPB
B. Metode Penelitian
Penelitian ini terdiri dari dua tahap, yaitu tahap penyiapan bahan biji bioplastik dan tahap penelitian utama. Tahap penelitian utama terdiri dari pembuatan bioplastik dan pengujian karakteristik bioplastik yang dihasilkan.
1. Persiapan Bahan Biji Bioplastik
Secara umum tahap persiapan bahan biji plastik terdiri dari dua tahapan utama, yaitu; (1) persiapan kultur dan media kultivasi, (2) kultivasi PHA, dan (3) Proses hilir PHA.
a. Persiapan kultur dan media kultivasi (Atifah, 2006)
Kultur R. eutropha yang digunakan dipelihara dalam bentuk
kering-beku. Kultur disegarkan setiap 2 minggu pada media cair Nutrient Broth pada suhu 34oC. Media yang digunakan adalah hidrolisat pati sagu sebagai sumber karbon, (NH4)2HPO4 sebagai sumber nitrogen, K2HPO4
dan KH2PO4 sebagai sumber fosfat, serta mikroelemen yang terdiri dari
FeSO4.7H2O, MnCl2.4H2O, CoSO4.7H2O, CaCl2.2H2O, CuCl2.2H2O, dan
ZnSO4.7H2O.
Sebelum dilakukan proses kultivasi pada bioreaktor, terlebih dahulu kultur R. eutropha ditumbuhkan pada media propagasi (volume 10
17
b. Kultivasi PHA secara fed-batch (Atifah, 2006)
Kultivasi fed-batch dilakukan pada bioreaktor skala 13 liter, volume kerja 10 liter, pH 6.9, agitasi 150 rpm, suhu 34oC dan aerasi 0.2 vvm. Kultivasi dilakukan selama 96 jam. Metode pengumpanan dilakukan pada saat mikroba memasuki fase pertumbuhan stationer yaitu pada jam ke-48. Umpan berupa hidrolisat pati sagu yang setara dengan 20 gram per liter kultur dengan kecepatan pengumpanan konstan 1.7 ml/menit.
c. Proses Hilir PHA (Atifah, 2006; Imamura et al., 2001 dan Lee, 1996)
Setelah proses kultivasi selesai, cairan kultivasi disentrifugasi pada kecepatan 13000 rpm selama 10 menit. Proses sentrifugasi terdiri dari empat tahap, yaitu; (i) pemisahan biomassa dari fase cair, (ii) pencucian endapan biomassa yang diperoleh dengan aquades, (iii) digest dengan NaOCl 0.2% selama 1 jam, (iv) pencucian endapan biomassa yang telah di
digest dengan aquades. Endapan biomassa yang diperoleh dikering dalam oven pada suhu ± 50oC selama 24 jam.
PHA kering yang diperoleh dari hasil sentrifugasi terlebih dahulu dihaluskan dan kemudian dilarutkan dalam kloroform dengan perbandingan 1 gram PHA kering banding 50 ml kloroform. Larutan kemudian diaduk dan dipanaskan pada suhu ± 50oC selama 24 jam. Untuk mencegah penguapan pelarut, maka dipasang pendingin tegak. Setelah itu, larutan disaring dengan menggunakan kertas saring whatman 42 pada penyaring vakum. Filtrat hasil saringan yang mengandung PHA yang terlarut dalam kloroform diuapkan pada lemari asam untuk memperoleh PHA kering yang lebih murni.
2. Pembuatan Bioplastik PHA
a. Motode pembuatan bioplastik (modifikasi Akmaliah, 2003)
pengadukan biasa sampai terbentuk larutan PHA-kloroform-isopropil palmitat yang homogen. Kemudian larutan yang telah homogen dituang pada cetakan (plat kaca). Diagram alir proses pembuatan bioplastik dapat dilihat pada Lampiran 1.
b. Penentuan jumlah kloroform
Menurut Lee (1996), untuk melarutkan satu bagian PHA diperlukan 20 bagian pelarut. Jumlah pelarut yang optimal akan ditentukan dengan cara melarutkan PHA pada kloroform dengan perbandingan PHA-kloroform 1:5, 1:10, 1:15 dan 1:20.
c. Penentuan jumlah PHA
Jumlah PHA yang digunakan disesuaikan dengan ketebalan bioplastik yang akan dihasilkan. Jumlah PHA yang optimal adalah jumlah PHA yang mampu menutupi seluruh permukaan cetakan dan memenuhi ketebalan yang ditentukan yaitu ± 0.05 mm.
d. Penentuan jumlah Isopropil Palmitat
Jumlah isopropil palmitat yang ditambahkan tergantung pada jumlah PHA yang akan digunakan. Pada penelitian ini akan diujikan konsentrasi isopropil palmitat mulai dari 0% (kontrol), 10%, 15%, dan 20% (b/b) dari jumlah PHA.
3. Pengujian Karakteristik Bioplastik
Pengujian karakteristik yang dilakukan terhadap bioplastik pada penelitian ini meliputi pengujian sifat fisik dan mekanis bioplastik. Analisa sifat mekanis bioplastik yang dilakukan adalah kuat tarik dan perpanjangan putus, sedangkan analisa sifat fisik bioplastik yang dilakukan adalah gugus fungsi, sifat termal, derajat kristalinitas, dan densitas.
a. Sifat Mekanis (ASTM D 638 M-III, 1998)
19 Pusat Penelitian Fisika, Lembaga Ilmu Pengetahuan Indonesia (LIPI) Bandung. Alat yang digunakan untuk pengujian adalah Universal Testing Machine (UTM) yang dibuat oleh Orientec Co. Ltd dengan model
UCT-5T. Lembaran sampel dipotong menjadi dumbbell ASTM D638 M-III.
Kondisi pengujian dilakukan pada temperatur ruang uji dengan suhu 27oC, kelembaban ruang uji 65%, kecepatan tarik 1 mm/menit, skala load cell
10% dari 50 N, dan pengukuran ketebalan sampel yang akan diuji menggunakan Digital Micrometer.
Kekuatan tarik dapat dihitung dengan menggunakan persamaan berikut : (Sutiani, 1997)
A Fmaks = τ
Keterangan :
τ : kekuatan tarik (MPa) Fmaks : gaya kuat tarik (N)
A : luas permukaan contoh (mm2)
Perpanjangan putus dapat dihitung dengan menggunakan persamaan berikut : (Sutiani, 1997)
% 100 % 0 0 × − = L L L E Keterangan :
% E : perpanjangan (%)
L0 : panjang sampel mula-mula
L : panjang sampel setelah diberi beban hingga putus
Elastic modulus dapat dihitung dengan menggunakan persamaan berikut : (ASTM D 638 M-III)
strain ing correspond in difference stress in difference Modulus Elastic =
b. Gugus Fungsi (ASTM E 1252-88, 1998)
Gugus fungsi PHA dapat dideteksi dengan menggunakan alat
ASTM E 1252-88 yaitu dengan menggunakan metode KBr (Kalium Bromida) yang dipadatkan. Metode ini digunakan pada selang bilangan gelombang antara 5000 – 400 cm-1 (2 – 25 µm).
Metode pengujian sebagai berikut; sampel dihaluskan terlebih dahulu dengan menggunakan Cryogenic crusher, kemudian sampel yang telah halus dicampurkan dengan pelet KBr sebanyak ±100 mg. Kemudian campuran tersebut dikompresi, dan terakhir tablet hasil pengompresan diletakkan di tempat sel spektrofotometer infra merah dengan lubang mengarah ke sumber radiasi.
c. Sifat Termal (ASTM D 3418, 1998)
Pengujian sifat termal dilakukan di Laboratorium Uji Polimer, Pusat Penelitian Fisika, Lembaga Ilmu Pengetahuan Indonesia (LIPI) Bandung. Alat yang digunakan adalah Differential Scanning Calorimetry
(DSC) dengan tipe Seiko Instruments Inc.. Analisa sifat termal meliputi pengukuran suhu pelelehan (melting point, Tm), suhu transisi kaca (glass transition temperature, Tg), dan perubahan entalpi sampel selama proses tersebut. Sampel ditimbang ±5 mg kemudian dimasukkan kedalam
crucible 40 µl. Analisa dilakukan dengan pemanasan sampel dari
temperatur kamar hingga 200oC. Kecepatan pemanasan adalah
10oC/menit. Nitrogen cair digunakan untuk pendinginan dengan kecepatan aliran 50 ml/menit.
d. Derajat Kristalinitas (Hahn et al. 1994)
21 Kristalinitas sampel dapat dihitung dengan menggunakan persamaan sebagai berikut :
% 100
0
× Δ Δ =
H H
Xc f
Keterangan :
Xc = kristalinitas (%),
ΔHf = entalpi pelelehan sampel (J/g),
ΔH0 = entalpi pelelehan PHB 100% kristalin (146 J/g)
e. Densitas (Rabek, 1983)
Penentuan densitas dilakukan dengan cara menghitung massa dan volume sampel. Densitas bioplastik dapat dihitung dengan menggunakan persamaan berikut :
v
m
ρ
=
Keterangan :
ρ : densitas (g/cm3)
m : massa bahan (g)
v : volume bahan (cm3)
C. Analisa Data
Analisa data yang digunakan adalah statistika deskriptif. Statistika deskriptif adalah metode-metode yang berkaitan dengan pengumpulan dan penyajian suatu gugus data sehingga memberikan informasi yang berguna. Penyusunan tabel, diagram, grafik, dan besaran-besaran lain termasuk ke dalam kategori statistika deskriptif ini (Sudjana 1994 dan Walpole 1995).
D. Waktu dan Tempat Penelitian
BAB IV
HASIL DAN PEMBAHASAN
A. Persiapan Bahan Biji Bioplastik
Tahap persiapan bahan biji bioplastik terdiri dari; kultivasi PHA secara
fed-batch, dan proses hilir PHA hasil kultivasi guna mendapatkan PHA yang lebih murni.
1. Kultivasi PHA
Kultivasi Ralstonia eutropha dilakukan secara fed-batch pada bioreaktor skala 13 liter dengan kapasitas kerja 10 liter. Kultivasi sistem fed-batch mampu meningkatkan konsentrasi PHA dan rendemen PHA di dalam sel sebesar lebih dari dua kali lipat apabila dibandingkan dengan kultivasi sistem curah (Atifah, 2006). Kultivasi dilakukan selama 96 jam dengan agitasi 150 rpm, aerasi 0.2 vvm, suhu 34oC, dan pada pH rata-rata 6.9.
[image:49.612.154.494.519.619.2]Sebelum dilakukan kultivasi pada bioreaktor, terlebih dahulu R. eutropha dibiakkan pada media propagasi (volume 10 mL, 100 mL, dan 1000 mL) selama 3 x 24 jam. Propagasi pertama dilakukan pada media nutrient broth, sedangkan propagasi kedua dan ketiga dilakukan pada media propagasi yang telah terlebih dahulu disiapkan. Komposisi media propagasi dan media kultivasi pada bioreaktor disajikan dalam Tabel 4.
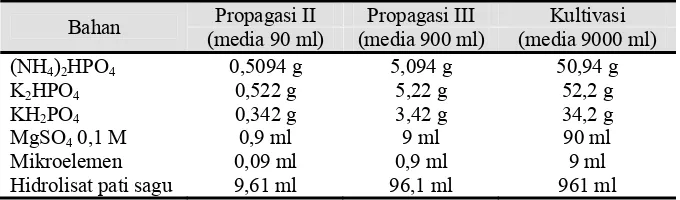
Tabel 4. Komposisi Media Propagasi II dan III Serta Media Kultivasi
Bahan Propagasi II Propagasi III Kultivasi (media 90 ml) (media 900 ml) (media 9000 ml) (NH4)2HPO4 0,5094 g 5,094 g 50,94 g
K2HPO4 0,522 g 5,22 g 52,2 g
KH2PO4 0,342 g 3,42 g 34,2 g
MgSO4 0,1 M 0,9 ml 9 ml 90 ml
Mikroelemen 0,09 ml 0,9 ml 9 ml Hidrolisat pati sagu 9,61 ml 96,1 ml 961 ml
23
hidupnya. Bakteri Ralstonia eutropha mengalami fase pertumbuhan
logaritmik hingga jam ke 36 dan memasuki fase pertumbuhan stasioner mulai jam ke 48. Pada fase stasioner konsentrasi residu gula mendekati titik nol (<1 g/L) seiring dengan laju pertumbuhan spesifik (μ) yang menunjukkan angka nol. Pada saat laju pertumbuhan spesifik mendekati nol, bakteri sebagian besar tidak lagi memperbanyak diri, sehingga sumber karbon pada media digunakan untuk pembentukan PHA di dalam sitoplasmanya.
Menurut Ayorinde et al. (1998), galur bakteri dan sumber karbon yang digunakan sangat berpengaruh terhadap PHA yang dihasilkan. Ralstonia eutropha dapat memproduksi PHB (poli-β-hidroksibutirat) menggunakan glukosa dan PHV (poli-β-hidroksivalerat) menggunakan glukosa dan asam propionat. PHB dapat disintesa oleh Ralstonia eutropha jika salah satu elemen nutrisi seperti N, P, S, O atau Mg ada dalam jumlah terbatas namun sumber karbon ada dalam jumlah berlebih (Lee dan Choi, 2001).
Pada penelitian ini, kultivasi dilakukan pada media yang mempunyai rasio C dan N sebesar 10:1 (Atifah, 2006). Nitrogen dijadikan sebagai elemen pembatas untuk pertumbuhan R. eutropha dalam mensintesis PHB. Sumber
nitrogen yang digunakan adalah (NH4)2HPO4. Perhitungan besarnya
(NH4)2HPO4 yang perlu ditambahkan pada saat formulasi media didasarkan
pada total gula sirup glukosa. Total gula pada media fermentasi adalah 30g/L. Konsentrasi C yang terdapat pada sirup glukosa (C6H12O6) adalah 40% dari
nilai total gula atau sebesar 12g/L sehingga konsentrasi N yang diperlukan adalah sebesar 1,2 g/L.
Selain C dan N, media yang digunakan juga mengandung sumber K, P, dan Mg. Sumber K dan P diperoleh dari K2HPO4 dan KH2PO4 dengan
konsentrasi sebesar 5,8 g/L dan 3,8 g/L. Sedangkan sumber Mg diperoleh dari MgSO4 dengan konsentrasi sebesar 10 ml/L.
2. Proses Hilir PHA
bahan-bahan pengotor seperti asam nukleat, protein, lemak maupun sisa media yang masih ada. Proses hilir dilakukan dalam dua tahap, yaitu tahap pertama digest dengan NaOCl 0.2 % dan sentrifugasi serta tahap kedua ekstraksi dengan pelarut.
[image:51.612.254.387.277.406.2]Endapan PHA yang diperoleh dari proses digest dengan NaOCl 0.2 % dan sentrifugasi, dikeringkan dalam oven dengan suhu ± 50oC selama 24 jam. Setelah PHA kering (Gambar 6), kemudian PHA dihaluskan dengan mortar. Bubuk PHA yang diperoleh ternyata masih kotor, karena bubuk PHA tidak dapat membetuk lembaran saat digunakan dalam pembuatan bioplastik dengan teknik casting. Untuk itu, bubuk PHA perlu dimurnikan lagi.
Gambar 6. PHA kering hasil digest dengan NaOCl 0.2 % dan sentrifugasi
Pemurnian bubuk PHA dilakukan dengan ekstraksi dengan pelarut. Pelarut yang digunakan untuk ekstraksi ini adalah kloroform (CHCl3). Karena
menurut Lafferty et al. (1988) kloroform merupakan jenis pelarut yang sering digunakan untuk mengekstrak PHA dari sel bakteri, karena PHA memiliki kelarutan yang tinggi di dalam kloroform. Atkinson dan Mavituna (1991)
menambahkan bahwa poli-β-hidroksialkanoat (PHA) dapat larut pada
berbagai pelarut seperti kloroform, metilen klorida, etilen klorida, piridin atau campuran diklorometan/etanol.
Dalam proses pemurnian ini, bubuk PHA dilarutkan dalam kloroform dengan perbandingan 1:50 (b/v). Larutan kemudian diaduk dengan
menggunakan magnetic stirer dan pendingin tegak digunakan untuk
25
Gambar 7. Proses pemurnian bubuk PHA dengan ekstraksi pelarut (reflux)
Setelah dilakukan pengadukan selama 24 jam, larutan PHA + kloroform disaring pada penyaring vakum dan mengunakan kertas saring whatman 42. Hasil penyaringan kemudian diuapkan dalam lemari asap. PHA murni yang terlarut dalam kloroform akan tertinggal dan membentuk lembaran (Gambar 8). PHA murni inilah yang digunakan dalam penelitian ini untuk membuat bioplastik.
Gambar 8. PHA murni hasil ekstraksi dengan kloroform (reflux)
Rendemen PHA murni yang diperoleh setelah proses pemurnian dengan kloroform adalah sebesar ± 40 % (5 gram dari 20 gram PHA kering), hal ini sesuai dengan pernyataan Lee dan Choi (2001), yaitu bahwa bakteri R.
eutropha dapat mengakumulasi PHA 30-80% dari bobot kering selnya. Rendemen PHA yang diperoleh tidak maksimal, karena ada beberapa hal yang dapat mempengaruhi, seperti; galur mikroba yang digunakan, jenis substrat yang dipakai, kondisi proses kultivasi, serta metode ekstraksi PHA.
[image:52.612.246.394.359.489.2]dihasilkan oleh Ralstonia eutropha dengan hidrolisat pati sagu sebagai sumber karbon pada saat kultivasi. Dari analisa dengan menggunakan FTIR (Fourier Transform Infra Red Spectroscopy) didapatkan hasil berupa spektrum infra merah yang ada pada PHA dari pati sagu, 15 dari 18 spektrum yang muncul sama dengan spektrum PHB murni (MERCK). Selain sesuai dengan ciri khas grup PHA, juga muncul gugus metil bebas (-CH3) dan metilen tunggal (-CH2-)
yang sesuai dengan struktur PHB sebagaimana disajikan pada Gambar 3. Oleh karena itu, dapat dikatakan bahwa PHA yang didapat dari kultivasi Ralstonia eutropha dengan hidrolisat pati sagu sebagai sumber karbon, merupakan jenis poli-β-hidroksibutirat (PHB).
Atifah (2006) juga menguji kadar atau tingkat kemurnian PHB yang
diperoleh dengan menggunakan Gas Chromatography (GC). Pada
kromatogram PHB yang dihasilkan muncul peak dominan pada waktu retensi yang mendekati standar (1,18) yaitu pada waktu retensi 1,25 menit dengan konsentrasi 69,69%. Dengan demikian, kadar atau kemurnian relatif PHB sagu terhadap PHB murni sebesar 76,57% (= 69,69 / 91,01 x 100%).
B. Pembuatan dan Karakterisasi Bioplastik
Tahap ini meliputi proses pembuatan bioplastik dengan menggunakan pemlastis isopropil palmitat (IPP) dan pengujian karakteristik bioplastik yang dihasilkan.
1. Pembuatan Bioplastik
Proses pembuatan bioplastik dilakukan dengan menggunakan teknik
solution casting. Penggunaan teknik ini didasarkan pada kesederhanaan alat maupun metode yang digunakan. Menurut Allcock dan Lampe (1981), teknik
solution casting merupakan pilihan yang cepat dan mudah untuk membuat film plastik pada skala laboratorium. Waddington (2000) menambahkan,
27 bagian PHA diperlukan 20 bagian pelarut. Namun setelah dilakukan percobaan dengan perbandingan PHA : pelarut sebesar 1:20 (b/b), 1:30 (b/b), 1:40 (b/b) dan 1:50 (b/b), maka diperoleh perbandingan yang tepat adalah 1:30 (b/b). Penggunaan perbandingan 1:20 (b/b) dapat menghasilkan lembaran PHA yang paling baik (berdasarkan penampakan fisik), namun pada saat penuangan larutan kedalam cetakan (plat kaca) banyak terdapat sisa PHA pada dinding botol yang digunakan untuk melarutkan PHA dengan kloroform. Hal ini dikarenakan larutan bersifat kental. Untuk itu jumlah pelarut yang digunakan dalam penelitian ini adalah 1:30 (b/b) karena pada perbandingan ini PHA tidak terlalu banyak menempel pada dinding botol.
Untuk mendapatkan ketebalan yang diinginkan (± 0.05 mm), maka terlebih dahulu ditentukan jumlah PHA optimum yang akan digunakan. Jumlah PHA optimum adalah jumlah PHA yang mampu menutupi seluruh bagian cetakan yang digunakan (4,5 x 19 cm). Dari hasil percobaan didapatkan jumlah PHA optimum untuk membuat lembaran bioplastik adalah sebesar 0.25 gram.
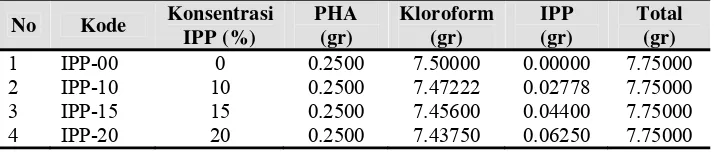
[image:54.612.150.507.527.603.2]Setelah menentukan jumlah kloroform dan PHA yang akan digunakan, langkah selanjutnya adalah menentukan jumlah isopropil palmitat (IPP) yang akan digunak