PENGUJIAN STABILITAS NATRIUM DIKLOFENAK
DALAM CANGKANG KAPSUL ALGINAT
SKRIPSI
OLEH: SYLVIA HALIM
NIM 071501037
FAKULTAS FARMASI
PENGUJIAN STABILITAS NATRIUM DIKLOFENAK
DALAM CANGKANG KAPSUL ALGINAT
SKRIPSI
Diajukan untuk melengkapi salah satu syarat untuk memperoleh Gelar Sarjana Farmasi pada Fakultas Farmasi
Universitas Sumatera Utara
OLEH: SYLVIA HALIM
NIM 071501037
FAKULTAS FARMASI
PENGESAHAN SKRIPSI
PENGUJIAN STABILITAS NATRIUM DIKLOFENAK
DALAM CANGKANG KAPSUL ALGINAT
OLEH: SYLVIA HALIM
NIM 071501037
Dipertahankan di hadapan Panitia Penguji Fakultas Farmasi
Universitas Sumatera Utara Pada tanggal : Desember 2011
Pembimbing I, Panitia Penguji,
Dra. Anayanti Arianto, M.Si., Apt. Prof. Dr. Karsono, Apt.
NIP 195306251986012001 NIP 195409091982011001
Pembimbing II, Dra. Anayanti Arianto, M.Si., Apt.
NIP 195306251986012001 .
Prof. Dr. Hakim Bangun, Apt. Dr. Kasmirul Ramlan Sinaga, M.S., Apt.
NIP 19520117198031002 NIP 195504241983031003
Dra. Azizah Nasution, M.Sc., Apt. NIP 195503121983032001
Medan, Desember 2011 Fakultas Farmasi
Universitas Sumatera Utara Dekan,
KATA PENGANTAR
Puji syukur ke hadirat Tuhan Yang Maha Kuasa yang telah melimpahkan rahmat dan karunia-Nya, sehingga penulis dapat menyelesaikan skripsi dengan judul “Pengujian Stabilitas Natrium Diklofenak dalam Cangkang Kapsul Alginat”.
Skripsi ini diajukan sebagai salah satu syarat guna memperoleh gelar Sarjana Farmasi dari Fakultas Farmasi Universitas Sumatera Utara. Pada kesempatan ini dengan segala kerendahan hati, penulis mengucapkan terima kasih yang sebesar-besarnya kepada:
1. Bapak Prof. Dr. Sumadio Hadisahputra, Apt., selaku Dekan Fakultas
Farmasi yang telah memberikan izin fasilitas sehingga penulis dapat menyelesaikan pendidikan.
2. Ibu Dra. Anayanti Arianto, M.Si., Apt. dan Bapak Prof. Dr. Hakim
Bangun, Apt., yang telah membimbing dan memberikan petunjuk serta saran-saran selama penelitian hingga selesainya skripsi ini.
3. Bapak Prof. Dr. Karsono, Apt., Bapak Dr. Kasmirul Ramlan Sinaga, M.S., Apt. dan Ibu Dra. Azizah Nasution, M.Sc., Apt., selaku penguji yang telah memberi kritik dan saran demi kesempurnaan skripsi ini.
4. Bapak Drs. David Sinurat, M.Si., Apt., selaku Kepala Laboratorium
Farmasi Fisik Fakultas Farmasi Universitas Sumatera Utara Medan yang telah memberikan izin dan fasilitas untuk penulis sehingga dapat mengerjakan dan menyelesaikan penelitian.
5. Ibu Dra. Fat Aminah, M.Sc., Apt., selaku Kepala Laboratorium Formulasi Sediaan Solid Fakultas Farmasi Universitas Sumatera Utara Medan yang telah memberikan izin dan fasilitas untuk penulis sehingga dapat mengerjakan dan menyelesaikan penelitian.
6. Bapak Prof. Dr. rer. nat. Effendy De Lux Putra, S.U., Apt., selaku
yang telah memberikan fasilitas kepada penulis selama pelaksanaan penelitian.
7. Ayah Hadi dan Ibu Veronica yang telah memberikan cinta dan kasih
sayang yang tidak ternilai dengan apapun, doa yang tulus serta pengorbanan baik materi maupun non-materi.
8. Saudara Handi Hendra serta seluruh teman-teman Farmasi USU stambuk
2007 yang tidak dapat disebutkan namanya satu per satu, atas segala dorongan motivasi dan bantuannya kepada penulis hingga selesainya penulisan skripsi ini
Penulis menyadari sepenuhnya bahwa dalam penulisan skripsi ini masih jauh dari kesempurnaan, oleh karena itu dengan segala kerendahan hati, penulis menerima kritik dan saran demi kesempurnaan skripsi ini.
Akhirnya, penulis berharap semoga skripsi ini dapat memberi manfaat bagi kita semua.
Medan, Desember 2011 Penulis,
Pengujian Stabilitas Natrium Diklofenak dalam Cangkang Kapsul Alginat
ABSTRAK
Natrium diklofenak, suatu Obat Anti Inflamasi Non Steroid (OAINS), memiliki efek samping dapat mengiritasi lambung dan penggunaan cangkang kapsul alginat dalam pembuatan suatu sediaan kapsul natrium diklofenak dapat mengurangi efek samping dari natrium diklofenak.
Tujuan penelitian ini adalah untuk mengetahui pengaruh penyimpanan dan penambahan bahan pemburam, titanium dioksida, pada cangkang kapsul terhadap stabilitas natrium diklofenak dari cangkang kapsul alginat.
Cangkang kapsul alginat dibuat dari natrium alginat 80-120cP dengan penambahan bahan pemburam titanium dioksida. Pengujiaan stabilitas fisik cangkang kapsul alginat meliputi pengamatan warna, uji waktu hancur, dan uji kerapuhan, sedangkan pengujian stabilitas fisik dan kimia cangkang kapsul alginat yang diisi natrium diklofenak meliputi pengamatan warna bahan obat, uji kerapuhan cangkang kapsul, penetapan kadar dan laju disolusi. Pengamatan warna dilakukan secara visual, uji waktu hancur menggunakan disintegration tester, kerapuhan kapsul diuji dengan capsule shell impact tester, kadar diukur secara spektrofotometri dan disolusi dilakukan dengan alat disolusi metode dayung dalam medium pH berganti. Penyimpanan dilakukan pada suhu 30°C dengan RH 70% dan suhu 40°C dengan RH 75% selama 3 bulan.
Hasil penelitian menunjukkan bahwa tidak terlihat adanya perubahan warna obat dan cangkang kapsul tidak menunjukan adanya kerapuhan setelah penyimpanan cangkang kapsul alginat yang berisi natrium diklofenak pada suhu 30°C dengan RH 70% selama 3 bulan demikian juga pada suhu 40°C dengan RH 75%. Kadar natrium diklofenak setelah penyimpanan selama 3 bulan pada suhu 30°C dengan RH 70% masih memenuhi persyaratan demikian pula pada penyimpanan suhu 40°C dengan RH 75% selama 3 bulan. Penyimpanan pada suhu 30°C dengan RH 70% dan suhu 40°C dengan RH 75% selama 3 bulan tidak berpengaruh terhadap laju disolusi. Penambahan pemburam titanium dioksida juga memperlambat laju disolusi dari natrium diklofenak dalam cangkang kapsul alginat.
Study of the Stability of Diclofenac Sodium in Alginate Capsule Shell
ABSTRACT
Diclofenac sodium, a Non-Steroidal Anti Inflammatory Drugs (NSAID), had adverse effect that could irritate stomach and the use of alginate capsule shell in a dosage form of diclofenac sodium capsule could reduce this adverse effect of diclofenac sodium.
The aim of this study is to know the effect of the storage and addition of opaque agent, titanium dioxide, to the stability of diclofenac sodium in alginate capsule shell.
Alginate capsule shell was made from sodium alginate 80 – 120 cP with the addition of opaque agent, titanium dioxide. The stability test of alginate capsule shell included observation of color, disintegration time, and brittleness, while the physical and chemical stability test of diclofenac sodium in capsule shell including observation of drug’s color, capsule shell’s brittleness, assay and dissolution. Color observation was made visually, disintegration time test was disintegration tester, brittleness test was using capsule shell impact tester, assay done by spectrophotometry and dissolution test was done by paddle method dissolution tester in changing pH. The storage was at temperature of 30°C with RH 70% and 40°C with RH 75% for 3 months.
The results showed that there was no visible color change in the drug and no presence of the capsule shell brittleness after storage of alginate capsule shell containing diclofenac sodium at a temperature of 30°C with RH 70%for 3 months as well at 40°C with 75% RH. Diclofenac sodium content after storage for 3 months at 30°C with 70% RH still qualified as well as after the storage at temperature of 40°C with 75% RH for 3 months. The storage at 30°C with 70% RH and 40°C with 75% RH for 3 months had no effect on dissolution rate. The addition of opaque agent, titanium dioxide, also slowed dissolution rate of diclofenac sodium in the alginate capsule shell.
DAFTAR ISI
Halaman
HALAMAN JUDUL ... 1
HALAMAN PENGESAHAN ... 3
KATA PENGANTAR ... 4
ABSTRAK ... 6
ABSTRACT ... 7
DAFTAR ISI ... 8
DAFTAR TABEL ... 13
DAFTAR GAMBAR ... 14
DAFTAR LAMPIRAN ... 15
BAB I PENDAHULUAN ... 16
1.1 Latar Belakang ... 16
1.2 Kerangka Pikir Penelitian ... 19
1.3 Perumusan Masalah ... 19
1.4 Hipotesis Penelitian ... 20
1.5 Tujuan Penelitian ... 20
1.6 Manfaat Penelitian ... 21
BAB II TINJAUAN PUSTAKA ... 22
2.1 Natrium Diklofenak ... 22
2.1.1 Uraian Bahan ... 22
2.1.2 Farmakologi Natrium Diklofenak ... 23
2.2 Kapsul ... 23
2.4 Titanium Dioksida ... 25
2.5 Natrium Alginat ... 25
2.6 Viskositas ... 27
2.7 Stabilitas ... 27
2.8 Waktu Hancur ... 28
2.9 Kerapuhan ... 28
2.10 Disolusi ... 29
BAB III METODE PENELITIAN ... 33
3.1 Alat-alat ... 33
3.2 Bahan-bahan ... 33
3.3 Prosedur Penelitian ... 34
3.3.1 Pembuatan Pereaksi ... 34
3.3.1.1 Larutan CaCl2 3.3.1.2 Larutan HCl 0,1 N ... 34
0,15 M ... 34
3.3.1.3 Larutan Na3PO4 3.3.1.4 Dapar fosfat pH 6,8 ... 34
0,2 M ... 34
3.3.1.5 Larutan NaOH 0,1 N ... 34
3.3.1.6 Larutan NaOH 5 N ... 34
3.3.2 Pembuatan Cangkang Kapsul Alginat ... 35
3.3.2.1 Pembuatan Larutan Natrium Alginat ... 35
3.3.2.2 Pengukuran Viskositas Larutan Natrium Alginat ... 36
3.3.2.3 Pembuatan Badan Cangkang Kapsul Alginat .. 37
3.3.2.4 Pembuatan Tutup Cangkang Kapsul Alginat ... 37
3.3.3 Pembuatan Kurva Serapan dan Kurva Kalibrasi Natrium
Diklofenak ... 38
3.3.3.1 Pembuatan Larutan Induk Baku Natrium Diklofenak ... 38
3.3.3.2 Pembuatan Kurva Serapan Larutan Natrium Diklofenak dalam Medium Cairan Lambung Buatan (pH 1,2) ... 38
3.3.3.3 Pembuatan Kurva Kalibrasi Larutan Natrium Diklofenak dalam Medium Cairan Lambung Buatan (pH 1,2) ... 38
3.3.3.4 Pembuatan Kurva Kalibrasi Larutan Natrium Diklofenak dalam Medium Cairan Usus Buatan (pH 6,8) ... 39
3.3.3.5 Pembuatan Kurva Kalibrasi Larutan Natrium Diklofenak dalam Medium Cairan Usus Buatan (pH 6,8) ... 39
3.3.4 Pengisian Natrium Diklofenak dalam Kapsul Alginat . 39 3.3.5 Penyimpanan ... 40
3.3.5.1 Penyimpanan pada Suhu 30°C; RH 70% ... 40
3.3.5.2 Penyimpanan pada Suhu 40°C; RH 75% ... 40
3.3.6 Pengujian ... 40
3.3.6.1 Penentuan Spesifikasi Cangkang Kapsul ... 40
3.3.6.1.1 Pengukuran Panjang dan Diameter Cangkang Kapsul ... 40
3.3.6.1.2 Penimbangan Berat Cangkang Kapsul ... 40
3.3.6.1.3 Pengukuran Ketebalan Cangkang Kapsul ... 41
3.3.6.1.4 Pengamatan Warna Cangkang Kapsul ... 41
3.3.6.2 Pengujian Pengamatan Warna ... 41
3.3.6.3 Uji Waktu Hancur (Disintegrasi) ... 41
3.3.6.4 Uji Kerapuhan ... 42
3.3.6.4.1 Cangkang Kapsul Kosong ... 42
3.3.6.1.2 Cangkang Kapsul Berisi (Uji Ketahanan terhadap Tekanan) ... 42
3.3.6.5 Penentuan Kadar Natrium Diklofenak dalam Kapsul Alginat ... 42
3.3.6.6 Uji Disolusi ... 43
BAB IV HASIL DAN PEMBAHASAN ... 45
4.1 Viskositas Larutan Natrium Alginat ... 45
4.2 Spesifikasi Cangkang Kapsul Alginat ... 45
4.3 Sifat Fisik Cangkang Kapsul dan Bahan Obat ... 47
4.3.1 Sifat Fisik Cangkang Kapsul ... 47
4.3.2 Sifat Fisik Bahan Obat dalam Cangkang Kapsul Alginat ... 48
4.4 Uji Waktu Hancur (Disintegrasi) ... 48
4.5 Penentuan Kadar Natrium Diklofenak dalam Kapsul Alginat. 54 4.6 Uji Kerapuhan ... 55
4.6.1 Cangkang Kapsul Kosong ... 56
4.6.2 Cangkang Kapsul Berisi (Uji Ketahanan Terhadap Tekanan) ... 57
4.7 Profil Disolusi Natrium Diklofenak dalam Kapsul Alginat 80 – 120 cP ... 58
4.7.1 Pengaruh Penyimpanan ... 58 4.7.1.1 Laju Disolusi Natrium Diklofenak dalam
4.7.1.2 Laju Disolusi Natrium Diklofenak dalam Kapsul Alginat Sebelum Penyimpanan dan Sesudah Penyimpanan 3 Bulan pada Suhu
40°C; RH 75% ... 61
4.7.2 Pengaruh Penambahan TiO2 Natrium Diklofenak dalam Cangkang Kapsul terhadap Pelepasan Alginat ... 64
BAB V KESIMPULAN DAN SARAN ... 67
5.1 Kesimpulan ... 67
5.2 Saran ... 69
DAFTAR PUSTAKA ... 70
DAFTAR TABEL
Tabel Halaman
4.1 Spesifikasi cangkang kapsul alginat 80 – 120 cP yang mengandung
TiO2
4.2 Spesifikasi cangkang kapsul alginat 80 – 120 cP yang tidak
... 46
mengandung TiO2 4.3 Spesifikasi cangkang kapsul menurut Pfizer Inc. Capsugel ... 46
Division ... 46
4.4 Ketebalan cangkang kapsul alginat 80 – 120 cP... 47
4.5 Sifat fisik cangkang kapsul alginat 80 – 120 cP ... 47
4.6 Persen pengembangan kapsul rata – rata dan waktu hancur rata – rata kapsul alginat 80 – 120 cP yang mengandung TiO2 4.7 Persen pengembangan kapsul rata – rata dan waktu hancur rata – ... 53
rata kapsul alginat 80 – 120 cP ... 54
4.8 Kadar Natrium diklofenak dalam cangkang kapsul alginat ... 55
DAFTAR GAMBAR
Gambar Halaman
1.1 Kerangka pikir penelitian ... 19
4.1 Cangkang kapsul alginat 80 – 120 cP sebelum dan sesudah
penyimpanan ... 47
4.2 Serbuk natrium diklofenak sebelum dan sesudah penyimpanan . 48
4.3 Uji waktu hancur kapsul mula – mula yang mengandung TiO2
4.4 Uji waktu hancur kapsul yang mengandung TiO
.. 49
2
penyimpanan selama 3 bulan suhu 30°C; RH 70% ... 51 setelah
4.5 Uji waktu hancur kapsul yang mengandung TiO2
penyimpanan selama 3 bulan suhu 40°C; RH 70% ... 52 setelah
4.6 Uji waktu hancur kapsul alginat yang tidak mengandung TiO2
4.7 Uji kerapuhan cangkang kapsul kosong mula - mula ... 56 .. 54
4.8 Uji kerapuhan cangkang kapsul kosong penyimpanan pada suhu
30°C; RH 70% ... 56
4.9 Uji kerapuhan cangkang kapsul kosong penyimpanan pada suhu
40°C; RH 75% ... 57
4.10 Uji kerapuhan cangkang kapsul mula – mula berisi ... 57
4.11 Uji kerapuhan cangkang kapsul berisi penyimpanan pada suhu
30°C; RH 70% ... 58
4.12 Uji kerapuhan cangkang kapsul berisi penyimpanan pada suhu
40°C; RH 75% ... 58
4.13 Pelepasan Natrium diklofenak dalam kapsul alginat sebelum penyimpanan dan setelah penyimpanan selama 3 bulan pada
suhu 30°C; RH 70% ... 59
4.14 Pelepasan Natrium diklofenak dalam kapsul alginat sebelum penyimpanan dan setelah penyimpanan selama 3 bulan pada
suhu 40°C; RH 75% ... 61
4.15 Pengaruh penambahan TiO2
DAFTAR LAMPIRAN
Lampiran Halaman
1 Pengukuran Viskositas Larutan Alginat ... 72
2 Penentuan spesifikasi cangkang kapsul alginat 80 – 120 cP ... 74
3 Data uji waktu hancur kapsul alginat 80 – 120 cP ... 79
4 Uji Independent T-Test waktu hancur Natrium diklofenak dalam
cangkang kapsul alginat 80 – 120 cP dengan dan tanpa TiO2
5 Uji Independent T-Test waktu hancur Natrium diklofenak dalam
... 82
cangkang kapsul alginat 80 – 120 cP sebelum dan setelah
penyimpanan pada suhu 30°C; RH 70% ... 84
6 Uji Independent T-Test waktu hancur Natrium diklofenak dalam
cangkang kapsul alginat 80 – 120 cP sebelum dan setelah
penyimpanan pada suhu 40°C; RH 75% ... 86
7 Hasil pengukuran kurva serapan Natrium diklofenak ... 88
8 Kurva Kalibrasi larutan Natrium diklofenak dalam medium pH
1,2 dan medium pH 6,8 ... 90
9 Contoh perhitungan penetapan kadar Natrium diklofenak dalam
cangkang kapsul alginat... 92
10 Data Hasil Penentuan Kadar Natrium Diklofenak dalam Kapsul
Alginat ... 94
11 % kumulatif disolusi Natrium diklofenak dalam cangkang
kapsul alginat 80 – 120 cP ... 96
12 Uji Independent T-Test Profil disolusi Natrium diklofenak dalam
cangkang kapsul alginat 80 – 120 cP dengan dan tanpa TiO2
13 Uji Independent T-Test Profil disolusi Natrium diklofenak dalam
... 112
cangkang kapsul alginat 80 – 120 cP sebelum dan sesudah
penyimpanan pada suhu 30°C; RH 70% ... 127
14 Uji Independent T-Test Profil disolusi Natrium diklofenak dalam
cangkang kapsul alginat 80 – 120 cP sebelum dan sesudah
penyimpanan pada suhu 40°C; RH 75% ... 144
Pengujian Stabilitas Natrium Diklofenak dalam Cangkang Kapsul Alginat
ABSTRAK
Natrium diklofenak, suatu Obat Anti Inflamasi Non Steroid (OAINS), memiliki efek samping dapat mengiritasi lambung dan penggunaan cangkang kapsul alginat dalam pembuatan suatu sediaan kapsul natrium diklofenak dapat mengurangi efek samping dari natrium diklofenak.
Tujuan penelitian ini adalah untuk mengetahui pengaruh penyimpanan dan penambahan bahan pemburam, titanium dioksida, pada cangkang kapsul terhadap stabilitas natrium diklofenak dari cangkang kapsul alginat.
Cangkang kapsul alginat dibuat dari natrium alginat 80-120cP dengan penambahan bahan pemburam titanium dioksida. Pengujiaan stabilitas fisik cangkang kapsul alginat meliputi pengamatan warna, uji waktu hancur, dan uji kerapuhan, sedangkan pengujian stabilitas fisik dan kimia cangkang kapsul alginat yang diisi natrium diklofenak meliputi pengamatan warna bahan obat, uji kerapuhan cangkang kapsul, penetapan kadar dan laju disolusi. Pengamatan warna dilakukan secara visual, uji waktu hancur menggunakan disintegration tester, kerapuhan kapsul diuji dengan capsule shell impact tester, kadar diukur secara spektrofotometri dan disolusi dilakukan dengan alat disolusi metode dayung dalam medium pH berganti. Penyimpanan dilakukan pada suhu 30°C dengan RH 70% dan suhu 40°C dengan RH 75% selama 3 bulan.
Hasil penelitian menunjukkan bahwa tidak terlihat adanya perubahan warna obat dan cangkang kapsul tidak menunjukan adanya kerapuhan setelah penyimpanan cangkang kapsul alginat yang berisi natrium diklofenak pada suhu 30°C dengan RH 70% selama 3 bulan demikian juga pada suhu 40°C dengan RH 75%. Kadar natrium diklofenak setelah penyimpanan selama 3 bulan pada suhu 30°C dengan RH 70% masih memenuhi persyaratan demikian pula pada penyimpanan suhu 40°C dengan RH 75% selama 3 bulan. Penyimpanan pada suhu 30°C dengan RH 70% dan suhu 40°C dengan RH 75% selama 3 bulan tidak berpengaruh terhadap laju disolusi. Penambahan pemburam titanium dioksida juga memperlambat laju disolusi dari natrium diklofenak dalam cangkang kapsul alginat.
Study of the Stability of Diclofenac Sodium in Alginate Capsule Shell
ABSTRACT
Diclofenac sodium, a Non-Steroidal Anti Inflammatory Drugs (NSAID), had adverse effect that could irritate stomach and the use of alginate capsule shell in a dosage form of diclofenac sodium capsule could reduce this adverse effect of diclofenac sodium.
The aim of this study is to know the effect of the storage and addition of opaque agent, titanium dioxide, to the stability of diclofenac sodium in alginate capsule shell.
Alginate capsule shell was made from sodium alginate 80 – 120 cP with the addition of opaque agent, titanium dioxide. The stability test of alginate capsule shell included observation of color, disintegration time, and brittleness, while the physical and chemical stability test of diclofenac sodium in capsule shell including observation of drug’s color, capsule shell’s brittleness, assay and dissolution. Color observation was made visually, disintegration time test was disintegration tester, brittleness test was using capsule shell impact tester, assay done by spectrophotometry and dissolution test was done by paddle method dissolution tester in changing pH. The storage was at temperature of 30°C with RH 70% and 40°C with RH 75% for 3 months.
The results showed that there was no visible color change in the drug and no presence of the capsule shell brittleness after storage of alginate capsule shell containing diclofenac sodium at a temperature of 30°C with RH 70%for 3 months as well at 40°C with 75% RH. Diclofenac sodium content after storage for 3 months at 30°C with 70% RH still qualified as well as after the storage at temperature of 40°C with 75% RH for 3 months. The storage at 30°C with 70% RH and 40°C with 75% RH for 3 months had no effect on dissolution rate. The addition of opaque agent, titanium dioxide, also slowed dissolution rate of diclofenac sodium in the alginate capsule shell.
BAB I PENDAHULUAN
1.1 Latar Belakang
Natrium diklofenak merupakan Obat Antiinflamasi Non-steroid (OAINS)
yang banyak digunakan sebagai obat anti radang. Obat ini dapat menyebabkan
masalah gastrointestinal pada sekitar 20% pasien (Goodman, 2011) yang berupa
nyeri epigastrik, mual, muntah dan diare. Pada beberapa orang juga terjadi
pengiritasian dinding lambung yang menyebabkan ulser peptik dan perdarahan
pada saluran cerna (Sweetman, 2009).
Tablet dan kapsul adalah cara yang paling terkenal dalam pemberian
suatu obat untuk penggunaan secara oral. Tablet dan kapsul nyaman untuk pasien
dan biasanya gampang ditangani dan diidentifikasi (Winfield, 2009). Standar
kapsul keras farmasi secara umum diproduksi dari gelatin namun, kesesuaian
bahan lain, misalnya hidroksi metil selulosa dan pati, telah diselidiki sebagai
pengganti yang cocok (Jones, 2007). Kapsul gelatin umumnya dirancang untuk
larut dalam asam lambung, melepaskan obat, yang akan diserap melalui dinding
lambung. Tetapi, ada beberapa zat aktif farmasi yang tidak cocok untuk pelepasan
di lambung misalnya obat tertentu yang dapat mengiritasi mukosa lambung, tidak
stabil atau reaktif pada pH asam lambung, dapat mempengaruhi metabolisme di
lambung, atau target obat dapat berlanjut sepanjang saluran pencernaan (WIPO,
2008).
Beberapa formulasi telah dikembangkan untuk membuat sediaan untuk
sediaan delayed release dengan salut enterik. Produk salut enterik dirancang untuk
tetap utuh dalam lambung kemudian melepaskan zat aktif pada bagian atas usus
halus (Meghal, et al., 2011). Sediaan obat berupa tablet natrium diklofenak telah
dibuat dengan salut enterik menggunakan Eudragit L 30 D-55 dan menghasilkan
tablet tidak larut dalam medium asam tetapi larut dalam medium basa dan
memenuhi persyaratan delayed release (Padmadisastra, dkk, 2007). Penyalutan
tablet dengan bahan penyalut enterik yang cocok yang dibutuhkan untuk
menghancurkan dan melepaskan obat pada usus halus tergantung pada
kekompakan dan jumlah dari zat tambahan.
Pada pembuatan kapsul gelatin yang disalut enterik, penyalutan kapsul
gelatin keras dapat menyebabkan kerapuhan pada cangkang oleh karena gaya
adhesi yang kurang dari penyalut pada cangkang kapsul gelatin. Kapsul yang
terbuat dari HPMC dapat menjadi alternatif untuk mengurangi bahan tambahan
pada pembuatan tablet dan tahap pengolahan yang banyak. Permukaan kapsul
HPMC yang kasar dapat memudahkan gaya adhesi untuk penyalutan polimer
enterik. Karena penyalutan kapsul HPMC tidak tergantung pada isi kapsul,
sehingga lebih menguntungkan untuk menyalut suatu kapsul daripada tablet. Selain itu, jumlah alat dan eksipien berikut juga langkah yang dibutuhkan pada saat memproduksi tablet dapat dikurangi pada bentuk sediaan kapsul (Meghal, et al., 2011).
Alginat merupakan polisakarida alami dari asam guluronat (G) dan
manuronat (M), yang cukup berlimpah di alam dari alga coklat (Phaeophyceae).
Alginat berasal dari alam sehingga aman untuk dikonsumsi. Cangkang kapsul
dalam medium usus buatan (pH 6,8) (Bangun, dkk., 2005) sehingga tidak
diperlukan penyalutan dalam pembuatan sediaan delayed release dari cangkang
kapsul alginat .
Ada dua tipe pemberi warna pada kapsul: pewarna yang larut air atau
pigmen yang tidak larut. Ada dua jenis pigmen yang dapat digunakan yaitu besi
oksida yang berwarna hitam, merah dan kuning dan juga titanium oksida, yang
berwarna putih untuk membuat kapsul menjadi buram. Dalam 20 tahun terakhir
penggunaan pewarna larut telah digantikan menjadi pigmen, karena pigmen tidak
diserap pada saluran pencernaan (Jones, 2007). Penggunaan pigmen pada
cangkang kapsul alginat diharapkan untuk memperbaiki sifat fisik dari cangkang
kapsul alginat dimana pada pengujian stabilitas pada suhu 40°C dengan RH 75
setelah 3 bulan didapatkan perubahan warna cangkang kapsul tanpa pigmen yang
transparan menjadi coklat (Ekasari, 2011).
Stabilitas merupakan suatu faktor yang penting dari mutu, keamanan dan
khasiat dari suatu produk obat. Suatu produk obat, yang tidak cukup stabil, dapat
menghasilkan perubahan fisik (seperti kekerasan, laju disolusi, pemisahan fasa,
dsb) demikian juga pada sifat kimia (membentukan zat dekomposisi yang
membahayakan kesehatan). Kajian stabilitas terdiri dari serangkaian uji untuk
mendapatkan jaminan stabilitas dari suatu produk obat, yaitu pertahanan dari
spesifikasi produk obat yang dikemas dalam bahan pengemas tertentu dan
disimpan dalam kondisi penyimpanan yang ditetapkan dalam jangka waktu yang
ditentukan (Anonima
Berdasarkan uraian diatas, maka peneliti tertarik untuk membuat
berupa TiO2 dan diisi dengan obat natrium diklofenak. Kemudian melihat
pengaruh penyimpanan terhadap stabilitas sediaan obat yang meliputi pengujian
sifat- sifat fisik cangkang kapsul yaitu perubahan warna, waktu hancur, kerapuhan
kapsul dan uji disolusi juga penetapan kadar natrium diklofenak.
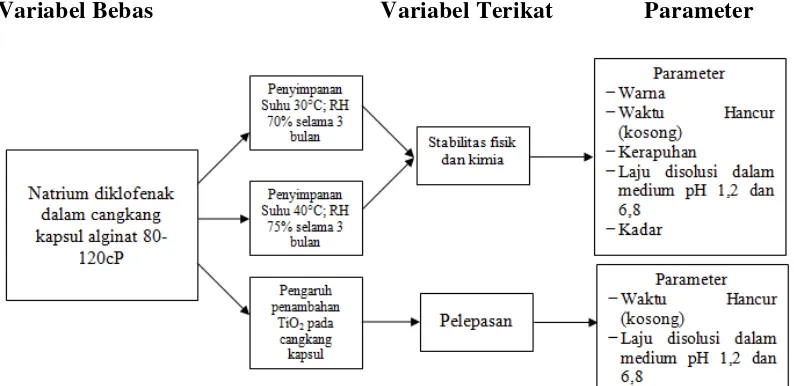
1.2 Kerangka Pikir Penelitian
Secara skematis kerangka pikir penelitian ditunjukkan pada Gambar 1.1
Variabel Bebas Variabel Terikat Parameter
Gambar 1.1 Kerangka pikir penelitian.
1.3 Perumusan Masalah
Berdasarkan uraian diatas, maka permasalahan dalam penelitian ini dapat
dirumuskan sebagai berikut :
a. Apakah penyimpanan pada suhu 30°C; RH 70% dan suhu 40°C; RH 75%
setelah 3 bulan mempengaruhi sifat – sifat fisik cangkang kapsul 80 – 120 cP
b. Apakah penyimpanan pada suhu 30°C; RH 70% dan suhu 40°C; RH 75%
setelah 3 bulan mempengaruhi sifat – sifat fisik dan kimia natrium diklofenak
dalam cangkang kapsul alginat 80 – 120 cP yang meliputi perubahan warna,
kerapuhan, laju disolusi dan kadar natrium diklofenak?
c. Apakah penambahan bahan pemburam titanium dioksida dapat
mempengaruhi laju disolusi natrium diklofenak?
1.4 Hipotesis Penelitian
Berdasarkan perumusan masalah diatas maka hipotesis penelitian ini
adalah sebagai berikut :
a. Penyimpanan pada suhu 30°C; RH 70% dan suhu 40°C; RH 75% setelah 3
bulan mempengaruhi sifat – sifat fisik cangkang kapsul 80 – 120 cP (kosong)
yang meliputi perubahan warna, kerapuhan dan waktu hancur.
b. Penyimpanan pada suhu 30°C; RH 70% dan suhu 40°C; RH 75% setelah 3
bulan mempengaruhi sifat – sifat fisik dan kimia natrium diklofenak dalam
cangkang kapsul alginat 80 – 120 cP yang meliputi perubahan warna,
kerapuhan, laju disolusi dan kadar natrium diklofenak.
c. Penambahan bahan pemburam titanium dioksida dapat mempengaruhi laju
disolusi natrium diklofenak.
1.5 Tujuan Penelitian
Tujuan penelitian ini adalah :
a. Mengetahui pengaruh penyimpanan pada suhu 30°C; RH 70% dan suhu
80 – 120 cP (kosong) yang meliputi perubahan warna, kerapuhan dan
waktu hancur.
b. Mengetahui pengaruh penyimpanan pada suhu 30°C; RH 70% dan suhu
40°C; RH 75% setelah 3 bulan terhadap sifat – sifat fisik dan kimia
natrium diklofenak dalam cangkang kapsul alginat 80 – 120 cP yang
meliputi perubahan warna, kerapuhan, laju disolusi dan kadar natrium
diklofenak.
c. Mengetahui pengaruh penambahan bahan pemburam titanium dioksida
terhadap laju disolusi natrium diklofenak.
1.6 Manfaat Penelitian
Penelitian ini bermanfaat untuk mengetahui stabilitas natrium diklofenak dalam
cangkang kapsul alginat setelah penyimpanan selama 3 bulan pada suhu 30°C;
RH 70% dan suhu 40°C; RH 75% serta pengaruh bahan pemburam terhadap
BAB II
TINJAUAN PUSTAKA
2.1 Natrium Diklofenak 2.1.1 Uraian Bahan
Rumus Bangun :
Rumus Molekul : C14H10Cl2NNaO
Nama Kimia : asam benzenasetat, 2-[(2,6-diklorofenil)amin]-,
garam monosodium
2
Nama lain : Natrium [o-(2,6-dikloroanilino)fenil]asetat
Berat Molekul : 318,13
(USP XXXII, 2009).
Pemerian : serbuk kristal putih atau sedikit kuning, agak
higroskopis
Kelarutan : Sedikit larut dalam air, mudah larut dalam
methanol, larut dalam etanol (96 persen), sedikit
pKa : 4,2 (Moffats, 2005).
2.1.2 Farmakologi Natrium Diklofenak
Diklofenak mempunyai aktivitas analgesik, antipiretik, dan anti radang.
Natrium diklofenak berpotensi terhadap COX-2 lebih besar daripada indometasin,
naproksen ataupun OAINS lainnya. Sebagai tambahan, diklofenak tampaknya
dapat mengurangi konsentrasi intrasel dari AA bebas dalam leukosit, mungkin
dengan mengubah pelepasan ataupun penyerapannya. Selektifitas dari diklofenak
terhadap COX-2 menyerupai celecoxib. Namun, efek merugikan terhadap
gastrointestinal serius tidak berbeda antara celecoxib dan diklofenak (Gillman,
2010).
2.2 Kapsul
Kapsul adalah sediaan padat dimana obat ditutup dalam suatu cangkang
yang keras maupun lunak. Cangkang tersebut biasanya dibuat dari gelatin; tetapi;
cangkang tersebut juga dapat dibuat dari pati ataupun zat lain yang cocok. Kapsul
cangkang keras berukuran dari No. 5, yang paling kecil, hingga No. 000, yang
paling besar, kecuali untuk ukuran penggunaan veteriner. Bagaimanapun, ukuran
No. 00 merupakan ukuran terbesar yang secara umum dapat diterima oleh pasien
(USP, 2009).
Kapsul tidak berasa, mudah pemberiannya, mudah pengisiannya tanpa
persiapan atau dalam jumlah yang besar secara komersil. Didalam praktek
peresepan, penggunaan kapsul gelatin keras diperbolehkan sebagai pilihan dalam
dianggap baik untuk pasien secara individual. Fleksibilitasnya lebih
menguntungkan daripada tablet. Beberapa pasien menyatakan lebih mudah
menelan kapsul daripada tablet, oleh karena itu lebih disukai bentuk kapsul bila
memungkinkan. Pilihan ini telah mendorong pabrik farmasi untuk memproduksi
sediaan kapsul dan di pasarkan, walaupun produknya sudah ada dalam bentuk
sediaan tablet (Gennaro, 2000).
2.3 Pemberi Warna Kapsul
Pemberian warna dan tanda dapat secara mudah ditambahkan pada
kapsul untuk melindungi kapsul dari cahaya dan kemudahan identifikasi
(Winfield, et. al, 2009). Ada dua tipe pemberi warna yang dapat digunakan:
pewarna larut air atau pigmen yang tidak larut. Untuk membuat pilhan warna,
pewarna dan pigmen dicampur bersama sebagai larutan atau suspensi. Pewarna
yang digunak umumnya dibuat secara sintetik dan dapat dikelompokan menjadi
pewarna azo (yang mempunyai suatu gugus –N=N– ) dan pewarna non-azo, yang
berasal dari bermacam – macam bahan kimia. Kebanyakan pewarna yang
digunakan adalah eritrosin, indigo karmin dan kuning kuinolin. Ada dua jenis
pigmen yang dapat digunakan: besi oksida dengan warna hitam, merah dan
kuning, dan titanium dioksida, yang berwarna putih dan digunakan untuk
memburamkan kapsul. Pewarna yang dapat digunakan untuk mewarnai obat –
obatan diatur oleh undang – undang, yang berbeda – beda tiap negara walaupun
didasari oleh pengujian toksikologi (Jones, 1993). Dalam 20 tahun terakhir ini
umumnya besi oksida, karena tidak diabsorbsi oleh saluran pencernaan. (Jones,
B.E, 2007).
2.4 Titanium Dioksida
Titanium dioksida secara luas digunakan dalam manisan, kosmetik dan
makanan, dalam industry plastik, dan pada formulasi farmasetik topikal dan oral
sebagai suatu pigmen pemutih. Titanium dioksida mempunyai indeks bias yang
tinggi sehingga dapat digunakan sebagai pigmen pemutik dan pengopak. Dalam
formulasi farmasetik, titanium dioksida digunakan sebagai pigmen pemutih dalam
supensi salut film, tablet salut gula dan kapsul gelatin. Titanium dioksida juga
dapat dicampur dengan pigmen lainnya. Titanium dioksida juga digunakan dalam
sediaan kulit dan kosmetik, contohnya sunscreen (Rowe, et al., 2009).
Titanium dioksida sangat stabil pada suhu yang tinggi. Hal ini
disebabkan karena kuatnya ikatan antara ion tetravalen titanium dan ion bivalen
oksigen. Bagaimanapun, titanium dioksida dapat kehilangan oksigen dalam
jumlah sedikit bila berinteraksi dengan energy radian. Oksigen ini dapat menyatu
kembali sebagai suatu bagian dari reaksi fotokimia yang reversible. Kehilangan
oksigen tersebut penting karena dapat menyebabkan perubahan yang jelas pada
sifat optik dan elektrik dari pigmen (Rowe, et al., 2009).
2.5 Natrium Alginat
Alginat merupakan polisakarida alami dari asam guluronat (G) dan
manuronat (M), yang cukup berlimpah di alam sebagai komponen berstruktur
dalam alga coklat (Phaeophyceae) dari spesies Macrocystis pyrifera, Laminaria,
bakteri tanah. Kandungan alga coklat pada umumnya mengandung mineral
ataupun komponen anorganik dan organik, dimana komponen organik umumnya
terdiri atas alginat, fucan dan karbohidrat lainnya. Proses isolasi alginat dari alga
coklat cukup mudah, termasuk tahap praekstraksi dengan asam hidroklorida,
diikuti oleh penyucian, penyaringan dan netralisasi dengan basa. Natrium alginat
diendapkan dari larutan dengan alkohol (isopropanol atau etanol) dan biasanya
diendapkan kembali (untuk mendapatkan kemurnian lebih tinggi) dengan cara
yang sama. Bagaimanapun, skema proses pembuatan alginat ini cukup kompleks,
yang terhitung sebanyak 15 langkah (Laurienzo, 2010).
Gambar 2. Struktur alginat
Asam alginat adalah kopolimer biner yang terdiri dari residu β
-D-mannuronat (M) dan α-L-asam guluronat (G) yang tersusun dalam blok-blok yang
membentuk rantai linear (Grasdalen, dkk., 1979). Kedua unit tersebut berikatan
pada atom C1 dan C4 dengan susunan homopolimer dari masing-masing residu
(MM dan GG) dan suatu blok heteropolimer dari dua residu (MG) (Thom, dkk.,
1980).
Asam alginat tidak larut dalam air, karena itu yang digunakan dalam
penambahan larutan garam-garam kalsium seperti kalsium glukonat, kalsium
tartrat dan kalsium sitrat. Pembentukan gel ini disebabkan oleh terjadinya kelat
antara rantai L-guluronat dengan ion kalsium (Thom, dkk., 1980).
2.6 Viskositas
Viskositas adalah suatu sifat dari cairan yang lebih bertahan untuk
mengalir. Viskositas dapat dianggap sebagai suatu sifat yang relatif dengan air
sebagai bahan rujukan dan semua viskositas dinyatakan dalam istilah-istilah
viskositas air murni pada suhu 20°C. Viskositas air dianggap satu centipoise
(sebenarnya 1,008 centipoise). Suatu bahan cair yang 10 kali kental (viscous)
dengan suhu yang sama viskositasnya sama dengan 10 centipoise. Singkatan
centipoise cp (dan jamaknya cps) merupakan istilah yang lebih sesuai dari pada
unit dasar satu poise sama dengan 100 centipoise (Ansel, 2005). Makin kental
suatu cairan, makin besar kekuatan yang diperlukan agar cairan tersebut mengalir
dengan laju tertentu (Martin, 1993).
2.7 Stabilitas
Tujuan pengujian stabilitas adalah untuk menyediakan suatu bukti
bagaimana kualitas dari suatu bahan aktif farmasi berbeda terhadap waktu pada
pengaruh perbedaan dari faktor lingkungan seperti suhu, kelembaban dan cahaya.
Program stabilitas juga termasuk penelitian tentang factor yang berhubungan
dengan produk yang mempengaruhi kualitasnya, sebagai contoh, interaksi dari
bahan aktif farmasi dengan eksipien, sisten penutupan wadah dan bahan
pengemas. Dalam dosis kombinasi interaksi antara dua atau lebih bahan aktif
produk harus didasari oleh pengetahuan dari sifat dari zat obat dan bentuk sediaan
(Anonima, 2005).
2.8 Waktu Hancur
Chiwele dkk. (2000) telah meneliti mengenai waktu hancur cangkang
kapsul gelatin kosong dan kapsul HPMC (Hydroxypropyl Methylcellulose) setelah
penyimpanan selama 24 jam pada kondisi tropis lembab (suhu 370
Hasil ini tidak jauh berbeda dengan yang dilaporkan Ogura (1998) bahwa
cangkang kapsul HPMC yang telah diisi dengan spiramisin dan disimpan pada
suhu 60
C, RH 75%)
dan pada temperatur kamar. Dalam metode ini, mereka menggunakan bola besi
sebagai bahan pengisi dalam kapsul. Pada penyimpanan kondisi tropis lembab,
cangkang kapsul gelatin tidak mengalami perubahan waktu hancur dalam medium
apapun, sedangkan waktu hancur kapsul HPMC tidak berubah hanya dalam
medium cairan lambung buatan (Honkanen, 2004).
0C, RH 75% selama 10 hari tidak mengalami perubahan sifat waktu
hancur. Tetapi, mereka menggunakan prosedur standar uji waktu hancur dalam
farmakope, yang tidak dapat menentukan waktu hancur cangkang kapsul dan
bahan obat secara terpisah. Sedangkan dalam metode yang digunakan Chiwele
dkk. (2000), bola besi yang digunakan tidak mempengaruhi waktu hancur
(Honkanen, 2004).
2.9 Kerapuhan
Perlu diketahui bahwa cangkang kapsul bukan tidak reaktif, secara fisika
dapat mempengaruhi sifat kapsul. Dengan terjadinya kenaikan temperatur dan
kelembaban dapat menyebabkan kapsul mengikat/melepaskan uap air. Sebagai
akibatnya kapsul dapat menjadi rapuh atau lunak (Margareth, dkk., 2009).
Laju pengeringan kapsul juga mempengaruhi kekerasan dan kerapuhan
kapsul, kemampuan pelarutan, dan kecenderungan untuk melekat satu sama lain..
Kadar uap air yang rendah pada kapsul dapat menghambat pertumbuhan mikroba.
Jika kadar uap air pada kapsul gelatin kurang dari 10%, kapsul cenderung menjadi
rapuh, dan sebaliknya jika kadar air lebih tinggi dari 18% kapsul gelatin melunak.
Kondisi penyimpanan yang direkomendasikan untuk bentuk sediaan kapsul
gelatin berkisar 15-30°C dan 30%-60% kelembaban relatif (RH). (Margareth,
dkk., 2009).
2.10 Disolusi
Uji disolusi yaitu uji pelarutan invitro mengukur laju dan jumlah
pelarutan obat dalam suatu media “aqueous” dengan adanya satu atau lebih bahan
tambahan yang terkandung dalam produk obat. Pelarutan obat merupakan bagian
penting sebelum kondisi absorbsi sistemik (Shargel dan Andrew, 1988).
Faktor-faktor yang mempengaruhi disolusi dibagi atas 3 kategori yaitu:
a. Faktor-faktor yang berhubungan dengan sifat fisikokimia obat, meliputi:
i. Efek kelarutan obat. Kelarutan obat dalam air merupakan faktor utama
dalam menentukan laju disolusi. Kelarutan yang besar menghasilkan laju
ii. Efek ukuran partikel. Ukuran partikel berkurang dapat memperbesar luas
permukaan obat yang berhubungan dengan medium, sehingga laju
disolusi meningkat.
b. Faktor-faktor yang berhubungan dengan sediaan obat, meliputi:
i. Efek formulasi. Laju disolusi suatu bahan obat dapat dipengaruhi bila
dicampur dengan bahan tambahan. Bahan pengisi, pengikat dan
penghancur yang bersifat hidrofil dapat memberikan sifat hidrofil pada
bahan obat yang hidrofob, oleh karena itu disolusi bertambah, sedangkan
bahan tambahan yang hidrofob dapat mengurangi laju disolusi.
ii. Efek faktor pembuatan sediaan. Metode granulasi dapat mempercepat laju
disolusi obat-obat yang kurang larut. Penggunaan bahan pengisi yang
bersifat hidrofil seperti laktosa dapat menambah hidrofilisitas bahan aktif
dan menambah laju disolusi.
c. Faktor-faktor yang berhubungan dengan uji disolusi, meliputi :
i. Tegangan permukaan medium disolusi. Tegangan permukaan mempunyai
pengaruh nyata terhadap laju disolusi bahan obat. Surfaktan dapat
menurunkan sudut kontak, oleh karena itu dapat meningkatkan proses
penetrasi medium disolusi ke matriks. Formulasi tablet dan kapsul
konvensional juga menunjukkan penambahan laju disolusi obat-obat yang
sukar larut dengan penambahan surfaktan kedalam medium disolusi.
ii. Viskositas medium. Semakin tinggi viskositas medium, semakin kecil laju
disolusi bahan obat.
iii. pH medium disolusi. Larutan asam cenderung memecah tablet sedikit
disolusi (Gennaro, 2000). Obat-obat asam lemah disolusinya kecil dalam
medium asam, karena bersifat nonionik, tetapi disolusinya besar pada
medium basa karena terionisasi dan pembentukan garam yang larut
(Martin, dkk., 1993).
United States Pharmacopeia (USP) XXI memberi beberapa metode resmi
untuk melaksanakan uji pelarutan yaitu:
a. Metode Keranjang (Basket)
Metode keranjang terdiri atas keranjang silindrik yang ditahan oleh
tangkai motor. Keranjang menahan cuplikan dan berputar dalam suatu labu bulat
yang berisi media pelarutan. Keseluruhan labu tercelup dalam suatu bak yang
bersuhu konstan 37o
b. Metode Dayung (Paddle)
C. Kecepatan berputar dan posisi keranjang harus memenuhi
rangkaian syarat khusus dalam USP yang terakhir beredar. Tersedia standar
kalibrasi pelarutan untuk meyakinkan bahwa syarat secara mekanik dan syarat
operasi telah dipenuhi.
Metode dayung terdiri atas suatu dayung yang dilapisi khusus, yang
berfungsi memperkecil turbulensi yang disebabkan oleh pengadukan. Dayung
diikat secara vertikal ke suatu motor yang berputar dengan suatu kecepatan yang
terkendali. Tablet atau kapsul diletakkan dalam labu pelarutan yang beralas bulat
yang juga berfungsi untuk memperkecil turbulensi dari media pelarutan. Alat
ditempatkan dalam suatu bak air yang bersuhu konstan, seperti pada metode
basket dipertahankan pada 37oC. Posisi dan kesejajaran dayung ditetapkan dalam
USP. Metode dayung sangat peka terhadap kemiringan dayung. Pada beberapa
mempengaruhi hasil pelarutan. Standar kalibrasi pelarutan yang sama digunakan
untuk memeriksa peralatan sebelum uji dilaksanakan.
c. Metode Disintegrasi yang Dimodifikasi
Metode ini dasarnya memakai disintegrasi USP ”basket and rack” dirakit
untuk uji pelarutan. Bila alat ini dipakai untuk pelarutan maka cakram
dihilangkan. Saringan keranjang juga diubah sehingga selama pelarutan partikel
tidak akan jatuh melalui saringan. Metode ini jarang digunakan dan dimasukkan
dalam USP untuk suatu formulasi obat lama. Jumlah pengadukan dan getaran
membuat metode ini kurang sesuai untuk uji pelarutan yang tepat (Shargel dan
BAB III
METODE PENELITIAN 3.1 Alat – alat
Alat disolusi metoda dayung (Yamato), spektrofotometer (UV-1800
Shimadzu Spectrophotometer), neraca analitik (Boeco), pH meter (Hanna),
viskometer Thomas-Stomer (Haake), termometer, climatic chamber (Memmeth),
alat uji waktu hancur (Copley), anak timbangan 50 g dan 2 kg, jangka sorong
(Tricle), mikrometer (Delta), alat pencetak kapsul yang terbuat dari batang
stainless steel berbentuk silindris dengan panjang 10 cm serta berdiameter 6,0 mm
untuk bagian badan cangkang kapsul dan 6,2 mm untuk bagian tutup cangkang
kapsul, bola besi berbahan stainless steel bediameter 1,44 mm dan berat 9 mg
(sebagai pengisi untuk uji waktu hancur), cincin disolusi, stopwatch, kamera
digital, labu tentukur 1000 ml (Pyrex), labu tentukur 25 ml (Pyrex), beaker glass
(Pyrex), pipet volume 5 ml (Pyrex), gelas ukur (Pyrex), pipet tetes, bola karet,
botol dan alat-alat laboratorium yang biasa digunakan.
3.2 Bahan – Bahan
Natrium alginat 80 – 120 cP adalah produk Wako Pure Chemical
industries, Ltd Japan, natrium diklofenak (PT. Indo Farma), Asam klorida pekat
(Merck), natrium fosfat dodekahidrat (Merck), natrium hidroksida (Merck),
kalsium klorida dihidrat (Merck), titanium dioksida, natrium metabisulfit (Merck),
3.3 Prosedur Penelitian 3.3.1 Pembuatan Pereaksi 3.3.1.1 Larutan CaCl2
Kalsium klorida dihidrat (CaCl
0,15 M
2·2H2O) sebanyak 22.05 g dilarutkan
dalam 1000 ml akuades bebas CO2
3.3.1.2 Larutan HCl 0,1 N
(Ditjen POM, 1995).
Asam klorida pekat sebanyak 8,35 ml diencerkan dengan akuades hingga
1000 ml (Ditjen POM, 1995).
3.3.1.3 Larutan Na3PO4
Dilarutkan 76 g natrium fosfat dodekahidrat (Na
0,2 M
3PO4.12H2
3.3.1.4 Dapar fosfat pH 6,8
O) dalam
akuades hingga diperoleh larutan sebanyak 1000 ml (USP, 2009).
Dicampur 250 ml larutan Na3PO4
3.3.1.5 Larutan NaOH 0,1 N
0,2 M dengan 750 ml HCl 0,1 N,
kemudian bila diperlukan, disesuaikan pH-nya dengan HCl 2 N atau NaOH 2 N
sampai pH 6,8±0,5 (USP, 2009).
Natrium hidroksida sebanyak 4 g dilarutkan dalam akuades bebas CO2
3.3.1.6 Larutan NaOH 5 N
hingga 1000 ml (Ditjen POM, 1995).
Natrium hidroksida (BM = 40) sebanyak 20 g dilarutkan dalam akuades
3.3.2 Pembuatan Cangkang Kapsul Alginat 3.3.2.1 Pembuatan Larutan Natrium Alginat
Formula I:
Natrium alginat 80 – 120 cP 4,5 g
Nipagin 0,25 g
Gliserin 2 g
Natrium metabisulfit 0,1 g
Titanium dioksida 0,4 g
Akuades ad 100 ml
Wadah dikalibrasi 100 ml. Sebanyak 0,25 g nipagin dilarutkan dalam 25
ml akuades sambil dipanaskan hingga larut (massa I). Sebanyak 2 g gliserin, 0,1 g
natrium metabisulfit dan 0,4 g titanium dioksida dilarutkan dalam 25 ml akuades
(massa II). Kemudian dicampur massa I dan massa II dan ditambahkan 25 ml
akuades (massa III). Kemudian natrium alginat ditaburkan dengan massa III
secara bergantian di mana dasar wadah dimasukkan massa III terlebih dahulu lalu
ditaburkan natrium alginat hingga menutupi permukaan massa III. Perlakuan ini
dilanjutkan bergantian hingga natrium alginat habis dan terakhir bagian atasnya
diakhiri dengan massa III juga. Larutan didiamkan selama 24 jam. Setelah 24 jam,
dicukupkan dengan akuades hingga batas garis kalibrasi dan diaduk perlahan
(agar tidak terbentuk gelembung udara) hingga terbentuk larutan yang dapat
Formula II:
Natrium alginat 80 – 120 cP 4,5 g
Nipagin 0,25 g
Gliserin 2 g
Natrium metabisulfit 0,1 g
Akuades ad 100 ml
Wadah dikalibrasi 100 ml. Sebanyak 0,25 g nipagin dilarutkan dalam 25
ml akuades sambil dipanaskan hingga larut (massa I). Sebanyak 2 g gliserin dan
0,1 g natrium metabisulfit dilarutkan dalam 25 ml akuades (massa II). Kemudian
dicampur massa I dan massa II dan ditambahkan 25 ml akuades (massa III).
Kemudian natrium alginat ditaburkan dengan massa III secara bergantian di mana
dasar wadah dimasukkan massa III terlebih dahulu lalu ditaburkan natrium alginat
hingga menutupi permukaan massa III. Perlakuan ini dilanjutkan bergantian
hingga natrium alginat habis dan terakhir bagian atasnya diakhiri dengan massa III
juga. Larutan didiamkan selama 24 jam. Setelah 24 jam, dicukupkan dengan
akuades hingga batas garis kalibrasi dan diaduk perlahan (agar tidak terbentuk
gelembung udara) hingga terbentuk larutan yang dapat dicetak.
3.3.2.2 Pengukuran Viskositas Larutan Natrium Alginat
Viskometer Thomas-Stromer diletakkan di tepi meja yang datar sehingga
alat penggerak dengan beban 100 g dapat jatuh tanpa gangguan. Kemudian dalam
beaker glass diisi akuades sebanyak 200 ml dan diletakkan diatas meja
pengukuran dan dinaikkan sampai rotor baling-baling terendam ditengah-tengah
akuades dan mencapai tanda pada tangkai rotor. Selanjutnya rem dilepaskan dan
menggunakan stopwatch. Dilakukan prosedur terhadap larutan natrium alginat dan
dibandingkan waktunya sehingga didapatkan viskositas larutan natrium alginat.
3.3.2.3 Pembuatan Badan Cangkang Kapsul Alginat
Alat pencetak kapsul dibuat dari bahan stainless steel dengan panjang 10
cm diameter 6,0 mm dicelupkan ke dalam larutan natrium alginat sedalam 3 cm,
kemudian batang stainless steel yang ujungnya telah dilapisi larutan natrium
alginat tersebut direndam dalam larutan kalsium klorida 0,15 M selama 75 menit
dan diaduk dengan bantuan pengaduk magnet. Setelah itu cangkang kapsul yang
telah mengeras direndam dalam akuades selama 24 jam untuk menghilangkan
kalsium yang menempel pada cangkang kapsul dan selanjutnya dikeringkan.
3.3.2.4 Pembuatan Tutup Cangkang Kapsul Alginat
Alat pencetak kapsul dibuat dari bahan stainless steel dengan panjang 10
cm diameter 6,2 mm dicelupkan ke dalam larutan natrium alginat sedalam 2,5 cm,
kemudian batang stainless steel yang ujungnya telah dilapisi larutan natrium
alginat tesebut direndam dalam larutan kalsium klorida 0,15 M selama 75 menit
dan diaduk dengan bantuan pengaduk magnet. Setelah itu cangkang kapsul yang
telah mengeras direndam dalam akuades selama 24 jam untuk menghilangkan
kalsium yang menempel pada cangkang kapsul dan selanjutnya dikeringkan.
3.3.2.5 Pengeringan Cangkang Kapsul Alginat
Pengeringan cangkang kapsul dilakukan dengan cara memasukkan
cangkang kapsul alginat basah dalam lemari pengering selama 1 hari dimana
cangkang kapsul alginat basah tetap berada pada alat pencetak kapsul yang
pencetak dan digabungkan badan dan tutup kapsul kemudian disimpan dalam
botol plastik.
3.3.3 Pembuatan Kurva Serapan dan Kurva Kalibrasi Natrium Diklofenak 3.3.3.1 Pembuatan Larutan Induk Baku Natrium Diklofenak
Natrium diklofenak ditimbang sebanyak 50 mg, dilarutkan dengan 10 ml
natrium hidroksida 0,1 N dalam labu takar 100 ml, dikocok sampai larut, lalu
ditambahkan akuades sampai garis tanda, dikocok sampai homogen. Konsentrasi
yang diperoleh 500 ppm (mcg/ml) (USP, 2009).
3.3.3.2 Pembuatan Kurva Serapan Larutan Natrium Diklofenak dalam Medium Cairan Lambung Buatan (pH 1,2)
Larutan induk baku natrium diklofenak (2.3.3.1) dipipet 0,7 ml,
dimasukkan ke dalam labu tentukur 25 ml, kemudian ditambahkan 0,5 ml NaOH
5 N dan dicukupkan dengan medium pH 1,2 sampai garis tanda, dikocok sampai
homogen. Konsentrasi natrium diklofenak adalah 14 mcg/ml. Serapan diukur
dengan spektrofotometer UV panjang gelombang 250-300 nm.
3.3.3.3 Pembuatan Kurva Kalibrasi Larutan Natrium Diklofenak dalam Medium Cairan Lambung Buatan (pH 1,2)
Larutan natrium diklofenak dibuat berbagai konsentrasi yaitu 1; 2; 4; 6;
8; 10; 12; 14; 16 mcg/ml dengan cara memipet larutan induk baku natrium
diklofenak (2.3.3.1) masing – masing 0,05; 1; 0,2; 0,3; 0,4; 0,5; 0,6; 0,7; 0,8 ml ke
dalam labu tentukur 25 ml, kemudian ditambahkan dengan 0,5 ml NaOH 5 N dan
dicukupkan dengan medium pH 1,2 sampai garis tanda, dikocok sampai homogen.
Serapan diukur dengan spektrofotometer UV pada panjang gelombang maksimum
3.3.3.4 Pembuatan Kurva Serapan Larutan Natrium Diklofenak dalam Medium Cairan Usus Buatan (pH 6,8)
Larutan induk baku natrium diklofenak (2.3.3.1) dipipet 0,7 ml,
dimasukkan ke dalam labu tentukur 25 ml, kemudian dicukupkan dengan medium
pH 6,8 sampai garis tanda, dikocok sampai homogen. Konsentrasi natrium
diklofenak adalah 14 mcg/ml. Serapan diukur dengan spektrofotometer UV pada
panjang gelombang 250-300 nm.
3.3.3.5 Pembuatan Kurva Kalibrasi Larutan Natrium Diklofenak dalam Medium Cairan Usus Buatan (pH 6,8)
Larutan induk baku natrium diklofenak (2.3.3.1) dibuat berbagai
konsentrasi yaitu 2; 4; 6; 8; 10; 15; 20; 25; 30 mcg/ml dengan cara memipet
Larutan Induk Baku masing – masing 0,1; 0,2; 0,3; 0,4; 0,5; 0,75; 1,0; 1,25; 1,5
ml ke dalam labu tentukur 25 ml, kemudian dicukupkan dengan medium pH 6,8
sampai garis tanda, dikocok sampai homogen. Serapan diukur dengan
spektrofotometer UV pada panjang gelombang maksimum yang telah ditentukan
sebelumnya.
3.3.4 Pengisian Natrium Diklofenak dalam Kapsul Alginat
Sebanyak 25 mg serbuk natrium diklofenak ditimbang dengan tepat
menggunakan neraca listrik, kemudian dicampur homogen dengan 35 mg laktosa,
lalu diisikan ke dalam bagian badan cangkang kapsul alginat melalui bagian ujung
yang terbuka lalu ditutup dengan bagian tutup cangkang kapsul dengan
mendorong ke bagian badan cangkang kapsul yang terbuka sehingga bagian tutup
kapsul dengan bagian badan kapsul menyatu dengan baik. Kemudian diberi
3.3.5 Penyimpanan
3.3.5.1 Penyimpanan pada Suhu 30°C; RH 70 %
Cangkang kapsul dan kapsul berisi natrium diklofenak disimpan dalam
botol plastik di dalam climatic chamber pada suhu 30±2°C; RH 70±5%. Setelah 3 bulan, cangkang kapsul dikeluarkan dan dilakukan pengujian terhadap cangkang
kapsul, meliputi pengamatan warna cangkang kapsul, uji waktu hancur, dan uji
kerapuhan. Pengujian terhadap kapsul yang berisi natrium diklofenak meliputi
pengamatan warna, uji kerapuhan dan uji disolusi.
3.3.5.2 Penyimpanan pada Suhu 40°C; RH 75%
Cangkang kapsul dan kapsul berisi natrium diklofenak disimpan dalam
botol plastik di dalam climatic chamber pada suhu 40°±2C; RH 75±5%. Setelah 3
bulan, cangkang kapsul dikeluarkan dan dilakukan pengujian terhadap cangkang
kapsul, meliputi pengamatan warna cangkang kapsul, uji waktu hancur, dan uji
kerapuhan. Pengujian terhadap kapsul yang berisi natrium diklofenak meliputi
pengamatan warna, uji kerapuhan dan uji disolusi.
3.3.6 Pengujian
3.3.6.1 Penentuan Spesifikasi Cangkang Kapsul
3.3.6.1.1 Pengukuran Panjang dan Diameter Cangkang Kapsul
Panjang dan diameter cangkang kapsul diukur menggunakan jangka
sorong.
3.3.6.1.2 Penimbangan Berat Cangkang Kapsul
3.3.6.1.3 Pengukuran Ketebalan Cangkang Kapsul
Ketebalan cangkang kapsul diukur menggunakan mikrometer.
Pengukuran dilakukan 5 kali untuk masing-masing sampel, satu kali di pusat dan
4 kali di bagian perifer, kemudian di rata-ratakan.
3.3.6.1.4 Pengamatan Warna Cangkang Kapsul
Warna cangkang kapsul diamati secara visual
3.3.6.1.5 Pengukuran Volume Cangkang Kapsul
Pengukuran volume cangkang kapsul dilakukan menggunakan pipet
volume 1 ml dimana badan kapsul diisi dengan akuades sampai penuh.
3.3.6.2 Pengujian Pengamatan Warna Bahan Obat
Pengujian Pengamatan warna bahan obat dilakukan secara visual, yaitu
dengan melihat perubahan warna pada obat yang terjadi setelah penyimpanan
selama 3 bulan.
3.3.6.3 Uji Waktu Hancur (Disintegrasi)
Bola besi berdiameter 1,44 mm sebanyak 70 buah (berat 1 bola = 9 mg)
dimasukkan ke dalam kapsul sehingga kapsul dapat tenggelam dalam medium.
Cangkang kapsul dimasukkan dalam tiap tabung dari keranjang yang dapat
dinaik-turunkan kemudian dijalankan alat dalam medium HCl 0,1 N bersuhu
37±2°C selama 2 jam. Kemudian dilanjutkan dalam medium dapar fosfat pH 6,8
bersuhu 37±2°C selama 1 jam. Uji ini dilakukan terhadap 6 kapsul. Kapsul
memenuhi persyaratan apabila :
a) Dalam medium HCl 0,1 N tidak ada kapsul yang pecah. Bila 1 atau 2
Persyaratan terpenuhi apabila tidak kurang dari 16 dari 18 kapsul yang
diuji tidak pecah.
b) Dalam medium dapar fosfat pH 6,8, semua kapsul pecah.
Kapsul dikatakan pecah dan dicatat waktunya apabila bola besi keluar
dari cangkang kapsul dan menyentuh dasar keranjang.
3.3.6.4 Uji Kerapuhan
3.3.6.1.1 Cangkang Kapsul Kosong
Cangkang kapsul kosong diletakkan dalam kotak akrilik, kemudian
dijatuhkan beban seberat 50 g dari ketinggian 10 cm. Diamati kerapuhan
cangkang kapsul. Uji ini dilakukan terhadap 6 cangkang kapsul.
3.3.6.1.2 Cangkang Kapsul Berisi (Uji Ketahanan terhadap Tekanan)
Cangkang kapsul yang berisi natrium diklofenak dan laktosa diletakkan
dalam kotak akrilik, kemudian ditekan dengan anak timbangan seberat 2 kg.
Diamati kerapuhan cangkang kapsul. Uji ini dilakukan terhadap 6 cangkang
kapsul.
3.3.6.5 Penentuan Kadar Natrium Diklofenak dalam Kapsul Alginat
Penentuan kadar natrium diklofenak dilakukan dengan mengeluarkan isi
serbuk dalam kapsul sebanyak 10 kapsul kemudian digerus hingga homogen dan
ditimbang keseluruhan serbuk. Kemudian ditimbang serbuk setara dengan 25 mg
natrium diklofenak dan dilarutkan dalam labu tentukur dengan medium pH 6,8
hingga 100 ml. Larutan yang telah dibuat dipipet sebanyak 1,2 ml dan
dimasukkan ke dalam labu tentukur 25 ml kemudian dilarutkan dengan medium
pH 6,8 hingga garis tanda dan diukur dengan menggunakan spektrofotometer UV
3.3.6.6 Uji Disolusi
Medium disolusi natrium diklofenak dalam kapsul alginat,
Medium pH berganti, yaitu :
1. Medium pH 1,2 selama 2 jam
2. Medium pH 6,8 selama 5 jam
Kecepatan pengadukan : 50 rpm
Volume medium : 900 ml
Suhu medium : 37 ± 0,5°C
Metoda : Dayung
Sampel : Natrium diklofenak dalam kapsul alginat
Prosedur Uji Disolusi:
Ke dalam wadah disolusi dimasukkan 900 ml medium lambung pH 1,2 kemudian
diatur suhu 37±0,5ºC dan kecepatan pengadukannya 50 rpm. Pada kapsul alginat
yang ingin didisolusi diberikan pemberat berbentuk ring kemudian dimasukan ke
dalam medium. Pada saat kapsul jatuh ke dasar wadah medium, baru tekan tombol
putar bersamaan dengan menghidupkan stopwach. Disolusi medium lambung pH
1,2 dilakukan selama 2 jam, dan pada interval waktu tertentu diambil aliquot
sebanyak 5 ml. Pengambilan dilakukan pada tempat yang sama yaitu pertengahan
antara permukaan medium disolusi dan bagian atas dari dayung tidak kurang 1 cm
dari dinding wadah (DitJen POM, 1995). Aliquot kemudian dimasukkan ke dalam
labu tentukur 25 ml dan ditambahkan 0,5 ml NaOH 5 N dan dicukupkan dengan
medium pH 1,2 sampai garis tanda. Setelah itu medium diganti dengan medium
pH 6,8 selama 5 jam dan pada interval waktu tertentu diambil aliquot sebanyak 5
medium pH 6,8 sampai garis tanda. Untuk menjaga volume medium disolusi tetap
konstan maka jumlah larutan yang diambil diganti dengan jumlah yang sama dari
larutan medium. Ukur konsentrasi obat dengan Spektofotometri UV dengan
panjang gelombang maksimum pada masing-masing pH yaitu λ 275,4 nm untuk
BAB IV
HASIL DAN PEMBAHASAN 4.1 Viskositas Larutan Natrium Alginat
Viskositas larutan natrium alginat diukur dengan menggunakan
viskometer Thomas-Stromer. Dari hasil pengukuran viskositas larutan alginat
80-120 cP yang mengandung titanium dioksida diperoleh viskositas sebesar 6151,65
cP dan viskositas larutan natrium alginat 80-120 cP yang tidak mengandung Titan
dioksida diperoleh viskositas sebesar 2759,67 cP. Larutan alginat tersebut
mempunyai sifat alir dan kekentalan yang sesuai untuk dapat dicetak menjadi
cangkang kapsul. Viskositas dihitung berdasarkan kurva kalibrasi khas yang dapat
menyajikan suatu konversi satuan kecepatan dan berat alat penggerak menjadi
viskositas dalam sentipois.
4.2 Spesifikasi Cangkang Kapsul Alginat
Pengukuran panjang, diameter, berat dan pengamatan warna cangkang
kapsul dilakukan terhadap badan cangkang kapsul, tutup cangkang kapsul dan
cangkang kapsul keseluruhan. Pengukuran ketebalan dilakukan terhadap badan
dan tutup cangkang kapsul. Sedangkan pengukuran volume hanya dilakukan
terhadap badan cangkang kapsul, karena umumnya bahan obat hanya diisikan ke
dalam badan cangkang kapsul sebelum ditutup dengan tutup kapsul. Air yang
digunakan untuk mengukur volume cangkang kapsul diisi sampai meniskus atas,
air menyentuh ujung kapsul untuk mencegah kelebihan pembacaan volume
Cangkang kapsul yang dibuat merupakan cangkang kapsul dengan
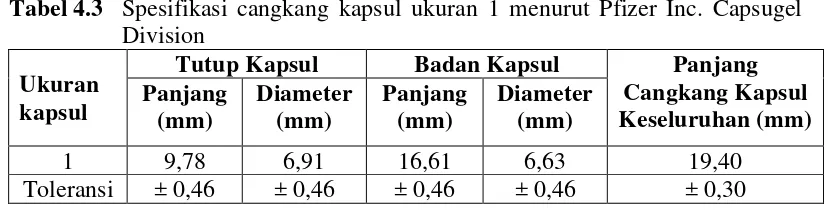
ukuran 1. Hal ini bisa dilihat dari spesifikasi cangkang kapsul alginat pada tabel
berikut.
Tabel 4.1 Spesifikasi cangkang kapsul alginat 80 – 120 cP yang mengandung TiO
No
2
Spesifikasi Tutup cangkang
Tabel 4.2 Spesifikasi cangkang kapsul alginat 80 – 120 cP yang tidak mengandung TiO
No
2 Spesifikasi Tutup
cangkang
4 Warna Putih transparan Putih transparan Putih transparan
5 Volume (ml) - 0,387 -
Tabel 4.3 Spesifikasi cangkang kapsul ukuran 1 menurut Pfizer Inc. Capsugel Division
Ukuran kapsul
Tabel 4.4 Ketebalan cangkang kapsul alginat 80 - 120cP
No Kapsul alginat Tebal Cangkang Kapsul Rata-Rata (mm) Dengan TiO2 Tanpa TiO2
1. Badan 0,108 0,099
2. Tutup 0,112 0,102
4.3 Sifat Fisik Cangkang Kapsul dan Bahan Obat 4.3.1 Sifat Fisik Cangkang Kapsul
Pada pengamatan ini, cangkang kapsul tidak menunjukkan perubahan
warna baik sebelum dan setelah penyimpanan 3 bulan pada suhu 30°C; RH 70%.
dan suhu 40°C; RH 75%. Pengamatan dilakukan secara visual
Tabel 4.5 Sifat Fisik Cangkang Kapsul Alginat 80 – 120 cP
No Perlakuan Warna
1 Mula – mula putih
2 Suhu 30°C; RH 70% putih
3 Suhu 40°C; RH 75% putih
(a) (b) (c)
Gambar 4.1 Cangkang kapsul alginat 80-120 cP sebelum dan sesudah penyimpanan
Keterangan : (a) Sebelum penyimpanan kapsul alginat 80 – 120 cP yang
mengandung TiO
(b) Setelah penyimpanan 3 bulan suhu 30°C; RH 70% kapsul
alginat 80-120 cP yang mengandung TiO
2
(c) Setelah penyimpanan 3 bulan suhu 40°C; RH 75% kapsul
alginat 80-120 cP yang mengandung TiO
2
4.3.2 Sifat Fisik Bahan Obat dalam Cangkang Kapsul Alginat
Pada pengamatan ini, bahan obat tidak menunjukkan perubahan warna
baik sebelum dan setelah penyimpanan 3 bulan pada suhu 30°C; RH 70% dan
suhu 40°C; RH 75%. Pengamatan dilakukan secara visual
(a) (b) (c)
Gambar 4.2 Serbuk natrium diklofenak sebelum dan sesudah penyimpanan
Keterangan : (a) Mula – mula
(b) Setelah penyimpanan 3 bulan suhu 30°C; RH 70%
(c) Setelah penyimpanan 3 bulan suhu 40°C; RH 75%
4.4 Uji Waktu Hancur (Disintegrasi)
Pada pengujian waktu hancur cangkang kapsul diisi dengan bola besi
sebagai bahan pengisi yang tetap tersuspensi dalam medium tetapi tidak terlarut,
mengembang atau berubah keadaan fisiknya dalam kondisi apapun, sehingga
tidak ada pengaruh dari bahan pengisi terhadap waktu hancur cangkang kapsul
(Chiwele, 2000).
Pada perlakuan terhadap kapsul mula – mula yang mengandung TiO2
selama 2 jam dalam medium HCl 0,1 N, dan dari hasil percobaan uji waktu
hancur ternyata cangkang kapsul alginat yang mengandung TiO2 tidak pecah
selama 2 jam dalam medium HCl 0,1 N. Hal ini menunjukkan bahwa kapsul
Dalam medium pH 1,2 terjadi pengembangan diameter, selain itu
cangkang kapsul juga menjadi sedikit lebih lunak. Hal ini karena sebagian
kalsium pada cangkang kapsul lepas ke dalam medium HCl 0,1 N (Bangun, dkk.,
2005). Setelah dalam HCl 0,1 N selama 2 jam, pengujian waktu hancur cangkang
kapsul dilanjutkan dalam medium dapar fosfat pH 6,8. Cangkang kapsul kalsium
alginat pecah dalam medium ini, dengan terlebih dahulu terjadi pengembangan
diameter cangkang kapsul sebelum akhirnya cangkang kapsul pecah. Dari hasil
pengujian, waktu hancur rata-rata kapsul alginat adalah 12,12 menit (dengan
cakram) dan 14,70 menit (tanpa cakram). Waktu hancur yang didapatkan lebih
kecil daripada 1 jam sehingga kapsul alginat yang mengandung TiO2 ini
memenuhi persyaratan British Pharmacopoeia (2009) untuk sediaan pelepasan
tertunda.
(a) (b)
(c) (d)
Gambar 4.3 Uji waktu hancur kapsul mula – mula yang mengandung TiO Keterangan : (a) Bola besi (Ø 1,44 mm) dan cangkang kapsul kosong
2
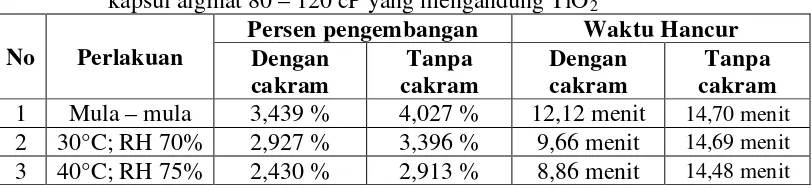
Setelah penyimpanan selama 3 bulan pada suhu 30°C; RH 70% cangkang
kapsul alginat yang mengandung TiO2 tetap mengembang dan tidak pecah dalam
medium HCl 0,1N, tetapi pecah dalam medium dapar fosfat pH 6,8 (tidak jauh
berbeda dengan keadaaan mula-mula). Pengembangan diameter cangkang kapsul
dengan % pengembangan rata-rata 2,927% (dengan cakram) dan 3,396% (tanpa
cakram) dan rata-rata waktu hancur dalam medium dapar fosfat pH 6,8 adalah
9,66 menit (dengan cakram) dan 14,69 menit (tanpa cakram) . Waktu hancur lebih
kecil daripada 1 jam menunjukkan bahwa kapsul alginat yang mengandung TiO2
Setelah dilakukan uji statistik terhadap waktu hancur kapsul menggunakan
cakram pada cangkang kapsul setelah penyimpanan pada suhu 30°C; RH 70% dan
cangkang kapsul awal dengan metode independent t-test dengan tingkat
kepercayaan 95% (α = 0,05) diperoleh t
setelah penyimpanan selama 3 bulan pada suhu 30°C; RH 70% masih memenuhi
persyaratan untuk kapsul yang tahan terhadap pH lambung (British
Pharmacopoeia, 2009).
hitung = 2,034 dan ttabel = ±2,776 dengan
signifikansi = 0,750 menunjukkan bahwa tidak terdapat perbedaan waktu hancur
dengan cakram pada cangkang kapsul alginat yang mengandung TiO2
Selanjutnya hasil uji statistik tehadap waktu hancur kapsul tanpa cakram
pada cangkang kapsul setelah penyimpanan pada suhu 30°C; RH 70% dan
cangkang kapsul awal dengan metode independent t-test dengan tingkat
kepercayaan 95% (α = 0,05) diperoleh t
setelah
disimpan selama 3 bulan pada suhu 30°C; RH 70%.
hitung = 0,008 dan ttabel = ±2,776 dengan
tanpa cakram pada cangkang kapsul alginat yang mengandung TiO2 setelah
disimpan selama 3 bulan pada suhu 30°C; RH 70%.
(a)
(b) (c)
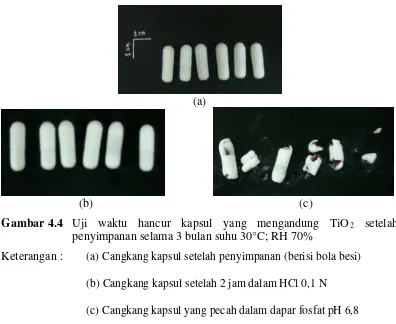
Gambar 4.4 Uji waktu hancur kapsul yang mengandung TiO2
Keterangan : (a) Cangkang kapsul setelah penyimpanan (berisi bola besi)
setelah penyimpanan selama 3 bulan suhu 30°C; RH 70%
(b) Cangkang kapsul setelah 2 jam dalam HCl 0,1 N (c) Cangkang kapsul yang pecah dalam dapar fosfat pH 6,8
Setelah penyimpanan selama 3 bulan pada suhu 40°C; RH 75% cangkang
kapsul alginat yang mengandung TiO2 tetap mengembang dan tidak pecah dalam
medium HCl 0,1N, tetapi pecah dalam medium dapar fosfat pH 6,8 (tidak jauh
berbeda dengan keadaaan mula-mula). Pengembangan diameter cangkang kapsul
dengan % pengembangan rata-rata 2,430% (dengan cakram) dan 2,913% (tanpa
cakram) dan rata-rata waktu hancur dalam medium dapar fosfat pH 6,8 adalah
8,66 menit (dengan cakram) dan 14,48 menit (tanpa cakram) . Waktu hancur lebih
kecil daripada 1 jam menunjukkan bahwa kapsul alginat yang mengandung TiO2
setelah penyimpanan selama 3 bulan pada suhu 40°C; RH 75% masih memenuhi
Setelah dilakukan uji statistik terhadap waktu hancur kapsul menggunakan
cakram pada cangkang kapsul setelah penyimpanan pada suhu 40°C; RH 75%
dengan metode independent t-test dengan tingkat kepercayaan 95% (α = 0,05)
diperoleh thitung = 3,373 dan ttabel = ±2,776 dengan signifikansi = 0,106
menunjukkan bahwa terdapat perbedaan waktu hancur dengan cakram pada
cangkang kapsul alginat yang mengandung TiO2
Selanjutnya hasil uji statistik tehadap waktu hancur kapsul tanpa cakram
pada cangkang kapsul setelah penyimpanan pada suhu 40°C; RH 75% dan
cangkang kapsul awal menggunakan metode independent t-test dengan tingkat
kepercayaan 95% (α = 0,05) diperoleh t
setelah disimpan selama 3 bulan
pada suhu 40°C; RH 75%.
hitung = 0,207 dan ttabel = ±2,776 dengan
signifikansi = 0,057 menunjukkan bahwa tidak terdapat perbedaan waktu hancur
tanpa cakram pada cangkang kapsul alginat yang mengandung TiO2 setelah
disimpan selama 3 bulan pada suhu 40°C; RH 75%.
(a)
(b) (c)
Gambar 4.5 Uji waktu hancur kapsul yang mengandung TiO2 setelah