TOKSISITAS DAN IMUNOGENISITAS PRODUK
EKSTRASELULER Streptococcus agalactiae TIPE
NON-HEMOLITIK PADA IKAN NILA Oreochromis niloticus
SEFTI HEZA DWINANTI
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
PERNYATAAN MENGENAI TESIS DAN
SUMBER INFORMASI
Dengan ini saya menyatakan bahwa tesis Toksisitas dan Imunogensitas Produk Ekstraseluler Streptococcus agalactiae Tipe Non-hemolitik pada Ikan Nila
Oreochromis niloticus adalah karya saya dengan arahan dari komisi pembimbing dan belum diajukan dalam bentuk apapun kepada perguruan tinggi manapun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka pada bagian akhir tesis ini.
Bogor, Desember 2011
Sefti Heza Dwinanti
ABSTRACT
SEFTI HEZA DWINANTI. Toxicity and Immunogenicity of Non-hemolytic
Streptococcus agalactiae Extracellular Products to Tilapia Oreochromis niloticus. Under direction of SUKENDA, MUNTI YUHANA and ANGELA MARIANA LUSIASTUTI.
Toxicity and immunogenicity of extracellular products (ECP) of non-hemolytic Streptococcus agalactiae were studied in the tilapia Oreochromis niloticus. The aim of this research was to analyse the toxicity and immunogenicity of ECP of non-hemolytic S. agalactiae and to evaluate ECP as a material vaccine for prevention of S. agalactiae. Toxicity to tilapia was detected in the ECP. There was a chronic mortality pattern which was shown after post ECP injection. By intraperitoneal injection into young tilapia (± 20 g), the median lethal dose were calculated at 633,9 µg/kg bodyweight for isolate 3 and 685,4 µg/kg bodyweight for isolate 5. Cytopathic effects of ECP to tilapia’s lymphocytes were observed during 0, 30, 60 and 180 minutes. A mixture of ECP caused nuclear granulation and cytoplasmic streaming after 60 minutes. Using immunodiffusion analysis, precipitate line was demonstrated against tilapia anti-ECP sera, and there was bio-specific type anti sera against for each isolate. The ECP vaccine effective to protect tilapia from S. agalactiae was injected intraperitoneally (IP) at 2 x 105
CFU/ml. Tilapia vaccinated with ECP from isolat 3 which protein 283 µg/kg bodyweight had a RPS value 60%. Tilapia vaccinated with ECP from isolat 5 which protein 408 µg/kg had a RPS value 68%.
RINGKASAN
SEFTI HEZA DWINANTI. Toksisitas dan Imunogenisitas Produk Ekstraseluler
Streptococcus agalactiae Tipe Non-hemolitik pada Ikan Nila Oreochromis niloticus. Dibimbing oleh SUKENDA, MUNTI YUHANA dan ANGELA MARIANA LUSIASTUTI.
Streptococcus agalactiae merupakan bakteri Gram positif yang menjadi patogen utama pada budidaya ikan nila di Indonesia. Bakteri ini diklasifikasikan menjadi tiga kelompok berdasarkan kemampuannya melisis sel darah merah, yaitu tipe β-hemolitik, α-hemolitik dan hemolitik. Menurut Hardi (2011) tipe non-hemolitik lebih bersifat virulen dibandingkan tipe β-hemolitik. Sheehan (2009) menyatakan bahwa dari survei terhadap 500 isolat Streptococci yang berasal dari 13 negara termasuk Indonesia, 58% penyakit streptococcosis yang terjadi pada ikan nila disebabkan oleh S. agalactiae tipe non-hemolitik. Sebagai patogen, bakteri ini memiliki faktor virulensi untuk menginfeksi inang. Salah satu faktor virulensi S. agalactiae adalah kandungan eksotoksin yang terlarut pada
extracellular product (ECP)-nya. Selama ini penyakit streptococcosis ditanggulangi dengan menggunakan antibiotika, akan tetapi penggunaan antibiotika potensial untuk mengobati penyakit bakterial pada ikan telah dilarang pemakaiannya karena membahayakan manusia dan lingkungan. Maka cara lain yang ditempuh untuk mengendalikan penyebaran penyakit streptococcosis adalah penggunaan vaksin. Untuk menentukan material vaksin diperlukan kajian terhadap faktor virulensi yang dimiliki bakteri terutama toksisitasnya. Oleh karena itu, maka penelitian ini bertujuan untuk menghasilkan kandidat vaksin yang mampu memproteksi ikan nila dari serangan penyakit streptococcosis dengan mengkaji toksisitas dan imunogenisitas dari ECP S. agalactiae tipe non-hemolitik.
Penelitian ini dilakukan di Laboratorium Kesehatan Ikan Departemen Budidaya Perairan, Fakultas Perikanan Ilmu Kelautan Institut Pertanian Bogor, Laboratorium Mikrobiologik Terpadu, Fakultas Kedokteran Hewan IPB dan Laboratorium Kesehatan Ikan Balai Riset Perikanan Budidaya Air Tawar Sempur, Bogor. Bakteri S. agalactiae yang digunakan merupakan koleksi Laboratorium Kesehatan Ikan Balai Riset Perikanan Air Tawar Bogor yaitu isolat 3 dan isolat 5. Ikan uji yang digunakan adalah ikan nila dengan ukuran rataan bobot tubuh 20 g/ekor.
Penelitian ini dibagi menjadi tiga tahapan. Pada tahapan pertama dilakukan pengujian karakteristik terhadap bakteri S. agalactiae dan identifikasi protein ECP-nya. Hasil pengujian karakteristik diketahui bahwa S. agalactiae
isolat 5 memiliki 3 pita protein dengan masing-masing berat protein 21,9 KDa; 53 KDa dan 76,3 KDa.
Pada tahapan kedua dilakukan pengujian toksisitas ECP baik secara in vitro dan in vivo. Pada pengujian secara in vitro dilakukan pengamatan terhadap kerusakan limfosit ikan nila yang dipaparkan dengan ECP pada 0, 30, 60 dan 180 menit. Sedangkan pada pengujian secara in vivo digunakan ikan nila sebanyak 15 ekor dengan bobot rataan 20 g/ekor. Dosis protein yang digunakan mengacu pada hasil pengukuran konsentrasi protein pada tahap I yaitu 283,75 µg/Kg; 425,625 µg/Kg; 567,5 µ g/Kg dan 709,375 µ g/Kg untuk isolat 3 dan dosis protein 408,75 µg/Kg, 613,125 µg/Kg, 817,5 µg/Kg dan 1021,875 µg/Kg untuk isolat 5. Selanjutnya ikan dipelihara selama 14 hari dan dilakukan pengamatan kematian ikan, perubahan pola renang dan patologi anatomi organ luar. Penentuan LD50 berdasarkan jumlah kematian yang tercatat pasca infeksi dan dihitung dengan menggunakan metode Karber. Dari hasil pengujian secara in vitro terlihat bahwa ECP mampu merusak limfosit setelah 60 menit pemaparan. Sedangkan secara in vivo nilai LD50
Pada tahapan ketiga dilakukan pengujian imunogenisitas ECP secara in vitro dan in vivo. Pada pengujian secara in vitro dilakukan pengamatan dengan analisa imunodifusi dimana sebagai antigen adalah ECP dan sebagai antibodi adalah serum anti ECP ikan nila. Pada pengujian secara in vivo digunakan ikan nila sebanyak 33 ekor dengan bobot rataan 20 g/ekor. ECP yang telah diinaktifkan dengan neutral buffer formaline 3% disuntikan secara intraperitoneal ke ikan nila sebanyak 0,1 ml/ekor. Pada hari ke-14 pemeliharaan dilakukan uji tantang dengan bakteri beserta ECP (sel dan media kultur) S. agalactiae yang dikultur selama 24 jam. Hasil pengujian secara in vitro menunjukkan bahwa ECP bersifat bio-tipe spesifik dimana persipitasi yang terbentuk hanya terjadi pada antibodi dan antigen dari isolat yang sama. Hasil pengujian secara in vivo menunjukkan bahwa vaksin ECP yang diberikan pada ikan nila efektif memproteksi ikan nila dari serangan bakteri S. agalactiae pada kepadatan 2 x 10
yang dihitung dengan metode Reed dan Muench (1938) dari isolat 3 adalah 633,9 µg/Kg dan isolat 5 adalah 685,4 µg/Kg. Pola kematian pada ikan nila akibat infeksi ECP adalah pola kematian kronis. Gejala klinis yang ditimbulkan oleh ECP hampir sama dengan yang ditimbulkan oleh bakteri yaitu abnormalitas pada mata (exopthalmia, purulens, opacity), kehilangan keseimbangan ketika berenang (whirling disease) dan bentuk badan seperti huruf “C”.
5
Dari penelitian yang dilakukan dapat disimpulkan bahwa ECP S. agalactiae tipe non-hemolitik mampu menyebabkan penyakit streptococcosis pada ikan nila dengan konsentrasi minimum protein adalah 283 µg/Kg untuk isolat 3 dan 408 µg/Kg untuk isolat 5. Pemanfaatan ECP sebagai kandidat vaksin untuk memproteksi ikan nila terhadap penyakit tersebut dapat dilakukan.
CFU/ml. Perlindungan relatif (relative percent survival/RPS) yang diberikan oleh isolat 3 yang mengandung protein 283 µg/kg adalah 60%, sedangkan RPS untuk isolat 5 yang mengandung protein 408 µg/kg adalah 68%.
Kata kunci : toksisitas, imunogenisitas, produk ekstraseluler (ECP), Streptococcus agalactiae tipe non-hemolitik, ikan nila Oreochromis niloticus
© Hak Cipta milik IPB, Tahun 2011
Hak Cipta dilindungi Undang-Undang
Dilarang mengutip sebagian atau seluruh karya tulis ini tanpa mencantumkan atau menyebutkan sumbernya. Pengutipan hanya untuk kepentingan pendidikan, penelitian, penulisan karya ilmiah, penyusunan laporan, penulisan kritik dan tinjauan suatu masalah; dan pengutipan tersebut tidak merugikan kepentingan yang wajar IPB
TOKSISITAS DAN IMUNOGENISITAS PRODUK
EKSTRASELULER Streptococcus agalactiae TIPE
NON-HEMOLITIK PADA IKAN NILA Oreochromis niloticus
SEFTI HEZA DWINANTI
Tesis
Sebagai salah satusyarat untuk memperoleh gelar Magister Sains pada
Program Studi Ilmu Akuakultur
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
PRAKATA
Puji dan syukur penulis panjatkan kepada Allah SWT atas segala karunia-Nya sehingga karya ilmiah ini berhasil diselesaikan. Tema yang dipilih dalam penelitian yang dilaksanakan sejak bulan April sampai dengan September 2011 ini ialah vaksin pada ikan nila, dengan judul Toksisitas dan Imunogenisitas Produk Ekstraseluler Streptococcus agalactiae Tipe Non-hemolitik pada Ikan Nila
Oreochromis niloticus.
Dengan keikhlasan hati penulis mengucapkan terima kasih kepada :
1. Bapak Dr. Sukenda, Ibu Dr. Munti Yuhana dan Ibu Dr. drh. Angela Mariana Lusiastuti selaku pembimbing, yang telah memberikan arahan dan masukkan terhadap kesempurnaan tesis ini
2. Ibu Dr. Widanarni selaku dosen tamu yang telah memberikan saran dan kritik terhadap kesempurnaan tersis ini
3. Ayahanda Sahupi dan Ibunda Asnimar serta Ayahanda Edy Siswanto dan Ibunda Ely Urda F yang selalu memberikan doa dan dukungan selama penulis menyelesaikan pendidikan
4. Suami tercinta Fadly Kusuma Siswanto dan ananda Aisyah Zahra Siswanto “my lovely strawberry” yang selalu memberikan semangat dan doa selama penulis menyelesaikan pendidikan
5. Semua saudara tercinta Sasmitesi, Sahera Nofyangtri, Putri, Imron dan Firdaus yang memberikan dukungan dan semangat dalam menyelesaikan pendidikan
6. Teman-teman Akuakultur 2009 yang selalu menemani penulis mulai dari awal pendidikan hingga selesai
7. Seluruh anggota Laboratorium Kesehatan Ikan BDP-IPB, terutama Bapak Ranta yang dengan ikhlas membantu penulis, angkatan BDP 44 yang selalu menemani dan memberikan bantuan selama penelitian.
8. Semua pihak yang membantu baik secara langsung maupun tidak langsung yang tidak bias disebutkan satu persatu
Semoga karya ilmiah ini bermanfaat.
Bogor, Desember 2011
RIWAYAT HIDUP
Penulis dilahirkan di Palembang pada tanggal 1 September 1984 dari Bapak Sahupi dan Ibu Asnimar. Penulis adalah putri kedua dari tiga bersaudara.
DAFTAR ISI
2.3 Pengendalian streptococcosis dengan vaksinasi ... 6
III. METODE PENELITIAN ... 8
3.3.1 Karakteristik bakteri dan produk ekstraseluler Streptococcus agalactiae ... 10
3.3.2 Pengujian toksisitas produk ekstraseluler Streptococcus agalactiae ... 10
3.3.3 Pengujian imunogenitas produk ekstraseluler Streptococcus agalactiae ... 11
IV. HASIL DAN PEMBAHASAN ... 12
4.1 Hasil ... 12
4.1.1 Karakteristik bakteri dan produk ekstraseluler Streptococcus agalactiae ... 12
4.1.2 Toksisitas produk ekstraseluler Streptococcus agalactiae ... 14
4.1.3 Immunogenisitas produk ekstraseluler Streptococcus agalactiae ... 17
4.2 Pembahasan ... 20
V. SIMPULAN DAN SARAN ... 24
DAFTAR PUSTAKA ... 25
DAFTAR TABEL
Halaman 1 Karakteristik bakteri Streptococcus agalactiae isolat 3 dan
isolat 5 ... 12 2 Kerusakan limfosit setelah pemaparan produk ekstraseluler
Streptococcus agalactiae ... 16 3 Persentase kematian dan nilai LD50 Streptococcus agalactiae
isolat 3 ... 16 4 Persentase kematian dan nilai LD50 Streptococcus agalactiae
DAFTAR GAMBAR
Halaman 1 Streptococcus pada media agar darah ... 04 2 Diagram alir penelitian ... 09 3 Alur pengujian efikasi vaksinasi Streptococcus agalactiae ... 11 4 Morfologi Streptococcus agalactiae isolat 3, 5 dan uji hemolisin
isolat 3 dan isolat 5... 13 5 Kurva standar pengukuran konsentrasi protein produk ekstraseluler
bakteri Streptococcus agalactiae ... 14 6 Berat molekul protein produk ekstraseluler Streptococcus agalactiae
isolat 3 dan isolat 5 pada gel acrylamide (SDS-PAGE) dengan
pewarna perak ... 14 7 Pemisahan limfosit dengan menggunakan Percoll ... 15 8 Perubahan morfologi sel limfosit dari 0,30, 60 dan 180 menit ... 15 9 Pola kematian ikan nila setelah diinfeksi produk ekstraseluler
Streptococcus agalactiae isolat 3 ... 16 10 Pola kematian ikan nila setelah diinfeksi produk ekstraseluler
Streptococcus agalactiae isolat 5... 17 11 Analisa immunodifusi produk ekstraselular
DAFTAR LAMPIRAN
Halaman 1 Metode karakterisasi bakteri Streptococcus agalactiae ... 28 2 Metode pengukuran konsentrasi protein dan penentuan
berat molekul ECP Streptococcus agalactiae ... 30 3 Metode pengujian toksisitas produk ekstraseluler
Streptococcus agalactiae ... 32 4 Metode pengujian imunogenisitas produk ekstraseluler
1
I. PENDAHULUAN
1.1 Latar belakang
Produksi ikan nila di Indonesia meningkat secara signifikan dari tahun ke
tahun. Pada tahun 2004 jumlah produksi ikan nila hanya 97.116 ton kemudian
meningkat menjadi 206.904 ton pada tahun 2007 dan tahun 2008 sudah mencapai
220.900 ton (KKP 2010). Seiring peningkatan produksi ikan nila, keberadaan
penyakit yang mampu menghambat produksi ikan nila saat ini belum bisa diatasi
dengan baik. Salah satu penyakit yang sering muncul pada budidaya ikan nila
adalah penyakit streptococcosis. Streptococcosis pada budidaya ikan nila telah
menyebabkan ikan sakit dan kematian sehingga menimbulkan kerugian yang
diestimasi mencapai $ 150 juta/tahun (Klesius et al. 2000). Salah satu bakteri
penyebab penyakit streptococcosis adalah bakteri Streptococcus agalactiae tipe
non hemolitik.
Streptococcus agalactiae merupakan bakteri Gram positif yang menjadi
patogen utama pada budidaya ikan nila di Indonesia. S. agalactiae pada budidaya
ikan nila yang menyebabkan penyakit streptococcosis memiliki dua tipe yaitu tipe β hemolitik dan tipe non hemolitik (Sheehan 2009). Secara umum kedua tipe bakteri ini menunjukkan gejala klinis yang sama yaitu abnormalitas pada mata
(exopthalmia, purulens, opacity), kehilangan keseimbangan ketika berenang
(whirling disease), bentuk badan seperti huruf “C”, nafsu makan menurun, warna
tubuh menjadi lebih gelap, bercak merah, asites dan pada kondisi akut dapat
menyebabkan ikan kehilangan cairan pada saluran pencernaan serta tidak
berfungsinya sebagian organ (Hardi 2011).
Seperti bakteri Gram positif lainnya, bakteri ini memiliki beberapa faktor
virulensi yang dapat menyebabkan penyakit. Salah satu faktor virulensinya adalah
kandungan eksotoksin yang terlarut pada extracellular product (ECP)-nya.
Sedangkan pada bakteri Gram negatif faktor virulensi lebih banyak terdapat pada
lipopolysacharida (endotoksin) (Williams et al. 2003). Diduga ECP S. agalactiae
yang terdiri dari kapsular polisakarida, protein permukaan dan beberapa sekresi
protein inilah yang membantu bakteri menempel pada sel epitel inang serta
menghindari mekanisme pertahanan tubuh inang (Glaser et al. 2002). ECP
2
tipe non hemolitik diduga sebagai tipe yang lebih virulen karena konsentrasi
protein pada ECP-nya lebih tinggi yaitu 13,64 ppm sedangkan tipe β hemolitik
8,18 ppm (Hardi 2011).
Salah satu upaya yang dapat dilakukan untuk mengendalikan penyakit ini
adalah dengan menggunakan vaksin. Vaksin merupakan antigen yang diperoleh
dari seluruh bagian atau zat toksin dari patogen yang diinaktifkan dengan tujuan
meningkatkan respon imun dari inang. Beberapa tipe vaksin yang digunakan
dalam budidaya ikan, berdasarkan bentuk patogennya antara lain bakteri inaktif,
virus inaktif, sub unit (teknologi rekombinan) dan DNA. Pemanfaatan bakteri baik
menggunakan keseluruhan sel bakteri (whole cells vaccine) maupun zat toksin
yang ada di bakteri (extracellular products vaccine) ataupun gabungan keduanya
mampu memberikan proteksi pada ikan nila dari infeksi S. agalactiae. Faktor
yang menghambat perkembangan efikasi vaksin (terutama vaksin sel utuh)
terhadap bakteri ini adalah kemampuan vaksin tersebut untuk memproteksi kedua tipe bakteri baik itu β hemolitik dan non hemolitik secara bersamaan (Hardi 2011). Vaksin yang terdiri dari tipe β hemolitik hanya mampu memproteksi ikan nila dari tipe β hemolitik saja begitu juga dengan tipe non hemolitik hanya mampu memproteksi ikan nila dari tipe non hemolitik (Sheehan 2009). Kajian mengenai
ECP S. agalactiae tipe non-hemolitik sebagai kandidat vaksin untuk memproteksi
ikan nila masih sedikit. S. agalactiae tipe non-hemolitik pertama kali ditemukan
pada ikan golden shiner (Robinson dan Mayer 1966). Kemudian Rasheed dan
Plumb (1984) yang mengkaji patogenesitas S. agalactiae pada ikan gulf killifish.
Elliots et al.(1990) mengkaji pola protein pada sel bakteri S. agalactiae non
hemolitik yang di isolasi dari ikan. Sheehan (2009) menyatakan bahwa dari survei
terhadap 500 isolat Streptococci yang berasal dari 13 negara termasuk Indonesia,
58% penyakit streptococcosis yang terjadi pada ikan nila disebabkan oleh
S. agalactiae tipe non-hemolitik. Oleh karena itu, perlu dilakukan pengkajian
terhadap vaksin dari tipe non hemolitik terutama pada aspek toksisitas dan
3
1.2 Perumusan masalah
Penyakit Streptococcosis yang terjadi pada budidaya ikan nila mengalami
peningkatan selama beberapa tahun terakhir sebagai konsekuensi dari kegiatan
akuakultur intensif, yang menyebabkan kerugian dalam industri budidaya ikan
nila. Salah satu agen utama penyebab penyakti Streptococcosis adalah
Streptococcus agalactiae tipe non-hemolitik. Upaya yang dapat dilakukan untuk
mengendalikan penyakit ini adalah vaksinasi. Peningkatan efikasi vaksin untuk
memberikan proteksi terbaik terhadap serangan bakteri Streptococcus agalactiae
tipe non hemolitik pada ikan nila terus dikaji mulai dari pemanfaatan sel utuh
bakteri, produk ekstraseluler dan gabungan keduanya.
1.3 Tujuan dan manfaat
Tujuan penelitian ini adalah untuk menganalisa toksisitas dan
imunogenisitas ECP Streptococcus agalactiae tipe non-hemolitik. Sehingga
diharapkan akan menghasilkan kandidat vaksin yang efektif untuk memproteksi
4
II. TINJAUAN PUSTAKA
2.1 Bakteri Streptococcus agalactiae
Streptococcus agalactiae dikelompokkan ke dalam grup B Streptococcus
(GBS) (Lancefield 1933). Berdasarkan kandungan kapsul polisakarida, terdapat
10 jenis tipe serotype yang telah teridentifikasi (Kong et al. 2002; Slotved et al.
2007). Secara umum karakteristik bakteri ini adalah bentuk kokus, Gram positif,
katalase (-), oksidase (-), CAMP (+) dan hidrolisa hippurate (-). Selain
pengelompokan Lancefield identifikasi S. agalactiae berdasarkan kemampuannya
menghemolisis darah pada media agar darah. Tipe hemolisis yang ada untuk
bakteri Streptococcus adalah alpa (α-), beta (β-) dan non (γ-) hemolitik. α
hemolitik memiliki kemampuan parsial menghemolisis media agar darah dan mengekspresikan zona kehijauan disekitar koloni, β hemolitik mengekspresikan zona bening disekitar koloni dan non hemolitik tidak mampu melisis darah pada
media agar (Gambar 1). S. agalactiae dibagi menjadi dua tipe yaitu β hemolitik
dan non hemolitik. Sedangkan berdasarkan pengujian ekspresi fenotif, derajat
hidrofobitas dan aktivitas hemaglutinasi, bakteri ini dikelompokkan dalam tipe
berkapsul dan non kapsul (Wibawan et al. 1992).
Gambar 1. Streptococcus pada media agar darah. (a) β-hemolitik, (b) α-hemolitik
dan (c) Non-hemolitik
Sebagai bakteri patogen, Streptococcus agalactiae memiliki faktor
virulensi untuk membantu proses infeksi pada inang. Streptococcus memproduksi
beberapa jenis toksin protein dan enzim yang mampu membunuh atau
menghancurkan susunan sel inang yang memungkinkan bakteri memanfaatkan
nutrisi inang untuk berkembangbiak. P
5
ada beberapa kasus, toksin protein dan enzim tersebut berperan penting dalam
resistensi terhadap sistem imun inang, baik komponen itu sendiri ataupun
kombinasi dengan faktor virulen pada sel seperti kapsul atau protein permukaan.
Segura dan Gottschalk (2004) menjelaskan faktor virulensi ekstraseluler pada
bakteri ini terdiri dari kapsul polisakarida, hemolisin, pirogenik eksotoksin,
hialuronidase, CAMP-faktor, superoksida dismutase dan bakteriosin. Sedangkan
Glaser et al. (2002) menjelaskan faktor virulensi bakteri ini terdapat pada produk
ekstraseluler diantaranya adalah kapsul polisakarida, protein permukaan dan
protein hasil metabolisme. Selain faktor virulensi yang menjelaskan karakteristik
interistik dari bakteri ini, patogenesitas S. agalactiae merupakan hal penting untuk
diketahui terkait dengan proses perjalanan bakteri dari awal infeksi hingga
menyebabkan kematian pada inang dalam upaya pengendalian penyakit. Hardi
(2011) menyatakan bahwa tipe non hemolitik lebih virulen dibandingkan dengan tipe β hemolitik dilihat dari jumlah kematian yang lebih cepat dan banyak, perubahan pola renang, pola makan dan patologi anatomi secara makroskopis dan
mikroskopis.
2.2 Streptococcosis pada ikan
Penyakit streptococcosis pada ikan pertama kali dilaporkan menyerang
budidaya ikan rinbow trout pada tahun 1957 di Jepang (Hoshina et al. 1958),
sedangkan pada ikan air tawar pertama kali ditemukan pada ikan golden sea
bream (Robinson dan Meyer 1966). Saat ini streptococcosis menyerang budidaya
ikan nila hampir di setiap negara Asia seperti di Cina, Vietnam, Filipina, Thailand
dan Indonesia sedangkan di negara Amerika Latin ditemukan di Ekuador,
Honduras, Meksiko dan Brazil (Sheehan 2009).
Streptococcosis pada ikan disebabkan oleh 6 spesies Gram positif yang
berbeda termasuk didalamnya streptococci, lactococci dan vagocci (Bercovier et
al. 1997). Spesies utama yang bersifat patogenik penyebab streptococcosis adalah
Streptococcus parauberis, S. iniae, S. agalactiae, Lactococcus garviae, L.
piscium, Vagococcus salmoninarum dan Carnobacterium piscicola (Bercovier et
6
Menurut Evans et al. (2006) penularan penyakit ini dapat terjadi melalui
persinggungan dengan ikan sakit. Gejala yang ditimbulkan tergantung pada
tingkat serangan, yaitu akut dan kronis. Pada tingkat kronis, gejala yang Nampak
yaitu adanya memar seperti luka dipermukaan tubuh, bercak merah pada sirip,
berenang lambat, sering berada didasar akuarium dan menyebabkan nafsu makan
menurun. Gejala lain yang sering muncul abonormalitas pada mata (exopthalmia,
opacity dan purulens) dan kehilangan keseimbangan (whirling disease). Apabila
serangan akut terjadi, maka akan terjadi kematian yang diduga karena adanya
toksin, kehilangan cairan pada saluran pencernaan dan tidak berfungsinya
sebagian organ. Streptococcosis menyebabkan meningoenchephalitis dan
septikemia pada ikan. Organ target yang diserang adalah bagian otak (cerebellum)
dimana terjadi degenerasi dan nekrosa di bagian kranial dan terjadi kongesti
(pembendungan) pada pembuluh darah otak belakang. Sedangkan pendarahan
juga terjadi pada jaringan dalam organ. Penyebaran S. agalactiae ke dalam organ
ikan melalui darah, dimana bakteri ini masuk kedalam aliran darah, dapat tumbuh
dan berkembang serta menyebar melalui darah (Hardi 2011).
2.3 Pengendalian streptococcosis dengan vaksinasi
Vaksin merupakan suatu substansi yang mengandung zat antigenik yang
mampu membangkitkan sistem imun untuk memproteksi inang dari serangan
patogen. Vaksinasi merupakan salah satu cara pengendalian penyakit dalam
budidaya ikan. Ada beberapa macam vaksin yang biasa digunakan dalam
budidaya ikan antara lain vaksin sel utuh, vaksin dari komponen sel dan vaksin
DNA. Pemilihan vaksin yang digunakan bergantung pada jenis bakteri yang
digunakan, kondisi ikan dan lingkungan. Ada berapa hal yang perlu
dipertimbangkan dalam pembuatan vaksin seperti antigen yang heterogen,
imunitas yang relatif rendah dan cara aplikasinya di lapangan (Pasaribu et al.
1990). Selain itu, efikasi vaksin sangat bergantung pada jenis dan kualitas vaksin,
teknik pemberian vaksin, kondisi ikan dan lingkungan.
Menurut Lindahl et al. (2005) protein permukaan merupakan kandidat
vaksin yang potensial untuk dikembangkan karena mampu memproteksi inang
7
yang baik, akan tetapi tidak semua molekul protein merupakan imunogen. Syarat
material vaksin adalah bersifat toksik pada kondisi normal dan bersifat
imunogenik setelah di inaktifkan. Penelitian terakhir yang telah dilakukan oleh
Hardi (2011) memberikan informasi bahwa pemanfaatan ECP yang diproduksi
oleh bakteri S. agalactiae sebagai material vaksin memiliki protein dengan berat
molekul 51,8 KDa; 55,8 KDa dan 62,3 KDa untuk tipe β hemolitik sedangkan tipe
nonhemolitik memiliki protein dengan berat molekul 55,8 KDa dan 62,3 KDa.
Hal yang sama juga dinyatakan oleh Pasnik et al. (2005) bahwa kandungan
protein ECP S. agalactiae yang digunakan sebagai vaksin ikan berkisar pada
47-75 KDa dan yang lebih dominan adalah protein dengan berat molekul 54 dan 55
KDa.
Hardi (2011) menyatakan vaksin gabungan produk ekstraseluler dan sel
utuh dari bakteri Streptococcus agalactiae tipe β hemolitik mampu memproteksi
ikan nila dengan RPS 92% dari infeksi bakteri setipe dan 75% untuk bakteri tipe
non hemolitik. Evans et al. (2004) menyatakan vaksin gabungan S. agalactiae tipe β hemolitik hanya memberikan proteksi pada ikan nila dengan nilai RPS 70% ketika diuji tantang dengan bakteri setipe. Selain vaksinasi pemberian imunisasi
pasif pada ikan nila terhadap S. agalactiae memberikan hasil 100% ikan mampu
hidup ketika diuji tantang dengan 1,5 x 104 CFU/ml selama 25 hari (Pasnik et al.
8
III. METODE PENELITIAN
Penelitian ini dilaksanakan melalui tiga tahapan, yaitu 1) isolasi dan
identifikasi, 2) pengujian toksisitas dan 3) pengujian respon imunogenisitas
produk ekstraselular Streptococcus agalactiae baik secara in vitro maupun in vivo.
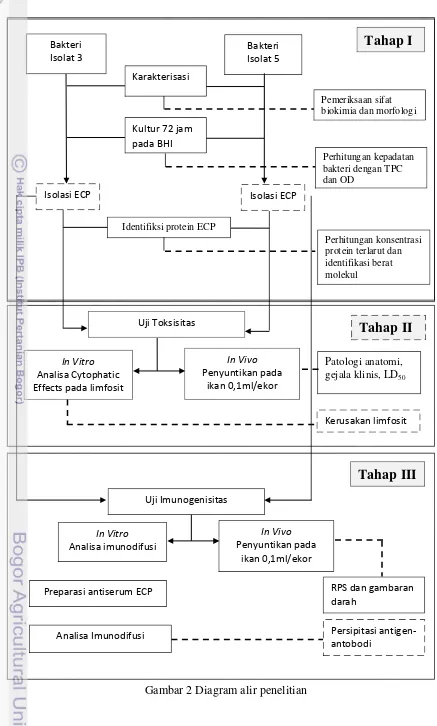
Pelaksanaan penelitian secara skematis disajikan pada Gambar 2.
3.1 Waktu dan tempat
Penelitian ini akan dilaksanakan mulai bulan April sampai dengan
September 2011 yang bertempat di Laboratorium Kesehatan Ikan Departemen
Budidaya Perairan, Fakultas Perikanan Ilmu Kelautan Institut Pertanian Bogor,
Laboratorium Mikrobiologik Terpadu, Fakultas Kedokteran Hewan IPB dan
Laboratorium Kesehatan Ikan Balai Riset Perikanan Budidaya Air Tawar, Bogor.
3.2 Materi Penelitian
3.2.1 Ikan uji
Ikan uji yang digunakan adalah ikan nila Oreochromis niloticus dengan
bobot rataan 20 g/ekor. Sebelum dilakukan pengujian, ikan diadaptasikan dalam
akuarium uji selama 7 hari. Ikan uji dipastikan tidak terinfeksi Streptococcus
berdasarkan diagnosa penyakit level 2 yaitu diagnosa secara mikrobiologi.
3.2.2 Bakteri uji
Bakteri uji yang digunakan adalah Streptococcus agalactiae isolat 3 dan
isolat 5. Bakteri ini berasal dari koleksi Laboratorium Kesehatan Ikan Balai Riset
Perikanan Air Tawar Bogor.
3.2.3 Produk ekstraseluler bakteri uji
Produk ekstraseluler dari Streptococcus agalactiae diperoleh dari hasil
kultur bakteri selama 72 jam pada media BHI (Difco). Pemisahan antara sel dan
produk ekstraseluler (supernatan) dilakukan dengan cara mensentrifugasi biakan
9
Isolasi ECP Isolasi ECP
Karakterisasi
Preparasi antiserum ECP RPS dan gambaran
darah
10
3.3 Prosedur Penelitian
3.3.1 Karakterisasi bakteri dan produk ekstraseluler Streptococcus agalactiae
Bakteri uji yang akan digunakan, sebelumnya dikarakterisasi
fisio-morfologi secara mikrobilogik. Sedangkan produk ekstraseluler (supernatan) yang
diperoleh selanjutnya di identifikasi berat molekul protein yang terkandung
didalamnya dengan analisa SDS-PAGE (Bio-Gen) yang menggunakan pewarnaan
perak dan konsentrasi proteinnya dengan metode Bradford dimana sebagai standar
digunakan BSA fraksi V (Fermentas) dan sebagai blanko digunakan BHI (Difco)
steril.
3.3.2 Pengujian toksisitas produk ekstraseluler Streptococcus agalactiae
Pengujian toksisitas ECP dilakukan secara in vitro dan in vivo. Pada
pengujian secara in vitro dilakukan pengamatan terhadap kerusakan limfosit ikan
nila yang dipaparkan dengan ECP dengan perbandingan 1:1 pada 0, 30, 60 dan
180 menit (Kawahara, Oshima dan Nomura 1990). Separasi limfosit dari darah
ikan menggunakan Percoll mengacu pada Blaxhall dan Sheard (1985) dengan
modifikasi pelarut sukrosa 0,25 M. Pewarnaan preparat ulas limfosit
menggunakan Giemsa 6,6%. Sedangkan pada pengujian secara in vivo digunakan
ikan nila sebanyak 15 ekor dengan bobot rataan 20 g/ekor. Dosis protein yang
digunakan mengacu pada hasil pengukuran konsentrasi protein pada tahap I yaitu
283,75 µg/Kg; 425,625 µg/Kg; 567,5 µg/Kg dan 709,375 µ g/Kg untuk isolat 3
dan dosis protein 408,75 µg/Kg, 613,125 µg/Kg, 817,5 µ g/Kg dan 1021,875
µg/Kg untuk isolat 5. Selanjutnya ikan dipelihara selama 14 hari dan dilakukan
pengamatan kematian ikan, perubahan pola renang dan patologi anatomi organ
luar. Penentuan LD50 berdasarkan jumlah kematian yang tercatat pasca infeksi
dan dihitung dengan menggunakan metode Reed dan Muench (1938).
3.3.3 Pengujian imunogenisitas produk ekstraseluler Streptococcus agalactiae
Pada pengujian secara in vitro dilakukan analisa imunodifusi pada agar
semi solid dimana sebagai antigen adalah produk ekstraseluler dan sebagai
antibodi adalah serum ikan nila. Preparasi serum dilakukan dengan cara
11
formaline 3% ke ikan nila. Pada hari ke-14 pemeliharaan dilakukan pemanenan
serum ikan nila.
Pengujian secara in vivo dilakukan dengan cara menyuntikkan vaksin
produk ekstraseluler yang telah diinaktifkan dengan neutral buffer formaline 3%
ke ikan nila. Pada hari ke-14 pemeliharaan dilakukan uji tantang dengan kultivan
(sel dan media BHI) Streptococcus aglactiae yang dikultur selama 24 jam.
Efektifitas vaksin mampu memproteksi ikan nila ditinjau dari nilai Relative
Percent Ratio (RPS) yang mengacu pada Ellis (1988) seperti rumus dibawah,
serta gambaran darah pada hari ke-0, ke-7 dan ke-14 setelah vaksinasi. Alur
pelaksanaan penelitian efikasi vaksinasi dilakukan seperti Gambar 3 berikut.
RPS =�1− ������������������������������ ���������������� ��� x 100
D0 D1 D7 D14 D15 D21 D28
Vaksinasi Uji tantang SR, RPS
Keterangan:
D 0, 1, 7: hari ke-0, 1, 7 dan seterusnya
12
IV. HASIL DAN PEMBAHASAN
4.1 Hasil
4.1.1 Karakterisasi bakteri dan produk ekstraseluler Streptococcus agalactiae
Isolat 3 dan isolat 5 yang diperoleh dari koleksi BBRPAT Bogor di
identifikasi sebelum digunakan sebagai bakteri uji. Hasil pengujian karakteristik
bakteri Streptococcus agalactiae secara biokimia disajikan pada Tabel 1.
Tabel 1 Karakteristik bakteri Streptococcus agalactiae isolat 3 dan isolat 5
Pengujian Karakteristik
Isolat 3 Isolat 5
Gram positif positif
Katalase negatif negatif
Oksidase negatif negatif
Oksidatif-Fermentatif fermentatif fermentatif
Motilitas non motil non motil
Morfologi kokus kokus
Produksi asam dari D-mannitol negatif negatif
Aktivitas hemolitik non hemolitik non hemolitik
Berdasarkan Tabel 1 diatas, karakteristik bakteri S. agalactiae adalah
Gram positif yang artinya dinding bakteri tersebut mengandung peptidoglikan
sehingga mampu menahan warna kristal violet. Bentuk bakteri tersebut adalah
kokus dengan susunan sel berantai mulai dari diplococcus hingga rantai panjang.
Bakteri ini tidak memiliki enzim katalase yang mampu memecah H2O2 menjadi
O2 dan juga tidak memiliki enzim intraseluler oksidase. Keberadaan oksigen
untuk proses metabolisme bakteri tidak mutlak diperlukan oleh bakteri ini karena
memiliki sifat fermentatif yang artinya bakteri tersebut mampu memecah gula
sebagai sumber energinya tanpa melibatkan oksigen dalam reaksi pemecahan
gula. Bakteri ini tidak memiliki organ untuk mobilitasnya seperti flagel sehingga
cenderung non motil. Produksi asam sebagai hasil dari fermentasi mannitol tidak
bisa dilakukan oleh bakteri ini. Pengujian aktivitas hemolitik dilakukan untuk
13
bahwa bakteri S. agalactiae yang digunakan adalah bakteri tipe non hemolitik
(Gambar 4).
(a) (b) (c)
Gambar 4 Morfologi Streptococcus agalactiae isolat 3 (a), isolat 5 (b) dan uji hemolisin isolat 3 dan isolat 5 (c)
Berdasarkan perhitungan kepadatan bakteri S. agalactiae dengan metode
cawan sebar atau total plate count (TPC) yang dibiakkan selama 72 jam diperoleh
kepadatan bakteri isolat 3 adalah 2 x 109 CFU/ml dan isolat 5 adalah 6 x 108
Penentuan identitas protein ECP diawali dengan menentukan konsentrasi
protein terlarut di ECP. Penentuan konsentrasi protein terlarut yang terkandung
dalam ECP bakteri dihitung berdasarkan nilai absorbansi yang terukur kemudian
di interpolasi pada persamaan y = 0,004x + 0,073 yang diperoleh dari kurva
standar (Gambar 5). Konsentrasi protein terlarut untuk isolat 3 yang memiliki nilai
absorbansi 0,3 adalah 56,75 ppm sedangkan untuk isolat 5 yang memiliki nilai
absorbansi 0,4 adalah 81,75 ppm. Selanjutnya pengukuran identifikasi berat
molekul protein ECP bakteri dengan analisa SDS-PAGE yang menggunakan
perwarnaan perak memberikan hasil bahwa isolat 3 memiliki 7 jenis protein dan
isolat 5 memiliki 3 jenis protein. Untuk mengetahui berat molekul yang terdapat
di ECP, dilakukan perhitungan masing-masing protein dengan membandingkan
jarak antar pita pada marker. Perkiraan berat molekul protein isolat 3 adalah 57,3
KDa; 66,2 KDa; 67,6 KDa; 78,9 KDa; 82,2 KDa; 92,8 KDa dan 106,2 KDa. CFU/ml. Sedangkan perhitungan kepadatan bakteri S. agalactiae dengan metode
kepadatan optik atau optical density (OD) yang dibaca pada panjang gelombang
595 nm diperoleh kepadatan optik isolat 3 adalah 0,426 sedangkan kepadatan
14
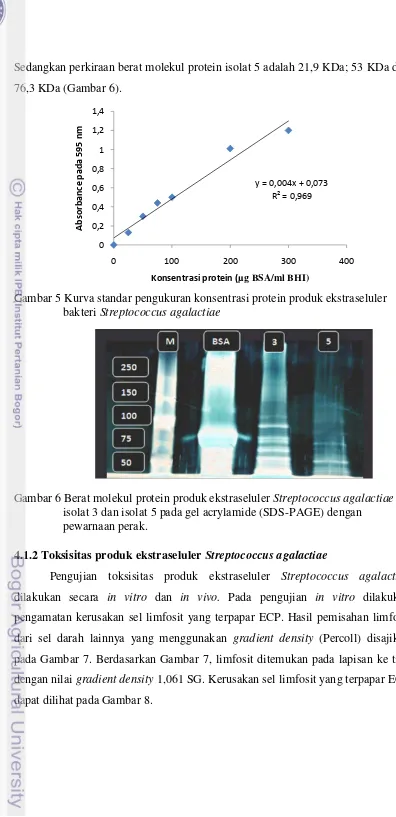
Sedangkan perkiraan berat molekul protein isolat 5 adalah 21,9 KDa; 53 KDa dan
76,3 KDa (Gambar 6).
Gambar 5 Kurva standar pengukuran konsentrasi protein produk ekstraseluler bakteri Streptococcus agalactiae
Gambar 6 Berat molekul protein produk ekstraseluler Streptococcus agalactiae isolat 3 dan isolat 5 pada gel acrylamide (SDS-PAGE) dengan pewarnaan perak.
4.1.2 Toksisitas produk ekstraseluler Streptococcus agalactiae
Pengujian toksisitas produk ekstraseluler Streptococcus agalactiae
dilakukan secara in vitro dan in vivo. Pada pengujian in vitro dilakukan
pengamatan kerusakan sel limfosit yang terpapar ECP. Hasil pemisahan limfosit
dari sel darah lainnya yang menggunakan gradient density (Percoll) disajikan
pada Gambar 7. Berdasarkan Gambar 7, limfosit ditemukan pada lapisan ke tiga
dengan nilai gradient density 1,061 SG. Kerusakan sel limfosit yang terpapar ECP
dapat dilihat pada Gambar 8.
y = 0,004x + 0,073
15
Gambar 7 Pemisahan limfosit dengan menggunakan Percoll. Darah ikan nila(a), percoll dengan konsentrasi 30%; gradient : 1,061SG(b), percoll dengan konsentrasi 40%; gradient : 1,064 SG(c), percoll dengan konsentrasi 50 %; gradient : 1,066 SG(d), lapisan I; gradient : 1,054 SG(A), lapisan II; gradient : 1,061 SG (Limfosit) (B), lapisan III; gradient : 1,050 SG(C), lapisan IV (sel darah merah) (D)
Isolat 3 Isolat 5
Gambar 8 Perubahan morfologi sel limfosit dari 0 menit (a), 30 menit (b), 60 menit (c) dan 180 menit (d)
Berdasarkan Gambar 8 diatas, kerusakan secara bertahap terjadi terhadap
struktur limfosit akibat pemaparan ECP dari isolat 3 dan isolat 5. Kekompakan
struktur limfosit berdasar pada inti dan sitoplasmanya masih terlihat bagus pada
pemaparan ECP selama 0 dan 30 menit. Berbeda halnya dengan pengamatan
limfosit setelah 60 menit pemaparan, mulai terjadi kerusakan sitoplasma limfosit.
Kerusakan pada inti sel serta sitoplasma terjadi setelah pemaparan 180 menit.
Persentase kerusakan limfosit akibat terpapar produk ekstraseluler S. agalactiae
16
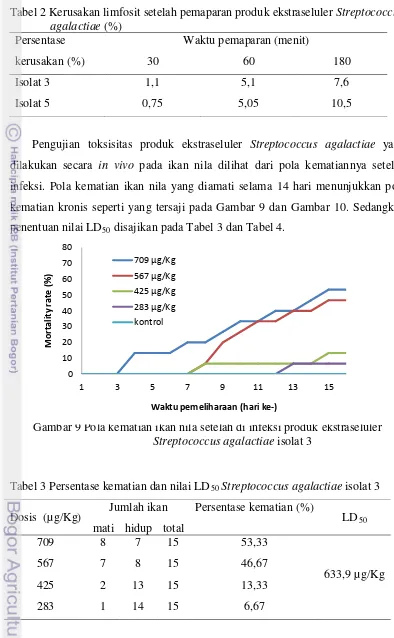
Tabel 2 Kerusakan limfosit setelah pemaparan produk ekstraseluler Streptococcus agalactiae (%)
Pengujian toksisitas produk ekstraseluler Streptococcus agalactiae yang
dilakukan secara in vivo pada ikan nila dilihat dari pola kematiannya setelah
infeksi. Pola kematian ikan nila yang diamati selama 14 hari menunjukkan pola
kematian kronis seperti yang tersaji pada Gambar 9 dan Gambar 10. Sedangkan
penentuan nilai LD50 disajikan pada Tabel 3 dan Tabel 4.
Gambar 9 Pola kematian ikan nila setelah di infeksi produk ekstraseluler Streptococcus agalactiae isolat 3
Tabel 3 Persentase kematian dan nilai LD50
Dosis (µg/Kg)
Streptococcus agalactiae isolat 3
Jumlah ikan Persentase kematian (%)
17
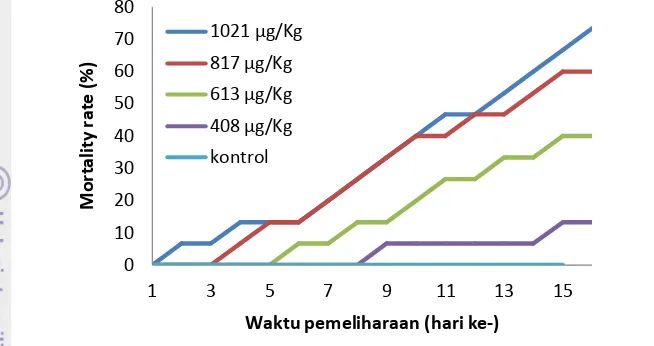
Gambar 10 Pola kematian ikan nila setelah di infeksi produk ekstraseluler Streptococcus agalactiae isolat 5
Tabel 4 Persentase kematian dan nilai LD50
Dosis (µg/Kg)
Streptococcus agalactiae isolat 5
Jumlah ikan Persentase kematian
Berdasarkan hasil pengamatan persentase dan pola kematian ikan setelah
infeksi dengan ECP pada konsentrasi tertentu terlihat bahwa kematian ikan terjadi
secara bertahap. Kematian akut tidak terjadi selama penelitian, sedangkan
persentase kematian yang paling tinggi terjadi pada konsentrasi tertinggi protein
ECP yaitu 14,19 µ g/ekor untuk isolat 3 dan 20,44 µg/ekor untuk isolat 5. Nilai
LD50 yang dihitung dengan menggunakan metode Reed dan Muench (1938) untuk
isolat 3 adalah 633,9 µg/Kg dan isolat 5 adalah 685,4 µ g/Kg.
4.1.3 Imunogenisitas produk ekstraseluler Streptococcus agalactiae
Pengujian imunogenisitas produk ekstraseluler Streptococcus agalactiae
dilakukan secara in vitro dan in vivo. Berdasarkan pengujian secara in vitro yang
18
imunogenik. Sifat imunogenisitas ECP hanya berlaku untuk isolat yang sama dan
tidak berlaku untuk isolat yang berbeda. (Gambar 11).
Gambar 11 Analisa immunodifusi produk ekstraselular Streptococcus agalactiae. (a) anti serum ikan nila dari S. agalactiae isolat 3, (b) produk ekstraseluler S. agalactiae isolat 3, (c) produk ekstraseluler S. agalactiae isolat 5 , (d) PBS dan (e) anti serum ikan nila dari S. agalactiae isolate 5.
Dari gambar diatas dapat dilihat bahwa produk ekstraseluler S. agalactiae
bersifat imunogenik dan spesifik. Endapan putih antara sumur yang terbentuk
pada gel merupakan ekspresi dari kompleks antigen-antibodi yang menunjukkan
bahwa ECP bersifat imunogenik. Sifat spesifik dari ECP terlihat dari tidak
terbentuknya endapan putih antara antiserum yang berasal dari isolat 3 dengan
ECP yang berasal dari isolat 5, begitu juga sebaliknya tidak terbentuk endapan
putih antara antiserum yang berasal dari isolat 5 dengan ECP yang berasal dari
isolat 3.
Berdasarkan pengujian secara in vivo diperoleh nilai perlindungan relatif
(relative percent survival/RPS) yang berbeda untuk isolat 3 dan isolat 5 (Tabel 5).
Uji tantang yang dilakukan pada perlakuan menggunakan bakteri sejenis dengan
kepadatan 2 x 105 CFU/ml. Nilai RPS untuk isolat 3 adalah 60% dan isolat 5
adalah 68%. Sebagai data pendukung terhadap perubahan status kesehatan ikan
sebelum dan setelah divaksin, maka dilakukan analisa gambaran darah yang
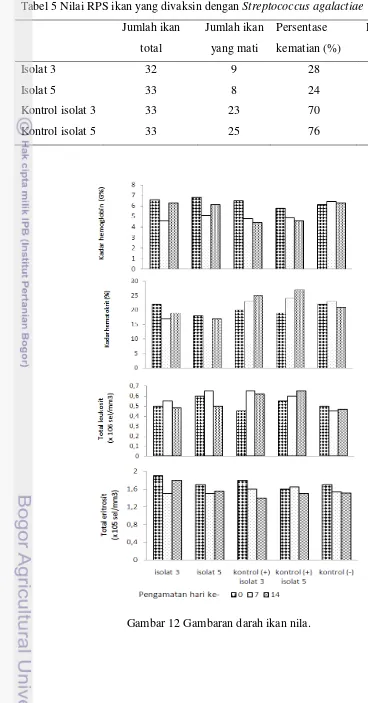
disajikan pada Gambar 12. a
19
Tabel 5 Nilai RPS ikan yang divaksin dengan Streptococcus agalactiae
Jumlah ikan
total
Jumlah ikan
yang mati
Persentase
kematian (%)
RPS
(%)
Isolat 3 32 9 28 60
Isolat 5 33 8 24 68
Kontrol isolat 3 33 23 70
Kontrol isolat 5 33 25 76
20
Berdasarkan Gambar 12, perubahan jumlah total eritrosit terjadi setelah 7
hari infeksi. Untuk ikan yang telah divaksin maupun ikan kontrol baik isolat 3 dan
isolat 5 secara umum mengalami penurunan jumlah eritrosit. Pada hari ke 14
setelah infeksi ikan yang telah divaksin mengalami peningkatan jumlah eritrosit
dibandingkan pada pengamatan hari ke7, sedangkan ikan kontrol (+) sebaliknya
dimana jumlah eritrosit tetap lebih kecil dari pada hari ke-7. Perubahan jumlah
total leukosit juga terjadi secara fluktuatif dimana trend yang ditunjukkan
merupakan kebalikan dari jumlah total eritrosit. Pada hari ke-7 setelah infeksi,
terjadi peningkatan jumlah total leukosit secara keseluruhan dibandingkan pada
hari ke-0. Perbedaan terjadi setalah 14 hari infeksi, dimana total leukosit pada
ikan yang divaksin mengalami penurunan sedangkan pada ikan kontrol (+) jumlah
total leukosit masih tinggi dibandingkan dengan hari ke-7. Kadar hemoglobin dan
kadar hematokrit juga memiliki trend yang berkebalikan untuk ikan kontrol (+),
penurunan kadar hemoglobin dan hematokrit pada hari ke-7 dan peningkatan
kembali nilai keduanya setelah hari ke-14 pada ikan yang telah divaksin tidak
diikuti oleh ikan kontrol (+). Pada ikan kontrol (+), terus terjadi penurunan nilai
hemoglobin dan kenaikan hematokrit pada hari ke-14 setelah uji tantang.
4.2 Pembahasan
Streptococcus agalactiae merupakan bakteri penyebab penyakit
streptococcosis atau meningoencephalitis pada ikan nila (Evans et al. 2008).
Infeksi pada otak ikan menyebabkan terganggunya keseimbangan dan
menimbulkan kelainan pada organ mata. Akibat dari infeksi tersebut kematian
pada ikan dapat terjadi baik secara akut ataupun kronis. Dari hasil karakteristik
bakteri uji, diperoleh bahwa bakteri S. agalactiae yang digunakan adalah tipe non
hemolitik. ECP merupakan salah satu faktor virulensi S. agalactiae dan tipe non
hemolitik diduga sebagai tipe yang lebih virulen (Hardi 2011). Berdasarkan
kemampuannya melisis sel darah merah, Streptococcus dibagi menjadi tiga
kelompok yaitu alpha hemolitik, beta hemolitik dan non hemolitik (Bullock
1981). Pada ikan, telah diisolasi tipe alpha hemolitik (Minami et a1. 1979), beta
hemolitik (Minami et al. 1979; Boomker et a1. 1979; Robinson and Meyer 1966),
21
osmolaritas lebih rendah dari pada osmolaritas eritrosit mengakibatkan eritrosit
akan terlisis ketika terpapar hemolisin (Dellmann 1989). Sebagai bakteri
septikemia, Streptococcus agalactiae menyebar melalui pembuluh darah. Eldar et
al. (1994) menemukan bakteri S. agalactiae tipe non hemolitik menyebabkan
septikemia dan meningoencephalitis pada ikan nila di Israel.
Sebagai bakteri patogen, S. agalactiae memiliki faktor virulensi untuk
menginfeksi inang. Salah satu faktor virulensinya adalah kandungan toksin yang
merupakan hasil metabolisme atau sering disebut produk ekstraselular (ECP).
Sebagai eksotoksin ECP bersifat imunogenik dengan target biokimia dari toksin
tersebut terletak pada proses intraseluler, komponen membran ataupun
neurotransmitter. Eksotoksin biasanya disekresikan oleh bakteri hidup selama fase
pertumbuhan eksponensial. Umumnya, strain bakteri yang patogen menghasilkan
toksin yang virulen. Toksin protein bakteri Streptococci merupakan zat antigenik
yang kuat dan bekerja secara luas serta menyebabkan kematian dengan gejala
yang tidak spesifik seperti nekrosis pada jaringan (Woolf 2000). Berdasarkan
analisa SDS-PAGE diperoleh berat molekul yang berbeda dari masing-masing
isolat. Menurut Pasnik et al. (2005) kandungan protein pada ECP S. agalactiae
yang digunakan sebagai vaksin pada ikan berkisar antara 47-75 KDa. Hardi
(2011) menyatakan bahwa berat molekul protein S. agalactiae tipe non-hemolitik
yang dibiakkan selama 72 jam pada media BHI adalah 62,3 KDa; 55,8 KDa; dan
51,8 KDa. Isolat 3 yang mengandung 7 jenis pita protein diduga bersifat
imunogenik karena memiliki 3 jenis pita dengan berat molekul berkisar 47-75
KDa, begitu pula dengan isolat 5 yang memiliki 2 jenis pita protein dengan berat
molekul berkisar 47-75 KDa.
Berdasarkan hasil penelitian, ECP bersifat toksik pada ikan nila dengan
nilai LD50 untuk isolat 3 adalah 633,9 µg/Kg dan isolat 5 adalah 685,4 µg/Kg.
Perbedaan nilai LD50 dari kedua isolat diduga akibat konsentrasi protein ECP
yang berbeda. Beberapa kajian menunjukkan ECP diduga menjadi salah satu
faktor virulensi bakteri dan dapat menyebabkan timbulnya penyakit atau
kematian. Kawahara et al. (1990) melakukan fraksinasi terhadap ECP Aeromonas
salmonicida dan menentukan nilai LD50 untuk salmolisin adalah >559 µg/Kg
22
menyatakan bahwa nilai LD50 dari ECP Mycobacterium spp yang disuntikan pada
ikan nila dan ikan rainbow trout adalah > 400 µg/ekor. Gejala klinis yang
ditimbulkan akibat infeksi ECP pada ikan nila hampir sama dengan gejala klinis
yang ditimbulkan akibat infeksi langsung dari bakteri. Kelainan organ mata,
kehilangan keseimbangan berenang dan penurunan nafsu makan terjadi setelah
injeksi yang dilakukan secara intraperitoneal pada ikan nila. Protein ECP yang
diduga mengandung toksin juga diujikan secara in vitro pada sel limfosit. Limfosit
merupakan salah satu sel utama yang memediasi respon imun pada tubuh ikan
(Blaxhall dan Sheard 1984). Kerusakan yang terjadi pada limfosit
mengindikasikan bahwa protein ECP mampu merusak mekanisme pertahanan
tubuh. Hal tersebut juga menjelaskan tentang proses patogenesis pada tingkat
seluler dimana ECP bekerja secara intraseluler. Mekanisme masuknya ECP ke
dalam limfosit dapat terjadi melalui dua cara. Alternatif pertama yaitu secara
langsung dimana subunit ECP berikatan dengan reseptor spesifik pada limfosit
dan menginduksi pembentukan pori pada membran dan selanjutnya ECP masuk
ke dalam sel. Alternatif kedua yaitu ECP mengikat limfosit, kemudian subunit
ECP masuk ke dalam sel melalui mekanisme endositosis reseptor-mediated
(RME). ECP dinetralisasi di dalam sel oleh endosome, akan tetapi keberadaan H+
Kerusakan yang terjadi setelah 3 jam pemaparan dengan ECP dan pola
kematian ikan yang terjadi secara kronik menjelaskan bahwa pada tingkat seluler
ECP mampu merusak sel dengan waktu yang singkat akan tetapi pada tingkat
individu yang lebih kompleks ECP hanya menyebabkan kematian bertahap. Pada di dalam endosome membantu subunit ECP terpisah. Subunit yang terpisah
tersebut bekerja sesuai fungsinya, di mana salah satu subunit tetap berada dalam
limfosit dan subunit lainnya keluar ke permukaan limfosit (Kenneth 2009).
Walaupun persentase kerusakan yang ditimbulkan setelah 3 jam pemaparan
dengan ECP berbeda antara kedua isolat, tetapi hal tersebut selaras dengan
semakin meningkatnya konsentrasi protein ECP dan lama waktu pemaparan,
maka kerusakan yang terjadi pada limfosit semakin tinggi. Secara visual
kerusakan pertama kali terjadi pada bagian sitoplasma sel kemudian diikuti
23
tingkat individu, ECP yang masuk ke dalam tubuh ikan mendapatkan perlawanan
imunitas baik secara humoral maupun secara seluler.
Selain bersifat toksik, kajian tentang sifat imunogenik protein ECP S.
agalactiae juga dilakukan. Berdasarkan pengujian imunodifusi terlihat bahwa
protein ECP bersifat imunogenik dan memiliki sifat proteksi spesifik bio-tipe. Hal
yang sama juga dinyatakan oleh Hardi (2011) bahwa pembentukan kompleks
antigen-antibodi hanya terbentuk dari isolat yang sama. Presipitasi kompleks ini
terjadi bila konsentrasi antigen dan antibodi ekuivalen dan dapat memberntuk
struktur besar makro molekul yang saling berkait sehingga menyebabkan
kekeruhan yang lebih dibandingkan jika dalam larutan itu hanya terdapat antibodi
atau antigen saja (kesetimbangan antigen-antibodi). Karena memiliki sifat yang
imunogenik pengembangan vaksin untuk memproteksi ikan nila dari serangan
bakteri ini dapat ditindaklanjuti. Inaktifasi ECP dengan neutral buffer formalin
3% untuk dijadikan kandidat vaksin bisa diterapkan. Efikasi vaksin ECP yang
memiliki nilai RPS sebesar 60% untuk isolat 3 dan 68% untuk isolat setelah diuji
tantang dengan kepadatan bakteri 2 x 105 CFU/ml, menunjukkan vaksin tersebut
efektif untuk diterapkan. Ellis (1988) menyatakan bahwa, suatu vaksin dikatakan
efektif apabila nilai RPS pada saat pengujian efikasi vaksin memiliki nilai >50%.
Status kesehatan ikan yang diamati dari gambaran darah menjelaskan pada hari
ke-7 setelah uji tantang kondisi fisiologi ikan terganggu akibat infeksi bakteri.
Penurunan jumlah eritrosit dan kadar hemoglobin serta meningkatnya jumlah
leukosit menunjukkan bahwa ikan sedang mengalami infeksi dan tubuh ikan
mengantisipasi kondisi tersebut dengan memproduksi leukosit lebih banyak
sebagai respon imunitas. Pada hari ke-14 sangat terlihat perbedaan kondisi
kesehatan ikan yang divaksin dengan ikan kontrol. Tahapan pemulihan kondisi
tubuh ikan sebagai upaya homeostatis dapat dilihat dari peningkatan jumlah
eritrosit dan kadar hemoglobin serta penurunan jumlah leukosit. Sedangkan pada
ikan kontrol penurunan jumlah eritrosit dan peningkatan jumlah leukosit tetap
terjadi. Secara keseluruhan dapat dikatakan bahwa vaksin ECP yang diberikan
24
V. SIMPULAN DAN SARA
N5.1 Simpulan
Protein produk ekstraseluler Streptococcus agalactiae tipe non hemolitik
dapat menyebabkan penyakit streptococcosis pada ikan nila pada konsentrasi
protein minimum terlarut 56,75 ppm atau setara dengan 283 µg/Kg untuk isolat 3
dan 81,75 ppm atau setara dengan 408 µg/Kg untuk isolat 5. ECP dapat
dimanfaatkan sebagai kandidat vaksin untuk memproteksi ikan nila terhadap
penyakit streptococcosis dengan nilai proteksi relatif 60% untuk isolat 3 dan 68%
untuk isolat 5.
5.2 Saran
Untuk mengetahui protein ECP yang berperan langsung dalam toksisitas
dan imunogenisitas pada ikan nila, perlu dilakukan pengkajian terhadap
25
DAFTAR PUSTAKA
Anderson DP, Siwicki AK. 1995. Basic haematology and serology for fish health programs. Paper presented in 2nd
Bercovier H, Ghittino C, Eldar A. 1997. Immunization with bacterial antigens: infections with streptococci and related organism. Development in biological standart. 90: 153-160.
symposium on disease in Asia aquaculture. Aquatic animal health and the environment. Phuket, Thailand. 1993. hlm 17.
Blaxhall PC, Sheard PR. 1985. Preliminary investigation of the characteristics of fish lymphocytes separated on a Percoll discontinuous gradient. Journal of fish biology. 26: 209-216.
Blaxhall PC, KW Daisley. 1973. Routine haematological methods for used with fish blood. Journal fish biology. 5: 577-581.
Boomker J, Imes GD, Cameron CM, Naude TW, Schoonbee HJ. 1979. Trout mortalities as a result of Streptococcus infection. Journal of veterinary research.
Bullock GL. 1981. Streptococcal infection of fish. Us fish & wildlife publications. University of Nebraska Lincoln.
46:71-78.
Chen SC, Adams A, Richards RH. 1997. Extracelluler products from Mycobacterium spp. in fish. Journal of fish desease. 20: 19-25.
Dellmann HD. 1989. Veterinary histology. Penerjemah: Hartono R. Universitas Indonesia Press. 297.
Eldar A, Bejerano Y, Livoff A, Horovitez A, Bercovier H. 1997. Development and efficacy of a vaccine against Streptococcus iniae infection in farmed rainbow trout. Veterinary immunology and immunopathology.
Eldar A, Ghittino C. 1999. Lactococcus garviae dan Streptococcus iniae infection in rainbow trout, Oncorhynchus mykiss: similar but different diseases. Diseases of aquatic organisms. 36 : 227-231.
56 : 175-183.
Eldar A, Bejerano Y, Bercovier H. 1994. Streptococcus shiloi and Streptococcus difficile: two new streptococcal species causing meningoenchephalitis in fish. Current microbiology 28:139-143.
Elliot JA, Facklam RR, Richter CB. Whole-cell protein patterns of nonhemolytic group B, type Ib, streptococci isolated from humans, mice, cattle, frogs and fish. Journal of clinical microbiology 28: 628-630.
Ellis AE. 1988. Fish vaccination. London: Academic Press Ltd.
Evans JJ, Klesius PH, Bohnsack JF, Pasnik DJ, Garcia JC, Whiting AA, Shoemaker CA. 2008. Genomic diversity of Streptoccocus agalactiae isolates from multiple hosts and their infectivity in nile tilapia. Proceedings of the 8th International Symposium on Tilapia in Aquaculture. Cairo, Egypt 12-14 Oktober 2008. 2: 1199-1209.
26
Evans JJ, Klesius PH, Shoemaker CA. 2006. An overview of Streptococcus in warm water fish. Aquaculture health international. 7: 10-14.
Glaser P, Rusniok C, Buchrieser C, Chevalier F, Frangeul L, Msadek T, Zouine M, Couvé E, Lalioui L, Poyart C, Trieu-Cuot P, Kunst F. 2002.
Molecular microbiology. 45:1499–1513.
Hardi EH. 2011. Kandidat vaksin potensial Streptococcus agalactiae untuk pencegahan penyakit streptococcosis pada ikan nila Oreochromis niloticus [disertasi]. Bogor: Program Pascasarjana, Institut Pertanian Bogor.
Hoshina T, Sano T, Morimoto Y. 1958. A Streptococcus pathogenic to fish. Journal of Tokyo university of fisheries. 44: 57-68.
Kawahara E, Oshima S, Nomura S. 1990. Separation of lymphocytes from the peripheral blood of coho salmon Oncorhynchus kisutch. Nippon suisan gakkaishi 56: 363.
Kawahara E, Oshima S, Nomura S. 1990. Toxicity and immunogenicity of Aeromonas salmonicida extracellular products to salmonid. Journal of fish deseases. 13: 495-503.
Kenneth T. 2009. The mechanism of bacterial pathogenicity. [terhubung berkala][14 Nov 2011].
Klesius PH, Shoemaker CA, Evans JJ. 2000. Vaccination: A health management practice for preventing diseases caused by Streptococcus in tilapia and other cultured fish. Fifth international symposium on tilapia aquaculture. Rio de Janeiro, Brazil Tanggal 3-7 September 2000. 558-564.
KKP. 2010. Nila, andalan produk perikana Maret 2010].
Kong F, Gowan S, Martin D, James G, Gilbert GL. 2002. Molecular profiles of group b streptococcal surface protein antigen Genes: relationship to molecular serotypes. Journal of clinical microbiology. 40 : 620–626
Lindahl G, Carlemalm MS, Areschoug T. 2005. Surface Proteins of Streptococcus agalactiae and Related Proteins in Other Bacterial Pathogens. Clinical microbiology. 18:102–127.
Minami T, Nakamura M, Ikeda Y, Ozaki H. 1979. A beta-hemolytic Streptococous isolated from cultured yellowtail. Fish pathology. 14: 33-38 Pasaribu FH, Dalimunthe N, Poeloengan M. 1990. Pengobatan dan pencegahan
penyakit ikan bercak merah. Prosiding Seminar Nasional II Penyakit Ikan dan Udang 16-18 Januari. Badan Penelitian dan Pengembangan Pertanian: 143-152.
Pasnik DJ, Evans JJ, Panangala VS, Shelby RA,. 2005. Antigenicity of Streptococcus agalactiae extracellular products and vaccine efficiency. Journal of fish disease 28: 205-212.
27
Rasheed V, Plumb J. 1984. Pathogenicity of a non-hemolytic group B Streptococcus sp. In gulf killfish, Fundulus grandis (Baird and Girard). Aquaculture 37: 97-105.
Reed, LJ,Muench H. (1938). A simple method of estimating fifty per cent endpoints. American journal of hygiene 27: 493
Robinson JA, Meyer FP. 1966. Streptococcal fish pathogen. Journal of bacteriology. 92:512.
Segura M, Gottschalk M. 2004. Extracellular Virulence Factors of Streptococci Associated With Animal Diseases. Frontiers in bioscience 9: 1157-1188. Sheehan B. 2009. Streptococcosis in tilapia: A more complex problem than
expected?. Proceeding of managing streptococcus in warmwater Fish. Veracruz, Mexico 25 September 2009. 3: 9-14.
Slotved HC, Kong F, Lambertsen L, Sauer S, Gilbert GL. 2007. Serotype IX, a Proposed New Streptococcus agalactiae Serotype. Journal of clinical microbiology. 45: 2929–2936.
Wedemeyer GA, Yasutake WT. 1977. Clinical methods for the assessment of the effect on environmental stress on fish health. Journal fish and wildlife service. 89: 1-17.
Wibawan IWT, Lammler C, Pasaribu FM. 1992. Role of hydrophobic surface proteins in mediating adherence of group B streptococci to epithelial cells. Journal of general microbiology. 138: 1237-1242.
Williams ML, Azadi P, Lawrence ML. 2003. Comparison of cellular and extracellular products expressed by virulent and attenuated strains of Edwardsiella ictaluri. Journal of aquatic animal health 15:264 – 273. Woolf N. 2000. Cell, tissue and disease the basis of pathology 3th
Zahra AS. Padilah B, Azila A, Rimatulhana R, Shahidan H. 2008. Multiple streptococcal species infection in cage-cultured red tilapia but showing similar clinical signs. Diseases in asian aquaculture VI. Fish health section, asian fisheries society, Manila, Philippines. 550.
28
Lampiran 1 Metode karakterisasi bakteri Streptococcus agalactiae
Pewarnaan Gram
a) Gelas objek terlebih dahulu dibersihkan dengan alkohol 70 % kemudian diberi label.
b) Pada permukaan gelas objek diteteskan 1 tetes akuades steril.
c) Isolat bakteri uji diambil dengan jarum Őse steril, kemudian dicampurkan dengan akuades dan diulas merata pada permukaan gelas objek.
d) Fiksasi udara terhadap isolat dilakukan dengan melewatkan preparat di atas api (jarak 15 cm) beberapa kali sampai terlihat kering.
e) Larutan crystal violet diteteskan pada preparat sampai merata dan didiamkan selama 1 menit
f) Preparat dicuci dengan air mengalir, kemudian dikeringanginkan.
g) Larutan iodine lugol diteteskan pada preparat sampai merata dan didiamkan selama 1 menit.
h) Preparat dicuci dengan air mengalir, kemudian dikeringanginkan.
i) Larutan alkohol aseton diteteskan pada preparat sampai merata dan didiamkan sampai maksimal 30 detik.
j) Preparat dicuci dengan air mengalir, kemudian dikeringanginkan
k) Larutan safranin diteteskan pada preparat sampai merata dan didiamkan selama 2 menit.
l) Preparat dicuci dengan air mengalir, kemudian dikeringanginkan.
m) Pengamatan bakteri hasil pewarnaan Gram dilakukan dengan menggunakan mikroskop.
n) Sifat bakteri Gram positif ditandai dengan sel bakteri berwarna ungu. o) Sifat bakteri Gram negatif ditandai dengan sel bakteri berwarna merah.
Katalase
a) Biakan bakteri diambil dengan jarum Őse secara aseptis kemudian dioleskan pada gelas objek, kemudian ditambahkan 1 tetes larutan H2O2
b) Bakteri bersifat katalase positif bila menghasilkan gelembung udara dalam waktu kurang dari 10 detik.
3 %.
Oksidase
a) Kertas saring yang telah disiapkan ditetesi dengan pereaksi oksidase. b) Isolat bakteri diambil dengan menggunakan jarum Ősedan selanjutnya
digoreskan pada kertas saring yang sudah diberi pereaksi oksidase.
29
Oksidatif-Fermentatif
a) Persiapan awal dilakukan dengan menyediakan 2 tabung reaksi yang berisi media O/F basal.
b) Isolat bakteri diambil dengan jarum Őse lurus steril kemudian diinokulasikan ke dalam tabung yang berisi media O/F basal dengan cara ditusukkan.
d) Salah satu tabung diisi dengan parafin cair steril hingga ketinggian 1 cm di atas permukaan media O/F basal, sedangkan tabung lainnya tanpa parafin cair. e) Preparat kemudian diinkubasikan pada suhu 25 °C - 30 °C selama 12 jam - 24
jam.
f) Reaksi negatif jika tidak ada perubahan warna pada kedua tabung reaksi. g) Reaksi oksidatif positif jika terjadi perubahan warna media pada tabung tanpa
parafin dari hijau ke kuning.
h) Reaksi fermentatif positif jika terjadi perubahan warna dari hijau ke kuning pada tabung yang tertutup parafin.
Motilitas dengan media semi solid
a) Media yang digunakan adalah media semi solid (SIM atau MIO).
b)Isolat bakteri diambil dengan jarum Őse lurus dan diinokulasikan dengan cara menusukkan pada media.
c) Inkubasi dilakukan pada suhu 28 °C selama 12 jam - 24 jam.
d)Reaksi positif ditandai dengan pertumbuhan bakteri yang menyebar dan reaksi negatif ditandai pertumbuhan bakteri yang tidak menyebar.
Produksi asam dari D-mannitol
a) Media yang digunakan adalah media phenol red broth base yang sudah ditambahkan dengan D-mannitol.
b) Isolat bakteri diambil dengan jarum Őse dan diinokulasikan ke dalam media c) Inkubasi dilakukan pada suhu 25 °C - 30 °C selama 12 jam - 24 jam.
d) Reaksi positif jika terbentuk warna kuning pada agar dan negatif bila tidak terjadi perubahan warna.
Aktivitas hemolitik
a) Media yang digunakan adalah media blood agar yang mengandung 5% darah domba steril.
b) Selanjutnya bakteri uji digoreskan pada media.
c) Inkubasi dilakukan pada suhu 25 °C - 30 °C selama 24 jam.
d) Reaksi positif alpha haemolisis jika terdapat zona kehijau-hijauan disekitar daerah koloni reaksi positif betha haemolisis jika terdapat zona bening disekitar daerah koloni.
30
Lampiran 2 Metode pengukuran konsentrasi protein dan penentuan berat molekul ECP Streptococcus agalactiae
Perhitungan konsentrasi protein dengan metode Bradford (1976)
a) Larutan standar yang digunakan adalah BSA (bovine serum albumin) dan BHIB (brain heart infusion broth) steril dengan konsentrasi 0, 25, 50, 75, 100, 200 dan 300 µg BSA/ml BHIB
b) Penambahan larutan Bradford kedalam masing-masing tabung uji dilakukan setelah larutan standar siap sebanyak 5 ml.
c) Semua larutan yang ada ditabung dihomogenkan dengan alat vortex dan dibiarkan antara lima belas menit sampai satu jam.
d) Satu per satu tabung selanjutnya dimasukkan ke dalam spektrofotometer untuk dibaca absorbansinya. Panjang gelombang yang digunakan adalah 595 nm. e) Kurva hubungan antara absorban dengan konsentrasi protein dalam tabung
beserta persamaan garisnya untuk selanjutnya dijadikan kurva standar.
f) Untuk larutan sampel protein, dilakukan hal yang sama dengan larutan standar yaitu dipipet ke dalam tabung reaksi dan ditambahkan reagent Bradford sebanyak 5 ml kemudian diaduk dan didiamkan selama lima belas hingga enam puluh menit dan selanjutnya diukur absorbansinya.
g) Pengukuran absorbansi pada larutan sampel diulang sebanyak dua kali. Nilai absorban yang diperoleh digunakan untuk menentukan konsentrasi sampel. h) Konsentrasi sampel ditentukan dengan memasukkan nilai absorban ke
persamaan garis dari kurva standar.
Analisa SDS-PAGE
a) Untuk gel uji digunakan gel acrylamide dengan konsentrasi 10% untuk gel pemisah dan 4% untuk gel penahan.
b) Gel dicetak pada gel caster, lapisan bawah adalah gel pemisah kemudian tambahkan gel penahan setelah itu sisipkan sisir cetakan kemudian diamkan selama 10 menit.
c) Setelah gel mengeras, sisir cetakan ditarik dan kemudian dimasukkan sampel ke masing-masing sumur yang telah terbentuk.
31
e) Pewarnaan perakdilakukan dengan cara merendam gel ke dalam larutan fiksasi (25% methanol, 12% Asam asetat) selama 1 jam, kemudian direndam dalam etanol 50% selama 20 menit. Setelah itu direndam kembali ke dalam etanol 30% selama 20 menit sebanyak 2 kali. Selanjutnya gel direndam (0,1 gram Na2S2O3.5H2O) dalam 500 ml akuades selama 1 menit, dibilas dengan akuades 20 detik dan diulangi sebanyak 3 kali. Selanjutnya dicelupkan ke dalam larutan perak nitrat (0,4 g AgNO3 dicampurkan dengan 70µm formaldehid dalam 200 ml akuades) selama 30 menit. Gel kembali dibilas dengan akuades selama 2 x 20 detik kemudian dicelupkan kedalam larutan yang terdiri dari 15 g Na2CO3 + 120 ml formaldehid. Setelah terlihat band hitam, saat itulah reaksi dengan larutan fiksasi dihentikan.
32
Lampiran 3 Metode pengujian toksisitas produk ekstraseluler Streptococcus agalactiae
Pemisahan limfosit dari darah ikan nila (Blaxhall dan Sheard 1985) dengan Percoll yang dimodifikasi pelarut sukrosa 0,25 M
a) Larutan percoll yang digunakan memiliki konsentrasi yaitu 30%, 40% dan 50%.
b) Darah ikan diambil dengan syringe yang telah dibilas dengan anti koagulan. c) Larutan Percoll dimasukkan kedalam tabung corning masing-masing 2 ml
untuk setiap konsentrasi.
d) Lapisan pertama pada tabung corning adalah percoll 50%, kedua percoll 40%, ketiga percoll 30% dan terakhir adalah darah ikan nila.
e) Segera setelah semua larutan dimasukkan, dilakukan sentrifugasi pada kecepatan 4500 rpm selama 20 menit.
f) Lapisan yang terbentuk setelah sentrifugasi diambil dan diulas dengan pewarnaan Giemsa 6,6% (direkomendasikan 10%) yang sebelumnya telah difiksasi dengan methanol 70%.
g) Semua larutan sebelum dan sesudah sentrifugasi diukur gradient density-nya dengan menggunakan refraktometer.
h) Pengamatan dilakukan dengan mikroskop pada pembesaran 1000x
Cytophatic effects
a) Limfosit terlebih dahulu dipisahkan dari sel darah lainnya.
b) Pencampuran ECP dan limfosit dilakukan pada perbandingan 1:1. c) Limfosit dipaparkan dengan ECP selama 0, 30, 60 dan 180 menit d) Preparat ulas limfosit dibuat setiap waktu pemaparan selesai.
e) Sebelum diwarnai dengan Giemsa 6,6% dilakukan fiksasi dengan methanol 70%.
f) Pegamatan dilakukan dengan mikroskop pada perbesaran 1000x.
g) Parameter yang diamati adalah persentase jumlah kerusakan dan kerusakan morfologi (sitoplasma dan inti sel) limfosit setelah terpapar ECP.