PERBEDAAN KANDUNGAN SENYAWA RESIN GAHARU
(
Aquilaria malaccensis
) HASIL INOKULASI
PADA TINGKAT SEMAI DAN POHON
MEMET SLAMET PURNAMA
DEPARTEMEN SILVIKULTUR FAKULTAS KEHUTANAN INSTITUT PERTANIAN BOGOR
PERNYATAAN MENGENAI SKRIPSI DAN
SUMBER INFORMASI SERTA PELIMPAHAN HAK CIPTA
Dengan ini saya menyatakan bahwa skripsi berjudul Perbedaan Kandungan Senyawa Resin Gaharu (Aquilaria malaccensis) Hasil Inokulasi pada Tingkat Semai dan Pohon adalah benar karya saya dengan arahan dari komisi pembimbing dan belum pernah diajukan dalam bentuk apa pun kepada perguruan tinggi atau lembaga manapun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir skripsi ini.
Dengan ini saya melimpahkan hak cipta dari karya tulis saya kepada Institut Pertanian Bogor.
Bogor, Desember 2013
Memet Slamet Purnama
ABSTRAK
MEMET SLAMET PURNAMA. Perbedaan Kandungan Senyawa Resin Gaharu (Aquilaria malaccensis) Hasil Inokulasi pada Tingkat Semai dan Pohon. Dibimbing oleh ULFAH JUNIARTI.
Gaharu merupakan salah satu komoditas hutan yang selain dapat dimanfaatkan kayunya, sering diambil resinnya yang bernilai sangat mahal. Salah satu jenis pohon gaharu yang berpotensi untuk membentuk gubal dengan mutu yang tinggi adalah
Aquilaria malaccensis. Informasi mengenai bahan-bahan kimia yang terkandung dalam gaharu penting untuk pengembangan produk ini, sehingga penelitian mengenai analisis kandungan resin pada gaharu perlu dilakukan. Tujuan penelitian ini adalah untuk mengamati perubahan senyawa resin pada semai dan pohon gaharu yang diinokulasi cendawan pembentuk gaharu. Induksi cendawan Fusarium solani dan Fusarium oxysporum dilakukanpada batang semai dan pohon A. malaccensis,kemudian kandungan
kimianya dianalisis dengan menggunakan gas chromatography mass
spectrophotometry (GCMS). Hasil penelitian menunjukkan senyawa konstituen gaharu terbentuk pada seluruh perlakuan. Terdapat 7 jenis senyawa konstituen gaharu yang dihasilkan isolat F. solani pada semai gaharu dengan konsentrasi relatif isolat asal Jambi sebesar 16.38% dan isolat asal Gorontalo sebesar 13.87%. Isolat F. oxysporum pada pohon gaharu menghasilkan 10 jenis senyawa konstituen gaharu dengan konsentrasi relatif sebesar 13.06%.
Kata kunci: Aquilaria malaccensis, Fusarium oxysporum, Fusarium solani, resin gaharu
ABSTRACT
MEMET SLAMET PURNAMA. Differences in Resin Chemical Components Obtained from Inoculated Agarwood (Aquilaria malaccensis) Seedlings and Trees. Supervised by ULFAH JUNIARTI
Agarwood is one of forest tree species that can be harvested for its timber and resin, which has high price. One of agarwood tree species which has ability to form agarwood with the high-quality is Aquilaria malaccensis. Information on chemicals contained in agarwood is important for the development of this product that research on chemical content of agarwood resin needs to be done. The purpose of this research is to observe changes in resin components of agarwood inoculated with agarwood inducing fungi. Induction of Fusarium solani and Fusarium oxysporum fungi was done on the stem of A. malaccensis seedlings and trees, and then the chemical components of their resins were analyzed using GCMS. The result showed that all treatments were successfully induced agarwood formation. There are 7 main chemical compounds of agarwood produced by F. solani inoculated seedlings with relative concentrations of 16.38% for isolates from Jambi, and 13.87% for isolate from Gorontalo. Innoculation of
F. oxysporum on trees generated 10 agarwood main compounds with relative concentration of 13.06%.
Skripsi
sebagai salah satu syarat untuk memperoleh gelar Sarjana Kehutanan
pada
Departemen Silvikultur
PERBEDAAN KANDUNGAN SENYAWA RESIN GAHARU
(
Aquilaria malaccensis
) HASIL INOKULASI
PADA TINGKAT SEMAI DAN POHON
MEMET SLAMET PURNAMA
DEPARTEMEN SILVIKULTUR FAKULTAS KEHUTANAN INSTITUT PERTANIAN BOGOR
Judul Skripsi : Perbedaan Kandungan Senyawa Resin Gaharu (Aquilaria malaccensis) Hasil Inokulasi pada Tingkat Semai dan Pohon
Nama : Memet Slamet Purnama NIM : E44090037
Disetujui oleh
Dr Ir Ulfah Juniarti, MAgr Pembimbing
Diketahui oleh
Prof Dr Ir Nurheni Wijayanto, MS Ketua Departemen
PRAKATA
Puji syukur kehadirat Allah SWT atas segala rahmat dan ridho-Nya sehingga penulis dapat menyelesaikan skripsi ini yang berjudul “Perbedaan Kandungan Senyawa Resin Gaharu (Aquilaria malaccensis) Hasil Inokulasi pada Tingkat Semai dan Pohon”. Penelitian ini merupakan salah satu syarat dalam memperoleh gelar Sarjana Kehutanan pada Fakultas Kehutanan Institut Pertanian Bogor.
Penulis mengucapkan terima kasih kepada Ibu Dr Ir Ulfah Juniarti, MAgr selaku dosen pembimbing yang telah memberikan arahan dan bimbingan kepada penulis dalam pelaksanaan dan penyelesaian skripsi ini. Ungkapan terima kasih juga disampaikan kepada ayah, ibu, serta seluruh keluarga atas doa dan semangatnya. Selain itu, penghargaan penulis sampaikan kepada seluruh staf Laboratorium Mikrobiologi Hutan, Bapak Erdi Santosa, Bapak Yani, Bapak Babas beserta staf Laboratorium Instrumentasi dan Proksimat Terpadu Badan Penelitian dan Pengembangan Kehutanan, Bapak Gustan, Ibu Pudji, Bapak Slamet, dan Bapak Dadang. Terima kasih juga kepada teman-teman satu bimbingan (Fitri, Rai, Ayu), Artha, Erfan, Dewi, Rian, Oki, Dayat, Opik, Jamal, Khalid serta teman-teman Silvikultur 46 yang telah memberi semangat dan dukungannya kepada penulis.
Penulis menyadari bahwa skripsi ini masih jauh dari sempurna. Penulis mengharapkan kritik dan saran yang membangun dari pembaca dan semoga skripsi ini dapat bermanfaat bagi semua pihak.
Bogor, Desember 2013
DAFTAR ISI
DAFTAR TABEL iv
DAFTAR GAMBAR iv
DAFTAR LAMPIRAN iv
PENDAHULUAN 1
Latar Belakang 1
Tujuan 1
METODE 1
Waktu dan Lokasi Penelitian 1
Bahan dan Alat 2
Prosedur Penelitian 2
Tahap Persiapan 2
Induksi Pembentukan Gubal Gaharu 2
Pengamatan Gejala Infeksi 2
Analisis Kandungan Resin Gaharu 3
HASIL DAN PEMBAHASAN 4
Gejala Infeksi Cendawan 4
Perubahan Warna Kayu 5
Hasil Analisis Senyawa Kimia Gaharu 6
Gaharu Tingkat Semai 6
Gaharu Tingkat Pohon 7
Senyawa Pembentuk Gaharu 8
SIMPULAN DAN SARAN 13
Simpulan 13
Saran 13
DAFTAR PUSTAKA 13
LAMPIRAN 16
DAFTAR TABEL
1 Senyawa-senyawa kimia berdasarkan beberapa referensi sebagai senyawa pertahanan tanaman dan terdeteksi pada gaharu tingkat semai
hasil inokulasi 10
2 Senyawa-senyawa kimia berdasarkan beberapa referensi sebagai senyawa pertahanan tanaman dan terdeteksi pada gaharu tingkat pohon
hasil inokulasi 10
3 Jumlah senyawa konstituen gaharu yang terdeteksi untuk seluruh
sampel 11
4 Jumlah senyawa berkarakter odorant yang terdapat pada seluruh sampel 12 5 Jumlah senyawa berkarakter odorant lain yang belum dikonfirmasi
sebagai konstituen gaharu 12
DAFTAR GAMBAR
1 Sampel semai gaharu yang digunakan: (a) setelah dilukai, dan (b)
diberikan pelet cendawan pembentuk gaharu 3
2 (a) Alat GCMS Shimadzu, dan (b) proses memasukkan sampel yang
dianalisis pada tabung helium 3
3 Gejala klorosis pada tanaman gaharu hasil induksi cendawan F. solani:
(a) asal Gorontalo, dan (b) asal Jambi 4
4 Perubahan warna kayu yang terjadi akibat isolat F. solani: (a) asal
Jambi, dan (b) asal Gorontalo 5
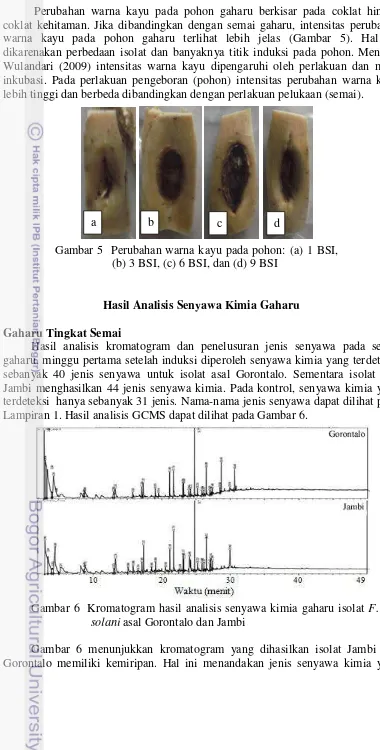
5 Perubahan warna kayu pada pohon: (a) 1 BSI, (b) 3 BSI, (c) 6 BSI, dan
(d) 9 BSI 6
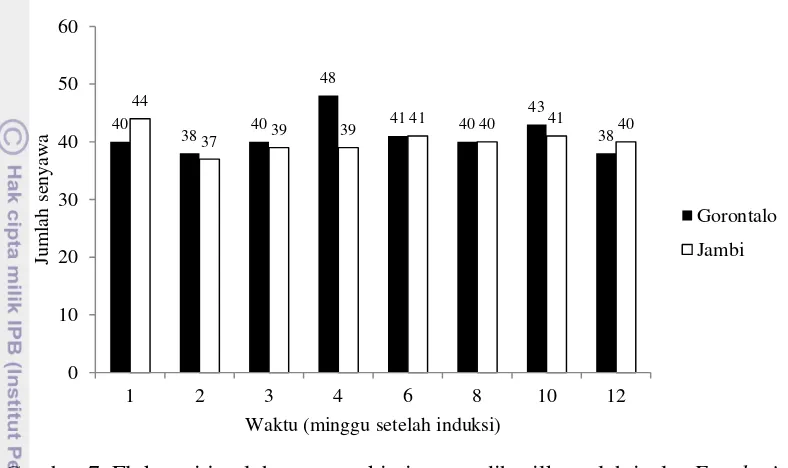
6 Kromatogram hasil analisis senyawa kimia gaharu isolat F. solani asal
Gorontalo dan Jambi 6
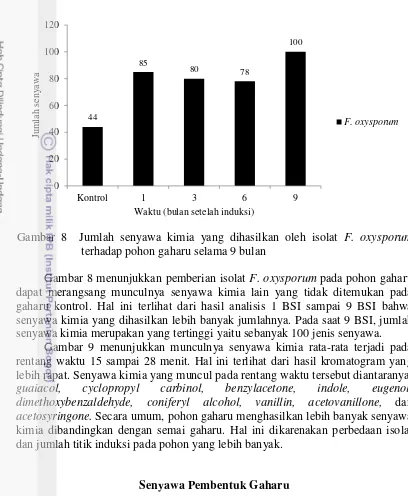
7 Fluktuasi jumlah senyawa kimia yang dihasilkan oleh isolat F. solani
asal Jambi dan Gorontalo terhadap semai gaharu selama 12 minggu 7 8 Jumlah senyawa kimia yang dihasilkan oleh isolat F. oxysporum
terhadap pohon gaharu selama 9 bulan 8
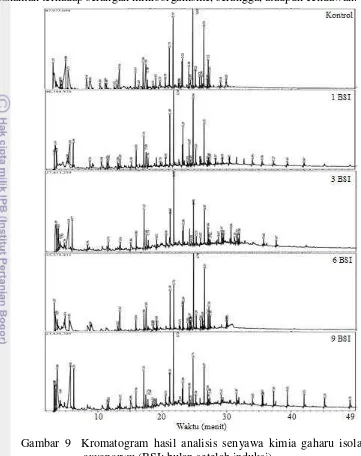
9 Kromatogram hasil analisis senyawa kimia gaharu isolat F. oxysporum 9
DAFTAR LAMPIRAN
1
PENDAHULUAN
Latar Belakang
Gaharu merupakan salah satu komoditas hutan yang selain dapat dimanfaatkan kayunya, sering diambil resinnya yang bernilai sangat mahal. Gaharu dihasilkan terutama oleh pohon-pohon dari famili Thymeleaeceae, genus
Aquilaria, Gyrinops, Gonystylus, Aetoxylon, Enkleia, Wikstroemia, dan
Dalbergia. Salah satu jenis pohon gaharu yang berpotensi untuk membentuk gubal dengan mutu yang tinggi adalah Aquilaria malaccensis (Hou 1960).
Resin gaharu diproduksi oleh pohon gaharu sebagai bentuk pertahanan terhadap suatu gangguan seperti infeksi cendawan. Mohamed et al. (2010) menemukan pembentukan gaharu yang wangi pada bekas luka yang disertai adanya miselium cendawan. Gejala umum akibat infeksi cendawan diantaranya terjadi perubahan warna pada daerah yang terinfeksi dan klorosis daun yang teramati beberapa hari setelah tanaman diinokulasi cendawan. Pada pohon gaharu yang terbentuk secara alami dan terinfeksi selama bertahun-tahun perubahan warna kayu terjadi hampir pada seluruh bagian kayu. Gejala klorosis daun tidak terlihat lagi, sehingga secara visual tanaman terlihat sehat (Barden et al. 2000).
Resin gaharu tergolong sesquiterpene dan derifat chromone (Shimada et al. 1986; Konishi et al. 2002; Yagura et al. 2003). Kandungan resin pada gaharu dapat menentukan seberapa baik kualitas gaharu tersebut. Semakin tinggi kandungan resin, maka semakin baik kualitas gaharunya. Informasi mengenai bahan-bahan kimia dalam gaharu penting untuk pengembangan produk ini, sehingga penelitian mengenai analisis kandungan resin gaharu perlu dilakukan.
Tujuan
Penelitian ini bertujuan untuk mengamati perubahan senyawa resin pada semai gaharu hasil inokulasi Fusarium solani dari minggu pertama sampai minggu keduabelas setelah induksi. Selain itu, untuk mengamati perubahan senyawa resin pada pohon gaharu hasil inokulasi Fusarium oxysporum dari bulan pertama sampai bulan kesembilan setelah induksi.
METODOLOGI
Waktu dan Lokasi Penelitian
2
senyawa resin gaharu dilakukan di Laboratorium Instrumentasi dan Proksimat Terpadu, Pusat Penelitian dan Pengembangan Kehutanan, Bogor.
Bahan dan Alat
Bahan yang digunakan untuk penelitian ini adalah gaharu jenis A. malaccensis, alkohol 70%, isolat Fusarium oxysporum, isolat Fusarium solani
asal Jambi dan Gorontalo. Bahan semai gaharu yang digunakan sebanyak 99 individu tanaman dengan tinggi rata-rata 40 cm, sedangkan pohon gaharu dengan tinggi rata-rata 7–8 meter diambil sebanyak 24 sampel kayunya yang merupakan hasil inokulasi Fusarium oxysporum. Alat-alat yang digunakan dalam penelitian ini adalah kapas, tissue, pisau/cutter, cawan petri, pinset, selotape, blender, dan mesin gas chromatography mass spectrophotometry (GCMS).
Prosedur Penelitian
Tahap Persiapan
Tahap persiapan yang dilakukan adalah sterilisasi alat dan persiapan bahan isolat. Sterilisasi alat dilakukan dengan mengolesi alat-alat dengan menggunakan alkohol 70%. Isolat F. solani yang berbentuk cendawan diblender agar terlarut dalam larutan pelet.
Induksi Pembentukan Gubal Gaharu
Induksi dilakukan dengan menempelkan masing-masing isolat F. solani asal Jambi dan Gorontalo pada 48 batang semai gaharu. Pertama, batang semai gaharu pada ketinggian 5–7 cm di atas permukaan tanah dilukai dengan menggunakan pisau/cutter sedalam sepertiga diameter batang (Gambar 1). Pelet cendawan F. solani ditempelkan pada batang tanaman menggunakan kapas yang kemudian dibalut dengan selotape. Isolat yang digunakan pada 22 sampel pohon gaharu adalah F. oxysporum asal Bontang, Kalimantan Timur. Batang utama pada ketinggian 0.3–0.5 m di atas permukaan tanah dilubangi dengan mata bor berukuran 8 mm pada kedalaman lubang maksimal ¼ diameter batang. Jarak antar lubang secara horizontal dan secara vertikal adalah 15 cm. Inokulan dimasukkan ke dalam lubang dibantu dengan kapas berisi agrosofsteril (gel).
Pengamatan Gejala Infeksi
3
Gambar 1 Sampel semai gaharu yang digunakan: (a) setelah dilukai, dan (b) diberikan pelet cendawan pembentuk gaharu
Analisis Kandungan Resin Gaharu
Analisis komposisi resin gaharu dilakukan menggunakan alat gas chromatography mass spectrophotometry (GCMS) secara pyrolysis (Gambar 2). Proses analisis menggunakan metode ionisasi serangan elektron (IE) pada kromatograf gas; kolom kapiler DB-5 ms (silika 60 mm × 0.25 mm × 0.25 m); Suhu kolom 50–280 °C pada laju 15 °C/menit. Kandungan dan komposisi suatu campuran senyawa dapat diketahui dengan cepat melalui analisis ini. Efektivitas isolat yang diinokulasikan pada penelitian ini dilakukan dengan membandingkan kandungan senyawa kimia batang yang tidak diinduksikan cendawan. Karakterisasi senyawa kimia yang terdeteksi ditentukan dari perkiraan nama senyawa.
Gambar 2 (a) Alat GCMS Shimadzu, dan (b) proses memasukkan sampel yang dianalisis pada tabung helium
Analisis pada semai gaharu dilakukan saat 1–4 minggu setelah induksi (MSI), 6 MSI, 8 MSI, 10 MSI, dan 12 MSI. Untuk mengatasi faktor keragaman antar individu, setiap sampel yang dianalisis merupakan gabungan dari 3 individu semai gaharu. Pada pohon gaharu, analisis dilakukan untuk sampel 1 bulan setelah induksi (BSI), 3 BSI, 6 BSI, dan 9 BSI. Untuk bahan analisis, dari batang utama gaharu diambil potongan kayu sebanyak ± 0.5 g yang kemudian dimasukkan ke dalam tabung helium. Proses analisis berlangsung selama 60 menit dan hasil yang diperoleh berupa data waktu munculnya senyawa, konsentrasi relatif, dan perkiraan nama senyawa.
a b
4
HASIL DAN PEMBAHASAN
Gejala Infeksi Cendawan
Inokulasi cendawan pada semai dan pohon gaharu dapat mempengaruhi kondisi fisik tanaman. Perubahan fisik ditunjukkan dengan klorosis daun sampai terjadinya gugur daun. Untuk semai gaharu, perubahan fisik mulai terlihat pada minggu pertama setelah inokulasi dengan adanya klorosis daun. Pada minggu kedua setelah inokulasi, beberapa semai gaharu daunnya terlihat kering seperti terbakar dan menggugurkan hampir seluruh daunnya. Di sisi lain, perubahan fisik pada pohon gaharu terlihat saat bulan pertama setelah inokulasi dengan gugurnya 30% tunas pucuk dan daun-daun pada pohon tanpa klorosis daun sebelumnya. Hal ini berbeda dengan gaharu kontrol yang tidak mengalami klorosis sampai akhir pengamatan. Secara umum, klorosis terjadi pada daun-daun yang letaknya di bawah dekat daerah induksi. Agrios (2004) dan Widyastuti (2009) menyatakan bahwa inokulasi cendawan dapat menyebabkan daun yang berada dekat dengan daerah induksi mengalami perubahan warna dari hijau menjadi kuning (klorosis).
Klorosis pada daun berhubungan dengan terganggunya ketersediaan unsur hara akibat adanya pelukaan. Ketersediaan unsur hara terganggu karena jalur distribusinya ke daun terhambat akibat pengeboran. Kekurangan hara tersebut menyebabkan daun menjadi kekurangan pigmen klorofil sehingga daun menjadi klorosis (Nieamann dan Visintini 2005). Selain itu, adanya inokulan juga menjadi penyebab klorosis. Hal ini diperkuat dengan pernyataan Agrios (2004) bahwa cendawan dapat menyebabkan klorosis dengan cara memanfaatkan nutrisi inang untuk perkembangan dan metabolismenya.
Pada minggu ketiga dan keempat setelah induksi, gejala klorosis semai gaharu tidak terlihat lagi. Daun-daun terlihat lebih hijau kembali. Hal ini diduga sebagai proses recover tanaman. Pada pohon, proses recover terlihat saat 3 bulan setelah induksi dengan berkurangnya gejala klorosis dan gugurnya daun-daun.
Gambar 3 Gejala klorosis pada tanaman gaharu hasil induksi cendawan F. solani: (a) asal Gorontalo, dan (b) asal Jambi
Semai gaharu memberikan respon yang berbeda terhadap infeksi cendawan
F. solani asal Jambi dan Gorontalo. Semai gaharu lebih tahan terhadap infeksi
5 isolat asal Jambi (Gambar 3b). Perubahan warna daun tidak sebanyak dan seluas dibandingkan dengan semai gaharu yang terinfeksi cendawan asal Gorontalo (Gambar 3a).
Perubahan Warna Kayu
Kayu pada semai dan pohon gaharu mengalami perubahan warna dari putih menjadi kecoklatan, coklat, hingga coklat kehitaman. Intensitas perubahan warna kayu sangat bervariasi untuk masing-masing perlakuan, sedangkan pada kontrol perubahan warna kayu tidak terjadi sampai akhir pengamatan. Perubahan warna kayu berkaitan dengan adanya infeksi cendawan pada jaringan kayu. Walker et al.
(1997) menyatakan bahwa terjadinya perubahan warna pada kayu menjadi coklat (browning) disebabkan oleh pelukaan, serangan oleh cendawan dan penggunaan senyawa kimia.
Perubahan warna kayu mengindikasikan bahwa mulai terbentuknya senyawa gaharu. Sumadiwangsa dan Zulnely (1999) menyatakan bahwa perubahan warna dari putih menjadi coklat kehitaman merupakan gejala awal terbentuknya senyawa gaharu. Senyawa gaharu ini terdeposit pada jaringan kayu (Rahayu dan Situmorang 2006).
Inokulasi F. solani pada semai gaharu mengakibatkan perubahan warna kayu berkisar pada putih, putih kecoklatan, hingga coklat. Semai gaharu memberikan respon yang berbeda terhadap isolat asal Jambi dan Gorontalo. Perubahan warna kayu terlihat lebih gelap pada semai gaharu yang diberikan isolat asal Jambi dibandingkan dengan pemberian isolat Gorontalo (Gambar 4). Perbedaan warna ini berkaitan dengan jumlah konsentrasi relatif senyawa pembentuk gaharu yang dihasilkan isolat asal Jambi lebih besar dibandingkan dengan isolat asal Gorontalo. Ng et al. (1997) dan Barden et al. (2000) menyatakan bahwa perubahan warna yang menjadi lebih gelap ini diduga akibat peningkatan akumulasi senyawa terpenoid yang disebabkan oleh infeksi cendawan. Semakin gelap warna yang dihasilkan, semakin tinggi tingkat gubal gaharu yang dihasilkan.
Gambar 4 Perubahan warna kayu yang terjadi akibat isolat
F. solani:(a) asal Jambi, dan (b) asal Gorontalo
6
Perubahan warna kayu pada pohon gaharu berkisar pada coklat hingga coklat kehitaman. Jika dibandingkan dengan semai gaharu, intensitas perubahan warna kayu pada pohon gaharu terlihat lebih jelas (Gambar 5). Hal ini dikarenakan perbedaan isolat dan banyaknya titik induksi pada pohon. Menurut Wulandari (2009) intensitas warna kayu dipengaruhi oleh perlakuan dan masa inkubasi. Pada perlakuan pengeboran (pohon) intensitas perubahan warna kayu lebih tinggi dan berbeda dibandingkan dengan perlakuan pelukaan (semai).
Gambar 5 Perubahan warna kayu pada pohon: (a) 1 BSI, (b) 3 BSI, (c) 6 BSI, dan (d) 9 BSI
Hasil Analisis Senyawa Kimia Gaharu
Gaharu Tingkat Semai
Hasil analisis kromatogram dan penelusuran jenis senyawa pada semai gaharu, minggu pertama setelah induksi diperoleh senyawa kimia yang terdeteksi sebanyak 40 jenis senyawa untuk isolat asal Gorontalo. Sementara isolat asal Jambi menghasilkan 44 jenis senyawa kimia. Pada kontrol, senyawa kimia yang terdeteksi hanya sebanyak 31 jenis. Nama-nama jenis senyawa dapat dilihat pada Lampiran 1. Hasil analisis GCMS dapat dilihat pada Gambar 6.
Gambar 6 Kromatogram hasil analisis senyawa kimia gaharu isolat F. solani asal Gorontalo dan Jambi
Gambar 6 menunjukkan kromatogram yang dihasilkan isolat Jambi dan Gorontalo memiliki kemiripan. Hal ini menandakan jenis senyawa kimia yang
7 dihasilkan sama. Senyawa kimia seperti ethylic acid, guaiacol, cyclopropyl carbinol, acetosyringone, dan eugenol ditemukan pada semai gaharu untuk isolat asal Jambi dan Gorontalo. Jumlah senyawa yang dihasilkan selama 8 kali analisis GCMS dapat dilihat pada Gambar 7.
Gambar 7 Fluktuasi jumlah senyawa kimia yang dihasilkan oleh isolat F. solani
asal Jambi dan Gorontalo terhadap semai gaharu selama 12 minggu Gambar 7 menunjukkan hasil analisis mengalami fluktuasi dari awal sampai akhir pengamatan. Jumlah senyawa tertinggi yang dihasilkan isolat asal Gorontalo yaitu saat 4 MSI sebanyak 48 jenis senyawa kimia. Untuk isolat asal Jambi dihasilkan saat 1 MSI sebanyak 44 jenis senyawa kimia. Pada kontrol, senyawa kimia yang dihasilkan sebanyak 31 jenis. Hal ini membuktikan bahwa pemberian isolat pada semai gaharu dapat merangsang munculnya senyawa kimia lain pada jaringan tanaman yang terinfeksi. Secara umum, dari awal pengamatan sampai akhir pengamatan senyawa kimia yang sering ditemukan yaitu jenis senyawa ethylic acid, guaiacol, cyclopropyl carbinol, acetosyringone, eugenol, corylon, dimethoxybenzaldehyde, coniferyl alcohol, dimethoxyphenol, dan propionic acid.
Gaharu Tingkat Pohon
8
Gambar 8 Jumlah senyawa kimia yang dihasilkan oleh isolat F. oxysporum
terhadap pohon gaharu selama 9 bulan
Gambar 8 menunjukkan pemberian isolat F. oxysporum pada pohon gaharu dapat merangsang munculnya senyawa kimia lain yang tidak ditemukan pada gaharu kontrol. Hal ini terlihat dari hasil analisis 1 BSI sampai 9 BSI bahwa senyawa kimia yang dihasilkan lebih banyak jumlahnya. Pada saat 9 BSI, jumlah senyawa kimia merupakan yang tertinggi yaitu sebanyak 100 jenis senyawa.
Gambar 9 menunjukkan munculnya senyawa kimia rata-rata terjadi pada rentang waktu 15 sampai 28 menit. Hal ini terlihat dari hasil kromatogram yang lebih rapat. Senyawa kimia yang muncul pada rentang waktu tersebut diantaranya,
guaiacol, cyclopropyl carbinol, benzylacetone, indole, eugenol, dimethoxybenzaldehyde, coniferyl alcohol, vanillin, acetovanillone, dan
acetosyringone. Secara umum, pohon gaharu menghasilkan lebih banyak senyawa kimia dibandingkan dengan semai gaharu. Hal ini dikarenakan perbedaan isolat dan jumlah titik induksi pada pohon yang lebih banyak.
Senyawa Pembentuk Gaharu
Kandungan gaharu terbentuk sebagai bentuk respon terhadap infeksi cendawan yang mengakibatkan keluarnya resin. Resin yang terbentuk tidak dikeluarkan dari pohon, melainkan disimpan pada jaringan kayu, sehingga jaringan kayu yang putih dan bertekstur halus berubah menjadi gelap dan keras. Bagian kayu akan menjadi berat dan mengeluarkan aroma harum jika dibakar (Hou 1960). Resin ini termasuk golongan sesquiterpena (Yuan 1995).
Hasil analisis GCMS dikelompokkan ke dalam senyawa pertahanan tanaman, senyawa konstituen gaharu, dan senyawa aromatis atau bersifat odorant.
Senyawa pertahanan tanaman terbentuk jika tanaman mengalami gangguan. Cowan (1999) menerangkan bahwa tanaman memiliki kemampuan yang tidak terbatas dalam mensintesis substansi aromatis yang kebanyakan merupakan senyawa fenol atau turunannya. Senyawa tersebut merupakan bagian dari
9 metabolit sekunder yang biasanya berperan dalam mekanisme pertahanan tanaman terhadap serangan mikroorganisme, serangga, ataupun cendawan.
Gambar 9 Kromatogram hasil analisis senyawa kimia gaharu isolat F. oxysporum (BSI: bulan setelah induksi)
10
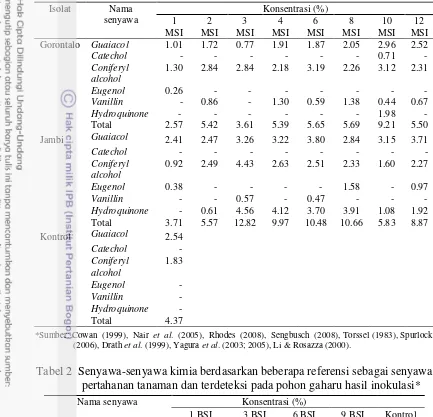
Tabel 1 Senyawa-senyawa kimia berdasarkan beberapa referensi sebagai senyawa pertahanan tanaman dan terdeteksi pada semai gaharu hasil inokulasi*
Isolat Nama
Tabel 2 Senyawa-senyawa kimia berdasarkan beberapa referensi sebagai senyawa pertahanan tanaman dan terdeteksi pada pohon gaharu hasil inokulasi*
Nama senyawa Konsentrasi (%)
11
Guaiacol merupakan intermediet dalam pembuatan eugenol dan vanillin
yang juga digunakan sebagai antiseptik dan parasitisida (Li dan Rosazza 2000). Senyawa ini ditemukan sejak pertama kali analisis. Konsentrasinya dalam semai gaharu sebesar 2.48%, sedangkan pada pohon gaharu sebesar 4.17%. Coniferyl alcohol merupakan senyawa pertahanan tipe fitoaleksin yang termasuk dalam grup fenil propanoid, contohnya adalah yang terdapat pada Limun usitiltissimum
(Sengbusch 2008). Konsentrasinya dalam semai gaharu sebesar 2.45%, sedangkan pada pohon gaharu sebesar 1.90%.
Eugenol merupakan senyawa yang bersifat bakteriostatik terhadap jamur dan bakteri (Cowan 1999). Eugenol digunakan dalam pembuatan parfum, minyak esensial, dan obat-obatan. Senyawa ini digunakan untuk menghasilkan isoeugenol yang diperlukan untuk membuat vanillin yang juga merupakan bahan yang penting dalam obat-obatan dan industri parfum dan pengharum. Eugenol dan
isoeugenol diturunkan dari prekursor lignin, yaitu asam ferulat ataupun coniferyl alcohol (Rhodes 2008). Senyawa ini jarang ditemukan pada semai gaharu.
Hydroquinone merupakan difenol yang mudah teroksidasi menjadi diketon yang disebut kuinon. Kuinon sangat potensial sebagai antimikrobial karena dapat membentuk kompleks dengan asam amino nukleofilik dalam protein, sering menyebabkan inaktivasi dan kehilangan fungsi protein. Contohnya antrakuinon yang diisolasi dari Cassia italica (Cowan 1999). Senyawa ini sangat jarang ditemukan pada pohon gaharu.
Hasil analisis GCMS selanjutnya ditemukan senyawa kimia yang tergolong ke dalam senyawa konstituen gaharu. Senyawa-senyawa tersebut berdasarkan para peneliti diyakini sebagai senyawa pembentuk gaharu. Lampiran 2, Lampiran 3, dan Lampiran 4 menyajikan senyawa yang tergolong konstituen gaharu dan diringkas pada Tabel 3.
Tabel 3 Jumlah senyawa konstituen gaharu yang terdeteksi untuk seluruh sampel
Gaharu Isolat Jumlah senyawa konstituen gaharu
Tingkat semai F. solani Gorontalo 7
F. solani Jambi 7
Tingkat pohon F. oxysporum Bontang 10
Kontrol - 3
Tabel 3 menunjukkan isolat asal Bontang menghasilkan senyawa konstituen gaharu tertinggi sebanyak 10 jenis senyawa, sedangkan isolat Jambi dan Gorontalo masing-masing menghasilkan 7 jenis senyawa. Pada Lampiran 2 sampai Lampiran 4 diperoleh konsentrasi relatif tertinggi pada isolat asal Jambi sebesar 16.38%, diikuti isolat asal Gorontalo sebesar 13.87%, dan isolat asal Bontang sebesar 13.06%. Isolat asal Jambi memberikan hasil gaharu artifisial yang relatif terbaik yang ditunjukkan oleh konsentrasi senyawa konstituen gaharu tertinggi.
Aromadendrena merupakan turunan senyawa sesquiterpena dan diyakini oleh para peneliti sebelumnya sebagai senyawa penciri dari gaharu dan dapat dijadikan salah satu parameter untuk menentukan mutu gaharu. Senyawa ini hanya terdeteksi pada semai gaharu (isolat Gorontalo) saat 2 MSI dan 4 MSI. Konsentrasi relatifnya berturut-turut sebesar 0.35% dan 0.34%.
12
Aquilaria sinensis (Burfield 2005). Senyawa benzylacetone mulai terdeteksi saat 2 MSI pada semai gaharu, sedangkan pada pohon gaharu terdeteksi saat pertama analisis.
Tabel 4 Jumlah senyawa berkarakter odorant yang merupakan pirolisis dari bagian kayu
Gaharu Isolat Jumlah senyawa
Tingkat semai F. solani Gorontalo 10
F. solani Jambi 8
Tingkat pohon F. oxysporum Bontang 9
Kontrol - 4
Tabel 4 menunjukkan jumlah senyawa odorant tertinggi dihasilkan oleh isolat Gorontalo sebanyak 10 jenis senyawa, diikuti isolat asal Bontang sebanyak 9 jenis senyawa dan isolat asal Jambi sebanyak 8 senyawa. Konsentrasi relatif tertinggi dihasilkan oleh isolat asal Bontang sebesar 10.54%, diikuti isolat Jambi 9.44% dan isolat Gorontalo 5.95%. Senyawa-senyawa tersebut sebenarnya bukan merupakan senyawa konstituen gaharu. Namun, keberadaannya dalam gaharu tidak bisa dikesampingkan karena peranannya terdapat pada wangi yang dihasilkan ketika gaharu dibakar. Novriyanti (2010) menyatakan bahwa penggunaan gaharu pada umumnya menghasilkan wangi jika kayu yang mengandung resin dibakar.
Tabel 5 Jumlah senyawa berkarakter odorant lain yang belum dikonfirmasi sebagai konstituen gaharu
Gaharu Isolat Jumlah senyawa
Tingkat semai F. solani Gorontalo 18
F. solani Jambi 15
Tingkat pohon F. oxysporum Bontang 24
Kontrol - 8
Tabel 5 menunjukkan isolat asal Bontang menghasilkan jenis senyawa
odorant lain tertinggi sebanyak 24 jenis senyawa, diikuti isolat asal Gorontalo dan Jambi sebanyak 18 dan 15 jenis senyawa. Pada Lampiran 2, konsentrasi relatif tertinggi dihasilkan isolat asal Jambi (19.58%), diikuti isolat asal Gorontalo (18.69%) dan isolat asal Bontang (18.02%). Keberadaan senyawa-senyawa ini terhadap wangi pada gaharu perlu dilakukan penelitian lanjutan karena para peneliti belum menetapkan sebagai konstituen dari gaharu.
Senyawa odorant yang ditemukan diantaranya ambrettolide, valerolactone, maltol, indole, benzylacetone, dan vanillin. Senyawa ambrettolide memiliki karakter wangi musk, manis buah, dan bunga. Dalam Novriyanti (2010) dijelaskan bahwa valerolactone memiliki wangi herbal yang dimanfaatkan dalam industri parfum dan pewangi. Komponen maltol mengeluarkan wangi karamel dan digunakan untuk menghasilkan wangi yang manis biasa dimanfaatkan sebagai penguat rasa dan aroma. Senyawa indole merupakan konstituen utama dalam minyak melati dan dalam berbagai wangi bunga dan parfum, sedangkan vanillin
13
SIMPULAN DAN SARAN
Simpulan
Proses pembentukan gaharu pada semai dan pohon ditunjukkan dengan terdeteksinya konstituen gaharu dan senyawa-senyawa aromatis mulai minggu pertama analisis hingga bulan terakhir analisis. Terdapat 7 jenis senyawa konstituen gaharu yang dihasilkan isolat F. solani pada semai A. malaccensis
dengan konsentrasi relatif isolat asal Jambi sebesar 16.38% dan isolat asal Gorontalo sebesar 13.87%. Isolat F. oxysporum pada pohon A. malaccensis
mampu menginduksi pembentukan senyawa konstituen gaharu sebanyak 10 jenis senyawa dengan konsentrasi relatif sebesar 13.06%.
Saran
Data konsentrasi relatif senyawa pembentuk gaharu masih mengalami fluktuasi setiap minggu dan bulannya, sehingga diperlukan penelitian lanjutan dengan kombinasi jenis gaharu dan isolat yang lebih beragam dan periode pengamatan yang lebih panjang.
DAFTAR PUSTAKA
Abrishami F, Teimuri-Mofrad R, Bayat Y, Shahrisa A. 2002. Synthesis of some aldoxime derivatives of 4H-pyran-4-ones. Molecules 7:239-244.
Agrios GN. 2004. Plant Pathologi. Ed ke-5. California (US): Academic Press. Inc.
Azah M, Chang YS, Mailina J, Said AA, Majid JA, Husni SS, Hasnida HN, Yasmin YN. 2008. Comparison of chemical profiles of selected gaharu oils from peninsular Malaysia. The Malaysian Journal of Analytical Sciences
12(2):338-340.
Baker CJ, Whitaker BD, Mock NM, Rice C, Robert CD, Deahl KL, Averyanov AA. 2004. Stimulatory Effect of Acetosyringone on Plant/Pathogen Recognition. [diunduh 2013 Sep 26]. Tersedia pada: http://www.ars.usda.gov/research/publications/publications.htm.
Barden A, Anak NA, Mulliken T, Song M. 2000. Heart of the matter: agarwood use and trade and CITES implementation for Aquilaria malaccensis [a traffic network report]. Cambridge (GB): Traffic International.
Bunke E, Schatkowski JD. 1997. Isolongifolanol Derivates, their Production and their Use. United State Patent. [diunduh 2013 Sep 24]. Tersedia pada: http://www.freepatentsonline.com
14
Castro JM, Salido S, Altarejos J, Nogueras M, Sánchez A. 2002. Synthesis of ambrox® from labdanolic acid. Tetrahedron 58(29):5941-5949.
Chem YQ. 2008. Dumasin; Succinaldehyde. [diunduh 2013 Sep 24]. Tersedia pada: http://www.chemyq.com/En/xz/xz11
Cowan M. 1999. Plant products as antimicrobial agents. Clinical Microbiology Review 12(4):564-582.
Drath KM, Knop DR, Frost JW. 1999. Shikimic acid and quinic acid: replacing isolation fro, plant sources with recombinant microbial biocatalyst. J Am Chem Society. 121(7):1603-1604.
[FAO] Food and Agriculture Organization. Food Safety and Quality: Flavoruing Index. [diunduh 2013 Sep 24]. Tersedia pada: http://www.fao.org/ag/agn/jecfa-flav/index.html?showSynonyms=1
Fotouhi L, Fatehi A, Heravi MM. 2008. Investigation of electrooxidation reaction of some tetrahydrobenzo[b]pyran derivatives. Int J Electrochem Sci. 3:721-726.
Hou D. 1960. Thymeleaceae. Flora Malesiana 6(1):1-48.
Hua SST. 2001. Inhibitory effect of acetosyringone on two aflatoxin biosynthetic genes. Applied Microbiology 32:278-281.
Konishi T, Konishima T, Shimada Y, Kiyosawa S. 2002. Six new 2-(2-phenylethyl) chromones from agarwood. Chemical and Pharmaceutical Bulletin 50:419-422.
Aquilaria malaccensis. Fungal Divers. 43:67-74.
Nair MK, Joy J, Vasudevan P, Hinckley L, Hoagland TA, Venkitanarayanan KS. 2005. Antimicrobial effect of caprylic acid and monocaprylin on major bacterial mastitis pathogens. J Dairy Sci. 88(10):88-95.
Ng LT, Chang YS, Kadir A. 1997. A review on agar (gaharu) producing Aquilaria
species. Trop Forest Prod. 2:272-285.
Nieamann KO, Visintini. 2005. Assesment of potential for remote sensing detection of bark beetle-infested areas during green attack: a literature review. Canada: Mountain Pine Beetle Initiative.
Novriyanti E. 2010. Kajian kimia gaharu hasil inokulasi Fusarium sp. pada
Aquilaria. Di dalam: Siran SA, Turjaman M, editor. Pengembangan Teknologi Produksi Gaharu Berbasis Pemberdayaan Masyarakat; 2010 Nop 5; Bogor, Indonesia. Bogor (ID): Pusat Penelitian dan Pengembangan dan Konservasi Alam. hlm 53-61.
Pedroso APD, Santos SC, Steil AA, Deschamps F, Barison A, Campos F, Biavatti MW. 2008. Isolation of syringaldehyde from Mikania laevigata medicinal: extract and its influence on the fatty acid profile of mice. Brazilian Jour of Pharmacognosy 18(1):63-69.
15 Rho HS, Baek HS, You JW, Kim S, Lee JY, Kim DH, Chang IS. 2007. New 5-Hydroxy-2-(hydroxymethyl)-4H-pyran-4-one Derivative has both tyrosinase inhibitory and antioxidant properties. Bull Korean Chem Soc. 28(3):471-473.
Rhodes D. 2008. Secondary Products Derived from Aromatic Amino Acids: Eugenol and Isoeugenol. [diunduh 2013 Sep 26]. Tersedia pada: www.hort.purdue.edu.
Rossi PG, Bao L, Luciani A, Panighi P, Desjobert JM, Costa J, Casanova J, Bolla JM, Berti L. 2007. (E)-Methy-lisoeugenol and elemicin: antibacterial components of Daucus carota L. essential oil against campylobacter jejuni.
J Agric Food Chem. 55(18):7332-7336.
Sengbusch PV. 2008. Phenolic Compounds. [diunduh 2013 Sep 26]. Tersedia pada: http://www.biologie.unihamburg. de/b-online/e20/20d.htm.
Sheikholeslam SN, Weeks DP. 1987. Acetosyringone promotes high efficiency transformation of Arabidopsis thaliana explants by Agrobacterium tumafacien. Plant Molecular Biology 8:291-198.
Shimada Y, Konishi T, Kiyosawa S, Miyahara K, Kawasaki T. 1986. Studies on the agarwood (Jinko). IV1)- structures of 2-(2-phenylethyl) chromone derivates, agaroterol and isoagarotetrol. Chemical and Pharmaceutical Bulletin 34:2766-2773.
Spurlock F. 2006. Brief comparison of phyrethrin and synthetic phyrethroid fatecharacteristic. Department of Pesticide Regulation. [diunduh 2013 Sep 26]. Tersedia pada: www.cdpr.ca.gov.
Sumadiwangsa S, Zulnely. 1999. Catatan mengenai gaharu di Kalimantan Timur dan NTB. Info Hasil Hutan 5(2):80-90.
Torssell KBG. 1983. Natural Product Chemistry. Singapore (SG): John Wiley & Son Limited.
Walker D Jr, Taylor RW, Mulrooney RP. 1997. Diagnosing Field Crop Problems. [diunduh 2013 Sep 26]. Tersedia pada: http://ag.udel.edu/extension.
Widyastuti FR. 2009. Pengaruh etilen dalam menginduksi pembentukan senyawa terpenoid pada pohon gaharu (Aquilaria microcarpa) [skripsi]. Bogor (ID): Institut Pertanian Bogor.
Wulandari E. 2009. Efektivitas Acremonium sp. dan Fusarium sp. sebagai penginduksi ganda terhadap pembentukan gaharu pada pohon Aquilaria microcarpa [skripsi]. Bogor (ID): Institut Pertanian Bogor.
Yagura T, Shibayama N, Ito M, Kiuchi F, Honda G. 2005. Three novel diepoxy tetrahydrochromones from agarwood artificially produced by intentional wounding. Tetrahedron Letters 46:4395-4398.
Yagura T, Ito M, Kiuchi F, Honda G, ShimadaY. 2003. Four new 2-(2-Phenylethyl) chromone derivatives from withered wood of Aquilaria sinensis. Chem Pharm Bull. 51:560-564.
16
Lampiran 1 Senyawa-senyawa yang ditemukan pada minggu pertama analisis
Konsentrasi (%) Nama senyawa
F. solani asal Gorontalo
9.51 Carbon dioxide (CAS) Dry ice
8.15 Cyclobutanol (CAS) Cyclobutyl hydroxide
8.92 1-propen-2-ol, acetate (CAS) Isopropenyl acetate
0.66 2,3-Butanedione (CAS) Diacetyl
9.51 Acetic acid (CAS) Ethylic acid
0.46 Propanal (CAS) Propinaldehyde
1.08 Propanoic acid, 2-oxo-, methyl ester (CAS) Methyl pyruvate
0.81 2(5H)-FURANONE
4.11 1,2-CYCLOPENTANEDIONE
0.35 2-Cyclopenten-1-one, 2-hydroxy-3-methyl- (CAS) Corylon
1.01 Phenol, 2-methoxy- (CAS) Guaiacol
3.34 Cyclopropyl carbinol
0.43 Cyclopropane, 1,1,2-trimethyl-3-(2-methyl-1-propenyl)- (CAS)
0.63 2-propenoic acid, 2-methyl-, ethyl ester (CAS) Ethyl methacrylate
2.62 Phenol, 4-ethenyl-2-methoxy-
3.33 Phenol, 2,6-dimethoxy- (CAS) 2,6-Dimethoxyphenol
0.55 4-Methoxy-3-(methoxymethyl)phenol
1.40 Phenol, 2-methoxy-3-(2-propenyl)- (CAS) Phenol, 3-Allyl-2-methoxy- (CAS)
10.28 1,6-ANHYDRO-BETA-D-GLUCOPYRANOSE (LEVOGLUCOSAN)
0.32 Benzene, 1,2,3-trimethoxy-5-methyl- (CAS) Toluene, 3,4,5-trimethoxy-
6.41 4-METHYL-2,5-DIMETHOXYBENZALDEHYDE
3.99 Phenol, 2,6-dimethoxy-4-(2-propenyl)- (CAS) 4-Allyl-2,6-dimethoxyphenol
0.83 benzaldehyde, 4-hydroxy-3,5-dimethoxy- (CAS) Syringaldehyde
0.81 Ethanone, 1-(4-hydroxy-3,5-dimethoxyphenyl)- (CAS) Acetosyringone
0.26 3-(p-hydroxy-m-methoxyphenyl)-2-propenal
0.91 2,4-Hexadienedioic acid, 3,4-diethyl-, dimethyl ester, (E,Z)- (CAS) CIS,TR
0.18 2-Heptadecanone (CAS) 2-HEPTADECANON
0.98 Hexadecanoic acid, methyl ester (CAS) Methyl palmitate
1.11 3-(3',5'-dimethoxy-4'-hydroxyphenyl)-E-2-propenal
1.02 9-Octadecenoic acid (Z)-, methyl ester (CAS) Methyl oleate
1.64 Acetic acid, anhydride (CAS) Acetic oxide
1.90 2,4-Imidazolidinedione, 3-methyl- (CAS) 3-Methylhydantoin
0.93 5-HYDROXYMETHYL-DIHYDRO-FURAN-2-ONE
0.66 2,4(3H, 5H)-Furandione, 3-methyl- (CAS) ALPHA-METHYLTETRONIC
ACID
0.80 7-methyl-1,4-dioxaspiro[2.4]heptan-5-one
0.52 2(3H)-FURANONE, DIHYDRO-4-HYDROXY-
1.81 2-ISOPROPENYL-2,5-DIMETHYLCYCLOHEXANONE-6,6-D2
0.26 Phenol, 2-methoxy-4-(2-propenyl)- (CAS) Eugenol
1.33 1,2,4-Trimethoxybenzene
17 Lanjutan Lampiran 1
Konsentrasi (%) Nama senyawa
F. solani asal Jambi
8.58 Carbamic acid, monoammonium salt (CAS) Ammonium carbamate
5.63 Acetic acid, anhydride (CAS) Acetic oxide
11.77 Acetic acid (CAS) Ethylic acid
5.41 2-propanone, 1-hydroxy- (CAS) Acetol
0.41 Butanedial (CAS) Succinaldehyde
1.43 Propanoic acid, 2-oxo-, methyl ester (CAS) Methyl pyruvate
1.13 2(5H)-FURANONE
2.08 1,2-CYCLOPENTANEDIONE
0.64 2,4-Imidazolidinedione, 3-methyl- (CAS) 3-Methylhydantoin
2.32 2-Cyclopenten-1-one, 2-hydroxy-3-methyl- (CAS) Corylon
0.39 5-HYDROXYMETHYL-DIHYDRO-FURAN-2-ONE
2.41 Phenol, 2-methoxy- (CAS) Guaiacol
3.76 Cyclopropyl carbinol
0.49 2H-Pyran-2-one, 6-ethyltetrahydro- (CAS) 6-ETHYL-DELTA-VALEROLA
0.62 Cyclopropane, 1,1,2-trimethyl-3-(2-methyl-1-propenyl)- (CAS)
0.99 Phenol, 4-ethyl-2-methoxy- (CAS) p-Ethylguaiacol
3.16 Phenol, 4-ethenyl-2-methoxy-
5.57 Phenol, 2,6-dimethoxy- (CAS) 2,6-Dimethoxyphenol
2.13 1,2,4-Trimethoxybenzene
1.89 Phenol, 2-methoxy-3-(2-propenyl)- (CAS) Phenol, 3-Allyl-2-methoxy-
(CAS)
2.40 1,6-ANHYDRO-BETA-D-GLUCOPYRANOSE (LEVOGLUCOSAN)
8.18 4-METHYL-2,5-DIMETHOXYBENZALDEHYDE
6.04 Phenol, 2,6-dimethoxy-4-(2-propenyl)- (CAS) 4-Allyl-2,6-dimethoxyphenol
0.37 benzaldehyde, 4-hydroxy-3,5-dimethoxy- (CAS) Syringaldehyde
0.88 Ethanone, 1-(4-hydroxy-3,5-dimethoxyphenyl)- (CAS) Acetosyringone
0.92 phenol, 4-(3-hydroxy-1-propenyl)-2-methoxy- (CAS) Coniferyl alcohol
1.05 2,4-Hexadienedioic acid, 3,4-diethyl-, dimethyl ester, (Z,Z)- (CAS) CIS,CIS
1.75 3-(2,5-DIMETHOXY-PHENYL)-PROPIONIC ACID
2.28 Formamide (CAS) Methanamide
0.95 BUTAN-3-ENOIC ACID METHYL ESTER
0.64 2,3-Butanedione (CAS) Diacetyl
0.92 2-Furanmethanol (CAS) Furfuryl alcohol
0.43 (2-HYDROXYCYCLOHEXYL)MERCURIC CHLORIDE
0.48 2-Nonen-1-ol, (E)- (CAS) trans-2-Nonenol
0.47 3-Ethyl-2-Hydroxy-2-cyclopenten-1-one
0.79 2-Methoxy-4-methylphenol
0.66 2-Propenoic acid, 2-methyl-, ethyl ester (CAS) Ethyl methacrylate
0.41 5-Acetyl-2-methylpyridine
0.38 beta-D-Glucopyranoside, methyl anhydro- (CAS) METHYL
3,6-ANHYDRO
18
Lanjutan Lampiran 1
5.69 1,2,3,4-Cyclopentanetetrol, (1.alpha.,2.beta.,3.beta.,4.alpha.)- (CAS)
0.36 3-(p-hydroxy-m-methoxyphenyl)-2-propenal
19
Lampiran 2 Senyawa pembentuk gaharu hasil inokulasi F. solani asal Jambi*
Nama senyawa 1 MSI 2 MSI 3 MSI 4 MSI 6 MSI 8 MSI 10 MSI 12 MSI
Senyawa konstituen gaharu
Phenol, 2,6-dimethoxy- (CAS) 2,6-Dimethoxyphenol 5.57 6.29 8.14 6.50 7.78 5.40 5.56 8.04
4-METHYL-2,5-DIMETHOXYBENZALDEHYDE 8.18 7.46 8.09 7.49 9.94 3.55 7.36 5.60
2,4-Hexadienedioic acid, 3,4-diethyl-, dimethyl ester, (Z,Z)- (CAS) CIS,CIS 1.05 1.13 1.36 - - - 0.94 1.41
2-Butanone, 4-phenyl- (CAS) Benzylacetone - 0.99 1.34 0.84 1.54 1.44 0.81 0.66
Benzaldehyde (CAS) Phenylmethanal - - 0.78 - - - - -
2-Butanone, 3-methyl- (CAS) 3-Methyl-2-butanone - - 1.14 - - 0.93 - -
2,4-Hexadienedioic acid, 3,4-diethyl-, dimethyl ester, (E,Z)- (CAS) CIS,TR - - 1.19 1.57 0.97 - -
Total 14.8 15.86 20.84 16.01 20.83 12.29 14.66 15.71
Rata-rata 16.38%
Senyawa berkarakter odorant
2-propanone, 1-hydroxy- (CAS) Acetol 5.41 4.88 6.74 6.55 2.44 1.98 3.11 1.89
Phenol, 2-methoxy- (CAS) Guaiacol 2.41 2.47 3.26 3.22 3.80 2.84 3.15 3.71
Phenol, 4-ethyl-2-methoxy- (CAS) p-Ethylguaiacol 0.99 1.25 1.35 0.43 0.77 - - 0.36
Ethanone, 1-(4-hydroxy-3,5-dimethoxyphenyl)- (CAS) Acetosyringone 0.88 0.92 0.60 1.17 1.01 0.59 1.16 1.78
2-Propanone, 1-(acetyloxy)- (CAS) Acetol acetate - - 0.53 1.63 - - - -
Phenol (CAS) Izal - - - 0.52 - - - -
3-Methoxy-pyrocatechol - - - 0.45 - -
Ethanone, 1-(4-hydroxy-3-methoxyphenyl)- (CAS) Acetovanillone - - - 0.32 0.99
Total 9.69 9.52 12.47 13.51 8.01 5.86 7.74 8.73
Rata-rata 9.44%
Senyawa odorant lainnya
2(5H)-FURANONE 1.13 1.64 1.82 1.66 1.23 - - -
20 Lanjutan Lampiran 2
2H-Pyran-2-one, 6-ethyltetrahydro- (CAS) 6-ETHYL-DELTA-VALEROLA 0.49 - 0.52 - - - - -
Phenol, 2,6-dimethoxy-4-(2-propenyl)- (CAS) 4-Allyl-2,6-dimethoxyphenol 6.04 3.89 8.55 6.62 9.48 8.55 4.82 9.42
benzaldehyde, 4-hydroxy-3,5-dimethoxy- (CAS) Syringaldehyde 0.37 0.83 1.34 - 1.60 0.41 0.48 1.31
3-(2,5-DIMETHOXY-PHENYL)-PROPIONIC ACID 1.75 3.73 3.63 2.50 1.13 2.01 1.68 1.63
2-Furanmethanol (CAS) Furfuryl alcohol 0.92 0.64 0.91 - 0.50 - - -
2-Methoxy-4-methylphenol 0.79 1.77 1.88 1.60 1.37 2.68 0.79 1.62
Phenol, 2-methoxy-4-(2-propenyl)- (CAS) Eugenol 0.38 - - - - 1.58 - 0.97
2-Furancarboxaldehyde (CAS) Furfural - - 0.75 0.83 0.77 0.66 - -
Benzaldehyde, 4-hydroxy-3-methoxy- (CAS) Vanillin - - 0.57 - 0.47 - - -
2-Butanone, 4-(4-hydroxy-3-methoxyphenyl)- (CAS) Zingerone - - - - 0.92 - - 0.49
1-TRICOSENE - - - 0.40 0.31 0.79
2H-Pyran-2-one, tetrahydro- (CAS) 5-Valerolactone - - - 0.79 - -
Oxacyclohepadec-8-en-2-one (CAS) Ambrettolide - - - 0.30 -
Total 15.61 23.23 24.99 17.34 21.46 20.93 11.90 21.18
Rata-rata 19.58%
*Sumber: FAO (2008); Abrishami et al. (2002); Rho et al. (2007); Fotouhi et al. (2008); Sheikholeslam & Weeks (1987); Baker et al. (2004); Hua et al. (2001); Azah et al. (2008); Castro et al. (2002); Lynd-Shiveley (2004); Chem YQ (2008); Rossi et al. (2007); Bunke & Schatkowski (1997); Pedroso et al. (2008).
Lampiran 3 Senyawa pembentuk gaharu hasil inokulasi F. solani asal Gorontalo*
Nama senyawa 1 MSI 2 MSI 3 MSI 4 MSI 6 MSI 8 MSI 10 MSI 12 MSI
Senyawa konstituen gaharu
Phenol, 2,6-dimethoxy- (CAS) 2,6-Dimethoxyphenol 3.33 3.95 4.75 4.62 4.91 4.39 6.14 5.31
4-METHYL-2,5-DIMETHOXYBENZALDEHYDE 6.41 7.07 8.86 4.17 9.02 7.50 3.69 8.23
21
Lanjutan Lampiran 3
Hexadecanoic acid, methyl ester (CAS) Methyl palmitate 0.98 - - - -
2-Butanone, 4-phenyl- (CAS) Benzylacetone - 1.82 1.43 0.54 0.54 0.83 1.54 0.65
2,4-Hexadienedioic acid, 3,4-diethyl-, dimethyl ester, (Z,Z)- (CAS) CIS,CIS - 1.04 1.44 - 1.41 0.64 1.35 -
AROMADENDRENEPOXIDE-(I) - 0.35 - 0.34 - - - -
Total 11.63 14.23 16.48 10.35 16.43 13.79 12.72 15.34
Rata-rata 13.87%
Senyawa Berkarakter Odorant
Phenol, 2-methoxy- (CAS) Guaiacol 1.01 1.72 0.77 1.91 1.87 2.05 2.96 2.52
Ethanone, 1-(4-hydroxy-3,5-dimethoxyphenyl)- (CAS) Acetosyringone 0.81 0.98 1.46 0.57 1.73 1.04 1.32 1.21
7-(Benzyloxy)-5-hydroxy-2-methyl-4H-1-benzopyran-4-one - 1.04 - - - -
2,3-Dihydro-5-hydroxy-6-methyl-4H-pyran-4-one - - 0.48 - - - - -
2-propanone, 1-hydroxy- (CAS) Acetol - - 1.87 3.07 2.83 4.16 4.78 1.38
4H-Pyran-4-one, 3-hydroxy-2-methyl- (CAS) Maltol - - - 0.33 - - - -
Ethanone, 1-(4-hydroxy-3-methoxyphenyl)- (CAS) Acetovanillone - - - 0.55 - - 0.37 0.52
3-Methoxy-pyrocatechol - - - 0.71 -
2-Propanone, 1-(acetyloxy)- (CAS) Acetol acetate - - - 1.16 -
Phenol, 4-ethyl-2-methoxy- (CAS) p-Ethylguaiacol - - - 0.47 -
Total 1.82 3.74 4.58 6.43 6.43 7.25 11.77 5.63
Rata-rata 5.95%
Senyawa Odorant lainnya
2(5H)-FURANONE 0.81 0.84 1.07 0.92 0.67 1.07 - 0.55
Cyclopropyl carbinol 3.34 3.88 4.75 3.85 3.70 4.67 3.93 4.16
Phenol, 2,6-dimethoxy-4-(2-propenyl)- (CAS) 4-Allyl-2,6-dimethoxyphenol 3.99 4.74 8.03 8.70 6.98 5.68 8.15 6.90
benzaldehyde, 4-hydroxy-3,5-dimethoxy- (CAS) Syringaldehyde 0.83 1.13 1.79 0.59 1.76 1.14 1.86 1.31
22 Lanjutan Lampiran 3
2(3H)-FURANONE, DIHYDRO-4-HYDROXY- 0.52 - - - -
Phenol, 2-methoxy-4-(2-propenyl)- (CAS) Eugenol 0.26 - - - 0.97 - - -
2-Butanone (CAS) Methyl ethyl ketone - 1.03 - - - -
Benzaldehyde, 4-hydroxy-3-methoxy- (CAS) Vanillin - 0.86 - 1.30 0.59 1.38 0.44 0.67
3-(2,5-DIMETHOXY-PHENYL)-PROPIONIC ACID - 4.35 - - - -
2(3H)-Furanone, 5-ethyldihydro- (CAS) GAMMA -N-CAPROLACTONE - 0.55 - - - -
2H-Pyran-2-one, 6-ethyltetrahydro- (CAS) 6-ETHYL- DELTAVALEROLA - 0.45 1.79 1.86 1.47 1.03 - -
2-Methoxy-4-methylphenol - - 1.35 1.90 1.64 1.46 0.98 1.80
2-heptanol, acetate (CAS) 2-HEPTYL ACETATE - - 1.16 - - - - -
3-(2,5-DIMETHOXY-PHENYL)-PROPIONIC ACID - - 1.83 1.79 1.38 3.91 2.35 3.37
2-Furancarboxaldehyde (CAS) Furfural - - - 0.53 - - 0.86 -
2-Butanone, 4-(4-hydroxy-3-methoxyphenyl)- (CAS) Zingerone - - - 0.43 -
HYDROXY DIMETHYL FURANONE - - - 0.56
Total 10.68 17.83 21.76 21.44 19.16 20.34 19.00 19.32
Rata-rata 18.69%
*Sumber: FAO (2008); Abrishami et al. (2002); Rho et al. (2007); Fotouhi et al. (2008); Sheikholeslam & Weeks (1987); Baker et al. (2004); Hua et al. (2001); Azah et al. (2008); Castro et al. (2002); Lynd-Shiveley (2004); Chem YQ (2008); Rossi et al. (2007); Bunke & Schatkowski (1997); Pedroso et al. (2008).
Lampiran 4 Senyawa pembentuk gaharu hasil inokulasi F. oxysporum*
Nama Senyawa 1 BSI 3 BSI 6 BSI 9 BSI
Senyawa Konstituen Gaharu
2-Butanone, 3-methyl- (CAS) 3-Methyl-2-butanone 0.44 0.19 - 0.32
Phenol, 2,6-dimethoxy- (CAS) 2,6-Dimethoxyphenol 7.67 8.55 5.73 5.35
23
Lanjutan Lampiran 4
2-Butanone, 4-phenyl- (CAS) Benzylacetone 0.69 1.76 - 0.51
2-Butanone, 1-(acetyloxy)- (CAS) 1-Acetoxy-2-butanone 0.51 - 0.66 0.43
2,4-Hexadienedioic acid, 3-methyl-4-propyl-, dimethyl ester, (Z,E)- (CAS) 0.05 - - -
2,4-Hexadienedioic acid, 3,4-diethyl-, dimethyl ester, (E,Z)- (CAS) CIS,TR 0.76 0.86 0.20 0.27
4H-1-Benzopyran-4-one, 7-hydroxy-2,5-dimethyl- 0.07 - - -
Hexadecanoic acid, methyl ester (CAS) Methyl palmitate - 0.55 - -
2,4-Hexadienedioic acid, 3,4-diethyl-, dimethyl ester, (Z,Z)- (CAS) CIS,CIS - - 0.29 -
Total 16.23 15.91 11.96 8.15
Rata-rata 13.06%
Senyawa Berkarakter Odorant
Phenol, 2-methoxy- (CAS) Guaiacol 4.19 4.64 3.25 4.59
Phenol, 4-ethyl-2-methoxy- (CAS) p-Ethylguaiacol 1.01 0.52 0.61 0.80
Ethanone, 1-(4-hydroxy-3-methoxyphenyl)- (CAS) Acetovanillone 0.56 0.22 0.29 0.27
Ethanone, 1-(4-hydroxy-3,5-dimethoxyphenyl)- (CAS) Acetosyringone 1.08 0.95 0.85 0.24
2-propanone, 1-hydroxy- (CAS) Acetol 3.10 4.28 2.06 3.62
2-Propanone, 1-(acetyloxy)- (CAS) Acetol acetate 0.81 0.65 0.82 0.89
Phenol (CAS) Izal - 0.53 0.30 0.28
1,2-Benzenediol (CAS) Pyrocatechol - - - 0.28
2,3-Dihydro-5-hydroxy-6-methyl-4H-pyran-4-one - - - 0.47
Total 10.75 11.79 8.18 11.44
Rata-rata 10.54%
Senyawa Odorant lainnya
Cyclopropyl carbinol 5.42 3.86 6.11 2.41
2H-Pyran-2-one, 6-ethyltetrahydro- (CAS) 6-ETHYL-DELTAVALEROLA 0.56 0.38 0.46 -
24 Lanjutan Lampiran 4
Benzaldehyde, 4-hydroxy-3-methoxy- (CAS) Vanillin 0.32 0.15 0.12 -
Phenol, 2,6-dimethoxy-4-(2-propenyl)- (CAS) 4-Allyl-2,6-dimethoxyphenol 7.49 6.36 6.13 3.20
2-Furanmethanol (CAS) Furfuryl alcohol 0.43 0.56 0.41 0.23
Phenol, 2-methoxy-4-(2-propenyl)- (CAS) Eugenol 3.16 2.95 3.23 2.22
benzaldehyde, 4-hydroxy-3,5-dimethoxy- (CAS) Syringaldehyde 0.89 0.84 0.84 0.15
2-Furancarboxaldehyde (CAS) Furfural 0.52 - 0.53 0.56
2(3H)-furanone, dihydro- (CAS) Butyrolactone 0.36 - 0.22 -
2(5H)-FURANONE 0.36 0.58 0.53 0.39
1H-Indole (CAS) Indole 0.06 - - -
2-Butanone, 4-(4-hydroxy-3-methoxyphenyl)- (CAS) Zingerone 0.09 - - 0.15
3-(2,5-DIMETHOXY-PHENYL)-PROPIONIC ACID 0.28 0.49 0.47 0.12
1-TRICOSENE 0.25 0.52 0.12 0.98
Oxacycloheptadec-8-en-2-one (CAS) Ambrettolide 0.06 0.27 - 0.23
ZINGERONE [4-(4-HYDROXY-3-METHOXYPHENYL)-2-BUTANONE - 0.28 - -
Oxacycloheptadecan-2-one (CAS) Dihydroambrettolide - 0.34 - 0.21
Muskolactone - - 0.18 -
Eicosane (CAS) n-eicosane - - 0.10 0.18
2(5H)-Furanone, 5-methyl- (identity?) (CAS) 2-Penten-4-olide - - - 0.11
5 METHYL FURFURAL - - - 0.10
2,5-DIMETHYL-4-HYDROXY-3(2H)-FURANONE - - - 0.18
3(2H)-Furanone, 4-methoxy-2,5-dimethyl- - - - 0.65
Total 21.17 18.33 20.15 12.44
Rata-rata 18.02%
25
RIWAYAT HIDUP
Penulis dilahirkan di Kuningan pada tanggal 23 Juli 1991. Penulis adalah anak pertama dari dua bersaudara pasangan Bapak Endo Suhanda dan Ibu Samsih. Penulis menyelesaikan sekolah menengah di SMA Negeri 3 Kuningan pada tahun 2009 dan pada tahun yang sama penulis lulus seleksi masuk Institut Pertanian Bogor (IPB) melalui jalur Undangan Seleksi Masuk IPB dan diterima di Departemen Silvikultur, Fakultas Kehutanan Institut Pertanian Bogor
Penulis mulai aktif pada berbagai organisasi mahasiswa dan kegiatan yang berlangsung di fakultas maupun departemen. Penulis bergabung dalam Himpunan Profesi Departemen Silvikultur, Tree Grower Community masa kepengurusan 2010-2011 sebagai Wakil Ketua. Pada masa kepengurusan 2011-2012 sebagai anggota Scientific Improvement. Penulis juga bergabung dalam Badan Eksekutif Mahasiswa Fakultas Kehutanan masa kepengurusan 2010-2011 sebagai Koordinator Bidang Pendidikan & Kesejahteraan Mahasiswa.
Selain organisasi di atas, penulis juga aktif dalam kegiatan kepanitiaan di tingkat fakultas maupun departemen, diantaranya sebagai anggota divisi publikasi dan dokumentasi kegiatan Save Mangrove for Our Earth 2010, anggota divisi dana dan usaha kegiatan Forester Cup 2011, anggota divisi publikasi dan dokumentasi kegiatan Tree Grower Community In Action 2011, anggota divisi publikasi dan dokumentasi kegiatan Seminar Nasional Jabon 2011, ketua pelaksana kegiatan Acara Keluarga Silvikultur 2011, anggota medis kegiatan Belantara 2011, anggota divisi publikasi dan dokumentasi kegiatan Tree Grower Community In Action 2012. Penulis juga pernah menjadi asisten praktikum pengelolaan ekosistem hutan tahun 2013.