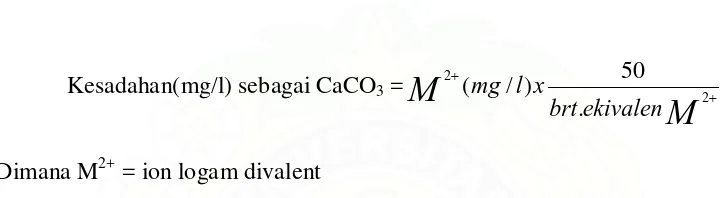Clara Derlismawan Aritonang : Kesadahan : Analisa Dan Permasalahannya Untuk Air Industri, 2008. USU Repository © 2009
KESADAHAN : ANALISA DAN PERMASALAHANNYA UNTUK
AIR INDUSTRI
KARYA ILMIAH
OLEH :
CLARA DERLISMAWAN ARITONANG
052401069
PROGRAM DIPLOMA-III KIMIA ANALIS
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
UNIVERSITAS SUMATERA UTARA
Clara Derlismawan Aritonang : Kesadahan : Analisa Dan Permasalahannya Untuk Air Industri, 2008. USU Repository © 2009
KESADAHAN : ANALISA DAN PERMASALAHANNYA UNTUK
AIR INDUSTRI
KARYA ILMIAH
Diajukan untuk melengkapi tugas dan memenuhi syarat mencapai gelar Ahlimadya
CLARA DERLISMAWAN ARITONANG
052401069
PROGRAM DIPLOMA-III KIMIA ANALIS
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
UNIVERSITAS SUMATERA UTARA
Clara Derlismawan Aritonang : Kesadahan : Analisa Dan Permasalahannya Untuk Air Industri, 2008. USU Repository © 2009
PERSETUJUAN
Judul : KESADAHAN : Analisa dan Permasalahannya
Untuk Air Industri
Kategori : KARYA ILMIAH
Nama : CLARA DERLISMAWAN ARITONANG
Nomor Induk Mahasiswa : 052401069
Program Studi : DIPLOMA (D3) KIMIA ANALIS
Departemen : KIMIA
Fakultas : MATEMATIKA DAN ILMU PENGETAHUAN
ALAM
(FMIPA) UNIVERSITAS SUMATERA UTARA
Disetujui Oleh :
Ketua Jurusan Dosen Pembimbing,
DR.Rumondang Bulan Nst,MS Drs. Usman Rasyid
Clara Derlismawan Aritonang : Kesadahan : Analisa Dan Permasalahannya Untuk Air Industri, 2008. USU Repository © 2009
PERNYATAAN
KESADAHAN : ANALISA DAN PERMASALAHANNYA UNTUK AIR INDUSTRI
KARYA ILMIAH
Saya mengakui bahwa karya ilmiah ini adalah hasil kerja saya sendiri, kecuali beberapa kutipan dan ringkasan masing-masing disebutkan sumbernya.
Medan, Juli 2008
Clara Derlismawan Aritonang : Kesadahan : Analisa Dan Permasalahannya Untuk Air Industri, 2008. USU Repository © 2009
PENGHARGAAN
Puji syukur pada Allah Bapa di surga atas berkat dan kasih karuniaNya sehingga penulis dapat menyelesaikan karya ilmiah ini dengan baik.
Penulisan karya ilmiah ini merupakan hasil pelaksanaan dari Praktek Kerja Lapangan (PKL) di PT.Clariant Indonesia-Duri, yang merupakan salah satu syarat untuk menyelesaikan program Diploma-3 Kimia Analis FMIPA USU. Dan dalam karya ilmiah ini penulis mengambil judul :” KESADAHAN : ANALISA DAN PERMASALAHANNYA UNTUK AIR INDUSTRI”.
Dalam penulisan karya ilmiah ini penulis banyak mendapat bantuan dari berbagai pihak. Dan dengan segala kerendahan hati penulis ingin menpersembahkan Karya Ilmiah ini kepada Ayahanda B.Aritonang dan Ibunda M.Silalahi, dan kakakku City , Nancy, Lidia,dan Eka serta Abangku Paraden Aritonang serta adik-adikku Rebecka, Heintje, Nineson, dan Endi Aritonang karena kalian adalah penyemangat terbesar dalam hidupku.Tak lupa juga buat B’Panjaitan, B’Gultom serta ponakan yang tercinta Lily, Thirza dan Bram
Terima kasih ku kepada Drs.Usman Rasyid karena bersedia membimbing penulis dengan sabar dan bijaksana. Dan tak lupa juga ku ucapkan terimakasih kepada teman – teman di Kimia Analis 05 Aquarina, Lusi, Risa, Oji, Iman Eka, Eci, dan semuannya PAKA’05.
Keluarga Besar JG’240, K’Intan,K’Olga,K’Winda, Hearty, Rina, Icha, dan Monica terima kasih untuk dukungan dan doanya. Akhir kata penulis berharap Karya Ilmiah ini dapat bermanfaat bagi pembaca.
Clara Derlismawan Aritonang : Kesadahan : Analisa Dan Permasalahannya Untuk Air Industri, 2008. USU Repository © 2009
Clara D.Aritonang
ABSTRAK
Kesadahan merupakan sifat air yang disebabkan oleh adanya ion-ion atau kation logam valensi dua. Salah satu kation penyebab utama dari kesadahan adalah Ca2+. Kalsium dalam air cenderung membentuk garam dengan karbonat atau bikarbonat. Bila didihkan bikarbonat berubah menjadi karbonat yang kecil nilai kelarutannya. Itulah sebabnya kesadahan air oleh bikarbonat/karbonat dapat dihilangkan dengan pemanasan.
Clara Derlismawan Aritonang : Kesadahan : Analisa Dan Permasalahannya Untuk Air Industri, 2008. USU Repository © 2009
ABSTRACT
Hardness is represent the nature of water which because of existence of divalence metal cation. One of the cations the root cause from hardness is Ca2+. Calcium in water to form salt with bicarbonate or carbonate. If boiled bicarbonate turn into carbonate with have a small of condensation value.That’s why hardness by bicarbonate/carbonate could be losted with warm-up.
Clara Derlismawan Aritonang : Kesadahan : Analisa Dan Permasalahannya Untuk Air Industri, 2008. USU Repository © 2009
DAFTAR ISI
Clara Derlismawan Aritonang : Kesadahan : Analisa Dan Permasalahannya Untuk Air Industri, 2008. USU Repository © 2009
2.3.4 Klasifikasi Kesadahan ... 10
2.3.4.1 Kesadahan Kalsium dan Magnesium ... 10
2.3.4.2 Kesadahan Karbonat dan non-karbonat ... 11
2.4 Metode Penentuan Kesadahan ... 12
2.4.1 Metode Total ... 12
2.4.2 Metode Titrasi EDTA ... 13
Bab 3. METODOLOGI PERCOBAAN 3.1 Alat dan Bahan ... 17
Bab 5 . Kesimpulan dan Saran 5.1 Kesimpulan ... 19
5.2 Saran ... 19
Clara Derlismawan Aritonang : Kesadahan : Analisa Dan Permasalahannya Untuk Air Industri, 2008. USU Repository © 2009
DAFTAR TABLE
Halaman
Tabel 2.3.1 9
Tabel 2.4.1 14
Tabel 4.1 18
Clara Derlismawan Aritonang : Kesadahan : Analisa Dan Permasalahannya Untuk Air Industri, 2008. USU Repository © 2009
BAB 1
PENDAHULUAN
1.1 Latar Belakang
Air adalah kehidupan. Air memegang peranan penting dalam kehidupan makhluk hidup, baik tanaman, hewan, dan terutama manusia. Dalam kehidupan manusia, fungsi air sangat bermacam-macam antara lain untuk kebutuhan rumah tangga, seperti minum, memasak, mencuci, kebutuhan pertanian, industri, transpotasi, sarana olahraga, rekreasi dan lain-lain.
Clara Derlismawan Aritonang : Kesadahan : Analisa Dan Permasalahannya Untuk Air Industri, 2008. USU Repository © 2009
kerusakan, dan bahaya bagi semua makhluk hidup yang bergantung pada sumber air.Oleh karena itu perlu pengelolahan terhadap sumber daya air.
Air banyak mengandung logam, baik logam ringan maupun logam berat, jarang sekali dalam bentuk atom tersendiri, tetapi biasanya terikat oleh senyawa lain sehingga berbentuk molekul. Kalsium karbonat (CaCO3) merupakan logam ringan yang banyak ditemukan dalam air. Dan kalsium karbonat merupakan unsur terpenting dalam kesadahan (Hardness). Dalam dunia industri Kalsium karbonat dapat menyebabkan perkaratan dan pada suhu rendah akan menyebabkan korosi.
Pada dunia industri air mempunyai banyak manfaat. Oleh karena itu air yang digunakan diharapkan dapat memenuhi standart mutu agar proses produksi dari perusahan tidak terganggu. Khusunya air pipa, diharapkan dapat memenuhi parameter yang telah ditentukan. Salah satu parameter yang harus dipenuhi adalah kadar kesadahan yang memenuhi standar mutu perusahaan.
Mengingat pentingnya analisa kesadahan dari air industri maka penulis tertarik untuk membahas masalah tersebut dalam karya ilmiah ini dengan mengambil judul ,”KESADAHAN : ANALISA DAN PERMASALAHANNYA UNTUK AIR INDUSTRI”.
1.2 Permasalahan
Clara Derlismawan Aritonang : Kesadahan : Analisa Dan Permasalahannya Untuk Air Industri, 2008. USU Repository © 2009
1.3 Tujuan
Untuk mengetahui kandungan kalsium karbonat pada air formasi 1.4 Manfaat
Untuk mengetahui pentingnya penentuan kalsium karbonat dalam air formasi.
BAB 2
TINJAUAN PUSTAKA
2.1 Sumber Air
Pada produksi minyak bumi dari formasi mempunyai kandungan air yang sangat besar, bahkan bisa mencapai kadar lebih dari 90%. Air yang terproduksi ini merupakan air tanah (Groundwater) merupakan air yang berada di bawah permukaan tanah. Pada dasarnya air tanah dapat berasal dari air hujan (prespitasi), baik melalui proses infiltrasi secara langsung ataupun secara tak langsung dari air sungai, danau, rawa dan genangan air lainnya.
Clara Derlismawan Aritonang : Kesadahan : Analisa Dan Permasalahannya Untuk Air Industri, 2008. USU Repository © 2009
senyawa – senyawa dalam air dengan jumlah yang melebihi kelarutannya pada keadaan kesetimbangan. Salah satu senyawa tersebut antara lain adalah kalsium karbonat, yang memberikan konstribusi terbesar dalam proses terjadinya kerak dan korosi. (Effendi,H.2003)
Air yang diperlukan dalam dunia industri dapat diambil dari setiap titik dalam siklus hidrologis, tergantung teknologi yang dimiliki dan biaya yang tersedia untuk pengambilan dan untuk memperbaiki kualitasnya sehingga sesuai untuk penggunaannya.
Sumber-sumber air ; 1. Air Hujan
2. Air Permukaan 3. Air Tanah
Ditinjau dari sudut kualitasnya, secara singkat diuraikan sebagai berikut: 2.1.1 Air Hujan
Dalam lintasan jatuhnya air hujan mengabsorpsi gas-gas dan uap-uap yang terdapat diudara, terutama oksigen, nitrogen dan karbon dioksida, yang merupakan komponen-komponen utama dari udara.
Air hujan mempunyai sifat agresif terutama terhadap pipa-pipa penyalur maupun bak-bak penampungan air, sehingga hal ini akan mempercepat terjadinya korosi, dan air hujan juga bersifat lunak, sehingga boros terhadap pemakaian sabun. Maka untuk menjadikan air hujan sebagai sumber air minum hendaknya pada waktu mulai turun dibiarkan dan diendapkan terlebih dahulu, karena masih banyak mengandung kotoran.
Clara Derlismawan Aritonang : Kesadahan : Analisa Dan Permasalahannya Untuk Air Industri, 2008. USU Repository © 2009
Air permukaaan yang mencakup : air sungai, air danau, air kolam dapat merupakan kumpulan air hujan yang jatuh dan mengalir diatas permukaan tanah atau campuran antara lain aliran permukaan dan air tanah ataupun air yang mengalir ke luar pada musim kemarau.
Secara alamiah, sungai, danau, kolam dapat tercemar pada daerah permukaan air saja. Pada sungai yang besar dan arus air yang deras, sejumlah kecil bahaya pencemar akan mengalami pengenceran sehingga tingkat pencemaran menjadi sangat rendah.Di Indonesia air permukaan ini banyak digunakan sebagai sumber air minum tetapi harus diolah terlebih dahulu agar sesuai dengan standar baku mutu.
2.1.1.3 Air Tanah
Air tanah umumnya mengandung garam-garam terlarut. Jenis dan kadar garam-garam terlarut yang tergantung dalam air tanah adalah tergantung pada kondisi tanah dalam lintasan aliran air tanah.
Umumnya, kadar konstituen terlarut dalam air tanah adalah lebih tinggi jika dibandingkan dengan kadarnya pada air permukaan, disebabkan oleh lebih lamanya periode kontak antara air dan zat-zat yang dapat larut yang berada dalam lapisan tanah.
Konstituen utama yang terdapat dalam air tanah adalah : - Kation : Ca2+, Mg2+
- Anion : CO32-, HCO3-, Cl- dan NO3
-Konstituen-konstituen yang dapat dijumpai dalam kadar yang relatif rendah atau sangat rendah adalah : Fe2+, Mn2+, Al3+, F-.
Clara Derlismawan Aritonang : Kesadahan : Analisa Dan Permasalahannya Untuk Air Industri, 2008. USU Repository © 2009
mengalir melalui daerah yang kaya akan zat organik yang sifatnya dapat terurai, dapat kehilangan kandungan oksigen terlarutnya. Oksigen tersebut digunakan oleh mikroorganisme dalam perombakan zat organik. (Fardias,S.1992)
Diantara sumber-sumber air yang ditinjau tersebut, air permukaan dan air tanah merupakan sumber-sumber air yang paling luas penggunaanya sebagai sumber air untuk berbagai keperluan, keperluan industri maupun keperluan konsumsi domestik. Mata air juga merupakan bagian dari air tanah. Mata air adalah air tanah yang keluar dengan sendirinya kepermukaan tanah. Mata air ini hampir tidak terpengaruh oleh musim dan kualitasnya sama dengan keadaan air pada bagian dalamnya.
Air tanah banyak mengandung ion Kalsium (Ca) dan Magnesium (Mg) yang menyebabkan air bersifat sadah. Air tanah ini juga membawa dan melarutkan berbagai mineral apalagi karena sifatnya yang asam (CO2 terlarut). Air tersebut memiliki kemampuan membentuk padatan kalsium karbonat. Bila keasaman hilang, air akan bersifat sadah (sementara). Penggunaan air tanah cenderung membentuk kerak pada ketel. Walau tak menimbulkan korosi, air tanah sering banyak mengandung besi dan mangan. (Effendi,H.2003)
2.2 Pencemaran Air
Clara Derlismawan Aritonang : Kesadahan : Analisa Dan Permasalahannya Untuk Air Industri, 2008. USU Repository © 2009
tertentu yang menyebabkan air berkurang atau tidak dapat berfungsi lagi sesuai kegunaannya.
Air merupakan substrat yang paling parah akibat pencemaran. Berbagai jenis pencemaran baik yang berasal dari :
a. Sumber domestik( rumah tangga), perkampungan, kota, pasar, jalan, dan sebagainya.
b. Sumber non-domestik( pabrik, industri, pertanian, peternakan, perikanan serta sumber-sumber lainnya).
banyak memasuki badan air. Secara langsung ataupun tidak langsung pencemar tersebut akan berpengaruh terhadap kualitas air, baik untuk keperluan air minum, air industri atuapun keperluan lainnya. Berbagai cara dan usaha telah banyak dilakukan agar kehadiran pencemar terhadap air dapat dihindari, dikurangi atau minimal dapat dikendalikan. (Fardias,S.1992)
Masalah pencemaran serta efisiensi penggunaan sumber air, merupakan pokok persoalan yang paling banyak dibahas. Hal ini mengingat keadaan perairan alami dibanyak negara yang cenderung semakin menyusut dan menurun. Baik kualitas maupun kuantitasnya. Sehingga tidak berlebihan pendapat peserta bahwa dikemudian hari dunia akan dilanda krisis air seperti halnya krisis pangan, energi dan sebagainya. Bahkan untuk beberapa negara masalah kekurangan air sudah terjadi sejak lama.
Beberapa pokok-pokok yang ditekankan pada pengertian Pencemaran air meliputi dasar-dasar sebagai berikut :
Clara Derlismawan Aritonang : Kesadahan : Analisa Dan Permasalahannya Untuk Air Industri, 2008. USU Repository © 2009
tingkat/keadaan tertentu dapat membahayakan fungsi air dari badan air tersebut.
2. Bahwa masing-masing fungsi air dalam badan-badan air memiliki suatu “sandart kualitas” yang perlu ditentukan terlebih dahulu sebagai batasan sebelum dapat dilakukan suatu penilaian apakah suatu pencemaran pada suatu badan air itu terjadi atau tidak. Jelasnya, masing-masing badan air sesuai dengan fungsinya mempunyai standar kualitas sendiri-sendiri.
3. Masing-masing standar tersebut diatas masih perlu ditentukan pula secara lokal, nasional, atau internasional. Dasar-dasar pertimbangan yang digunakan untuk penentuan stndar tersebut bermacam-macam, tergantung pada dominasi sasaran yang akan dilindungi.
Karena air memiliki jaringan aliran yang luas (hydrological cycle), maka air yang berada di suatu tempat baik mengalir maupun menetap ( relatif) pada permukaan tanah disebut “Badan air”. Yang termasuk dalam klasifikasi badan air adalah sungai, waduk, saluran air, rawa-rawa dan lain-lain.( Suriawiria,U.1993)
2.3 Kesadahan
2.3.1 Pengertian Kesadahan
Clara Derlismawan Aritonang : Kesadahan : Analisa Dan Permasalahannya Untuk Air Industri, 2008. USU Repository © 2009
Air sadah umumnya digambarkan sebagai reaksi air terhadap sabun untuk menghasilkan busa atau kemampuan menimbulkan kerak pada pipa air panas, boiler, dan peralatan logam lainnya.
Kesadahan air sangat penting sehubungan dengan berbagai penggunaan air, karena kecenderungan membentuk kerak. Air yang kesadahannya amat rendah, dengan sedikit sabun saja telah berbuih banyak, tetapi jika terdapat kesadahan air tinggi, dapat menyebabkan pemborosan sabun. Kesadahan air harus optimum, karena apabila terlalu tinggi akan menimbulkan kerak, dan apabila terlalu rendah menyebabkan korosi pada suhu tinggi.
Kesadahan air bervariasi dari satu tempat dengan tempat lain. Umumnya, air permukaan lebih sadah dari pada air tanah. Kesadahan air bergantung pada formasi geologi alami dengan apa air tersebut mengalami kontak.Air yang sadah ditemukan di negara Inggris, Atlantik Selatan, Bagian Utara Pasifik. Lowa, India, Arizona, Mexico adalah negara yang memiliki kesadahan air cukup tinggi. (Sawyer and Mc Carty.1998)
Tabel 2.3.1 Klasifikasi air dengan tingkat kesadahannya, yaitu:
mg/l CaCO3 Tingkat kesadahan
0-75 Lembut
75-150 Agak Sadah
150-300 Sadah
>300 Sangat Sadah
2.3.2 Penyebab Kesadahan
Clara Derlismawan Aritonang : Kesadahan : Analisa Dan Permasalahannya Untuk Air Industri, 2008. USU Repository © 2009
kehadiran anion dalam air untuk membentuk kerak. Dalam prinsipnya kesadahan disebabkan kation antara lain, Ca2+, Mg2+ ,Sr2+, Fe2+, dan Mn2+.
Kesadahan air juga disebabkan kontak dengan tanah dan formasi bebatuan. Air hujan sebenarnya tidak memiliki kemampuan untuk melarutkan ion-ion penyusun kesadahan yang banyak terikat di dalam tanah dan batuan kapur, meskipun memiliki kadar karbondioksida yang relatif tinggi. Larutnya ion-ion yang dapat meningkatkan nilai kesadahan tersebut lebih banyak disebabkan oleh aktivitas bakteri didalam tanah, yang banyak mengeluarkan karbondioksida.
Keberadaan karbondioksida membentuk kesetimbangan dengan asam karbonat. Pada kondisi yang relatif asam, senyawa-senyawa karbonat yang terdapat di dalam tanah dan batuan kapur yang sebelumnya tidak larut berubah menjadi senyawa bikarbonat yang bersifat larut. Batuan kapur pada dasarnya tidak hanya menngandung karbonat, tetapi juga mengandung sulfat, klorida dan silikat. Ion-ion ini juga ikut terlarut dalam air.
2.3.3 Klasifikasi Kesadahan
Klasifikasi kesadahan berdasarkan dua cara, yaitu berdasarkan ion logam dan berdasarkan anion yang berasosiasi dengan ion logam. Berdasarkan ion logam, kesadahan dibedakan menjadi kesadahan kalsium dan kesadahan magnesium. Berdasarkan anion yang berasosiasi dengan ion logam, kesadahan dibedakan menjadi kesadahan karbonat dan kesadahan non-karbonat
2.3.3.1 Kesadahan Kalsium dan Magnesium
Clara Derlismawan Aritonang : Kesadahan : Analisa Dan Permasalahannya Untuk Air Industri, 2008. USU Repository © 2009
kation kalsium dan magnesium. Kesadahan kalsium dan magnesium sering kali perlu diketahui untuk menentukan jumlah kapur dan soda abu yang dibutuhkan dalam proses pelunakan air
(lime-soda ash softening). Jika nilai kesadahan kalsium diketahui maka kesadahan magnesium dapat ditentukan melalui persamaan.( Cole,G.A.1998)
Kesadahan Total – Kesadahan Kalsium = Kesadahan magnesium
Pada penentuan nilai kesadahan baik kesadahan total, kesadahan kalsium maupun kesadahan magnesium, keberadaan besi dan mangan dianggap sebagai penganggu karena dapat bereaksi dengan pereaksi yang digunakan. Oleh karena itu, kesadahan kalsium dianggap lebih besar dari kadar ion kalsium, dan sebaliknya. Untuk mendapatkan kadar ion kalsium dan ion magnesium dari nilai kesadahan, digunakan persamaan
Kadar Ca2+ (mg/liter) = 0,4 x kesadahan kalsium Kadar Mg2+ (mg/liter) = 0,243 x kesadahan magnesium ( Effendi,H.2003)
2.3.3.2 Kesadahan Karbonat dan Non-karbonat
Pada kesadahan karbonat, kalsium dan magnesium berasosiasi dengan ion CO32- dan HCO3-. Pada kesadahan non-karbonat, kalsium dan magnesium berasosiasi dengan ion SO42-, Cl-, dan NO3-. Kesadahan karbonat sangat sensitif terhadap panas dan mengendap dengan mudah pada suhu tinggi. Seperti reaksi berikut ini :
Ca(HCO3)2 CaCO3 endapan + CO2 + H2O
Clara Derlismawan Aritonang : Kesadahan : Analisa Dan Permasalahannya Untuk Air Industri, 2008. USU Repository © 2009
Oleh karena itu, kesadahan karbonat disebut juga kesadahan sementara. Kesadahan non-karbonat disebut kesadahan permanen karena kalsium dan magnesium yang berikatan dengan sulfat dan klorida tidak mengendap dan nilai kesadahan tidak berubah meskipun suhu tinggi.
Bagian dari total kesadahan yaitu ekuivalen dengan bikarbonat yang berperan serta dalam kehadiran alkalinitas karbonat sesuai dengan kesadahan karbonat. Sejak alkalinitas dan kesadahan ditentukan dalam CaCO3, kesadahan karbonat dapat dihitung berdasarkan :
Apabila alkalinitas total < kesadahan total : Maka kesadahan karbonat = alkalinitas total.
Apabila alkalinitas total ≥ kesadahan total : Maka kesadahan karbonat = kesadahan total.
Kesadahan non-karbonat=kesadahan total – kesadahan karbonat. (Sawyer and Mc Carty.1998)
Jika alkalinitas total melebihi kesadahan total maka sebagian dari anion penyusun alkalinitas (bikarbonat dan karbonat) berasosiasi dengan kation valensi satu (monovalent), misalnya kalium(K+) dan Natrium(Na+) yang tidak terdeteksi pada penentuan kesadahan. Sebaliknya, jika kesadahan total melebihi alkalnitas total maka sebagian dari kation penyusun kesadahan (kalsium dan magnesium) berikatan dengan sulfat (SO42-), klorida (Cl-), silikat( SiO32-) atau nitrat(NO3-) yang tidak terdeteksi pada penentuan alkalinitas. Oleh karena itu hubungan antara kesadahan dan alkalinitas tidak selalu positif; atau semakin besar kesadahan tidak selalu disertai dengan semakin tingginya alkalinitas dan sebaliknya.( Effendi,H.2003)
Clara Derlismawan Aritonang : Kesadahan : Analisa Dan Permasalahannya Untuk Air Industri, 2008. USU Repository © 2009
Kesadahan biasanya dinyatakan sebagai CaCO3. Beberapa metode telah digunakan untuk menganalisa kesadahan. Diantaranya ang biasa digunakan adalah : 2.4.1 Metode Total
Metode ini menghitung kesadahan berdasarkan konsentrasi ion – ion divalent dalam air, dianataranya Ca2+, Mg2+, dan Sr2+.
Perhitungan kesadahan berdasarkan konsentrasi ion-ion divalen tersebut menggunakan persamaan :
Contoh: Dari hasil analisa air diketahui kandungan ion-ionnya (mg/l) sebagai berikut: Hanya kation divalent ,Ca2+, Mg2+, dan Sr2+ yang diperhitungkan sebagai penyebab kesadahan, maka kesadahan total berdasarkan konsentrasi dan berat ekivalen masing-masing ion divalent kesadahan :
Tabel 2.4.1 Perhitungan Kesadahan Metode Total
Ion Divalen Konsentrasi (mg/l) Berat Ekivalen Kesadahan(mg/l)sebagai CaCO3
Ca2+ 15 20.0 (15)(50)/(20.0) = 37.5
Mg2+ 10 12.2 (10)(50)/(12.2) = 41.0
Sr2+ 2 43.8 (2)(50)/(43.8) = 2.3
Clara Derlismawan Aritonang : Kesadahan : Analisa Dan Permasalahannya Untuk Air Industri, 2008. USU Repository © 2009
2.4.2 Metode Titrasi EDTA
Titrasi kompleksometri meliputi reaksi pembentukan ion-ion kompleks ataupun pembentukan molekul netral yang terdisosiasi dalam larutan. Persyaratan mendasar terbentuknya kompleks demikian adalah tingkat kelarutannya tinggi. Titik akhir titrasi ditetapkan dengan indikator logam ataupun secara potensiometer dan spektrofotometri.(Khopkar,2003)
Metode ini menggunakan larutan EDTA (ethylenediamine tetra eacetic acid) sebagai larutan standarnya. Untuk mengetahui titik akhir titrasi digunakan indikator logam. Diantara indikator yang biasa digunakan adalah Eriochrome Black T (EBT). (Sawyer and Mc Carty.1998)
Eriochrome Black T sebagai indikator akan membentuk senyawa kompleks seluruhnya dengan EDTA yang ditambahkan, dengan kata lain kapan penambahan larutan EDTA mulai berlebih yang ditunjukkan oleh perubahan warna larutan dari merah menjadi biru. Reaksi ini berlangsung sempurna pada pH 8-10. Untuk mempertahankan larutan pada pH tersebut ditambahkan larutan buffer salmiak.Ca2+ dan Mg2+ akan membentuk senyawa kompleks warna merah anggur, dengan EBT.
M2+ + EBT (M EBT)kompleks merah anggur
Perubahan semakin jelas bila pH semakin tinggi, namun pH yang tinggi dapat menyebabkan ion-ion kesadahan hilang dari larutan, karena terjadi pengendapan Mg(OH)2 dan CaCO3. Pada pH >9, CaCO3 sudah mulai terbentuk.
Clara Derlismawan Aritonang : Kesadahan : Analisa Dan Permasalahannya Untuk Air Industri, 2008. USU Repository © 2009
BAB 3
Clara Derlismawan Aritonang : Kesadahan : Analisa Dan Permasalahannya Untuk Air Industri, 2008. USU Repository © 2009
Dalam penentuan kesadahan pada air formasi, digunakan metode titrasi EDTA. Penentuan kesadahan ini bertujuan untuk menganalisa pembentukan kerak yang terjadi pada dinding pipa.
3.1. Alat dan Bahan
3.1.1 Alat
− Alat-alat Gelas
− Kertas saring Whatman 42
− Botol
− Pemanas listrik
− Pengaduk magnetik
− Neraca analitis
3.1.2 Bahan-bahan
- Larutan Standart EDTA 0,02 M - Buffer Salmiak
- Indikator EBT
3.2 Prosedur Percobaan
3.2.1 Pembuatan Larutan
Clara Derlismawan Aritonang : Kesadahan : Analisa Dan Permasalahannya Untuk Air Industri, 2008. USU Repository © 2009
- Larutan Indikator EBT 10%, dibuat dengan melarutkan 10 gr indikator EBT dalam 100ml aquades.
- Larutan Standart EDTA 0.02 M
Timbang 7.4448 gram Titriplex ( ethylenediamine tetrae aceticacid), larutkan dalam gelas beaker 250 ml dengan aquades. Lalu dimasukkan kedalam labu takar 1000ml dan diencerkan sampai garis batas diaduk sampai homogen.
3.2.2 Cara Kerja
Dipipet 50 ml sampel lalu dimasukkan kedalam gelas erlenmeyer 250 ml, ditambahkan dengan larutan buffer salmiak, ditambahkan 5 tetes indikator EBT, kemudian dititrasi dengan larutan EDTA 0,02 M, hingga terjadi perubahan warna menjadi biru. Lalu catat volume larutan EDTA 0,02 M yang digunakan dan dihitung kesadahan Ca.
.
BAB 4
Clara Derlismawan Aritonang : Kesadahan : Analisa Dan Permasalahannya Untuk Air Industri, 2008. USU Repository © 2009
4. Hasil dan Pembahasan
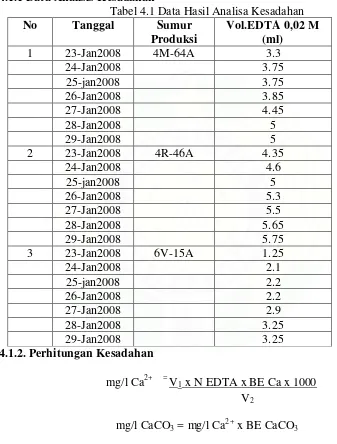
Pada pengukuran analisan kesadahan yang dilakukan selama Praktek Kerja Lapangan di PT.Clariant Indonesia Duri diperoleh data yang tertera pada table di bawah berikut :
4.1.1Data Analisis Kesadahan
Clara Derlismawan Aritonang : Kesadahan : Analisa Dan Permasalahannya Untuk Air Industri, 2008. USU Repository © 2009
N EDTA = 0,02
Berat Ekivalen Ca = 40,08 Berat Ekivalen CaCO3 = 2,4973
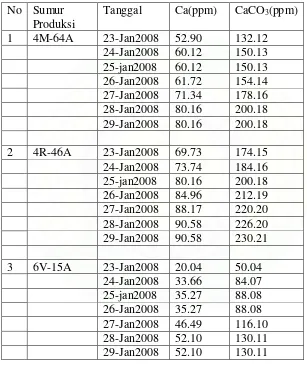
Setelah dilakukan perhitungan diperoleh kesadahan sebagai CaCO3 dalam tabel berikut ini :
Tabel 4.2 CaCO3 sebagai kesadahan No Sumur
Produksi
Tanggal Ca(ppm) CaCO3(ppm)
1 4M-64A 23-Jan2008 52.90 132.12
24-Jan2008 60.12 150.13 25-jan2008 60.12 150.13 26-Jan2008 61.72 154.14 27-Jan2008 71.34 178.16 28-Jan2008 80.16 200.18 29-Jan2008 80.16 200.18
2 4R-46A 23-Jan2008 69.73 174.15
24-Jan2008 73.74 184.16 25-jan2008 80.16 200.18 26-Jan2008 84.96 212.19 27-Jan2008 88.17 220.20 28-Jan2008 90.58 226.20 29-Jan2008 90.58 230.21
3 6V-15A 23-Jan2008 20.04 50.04
24-Jan2008 33.66 84.07 25-jan2008 35.27 88.08 26-Jan2008 35.27 88.08 27-Jan2008 46.49 116.10 28-Jan2008 52.10 130.11 29-Jan2008 52.10 130.11
Clara Derlismawan Aritonang : Kesadahan : Analisa Dan Permasalahannya Untuk Air Industri, 2008. USU Repository © 2009
Dari hasil analisa yang dilakukan selama praktek lapangan di PT. Clariant Indonesia-Duri, dapat dilihat kesadahan air sebagai CaCO3 dari tanggal 23-29 Januari 2008 adalah :
a. Pada sumur produksi 4M-64A. kadar kesadahannya antara : 132.12 mg/l – 200.18 mg/l.
b. Pada sumur produksi 4R-46A kadar kesadahannya antara 174.15 mg/l -230.21 mg/l.
c. Pada sumur produksi 6V-15A kadar kesadahannya adalah 50.04 mg/l – 130.11 mg/l.
Dari data diatas dapat terlihat kesadahan air pada air tanah yang digunakan perusahaan industri minyak bumi. Pada PT.Clariant ambang batas dari nilai kesadahan air ≤ 300mg/l, bila nilai kesadahan tersebut ≥ 300 mg/l dalam sumur produksi perlu disuntikkan bahan kimia yang berfungsi untuk mengatasi nilai kesadahan air tersebut. Data diatas terlihat bahwa kesadahan belum mencapai nilai maksimum , hal ini dikarenakan adanya pengaruh penambahan bahan kimia yang digunakan pada proses pengolahan.
Kesadahan air harus optimum, karena apabila terlalu tinggi akan menimbulkan kerak dalam bentuk endapan CaCO3 dan jika terlalu tinggi akan menyebabkan korosi pada suhu tinggi.
Nilai kesadahan air diperlukan dalam penilaian kelayakan air tersebut. Nilai kesadahan juga digunakan sebagai dasar bagi pemilihan metode yang diterapkan dalam proses pelunakan(softening) air. (Fardias,S.1992)
Clara Derlismawan Aritonang : Kesadahan : Analisa Dan Permasalahannya Untuk Air Industri, 2008. USU Repository © 2009
Clara Derlismawan Aritonang : Kesadahan : Analisa Dan Permasalahannya Untuk Air Industri, 2008. USU Repository © 2009
BAB 5
KESIMPULAN DAN SARAN
5.1 Kesimpulan
- Kesadahan sebagai CaCO3 yang diperoleh dari hasil titrasi yang dilakukan pada bulan Januari 2008 adalah pada sumur produksi :
a. Pada sumur produksi 4M-64A. kadar kesadahannya antara : 132.12 mg/l – 200.18 mg/l.
b. Pada sumur produksi 4R-46A kadar kesadahannya antara 174.15 mg/l -230.21 mg/l.
c. Pada sumur produksi 6V-15A kadar kesadahannya adalah 50.04 mg/l – 130.11 mg/l.
- Pada ketiga sumur produksi tersebut belum terjadi pembentukan kerak yang disebabkan endapan CaCO3, sehingga bahan kimia yang digunakan untuk mengatasi terjadinya endapan CaCO3 tidak perlu diberikan karena belum melewati nilai maksimum yang keluarkan PT.Clariant yaitu 300 mg/liter.
Clara Derlismawan Aritonang : Kesadahan : Analisa Dan Permasalahannya Untuk Air Industri, 2008. USU Repository © 2009
Clara Derlismawan Aritonang : Kesadahan : Analisa Dan Permasalahannya Untuk Air Industri, 2008. USU Repository © 2009
DAFTAR PUSTAKA
Alaerts,G.,dan Sri S.S.1997. Metode Penelitian Air , Usaha Nasional, Surabaya. Cole,G.A.1998.Text Book of Limnology , Thirdt Edition, Waveland Press, Inc.,
Illions, USA.
Effendi,H.2003. Telaah Kualitas Air , Kanisius, Yogyakarta. Fardias,S.1992, Polusi Air dan Udara , Penerbit Kanisius, Bogor. Khopkar,S.M.2003.Konsep Dasar Kimia Analitik, UI-Press,Jakarta.
Sawyer and Mc Carty.1998, Chemistry For Environmental Engineering , 3th Edition, Mc Graw Hill- KOGAKUSHA LTD, TOKYO.
Suriawiria,U.1993, Mikrobiologi Air , Edisi Kedua, Cetakan Pertama, Penerbit Alumni, Bandung.