DIFERENSIASI KELAMIN DAN PERFORMANSI
TIGA GENOTIPE IKAN NILA YANG DIBERI BAHAN
AROMATASE INHIBITOR HINGGA TAHAP
PEMBESARAN
DIDIK ARIYANTO
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
PERNYATAAN MENGENAI TESIS
DAN SUMBER INFORMASI
Dengan ini saya menyatakan bahwa tesis Diferensiasi Kelamin dan Performansi Tiga Genotipe Ikan Nila yang diberi Bahan Aromatase Inhibitor
hingga Tahap Pembesaran adalah karya saya dengan arahan dari komisi pembimbing dan belum diajukan dalam bentuk apa pun kepada perguruan tinggi mana pun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam daftar pustaka di bagian akhir tesis ini.
Bogor, Januari 2010
ABSTRACT
DIDIK ARIYANTO. Sex Differensiation and Performance of Three Genotypes of Nile Tilapia Administered with Aromatase Inhibitor until The Grow-out Period. Under direction of KOMAR SUMANTADINATA and AGUS OMAN SUDRAJAT .
Tilapias are endemic to Africa, but interest in their aquacultural potential led to nearly worldwide distribution within more than the past fifty years. The desirability of monosex populations for tilapia culture is well established. Grow-out of monosex male populations prevents or minimizes recruitment and thereby competition between recruits and stocked fish which, in mixed sex populations, can significantly reduce harvested yields. This study conducted to know the effect of dietary administration of aromatase inhibitor imidazole for sex reversal in three genotypes of Nile tilapia i.e. XX, XY and YY genotype. Sex reversed tilapia with methyl-testosterone was used as positive control. Application of imidazole was given to 7 days after-hatching larvae for 28 days. Both of control negative and mixed sex population were fed a standard commercial ration. We also want to evaluate the performance of these populations in growing period in ponds. Mixed sex population, consisting of 50% XX genotype and 50% XY genotype was used as check population. The results showed that dietary administration of imidazole in XX genotype were significantly increased male proportion.The same treatment in XY genotype did not significantly increased the proportion of male but significantly increased male proportion in YY genotype. Until the end of fingerling rearing period, all genotypes and treatments did not significantly affect on both of growth and survival rate, except in YY genotype.Over the grow-out culture period of 120 days, all male populations especially in XY genotype and sex reversed from XX genotype have a better both of growth rate and harvest yield than those of all female and mixed sex populations. All genotypes and all treatments did not significantly affect on size variability, survival rate and food conversion ratios, except in YY genotype. Generally, YY genotype has a lowest performance until the end of grow-out period.
RINGKASAN
DIDIK ARIYANTO. Diferensiasi Kelamin dan Performansi Tiga Genotipe Ikan Nila yang diberi Bahan Aromatase Inhibitor hingga Tahap Pembesaran. Dibimbing oleh KOMAR SUMANTADINATA dan AGUS OMAN SUDRAJAT.
Laju pertumbuhan ikan nila dipengaruhi oleh jenis kelamin (sexual dimorphism). Ikan nila jantan mempunyai laju pertumbuhan lebih cepat dibanding ikan betina sehingga budidaya menggunakan populasi tunggal kelamin jantan diharapkan mempunyai produktivitas lebih baik dibanding populasi campuran. Salah satu metode produksi masal benih ikan nila tunggal kelamin jantan adalah dengan menambahkan hormon sintetik 17a-methyltestosterone. Namun demikian, saat ini penggunaan bahan sintetik tersebut sudah sangat dibatasi. Selain karena bersifat karsinogenik, hormon tersebut berpotensi menimbulkan pencemaran lingkungan. Dalam rangka mendapatkan bahan alternatif penggantinya, dilakukan penelitian pemanfaatan bahan aromatase inhibitor, khususnya imidazole. Bahan ini dapat digunakan dalam proses pembalikan kelamin karena menghambat sekresi enzim aromatase yang bertanggung jawab dalam konversi hormon androgen menjadi estrogen. Tingginya kadar androgen dalam tubuh akan mengarahkan proses diferensiasi kelamin ke arah kelamin jantan. Beberapa kegiatan penelitian sex reversal, umumnya menggunakan bahan genotipe campuran antara XX dan XY sehingga akurasi tingkat efektivitas dan efisiensi bahan aktif yang digunakan tidak optimal. Selain itu, sebagain besar penelitian sex reversal berhenti pada hasil nisbah kelamin yang diperoleh. Evaluasi performansi banih yang dihasilkan melalui kegiatan sex reversal, kaitannya dengan kegiatan akuakultur belum banyak dilakukan. Penelitian ini bertujuan untuk mengetahui pengaruh penambahan bahan aromatase inhibitor, khususnya imidazole terhadap tiga genotipe ikan nila, yaitu genotipe XX, XY dan YY, khususnya terhadap nisbah kelamin yang dihasilkan, laju pertumbuhan serta tingkat sintasan sampai tahap pendederan. Selain itu, penelitian ini juga bertujuan untuk mengevaluasi performansi benih tiga genotipe ikan nila yang diberi imidazole tersebut sampai tahap pembesaran, khususnya pada karakter laju pertumbuhan, sintasan, keragaman ukuran, food conversion ratios, bobot panen dan perkembangan organ reproduksi.
dalam jaring ukuran 4x4x1,5 m yang ditempatkan di kolam. Pemeliharaan tahap pembesaran dilakukan selama 120 hari.
Hasil penelitian menunjukkan bahwa penambahan imidazole secara nyata meningkatkan rasio kelamin jantan, khususnya pada genotipe XX, yaitu mencapai 82,44%. Populasi kontrol (-) genotipe XX mempunyai persentase kelamin jantan sebesar 7,55%. Penambahan hormon 17a-mt sebagai kontrol (+) menghasilkan persentase kelamin jantan sebesar 82,42% tidak berbeda nyata dibanding pemberian imidazole. Pemberian imidazole dan hormon 17a-mt pada genotipe XY, meskipun tidak terlalu nyata tetapi juga meningkatkan rasio kelamin jantan, yaitu mencapai 82,03 dan 85,13 % dari populasi kontrol (-) genotipe XY sebesar 79,81%. Namun demikian, perlakuan yang sama pada genotipe YY secara signifikan meningkatkan rasio kelamin jantan mencapai 97,12 dan 99,10 % dari kontrol (-) genotipe YY sebesar 83,01%. Sampai akhir tahap pendederan, semua perlakuan dan genotipe yang berbeda tidak memberikan efek yang berbeda nyata terhadap laju pertumbuhan maupun nilai sintasan, kecuali pada genotipe YY yang mempunyai bobot dan sintasan paling rendah. Pada tahap pembesaran, penggunaan populasi tunggal kelamin jantan selain genotipe YY, yaitu genotipe XY maupun genotipe XX yang diberi imidazole mempunyai laju pertumbuhan dan hasil panen lebih baik dibandingkan populasi populasi campuran XX- XY, masing-masing sebesar 38,14 dan 23,58%. Sampai akhir tahap pembesaran, semua perlakuan dan genotipe yang berbeda tidak memberikan dampak yang berbeda nyata terhadap nilai keragaman ukuran, sintasan maupun nilai food conversion ratios, kecuali pada genotipe YY. Rendahnya laju pertumbuhan, sintasan dan hasil panen serta tingginya tingkat keragaman ukuran dan nilai food conversion ratios pada genotipe YY disebabkan tingkat inbreeding yang tinggi pada populasi tersebut. Selama kegiatan penelitian, organ reproduksi pada semua populasi berkembang normal. Populasi campuran genotipe XX- XY mempunyai perkembangan organ reproduksi lebih cepat dibanding populasi tunggal kelamin.
@ Hak cipta milik IPB, tahun 2010
Hak cipta dilindungi Undang-Undang
Dilarang mengutip sebagian atau seluruh karya tulis ini tanpa mencantumkan atau menyebutkan sumbernya.Pengutipan hanya untuk kepentingan pendidikan, penelitian, penulisan karya ilmiah, penyusunan laporan, penulisan kritik atau tinjauan suatu masalah; dan pengutipan tersebut tidak merugikan kepentingan yang wajar IPB.
DIFERENSIASI KELAMIN DAN PERFORMANSI
TIGA GENOTIPE IKAN NILA YANG DIBERI BAHAN
AROMATASE INHIBITOR HINGGA TAHAP
PEMBESARAN
DIDIK ARIYANTO
Tesis
Sebagai salah satu syarat untuk memperoleh gelar Magister Sains pada
Program Studi Ilmu Akuakultur
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
Judul Tesis : Diferensiasi Kelamin dan Performansi Tiga Genotipe Ikan Nila yang diberi Bahan Aromatase Inhibitor hingga Tahap Pembesaran
Nama : Didik Ariyanto
NRP : C151070181
Komisi Pembimbing
Dr. Ir. Agus Oman Sudrajat, M.Sc. Prof. Dr. Ir. Komar Sumantadinata, M.Sc.
Anggota Ketua
Diketahui
Ketua Program Studi Ilmu Akuakultur
Dekan Sekolah Pascasarjana IPB
Prof. Dr. Ir. Enang Harris, M.Si. Prof. Dr. Ir. Khairil A. Notodiputro, M.S.
PRAKATA
Puji dan syukur penulis panjatkan kepada Allah SWT atas segala rahmat dan karunia-Nya sehingga tesis ini bisa diselesaikan. Tema yang dipilih dalam penelitian yang dilakukan sejak bulan Oktober 2008 ini adalah teknik sex reversal
ikan nila dan performansi benih ikan hasil sex reversal dalam kegiatan budidaya, dengan judul ”Diferensiasi Kelamin dan Performansi Tiga Genotipe Ikan Nila yang diberi Bahan Aromatase Inhibitor hingga Tahap Pembesaran”.
Terima kasih penulis ucapkan kepada Bapak Prof. Dr. Ir. Komar Sumantadinata, MSc. dan Bapak Dr. Ir. Agus Oman Sudrajat, MSc., selaku pembimbing. Disamping itu, terima kasih juga disampaikan kepada Komisi Pengembangan SDM Badan Riset Kelautan dan Perikanan, DKP atas kesempatan dan beasiswa untuk mengikuti Program Magister Ilmu Akuakultur, di IPB dan juga kepada Ibu Ir. Retna Utami, MSc., selaku Kepala Loka Riset Pemuliaan dan Teknologi Budidaya Perikanan Air Tawar, Sukamandi atas segala dukungan dana dan fasilitas penelitian serta masukannya. Terima kasih juga disampaikan kepada Dr. Ir. Mennofatria Boer atas saran dan masukannya dalam analisis statistik hasil penelitian. Ungkapan terima kasih juga disampaikan kepada teman-teman peneliti dan teknisi di Loka Riset Pemuliaan dan Teknologi Budidaya Perikanan Air Tawar, Sukamandi dan juga teman-teman di Program Studi Ilmu Akuakultur, IPB atas segala kebersamaan dan dukungannya. Selain itu, kepada ibu, bapak (alm.), saudara-saudaraku, istri dan anak-anakku, terima kasih atas segala doa, dorongan dan kasih sayang yang tiada terhingga.
Semoga karya ilmiah ini bermanfaat dalam pengembangan ilmu pengetahuan pada umumnya dan bidang akuakultur pada khususnya.
Bogor, Januari 2010
RIWAYAT HIDUP
Penulis dilahirkan pada tanggal 29 Maret 1973 di Kulonprogo, D.I. Yogyakarta, merupakan putra ke 4 dari 4 bersaudara, anak dari pasangan Bapak Sadiyo dengan Ibu Siswantinah.
DAFTAR ISI
Halaman
DAFTAR TABEL ………. xii
DAFTAR GAMBAR ..………. xiii
DAFTAR LAMPIRAN .……….. xiv
PENDAHULUAN ... Latar Belakang .……….. Perumusan Masalah ……… Tujuan .……… Hipotesis …….……… 1 3 4 5 TINJAUAN PUSTAKA ... Ikan Nila ... Determinasi dan Diferensiasi kelamin ... Sex Reversal ... Hormon Steroid ... Aromatase dan Aromatase Inhibitor ... Genetically Male Tilapia ... 6 7 8 8 9 11 BAHAN DAN METODE ………... Tempat dan Waktu ...………... Bahan Penelitian ... Metode Percobaan 1 ... Pengamatan ... Analisis Data ... Metode Percobaan 2 ... Pengamatan ... Analisis Data ... 12 12 12 14 15 15 16 18 HASIL DAN BAHASAN ... Percobaan tahap 1 ... Percobaan tahap 2 ... 20 29 KESIMPULAN ... 47
SARAN ... 47
DAFTAR PUSTAKA ... 48
DAFTAR TABEL
Halaman
1. Persentase kelamin jantan, bobot individu rata-rata dan sintasan
benih ikan nila pada akhir tahap pendederan ………... 21
2. Hasil analisis kualitas air media pemeliharaan ikan nila di akuarium dan kolam pendederan …..…... 21
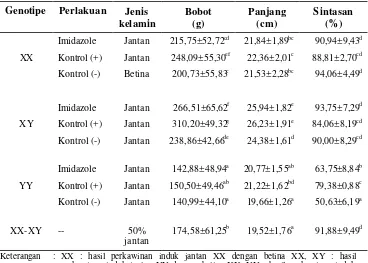
3. Bobot dan panjang akhir individu serta sintasan ikan nila pada akhir
tahap pembesaran ………....……… 30
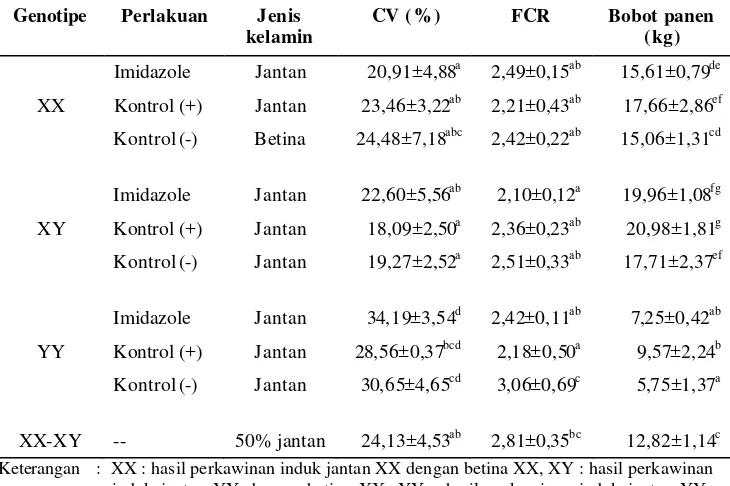
4. Hasil analisis coefficient of variance (CV) karakter bobot, food corversion ratios (FCR) dan bobot panen ikan nila pada akhir tahap
pembesaran ………..……… 31
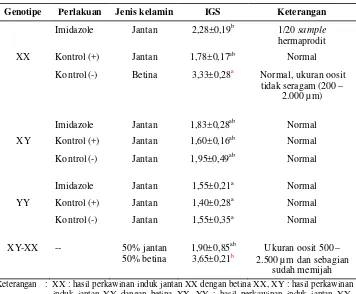
5. Indeks gonad somatik (IGS) ikan nila pada akhir tahap pembesaran .. 35
6. Hasil analisis kualitas air media pemeliharaan ikan nila selama tahap
DAFTAR GAMBAR
Halaman
1. Ikan nila dewasa ... 6
2. Skema pelaksanaan penelitian dari percobaan tahap 1 sampai tahap 2 ………... 19
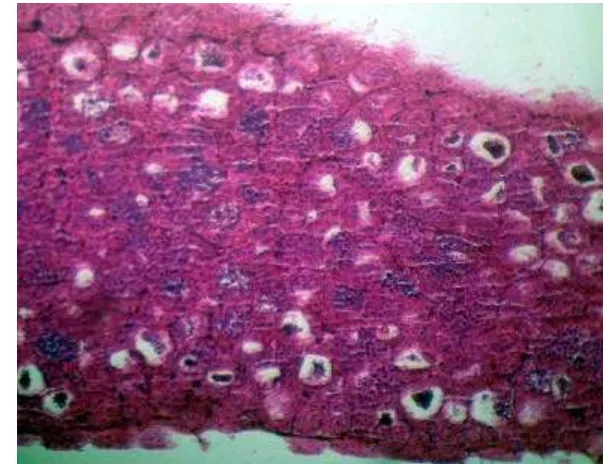
3. Hasil analisis histologis ovari ikan nila dari populasi tunggal kelamin betina XX, umur 95 hari ... 28
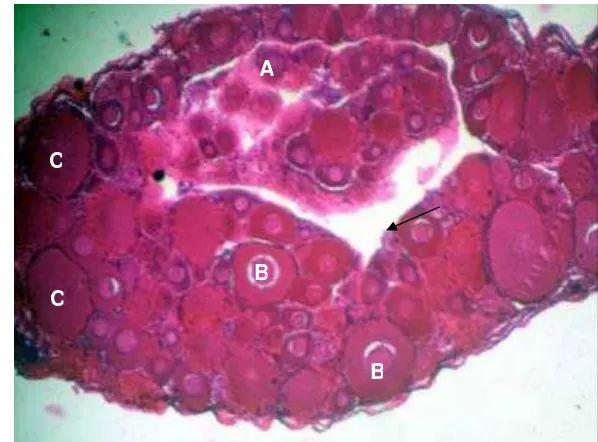
4. Hasil analisis histologis ovari ikan nila dari populasi campuran XX-XY, umur 95 hari ... 29
5. Pola pertumbuhan populasi ikan nila genotipe XX, XY dan YY tanpa perlakuan, penambahan hormon 17a-mt serta penambahan
imidazole ...………. 35
6. Hasil analisis histologis gonad ikan nila genotipe XX yang diberi imidazole ……... 36
7. Hasil analisis histologis gonad ikan nila genotipe XX yang diberi hormon 17a-mt ... 36
8. Hasil analisis histologis gonad ikan nila genotipe XX pada populasi tunggal kelamin betina ………... 37
9. Hasil analisis histologis gonad ikan nila genotipe XY yang diberi imidazole ……... 37
10. Hasil analisis histologis gonad ikan nila genotipe XY yang diberi hormon 17a-mt ... 38
11. Hasil analisis histologis gonad ikan nila genotipe XY ... 38
12. Hasil analisis histologis gonad ikan nila genotipe YY yang diberi imidazole ……... 39
13. Hasil analisis histologis gonad ikan nila genotipe YY yang diberi hormon 17a-mt ... 39
14. Hasil analisis histologis gonad ikan nila genotipe YY ... 40
15 Hasil analisis histologis gonad ikan nila betina pada populasi campuran ……... 40
DAFTAR LAMPIRAN
Halaman
1. Jumlah kebutuhan ikan uji dan sarana penelitian ... 55
2a. Analysis of variance (ANOVA) untuk persentase kelamin jantan ikan nila pada akhir tahap pendederan …...……...
56
2b. Analisis Duncan untuk persentase kelamin jantan ikan nila pada akhir tahap pendederan ……….………
56
3a. Analysis of variance (ANOVA) untuk bobot ikan nila pada akhir pendederan ……….………
57
3b. Analisis Duncan untuk bobot ikan nila pada akhir tahap pendederan 57
4a. Analysis of variance (ANOVA) untuk sintasan ikan nila pada akhir pendederan ………..………..
58
4b. Analisis Duncan untuk sintasan ikan nila pada akhir pendederan …. 58
5a. Analysis of variance (ANOVA) untuk bobot ikan nila pada akhir tahap pembesaran ………...………
59
5b. Analisis Duncan untuk bobot ikan nila pada akhir tahap pembesaran ………....
59
6a. Analisys of variance (ANOVA) untuk panjang total ikan nila pada akhir tahap pembesaran ……….
60
6b. Analisis Duncan untuk panjang total ikan nila pada akhir tahap pembesaran ....…. ……….
60
7a. Analysis of variance (ANOVA) untuk keragaman fenotip benih ikan nila pada akhir tahap pembesaran …………..………
61
7b. Analisis Duncan untuk keragaman fenotip ikan nila pada akhir tahap pembesaran ………...………
61
8a. Analysis of variance (ANOVA) untuk sintasan ikan nila pada akhir tahap pembesaran ………..
62
8b. Analisis Duncan untuk sintasan ikan nila pada akhir pembesaran .... 62
9a. Analysis of variance (ANOVA) untuk FCR ikan nila pada akhir tahap pembesaran ………..
9b. Analisis Duncan untuk FCR ikan nila pada akhir tahap pembesaran 63
10a. Analysis of variance (ANOVA) untuk bobot panen ikan nila pada akhir tahap pembesaran ……….
64
10b. Analisis Duncan untuk bobot total panen pada akhir tahap pembesaran ………...
64
11a. Analysis of variance (ANOVA) untuk nilai indeks gonad somatik (IGS) benih ikan nila pada akhir pembesaran (benih berumur 215 hari) ... 65
11b. Analisis Duncan untuk nilai indeks gonad somatik (IGS) benih ikan nila jantan pada akhir pembesaran (benih berumur 215 hari) ……. 65
11c. Analisis Duncan untuk nilai indeks gonad somatik (IGS) benih ikan nila betina pada akhir pembesaran (benih berumur 215 hari) …….
65
PENDAHULUAN
Latar Belakang
Ikan nila (Oreochromis niloticus) merupakan salah satu jenis ikan tilapia yang indigenous di Benua Afrika. Namun demikian, pada saat ini ikan nila telah menyebar di berbagai negara di dunia termasuk Indonesia (Popma & Lovshin
1995). Secara global, ikan tilapia merupakan salah satu komoditas penting dengan
produksi dan kebutuhan yang semakin meningkat (Fitzsimmons 2008).
Departemen Kelautan dan Perikanan (DKP) juga menempatkan ikan nila sebagai
salah satu ikan budidaya air tawar yang mempunyai nila i ekonomis penting dan
merupakan salah satu dari 10 komoditas utama kegiatan budidaya.
Secara biologis, laju pertumbuhan ikan nila jantan lebih cepat
dibandingkan dengan ikan nila betina (sexual dimorphism) (Popma & Masser 1999). Data-data empiris pada budidaya ikan nila menunjukkan penggunaan
populasi tunggal kelamin (mono-sex) jantan akan memberikan produksi lebih baik dibandingkan populasi campuran (mixed-sex) (Rakocy & McGinty 1989; Tave 1993; Tave 1996; Chapman 2000; Dunham 2004; Gustiano 2006). Selain
disebabkan oleh fenomena sexual dimorphism, budidaya ikan nila menggunakan benih dengan kelamin jantan dan betina yang dicampur juga mengalami
pertumbuhan yang relatif lebih lambat. Hal ini karena terjadinya kematangan
kelamin dini pada populasi campuran (Mair et al. 1995). Dijelaskan lebih lanjut bahwa kematangan kelamin dini tersebut dapat menghambat pertumbuhan
populasi karena energi yang digunakan untuk pertumbuhan sebagian terbagi untuk
perkembangan kematangan gonad. Selain itu, adanya anakan yang tidak
dikehendaki pada populasi kelamin campuran juga mengakibatkan energi yang
harus dikeluarkan dalam rangka kompetisi mencari makan semakin besar.
Dampak yang terjadi adalah rendahnya biomasa ikan pada waktu panen yang
dapat mencapai 30-50%. Untuk menghindari fenomena yang merugikan tersebut,
perlu dilakukan budidaya ikan nila tunggal kelamin, khususnya tunggal kelamin
jantan.
Salah satu metode untuk mendapatkan populasi ikan nila tunggal kelamin
reversal. Teknik sex reversal pada ikan nila yang banyak dilakukan adalah dengan penambahan hormon sintetik 17a-methyltestosterone (17a-mt). Hasil penelitian
menunjukkan bahwa penambahan hormon 17a-mt pada pakan dengan dosis 40-60
mg/kg pakan selama 3-4 minggu pada benih ikan nila berumur 7-9 hari setelah
menetas efektif untuk sex reversal dan mampu menghasilkan populasi jantan mendekati 100% ( Bowker et al. 2007). Namun berdasarkan Surat Keputusan Menteri Kelautan dan Perikanan nomor KEP.20/MEN/2003, hormon 17a-mt
termasuk dalam klasifikasi obat keras yang berarti bahwa peredaran dan
pemanfaatannya menjadi semakin dibatasi terkait dengan dampak negatif yang
dapat ditimbulkan, baik kepada ikan, manusia maupun lingkungan. Hormon
17a-mt yang notabene merupakan hormon sintetik bersifat karsinogenik bagi manusia.
Selain itu, hormon ini juga berpotensi menimbulkan pencemaran lingkungan
karena sulit terdegradasi secara alami. Contreras-S?ncez et al. (2001) melaporkan bahwa residu anabolik 17a-mt masih tertinggal dalam sedimen kolam setelah 3
bulan penggunaannya pada maskulinisasi benih ikan nila.
Dalam rangka menggantikan fungsi hormon 17a-mt, mulai dikembangkan
penggunaan bahan-bahan alternatif yang lebih aman untuk “dikonsumsi”. Salah
satu bahan alternatif yang mulai banyak digunakan adalah bahan aromatase
inhibitor. Aromatase inhibitor adalah bahan kimia yang mampu menghambat sekresi enzim aromatase yang berperan dalam sintesis estrogen dari androgen.
Penghambatan ini akan menyebabkan tidak aktifnya proses transkripsi gen-gen
aromatase yang mengakibatkan mRNA tidak terbentuk, sehingga terjadi
penurunan konsentrasi estrogen yang mengarah pada tidak aktifnya transkripsi
dari gen aromatase sebagai feedback-nya (Sever et al. 1999). Penurunan rasio estrogen terhadap androgen menyebabkan terjadinya perubahan penampakan dari
betina menjadi menyerupai jantan, atau terjadi maskulinisasi karakteristik seksual
sekunder.
Penelitian pemanfataan bahan aromatase inhibitor untuk sex reversal ikan di Indonesia telah dilakukan pada beberapa spesies ikan antara lain pada ikan lele
varietas Sangkuriang (Jufrie 2006; Utomo 2006), udang galah (Sarida 2006), ikan
pada spesies ikan nila, menunjukkan bahwa bahan aromatase inhibitor berhasil meningkatkan nisbah kelamin jantan antara 65-85%. Pada umumnya, penelitian
dilakukan menggunakan bahan uji berupa larva ikan nila hasil pemijahan normal
yang terdiri atas genotipe campuran XX dan XY. Hal ini berimplikasi terhadap
tidak akuratnya tingkat efektifitas dan efisiensi bahan aromatase inhibitor yang digunakan untuk sex reversal dalam meningkatkan persentase kelamin jantan. Selain itu, penelitian yang dilakukan berhenti sampai dengan diperolehnya nisbah
kelamin ikan nila setelah diberi perlakuan, sedangkan evaluasi performansi benih
ikan nila hasil sex reversal terutama pada tahap pembesaran belum dilakukan. Selain melalui metode sex reversal, produksi benih ikan nila tunggal kelamin jantan juga dapat dilakukan dengan menggunakan induk jantan super
(supermale). Program pembentukan induk ikan nila jantan super di Indonesia telah berhasil dengan dilepasnya varietas GESIT (Genetically Supermale of Indonesian Tilapia) oleh Balai Besar Pengembangan Budidaya Air Tawar, Sukabumi pada tahun 2006. Induk jantan super yang bergenotipe YY jika
dikawinkan dengan induk betina normal dengan genotipe XX akan menghasilkan
keturunan 100% bergenotipe XY atau biasa disebut GMT (Genetically Male Tilapia).
Perumusan Masalah
Aplikasi hormon sintetik 17a-mt untuk sex reversal ikan nila sudah dilarang. Dalam rangka mencari bahan alternatif yang aman, telah dilakukan
beberapa penelitian menggunakan bahan aromatase inhibitor, khususnya imidazole. Sebagian besar penelitian pemanfaatan imidazole untuk sex reversal
menggunakan bahan ikan nila genotipe campuran XX dan XY hasil pemijahan
normal dalam proporsi yang tidak tetap. Hal ini menyebabkan efektivitas dan
efisiensi bahan aromatase inhibitor dalam mengarahkan pembentukan kelamin jantan suatu populasi ikan nila menjadi bias. Selain itu, penelitian yang dilakukan
dititikberatkan pada pengaruh bahan aromatase inhibitor terhadap peningkatan nisbah kelamin jantan yang dihasilkan, sedangkan dampak penggunaan bahan
tersebut terhadap performansi benih jantan yang dihasilkan, kaitannya dengan
produksi pada waktu panen belum dilakukan. Dalam rangka mengatasi
permasalahan tersebut, perlu dilakukan penelitian sex reversal menggunakan bahan ikan nila tunggal genotipe (XX, XY dan YY). Selain itu, juga perlu
dilakukan penelitian secara komprehensif untuk mengetahui pengaruh pemberian
bahan aromatase inhibitor terhadap nisbah kelamin yang dihasilkan serta mengevaluasi dampak pemberian bahan tersebut terhadap performansi benih yang
dihasilkan mulai dari larva sampai tahap pembesaran.
Di sisi lain, keberhasilan pembentukan induk jantan super ikan nila di
Indonesia memungkinkan produksi masal benih tunggal kelamin jantan dapat
dilakukan dengan ”aman”. Pemijahan induk jantan super dengan betina normal
akan menghasilkan benih tunggal kelamin jantan genotipe XY. Aplikasi di
lapangan menunjukkan bahwa tidak 100% genotipe XY bekelamin fenotipe
jantan. Dalam rangka menjawab permasalahan tersebut, perlu dilakukan penelitian
mengenai pengaruh penambahan bahan aromatase inhibitor untuk meningkatkan persentase kelamin jantan pada populasi turunan induk jantan super yang
bergenotipe XY. Selain itu, performansi benih berkelamin jantan anakan induk
jantan super ini jika dibandingkan dengan benih berkelamin jantan hasil sex reversal juga belum banyak diketahui.
Evaluasi performansi ikan nila genotipe YY, turunan induk jantan super
genotipe XY dan populasi hasil sex reversal genotipe XX hingga tahap pembesaran ini dilakukan dalam rangka mengetahui benih-benih ikan nila terbaik
yang akan digunakan untuk kegiatan budidaya.
Tujuan
1. Mengetahui pengaruh pemberian bahan aromatase inhibitor terhadap nisbah kelamin, bobot individu rata-rata dan sintasan benih tiga genotipe (XX, XY
dan YY) ikan nila sampai tahap pendederan.
2. Mengevaluasi dampak pemberian bahan aromatase inhibitor terhadap performansi benih meliputi bobot dan panjang individu, keragaman ukuran,
Hipotesis
1. Pemberian bahan aromatase inhibitor berpengaruh terhadap nisbah kelamin, bobot individu dan sintasan benih tiga genotipe (XX, XY dan YY) ikan nila
sampai tahap pendederan.
2. Pemberian bahan aromatase inhibitor berdampak terhadap bobot dan panjang individu, keragaman ukuran, sintasan, food conversion ratio, bobot panen serta perkembangan organ reproduksi tiga genotipe (XX, XY dan YY) ikan
TINJAUAN PUSTAKA
Ikan nila
Ikan nila (Oreochromis niloticus) termasuk dalam family Chiclidae. Ciri yang spesifik pada ikan nila adalah adanya garis vertikal berwarna gelap di tubuh
berjumlah 6-9 buah dan di sirip ekor sebanyak 6-7 buah. Garis-garis tersebut juga
ditemui di sirip punggung dan sirip dubur (Trewavas 1983).
Gambar 1. Ikan nila dewasa
Dilihat dari ciri kelamin primer, ikan nila jantan dan betina dapat
dibedakan berdasarkan jumlah lubang di sekitar anus. Pada ikan nila jantan
terdapat 2 lubang yaitu lubang anus dan lubang urogenital, sedangkan pada ikan
nila betina terdapat 3 lubang yaitu lubang anus, lubang ureter dan lubang genital.
Ciri kelamin sekunder biasanya ditunjukkan dengan ukuran ikan jantan yang lebih
besar dibanding dengan ikan betina (Rokhmulyenti 2003).
Pada ikan nila terdapat fenomena sexual dimorphism, yaitu suatu kondisi yang menunjukkan bahwa pertumbuhan ikan nila jantan lebih cepat dibandingkan
dengan ikan betina. Popma dan Masser (1999) menyebutkan bahwa laju
pertumbuhan ikan nila jantan 2 kali lebih cepat dibandingkan dengan ikan nila
betina. Ditambahkan oleh Griffin (2005) bahwa selain tumbuh lebih cepat, nila i
rasio konversi pakan ikan nila jantan juga lebih baik dibanding ikan nila betina.
Beberapa penelitian lainnya juga melaporkan bahwa budidaya ikan nila tunggal
lebih cepat (Rakocy & McGinty 1989; Tave 1993; Mair et al. 1995; Tave 1996; Chapman 2000; Dunham 2004; Gustiano 2006).
Kematangan seksual pada ikan nila dipengaruhi oleh umur, ukuran dan
kondisi lingkungan. Populasi ikan nila yang berada pada perairan yang luas
mencapai kematangan lebih lambat dibandingkan yang dipelihara di kolam.
Sebagai gambaran, ikan nila pada beberapa danau di Afrika Timur matang
kelamin pada umur 10-12 bulan pada ukuran 350-500 g. Jika dipelihara di kolam
budidaya dengan kondisi optimal, ikan ini akan mencapai kematangan kelamin
pada umur 5-6 bulan dengan ukuran 150-200 g, tetapi jika kondisi kolam
budidaya tidak optimal, usia kematangan akan lebih lama sekitar 1-2 bulan tetapi
akan memijah pada ukuran yang lebih kecil yaitu sekitar 20 g (Popma & Masser
1999).
Determinasi dan diferensiasi kelamin
Jenis kelamin individu ditentukan oleh faktor genetik dan faktor
lingkungan. Secara genetik, jenis kelamin ditentukan oleh kromosom dan sudah
ditentukan sejak terjadinya proses pembuahan (Maty 1985). Yamamoto (1969)
menyatakan jika faktor jantan lebih dominan daripada faktor betina maka zigot
akan tumbuh dan berkembang menjadi jantan, demikian pula sebaliknya. Proses
diferensiasi merupakan proses perkembangan gonad menjadi jaringan definitif.
Hunter dan Donaldson (1983) menjelaskan bahwa proses ini terdiri dari
serangkaian kejadian yang memungkinkan kelamin genotipe terekspresi menjadi
kelamin fenotipe. Diferensiasi kelamin merupakan proses yang relatif labil
khususnya diferensiasi kelamin pada ikan dibanding vertebrata yang lebih tinggi.
Kondisi ini memungkin kan untuk dilakukannya rekayasa kelamin. Periode labil
ini dapat digambarkan melalui studi histologi pada saat diferensiasi kelamin.
Beberapa hasil studi yang telah dilakukan menyimpulkan bahwa terdapat 2
kelompok utama proses diferensiasi kelamin yang terjadi pada ikan teleostei
(bertulang keras). Kelompok pertama adalah spesies yang berdiferensiasi pada
saat menetas dan berakhir selama waktu yang relatif pendek, yaitu 10-40 hari.
juvenil dan berakhir selama periode 150-500 hari (Yamazaki 1983; Shelton &
Jensen 1979, diacu dalam Pandian & Sheela 1995).
Walaupun determinasi kelamin individu pada awalnya ditentukan oleh
genom individu tersebut, tetapi pengalihan dari kelamin genotipe ke kelamin
fenotipe dilakukan melalui mekanisme biokimia yang dapat dipengaruhi oleh
lingkungan (Chan & Yeung 1983). Ditambahkan oleh Dunham (1990) bahwa
meskipun jenis kelamin genotipe ditentukan pada saat terjadinya fertilisasi, tetapi
penetuan jenis kelamin fenotipe dipengaruhi oleh perkembangan individu
tersebut. Jika selama perkembangan individu tersebut diintervensi dengan
bahan-bahan tertentu, misalnya hormon androgen atau estrogen, maka perkembangan
gonad dapat berlangsung secara berlawanan dengan yang seharusnya.
Sex reversal
Sex reversal merupakan suatu teknik untuk mengubah jenis kelamin secara buatan dari ikan jantan menjadi betina atau sebaliknya. Borg (1994) menyatakan
bahwa sex reversal merupakan teknik pembalikan jenis kelamin pada saat diferensiasi kelamin, yaitu pada saat otak dan embrio masih berada pada keadaan
bi-potential dalam pembentukan kelamin secara fenotipe (morfologis, tingkah laku dan fungsi). Hal ini dijelaskan pula oleh Yamamoto (1969) bahwa perubahan
kelamin secara buatan akan sempurna jika dilakukan pada saat mulainya proses
diferensiasi kelamin dan berlanjut sampai diferensiasi kelamin terjadi.
Hormon steroid
Salah satu teknik sex reversal adalah dengan memberikan hormon steroid pada fase labil kelamin. Pada beberapa spesies ikan jenis teleost gonochoristic, fisiologi kelamin dapat dengan mudah dimanipulasi melalui pemberian hormon
steroid (Piferrer et al. 1994). Nagy et al. (1981) menjelaskan bahwa keberhasilan manipulasi kelamin pada ikan menggunakan hormon dipengaruhi oleh beberapa
faktor antara lain jenis dan umur ikan, dosis hormon, lama waktu dan cara
pemberian hormon serta lingkungan tempat pemberian hormon dilakukan.
hormon sangat tergantung pada interval waktu perkembangan gonad, yaitu pada
saat gonad dalam keadaan labil sehingga mudah dipengaruhi oleh hormon.
Hormon steroid yang dihasilkan oleh jaringan steroidogenik pada gonad
terdiri atas hormon androgen untuk maskulinisasi, estrogen untuk feminisasi dan
progestin yang berhubungan dengan proses kehamilan (Hadley 1992). Namun,
pada tahap perkembangan gonad belum terdiferensiasi menjadi jantan atau betina,
hormon steroid belum terbentuk sehingga pembentukan gonad dapat diarahkan
dengan menggunakan hormon steroid sintetik (Hunter & Donaldson 1983). Salah
satu jenis hormon steroid sintetik yang banyak digunakan untuk proses sex reversal pada ikan, khususnya ikan nila, adalah hormon 17a-methyltestosterone (mt). Hormon 17a-mt merupakan hormon androgen yang bersifat stabil dan
mudah dalam penanganan (Yamazaki 1983). Pemberiannya dapat dilakukan
secara oral (Misnawati 1997), perendaman embrio alevin maupun larva (Laining 1995) maupun implantasi dan injeksi (Mirza & Shelton 1988).
Aromatase dan Aromatase Inhibitor
Selain dengan pemberian hormon steroid, diferensiasi kelamin juga
dipengaruhi oleh ekspresi dari gen yang menghasilkan enzim aromatase (Patino
1997). Aromatase adalah enzim cytochrome P-450 yang mengkatalis perubahan
dari androgen menjadi estrogen. Aktivitas enzim aromatase terbatas pada daerah
dengan target estradiol dan berfungsi untuk mengatur jenis kelamin, reproduksi
dan tingkah laku (Callard et al. 1990). Ada 2 bentuk gen aromatase pada ikan yaitu aromatase otak dan aromatase ovari. Aromatase otak berperan sebagai
pengatur perilaku sex spesifik pada mamalia dan burung (Schlinger & Callard 1990, diacu dalam Melo & Ramsdell 2001) dan juga mengatur reproduksi pada
ikan (Pasmanik et al. 1988, diacu dalam Melo & Ramsdell 2001). Aktivitas enzim aromatase pada otak teleostei 100-1000 kali lebih tinggi dibanding pada mamalia.
Aktivitas enzim aromatase ovari kurang dari 1/10 kali aktivitas enzim aromatase
otak (Gelinas & Callard 1993, diacu dalam Tchaudakova & Callard 1998).
Fungsi cytocrome P-450 pada determinasi jenis kelamin telah teruji karena
merupakan enzim yang bertanggung jawab dalam proses aromatisasi dari
(Jeyasuria et al. 1986, diacu dalam Kwon et al. 2000). Aktivitas enzim aromatase berkorelasi dengan struktur gonad, yaitu larva dengan aktivitas aromatase rendah
akan mengarah pada terbentuknya testis, sedangkan aktivitas aromatase yang
tinggi akan mengarah pada terbentuknya ovari (Sever et al. 1999).
Pada ikan tilapia, sel yang memproduksi enzim aromatase positif terdapat
pada gonad XX berumur 7 hari setelah menetas. Aromatase ini penting bagi
sintes is estrogen yang selanjutnya akan mempengaruhi penentuan jenis kelamin.
Aromatase diekspresikan pada gonad XX 10 hari sampai dengan 2 minggu
sebelum diferensiasi ovari (Brodie 1991). Selain pada genotipe XX, aktivitas
enzim aromatase juga terdeteksi pada genotipe XY dengan tingkat yang lebih
rendah (D’Cotta et al. 2001).
Aromatase inhibitor berfungsi untuk menghambat kerja enzim aromatase dalam sintesis estrogen. Adanya penghambatan ini mengakibatkan terjadinya
penurunan konsentrasi estrogen yang mengarah kepada tidak aktifnya transkripsi
gen aromatase sebagai feedback-nya (Sever et al. 1999). Penurunan rasio estrogen terhadap androgen menyebabkan terjadinya perubahan penampakan dar i betina
menjadi menyerupai jantan, dengan kata lain terjadi maskulinisasi karakteristik
seksual sekunder (Davis et al. 1990). Secara umum, aromatase inhibitor
menghambat aktivitas enzim melalui 2 cara, yaitu dengan menghambat proses
transkripsi gen aromatase sehingga mRNA tidak terbentuk dan sebagai
konsekuensinya enzim aromatase tidak ada (Sever et al. 1999). Cara kedua adalah melalui cara bersaing dengan substrat selain testosterone sehingga aktivitas enzim
aromatase tidak berjalan (Brodie 1991).
Pada beberapa spesies, penghambatan aromatase menyebabkan pengaruh
maskulinisasi sama seperti pengaruh androgen (Kwon et al. 2000). Pada ikan salmon, penambahan aromatase inhibitor jenis imidazole mampu menghasilkan jantan fungsional sebesar 20% melalui perendaman telur selama 2 jam dengan
dosis 10 mg/liter (Piferrer et al. 1994). Pada ikan nilem, perendaman telur selama 4 jam dengan dosis 45 mg/liter mampu menghasilkan 84,83% anakan berkelamin
jantan (Wijayanti 2002). Pada ikan nila merah, perendaman embrio dengan dosis
30 mg/liter menghasilkan anakan berkelamin jantan sebesar 82,22% (Wulansari
ikan nila hampir 100% jantan melalui penambahan aromatase inhibitor jenis fadrozole pada pakan dengan dosis 400 dan 500 mg/kg pakan.
Genetically Male Tilapia
Genetically Male Tilapia (GMT) diperoleh dengan mengawinkan ikan nila jantan super (supermale) yang bergenotipe YY dangan induk betina normal yang bergenotipe XX. Perkawinan antara jantan super dengan betina normal
diperkirakan akan menghasilkan keturunan 100% berkelamin jantan jika sistem
determinasi kelamin dari spesies tersebut hanya melibatkan kromosom kelamin X
dan Y (Mair et al. 1997). Namun dalam perkembangan lebih lanjut, diferensiasi kelamin ikan tidak hanya ditentukan oleh faktor genetik, tetapi juga dipengaruhi
oleh faktor lingkungan seperti suhu, photoperiod, salinitas dan kepadatan. Selain itu, diferensiasi kelamin ikan juga dipengaruhi oleh adanya interaksi antara faktor
genetik dan lingkungan (Tave 1993).
Secara umum, pembentukan ikan nila jantan super dilakukan melalui suatu
proses yang cukup panjang. Pada awal pembentukannya, benih ikan nila normal
diberi hormon estrogen untuk mendapatkan induk betina fungsional bergenotipe
XY. Kepastian induk betina fungsional tersebut dilakukan melalui uji anakan
(progeny). Setelah didapatkan induk betina fungsional bergenotipe XY kemudian dikawinkan dengan induk jantan normal bergenotipe XY. Secara teori, anakan
yang dihasilkan akan terdistribusi sebanyak 25% berkelamin betina (genotipe
XX), 50% berkelamin jantan (genotipe XY) dan 25% berkelamin jantan (genotipe
YY). Untuk mengidentifikasi genotipe individu, anakan dipelihara sampai tahap
induk, kemudian dilakukan uji anakan (progeny) kedua. Uji anakan ini ditujukan untuk mendapatkan induk jantan bergenotipe YY yang dicirikan dengan
anakannya yang 100% berkelamin jantan. Selanjutnya jika induk- induk jantan
bergenotipe YY tersebut dikawinkan dengan induk- induk betina normal (genotipe
BAHAN DAN METODE
Tempat dan waktu
Penelitian dilakukan di Laboratorium Pemuliaan dan Genetika dan kolam
percobaan pada Loka Riset Pemuliaan dan Teknologi Budidaya Perikanan Air
Tawar, Jl. Raya 2 Sukamandi, Subang, Jawa Barat pada Bulan Oktober 2008
sampai Juli 2009.
Metode penelitian
Penelitian dibagi menjadi 2 tahap. Tahap 1 adalah evaluasi pemberian
bahan aromatase inhibitor terhadap nisbah kelamin, bobot individu dan sintasan benih 3 genotipe ikan nila (XX, XY dan YY). Tahap 2 adalah evaluasi
performansi benih 3 genotipe ikan nila (XX, XY dan YY) yang diberi
penambahan bahan aromatase inhibitor pada tahap pembesaran meliputi bobot dan panjang individu, keragaman ukuran, sintasan, konversi rasio pakan, bobot
panen dan perkembangan organ reproduksi. Secara keseluruhan, tahapan
penelitian dari percobaan tahap 1 sampai tahap 2 disajikan secara skematik pada
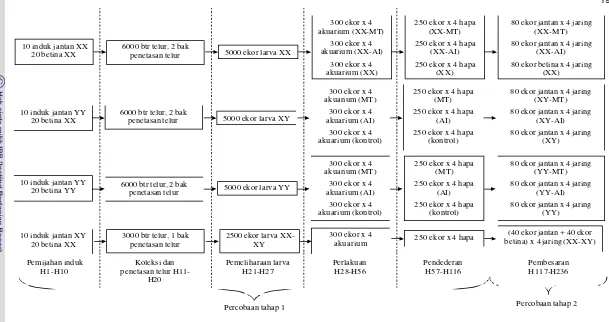
Gambar 2.
Percobaan 1. Pengaruh pe mberian bahan aromatase inhibitor pada tiga genotipe ikan nila sampai tahap pendederan.
Rancangan percobaan yang digunakan adalah r ancangan faktorial, 2
faktor. Faktor uji 1 terdiri atas 3 taraf, yaitu pemberian bahan aromatase inhibitor, penambahan hormon 17a-mt sebagai kontrol (+) dan tanpa penambahan bahan
apapun sebagai kontrol (-). Faktor uji 2 juga terdiri atas 3 taraf, yaitu genotipe
ikan nila XX, XY dan YY. Sebagai pembanding digunakan populasi ikan nila
genotipe campuran antara XX dan XY. Masing-masing perlakuan dilakukan
pengulangan 4 kali.
Bahan utama percobaan berupa larva ikan nila genotipe XX diperoleh
dengan mengawinkan induk ikan nila jantan genotipe XX dengan induk betina
normal. Larva ikan nila genotipe XY diperoleh dengan mengawinkan induk ikan
larva genotipe YY diperoleh dengan mengawinkan induk ikan nila jantan genotipe
YY varietas GESIT dengan induk betina genotipe YY. Induk ikan nila jantan
genotipe YY dan nila jantan genotipe XX berasal dari BBPBAT Sukabumi,
sedangkan induk betina yang digunakan adalah varietas NIRWANA (Nila Ras
Wanayasa) yang berasal dari BPBI Wanayasa. Khusus larva genotipe YY
diperoleh dari BBPBAT, Sukabumi. Hal ini karena induk betina genotipe YY
hanya tersedia di institusi tersebut dan tidak diperjual-belikan. Sebagai populasi
pembanding digunakan populasi larva ikan nila genotipe campuran XX dan XY,
diperoleh dengan mengawinkan induk jantan normal dengan induk betina normal.
Induk jantan dan betina yang digunakan dalam perkawinan normal ini adalah ikan
nila varietas NIRWANA.
Sebelum pemijahan, dilakukan pemilihan induk dari masing-masing
genotipe dan dipelihara secara terpisah antara jantan dan betina. Setelah melalui
masa conditioning selama 2 minggu, induk jantan dan betina dimasukkan ke kolam pemijahan ukuran 4x4x0,75 m. Jumlah induk yang dipijahkan untuk
masing-masing kombinasi sebanyak 10 jantan dengan 20 betina. Setelah 10 hari di
kolam pemijahan, dilakukan pengecekan induk betina. Telur yang terdapat di
dalam mulut induk- induk betina yang memijah diambil dan ditampung dalam
wadah berisi air yang diaerasi. Selanjutnya telur hasil koleksi dimasukkan ke
dalam bak penetasan dengan kepadatan 3.000 butir/bak. Jumlah bak penetasan
yang digunakan untuk masing-masing kombinasi pemijahan sebanyak 2 unit.
Selanjutnya larva hasil penetasan telur ditampung dalam bak fiber volume 500
liter secara terpisah untuk masing-masing genotipe. Pada hari ke 5 setelah
menetas, larva ditebar dalam akuarium ukuran 60x40x40 cm yang diisi 75 liter air
dan diaerasi. Padat tebar yang digunakan adalah 4 ekor/l atau setara dengan 300
ekor per akuarium. Jumlah akuarium yang digunakan sebanyak 3 perlakuan x 3
genotipe x 4 ulangan = 36 buah, ditambah 4 buah akuariu m untuk populasi
campuran XX-XY sehingga jumlah total akuarium sebanyak 40 buah.
Bahan aromatase inhibitor yang digunakan adalah imidazole. Pemberian imidazole dilakukan melalui pakan, yaitu dengan mencampur 25 mg imidazole
yang dilarutkan dalam alkohol 70% ke dalam 1 kg pakan komersial dengan
sebagai kontrol (+) juga dilakukan melalui pakan, yaitu dengan mencampur 60 mg
hormon 17a-mt yang sudah dilarutkan dalam alkohol 70% ke dalam 1 kg pakan
komersial dengan kandungan protein kasar 40%. Pakan yang diberikan untuk
populasi kontrol (-) dan populasi campuran XX-XY berupa pakan komersial yang
sama dengan pakan di atas tanpa penambahan bahan apapun. Pemberian pakan
kepada larva dimulai pada hari 7 setelah menetas dan dilakukan secara ad-satiasi
dengan frekuensi 5-6 kali sehari. Pemberian perlakuan melalui pakan dilakukan
selama 28 hari.
Selanjutnya 10 populasi benih ikan nila tersebut dipindahkan ke dalam 40
unit hapa pendederan ukuran 2x2x1 m yang ditempatkan di kolam tanah ukuran
400 m2. Jarak antar masing-masing hapa adalah 0,5 m. Kepadatan benih yang
ditebar sebanyak 250 ekor/hapa. Selama 60 hari masa pendederan, benih diberi
pakan komersial dengan kandungan protein 32% secara ad-satiasi dengan
frekuensi 3 kali sehari yaitu pagi, siang dan sore.
Pengamatan
1. Persentase kelamin jantan.
Persentase kelamin jantan =
? ? ?
? ? ? ? ?
N? = Jumlah individu berkelamin jantan
N = Jumlah total individu yang diamati. 2. Bobot individu
Bobot individu ditimbang menggunakan alat timbang digital dengan ketelitian
0,01 g. Jumlah sample sebanyak 30 ekor setiap ulangan pada semua perlakuan. Penimbangan bobot individu sample dilakukan setiap 30 hari. 3. Sintasan
Sintasan dihitung berdasarkan jumlah individu yang mampu bertahan hidup
sampai batas akhir percobaan. Nilai sintasan dihitung berdasarkan formula
sebagai berikut :
Sintasan = ? ?
? ?
? ? ? ? ?
Nt = Jumlah individu pada waktu t (akhir percobaan)
4. Kualitas air
Pengamatan dilakukan terhadap air media pemeliharaan di akuarium selama
perlakuan dan di kolam pendederan. Parameter kualitas air yang diamati
meliputi suhu, kandungan oksigen terlarut, pH, amonia dan nitrit. Pengamatan
menggunakan alat ukur digital dan dilakukan setiap 2 minggu sekali.
Termometer maksimum-minimum digunakan untuk mengukur kisaran suhu
maksimal dan minimal pada media perairan.
Analisis data
Data persentase kelamin jantan, bobot individu dan sintasan benih ikan
nila dianalisis menggunakan analysis of variance (ANOVA). Jika hasilnya berbeda nyata, maka untuk membedakan nila i tengah antar semua genotipe dan
perlakuan digunakan uji wilayah ganda Duncan (Duncan’s multiple range test) pada taraf kepercayaan 95%. Tabulasi dan analisis data di komputer dilakukan
menggunakan program Excell 2007 dan SPSS versi 12. Data kualitas air dianalisis
secara deskriptif dan dibandingkan denganreferensi yang ada.
Percobaan 2. Performansi tiga genotipe ikan nila yang diberi imidazole, sebagai bahan aromatase inhibitor, pada tahap pembesaran.
Rancangan percobaan yang digunakan adalah r ancangan faktorial, 2
faktor. Faktor uji 1 terdiri atas 3 taraf, yaitu pemberian imidazole, penambahan
hormon 17a-mt sebagai kontrol (+) dan tanpa penambahan bahan apapun sebagai
kontrol (-). Faktor uji 2 terdiri atas 3 taraf, yaitu genotipe ikan nila XX, XY dan
YY. Sebagai pembanding digunakan populasi ikan nila genotipe campuran antara
XX dan XY. Masing-masing perlakuan dilakukan pengulangan 4 kali.
Bahan utama pada percobaan 2 adalah benih ikan nila hasil percobaan 1
yang berumur 95 hari setelah menetas, terdiri atas 8 populasi benih berkelamin
jantan, 1 populasi benih berkelamin betina dan 1 populasi benih berkelamin
campuran antara jantan dan betina dalam proporsi yang sama. Delapan populasi
benih berkelamin jantan terdiri atas dua populasi benih genotipe XX yang diberi
imidazole dan hormon 17a-mt (kontrol (+)), tiga populasi benih genotipe XY
genotipe YY (penambahan imidazole, kontrol (+) dan kontrol (-)). Populasi benih
tunggal kelamin betina adalah populasi benih genotipe XX tanpa perlakuan,
sedangkan 1 populasi benih berkelamin campuran adalah populasi benih genotipe
XX-XY yang terdiri atas 50% jantan dan 50% betina. Selanjutnya 10 populasi
benih ikan nila yang mempunyai bobot individu rata-rata relatif sama ditebar
dalam 40 unit waring pembesaran ukuran 4x4x1,5 m yang ditempatkan di kolam
tanah ukuran 400 m2. Penempatan masing-masing ulangan pada setiap perlakuan
dilakukan secara acak. Namun demikian, benih dengan jenis kelamin jantan,
betina dan campuran ditempatkan di kolam yang terpisah untuk menghindari
terjadinya kematangan gonad lebih awal. Padat penebaran benih yang digunakan
sebanyak 5 ekor/m2 sehingga jumlah benih di dalam masing-masing waring
sebanyak 80 ekor. Selama 120 hari pemeliharaan, benih diberi pakan buatan
komersial berbentuk pelet dengan kandungan protein 30-32%. Jumlah pakan yang
diberikan pada 30 hari pertama sampai ke-empat secara berturut sebanyak 10; 7,5;
5 dan 2,5% dari biomasa ikan per hari. Pemberian pakan dilakukan dengan
frekuensi 3 kali sehari yaitu pagi, siang dan sore.
Pengamatan
1. Bobot dan panjang individu
Bobot individu ditimbang menggunakan alat timbang digital dengan ketelitian
0,01 g sedangkan panjang diukur menggunakan mistar dengan ketelitian 0,1
cm. Jumlah sample sebanyak 30 ekor setiap perlakuan dan setiap ulangan. Pengamatan bobot dan panjang individu dilakukan setiap 30 hari. Sample yang telah diamati dimasukkan kembali dalam unit percobaan yang sama.
2. Keragaman ukuran
Keragaman ukuran bobot individu equivalen dengan nilai coefficient of variance (CV) karakter tersebut. Keragaman ukuran bobot dapat dihitung dengan formula sebagai berikut :
Keragaman ukuran = ? ?
?
? ? ? ? ?
SD = standar deviasi bobot individu setiap perlakuan
3. Sintasan
Sintasan dihitung berdasarkan jumlah individu yang mampu bertahan hidup
sampai batas akhir percobaan. Nilai sintasan dihitung berdasarkan formula :
Sintasan = ? ?
? ?
? ? ? ? ?
Nt = Jumlah individu pada waktu t (akhir percobaan)
N0 = Jumlah individu pada waktu awal penebaran. 4. Food conversion ratio
FCR dihitung berdasarkan jumlah pakan yang diberikan dan pertambahan
bobot yang dihasilkan sampai akhir percobaan.
FCR =
? ?
?? ?? ? ? ?
Wp= bobot total pakan yang diberikan
Wt = bobot total panen
W0= bobot total awal
5. Bobot panen
Bobot panen dihitung menggunakan alat timbang digital dengan ketelitian
0,01 g. Penimbangan dilakukan pada setiap perlakuan dan setiap ulangan.
6. Perkembangan organ reproduksi
Perkembangan organ reproduksi diamati pada akhir percobaan yaitu dengan
menghitung indeks gonad somatik (IGS) dan melakukan analisis histologis.
Jumlah sample yang dibedah sebanyak 5 ekor setiap ulangan. Sample diambil secara acak pada waktu panen. Indeks gonad somatik dihitung sesuai dengan
formula sebagai berikut :
IGS = ? ? ? ? ? ? ? ? ? ?
? ? ? ? ? ? ? ? ? ?
? ? ? ?
7. Kualitas air
Parameter kualitas air media pemeliharaan meliputi suhu, kandungan oksigen
terlarut, pH, amonia dan nitrit. Pengamatan menggunakan alat ukur digital dan
dilakukan setiap 2 minggu sekali. Pengukuran dilakukan pada kedalaman ±40
cm dari permukaan air. Pada awal, pertengahan dan akhir percobaan dilakukan
pengukuran suhu dan kandungan oksigen terlarut setiap 2 jam sekali selama
Analisis data
Bobot dan panjang individu, sintasan, keragaman individu, food conversion ratios dan bobot panen dianalisis menggunakan prosedur analysis of variance ( ANOVA). Jika hasilnya berbeda nyata, maka untuk membedakan nila i tengah antar semua genotipe dan perlakuan digunakan uji wilayah ganda Duncan
(Duncan’s multiple range test) pada taraf kepercayaan 95%. Tabulasi dan analisis data di komputer dilakukan menggunakan program Excell 2007 dan SPSS versi
12. Data kualitas air dianalisis secara deskriptif dan dibandingkan dengan
Gambar 2. Skema pelaksanaan penelitian dari percobaan tahap 1 sampai tahap 2.
10 induk jantan XX 20 betina XX
10 induk jantan YY 20 betina XX
10 induk jantan YY 20 betina YY
10 induk jantan XY 20 betina XX
6000 btr telur, 2 bak penetasan telur
3000 btr telur, 1 bak penetasan telur 6000 btr telur, 2 bak
penetasan telur 6000 btr telur, 2 bak
penetasan telur
5000 ekor larva XX
5000 ekor larva XY
2500 ekor larva XX-XY 5000 ekor larva YY
akuarium (XX-MT) 300 ekor x 4 akuarium (XX-AI)
300 ekor x 4 akuarium (XX)
(XX-MT) 250 ekor x 4 hapa
(XX-AI)
250 ekor x 4 hapa (XX)
300 ekor x 4
akuarium 250 ekor x 4 hapa
(XX-MT) 80 ekor jantan x 4 jaring
(XX-AI)
80 ekor betina x 4 jaring (XX)
(40 ekor jantan + 40 ekor betina) x 4 jaring (XX-XY) 300 ekor x 4
akuarium (MT) 300 ekor x 4 akuarium (AI) 300 ekor x 4 akuarium (kontrol)
300 ekor x 4 akuarium (MT)
300 ekor x 4 akuarium (AI) 300 ekor x 4 akuarium (kontrol)
250 ekor x 4 hapa (MT) 250 ekor x 4 hapa
(AI) 250 ekor x 4 hapa
(kontrol)
250 ekor x 4 hapa (MT) 250 ekor x 4 hapa
(AI) 250 ekor x 4 hapa
(kontrol)
80 ekor jantan x 4 jaring (XY-MT) 80 ekor jantan x 4 jaring
(XY-AI) 80 ekor jantan x 4 jaring
(XY)
80 ekor jantan x 4 jaring (YY-MT) 80 ekor jantan x 4 jaring
(YY-AI) 80 ekor jantan x 4 jaring
(YY)
Pemijahan induk H1-H10
Koleksi dan penetasan telur
H11-H20 Pemeliharaan larva H21-H27 Perlakuan H28-H56 Pendederan H57-H116 Pembesaran H117-H236
HASIL DAN BAHASAN
Hasil penelitian ini dibagi menjadi 2 bagian. Bagian pertama adalah hasil
percobaan tahap 1 meliputi nisbah kelamin, bobot individu dan sintasan benih
ikan nila sampai umur 95 hari setelah menetas. Bagian kedua adalah hasil
percobaan tahap 2 meliputi bobot dan panjang individu, keragaman ukuran
karakter bobot, sintasan, FCR dan bobot panen serta perkembangan organ
reproduksi sampai benih berumur 215 hari setelah menetas.
Percobaan 1. Pengaruh pe mberian bahan aromatase inhibitor pada tiga genotipe ikan nila sampai akhir tahap pendederan.
Persentase jumlah individu berkelamin jantan, bobot individu rata-rata dan
sintasan pada masing-masing genotipe dan perlakuan disajikan pada Tabel 1.
Analisis dilakukan pada akhir tahap pendederan, yaitu pada saat benih beumur 95
hari. Hasil analisis statistik menunjukkan bahwa genotipe dan perlakuan maupun
interaksi antara genotipe dan perlakuan berpengaruh nyata (P<0,05) terhadap
persentase ikan nila berkelamin jantan (lampiran 2). Pemberian imidazole sebagai
bahan penghambat sekresi enzim aromatase secara nyata meningkatkan persentase
individu berkelamin jantan pada genotipe XX, dari 7,55% menjadi 82,44%.
Penambahan imidazole pada genotipe YY secara nyata juga meningkatkan
persentase kelamin jantan dari 83,01% menjadi 97,12%. Pada genotipe XY,
pember ian imidazole tidak berpengaruh terhadap persentase kelamin jantan
populasi tersebut. Semua populasi, kecuali genotipe XX tanpa perlakuan, secara
nyata mempunyai persentase kelamin jantan lebih tinggi daripada populasi
campuran XX-XY. Secara umum, genotipe XX dan XY mempunyai bobot
individu rata-rata lebih baik dibanding genotipe YY pada semua perlakuan
maupun populasi campuran XX-XY (lampiran 3). Pada percobaan ini, genotipe
YY mempunyai bobot individu rata-rata paling kecil dibandingkan genotipe
lainnya. Selain itu, genotipe YY pada semua perlakuan secara nyata juga
mempunyai tingkat sintasan paling rendah dibandingkan dengan genotipe lainnya
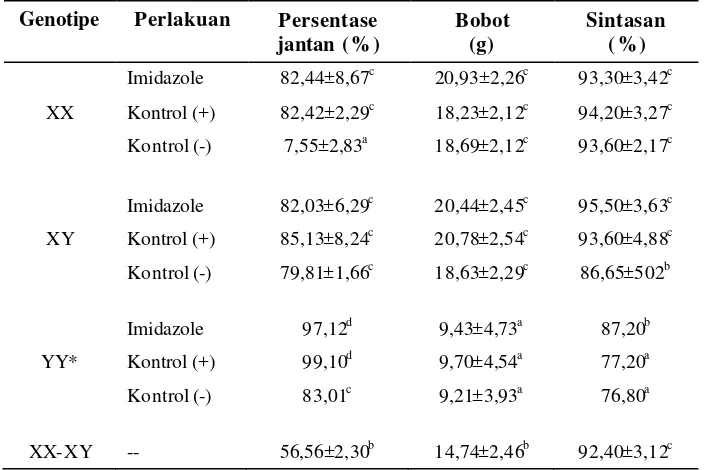
Tabel 1 Persentase kelamin jantan, bobot individu rata-rata dan sintasan benih ikan nila sampai akhir tahap pendederan
Genotipe Perlakuan Persentase jantan (%)
Bobot (g)
Sintasan (%)
Imidazole 82,44±8,67c 20,93±2,26c 93,30±3,42c
XX Kontrol (+) 82,42±2,29c 18,23±2,12c 94,20±3,27c
Kontrol (-) 7,55±2,83a 18,69±2,12c 93,60±2,17c
Imidazole 82,03±6,29c 20,44±2,45c 95,50±3,63c
XY Kontrol (+) 85,13±8,24c 20,78±2,54c 93,60±4,88c
Kontrol (-) 79,81±1,66c 18,63±2,29c 86,65±502b
Imidazole 97,12d 9,43±4,73a 87,20b
YY* Kontrol (+) 99,10d 9,70±4,54a 77,20a
Kontrol (-) 83,01c 9,21±3,93a 76,80a
XX-XY -- 56,56±2,30b 14,74±2,46b 92,40±3,12c
Keterangan : XX : hasil perkawinan induk jantan XX dengan betina XX, XY : hasil perkawinan induk jantan YY dangan betina XX, YY : hasil perkawinan induk jantan YY dengan betina YY, XX-XY : hasil perkawinan induk jantan XY dengan betina XX. Kontrol (+) : pakan dengan penambahan hormon 17a-mt, kontrol (-) : pakan tanpa penambahan bahan apapun. Nilai yang diikuti huruf superscript yang sama dalam kolom yang sama tidak berbeda nyata, P>0,05. Tanda * : Semua perlakuan genotipe YY dilakukan tanpa ulangan karena keterbatasan jumlah individu.
Sebagai data pendukung, dilakukan analisis kualitas air media
pemeliharaan di akuarium dan di kolam pendederan. Hasil analisis kualitas air
media pemeliharaan disajikan pada Tabel 2.
Tabel 2 Hasil analisis kualitas air media pemeliharaan di akuarium dan di kolam pendederan ikan nila
Parameter Akuarium Kolam pendederan
Suhu (ºC) 24,45 – 26,60 28,23 – 29,75
O2 terlarut (mg/l) 3,64 – 7,34 1,23 – 4,00
pH 7,91 – 8,22 7,26 – 7,33
NO2
(mg/l) 0,03 – 0,13 0,04 – 0,05
[image:36.596.130.482.113.348.2]Bahasan
Diferensiasi kelamin ikan dipengaruhi oleh faktor internal (genetik),
eksternal (lingkungan) maupun interaksi antara keduanya. Faktor genetik yang
mempengaruhi arah diferensiasi kelamin antara lain sistem hormonal (endokrin)
dan aksi gen pada kromosom maupun autosom. Sedangkan pengaruh lingkungan
antara lain penambahan bahan-bahan tertentu seperti hormon (exogenous hormone) dan bahan kimia lainnya serta kondisi fisiko-kimia media pemeliharaan ikan selama periode labil kelamin (Devlin & Nagahama 2002).
Pengaruh penambahan suatu bahan pada organisme dalam diferensiasi
kelamin dapat dilihat melalui beberapa parameter antara lain nisbah jenis kelamin,
pertumbuhan dan sintasan. Nagy et al. (1981) menjelaskan bahwa tingkat keberhasilan suatu bahan dalam mempengaruhi pengarahan pembentukan jenis
kelamin dipengaruhi oleh umur organisme, waktu pemberian, lama waktu
pemberian dan dosis pemberian serta faktor lingkungan. Ditambahkan oleh
Hunter dan Donaldson (1983) bahwa keberhasilan pemberian bahan tambahan
sangat tergantung pada interval waktu perkembangan gonad, yaitu pada saat
gonad dalam keadaan labil sehingga mudah dipengaruhi oleh bahan tersebut.
Menurut Yamazaki (1983), usaha pengubahan jenis kelamin setiap spesies harus
dilakukan pada waktu yang tepat dan jangka waktu yang tepat pula. Hal ini
berkaitan dengan diferensiasi yang bersifat khas pada setiap spesies. Pemberian
bahan tertentu yang berakhir sebelum masa diferensiasi kelamin hasilnya tidak
efektif. Hal ini karena sel-sel germinal sebelum masa diferensiasi kelamin tidak
memberikan respon terhadap bahan tertentu tersebut. Demikian juga pemberian
perlakuan yang dimulai setelah masa diferensiasi kelamin. Yamamoto (1969)
menyatakan bahwa pengubahan kelamin akan sempurna jika perlakuan mulai
diberikan pada saat dimulainya diferensiasi kelamin dan berlanjut sampai periode
diferensiasi kelamin berakhir.
Penambahan imidazole sebagai bahan penghambat sekresi enzim
aromatase pada populasi ikan nila genotipe XX menghasilkan persentase individu
berkelamin jantan sebesar 82,44%. Jika dibandingkan dengan populasi kontrol (-)
genotipe XX yang mempunyai persentase individu berkelamin jantan sebesar
pakan cukup efektif mempengaruhi proses diferensiasi kelamin ikan nila.
Mengacu kepada beberapa teori diatas, hasil percobaan ini menunjukkan bahwa
waktu awal perlakuan benih ikan nila yaitu pada umur 7 hari setelah menetas
sudah tepat. Pada umur 7 hari setelah menetas, benih mulai mengalami proses
diferensiasi kelamin, tetapi belum terjadi pembentukan organ kelamin secara
definitif. Demikian juga lama waktu pemberian imidazole dalam percobaan ini
relatif sesuai dalam mempengaruhi terbentuknya kelamin jantan. Hasil percobaan
ini sesuai dengan pernyataan Brodie (1991) bahwasanya pada ikan tilapia, sel
yang memproduksi aromatase positif terdapat pada gonad XX benih umur 7 hari
setelah menetas. Selanjutnya aromatase diekspresikan pada gonad XX pada saat
10 hari sampai dengan 2 minggu sebelum diferensiasi ovari. Seperti telah
diketahui bahwa aromatase merupakan enzim yang bertanggung jawab pada
sintesis estrogen dari androgen. Pemberian aromatase inhibitor dalam pakan benih memberikan pengaruh terhadap pembentukan jenis kelamin, karena bahan ini
menghambat kerja enzim aromatase di otak dalam bio-sintesis estrogen (proses
aromatisasi) dari androgen. Mekanismenya adalah dengan cara menghambat
proses transkripsi dari gen aromatase sehingga mRNA tidak terbentuk. Ketiadaan
mRNA aromatase berakibat pada tidak berlangsungnya proses translasi dalam
rangka pembentukan enzim aromatase. Hal ini mengakibatkan laju konversi
androgen menjadi estrogen menurun sehingga terjadi penurunan konsentrasi
estrogen dibanding androgen. Penurunan konsentrasi estrogen ini selanjutnya
mengarah pada tidak aktifnya transkripsi dari gen aromatase sebagai feedback-nya (Sever et al. 1999). Penelitian Ankley et al. (2002) pada fathead minnow (Pimephales promelas) menunjukkan bahwa pemberian aromatase inhibitor
secara nyata menurunkan aktivitas aromatase otak sehingga mengakibatkan
sintesis estradiol dan produksi vitelogenin menurun. Hasil tersebut sesuai dengan
penelitian Lee et al. (2002) pada ikan protandi black porgy (Acanthopagrus schlegeli) yang menunjukkan bahwa pemberian bahan aromatase inhibitor secara nyata menurunkan tingkat aktivitas aromatase otak serta meningkatkan
konsentrasi plasma 11-ketotestosterone dan LH yang merupakan produk hormon
karakteristik pada individu jantan. Fenomena yang sama diduga terjadi pada
rasio estrogen terhadap androgen. Hal ini menyebabkan terjadinya perubahan
penampakan dari betina menjadi menyerupai jantan, dengan kata lain terjadi
maskulinisasi karakteristik seksual sekunder.
Penambahan hormon 17a-mt sebagai kontrol (+) juga berhasil
meningkatkan persentase individu berkelamin jantan genotipe XX sebesar
82,42%. Menurut Phelps dan Popma (2000), hormon 17a-mt yang merupakan
hormon sintetis berperan sebagai hormon androgenik yang mengarahkan
perkembangan gonad ke pembentukan kelamin jantan. Penambahan hormon
androgen yang diberikan bersama pakan pada percobaan ini diduga meningkatkan
level testosterone dalam tubuh ikan nila sehingga mempengaruhi proses
diferensiasi ke arah terbentuknya kelamin jantan.Hasil percobaan ini menunjukan
bahwa penambahan imidazole dengan dosis 25 mg/kg pakan dapat meningkatkan
persentase individu berkelamin jantan pada ikan nila setara dengan penambahan
60 mg hormon 17a-mt/kg pakan.
Pemberian imidazole pada genotipe XY menghasilkan persentase kelamin
jantan sebesar 82,03%. Nilai ini tidak berbeda nyata dibandingkan dengan kontrol
(-) genotipe XY sebesar 79,81%. Pemberian imidazole sebagai penghambat
sekresi enzim aromatase pada genotipe XY diduga tidak terlalu berpengaruh
terhadap aktivitas enzim aromatase. Hasil penelitian D’Cotta et al. (2001) menunjukkan bahwa penurunan aktifitas aromatase di otak ikan nila genotipe XY
yang dipelihara pada suhu tinggi tidak sebesar penurunan aktivitas aromatase ikan
nila genotipe XX yang dipelihara pada suhu yang sama. Aktivitas aromatase pada
genetipe XX pada perlakuan tersebut mencapai 1/3 kali kondisi normal sedangkan
pada genotipe XY pada perlakuan yang sama menghasilkan aktivitas aromatase
sebesar 2/3 kali kondisi normal. Penelitian Lee et al. (2002) juga menunjukkan bahwa pemberian beberapa jenis aromatase inhibitor pada ikan black porgy betina secara signifikan menurunkan aktifitas aromatase, tetapi pemberian bahan yang
sama pada populasi jantan tidak mengakibatkan penurunan aktivitas aromatase
secara signifikan. Hal yang sama diduga terjadi pada percobaan ini. Rendahnya
pengaruh imidazole terhadap aktivitas enzim aromatase pada genotipe XY
menyebabkan proses diferensiasi kelamin berlangsung seperti pada populasi
jantan pada kedua populasi tersebut tidak berbeda. Kontrol (+) genotipe XY pada
percobaan ini menghasilkan persentase kelamin jantan sebesar 85,13%. Meskipun
peningkatan persentase kelamin jantan yang dihasilkan lebih tinggi tetapi secara
statistik tidak berbeda.
Pada genotipe YY, pemberian imidazole sebagai aromatase inhibitor
berpengaruh nyata dalam meningkatkan persentase individu berkelamin jantan.
Pemberian imidazole pada populasi hasil persilangan YY supermale dengan betina YY ini menghasilkan persentase kelamin jantan sebesar 97,12%. Jika
dibandingkan dengan kontrol (-) genotipe YY sebesar 83,01% menunjukkan
bahwa imidazole efektif dalam mempengaruhi nisbah kelamin ikan nila genotipe
YY. Selain adanya reduksi aktifitas aromatase sebagai akibat pemberian
imidazole, peningkatan persentase individu berkelamin jantan pada populasi
genotipe YY diduga dipengaruhi oleh aksi gen yang secara langsung linked
dengan kromosom Y. Pada genotipe yang mempunyai kromosom homogamet,
diduga aksi gen ini bersifat epistasi (Tave, 1993). Kondisi yang sama juga terjadi
pada genotipe XX, dimana pemberian imidazole mempunyai pengaruh yang nyata
terhadap peningkatan jumlah individu berkelamin jantan. Pada genotipe XY yang
notabene mempunyai kromosom heterogamet, aksi gen yang terjadi tidak bersifat
epistasi sehingga pemberian imidazole tidak terlalu berdampak terhadap
peningkatan individu berkelamin jantan. Pemberian bahan aromatase inhibitor
pada genotipe YY yang menghasilkan hampir 100% individu berkelamin jantan
ini menjadi sesuatu yang sangat penting. Hal ini karena tujuan utama dari
pembentukan YY supermale adalah untuk pembentukan induk jantan yang diharapkan dapat menghasilkan populasi anakan tunggal kelamin jantan.
Persentase kelamin jantan pada semua genotipe dan perlakuan pada
percobaan ini tidak mencapai 100%. Seperti telah disampaikan di depan, selain
ditentukan oleh faktor internal, diferensiasi kelamin ikan juga dipengaruhi oleh
faktor eksternal. Salah satu faktor eksternal yang berpengaruh kuat terhadap arah
diferensiasi kelamin ikan tilapia adalah suhu (Baroiller et al. 1999). Pemeliharaan ikan nila selama tahap diferensiasi kelamin pada suhu rendah cenderung akan
menghasilkan persentase individu berkelamin betina lebih banyak. Selain suhu
betina lebih banyak. Dijelaskan oleh Phelps dan Popma (2000) bahwa sex reversal
ikan nila yang dilakukan pada suhu kurang dari 24°C akan mengurangi
keberhasilan pembentukan individu berkelamin jantan dan juga akan berpengaruh
terhadap penurunan laju pertumbuhan. Penelitian Varadaraj et al. ( 1994), diacu dalam Phelps dan Popma (2000) juga menunjukkan bahwa populasi ikan O. mossambicus yang dipelihara pada suhu rendah dan berfluktuasi antara 23-25 °C mempunyai jumlah individu betina lebih banyak dibandingkan dengan yang
dipelihara pada suhu lebih tinggi dan stabil. Hasil analisis kualitas air
pemeliharaan larva di akuarium selama percobaan relatif rendah dan berfluktuasi
antara 24,45-26,60°C. Rendah dan relatif berfluktuasinya suhu pada media
pemeliharaan tersebut diduga kuat menjadi salah satu faktor penyebab tidak
tercapainya 100% individu yang berkelamin jantan pada percobaan ini. Selain
suhu, beberapa faktor lingkungan media pemeliharaan larva yang diduga juga
mempengaruhi proses diferensiasi kelamin antara lain pH (Rubin 1985),
kepadatan (Olivier & Kaiser 1997), polusi (Andersson et al. 1999; Harries et al. 1999) dan interaksi sosial lainnya (Toguyeni et al. 1997).
Selain nisbah kelamin pada ketiga genotipe ikan nila yang diuji,
pengamatan juga dilakukan terhadap karakter bobot individu dan sintasan. Pada
percobaan ini, genotipe dan perlakuan maupun interaksi antara keduanya tidak
mempengaruhi bobot ikan nila sampai akhir tahap pendederan kecuali pada
genotipe YY. Genotipe YY mempunyai bobot individu rata-rata paling rendah
dibandingkan semua populasi, berkisar antara 9,21-9,70 gram/ekor. Hasil ini
berbeda dengan penelitian Saputra (2007) yang menerangkan bahwa sampai akhir
masa pendederan, populasi benih ikan nila genotipe YY mempunyai bobot
individu rata-rata tidak berbeda nyata dibandingkan benih ikan nila jantan hasil
sex reversal maupun GMT (Genetically Male Tilapia). Penelitian yang dilakukan Saputra (2007) di BBPBAT, Sukabumi menggunakan larva ikan nila yang diduga
semuanya berasal dari sumber induk betina yang sama. Sedangkan pada
percobaan ini, semua bahan percobaan berupa larva ikan nila didapatkan dari
induk betina varietas Nirwana kecuali larva genotipe YY yang berasal dari
BBPBAT, Sukabumi. Perbedaan sumber induk betina yang digunakan ini
Selain itu, rendahnya bobot ikan nila genotipe YY pada percobaan ini diduga
disebabkan adanya fenomena inbreeding. Inbreeding pada populasi genotipe YY terjadi karena keterbatasan jumlah individu terseleksi pada saat awal pembentukan
induk jantan super genotipe YY maupun pada saat produksi masal induk jantan
super genotipe YY pada tahap selanjutnya. Produksi masal induk jantan super
genotipe YY dilakukan dengan menyilangkan induk jantan super genotipe YY
dengan induk betina genotipe YY. Kedua induk bergenotipe YY ini berasal dari
populasi yang sama sehingga peluang terjadinya inbreeding sangat tinggi. Namun demikian, rendahnya laju pertumbuhan ikan nila genotipe YY bukan menjadi
masalah yang utama karena tujuan utama pembentukan ikan nila YY supermale
adalah untuk menghasilkan induk ikan nila yang secara genotipe mampu
menghasilkan keturunan 100% berkelamin jantan, bukan menghasilkan ikan nila
dengan laju pertumbuhan yang cepat.
Secara umum, populasi ikan nila genotipe XY dan XX mempunyai bobot
individu rata-rata lebih baik dibandingkan dengan populasi campuran genotipe
XX-XY. Hal ini diduga disebabkan oleh adanya sharing energi untuk perkembangan gonad dan juga adanya pengaruh interaksi sosial. Meskipun masih
relatif muda, ikan nila yang dipelihara secara campuran antara jantan dan betina
diduga mempunyai perkembangan gonad lebih cepat dibandingkan populasi
tunggal kelamin. Pada umur 95 hari setelah menetas, diameter oosit pada goand
betina yang berasal dari populasi tunggal kelamin betina XX maupun campuran
XX-XY relatif sama, yaitu sekitar 500-875 µm. Menurut Popma dan Masser
(1999) bahwa ikan nila yang dipelihara di kolam akan mencapai kematangan
gonad pada umur 5-6 bulan dengan bobot berkisar antara 150-200 gram. Selain
itu, berdasarkan SNI No. 6138-2009 tentang induk ikan nila, disebutkan bahwa
ikan nila matang gonad pada ukuran diameter oosit = 2.500 µm. Berdasarkan hal
tersebut, mestinya populasi tunggal kelamin betina XX dan populasi campuran
XX-XY mempunyai kondisi yang relatif sama. Namun demikian, meskipun
diameter oosit antara kedua populasi tersebut relatif sama, hasil analisis histologis
gonad ikan nila betina yang berasal dari populasi tunggal kelamin betina XX dan
populasi campuran XX-XY menunjukkan adanya perbedaan. Oosit tertua pada
Gambar

Garis besar
Dokumen terkait
Pendidikan anak usia dini (PAUD) adalah suatu upaya pembinaan yang ditujukan kepada anak sejak lahir sampai dengan usia enam tahun yang dilakukan melalui pemberian
N Minimum Maximum Mean Std. Test distribution is Normal. Calculated from data.. 2) Variabel dependen NIM Sebelum Tranformasi.. One-Sample
Tujuan pengujian ini adalah untuk mengetahui seberapa jauh pengaruh variabel bebas yaitu kepercayaan, kemudahan penggunaan dan keamanan yang dirasakan secara
Penelitian yang akan dilakukan adalah menghitung secara numerik pelat isotropik bertumpu pada pondasi elastis winkler yang diakibatkan oleh kecepatan beban berjalan yang
15 PKM Penelitian peningkatan perilaku Asertivitas pada Anak Pengaruh Pola Asuh Orang Tua
Variabel Celebrity endorser ( visibility , credibility , attractivness dan power ) JKT48 memiliki pengaruh positif terhadap minat beli produk IM3 Play khususnya di dalam
Selain itu, Afiani (2010) menyatakan bahwa kultur campuran untuk starter sangat diperlukan agar terjadi interaksi selama proses fermentasi, akibatnya menghasilkan