MODIFIKASI SELULOSA AMPAS SAGU DENGAN
POLIMERISASI PENCANGKOKAN DAN
PENAUTAN-SILANGAN
BAYU AGUS JUMANTARA
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
ABSTRAK
BAYU AGUS JUMANTARA. Modifikasi Selulosa Ampas Sagu dengan
Polimerisasi Pencangkokan dan Penaut-silangan. Dibimbing oleh TUN TEDJA
IRAWADI dan HENNY PURWANINGSIH.
Limbah ampas sagu memiliki kadar selulosa yang cukup tinggi. Sebelum
dimodifikasi, ampas sagu diisolasi selulosanya melalui 4 tahap, yaitu: ampas sagu
dicuci dengan air suling, dibebaskan dari pati, dihilangkan hemiselulosanya, dan
dihilangkan ligninnya. Modifikasi selulosa ampas sagu dilakukan dengan cara
pencangkokan dan penautan-silangan menggunakan monomer akrilamida,
N,N’
-metilena-bis-akrilamida sebagai penaut-silangan, dan amonium peroksidisulfat
sebagai inisiator. Spektrum fourier transformation infrared (FTIR) selulosa hasil
pencangkokan penautan-silangan memperlihatkan keberhasilan modifikasi dengan
munculnya serapan ulur ikatan C=O pada bilangan gelombang 1654.92 cm
-1dan
intensitas gugus fungsi
–
NH
2terlihat pada bilangan gelombang 3182.64 cm
-1menandakan keberadaan polimer dan penaut-silangan pada selulosa hasil
modifikasi. Polimer yang terbentuk memiliki rerata nisbah pencangkokan sebesar
300.7 dan rerata efisiensi pencangkokan sebesar 59.1% sehingga diperoleh
rata-rata derajat penaut-silangan perlakuan 24 jam sebesar 31.5 g air/g polimer dan
perlakuan 48 jam sebesar 35.4 g air/g polimer.
ABSTRACT
BAYU AGUS JUMANTARA. Modification of Sago Palm Cake through Grafting
and Crosslinking Polymerisation. Supervised by TUN TEDJA IRAWADI and
HENNY PURWANINGSIH.
Sago palm cake has high cellulose content. Prior to modification, cellulose of
the sago palm cake was isolated in 4 stages: washed with distilled water, freed
from starch, removed from hemicellulose, and removed from lignin. Modification
of the sample was done by grafting and crosslinking using acrylamide as
monomer,
N,N'
-methylene-bis-acrylamide as crosslinker, and ammonium
peroksidisulfat as initiator. Fourier tranformation infrared (FTIR) spectra of
cellulose results showed the success of grafting and crosslinking modification.
This can be evidenced by the emergence of bond stretching absorption of C=O at
1654.92 cm
-1wave number and intense -NH
2functional group appeared at wave
MODIFIKASI SELULOSA AMPAS SAGU DENGAN
POLIMERISASI PENCANGKOKAN DAN
PENAUTAN-SILANGAN
BAYU AGUS JUMANTARA
Skripsi
sebagai salah satu syarat memperoleh gelar
Sarjana Sains pada
Departemen Kimia
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
Judul Skripsi : Modifikasi Ampas Sagu dengan Polimerisasi Pencangkokan dan
Penautan-Silangan
Nama
: Bayu Agus Jumantara
NIM
: G44050437
Disetujui
Pembimbing I,
Pembimbing II,
Prof. Dr. Ir. Tun Tedja Irawadi, MS
Henny Purwaningsih, SSi, MSi
NIP 19501227 197603 2 002
NIP 19741201 200501 2 001
Mengetahui
Ketua Departemen Kimia,
Prof. Dr. Ir. Tun Tedja Irawadi, MS
NIP 19501227 197603 2 002
PRAKATA
Puji dan syukur penulis panjatkan kepada Allah SWT atas segala rahmat dan
karunia-Nya sehingga karya ilmiah ini dapat diselesaikan. Tulisan ini disusun
berdasarkan hasil penelitian yang dilaksanakan pada bulan Mei 2010 hingga
Februari 2011 di Laboratorium Kimia Terpadu IPB. Penelitian ini dilakukan
untuk memodifikasi selulosa ampas sagu dengan polimerisasi pencangkokan dan
penautan-silangan.
Penulis mengucapkan terima kasih kepada Prof. Dr. Ir . Tun Tedja Irawadi, MS
dan Henny Purwaningsih, SSi, MSi selaku pembimbing yang telah memberi
banyak arahan, inspirasi, dan saran selama penulis melaksanakan penelitian ini.
Penulis juga mengucapkan terima kasih kepada orang tua (Djuarsa dan almarhum
Otih Martinah) dan kakak saya (Dini) yang telah memberi banyak kasih sayang,
semangat, dan doa selama penulis menempuh studi, penelitian, dan penulisan
karya ilmiah ini.
Penulis juga mengucapkan terima kasih kepada
Dr. Zainal Alim Mas’ud, DEA,
Prof. Dr. Ir. H. M. Anwar Nur, MSc, Drs. Muhammad Farid, Drs. Ahmad
Sjahriza, dan seluruh staf yang bekerja di Laboratorium Kimia Terpadu IPB
Baranangsiang yang telah banyak memberi dukungan teknis dalam pelaksanaan
penelitian ini. Tidak lupa, ungkapan terima kasih juga penulis sampaikan kepada
rekan-rekan seperjuangan selama di Departemen Kimia (Mario, Alvin, Maired,
Nana, dan Jazuli), rekan-rekan peneliti di Laboratorium Kimia Terpadu IPB
(Indah, Vicky, Rita, Ema, Maya, Rina, Hisyam, dan Roni), dan teman-teman di
Departemen Kimia angkatan 42 lainnya.
Semoga karya ilmiah ini bermanfaat.
Bogor, April 2011
RIWAYAT HIDUP
Penulis adalah anak kedua dari Bapak Djuarsa dan Ibu Otih Martinah yang
dilahirkan di Bogor pada tanggal 17 Agustus 1987. Penulis lulus dari SMU Negeri
6 Bogor pada tahun 2005. Penulis kemudian diterima di Institut Pertanian Bogor
(IPB) melalui jalur Undangan Seleksi Masuk IPB (USMI) pada tahun yang sama
dan memilih Mayor Kimia di Fakultas Matematika dan Ilmu Pengetahuan Alam.
DAFTAR ISI
Halaman
DAFTAR TABEL ... vi
DAFTAR GAMBAR ... vi
DAFTAR LAMPIRAN ... vi
PENDAHULUAN ... 1
TINJAUAN PUSTAKA
Tanaman Sagu ... 2
Limbah Industri Pati Sagu ... 2
Selulosa ... 2
Pemutihan ... 2
Akrilamida ... 3
Polimerisasi Pencangkokan dan Penautan-Silangan ... 3
BAHAN DAN METODE
Bahan dan Alat ... 6
Metode Penelitian ... 6
HASIL DAN PEMBAHASAN
Isolasi Ampas Sagu ... 7
Pencangkokan dan Penautan-Silangan ... 9
Analisis FTIR ... 10
SIMPULAN DAN SARAN
Simpulan ... 11
Saran ... 11
DAFTAR PUSTAKA ... 11
DAFTAR TABEL
Halaman
1 Komposisi ampas dan kulit batang sagu dibandingkan dengan
kayu secara umum ... 2
2 Analisis proksimat ampas sagu ... 7
3 Hidrolisis pati dengan HCl 3% (v/v) 80
oC ... 8
4 Nisbah dan efisiensi pencangkokan
... 10
5 Derajat penautan-silangan ... 10
DAFTAR GAMBAR
Halaman
1 Struktur selulosa ... 2
2 Mekanisme penguraian H
2O
2... 3
3 Rumus struktur akrilamida ... 3
4 Tiga kemungkinan reaksi terminasi penautan-silangan ... 6
5 Bentuk fisik ampas sagu ... 8
6 Proses pembengkakan polimer oleh air ... 10
DAFTAR LAMPIRAN
Halaman
1 Bagan alir penelitian ... 15
2 Bagan proses preparasi dan isolasi selulosa ampas sagu ... 16
3 Rancangan reaktor kopolimerisasi pencangkokan dan penautan-silangan
... 17
4 Hidrolisis pati dengan HCl 3% 80
–
85
oC ... 18
5 Merserisasi dengan NaOH 20% 1
–
5
oC selama 1 jam ... 18
6 Delignifikasi dengan H
2O
21.5% pH 12 pada suhu 45
oC selama 14 jam ... 18
7 Total bobot sampel akhir dari sampel awal ... 18
1
PENDAHULUAN
Potensi sagu di Indonesia (1.4 juta ha) mencapai lebih dari 50% potensi pertanian sagu dunia (2.2 juta ha) (Susanto 2006). Areal penanaman sagu di Indonesia tersebar di banyak daerah seperti Papua, Maluku, Riau, Sulawesi Utara, Sulawesi Selatan, dan Sulawesi Tenggara. McClatchey et al. (2006) melaporkan bahwa Papua memiliki 1 juta ha tanaman sagu. Karena begitu besarnya produksi sagu di Indonesia, sangat diperlukan usaha pemanfaatan sagu dan produk turunannya, termasuk limbah (ampas sagu/Ela) yang dihasilkan dari proses produksi sagu. Di Indonesia, sebagian besar bahan baku sagu diolah menjadi tepung sagu.
Limbah dari hasil panen pohon sagu bermacam-macam dan umumnya belum dimanfaatkan, antara lain kulit batang dan ampas sagu. Apabila dibiarkan, limbah ini dapat menimbulkan pencemaran lingkungan berupa bau dan peningkatan kemasaman tanah (pH < 4), yang dapat menghambat pertumbuhan, bahkan menyebabkan kematian tanaman (Syakir et al. 2009). Menurut Djoefrie dan Sudarman (1996), ampas sagu selain banyak mengandung unsur hara yang bermanfaat bagi tanaman, juga mengandung unsur racun yang justru akan mematikan tanaman bila dijadikan media tanam.
Limbah sagu merupakan biomassa lignoselulosa yang mengandung komponen penting seperti pati dan selulosa. Ampas sagu mengandung 64.6% pati dan sisanya serat kasar 14% , protein kasar 3.3%, lemak 0.3%, dan abu 5.0% (Hasibuan 2009). Ampas sagu mengandung residu lignin sebesar 21%, sedangkan kandungan selulosa di dalamnya sebesar 20% dan sisanya merupakan zat ekstraktif dan abu (Kiat 2006).
Jika dilihat dari komponen kimia utama ampas sagu, maka diperlukan penghilangan pati dan lignin untuk mengisolasi selulosa yang menjadi senyawa target untuk dimodifikasi dalam penelitian ini. Proses hidrolisis pati dapat dilakukan secara enzimatis dan non-enzimatis. Proses produksi sirup glukosa dari pati sagu melalui hidrolisis enzimatis yang terdiri dari tahap likuifikasi dan sakarifikasi menggunakan enzim α -amilase (Fridayani 2006), sedangkan cara non-enzimatis dapat menggunakan asam atau dengan perendaman air. Fridayani (2006) melakukan hidrolisis pati sagu dengan HCl 0.1% hingga mencapai pH 2 yang kemudian dipanaskan hingga suhu 121 oC selama 1 jam. Pada penelitian ini digunakan larutan HCl 3%
karena proses penghilangan patinya lebih cepat dibandingkan dengan perendaman air suling bersuhu 80–100 oC.
Fang et al. (2000) melakukan isolasi selulosa dari gandum menggunakan hidrogen peroksida. Isolasi tersebut berhasil mengurangi 44.2–71.9% hemiselulosa dan 52.7–87.8% lignin. Irfana (2009) mengisolasi selulosa menggunakan NaClO2. Namun, cara
ini tidak ramah bagi lingkungan karena dapat mengakibatkan reaksi radikal klorin dan ozon sehingga ozon menipis. Nakatama et al. (2004) melaporkan adanya kloroform dalam cairan limbah maupun di udara sekitar proses pemutihan dengan NaClO2. Oleh sebab itu,
perlu dilakukan penelitian-penelitian untuk mencari alternatif pengganti yang lebih ramah lingkungan untuk senyawa klorin, salah satunya hidrogen peroksida. Proses isolasi selulosa dalam penelitian ini menggunakan hidrogen peroksida.
Selulosa hasil isolasi selanjutnya dimodifikasi dengan pencangkokan dan penautan-silangan. Selulosa digunakan sebagai tulang punggung dalam polimerisasi karena strukturnya yang beraturan dan panjang. Selain itu, selulosa mudah diperoleh di alam dan biodegradabel. Pencangkokan dan penautan-silangan digunakan karena pencangkokan dapat meningkatkan keefektifan drag reduction dan stabilitas geser. Hal ini dipengaruhi oleh panjang dan jumlah yang tercangkok pada polimer (Desmukh et al. 1991). Ikatan polimernya juga menjadi lebih kuat karena adanya tautan-silang.
Irfana (2010) memodifikasi selulosa ampas sagu dengan asetilasi tanpa-pelarut menggunakan anhidrida asetat dan katalis I2
2
TINJAUAN PUSTAKA
Tanaman Sagu
Tanaman sagu adalah spesies dari genus Metroxylon yang termasuk ke dalam famili Palmae. Sagu tumbuh di daerah tropis yang panas dan lembap di Asia Tenggara (Indonesia, Thailand, Filipina, dan Vietnam) dan Oseania (Papua Nugini, Kepulauan Mikronesia, dan Kepulauan Oseania). Tiga produsen utama sagu di dunia adalah Malaysia, Indonesia, dan Papua Nugini, di mana sagu tumbuh secara komersial untuk produksi pati sagu dan atau dikonversi menjadi pakan hewan atau etanol. Indonesia memiliki hutan sagu liar yang luas (>700 000 ha) (Singhal et al. 2008).
Sagu merupakan tanaman pangan penghasil pati paling produktif (15–25 ton pati kering/ha/tahun). Kandungan pati terdapat di dalam batang tanaman dewasa. Selain dijadikan sebagai bahan makanan, pati sagu juga dimanfaatkan dalam aneka bidang industri (Kasi dan Sumaryono 2006).
Limbah Industri Ekstraksi Pati Sagu
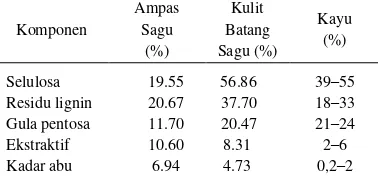
Industri ekstraksi pati sagu menghasilkan 3 jenis limbah, yaitu residu selular empulur sagu berserat (ampas), kulit batang sagu (bark), dan air buangan (wastewater). Pada umumnya, jumlah kulit batang sagu dan ampas sagu berturut-turut sekitar 26% dan 14% berdasar bobot total balak sagu (Kiat 2006). Limbah ampas dan kulit batang sagu merupakan bahan lignoselulosa yang sebagian besar tersusun atas selulosa, hemiselulosa, dan lignin. Tabel 1 menyajikan komposisi kimiawi limbah sagu dibandingkan dengan komposisi kayu secara umum.
Tabel 1 Komposisi ampas dan kulit batang sagu dibandingkan dengan kayu secara umum (Kiat 2006).
Komponen Ampas Sagu (%) Kulit Batang Sagu (%) Kayu (%) Selulosa Residu lignin Gula pentosa Ekstraktif Kadar abu 19.55 20.67 11.70 10.60 6.94 56.86 37.70 20.47 8.31 4.73
39–55 18–33 21–24 2–6 0,2–2
Kulit batang sagu memiliki kadar selulosa dan lignin yang lebih tinggi daripada kayu sehingga memiliki sifat fisik yang keras dan alot. Ampas sagu sebenarnya masih cukup
banyak mengandung pati, karena industri ekstraksi pati sagu di Indonesia masih mengandalkan teknologi yang sangat sederhana. Telah dilaporkan bahwa ampas sagu digunakan sebagai ruahan untuk fermentasi rumen dan pelepah sagu digunakan dalam industri pulp dan kertas (Kiat 2006). Ampas sagu mengandung protein kasar sebesar 2.7%, serat kasar sebesar 2.2%, dan lemak kasar sebesar 0.3% (Murni et al. 2008).
Sebagian besar penelitian limbah sagu sejauh ini berarah pada pemanfaatan limbah sagu (terutama ampas sagu) sebagai bahan baku pembuatan bahan bakar hayati dan substrat pertumbuhan cendawan atau bakteri untuk memproduksi enzim-enzim ekstraselular (Akmar & Kennedy 2001).
Selulosa
Selulosa adalah polimer alam yang terdiri atas subunit-subunit D-glukosa yang ditautkan satu sama lain dengan ikatan -1,4-glikosida (Fengel & Wegener 1989). Struktur kimia polimer yang paling melimpah di alam ini disajikan pada Gambar 1. Selulosa dalam tumbuhan terdiri atas bagian yang memiliki struktur kristalin yang teratur, dan bagian dengan struktur amorf yang tidak terlalu teratur dengan baik. Galur-galur selulosa tergabung bersama dan membentuk fibril-fibril selulosa. Bentuk ini sebagian besar bebas dan berinteraksi satu sama lain melalui ikatan hidrogen (Bobleter 1994).
Gambar 1 Struktur selulosa. Bagian selulosa yang tidak larut di dalam basa kuat (misalnya, NaOH 18%) disebut sebagai -selulosa. Selulosa yang terlarut di dalam larutan ini terendapkan sebagian pada medium netral, dan endapan ini disebut -selulosa. Sisa selulosa yang masih terlarut di dalam larutan basa kuat disebut -selulosa (Bobleter 1994).
Pemutihan
Untuk mendapatkan warna yang lebih cerah, umumnya ampas sagu kering yang berwarna cokelat diputihkan dengan perendaman dalam larutan yang mengandung
3
oksidator. Pada penelitian ini, dipakai hidrogen peroksida, oksidator yang lebih ramah lingkungan dibandingkan dengan oksidator lainnya seperti NaClO2. Reaksi
pemecahan H2O2 di alam tidak menimbulkan
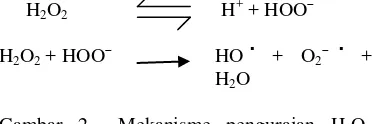
ancaman bagi lingkungan karena menghasilkan oksigen dan air (Gambar 2).
H2O2 H+ + HOO¯
H2O2 + HOO¯ HO▪ + O2¯ ▪ +
H2O
Gambar 2 Mekanisme penguraian H2O2
(Selig et al. 2009).
Pada kondisi asam, H2O2 sangat stabil,
pada kondisi basa mudah terurai. Penguraian H2O2 juga dipercepat oleh naiknya suhu. Zat
reaktif dalam sistem pemutihan dengan H2O2
dalam suasana basa adalah anion perhidroksil (HOO¯ ) (Dence dan Reeve 1996).
Reaksi dekomposisi yang disebabkan oleh pengaruh katalitik ion-ion logam transisi harus dicegah, karena tidak memberikan dampak yang efektif pada proses pemutihan (Brelid 1998).
Akrilamida
Akrilamida (C3H5NO) lazim digunakan
untuk memproduksi plastik dan bahan pewarna. Akrilamida (Gambar 3) merupakan salah satu monomer hidrofilik yang digunakan sebagai bahan baku pembuatan poliakrilamida, berwarna putih, tidak berbau, berbentuk kristal padat yang sangat mudah larut dalam air, metanol, etanol, etil asetat, eter, aseton, sedikit larut dalam kloroform dan mudah bereaksi melalui reaksi amida atau ikatan rangkapnya.
O
NH2
Gambar 3 Rumus struktur akrilamida. Monomer akrilamida mudah berpolimerisasi pada titik leburnya atau di bawah sinar ultraviolet. Akrilamida dalam larutan bersifat stabil pada suhu kamar dan tidak berpolimerisasi secara spontan (Harahap 2006). Akrilamida tidak kompatibel dalam suasana asam, basa, bahan pengoksidasi, dan besi. Pada kondisi normal, akrilamida terdekomposisi menjadi amonia tanpa
pemanasan atau menjadi karbon dioksida, karbon monoksida, dan oksida nitrogen dengan pemanasan.
Poliakrilamida adalah bahan yang digunakan untuk membersihkan air, agar dapat digunakan sebagai air minum. Bahan ini juga digunakan dalam pengolahan air limbah, yaitu untuk menggumpalkan kotoran agar mudah dipisahkan. Poliakrilamida juga banyak digunakan di laboratorium untuk penelitian dan analisis. Akrilamida juga digunakan sebagai bahan baku untuk membuat beberapa jenis zat penjernih, perekat, tinta cetak, zat warna sintetik, zat penstabil emulsi, kertas, dan kosmetik. Akrilamida juga digunakan sebagai kopolimer pada pembuatan lensa kontak dan juga digunakan dalam konstruksi pondasi bendungan atau terowongan (Harahap 2006).
Polimerisasi Pencangkokan dan Penautan-Silangan
Kopolimerisasi pencangkokan merupakan salah satu metode yang paling umum digunakan untuk memodifikasi sifat-sifat kimia dan fisika polimer alami dan sintetik. Kopolimer cangkok dibuat dengan cara menumbuhkan atau menggabungkan polimer sintetik pada tulang punggungpolimer alami.
Ada tiga metode sintesis kopolimer cangkok: Pertama, pencangkokan dari, yaitu polimer tulang punggung membawa tapak aktif yang digunakan untuk menginisiasi polimerisasi monomer, kedua, pencangkokan ke, yaitu polimer tulang punggung membawa gugus fungsi X reaktif yang terdistribusi secara acak, bereaksi dengan polimer lain yang membawa gugus fungsi Y. Ketiga, pencangkokan melalui, yaitu adanya makromer dengan BM rendah dan tapak tak jenuh, polimer yang sedang tumbuh dapat bereaksi pada tapak tak jenuh tersebut menghasilkan kopolimer cangkok (Silvianita et al. 2004).
4
Pembentukan radikal inisiator amonium peroksidisulfat (Anah et al. 2010)
Inisiasi radikal selulosa oleh inisiator amonium peroksidisulfat (Anah et al. 2010)
Reaksi pencangkokanmonomer akrilamida pada selulosa (Anah et al. 2010) Tahap Inisiasi:
5
Reaksi pembentukan homopolimer (Anah et al. 2010) Tahap Terminasi:
(a)
(b)
6
(c)
BAHAN DAN METODE
Bahan dan Alat
Bahan-bahan yang digunakan adalah ampas sagu dari Cimahpar Bogor, akuades, gas nitrogen, akrilamida, amonium persulfat (APS), N,N-metilena-bis-akrilamida (MBA), metanol teknis, etanol teknis, aseton Merck, NaOH p.a Merck, HCl 37% Merck, H2O2
35% Merck, dan indikator pH universal Merck.
Alat-alat yang digunakan adalah reaktor pencangkokan, oven, pengaduk magnetik, peralatan kaca, penghalus sampel (blender), neraca analitik, dan spektrofotometer inframerah transformasi fourier (FTIR) Prestige-21 Shimadzu.
Metode Penelitian
Preparasi Contoh Ampas Sagu
Preparasi ini merupakan tahap pertama pada bagan alir penelitian (Lampiran 1). Ampas sagu yang baru diambil dari pabrik tepung sagu di daerah Cimahpar Bogor dicuci di bawah aliran air keran hingga air cuciannya jernih, kemudian dikeringkan di bawah sinar matahari selama 3–4 hari. Ampas sagu kering dihaluskan dalam penghalus sampel selama 5 menit lalu diayak dengan saringan 200 mesh hingga terpisah dari bagian berseratnya. Bagian yang berupa tepung disimpan dalam wadah bertutup rapat.
Hidrolisis Pati
Cara Pertama. Ampas sagu dicuci dengan air suling bersuhu 100 oC, diaduk dengan pengaduk magnetik. Keberadaan pati diuji menggunakan larutan iodin. Ampas sagu dinyatakan bebas-pati jika hasil uji larutan berwarna cokelat seperti larutan iodin, masih terdapat pati jika hasil uji larutan berwana biru atau hitam (Lampiran 2).
Cara Kedua. Sebanyak 10, 20, dan 50 g tepung ampas sagu dicampurkan dengan larutan HCl 3% dengan nisbah sampel dan larutan 1:15, kemudian dipanaskan pada suhu 80 oC di atas penangas air selama 30–40 menit. Keberadaan pati diperiksa menggunakan larutan iodin. Sampel lalu dinetralkan dengan akuades dan dikeringkan dalam oven 60 oC hingga diperoleh bobot konstan (Lampiran 2).
Merserisasi Ampas Sagu
(Ass et al. 2006 & de Paula et al. 2008)
Serbuk ampas sagu bebas-pati dimerserisasi menggunakan larutan NaOH 20% (b/v) dengan nisbah sampel dan larutan NaOH 20% 1:50 selama 1 jam sambil diaduk pada suhu 0–5 °C. Ampas sagu bebas-pati termerserisasi kemudian disaring, dibilas dengan akuades hingga pH-nya netral, dan dikeringkan pada suhu 60 °C hingga bobotnya konstan (Lampiran 2).
Pemucatan Ampas Sagu (Delignifikasi) (modifikasi Sun et al. 2004)
Serbuk ampas sagu hasil merserisasi disuspensikan ke dalam larutan basa pH 12 atau
7
(dikondisikan dengan pelet NaOH) yang mengandung H2O2 1.5% (v/v) dengan nisbah
terhadap sampel 25:1 (mL/g). Suspensi diaduk dengan pengaduk magnetik selama 14 jam pada 45 oC. Sampel dicuci dengan akuades hingga pH filtratnya netral. Residu kemudian dikeringkan dalam oven bersuhu 60 °C hingga bobotnya konstan (Lampiran 2).
Proses Pencangkokan dan Penautan-Silangan (modifikasi Doane et al. 2009)
Air bebas-ion sebanyak 60 mL ditambahkan ke dalam 2 g serbuk ampas sagu hasil delignifikasi di dalam labu leher 3 (Lampiran 3). Campuran diaduk dengan pengaduk hingga homogen, kemudian gas nitrogen dialirkan selama 15 menit, untuk menghilangkan oksigen. Selama proses sintesis, gas nitrogen tidak boleh mati. Sampel dipanaskan pada kisaran suhu 90–95 oC selama 30 menit lalu didinginkan hingga 65
o
C. Inisiator APS sebanyak 100 mg ditambahkan ke dalam campuran dan diaduk selama 15 menit. Selanjutnya campuran 10 g monomer akrilamida dan 10 mg penaut-silangan MBA dilarutkan ke dalam 80 mL akuades dan suhu dinaikkan menjadi 70 oC selama 3 jam. Produk yang berbentuk gel dicuci dengan metanol, lalu etanol. Kemudian, dilakukan pemisahan polimer dari rantai pendek dengan refluks menggunakan aseton pada suhu 70 oC di atas penangas air selama 1 jam. Residunya dikeringkan dalam oven 60
o
C.
Penentuan Nisbah dan Efisiensi Pencangkokan, Derajat Penautan-Silangan, dan Pengujian Kapasitas Absorpsi Air
Sebanyak 0.1 g sampel dimasukkan ke dalam botol dan ditambahkan 100 mL akuades. Campuran didiamkan selama 24 jam, lalu disaring dan ditimbang bobot sampel yang telah mengalami pembengkakan terhadap air. [ [ ⁄⁄ ]] Keterangan:
RG = nisbah pencangkokan EG = efisiensi pencangkokan DC = derajat penautan-silangan
Analisis FTIR
Sebanyak 10 mg sampel yang halus dicampurkan dengan 100 mg serbuk kalium bromida, kemudian dipanaskan dalam oven 60 oC. Campuran digerus hingga homogen lalu dibentuk menjadi pelet dan dianalisis dengan FTIR.
HASIL DAN PEMBAHASAN
Isolasi Ampas Sagu
Ampas sagu yang digunakan dalam penelitian ini memiliki kadar air, abu, lemak, protein, serat kasar, dan karbohidrat sebagaimana tercantum pada Tabel 2. Ampas sagu yang digunakan sudah melalui tahap pencucian dengan air keran kemudian dikeringkan di bawah sinar matahari selama 3 hari. Kadar serat kasar dan karbohidrat yang tinggi menunjukkan bahwa ampas sagu yang digunakan mengandung banyak selulosa, pati, dan sakarida lain yang larut air.
Tabel 2 Analisis proksimat ampas sagu basah Cimahpar Bogor (Irfana 2009). Parameter Kadar (%) Air Abu Lemak Protein Serat kasar Karbohidrat 40.60 4.30 0.16 4.99 33.33 50.61
Ampas yang digunakan dalam penelitian ini masih mengandung karbohidrat yang cukup tinggi. Karbohidrat ini perlu dihilangkan agar tidak mengganggu proses sintesis kopolimer selulosa. Terdapat 2 cara yang digunakan untuk menghilangkan karbohidrat. Pertama, dengan pencucian menggunakan air dengan suhu 80–90 oC. Cara ini kurang efektif karena waktu yang dibutuhkan hingga ampas sagu bebas-pati cukup lama, yaitu 3 hingga 4 hari. Selain itu, dibutuhkan sangat banyak air sehingga cara ini sangat tidak efektif dari segi waktu dan jumlah pemakaian pelarut.
8
dengan cara pertama yang dapat menghabiskan >50 L air sadah.
Tabel 3 Hidrolisis pati dengan HCl 3% (v/v) 80oC
t det
Perlakuan 1 Perlakuan 2 Perlakuan 3 U1 U2 U1 U2
5 ++++ ++++ ++++ ++++ ++++
10 ++++ ++++ ++++ ++++ ++++ 15 +++- ++++ ++++ ++++ ++++
20 ++-- ++-- ++-- ++-- ++++ 25 ++-- +--- +--- ++-- ++--
30 +--- ---- ---- +--- +--- 35 +--- ---- ---- ---- +---
40 ---- ---- ---- ---- ---- 45 ---- ---- ---- ---- ----
50 ---- ---- ---- ---- ---- Keterangan :
(+) = Larutan berwarna hitam ( - ) = Larutan berwarna cokelat
Perlakuan 1 = 10 g ela & 150 mL HCl 3% Perlakuan 2 = 20 g ela & 300 mL HCl 3% Perlakuan 3 = 50 g ela & 750 mL HCl 3%
Pati terhidrolisis oleh HCl membentuk senyawa gula sederhana. Keberadaan pati dapat diuji menggunakan larutan iodin. Ampas sagu dinyatakan bebas-pati jika pemberian larutan iodin menghasilkan warna biru atau cokelat pekat, sebaliknya ampas sagu belum bebas-pati jika hasil uji larutan berwana cokelat seperti larutan iodin. Menurut Fessenden dan Fessenden (1999), warna biru tua timbul dari antaraksi amilosa dengan iodin. Warna ini merupakan dasar uji iodin untuk pati. Gambar 5a dan b memperlihatkan perubahan bentuk fisik ampas sagu selama penghilangan pati menjadi berwarna agak merah dan kasar. Bobot yang hilang ketika proses ini diperoleh rata-rata sebesar 72.30% (Lampiran 4). Bobot yang hilang diduga berupa pati yang terhidrolisis, selulosa yang terdegradasi, dan logam-logam.
Judoamidjojo et al. (1992) menyatakan bahwa asam akan memecah molekul pati secara acak dan gula yang dihasilkan sebagian besar adalah gula pereduksi. Katalis asam yang umum dipakai adalah asam klorida (HCl), karena merupakan asam kuat dan bersifat atsiri.
(a) (b)
(c) (d)
Gambar 5 Bentuk fisik ampas sagu, belum bebas-pati (a), bebas-pati (b), hasil merserisasi (c), dan hasil delignifikasi (d).
Tekstur ampas sagu hasil merserisasi dalam NaOH 20% (v/v) selama 1 jam pada suhu 0–5 oC lebih halus, lebih keras, dan lebih cokelat dibandingkan dengan sebelum dimerserisasi (Gambar 5c). Hal ini dapat diakibatkan oleh terbukanya untaian bagian kristalin selulosa sehingga sebagian besar lignin akan lebih terpajan keluar. Larutan NaOH dalam air bersifat protik polar, sehingga keberadaannya di antara rantai selulosa dapat memutus ikatan hidrogen intra dan antarrantai selulosa kristalin (Klemm et al. 1998). Terbentuknya interaksi baru yang lebih kuat antara gugus hidroksil selulosa ampas sagu dan larutan NaOH menyebabkan terbukanya bagian kristalin selulosa tersebut sehingga gugus-gugus hidroksil selulosa menjadi lebih mudah dijangkau oleh pereaksi (Pusic et al. 1999). Bobot hasil proses merserisasi menurun rata-rata sebesar 39.00% (Lampiran 5) dari bobot awal. Bobot yang hilang diduga berupa hemiselulosa, selulosa yang terdegradasi, dan logam-logam, karena pelarut dalam proses ini dapat melarutkan senyawa-senyawa tersebut.
Proses penghilangan lignin dengan H2O2
pH 12 selama 14 jam pada suhu 45 oC menghasilkan ampas sagu yang lebih putih dan lebih halus (Gambar 5d). Proses ini sangat penting untuk proses selanjutnya karena lignin dapat menghambat pembentukan kopolimer selulosa dengan akrilamida ketika sintesis berlangsung.
9
(OH¯ ). Ion perhidroksil adalah bahan yang aktif bereaksi dengan struktur karbonil pada lignin sehingga lignin terpecah-pecah, larut, dan terekstraksi dalam larutan NaOH. Konsentrasi ion perhidroksil meningkat dengan bertambahnya konsentrasi H2O2 dan
NaOH. Hidrogen peroksida efektif memecahkan dan melarutkan struktur karbonil dan kuinon, sedangkan klorin oksida (ClO¯ ) tidak dapat menghancurkan secara sempurna (Dence dan Reeve 1996). Bobot yang hilang dari proses ini sebesar 45.03% (Lampiran 6). Bobot yang hilang berupa lignin dan selulosa yang terdegradasi yang larut dalam proses ini. Bobot hilang total dari awal proses hingga akhir proses adalah sebesar 90.69% (Lampiran 7).
Pencangkokan dan Penautan-Silangan
Kerangka utama yang digunakan pada kopolimerisasi adalah selulosa hasil isolasi dari ampas sagu. Selulosa dijadikan kerangka utama karena keberadaannya yang begitu banyak di alam dan mudah diperoleh. Monomer yang dicangkokkan adalah akrilamida. Akrilamida memiliki ikatan rangkap sehingga sangat memungkinkan terjadinya pencangkokan.
Proses pencangkokan dan penautan-silangan dilakukan di dalam labu leher 3 dengan kondisi bebas-oksigen. Kondisi ini sangat penting karena oksigen dapat membentuk peroksida yang mengganggu proses sintesis dan membantu terbentuknya homopolimer yang tidak diharapkan. Homopolimer terbentuk dari penggabungan monomer sejenis dengan unit berulang yang sama. Untuk mencegah hal ini, gas nitrogen perlu disalurkan terus-menerus hingga proses sintesis selesai.
Metode pencangkokan dan penautan-silangan yang digunakan tidak simultan, artinya selulosa direaksikan dengan inisiator terlebih dahulu. Tujuannya, meminimumkan terbentuknya homopolimer pada hasil akhir. Inisiator berfungsi mengaktifkan gugus fungsi selulosa dan monomer sehingga menjadi senyawa radikal. Tahap pengaktifan gugus fungsi ini disebut inisiasi. Tahap inisiasi terjadi pada inisiator APS membentuk radikal APS dan radikal selulosa.
Tahap propagasi terjadi setelah inisiasi. Pada tahap ini terjadi penggabungan senyawa utama dengan monomer. Monomer akrilamida dicangkokkan ke radikal selulosa yang berperan sebagai senyawa utama. Bila reaksi
tidak sempurna, tahap ini akan menghasilkan homopolimer.
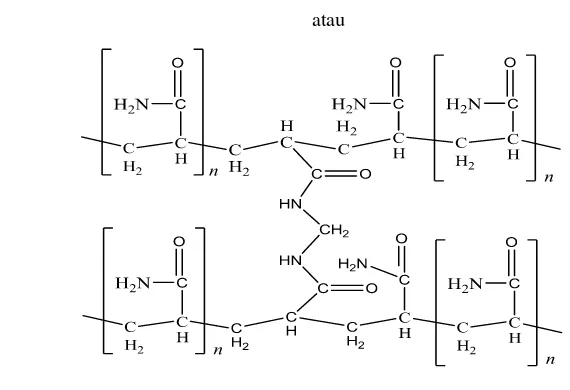
Tahap akhir dalam polimerisasi adalah terminasi, yaitu tahap terbentuknya produk. Pada tahap ini, penautan-silangan bereaksi dengan monomer dan selulosa membentuk produk dengan 3 kemungkinan tautan- silang, yaitu tautan-silang antarmonomer
pada monomer yang sudah tercangkok ke selulosa, tautan-silang antarselulosa, dan tautan-silang antarmonomer pada homopolimer. Penaut-silang MBA menaut-silangkan polimer atau monomer sehingga menjadi lebih kuat dan tidak mudah terurai oleh pelarut.
Pada selulosa, atom O di C6 memiliki
reaktivitas lebih tinggi karena pengaruh subtituen-subtituen di sekitarnya, dan menjadi tapak aktif yang menginisiasi pembentukan radikal monomer. Radikal monomer memungkinkan terjadinya reaksi antarmonomer membentuk homopolimer.
Hasil pencangkokan yang berupa gel setelah direaksikan selama 3 jam dipresipitasi berdasarkan tingkat kepolarannya, yaitu menggunakan metanol, etanol 96%, dan aseton pada suhu 70 oC selama 1 jam. Tujuan presipitasi ini adalah melarutkan air dalam gel sehingga bentuknya lebih padat. Metanol berfungsi melarutkan senyawa yang lebih polar seperti air, sedangkan etanol melarutkan senyawaan yang lebih nonpolar. Perendaman dengan aseton pada suhu 70 oC selama 1 jam bertujuan melarutkan homopolimer atau polimer-polimer berantai pendek, karena yang diharapkan pada hasil akhir adalah polimer berantai panjang. Sisa rantai yang terputus dan homopolimer dapat terlarut saat dicuci dengan aseton (Silvianita et al. 2004).
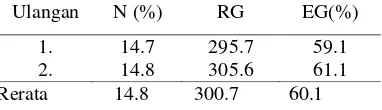
Hasil pencucian dengan aseton berupa bongkahan polimer padat yang kemudian dikeringkan dalam oven bersuhu 50–60 oC. Dari 2 kali pengulangan diperoleh bobot polimer padat hasil pengeringan sebesar 12.2205 dan 11.9907 g. Tabel 4 menunjukkan rerata RG dan rerata EG dari 2 kali ulangan (Lampiran 8). RG menunjukkan nisbah pencangkokan terhadap selulosa yang sebenarnya terlibat pada reaksi, sementara EG adalah persen pencangkokan terhadap bobot selulosa awal.
Tabel 4 Nisbahdan efesiensi pencangkokan
Rerata 14.8 300.7 60.1 Ulangan N (%) RG EG(%)
10
Bongkahan polimer hasil sintesis dihaluskan terlebih dahulu kemudian disaring dengan penyaring 60–80 mesh sebelum diuji kapasitas absorpsi airnya untuk memperoleh nilai derajat penautan-silangan(DC). Nilai ini menunjukkan seberapa besar penaut-silang yang berhasil bertautan-silang dengan monomer-monomer. Ada beberapa cara untuk mengukur kapasitas absorpsi air. Metode volumetrik mengukur perubahan volume air sebelum dan sesudah absorpsi, metode gravimetrik mengukur perubahan bobot polimer superabsorben, metode spektroskopi mengukur perubahan spektrum UV polimer, dan metode mikrogelombang mengukur perubahan energi absorpsinya (Buchholz 1997). Metode yang digunakan dalam penelitian ini adalah metode volumetrik. Tabel 5 menunjukkan dari 2 kali pengulangan diperoleh hasil yang tidak jauh berbeda.
Tabel 5 Derajat penautan-silangan Ulangan
Derajat Penautan-silangan (g air/ g)
24 jam 48 jam 1 31.5 35.0 2 31.5 35.8 Rerata 31.5 35.4
Uji kapasitas absorpsi dilakukan dengan jalan memasukkan polimer ke dalam pelarut air. Air akan terabsorpsi ke polimer karena adanya gugus hidrofilik. Setelah mencapai tahap kesetimbangan, air yang terserap akan berikatan hidrogen dengan gugus karboksilat sehingga tetap tertahan pada polimer dan membengkakkannya (Swantomo et al. 2008; Gambar 6).
Gambar 6 Proses pembengkakan polimer oleh air (Swantomo et al. 2008) Derajat penautan-silangan polimer yang disintesis pada penelitian ini diperoleh rerata sebesar 31.5 dan 35.4 g air/g polimer berturut-turut dari perlakuan 24 dan 48 jam. Hasil ini masih jauh di bawah hasil derajat pentautan-silangan dari polimerisasi selulosa komersial yang telah dilakukan oleh Rinawita (2011), yaitu perendaman selama 24 jam mampu menyerap sebesar 67.6 g air/g polimer dari bobot awalnya (0.2893 g) dan perendaman
selama 48 jam mampu menyerap 91.9 g air/g polimer. Diduga jumlah gugus hidrofilik yang terkandung dalam polimer hasil penelitian ini lebih sedikit dibandingkan dengan hasil penelitian Rinawita (2011).
Analisis FTIR
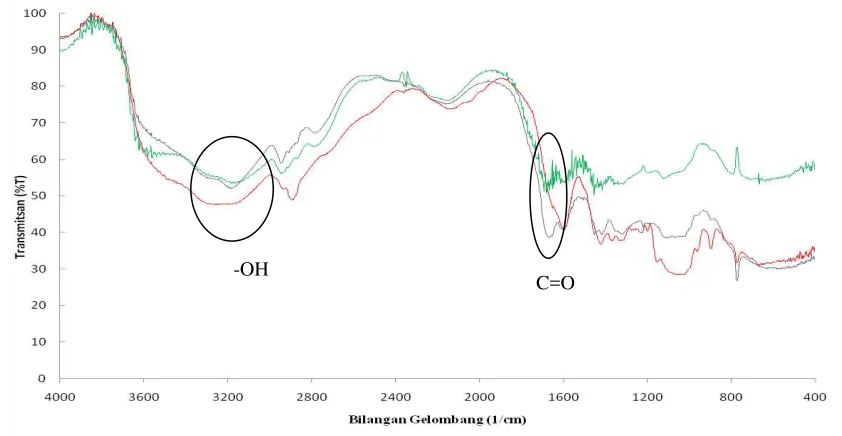
Analisis FTIR berguna untuk mengetahui ciri struktural senyawaan kimia pada sampel dan mendeteksi substitusi akibat modifikasi. Menurut FAO (1996), spektrum inframerah selulosa dicirikan serapan bilangan gelombang sekitar 3500 cm-1 (ulur –OH), 2800–3200 cm-1 (ulur C-H), dan daerah sidik jari dengan puncak ganda pada daerah 1000– 1100 cm-1. Hasil penelitian ini menunjukkan pada spektrum inframerah selulosa hasil isolasi terdapat serapan ulur –OH pada bilangan gelombang 3161.33 cm-1, serapan unsur C-H pada 2891.30 cm-1, dan 1054.68 cm-1 menunjukkan sidik jari dengan puncak ganda.
Setelah pencangkokan dan penautan-silangan, pada spektrum FTIR terlihat kemunculan serapan C=O pada bilangan gelombang 1654.92 cm-1 dan serapan ulur N-H pada bilangan gelombang 3180.62 cm-1. Serapan C=O mengindikasikan keberhasilan pencangkokan dan serapan N-H menunjukkan keberadaan monomer dan penaut-silang. Gambar 7 menunjukkan kemiripan spektrum dari 4000 cm-1 hingga 1600 cm-1 antara hasil polimerisasi selulosa komersial dan selulosa isolasi dari ampas sagu. Hal ini menandakan bahwa selulosa dari hasil isolasi ampas sagu memiliki kualitas yang hampir mirip dengan selulosa komersial.
11
Gambar 7 Spektrum FTIR, garis merah adalah selulosa hasil delignifikasi, garis hitam adalah hasil pencangkokan selulosa hasil isolasi, dan garis hijau adalah hasilpencangkokan selulosa komersial dengan metode sama yang telah di kerjakan oleh Rinawita (2011).
SIMPULAN DAN SARAN
Simpulan
Modifikasi selulosa ampas sagu dengan pencangkokan dan penautan-silangan telah berhasil dilakukan. Polimer yang terbentuk tidak termasuk ke dalam polimer superabsorben karena memiliki derajat tautan-silang di bawah 90 g air/g polimer. Perlakuan perendaman polimer dengan air selama 48 jam tidak terlalu berpengaruh banyak pada derajat tautan-silang jika dibandingkan dengan perlakuan perendaman selama 24 jam.
Saran
Metode kopolimerisasi ini perlu diperhatikan dalam segi sintesisnya, yaitu suhu dan pengaliran nitrogen ke dalam reaktor, karena sangat memengaruhi hasil akhir. Selain itu, perlu dilakukan optimasi metode kopolimerisasinya.
DAFTAR PUSTAKA
Achmad S, Radiman CL, Ariwahjoedi B, Noerati. 2006. Proses esterifikasi pada kain kapas dengan turunan karboksilat untuk menaikkan ketahanan kusut kapas. Akta Kimindo 2:57-62.
Akmar PF, Kennedy JF. 2001. The potential of oil and sago palm trunk wastes as carbohydrate resources. Wood Sci Technol 35: 467-473.
Anah L, Astrini N, Suharto, Nurhikmat A, Haryono A. 2010. Studi awal sintesa komposit hidrogel polimer superabsorben carboxymethyl cellulose-graft-poly(acrylic acid)/montmorilonit melalui proses kopolimerisasi cangkok. Berita Selulosa 45:1-8.
Ass BAP, Belgacem MN, Frollini E. 2006. Mercerized linter cellulose: characterization and acetylation in N,N -di-methylacetamide or lithium chloride. Carbohydr Polym 63:19-29.
Bobleter O. 1994. Hydrothermal degradation of polymers derived from plants. Prog Polym Sci 19:797-841.
Brelid H. 1998. TCF bleaching of soft wood kraft pulp [disertasi]. Chalmers: University of Technology Gotenberg.
Buchholz FL. 1998. Application of Superabsorbent Polymers. Di dalam: Buchholz FL, Graham AT, editor. Modern Superabsorbent Polymer Technology. New York: Wiley.
de Paula P, Lacerda TM, Frollini E. 2008. Sisal cellulose acetates obtained from -OH
12
heterogenous reactions. Express Polym Lett 2:423-428.
Dence CW, Reeve DW. 1996. Pulp Bleaching Principle and Practice. Atlanta: Tappi Pr. Desmukh SR, Sudhakar K, Singh RP. 1991.
Drag-reduction efficiency, shear stability, and biodegradation resistance of carboxymethyl cellulose-based and starch-based graft coplymers. J Appl Sci 43:1091-1101.
Djoefrie MHB dan Sudarman M. 1996. Pemanfaatan campuran ampas sagu dengan kotoran sapi sebagai media pembibitan kelapa sawit. Di Dalam: Prosiding Simposium Nasional Sagu III; Pekanbaru, 27-28 Februari 1996. Bogor: Institut Pertanian Bogor.
Doane WM, Doane SM, Savich MH, penemu; Absorbent Technology, Inc. 12 Mar 2009. Superabsorbent polymers in agricultural application. US patent 0 069 185.
Elliot M. 1997. Superabsorbent Polymers. BASF Product Development Scientist. Fang JM, Sun RC, Tomkinson J. 2000.
Isolation and characterization of hemicelluloses and cellulose from rye straw by alkaline peroxide extraction. Cellulose 7: 87-107.
Fessenden JR, Fessenden JS. 1999. Kimia Organik. Ed ke-3. Pudjaatmaka AH, penerjemah; Jakarta: Erlangga.
Fengel D, Wegener G. 1989. Wood Chemistry. Ultrastructure and Reactions. New York: Walter de Gruyter.
Food and Agricultural Organization [FAO]. 1996. Compendium of Food Aditive Specification. Adendum 5. [Berkala sambung jaring] http://www.fao.org/ docrep/w6355e/w6355e0l.htm.
Fridayani. 2006. Produksi sirup glukosa dari pati sagu yang berasal dari beberapa wilayah di Indonesia [skripsi]. Bogor: Fakultas Teknologi Pertanian, Institut Pertanian Bogor.
Harahap Y. 2006. Pembentukan akrilamida dalam makanan dan analisisnya. WWW Maj Ilmu Kefarmasian 3.
[terhubung berkala]. http://jurnal. farmasi.ui.ac.id/pdf/2006/v03n03/akrilami d.pdf?PHPSESSID=2d09a4864d7b99981e 25b664aeb9440b.html [10 Des 2010].
Hasibuan M. 2009. Pembuatan film layak makan dari pati sagu menggunakan bahan pengisi serbuk batang sagu dan gliserol sebagai plasticizer, Sumatera Utara [tesis]. Medan: Universitas Sumatera Utara.
Irfana L. 2010. Asetilasi selulosa ampas sagu dengan katalis I2 dan aplikasinya sebagai fasa diam kromatografi kolom [skripsi]. Bogor: Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor.
Judoamidjojo M, Said G, Hartoto L. 1992. Teknologi Fermentasi. Bogor; Pusat Antar Universitas Bioteknologi Institut Pertanian Bogor.
Kasi PD, Sumaryono. 2006. Keragaman morfologi selama perkembangan embrio somatik sagu. Menara Perkebunan 74:44-52.
Kiat LJ. 2006. Preparation and characterization of carboxymethyl sago
waste and it’s hydrogel [tesis]. Malaysia: Master of Science, Universiti Putra Malaysia.
Klemm et al. 1998. Comprehensive Cellulose Chemistry. Volume 1, Fundamentals and analytical Methods. Jerman: Weinhelm. McClatchey W, Manner HI, Elevitch CR.
2006. Metroxylon amicarum, M. paulcoxii, M. sagu, M. salomonense, M. vitiense, and M. warburgii (sago palm) Arecaceae (palm family). Permanent Agriculture Resources 2:1-23.
Murni R, Suparjo, Akmal, Ginting BL. 2008. Pemanfaatan Limbah sebagai Bahan Pakan Ternak. Jambi: Fakultas Peternakan Universitas Jambi, http://jajo66.files.wordpress.com/2008/11/ 03pemanfaatan.pdf [23 Apr 2011].
13
Pusic T, Grancaric, AM, Soljacic I, Ribitsch V. 1999. The effect of mercerization on the electrokinetic potential of cotton. JSDC 115:121-124.
Rath SK, Singh RP. 1997. Flocculation characteristic of grafted and ungrafted starch, amylose, and amylopectin. J Polym Sci 66:1721-1729.
Rinawita. 2011. Modifikasi selulosa dengan teknik pencangkokan dan pertautan-silangan [skripsi]. Bogor: Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor.
Selig MJ, Vinzant TB, Himmel ME, Decker SR. 2009. The effect of lignin removal by alkaline peroxide pretreatment on the susceptibility of corn stover to purified cellulolytic and xylanolytic enzymes. Appl Biochem Biotechnol 155:397-406.
Silvianita S, Nurmasari I, Sulistio A, Kurniawan F, Sumarno. 2004. Kopolimerisasi dari poliakrilamida pada pati dengan metode grafting. Di dalam: Prosiding Seminar Nasional Rekayasa Kimia dan Proses; Semarang, 21-22 apr 2004. Surabaya: Institut Teknologi Sepuluh November.
Singhal RS, Kennedy JF, Gopalakrishnan SM, Kaczmarek A, Knill CJ, Akmar PF. 2008. Industrial production, processing, and utilization of sago palm-derived products. Carbohydr Polym 72:1-20. Sun JX, Xu F, Sun XF, Xiao B, Sun RC.
2004. Physicochemical and thermal characterization of cellulose from barley straw. Polym Degradation Stability. 88:521-531.
Susanto AN. 2006. Potensi dan perhitungan luas lahan sagu untuk perencanaan ketahanan pangan spesifik lokasi di Provinsi Maluku. Di dalam: Prosiding Lokakarya Sagu dalam Revitalisasi Pertanian Maluku; Ambon 29-31 Mei 2006. Ambon: Fakultas Pertanian Universitas Pattimura. hlm 173-184. Swantomo D, Megasari K, Saptaji R 2008.
Pembuatan komposit polimer superabsorben dengan mesin berkas elektron. Family Nursing 2:1978-8738. Syakir M, Bintoro MH, Agusta H. 2009.
15
Lampiran 1
Bagan alir penelitian
Preparasi Ampas Sagu
Pemucatan (H
2O
2)
(Sun
et al.
2004)
Pencangkokan dan
Penautan-Silangan
(Doane
et al.
2009)
- Nisbah pencangkokan
(%)
- Efisiensi pencangkokan (%)
- Derajat penautan-silangan (%)
- Uji absorpsi
- FTIR
Preparasi dan Pencucian
Merserisasi
(NaOH 20% [b/v], 0
–
5 °C, 1 jam)
Hidrolisis pati
(HCl 3% [v/v], 80
oC, 30 menit)
Hidrolisis pati
16
Lampiran 2
Bagan proses preparasi dan isolasi selulosa ampas sagu
Ampas sagu segar
Residu I
Residu II
Residu III
Residu IV (Selulosa ampas sagu)
Pencucian dalam aliran air keran, pengeringan dengan sinar matahari
selama 2 hari
Hidrolisis pati cara pertama dengan larutan HCl 3% suhu 80
oC
selama 30
–
40 menit (diuji dengan larutan iodin); pencucian hingga pH
netral; pengeringan pada 60 °C hingga bobot konstan. Cara kedua dengan
pengadukan menggunakan akuades pada suhu 100
oC.
Delignifikasi dalam campuran larutan basa pH 12 (dikondisikan
dengan NaOH 12 M) yang mengandung H
2O
21.5% (v/v) pada nisbah
terhadap sampel 25:1 (mL/g). Suspensi diaduk dengan pengaduk
selama
14 jam pada 45
oC. Campuran kemudian disaring dengan bantuan vakum
dan endapannya dicuci dengan akuades hingga pH filtratnya sama
dengan 7.0. Residu dikeringkan dalam oven bersuhu 60 °C hingga
bobotnya konstan atau selama 16 jam.
17
Lampiran 3 Rancangan reaktor kopolimerisasi pencangkokan dan pentautan
silangan
Keterangan:
a.
Labu leher 3.
b.
Pengaduk magnetik.
c.
Termometer.
d.
Pipa penyaluran gas nitrogen.
18
Lampiran 4
Hidrolisis pati dengan HCl 3% 80
–
85
oC
Bobot sampel (g)
Bobot bebas-pati (g)
Bobot hilang (%)
10.0068
2.7335
72.68
10.0060
2.6455
73.56
20.5323
5.8050
71.72
20.6604
5.8957
71.46
50.2122
14.0211
72.07
Rata-rata
72.30
Lampiran 5
Merserisasi dengan NaOH 20% 1
–
5
oC selama 1 jam
Lampiran 6
Delignifikasi dengan H
2O
21.5% pH 12 pada suhu 45
oC selama 14
jam
Bobot merserisasi (g)
Bobot delignifikasi (g)
Bobot hilang (%)
1.5311
0.8443
44.86
1.5169
0.8020
47.13
3.7595
2.1620
42.49
3.6955
2.1180
42.68
8.9981
4.6790
48.00
Rata-rata
45.03
Lampiran 7
Total bobot hilang sampel akhir dari sampel awal
Bobot sampel awal(g)
Bobot delignifikasi(g)
Bobot sampel akhir(%)
10.0068
0.8443
91.56
10.0060
0.8020
91.98
20.5323
2.1620
89.47
20.6604
2.1180
89.74
50.2122
4.6790
90.68
Rata-rata
90.69
Bobot bebas-pati (g)
Bobot merserisasi (g)
Bobot hilang (%)
2.7335
1.5311
43.99
2.6455
1.5169
42.66
5.8050
3.7595
35.23
5.8957
3.6955
37.31
14.0211
8.9981
35.82
19
Lampiran 8 Nisbah pencangkokan, efisiensi pencangkokan, dan derajat
penautan-silangan
Ulangan 1
Kadar Nitrogen
Bobot sampel = 0.1384 g
V
titran = 14.9 ml
N
HCl = 0.0980 N
[
[
⁄
⁄
]
]
[
⁄
]
[
⁄
]
Perendaman selama 24 jam:
⁄
Perendaman selama 48 jam:
20
Ulangan 2.
Kadar Nitrogen
Bobot sampel = 0.1262 g
V titran = 13.7 ml
N HCl = 0.0980 N
[
[
⁄
⁄
]
]
[
⁄
]
[
⁄
]
Perendaman selama 24 jam:
⁄