STUDI KASUS MYCOBACTERIUM TUBERCULOSIS YANG
RESISTEN TERHADAP ANTIBIOTIK LINI PERTAMA PADA
PASIEN TUBERKULOSIS DI RSUP FATMAWATI
SKRIPSI
Diajukan Sebagai Salah Satu Syarat untuk Memperoleh Gelar Sarjana
Farmasi (S.Far)
Oleh :
OGI ANDYKA PUTRA
NIM : 108102000033
PROGRAM STUDI FARMASI
FAKULTAS KEDOKTERAN DAN ILMU KESEHATAN
UNIVERSITAS ISLAM NEGERI SYARIF HIDAYATULLAH
KATA PENGANTAR
Puji syukur kepada Allah SWT atas limpahan rahmat dan karunia-Nya kepada umat manusia. Sholawat dan salam senantiasa dicurahkan kepada Nabi Muhammad SAW, yang menjadi suri tauladan bagi kita hingga akhir zaman. Salah satu nikmat yang telah Allah SWT berikan kepada penulis yaitu dapat terselesainya skripsi yang berjudul “Studi Kasus Mycobacterium Tuberculosis yang resisten Terhadap Antibiotik Lini Pertama pada Pasien Tuberkulosis di RSUP Fatmawati”.
Dengan ini penulis ingin mengucapkan terima kasih kepada:
1. Prof. Dr. (hc) dr. M. K. Tadjudin, Sp.And selaku dekan Fakultas Kedokteran dan Ilmu Kesehatan UIN Syarif Hidayatullah Jakarta.
2. Drs. Umar Mansur, M.Sc selaku ketua program studi Farmasi UIN Syarif Hidayatullah Jakarta.
3. Dr. Delina Hasan, M.Kes, Apt selaku Pembimbing I yang telah memberikan kesempatan, arahan dan dukungannya kepada penulis sehingga skripsi ini dapat terselesaikan.
4. dr. Anti Dharmayanti, Sp. PK selaku Pembimbing II yang telah memberikan arahan dan dukungannya kepada penulis untuk menyelesaikan penyusunan skripsi ini.
5. Dra. Farida Indyastuti, MM yang telah membantu perijinan dan arahannya sehingga penulis dapat melakukan penelitian di RSUP Fatmawati.
6. Ayahanda H.Samsul Bahri Ali, ibunda tercinta Hj.Nurbi Yusnaini,S.KM, abang dan adik sekeluarga dr.Rian, Agil, Andri dan Dinda yang tiada henti mendoakan, memberikan semangat dan dukungannya, baik moral maupun materil yang tak terhingga kepada penulis.
7. Bu Nurmeilis,M.Si, Apt dan Mba Pia yang telah membantu perijinan penelitian dan penggunaan laboratorium di RSUP Fatmawati selama masa penelitian.
8. Pak Asep, dr. Sita dan seluruh staf diklit RSUP Fatmawati yang telah membantu perijinan dan penelitian di laboratorium patologi klinik RSUP. Fatmawati.
9. Pak Wiwid, Pak Taufik, Pak Joko, Bu Erma, Bu Ros, Bu Desi, Pak Maryo seluruh staf Laboratorium Klinik Instalasi Patologi yang telah mengijinkan saya melakukan penelitian di sana.
11. Dr. Irianny Pudjiastuti,MARS., Bu Diah, Ka Vian, Bu Astuti seluruh staf IRMIK yang telah membantu saya mengumpulkan data rekam medis dan populasi penelitian.
12. Ibu dan bapak dosen yang mengajar di Program Studi Farmasi Fakultas Kedokteran dan Ilmu Kesehatan UIN Syarif Hidayatullah Jakarta yang telah mendidik dan memberikan begitu banyak ilmu pengetahuan bagi penulis, yang sangat bermanfaat terutama dan penyelesaian skripsi ini.
13. Teman terbaik penulis, Ayu, Faritz, Ikhsan, Endah yang senantiasa membantu dan bertukarpikiran demi kelancaran skripsi penulis.
14. Rekan satu bimbingan, Irfan, Dini, Febri, Eva, Amel yang telah bersama-sama peneliti melakukan diskusi selama penelitian.
15. Teman-teman seperjuangan Alcoolique dan farmasi angkatan 2008 yang telah menemani penulis selama lebih kurang 3,5 tahun di Program Studi Farmasi.
16. Kakak dan adik kelas Program Studi Farmasi seluruh angkatan yang menjadi motivator, penghibur sekaligus teman curhat penulis selama menempuh perkuliahan di farmasi.
Penulis menyadari bahwa penyusunan skripsi ini masih memiliki banyak kekurangan dan ketidaksempurnaan. Oleh karena itu, kritik dan saran dari para pembaca diharapkan oleh penulis guna meningkatkan kualitas diri penulis ke depan.
Jakarta, 12 November 2012
DAFTAR ISI
2.2.1. Morfologi dan Fisiologi...11
2.4.4. Pembacaan Jumlah Bakteri...15
2.8. Pengobatan Tuberkulosis... 30
2.9. Resistensi Tuberkulosis...32
2.9.1. Mekanisme Resistensi...33
2.9.2. Konfirmasi MDR-TB Secara Mikrobiologik...37
2.10. Landasan Teori...39
BAB III KERANGKA KONSEP, DEFINISI OPERASIONAL, HIPOTESIS...41
3.1. Kerangka Konsep...41
3.2. Definisi Operasional...41
3.2.1. Drug Resistance Tuberculosis (DR-TB)...41
3.2.2. Multidrug Resistance Tuberculosis (MDR-TB)...42
3.2.3. Subyek...42
3.2.4. Pemeriksaan BTA...42
3.2.5. Jumlah Kuman...42
3.2.6. Hasil pemeriksaan sputum BTA (SPS) yang dicantumkan...42
3.2.7. Rifampisin...43
3.2.8. Streptomisin...43
3.2.9. Laboratorium rujukan...43
3.2.10. Kultur Mycobacterium Tuberculosis Sensitif...43
3.2.11. Kultur Mycobacterium Tuberculosis Resisten...43
3.2.12. Pasien sensitif tuberkulosis...43
3.3. Hipotesis ...43
3.3.1. Rifampisin sudah mengalami resistensi...43
BAB IV METODE PENELITIAN...44
4.1. Lokasi dan Waktu Penelitian...44
4.1.1. Lokasi...44
4.1.2. Waktu Penelitian...44
4.2. Rancangan Penelitian...44
4.3. Populasi dan Sampel...44
4.3.1. Populasi...44
4.3.2. Sampel...44
4.4. Kriteria Inklusi dan Ekslusi...45
4.4.1. Kriteria Inklusi...45
4.4.2. Kriteria Eksklusi...45
4.5. Langkah – Langkah Penelitian...45
4.5.1. Alat Ukur...45
4.5.2. Pengumpulan Data...45
4.5.2.1. Data yang Dikumpulkan...46
4.5.2.2. Manajemen Data...46
4.5.2.3. Analisis Data...47
4.5.3. Validitas dan Reliabilitas Data...48
BAB V HASIL DAN PENELITIAN...50
5.1. Hasil...50
5.1.1. Jumlah Populasi...50
5.1.2. Jumlah Sampel...50
5.1.3. Karakteristik Sampel Penelitian...51
5.1.4. Kasus Resistensi M.tuberculosis Terhadap Antibiotik Lini Pertama...55
5.1.5. Faktor Dominan Penyebab Resistensi...56
BAB VI PEMBAHASAN...61
6.1. Keterbatasan Penelitian...61
6.2. Pembahasan...61
BAB VII KESIMPULAN DAN SARAN...66
7.1. Kesimpulan...66
7.2. Saran...66
DAFTAR PUSTAKA...67
DAFTAR TABEL
Tabel 1. Jenis dan Dosis OAT...31
Tabel 2. Dosis paduan OAT kombinasi dosis tetap untuk kategori I...31
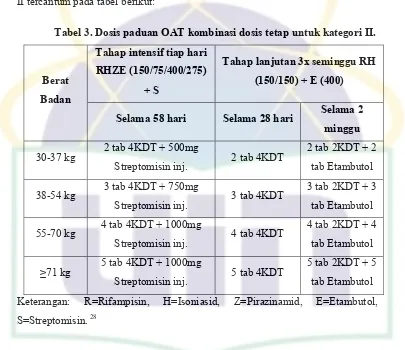
Tabel 3. Dosis paduan OAT kombinasi dosis tetap untuk kategori II...32
Tabel 4. Dosis paduan OAT kombinasi dosis tetap untuk pasien TB anak...32
Tabel 5. Jumlah pasien tuberkulosis BTA (+) dengan/tanpa hasil kultur resistensi di RSUP. Fatmawati selama periode Juli 2009 – Juli 2012...50
Tabel 6. Pasien TB dengan hasil pemeriksaan sputum dan pengujian kultur resistensi di RSUP Fatmawati selama periode Juli 2009 – Juli 2012...51
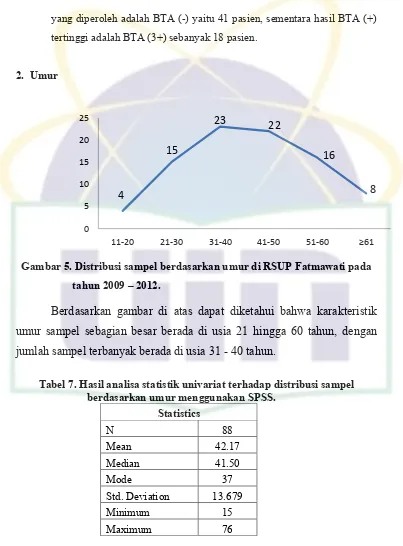
Tabel 7. Hasil analisa statistik univariat terhadap distribusi sampel berdasarkan umur menggunakan SPSS...53
Tabel 8. Karakteristik sampel penelitian berdasarkan jenis pasien di RSUP. Fatmawati pada tahun 2009-2012...54
Tabel 9. Karakteristik sampel penelitian berdasarkan tipe TB paru di RSUP. Fatmawati pada tahun 2009-2012...55
Tabel 10. Hasil uji resistensi Mycobacterium tuberculosis terhadap antibiotik lini pertama pengobatan tuberkulosis di RSUP. Fatmawati sejak Juli 2009 – Juli 2012...55
Tabel 11. Faktor dominan resistensi tuberkulosis di RSUP. Fatmawati berdasarkan jenis pasien pada tahun 2009-2012...58
Tabel 12. Faktor dominan resistensi tuberkulosis di RSUP. Fatmawati berdasarkan tipe TB paru pada tahun 2009-2012...59
DAFTAR GAMBAR
Gambar 1. Skema Patogenesis Tuberkulosis...8
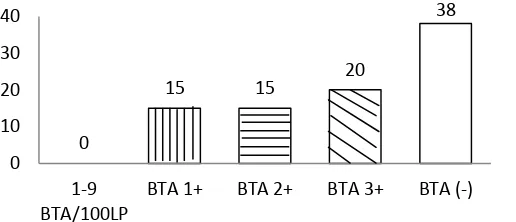
Gambar 2. Hasil pemeriksaan mikroskopis sputum BTA sewaktu
(sputum pada saat kunjungan pertama)...51
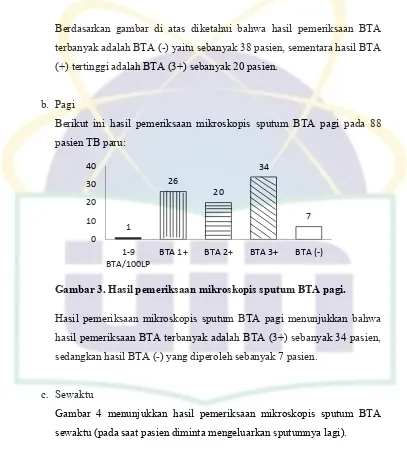
Gambar 3. Hasil pemeriksaan mikroskopis sputum BTA pagi...52
Gambar 4. Hasil pemeriksaan mikroskopis sputum BTA sewaktu (pada
saat pasien diminta mengeluarkan sputumnya lagi)...52
Gambar 5. Distribusi sampel berdasarkan umur di RSUP Fatmawati pada
tahun 2009 – 2012...53
Gambar 6. Karakteristik jenis kelamin pasien TB paru BTA (+) dengan hasil
kultur resistensi laboratorium rujukan RSUP. Fatmawati periode
1 Juli 2009-31 Juli 2012...54
Gambar 7. Persentase resistensi sampel penelitian terhadap antibiotik lini
pertama di RSUP Fatmawati sejak Juli 2009 - Juli 2012...56
Gambar 8. Faktor dominan pasien resisten tuberkulosis di RSUP. Fatmawati
ditinjau dari jenis kelamin pada tahun 2009 - 2012...57
Gambar 9. Faktor dominan pasien resisten tuberkulosis di RSUP. Fatmawati
DAFTAR LAMPIRAN
Lampiran 1. Hasil pemeriksaan sputum dan pengujian resistensi...70
Lampiran 2. Karakteristik sampel penelitian...72
Lampiran 3. Surat Ijin Penelitian di RSUP. Fatmawati...74
DAFTAR SINGKATAN
AIDS : Acquired Immune Deficiency Syndrome
ASKES : Asuransi Kesehatan
ATP : Adenosin Triphosphate
BACTEC : Battle Area Clearance and Training Equipment Consultants
BB : Berat Badan
BJH : Biopsi Jarum Halus
BTA : Basil Tahan Asam
DKI : Daerah Khusus Ibukota
DM : Diabetes Melitus
DNA : Deoxyribonucleic Acid
DOTS : Directly Observed Treatment Short Course
DR-TB : Drug Resistance Tuberculosis
E : Etambutol
EMB : Etambutol
ETH : Etionamid
FDA : Federal Drug Administration
FQs : Fluoroquinolon
H : Isoniasid
HDL : Hospital DOTS Linkage
HIV : Human Immunodeficiency Virus
INH : Isoniasid
ISTC : International Standard for Tuberculosis Care
IUATLD : International Union Againt Tuberculosis Lung Disease
JAMKESMAS : Jaminan Kesehatan Masyarakat
JAMSOSTEK : Jaminan Sosial Tenaga Kerja
KDT : Kombinasi Dosis Tetap
KHM : Konsentrasi Hambat Minimum
LJ : Lowenstein Jensen
MDR-TB : Multidrug Resistance Tuberculosis
MENKES : Menteri Kesehatan
MGIT : Mycobacterial Growth Indicator Tube
MOTT : Mycobacterium Other Than Tuberculosis
M.Tb : Mycobacterium tuberculosis
MTT : 3-(4,5-dimethylthiazol-2-yl)-2,5-diphenyl tetrazolium bromide
M.Tuberculosis : Mycobacterium tuberculosis
NRA : Nitratre Reduction Assay
OAT : Obat Anti Tuberkulosis
PAS : Para Amino Salisilat
PDPI : Perhimpunan Dokter Paru Indonesia
PMO : Pengawas Menelan Obat
PPM : Public Private Mix
PPP : Public Private Partnership
PZA : Pirazinamid
R : Rifampisin
REMA : Resazurin Microtiter Assay
RISKESDAS : Riset Kesehatan Dasar
RMP : Rifampisin
RNA : Rybonucleic Acid
rRNA : Ribosom Rybonucleic Acid
RS : Rumah Sakit
RSUP : Rumah Sakit Umum Pusat
S : Streptomisin
SD : Standar Deviasi
SK : Surat Keputusan
SM : Streptomisin
SPS : Sewaktu, Pagi, Sewaktu.
TB : Tuberkulosis
TBC : Tuberculosis
WHO : World Health Organization
XDR-TB : Extensively Drug Resistance Tuberculosis
Z : Pirazinamid
(+) : Positif
ABSTRAK
Judul: Studi Kasus Mycobacterium tuberculosis yang Resisten Terhadap Antibiotik Lini Pertama pada Pasien Tuberkulosis di RSUP Fatmawati
Penyakit tuberkulosis telah menjadi masalah kesehatan di dunia, termasuk
Indonesia. Prevalensi tuberkulosis di Indonesia terus meningkat tiap tahunnya,
sementara pengobatan TB yang tidak adekuat dapat menyebabkan resistensi
bakteri tuberkulosis terhadap OAT, terutama antibiotik lini pertama yang sudah
lama digunakan pada pengobatan tuberkulosis. Penelitian ini bertujuan untuk
melakukan studi kasus Mycobacterium tuberculosis yang telah resisten terhadap antibiotik lini pertama pasien tuberkulosis di RSUP Fatmawati dalam kurun
waktu tiga tahun (1 Juli 2009 – 31 Juli 2012) berdasarkan hasil pemeriksaan
sputum BTA Laboratorium Patologi Klinik RSUP Fatmawati dan pengujian
kultur resistensi laboratorium rujukan. Populasi pasien TB dengan BTA (+)
selama Juli 2009-Juli 2012 sebanyak 609 pasien, sedangkan pasien yang
mendapatkan hasil pengujian kultur dan dijadikan sebagai sampel penelitian
berjumlah 88 pasien (14,45%). Hasil uji resistensi menunjukkan bahwa terjadi 31
kasus M.tb yang resisten terhadap antibiotik lini pertama rifampisin, dan 17 kasus
M.tb yang resisten terhadap antibiotik lini pertama streptomisin. Karakteristik sampel antara lain umur pasien memiliki nilai rata-rata 42 tahun dengan standar
deviasi 13,6, jenis kelamin 47,7% laki-laki dan 52,3% perempuan, jenis pasien
terbanyak adalah pasien umum (64,7%), dan tipe TB paru pasien kasus baru dan
kasus kambuh sama banyak, yaitu 43,18%.
ABSTRACT
Title: Case Study of Resistant Mycobacterium tuberculosis to the First Line Antibiotics from Tuberculosis Patient at RSUP Fatmawati
Tuberculosis has become a health problem in the world, including Indonesia.
Prevalence of tuberculosis keeps increasing yearly, meanwhile inadequate
tuberculosis medication can causes some drug resistances to occur, especially for
the first line antibiotics which have been used in medication for a long time. This
research’s main purpose is to find out about case of resistant Mycobacterium tuberculosis is to the first line antibiotics on tuberculosis patient at RSUP Fatmawati for three years (July 1st 2009 – July 31th 2012) based on sputum
check up data from Clinical Pathology Laboratory RSUP Fatmawati and
resistance culture test from a partner laboratory. Tuberculosis patient population
with BTA (+) since July 2009 until July 2012 was 609 patients, which patient
with resistance culture test result and become sample was counted 88 patients
(14,45%). Resistance culture test result showed that there was 31 cases of M.tb
resistant to the first line antibiotic rifampycin , and 17 case of M.tb resistance to the first line antibiotic streptomycin. Some of sample characteristics were
patient’s age mean was 42 years with SD value was counted 13,6, male patient
was 47,7% and female patient was 52,3%, the biggest value of patient’s type was
public (64,7%), and tuberculosis type for new case and relaps had a same value
(43,18%).
BAB I
PENDAHULUAN
1.1. Latar Belakang
Penyakit tuberkulosis merupakan penyakit yang menjadi masalah
kesehatan di dunia, terutama pada negara berkembang, termasuk Indonesia.
Setidaknya diperkirakan terjadi kasus TB paru sebanyak 3,90 juta kasus tiap
tahunnya dengan diagnosa Basil Tahan Asam (BTA) positif, di mana 80% kasus
tersebut terjadi di negara berkembang dan sepertiganya berada di Asia Tenggara.1
Indonesia menduduki peringkat ketiga kasus TB terbanyak di dunia setelah Cina
dan India.2 Hasil riset kesehatan dasar (RISKESDAS) menunjukkan pada tahun
2007, prevalensi kasus tuberkulosis di Indonesia yang terdiagnosis oleh tenaga
medis mencapai 400 per 100.000 penduduk.3 Prevalensi tuberkulosis ini terus
meningkat, terbukti pada tahun 2010, angka prevalensi kasus tuberkulosis di
Indonesia sudah mencapai 725 per 100.000 penduduk.4
Pengobatan TB yang tidak adekuat dapat menyebabkan timbulnya
resistensi bakteri tuberkulosis terhadap OAT. Timbulnya resistensi
M.tuberculosis dapat berupa resistensi obat tunggal (DR-TB) maupun sejumlah atau keseluruhan OAT lini pertama (Multidrug Resistance Tuberculosis). Secara umum resisten adalah suatu keadaan di mana organisme normal telah memiliki
kemampuan untuk melawan agen di sekitarnya yang mempengaruhi pertumbuhan
dan perkembangan alaminya.1
Drug Resistance Tuberculosis (DR-TB) seringkali muncul akibat kesalahan penatalaksanaan penyakit tuberkulosis. Terapi TB yang tidak tepat
seperti monoterapi OAT tunggal akan menyebabkan bakteri yang rentan akan
mati, namun bakteri yang tidak sensitif terhadap OAT tersebut akan tetap hidup.
Kelompok bakteri yang masih hidup ini akan menghasilkan populasi bakteri
resisten yang lebih besar terhadap obat yang telah diberikan.5 Mekanisme
resistensi secara molekuler telah dapat dijelaskan baik pada keseluruhan OAT lini
pertama maupun beberapa OAT lini kedua, seperti rifampisin, isoniasid,
pirazinamid, etambutol, beberapa antibiotik golongan aminoglikosida dan
Laporan terbaru dari Anti-tuberculosis Drug Resistance Surveillance Global Project yang dipublikasikan oleh WHO dan International Union Against Tuberculosis and Lung Disease (The Union) memaparkan persentase timbulnya
multidrug resistance (MDR) pada paling tidak rifampisin (RMP) dan isoniasid (INH) untuk kasus-kasus baru berkisar 0% sampai 22,3%. Persentase terbesar
timbulnya MDR-TB sebanyak 60% pada kasus-kasus yang sebelumnya ditangani.
Sementara itu kemungkinan timbulnya extensively drug-resistance TB (XDR-TB) yang didefinisikan sebagai MDR-TB dengan tambahan resistensi antibiotika
golongan fluoroquinolon (FQs) dan setidaknya satu obat injeksi lini kedua
memiliki persentase berkisar antara 0% sampai 30%. Ditemukan sekitar 40.000
kasus XDR-TB di dunia tiap tahunnya.7
Berbagai kemajuan telah dicapai untuk menangani penyakit tuberkulosis
di Indonesia, antara lain program DOTS (Directly Observed Treatment Short Course) di mana Indonesia hampir mencapai target 70/85 (70% kasus TB berhasil ditemukan dan 85% diantaranya berhasil ditangani. Selain itu diperkenalkan juga
program HDL (Hospital DOTS Linkage) untuk menjalankan program DOTS di rumah sakit, PPP (Public Private Partnership) atau PPM (Public Private Mix) di mana melibatkan sektor privat untuk menangani kasus TB di Indonesia. Selain itu
juga diadakan program DOTS plus untuk menangani kasus-kasus MDR-TB.8
Program DOTS melibatkan komitmen pemerintah untuk menjalankan program
TB nasional, dengan kasus TB yang harus dikuatkan melalui pemeriksaan BTA
mikroskopik, pemberian obat jangka pendek yang diawasi secara langsung dan
berkesinambungan oleh PMO (Pengawas Menelan Obat) baik petugas kesehatan,
keluarga, ataupun tokoh masyarakat yang memonitor penggunaan obat anti
tuberkulosis kepada pasien.9
Selain program DOTS, pada tahun 2006 WHO telah mencanangkan
standar pelayanan kasus TB yaitu International Standard for Tuberculosis Care (ISTC). ISTC merupakan standar yang melengkapi penatalaksanaan penanggulangan tuberkulosis nasional yang konsisten. ISTC mencakup standar
untuk diagnosa, pengobatan dan standar yang berhubungan dengan kegiatan
kesehatan masyarakat.9
Beberapa penelitian telah dilakukan untuk mengetahui kasus resistensi
pada tahun 2009 menyebutkan bahwa ditemukan kasus resistensi Mycobacterium tuberculosis terhadap antibiotik rifampisin sebesar 10,28% dan resistensi terhadap antibiotik streptomisin sebesar 14,95%.10 Persentase yang lebih besar
ditemukan pada penelitian mengenai pola resistensi Mycobacterium tuberculosis
pada narapidana di lembaga permasyarakatan kelas 1 pria di Tanjung Gusta
Medan periode Juli-Desember 2007, di mana diketahui telah terjadi resistensi
antibiotik rifampisin (40%) dan streptomisin (86,7%).1 Kasus resistensi ini dapat
terus meningkat, terlebih lagi di kawasan padat penduduk dengan tingkat
penularan yang lebih besar.11 Hanya saja informasi mengenai perkembangan
kasus resistensi Mycobacterium tuberculosis terhadap OAT lini pertama masih sangat minim, sementara penggunaan obat antituberkulosis harus selalu dilakukan
pengkajian untuk memastikan efektifitasnya, terutama penggunaan antibiotik lini
pertama. Butuh pengetahuan yang terus berkembang untuk menangani
pengobatan TB dengan baik.8
Dalam konteks isu epidemiologi global TB, maka penatalaksanaan kasus
TB dititikberatkan pada manfaat surveilens berbasis uji kultur TB dan sensitifias
obat terutama pada negara-negara berkembang. Meskipun prevalensi MDR-TB
yang tinggi mengakibatkan biaya pengobatan menjadi sangat mahal, akan lebih
buruk akibatnya apabila sistem surveilens resistensi obat tersebut tidak
dilakukan.12 Oleh karena itu deteksi dini kemungkinan resisten obat
antituberkulosis perlu dilakukan. Tidak hanya pada pasien yang dicurigai
mengalami MDR-TB, namun juga pasien TB kasus baru yang belum memiliki
riwayat pengobatan TB sebelumnya, tujuannya adalah untuk mengetahui sejauh
mana penularan M.Tuberculosis terhadap lingkungan masyarakat seiring dengan meningkatnya penemuan kasus TB di Indonesia. Oleh karena itu perlu dilakukan
penelitian mengenai prevalensi kasus resistensi antibiotik tuberkulosis pada
penderita TB di RSUP Fatmawati.
1.2. Perumusan Masalah
Dari uraian di atas menunjukkan bahwa:
- Penyakit tuberkulosis tiap tahun terus mengalami peningkatan. Hasil riset
kesehatan dasar (RISKESDAS) menunjukkan pada tahun 2007, angka
prevalensi kasus tuberkulosis di Indonesia mencapai 400 per 100.000
penduduk dan meningkat pada tahun 2010 angka prevalensi kasus
- Penderita tuberkulosis pada umumnya menolak untuk berobat ke fasilitas
kesehatan seperti rumah sakit atau puskesmas dikarenakan kesulitan
pengobatan dan pengaruh dari lingkungan masyarakat.
- Penyakit tuberkulosis yang diderita oleh satu orang, apabila tidak diobati
dapat menularkan Mycobacterium tuberculosis pada 5-10 orang lainnya. - Pada umumnya penderita tuberkulosis merasa enggan mengkonsumsi obat anti
tuberkulosis (OAT) setiap harinya selama paling tidak 6 bulan, sehingga
diperlukan pengawas minum obat (PMO) yang bertanggung jawab mengawasi
dan memastikan penderita meminum OAT setiap hari. Apabila ini tidak
dilaksanakan dapat meningkatkan kemungkinan kegagalan pengobatan. Hal
ini dapat memicu terjadinya resistensi tuberkulosis.
- Obat anti tuberkulosis (OAT) lini pertama, terutama antibiotik rifampisin dan
streptomisin sudah lama digunakan di berbagai fasilitas kesehatan termasuk
puskesmas dan rumah sakit. Dikhawatirkan dengan tidak rasionalnya
penggunaan obat ini menyebabkan Mycobacterium tuberculosis mengalami resistensi terhadap obat anti tuberkulosis lini pertama tersebut.
Berdasarkan permasalahan tersebut diketahui bahwa penderita
tuberkulosis dapat menularkan bakteri M.tuberculosis resisten sehingga ditemukan kasus-kasus TB baru dengan bakteri yang telah resisten dengan OAT
lini pertama. Tidak adanya deteksi dini dengan pengujian kultur resistensi dapat
menambah daftar panjang resistensi obat-obat anti tuberkulosis pada penderita
TB tersebut.
1.3. Pertanyaan Penelitian
- Apakah sudah terjadi resistensi M.tuberculosis terhadap antibiotik lini pertama pada pasien tuberkulosis di RSUP Fatmawati?
- Berapakah persentase resistensi M.tuberculosis terhadap antibiotik lini pertamayang muncul pada penderita TB di RSUP Fatmawati?
1.4. Tujuan Penelitian 1.4.1. Tujuan Umum
Penelitian ini bertujuan unuk mengetahui jumlah kasus resistensi kuman
1.4.2. Tujuan Khusus
- Untuk mengetahui jumlah pasien tuberkulosis yang mengalami Drug Resistance Tuberculosis (DR-TB) di RSUP Fatmawati.
- Untuk mengetahui jumlah kasus (persentase) resistensi Mycobacterium tuberculosis terhadap antibiotik lini pertama (rifampisin dan streptomisin) yang digunakan pasien di RSUP Fatmawati berdasarkan data pemeriksaan
laboratorium.
1.5. Manfaat Penelitian a. Secara Metodelogi
Metode penelitian ini dapat menjadi contoh atau dapat dijadikan metode
untuk mengetahui kasus resistensi dalam penggunaan antibiotik lainnya dalam
pengobatan.
b. Secara Aplikatif
1. Hasil penelitian ini dapat digunakan oleh RSUP Fatmawati sebagai data dasar
untuk mengetahui resistensi antibiotik lini pertama pengobatan tuberkulosis di
RSUP Fatmawati atau di rumah sakit lainnya yang mempunyai karakteristik
pasien yang sama dengan pasien di RSUP Fatmawati.
2. Hasil penelitian ini hendaknya dapat menjadi informasi untuk membuat
pengobatan tuberkulosis menjadi lebih efektif.
1.6. Justifikasi
Penelitian yang berjudul “Studi Kasus Mycobacterium tuberculosis yang Resisten Terhadap Antibiotik Lini Pertama pada Pasien Tuberkulosis di RSUP Fatmawati” belum dilakukan di RSUP Fatmawati. Kemungkinan di daerah lain sudah pernah dilakukan, namun berbeda dengan penelitian yang
dilakukan ini, dalam hal besar sampel, waktu penelitian, lokasi penelitian dan
kriteria-kriteria inklusi (pasien, jenis penyakit dan jumlah basil pada sputum).
1.7. Ruang Lingkup
Permasalahan tuberkulosis sangat luas baik pengobatan maupun
tuberculosis yang resisten terhadap antibiotik lini pertama pada pasien tuberkulosis di RSUP Fatmawati.
- Penelitian ini dilaksanakan di RSUP Fatmawati tepatnya di Laboratorium
Klinik Instalasi Patologi dan Instalasi Rekam Medis dan Infokes RSUP
Fatmawati.
- Waktu penelitian dimulai dari bulan Agustus sampai bulan September 2012.
- Populasi adalah pasien TB paru dengan BTA (+) di RSUP Fatmawati.
- Besar sampel dalam penelitian ini adalah seluruh pasien tuberkulosis di RSUP
Fatmawati dengan hasil BTA positif dan memiliki hasil pengujian kultur
resistensi tuberkulosis laboratorium rujukan dalam kurun waktu tiga tahun (1
Juli 2009 hingga 31 Juli 2012). Sampel ditentukan secara purposif sebanyak
100 pasien.
- Obat yang dikumpulkan data resistensinya terhadap M.tuberculosis adalah antibiotik lini pertama pengobatan tuberkulosis, yaitu rifampisin dan
streptomisin.
- Desain penelitian ini adalah cross sectional.
- Pengumpulan data resistensi M.tuberculosis terhadap antibiotik diperoleh dari hasil pemeriksaan sputum RSUP Fatmawati dan pengujian kultur resistensi
BAB II
TINJAUAN PUSTAKA
2.1. Tuberkulosis (TB)
Tuberkulosis adalah penyakit yang disebabkan oleh infeksi
Mycobacterium tuberculosis complex.9 Tuberkulosis merupakan penyakit infeksi yang menjadi salah satu penyebab terjadinya kematian, bahkan menjadi urutan
kedua setelah infeksi virus HIV-AIDS.13 Mycobacterium tuberculosis telah menjadi patogen dan menginfeksi manusia sejak ratusan tahun. Meskipun uji
diagnosa, kemoterapi dan vaksin telah tersedia, penyakit tuberkulosis ini masih
sulit untuk dimusnahkan.14 Meningkatnya penyakit tuberkulosis kini
berhubungan dengan peningkatan infeksi HIV-AIDS, sehingga strategi DOTS
sebagai pengobatan tuberkulosis tidak cukup ampuh untuk mengontrol
tuberkulosis, terutama di Afrika dan Uni Soviet.13
2.1.1. Patogenesis
Kuman tuberkulosis yang masuk melalui saluran napas akan bersarang di
jaringan paru sehingga akan terbentuk suatu sarang pneumonik, yang disebut
sarang primer atau afek primer. Masa inkubasi M.tuberkulosis hingga membentuk afek primer biasanya berlangsung dalam waktu 10-20 hari.15 Dari
sarang primer akan terlihat peradangan saluran getah bening menuju hilus
(limfangitis lokal). Peradangan tersebut diikuti oleh pembesaran kelenjar getah
bening di hilus (limfadenitis regional). Afek primer bersama-sama dengan
limfangitis regional dikenal sebagai kompleks primer (tuberkulosis). Komplek
primer tersebut akan mengalami beberapa kemunginan:
1. Sembuh dengan tidak meninggalkan cacat sama sekali (restitution ad integrum).
2. Sembuh dengan meninggalkan sedikit bekas (antara lain Ghon, garis
fibrotik, sarang perkapuran di hilus).
3. Menyebar dengan cara:
Perkontinuitatum, menyebar ke daerah di sekitarnya. Misalnya pada epituberkulosis, yaitu suatu kejadian penekanan bronkus, biasanya bronkus
lobus medius oleh kelenjar hilus yang membesar sehingga menimbulkan
obstruksi pada saluran napas dengan akibat atelektasis. Kuman tuberkulosis
atelektasis dan menimbulkan peradangan pada lobus yang atelektasis
tersebut, yang dikenal sebagai epituberkulosis.
Penyebaran secara bronkogen, baik di bagian paru tersebut maupun ke paru sebelahnya.
Penyebaran secara hematogen dan limfogen. Penyebaran ini berkaitan dengan daya tahan tubuh, jumlah dan virulensi kuman. Sarang yang
ditimbulkan dapat sembuh secara spontan, akan tetapi bila tidak terdapat
imunitas yang adekuat, penyebaran ini akan menimbulkan keadaan cukup
gawat seperti tuberkulosis milier, meningitis tuberkulosa, typhobacillosis Landouzy. Penyebaran ini juga dapat menimbulkan tuberkulosis pada alat tubuh lainnya, misalnya tulang, ginjal, anak ginjal, genitalia dan sebagainya.
Komplikasi dan penyebaran ini kemungkinan berakhir dengan kesembuhan
yang meninggalkan sekuele (misalnya pertumbuhan terbelakang pada anak
setelah menderita ensefalomeningitis, tuberkuloma) atau meninggal.9
Secara ringkas patogenesis terjadinya tuberkulosis digambarkan dalam
skema berikut ini (gambar 1.):
Gambar 1. Skema Patogenesis Tuberkulosis.9
2.1.2. Gejala Tuberkulosis
Gejala klinis tuberkulosis dibagi menjadi dua golongan, yaitu gejala lokal
dan gejala sistemik. Bila organ yang terkena adalah paru maka disebut sebagai
gejala lokal, yaitu gejala respiratorik (gejala lokal sesuai organ yang terlibat).
Gejala sistemik adalah gejala yang dirasakan di seluruh tubuh dan tidak spesifik
1. Gejala respiratorik:
- Batuk-batuk selama dua minggu atau lebih.
- Batuk berdarah.
- Sesak napas.
- Nyeri dada.
Gejala respiratorik sangat bervariasi, dari mulai tidak ada gejala sampai
gejala yang cukup berat tergantung dari luas lesi. Kadang pasien terdiagnosis
pada saat medical check up. Bila bronkus belum terlibat dalam proses penyakit, maka pasien mungkin tidak ada gejala batuk. Batuk yang pertama terjadi karena
iritasi bronkus, dan selanjutnya batuk diperlukan untuk membuang dahak ke
luar.9
2. Gejala sistemik: - Demam.
- Malaise.
- Anoreksia.
- Keringat malam.
- Berat badan menurun.
Pada tuberkulosis ekstra paru, gejala yang timbul tergantung dari organ
yang terlibat, misalnya pada limfadenitis tuberkulosa akan terjadi pembesaran
yang lambat dan tidak nyeri dari kelenjar getah bening, pada meningitis
tuberkulosa akan terlihat gejala meningitis, sementara pada pleuritis tuberkulosa
terdapat gejala sesak napas & kadang nyeri dada pada sisi yang rongga pleuranya
terdapat cairan.9
2.1.3. Manifestasi Klinik
Tuberkulosis paru mempunyai onset yang cepat dan dapat menular
dengan cepat. Manifestasi klinik yang umum terlihat pada penderita tuberkulosis
adalah batuk kronik dengan produksi sputum, penurunan berat badan dan rasa
lemah.16
2.2. Mycobacterium Tuberculosis
Mycobacterium tuberculosis berbentuk batang lurus atau sedikit melengkung, tidak berspora dan tidak berkapsul. Bakteri ini berukuran lebar 0,3 –
Penyusun utama dinding sel M. tuberculosis ialah asam mikolat, lilin kompleks (complex-waxes), trehalosa dimikolat yang disebut cord factor, dan
mycobacterial sulfolipids yang berperan dalam virulensi. Asam mikolat merupakan asam lemak berantai panjang (C60 – C90) yang dihubungkan dengan
arabinogalaktan oleh ikatan glikolipid dan dengan peptidoglikan oleh jembatan
fosfodiester. Unsur lain yang terdapat pada dinding sel bakteri tersebut adalah
polisakarida seperti arabinogalaktan dan arabinomanan. Struktur dinding sel yang
kompleks tersebut menyebabkan bakteri M.tuberculosis bersifat tahan asam, yaitu apabila sekali diwarnai akan tetap tahan terhadap upaya penghilangan zat
warna tersebut dengan larutan asam – alkohol.9
Mycobacterium tuberculosis tidak dapat diwarnai dengan cara gram, tetapi dengan pewarnaan tahan asam. Dibandingkan dengan kuman lainnya,
golongan Mycobacterium tahan terhadap asam dan alkali sehingga apabila bahan spesimen mengandung kuman lain mudah dapat dibunuh sehingga spesimen
menjadi lebih murni. Tetapi harus diperhatikan kepekatan zat asam dan alkali
karena terlalu pekat juga akan membunuh Mycobacterium.17 Komponen antigen
ditemukan di dinding sel dan sitoplasma yaitu komponen lipid, polisakarida dan
protein. Karakteristik antigen M.tuberculosis dapat diidentifikasi dengan menggunakan antibodi monoklonal.9
M.tuberculosis dapat dengan mudah mati bila terpapar sinar matahari langsung, tetapi dapat bertahan hidup pada suhu rendah (dapat bertahan
bertahun-tahun di dalam lemari es). Hal ini disebabkan karena bakteri tersebut berada
dalam keadaan dormant. Pada kondisi ini kuman dapat dibangkitkan kembali dan menjadi bakteri tubekulosis yang aktif.1
Daya tahan Mycobacterium tuberculosis lebih besar apabila dibandingkan dengan kuman lainnya karena sifat hidrofobik permukaan sel.
Malakhit hijau dapat membunuh kuman lain tetapi tidak membunuh
Mycobacterium tuberculosis, demikian juga dengan alkali. Dengan fenol 5% diperlukan waktu 24 jam untuk membunuh Mycobacterium tuberculosis.17 Basil ini dihancurkan oleh iodium tinktur dalam 5 menit, dengan alkohol 80 % akan
2.2.1. Morfologi dan Fisiologi a. Mikroskopik:
Pada jaringan tubuh kuman tuberkulosis berbentuk batang halus
berukuran 3x0,5 µm. Pada pembenihan berbentuk kokoid dan berfilamen. Tidak
berspora dan tidak bersimpai. Pada pewarnaan dengan cara Ziehl-Neelsen atau
Tan Thiam Hok kuman berwarna merah dengan latar belakang berwarna biru.
Pada pewarnaan fluorochrom kuman berfluoresensi dengan warna kuning
oranye.17
b. Kultur:
i. Pembenihan cair.
Medium asam oleat-albumin (Dubos). Pada medium ini mengandung
Tween-80, kuman akan tumbuh merata pada seluruh medium. Biasanya pada
medium cair, pertumbuhan lebih cepat.9
ii. Pembenihan padat.
Lowenstein-Jensen, medium ini mengandung telur, gliserol, garam-garam mineral, malakhit hijau dan biasanya dicampur dengan penisilin untuk
membunuh kuman penyerta lainnya.17 Medium berbasis telur lainnya antara
lain Ogawa dan Kudoh. Untuk medium agar dapat digunakan media Middle Brook.9
2.2.2. Sifat-Sifat Pertumbuhan
Mycobacterium tumbuh secara aerob obligat. Energi didapat dari
oksidasi senyawa karbon sederhana yang dapat merangsang pertumbuhan.
Pertumbuhannya lambat, waktu pembelahan sekitar 20 jam. Suhu pertumbuhan
optimum 37oC. Pada perbenihan, pertumbuhan tampak setelah 2-3 minggu.
Koloni cembung, kering, berwarna kuning gading. Pengaruh pemanasan daya
tahannya sama dengan kuman lainnya, jadi dengan pasteurisasi kuman
tuberkulosis ini sudah dapat dibunuh.17
2.3. Diagnosa
Diagnosis tuberkulosis dapat ditegakkan berdasarkan gejala klinik,
pemeriksaan fisik/jasmani, pemeriksaan bakteriologik, radiologik dan
pemeriksaan penunjang lainnya. Pada tuberkulosis paru, kelainan yang didapat
penyakit umumnya tidak (atau sulit sekali) menemukan kelainan. Kelainan paru
pada umumnya terletak di daerah lobus superior terutama daerah apeks dan
segmen posterior (S1 & S2) , serta daerah apeks lobus inferior (S6). Pada
pemeriksaan jasmani dapat ditemukan antara lain suara napas bronkial, amforik,
suara napas melemah, ronki basah, tanda-tanda penarikan paru, diafragma &
mediastinum.9
Pada pleuritis tuberkulosa, kelainan pemeriksaan fisik tergantung dari
banyaknya cairan di rongga pleura. Pada perkusi ditemukan pekak, pada
auskultasi suara napas yang melemah sampai tidak terdengar pada sisi yang
terdapat cairan. Pada limfadenitis tuberkulosa, terlihat pembesaran kelenjar getah
bening, tersering di daerah leher, terkadang di daerah ketiak.9
2.4. Diagnosa Laboratorium
Diagnosis yang paling pasti dari penyakit tuberkulosis adalah dengan
pemeriksaan mikrobiologi dengan cara mengisolasi kumannya. Proses
pemeriksaan laboratorium ini melalui beberapa tahapan dan didasarkan pada
sampel dan tujuan pemeriksaan.9
2.4.1. Bahan Spesimen
Bahan spesimen dapat berupa dahak segar, cairan lambung, urin, cairan
pleura, cairan otak, cairan sendi, bahan biopsi dan lain-lain. Cara pengumpulan
dan pengiriman bahan antara lain:
1. Cara pengambilan dahak tiga kali (SPS) dalam dua kali kunjungan
a. Sewaktu/spot (dahak sewaktu saat kunjungan pertama kali).
b. Pagi (keesokan harinya dengan membawa sputum pagi).
c. Sewaktu/spot (pada saat pada saat pasien diminta mengeluarkan
sputumnya lagi).19
Spesimen dahak yang ada dalam pot (jika pada gelas objek dimasukkan
ke dalam kotak sediaan) yang akan dikirim ke laboratorium, harus dipastikan
telah tertulis identitas pasien yang sesuai dengan formulir permohonan
pemeriksaan laboratorium. Berdasarkan SK Menkes nomor 241 tahun 2006
tentang standar pelayanan laboratorium kesehatan pemeriksa HIV dan infeksi
oportunistik menyatakan persayaratan permintaan pemeriksaan laboratorium
1. Tanggal permintaan.
2. Tanggal dan jam pengambilan bahan pemeriksaan.
3. Identitas pasien (nama,umur/tanggal lahir, jenis kelamin, alamat, nomor
telepon) atau identitas bahan pemeriksaan.
4. Identitas pengirim (nama, alamat, nomor telepon).
5. Diagnosis/keterangan klinik.
6. Obat-obatan yang telah diberikan dan lama pemberian.
7. Pemeriksaan laboratorium yang diminta.
8. Nama pengambil bahan pemeriksaan.20
Sementara label wadah bahan pemeriksaan yang akan dikirim ke
laboratorium harus mencantumkan:
1. Tanggal dan jam pengambilan bahan pemeriksaan.
2. Identitas pasien atau identitas bahan pemeriksaan.
3. Jenis bahan pemeriksaan.20
2. Pengambilan spesimen cairan
Bahan pemeriksaan/spesimen yang berbentuk cairan
dikumpulkan/ditampung dalam pot yang bermulut lebar, berpenampang 6 cm
atau lebih dengan tutup berulir, tidak mudah pecah dan tidak bocor. Apabila ada
fasiliti, spesimen tersebut dapat dibuat sediaan apus pada gelas objek (difiksasi)
sebelum dikirim ke laboratorium.9
3. Pengambilan spesimen biopsi
Bahan pemeriksaan hasil biopsi jarum halus (BJH), dapat dibuat sediaan
apus kering di gelas objek, atau untuk kepentingan biakan dan uji resistensi dapat
ditambahkan NaCl 0,9% 3-5 ml sebelum dikirim ke laboratorium.9
2.4.2. Mikroskopik
Pemeriksaan mikroskopik untuk diagnostik adalah yang termudah,
tercepat dan termurah. Untuk mendapat hasil yang sebaik-baiknya, maka harus
dibuat sediaan yang sebaik-baiknya dan diwarnai dengan cara Tan Thiam Hok
(Kinyoun-Gabbett) atau cara Ziehl-Neelsen. Pada pewarnaan tahan asam akan
terlihat kuman berwarna merah dan latar belakang berwarna biru. Daya
mikroskop cahaya biasa sangat terbatas untuk mendeteksi jumlah kuman yang
luas pandangan yang lebih besar karena lensa objektif yang lebih besar dan
gambar yang terlihat cukup jelas karena berfluoresensi dengan zat warna auramin
rhodamin. Hasil positif secara mikroskop tentu saja tidak berarti definitif, begitu
pula sebaliknya dapat dimengerti bahwa hasil negatif belum tentu tidak ada
kuman, harus dipastikan dengan cara pembenihan.17
2.4.3. Cara Pewarnaan
1. Ziehl-Neelsen (Direct Smear Examination):
a. Alat dan bahan yang diperlukan:
- Botol gelas berwarna coklat berisi larutan Carbol Fuchsin 0,3%. - Botol gelas berwarna coklat berisi asam akohol (HCl-Alcohol 3%). - Botol coklat berisi larutan Methylen Blue 1%.
- Rak untuk pengecatan slide.
- Baskom untuk ditempatkan di bawah rak.
- Corong dengan kertas filter.
- Pipet.
- Pinset.
- Pengukur waktu (timer).
- Api spiritus.
- Air yang mengalir berupa air ledeng atau botol berpipet berisi air.
- Beberapa rak cadangan.
b. Cara pewarnaan:
- Sediaan dahak yang telah difiksasi diletakkan pada rak dengan
hapusan dahak menghadap ke atas.
- Diteteskan Carbol Fuchsin 0,3% pada hapusan dahak sampai menutupi seluruh permukaan sediaan dahak.
- Dipanaskan dengan nyala api spiritus sampai mengeluarkan uap. Zat
warna tidak boleh mendidih atau kering. Apabila mendidih atau kering
maka Carbol Fuchsin akan membentuk kristal (partikel kecil) yang dapat terlihat seperti kuman TB.
- Api spiritus disingkirkan, sediaan didiamkan selama lima menit.
- Sediaan dibilas dengan air mengalir pelan sampai zat warna yang
- Sediaan diteteskan dengan asam alkohol (HCl Alcohol 3%) sampai warna merah pada Fuchsin menghilang.
- Dibilas dengan air mengalir perlahan.
- Diteteskan dengan larutan Methylen Blue 1% pada sediaan sampai menutupi seluruh permukaan.
- Didiamkan selama 10-20 detik.
- Larutan dibuang dan dibilas dengan air mengalir perlahan.
- Sediaan dikeringkan di atas rak pengering di udara terbuka (jangan di
bawah sinar matahari langsung).21
2.4.4. Pembacaan Jumlah Bakteri
Interpretasi hasil pemeriksaan dahak dari tiga kali pemeriksaan adalah:
- Tiga kali positif atau dua kali positif, satu kali negatif → BTA positif.
- Satu kali positif, dua kali negatif → Pemeriksaan BTA diulang tiga kali
kecuali bila ada fasilitas foto toraks, kemudian jika hasil ulangan diperoleh
satu kali positif, dua kali negatif → BTA positif. - Bila tiga kali negatif → BTA negatif.9
Interpretasi pemeriksaan mikroskopik dibaca dengan skala IUATLD
(rekomendasi WHO). Skala IUATLD (International Union Against Tuberculosis and Lung Disease) yaitu:
- Tidak ditemukan BTA dalam 100 lapang pandang, disebut negatif.
- Ditemukan 1-9 BTA dalam 100 lapang pandang, ditulis jumlah kuman yang
ditemukan.
- Ditemukan 10-99 BTA dalam 100 lapang pandang disebut + (1+).
- Ditemukan 1-10 BTA dalam 1 lapang pandang, disebut ++ (2+).
- Ditemukan >10 BTA dalam 1 lapang pandang, disebut +++ (3+).19
2.4.5. Pembiakan
Pembiakan adalah cara yang paling sensitif untuk mendiagnosis
tuberkulosis terutama untuk dahak yang sedikit kumannya dan sulit ditemukan
dengan cara mikroskopik. Pembiakan juga penting untuk dapat melakukan tes
kepekaan kuman terhadap obat-obatan.17
Pada hasil kultur positif, langsung dapat diperkirakan jenis kuman tahan
asam dengan melihat lama pertumbuhan (cepat bila tumbuh dalam 3-4 hari), ada
tumbuh setelah 2-3 minggu dengan koloni yang timbul dari permukaan berwarna
kuning susu atau cream.17
Pemeriksaan kultur (Culture Examination) dengan menggunakan media
Ogawa dilakukan dengan cara sebagai berikut: a. Komposisi media Ogawa:
- Larutan Potasium hydrogen phosphate anhydrous (KH2PO4) 3 gram.
- Sodium glutamate 1 gram. - Aquadest 100 ml.
- Glycerol 6 ml.
- Malachite green 2% 6 ml. - Telur yang telah dikocok 200 ml.
b. Alat dan bahan:
- Pipet 10 ml.
- Tabung pembenihan (18x180 mm) dengan tutup.
- Rak tabung.
- Penyangga miring.
- Inkubator.
- Media Ogawa 3%.
- Larutan NaOH 4%.
- Lidi kapas steril.
- Vortex.
- Lilin cair.
c. Cara kerja:
- Larutan NaOH 4% ditambahkan kira-kira sebanyak empat volume dalam
sediaan sputum.
- Disimpan dalam inkubator 37oC selama 15 menit.
- Diaduk dengan menggunakan vortex.
- Diambil lebih kurang 0,10 ml (volume variatif) menggunakan lidi kapas
steril untuk diinokulasikan dengan meratakannya pada dua tabung kultur
yang berisi media Ogawa 3%.
- Tabung diletakkan pada rak miring dengan tutup dikendorkan sampai
bahan inokulasi kering dan merata, ditutup terlebih dahulu dengan tutup
- Pembenihan yang telah ditanami disimpan pada inkubator 37oC sampai
sekurang-kurangnya 4 minggu dan diamati setiap minggunya.1
Pemeriksaan kultur dengan medium Lowenstein Jensen dipersiapkan sesuai dengan petunjuk pembuatan produsennya (BBL,Merck). Medium tersebut
dipersiapkan dengan cara sebagai berikut:
a. Alat dan bahan:
- Pipet 10 ml.
- Tabung pembenihan (20x150 mm) dengan tutup baling-baling (screw capped tubes).
- Rak tabung.
- Basis medium Lowenstein-Jensen (Merck) 18,65 gram - Inkubator.
- Aquadest 300 ml.
- Gliserol (grade reagen) 6 ml.
- Telur utuh 500 ml.
b. Cara kerja:
- Ditimbang sebanyak 18,65 gram basis medium LJ.
- Dilarutkan dalam 300 ml air destilata.
- Ditambahkan 6 ml gliserol (grade reagen) dan diaduk hingga homogen.
- Larutan tersebut disterilkan dalam autoklaf pada suhu 121oC selama 30
menit, kemudian didinginkan.
- Ditambahkan 500 ml telur utuh yang telah dihomogenkan terlebih dahulu
ke dalam medium, diaduk hingga homogen.
- Sekitar 6-8 ml medium dituangkan ke dalam tube bertutup baling-baling
(screw capped tubes) dengan ukuran 20x150 mm.
- Tube tersebut kemudian disimpan pada suhu 80oC selama 50 menit.
- Untuk pemeriksaan sterilitas medium, medium yang telah disiapkan
tersebut diinkubasi dalam inkubator pada suhu 37oC selama 48 jam,
kemudian disimpan dalam refrigerator untuk penyimpanan ketika tidak
ditemukan kontaminan.22
Jumlah koloni Mycobacterium tuberculosis yang tumbuh dalam biakan dihitung dan dilaporkan sebagai berikut:
- 1-19 koloni : Jumlah koloni yang terlihat.
- 2+ : 101 - 200 koloni.
- 3+ : 201 - 500 koloni.
- 4+ : >500 koloni.
2.4.6. Tes Biokimia
Tes biokimia dilakuan untuk mengidentifikasi keberadaan
Mycobacterium tuberculosis dengan Mycobacterium Other Than Tuberculosis
(MOTT). Berbagai tes tersebut antara lain:
1. Merah netral: Untuk membedakan antara Mycobacterium tuberculosis dan
Mycobacterium bovis terhadap mycobacterium lainnya. Hasil pada
Mycobacterium tuberculosis dan Mycobacterium bovis adalah positif. 2. Percobaan niasin: Hasil positif berarti Mycobacterium tuberculosis.
3. Nikotinamida 5000 mikrogram(µg)/ml: Hasil negatif berarti Mycobacterium tuberculosis.
4. Arysulfatasa: Berdasarkan ada tidaknya enzim arylsulfatasa pada kuman.
Enzim ini dapat melepaskan phenolphtalein dari ikatannya pada medium yang
dapat dideteksi dengan alkali. Hasil pada Mycobacterium tuberculosis adalah negatif.
5. Reduksi nitrat: Berdasarkan ada tidaknya enzim nitrat reduktasa yang dapat
merubah nitrat menjadi nitrit. Adanya nitrit dapat diketahui dengan reagen
asam sulfanilat. Hasil pada Mycobacterium fortuitum dan Mycobacterium kansasii adalah positif, sedangkan Mycobacterium tuberculosis bisa positif atau negatif.
6. Hidrolisis Tween-80 selama 10 hari: Berdasarkan ada atau tidaknya hidrolisis
dilihat dengan indikator merah netral. Hasil pada Mycobacterium kansasii
adalah positif dan Mycobacterium tuberculosis adalah negatif.
7. Pertumbuhan pada 4 (p)-nitro-benzoic-acid 500 µg/ml: Mycobacterium tuberculosis tidak tumbuh, sedangkan Mycobacterium fortuitum tumbuh. 8. Pertumbuhan pada thiacetazone: Mycobacterium tuberculosis tidak tumbuh,
sedangkan Mycobacterium fortuitum tumbuh.17
2.5. Klasifikasi Tuberkulosis
Tipe pasien tuberkulosis ditentukan berdasarkan riwayat pengobatan TB
1. TB kasus baru, yaitu pasien TB yang belum pernah mendapat pengobatan dengan OAT sebelumnya, atau sudah pernah menggunakan OAT kurang dari
satu bulan.9
2. TB kasus kambuh (relaps), pasien tuberkulosis yang pernah mendapat pengobatan tuberkulosis sebelumnya dan telah dinyatakan sembuh atau
pengobatan tuntas, kemudian kembali lagi berobat dengan hasil pemeriksaan
dahak BTA positif atau kultur TB positif.9
3. TB kasus putus obat/default/drop out, yaitu pasien TB yang tidak mengambil obat selama 2 bulan berturut-turut atau lebih sebelum masa pengobatannya
selesai.9
4. TB gagal terapi, yaitu pasien TB dengan BTA positif yang masih tetap positif atau kembali menjadi positif pada akhir bulan ke-5 (satu bulan sebelum akhir
pengobatan).9
5. TB kasus kronik (persisten), pasien TB dengan hasil pemeriksaan BTA masih positif setelah selesai pengobatan ulang kategori 2 dengan pengawasan yang
baik.9
2.6. Faktor Risiko
Faktor risiko dapat dibedakan menjadi faktor risiko yang dapat diubah
(modifiable risk factor) dan faktor risiko yang tak dapat diubah (unmodifiable risk factor).23 Faktor risiko tuberkulosis meliputi usia, jenis kelamin, penyakit penyerta, kepadatan hunian dan kondisi rumah, status sosial ekonomi dan
perilaku individu.
1. Usia.
Berdasarkan hasil Riset Kesehatan Dasar (RISKESDAS) tahun 2010 menunjukkan peningkatan infeksi tuberkulosis aktif yang terdiagnosa secara
bermakna sesuai dengan bertambahnya umur. Hasil RISKESDAS menunjukkan
angka tertinggi prevalensi tuberkulosis pada tahun 2010 berada pada usia 55-64
tahun. Di Indonesia, sebagian besar penderita tuberkulosis terjadi mulai dari usia
produktif (15-50 tahun) sampai lanjut usia (> 60 tahun).4
2. Jenis kelamin.
Hasil survey menunjukkan laki-laki lebih banyak mengalami penyakit
hal tersebut, terutama pengaruh pola hidup yang tidak sehat termasuk
kebiasaan merokok. Pada tahun 2010 hasil survey menunjukkan di Indonesia
sebagian besar penderita tuberkulosis dialami oleh pria (0,819%)
dibandingkan dengan wanita (0,634%).4
3. Penyakit penyerta.
Umumnya penderita tuberkulosis dalam kondisi malnutrisi dengan berat
badan berkisar 30-50 kg atau indeks masa tubuh kurang dari 18,5 pada orang
dewasa. Hal ini juga didukung oleh faktor ekonomi yang buruk terutama
untuk menyediakan makanan bergizi cukup sehingga banyak ditemukan
pasien tuberkulosis dengan status gizi buruk. Selain faktor gizi, penyakit
seperti Diabetes Melitus (DM) dan infeksi HIV-AIDS merupakan salah satu
faktor risiko yang tidak berketergantungan untuk meningkatkan kemungkinan
terjadinya tuberkulosis. Dalam wabah ini, lebih dari 90% penderita terinfeksi
HIV cenderung terkena infeksi TB dengan cepat dan aktif serta serangan
infeksi TB juga relatif tinggi dengan mortalitas tinggi.24
4. Kepadatan hunian.
Kepadatan penghuni merupakan suatu proses penularan penyakit.
Semakin padat maka perpindahan penyakit khususnya penyakit menular
melalui udara akan semakin mudah dan cepat, apalagi terdapat anggota
keluarga yang menderita TB dengan BTA(+).
Kondisi kepadatan hunian perumahan atau tempat tinggal lainnya seperti
penginapan, panti-panti tempat penampungan akan besar pengaruhnya
terhadap risiko penularan. Di daerah perkotaan (urban) yang lebih padat
penduduknya dibandingkan pedesaan (rural) peluang terjadinya kontak
dengan penderita TB lebih besar.11 Namun demikian, hasil RISKESDAS pada
tahun 2010 menunjukkan hasil yang sedikit berbeda. Prevalensi tuberkulosis
pada tahun 2010 lebih banyak terjadi pada penderita yang tinggal di pedesaan
(0,750%) dibandingkan dengan perkotaan (0,703%).4
5. Kondisi rumah.
Dari kondisi lingkungan tempat tinggal dapat terlihat tingkat
Rumah dikatakan baik dan aman, apabila kualitas bangunan dan lingkungan
dibuat dengan serasi. Adapun karakteristik rumah sehat antara lain:
a. Bahan bangunannya memenuhi syarat.
b. Ventilasi cukup, yaitu minimal luas jendela/ventilasi adalah 15% dari
luas lantai.
c. Cahaya matahari cukup, di mana cahaya matahari ini dapat diperoleh dari
ventilasi maupun jendala/genting kaca. Suhu udara yang ideal di dalam
rumah antara 18-30oC. Suhu optimal pertumbuhan bakteri sangat
bervariasi, Mycobacterium tuberculosis tumbuh optimal pada suhu 37oC. d. Luas bangunan rumah cukup, yaitu luas lantai bangunan rumah harus
cukup sesuai dengan jumlah penghuninya.11
6. Status sosial ekonomi keluarga
Sosial ekonomi yang rendah akan menyebabkan kondisi kepadatan
hunian yang tinggi dan buruknya lingkungan, selain itu masalah kurang gizi
dan rendahnya kemampuan untuk mendapatkan pelayanan kesehatan yang
layak juga menjadi problem bagi golongan sosial ekonomi rendah.
Berdasarkan hasil RISKESDAS pada tahun 2010 diketahui bahwa sebagian
besar penderita tuberkulosis tidak memiliki pekerjaan yang memadai.
Sebagian bekerja sebagai buruh, nelayan atau petani, sementara sebagian
lainnya tidak memiliki pekerjaan. Sama halnya dengan status pendidikan di
mana sebagian besar penderita tuberkulosis tidak pernah mendapatkan
pendidikan formal/sekolah.4
7. Perilaku
Perilaku dapat terdiri dari pengetahuan, sikap dan tindakan. Pengetahuan
penderita TB Paru yang kurang tentang cara penularan, bahaya dan cara
pengobatan akan berpengaruh terhadap sikap dan prilaku sebagai orang sakit
dan akhinya berakibat menjadi sumber penular bagi orang disekelilingnya.
Kebiasaan merokok menjadi salah satu faktor risiko yang sangat mungkin
menyebabkan seseorang terinfeksi kuman Mycobacterium tuberculosis. Hasil penelitian Susanto menyatakan bahwa perempuan lebih sering terlambat
datang ke pelayanan kesehatan dibandingkan dengan laki-laki. Hal ini
mungkin berhubungan dengan aib dan rasa malu lebih dirasakan pada
kekhawatiran akan dikucilkan dari keluarga dan lingkungan akibat
penyakitnya.25
2.7. Obat 2.7.1. Rifampisin
- Rumus struktur :
- Rumus molekul : C43H58N4O12.26
- Nama kimia : 5,6,9,17,19,21-Heksahidroksi-23-metoksi 2,4,12,16,18, 20, 22- heptametil-8- [N-(4-metil-1-piperazinil) formimidoil] - 2,7
(epoksipentadeka [1,11,13]trienimino]nafto[2,1-b]furan-1,11-(2H)-dion
21-asetat [13292-46-1].26
- Berat molekul : 823.26
- Pemerian : Serbuk hablur, coklat merah.26
- Kelarutan : Sangat sukar larut dalam air, mudah larut dalam kloroform, larut dalam etil asetat dan dalam metanol.26
- pH sediaan : 4,5-6,5 pada sediaan suspensi 10 gram/liter dalam air bebas CO2..26
- Farmakologi :
Antibiotik ini adalah derivat semisintetis dari rifamisin B yang dihasilkan
oleh Streptomyces mediterranei. Rifampisin bersifat bakterisid luas terhadap fase pertumbuhan Mycobacterium tuberkulosis dan Mycobacterium leprae, baik yang berada di luar maupun di dalam sel. Obat ini mematikan kuman yang dorman
selama fase pembelahan yang singkat. Maka, obat ini sangat penting untuk
membasmi semua basil guna mencegah kambuhnya TBC.
Rifampisin juga aktif terhadap kuman positif dan kuman
gram-negatif. Mekanisme kerjanya berdasarkan perintangan spesifik dari suatu enzim
Resorpsinya di usus sangat tinggi, distribusinya ke jaringan dan cairan
tubuh juga baik. Plasma t1/2 nya berkisar antara 1,5 sampai 5 jam dan meningkat
bila ada gangguan fungsi hati. Di lain pihak, masa paruh ini akan turun pada
pasien yang bersamaan waktu menggunakan isoniazid. Dalam hati terjadi
deasetilasi dengan terbentuknya metabolit-metabolit dengan kegiatan antibakteri.
Ekskresinya melalui empedu.27
- Efek samping :
Menimbulkan warna oranye yang tidak berbahaya pada urin, keringat, air
mata dan lensa mata. Efek samping yang sering terjadi termasuk kulit kemerahan,
trombositopenia, nefritis dan gangguan fungs hati.27
- Dosis :
Oral 1 dd 450-600 mg sekaligus pagi hari sebelum makan, selalu
diberikan dalam kombinasi dengan isoniazid 300 mg dan untuk 2 bulan pertama
ditambah pula dengan 1,5-2 g pirazinamid setiap hari.27 Dosis rifampisin yang
digunakan untuk pengujian resistensi tuberkulosis secara in vitro adalah berkisar
antara 2,5 – 10 ppm.7
2.7.2. Streptomisin
- Rumus struktur :
- Rumus molekul : (C21H39N7O12)2,3H2SO4.26
- Nama kimia : bis[N,N¢-bis(aminoiminomethyl)-4-O-[5-deoxy-2-O -[2-deoxy-2-(methylamino)-a-L-glucopyranosyl]-3-C
-formyl-a-L-lyxofuranosyl]-D-streptamine] trisulphate.26
- Pemerian : Serbuk berwarna putih atau keputihan.26
- Kelarutan : Sangat mudah larut dalam air, praktis tidak larut etanol.26
- pH sediaan : pH larutan berkisar 4,5-7,0.26
- Farmakologi :
Antibiotik ini merupakan antibiotik yang termasuk ke dalam golongan
aminoglikosida. Antibiotik golongan ini secara umum digunakan untuk melawan
bakteri enterik gram negatif, termasuk tuberkulosis. Streptomisin aktif terutama
melawan basil tuberkulosis ektraseluler. Aminoglikosida bertindak sebagai
inhibitor irreversibel terhadap sintesis protein. Streptomisin masuk ke dalam sel
melalui difusi pasif lewat pori-pori dari membran terluar. Obat kemudian
diteruskan melalui membran ke dalam sitoplasma melalui proses oxygen-dependent. Tranport ke dalam sel dapat ditingkatkan dengan penambahan senyawa yang aktif terhadap dinding sel bakteri misalnya penisilin atau
vankomisin.
Di dalam sel, streptomisin mengikat secara spesifik protein ribosom
subunit-30S. Proses inhibisi sintesis protein dapat dilakukan dengan tiga cara:
1. Berinteraksi dengan kompleks inisiasi bentuk peptida.
2. Kesalahan pembacaan mRNA yang menyebabkan kesalahan
pembentukan asam amino, berakibat pada ketidakberfungsian protein
atau protein yang toksik.
3. Pemutusan polysome menjadi monosome yang tidak berfungsi, efek ini
secara umum bersifat irreversibel dan menyebabkan kematian sel.27
- Efek samping :
Streptomisin bersifat ototoksik dan nefrotoksik. Vertigo dan gangguan
pendengaran adalah efek samping yang sering terjadi dan dapat bersifat
permanen. Efek samping meningkat terutama untuk pasien lanjut usia.27
- Dosis :
Dosis streptomisin untuk penyakit tuberkulosis adalah 15 mg/kgBB/hari
secara intramuskular. Dosis untuk pemberian intra vena pada orang dewasa
(20-40 mg/kgBB/hari) dan tidak melebihi 1-1,5 gram untuk anak-anak, diberikan
seminggu selama beberapa bulan. Dosis streptomisin harus disesuaikan dengan
fungsi ginjal. Sebisa mungkin terapi streptomisin tidak lebih dari 6 bulan.
Secara in vitro, kebanyakan basil tuberkulosis akan dihambat dengan
streptomisin pada dosis 1-10 ppm. Rata-rata, satu dari 108 basil tuberkulosis dapat
menjadi resisten terhadap streptomisin pada dosis 10-100 ppm.27
2.7.3. Pirazinamid
- Rumus struktur :
- Rumus molekul : C5H5N3O.26
- Nama kimia : pyrazine-2-carboxamide.26 - Berat molekul : 123,1.26
- Pemerian : Serbuk hablur, putih hingga praktis putih, tidak berbau atau praktis tidak berbau.26
- Kelarutan : Agak sukar larut dalam air, sukar larut dalam alkohol dan metil klorida.26
- pH sediaan : Pirazinamid tidak aktif pada pH netral, tetapi pada pH 5,5 dapat menghambat basil tuberkulosis dan beberapa mikobakterium
lainnya.26
- Farmakologi :
Pirazinamid (PZA) merupakan golongan nikotinamid, stabil dan sukar
larut di dalam air. Pirazinamid tidak aktif pada pH netral, tetapi pada pH 5,5
dapat menghambat basil tuberkulosis dan beberapa mikobakterium lainnya
pada konsentrasi sekitar 20 ppm. Obat akan ditangkap oleh makrofag dan
menimbulkan aktivitasnya melawan mikobakteria yang berada pada
lingkungan asam pada lisosom. Pirazinamid diubah menjadi asam pirazinoik,
yaitu suatu bentuk aktif obat yang diaktifkan oleh pirazinamidase
mikobakterium dan dikoding oleh pncA.
Pirazinamid diserap dengan baik dalam saluran gastrointestinal dan
secara luas didistribusikan ke jaringan tubuh, termasuk sumsum tulang yang
mengalami peradangan. Waktu paruh pirazinamid adalah 8-11 jam.
melalui ginjal. Pirazinamid adalah obat anti tuberkulosis lini pertama yang
dikonjugasikan bersama isoniasid dan rifampisin dalam pengobatan jangka
pendek (umumnya 6 bulan) sebagai regimen sterilizing agent melawan organisme intraseluler yang dapat menyebabkan kekambuhan. Basil
tuberkulosis dapat menjadi resisten terhadap pirazinamid, tetapi tidak
ditemukan resistensi silang terhadap isoniasid atau obat antituberkulosis
lainya.27
- Efek samping :
Efek yang umum terjadi pada penggunaan pirazinamid adalah mual,
muntah, deman karena obat, hiperurisemia dan hepatotoksisitas (1-5% pasien).
Efek samping lain yang muncul pada dasarnya bukan menjadi alasan untuk
menghentikan pengobatan. Hiperurisemia dapat memicu arthritis gout akut.27
- Dosis :
Konsentrasi serum sebanyak 30-50 ppm selama 1-2 jam setelah
pemberian oral diperoleh pada dosis 25 mg/kgBB/hari. Pirazinamid harus
diberikan 25-35 mg/kgBB tiga kali seminggu (bukan harian) pada pasien
dengan hemodialisa dan bagi orang-orang yang memiliki kreatinin klirens
kurang dari 30 ml/menit. Pada pasien dengan fungsi ginjal normal, dosis
pirazinamid yang digunakan adalah 40-50 mg/kgBB tiga kali setiap
minggunya.27 Dosis pirazinamid yang digunakan untuk pengujian resistensi
tuberkulosis secara in vitro berkisar pada 6,25-50 ppm.7
2.7.4. Isoniasid
- Rumus struktur :
- Rumus molekul : C3H7N3O.26
- Nama kimia : Pyridine-4-carbohydrazide.26 - Berat molekul : 137,1.26
- Pemerian : Serbuk kristal atau kristal tak berwarna, putih atau hampir putih.26
- Farmakologi :
Isoniasid (INH) adalah obat yang paling aktif digunakan dalam
pengobatan tuberkulosis yang disebabkan strain tuberkulosis yang rentan.
Secara in vitro, isoniasid menghambat pertumbuhan basil pada konsentrasi 0,2
ppm atau lebih rendah dari itu. Isoniasid aktif melawan basil tuberkulosis yang
sedang tumbuh. Isoniasid kurang efektif melawan spesies mikobakterium
atipikal. Isoniasid mempenetrasi ke dalam makrofag dan aktif melawan baik
organisme intraseluler dan ekstraseluler.
Isoniasid menghambat sintesis asam mikolat, di mana merupakan
komponen esensial dari dinding sel mikobakterium. Isoniasid adalah prodrug
yang diaktifkan oleh KatG, yaitu suatu mikobakterial katalase-peroksidase.
Bentuk aktif dari isoniasid merupakan kompleks kovalen dengan suatu asil
pembawa protein (AcpM) dan KasA, suatu beta-ketoasil pembawa protein
sintetase, yang memblok sintesis asam mikolat dan membunuh sel.
Isoniasid dapat secara langsung diabsorpsi ke dalam saluran
gastrointestinal. Isoniasid berdifusi dengan bebas ke seluruh cairan tubuh dan
jaringan. Konsentrasi di dalam sistem saraf pusat dan cairan serebrospinal
berkisar antara 20% dan 100% pada konsentrasi serum secara simultan.
Metabolisme isoniasid terjadi terutama pada proses asetilasi di dalam hati
oleh N-asetiltransferase. Konsentrasi plasma rata-rata dari isoniasid pada asetilator cepat yaitu sekitar 1/3 sampai 1/2 pada asetilator lambat. Waktu
paruh rata-rata isoniasid kurang dari satu jam dan tiga jam, berturut-turut.
Klirens yang lebih cepat terhadap isoniasid yang disebabkan oleh asetilator
cepat umumnya tidak memiliki konsekuensi terapetik ketika dosis yang sesuai
telah diberikan setiap harinya, tetapi konsentrasi subterapi dapat muncul bila
obat diberikan sekali seminggu atau jika terjadi malabsorbsi.
Metabolit isoniasid dan sebagian kecil dari obat yang tidak berubah
dieksresikan terutama melalui urin. Dosis isoniasid tidak perlu disesuaikan
untuk pasien dengan gagal ginjal. Pengaturan dosis untuk pasien dengan
gangguan hati belum dapat ditentukan dengan pasti (isoniasid
- Efek samping :
Demam dan ruam kulit adalah hal yang sering terjadi. Efek merugikan yang dapat diakibatkan oleh penggunaan isoniasid adalah lupus eritema,
hepatotoksisitas, dan gangguan saraf. Efek lain yang dapat terjadi antara lain
hilangnya nafsu makan, mual, muntah, penyakit kuning dan bahkan kematian
apabila obat tidak digunakan dengan benar.27
- Dosis :
300 mg dosis oral (5 mg/kgBB pada anak-anak) akan mencapai
konsentrasi plasma puncak pada 3-5 ppm dalam 1-2 jam. Dosis isoniasid yang
umum digunakan adalah 5 mg/kgBB/hari; dosis dewasa biasanya diberikan
sebanyak 300 mg setiap hari. Sampai 10 mg/kgBB/hari dapat diberikan pada
infeksi yang serius atau jika terjadi masalah malabsorbsi. Dosis 15 mg/kgBB
atau 900 mg dapat digunakan dua kali seminggu dengan kombinasi
antituberkulosis lainnya (misalnya rifampisin 600 mg). Piridoksin, 25-50
mg/hari direkomendasikan pada orang-orang yang cenderung mengalami
neuropathy, yaitu efek yang tidak diinginkan dari penggunaan isoniasid.
Isoniasid biasanya diberikan secara oral tapi dapat juga diberikan secara
parenteral dengan dosis yang sama. Isoniasid sebagai pengobatan tunggal juga
diindikasikan pada tuberkulosis laten. Dosis yang digunakan adalah 300
mg/hari (5 mg/kgBB/hari) atau 900 mg dua kali per minggu selama 9 bulan.27
Dosis isoniasid yang digunakan untuk pengujian resistensi tubekulosis secara
in vitro berkisar pada 0,02-0,2 ppm.7
2.7.5. Etambutol
- Rumus struktur :
- Rumus molekul : C10H26Cl2N2O2.26
- Nama kimia : (2S,2’S) - 2,2’- (ethylenediimino)dibutan -1- ol dihydrochloride.26
- Berat molekul : 277,2.26