KARAKTERISTIK REPRODUKSI
BANDIKUT (Echymipera kalubu) JANTAN
ANGELINA NOVITA TETHOOL
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
Dengan ini Saya menyatakan bahwa tesis Karakteristik Reproduksi Bandikut (Echymipera kalubu) Jantan adalah karya saya sendiri dan belum diajukan dalam bentuk apapun kepada perguruan tinggi manapun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam daftar pustaka di bagian akhir tesis ini.
Bogor, Oktober 2011
ABSTRACT
ANGELINA NOVITA TETHOOL. Characteristic reproduction of males Bandicoot (Echymipera kalubu). Under direction of RADEN IIS ARIFIANTINI and SRIHADI AGUNGPRIYONO
Bandicoot (Echymipera kalubu) is one of endemic species in Papua, which has various benefits for the people in Papua. The purpose of this research was to study male reproductive organs characteristics, the quality of cauda epididymal spermatozoa and spermatogenesis processes. This study used 21 males E. kalubu of three different stages of age. Sperm morphology was assessed by using Carbofuchsin (William’sstain) and the stages of spermatogenesis was analized by using Periodic Acid Schiff (PAS) stain. The results showed that reproductive organs comprised of gonad (testis), accessory glands and penis. Testis were elipsoid in shape, the accessory glands consisted of prostat gland and Cowper gland, and the penis was bhipid. Epididymal sperm concentration and motility increased with sperm maturity. The length of sperm head, midpiece andprincipal piece were 2.91±0.40μm, 13.99±0.87 μm and 145.59±5.38 μm, respectively and the total length of spermatozoa was 162.51±5.12 μm. Finally,E. kalubu had nine stages of spermatogenesis with ten step development of spermatids into spermatozoa.
ANGELINA NOVITA TETHOOL. Karakteristik Reproduksi Bandikut (Echymipera kalubu) Jantan. Dibimbing oleh RADEN IIS ARIFIANTINI dan SRIHADI AGUNGPRIYONO
Bandikut (Echymipera kalubu) merupakan salah satu satwa endemik Papua yang saat ini statusnya masih sebagai hewan liar dan populasinya masih berlimpah pada habitat yang sesuai. Echymipera kalubu memiliki beberapa keunggulan, antara lain: memiliki laju reproduksi yang paling tinggi diantara semua marsupialia dengan jumlah anak perkelahiran 2-4 ekor, merupakan hewan marsupialia (berkantung) yang dagingnya dimanfaatkan sebagai sumber protein hewani serta memiliki nilai etno-zoologis (rambut, tulang dan anak bandikut umur 12 hari dipercaya berkhasiat untuk pengobatan) bagi masyarakat di Papua dan mempunyai struktur organ reproduksi yang unik, dimana saluran akhir alat reproduksi, saluran kencing dan pembuangan feces bermuara dalam satu saluran anus mirip kloaka pada unggas. Informasi mengenai status biologi reproduksiE. kalubu yang hidup liar di alam hingga saat ini belum banyak dilaporkan. Hal ini menyebabkan perlu dilakukan penelitian mengenai karakteristik dari organ reproduksi jantan, yang terdiri dari: morfologi organ kelamin, kualitas spermatozoa yang berasal dari epididimis serta gambaran spermatogenesis padaE. kalubu sebagai data dasar yang akan mendukung perkembangbiakan di penangkaran.
Bandikut (E. kalubu) jantan yang digunakan sebanyak 21 ekor berasal dari kabupaten Manokwari. Penelitian terbagi menjadi tiga tahap, yaitu pengamatan karakteristik organ reproduksi, karakteristik spermatozoa asal epidimis (motilitas, konsentrasi dan morfologi spermatozoa) dan tahapan spermatogenesis. Data-data yang diperoleh kemudian dianalisis secara deskriptif dan variabel yang diukur adalah rata-rata yang didapat dari setiap variabel dengan menggunakan standar deviasi.
Hasil yang diperoleh menunjukkan bahwa testis E. kalubu berada di luar abdomen dan terbungkus oleh skrotum yang tidak berpigmen dengan organ reproduksi terdiri atas testis, epididimis, vas deferens dan dua buah kelenjar asesoris (kelenjar prostat dan cowper) serta memiliki ciri khas pada glans penis yang berbentuk bhipid (bercabang) dan tidak memiliki kelenjar vesikularis. Motilitas dan konsentrasi spermatozoa asal kauda epididimis meningkat sejalan dengan peningkatan kedewasaan. SpermatozoaE. kalubu memiliki bentuk kepala yang kecil dan batas antara kepala dengan ekor tidak sejelas pada spermatozoa ternak pada umumnya. Panjang kepala spermatozoa 2,91±0,40 μm, midpiece 13,99±0,87 μm dan principal pieceadalah 145,59±5,38 μm dengan panjang total adalah 162,51±5,12 μm. Bandikut (E. kalubu) memiliki sembilan tahapan spermatogenesis dengan sepuluh langkah transformasi (perkembangan) spermatid menjadi spermatozoa.
© Hak Cipta milik Institut Pertanian Bogor Tahun 2011
Hak Cipta dilindungi Undang-Undang
1. Dilarang mengutip sebagian atau seluruh karya tulis ini tanpa atau mencantumkan atau menyebutkan sumber.
a. Pengutipan hanya untuk kepentingan pendidikan, penelitian, penulisan karya ilmiah, penyusunan laporan, penulisan kritik, atau tinjauan suatu masalah.
b. Pengutipan tersebut tidak merugikan kepentingan yang wajar IPB.
ANGELINA NOVITA TETHOOL
Tesis
sebagai salah satu syarat untuk memperoleh gelar Magister Sains pada
Program Studi Biologi Reproduksi
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
NRP : B352090011
Disetujui
Komisi Pembimbing
Dr. Dra. R. Iis Arifiantini, M.Si drh. Srihadi Agungpriyono, Ph.D, PAVet (K)
Ketua Anggota
Diketahui
Ketua Program Studi Dekan Sekolah Pascasarjana IPB
Biologi Reproduksi
Dr. drh. M. Agus Setiadi Dr. Ir. Dahrul Syah, M.Sc.Agr
PRAKATA
Puji syukur kehadirat Tuhan Yang Maha Kuasa atas limpahan kasih,
berkat dan anugerahNya sehingga penulis dapat menyelesaikan penulisan tesis
yang berjudul Karakteristik Reproduksi Bandikut (Echymipera kalubu) Jantan.
Penulis menyampaikan terima kasih dan penghargaan kepada
Dr. Dra. R. Iis Arifiantini, M.Si dan drh. Srihadi Agungpriyono Ph.D, PAVet (K)
selaku pembimbing, yang telah banyak memberikan arahan dan koreksi selama
proses penyelesaian karya ilmiah ini. Ucapan terimakasih juga penulis sampaikan
kepada Prof. Dr. drh. Tuty L. Yusuf, M.Si sebagai penguji luar komisi pada saat
ujian tesis, Bapak Dr. drh. M. Agus Setiadi sebagai ketua Program studi serta
seluruh staf pengajar Program studi Biologi Reproduksi atas segala ilmu yang
diberikan selama ini, kepada Rektor, Dekan Fakultas Peternakan Perikanan dan
Ilmu Kelautan Universitas Negeri Papua yang telah memberikan kesempatan
tugas belajar, kepada Departemen Pendidikan Nasional (DITJEN DIKTI) atas
bantuan beasiswa sehingga penulis dapat menyelesaikan studi pada program
Pascasarjana di IPB. Ucapan terima kasih penulis sampaikan pula kepada Ibu
Dr. drh. Savitri Novelina, drh. Sri Wahyuni, M.Si, mas Rudi, teman-teman KRP
2009 (Arie, mas Fitra, mas Ibnu, P’Ullum, P’Mazda, P’Riky, P’Herry, Bu Sri dan
Bu Nur), rekan-rekan Lab. Fisiologi dan Reproduksi FPPK UNIPA (P’Jen,
P’Priyo, P’Irba dan K’Uni) serta rekan-rekan yang tidak dapat penulis sebutkan
satu persatu atas bantuan dan saran-sarannya. Kepada Papa, Mama, Kakak-kakak,
Adik-adik di Manokwari, Ibu mertua, kakak dan adik di Manado terima kasih atas
dukungan moril dan doa selama ini. Ucapan terima kasih juga Penulis sampaikan
kepada suami tercinta Luky Sembel dan anak tersayang Nicky Fidelis Adrie
Sembel atas semangat, perhatian, pengertian dan kasih sayangnya selama ini.
Penulis menyadari bahwa karya ilmiah ini masih jauh dari sempurna, oleh
karena itu kritik dan saran sangat diharapkan. Akhirnya penulis berharap semoga
Tesis ini dapat digunakan bagi perkembangan ilmu pengetahuan.
Bogor, Oktober 2011
1980 dari ayah Johannes Tethool dan ibu Susana Jamlaay. Penulis merupakan
anak ketiga dari lima bersaudara.
Pendidikan sarjana ditempuh di Program Studi Produksi Ternak Fakultas
Peternakan Perikanan dan Ilmu Kelautan Universitas Negeri Papua dan lulus
tahun 2004. Penulis bekerja sebagai tenaga pengajar di Universitas Negeri Papua
sejak tahun 2005 sampai sekarang. Penulis melanjutkan ke Program Magister
Sains pada Program Studi Biologi Reproduksi Fakultas Kedokteran Hewan
Institut Pertanian Bogor tahun 2009 dengan Beasiswa BPPS Departemen
DAFTAR ISI
Sistematika dan Penyebaran Bandikut ... 5Anatomi dan Morfologi Organ Reproduksi Jantan ... 7
Morfologi Spermatozoa ... 9
Spermatogenesis dan Tahapan Tubuli Seminiferi ... 12
Parameter Kualitas Spermatozoa ... 15
BAHAN DAN METODE Tempat dan Waktu ... 19
Metode Penelitian ... 19
Karakteristik Organ Reproduksi ... 19
Karakteristik Spermatozoa Asal Epididimis ... 20
Tahapan Spermatogenesis ... 22
Analisis Data ... 22
HASIL DAN PEMBAHASAN Organ ReproduksiEchymipera kalubuJantan ... 23
Testis ... 24
Epididimis ... 25
Vas deferens... 25
Kelenjar Asesoris... 25
Organ Kopulatoris ... 28
Karakteristik Spermatozoa Asal Epididimis ... 29
Motilitas Spermatozoa ... 30
Konsentrasi Spermatozoa ... 31
Morfologi dan Morfometri Spermatozoa ... 32
Halaman
1. Dimensi Prostat pada Beberapa Spesies Marsupial ... 26
2. Morfometri Organ ReproduksiEchymipera kalubuJantan ... 29
3. Motilitas (%) dan Konsentrasi (x106/mL) SpermatozoaEchymipera kalubuyang Dikoleksi dari Kauda Epididimis ... 32
4. Tingkat Abnormalitas SpermatozoaE. kalubu(%) ... 35
DAFTAR GAMBAR
Halaman
1. Echymipera kalubuJantan ... 5
2. Saluran Reproduksi Tammar wallaby (Macropus eugenii) Jantan ... 7
3. Penampakan Ventral Saluran Reproduksi Bandikut (Isoodon Macrourus) Jantan ... 9
4. Struktur Spermatozoa pada Mamalia ... 9
5. Tahapan Fase Spermiogenesis ... 11
6. Proses Spermatogenesis pada Mamalia ... 13
7. Perkembangan Sel-Sel Germinal pada Tahapan Spermatogenesis Tikus ... 15
8. Testis dan PenisEchymipera kalubu ... 23
9. Organ ReproduksiE. kalubuJantan ... 24
10. Kelenjar Prostat ... 27
11. Kelenjar Cowper ... 28
12. Grafik Motilitas SpermatozoaE. kalubuyang Dikoleksi dari Kauda Epididimis (%) ... 30
13. Grafik Konsentrasi Spermatozoa E. kalubu yang Dikoleksi dari Kauda Epididimis (x106/mL) ... 31
14. Spermatozoa NormalE. kalubu ... 32
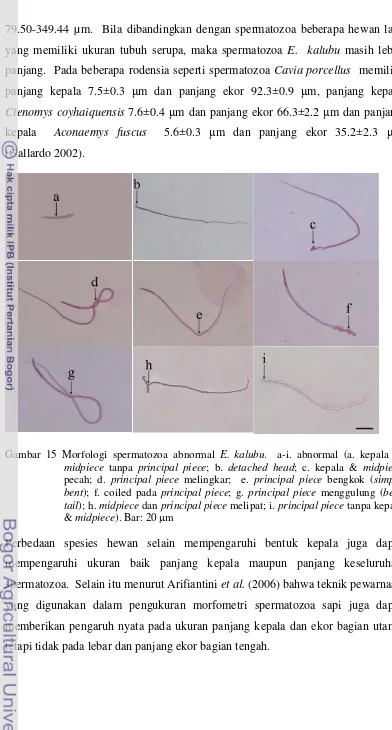
15 Morfologi Spermatozoa AbnormalE. kalubu ... 33
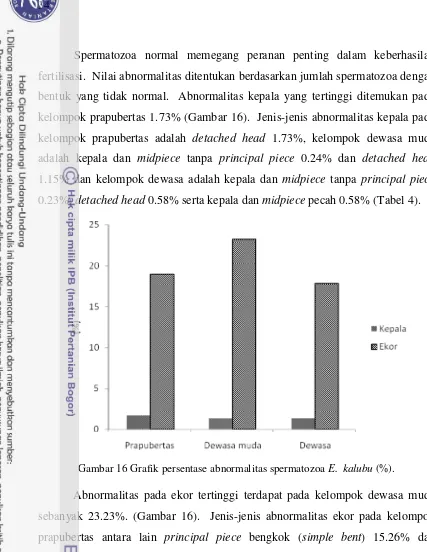
16. Grafik Persentase Abnormalitas Spermatozoa E. kalubu ... 34
17. Tahapan Siklus Tubuli Seminiferi pada SpermatogenesisE. kalubu (I-IX) ... 37
18. Sembilan Tahapan Morfologi Siklus Tubuli SeminiferiE. kalubu ... 38
Bandikut (Echymipera kalubu) merupakan salah satu satwa endemik
Papua yang saat ini statusnya masih sebagai hewan liar dan populasinya masih
berlimpah pada habitat yang sesuai (Learyet al.2008). Satwa ini tergolong Ordo
Peramelemorphia dengan Famili Peramelidae dan Peroryctidae. Famili
Peramelidae banyak terdapat di Australia, sedangkan Famili Peroryctidae
terutama genusEchymiperabanyak ditemukan pada daerahNew Guineatermasuk
Papua (Gordon & Hulberth 1989). Hewan ini merupakan hewan berkantung
(Marsupialia) yang memiliki sifat nokturnal, soliter dan omnivora
(Menzies 1991).
Bandikut memiliki laju reproduksi yang paling tinggi diantara semua
marsupialia dengan jumlah anak perkelahiran 2-4 ekor dan frekuensi beranak
sebanyak 5-6 kali dalam setahun (Petocz 1994). Bandikut adalah hewan
marsupialia (berkantung) yang dimanfaatkan sebagai sumber protein hewani dan
memiliki nilai etno-zoologis (rambut, tulang dan anak Bandikut umur 12 hari
dipercaya berkhasiat untuk pengobatan) bagi masyarakat Papua (Warsono 2009).
Penggunaan Bandikut sebagai model dalam penelitian hewan marsupial perlu
mendapat perhatian mengingat hewan ini memiliki ukuran tubuh yang kecil
sehingga memudahkan dalam penanganan, ekonomis dalam menggunakan bahan
coba, lebih efisien dalam pemakaian ruang dan mudah untuk melakukan
percobaan ulang karena statusnya yang masih melimpah pada habitat aslinya.
Satwa ini memiliki struktur organ reproduksi yang unik, dimana saluran akhir alat
reproduksi, saluran kencing dan saluran pembuangan kotoran bermuara dalam
satu saluran anus mirip kloaka pada unggas (Warsono 2009).
Pemanfaatan satwa liar secara umum yang berasal dari alam, nantinya
dapat menyebabkan menurunnya jumlah populasi sehingga perlu adanya suatu
upaya penanganan yang mengarah pada kegiatan konservasi. Konservasi
merupakan upaya yang umumnya bertujuan untuk melestarikan dan melindungi
keanekaragaman genetika, species atau jenis dan untuk memanfaatkannya bagi
kepentingan manusia. Konservasi secara in situdanex situ merupakan kegiatan
2
biologi reproduksi dari satwa liar sangat penting untuk pelaksanaan kegiatan
konservasi ex situ. Salah satu aspek dalam biologi reproduksi satwa liar adalah
pengetahuan tentang anatomi dan fisiologi dari organ reproduksi baik jantan
maupun betina, yang dapat digunakan untuk proses pembudidayaan,
perkembangbiakkan, serta bahan penentu kebijakan dalam pengelolaan kehidupan
satwa di penangkaran.
Proses pembudidayaan Bandikut (E. kalubu) sebagai salah satu satwa
harapan untuk dijadikan sumber protein hewani (ternak pedaging) diperlukan
beberapa tahapan pengkajian. Komponen yang perlu diteliti meliputi jenis pakan,
tingkah laku, habitat yang disenangi, upaya untuk mengubah pakan alami, daya
adaptasi selama proses budidaya serta faktor reproduksi yang merupakan faktor
penentu dalam keberhasilan budidaya (Warsono 2009). Faktor-faktor ini
merupakan dasar yang dapat dijadikan sebagai acuan dalam mengoptimalkan
produktivitas serta usaha domestikasi Bandikut (E. kalubu).
Keberhasilan budidaya sangat dipengaruhi oleh aspek fisiologi organ
reproduksi. Organ reproduksi hewan jantan berkaitan dengan tingkat fertilitas
yang dapat diketahui dengan melihat kondisi semen dan spermatozoa. Informasi
mengenai kualitas spermatozoa juga dapat digunakan sebagai dasar dalam upaya
preservasi maupun kriopreservasi. Spermatozoa dapat dikoleksi dari epididimis
ternak atau hewan dan dapat dimanfaatkan dalam prosedur teknologi reproduksi.
Menurut Hafez dan Hafez (2000) pada fertilisasiin vitro (IVF) spermatozoa yang
berasal dari kauda epididimis telah memiliki motilitas dan kemampuan membuahi
oosit yang sama baiknya dengan spermatozoa hasil ejakulasi. Beberapa upaya
telah dilakukan untuk memanfaatkan spermatozoa epididimis satwa liar
diantaranya pada Petaurus breviceps papuanus T. (Suarni & Ermayanti 2009),
Iberian red deer (Cervus elaphus hispanicus) (Santoz et al. 2006), Elan
(Taurotragus oryx) (Bisset & Bernard 2010),Kucing (Cocchiaet al. 2009).
Informasi tentang reproduksi hewan jantan secara khusus mengenai
dinamika spermatogenesis merupakan hal mendasar yang dapat digunakan untuk
mencegah spesies dari kepunahan serta meningkatkan program pemuliaan pada
spesies tertentu secara alami maupun buatan (Comizzoli et al. 2000).
dengan proliferasi secara mitosis spermatogonium dan kemudian spermiogenesis
dimana spermatid haploid akan berkembang menjadi spermatozoa (Almeidaet al.
2006). Aktivitas spermatogenesis dapat diamati secara morfologi melalui sediaan
histologi, melalui pendeteksian imunohistokimia (keberadaan hormon steroid di
jaringan testis) dan histokimia (keberadaan ikatan lektin). Tehnik-tehnik ini dapat
digunakan untuk mengetahui dan menduga proses-proses spermatogenesis yang
terjadi di dalam tubuli seminiferi.
Berbagai penelitian terkait reproduksi Bandikut di Australia telah banyak
dilakukan diantaranya meliputi reproduksi Northen Brown Bandicoot (Isoodon
macrourus) (Vernes & Pope 2009), ritme aktivitas dari Southern Brown
Bandicoot (Isoodon obelus) di penangkaran (Larcombe 2003), fisiologi
reproduksi Bilby betina (Macrotis lagotisThylacomidae) (Ballantyneet al. 2009),
pengaruh perubahan musim pada saluran reproduksi Bandikut jantan (Isoodon
macrourus) (Thodunter & Gemmel 1987) dan kebiasaan Bandikut menggali
sebagai suatu upaya adaptasi lingkungan (Long 2009). Saat ini penelitian
mengenai Bandikut yang tersebar di daerah Papua belum banyak dilaporkan,
beberapa penelitian yang telah dilakukan meliputi sifat biologis dan karkas daging
Bandikut (Warsono 2009) serta tingkah laku harian Bandikut di penangkaran
(Manufandu 2000). Sehubungan dengan hal tersebut, perlu dilakukan suatu
penelitian untuk memperoleh informasi mengenai karakteristik reproduksi
Bandikut (E. kalubu) jantan sebagai upaya untuk mendapatkan informasi tentang
status biologi reproduksi yang dimiliki pada spesies ini.
Tujuan
Penelitian ini dilaksanakan dengan tujuan:
1. Mempelajari karakteristik organ reproduksi Bandikut (E. kalubu) jantan.
2. Mempelajari kualitas spermatozoa Bandikut (E. kalubu) asal kauda
epididimis.
4
Manfaat
Hasil penelitian ini berguna sebagai data dasar dan informasi yang penting
dalam upaya perkembangbiakkan dan preservasi sumber genetik Bandikut
(E. kalubu) untuk menunjang upaya konservasi yang akan dilakukan pada spesies
Sistematika zoologis Bandikut adalah sebagai berikut (Petocz 1994)
(Gambar 1):
Kingdom : Animalia
Phylum : Chordata
Subphylum : Vertebrata
Class : Mammalia
Infraclass : Methatheria
Superordo : Marsupialia
Ordo : Peramelemorphia
Famili : Peroryctidae
Genus : Echymipera
Species : Echymipera kalubu
Gambar 1 Echymipera kalubujantan
Bandikut memiliki ordo yang dibedakan dalam dua famili, yaitu
Peramelidae(bandicoots and bilbies) memiliki empat genus, sepuluh spesies, dan
Peroryctidae(Peroryctid bandicoots) mempunyai empat genus dan sebelas spesies
6
sedangkan famili Peroryctidae terutama genus Echymipera banyak ditemukan di
kepulauan Maluku dan New Guinea (Menzies 1991). Daratan New Guinea
memiliki tiga genus (Peroryctes, Microperoryctes dan Rhynchomeles) dengan
sebelas spesies merupakan endemik dan genusEchymiperayang merupakan pusat
genus di New Guinea dengan empat spesies dan satu spesies diantaranya meluas
sampai di bagian utara Australia. Genus lain (Isodoon) merupakan pusat genus di
Australia dengan satu spesies juga penyebarannya meluas sampai keNew Guinea
bagian selatan (Graeme & Maynes 1990).
Bandikut merupakan hewan nokturnal, soliter dan omnivora. Jumlah
spesies Bandikut di dunia adalah sebanyak 21 spesies, sebagian besar hanya
ditemukan diNew Guineadan sedikit di pesisir utara dan timur Australia. Secara
umum daerah penyebaran Bandikut dari ketinggian 0-4300 meter dari permukaan
laut pada habitat padang rumput alam, alang-alang, hutan terbuka, hutan hujan
dataran rendah, hutan lebat, hutan lumut dan areal pepohonan (Menzies 1991).
Echymipera kalubu dikenal juga sebagai bandikut kepala hitam. Bagian
kepala berwarna kehitaman dan memiliki warna yang lebih terang pada bagian
tenggorokan dan pipi. Bandikut jenis ini mempunyai ciri rambut yang tajam,
bagian punggung kehitaman dengan sejumlah variasi kuning kecoklatan sampai
leher. Warna rambut coklat muda pada bagian ventral dan coklat gelap kehitaman
dengan ujung lebih pucat. Moncong agak panjang, telinga ekor dan kaki pendek
serta memiliki empat pasang gigi seri (Graeme & Maynes 1990). Telapak kaki
belakang berwarna hitam dan tidak terlalu berkembang dengan sempurna
dibandingEchymipera pada umumnya. Bobot badan jantan lebih besar daripada
betina dengan kisaran 1483.75 g untuk jantan dan 850.71 g untuk betina (Warsono
2009). Spesies ini merupakan bentuk fauna peralihan antara Australia Utara dan
New Guinea. Populasinya tersebar luas di dataran rendah pada habitat hutan
tertutup, hutan terbuka, padang rumput dan semak belukar yang lebih kering di
pulau Waigeo, Biak dan Yapen serta bagian utara, timur, Manokwari, Merauke
dan selatan New Guineadengan ketinggian 1550 m dari permukaan laut (Gordon
Anatomi dan Morfologi Organ Reproduksi Jantan
Sistem reproduksi hewan jantan secara umum terdiri atas sepasang testis,
vas deferens, epididimis, kelenjar asesoris dan penis. Marsupial jantan memiliki
saluran reproduksi yang terdiri atas testis, epididimis, vas deferens, kelenjar
prostat, kelenjar Cowper, penis dan glans penis yang berbentuk bhipid atau
tunggal (Renfree 1993). Bagian-bagian organ reproduksi marsupial jantan dapat
dilihat pada Gambar 2.
Gambar 2 Saluran reproduksi Tammar Wallaby jantan (Macropus eugenii) (Sumber: Renfree 1993).
Testis merupakan organ reproduksi primer tempat dihasilkannya spermatozoa
yang akan membuahi oosit pada hewan betina sewaktu terjadi perkawinan dan
fertilisasi. Testis mengandung lobuli testis yang membentuk saluran-saluran kecil
yang disebut tubuli seminiferi tempat berlangsungnya proses spermatogenesis.
Pada bagian mediastinum testis, tubuli bergabung membentuk rete testis
kemudian melalui duktus eferens dihubungkan dengan bagian kepala epididimis
(kaput epididimis).
Epididimis merupakan suatu struktur memanjang yang bertaut rapat
dengan testis. Epididimis terbagi menjadi tiga bagian, yaitu kaput epididimis
8
yang berfungsi dalam penyerapan cairan, korpus epididimis (badan) berada pada
bagian tengah yang berfungsi dalam pematangan spermatozoa dan kauda
epididimis (ekor) berada pada ujung distal dari testis yang berfungsi sebagai
tempat penyimpanan spermatozoa (Biscoe & Renfree 1987). Kauda epididimis
merupakan tempat penyimpanan spermatozoa dan mengandung sekitar 75% total
spermatozoa epididimis (Hafez 2000).
Kelenjar prostat merupakan kelenjar yang tidak berpasangan dan
mengelilingi pelvis uretra. Kelenjar ini menghasilkan sekresi alkalin yang
memberikan bau khas pada cairan semen serta berfungsi mensekresikan cairan
untuk membersihkan dan menetralisir uretra dari bekas urine dan kotoran-kotoran
lain sebelum ejakulasi. Kelenjar Cowper merupakan sepasang kelenjar kecil yang
terletak pada tiap sisi pelvis uretra.
Penis merupakan organ kopulatoris dan berfungsi sebagai tempat
pengeluaran urine dan deposisi semen ke dalam saluran reproduksi betina. Penis
mamalia memiliki tiga bagian cekungan yang terdapat pada sekitar penile uretra
(Hafez 2000). Skrotum merupakan suatu kantong yang berfungsi untuk
melindungi testis dan epididimis serta mempertahankan suhu yang lebih rendah
daripada suhu badan yang diperlukan untuk proses spermatogenesis.
Pada Eastern barred bandicoot testes berada di luar dan dibungkus
dengan skrotum. Perkembangan terjadi pada kelenjar-kelenjar asesoris, seperti
kelenjar prostat yang berada subkutan dan terletak pada anterior kloaka
(Gambar 3). Penis pada hewan ini berbentuk S dan berakhir pada glans penis
yang berbentuk bhipid. Glans penis yang berbentuk bhipid kemungkinan
berhubungan dengan bentuk vagina marsupial yang terdiri atas dua bagian, yaitu
dua lateral vagina dan median vagina (Biscoe & Renfree 1987). Selanjutnya
kantung kencing yang dimiliki hewan ini terletak pada bagian dorsal prostat
(Seebeck 2001). Echymipera kalubu jantan ditandai dengan adanya dua buah
testes yang terbungkus dalam skrotum menggantung keluar abdomen sekitar tiga
cm dari anus. Saluran akhir alat reproduksi, saluran kencing dan saluran
pembuangan kotoran bermuara dalam satu saluran anus mirip kloaka pada unggas
A B
Gambar 3 Penampakan ventral saluran reproduksi Bandikut (Isoodon macrourus) jantan (A) selama musim tidak kawin (B) selama musim kawin. B: Bladder, P: Prostat, V: Vas deferens, M: Membranous urethra, T: Testis, E: Epididimis (Sumber: Thodunter & Gemmel 1987).
Morfologi Spermatozoa
Spermatozoa memiliki dua bagian utama yaitu kepala yang mengandung
inti (nukleus) dan ekor (flagellum) (Gambar 4). Bagian ekor terdiri atas leher
(neck piece), badan (middle piece), ekor utama (principal piece) dan ujung ekor
(end piece).
Gambar 4 Struktur spermatozoa pada mamalia. a. Spermatozoa tikus. b. Spermatozoa manusia. H: Kepala, Ne: Leher, MP-EP: Ekor (MP: Middle piece, PP:
Principal piece, EP:End piece) (Sumber: Toshimori 2009).
Struktur kepala
Kepala spermatozoa berfungsi sebagai pembawa dan menjaga DNA
hingga terjadinya fertilisasi. Bagian kepala spermatozoa terdiri atas daerah
10
akrosom. Pembentukan akrosom terjadi pada tahap spermiogenesis dari proses
spermatogenesis. Fase spermiogenesis terdiri atas fase golgi, fase cap (tudung),
fase akrosomal dan fase pematangan atau maturasi (Senger 2005) (Gambar 5).
Akrosom adalah derivat dari apparatus golgi yang terbentuk sepanjang
tahap awal spermatogenesis. Akrosom spermatozoa berfungsi dalam menginisiasi
reaksi fisikokimia pada saat fertilisasi dan mengandung glikoprotein yang
disekresikan oleh retikulum endoplasma serta apparatus golgi, termasuk
enzim-enzim yang digunakan pada waktu penetrasi spermatozoa.
Pembentukan akrosom terjadi pada tahap spermiogenesis dari
spermatogenesis. Fase spermiogenesis terdiri atas empat tahap (Gambar 6), yaitu:
Fase Golgi
Fase golgi merupakan tahap pertama dari pembentukan akrosom. Pada
tahap ini terbentuk granula proakrosomal pada gelembung golgi yang kemudian
bergabung membentuk butir akrosom tunggal dalam gelembung akrosomal.
Sentriol proksimal akan bergerak dari sitoplasma ke dasar nukleus yang nantinya
akan menjadi leher antara kepala dan ekor. Sentriol distal berkembang menjadi
aksonema (flagella di ekor).
Fase Cap (Tudung)
Terjadi pergerakan butir akrosom ke arah anterior. Butir-butir akrosom
akan memipih yang disebut inner dan outer akrosom serta terdapat membran.
Ekor akan terbentuk dari sentriol distal. Spermatid akan bergerak ke arah lumen
tubuli seminiferi.
Fase akrosomal
Akrosom kemudian akan berkembang menutup duapertiga area kepala.
Kepala dan sitoplasma akan memanjang dan inti akan mengalami kondensasi.
Terdapat mikrotubulus dari selubung yang akan menjadi postnuclear cap.
A B
C D
Gambar 5 Tahapan fase spermiogenesis. A. Fase golgi, B. Fase cap (tudung), C. Fase akrosomal, D. Fase pematangan (maturation) (Sumber: Senger 2005).
Fase pematangan (maturation)
Spermatid akan memanjang dan akan dilepaskan ke lumen dan sisa
sitoplasma akan bergerak ke arah posterior. Mitokondria akan mengelilingi
flagella dari dasar inti sampai dengan sepertiga dari ekor. Granul kromatin yang
berkondensasi akan diganti dengan protamin di dalam inti.
Struktur Ekor
Bagian ekor terdiri atas leher (neck piece), badan ekor (middle piece), ekor
utama (principal piece) dan ujung ekor (end piece). Leher (neck piece)
merupakan bagian yang paling pendek dan terletak antara kepala dan leher.
Badan ekor (middle piece) merupakan bagian dari ujung bagian bawah leher
hingga annulus (struktur pita yang melingkar antara bagian badan dan ekor
utama). Ekor utama (principal piece) merupakan bagian terpanjang dari flagella
mulai dari annulus hingga ujung atas dari bagian ujung ekor. Ujung ekor (end
piece) merupakan bagian akhir dari ekor, bagian ini diawali dari berakhirnya
12
Leher (connecting piece)
Leher adalah bagian terpendek dan terletak antara kepala dan ekor.
Bagian utama adalah kapitulum yang merupakan bagian berkolom dan dan
memiliki struktur serabut yang pekat. Pada bagian yang berkolom terdapat
sentriol proksimal, dimana sentriol ini berperan dalam pembentukan aksonema
selama spermiogenesis. Pada spermatozoa dewasa fungsi sentriol ini belum
diketahui.
Badan (midpiece)
Bagian ini dimulai dari ujung bawah bagian leher hingga annulus (struktur
pita yang melingkar antara bagian badan dan ekor utama). Ciri dari bagian ini
adalah adanya mitokondria yang tersusun heliks sebagai sumber energi untuk
pergerakan spermatozoa dan selubung mitokondria. Membran mitokondria sangat
stabil dan tahan terhadap tekanan selama pergerakan flagella.
Ekor utama (principal piece)
Ekor utama adalah bagian terpanjang dari flagella yang dimulai dari
annulus hingga ujung atas bagian ujung ekor. Pada bagian ini terdapat selubung
serabut, struktur skeletal yang mengelilingi aksonema dan serabut tebal. Fungsi
selubung serabut mirip dengan serabut tebal yaitu untuk mengontrol pergerakan
flagella.
Ujung ekor (endpiece)
Bagian ini merupakan bagian akhir dari ekor, dimana bagian ini diawali
dari berakhirnya selubung serabut. Ujung ekor merupakan tempat berakhirnya
elemen aksonema yang ditandai dengan adanya mikrotubul subunit A tanpa
dyenin dan ketiadaan mikrotubul subunit B.
Spermatogenesis dan Tahapan Tubuli Seminiferi
Spermatogenesis merupakan proses pembentukan spermatozoa yang
diawali terbentuknya spermatogonia yakni sel germinal di dalam tubuli seminiferi.
Spermatogenesis terjadi dalam struktur ekstensif tubuli seminiferi dari testis.
Tubuli seminiferi dilapisi oleh epitel seminiferi dan mengandung cairan lumen,
dimana spermatozoa dilepaskan sepenuhnya terbentuk. Epitel seminiferi terdiri
ditemukan pada tahapan yang berbeda dari dasar tubuli hingga lumen dan
dikelilingi oleh sitoplasma dari sel somatik dan sel Sertoli (Hess 1999).
Gambar 6 Proses spermatogenesis pada mamalia (Sumber: Anonim 2010).
Spermatogenesis terbagi atas tiga fase, yaitu fase proliferasi, meiosis dan
spermiogenesis (Hess 1999; Senger 2005; Dreef et al. 2007). Fase proliferasi
merupakan fase pertama, dimana spermatogonium adalah sel yang paling matang
dan terletak di sepanjang dasar epitel seminiferi. Pada tahap mitosis,
spermatogonia yang berkumpul di membran basalis (spermatogonia tipe A)
membelah empat kali untuk membentuk 16 sel yang selanjutnya disebut
spermatogonia tipe B. Spermatogonia B merupakan tahap terakhir pada
pembelahan secara mitosis. Tahap ini menghasilkan sel untuk memasuki fase
kedua, yaitu spermatosit preleptotene yang akan bergerak menjauhi dasar tubuli
seminiferi dan mendekati sertolijunction(Gambar 7) (Hess 1999).
Fase meiosis terjadi proses reduction-division, yang merupakan
mekanisme biologis dimana sebuah sel germinal tunggal dapat meningkatkan
14
germinal individu yang mengandung untai tunggal setiap kromosom atau setengah
jumlah kromosom yang biasanya ditemukan dalam sel-sel tubuh (Hess 1999).
Tahap pembelahan meiosis, terjadi sintesis DNA serta pembelahan spermatosit
primer yang mengandung 23 pasang kromosom menjadi spermatosit sekunder
yang mengandung 23 pasang kromosom. Spermatosit ini akan mengalami
pembelahan meiosis kedua untuk memproduksi spermatid dengan jumlah
kromosom 23. Proses meiosis diperpanjang selama jangka waktu yang panjang,
karena itu spermatosit ditemukan di setiap tahap spermatogenesis dan dua jenis
spermatosit yang berbeda dapat diamati dalam beberapa tahap (Gambar 7).
Tahap spermiogenesis merupakan tahap dimana setiap spermatid dibentuk
kembali secara fisik oleh sel sertoli dengan menghilangkan beberapa sitoplasma;
mengatur kembali bahan kromatin dari inti spermatid untuk membentuk satu
kepala yang padat dan megumpulkan sisa sitoplasma dan membran sel pada salah
satu ujung dari sel untuk membentuk ekor (Gambar 6). Fase spermiogenesis
terdiri dari tiga tahapan secara umum, yaitu: inti memanjang dan kromosom
berkondensasi, aparatus golgi menghasilkan lisosom seperti granul dan sel
membentuk ekor panjang yang dilapisi mitokondria (Hess 1999).
Epitel tubuli seminiferi dari marsupial terdiri atas lapisan-lapisan germinal
sel dan sel-sel Sertoli (Biscoe & Renfree 1987). Lebih lanjut dikatakan bahwa
siklus di dalam tubuli seminiferi dapat dikelompokkan berdasarkan tahapan
spermatogenesis yang berlangsung di dalam tubuli seminiferi pada testis. Lapisan
epitel tubuli seminiferi testis terdiri atas spermatogonia, spermatosit dan
spermatid. Pada proses spermatogenesis terjadi proses diferensiasi spermatogonia
(diploid) menjadi spermatozoa (haploid). Pembentukan spermatozoa dari
spermatogonia terjadi melalui beberapa tahapan tertentu yang ditandai dengan
perubahan sel-sel spermatogenik (Biscoe & Renfree 1987).
Proses spermatogenesis merupakan proses yang dikendalikan oleh susunan
syaraf pusat, melalui poros hipotalamus-hipofisis dan juga secara lokal pada testis.
Kelenjar hipofisis anterior mensekresikan hormon gonadotropin Follicle
Stimulating Hormone (FSH) dan Luteinizing Hormone (LH) di bawah pengaruh
GnRH dimana FSH mempunyai peranan terhadap perkembangan sel-sel sertoli,
mensekresikan testosterone. Testosterone yang dihasilkan akan berdifusi ke
tubuli seminiferi untuk mengatur spermatogenesis dan bertugas memelihara
sel-sel Sertoli. Sel sertoli merupakan sel-sel pemelihara sel-sel-sel-sel spermatogenik (Senger
2005).
Gambar 7 Perkembangan sel-sel germinal pada tahapan spermatogenesis tikus (Sumber: Dreef 1999).
Parameter Kualitas Spermatozoa
Evaluasi yang dilakukan untuk mengetahui kualitas spermatozoa meliputi
evaluasi makroskopis dan mikroskopis. Evaluasi makroskopis meliputi volume
semen, warna, konsistensi (kekentalan) dan pH (derajat keasaman). Evaluasi
mikroskopis meliputi gerakan massa, motilitas, konsentrasi, morfologi dan
abnormalitas spermatozoa.
Volume semen bagi setiap individu bervariasi tergantung pada perbedaan
umur, bangsa, nutrisi, libido dan kondisi dari individu itu sendiri. Warna semen
umumnya berkaitan erat dengan konsentrasi dan konsistensi. Semakin tinggi
konsentrasi spermatozoa dapat mengakibatkan meningkatnya konsistensi dan
16
pH (derajat keasaman) dapat mempengaruhi daya tahan spermatozoa.
Semakin rendah atau semakin tinggi dari pH normal dapat menyebabkan kematian
spermatozoa. pH semen normal bervariasi antara 6.5-6.9 dengan rata-rata 6.75.
Variasi pH semen kemungkinan dipengaruhi oleh konsentrasi asam laktat yang
dihasilkan dalam proses akhir metabolisme. Metabolisme spermatozoa dalam
keadaan anaerobik akan menghasilkan asam laktat yang tertimbun dan
meningkatkan atau menurunkan derajat keasaman.
Konsentrasi spermatozoa penting untuk diketahui karena hal ini sebagai
kriteria penentu kualitas semen. Derajat kekeruhan spermatozoa ditentukan oleh
konsentrasi spermatozoa. Semakin banyak konsentrasi spermatozoa
menyebabkan semakin keruh warna semennya.
Motilitas atau daya gerak spermatozoa ditentukan setelah melakukan
penampungan semen. Faktor yang mempengaruhi motilitas spermatozoa terbagi
menjadi dua, yaitu faktor endogen yang meliputi umur sperma, maturasi sperma,
penyimpanan energi (ATP), agen aktif dan faktor eksogen yang meliputi biofisik
dan fisiologi, cairan suspensi dan adanya rangsangan hambatan (Ax et al. 2000).
Pengamatan motilitas spermatozoa dapat dilakukan menggunakan mikroskop
dengan lensa objektif 40X pada ulasan semen di atas objek glass yang ditutup
cover glass. Motilitas spermatozoa berperan dalam penentuan kualitas semen
karena akan berkaitan erat dengan kemampuan spermatozoa dalam melakukan
aktivitas fertilisasi.
Gerakan merupakan cerminan dari motilitas spermatozoa. Semakin aktif
dan semakin banyak bergerak ke depan maka nilai dari gerakan tersebut semakin
baik. Gerakan individu yang progresif akan menyebabkan spermatozoa menjadi
semakin cepat bertemu dengan ovum. Gerak melingkar atau mundur yang terjadi
pada spermatozoa menunjukkan bahwa terjadicold shock, penurunan suhu secara
mendadak, panas yang berlebihan, adanya bahan-bahan kimia dan benda asing.
Secara morfologi abnormalitas spermatozoa dikategorikan menjadi
abnormalitas primer (berkaitan dengan kepala sperma dan akrosom), sekunder
(berkaitan dengan keberadaan droplet pada bagian tengah ekor) dan tersier
(berkaitan dengan kerusakan ekor) (Ax et al. 2000). Barham dan Pennington
sekunder. Abnormalitas primer merupakan bentuk-bentuk perubahan yang terjadi
pada proses spermatogenesis di dalam tubuli seminiferi. Bentuk-bentuk
abnormalitas ini antara lain kepala yang terlampau besar (macrocephalus) dan
kecil (microcephalus), kepala pendek dan melebar, ekor ganda dan ekor
melingkar (coiled), putus atau terbelah. Abnormalitas sekunder terjadi setelah
spermatozoa meninggalkan tubuli seminiferi, selama perjalanan melalui
epididimis, ejakulasi atau penampungan ejakulat termasuk pemanasan yang
berlebihan, pendinginan yang cepat, kontaminasi dengan air, urin dan antiseptik.
Bentuk-bentuk abnormalitas ini meliputi kepala tanpa ekor, bagian tengah yang
melipat, adanya butiran-butiran sitoplasmik proksimal atau distal dan selubung
BAHAN DAN METODE
Tempat dan Waktu
Penelitian ini dilaksanakan dari bulan Februari-Juli 2011 di Laboratorium
Fisiologi dan Reproduksi Fakultas Peternakan Perikanan dan Ilmu Kelautan
Universitas Negeri Papua, Laboratorium Unit Rehabilitasi Reproduksi
Departemen Klinik Reproduksi dan Patologi dan Laboratorium Riset Anatomi
Departermen Anatomi Fisiologi dan Farmakologi Fakultas Kedokteran Hewan
Institut Pertanian Bogor.
Metode Penelitian
Penelitian ini menggunakan 21 ekor Bandikut (E. kalubu) jantan dari
kabupaten Manokwari yang dibedakan menjadi tiga kelompok berdasarkan berat
badan, yaitu kelompok prapubertas: 370-640 g, dewasa muda: > 640-850 g dan
dewasa: > 850 g (dewasa). Echymipera kalubujantan mulai kawin dengan berat
badan 650 g (Lyne 1964, diacu dalam Warsono 2009) dan jantan dewasa dengan
kisaran berat badan 840-1500 g (Flannery 1995).
Penelitian yang dilakukan terdiri dari tiga macam pengamatan, yaitu
pengamatan karakteristik organ reproduksi (bagian dari organ reproduksi),
karakteristik spermatozoa asal kauda epididimis (motilitas spermatozoa,
konsentrasi spermatozoa dan morfologi yang meliputi abnormalitas spermatozoa
serta morfometri spermatozoa) dan gambaran tahapan spermatogenesis yang
diamati melalui gambaran tubuli seminiferi dari sediaan histologi. Untuk
pengamatan ini hewan dikorbankan dengan cara pengeluaran darah (exsanguinasi)
dari artericarotis communissetelah hewan dianastesi dengan kombinasi
ketamin-hidroklorida (50 mg/kgBB) dan xylazin-ketamin-hidroklorida (10 mg/kgBB) (Schaeffer
1997; Fowler 2008).
1. Karakteristik Organ Reproduksi
Pengamatan makroskopis dilakukan terhadap bentuk dari organ reproduksi
jantan. Pengamatan morfometri dilakukan melalui pengukuran panjang, lebar
Vas deferens, Kelenjar Prostat, Kelenjar Cowper (Kelenjar Cowper 1 dan Cowper
2), Crus Penis, Penis, Glans penis (Thodunter & Gemmel 1987; Renfree 1993).
Bahan yang digunakan kertas tissue, NaCl fisiologis, sedangkan alat yang
digunakan adalah spuit 1 mL, scalpel, pinset, gunting, kaliper (mm) dan pita ukur
(cm).
Testis: pengukuran panjang dan diameter dilakukan dengan menggunakan kaliper. Pengukuran panjang dimulai pada ujung testis dari salah satu sisi ke sisi
yang lain tanpa epididimis. Pengukuran diameter dilakukan pada bagian tengah
dari testis kemudian dilakukan penimbangan.
Epididimis: pengukuran panjang dilakukan dengan menggunakan kaliper, dimulai dari kaput hingga kauda epididimis, kemudian dilakukan penimbangan.
Vas deferens: panjang vas deferens diukur dengan menggunakan kaliper yang dimulai dari akhir kauda epididimis hingga ujung akhir vas deferens yang berada
dekat prostat.
Kelenjar Prostat:pengukuran panjang, lebar dan tebal menggunakan kaliper dan selanjutnya ditimbang.
Kelenjar Cowper 1: pengukuran tebal menggunakan kaliper selanjutnya ditimbang.
Kelenjar Cowper 2: pengukuran tebal menggunakan kaliper selanjutnya ditimbang.
Crus Penis:pengukuran tebal menggunakan kaliper dan selanjutnya ditimbang. Penis:pengukuran panjang total penis dimulai dari pangkal penis hingga ke ujung penis dan juga dilakukan pengukuran panjang glans penis.
2. Karakteristik Spermatozoa Asal Epididimis
Koleksi spermatozoa dilakukan dengan menyayat kauda epididimis.
Evaluasi yang dilakukan terhadap spermatozoa epididimis meliputi: Motilitas
spermatozoa, Konsentrasi spermatozoa dan Morfologi spermatozoa.
Bahan dan alat yang digunakan adalah epididimis, NaCl, formolsaline,
pewarna Carbofuchsin (William’s stain), alkohol absolut, chloramin 0.5%, alkohol
95%, air destilasi dan kertas tissue. Peralatan yang digunakan meliputi object
glass, cover glass, jarum suntik 5 mL, mikropipet 1-10 µL, kotak hitung
21
Motilitas spermatozoa
Motilitas spermatozoa dihitung dengan menempelkan kauda yang telah
disayat pada object glasskemudian diteteskan NaCl sebanyak 1 tetes. Campuran
spermatozoa dan NaCl tadi diambil satu tetes dan diteteskan pada object glass
yang lain dan ditutup dengan cover glass. Motilitas spermatozoa selanjutnya
diamati aktivitas gerak spermatozoa dimana spermatozoa hidup akan bergerak dan
spermatozoa dinilai dari lima lapang pandang. Spermatozoa yang motil akan
bergerak ke depan dan spermatozoa yang bergerak ditempat, bergerak melingkar,
bergerak mundur dan diam sebagai spermatozoa yang tidak motil, penilaian
menggunakan skoring 0-100%.
Konsentrasi spermatozoa
Kauda epididimis disayat-sayat kemudian di flushing menggunakan NaCl
sebanyak 5 mL. Spermatozoa yang telah di flushing kemudian disentrifugasi
dengan kecepatan 1500 rpm selama 5 menit (Setiadi et al. 2006). Cairan diatas
kemudian dibuang, suspensi padat yang terdapat di bagian bawah diambil
sebanyak 5 μL dan diencerkan dengan formolsaline, dihomogenkan dan
diteteskan satu tetes pada kotak hitung Neubauer. Konsentrasi spermatozoa
merupakan jumlah spermatozoa yang telah diperoleh dikalikan dengan faktor
pengencer dan faktor hemositometer.
Morfologi spermatozoa
Morfologi spermatozoa diamati pada sediaan ulas yang diwarnai dengan
Carbofuchsin (William’s stain). Spermatozoa epididimis yang telah dicampur
dengan NaCl, dihomogenkan dengan batang pengaduk, dibuat preparat ulas tipis
(smear) dan dikeringudarakan. Kemudian preparat ulas ini difiksasi dan dicuci
dengan alkohol absolut selama 4 menit dan keringudarakan. Setelah itu preparat
dimasukkan di dalam chloramin 0.5% selama 2 menit dan dicuci dengan air
destilasi, alkohol 95% dan diwarnai dengan larutan William’s selama 8-10 menit.
Tahap akhir preparat dicuci dengan air mengalir perlahan dan dikeringkan.
Morfologi dan abnormalitas spermatozoa dievaluasi dari 10 lapang pandang
menggunakan mikroskop cahaya dengan pembesaran lensa objektif 40X
3. Tahapan Spermatogenesis
Bahan dan alat yang digunakan adalah testis, NaCl fisiologis, kertas tissue,
paraformaldehid 4%, alkohol dengan konsentrasi bertingkat (70, 80, 90, 95 dan
100%), xylol, paraffin, aquades, pewarna periodic acid Schiff (PAS) dan perekat
entelan. Peralatan yang digunakan adalah botol sampel, pinset, wadah penyimpan
jaringan,object glassdan penutup, inkubator 370C, inkubator paraffin, blok kayu,
bunsen, mikrotom, water bath, meja pemanas, termometer, mikroskop Olympus
BX41.
Untuk pengamatan spermatogenesis (proses pembentukan spermatozoa)
yang berlangsung di dalam tubuli seminiferi, testis difiksasi dengan larutan
paraformaldehid 4% selama 3x24 jam, kemudian jaringan diproses hingga
menjadi blok parafin. Jaringan dalam blok paraffin dipotong menggunakan
mikrotom dengan ketebalan 3 µm dan dilekatkan pada object glass. Sediaan
histologi kemudian diwarnai dengan Periodic Acid Schiff (PAS) untuk
menentukan tahapan spermatogenesis (Kiernan 1990). Frekuensi tahapan
spermatogenesis ditentukan dengan cara jumlah tubuli pada masing-masing
tahapan dibagi dengan jumlah total tubuli dikali dengan 100.
Analisis Data
Data yang diperoleh dianalisis secara deskriptif dan konfirmatif dengan
variabel yang diukur adalah rata-rata yang didapat dari setiap variabel dengan
HASIL DAN PEMBAHASAN
Bandikut (E. kalubu) memiliki dua buah testis diluar abdomen dengan
posisi menggantung secara transversal. Testis terbungkus oleh skrotum yang
tidak berpigmen (berwarna putih) dan tidak ditumbuhi rambut. Menurut Biscoe
dan Renfree (1987), beberapa kelompok marsupial memiliki skrotum yang
berpigmen dan tidak berpigmen. Penis dikeluarkan melalui satu saluran
bersama-sama dengan saluran pembuangan kotoran (satu saluran anus mirip kloaka)
(Gambar 8). Pada E.kalubu dewasa jarak antara kloaka dengan testis adalah
22.25±0.3 mm.
Gambar 8 Testis dan PenisEchymipera kalubu.
Organ ReproduksiEchymipera kalubuJantan
Struktur organ reproduksi E. kalubujantan mirip dengan organ reproduksi
marsupial jantan lainnya yaitu tidak memiliki kelenjar vesikularis. Organ-organ
tesebut terdiri atas sepasang testis, epididimis dan vas deferens, kelenjar prostat,
dua buah kelenjar Cowper (bulbouretral), crus penis, penis serta glans penis yang
berbentuk bhipid (bercabang dua) (Gambar 9). Hasil penelitian ini mirip dengan
hasil penelitian Paris et al. (2005) pada Tammar wallaby (Macropus eugenii),
namun Tammar wallaby memiliki glans penis yang tunggal dan tiga buah kelenjar
Cowper.
Gambar 9 diambil dari kelompok E. kalubu dewasa. Gambaran organ
reproduksi dapat dilihat secara jelas pada kelompok dewasa, karena pada
kelompok ini organ-organ reproduksi telah terbentuk dengan sempurna serta tidak
Gambar 9 Organ reproduksi E. kalubu jantan; 1). Testis; 2). Epididimis; 3). Vas deferens; 4). Kelenjar Prostat; 5). Kelenjar Cowper; 6). Crus penis; 7). Penis; 8). Uretra; 9).Vesica urinaria; 10). Ginjal. Bar: 1 cm
Testis
Testis berfungsi untuk menghasilkan spermatozoa dan sekresi hormon
androgen (Senger 2005). Testis E. kalubu berbentuk elipsoid dengan ukuran
(panjang dan berat) yang meningkat seiring dengan perkembangan kedewasaan.
Hasil yang diperoleh sesuai dengan pernyataan Biscoe dan Renfree (1987), bahwa
testis pada marsupial dewasa umumnya berbentuk elipsoid. Ukuran panjang dan
berat testis berbeda pada setiap kelompok, yaitu prapubertas mempunyai panjang
9.83±0.16 mm, meningkat pada dewasa muda, yaitu 14.30±0.11 mm dan paling
besar pada dewasa, yaitu 14.98±0.24 mm serta memiliki berat masing-masing
0.33±0.01 g, 0.83±0.01 g dan 0.94±0.03 g.
Berat testis E. kalubu hasil penelitian lebih kecil bila dibandingkan
dengan kelompok marsupial lainnya, seperti berat testis Tammar wallaby adalah
12,5±1,5 g (Paris et al. 2005); berat testis dan epididimis Isoodon macrourus
berkisar antara 5,6-7,9 g (Thodunter & Gemmel 1987). Perbedaan ini
kemungkinan disebabkan karena perbedaan spesies serta ukuran dan berat badan
dari masing-masing kelompok hewan tersebut. Menurut Biscoe dan Renfree
(1987), berat testis bervariasi pada spesies marsupial dan berhubungan dengan
25
Epididimis
Epididimis dihubungkan dengan testis oleh duktus efferens yang
berfungsi menyalurkan spermatozoa dan menyerap sebagian besar cairan yang
dikeluarkan oleh testis. Epididimis terbagi menjadi tiga bagian yaitu: kaput,
corpus dan kauda yang masing-masing bertanggung jawab terhadap penyerapan,
pematangan dan penyimpanan spermatozoa. Panjang dan berat epididimis
E. kalubu juga berbeda-beda tergantung pada perkembangan kedewasaannya.
Pada kelompok prapubertas panjang ataupun beratnya paling kecil. Pada
kelompok dewasa muda panjangnya berbeda dengan yang dewasa tetapi
mempunyai berat yang sama yaitu 0,26±0,01 g (Tabel 2). Ukuran ini termasuk
kecil bila dibandingkan dengan hewan marsupial lainnya, seperti Tammar wallaby
yang memiliki berat epididimis 3,2±0,30 g (Paris et al. 2005) dan pada Honey
possumsepididimis kiri 56,20±15,70 g serta kanan 51,5±16,0 g (Russel & Renfree
1989). Berat dan panjang yang berbeda-beda selain disebabkan oleh perbedaan
spesies hewan kemungkinan juga karena epididimis setiap individu memiliki
kapasitas yang berbeda dalam penyimpanan spermatozoa, seperti yang dikatakan
Cummins et al. (1986), bahwa beberapa spesies marsupial memiliki kapasitas
penyimpanan spermatozoa yang terbatas hanya untuk beberapa juta spermatozoa.
Vas deferens
Vas deferens merupakan saluran yang menghubungkan epididimis dengan
uretra, saluran ini berfungsi sebagai saluran transportasi spermatozoa dari
epididimis yang nantinya akan bercampur dengan sekresi dari kelenjar prostat dan
Cowper. Panjang dan diameter vas deferens hasil penelitian ini berbeda-beda,
paling pendek terdapat pada kelompok prapubertas 41.99±0.38 dengan diameter
1.44±0.23 dan paling panjang terdapat pada kelompok dewasa yaitu 67,21±0,57
mm dengan diameter 1.97±0.56 mm.
Kelenjar asesoris
Kelenjar asesoris berfungsi mengeluarkan sekresi yang akan bercampur
dengan spermatozoa, dimana sekresi dari kelenjar asesoris ini berfungsi untuk
mempertahankan kelangsungan hidup dan pergerakan spermatozoa. Echymipera
kalubuhanya memiliki dua buah kelenjar asesoris, yaitu kelenjar prostat (Gambar
dihasilkan oleh kedua kelenjar tersebut, hal ini berbeda dengan ternak pada
umumnya dimana plasma semen 75% dihasilkan oleh kelenjar vesikularis.
Prostat
Kelenjar prostat memberikan sekresi pada semen yang membantu sebagai
pelicin pada spermatozoa. Menurut Biscoe dan Renfree (1987), kelenjar prostat
mensekresikan seminal plasma yang mengandung karbohidrat dan berfungsi
dalam mempengaruhi motilitas spermatozoa. Hasil penelitian memperlihatkan
bahwa kelenjar prostatE. kalubumemiliki ukuran yang berbeda-beda untuk setiap
perkembangan kedewasaan. Panjang, lebar dan berat paling kecil terdapat pada
kelompok prapubertas dan paling besar pada kelompok dewasa, yaitu panjang
11,05±2,08 mm, lebar 9,66±1,89 mm dan berat 0,66±0,27 g (Tabel 2). Pada
daerah yang memiliki perbedaan musim ukuran kelenjar prostat dipengaruhi oleh
musim kawin. Hal ini dapat dilihat padaI. macrourus saat tidak terjadi musim
kawin berat kelenjar prostat hanya 2.5-7.4 g dan saat terjadi musim kawin
beratnya meningkat menjadi 6.9-8.9 g (Thodunter & Gemmel 1987). Lebih lanjut
menurut Paris et al. (2005) berat prostat Tammar wallaby adalah 15.2±1.8 g.
Beberapa penelitian sebelumnya juga menunjukkan bahwa dimensi kelenjar
prostat berbeda-beda pada beberapa spesies marsupial (Tabel 1).
Tabel 1 Dimensi prostat pada beberapa spesies marsupial
Spesies Prostat (mm)
(Panjang x Lebar) Sumber
Isoodon macrourus 25-33x19-28 Thodunter & Gemmel 1987
Neophascogale lorentzi 22.5x6.0 Wooley 2001
Myotic wallacei 25.5x5.0 Wooley 2001
Dasyurus albopunctatus 28.5x 5.5 Wooley 2001
Kelenjar prostat marsupial umumnya terbagi menjadi dua bentuk, yaitu
bentuk jantung dan wortel (Biscoe & Renfree 1987). Gambar 10A menunjukkan
bahwa kelenjar prostat E. kalubu berbentuk seperti jantung, sedangkan kelenjar
prostat Tammar wallaby berbentuk seperti wortel (Gambar 10B). Hal ini sesuai
dengan pendapat Biscoe dan Renfree (1987), bahwa kelenjar prostat pada
kelompok hewan Peramelidae dan Phascolarctidae berbentuk seperti jantung,
27
Petauridae, Phalangeridae, Notoryctidae dan Lasiorhinus latifrons berbentuk
seperti wortel.
A B
Gambar 10 Kelenjar Prostat A). Bandikut (E. kalubu); B). Tammar wallaby (Macroupus eugenii) (Pariset al.2005). Bar: 1 cm
Cowper (Bulbouretral)
Kelompok hewan marsupial memiliki jumlah kelenjar Cowper yang
bervariasi dari satu hingga tiga buah. Kelenjar ini berbentuk struktur bulbus yang
bergabung dengan uretra melalui saluran-saluran yang dikelilingi oleh otot-otot
yang halus (Biscoe & Renfree 1987). Echymipera kalubu memiliki dua buah
kelenjar Cowper yang terbentang sepanjang bagian dari uretra dan bentuknya
berbeda pada hewan mamalia pada umumnya, karena berbentuk lobulus-lobulus
(Gambar 11A). Kelenjar Cowper yang ditemukan jumlahnya sama dengan yang
dimiliki oleh Isoodon macrourus, Neophascogale lorentzi dan Sugar glider
(Tedman 1990; Wooley 2001). Menurut Tedman (1990) Sugar glider memiliki
dua multilobus kelenjar Cowper yang terbentang dorsal dan lateral pada rektum.
Kelompok hewan marsupial lainnya, seperti Tammar wallaby, Myotic wallacei,
Dasyurus albopunctatus dan Dasyurus spartacus memiliki tiga buah kelenjar
Cowper (Pariset al2005; Wooley 2001).
Bandikut (E. kalubu) memiliki kelenjar Cowper 1 yang berada dekat
saluran uretra dan memiliki ukuran kelenjar Cowper 1 yang relatif lebih besar,
sedangkan kelenjar Cowper 2 berdekatan dengan kelenjar Cowper 1 namun
memiliki ukuran yang selalu lebih kecil bila dibandingkan dengan kelenjar
Cowper 1. Kisaran tebal dan berat masing-masing kelenjar Cowper adalah
1.37±0.01-3.27±1.89 mm dan berat 0.02±0.01-0.10±0.06 g (Gambar 11A). Hasil yang
diperoleh ini sama seperti hasil penelitian Paris et al. 2005 bahwa tiga buah
kelenjar Cowper yang dimiliki Tammar wallaby juga memiliki ukuran yang tidak
sama, yaitu kelenjar Cowper 1 adalah 0.20±0.02 g, Cowper 2 adalah 0.7±0.10 g,
Cowper 3 adalah 0.6±0.10 g.
A B
Gambar 11 A). E. kalubu; 1. Glans penis; 2. Penis; 3. Urethral bulb; 4. Crus penis; 5. Cowper 1; 6. Cowper 2; B). Tammar wallaby; Ub. Urethral Bulb; Cp: Crus penis; Cg2: Cowper 2; Cg3: Cowper 3 (Paris et al 2005). Bar: 1 cm
Organ kopulatoris
Penis
Penis E. kalubu yang dalam keadaan normal berbentuk sigmoid dan
memiliki glans penis yangbhipidatau bercabang (Gambar 10A). Struktur glans
penis marsupial umumnya bercabang, meskipun ada juga yang tidak bercabang
(Dawson et al. 1999). Glans penis yang berbentuk bhipid kemungkinan
berhubungan dengan bentuk vagina marsupial yang terdiri atas dua bagian, yaitu
dua vagina lateral dan vagina median (Biscoe & Renfree 1987; Gordon &
Hulberth 1989). Penis marsupial biasanya memiliki struktur berbentuk sigmoid di
dalam kantung preputial pada kloaka (Biscoe & Renfree 1987). Lebih lanjut
dikatakan bahwa penis biasanya dikeluarkan hanya pada saat terjadi interaksi
seksual dan pada berbagai spesies penis sulit untuk dikeluarkan diluar musim
kawin. Hasil penelitian diperoleh panjang penis pada kelompok prapubertas
13.56±4.23 mm, kelompok dewasa muda 21.9±2.41 mm dan paling panjang pada
29
Urethral bulb berperan dalam membantu aktivitas otot bulbo-cavernosus
dalam proses pengosongan uretra. Crus penis pada marsupial memisahkan dua
kelenjar Cowper yang ukurannya lebih kecil dan berperan pada proses terjadinya
ereksi (Allen & Cantab 1893; Biscoe & Renfree 1987).
Karakteristik Spermatozoa asal Kauda Epididimis
EpididimisE. kalububerukuran agak kecil (Tabel 2) sehingga tidak semua
evaluasi terhadap karakteristik spermatozoa kauda epididimis dapat dilakukan,
kondisi ini menyebabkan evaluasi mikroskopis hanya dilakukan terhadap
motilitas, konsentrasi dan morfologi spermatozoa.
Tabel 2 Morfometri organ reproduksiE. kalubujantan
Organ Keterangan Echymipera kalubu
Prapubertas Dewasa muda Dewasa
Testis
Panjang (mm) 9.83±0.16 14.30±0.11 14.98±0.24 Diameter (mm) 7.17±0.14 10.05±0.02 10.08±0.28 Berat (g) 0.33±0.01 0.83±0.01 0.94±0.03
Epididimis
Panjang (mm) 18.24±0.89 26.1±0.64 27.79±0.55 Berat (g) 0.07±0.02 0.22±0.01 0.26±0.01
Vas deferens
Panjang (mm) 41.99±0.38 61.86±3.70 67.21±0.57 Diameter (mm) 1.44±0.23 1.79±0.05 1.97±0.56
Prostat
Panjang (mm) 4.82±1.82 9.67±0.78 11.05±2.08 Lebar (mm) 5.08±2.83 9.12±1.25 9.66±1.89 Tebal (mm) 3.01±2.71 6.97±0.66 7.34±1.54 Berat (g) 0.17±0.11 0.54±0.12 0.66±0.27
Cowper 1
Tebal (mm) 1.47±0.03 2.72±0.12 3.30±0.09 Berat (g) 0.01±0.01 0.05±0.01 0.10±0.01
Cowper 2
Tebal (mm) 1.37±0.009 2.39±0.28 3.27±1.89 Berat (g) 0.02±0.01 0.03±0.01 0.10±0.06
Crus penis
Tebal (mm) 2.68±0.05 3.81±0.01 5.25±0.27 Berat (g) 0.05±0.01 0.15±0.01 0.31±0.01
Penis
Panjang (mm) 13.56±4.23 21.9±2.41 26.59±4.44 Diameter (mm) 2.61±1.03 2.83±0.64 3.67±0.82
Glans penis
Motilitas spermatozoa
Motilitas spermatozoa merupakan salah satu faktor dalam menentukan
kualitas spermatozoa karena menunjukkan persentase spermatozoa yang hidup.
Motilitas spermatozoa biasanya digunakan sebagai indikator dari viabilitas sel,
integritas membran dan fungsi metabolisme intrasel. Motilitas juga merupakan
salah satu parameter untuk menentukan fertilitas tetapi tidak berkorelasi dengan
kemampuan fertilisasi baik secarain vitromaupunin vivo(Durrant 1990).
Motilitas spermatozoa epididimis hasil penelitian pada setiap kelompok
cenderung mengalami peningkatan, paling rendah pada kelompok prapubertas
hanya 33,33±25,17%, meningkat pada kelompok dewasa muda menjadi
41,67±12,58% dan paling tinggi terdapat pada kelompok dewasa, yaitu
57,50±3,54% (Gambar 12). Peningkatan motilitas spermatozoa ketiga kelompok
ini kemungkinan disebabkan karena peningkatan perkembangan seksual dan
kedewasaan. Informasi mengenai motilitas spermatozoa dari kauda epididimis
E. kalubu belum pernah dilaporkan, pada koala motilitas semen segar yang
dikoleksi menggunakan ejakulator menunjukkan motilitas spermatozoa rata-rata
78,8 ± 2,8% (49-95%) (Johnston et al. 2000). Perbedaan ini dapat dipahami
mengingat teknik koleksi semen yang berbeda, adanya perbedaan ras dan oleh
beberapa faktor antara lain faktor endogen yang meliputi umur dan maturasi
spermatozoa serta penyimpanan energi (ATP) (Axet al.2000).
31
Konsentrasi spermatozoa
Konsentrasi spermatozoa sangat penting dalam penentuan kemampuan seekor
pejantan dalam membuahi sel telur. Konsentrasi spermatozoa E. kalubu yang
diperoleh mengalami peningkatan sejalan dengan peningkatan kedewasaan
(Gambar 13). Kosentrasi spermatozoa paling rendah pada kelompok prapubertas
1.75±1.14x106/mL dan paling banyak pada kelompok dewasa 12.56±6.33x106/mL
(Tabel 3). Angka konsentrasiE. kalubumasih lebih rendah dibandingkan dengan
konsentrasi spermatozoa epididimis Isoodon obesulus dan I. macrourus dengan
jumlah spermatozoa 48x106/mL 70.97x106/mL (Biscoe & Renfree 1987), namun
masih lebih tinggi dari spermatozoa epididimis Brown marsupial mouse
(Antechinus stuartii) yang hanya 3.5x106/mL sampai dengan 4.4x106/mL (Taggart
& Smith 1990).
Gambar 13 Grafik konsentrasi spermatozoa E. kalubu yang dikoleksi dari kauda epididimis (x106/mL).
Konsentrasi spermatozoa ditentukan oleh ukuran testis dan aktivitas
spermatogenesis yang sebanding dengan perkembangan seksual dan kedewasaan,
serta kualitas makanan dan status kesehatan dari pejantan (Salisbury &
VanDemark 1985; Sumeidiana et al. 2007). Selain itu variasi konsentrasi pada
individu jantan berhubungan dengan aktivitas seksual sepertimating(perkawinan)
sebelum penampungan akan menurunkan konsentrasi dan stres (kemampuan
beradaptasi) (Haron et al. 1999; Sumeidianaet al. 2007). Lebih lanjut dikatakan
pula bahwa perbedaan konsentrasi spermatozoa dapat juga dipengaruhi oleh
Tabel 3 Motilitas (%) dan Konsentrasi (x106/mL) spermatozoaE. kalubuyang dikoleksi dari kauda epididimis
Kelompok Motilitas (%) Konsentrasi (x106/mL)
Prapubertas 33.33±25.17 1.75±1.14
Dewasa muda 41.67±12.58 8.86±4.21
Dewasa 57.50±3.54 12.56±6.33
Morfologi dan Morfometri Spermatozoa
SpermatozoaE. kalubumemiliki bentuk kepala yang kecil dan batas antara
kepala dengan ekor tidak sejelas pada spermatozoa ternak pada umumnya
(Gambar 14). Karakteristik morfologi spermatozoa ini mirip dengan unggas.
Ukuran dan bentuk spermatozoa antar spesies hewan dapat berbeda-beda, namun
memiliki struktur morfologi yang sama yaitu terdiri atas kepala dan ekor. Hasil
penelitian diperoleh bahwa panjang keseluruhan spermatozoa E. kalubu adalah
162.51±5.12 μm dengan panjang kepala 2.91±0.40 μm, panjang midpiece
13.99±0.87μm dan panjang ekor utama adalah 145.59±5.38μm (Gambar 14).
Gambar 14 Spermatozoa normalE. kalubu. Pewarnaan William’s.
Morfometri spermatozoa hasil penelitian lebih pendek dari beberapa
spesies marsupial lain seperti Perrameles nasuta dengan panjang kepala 5.7 μm,
midpiece 14 μm dan panjang keseluruhan 199.8 μm, I. macrourus memiliki
panjang kepala 6 μm,midpiece 10.7 μm dan panjang keseluruhan 171.1 μm dan
Tarsipes rotatus dengan panjang kepala 10.6 μm, midpiece 91 μm dan panjang
keseluruhan 342.6μm (Hardinget al.1990). Menurut Tourmente (2011), panjang
33
79.50-349.44 µm. Bila dibandingkan dengan spermatozoa beberapa hewan lain
yang memiliki ukuran tubuh serupa, maka spermatozoa E. kalubu masih lebih
panjang. Pada beberapa rodensia seperti spermatozoa Cavia porcellus memiliki
panjang kepala 7.5±0.3 μm dan panjang ekor 92.3±0.9 μm, panjang kepala
Ctenomys coyhaiquensis 7.6±0.4μm dan panjang ekor 66.3±2.2 μm dan panjang
kepala Aconaemys fuscus 5.6±0.3 μm dan panjang ekor 35.2±2.3 μm
(Gallardo 2002).
Gambar 15 Morfologi spermatozoa abnormal E. kalubu. a-i. abnormal (a. kepala &
midpiece tanpa principal piece; b. detached head; c. kepala & midpiece
pecah; d. principal piece melingkar; e. principal piece bengkok (simple bent); f. coiled pada principal piece; g. principal piece menggulung (bent tail); h.midpiecedanprincipal piecemelipat; i.principal piecetanpa kepala &midpiece). Bar: 20μm
Perbedaan spesies hewan selain mempengaruhi bentuk kepala juga dapat
mempengaruhi ukuran baik panjang kepala maupun panjang keseluruhan
spermatozoa. Selain itu menurut Arifiantiniet al.(2006) bahwa teknik pewarnaan
yang digunakan dalam pengukuran morfometri spermatozoa sapi juga dapat
memberikan pengaruh nyata pada ukuran panjang kepala dan ekor bagian utama
Spermatozoa normal memegang peranan penting dalam keberhasilan
fertilisasi. Nilai abnormalitas ditentukan berdasarkan jumlah spermatozoa dengan
bentuk yang tidak normal. Abnormalitas kepala yang tertinggi ditemukan pada
kelompok prapubertas 1.73% (Gambar 16). Jenis-jenis abnormalitas kepala pada
kelompok prapubertas adalah detached head 1.73%, kelompok dewasa muda
adalah kepala dan midpiece tanpa principal piece 0.24% dan detached head
1.15% dan kelompok dewasa adalah kepala dan midpiece tanpa principal piece
0.23%,detached head0.58% serta kepala danmidpiecepecah 0.58% (Tabel 4).
Gambar 16 Grafik persentase abnormalitas spermatozoaE. kalubu(%).
Abnormalitas pada ekor tertinggi terdapat pada kelompok dewasa muda
sebanyak 23.23%. (Gambar 16). Jenis-jenis abnormalitas ekor pada kelompok
prapubertas antara lain principal piece bengkok (simple bent) 15.26% dan
principal piece menggulung (bent tail) 3.57%, midpiece dan principal piece
melipat 0.11%, kelompok dewasa muda adalah principal piece bengkok (simple
bent) 16.52%, principal piece melingkar 0.60%, coiled pada principal piece
0.06%, principal piece menggulung (bent tail) 3.33%, midpiece dan principal
piece melipat 2.72% dan kelompok dewasa adalah principal piece bengkok
(simple bent) 12.97%, principal piece melingkar 0.23%, coiled pada principal
piece 0.46%, ekor utama menggulung 0.35%, midpiece dan principal piece
35
Tabel 4 Tingkat abnormalitas spermatozoaE. kalubu(%)
Kelompok Abnormalitas Persentase
Prapubertas Kepala Kepala danmidpiecetanpaprincipal piece
-Detached head 1.73
Kepala danmidpiecepecah -1.73
Ekor Principal piecebengkok (simple bent) 15.26
Principal piecemelingkar -Coiled padaprincipal piece
-Principal piecemenggulung (bent tail) 3.57
Midpiecedanprincipal piecemelipat 0.11
Principal piecetanpa kepala danmidpiece -18.94
Dewasa muda
Kepala Kepala danmidpiecetanpaprincipal piece 0.24
Detached head 1.15
Kepala danmidpiecepecah -1.39
Ekor Principal piecebengkok (simple bent) 16.52
Principal piecemelingkar 0.60 Coiled padaprincipal piece 0.06
Principal piecemenggulung (bent tail) 3.33
Midpiecedanprincipal piecemelipat 2.72
Principal piecetanpa kepala danmidpiece -23.23
Dewasa Kepala Kepala danmidpiecetanpaprincipal piece 0.23
Detached head 0.58
Kepala danmidpiecepecah 0.58 1.39
Ekor Principal piecebengkok (simple bent) 12.97
Principal piecemelingkar 0.23 Coiled padaprincipal piece 0.46
Principal piecemenggulung (bent tail) 0.35
Midpiecedanprincipal piecemelipat 3.62
Principal piecetanpa kepala danmidpiece 0.23 17.86
Tingkat abnormalitas spermatozoa asal kauda epididimis pada kelompok
prapubertas dan dewasa muda cenderung lebih tinggi, hal ini kemungkinan
disebabkan karena proses spermatogenesis yang terjadi di dalam tubuli seminiferi
belum terjadi secara sempurna. Menurut Holt dan Pickard (1999) salah satu
faktor yang dapat mempengaruhi tingkat abnormalitas morfologi spermatozoa
adalah tahapan spermatogenesis akhir serta faktor hormonal yang mempengaruhi
Abnormalitas spermatozoa dapat terjadi pada bagian kepala dan ekor
spermatozoa (Bonet et al.1993) dan dapat terjadi selama proses spermatogenesis
maupun setelah keluar dari saluran epididimis (Toelihere 1993; Bonetet al.1993;
Ax et al. 2000 dan Johnson et al. 2000). Barham dan Pennington (2009)
membagi abnormalitas atas abnormalitas primer dan abnormalitas sekunder.
Abnormalitas primer ini terjadi karena kelainan yang terjadi pada saat fase
spermatogenesis di tubuli seminiferi, sedangkan abnormalitas sekunder ini terjadi
saat perjalanan spermatozoa dari tubuli seminiferi menuju epididimis, saat terjadi
ejakulasi, perlakuan semen saat koleksi semen termasuk tahapan selanjutnya
seperti pemanasan, pendinginan, penambahan antibiotik dan terkontaminasi zat
berbahaya lainnya. Abnormalitas primer yang diperoleh dari hasil penelitian
meliputi kepala dan midpiece tanpa principal piece, detached head serta kepala
dan midpiece pecah, sedangkan abnormalitas sekunder meliputi coiled pada
principal piece, principal piece bengkok (simple bent), principal piece
menggulung (bent tail) dan principal piece tanpa kepala dan midpiece
(Gambar 15).
Tahapan Spermatogenesis
Spermatogenesis merupakan suatu proses kompleks, dinamis dan terus
menerus dalam memproduksi spermatozoa haploid yang terjadi di dalam tubuli
seminiferi testis (Dreefet al. 2007). Proses spermatogenesis terbagi menjadi tiga
fase perkembangan penting, yaitu fase proliferatif, fase meiosis dan
spermiogenesis (Hess 1999).
Pewarnaan PAS mewarnai akrosom sehingga dapat dibedakan spermatid
pada berbagai fase dan spermatozoa. Menurut Russel et al. (1990) tahapan
spermatogenesis dapat dibedakan berdasarkan ciri khas dari perkembangan
spermatogonia dan aspek morfologi dari sel germinatif setiap tahap
spermatogenesis. Tahapan spermatogenesis dapat dibedakan juga berdasarkan
kriteria utama yang terletak pada karakteristik morfologi spermatid, letak inti dan
sistem akrosomik. Dengan menggunakan mikroskop cahaya dan pewarnaan PAS
(periodic acid schiff), maka dengan mudah akan didapatkan gambaran