DEGRADASI BAHAN ORGANIK
DAN PEMANFAATANNYA SEBAGAI PENGHASIL ENERGI
LISTRIK PADA SEDIMEN TAMBAK UDANG MELALUI
SEDIMENT MICROBIAL FUEL CELL
YAYAN FIRMANSYAH C34062363
DEPARTEMEN TEKNOLOGI HASIL PERAIRAN
FAKULTAS PERIKANAN DAN ILMU KELAUTAN
RINGKASAN
YAYAN FIRMANSYAH. C34062363. Degradasi Bahan Organik dan Pemanfaatannya sebagai Penghasil Energi Listrik pada Sedimen Tambak Udang melalui Sediment Microbial Fuel Cell. Dibimbing oleh BAMBANG RIYANTO dan AKHIRUDDIN MADDU.
Permasalahan-permasalahan besar sering terjadi pada pengembangan budidaya udang di dunia. Kejadian-kejadian tersebut meliputi pencemaran sedimen tambak akibat sisa pakan, penggunaan bahan kimia, zat antibiotik, dan timbulnya penyakit pada udang. Berbagai teknik dan manajemen budidaya tambak telah banyak dikembangkan, namun penggunaan sediment microbial fuel cell (SMFC) sebagai teknologi pendegradasi atau penurunan akumulasi bahan organik pada tambak udang belum pernah diterapkan. Tujuan dari penelitian ini adalah menganalisis penurunan akumulasi bahan organik dan energi listrik yang dihasilkan pada sedimen tambak udang melalui sediment microbial fuel cell.
Pelaksanaan penelitian ini dilakukan dalam beberapa tahapan. Tahap pertama adalah penentuan tempat pengambilan sampel dan kondisi tempat pengambilan sampel sedimen pada tambak udang. Tahap kedua meliputi pengukuran kualitas air tambak udang serta analisis karakterisasi sedimen tambak udang yang ada. Tahap ketiga adalah berupa pembuatan rangkaian SMFC.Tahap keempat adalah pengukuran arus listrik dan tegangan yang dihasilkan SMFC dengan menggunakan multimeter dan tahap kelima meliputi karakterisasi pada substrat hasil dari proses degradasi bahan organik melalui SMFC, sehingga dapat dilihat adanya perubahan terhadap kadar akumulasi bahan organik pada sedimen tambak udang yang ada.
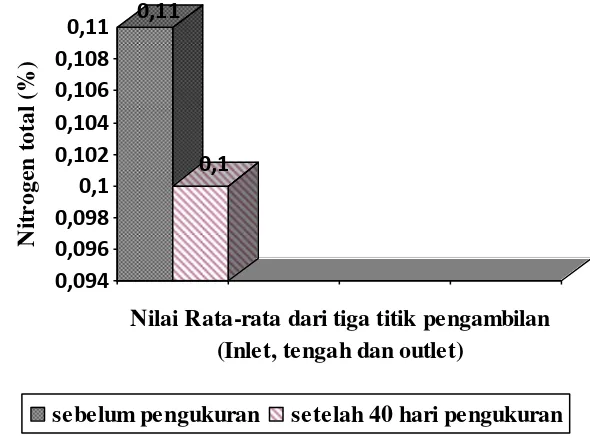
Kualitas air tambak udang di Desa Jayamukti memiliki suhu berkisar antara 29-30oC, salinitas 18-20 ppm, pH 7,5-8,5, DO 3-4 mg/l dan kecerahan sebesar 25-30 cm. Analisis terhadap tekstur sedimen tambak menunjukkan bahwa sedimen tambak udang di Desa Jayamukti tergolong jenis tanah liat, dengan kandungan bahan organik berupa karbon organik (C) 1,45±0,44%, Nitrogen (N) 0,11±0,03%, rasio C/N 13 dan Fosfor (P) 59 ppm. Sedangkan kandungan bahan organik pada sedimen setelah 40 hari pengukuran mengalami penurunan yaitu, karbon organik 1,29±0,34 %, Nitrogen 0,10±0,02 %, sehingga ratio C/N sebesar 12 dan kandungan P yang tersedia 40±4,08 ppm. Nilai kapasitas tukar kation (KTK) setelah 40 hari pengukuran mengalami penurunan menjadi 21,53±2,7 (cmol(+)/kg), dan secara umum nilai kation basa ditukarpun mengalami penurunan yaitu pada Mg 22,30±3,07 (cmol(+)/kg), K 4,18±0,85 (cmol(+)/kg), dan Na 46,48±14 (cmol(+)/kg).
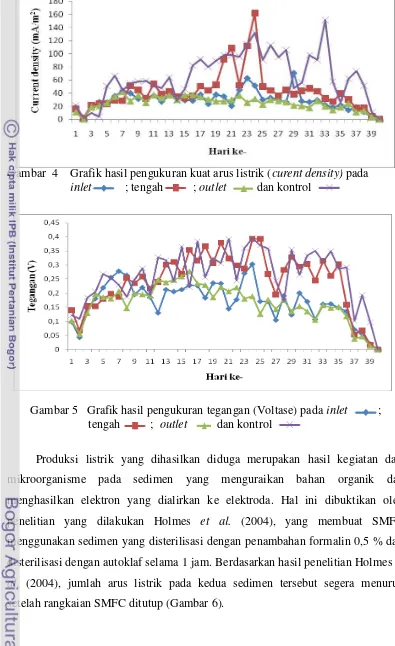
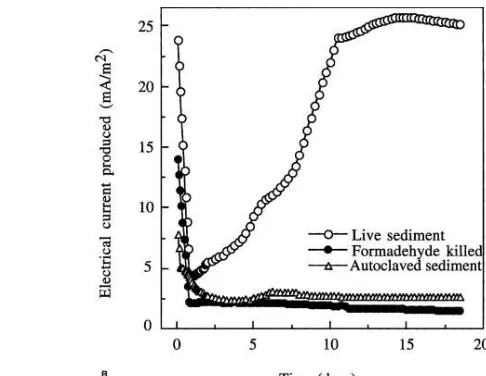
SMFC dengan substrat sedimen tambak udang dapat menghasilkan arus listrik yang mencapai puncak produksi arus listrik pada hari ke-24, yaitu ~161,99 mA/m2dan tegangan sebesar ~0,39 V.
DAN PEMANFAATANNYA SEBAGAI PENGHASIL ENERGI
LISTRIK PADA SEDIMEN TAMBAK UDANG MELALUI
SEDIMENT MICROBIAL FUEL CELL
YAYAN FIRMANSYAH C34062363
Skripsi
sebagai salah satu syarat untuk memperoleh gelar Sarjana Perikanan pada fakultas Perikanan dan Ilmu Kelautan
Institut Pertanian Bogor
DEPARTEMEN TEKNOLOGI HASIL PERAIRAN
FAKULTAS PERIKANAN DAN ILMU KELAUTAN
INSTITUT PERTANIAN BOGOR
BOGOR
PERNYATAAN MENGENAI SKRIPSI DAN SUMBER INFORMASI
Dengan ini saya menyatakan bahwa skripsi yang berjudul ”Degradasi Bahan Organik dan Pemanfaatannya sebagai Penghasil Energi Listrik pada Sedimen Tambak Udang melalui Sediment Microbial Fuel Cell” adalah karya saya sendiri dan belum diajukan dalam bentuk apapun pada perguruan tinggi manapun. Sumber informasi
yang dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain
telah disebutkan dalam teks dan dicantumkan dalam daftar pustaka di bagian akhir
skripsi ini.
Bogor, Juli 2011
Judul Penelitian : Degradasi Bahan Organik dan Pemanfaatannya sebagai Penghasil Energi Listrik pada Sedimen Tambak Udang melalui Sediment Microbial Fuel Cell
Nama Mahasiswa : Yayan Firmansyah
NRP : C34062363
Menyetujui :
Pembimbing I Pembimbing II
Bambang Riyanto, S.Pi. M.Si Dr. Akhiruddin Maddu NIP. 19690603 199802 1001 NIP. 19660907 199802 1006
Mengetahui,
Ketua Departemen Teknologi Hasil Perairan
Dr. Ir. Ruddy Suwandi, MS., M.Phil NIP. 19580511 198503 1 002
KATA PENGANTAR
Puji syukur penulis panjatkan kehadirat Allah SWT, karena berkat rahmat serta
hidayah-Nya, penulis dapat menyelesaikan skripsi ini dengan baik. Skripsi ini
mengambil judul ”Degradasi Bahan Organik dan Pemanfaatannya sebagai Penghasil Energi Listrik pada Sedimen Tambak Udang melalui Sediment Microbial Fuel Cell”. Penelitian ini merupakan salah satu syarat untuk memperoleh gelar sarjana pada
Departemen Teknologi Hasil Perairan, Fakultas Perikanan dan Ilmu Kelautan,
Institut Pertanian Bogor.
Penulis menyampaikan rasa terimakasih kepada :
1. Bapak Bambang Riyanto, S.Pi, M.Si dan Bapak Dr. Akhiruddin Maddu selaku
dosen pembimbing, atas segala bimbingan dan pengarahan yang diberikan
kepada penulis.
2. Bapak Dr. Ir. Tatag Budiardi, M.Si selaku dosen penguji, atas segala saran dan
masukannya yang diberikan kepada penulis.
3. Bapak Dr. Ir. Agoes M. Jacoeb, Dipl Biol sebagai komisi pendidikan
Departemen Teknologi Hasil Perairan.
4. Keluarga terutama Ibunda, Almarhum Ayah tercinta, Adikku Novi Fajriani, dan
kakaku Asep Gunawan, keluarga Dewi K Indiana yang telah memberikan
semangat dan membantu penulis dalam menyelesaikan kuliah dan penyusunan
skripsi ini.
5. Dosen dan Staf THP, Laboran THP (Ibu Ema, Lastri, Mas Zaky dan Mas Ipul)
dan Laboran Balai Tanah Bogor (Ibu Nurjanah) atas bantuan dan kerjasama
selama penelitian berlangsung.
6. Rizky Chairunisah atas semangat, perhatian, kesetiaan dan bantuannya kepada
penulis selama penelitian dan penyususnan skripsi ini.
7. Teman-teman satu bimbingan “Tim Smart”, Supri, Ratna dan Cece, terimakasih atas kebersamaan dan bantuannya dalam satu bimbingan.
8. Teman-teman PKMP (Fitriani Idham, Abdul Basir, Rizky Chairunisah, Dini
Aulia dan Dianita), Wahyu Ramadhan, Reza, Uty, Rizal, Adi, Nabila, Nadya,
Cen-cen, Linda, Pak Budi dan Mas Tedi yang telah memberikan saran dan
9. Teman-teman THP 43, 44, 45 dan 46, terimakasih atas kebersamaannya selama
di THP tercinta.
Penulis menyadari bahwa dalam penulisan skripsi ini masih banyak
kekurangannya. Oleh karena itu kritik dan saran yang bersifat membangun sangat
diharapkan, dalam proses penyempurnaan skripsi ini.
Bogor, Juli 2011
RIWAYAT HIDUP
Penulis dilahirkan di Subang, pada tanggal 19 Agustus 1987,
yang merupakan anak kedua dari tiga bersaudara pasangan
Bapak Alm. Awing dan Ibu Yati. Penulis memulai jenjang
formal di Sekolah Dasar Negeri Kertamukti Desa Jayamukti
Kecamatan Blanakan dan lulus pada tahun 2000. Kemudian
melanjutkan ke Sekolah Menegah Pertama Negeri 1 Blanakan
dan lulus pada tahun 2003 serta Sekolah Menengah Atas di
SMA Negeri 1 Subang dan lulus pada tahun 2006.
Pada tahun 2006 penulis diterima di IPB melalui jalur Undangan Seleksi
Masuk Institut Pertanian Bogor (USMI). Penulis diterima di Departemen Teknologi
Hasil Perairan, Fakultas Perikanan dan Ilmu Kelautan, dengan minor Manajemen
Fungsional Pemasaran, Institut Pertanian Bogor. Selama menjalani pendidikan
akademik di IPB penulis pernah aktif sebagai Wakil Ketua Himpunan Profesi
Teknologi Hasil Perikanan (HIMASILKAN) tahun 2008, dan Badan Pengawas
Himpunan Profesi Teknologi Hasil Perikanan (HIMASILKAN) tahun 2009. Ketua
Gerakan Makan Ikan (GMI) tahun 2009. Asisten Praktikum mata kuliah Avertebrata
Air (2008), sebagai Koordinator Asisten Praktikum mata kuliah Avertebrata Air
(2009) dan Koordinator Asisten Praktikum Mata Kuliah Teknologi Produk
Tradisional Hasil Perairan. Selain itu penulis juga aktif dalam kegiatan yang bersifat
prestatif, diantaranya penyaji PIMNAS bidang PKMK ke XXII – UNIBRAW Malang 2009, juara setara emas poster PIMNAS ke XXII – UNIBRAW Malang 2009, juara II teater se-Bogor TETRANOLOGI 2009.
Sebagai salah satu syarat meraih gelar sarjana, penulis melakukan penelitian yang berjudul “Degradasi Bahan Organik dan Pemanfaatannya sebagai Penghasil Energi Listrik pada Sedimen Tambak Udang melalui Sediment Microbial Fuel
DAFTAR ISI
3.3.1 Penentuan lokasi pengambilan sampel ... 12
3.3.2 Pengukuran kualitas air tambak udang serta analisis karakterisasi sedimen tambak udang ... 13
3.3.3 Pembuatan rangkaian SMFC ... 13
3.3.4 Pengukuran arus listrik dan tegangan SMFC tambak ... 14
3.3.5 Karakterisasi substrat SMFC ... 15
3.4 Prosedur Pengujian ... 15
3.4.1 Penentuan tekstur tanah dengan metode pipet... 15
3.4.2 Pengukuran pH ... 17
3.4.3 Pengukuran daya hantar listrik ... 17
3.4.4 Penetapan C-organik ... 17
3.4.5 Penetapan N ... 18
3.4.6 Penetapan P-tersedia ... 18
3.4.6 Penetapan kapasitas tukar kation dan kation basa ... 19
4 HASIL DAN PEMBAHASAN ... 20
4.1 Kualitas Air Tambak Udang Desa Jayamukti ... 20
4.2 Karakterisasi Sedimen Tambak Udang Desa Jayamukti Blanakan .. 22
4.4 Karakteristik Substrat SMFC Tambak Udang Desa Jayamukti ... 31
5 KESIMPULAN DAN SARAN ... 35
5.1 Kesimpulan ... 35
5.2 Saran ... 35
DAFTAR PUSTAKA ... 36
DAFTAR TABEL
Halaman
1 Kualitas air tambak udang desa Jayamukti ... 20
2 Karakteristik sedimen tambak Desa Jayamukti Blanakan ... 23
3 Karakteristik substrat SMFC sedimen tambak udang di Desa
DAFTAR GAMBAR
Halaman
1 Microbial Fuel cell ... 8
2 Model produksi listrik MFC pada sedimen laut ... 9
3 Susunan SMFC ... Error! Bookmark not de
4 Grafik hasil pengukuran kuat arus listrik ... 29
5 Grafik hasil pengukuran tegangan ... 29
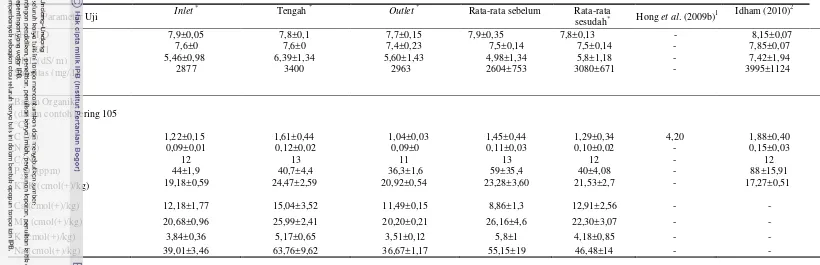
6 Produksi arus listrik pada sedimen hidup dan sedimen steril yang
dilakukan Holmes et al (2004) ... 30
7 Perubahan warna sedimen tambak udang ... 31
8 Persentase kandungan karbon organik pada sedimen sebelum dan setelah 40 hari pengukuran ... 33
9 Persentase kandungan nitrogen total pada sedimen sebelum dan setelah 40 hari pengukuran ... 34
DAFTAR LAMPIRAN
Halaman
1 Letak pengambilan sedimen tambak di Desa Jayamukti ... 43
2 Pengukuran kualitas air tambak ... 44
3 Pengukuran arus listrik dan tegangan, serta rangkaian SMFC ... 45
4 Data pengukuran arus listrik ... 46
5 Data pengukuran tegangan ... 47
6 Data hasil pengujian sedimen tambak udang Desa Jayamukti Kecamatan Blanakan di Balai Tanah Bogor (sebelum dirangkaikan dengan SMFC) ... 48
7 Data hasil pengujian karakteristik substrat SMFC tambak udang Desa Jayamukti (setelah dirangkaikan SMFC)... 49
1 PENDAHULUAN
1.1 Latar Belakang
Peningkatan produksi udang dunia dan perkembangan perdagangan udang
global selalu diiringi dengan berbagai isu dan permasalahan besar dalam
budidaya. Pencemaran tambak akibat sisa pakan, treatment kimia dan antibiotik,
dan perkembangan penyakit, merupakan contoh kasus dalam budidaya udang
yang sering muncul (Ahn et al. 2010). Budidaya udang juga disinyalir
menimbulkan hilangnya keanekaragaman hayati, menurunnya kualitas tanah,
pemanasan global, pencemaran air, serta kontaminasi sedimen tambak pada
lingkungan sekitar (Bergheim & Asgard 1996).
Jackson et al. (2003) menyampaikan bahwa hampir 90% sumber protein
pada perairan tambak berasal dari pelet, dimana 22% dikonversi menjadi
biomassa udang, 7% dimanfaatkan oleh aktifitas mikroorganisme, 14%
terakumulasi pada sedimen dan 57% tersuspensi di air tambak. Limbah organik
yang terbuang ini dapat menyebabkan ledakan plankton dan masalah kekurangan
oksigen pada perairan, peristiwa ini dikenal sebagai pembusukan di perairan.
Apabila pembusukan tidak berlangsung lancar, maka akan terjadi penumpukan
amonia sampai pada konsentrasi yang membahayakan udang dan hewan air
lainnya. Secara umum produksi amonia yang berasal dari ekskresi dan
pembusukan kotoran udang dan sisa pakan di tambak udang bervariasi antara
4,5% - 5,5% dari biomassa udang yang diproduksi (Chàvez-Crooker dan
Obreque-Contreras 2010).
Avnimelech dan Ritvo (2001) menjelaskan bahwa tingkat pemberian pakan
yang tinggi tersebut akan mengakibatkan peningkatan hasil-hasil metabolisme
udang dan dekomposisi bahan-bahan organik pada sedimen tambak menjadi
sebesar 10.000-200.000 mg/kg. Kemudian Boyd (2000), menyampaikan bahwa
oksidasi dari sulfida akan menghasilkan asam sulfat yang dapat menyebabkan
kondisi lingkungan tambak menjadi asam (pH 4-5,5), sehingga dapat
membahayakan kondisi udang. Selanjutnya Avnimelech dan Rivto (2003)
menambahkan bahwa bahan organik yang mengandung nitrogen dapat digunakan
mengakibatkan berkurangnya oksigen dalam tambak dan menyebabkan
meningkatnya permintaan oksigen pada sedimen (Sediment Oxygen
Demand/SOD) dari rata-rata 0,06 g O2 m-2 h-1 menjadi 0,24 g O2 m-2 h-1 dalam
3 minggu. Yuvanatemya (2007) lebih lanjut menyampaikan bahwa tingginya
bahan organik (10-100 mg/kg pada air tambak dan 10.000-200.000 mg/kg pada
sedimen tambak) dapat mengakibatkan blooming alga, yang berakibat pada
kematian massal udang secara mendadak. Secara praktis, Lemonnier dan Brizard
(2001) menyampaikan bahwa penumpukan bahan organik pada sedimen tambak
telah mengakibatkan penurunan tingkat kelangsungan hidup udang dari 60%
menjadi 10%.
Bahan organik di dasar akan meningkat seiring dengan masa pemeliharaan
udang, karena adanya penambahan hasil ekskresi dan sisa pakan yang tidak
dibuang seluruhnya ke luar tambak. Besarnya limbah yang dibuang dan masuk ke
perairan bergantung pada luas tambak yang dioperasikan dan jenis teknik
budidaya yang digunakan serta kemampuan peraiaran melakukan pengenceran
melalui arus pasang surut di perairan (Chàvez-Crooker dan Obreque-Contreras
2010).
Selain itu, pencemaran pada sedimen tambak dapat terjadi karena adanya
residu kimia, seperti antibiotik dan pestisida. Graslund et al. (2003) mencatat
bahwa petambak udang di Thailand, rata-rata menggunakan 13 jenis bahan kimia,
4 pestisida dan disinfektan, dan 3 produk untuk peningkatan kualitas tanah dan air
tambak. Penggunaan antibiotik ini disinyalir oleh Boyd et al. (2000) akan
mengakibatkan resistensi bakteri patogen dan mengubah komposisi komunitas
bakteri pada sedimen tambak, sehingga mengakibatkan perubahan proses
biogeokimia.
Selama masa budidaya, bahan organik yang terakumulasi pada sedimen
biasanya diberi perlakuan agar dapat menghilangkan racun dan bahan yang tidak
diinginkan. Manajemen tambak yang umum dilakukan adalah dengan cara
pengeringan dan pengapuran (kalsifikasi) serta penyiponan. Selain itu
dikembangkan pula teknik-teknik modern, seperti bioremediasi (Thomas et al.
1992), probiotik (Wang and Hang 2007), minimal water exchange system
Boyd (2000) menyampaikan bahwa pengeringan dasar tambak dilakukan
untuk mempercepat degradasi bahan organik, sedangkan pengapuran dilakukan
untuk menetralkan keasaman dan aktivitas mikrobial. Sedangkan bioremediasi
secara umum adalah proses pembersihan pencemaran tanah dengan menggunakan
mikroorganisme (jamur, bakteri). Aiyushirota (2009) menyampaikan bahwa pada
dasarnya bioremediasi pada tambak digunakan untuk meningkatkan kesuburan
tambak, dan teknologi ini lebih baik jika diterapkan pada tahap persiapan tambak.
Sedangkan probiotik dalam sistem budidaya udang merupakan penambahan ke
dalam lingkungan tambak berupa jenis-jenis bakteri non patogenik (tidak
menyebabkan penyakit) yang bertujuan untuk perbaikan mutu tambak. Menurut
Thomas et al. (1992), beberapa spesies bakteri yang dipakai dalam probiotik
adalah Bacillus, Pseudomonas, Acinetobacter, Cellulomonas, Rhodoseudomonas,
Nitrosomonas, dan Nitrobacter, yang diduga dapat membantu proses mineralisasi
limbah organik. Aplikasi probiotik pada dasar tambak menurut laporan Wang and
Han (2007) dapat mempercepat dekomposisi limbah organik, namun Hariati
(2008) menyampaikan bahwa konsep probiotik ini memiliki kelemahan, yaitu:
kemampuan bertahan, kolonisasi, kompetisi nutrien dari bakteri probiotik ini
cukup bervariasi untuk masuk ke dalam satu lingkungan ekosistem yang sudah
mengandung beberapa ratus jenis spesies bakteri lainnya.
Minimal water exchange system merupakan suatu metode yang digunakan
dalam manajemen penanganan limbah air tambak dengan cara penggantian air
yang minimal, terutama di 60 hari pertama masa budidaya. Penggantian air hanya
untuk mengganti penyusutan air karena penguapan dan rembesan di bulan
pertama budidaya. Volume penggantian air maksimal 5% per hari. Minimal water
exchange system hanya mampu membuang akumulasi bahan organik yang ada
pada perairan tambak, sedangkan bahan organik yang terakumulasi pada sedimen
tetap mengendap dan tidak terbuang, sehingga hal ini dapat membahayakan
komoditas budidaya dalam tambak (Aiyushirota 2009).
Adapun teknologi lain yang sering digunakan dalam memperbaiki masalah
tambak adalah bioflok. Bioflok merupakan teknologi budidaya yang didasarkan
pada prinsip assimilasi nitrogen anorganik (ammonia, nitrit dan nitrat) oleh
oleh organisme budidaya sebagai sumber makanan (Kuhn et al. 2010). Lumpur aktif dapat diibaratkan sebagai „sup mikroba‟ yang terbentuk dari pemberian aerasi secara terus-menerus pada biomassa tersuspensi dan mikroorganisme
pengurai dalam limbah cair. Teknik ini mencoba untuk mengolah limbah
budidaya secara langsung di dalam petak budidaya dengan mempertahankan
kecukupan oksigen, mikroorganisme, dan rasio C/N dalam tingkat tertentu
(Kuhn et al. 2010). Penggunaan teknik ini di Indonesia pada budidaya Vannamei
mampu menurunkan feeding convertion rate sebesar 20% dan menghasilkan
50 ton udang/ha dengan panen bertahap (Aiyushirota 2009). Aiyushirota (2009)
menyampaikan bahwa komposisi mikroorganisme pada bioflok terdiri dari bakteri
70% dan plankton 30%. Penggunaan bioflok di Indonesia belum ideal, karena
persyaratan lingkungan tambak intensif belum terpenuhi (kepadatan tebar yang
baik 80 sampai 120 ekor per m2 dengan sistem tertutup). Ditambahkan, bahwa
bioflok akan lebih efektif pada tambak dengan dasar plastik atau semen, selain itu
air tambak harus selalu berputar. Hal ini menyebabkan dalam aplikasinya,
teknologi bioflok harus menggunakan kincir air lebih banyak (1 kincir untuk 30
kg biomassa), sehingga menuntut penggunaan listrik yang lebih besar.
Biofuel cell secara umum terdiri dari microbial fuel cell (MFC) dan
enzimatik fuel cell (Hong et al. 2008). Penggunaan mikroba dalam fuel cell ini
menggantikan fungsi dari enzim, sehingga dihasilkan substrat yang lebih murah
(Shukla et al. 2004a). Sediment microbial fuel cell (SMFC) merupakan salah satu
model dari MFC (Hong 2009a). Prinsip kerja dari SMFC ini sangat sederhana,
yaitu menempatkan dua elektroda yang saling terhubung, yaitu anoda pada
sedimen yang bersifat anaerobik dan katoda pada badan air yang mengandung
oksigen terlarut (Lovley 2006). Secara mekanisme, SMFC dilakukan dengan
memanfaatkan mikroorganisme yang terdapat pada sedimen untuk mendegradasi
bahan organik dan menghasilkan elektron yang ditransfer ke anoda kemudian
dialirkan melaui sirkuit eksternal sebelum bereaksi dengan penerima elektron di
katoda (Chae et al. 2008 & Pant et al. 2010).
Kajian pada bidang perikanan, MFC telah dikembangkan sebagai teknologi
dalam pengolahan limbah hasil perikanan (You 2009) dan mengurangi tingkat
pengembangan SMFC pada perairan saat ini adalah telah dicobakan berbagai jenis
sedimen, antara lain sedimen estuaria dari dekat Pantai Raritan USA dan sedimen
rawa asin dari Tuckerton USA (Reimers et al. 2001), sedimen Danau Ilgam Seoul
(Hong et al. 2008), sedimen Sungai Gongji (Hong et al. 2009a), sedimen Danau
Sihwa (Hong et al. 2009b), sedimen laut Teluk Jakarta (Idham 2010), sedimen
Danau Hussain Sagar Hyderabad dan sedimen Sungai Uppal Hyderabad (Mohan
et al. 2009), serta sedimen laut Pelabuhan Boston (Holmes et al. 2004). SMFC ini
ternyata dapat menurunkan bahan organik yang terkandung dalam sedimen, pada
penelitian Hong et al. (2008) kandungan karbon organik pada sedimen Danau
Ilgam Seoul mengalami penurunan setelah dirangkaikan dengan SMFC dari
3,52% menjadi 2,37%, sedangkan pada penelitian Hong et al.(2009b) kandungan
karbon organik pada sedimen Danau Sihwa Korea mengalami penurunan setelah
dirangkaikan dengan SMFC dari 6,4% menjadi 4,20%. Pada penelitian Idham
(2010), bahan organik pada sedimen laut Teluk Jakarta mengalami penurunan
setelah dirangkaikan dengan SMFC, masing-masing karbon organik (dari
2,19±0,44% menjadi 1,88±0,07%), nitrogen total (dari 0,19±0,06% menjadi
0,15±0,03), dan fosfor (dari 128±4,95% menjadi 88±15,91%).
Sediment Microbial Fuel Cell (SMFC) sebagai teknologi baru proses
percepatan penurunan kadar akumulasi bahan organik pada tambak udang belum
pernah dikembangkan. Selain itu diharapkan, SMFC dapat dikembangkan pula
untuk menghasilkan energi listrik. Secara teoritis menurut Logan (2008), energi
listrik yang dihasilkan dari SMFC, ditimbulkan dari proses degradasi bahan
organik oleh mikroorganisme melalui reaksi katalitik atau melalui mekanisme
sistem bioelektrokimia dari mikroorganisme. Oleh karena itu, penelitian untuk
mempelajari fungsionalisasi kualitas sedimen tambak udang dengan menggunakan
teknologi SMFC menjadi sangat penting untuk dilakukan.
1.2 Tujuan
Tujuan dari penelitian ini adalah menganalisis penurunan akumulasi bahan
organik dan energi listrik yang dihasilkan pada sedimen tambak udang melalui
2 TINJAUAN PUSTAKA
2.1 Pencemaran Sedimen Tambak
Sedimen merupakan bagian terpenting dalam usaha budidaya udang.
Keadaan sedimen akan mempengaruhi kualitas air tambak hasil produksi
(Boyd 2000). Menurunnya kondisi kualitas air dan sedimen dasar tambak akibat
meningkatnya akumulasi bahan organik dan timbulnya senyawa toksik seperti
amonium dan nitrit merupakan salah satu faktor penyebab penurunan produksi
udang. Garno (2004), mengemukakan bahwa akumulasi bahan organik pada
sistem tambak udang sudah dapat dideteksi sejak awal masuknya pakan buatan
(pelet) ke dalam sistem tambak tersebut, dan kegagalan budidaya udang lebih
diakibatkan oleh pencemaran organik yang terakumulasi di sedimen tambak dari
pada akibat pencemaran yang berasal dari luar sistem tambak. Menurut Sabar dan
Widiyanto (1998), peningkatan bahan organik pada tambak semi intensif terjadi
mulai hari ke-60, diawal operasional konsentrasi bahan organik pada sedimen
tambak sebesar 41,0 mg/L dan setelah 60 hari operasional konsentrasinya
meningkat menjadi 140 mg/L, yang terdiri dari unsur nitrogen, fosfat, dan sulfur.
Meningkatnya konsentrasi senyawa toksik amonium dan nitrit di tambak
merupakan faktor penghambat dalam budidaya udang. Senyawa-senyawa
toksik tersebut diproduksi oleh aktifitas mikroba dan hasil ekskresi udang yang
dibudidayakan. Amonia dihasilkan oleh bakteri amonifikasi dan senyawa nitrit
diproduksi dari proses reduksi nitrat oleh bakteri denitrifikasi. Nitrit juga berupa
senyawa intermediat dari proses nitrifikasi. Senyawa amonium dan nitrit bersifat
toksik bila konsentrasinya sudah melebihi ambang batas. Konsentrasi senyawa
toksik di tambak udang umumnya menunjukkan peningkatan pada hari ke-15
setelah udang ditebar, yaitu untuk amonium di sedimen mencapai 500 µM, total
nitrat dan nitrit mencapai 15 µM, sedangkan konsentrasi nitrogen organik terlarut
pada hari ke tiga sudah mencapai sekitar 100 –120 µM (Burford et al. 2002). Meningkatnya konsentrasi amonium bersifat toksik pada sistem tambak
udang, walaupun mekanisme toksisitasnya belum diketahui dengan jelas akan
tetapi terlihat keterkaitan antara jumlah amonia dan aktifitas fisiologis udang,
et al. 1985). Sedangkan senyawa nitrit bersifat toksik dan akan menghambat
proses pengikatan oksigen oleh hemoglobin di dalam darah. Apabila senyawa
nitrit diikat oleh darah akan terbenbentuk methemoglobin (Hb + NO2 = Met-Hb),
dan darah yang mengandung Met-Hb berwarna coklat (brown blood diseases)
(Boyd, 1990).
2.2 Microbial Fuel Cell (MFC)
Fuel cell adalah komponen elektrokimia yang mengubah energi pada reaksi
kimia secara langsung menjadi energi listrik, air dan panas. Fuel cell memiliki
prinsip yang sama dengan baterai, namun bahan bakar dan oksidanya berada di
luar, sehingga memungkinkan fuel cell dioperasikan terus-menerus sepanjang
reaktan terus disuplai. Salah satu fuel cell berbasis biologi adalah microbial fuel
cell. Prinsip kerja MFC mirip dengan hidrogen fuel cell, yaitu terdapat aliran
proton dari ruang anoda menuju ruang katoda melalui membran elektrolit dan
aliran elektron yang bergerak ke arah yang sama melalui kabel konduksi (Hoogers
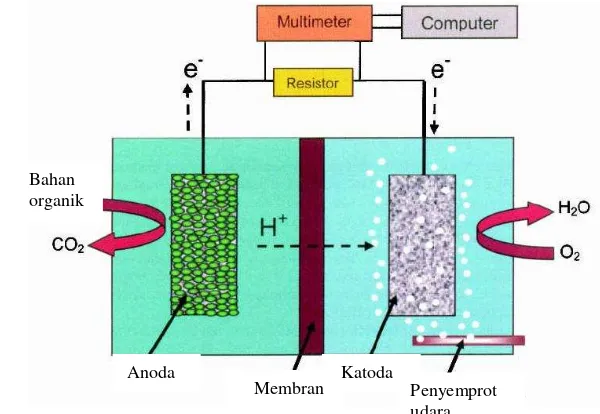
2002). Prinsip kerja microbial fuel cell secara umum dapat dilihat pada Gambar 1.
Elektron diperoleh dari substrat yang telah dioksidasi dan ditransfer ke
anoda (Reguera et al. 2005). Ada beberapa mekanisme transfer elektron dari
bakteri menuju elektroda, yaitu menggunakan mediator eksternal seperti tionin
dan neutral red yang biasanya mahal dan beracun, transfer elektron secara
langsung dari dinding bakteri ke anoda, menggunakan mediator yang dihasilkan
oleh bakteri (Rabaey dan Verstraete 2005), dan menggunakan bakteri yang dapat
menghantarkan listrik (Gorby et al. 2006). Elektron yang diterima di anoda
kemudian dialirkan melaui sirkut eksternal sebelum bereaksi dengan penerima
elektron di katoda. Berbagai kajian terakhir MFC dilakukan terhadap elektroda
(Cheng 2006a, Cheng 2006b), membran (Cheng 2006b), desain reaktor MFC (Liu
dan Logan 2004), jenis bakteri yang digunakan (Nimje et al. 2009), jenis substrat
yang digunakan (Lu et al. 2009, Moon et al. 2006) dan variasi parameter
Gambar 1 MicrobialFuel cell (Logan 2008).
2.3 Sedimen Microbial Fuel Cell (SMFC)
Sediment microbial fuel cell (SMFC) merupakan bentuk pengembangan dari
microbial fuel cell (MFC). Secara alami, mikroorganisme mengoksidasi bahan
organik yang tersedimentasi dari kolom air dan mereduksi Fe (III) atau Mn (IV).
Beberapa jenis mikroorganisme juga mendegradasi bahan organik kompleks
sehingga menghasilkan produk fermentasi (asetat), dan penerima electron
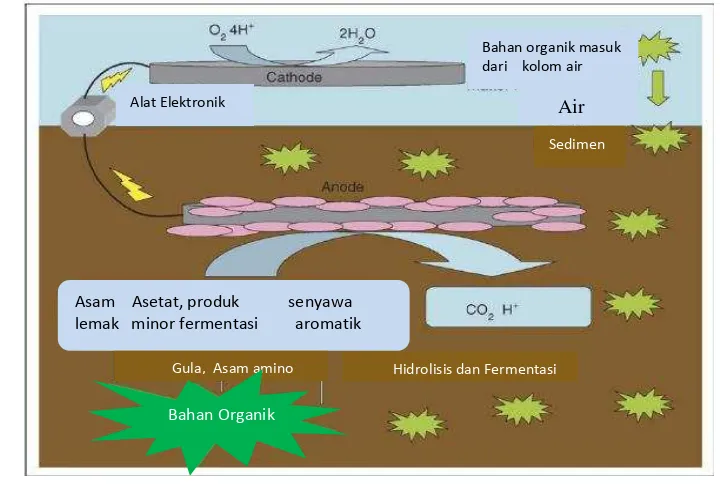
(senyawa aromatic dan asam lemak rantai panjang). Asumsi mekanisme kerja
SMFC pada sedimen laut serupa dengan rantai makanan mikroorganisme yang
menggunakan anoda (elektroda) sebagai penerima electron menggantikan Fe (III)
dan Mn (IV) (Gambar 2). Bahan
organik
Anoda Katoda
Membran Penyemprot
Gambar2 Model produksi listrik MFC pada sedimen laut (Lovley 2006).
Prinsip kerja dari SMFC yang menggunakan mikroorganisme hidup dalam
reaksi elektrokimia, menjadikan sistem MFC sangat sensitif terhadap perubahan
kondisi lingkungan yang dapat membunuuh mikroorganisme tersebut (Mench
2008). Struktur dan aktivitas mikroorganisme dipengaruhi oleh berbagai
parameter yaitu suhu, pH, potensial redoks, dan kekuatan ion (Torres et al. 2008).
Liu et al. (2005) juga menyatakan bahwa kinerja SMFC secara umum
tergantung dari komponen-komponen penyusunnya, yang meliputi jenis dan
struktur elektroda, ada atau tidaknya membrane penukar proton, serta kelengkapan
membrane. Jenis bahan dan struktur anoda berdampak pada penempelan
mikroorganisme, transfer electron, dan oksidasi substrat. Bahan yang biasa
digunakan sebagai anoda adalah karbon (carbon cloth atau graphite felt) karena
stabil terhadap kultur mikroba, memiliki konduktivitas yang tinggi, dan luas
permukaan yang besar (Watanabe 2008). Namun penggunaan elektroda berbasis
karbon pada katoda akan mengakibatkan ketidakefisienan (Kim et al. 2002),
sehingga perlu dilakukan pelapisan dengan katalis, misalnya platinum
(Pham et al.2004).
Kondisi lingkungan seperti konduktivitas, juga mempengaruhi kinerja dari
SMFC. Air laut memiliki konduktivitas listrik yang tinggi dibandingkan air
sungai, yaitu ∼50,000 dan 500 S/cm pada 20 °C. Oleh karena itu, SMFC dengan
Air
Alat Elektronik
Bahan organik masuk dari kolom air
Sedimen
Asam Asetat, produk senyawa lemak minor fermentasi aromatik
Hidrolisis dan Fermentasi Gula, Asam amino
menggunakan air laut dapat menghasilkan energi yang lebih besar dibandingkan
dengan menggunakan air sungai (tawar). Produksi listrik pada SMFC juga
ditentukan oleh jenis katalis pada katoda, bahan yang digunakan pada elektroda,
3 METODE
3.1 Waktu dan Tempat
Penelitian ini dilaksanakan pada bulan Februari 2011 sampai bulan Juni
2011 di Tambak Udang Desa Jayamukti, Kecamatan Blanakan, Subang-Jawa
Barat, Laboratorium Bahan Baku dan Laboratorium Biokimia, Departemen
Teknologi Hasil Perairan Fakultas Perikanan dan Ilmu Kelautan, Institut Pertanian
Bogor serta Balai Penelitian Tanah Bogor.
3.2 Bahan dan Alat
Bahan yang digunakan dalam penelitian ini adalah bahan untuk treatment
elektroda pada rangkaian SMFC meliputi HCl 1N, NaOH 1N, akuades, dan air
tambak. Bahan-bahan yang digunakan untuk pengujian karakteristik sedimen
SMFC adalah akuades, air bebas ion, air bebas ion yang bebas CO2, NaCl, KCl,
HCl, larutan ekstraksi Olsen 20 ml, carbon hitam, amonium asetat, kalium
dikromat, larutan standar 5000 ppm C, etanol 96%, pasir kuarsa bersih, filter pulp,
larutan buffer pH 7,0 dan pH 4,0.
Alat-alat yang digunakan meliputi peralatan untuk pengambilan sedimen dan
air tambak yang terdiri dari botol, tali, plastik ukuran 5 kg, alat tulis, kertas label
dan Eikmann Grab volume 1 liter. Peralatan yang digunakan dalam pembuatan
rangkaian dan pengukuran arus serta tegangan dari SMFC adalah gelas ukur 500
ml, multimeter (Masda DT830D), elektroda karbon grafit (berbentuk silinder
dengan dimensi (39 x 7 mm), resistor 560 Ω ± 5% dan kabel N.Y.A ETERNA (1 x 2,5mm). Alat-alat yang digunakan untuk menganalisis kualitas air tambak
meliputi pH meter (kertas lakmus), alat portable waterproof dissolved oxygent
meter (HI 9142) refraktometer (Milwaukee MR 100 ATC Salinity Refractometer),
keping secci disc. Alat-alat yang digunakan untuk analisis fisika kimia sedimen
tambak meliputi oven, desikator, destilator, freeze dried (Freeze dryer ALPHA
3.3 Prosedur Penelitian
Pelaksanaan penelitian ini dilakukan dalam beberapa tahapan. Tahap
pertama adalah penentuan tempat pengambilan sampel dan kondisi tempat
pengambilan sampel sedimen pada tambak udang (Ghangrekar et al. 2003). Tahap
kedua adalah pengukuran kualitas air tambak udang serta analisis karakterisasi
sedimen tambak udang yang ada (mengacu Hong et al. 2009). Tahap ketiga
adalah berupa pembuatan rangkaian SMFC yang mengacu pada penelitian
Holmes et al.(2004). Tahap keempat adalah pengukuran arus listrik dan tegangan
yang dihasilkan SMFC dengan menggunakan multimeter masda DT830D
(Holmes et al. 2004). Tahap kelima adalah karakterisasi pada substrat hasil dari
proses degradasi bahan organik melalui SMFC (Hong et al. 2009), sehingga dapat
dilihat adanya perubahan terhadap kadar akumulasi bahan organik pada sedimen
tambak udang tersebut.
3.3.1 Penentuan lokasi pengambilan sampel
Tambak yang dijadikan tempat pengambilan sampel merupakan satu petak
tambak udang milik warga (perorangan/rakyat) dengan produktivitas yang sangat
rendah (ketetapan tersebut berdasarkan informasi dari kelompok petani tambak
Desa Jayamukti). Lokasi tambak ini sangat dekat dengan aliran sungai sebagai
sumber air laut dan air tawar. Pengambilan dilakukan pada 3 stasiun (stasiun I
pada daerah air masuk atau inlet, stasiun II di tengah tambak, stasiun III pada
sekitar saluran pembuangan air atau outlet), masing-masing stasiun dilakukan
pengambilan kembali (ulangan) sebanyak 3 kali pada area yang berlainan
(Ghangrekar et al. 2003). Gambaran lokasi dapat dilihat pada Lampiran 1.
Pengambilan sedimen dilakukan pada dasar tambak dengan kedalaman
± 130 cm menggunakan alat Eikmann Grab volume 1 liter. Sedimen yang telah
diambil selanjutnya langsung dimasukkan ke dalam polybag dengan kondisi
sampel masih terendam air. Kondisi lain yang dilakukan adalah udara yang masih
terdapat di dalam polybag dikeluarkan terlebih lalu, baru kemudian diikat rapat
(Idham 2010). Semua sampel sedimen dan air tambak, selanjutnya disimpan pada
cool box agar suhu sampel terjaga untuk kemudian dibawa ke laboratorium untuk
3.3.2 Pengukuran kualitas air tambak udang serta analisis karakterisasi sedimen tambak udang
Pengukuran parameter fisik terhadap kualitas air tambak, yaitu : suhu, DO,
pH, salinitas dan kecerahan (BSN 2009), dilakukan di lapangan pada pukul 10.00
WIB. Pengukuran suhu air tambak dilakukan dengan menggunakan termometer
pada tiga titik (inlet, tengah dan oulet) masing-masing tiga kali ulangan.
Pengukuran dissolved oxigen (DO) air tambak dilakukan dengan menggunakan
alat portable waterproof dissolved oxygent meter (HI 9142) pada tiga titik (inlet,
tengah dan oulet) masing-masing tiga kali ulangan. Pengukuran pH air tambak
dilakukan dengan menggunakan kertas lakmus pada tiga titik (inlet, tengah dan
oulet) masing-masing tiga kali ulangan. Pengukuran salinitas air tambak
dilakukan dengan menggunakan refraktometer pada tiga titik (inlet, tengah dan
oulet) masing-masing tiga kali ulangan. Adapun karakterisasi sedimen tambak
udang yang dilakukan mengacu pada penelitian Hong et al. (2010), yaitu tekstur
tanah, pH (H2O dan KCl), daya hantar listrik (DHL), jumlah karbon organik,
jumlah nitrogen total, fosfor tersedia (BSN 2009), kapasitas tukar kation (KTK),
K dapat ditukar (K dd), Ca dapat ditukar (Ca dd), dan Mg dapat ditukar (Mg dd)
(Wignyosukarto 1998).
3.3.3 Pembuatan rangkaian SMFC
Elektroda yang digunakan untuk penyusunan SMFC adalah grafit yang
diperoleh dari baterai AA terbuang atau yang tidak terpakai lagi. Sebelum
digunakan, elektroda karbon dinetralkan dengan perlakuan yang mengacu
Holmes et al.(2004), antara lain :
1) Elektroda direndam dengan 1N HCl selama 1 hari kemudian dibilas dengan
akuades.
2) Elektroda direndam dengan 1N NaOH selama 1 hari kemudian dibilas dengan
akuades.
3) Elektroda direndam dengan akuades hingga saat akan digunakan.
Masing-masing elektroda yang telah diberi perlakuan, dilubangi dengan bor
kemudian dihubungkan dengan kabel dengan menggunakan epoxy. Keberhasilan
hasil sambungan antara elektroda dengan kabel diuji dengan mengunakan
multimeter. Pengujian hasil perangkaian elektroda dan kabel dilihat dari adanya
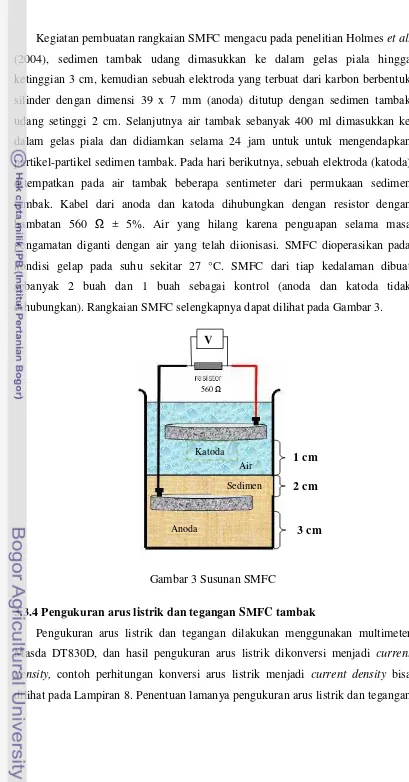
Kegiatan pembuatan rangkaian SMFC mengacu pada penelitian Holmes et al.
(2004), sedimen tambak udang dimasukkan ke dalam gelas piala hingga
ketinggian 3 cm, kemudian sebuah elektroda yang terbuat dari karbon berbentuk
silinder dengan dimensi 39 x 7 mm (anoda) ditutup dengan sedimen tambak
udang setinggi 2 cm. Selanjutnya air tambak sebanyak 400 ml dimasukkan ke
dalam gelas piala dan didiamkan selama 24 jam untuk untuk mengendapkan
partikel-partikel sedimen tambak. Pada hari berikutnya, sebuah elektroda (katoda)
ditempatkan pada air tambak beberapa sentimeter dari permukaan sedimen
tambak. Kabel dari anoda dan katoda dihubungkan dengan resistor dengan
hambatan 560 Ω ± 5%. Air yang hilang karena penguapan selama masa pengamatan diganti dengan air yang telah diionisasi. SMFC dioperasikan pada
kondisi gelap pada suhu sekitar 27 °C. SMFC dari tiap kedalaman dibuat
sebanyak 2 buah dan 1 buah sebagai kontrol (anoda dan katoda tidak
dihubungkan). Rangkaian SMFC selengkapnya dapat dilihat pada Gambar 3.
Gambar 3 Susunan SMFC
3.3.4 Pengukuran arus listrik dan tegangan SMFC tambak
Pengukuran arus listrik dan tegangan dilakukan menggunakan multimeter
Masda DT830D, dan hasil pengukuran arus listrik dikonversi menjadi current
density, contoh perhitungan konversi arus listrik menjadi current density bisa
dilihat pada Lampiran 8. Penentuan lamanya pengukuran arus listrik dan tegangan V
3 cm 2 cm 1 cm
560 Ω
Air
Sedimen
berdasarkan pada pola kecenderungan perubahan arus listrik dan tegangan yang
dihasilkan oleh penguraian bahan organik oleh mikroorganisme pada sedimen
SMFC tambak udang, dimana dalam pengukuran akan diperoleh puncak produksi
arus listrik dan penurunan arus listrik hingga akhir pengukuran (Holmes et al.
2004).
Pengukuran arus listrik dan tegangan dilakukan dengan 2 perlakuan yaitu
pengukuran arus listrik dan tegangan terhadap sedimen tambak udang yang telah
dirangkaikan dengan SMFC menggunakan multimeter yang dihubungkan secara
paralel dengan resistor (dibuat sebanyak 9 buah), dan pengukuran terhadap
kontrol yaitu terhadap sedimen tambak yang dirangkaikan SMFC dengan
menggunakan multimeter tanpa dihubungkan secara parallel dengan resistor
(dibuat sebanyak 3 buah). Konversi current density diperhitungkan dengan
membagi jumlah arus yang dihasilkan terhadap luas permukaan anoda.
3.3.5 Karakterisasi substrat SMFC
Analisis karakteristik substrat SMFC bertujuan untuk melihat perubahan
kandungan bahan organik pada sedimen tambak udang yang digunakan akibat
proses dalam SMFC. Jenis analisis yang digunakan sama dengan analisis
karakterisasi sedimen tambak udang,yaitu analisis kandungan karbon organik,
nitrogen, fosfor, pengukuran pH, daya hantar listrik (DHL), K dapat ditukar (K
dd), Ca dapat ditukar (Ca dd), dan Mg dapat ditukar (Mg dd), serta kapasitas tukar
kation (KTK) (Hong et al. 2010 dan Wignyosukarto 1998).
3.4 Prosedur Pengujian
Pengujian yang dilakukan meliputi karakteristik sedimen tambak udang dan
karakteristik substrat SMFC dari beberapa perlakuan. Pengujian meliputi
penentuan tekstur tanah metode pipet, pengukuran pH, penentuan daya hantar
listrik, penetapan C-organik Walkey & Black, penetapan jumlah N Kjeldhal,
penetapan P-tersedia Olsen, K dapat ditukar (K dd), Ca dapat ditukar (Ca dd), dan
Mg dapat ditukar (Mg dd) serta penetapan kapasitas tukar kation.
3.4.1 Penetuan tekstur tanah dengan metode pipet (Sudjadi et al. 1997)
Pengujian diwali dengan penimbangan 10 gram contoh tanah (<2 mm), yang
dibiarkan semalam. Keesokannya campuran tersebut ditambah 25 ml H2O2 30%
dan dipanaskan sampai tidak berbusa. Selanjutnya ditambahkan 180 ml air bebas
ion dan 20 ml HCl 2N kemudian dididihkan selama 10 menit. Setelah agak dingin
campuran diencerkan dengan air bebas ion menjadi 700 ml, kemudian dicuci
menggunakan penyaring Berkefield sampai bebas asam. Selanjutnya ditambah 10
ml larutan peptisator Na4P2O7 4%.
Pemisahan pasir dilakukan dengan pengayakan suspensi tanah yang telah
diberi peptisator dengan ayakan 50 mikron sambil dicuci dengan air bebas ion.
Filtrat ditampung dalam silinder 500 ml untuk pemisahan debu dan liat. Butiran
yang tertahan ayakan dipindahkan dalam pinggan alumunium yang telah diketahui
bobotnya dengan air bebas ion. Selanjutnya dilakukan pengeringan dalam oven
pada suhu 105 oC, didinginkan dalam desikator, dan ditimbang
(berat pasir = A gram). Pemisahan debu dan liat dilakukan dengan pengenceran
filtrat dalam silinder menjadi 500 ml dan diaduk selama 1 menit. Setelah itu filtrat
segera dipipet sebanyak 20 ml kedalam pinggan alumunium. Kemudian filtrat
dikeringkan pada suhu 105 oC selama semalam, didinginkan dalam desikator, dan
ditimbang (berat debu+liat+peptisator=B gram).
Pemisahan liat dilakukan dengan pengadukan lagi selama 1 menit, lalu
dibiarkan selama 3 jam 30 menit pada suhu kamar. Suspensi liat dipipet sebanyak
20 ml pada kedalaman 5,2 cm dari permukaan cairan dan dimasukkan ke dalam
pinggan alumunium, kemudian dikeringkan dalam oven pada suhu 105 oC,
didinginkan dalam desikator, dan ditimbang (berat liat + peptisator = C gram).
Penentuan jumlah pasir, debu, dan liat dilakukan berdasarkan perhitungan :
3.4.2 Pengukuran pH (Rayment & Hingginson 1992)
Pengukuran pH tanah dalam KCl dilakukan dengan penimbangan 20 gram
tanah yang dimasukkan ke dalam gelas piala. Kemudian ditambahkan 20 ml 1 N
KCl dan didiamkan selama 30 menit sambil diaduk beberapa kali. Penentuan pH
dengan menggunakan pH meter.
Pengukuran pH tanah dalam H2O dilakukan dengan penimbangan 20 gram
tanah kering yang dimasukkan pada gelas piala berukuran 50 ml, kemudian
ditambahkan 20 ml akuades dan didiamkan selama 30 menit sambil diaduk
beberapa kali. Pengukuran pH tanah dengan menggunakan pH meter.
3.4.3 Pengukuran daya hantar listrik (Rayment & Hingginson 1992)
Penimbangan 10 gram contoh tanah ke dalam botol kocok, tambahkan 50
ml air bebas ion. Kemudian botol kocok selama 30 menit. Pengukuran DHL
suspensi tanah dilakukan dengan konduktometer yang telah dikalibrasi
menggunakan larutan baku NaCl dan dibaca setelah angka konstan. Nilai DHL
dilaporkan dalam satuan dS m-1.
3.4.4 Penetapan C-organik metode Walkey & Black (Rayment & Hingginson 1992)
Penimbangan 0,5 gram tanah ukuran <0,5 mm dan dimasukkan kedalam
labu ukur 100 ml. kemudian ditambahkan 5 ml K2Cr2O7 1 N dan dikocok.
Selanjutnya ditambahkan 7,5 ml H2SO4 pekat dan dikocok lalu diamkan selama
30 menit. Larutan tersebut kemudian diencerkan dengan air bebas ion lalu biarkan
dingin dan diimpitkan. Keesokan harinya dilakukan pengukuran absorbansi
larutan jernih dengan spektrofotometer pada panjang gelombang 561 nm. Sebagai
pembanding dibuat standar 0 dan 250 ppm, dengan memipet 0 dan 5 ml larutan
standar 5.000 ppm ke dalam labu ukur 100 ml dengan perlakuan yang sama
dengan pengerjaan sampel. Penetapan C-organik dilakukan perhitungan :
C-organik (%) = ppm kurva x ml ekstrak 1.000 ml – 1 x 100 mg contoh-1xfk = ppm kurva x 100 x 1.000-1 x 100 x 500 – 1 x fk
= ppm kurva x 10 x 500 – 1 x fk Keterangan
Ppm kurva : kadar contoh yang didapat dari kurva hubungan antara kadar deret standar dengan pembacaannya setelah dikoreksi blanko.
100 : konversi ke %
3.4.5 Penetapan N metode Kjeldhal (Burt 2004)
Ke dalam labu Kjeldhal 25 ml dimasukan 0,5 gram tanah, selanjutnya
ditambahkan 1,9 gram campuran Se, CuSO4, dan NaSO4. Kemudian 5 ml H2SO4
pekat dan digoyangkan perlahan agar semua tanah terbasahi oleh H2SO4.
Campuran lalu ditetesi dengan paraffin cair sebanyak 5 tetes. Labu Kjeldhal
dipanaskan dengan api kecil kemudian secara bertahap api dibesarkan hingga
diperoleh cairan yang berwarna terang (hijau-biru). Selanjutnya ditambahkan air
sebanyak 50 ml dan dihomogenkan dengan cara digoyangkan. Setelah itu,
ditambahkan 5 ml NaOH 50%. Proses destilasi dimulai dan hasil destilat
ditampung dalam erlenmeyer yang berisi campuran 10 ml H3BO4 4% dan 5 tetes
indikator Conway. Destilasi dilakukan sampai isi destilasi mencapai 1000 ml.
Hasil destilat dititrasi dengan HCl yang telah dibakukan sampai terjadi perubahan
warna dari hijau ke merah. Penetapan N ditentukan berdasarkan perhitungan
Kadar N (%) = isi HCl (contoh-blanko) x N HCl x 14 x 100 Berat sampel x 1000 x faktor koreksi
3.4.6 Penetapan P-tersedia metode Olsen (Watanabe & Olsen 1965)
Penimbangan 1 gram tanah ukuran <0,2 mm kemudian dimasukkan dalam
botol kocok. Kemudian ditambahkan 20 ml pengekstrak Olsen dan dikocok
selama 30 menit. Selanjutnya dilakukan penyaringan. Apabila larutan keruh maka
dilakukan penyaringan kembali. Ekstrak yang didapat kemudian dipipet sebanyak
2 ml ke dalam tabung reaksi. Selanjutnya bersama deret standar ditambahkan 10
ml pereaksi pewarna fosfat dan dikocok hingga homogen. Absorbansi larutan
diukur dengan spektrofotometer pada panjang gelombang 693 nm. Penetapan
P-tersedia ditentukan berdasarkan perhitungan : deret standar dengan pembacaannya setelah dikoreksi blanko. fp : faktor pengenceran (bila ada)
142/90 : faktor konversi bentuk PO4 menjadi P2O5
3.4.7 Penetapan kapasitas tukar kation dan kation basa (Ca, K, Mg dan Na) (Burt 2004)
Penimbangan 2,5 gram tanah kering yang telah diayak kemudian
dimasukkan ke dalam tabung sentrifugasi 15 ml, selanjutnya ditambahkan 1 ml
larutan NH4OAc pH 7. Campuran dikocok sampai merata dan dibiarkan semalam.
Selanjutnya dikocok kembali lalu disentrifuse selama 10 menit dengan kecepatan
2500 rpm. Ekstrak NH4OAc didekantasi, disaring dengan saringan, dan filtrat
ditampung dalam labu ukur 100 ml. Penambahan NH4OAc diulangi sampai 3 kali.
Setiap kali penambahan diaduk merata, disentrifuse dan ekstraksinya didekantasi
ke dalam labu ukur 100 ml, setelah itu ditambahkan larutan NH4OAc. Ekstraksi
ini digunakan dalam penetapan kadar K, Na, Ca, dan Mg yang dapat
dipertukarkan serta untuk penetapan kejenuhan basa. Untuk pencucian kelebihan
NH4+ tambahkan 10 ml alkohol 80% ke dalam tabung sentrifuse yang berisi residu
tanah tersebut. Campuran tersebut diaduk sampai merata, disentrifuse,
didekantasi, dan filtratnya dibuang. Pencucian kelebihan NH4dengan alkohol ini
dilakukan sampai tanah dalam tabung sentrifuse bebas NH4. Hal ini dapat
diketahui dengan menambahkan beberapa tetes pereaksi Nessier pada filtrate
tersebut. Apabila terdapat endapan kuning berarti masih terdapat ion NH4+.
Setelah bebas dari NH4+, tanah dipindahkan secara kuantitatif dari tabung
sentrifuse ke dalam labu didih. Kemudian air ditambahkan sebanyak 450 ml
kedalam labu didih. Pada labu didih ditambahkan beberapa butir labu didih, 5-6
tetes paraffin cair dari 20 ml NaOH 50%, kemudian didestilasi. Destilat
ditampung dalam erlenmeyer 250 ml yang berisi 25 ml H2SO4 0,4 N dan 5-6 tetes
indikator Conway. Destilasi dihentikan jika destilat yang ditampung mencapai
150 ml, kelebihan asam dititrasi dengan NaOH 0,1 N. sampai dicapai warna
berubah menjadi hijau. Penetapan nilai KTK dan kation basa dihitung berdasarkan
rumus :
KTK (me/100 g) = (ml blanko – ml contoh) x N NaOH x 100 Bobot contoh tanah 105 oC
4 HASIL DAN PEMBAHASAN
4.1 Kualitas Air Tambak Udang Desa Jayamukti
Kualitas air tambak udang Desa Jayamukti yang diukur meliputi suhu,
derajat keasaman (pH), salinitas, kecerahan dan oksigen terlarut (Dissolve Oxygen
atau DO). Hasil pengukuran kualitas air tambak udang Desa Jayamukti dapat
dilihat pada Tabel 1.
Tabel 1 Kualitas Air Tambak Udang Desa Jayamukti
Parameter Satuan Hasil penelitian Standar* Optimum**
Salinitas ppm 18-20 15 – 30 15 – 25
Nilai standar untuk budidaya udang Windu Berdasarkan SNI 7310:2009 (BSN2009). **
Nilai optimum untuk budidaya udang Windu (Wignyosukarto 1998).
Salinitas air tambak udang di Desa Jayamukti berkisar anatara 18-20 ppm.
Nilai salinitas ini berdasarkan SNI 7310:2009 (BSN 2009) masih dalam kisaran
standar untuk budidaya udang (15-30 ppm), dengan nilai optimum berkisar antara
15-25 ppm (Wignyosukarto 1998). Nilai salinitas air tambak di Desa Jayamukti
tersebut masih baik untuk pertumbuhan dan kelangsungan hidup udang. Palafox
et al. (1996), menyatakan bahwa salinitas berhubungan dengan osmoregulasi
udang, dan apabila udang dipaksa untuk menyesuaikan diri di luar batas kisaran
salinitas yang optimum, maka udang akan banyak mengeluarkan energi. Apabila
terus-menerus energi ini dipakai maka energi untuk pertumbuhan udang akan
berkurang dan menyebabkan laju pertumbuhan udang menjadi rendah. Selain itu
perubahan salinitas secara cepat juga akan menyebabkan tingkat kematian udang
tinggi.
Nilai pH air pada tambak udang Desa Jayamukti berkisar antara 7,5-8,5,
nilai ini berdasarkan SNI 7310:2009 (BSN 2009) masih dalam kisaran standar
untuk budidaya udang (7,5-8,5), sehingga nilai pH tersebut masih baik untuk
pertumbuhan dan kelangsungan hidup udang. Adapun nilai pH optimum untuk
budidaya udang berkisar 8-8,5 (Wignyosukarto 1998). Kondisi perairan yang
gangguan fisiologi udang, pelunakan kulit (karapas), serta penurunan derajat
kelangsungan hidup dan laju pertumbuhan (Chien 1992). Wardoyo (1997), nilai
pH yang ideal untuk udang adalah 6,8-9,0 sedangkan pH air dengan kisaran
4,5-6,0 dan 9,8-11,0 menyebabkan terganggunya metabolisme udang bahkan dapat
menyebabkan kematian udang.
Suhu air tambak Desa Jayamukti hasil pengukuran pada pukul 10 pagi
dengan menggunakan termometer berkisar antara 29-30 oC. Nilai tersebut
berdasarkan SNI 7310:2009 (BSN 2009) masih dalam kisaran standar untuk
budidaya udang yaitu 28-32 oC, sehingga nilai suhu tersebut masih baik untuk
pertumbuhan dan kelangsungan hidup udang, sedangkan nilai suhu optimum
untuk budidaya udang berkisar 29-31 oC (Wignyosukarto 1998). Wyban et al.
(1995), menyatakan bahwa suhu air mempengaruhi reaksi kimia yang terjadi
didalam perairan dan juga reaksi biokimia yang terjadi didalam tubuh udang.
Suhu air yang optimum bagi perkembangan hidup udang adalah 28-30oC. Kisaran
suhu pada kondisi optimum konsumsi oksigen cukup tinggi sehingga nafsu makan
udang tinggi, sedangkan suhu dibawah 18-25 oC nafsu makan udang menurun.
Kecerahan perairan tambak Desa Jayamukti berkisar antara 25-30 cm, nilai
kecerahan ini berdasarkan SNI 7310:2009 (BSN 2009) masih dalam kisaran
standar untuk budidaya udang yaitu 30-45 cm, nilai kecerahan tersebut masih baik
untuk pertumbuhan dan kelangsungan hidup udang, sedangkan kecerahan
optimum untuk budidaya udang berkisar antara 30-40 cm (Wignyosukarto 1998).
Kecerahan air bergantung pada warna dan kekeruhan. Kecerahan adalah ukuran
transparasi perairan dan ditentukan secara visual dengan menggunakan keping
secchi (Jeffries dan Mils 1996 dalam Effendi 2000). Kecerahan air merupakan
fungsi dari bahan yang tersuspensi dan terkoloid dalam air, untuk perairan tambak
bahan-bahan tersebut terutama terdiri dari plankton dan bahan organik (Wardoyo
1997). Nilai kecerahan sangat dipengaruhi oleh keadaan cuaca, kekeruhan,
padatan tersuspensi, serta waktu dan ketelitian pengukuran (Effendi 2000).
Oksigen terlarut (DO) pada perairan tambak Desa Jayamukti berkisar antara
3-4 mg/l, nilai ini berdasarkan SNI 7310:2009 (BSN 2009) masih dalam kisaran
standar untuk budidaya udang yaitu >3 mg/l, nilai oksigen terlarut tersebut masih
untuk budidaya udang berkisar antara 4-7 mg/l (Wignyosukarto 1998). Kadar
oksigen terlarut bersifat fluktuatif secara harian (diurnal) dan musim bergantung
pada pencampuran (mixing) dan pergerakan (turbulence) massa air, aktivitas
fotosintesis, respirasi, dan limbah (effluent) yang masuk ke dalam air (Effendi
2000). Boyd (1991) menyatakan bahwa, kandungan oksigen terlarut yang dapat
menunjang kehidupan udang secara normal dan baik untuk pertumbuhan adalah
5 mg/l sampai konsentrasi jenuh. Lebih lanjut dinyatakan bahwa kandungan
oksigen yang kurang dari 1 mg/l dapat menyebabkan kematian jika berlangsung
selama beberapa jam, dan untuk kisaran oksigen antara 1-5 mg/l pertumbuhan
akan terganggu jika berlangsung secara terus-menerus.
4.2 Karakterisasi Sedimen Tambak Udang Desa Jayamukti Blanakan
Penilaian kesuburan tanah didasarkan pada analisis laboratorium terhadap
parameter fisik (tekstur), kimia (pH, C-organik dan N total, P, Ca, Mg, K dan Na).
Secara kimiawi, analisis kualitas tanah akan berguna untuk mengetahui antara lain
proses pertukaran ion antara tanah dengan air dan kondisi redoks yang dapat
berpengaruh terhadap ikan atau udang. Kepentingan secara biologis, tidak hanya
terkait langsung bagi kepentingan udang sendiri, namun lebih spesifik, yaitu
stimulasi dan kontinuitas dalam penyediaan hara bagi pertumbuhan plankton dan
makanan alami yang diperlukan oleh udang serta pemulihan dasar tambak oleh
komunitas bakteri serta kestabilan mutu air. Berdasarkan hasil analisis
laboratorium menunjukkan bahwa sedimen tambak udang Desa Jayamukti
Blanakan berupa tanah lumpur bewarna abu-abu kehitaman yang terdiri atas pasir
0%, debu 23,6% dan liat 76,4%. Sedimen tambak ini memiliki tekstur tanah liat.
Kandungan bahan organik sedimen tersebut meliputi karbon organik
1,45±0,32%, nitrogen 0,11±0,03% sehingga ratio C/N ialah sebesar 13,
kandungan P yang tersedia ialah 59±4,95 ppm, pH (H2O) 7,9±0,15, daya hantar
listrik (DHL) 4,98 dS/m, salinitas 2604±84 mg/l, dan kapasitas tukar kation
(KTK) 23,28±3,60 cmol(+)/kg, dan nilai kation basa ditukar Ca 8,86±1,3 (cmol(+)/kg), Mg 26,16±4,6 (cmol(+)/kg), K 5,8±16 (cmol(+)/kg), dan Na
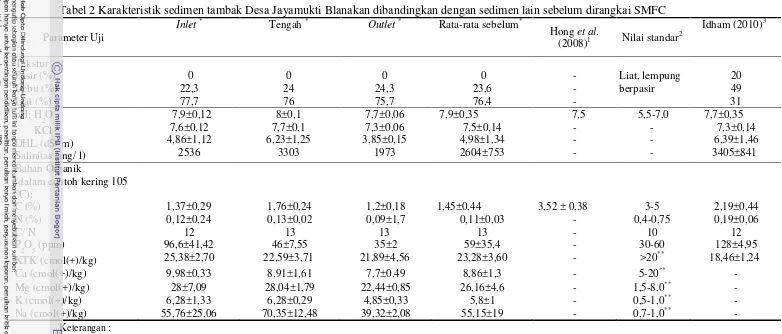
Tabel 2 Karakteristik sedimen tambak Desa Jayamukti Blanakan dibandingkan dengan sedimen lain sebelum dirangkai SMFC
Karakteristik sedimen tambak udang (inlet, tengah dan outlet) Desa Jayamukti sebelum dirangkaikan dengan SMFC berdasarkan hasil penelitian ini (diuji di Balai Penelitian Tanah, Bogor),** Nilai standar untuk budidaya udang windu berdasarkan Wignyosukarto (1998)
1
Karakteristik sedimen Danau Ilgam, Seoul berdasarkan hasil penelitian Hong et al. (2008) 2
Nilai standar untuk budidaya udang berdasarkan SNI 7310:2009 (2009) 3
Tekstur tanah merupakan variabel primer dalam penentuan kelas kesesuaian
lahan sehingga bobot yang diberikanpun juga besar. Informasi mengenai tekstur
tanah sangat penting karena tanah dengan segala aspek fisika, kimia maupun
biologi menentukan produktivitas dari suatu lahan. Berdasarkan hasil analisis
laboratorium menunjukkan bahwa sedimen tambak udang Desa Jayamukti
memiliki jenis tekstur tanah liat. Menurut Brady (1990) partikel liat merupakan
bagian terkecil dari bagian padat penyusun tanah yang memiliki diameter < 0,002
mm. Luas permukaan (8 x 106 per cm), jumlah partikel (90.260.853 x 103 per
gram) dan muatan listriknya tiap satuan massa sangat besar dibanding fraksi
penyusun tanah yang lain (pasir dan debu), sehingga memungkinkan partikel liat
ini mengikat ion-ion kimia, partikel ini merupakan koloid tanah yang dapat
menyelaputi atau bersifat perekat/semen dan butir-butir primer tanah sehingga
dapat membentuk agregat mikro yang dapat menyerap atau mengikat unsur hara.
Tanah dengan dominansi liat mempunyai kemampuan mengikat hara lebih besar,
hal inilah yang menjadi jawaban mengapa tanah dengan kandungan liat tinggi
mempunyai kecepatan tumbuh klekap lebih tinggi, sehingga akan menguntungkan
untuk kegiatan budidaya baik ikan maupun udang dengan sistem tradisional.
Derajat keasaman (pH) sedimen tambak udang Desa Jayamukti tergolong
sedikit alkalis yaitu 7,9±0,35. Penentuan kelas pH didasarkan pada kemampuan
untuk mempengaruhi ketersediaan unsur hara dalam tanah. Pada kisaran pH
6,5-7,5 unsur hara tersedia dalam jumlah yang cukup banyak (optimal), karena bakteri
yang bertindak sebagai dekomposer, juga mampu hidup optimal pada kisaran pH
tersebut. Pada pH kurang dari 6,0 maka ketersediaan unsur hara (fosfor, kalium,
belerang, kalsium, magnesium) menurun dengan cepat, sedangkan pH tanah lebih
besar dari 8,0 akan menyebabkan unsur-unsur nitrogen, besi, mangan, borium,
tembaga dan seng ketersediaannya relatif jadi sedikit (Sarief 1985 dalam A`in
2009).
Variabel C-organik diketahui melalui konversi dari rumusan bahan organik
total atau total organic matter (Sudjadi et al.1997). Kandungan C-organik dalam
tanah merupakan representasi dari bahan organik tanah hasil perombakan dan
penyusunan yang dilakukan jasad renik tanah. Senyawa karbon merupakan
tinggi maupun rendah (fitoplankton) sehingga penting diketahui untuk bahan
pertimbangan kesesuaian lahan. Hasil analisis kualitas tanah menunjukkan
kandungan C-organik pada sedimen tambak udang di Desa Jayamukti tergolong
rendah yaitu 1,45±0,44% (inlet 1,37±0,29%, tengah 1,76±0,24%, dan outlet
1,2±0,18%), sedangkan standar kandungan C-organik pada sedimen tambak untuk
budidaya udang adalah 3-5% (BSN 2009). Kandungan karbon organik pada
ekosistem tertutup, seperti sedimen tambak udang Desa Jayamukti dan danau
(Hong et al. 2008) relatif lebih tinggi dibandingkan pada ekosistem terbuka,
seperti laut dan sungai (Hong et al. 2010). Hal ini dikarenakan, akumulasi bahan
organik yang sangat dipengaruhi oleh jumlah materi organik yang masuk (sisa
pakan dan aktivitas metabolisme udang), laju pengendapan pada sedimen, dan
kecepatan degradasi bahan organik (Killops & Killops 1993). Adanya perbedaan
karakteristik substrat dan jumlah bahan organik diduga akan berdampak pada
kinerja SMFC yang ada (Chadhuri & Lovley 2003).
Aspek penting lain keberhasilan budidaya sistem tradisional adalah
ketersediaan pakan alami. Jumlah pakan alami ini tidak terlepas dari sediaan
nutrien dasar. Nitrogen dan fosfor bersama dengan karbon dan hidrogen, diakui
sebagai unsur pokok terpenting bagi makhluk hidup, diantaranya untuk
perkembangan protoplasma sel sehingga unsur-unsur ini disebut sebagai “famous nutrient”. Menurut Rosmarkam dan Yuwono (2002), kandungan nitrogen dalam tanah sangat bervariasi bergantung pada pengelolaan dan penggunaan lahan
tersebut. Hasil analisis kualitas tanah menunjukkan kandungan N total pada
sedimen tambak udang Desa Jayamukti tergolong rendah yaitu 0,11±0,03% (inlet
0,12±0,24%, tengah 0,13±0,02%, outlet 0,09±1,7%), sedangkan standar optimum
kandungan N total pada sedimen tambak untuk budidaya udang adalah
0,40-0,75% (BSN 2009).
C/N rasio merupakan suatu cara mudah untuk mengetahui laju proses
dekomposisi. Ada 2 (dua) tahap dalam usaha budidaya, dimana laju proses
dekomposisi sangat berpengaruh penting dalam menjamin kualitas tanah sebagai
media budidaya. Pertama yaitu persiapan pengolahan lahan/tanah dan kedua pasca
pemanenan, tanah yang telah digunakan untuk proses produksi banyak
dikembalikan kualitasnya. Kelas C/N ratio dikelompokkan dengan pertimbangan
pengaruh C/N ratio terhadap status bahan organik (Foth 1979 dalam A`in 2009).
Berdasarkan perhitungan hasil analisis terhadap kandungan karbon dan nitrogen
diperoleh perbandingan antara persentase karbon terhadap nitrogen (C/N ratio)
pada sedimen tambak di Desa Jayamukti sebesar 13 (inlet 12, tengah 13 dan outlet
13). Nilai C/N ratio tersebut lebih kecil dari 15 sehingga menunjukkan terjadinya
mineralisasi N. Pengertian mineralisasi N adalah proses perubahan N-organik
menjadi N-anorganik oleh mikroba dekomposer. Apabila rasio C/N lebih besar
dari 30 berarti terjadi immobilisasi N, dan jika berada diantara 15–30 berarti mineralisasi seimbang dengan immobilisasi. Proses mineralisasi dan immobilisasi
N dalam tanah sangat ditentukan oleh aktivitas mikroorganisme tanah, baik jamur,
bakteri, dan sebagainya (Foth 1979 dalam Arshad & Coen 1992).
Fosfat merupakan unsur hara yang sangat berpengaruh terhadap
pertumbuhan dan metabolisme plankton. Oleh sebab itulah, kandungan fosfat
dalam tanah amat diperhatikan untuk evaluasi kesesuaian lahan. Pada fiksasi
fosfor, beberapa jenis fosfor termasuk diantaranya adalah fosfat tanah diikat dan
dilepaskan ke dalam larutan tanah dan berperan dalam kesuburan tanah (Sarief
1985 dalam A`in 2009). Fosfor di dalam tanah terdapat dalam berbagai bentuk
senyawa, baik persenyawaan an-organik yang terikat dengan mineral-mineral
tanah maupun persenyawaan organik yang berhubungan dengan bahan organik
tanah. Posfor di dalam tanah senantiasa diikat oleh Fe, Al dan Ca dalam senyawa
Fe-P, Al-P dan Ca-P. Hasil analisis menunjukkan kandungan P tersedia pada
sedimen tambak udang Desa Jayamukti sebesar 59±35,4 ppm (inlet 96,6±41,42
ppm, tengah 46±7,55 ppm, outlet 35±2 ppm) dan tergolong dalam nilai optimum
untuk budidaya udang yaitu 30-60 ppm (BSN 2009).
Salah satu sifat kimia tanah yang memegang peranan dalam penentuan
kesuburan adalah kapasitas tukar kation (KTK) tanah. Kapasitas Tukar Kation
suatu tanah dapat didefinisikan sebagai suatu kemampuan koloid tanah menjerap
dan mempertukarkan kation. Secara implisit tingkat KTK juga menunjukkan
keseimbangan reaksi dalam tanah sehingga semua proses yang terdapat
Melalui KTK kemampuan daya jerap unsur hara dari koloid tanah dapat
ditentukan dengan mudah. Mengingat peranannya yang besar, maka variabel ini
menjadi tolak ukur penilaian kesesuaian lahan untuk lahan pertambakan, kelas
KTK ditentukan berdasarkan standar umum dalam persyaratan budidaya tambak.
Nilai KTK sangat dipengaruhi oleh reaksi tanah (pH), bahan organik, jumlah dan
jenis mineral liat (Notohadiprawiro 2000). Semakin tinggi nilai KTK suatu tanah,
semakin tinggi pula kemampuannya untuk menyerap dan melepaskan unsur hara.
Kation yang dapat ditukar Ca, Mg, K dan Na dapat memberikan indikasi nilai
KTK serta tingkat kesuburan tanah.
Kation yang dapat ditukar Ca, Mg, K dan Na dapat memberikan indikasi
nilai KTK serta tingkat kesuburan tanah. Hasil analisis laboratorium menunjukkan
bahwa nilai KTK pada sedimen tambak udang Desa Jayamukti sebesar
23,28±3,60 cmol(+)/kg (inlet 25,38±2,70 cmol(+)/kg, tengah 22,59±3,71
cmol(+)/kg, outlet 21,89±4,56cmol(+)/kg) dan tergolong dalam nilai optimum
untuk budidaya udang yaitu > 20 cmol(+)/kg (BSN 2009).
Kation-kation dapat ditukar (Ca, Mg, K dan Na) merupakan kation-kation
yang dapat dipertukarkan dan terjerap pada permukaan kompleks jerapan tanah.
Semakin tinggi kation dapat ditukar suatu unsure, maka potensi koloid untuk
memasok larutan tanah dengan unsur-unsur bersangkutan semakin besar (Bailey
et al. 1986 dalam Shukla et al. 2004b).
Hasil analisis laboratorium terhadap sedimen tambak udang di Desa
Jayamukti dibandingkan dengan nilai optimum untuk budidaya tambak udang
(pada Tabel 2) menunjukkan bahwa nilai-nilai kation dapat ditukar untuk Ca
tergolong sedang yaitu 8,86±1,3(cmol(+)/kg) (inlet 9,98±0,33cmol(+)/kg, tengah
8,91±1,61cmol(+)/kg, outlet 7,7±0,49cmol(+)/kg); Mg tergolong tinggi yaitu
26,16±4,6 (cmol(+)/kg) (inlet 28±7,09cmol(+)/kg, tengah 28,04±1,79cmol(+)/kg,
outlet 22,44±0,85cmol(+)/kg); K tergolong tinggi yaitu 5,8±16 (cmol(+)/kg) (inlet
6,28±1,33cmol(+)/kg, tengah 6,28±0,29cmol(+)/kg, outlet 4,85±0,33cmol(+)/kg);
dan Na tergolong tinggi yaitu 55,15±19 (cmol(+)/kg) (inlet
55,76±25,06cmol(+)/kg, tengah 70,35±12,48cmol(+)/kg, outlet