UJI EFEK DIURETIK EKSTRAK ETANOL DAUN ANDONG HIJAU (Cordyline fruticosa. Goepp) TERHADAP
TIKUS PUTIH JANTAN
SKRIPSI
OLEH: SISMA ARITA NIM 071524066
PROGRAM EKSTENSI FARMASI FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA MEDAN
UJI EFEK DIURETIK EKSTRAK ETANOL DAUN ANDONG HIJAU (Cordyline fruticosa. Goepp) TERHADAP
TIKUS PUTIH JANTAN
SKRIPSI
Diajukan Untuk Melengkapi Salah Satu Syarat Untuk Memperoleh Gelar Sarjana Farmasi Pada Fakultas Farmasi
Universitas Sumatera Utara
OLEH: SISMA ARITA NIM 071524066
PROGRAM EKSTENSI FARMASI FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA MEDAN
Pengesahan Skripsi
UJI EFEK DIURETIK EKSTRAK ETANOL DAUN ANDONG HIJAU (Cordyline fruticosa. Goepp) TERHADAP
TIKUS PUTIH JANTAN
OLEH: SISMA ARITA NIM 071524066
Dipertahankan di Hadapan Penguji Skripsi Fakultas Farmasi Universitas Sumatera Utara
Pada tanggal: September 2010
Pembimbing I, Panitia Penguji,
(Drs. Nahitma Ginting, M.Si.,Apt.) (
NIP 195504241983031003 NIP 195409091982011001 Dr. Karsono, Apt.)
(Dr. Kasmirul R. Sinaga, M.S., Apt.)
Pembimbing II, NIP 195504241983031003
(Dr. Dr. Edy Suwarso, SU,.Apt.) (
NIP 195709091985112001 NIP 195109081985031002
Drs. Suryadi Achmad, M.Sc., Apt)
(
NIP 195011171980022001 Dra. Fat Aminah, M.Sc., Apt)
Dekan,
(Prof. Dr. Sumadio Hadisahputra, Apt NIP 195311281983031002
KATA PENGANTAR
Puji dan syukur Alhamdulillah kehadirat Allah SWT atas limpahan berkah dan
karuniaNya yang luar biasa besar, sehingga penulis dapat menyelesaikan
penelitian dan penyusunan skripsi ini. Skripsi ini diajukan untuk memenuhi
persyaratan dalam mencapai gelar Sarjana Farmasi pada Fakultas Farmasi
Universitas Sumatera Utara.
Penulis menyampaikan rasa terima kasih yang tiada terhingga kepada
Ayahanda Tawar, SE.MM dan Ibunda Siti Rahmah, Kakanda Andriadi, serta
Adinda Apriandiora, Rizki Pira Seni dan Reni Mahara yang senantiasa
mendoakan dan memberikan dukungan moril dan materil yang tiada
putus-putusnya.
Penulis juga menyampaikan ucapan terima kasih serta penghargaan kepada:
1. Bapak Prof. Dr. Sumadio Hadisahputra, Apt., selaku Dekan beserta para
Pembantu Dekan Fakultas Farmasi Universitas Sumatera Utara yang telah
memberikan fasilitas serta sarana.
2. Bapak Drs. Nahitma Ginting, M.Si.,Apt sebagai penasehat akademik, sebagai
pembimbing, terima kasih atas segala arahan dan nasehat selama melakukan
penelitian hingga selesainya penulisan skripsi ini.
3. Bapak Dr. Edy Suwarso, SU,.Apt sebagai pembimbing terima kasih atas
segala arahan dan nasehat selama melakukan penelitian hingga selesainya
penulisan skripsi ini.
4. Bapak dan Ibu Panitia Penguji atas segala arahan dan masukan yang sangat
5. Bapak dan Ibu staf pengajar Fakultas Farmasi USU yang telah mendidik
penulis dalam perkuliahan.
6. Bapak Drs.Panal Sitorus, M.Si,.Apt selaku Kepala Laboratorium
Farmakognosi dan Drs. Syaiful Bahri M.Si.,Apt selaku Kepala Laboratorium
Farmakologi beserta seluruh staf yang telah mengizinkan penulis
menggunakan fasilitas laboratorium selama penelitian.
Penulis paham bahwa tulisan ini masih jauh dari titik kesempurnaan, untuk itu
sangat diharapkan masukan berupa kritik dan saran yang konstruktif demi
penyempurnaannya. Akhir kata, harapan penulis semoga skripsi ini bermanfaat
bagi kita semua dan dapat menjadi sumbangan yang berarti bagi ilmu pengetahuan
khususnya di bidang farmasi.
Medan, September 2010
Penulis,
ABSTRAK
Serbuk daun andong (Cordyline fruticosa. Goepp) mula-mula di ekstraksi
dengan etanol 80% secara perkolasi, diuapkan dengan bantuan rotary evaporator
lalu difreez driyer didapat ekstrak kental. Ekstrak etanol diuji pada hewan
percobaan untuk mengetahui efek diuretic dan dibandingkan menggunakan
furosemid (3,6 mg/kg BB). Setelah itu volume urin di ukur dan di hitung kadar
natrium dan kalium dengan alat AAS.
Hasil karakterisasi serbuk daun andong (Cordyline fruticosa. Goepp) di
peroleh hasil kadar air 5,99%, kadar abu total 6,81%, kadar abu total tidak larut
dalam asam 1,46%, kadar sari larut air 28,32%, kadar sari larut dalam etanol
14,48%.
Ekstrak etanol 80% daun andong dengan dosis 100 mg/kg BB, dosis 200
mg/kg BB, dan dosis 400 mg/kg BB memberikan efek diuretika dibandingkan
dengan kontrol (CMC 5 mg) yang diberikan secara oral selama 6 jam. Setelah
pemberian ekstrak etanol daun andong (EEDA) dengan dosis yang bervariasi
yaitu untuk control CMC ( 5 mg), dosis 100 mg/kg BB, dosis 200 mg/kg BB,
dosis 400 mg/kg BB dan Furosemid( 3,6 mg/kg BB) sebagai pembanding.
Didapat volume urin total secara berturut-turut yaitu 18,4 ml; 23,2 ml; 27,5 ml;
30,4 ml dan 34,1 ml. Kemudian dihitung kadar natrium dan kalium dengan alat
AAS. Rata-rata kadar natrium didapat hasilnya secara berturut-turut adalah 15,80
mcg; 19,22 mcg; 19,86 mcg; 32,44 mcg; dan 42,49 mcg. Rata-rata kadar kalium
didapat hasilnya secara berturut-turut adalah 61,45 mcg; 62,35 mcg; 77,71 mcg;
81,29 mcg; dan 91,80 mcg.
Dapat disimpulkan bahwa pada pemberian ekstrak etanol daun andong
dosis 100 mg/kg BB, dosis 200 mg/kg BB dan dosis 400 mg/kg BB menunjukkan
efek sebagai diuretika. Semakin tinggi dosis EEDA yang digunakan maka akan
bersifat diuretika.
ABSTRACT
Andong leaf powder (Cordyline fruticosa. Goepp) first in the extraction
with 80% ethanol by percolation, evaporated with the aid of rotary evaporator and
the extract obtained driyer difreez thick. The ethanol extract was tested in animal
experiments to determine the effect of diuretics and compared using furosemide
(3.6 mg / kg BW). After urine volume was measured and calculated levels of
sodium and potassium by means of AAS.
The results of powder characterization andong leaf (Cordyline fruticosa.
Goepp) was obtained the results of water content 5.99%, 6.81% total ash, total ash
insoluble in acid 1.46%, water soluble extract concentration 28.32%, soluble in
ethanol extract concentration 14.48%.
80% ethanol extract of leaves of carriage with a dose of 100 mg / kg, a
dose of 200 mg / kg, and doses of 400 mg / kg BW diuretic effect compared to
controls (CMC 5 mg) given orally for 6 hours. After treatment with ethanol
extract of leaves of carriage (EEDA) with varying doses for the control of CMC
(5 mg), doses of 100 mg / kg, a dose of 200 mg / kg, a dose of 400 mg / kg BW
and furosemide (3.6 mg / kg BW) as a comparison. Obtained a total volume of
urine in a row is 18.4 ml, 23.2 ml, 27.5 ml, 30.4 ml and 34.1 ml. Then the
calculated concentration of sodium and potassium by means of AAS. Average
sodium content of the results obtained in a row is 15.80 mcg; 19.22 mcg; 19.86
mcg; 32.44 mcg; and 42.49 mcg. Average potassium content of the results
obtained in a row is 61.45 mcg; 62.35 mcg; 77.71 mcg; 81.29 mcg; and 91.80
mcg.
It can be concluded that the ethanol extract of leaves andong dose 100 mg
/ kg, a dose of 200 mg / kg bw and the dose of 400 mg / kg BW showed a diuretic
effect.The higher dose used EEDA will be diuretic.
DAFTAR ISI
1.6 Kerangka Konsep Penelitian ... 5
2.2 Uraian Kimia ... 8
2.2.1 Triterpenoida dan Steroida ... 8
2.3 Metode Ekstraksi ... 9
2.4 Diuretika ... 12
2.4.1 Furosemid ... 13
2.5 Mekanisme Kerja Diuretik ... 13
2.6 Mekanisme Pembentukan Urin... 15
2.7 Spektrofotometri Serapan Atom ... 16
BAB II METODE PENELITIAN ... 18
3.1 Alat – alat yang digunakan ... 18
3.2 Bahan – bahan yang digunakan ... 19
3.2.1 Bahan Tumbuhan . ... 19
3.2.2 Bahan Kimia. ... 19
3.3 Pembuatan Larutan Pereaksi ... 19
3.3.1 Asam Klorida 2 N b/v ... 19
3.3.2 Besi (III) Klorida 10 % b/v ... 19
3.3.3 Timbal (II) Asetat 0,4 M b/v ... 19
3.3.4 Pereaksi Molish ... 20
3.3.5 Pereaksi Meyer ... 20
3.3.6 Pereaksi Bouchardat ... 20
3.3.7 Pereaksi Dragendorff ... 20
3.3.8 Natrium Klorida 0,9% b/v ... 20
3.3.9 Natrium Klorida 0,0113 N ... 20
3.3.11 Kalium Kromat 5% ... 21
3.3.12 Larutan Induk Kalium ... 21
3.3.13 Larutan Induk Natrium... 21
3.4 Penyiapan Bahan ... 21
3.4.1 Determinasi Tumbuhan ... 21
3.4.2 Pengumpulan Sampel ... 21
3.4.3 Pengolahan Sampel ... 22
3.5 Pembuatan Ekstrak Etanol ... 22
3.6 Karakterisasi Simplisia ... 23
3.6.1 Penetapan Kadar Air ... 23
3.6.2 Penetapan Kadar Abu Total ... 24
3.6.3 Penetapan Kadar Abu Tidak Larut Dalam Asam ... 24
3.6.4 Penetapan Kadar Sari Larut Dalam Air ... 24
3.6.5 Penetapan Kadar Sari Larut Dalam Etanol ... 24
3.6.6 Pemeriksaan Makroskopik Simplisia... 25
3.6.7 Pemeriksaan Mikroskopik Simplisia ... 25
3.7 Skrining Fitokimia Serbuk Simplisia ... 25
3.7.1 Pemeriksaan Alkaloida ... 25
3.7.2 Pemeriksaan Glikosida... 26
3.7.3 Pemeriksaan Flavonoida ... 27
3.7.4 Pemeriksaan Saponin ... 27
3.7.5 Pemeriksaan Tanin... 28
3.7.6 Pemeriksaan Steroida / Triterpenoida ... 28
3.9 Pembuatan Suspensi CMC 0,5% ... 28
3.10 Pembuatan Suspensi Furosemid ... 29
3.11 Pembuatan Larutan Induk Suspensi Ekstrak Etanol ... 29
3.12 Persiapan Hewan Percobaan... 29
3.13 Prosedur Kerja Untuk Pengujian Farmakologi ... 30
3.14 Penentuan Kadar Na dan K dengan alat AAS (Atomic Absorption Spectrophotometry) ... 30
3.15 Pengolahan Data ... 31
BAB IV HASIL DAN PEMBAHASAN ... 32
4.1 Hasil Karakterisasi Simplisia ... 32
4.2 Hasil Pengujian Farmakologi ... 33
BAB V KESIMPULAN DAN SARAN... 44
5.1 Kesimpulan ... 44
5.2 Saran ... 45
DAFTAR PUSTAKA ... 46
DAFTAR LAMPIRAN
Lampiran Halaman
1. Hasil Identifikasi / Determinasi Tumbuhan Andong
Hijau (Cordyline fruticosa. Goepp) ... 48
2. Gambar Tumbuhan daun Andong Hijau ... 49
3. Simplisia Daun Andong Hijau dan Serbuk Daun Andong Hijau... 50
4. Gambar Hewan Tikus Putih Jantan ... 51
5. Mikroskopis penampang melintang daun Andong Hijau dengan perbesaran 10x40 ... 52
6. Mikroskopis penampang membujur atas daun Andong Hijau dengan perbesaran 10x40 ... 53
7. . Mikroskopis penampang membujur bawah daun Andong Hijau dengan perbesaran 10x40 ... 54
8. Mikroskopis serbuk daun Andong Hijau dengan perbesaran 10x40 ... 55
9. Hasil Skrining Golongan Senyawa Kimia Daun Andong Hijau ... 56
10. Perhitungan Penetapan Kadar Air Simplisia Daun Andong Hijau ... 57
11. Perhitungan Penetapan Kadar Sari Larut Etanol Simplisia Daun Andong Hijau ... 58
12. Perhitungan Penetapan Kadar Sari Larut Air Simplisia Daun Andong Hijau ... 59
13. Perhitungan Penetapan Kadar Abu Total ... 60
14. Seperangkat Alat Modifikasi Penampung Urin Tikus... 62
16. Bagan Pembuatan Ekstrak Etanol Daun Andong Hijau ... 64
17. Perhitungan CMC 0,5% ... 65
18. Perhitungan Dosis Furosemid 40 mg ... 66
19. Perhitungan Dosis Ekstrak Etanol Daun Andong Hijau ... 67
20. Perhitungan Kadar Na dan K ... 68
21. Tabel Hasil Penelitian ... 70
22. Grafik Volume total urin,kadar natrium urin total dan kadar kalium urin total, pada pemberian Ekstrak Daun Andong Hijau (EEDAH) dosis 100 mg/kgbb, 200 mg/kgbb, 400 mg/kgbb dan Furosemid 3,6 mg/kgbb ... 71
23. Prosedur Kerja Perlakuan Terhadap Tikus... 73
DAFTAR TABEL
Tabel Halaman
1. Data volume urin total ± SD pada pemberian EEDAH dosis 100 mg/Kg BB, 200 mg/kg BB, 400 mg/Kg BB, Furosemid 3,6 mg/Kg BB dan Kontrol (CMC 1 mg/Kg BB) dengan
Pengulangan n=6 ... 34
2 . Perhitungan SPSS dari Volume Total Urin ... 35
3. Data kadar natrium urin total ± SD pada pemberian EEDAH dosis 100 mg/Kg BB, 200 mg/kg BB, 400 mg/Kg BB, Furosemid 3,6 mg/Kg BB dan Kontrol (CMC 1 mg/Kg BB) dengan
Pengulangan n=6 ... 38
4. Hasil Perhitungan SPSS dari Kadar Urin Total ... 39
5. Data kadar kalium urin total ± SD pada pemberian EEDAH dosis 100 mg/Kg BB, 200 mg/kg BB, 400 mg/Kg BB, Furosemid 3,6 mg/Kg BB dan Kontrol (CMC 1 mg/Kg BB) dengan
Pengulangan n=6 ... 41
6. Hasil Perhitungan SPSS dari Kadar Kalium Urin Total ... 42
7. Hasil Skrining Golongan Senyawa Kimia Daun Andong Hijau
(Cordyline fruticosa. Goepp ... 56
8. Tabel Hasil Penelitian ... 70
DAFTAR GAMBAR
7. Mikroskopis penampang melintang daun Andong Hijau dengan perbesaran 10x40 ... 52
8. Mikroskopis penampang membujur daun Andong Hijau dengan perbesaran 10x40 ... 53
9. Mikroskopis serbuk daun Andong Hijau dengan perbesaran 10x40 ... 54
10. Seperangkat Alat Modifikasi Penampung Urin Tikus ... 62
11. Kandang Metabolik (A), Neraca hewan (Presica, Geniweight (GW – 1500) (B), Penangas Air (C) dan Neraca Listrik (D) ... 63
12. Grafik volume total urin pada pemberian Ekstrak Daun Andong Hijau (EEDAH) dosis 100 mg/kg BB, 200 mg/kg BB, 400 mg/kg BB dan Furosemid 3,6 mg/kg BB ... 71
13. Grafik kadar natrium urin total pada pemberian Ekstrak Daun Andong Hijau dosis 100 mg/kg BB, 200 mg/kg BB, 400 mg/kg BB dan Furosemid 3,6 mg/kg BB ... 71
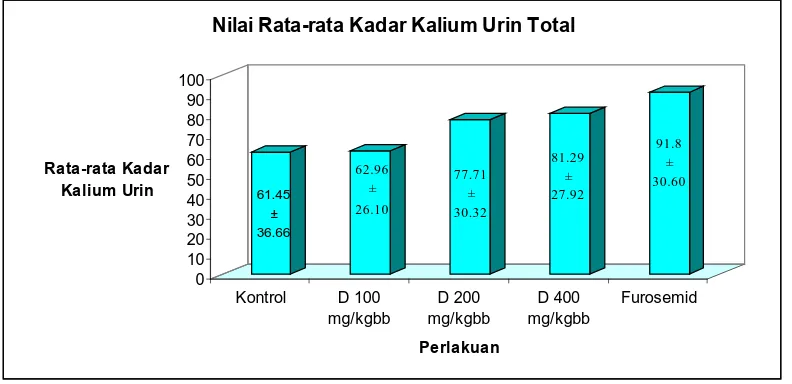
14. Grafik kadar kalium urin total pada pemberian Ekstrak Daun Andong Hijau dosis 100 mg/kg BB, 200 mg/kg BB, 400 mg/kg BB dan Furosemid 3,6 mg/kg BB ... 72
ABSTRAK
Serbuk daun andong (Cordyline fruticosa. Goepp) mula-mula di ekstraksi
dengan etanol 80% secara perkolasi, diuapkan dengan bantuan rotary evaporator
lalu difreez driyer didapat ekstrak kental. Ekstrak etanol diuji pada hewan
percobaan untuk mengetahui efek diuretic dan dibandingkan menggunakan
furosemid (3,6 mg/kg BB). Setelah itu volume urin di ukur dan di hitung kadar
natrium dan kalium dengan alat AAS.
Hasil karakterisasi serbuk daun andong (Cordyline fruticosa. Goepp) di
peroleh hasil kadar air 5,99%, kadar abu total 6,81%, kadar abu total tidak larut
dalam asam 1,46%, kadar sari larut air 28,32%, kadar sari larut dalam etanol
14,48%.
Ekstrak etanol 80% daun andong dengan dosis 100 mg/kg BB, dosis 200
mg/kg BB, dan dosis 400 mg/kg BB memberikan efek diuretika dibandingkan
dengan kontrol (CMC 5 mg) yang diberikan secara oral selama 6 jam. Setelah
pemberian ekstrak etanol daun andong (EEDA) dengan dosis yang bervariasi
yaitu untuk control CMC ( 5 mg), dosis 100 mg/kg BB, dosis 200 mg/kg BB,
dosis 400 mg/kg BB dan Furosemid( 3,6 mg/kg BB) sebagai pembanding.
Didapat volume urin total secara berturut-turut yaitu 18,4 ml; 23,2 ml; 27,5 ml;
30,4 ml dan 34,1 ml. Kemudian dihitung kadar natrium dan kalium dengan alat
AAS. Rata-rata kadar natrium didapat hasilnya secara berturut-turut adalah 15,80
mcg; 19,22 mcg; 19,86 mcg; 32,44 mcg; dan 42,49 mcg. Rata-rata kadar kalium
didapat hasilnya secara berturut-turut adalah 61,45 mcg; 62,35 mcg; 77,71 mcg;
81,29 mcg; dan 91,80 mcg.
Dapat disimpulkan bahwa pada pemberian ekstrak etanol daun andong
dosis 100 mg/kg BB, dosis 200 mg/kg BB dan dosis 400 mg/kg BB menunjukkan
efek sebagai diuretika. Semakin tinggi dosis EEDA yang digunakan maka akan
bersifat diuretika.
ABSTRACT
Andong leaf powder (Cordyline fruticosa. Goepp) first in the extraction
with 80% ethanol by percolation, evaporated with the aid of rotary evaporator and
the extract obtained driyer difreez thick. The ethanol extract was tested in animal
experiments to determine the effect of diuretics and compared using furosemide
(3.6 mg / kg BW). After urine volume was measured and calculated levels of
sodium and potassium by means of AAS.
The results of powder characterization andong leaf (Cordyline fruticosa.
Goepp) was obtained the results of water content 5.99%, 6.81% total ash, total ash
insoluble in acid 1.46%, water soluble extract concentration 28.32%, soluble in
ethanol extract concentration 14.48%.
80% ethanol extract of leaves of carriage with a dose of 100 mg / kg, a
dose of 200 mg / kg, and doses of 400 mg / kg BW diuretic effect compared to
controls (CMC 5 mg) given orally for 6 hours. After treatment with ethanol
extract of leaves of carriage (EEDA) with varying doses for the control of CMC
(5 mg), doses of 100 mg / kg, a dose of 200 mg / kg, a dose of 400 mg / kg BW
and furosemide (3.6 mg / kg BW) as a comparison. Obtained a total volume of
urine in a row is 18.4 ml, 23.2 ml, 27.5 ml, 30.4 ml and 34.1 ml. Then the
calculated concentration of sodium and potassium by means of AAS. Average
sodium content of the results obtained in a row is 15.80 mcg; 19.22 mcg; 19.86
mcg; 32.44 mcg; and 42.49 mcg. Average potassium content of the results
obtained in a row is 61.45 mcg; 62.35 mcg; 77.71 mcg; 81.29 mcg; and 91.80
mcg.
It can be concluded that the ethanol extract of leaves andong dose 100 mg
/ kg, a dose of 200 mg / kg bw and the dose of 400 mg / kg BW showed a diuretic
effect.The higher dose used EEDA will be diuretic.
BAB I PENDAHULUAN
1.1 Latar Belakang
Menjaga kelancaran pengeluaran air seni adalah tindakan yang benar dan
di anjurkan dalam dunia kesehatan. Air seni merupakan campuran air dengan
senyawa-senyawa polar yang harus dikeluarkan oleh tubuh. Pengeluaran air seni
yang tidak lancar pada kandung kemih atau ginjal dalam waktu yang lama akan
menimbulkan pengkristalan dari zat-zat yang akan di buang. Zat-zat tersebut
adalah kalsium karbonat, kalsium urat, kalsium oksalat, dan kalsium lemak
(Permadi, 2006).
Dalam dunia medis sudah banyak obat kimia yang diproduksi sebagai
peluruh air seni atau diuretika. Bukan hanya obat kimia saja yang berfungsi
sebagai peluruh air seni atau diuretika. Banyak tanaman yang sudah lama dikenal
oleh nenek moyang kita yang digunakan sebagai peluruh air seni (Permadi, 2006).
Furosemida merupakan kelompok diuretika kuat yang telah teruji secara
ilmiah. Sebagai diureika kuat furosemida merupakan yang paling sering di
gunakan di Indonesia, yaitu sekitar 60% di bandingkan degan diuretika kuat
lainnya. Hal ini terjadi karena mula kerja, waktu paruh dan waktu kerja relatif
singkat, sehingga efek diuretiknya cepat timbul dan sangat cocok digunakan untuk
keadaan akut, namun pemakaian furosemida sangat disayangkan, karena dapat
menimbulkan efek samping gangguan keseimbangan cairan dan elektrolit,
bisa menimbulkan hiponatremia dan hipokalemia (Muttscler E, 1991). Furosemid
yang digunakan dalam penelitian ini adalah furosemid Generik yang di produksi
oleh pabrik Kimia Farma @40 mg.
Dewasa ini, penelitian dan pengembangan tumbuhan obat, baik didalam
maupun di luar negeri berkembang pesat. Penelitian yang berkembang, terutama
pada segi farmakologi maupun fitokimianya berdasarkan indikasi tumbuhan obat
yang telah digunakan oleh sebagian masyarakat dengan khasiat yang teruji secara
empiris. Hasil penelitian tersebut, tentunya lebih memantapkan para pengguna
tumbuhan obat akan khasiat maupun penggunaannya (Dalimartha, 2006).
Menurut penelitian masa kini, obat-obatan tradisional sangat bermamfaat
bagi kesehatan. Penggunaanya lebih mudah dijangkau masyarakat baik harga
maupun ketersediaannya dan tidak terlalu menimbulkan efek samping, karena
masih bisa dicerna oleh tubuh. Obat tradisional merupakan bahan atau ramuan
bahan yang berupa bahan tumbuhan, bahan hewan, bahan mineral, sediaan sarian
atau galenik, atau campuran dari bahan tersebut, yang secara turun temurun telah
digunakan untuk pengobatan berdasarkan pengalaman.
Salah satu tanaman yang digunakan masyarakat sebagai obat tradisional
adalah tumbuhan daun andong (Cordyline fruticosa. Goepp) yang berkhasiat
diuretika (peluruh air seni). Dimana kandungan kimia yang terkandung didalam
daunnya adalah tanin, saponin, flavonoid, polifenol, steroida, kalsium oksalat, dan
zat besi (Dalimartha, 2006).
Menurut pengalaman yang di peroleh dari masyarakat desa Munte, Karo
bahwa daun andong hijau dapat di gunakan sebagai obat sakit pinggang dan
setempat yaitu dengan merebus daun segar 15-30 g lalu diminum airnya
(Dalimartha, 2006).
Berdasarkan literatur dan pemaparan diatas maka menarik untuk diuji efek
farmakologi dari daun andong hijau sebagai obat diuretika dan mengangkatnya
sebagai data klinis.
1.2 Perumusan Masalah
Dari latar belakang yang telah di uraikan diatas, maka dapat dirumuskan
permasaalahan sebagai berikut:
a. bagaimana karakterisasi dari daun andong.
b. golongan apa sajakah yang terdapat dalam daun andong.
c. apakah ekstrak etanol daun andong (EEDA) mempunyai efek diuretika
terhadap tikus putih jantan.
d. apakah ada kesetaraan antara EEDA dengan furosemid sebagai diuretika.
1.3 Hipotesis
a. diduga karakterisasi simplisia daun andong hijau dapat dilakukan.
b. diduga dapat diketahui golongan senyawa kimia yang terdapat dalam daun
andong hijau
c. diduga ekstrak etanol daun andong hijau mempunyai efek diuretika terhadap
tikus putih jantan.
d. diduga terdapat kesetaraan antara EEDAH dengan furosemid sebagai
diuretika.
1.4 Tujuan Penelitian
Dari rumusan masalah yang diuraikan di atas, dapat dirumuskan tujuan
a. melakukan karakterisasi simplisia daun andong hijau.
b. menganalisis golongan senyawa kimia yang terdapat didalam daun andong
hijau .
c. membuktikan efek diuretika EEDAH terhadap tikus jantan.
d. mengetahui kesetaraan antara EEDAH dengan furosemid sebagai diuretika.
1.5 Manfaat Penelitian
a. sebagai sumber informasi mengenai karakterisasi simplisia daun andong hijau.
b. sebagai sumber informasi mengenai golongan senyawa kimia daun andong
hijau.
c. sebagai sumber informasi mengenai efek diuretika dari ekstrak etanol daun
andong hijau.
1.6 Kerangka Konsep Penelitian
Penelitian ini dilaksanakan dengan kerangka konsep pada Gambar berikut ini :
BAB II
TINJAUAN PUSTAKA
2.1 Uraian Tumbuhan Andong
Tanaman andong termasuk suku bawang-bawangan biasa di tanam sebagai
tanaman hias di pekarangan, taman, atau kuburan. Biasa juga dipakai sebagai
tanaman pagar atau pembatas di perkebunan teh. Andong berasal dari Asia Timur
dan biasa di temukan dari dataran rendah sampai ketinggian 1.900 m dpl
(Dalimartha, 2006).
2.1.1 Sinonim
Sinonim dari tumbuhan Andong (Cordyline fruticosa. Goepp) adalah :
Cordyline fruticosa Backer, Cordyline terminalis Planch., Cordyline terminalis
(L) Kunth., Asparagus terminalis L., Dracaena terminalis Rich., Taetsia fruticosa
Merr., Convallaria fruticosa L (Dalimartha, 2006).
2.1.2. Klasifikasi
Kingdom : Plantae
Divisi : Spermatophyta
Sub divisi : Monocotyledoneae
Bangsa : Liliales
Suku : Agavaceae
Marga : Cordyline
2.1.3. Nama Daerah
Melayu: andong, juwang. Sumatera: bak juang, lak-lak (Ac), kalinjuhang,
linjuhang, katunggal (Bt), anjiluang, linjuwang (Mk) anderuang (Lp), renjuang,
sabang, sawang (Dy). Jawa: hanjuang ( sunda), andong, ending (Jawa), kayu urip (
Madura),. Nusa Tenggara: andong, ending, handwang (Bali). Kalimantan:
renjuang, sabang (Dayak). Sulawesi: tabongo (Gr), Panili, siri (Ms), panyaureng.
Maluku: ai buru (Sr), weluga, wersingin, werusisi (Ab), pitako (Am). Irian:
katopari, ngasi, jasir (Dalimartha, 2006).
2.1.4 Morfologi Tanaman
Tumbuhan ini termasuk perdu tegak dengan tinggi 2-4 m, jarang
bercabang, batang bulat, keras, bekas daun rontok berbentuk cincin. Daun tunggal
dengan warna hijau ada juga yang berwarna merah kecoklatan. Letak daun
tersebar pada batang, terutama berkumpul di ujung batang. Helaian dan panjang
berbentuk lanset dengan panjang 20-60 cm dan lebar 5-13 cm. Ujung dan
pangkalnya runcing, tepi rata, pertulangan menyirip, dan tangkai daunnya
berbentuk talang. Bunga majemuk berbentuk malai, keluar dari ketiak daun,
panjang sekitar 30 cm, berwarna dadu, hijau keunguan, atau kuning muda. Buah
buni berbentuk seperti bola dengan warna merah mengilap. Biji hitam mengilap.
Daun muda yang berwarna hijau bias dimakan sebagai sayuran. Bila menanak
nasi dengan bungkusan daun andong yang tua akan memberikan rasa sedap.
2.1.5 Sifat dan Khasiat
Rasa andong manis, tawar, dan bersifat sejuk. Berkhasiat sebagai penyejuk
darah, menghentikan perdarahan (hemostatis), dan meghancurkan darah beku
pada memar (Dalimartha,2006).
2.1.6 Kandungan kimia
Tanaman andong (Cordyline fruticosa. Goepp) mengandung saponin,
tannin, flavonoid, polifenol, steroida, polisakarida, kalsium oksalat, dan zat besi
(Dalimartha,2006).
2.2 Uraian Kimia
2.2.1 Triterpenoida dan Steroida
Triterpenoida adalah senyawa yang kerangka karbonnya berasal dari enam
satuan isoprene dan secara biosintesis diturunkan dari hidrokarbon C30 asiklik
yaitu skualena. Senyawa ini berstruktur siklik yang agak rumit, kebanyakan
berupa alcohol, aldehisa atau asam karboksilat. Triterpenoida dapat dibagi
menjadi empat golongan senyawa yaitu triterpen, steroida, saponin dan glikosida
jantung ( Harbone, 1987).
Berbagai macam aktivitas fisiologi dari triterpenoida yang merupakan
komponen aktif dalam tumbuhan obat yang telah du gunakan untuk penyakit
diabetes, gangguan menstruasi, gangguan kulit, kerusakan hati dan malaria.
Stereoida adalah triterpen yang kerangka dasarnya system cincin siklopentana
peridropenantrena ditunjukkan pada gambar.
Aktivitas biologis dari dari steroida antara lain sebagai hormone
pengganti kulit pada serangga (ekdison), menginduksi reproduksi seksual pada
jamur air (antheridiol), kardiotonik (digitoksin), prekusor vitamin D (ergosterol),
oral kontrasepsi, (estrogen dan progestin semisintetik) dan obat antiinflamasi
(kortikosteroida) (Tyler et al., 1976).
2.3 Metode Ekstraksi
Ekstraksi adalah kegiatan penarikan kandungan kimia yang dapat larut
sehingga terpisah dari bahan yang tidak dapat larut dengan pelarut cair. Simplisia
yang diekstrak mengandung senyawa aktif yang dapat larut dan senyawa yang
tidak larut seperti serat, karbohidrat, protein, dan lain-lain. Senyawa aktif yang
terdapat dalam berbagai simplisia dapat di golongkan kedalam golongan minyak
atsiri, alkaloid, dan flavonoida, dengan diketahuinya senyawa aktif yang
dikandung simplisia maka akan mempermudah pemisahan pelarut dan cara
ekstraksi yang tepat (Ditjen POM, 2000).
Berdasarkan atas sifatnya ekstrak dikelompokkan sebagai berikut ( Voigt,
1995):
1. Ekstrak encer (Extractum tenue). Sediaan ini memiliki konsistensi
semacam madu dan dapat dituang.
2. Ekstrak kental (Extractum spissum). Sediaan ini liat dalam keadaan dingin
dan tidak dapat dituang.
3. Ekstrak kering (Extractum siccum). Sediaan ini memiliki konsistensi
kering dan mudah digososk.
4. Ekstrak cair ( Extractum fluidum). Dalam hal ini diartikan sebagai ekstrak
cair, yang dibuat sedemikian rupa sehingga 1 bagian simplisia sesuai
Beberpa metode ekstraksi dengan menggunakan pelarut, yaitu:
1. Maserasi
Maserasi berasal dari kata ”macerare” artinya melunakkan. Maserat
adalah hasil penarikan simplisia dengan cara maserasi, sedangkan maserasi adalah
cara penarikan simplisia dengan merendam simplisia tersebut dalam cairan
penyari (Syamsuni, 2006). Maserasi adalah proses pengekstrakan dengan
menggunakan pelarut dengan beberapa kali pengocokan atau pengadukan pada
temperatur ruangan. Remaserasi berarti dilakukan pengulanagn penambahan
pelarut setelah dilakukan penyaringan maserat dan seterusnya (Ditjen POM,
2000).
2. Perkolasi
Perkolasi berasal dari kata ”perkolare” yang artinya penetesan (Voigt,
1995). Perkolasi adalah ekstraksi dengan pelarut yang selalu baru sampai
sempurna yang umumnya dilakukan pada temperatur ruangan. Serbuk simplisia
yang akan diperkolasi tidak langsung dimasukkan kedalam bejana perkolator,
tetapi dibasahi atau dimaserasi terlebih dahulu dengan cairan penyari
sekurang-kurangnya selama 3 jam. Maserasi ini penting terutama pada serbuk simplisia
yang keras dan mengandung bahan yang mudah mengembang. Bila serbuk
simplisia tersebut langsung dialiri dengan penyari, maka cairan penyari tidak
dapat menembus keseluruh sel dengan sempurna (Depkes, 1979; Ditjen POM,
3. Refluks
Refluks adalah ekstraksi dengan pelarut pada temperatur titik didihnya
selama waktu tertentu dan jumlah pelarut terbatas yang relatif konstan dengan
adanya pendingin balik (Ditjen POM, 2000).
4. Sokletasi
Sokletasi adalah ekstraksi dengan menggunakan pelarut yang selalu baru
yang umumnya dilakukan dengan menggunakan alat soklet sehingga terjadi
ekstraksi kontinu dengan jumlah pelarut relatif konstan dengan adanya pendingin
balik (Ditjen POM, 2000).
5. Digesti
Digesti adalah maserasi kinetik dengan pengadukan kontinu pada
temperatur yang tinggi dari temperatur ruangan, yaitu secara umum dilakukan
pada temperatur 40-500C (Ditjen POM, 2000). Dengan cara ini perolehan bahan
aktif agak lebih banyak meskipun pada saat pendinginannya pada suhu kamar
bahan ekstraktif dalam skala besar mengendap (Voigt, 1995).
6. Infus
Infus adalah ekstraksi dengan pelarut air pada temperatur penangas air
(bejana infus tercelup dalam penangas air mendidih, temperatur teukur 96-980C)
selama waktu tertentu (15-20 menit)( Ditjen POM, 2000; Syamsuni, 2006).
7. Dekok
Dekok adalah perebusan simplisia halus dicampur dengan air bersuhu
kamar atau dengan air bersuhu > 900C sambil diaduk berulang-ulang dalam
panas-panas(Voigt, 1995). Dekok adalah infus pada waktu yang lebih lama (≥30 menit)
dan temperatur sampai titik didih air (Ditjen POM, 2000).
2.4 Diuretika
Diuretika adalah zat-zat yang dapat memperbanyak pengeluaran kemih
(diuresis) melalui kerja langsung terhadap ginjal. Fungsi utama ginjal adalah
memelihara kemurnian darah dengan jalan mengeluarkan semua zat asing dan sisa
pertukaran zat dari dalam darah. Sehingga darah mengalami filtrasi, dimana
semua komponennya melintasi saringan ginjal kecuali zat putih telur dan sel-sel
darah. Setiap ginjal mengandung lebih kurang satu juta filter kecil ini (glomeruli),
dan setiap 50 menit (ca 5 liter telah dimurnikan dengan melewati saringan
tersebut). Fungsi peting yang lainnya adalah meregulasi kadar garam dan cairan
tubuh (Tjay dan Rahardja, 2002).
Walaupun kerjanya pada ginjal, diuretik bukan ”obat ginjal”, artinya
senyawa ini tidak dapat memperbaiki atau menyembuhkan penyakit ginjal,
demikian juga pada pasien insufisiensi ginjal jika diperlukan dialisis, tidak akan
dapat ditangguhkan dengan penggunaan senyawa ini. Beberapa diuretika pada
awal pengobatan justru memperkecil ekskresi zat-zat penting urin dengan
mengurangi laju filtrasi glomerulus sehingga akan memperburuk insufisiensi
ginjal (Mutschler, 1991).
Dengan demikian obat yang dapat digunakan secara terapetik hanyalah
yang mempunyai kemampuan untuk mempengaruhi gerakan air dan elektrolit
dalam organisme. Pengaruh terhadap proses transport hanya seakan-akan saja
khas terhadap ginjal. Karena konsentrasi diuretika pada saat melewati nefron
efek pada organ lain lebih dominan. Jika pada peningkatan ekskresi air terjadi
juga peningkatan garam-garam, maka diuretika ini dinamakan saluretika atau
natriuretika (diuretika dalam arti sempit) (Mutschler,1991).
2.4.1 Furosemida
Furosemida termasuk dalam golongan diuretic erat Henle. Kerja diuretic
golongan ini adalah selektif menghambat reabsorsinya dari NaCl pada cabang
menaik yang tebal dari jerat Henle (Katzung, 2001). Diuretik jerat Henle tipe
furosemida sangat bermanfaat, jika diperlukan kerja yang cepat dan intensif,
seperti misalnya pada udem paru-paru (Mutschler, 1991).
2.5. Mekanisme Kerja Diuretika
Kebanyakan diuretika bekerja dengan mengurangi reaksopsi natrium,
sehingga pengeluarannya lewat kemih dan demikian juga dari air diperbanyak.
Obat-obat diuretika biasanya bekerja khusus terhadap tubuli, tetapi juga di tempat
lain, yakni:
1. Tubuli proksimal
Garam reabsorbsi secara aktif (70%), antara lain Na+ dan air, begitu pula
glukosa dan ureum. Reabsorbsi berlangsung secara proporsional sehingga susunan
filtrat tidak berubah dan tetap isotonis terhadap plasma. Diuretika osmosis
(manitol, sorbitol) bekerja disini dengan merintangi reabsorpsi air dan natrium
(Tjay dan Rahardja, 2002).
2. Lengkungan Henle
Di bagian menaik lengkungan Henle ini 2,5% dari semua Cl- yang telah
difiltrasi direabsorpsi secara aktif, disusul dengan reabsorpsi pasif dari Na+ dan
(furosemid, bumetamida, etakrinat) bekerja dengan merintangi transport Cl- dan
demikian reabsorpsi Na+, pengeluaran K+ dan air diperbanyak (Tjay dan
Rahardja, 2002).
3. Tubuli Distal
Di bagian pertama tubuli ini, Na+ direabsorpsi secara aktif tanpa air
hingga difiltrat menjadi lebih cair dan hipotonis. Senyawa tiazida dan klortalidon
bekerja di tempat ini. Dibagian kedua segmen ini, ion Na+ ditukarkan dengan ion
K+ atau NH4+ proses ini dikendalikan oleh hormon anak ginjal aldosteron.
Antagonis aldosteron (spironolakton) dan zat-zat penghemat kalium (amilorid dan
triamteren) bekerja disini (Tjay dan Rahardja, 2002).
4. Saluran pengumpul
Hormon antidiuretik ADH (vasopressin) hipofise bertitik kerja di sini
dengan jalan mempengaruhi permeabilitas bagian air dari sel-sel saluran ini (Tjay
dan Rahardja, 2002).
Diuretik selain memperbanyak pengeluaran air juga dapat menambah
pengeluaran elektrolit. Maka diuretik dapat menyebabkan gangguan
keseimbangan elektrolit dan air. Secara umum diuretik dapat di bagi menjadi dua
golongan besar yaitu diuretik osmotik dan penghambat transport elektrolit di
Gambar 1. Diagram nefron yang membentuk bagian tubulus renalis
2.6 Mekanisme Pembentukan Urin
Darah yang mengalir ke ginjal di filtrasi di glomeruli.dalam filtrasi ini
lebih kurang 13% cairan saja yang dapat melalui glomeruli dan masuk ke dalam
tubulus proksimal. Sewaktu filtrat glomerulus menuruni tubulus, maka volumenya
berkurang dan komposisinya diubah oleh proses reabsorbsi tubulus (penyingkiran
air dan solut dari cairan tubulus) dfalam bentuk urin yang memasuki pelviss
renalis. Dari pelvis renalis, urin berjalan dalam vesica urinaria dan dikeluarkan ke
Gambar 2. Oragan-organ yang membentuk saluran urinari.
2.7. Spektrofotometri Serapan Atom
Spektrofotometri serapan atom adalah suatu spektrofotometri serapan yang
digunakan untuk mendeteksi uap atom logam.
Cara kerja alat ini berdasarkan penguapan larutan sampel, kemudian
logam yang terkandung didalamnya diubah menjadi atom bebas. Atom tersebut
mengabsorbsi radiasi dari sumber cahaya yang dipancarkan dari lampu katoda
(hallow cathode lamp) yang mengandung unsur yang akan ditentukan. Banyaknya
penyerapan radiasi kemudian diukur pada panjang gelombang tertentu menurut
Alat-alat Spektrofotometri Serapan Atom
1. Sumber sinar (Hollow Cathode Lamp)
Fungsi dari hollow cathode lamp adalah sebagai sumber energi radiasi.
Energi radiasi merupakan karakterisasi dari elemen katoda dan neon. Ion-ion neon
yang dipercepat mempengaruhi permukaan katoda yang menyebabkan atom-atom
logam mendidih pada permukaan katoda. Banyak dari atom-atom di hyamburkan
ke fase gas yakni tingkat petama tereksitasi.
2. Burner dan nyala
Nyala, burner dan nebulizer pada alat AAS menyebabkan kation-kation
logam dalam larutan menghasilkan atom-atom logam. Alat AAS membuat
penyerapan pada keadaan dasar.
3. Monokromator
Monokromator menghamburkan radiasi yang berasal dari nyala pada
panjang gelombang tertentu ke detektor.
4. Detektor
Detektor digunakan untuk mengukur intensitas sinar dari sumber sinar.
Intensitas sinar sebanding dengan jumlah atom dalam sampel.
5. Alat penunjuk (Readout Devic)
Alat penunjuk berupa recorder. Hasil diubah dalam absorbansi atau
konsentrasi. Bagan alat spektrofotometri Serapan Atom dapat dilihat pada gambar
BAB III
METODE PENELITIAN
Metodelogi penelitian ini adalah metodelogi eksperimental (experimental
reseacrch). Metodelogi penelitian ini meliputi determinasi tumbuhan,
pengumpulan sampel, pengolahan sampel, pemeriksaan makroskopik dan
mikrokospik sampel, penetapan kadar air, skrining fitokimia, pembuatan ekstrak
dengan cara perkolasi, setelah itu diukur volume total urin tikus, menentukan
kadar Natrium dan Kalium urin dengan alat AAS. Pengolahan data dilanjutkan
secara statistik dengan menggunakan Statistical Product and Service Solution
(SPSS) 16.0 dalam rancangan acak lengkap (RAL). Data numerik lebih dari dua
variable diuji dengan oneway Anava, serta dilanjutkan dengan anlisis Duncan α =
0,5 yaitu uji beda rata-rata perlakuan dengan kontrol (Hanafiah, 2005).
3.1 Alat – alat yang Digunakan
Alat-alat gelas, neraca kasar (Ohaus), neraca listrik (Metter takeda), neraca
hewan (Presica, Geniweight GW–1500), alat penetapan kadar air (cara azotropi),
mikroskop, objek glass, deck glass, perkolator, penguap vakum putar (Heidolph
vv 2000), freeze dryer (Medulyo, Edwards), mortir dan stamfer, alat tikus
metabolik (Metabolism Restrainer), seperangkat alat tikus modifikasi, oral sonde
spuit 3 ml dan 10 ml (terumo), AAS (Atomic Absorption Spectrophotometry),
3.2 Bahan – bahan yang Digunakan 3.2.1 Bahan Tumbuhan
Daun Andong (Cordyline fruticosa, Goepp).
3.2.2 Bahan Kimia
Etanol 96% (E. Merck), akuades ( lokal, dari laboratorium kimia
kuantitatif), CMC (E.Merck), toluen (E.Merck), kloral hidrat (E.Merck), Pb (II)
asetat (E.Merck), besi (III) (E.Merck), klorida (E.Merck), kalium iodida
(E.Merck), iodium, α- naftol (E.Merck), asam nitrat ( E. Merck), bismuth nitrat
(E.Merck), eter (E.Merck), kloroform (E.Merck), isopropanol (E.Merck), metanol
(E.Merck), natrium sulfat anhidrat (E.Merck), etil asetat (E.Merck), serbuk seng
(E.Merck), asam klorida (E.Merck), asam sulfat P (E.Merck), natrium klorida
(E.Merck), kalium klorida (E.Merck), furosemid (Kimia Farma). Bahan – bahan
yang tidak di sebutkan adalah pro analisis E.Merck.
3.3 Pembuatan Larutan Pereaksi 3.3.1 Asam Klorida 2 N
Sebanyak 72,93 g asam klorida (p) diencerkan dengan air suling sampai
1000 ml (Farmakope Indonesia, 1979).
3.3.2 Besi (III) Klorida 10 %
Sebanyak 10 g besi (III) klorida dilarutkan dalam air suling sampai 100 ml
(Farmakope Indonesia, 1979).
3.3.3 Timbal (II) Asetat 0,4 M
Timbal (II) asetat sebanyak 15,7 g dilarutkan dalam aquadest bebas CO2
3.3.4 Pereaksi Molish
Sebanyak 3 g α- naftol dilarutkan dalam asam nitrat 0,5 N secukupnya
hingga 100 ml (Materia Medika Indonesia, 1978).
3.3.5 Pereaksi Meyer
Sebanyak 5 g kalium iodida dilarutkan dalam 20 ml air suling kemudian
ditambahkan larutan 1,36 g merkuri (II) klorida dalam 60 ml air. Larutan dikocok
dan ditambahkan air suling hingga 100 ml (Materia Medika Indonesia, 1978).
3.3.6 Pereaksi Bouchardat
Sebanyak 4 g kalium iodida dilarutkan dalam 20 ml air suling kemudian
ditambahkan 2 g Iodium sambil diaduk sambil larut, lalu ditambah air suling
hingga 100 ml (Materia Medika Indonesia,1978).
3.3.7 Pereaksi Dragendorff
Sebanyak 8 g bismuth nitrat dilarutkan dalam asam nitrat 20 ml kemudian
dicampur dengan larutan Kalium Iodida sebanyak 27,2 g dalam 50 ml air suling.
Campuran didiamkan sampai memisah sempurna. Larutan jernih diambil dan
diencerkan dengan air secukupnya hingga 100 ml (Materia Medika Indonesia,
1978).
3.3.8 Natrium Klorida 0,9%
Sebanyak 0,9 g natrium klorida dilarutkan dalam air suling 100 ml
(Farmakope Indonesia, 1979).
3.3.9 Natrium Klorida 0,0113 N
Natrium klorida sebanyak 665,0 mg (setelah dioven pada T 1100 C selama
2 jam) dilarutkan dalam air suling 100 ml di dalam labu ukur 1000 ml, lalu
3.3.10 Perak Nitrat 0,0141 N
Perak nitrat sebanyak 2,395 g dilarutkan dalam air suling 100 ml, di dalam
labu ukur 1000 ml, lalu di tambahkan air suling sampai pada garis tanda
(Basset et al., 1994).
3.3.11 Kalium Kromat 5%
Sebanyak 5 g kalium kromat dilarutkan dalam air suling 100 ml (Basset et
al., 1994).
3.3.12 Larutan Induk Kalium
Sebanyak 1,907 g kalium klorida dilarutkan dalam air suling 100 ml di
dalam labu ukur 1000ml, lalu di tambahkan air suling sampai pada tanda tara
(Basset et al, 1994).
3.3.13 Larutan Induk Natrium
Sebanyak 2,054 g (setelah di oven pada T 1100 C selama 2 jam) natrium
klorida dilarutkan dalam air suling 100 ml di dalam labu ukur 1000 ml, lalu di
tambah kan air suling samapi tanda tara ( Basset et al., 1995).
3.4 Penyiapan Bahan
Penyiapan bahan meliputi determinasi tumbuhan , pengumpulan bahan,
pengolahan sampel, pemeriksaan makroskopik dan mikrokospik sampel.
3.4.1 Determinasi Tumbuhan
Determinasi tumbuhan dilakukan di Laboratorium Taksonomi Tumbuhan,
Departemen Biologi, FMIPA Universitas Sumatra Utara.
3.4.2 Pengumpulan Sampel
Sampel yang digunakan adalah daun andong hijau yang diambil dari
perfosif yaitu mengambil daun tanpa membandingkan dengan tumbuhan yang
sama dari daerah lain.
3.4.3 Pengolahan Sampel
Daun andong (Cordyline fruticosa. Goepp) yang baru dipetik, dibersihkan
dari kotoran, dicuci dengan air bersih, ditiriskan lalu ditimbang. Kemudian
daun-daun tersebut dikeringkan di lemari pengering pada suhu kamar atau
diangin-anginkan terhindar dari pengaruh sinar matahari, setelah kering simplisia di
timbang dan di peroleh 1249 g simplisia kering dari 14 kg daun basah. Setelah itu,
simplisia di serbuk menggunakan blender dan di ayak.
3.5 Pembuatan Ekstrak Etanol
Pembuatan ekstrak daun andong dilakukan dengan cara perkolasi
menggunakan pelarut etanol 80%.
Sebanyak 300 g serbuk simplisia dimasukkan kedalam bejana tertutup dan
direndam dengan cairan penyari etanol 80%, direndam sekurang-kurangnya
selama 3 jam. Massa dipindahkan sedikit demi sedikit kedalam perkolator, sampel
tiap kali ditekan dengan hati–hati, kemudian cairan penyari dituangkan
secukupnya sampai cairan mulai menetes dan diatas simplisia masih terdapat
kira-kira 1cm atau lebih cairan penyari, perkolator ditutup dengan aluminium foil
dan dibiarkan selama 24 jam. Cairan biarkan menetes dengan kecepatan 20-60
tetes/menit, cairan penyari ditambahkan dari atas dengan menggunakan corong
pisah dengan kecepatan aliran sama dengan perkolator, sehingga selalu terdapat
kira-kira 1 cm atau lebih cairan penyari diatas simplisia, perkolasi dilakukan
sampai sempurna, diperoleh ekstrak etanol daun andong hijau 3 Liter, kemudian
etanol. Ekstrak yang diperoleh dikeringkan pada Freeze dryer. (Ditjen POM
DepKes RI, 1974). Ekstrak kental yang diperoleh sebanyak 33,450 g.
3.6 Karakterisasi Simplisia
Pemeriksaan karakterisasi simplisia meliputi penetapan kadar air,
penetapan kadar abu total, penetapan kadar abu tidak larut dalam asam,
penetapan kadar sari larut dalam air, penetapan kadar sari larut dalam etanol,
pemeriksaan makroskopik dan mikroskopik simplisia.
3.6.1 Penetapan Kadar Air
Penetapan kadar air dilakukan dengan metode Azeotropi (destilasi
toluena). Alat meliput i labu alas 500 ml, alat penampung, tabung penerima 5 ml
berskala 0,05 ml, pendingin, tabung penyambung, pemanas (WHO, 1992).
Cara Penetapan :
Ke dalam labu alas bulat di masukkan 200 ml Toluen dan 2 ml air suling,
di destilasi selama 2 jam, biarkan mendingin selama 30 menit, di dinginkan dan
volumen air pada tabung penerima di baca. Selanjutnya ke dalam labu di
masukkan 5 g serbuk simplisia yang telah di timbang seksama, lalu di panaskan
hati-hati selama 15 menit. Setelah Toluen mendidih kecepatan tetesan diatur 2
tetes tiap detik hingga sebagian air tersuling, kemudian kecepatan penyulingan di
naikkan 4 tetes tiap detik. Setelah semua air tersuling bagian dalam pendinginan
di bilas dengan Toluen. Destilasi di lanjutkan selama 2 menit, kemudian tabung
penerima di biarkan dingin sampai suhu kamar, setelah air dan Toluen memisah
sempurna volumen dibaca dengan ketelitian 0,05 ml. Selisih kedua volumen air
yang di baca sesuai kandungan air yang terdapat dalam vahan yang di periksa.
3.6.2 Penetapan Kadar Abu Total
Zat ditimbang ± 2 g dengan seksama dan dimasukkan ke dalam krus
porselin bertutup yang telah dipijar dan ditara, kemudian diratakan. Krus dipijar
perlahan-lahan sampai arang habis kemudian didinginkan dan ditimbang sampai
diperoleh bobot yang tetap (Ditjen POM, 2000).
3.6.3 Penetapan Kadar Abu Tidak Larut Dalam Asam
Abu yang diperoleh dari penetapan kadar abu total didihkan dengan 25 ml
asam klorida encer selama 5 menit. Bagian yang tidak larut dalam asam
dikumpulkan, disaring dengan kertas saring, lalu dicuci dengan air panas.
Kemudian residu dan kertas saring dipijarkan samapi diperoleh bobot tetap,
didinginkan dan ditimbang beratnya (Ditjen POM, 2000).
3.6.4 Penetapan Kadar Sari Larut Dalam Air
Sebanyak 5 g simplisia dimaserasi selama 24 jam dalam 100 ml
air-kloroform (2,5 ml air-kloroform dalam akuades samapi 1000 ml) dengan
menggunakan botol bersumbat warna coklat sambil sekali-kali dikocok selama 6
jam pertama, kemudian dibiarkan selama 18 jam dan disaring. Sejumlah 20 ml
filtrat pertama diuapkan hingga kering dalam cawan yang telah dipanaskan dan
ditara. Residu dipanaskan dalam oven pada suhu 1050C sampai diperoleh bobot
tetap (Depkes, 1995).
3.6.5 Penetapan Kadar Sari Larut Dalam Etanol
Sebanyak 5 g simplisia dimaserasi selama 24 jam dalam 100 ml etanol
96% dengan menggunakan botol bersumbat warna coklat sambil sekali-kali
dikocok selama 6 jam pertama, kemudian dibiarkan selama 18 jam dan disaring.
dipanaskan dan ditara. Residu dipanaskan dalam oven pada suhu 1050C sampai
diperoleh bobot tetap (Depkes, 1995).
3.6.6 Pemeriksaan Makroskopik Simplisia
Pemeriksaan makroskopik dilakukan pada daun andong (Cordyline
fruticosa.Goepp) dengan mengamati morfologi luar.
3.6.7 Pemeriksaan Mikroskopik Simplisia
Pemeriksaan mikroskopik terhadap simplisia daun andong dilakukan
dengan cara menaburkan serbuk simplisia di atas kaca objek yang telah diteteskan
dengan kloralhidrat dan ditutup dengan kaca penutup kemudian dilihat di bawah
mikroskop.
3.7 Skrining Fitokimia Serbuk Simplisia
Skrining fitokimia serbuk simplisia diawali dengan pemeriksaan
organoleptis kemudian dilanjutkan dengan pemeriksaan golongan alkaloida,
glikosida, saponin, tannin, dan steroida/triterpenoida.
3.7.1 Pemeriksaan Alkaloida
Sebanyak 500 mg serbuk simplisia ditambahkan 10 ml asam klorida 2 N
dipanaskan diatas penangas air selama 10 menit, didinginkan dan disaring,
kemudian 3 tetes filtrat dipindahkan pada kaca arloji dan tambahkan 2 tetes
pereaksi Bouchardart terbentuk endapan berwarna coklat sampai hitam, maka ada
kemungkinan terdapat alkaloid . Pada filtrat yang lain ditambahkan 2 tetes
pereaksi Meyer akan terdapat endapan mengumpul berwarna putih atau kuning
yang larut dalam metanol. Jika pada kedua percobaan tidak terjadi endapan , maka
serbuk tidak mengandung Alkaloid. Jika hanya terjadi kekeruhan, pemeriksaan
campuran 3 bagian volume eter dan 1 bagian volume kloroform. Fase organik
diambil dan ditambahkan natrium sulfat anhidrat P, disaring. Filtrat diuapkan di
atas penangas air, sisanya dilarutkan dalam sedikit asam klorida 2 N. Percobaan
dilakukan dengan pereaksi Meyer , Bouchardart, dan Dragendorf. Serbuk
mengandung Alkaloid jika sekurang-kurangnya terbentuk endapan dengan
menggunakan dua pereaksi. (Materia Medika Indonesia,1978).
3.7.2 Pemeriksaan Glikosida
A. Larutan Percobaan
Sebanyak 3 g serbuk simplisia disari dengan 30 ml campuran etanol 96 %
dengan air suling (7:3) dan 10 ml asam sulfat 2 N lalu di refluks selama 1
jam,dinginkan dan disaring. Pada 20 ml filtrat ditambahkan 25 ml air dan 25 ml
Timbal (II) asetat 0,4 M. Dikocok dan didiamkan selama 5 menit, disaring. Sari
filtrat 3 kali , tiap kali dengan 20 ml campuran 3 bagian volume kloroform P, dan
2 bagian volume isopropanol P. Pada kumpulan sari tambahkan Natrium Sulfat
anhidrat P, disaring dan diuapkan pada suhu tidak lebih dari 50 ˚C. Larutkan sisa
dengan 2 ml metanol.
B. Percobaan Umum Terhadap Glikosida
Cara percobaan:
a. Sebanyak 0,1 ml larutan percobaan diuapkan diatas penangas air, sisa
dilarutkan dalam 5 ml asam asetat anhidrat dan 10 tetes asam sulfat P akan terjadi
warna biru atau hijau menunjukan adanya glikosida (Reaksi Liberman- Bouchard)
b. Sebanyak 0,1 ml diuapkan diatas penangas air , pada sisa tambahkan 2 ml air
terbentuk cincin warna ungu pada batas cairan, menunjukan adanya ikatan gula
(reaksi molish) (Materia Medika Indonesia,1978).
3.7.3 Pemeriksaan Flavonoida
Larutan percobaan : Sebanyak 0,5 g serbuk di sari dengan 10 ml metanol
P, lalu di refluks selama 10 menit. Kemudian disaring panas-panas melalui kertas
saring kecil berlipat. Filtrat diencerkan dengan 10 ml air, setelah dingin
ditambahkan dengan 5 ml eter minyak tanah P, kocok hati-hati dan diamkan.
Ambil lapisan metanol, lalu diuapkan pada suhu 40˚C, sisanya dilarutkan dengan
5 ml etil asetat P, saring. Filtrat digunakan untuk uji Flavonoida dengan cara
berikut :
a. Sebanyak 1 ml larutan percobaan diuapkan sampai kering, sisa dilarutkan dalam
1 sampai 2 ml etanol 95 % P, lalu ditambahkan 0,5 g serbuk seng dan 2 ml asam
klorida 2 N, didiamkan selama 1 menit. Ditambahkan 10 tetes asam klorida P, jika
dalam waktu 2 sampai 5 menit terjadi warna merah intensif, menunjukan adanya
flavonoida (glikosida-3-Flavonol).
b. Sebanyak 1 ml larutan percobaan diuapkan sampai kering, sisa dilarutkan
dalam 1 ml etanol 95 %, lalu ditambahkan 0,1 g serbuk magnesium dan 10 tetes
asam klorida P, jika terjadi warna merah jingga hingga merah ungu menunjukan
adanya flavonoid. Jika terjadi warna kuning jingga menunjukan adanya flavon,
klakon, dan auron (Materia Medika Indonesia, 1989).
3.7.4 Pemeriksaan Saponin
Sebanyak 0,5 g serbuk dimasukkan dalam tabung pereaksi ditambahkan 10
ml air panas, dinginkan kemudian dikocok kuat–kuat selama 10 detik, (jika yang
air dan kocok kuat-kuat selama 10 menit), terbentuklah buih yang mantap selama
tidak kurang dari 10 menit, setinggi 1 sampai 10 cm. Pada penambahan 1 tetes
Asam Klorida 2 N, buihnya tidak hilang (Materia Medika Indonesia, 1989).
3.7.5 Pemeriksaan Tanin
Sebanyak 500 mg serbuk simplisia, dimasukkan kedalam tabung reaksi.
Ditambahkan 10 ml air, dikocok–kocok dan disaring. Ambil sedikit filtratnya,
kemudian diencerkan dengan air sampai hampir tidak berwarna. Teteskan tetes
demi tetes dengan larutan feri klorida 10 % sampai terbentuk warna biru hitam /
kehijauan (Farnsworth, 1996).
3.7.6 Pemeriksaan Steroida/Triterpenoida
Sejumlah 1 g serbuk simplisia dimaserasi dengan 20 ml eter selama 2 jam
kemudian disaring. Filtrat digunakan untuk reaksi berikut : 5 ml larutan eter
diuapkan dalam cawan penguap kedalam sisa ditambahkan 2 tetes asam asetat
anhidrat dan 1 tetes asam sulfat P. Reaksi steroida/triterpenoida positif bila terjadi
warna ungu atau biru hijau (Harbone,1987).
3.8 Penyiapan Bahan Uji, Kontrol, dan Obat Pembanding
Ekstrak etanol daun andong hijau dibuat dalam bentuk suspensi (CMC 5
mg), dosis EEDA adalah 100 mg/kgbb, 200 mg/kgbb , 400mg/kgbb . Obat
pembanding furosemid dosis 3,6 mg/kgbb dibuat dalam bentuk suspensi. Kontrol
yang digunakan adalah suspensi CMC 5 mg.
Sebanyak 0,5 g CMC ditaburkan kedalam lumpang yang berisi aquadest
yang panas sebanyak 10 ml gerus cepat hingga diperoleh masa yang transparan.
Kemudian setelah kembang digerus lalu diencerkan dengan sedikit air, kemudian
dimasukkan kedalam labu tentukur 100 ml, volumenya dicukupkan hingga 100
ml.
3.10 Pembuatan Suspensi Furosemid
Dalam lumpang yang berisi 40 mg furosemid yang telah digerus halus
ditambahkan suspensi CMC 0,5% sedikit demi sedikit sambil terus digerus,
kemudian dimasukkan kedalam labu tentukur 10 ml, volumenya dicukupkan
hingga 10 ml. Perhitungan pembuatan suspense furosemid dapat di lihat pada
Lampiran 18, halaman 50.
3.11 Pembuatan Larutan Induk Dosis 100 mg/kgbb, dosis 200 mg/kgbb, dan dosis 400 mg/kgbb Suspensi Ekstrak Etanol Daun Andong
Dalam lumpang yang berisi ekstrak etanol daun andong hijau 1,0 g
tambahkan suspensi CMC 0,5 % sedikit demi sedikit sambil terus digerus lalu
masukkan kedalam labu tentukur 50 ml, kemudian dicukupkan volumenya
hingga 50 ml. Perhitungan pembuatan suspensi ekstrak etanol pada dosis
100 mg/kgbb dapat di lihat pada Lampiran 19, halaman 51.
3.12 Persiapan Hewan Percobaan
Hewan percobaan yang digunakan didalam percobaan ini adalah tikus
putih jantan yang sehat dengan berat badan antara 180g-220g sebanyak 30 ekor..
Beberapa hari sebelum percobaan dimulai dilakukan pra perlakuan untuk
sehat ditandai dengan kenaikan berat badan yang teratur dan memperlihatkan
gerakan yang lincah.
3.13 Prosedur Kerja Untuk Pengujian Farmakologi
Untuk pengujian farmakologi digunakan CMC 5 mg sebagai kontrol
negatif, suspensi EEDAH dosis 100 mg/kgbb, dosis 200 mg/kgbb, dosis 400
mg/kgbb, suspensi Furosemid dengan dosis 3,6 mg/kgbb sebagai pembanding.
Tikus dibagi dalam 5 kelompok dengan setiap kelompok terdiri dari 6 ekor tikus
putih jantan.
Kelompok I : kontrol negatif (CMC 5 mg)
Kelompok II : kontrol positif ( Furosemid dosis 3,6 mg/kgbb)
Kelompok III : diberi suspensi bahan uji dengan dosis kecil 100 mg/kgbb
Kelompok IV : diberi suspensi bahan uji dengan dosis sedang 200 mg/kgbb
Kelompok V : diberi suspensi bahan uji dengan dosis sedang 400 mg/kgbb
Selanjutnya sebelum dilakukan pengujian terlebih dahulu hewan
dipuasakan dari makan dan minum selama 18 jam. Kemudian masing-masing
hewan uji bobot tubuhnya ditimbang. Selanjutnya hewan uji diletakkan didalam
kandang metabolisme modifikasi yang terbuat dari silinder plastik yang
dihubungkan dengan corong besar dan botol penampung dibawahnya urin yang
dikeluarkan. Volume urin yang diekskresikan dicatat selama 6 jam. (Wattimena,
1993).
3.14 Penentuan Kadar Natrium dan Kalium dengan AAS (Atomic Absorption Spectrophotometry)
Satu ml urin tikus diencerkan sampai 50 ml dengan aquabidest. Pada
perlahan-lahan dan uapkan di hot plate pada temperatur 150 ˚C hingga volume
sampai larutan menjadi 20 ml. Dan hingga larutan jernih-berwarna, kemudian di
saring dengan kertas whatman 0,45 µm. Filtrat di pindahkan dalam labu ukur 100
mL bilas beker dengan bantuan 5 mL air suling, hasil cuciannya di masukan ke
dalam labu ukur dan volume larutan ditepatkan menjadi 100 ml maka larutan siap
untuk diukur (SNI, 2004). Dengan alat AAS untuk natrium pada panjang
gelombang 589 nm dan kalium pada panjang gelombang 766,5 nm dan gas yang
dipakai adalah gas asetilen dengan suhu nyala 1900-2200˚C.
3.15 Pengolahan Data
Data hasil pengukuran volume urin total tikus, kadar Natrium dan Kalium
urin yang didapatkan, kemudian diolah secara statistik dengan menggunakan
Statistical Product and Service Solution (SPSS) 16.0 dalam rancangan acak
lengkap (RAL). Data numeric lebih dari dua variable diuji dengan oneway Anava,
serta dilanjutkan dengan analisa Duncan α = 0,5 yaitu uji beda rata-rata perlakuan
BAB IV
HASIL DAN PEMBAHASAN
Pada penelitian ini digunakan daun andong hijau (Cordyline fruticosa.
Goepp) untuk diuji efek diuretika yang sebelumnya telah dilakukan determinasi
tumbuhan Laboratorium Taksonomi Tumbuhan, Departemen Biologi (FMIPA)
Universitas Sumatra Utara. Hasil dapat dilihat pada lampiran 1, halaman 32,
gambar tumbuhan dapat dilihat pada lampiran 2 hal 33.
Penyarian terhadap daun andong dilakukan secara perkolasi dengan
pelarut etanol 80%, dimana diharapkan senyawa kimia yang terkandung
didalamnya dapat tersari. Hasil pengumpulan sampel sebanyak 14 kg
menghasilkan 1,249 kg simplisia kering dan dari 1 kg simplisia kering didapat
300 g serbuk simplisia diperoleh ekstrak etanol kental 33,45 g.
4.1 Hasil Karakterisasi Simplisia
Standarisasi simplisia daun andong belum tercantum dalam monografi
tumbuhan ( Materia Medika Indonesia). Hasil penetapan kadar air simplisia daun
andong adalah 5,99%, jika dilihat dari standarisasi pemeriksaan kadar air diatas
memenuhi persyaratan dalam MMI yaitu < 10%. Hasil karakterisasi simplisia dun
andong yag didapat ini diharapkan sebagai acuan guna pemenuhan terhadap
persyaratan sebagai bahan dan penetapan nilai berbagai parameter dari produk.
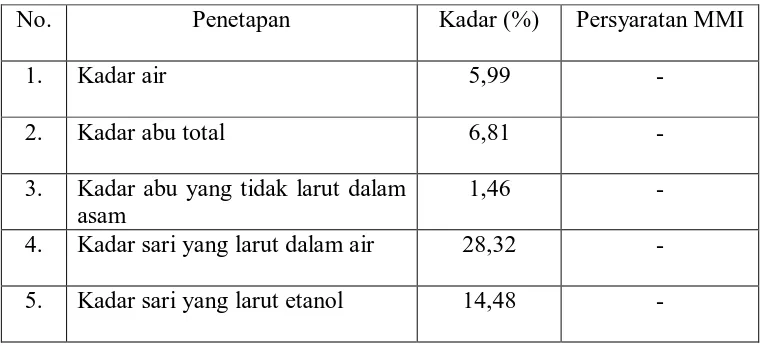
Hasil pemeriksaan karakterisasi simplisia daun andong dapat dilihat pada tabel 1
Tabel 1. Hasil Karakterisasi Simplisia Daun Andong
Penetapan kadar air dilakukan untuk memberi batasan atau rentang
besarnya kandungan air didalam simplisia, karena tingginya kandungan air
menyebabkan ketidakstabilan sediaan obat (cemaran bakteri) dan bahan aktifnya
(penguraian secara kimia). Penetepan kadar sari larut dalam air dan etanol untuk
mengetahui banyaknya senyawa polar yang larut dalam air etanol. Sedangkan
penetapan kadar abu total dan kadar abu tidak larut larut asam untuk mengetahui
kandungan mineral yang ada pada simplisia, kadar abu total yang tinggi
menunjukkan banyaknya kandungan zat anorganik seperti logam-logam yang
dalam jumlah yang tinggi dapat membahayakan kesehatan.
4.2 Hasil Pengujian Farmakologi
Pada penelitian ini digunakan 3 kelompok perlakuan yaitu kelompok
kontrol, kelompok uji dan kelompok pembanding. Kelompok kontrol dilakukan
untuk mengetahui volume total urin, kadar natrium urin dan kadar kalium urin.
Kelompok uji yang terdiri dari 3 perlakuan dengan pemberian ekstrak etanol
dengan dosis yang berbeda yaitu dosis 100 mg/kgbb, 200 mg/kgbb dan 400
mg/kgbb dilakukan untuk mengetahui kemampuan bahan uji dalam memberikan
No. Penetapan Kadar (%) Persyaratan MMI
1. Kadar air 5,99 -
2. Kadar abu total 6,81 -
3. Kadar abu yang tidak larut dalam asam
1,46 -
4. Kadar sari yang larut dalam air 28,32 -
efek diuretika. Sedangkan kelompok pembanding yang menggunakan furosemid
dengan dosis 3,6 mg/kgbb diperlukan untuk melihat pengaruh obat diuretika oral
yang telah terbukti khasiatnya untuk meningkatan pengeluaran urin, natrium dan
kalium. Penentuan kadar natrium dan kalium dalam urin menggunakan alat
Spektrofotometer Serapan Atom (Atomic Absorbsion Spectrofotometer/AAS).
Data volume urin total dapat dilihat pada Tabel 3.1.
Tabel 3.1 : Data volume urin total ± SD pada pemberian EEDA dosis 100 mg/kgbb, 200 mg/kgbb, 400 mg/kgbb, Furosemid 3,6 mg/kgbb dan Kontrol (CMC 5 mg) dengan pengulangan n=6.
Dari Tabel 3.1 didapat bahwa rata-rata jumlah volume urin total pada
kontrol (CMC 5 mg) volume total dan SD adalah 3,06±0,39 ml, dosis 100
mg/kgbb volume total dan SD adalah 3,86±0,34 ml, dosis 200 mg/kgbb volume
total dan SD adalah 4,58±1,33 ml, pada dosis 400 mg/kgbb volume total dan SD
adalah 5,06±0,81 ml dan furosemid volume total dan SD adalah 5,68±0,96 ml.
Berdasarkan data volume urin total yang dihasilkan maka dapat dikatakan bahwa
furosemid memberikan efek diuretika yaitu peningkatan jumlah volume urin yang
dikeluarkan oleh tubuh dibandingkan terhadap volume urin total dari kelompok
kontrol (CMC 5 mg). Dari Tabel 3.1 selanjutnya dilakukan uji Anava, rancangan
acak lengkap (RAL) dapat dilihat pada Tabel 3.2 dan untuk uji Duncan dapat
disajikan pada table 3.3.
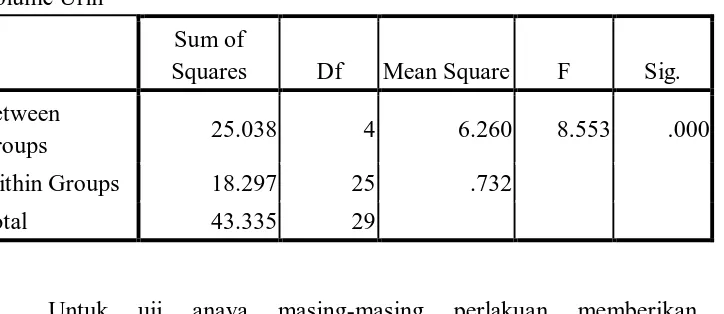
Table 3.2 Hasil Perhitungan SPSS dari Volume Urin
ANAVA
Untuk uji anava masing-masing perlakuan memberikan nilai
signifikansinya adalah 0,00 sehingga dapat dinyatakan bahwa perbedaan antara
perlakuan adalah bermakna, untuk ini maka perlu dilanjutkan dengan uji beda
rata-rata dari masing-masing perlakuan dengan uji Duncan. Uji Duncan dapat di
sajikan pada Tabel 3.3. Volume Urin
Sum of
Squares Df Mean Square F Sig.
Between
Groups 25.038 4 6.260 8.553 .000
Within Groups 18.297 25 .732
3.3 Hasil Perhitungan SPSS dari Volume Urin DUNCAN
Homogeneous Subset
Hasil uji Duncan menunjukkan bahwa EEDA dosis 400 mg/kgbb yang
menunjukkan kesetaraannya dengan furosemid dengan signifikasinya 0.337 yang
lebih besar dari 0.05 (p>0,05). Jadi EEDAH dosis 400 mg/kgbb dapat dikatakan
memberikan efek diuretika.
Volume Urin
Perlakuan N
Subset for alpha = 0.05
1 2 3 4
Duncana Kontrol (CMC 5 mg) 6 3.0667
EEDAH 100 mg/kgbb 6 3.8667 3.8667
EEDAH 200 mg/kgbb 6 4.5833 4.5833
EEDAH 400 mg/kgbb 6 5.0667 5.0667
Furosemid 3,6
mg/kgbb 6 5.6833
Sig. .118 .159 .337 .223
Untuk kelompok kontrol didapatkan nilai yang setara dengan perlakuan
EEDAH dosis 100 mg/kgbb dan untuk EEDAH 200 mg/kgbb setara dengan
EEDAH dosis 400 mg/kgbb, sedangkan nilai EEDAH 400 mg/kgbb setara dengan
furosemid dosis 3,6 mg/kgbb. Maka dapat dikatakan dosis EEDAH 100 mg/kgbb,
EEDAH 200 mg/kgbb menunjukkan nilai yang berbeda dengan suspensi
furosemid sebagai pembanding positif efek diuretika. Dan pada dosis 400
mg/kgbb menunjukkan efeknya sebagai diuretika yang setara efeknya dengan
furosemid sebagai diuretika. Selain volume urin total yang di uji dalam
menentukan diuretika dalam urin dari uji EEDAH, dilakukan pula uji penentuan
kadar natrium dalam urin dengan menggunakan alat AAS datanya dapat di lihat
pada Tabel 3.4.
Untuk dapat memperjelas penjelasan di atas dapat dilihat lebih lanjut pada gambar
3.1. Nilai Rata-rata Volume Urin Tikus
3.06
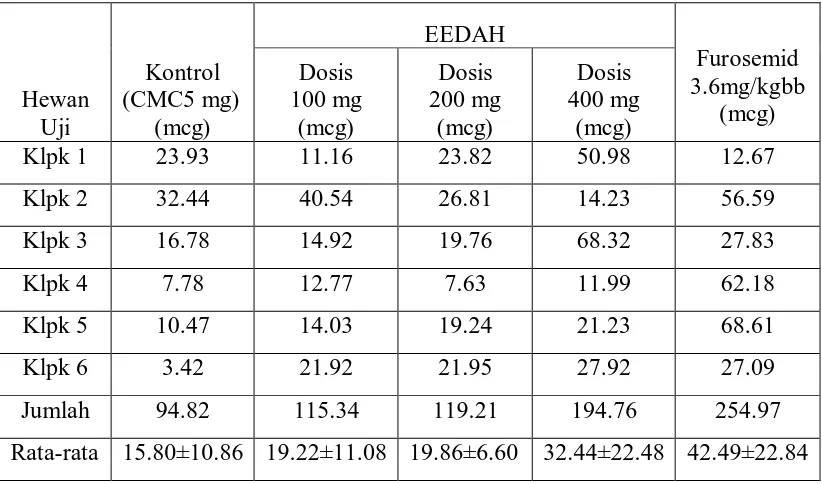
Tabel 3.4 : Data kadar natrium urin total ± SD pada pemberian EEDAH dosis 100 mg/kgbb, 200 mg/kgbb, 400 mg/kgbb, kontrol (CMC mg) dan furosemid 3,6 mg/kgbb dengan pengulangan n=6
Dari Tabel 3.4 didapat bahwa rata-rata jumlah kadar natrium urin total
pada kontrol (CMC 5 mg) adalah 15,80±10,86 mcg, EEDAH dosis 100 mcg
adalah 19.22±11.08 mcg, EEDAH dosis 200 mcg adalah 19,86±6,60 mcg
EEDAH pada dosis 400 mg adalah 32,44±22,48 mcg dan furosemid adalah
42,49±22,84 mcg,. Berdasarkan data kadar natrium urin total yang dihasilkan
maka dapat dikatakan bahwa furosemid memberikan efek diuretika yaitu
peningkatan jumlah volume urin yang dikeluarkan oleh tubuh dibandingkan
terhadap kadar natrium urin total dari kelompok kontrol (CMC 5 mg). Dari Tabel
3.4 selanjutnya dilakukan uji Anava, rancangan acak lengkap (RAL) dapat dilihat
pada table 3.5 untuk uji Duncan dapat disajikan pada table 3.6. Hewan
3.5 Hasil Perhitungan SPSS dari Kadar Natrium Urin
Untuk uji anava masing-masing perlakuan memberikan nilai
signifikansinya adalah 0,44 sehingga dapat dinyatakan bahwa perbedaan antara
perlakuan adalah bermakna, untuk ini maka perlu dilanjutkan dengan uji beda
rata-rata dari masing-masing perlakuan dengan uji Duncan.
3.6 Hasil Perhitungan SPSS dari Kadar Natrium Urin DUNCAN
Means for groups in homogeneous subsets are displayed. a. Uses Harmonic Mean Sample Size = 6.000.
Hasil uji Duncan menunjukkan bahwa EEDAH dosis 400 mg/kgbb yang
menunjujkkan kesamaannya dengan furosemid dengan signifikasinya 0,293 yang
lebih besar dari 0,05 (p>0,05). Jadi EEDAH dosis 400 mg/kgbb dapat dikatakan
memberikan efek diuretika. Selain volume urin total yang di uji dalam
menentukan diuretika dalam urin dari uji EEDAH, dilakukan pula uji penentuan
kadar kalium dalam urin dengan menggunakan alat AAS datanya dapat di lihat
pada Tabel 3.7.
Untuk kelompok kontrol didapatkan nilai yang setara dengan perlakuan
EEDAH dosis 100 mg/kgbb dan untuk EEDAH 200 mg/kgbb setara dengan
EEDAH dosis 400 mg/kgbb, sedangkan nilai EEDAH 400 mg/kgbb setara dengan
furosemid dosis 3,6 mg/kgbb. Maka dapat dikatakan dosis EEDAH 100 mg/kgbb,
EEDAH 200 mg/kgbb menunjukkan nilai yang berbeda dengan suspensi
furosemid sebagai pembanding positif efek diuretika. Dan pada dosis 400
mg/kgbb menunjukkan efeknya sebagai diuretika yang setara efeknya dengan
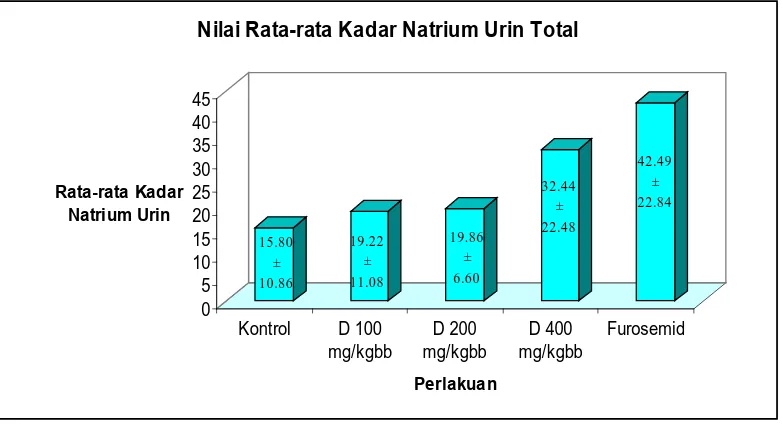
furosemid sebagai diuretika. Untuk memperjelas penjelasan di atas dapat dilihat
lebih lanjut pada gambar 3.2.
0
Nilai Rata-rata Kadar Natrium Urin Total
15.80
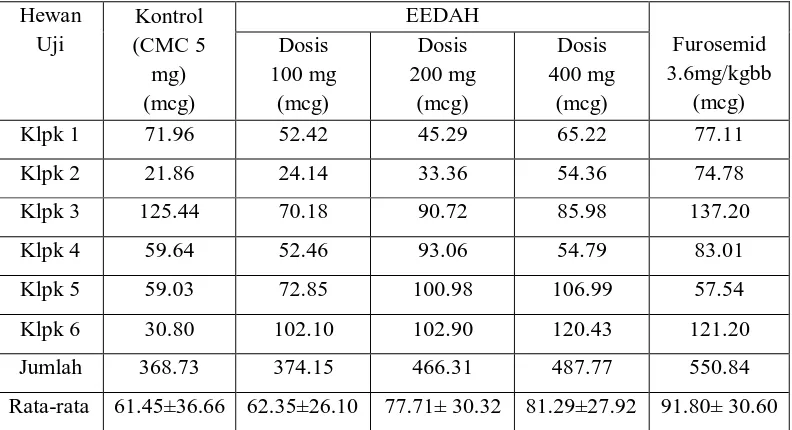
Tabel 3.7 : Data kadar kalium urin total ± SD pada pemberian EEDA dosis 100 mg/kgbb, 200 mg/kgbb, 400 mg/kgbb, kontrol (CMC 5 mg), dan furosemid 3,6 mg/kg bb dengan pengulangan n=6.
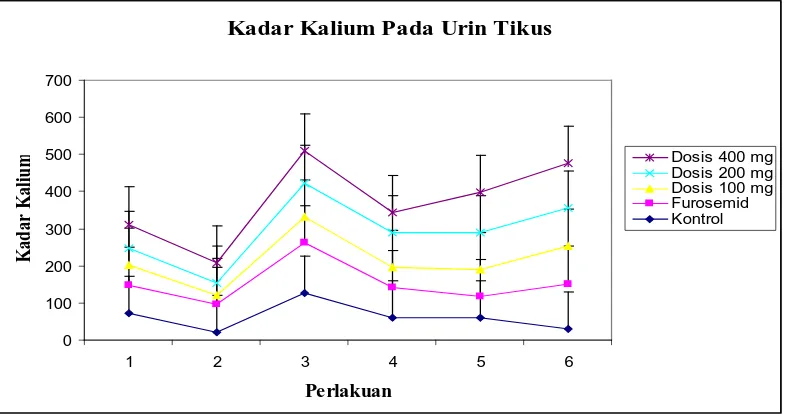
Dari tabel 3.7 didapat bahwa rata-rata jumlah kadar kalium urin total pada
kontrol (CMC 5 mg) volume total dan SD adalah 61,45±36,66 ml, dosis 100
mg/kgbb volume total dan SD adalah 62,35±26,10 ml, dosis 200 mg/kgbb volume
total SD adalah 77,71±30,32 ml, pada dosis 400 mg/kgbb volume total dan SD
adalah 81,29±27,92 ml dan furosemid (3,6 mg/kgbb) volume total dan SD adalah
91,80±30,60 ml. Berdasarkan data di atas kadar kalium urin yang dihasilkan maka
dapat dikatakan bahwa furosemid memberikan efek diuresis yaitu peningkatan
jumlah kadar kalium yang dikeluarkan oleh tubuh dibandingkan terhadap kadar
kalium urin total dari kelompok kontrol (CMC 5 mg). Dari tabel 3.7 selanjutnya
dilakukan dengan uji Anava rancangan acak lengkap (RAL) dapat dilihat pada
Tabel 3.8.