Ekstrak kental etanol
buah adas manis
Ekstrak kering buah adas manis
Skrining fitokimia untuk pemeriksaan : a. Alkaloida
b. Flavanoida c. Glikosida
d. Antrakinon glikosida e. Saponin
f. Tanin
g. Steroida / triterpenoida
Uji toksisitas akut
Dikeringkan dengan freeze dryer pada suhu -40oC
500g buah adas manis
Dibersihkan
Dimaserasi dengan pelarut etanol 80%
Maserat
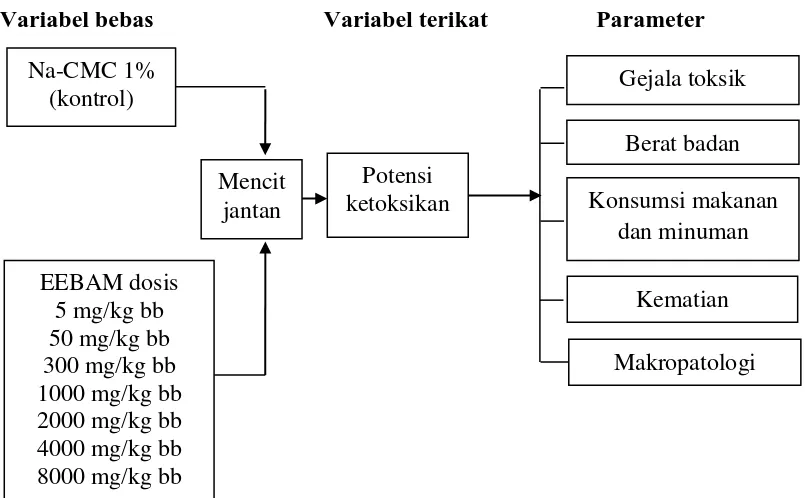
Lampiran 5. Bagan penelitian uji toksisitas ekstrak etanol buah adas manis
Gejala klinis, konsumsi makanan dan minuman, berat badan, kematian, makropatologi organ hewan coba (14 hari)
Berat badan mencit 25 kg dengan dosis EEBAM 1000 mg/kg bb
Dosis = 1000 mg/kg bb
= (25 : 1000 kg) x 1000 mg/kg
= 25 mg
Konsentrasi ekstrak yang dibuat 8 % = 8 g/ 100 ml
= 8000 mg/100 ml
= 80 mg/ml
Jumlah obat yang disuntik = 25 mg : 80 mg/ml
= 0,31 ml
Lampiran 7. Hasil pengukuran berat badan 1. Berat badan pada minggu pertama
Perlakuan Berat badan hari ke- (g)
0 3 7
kontrol I 25,78 28,08 28,02
kontrol II 27,09 29,48 28,37
kontrol III 29,98 29,89 29,17
kontrol IV 30,16 30,79 29,93
kontrol V 30,84 30,81 30,66
Dosis 5 mg/kg bb 27,86 28,05 28,28
Dosis 5 mg/kg bb 28,19 28,16 29,25
Dosis 5 mg/kg bb 28,55 29,48 30,56
Dosis 5 mg/kg bb 29,68 29,99 31,39
Dosis 5 mg/kg bb 30,52 31,57 31,77
Dosis 50 mg/kg bb 27,25 27,55 28,78
Dosis 50 mg/kg bb 27,68 28,87 29,69
Dosis 50 mg/kg bb 28,46 29,61 29,84
Dosis 50 mg/kg bb 30,28 29,67 30,56
Dosis 50 mg/kg bb 31,98 31,55 31,03
Dosis 300 mg/kg bb 30,72 32,14 33,18
Dosis 300 mg/kg bb 28,69 29,09 29,24
Dosis 300 mg/kg bb 29,55 29,73 29,83
Dosis 300 mg/kg bb 29,5 31,01 31,13
Dosis 300 mg/kg bb 29,96 30,17 30,59
Dosis 1000 mg/kg bb 31,02 31,19 33,11
Dosis 1000 mg/kg bb 28,97 28,63 28,77
Dosis 1000 mg/kg bb 29,28 31,27 28,15
Dosis 1000 mg/kg bb 25,94 27,42 29,55
Dosis 1000 mg/kg bb 29,03 30,43 29,03
Dosis 2000 mg/kg bb 30,97 32,84 31.69
Dosis 2000 mg/kg bb 28,93 29,01 29,29
1. Berat badan pada minggu pertama
Perlakuan Berat badan hari ke- (g)
0 3 7
Dosis 2000 mg/kg bb 29,05 29,65 30,41
Dosis 2000 mg/kg bb 29,09 30,95 30,59
Dosis 4000 mg/kg bb 32,65 31,33 33,98
Dosis 4000 mg/kg bb 28,95 29,45 28,65
Dosis 4000 mg/kg bb 31,09 31,66 31,93
Dosis 4000 mg/kg bb 31,02 30,16 31,13
Dosis 4000 mg/kg bb 30,96 30,86 32,39
Dosis 8000 mg/kg bb 31,26 31,93 33,19
Dosis 8000 mg/kg bb 29,21 30,68 29,26
Dosis 8000 mg/kg bb 30,47 30,54 31,38
Dosis 8000 mg/kg bb 30,81 30,89 31,37
Lampiran 7. (lanjutan)
2. Berat badan pada minggu kedua
Perlakuan Berat badan hari ke- (g)
0 10 14
kontrol I 25,78 28,89 29,07
kontrol II 27,09 29,02 29,13
kontrol III 29,98 29,16 29,98
kontrol IV 30,16 30,38 31,13
kontrol V 30,84 31,45 31,24
Dosis 5 mg/kg bb 27,86 29,17 29,97
Dosis 5 mg/kg bb 28,19 29,43 30,66
Dosis 5 mg/kg bb 28,55 30,98 30,74
Dosis 5 mg/kg bb 29,68 31,08 32,64
Dosis 5 mg/kg bb 30,52 32,14 32,69
Dosis 50 mg/kg bb 27,25 29,29 29,86
Dosis 50 mg/kg bb 27,68 29,42 30,19
Dosis 50 mg/kg bb 28,46 29,68 30,99
Dosis 50 mg/kg bb 30,28 31,65 31,18
Dosis 50 mg/kg bb 31,98 31,66 31,68
Dosis 300 mg/kg bb 30,72 33,16 34,16
Dosis 300 mg/kg bb 28,69 29,33 30,93
Dosis 300 mg/kg bb 29,55 31,09 32,21
Dosis 300 mg/kg bb 29,5 31,98 33,14
Dosis 300 mg/kg bb 29,96 31,58 32,64
Dosis 1000 mg/kg bb 31,02 32,24 33,72
Dosis 1000 mg/kg bb 28,97 29,19 30,49
Dosis 1000 mg/kg bb 29,28 30,99 32,37
Dosis 1000 mg/kg bb 25,94 30,91 32,43
Dosis 1000 mg/kg bb 29,03 30,88 32,54
Dosis 2000 mg/kg bb 30,97 33,25 33,48
Dosis 2000 mg/kg bb 28,93 29,86 30,44
2. Berat badan pada minggu kedua
Perlakuan Berat badan hari ke- (g)
0 10 14
Dosis 2000 mg/kg bb 29,05 30,63 31,61
Dosis 2000 mg/kg bb 29,09 31,75 32,11
Dosis 4000 mg/kg bb 32,65 34,12 34,17
Dosis 4000 mg/kg bb 28,95 30,91 31,75
Dosis 4000 mg/kg bb 31,09 32,06 33,15
Dosis 4000 mg/kg bb 31,02 31,82 32,98
Dosis 4000 mg/kg bb 30,96 32,66 34,68
Dosis 8000 mg/kg bb 31,26 33,18 33,68
Dosis 8000 mg/kg bb 29,21 32,19 32,78
Dosis 8000 mg/kg bb 30,47 31,54 31,82
Dosis 8000 mg/kg bb 30,81 32,19 32,61
Lampiran 8. Perhitungan karakterisasi simplisia buah adas manis
Volume air akhir Volume air sebenarnya
1 5,0000 1,4000 1,7500 0,3500
2 5,1550 2,0000 2,4500 0,4500
b. Penetapan kadar sari larut etanol
Lampiran 8. (Lanjutan)
c. Penetapan kadar sari larut air
Lampiran 8. (Lanjutan)
e. Penetapan kadar abu tidak larut asam
Lampiran 9. (Lanjutan) b. Penetapan kadar abu total
Lampiran 10. Hasil analisis data SPSS berat badan mencit
Test of Homogeneity of Variances
Levene Statistic df1 df2 Sig.
2.098 7 32 .073
Tukey
(I) perlakuan (J) perlakuan
Lampiran 10. (Lanjutan) b. Berat badan minggu I
Descriptives
Test of Homogeneity of Variances
Levene Statistic df1 df2 Sig.
.215 7 32 .979
Tukey
(I) perlakuan (J) perlakuan
Lampiran 10. (Lanjutan) c. Berat badan minggu 2
Descriptives
(I) perlakuan (J) perlakuan
Mean
Test of Homogeneity of Variances Levene
Statistic df1 df2 Sig.
Lampiran 11. Hasil analisis data SPSS konsumsi makanan mencit a. Berat Makanan minggu I
Descriptives
(I) perlakuan (J) perlakuan
Lampiran 11. (Lanjutan) b. Berat makanan minggu II
Descriptives
(I) perlakuan (J) perlakuan
Lampiran 12. Hasil analisis data SPSS konsumsi minuman mencit a. Volume minuman minggu I
Descriptives
(I) perlakuan (J) perlakuan
Lampiran 12. (Lanjutan)
b. Volume minuman minggu II
Descriptives
(I) perlakuan (J) perlakuan
Lampiran 13. Gambar makropatologi organ hati dan ginjal mencit 1. Organ hati
CMC Na 1% EEBAM 5 mg/kg bb
EEBAM 50 mg/kg bb EEBAM 300 mg/kg bb
EEBAM 1000 mg/kg bb EEBAM 2000 mg/kg bb
2. Organ ginjal
CMC Na 1% EEBAM 5 mg/kg bb
EEBAM 50 mg/kg bb EEBAM 300 mg/kg bb
DAFTAR PUSTAKA
Anggraini, D.R. (2008). Gambaran Makroskopik dan Mikroskopik Hati dan Ginjal Mencit Akibat Pemberian Plumbum Asetat. Tesis. Medan: Sekolah Pascasarjana Universitas Sumatera Utara.
BPOM RI. (2014). Peraturan Kepala Badan Pengawas Obat Dan Makanan Republik Indonesia Nomor 7 Tahun 2014 Tentang Pedoman Uji Toksisitas Nonklinik Secara In Vivo. Jakarta: Badan Pengawasan Obat dan Makanan RI. Halaman 3-4, 9, 11-12,28-32.
Chatterjee, S., Goeswami, N., dan Bhatnagar, P. (2012). Estimation of Phenolic Components and in vitro Antioxidant Activity of Fennel (Foeniculum vulgare) and Ajwain (Trachyspermum ammi) seeds. Advances in Bioresearch. 3(2): 109-118.
Cheville, N.F. (1999). Introduction to Veterinary Pathology. Edisi II. Lowa: Low State University Press. Halaman 214.
Covelli, V. (1972). Guide to The Necropsy of The Mouse. Diakses tanggal 26 Desember 2015. http://www.eulep.org/Necropsy-of-the-Mouse.php? file=Chapter-4html.
Dalimartha, setiawan. (1999). Atlas Tumbuhan Obat Indonesia. Jilid I. Jakarta: Trubus Agriwidya. Halaman 1-6.
Depkes RI. (1989). Materia Medika Indonesia. Jilid V. Jakarta: Departemen Kesehatan RI. Halaman 194-197.
Depkes RI. (1995). Materia Medika Indonesia. Jilid VI. Jakarta: Departemen Kesehatan Republik Indonesia. Halaman 333-337.
Depkes RI. (2001). Inventaris Tanaman Obat Indonesia. Jilid I. Jakarta: Badan Penelitian dan Pengembangan Kesehatan. Halaman 143-144.
Dewoto, H.R. (2007). Pengembangan Obat Tradisional Indonesia Menjadi Fitofarmaka. Jurnal Majalah Kedokteran Indonesia. 57(7): 208.
Ditjen POM RI. (1979). Farmakope Indonesia. Edisi III. Jakarta: Departemen Kesehatan Republik Indonesia. Halaman. 7, 33, 744, 748.
Ditjen POM RI. (2000). Parameter Standar Umum Ekstrak Tumbuhan Obat. Jakarta: Departemen Kesehatan RI. Halaman 10-11, 17.
Ditjen POM RI. (2008). Farmakope Herbal Indonesia. Jilid I. Jakarta: Departemen Kesehatan Republik Indonesia. Halaman 2.
Journal of Pharmaceutical Science. 55(3): 262-263.
Ganiswara, S.G. (1995). Farmakologi Dan Terapi. Edisi IV. Jakarta: Bagian Farmakologi Fakultas Kedokteran Universitas Indonesia. Halaman 763-764.
Gupta, D., dan Bhardwaj, S. (2012). Study of Acute, Subacute and Chronic Toxicity Test. International Journal of Advanced Research in Pharmaceutical and Bio Sciences (IJARPB). 1(2): 103-129.
Guyton, A.C., dan Hall, J.E. (2008). Buku Ajar Fisiologi Kedokteran. Edisi XXII. Jakarta: Penerbit Buku Kedokteran EGC.
Hage, L.S. (1982). The Anatomy Workbook. Philadelphia: Printed Lipincott Company. Halaman 83.
Husada, Y. (1996). Fisiologi dan Pemeriksaan Biokimiawi Hati dalam:
Soeparman. Ilmu Penyakit Dalam Jilid 1. Edisi III. Jakarta: Balai Penerbit FKUI. Halaman 244- 37.
Iwuanyanwu K., Amadi, U., Charles, I., dan Ayalogu, E. (2012). Evaluation of Acute and Subchronic Oral Toxicity Studi of Baker Cleanser Bitters A Polyherbal Drug On Experimental Rat. EXCLI Journal 11(1): 632-640. Janwal, N., Kumar, S., dan Rana, A. (2013). Phytochemical and Pharmacological
Review on Foeniculum vulgar. Pharma Science Monitor 4 (3): 324-341. Jenova, R. (2009). Uji Toksisitas Akut yang Diukur dengan Penentuan LD50
Ekstrak Herba Putr I Malu (Mimosa pudicaL.) terhadap Mencit BALB/C.
Skripsi. Semarang: Fakultas Kedokteran Universitas Diponegoro.
Jones, L.M., Nicholson, H.B., Leslie, E.M., dan Donald. (1997). Veterinary Pharmacology and Therapeutics. Fouth Edition. New Delhi: Oxford and IBH Publishing. Halaman 1223-1232.
Jubb, K.V.F., Kennedy, P.C., dan Peter, C. (1993). Pathology of Domestic Animal. London: Academic Press. Halaman 325-327.
Koeman, J.H. (1987). Pengantar Umum Toksikologi. Terjemahan oleh Yudono R.H. Yogyakarta: Gadjah Mada University Press. Halaman 3 - 6, 23 - 34.
Kusdarwati, R., Sari, L., dan Mukti, A. (2010). Daya Antibakteri Ekstrak Buah Adas (Foeniculum vulgare) Terhadap Bakteri Micrococcus luteus Secara In Vitro. Jurnal Ilmiah Perikanan dan Kelautan. 2(1): 31-35.
Lu, F. C. (1995). Toksikologi Dasar: Asas, Organ Sasaran, dan Penilaian Resiko. Edisi II. Jakarta: UIP. Halaman 85-86.
Malole, M.B.M., dan Pramono. C.S.U. (1989). Penggunaan Hewan Percobaan di Laboratorium. Bogor: Institut Pertanian Bogor. Halaman 45.
Nandy, S., dan Datta. (2012). Acute and Subacute Toxicity Studies of Methanolic Leaves Extract of Pterospermum acerifolium (L.) Willd in Rodents. Int. J. of Pharm. And Life Sci 3(3): 1519-1529.
Nassar, I., M., Aboutabl, E., A., Makled, Y., A., dan Osman, A., F. (2010). Secondary Metabolites and Pharmacology of Foeniculum vulgare Mill. Subsp. Piperitum. Rev. Latinoamer. Quim 38(2): 103-112.
Nuris, D. N. (2011) Aneka Manfaat Biji-bijian. Yogyakarta: Penerbit Gava Media. Halaman 3-6.
Oktriana, N.H., dan Nurlela. (2011). Toksisitas Pemberian Berulang Infusa Pegagan (Centella asiatica (L.) Urb) terhadap Tikus Jantan Galur Aprague-Dawley Tinjauan Terhadap Parameter Hematologis. Prosiding Seminar Nasional Sains dan Teknologi ke-2. Halaman 57.
Oulmouden, F., Saile, R., Gnaoui, N., Benomar, H., Lkhider, M., Amrani, S., dan Ghalim, M. (2014). Hypolipidemic and Anti-Atherogenic Effect In An Experimental Model Of Atherosclerosis Induced By Triton WR-1339.
European Journal Of Scientific Research. 3(1): 42-52..
Praptiwi, Wulansari, D., dan Chairul. (2010). Efek Toksisitas Ekstrak Pegagan (Centella asiatica Linn.) pada Organ dan jaringan mencit (Mus musculus).
Majalah Farmasi Indonesia 21 (1). Halaman 45-46.
Price, S.A., dan Wilson L.M. (2006). Patofisiologi: Konsep Klinis Proses-Proses Penyakit. Edisi VI. Jakarta: ECG. Halaman 867- 875.
Purnomo, B. (2009). Dasar-dasar Urologi. Jakarta: Sagung Seto.
Priyatno. (2009). Toksikologi Mekanisme, Terapi Antidotum, dan Penilaian Resiko. Jakarta: Leskonfi (Lembaga Studi dan Konsultasi Farmakologi). Halaman 9 - 15, 41 - 56, 151 - 167.
(Pandanus conoideus Lam.) Secara In Vivo. Bogor: Fakultas Teknologi
Pertanian Institut Pertanian Bogor. Halaman 30-31.
https://core.ac.uk/download/pdf/32348084.pdf.
Robinson, T. (1995). Kandungan Organik Tumbuhan Tinggi. Edisi VI Terjemahan Kosasih Padmawinata. Bandung: ITB Press. Halaman 157.
Sihombing, M. (2010). Status Gizi Dan Fungsi Hati Mencit (Galur CBS-Swiss) Dan Tikus Putih (Galur Wistar) Di Laboratorium Hewan Percobaan Puslitbang Biomedis Dan Farmasi. Media Litbang Kesehatan. 20(1):33-40. Singh, G., Maurya, S., Lampasona, M., dan Catalan, C., (2006). Chemical constituents, Antifungal And Antioxidative Potential Of Foeniculum vulgare Volatile Oil And Its acetone Extract. Elsevier. 17: 745-752.
Smith, J., dan Mangkoewidjojo, S. (1988). Pemeliharaan Pembiakan dan Penggunaan Hewan Percobaan Di Daerah Tropis. Jakarta: Universitas Indonesia Press. Halaman 23.
Soemardji, A. A., Endang K., dan Cucu A. (2002). Toksisitas Akut dan Penentuan DL50 Oral Ekstrak Air Daun Gandarusa (Justicia gendarussa Burm. F.)
pada Mencit Swiss Webster. Jurnal Matematika dan Sains. Vol. 7. No.2. Halaman 57-58.
Suharmiati dan Handayani, L. (2005). Cara Benar Meracik Obat Tradisional. Jakarta: Penerbit Agromedia Pustaka. Halaman 1-2.
Sukandar, E.Y. (2011). Trend dan Paradigma Dunia Farmasi, Industri-Klinik Teknologi Kesehatan, Disampaikan Dalam Orasi Ilmiah Dies Natalis ITB.
http://itb.ac.id./focus/focus_file/orasi-ilmiah-dies-45.pdf. Diakses tanggal 05 April 2013.
Suyanti, L. (2008). Gambaran Histopatologi Ginjal Tikus Pada Pemberian Fraksi Asam Amino Non Protein Lantara Nera (Acacia villosa) pada Uji Toksisitas Akut. Skripsi. Bogor: IPB.
Tanira. M., Shah, A., Mohsin, A., Ageel, A., dan Qureshi, S. (1996). Pharmacological and Toxicologica Investigations on Foeniculum vulgare
Wilson N., Jerry F. H., dan Johnnie R. H. (2001). Short-term, Subchronic and Chronic Toxicology Studies. Dalam:Taylor & Francis, penyunting.
Principles and Methods of Toxicology. Edisi ke-4. Philadelphia: Lippincot Williams and Wilkins. Pages 917-956.
Wirasuta, Gelgel M.A., dan Niruri, R. (2007). Toksikologi Umum (Buku Ajar). Bali: Jurusan Farmasi Fakultas MIPA Universitas Udayana. Halaman 28.
World Health Organization. (1992). Quality Control Methods for Medicinal Plant Material. Switzerland: Geneva. Halaman. 25-28.
Zainul, H. (2010). Penentuan Ketoksikan Akut Phyllanthus niruri. Semarang:
Artikel Ilmiah. Universitas Diponegoro. Halaman 8 - 11.
Zhaoa, N. N, Zhoub, L., Liua, Z. L., Duc, S. S dan Dengd, Z. W. 2012. Evaluation of the toxicity of the essential oils of same common Chinese spices gainst
METODE PENELITIAN
Metode penelitian ini dilakukan secara ekperimental. Penelitian ini meliputi
pengambilan dan pengolahan sampel, karakterisasi simplisia dan ekstrak etanol
buah adas manis, skrining fitokimia simplisia dan ekstrak etanol buah adas manis,
pembuatan ekstrak, pengujian efek toksisitas akut serta analisis data dengan
menggunakan metode analysis of variance (ANOVA) dilanjutkan dengan uji Post Hoc Tukey menggunakan program Statistical Product and Service Solution (SPSS) versi 22.
3.1 Alat dan Bahan 3.1.1 Alat
Alat-alat yang digunakan dalam penelitian ini meliputi alat-alat gelas
laboratorium, blender (Miyako), desikator, freeze dryer (Edward), rotary evaporator (Buchi), mikroskop (Olimpus), kandang mencit, krus porselin, krus tang, lemari pengering, neraca hewan (presica Geniweigher GW-1500), neraca kasar (Ohaus), neraca listrik (Chyo JP2-600), oral sonde, penangas air (Yenaco), timbangan, dan tanur (Gallenkamp).
3.1.2 Bahan
benzen, besi (III) klorida, bismut (III) nitrat, etanol, isopropanol, kalium iodida,
karboksil metil selulosa (CMC), kloralhidrat, kloroform, natrium hidroksida,
timbal (II) asetat dan toluena.
3.2 Hewan Percobaan
Hewan percobaan yang akan digunakan adalah mencit putih (Mus musculus) dengan berat badan 25-35 gram, berumur 2-3 bulan sebanyak 40 ekor dibagi dalam 8 kelompok yang masing-masing terdiri 5 ekor mencit. Sebelum
pengujian, hewan percobaan diaklimatisasi terlebih dahulu selama 7-14 hari
(BPOM, RI., 2014). Hewan percobaan dipuasakan selama 18 jam agar usus yang
digunakan dalam keadaan kosong. Hewan uji diberi makanan pelet selama
penelitian berlangsung.
3.3 Pengambilan dan Pengolahan Sampel 3.3.1 Pengambilan buah adas manis
Sampel yang digunakan dalam penelitian ini adalah buah adas manis
(Foeniculum vulgare Mill.) yang dibeli dari Pasar Central Medan. Pengambilan sampel dilakukan secara purposif tanpa membandingkan dengan sampel yang
sama dari daerah lain.
3.3.2 Identifikasi buah adas manis
Identifikasi buah adas manis (Foeniculum vulgare Mill.) dilakukan di Pusat Penelitian Biologi Lembaga Ilmu Pengetahuan Indonesia (LIPI), Bogor.
3.3.3 Pengolahan buah adas manis
Buah adas manis sebanyak 500g dibersihkan dari pengotor-pengotor tanpa
disimpan dalam wadah tertutup rapat.
3.4 Pembuatan Larutan Pereaksi 3.4.1 Larutan pereaksi Mayer
Sebanyak 1,36 g raksa (II) klorida, kemudian dilarutkan dalam air suling
hingga 60 ml. Pada wadah lain ditimbang sebanyak 5 g kalium iodida lalu
dilarutkan dalam 20 ml air suling. Kedua larutan dicampurkan dan ditambahkan
air suling hingga diperoleh larutan 100 ml (Depkes RI, 1995).
3.4.2 Larutan pereaksi Dragendorff
Sebanyak 0,8 g bismuth (III) nitrat dilarutkan dalam asam nitrat pekat 20
ml kemudian dicampurkan dengan larutan kalium iodida sebanyak 27,2 g dalam
50 ml air suling. Didiamkan sampai memisah sempurna. Larutan jernih diambil
dan diencerkan dengan air suling secukupnya hingga 100 ml (Depkes RI, 1995).
3.4.3 Larutan pereaksi Bouchardat
Sebanyak 4 g kalium iodida dilarutkan dalam air suling secukupnya
kemudian ditambahkan 2 g iodium sedikit demi sedikit, cukupkan dengan air
suling hingga 100 ml (Depkes RI, 1995).
3.4.4 Larutan pereaksi Molish
Sebanyak 3 g α-naftol dilarutkan dalam asam nitrat 0,5 N secukupnya
3.4.6 Larutan pereaksi besi (III) klorida 1%
Sebanyak 1 g besi (III) klorida dilarutkan dalam air suling hingga 100 ml
kemudian disaring (Depkes RI, 1995).
3.4.7 Larutan timbal (II) asetat
Sebanyak 15,17 g timbal (II) asetat ditimbang, kemudian dilarutkan dalam
air suling hingga 100 ml (Ditjen POM RI, 1979)
3.4.8 Larutan natrium hidroksida 2N
Sebanyak 8 g kristal natrium hidroksida dilarutkan dalam air suling hingga
diperoleh larutan 100 ml (Ditjen POM RI, 1979)
3.4.9 Larutan asam klorida 2N
Sebanyak 17 ml asam klorida pekat diencerkan dengan air suling sampai
100 ml (Ditjen POM RI, 1979)
3.4.10 Larutan kloralhidrat
Sebanyak 50 g kristal kloralhidrat ditimbang lalu dilarutkan dalam 20 ml air
suling (Ditjen POM RI, 1995).
3.5 Pemeriksaan Karakteristik Simplisia
Pemeriksaan karakteristik simplisia meliputi makroskopik, penetapan kadar
air, penetapan kadar abu total, pemeriksaan kadar abu yang tidak larut dalam asam,
penetapan kadar sari yang larut dalam etanol dan penetapan kadar sari yang larut
dalam air-kloroform (Depkes RI, 1995; WHO, 1992).
3.5.1 Pemeriksaan makroskopik
Pemeriksaan makroskopik dilakukan terhadap simplisia buah adas manis
Penetapan kadar air dilakukan dengan metode azeotropi (destilasi toluene). Alat terdiri dari labu alas bulat 500 ml, alat penampung, pendingin, tabung
penyambung dan tabung penerima 10 ml.
3.5.2.1 Penjenuhan toluena
Toluena sebanyak 200 ml dan air suling sebanyak 2 ml dimasukkan ke
dalam labu alas bulat, kemudian di destilasi selama 2 jam. Setelah itu toluena
didinginkan selama 30 menit dan dibaca volume air pada tabung penerima dengan
ketelitian 0,05 ml (volume I).
3.5.2.2 Penetapan kadar air simplisia
5 gserbuk simplisia buah adas manis yang telah ditimbang seksama di
masukkan ke dalam labu alas bulat tersebut, lalu dipanaskan hati-hati selama 15
menit. Setelah toluena mulai mendidih, destilasi dengan kecepatan 2 tetes tiap
detik, hingga sebagian besar air terdestilasi. Kemudian kecepatan destilasi
ditingkatkan hingga 4 tetes tiap detik. Setelah 2 jam didestilasi (semua air
terdestilasi), bagian dalam pendingin dibilas dengan toluena yang telah
dijenuhkan. Destilasi dilanjutkan selama 5 menit, kemudian tabung penerima
dibiarkan mendingin sampai suhu kamar. Setelah air dan toluena memisah
sempurna, volume air dibaca dengan ketelitian 0,05 ml (Volume II). Selisih kedua
volume air yang dibaca sesuai dengan kandungan air yang terdapat dalam bahan
pemijaran dilakukan pada suhu 600oC selama 3 jam. Kemudian didinginkan dan
ditimbang sampai diperoleh bobot tetap. Kadar abu dihitung terhadap bahan yang
telah dikeringkan diudara (Depkes RI, 1995).
3.5.4 Penetapan kadar abu yang tidak larut dalam asam
Abu yang telah diperoleh dalam penetapan abu dididihkan dengan 25 ml
asam klorida encer selama 5 menit, bagian tidak larut dalam asam dikumpulkan,
disaring dengan kertas saring bebas abu, cuci dengan air panas, dipijarkan sampai
bobot tetap, kemudian didinginkan dan ditimbang. Kadar abu yang tidak larut
dalam asam dihitung terhadap bobot yang dikeringkan diudara (Depkes RI, 1995).
3.5.5 Penetapan kadar sari yang larut dalam etanol
Sebanyak 5 g serbuk simplisia yang telah dikeringkan dimaserasi selama
24 jam dalam 100 ml etanol 96% dalam labu bersumbat sambil dikocok selama 6
jam pertama, dan dibiarkan selama 18 jam. Kemudian disaring, 20 ml filtrat
diuapkan sampai kering dalam cawan dangkal berdasar rata yang telah ditara dan
sisanya dipanaskan pada suhu 105oC sampai bobot tetap. Kadar sari larut dalam
etanol dihitung terhadap bahan yang telah dikeringkan (Depkes RI, 1995).
3.5.6 Penetapan kadar sari yang larut dalam air
Sebanyak 5 g simplisia adas manis yang telah dikeringkan di udara,
dimaserasi selama 24 jam dalam 100 ml air kloroform (2,5 ml kloroform dalam air
suling 1000 ml) dalam labu bersumbat sambil sesekali dikocok selama 6 jam
pertama, dibiarkan selama 18 jam, kemudian disaring. Diuapkan 20 ml filtrat
sampai kering dalam cawan penguap yang berdasar rata yang telah dipanaskan dan
ditara. Sisa dipanaskan pada suhu 105oC sampai bobot tetap. Kadar dalam persen
sari yang larut dalam air – kloroform dihitung terhadap bahan yang telah
Skrining fitokimia serbuk simplisia dan ekstrak etanol buah adas manis
meliputi pemeriksaan senyawa gologan alkaloid, flavonoid, glikosid, glikosida
antrakinon, saponin, tanin dan steroid/triterpenoid (Depkes RI, 1989; Farnsworth,
1996). Skrining fitokimia ekstrak etanol dilakukan dengan cara yang sama dengan
skrining fitokimia serbuk simplisia.
3.6.1 Pemeriksaan alkaloida
Serbuk simplisia ditimbang sebanyak 0,5 g, kemudian ditambah 1 ml asam
klorida 2 N dan 9 ml air suling, dipanaskan di atas penangas air selama 2 menit.
Dinginkan dan disaring. Filtrat dipakai untuk percobaan berikut :
a. Filtat sebanyak 3 tetes ditambah dengan 2 tetes larutan pereaksi Mayer, akan
terbentuk endapan menggumpal berwarna putih atau kuning bila terdapat
alkaloida.
b. Filtrat sebanyak 3 tetes ditambah dengan 2 tetes larutan pereaksi Bouchardat,
akan terbentuk endapan berwarna coklat sampai hitam bila terdapat alkaloida.
c. Filtrat sebanyak 3 tetes ditambah dengan 2 tetes pereaksi Dragendorf akan
terbentuk warna merah atau jingga bila terdapat alkaloida.
3.6.2 Pemeriksaan flavonoida
Sebanyak 10 g serbuk simplisia ditambah 100 ml air panas, dididihkan
selama 5 menit dan saring dalam keadaan panas. Kedalam 5 ml filtrat ditambahkan
ditambahkan 10 ml air panas, dinginkan kemudian dikocok selama 10 detik. Jika
terbentuk busa setinggi 1 sampai 10 cm yang stabil tidak kurang dari 10 menit dan
tidak hilang dengan penambahan asam klorida 2 N menunjukkan adanya saponin.
3.6.4 Pemeriksaan tanin
Sebanyak 0,5 g serbuk simplisia buah adas manis disari dengan 10 ml air
suling lalu disaring, filtratnya diencerkan dengan air sampai tidak berwarna.
Larutan diambil sebanyak 2 ml dan ditambahkan 1-2 tetes pereaksi besi (III)
klorida 1%. Jika terjadi warna biru atau hijau kehitaman menunjukkan adanya
tanin.
3.6.5 Pemeriksaan glikosida
Sebanyak 3 g serbuk simplisia buah adas manis disari dengan 30 ml
campuran etanol 96% dengan air (7:3) dan 10 ml asam sulfat 2 N, direfluks selama
1 jam, didinginkan dan disaring. Pada 20 ml filtrat ditambahkan 25 ml air dan 25
ml timbal asetat 0,4 M, dikocok, diamkan 5 menit lalu disaring. Filtrat disari
dengan 20 ml campuran isopropanol dan kloroform (2:3), dilakukan sebanyak 3
kali. Kumpulan sari ditambahkan natrium sulfat anhidrat, saring dan diuapkan
pada temperatur tidak lebih dari 500C. Sisanya dilarutkan dalam 2 ml metanol.
Larutan sisa dimasukkan dalam tabung reaksi selanjutnya, diuapkan di atas
penangas air, pada sisa ditambahkan 2 ml air dan 5 tetes pereaksi Molish.
Tambahkan hati- hati 2 ml asam sulfat pekat melalui dinding tabung, terbentuknya
cincin ungu pada batas kedua cairan menunjukkan adanya gula.
3.6.6 Pemeriksaan antrakinon
Sebanyak 0,2 g serbuk simplisia buah adas manis dicampur dengan 5 ml
asam sulfat 2 N, dipanaskan sebentar, lalu didinginkan, ditambahkan 10 ml
dan lapisan benzena tidak berwarna menunjukkan adanya glikosida antrakinon.
3.6.7 Pemeriksaan steroida/triterpenoida
Sebanyak 1 g serbuk simplisia buah adas manis dimaserasi dengan 20 ml n -heksan selama 2 jam, disaring, filtrat diuapkan dalam cawan penguap dan pada
sisanya ditambahkan 2 tetes Liebermann-Burchard. Apabila terbentuk warna ungu
atau merah berubah menjadi ungu atau biru hijau menunjukkan adanya
steroida/triterpenoida.
3.7 Pembuatan Ekstrak Etanol Buah Adas Manis (EEBAM)
Pembuatan EEBAM dilakukan secara maserasi menggunakan pelarut
etanol 80% (Ditjen POM RI, 1979). Cara kerjanya yaitu Sebanyak 500 g serbuk
simplisia buah adas manis dimasukkan ke dalam wadah kaca berwarna gelap,
kemudian dituangi dengan 3500 ml etanol 80%. Ditutup dan dibiarkan selama 5
hari yang terlindung dari cahaya sambil sesekali diaduk, disaring hingga didapat
maserat pertama. Ampas yang diperoleh dibilas dengan menambahkan etanol 80%
hingga diperoleh 5.000 ml ke dalam wadah tertutup, dibiarkan di tempat sejuk
terlindung dari cahaya selama 2 hari, lalu disaring hingga didapat maserat kedua.
Maserat pertama dan kedua digabung. Maserat diuapkan dengan menggunakan
dimasukkan ke dalam lumpang, dan ditambahkan CMC-Na 1 % digerus hingga
merata. Sediaan uji EEBAM dimasukkan ke dalam labu ukur, cukupkan dengan
CMC-Na 1 % hingga dicapai batas volume.
3.8.2 Uji toksisitas akut
Mencit dikelompokkan ke dalam 8 kelompok, yaitu kelompok kontrol
normal (suspensi CMC-Na 1%), kelompok bahan uji (Suspensi ekstrak).
a. kelompok perlakuan 1 (P1): diberi EEBAM dosis 5 mg/kg bb
b. kelompok perlakuan 2 (P2): diberi EEBAM dosis 50 mg/kg bb
c. kelompok perlakuan 3 (P3): diberi EEBAM dosis 300 mg/kg bb
d. kelompok perlakuan 4 (P4): diberi EEBAM dosis 1000 mg/ kg bb
e. kelompok perlakuan 5 (P5): diberi EEBAM dosis 2000 mg/ kg bb
f. kelompok perlakuan 6 (P6): diberi EEBAM dosis 4000 mg/ kg bb
g. kelompok perlakuan 7 (P7): diberi EEBAM dosis 8000 mg/ kg bb
3.8.3 Pengamatan
Pengamatan mencit dilakukan pada 30 menit pertama setelah pemberian
sediaan uji, dan secara periodik setiap 4 jam selama 24 jam pertama dan sehari
sekali setelah itu selama 14 hari (BPOM, RI., 2014).
3.8.3.1 Gejala toksik
Pengamatan seperti tremor, salivasi, diare, lemas, muntah, gerak-gerik
hewan seperti berjalan mundur dan jalan menggunakan perut (BPOM, RI., 2014).
3.8.3.2 Berat badan
Mencit ditimbang dua kali dalam seminggu selama 14 hari. Perubahan berat
badan dianalisis seminggu sekali. Pada akhir penelitian hewan yang masih hidup
Jumlah makanan dan minuman yang dikonsumsi ditimbang dan diukur
setiap hari (BPOM, RI., 2014).
3.8.3.4 Kematian hewan
Kematian mencit diamati dari hari pertama sampai hari terakhir dan mencit
yang mati selama waktu pemberian sediaan uji segera diotopsi (Hendriani, 2007;
Klasseen, 2001).
3.8.3.5 Makropatologi
Mencit yang mati segera diotopsi dan dilakukan pengamatan (OECD,
2008). Pengamatan meliputi warna dan permukaan organ hati dan ginjal secara
visual (Anggraini, 2008; Pratiwi, 2010).
3.8.4 Analisis data
Data jumlah hewan uji yang mati dianalisa secara statistik menggunakan
BAB IV
HASIL DAN PEMBAHASAN
4.1 Hasil Identifikasi Tumbuhan
Hasil identifikasi tumbuhan yang dilakukan di Herbarium Bogoriense,
Bidang Botani Pusat, Pusat Penelitian Biologi, Lembaga Ilmu Pengetahuan
Indonesia (LIPI) Bogor menunjukkan bahwa sampel termasuk suku Apiaceae spesies Foeniculum vulgare Mill. Dapat dilihat pada Lampiran 1 halaman 51.
4.2 Hasil Karakterisasi
4.2.1 Pemeriksaan makroskopik
Pemeriksaan makroskopik diperoleh bahwa simplisia buah adas manis
berwarna kuning kecoklatan atau coklat kehijauan. Panjang 5-6 mm dan
berdiameter 1-2 mm, memiliki aroma yang khas dan rasa manis dapat dilihat pada
Lampiran 2 halaman 52.
4.2.2 Pemeriksaan karakteristik simplisia dan ekstrak
Hasil karaketerisasi serbuk simplisia dan ekstrak adas manis yang diperoleh
dan berdasarkan Farmakope Herbal Indonesia (FHI) dapat dilihat pada Tabel 4.1.
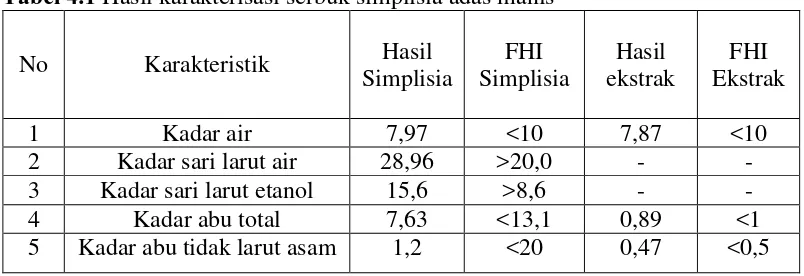
Tabel 4.1 Hasil karakterisasi serbuk simplisia adas manis
No Karakteristik Hasil
Simplisia
FHI Simplisia
Hasil ekstrak
FHI Ekstrak
1 Kadar air 7,97 <10 7,87 <10
2 Kadar sari larut air 28,96 >20,0 - -
3 Kadar sari larut etanol 15,6 >8,6 - -
4 Kadar abu total 7,63 <13,1 0,89 <1
5 Kadar abu tidak larut asam 1,2 <20 0,47 <0,5
manis sebesar 7,97% dan 7,87% kadar tersebut memenuhi persyaratan Farmakope
Herbal Indonesia yaitu lebih kecil dari 10%. Kadar air yang lebih besar dari 10%
dapat menjadi media pertumbuhan kapang dan jasad renik lainnya (Depkes RI,
1995).
Penetapan kadar sari yang larut dalam air menyatakan jumlah zat yang
tersari dalam pelarut air seperti glikosida, gula, gom, protein, enzim, zat warna dan
asam-asam organik, sedangkan penetapan kadar sari yang larut dalam etanol
seperti glikosida, antrakinon, steroid, flavonoid, klorofil, saponin, tannin dan yang
larut dalam jumlah sedikit yaitu lemak (Depkes RI, 1995).
Penetapan kadar abu total dan kadar abu tidak larut asam bertujuan untuk
memberikan jaminan bahwa simplisia dan ekstrak etanol buah adas manis tidak
mengandung logam berat tertentu melebihi nilai yang ditetapkan karena dapat
berbahaya (toksik) bagi kesehatan. Penetapan kadar abu total menyatakan jumlah
kandungan senyawa anorganik dalam simplisia misalnya Mg, Ca, Na, Zn, dan K.
Kadar abu tidak larut dalam asam untuk mengetahui kadar senyawa anorganik
yang tidak larut dalam asam, misalnya silikat. Abu total terbagi dua, yaitu abu
fisiologis dan abu non fisiologis. Abu fisiologis adalah abu yang berasal dari
jaringan tumbuhan itu sendiri, sedangkan abu non fisiologis adalah sisa setelah
pembakaran yang berasal dari bahan-bahan luar yang terdapat pada permukaan
4.3 Hasil Skrining Fitokimia
Hasil skrining fitokimia serbuk simplisia dan ekstrak etanol buah adas
manis diperoleh senyawa kimia golongan saponin, glikosida, flavonoida,
steroida/triterpenoida dan tannin. Hasilnya dapat dilihat pada Tabel 4.2.
Tabel 4.2 Hasil skrining fitokimia serbuk simplisia dan EEBAM
No. Pemeriksaan
Hasil
Serbuk simplisia Ekstrak etanol buah adas manis
1 Alkaloid - -
2 Flavonoida + +
3 Glikosida + +
4 Glkosida antrakuinon - -
5 Saponin + +
6 Tanin + +
7 Steroida/Triterpenoida + +
Keterangan: (+) = mengandung golongan senyawa; (-) = tidak mengandung golongan senyawa
Penambahan serbuk Mg, asam klorida pekat dan amil alkohol
memberikan warna merah yang menunjukkan adanya flavanoida (Farnsworth,
1966). Skrining glikosida ditunjukkan dengan terbentuknya cincin ungu dengan
penambahan Molish dan asam sulfat pekat (Depkes RI, 1995). Penambahan FeCl3
1% memberikan warna biru kehitaman yang menunjukkan adanya tanin yaitu 3
buah gugus hidroksil (Depkes RI, 1995). Penambahan pereaksi
Lieberman-Bourchard memberikan warna merah ungu menunjukkan adanya
triterpenoid/steroid.
4.4 Hasil Pengujian Toksisitas Akut
Berdasarkan hasil uji pendahuluan dari EEBAM maka diberikan dosis
untuk pengujian toksisitas akut yaitu dosis 5, 50, 300, 1000, 2000, 4000, 8000
hati dan ginjal.
4.4.1 Hasil pengamatan gejala toksik
Hasil pengamatan yang dilakukan setiap hari selama 14 hari terhadap
adanya tremor, diare, salivasi, lemas, muntah dan gerak-gerik hewan seperti
berjalan mundur dan berjalan dengan perut dapat dilihat pada Tabel 4.3.
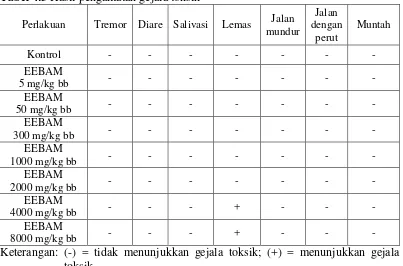
Tabel 4.3 Hasil pengamatan gejala toksik
Perlakuan Tremor Diare Salivasi Lemas Jalan mundur
Jalan dengan
perut
Muntah
Kontrol - - - -
EEBAM
5 mg/kg bb - - - -
EEBAM
50 mg/kg bb - - - -
EEBAM
300 mg/kg bb - - - -
EEBAM
1000 mg/kg bb - - - -
EEBAM
2000 mg/kg bb - - - -
EEBAM
4000 mg/kg bb - - - + - - -
EEBAM
8000 mg/kg bb - - - + - - -
Keterangan: (-) = tidak menunjukkan gejala toksik; (+) = menunjukkan gejala toksik.
Pada Tabel 4.3 terlihat bahwa pemberian EEBAM tidak ditemukan
adanya gejala toksik pada kelompok kontrol, dosis 5, 50, 300, 1000 dan 2000
mg/kg bb. Pada dosis 4000 dan 8000 mg/kg bb ditemukan gejala toksik yaitu
Setiap zat bila diberikan dengan dosis yang cukup besar akan
menimbulkan gejala-gejala toksik (Ganiswara, 1995). Makin besar dosis yang
diberikan makin besar efek toksik yang timbul (Lu, 1995). Tanda toksik yang
muncul pada organ dan sistem antara lain: pada sistem gastrointestinal meliputi
melemas, diare, salivasi, keluar air seni, pada perilaku meliputi sedasi, gelisah,
depresi berat, sikap agresif atau defensif, ketakutan, bingung , aktivitas yang aneh,
dll (Lu, 1995).
4.4.2 Hasil pengamatan berat badan
Penimbangan berat badan dilakukan setiap hari dari hari 0 sampai hari ke
14 dan dianalisis secara statistik dilakukan seminggu sekali. Hasil pengamatan
berat badan dapat dilihat pada Tabel 4.4 dan Gambar 4.1 di bawah ini:
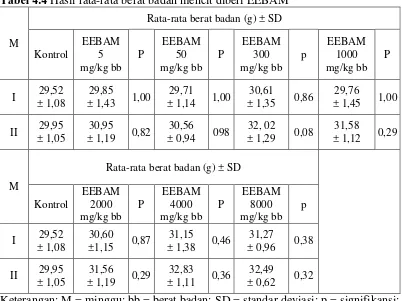
Tabel 4.4 Hasil rata-rata berat badan mencit diberi EEBAM
M
Rata-rata berat badan (g) ± SD
Kontrol
Rata-rata berat badan (g) ± SD
Kontrol
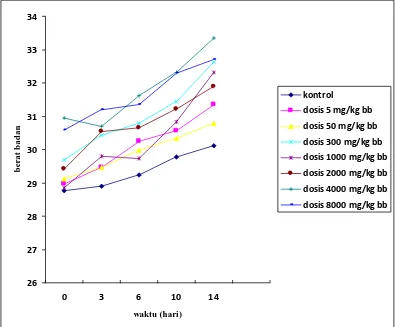
Gambar 4.1 Grafik perubahan berat badan mencit selama 14 hari
Berdasarkan hasil pengamatan terjadi perubahan berat badan kelompok
kontrol dan perlakuan dengan pemberian ekstrak etanol buah adas manis yaitu
pertambahan berat badan sedangkan berdasarkan hasil analisis secara statistik
terlihat bahwa tidak terdapat perbedaan berat badan yang signifikan antara
kelompok kontrol dan perlakuan dengan pemberian ekstrak etanol buah adas
manis dimana p ≥ 0,05. Menurut Sihombing (2010) kenaikkan berat badan mencit
sebanding dengan bertambahnya umur, ini memperlihatkkan pertumbuhan mencit
berkembang secara normal. Sehingga menunjukkan tidak adanya pengaruh
26 27 28 29 30 31 32 33
0 3 6 10 14
waktu (hari)
b
er
at b
ad
an
kontrol
dosis 5 mg/kg bb
dosis 50 mg/kg bb
dosis 300 mg/kg bb
dosis 1000 mg/kg bb
dosis 2000 mg/kg bb
dosis 4000 mg/kg bb
dan Datta, 2012). Penurunan berat badan yang cepat dan bermakna biasanya
merupakan pertanda kesehatan yang buruk. Penurunan berat badan dapat
disebabkan oleh kurangnya konsumsi makanan dan minuman, penyakit ataupun
tanda toksik spesifik (Wilson, et al., 2001).
4.4.3 Hasil pengamatan konsumsi makanan dan minuman
Hasil pengamatan uji konsumsi makanan dan minuman yang diberikan
pada mencit sesudah perlakuan pada Tabel 4.5 di bawah ini.
Tabel 4.5 Rata-rata konsumsi makanan dan minuman sesudah diberi EEBAM
M
Rata-rata konsumsi makanan (g) ± SD
Kontrol
Rata-rata konsumsi minuman (ml) ± SD
Kontrol
yang dapat mempengaruhi perkembangan berat badan (Oktriana dan Nurlaela,
2011). Hasil pengukuran asupan makanan menunjukkan bahwa kelompok kontrol,
dosis 1000, 2000, 4000 dan 8000 mg/kg bb memiliki perbedaan dalam jumlah
konsumsi makanan dan minuman. Sedangkan berdasarkan hasil analisa statistik
menunjukkan tidak terdapat perbedaan yang signifikan pada konsumsi makanan
dan minuman antara kelompok kontrol dengan perlakuan yang ditunjukkan setelah
pemberian ekstrak etanol buah adas manis dengan nilai p ≥ 0,05. Menurut Smith
dan Mangkoewidjojo (1988), seekor mencit dewasa dapat mengkonsumsi makanan
3-5 g/hari dan konsumsi air minum setiap hari berkisar antara 4-8 ml. Dengan
demikian menunjukkan tidak adanya pengaruh pemberian ekstrak etanol adas
manis terhadap konsumsi makanan dan minuman pada mencit jantan.
4.4.4 Hasil pengamatan kematian
Hasil pengamatan uji kuantitatif selama 14 hari, berupa jumlah mencit
yang mati ditunjukkan pada Tabel 4.6.
Tabel 4.6 Jumlah mencit yang mati setelah pemberian EEBAM selama 14 hari
Kelompok Jumlah Mencit Jumlah Mencit Mati
Kontrol 5 0
EEBAM 5 mg/kg bb 5 0
EEBAM 50 mg/kg bb 5 0
Berdasarkan Tabel 4.6 menunjukkan bahwa dengan pemberian ekstrak etanol
buah adas manis dosis tunggal secara oral sampai dengan dosis 8000 mg/kg bb
tidak menimbulkan kematian pada mencit dari semua kelompok hingga sampai
hari ke-14 dengan demikian LD50 dari ekstrak etanol buah adas manis tidak dapat
ditentukan). Kematian tidak terjadi disebabkan karena sangat sedikitnya
kandungan estragole dalam buah adas manis. Buah adas manis mengandung tidak
kurang dari 1,40% minyak atsiri dimana kandungan terbesarnya adalah trananethol
(72,2%) diikuti dengan estragole (7,6 %), limonene (6,8%) dan fenchone (3,9%).(
Zhaoa, et al., 2012). Efek karsinogen dari estragole tidak bekerja secara langsung.
Efek karsinogen muncul dari aktivitas metabolit dari estragole, dimana metabolit
dari estragole akan membentuk molekul yang tidak stabil dan reaktif sehingga
dapat berikatan dengan asam nukleat dengan demikian akan terjadi kerusakan
DNA (Rather, et al., 2012).
Berdasarkan kesepakatan para ahli, bila pada dosis maksimal tidak ada
kematian pada hewan uji, maka jelas ekstrak etanol buah adas manis tersebut
termasuk dalam kriteria “praktis tidak toksik” (Jenova, 2009 ; Iwuanyanwu, dkk.,
2012).
4.4.5 Hasil pengamatan makropatologi organ
Hasil pengamatan makropatologi meliputi pengamatan warna dan
permukaan organ hati dan ginjal. Hasil pengamatan makropatologi hati dan ginjal
dapat dilihat pada Tabel 4.7 dan Tabel 4.8.
Tabel 4.7 Hasil pengamatan makropatologi hati
Kelompok Pengamatan
Warna Permukaan
Kontrol Merah kecoklatan Licin
Dosis 5 mg Merah kecoklatan Licin
Tabel 4.8 Hasil pengamatan makropatologi ginjal
Kelompok Pengamatan
Warna Permukaan
Kontrol Merah kecoklatan Licin
Dosis 5 mg Merah kecoklatan Licin
Dosis 50 mg Merah kecoklatan Licin
Dosis 300 mg Merah kecoklatan Licin
Dosis 1000 mg Merah kecoklatan Licin
Dosis 2000 mg Merah kecoklatan Licin
Dosis 4000 mg Merah bata Licin
Dosis 8000 mg Pucat Tidak licin
Berdasarkan pengamatan makropatologi organ hati dan ginjal pada kontrol
dan kelompok dosis 5, 50, 300, 1000 dan 2000 mg/kg bb tidak terlihat adanya
perubahan yaitu berwarna merak kecoklatan. Pada dosis 4000 mg/kg bb mulai
terjadi perubahan warna pada organ hati dan ginjal yaitu berwarna merah bata,
sedangkan pada dosis 8000 mg/kg bb warna organ hati dan ginjal menjadi lebuh
pucat.
Hati dan ginjal memiliki kapasitas yang besar dalam mengikat senyawa
kimia. Kedua organ ini mungkin memiliki konsentrasi toksikan yang lebih banyak
dibandingkan seluruh organ lainnya ( Klassen, 2001). Perubahan warna menjadi
salah satu parameter terjadinya efek toksik yang bertujuan mendapatkan informasi
mengenai toksisitas zat uji yang berkaitan dengan organ sasaran dan efek terhadap
Dosis 300 mg Merah kecoklatan Licin
Dosis 1000 mg Merah kecoklatan Licin
Dosis 2000 mg Merah kecoklatan Licin
Dosis 4000 mg Merah bata Licin
4000 mg/kg bb. Pada dosis 8000 mg/kg bb warna hati dan ginjal menjadi lebih
pucat. Menurut Tang dalam Praptiwi (2010) Perubahan yang terjadi pada organ
akibat pemberian ekstrak disebabkan adanya kandungan kimia pada ekstrak
tersebut, misalnya saponin, turunan triterpenoid (asam asiastika, dan asam
brahmida) dan ion potasium (K). Biji adas manis (Foeniculum vulgare Mill.) mengandung metabolit sekunder golongan alkaloid, glikosida, flavonoid, saponin,
steroid/terpenoid dan tannin (Chatterjee, et al., 2012). Buah adas manis
mengandung sekitar 8% minyak atsiri yaitu transanethole, fenchone, estragole dan
α-phellandrene dan kaya akan potasium (Barros, A., 2010; Janwal, et al., 2013;
Rather, et al., 2012).
Saponin yang merupakan salah satu kandungan ekstrak buah adas manis yang
dapat menyebabkan hemolisis dan menurunkan tekanan permukaan sehingga dapat
mengakibatkan kerusakan pada sel dan jaringan otot, pendarahan pada sinusoid,
nekrosis pada tubuli. Kelebihan ion potassium (K) juga dapat menurunkan fungsi
ginjal sehingga terjadi kerusakan pada gromerolus dan juga adanya degenerasi
KESIMPULAN DAN SARAN
5.1 Kesimpulan
Berdasarkan penelitian yang telah dilakukan, maka kesimpulan dari
penelitian ini adalah EEBAM pada kelompok kontrol dan dosis 5, 50, 300, 1000
dan 2000 mg/kg bb tidak menimbulkan efek toksik pada mencit. Pada dosis 4000
dan 8000 mg/kg bb menimbulkan efek toksik yaitu lemas. EEBAM sampai dengan
dosis 8000 mg/kg bb tidak menimbulkan kematian sehingga EEBAM tersebut
termasuk dalam kriteria “praktis tidak toksik”.
5.2 Saran
Diperlukan penelitian lebih lanjut untuk meneliti potensi toksisitas subkronis dan
BAB II
TINJAUAN PUSTAKA
2.1 Uraian Tumbuhan 2.1.1 Habitat
Tumbuhan adas manis (Foeniculum vulgare Mill.) berasal dari Eropa Selatan dan Asia, karena manfaatnya kemudian banyak di tanam di Indonesia,
India, Argentina, Eropa dan Jepang. Tanaman ini dibudidayakan untuk diambil
buahnya. Di Indonesia tanaman adas digunakan untuk bumbu atau tanaman obat.
Tumbuhan adas banyak ditemukan di daerah tropika, tumbuh di dataran rendah
sampai ketinggian 1800 m di atas permukaan laut, tetapi akan tumbuh lebih baik
pada dataran tinggi (Dalimartha, 1999).
2.1.2 Morfologi
Tumbuhan adas manis merupakan tumbuhan perdu, tahunan dan ketinggian
lebih kurang 2 m, batang beralur, tumbuh tegak dan merumpun. Satu rumpun
biasanya terdiri dari 3-5 batang. Batang hijau keputih-putihan, beralur, beruas,
berlubang, bila memar baunya wangi. Daun berseling, majemuk menyirip ganda
dua dengan sirip-sirip yang sempit. Bentuk daun seperti jarum, ujung dan pangkal
runcing, tepi rata. Bunga kecil berwarna kuning, tersusun sebagai bunga payung
majemuk. Perbungaan terdiri dari 6-40 gagang bunga, panjang ibu gagang bunga
5-10 cm, panjang gagang bunga 2-5 mm, mahkota berwarna kuning, keluar dari
ujung batang. Buah lonjong, berusuk, panjang 6-10 mm, lebar 3-4 mm, masih
muda berwarna hijau setelah tua berwarna cokelat agak hijau atau cokelat agak
kuning sampai sepenuhnya berwarna cokelat. Warna buah adas berbeda-beda
dalam jumlah yang banyak (Depkes RI, 2001).
2.1.3 Sistematika tumbuhan
Tumbuhan adas manis memiliki sistematika sebagai berikut (Depkes RI,
2001):
Divisi : Spermatophyta
Subdivisi : Angiospermae
Kelas : Dicotyledoneae
Bangsa : Umbellales
Suku : Umbelliferae
Marga : Foeniculum
Jenis : Foeniculum vulgare Mill.
2.1.4 Nama lain
Tumbuhan adas manis memiliki nama lain yaitu Anethum foeniculum clairv.,
Foeniculum azoricum Mill. (Janwal, et al., 2013), dengan nama daerah das pedas (Aceh), adeh manih (Minangkabau), hades (Sunda), adas, adas londa, adas landi
(Jawa), adhas (Madura), paapang, paampas (Menado), popaas (Alfuru),
denggu-denggu (Gorontalo), papaato (Buol), porotomu (Baree), adasa, rempasu (Makasar),
adase (Bugis), kumpasi (Sangir Talaut), Adas (Bali) (Dalimartha, 1999).
Nama asing adalah Hsiao hui (Cina), Mellet karee (Thailand), Jintan manis
teratur, menambah ASI, mengatasi susah tidur, pembengkakan saluran sperma,
penimbunan cairan dalam kantung buah zakar, rematik, keracunan tumbuhan obat
dan jamur (Nuris, 2011). Hasil penelitian yang telah dilakukan terhadap buah adas
manis antara lain, sebagai antijamur (Singh, et al., 2005), hipolipedimia
(Oulmouden, et al., 2014), antibakteri, antioksidan, antidiabetes (Rather, et al.,
2012), antiinflamasi (Nassar, et al., 2010), analgetik, antipiretik dan diuretik
(Tanira, et al., 1996).
2.1.6 Kandungan kimia
Buah adas manis (Foeniculum vulgare Mill.) mengandung metabolit sekunder golongan alkaloid, glikosida, flavonoid, saponin, steroid/terpenoid dan
tannin (Chatterjee, et al., 2012). Buah adas manis mengandung tidak kurang dari
1,40% minyak atsiri yang mengandung transanethole, fenchone, estragole (Ditjen
POM RI, 2008; Rather, et al., 2012).
2.2 Ekstraksi
Ekstraksi adalah kegiatan penarikan kandungan kimia yang dapat larut
sehingga terpisah dari bahan yang tidak dapat larut dengan menggunakan suatu
pelarut cair. Senyawa aktif yang terdapat dalam berbagai simplisia dapat
digolongkan kedalam golongan minyak atsiri, alkaloida, flavonoida dan lain-lain.
Dengan diketahuinya senyawa aktif yang dikandung simplisia akan mempermudah
pemilihan pelarut dengan cara ekstraksi yang tepat (Ditjen POM RI, 2000).
Ekstrak adalah sediaan kering, kental atau cair dibuat dengan menyari simplisia
nabati atau hewani menurut cara yang cocok di luar pengaruh cahaya matahari
(Syamsuni, 2006).
Beberapa metode ekstraksi yang sering digunakan dalam berbagai penelitian
antara lain yaitu:
a. Cara dingin
i. Maserasi
Maserasi adalah proses penyarian simplisia menggunakan pelarut dengan
beberapa kali pengocokan atau pengadukan pada temperatur ruangan, sedangkan
remaserasi merupakan pengulangan penambahan pelarut setelah dilakukan
penyaringan maserat pertama dan seterusnya (Ditjen POM RI, 2000).
Maserasi dilakukan dengan cara masukkan 10 bagian simplisia atau
campuran simplisia dengan derajat halus yang cocok ke dalam sebuah bejana,
tuangi dengan 75 bagian cairan penyari, tutup, biarkan selama 5 hari terlindung
dari cahaya sambil sering diaduk, serkai, peras, cuci ampas dengan cairan penyari
secukupnya hingga dipreoleh 100 bagian. Dipindahkan ke dalam bejana tertutup,
biarkan di tempat sejuk, terlindung dari cahaya selama 2 hari. Enap tuangkan dan
saring (Ditjen POM RI, 1979).
ii. Perkolasi
Perkolasi adalah suatu proses penyarian simplisia menggunakan alat yang
disebut perkolator dimana simplisia terendam dalam cairan penyari, zat-zat akan
penyari, dimasukkan ke dalam bejana tertutup sekurang-kurangnya selama 3 jam.
Massa dipindahkan ke dalam perkolator sambil tiap kali di tekan hati-hati, dituangi
dengan cairan penyari secukupnya sampai cairan mulai menetes dan di atas
simplisia masih terdapat selapis cairan penyari, tutup perkolator, biarkan selama
24 jam. Cairan dibiarkan menetes dengan kecepatan 1 ml per menit, cairan
penyari berulang-ulang ditambahkan secukupnya sehingga selalu terdapat selapis
cairan penyari di atas simplisia, hingga diperoleh 80 bagian perkolat. Massa
diperas, cairan perasan dicampurkan ke dalam perkolat, ditambahkan cairan
penyari secukupnya hingga diperoleh 100 bagian. Cairan dipindahkan ke dalam
bejana, ditutup, dibiarkan selama 2 hari di tempat yang sejuk, terlindung cahaya
dan dienaptuangkan atau disaring (Ditjen POM RI, 1979).
b. Cara panas
i. Refluks
Refluks adalah proses penyarian simplisia dengan menggunakan alat pada
temperatur titik didihnya dalam waktu tertentu dimana pelarut akan terkondensasi
menuju pendingin dan kembali ke labu (Ditjen POM RI, 2000).
ii. Sokletasi
Sokletasi adalah proses penyarian dengan menggunakan pelarut yang selalu
baru, dilakukan dengan menggunakan alat soklet dimana pelarut akan
terkondensasi dari labu menuju pendingin, kemudian jatuh membasahi sampel
(Ditjen POM RI, 2000).
iii.Digesti
Digesti adalah proses penyarian dengan pengadukan kontinu pada
temperatur lebih tinggi dari temperatur kamar, yaitu secara umum dilakukan pada
Infudasi adala proses penyarian dengan menggunakan pelarut air pada
temperatur 90°C selama 15 menit (Ditjen POM RI, 2000).
v. Dekoktasi
Dekoktasi adalah proses penyarian dengan menggunakan pelarut air pada
temperatur 90°C selama 30 menit (Ditjen POM RI, 2000).
2.3 Biologi Mencit
Mencit termasuk mamalia pengerat (rodensia) merupakan salah satu hewan
percobaan yang sering digunakan dalam penelitian. Hewan ini dinilai cukup efisien
ekonomis karena mudah dipelihara, tidak memerlukan tempat yang luas, waktu
kebuntingan yang singkat dan banyak memilki anak perkelahiran. Mencit
mempunyai sifat-sifat produksi dan reproduksi yang mirip dengan mamalia besar
serta memiliki siklus estrus yang pendek (Malole dan Pramono, 1989). Mencit dan
tikus putih memiliki banyak data toksikologi, sehingga mempermudah
membandingkan toksisitas zat - zat kimia (Lu, 1995). Sistem taksonomi mencit
menurut Malole etal (1989) adalah:
Divisi : Chordata
Subdivisi : Vertebrata
Penelitian dalam bidang toksikologi dan farmakologi memerlukan
serangkaian percobaan untuk mengetahui tingkat toksisitas dan keamanan obat.
Penggunaan berbagai tingkat dosis obat terhadap hewan percobaan dilakukan
untuk mendapatkan dosis terbesar yang tidak memberikan efek merugikan. Respon
berbagai hewan percobaan terhadap uji toksisitas berbeda-beda karena kepekaan
terhadap zat toksik antara individu sejenis maupun berbeda jenis dapat bervariasi.
Hal ini disebabkan oleh perbedaan anatomi, fisiologis, variasi dalam sifat
keturunan, umur dan kondisi tubuh individu dalam satu jenis (Koeman, 1987).
2.4 Toksisitas
Uji toksisitas adalah suatu uji untuk mendeteksi efek toksik suatu zat pada
sistem biologi dan untuk memperoleh data dosis-respon yang khas dari sediaan uji.
Data yang diperoleh dapat digunakan untuk memberi informasi mengenai derajat
bahaya sediaan uji tersebut bila terjadi pemaparan pada manusia, sehingga dapat
ditentukan dosis penggunaannya demi keamanan manusia. Uji toksisitas
menggunakan hewan uji sebagai model berguna untuk melihat adanya reaksi
biokimia, fisiologik dan patologik pada manusia terhadap suatu sediaan uji. Hasil
uji toksisitas tidak dapat digunakan secara mutlak untuk membuktikan keamanan
suatu sediaan pada manusia, namun dapat memberikan petunjuk adanya toksisitas
relatif dan membantu identifikasi efek toksik bila terjadi pemaparan pada manusia
(BPOM, RI., 2014).
1. Uji toksisitas akut oral
Uji toksisitas akut oral adalah suatu pengujian untuk mendeteksi efek
toksik yang muncul dalam waktu singkat setelah pemberian sediaan uji yang
beberapa tingkat dosis diberikan pada beberapa kelompok hewan uji dengan satu
dosis per kelompok, kemudian diamati adanya efek toksik dan kematian. Hewan
yang mati selama percobaan dan yang hidup sampai akhir percobaan diotopsi
untuk dievaluasi adanya gejala-gejala toksisitas (BPOM, RI., 2014).
Tujuan dilakukannya uji toksisitas akut sebenarnya bukan hanya untuk
menetukan dosis letal 50% melainkan juga untuk mengetahui mekanisme dan
target organ dari zat toksik yang diuji, tetapi sangat luas yaitu meliputi:
i. Menentukan range dosis (interval dosis) untuk uji berikutnya (uji farmakologi, toksisitas subkronis dan toksisitas kronis).
ii. Untuk mengklasifikasikan zat uji, apakah kategori praktis tidak toksik, super
toksik atau yang lain, sebagaimana tabel dibawah.
Tabel 2.1 Klasifikasi toksisitas sediaan uji (BPOM, RI., 2014)
Tingkat toksisitas LD50 oral (mg/kg bb) Klasifikasi
1 <1 Sangat toksik
2 1 – 50 Toksik
3 50 – 500 Toksik sedang
4 500 – 5000 Toksik ringan
5 5000 – 15000 Praktis tidak toksik
6 >15000 Relatif tidak membahayakan
Sumber: BPOM, RI., 2014
iii. Mengidentifikasikan kemungkinan target organ atau sistem fisiologi yang
dipengaruhi.
iv. Mengetahui hubungan antara dosis dengan timbulnya efek seperti perubahan
vii. Mengetahui pengaruh umur, jenis kelamin, cara pemberian dan faktor
lingkungan terhadap toksisitas suatu zat (Priyanto, 2009).
LD50 adalah besarnya dosis yang menyebabkan kematian 50% dari hewan
yang dicoba dalam jangka waktu tertentu. Hal ini memberikan gambaran besarnya
daya racun suatu zat; makin kecil LD50, maka makin besar daya racun suatu zat,
begitu juga sebaliknya (Elya, 2010).
Faktor-faktor yang berpengaruh pada LD50 sangat bervariasi antara jenis
yang satu dengan jenis yang lain dan antara individu yang satu dengan individu
yang lain dalam satu jenis. Faktor tersebut antara lain (Retnomurti, 2008):
i. Spesies, strain dan keragaman individu
Setiap spesies dan strain yang berbeda memiliki sistem metabolisme dan
detoksikasi yang berbeda. Setiap spesies mempunyai perbedaan kemampuan
bioaktivasi dan toksikasi suatu zat.
ii. Perbedaan jenis kelamin
Perbedaan jenis kelamin mempengaruhi toksisitas akut yang disebabkan
oleh pengaruh langsung dari kelenjar endokrin. Hewan betina mempunyai sistem
hormonal yang berbeda dengan hewan jantan sehingga menyebabkan perbedaan
kepekaan terhadap suatu toksikan.
iii. Umur
Hewan-hewan yang lebih muda memiliki kepekaan yang lebih tinggi
terhadap obat karena enzim untuk biotransformasi masih kurang dan fungsi ginjal
belum sempurna. Pada hewan yang tua kepekaan individu meningkat karena
fungsi biotransformasi dan ekskresi sudah menurun.
iv. Berat badan
diberikan semakin besar.
v. Cara pemberian
Lethal dosis juga dapat dipengaruhi oleh cara pemberian. Pemberian obat
peroral tidak langsung didistribusikan ke seluruh tubuh. Pemberian obat atau
toksikan peroral didistribusikan ke seluruh tubuh setelah terjadi penyerapan di
saluran cerna sehingga mempengaruhi kecepatan metabolisme di dalam tubuh.
vi. Faktor lingkungan
Beberapa faktor lingkungan yang mempengaruhi toksisitas akut antara lain
temperatur, kelembaban, iklim, perbedaan siang dan malam. Perbedaan temperatur
suatu tempat akan mempengaruhi keadaan fisiologis suatu hewan.
vii. Kesehatan hewan
Status hewan dapat memberikan respon yang berbeda terhadap suatu
toksikan. Kesehatan hewan sangat dipengaruhi oleh kondisi hewan dan
lingkungan. Hewan yang tidak sehat dapat memberikan nilai LD50 yang berbeda
dibandingkan dengan nilai LD50 yang didapatkan dari hewan sehat.
viii. Diet
Komposisi makanan hewan percobaan dapat mempengaruhi nilai LD50.
Komposisi makanan akan mempengaruhi status kesehatan hewan percobaan.
2. Uji toksisitas subkronis oral
Prinsip dari uji toksisitas subkronis oral adalah sediaan uji dalam beberapa
tingkat dosis diberikan setiap hari pada beberapa kelompok hewan uji dengan satu
dosis per kelompok selama 28 atau 90 hari, bila diperlukan ditambahkan kelompok
satelit untuk melihat adanya efek tertunda atau efek yang bersifat reversibel.
Selama waktu pemberian sediaan uji hewan harus diamati setiap hari untuk
menentukan adanya toksisitas. Hewan yang mati selama periode pemberian
sediaan uji bila belum melewati periode rigor mortis (kaku) segera diotopsi dan
organ serta jaringan diamati secara makropatologi dan histopatologi.
Semua hewan yang masih hidup pada akhir periode pemberian sediaan uji
diotopsi selanjutnya dilakukan pengamatan secara makropatologi pada setiap
organ dan jaringan, pemeriksaan hematologi, biokimia klinis dan histopatologi.
Tujuan uji toksisitas subkronis oral adalah untuk memperoleh informasi
adanya efek toksik zat yang tidak terdeteksi pada uji toksisitas akut, informasi
kemungkinan adanya efek toksik setelah pemaparan sediaan uji secara berulang
dalam jangka waktu tertentu, informasi dosis yang tidak menimbulkan efek toksik
(No Observed Adverse Effect Level / NOAEL) dan mempelajari adanya efek kumulatif dan efek reversibilitas zat tersebut (BPOM, RI., 2014).
3. Uji toksisitas kronis oral
Uji toksisitas kronis oral adalah suatu pengujian untuk mendeteksi efek
toksik yang muncul setelah pemberian sediaan uji secara berulang sampai seluruh
umur hewan. Uji toksisitas kronis pada prinsipnya sama dengan uji toksisitas
subkronis, tetapi sediaan uji diberikan selama tidak kurang dari 12 bulan. Tujuan
dari uji toksisitas kronis oral adalah untuk mengetahui profil efek toksik setelah
pemberian sediaan uji secara berulang selama waktu yang panjang dan untuk
informasi toksisitas secara umum meliputi efek neurologi, fisiologi, hematologi,
biokimia klinis dan histopatologi (BPOM, RI., 2014).
4. Uji teratogenisitas
Uji teratogenisitas adalah suatu pengujian untuk memperoleh informasi
adanya abnormalitas fetus yang terjadi karena pemberian sediaan uji selama masa
pembentukan organ fetus (masa organogenesis). Informasi tersebut meliputi
abnormalitas bagian luar fetus (morfologi), jaringan lunak serta kerangka fetus.
Prinsip uji teratogenisitas adalah pemberian sediaan uji dalam beberapa
tingkat dosis pada beberapa kelompok hewan bunting selama paling sedikit masa
organogenesis dari kebuntingan, satu dosis per kelompok. Satu hari sebelum waktu
melahirkan induk dibedah, uterus diambil dan dilakukan evaluasi terhadap fetus
(BPOM, RI., 2014).
5. Uji sensitisasi kulit
Uji sensitisasi kulit adalah suatu pengujian untuk mengidentifikasi suatu zat
yang berpotensi menyebabkan sensitisasi kulit. Prinsip uji sensitisasi kulit adalah
hewan uji diinduksi dengan dan tanpa Freund’s Complete Adjuvant (FCA) secara
injeksi intradermal dan topikal untuk membentuk respon imun, kemudian
dilakukan uji tantang (challenge test). Tingkat dan derajat reaksi kulit dinilai
berdasarkan skala Magnusson dan Kligman (BPOM, RI., 2014).
digunakan sebagai kontrol. Derajat iritasi/korosi dievaluasi dengan pemberian skor
terhadap cedera pada konjungtiva, kornea, dan iris pada interval waktu tertentu.
Tujuan uji iritasi mata adalah untuk memperoleh informasi adanya kemungkinan
bahaya yang timbul pada saat sediaan uji terpapar pada mata dan membran
mukosa mata (BPOM, RI., 2014).
7. Uji mutagenik
Uji mutagenik adalah uji yang dilakukan untuk memperoleh informasi
mengenai kemungkinan terjadinya efek mutagenik suatu senyawa. Efek mutagenik
merupakan efek yang menyebabkan terjadinya perubahan pada sifat genetika sel
tubuh makhluk hidup (Lu, 1995).
8. Uji karsinogenik
Uji karsinogenik dilakukan untuk memperoleh informasi mengenai efek
korsinogenik suatu senyawa pada hewan percobaan. Suatu senyawa bersifat
karsinogenik jika senyawa tersebut dapat menginduksi karsinoma (pembentukan
tumor). Uji ini memerlukan biaya yang banyak dan waktu yang lama (Lu, 1995).
2.5 Hati
Salah satu organ yang sering menderita karena adanya zat-zat toksik adalah
hati, bahan kimia kebanyakan mengalami metabolisme dalam hati dan oleh
karenanya maka banyak bahan kimia yang berpotensi merusak sel-sel hati. Bahan
kimia yang dapat mempengaruhi hati disebut hipotoksik (Wicaksono, 2002).
Secara anatomi hati terdiri dari beberapa lobus, tergantung pada spesiesnya.
Hepar mencit (Mus musculus L.) memiliki empat lobus utama yang saling berhubungan satu sama lain dan dapat tampak keseluruhannya pada bagian dorsal