KANDUNGAN LOGAM BERAT Hg, Pb DAN Cr PADA AIR, SEDIMEN DAN KERANG HIJAU (Perna viridis L.) DI PERAIRAN KAMAL
MUARA, TELUK JAKARTA
DANDY APRIADI
DEPARTEMEN MANAJEMEN SUMBERDAYA PERAIRAN FAKULTAS PERIKANAN DAN ILMU KELAUTAN
PERNYATAAN MENGENAI SKRIPSI
Dengan ini saya menyatakan bahwa Skripsi yang berjudul
KANDUNGAN LOGAM BERAT Hg, Pb DAN Cr PADA AIR, SEDIMEN DAN KERANG HIJAU (Perna viridis L.) DI PERAIRAN KAMAL MUARA, TELUK
JAKARTA
Adalah benar merupakan hasil karya sendiri dan belum pernah diajukan dalam bentuk apapun kepada perguruan tinggi mana pun. Semua sumber data dan informasi yang berasal atau dikutip dari karya yang diterbitkan maupun yang tidak diterbitkan oleh penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir Skripsi ini
Bogor, Desember 2005
ABSTRAK
DANDY APRIADI. Kandungan Logam Berat Hg, Pb dan Cr Pada Air, Sedimen dan Kerang hijau (Perna viridis L.) di Perairan Muara Kamal, Teluk Jakarta. Dibimbing oleh ETTY RIANI dan HEFNI EFFENDI.
Pencemaran di laut salah satunya disebabkan oleh logam berat. Logam berat merupakan bahan anorganik yang bersifat toksik dan dapat terakumulasi dalam tubuh biota air. Kerang hijau (Perna viridis L.) adalah biota yang digunakan sebagai bioindikator adanya pencemaran logam berat.
Peneilitian ini dilaksanakan di Perairan Kamal Muara, Teluk Jakarta dari bulan September hingga November 2004. peneiltian ini mengkaji kandungan logam berat Hg, Pb dan Cr dalam air, sedimen dan kerang hijau (Perna viridis L.) dan melihat peranan parameter kualitas air terhadap kandungan logam berat di dalam tubuh kerang hijau (Perna viridis L.). Pengambilan contoh air, sedimen dan kerang hijau (Perna viridis L.) dilakukan di 3 stasiun dengan selang waktu pengambilan contoh adalah selama 1 bulan.
Hasil penelitian ini menunjukkan rata-rata kualitas Perairan Kamal Muara masih berada pada kisaran normal. Kandungan logam Hg, Pb dan Cr di kolom air berfluktuatif antara 0,00004 – 0.056 ppm. Pada sedimen nilai rata-ratanya antara 0,019 – 13,15 ppm. Dan rata-rata nilai kandungan logam di dalam tubuh kerang hijau (Perna viridis L.) sebesar 0,062 – 47,813 ppm. Rata-rata nilai faktor konsentrasi dalam tubuh kerang hijau (Perna viridis L.) 64,68 – 11270,40. logam Pb dan Cr cenderung diakumulatif tinggi dibanding dengan logam Hg oleh kerang hijau (Perna viridis L.). Hasil analisis PCA menunjukkan adanya peranan dari parameter kualitas perairan terhadap kandungan logam berat Hg, Pb dan Cr di dalam tubuh kerang hijau (Perna viridis L.).
KANDUNGAN LOGAM BERAT Hg, Pb DAN Cr PADA AIR, SEDIMEN DAN KERANG HIJAU (Perna viridis L.) DI PERAIRAN KAMAL
MUARA, TELUK JAKARTA
DANDY APRIADI
Skripsi
sebagai salah satu syarat untuk memperoleh gelar Sarjana Perikanan pada
Departemen Manajemen Sumberdaya Perairan
DEPARTEMEN MANAJEMEN SUMBERDAYA PERAIRAN FAKULTAS PERIKANAN DAN ILMU KELAUTAN
SKRIPSI
Judul Skripsi : Kandungan Logam Berat Hg, Pb dan Cr pada Air, Sedimen dan Kerang hijau (Perna viridis L.) di Perairan Muara Kamal, Teluk Jakarta
Nama : Dandy Apriadi
NIM : C02400070
Disetujui,
Pembimbing I Pembimbing II
Dr. Ir. Etty Riani. H, MS. Dr. Ir. Hefni Effendi M.Phil. NIP. 131 619 682 NIP. 131 841 731
Mengetahui,
Dekan Fakultas Perikanan dan Ilmu Kelautan
Dr. Ir. Kadarwan Soewardi NIP. 130 805 031
PRAKATA
Puji syukur penulis panjatkan kehadirat Allah SWT atas segala curahan rahmat dan hidayah-Nya sehingga akhirnya penulis dapat menyelesaikan skripsi dengan judul Kandungan Logam Berat Hg, Pb dan Cr pada Air, Sedimen dan Kerang Hijau (Perna viridis L.) di Perairan Kamal Muara, Teluk Jakarta.
Penulis mengucapkan terima kasih kepada :
1. Ibu Dr. Ir. Etty Riani, MS dan Bapak Dr. Ir. Hefni Effendi, M.Phil selaku komisi pembimbing skripsi yang telah banyak memberikan bimbingan, pengarahan dan perbaikan sehingga penulis dapat menyelesaikan skripsi ini.
2. Ibu Ir. Nurlisa A. Butet, M.Sc selaku pembimbing akademik yang telah banyak memberikan bimbingan, saran selama penulis menjalankan studi.
3. Bapak Ir. Agustinus Samosir M.Phil selaku dosen penguji tamu, dan Ibu Dr.Ir. Yunizar Ernawati, MS. Selaku dosen penguji dari Departemen MSP.
4. Papa, Mama , dan adik-adikku (Ary,Anggi) yang telah memberikan doa, perhatian, kasih sayang dan semangat selama dalam menyelesaikan skripsi ini.
5. Bang Iwan Mulyawan dan Pak Maga yang telah banyak membantu penulis selama menjalani penelitian.
6. Rekan-rekan Atheners di Rumah Kita (bram, fery, oliz, dodie, moko, rudi, zahid, dian, jimmy, heriman) atas segala saran, pendapat dan dukungan selama penelitian. All of MeSePers dan teman-teman kost selama di IPB .
Penulis menyadari skripsi ini masih banyak terdapat kekurangan, dan penulis berharap akan mendapat banyak masukan yang dapat digunakan untuk perbaikan di masa yang akan datang.
Bogor, Desember 2005
DAFTAR ISI
B. Pembahasan ... 39
V. KESIMPULAN DAN SARAN ... 44
DAFTAR PUSTAKA ... 46
DAFTAR TABEL
Halaman
1. Logam di dalam Hidrosfer ... 13
2. Parameter-parameter kualitas air, sedimen dan biota air yang diamati ... 18 3. Hasil analisis Principal Component Analysis (PCA) untuk logam
Hg terhadap semua ukuran tubuh kerang hijau ... 35
4. Hasil analisis Principal Component Analysis (PCA) untuk logam
Pb terhadap semua ukuran tubuh kerang hijau ... 37
5. Hasil analisis Principal Component Analysis (PCA) untuk logam
Cr terhadap semua ukuran tubuh kerang hijau ... 38
6. Koefisien variabel dalam fungsi linear sumbu utama logam Hg
pada kerang hijau ukuran besar ... 64 7. Koefisien variabel l dalam fungsi linear sumbu utama logam Hg
pada kerang hijau ukuran sedang ... 65 8. Koefisien variabel dalam fungsi linear sumbu utama logam Hg
pada kerang hijau ukuran kecil ... 66 9. Koefisien variabel dalam fungsi linear sumbu utama logam Pb
pada kerang hijau ukuran besar ... 67 10. Koefisien variabel dalam fungsi linear sumbu utama logam Pb
pada kerang hijau ukuran sedang ... 68 11. Koefisien variabel dalam fungsi linear sumbu utama logam Pb
pada kerang hijau ukuran kecil ... 69 12. Koefisien variabel dalam fungsi linear sumbu utama logam Cr
pada kerang hijau ukuran besar ... 70 13. Koefisien variabel dalam fungsi linear sumbu utama logam Cr
pada kerang hijau ukuran sedang ... 71 14. Koefisien variabel dalam fungsi linear sumbu utama logam Cr
KANDUNGAN LOGAM BERAT Hg, Pb DAN Cr PADA AIR, SEDIMEN DAN KERANG HIJAU (Perna viridis L.) DI PERAIRAN KAMAL
MUARA, TELUK JAKARTA
DANDY APRIADI
DEPARTEMEN MANAJEMEN SUMBERDAYA PERAIRAN FAKULTAS PERIKANAN DAN ILMU KELAUTAN
PERNYATAAN MENGENAI SKRIPSI
Dengan ini saya menyatakan bahwa Skripsi yang berjudul
KANDUNGAN LOGAM BERAT Hg, Pb DAN Cr PADA AIR, SEDIMEN DAN KERANG HIJAU (Perna viridis L.) DI PERAIRAN KAMAL MUARA, TELUK
JAKARTA
Adalah benar merupakan hasil karya sendiri dan belum pernah diajukan dalam bentuk apapun kepada perguruan tinggi mana pun. Semua sumber data dan informasi yang berasal atau dikutip dari karya yang diterbitkan maupun yang tidak diterbitkan oleh penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir Skripsi ini
Bogor, Desember 2005
ABSTRAK
DANDY APRIADI. Kandungan Logam Berat Hg, Pb dan Cr Pada Air, Sedimen dan Kerang hijau (Perna viridis L.) di Perairan Muara Kamal, Teluk Jakarta. Dibimbing oleh ETTY RIANI dan HEFNI EFFENDI.
Pencemaran di laut salah satunya disebabkan oleh logam berat. Logam berat merupakan bahan anorganik yang bersifat toksik dan dapat terakumulasi dalam tubuh biota air. Kerang hijau (Perna viridis L.) adalah biota yang digunakan sebagai bioindikator adanya pencemaran logam berat.
Peneilitian ini dilaksanakan di Perairan Kamal Muara, Teluk Jakarta dari bulan September hingga November 2004. peneiltian ini mengkaji kandungan logam berat Hg, Pb dan Cr dalam air, sedimen dan kerang hijau (Perna viridis L.) dan melihat peranan parameter kualitas air terhadap kandungan logam berat di dalam tubuh kerang hijau (Perna viridis L.). Pengambilan contoh air, sedimen dan kerang hijau (Perna viridis L.) dilakukan di 3 stasiun dengan selang waktu pengambilan contoh adalah selama 1 bulan.
Hasil penelitian ini menunjukkan rata-rata kualitas Perairan Kamal Muara masih berada pada kisaran normal. Kandungan logam Hg, Pb dan Cr di kolom air berfluktuatif antara 0,00004 – 0.056 ppm. Pada sedimen nilai rata-ratanya antara 0,019 – 13,15 ppm. Dan rata-rata nilai kandungan logam di dalam tubuh kerang hijau (Perna viridis L.) sebesar 0,062 – 47,813 ppm. Rata-rata nilai faktor konsentrasi dalam tubuh kerang hijau (Perna viridis L.) 64,68 – 11270,40. logam Pb dan Cr cenderung diakumulatif tinggi dibanding dengan logam Hg oleh kerang hijau (Perna viridis L.). Hasil analisis PCA menunjukkan adanya peranan dari parameter kualitas perairan terhadap kandungan logam berat Hg, Pb dan Cr di dalam tubuh kerang hijau (Perna viridis L.).
KANDUNGAN LOGAM BERAT Hg, Pb DAN Cr PADA AIR, SEDIMEN DAN KERANG HIJAU (Perna viridis L.) DI PERAIRAN KAMAL
MUARA, TELUK JAKARTA
DANDY APRIADI
Skripsi
sebagai salah satu syarat untuk memperoleh gelar Sarjana Perikanan pada
Departemen Manajemen Sumberdaya Perairan
DEPARTEMEN MANAJEMEN SUMBERDAYA PERAIRAN FAKULTAS PERIKANAN DAN ILMU KELAUTAN
SKRIPSI
Judul Skripsi : Kandungan Logam Berat Hg, Pb dan Cr pada Air, Sedimen dan Kerang hijau (Perna viridis L.) di Perairan Muara Kamal, Teluk Jakarta
Nama : Dandy Apriadi
NIM : C02400070
Disetujui,
Pembimbing I Pembimbing II
Dr. Ir. Etty Riani. H, MS. Dr. Ir. Hefni Effendi M.Phil. NIP. 131 619 682 NIP. 131 841 731
Mengetahui,
Dekan Fakultas Perikanan dan Ilmu Kelautan
Dr. Ir. Kadarwan Soewardi NIP. 130 805 031
PRAKATA
Puji syukur penulis panjatkan kehadirat Allah SWT atas segala curahan rahmat dan hidayah-Nya sehingga akhirnya penulis dapat menyelesaikan skripsi dengan judul Kandungan Logam Berat Hg, Pb dan Cr pada Air, Sedimen dan Kerang Hijau (Perna viridis L.) di Perairan Kamal Muara, Teluk Jakarta.
Penulis mengucapkan terima kasih kepada :
1. Ibu Dr. Ir. Etty Riani, MS dan Bapak Dr. Ir. Hefni Effendi, M.Phil selaku komisi pembimbing skripsi yang telah banyak memberikan bimbingan, pengarahan dan perbaikan sehingga penulis dapat menyelesaikan skripsi ini.
2. Ibu Ir. Nurlisa A. Butet, M.Sc selaku pembimbing akademik yang telah banyak memberikan bimbingan, saran selama penulis menjalankan studi.
3. Bapak Ir. Agustinus Samosir M.Phil selaku dosen penguji tamu, dan Ibu Dr.Ir. Yunizar Ernawati, MS. Selaku dosen penguji dari Departemen MSP.
4. Papa, Mama , dan adik-adikku (Ary,Anggi) yang telah memberikan doa, perhatian, kasih sayang dan semangat selama dalam menyelesaikan skripsi ini.
5. Bang Iwan Mulyawan dan Pak Maga yang telah banyak membantu penulis selama menjalani penelitian.
6. Rekan-rekan Atheners di Rumah Kita (bram, fery, oliz, dodie, moko, rudi, zahid, dian, jimmy, heriman) atas segala saran, pendapat dan dukungan selama penelitian. All of MeSePers dan teman-teman kost selama di IPB .
Penulis menyadari skripsi ini masih banyak terdapat kekurangan, dan penulis berharap akan mendapat banyak masukan yang dapat digunakan untuk perbaikan di masa yang akan datang.
Bogor, Desember 2005
DAFTAR ISI
B. Pembahasan ... 39
V. KESIMPULAN DAN SARAN ... 44
DAFTAR PUSTAKA ... 46
DAFTAR TABEL
Halaman
1. Logam di dalam Hidrosfer ... 13
2. Parameter-parameter kualitas air, sedimen dan biota air yang diamati ... 18 3. Hasil analisis Principal Component Analysis (PCA) untuk logam
Hg terhadap semua ukuran tubuh kerang hijau ... 35
4. Hasil analisis Principal Component Analysis (PCA) untuk logam
Pb terhadap semua ukuran tubuh kerang hijau ... 37
5. Hasil analisis Principal Component Analysis (PCA) untuk logam
Cr terhadap semua ukuran tubuh kerang hijau ... 38
6. Koefisien variabel dalam fungsi linear sumbu utama logam Hg
pada kerang hijau ukuran besar ... 64 7. Koefisien variabel l dalam fungsi linear sumbu utama logam Hg
pada kerang hijau ukuran sedang ... 65 8. Koefisien variabel dalam fungsi linear sumbu utama logam Hg
pada kerang hijau ukuran kecil ... 66 9. Koefisien variabel dalam fungsi linear sumbu utama logam Pb
pada kerang hijau ukuran besar ... 67 10. Koefisien variabel dalam fungsi linear sumbu utama logam Pb
pada kerang hijau ukuran sedang ... 68 11. Koefisien variabel dalam fungsi linear sumbu utama logam Pb
pada kerang hijau ukuran kecil ... 69 12. Koefisien variabel dalam fungsi linear sumbu utama logam Cr
pada kerang hijau ukuran besar ... 70 13. Koefisien variabel dalam fungsi linear sumbu utama logam Cr
pada kerang hijau ukuran sedang ... 71 14. Koefisien variabel dalam fungsi linear sumbu utama logam Cr
21. Rata-rata kandungan logam berat Cr
pada kerang hijau ukuran sedang ( 4 – 6 cm) ... 32
22. Rata-rata kandungan logam berat Pb pada kerang hijau ukuran kecil (< 4 cm) ... 32
23. Rata-rata faktor logam berat Hg pada kerang hijau ... 33
24. Rata-rata faktor logam berat Pb pada kerang hijau ... 34
25. Rata-rata faktor logam berat Cr pada kerang hijau ... 35
26. Hasil analisis PCA (F1xF2) parameter fisika-kimia dengan kerang hijau berukuran besar (> 6 cm) ... 64
27. Hasil analisis PCA (F1xF2) parameter fisika-kimia dengan kerang hijau berukuran sedang (4 - 6 cm) ... 65
28. Hasil analisis PCA (F1xF2) parameter fisika-kimia dengan kerang hijau berukuran kecil (< 4 cm) ... 66
29. Hasil analisis PCA (F1xF2) parameter fisika-kimia dengan kerang hijau berukuran besar (> 6 cm) ... 67
30. Hasil analisis PCA (F1xF2) parameter fisika-kimia dengan kerang hijau berukuran sedang (4 - 6 cm) ... 68
31. Hasil analisis PCA (F1xF2) parameter fisika-kimia dengan kerang hijau berukuran kecil (< 4 cm) ... 69
32. Hasil analisis PCA (F1xF2) parameter fisika-kimia dengan kerang hijau berukuran besar (> 6 cm) ... 70
33. Hasil analisis PCA (F1xF2) parameter fisika-kimia dengan kerang hijau berukuran sedang (4 - 6 cm) ... 71
34. Hasil analisis PCA (F1xF2) parameter fisika-kimia dengan kerang hijau berukuran kecil (< 4 cm) ... 72
DAFTAR LAMPIRAN
Halaman
1. Kandungan logam berat (Hg,Pb dan Cr) pada kerang hijau (Perna viridis L.) di Perairan Kamal Muara, Teluk Jakarta ... 51 2. Kualitas air fisika dan kimia di Perairan Kamal Muara,
Teluk Jakarta ... 53 3. Kandungan logam pada kolom air dan sedimen
di Perairan Kamal Muara, Teluk Jakarta ... 54 4. Baku mutu air laut untuk biota laut berdasarkan Keputusan Menteri
Negara Lingkungan Hidup No. 51 Tahun 2004 ... 56 5. Prosedur analisis logam berat
I. PENDAHULUAN
A. Latar Belakang
Perkembangan industri yang demikian pesat dewasa ini selain memberikan dampak yang positif juga memberikan dampak negatif. Dampak positif berupa perluasan lapangan pekerjaan dan pemenuhan kebutuhan hidup manusia, sedangkan dampak negatif yang muncul adalah penurunan kualitas perairan akibat buangan air limbah (pencemaran) yang melampaui ambang batas.
Di suatu industri, limbah yang dihasilkan sangat bervariasi tergantung dari jenis dan ukuran industri, pengawasan pada proses industri, derajat penggunaan air, dan derajat pengolahan air limbah yang ada. Selain limbah cair, limbah padat (sampah) juga merupakan beban pencemaran yang dapat masuk ke perairan baik secara langsung maupun tak langsung. Pada limbah industri seringkali terdapat bahan pencemar yang sangat membahayakan seperti logam berat (Palar, 1994).
Salah satu perairan laut yang kualitas perairannya sudah melewati batas ambang baku mutu kualitas perairan menurut kriteria Men LH (1988) adalah Teluk Jakarta. Sejak tahun 1972 Perairan Teluk Jakarta telah mengalami pencemaran bahan organik dan logam berat yang telah melampaui ambang batas (Kompas, 2004). Diduga penyebabnya adalah masukan (load) limbah ke dalam Perairan Teluk Jakarta yang dibawa oleh 13 sungai yang bermuara ke dalamnya. Adapun limbah yang masuk ke dalam perairan ini berasal dari kegiatan manusia yaitu kegiatan industri pengolahan (97,82 % yakni 1.632.896,47 m3/tahun), domestik (2,17 % yakni 36.229,90 m3/tahun) dan limbah industri pertanian (0,01% yakni 232,25 m3/tahun) (KPPL, 1997). Namun bukan hanya limbah bahan organik saja yang dihasilkan dari kegiatan manusia tersebut, tetapi limbah bahan beracun (anorganik) seperti logam berat juga terkandung di dalamnya.
dan biomagnifikasi melalui beberapa jalan yaitu: melalui saluran pernapasan, saluran makanan dan melalui kulit (Darmono, 2001).
Jenis kerang-kerangan merupakan bioindikator pencemaran yang efisien untuk menduga pencemaran lo gam berat, karena merupakan filter feeder dan mempunyai toleransi yang besar terhadap tekanan ekologis yang tinggi. Kerang hijau (Perna viridis L.) merupakan salah satu jenis kerang-kerangan (moluska, kelas bivalvia) yang dapat bertahan hidup dan berkembang biak pada kondisi tekanan ekologis yang tinggi. Kemampuan dalam mengakumulasi logam berat di kerang hijau dapat digunakan untuk memperoleh gambaran tingkat pencemaran logam berat pada lingkungan dimana kerang hijau itu hidup.
Penelitian mengenai logam berat dengan kerang hijau (Perna viridis L) sebagai bioindikator telah banyak dilakukan, diantaranya adalah pendugaan tingkat akumulasi logam berat Pb, Cd, Cu, Zn dan Ni pada kerang hijau berukuran kurang dari 5 cm (Akbar, 2002 ) dan pada kerang hijau berukuran lebih dari 4,7 cm (Suryanto, 2002). Selain itu, penelitian yang dilakukan adalah pendugaan logam berat pada air dan sedimen (Tresnasari, 2001). Namun penelitian baru relatif belum didapatkan padahal logam berat diakumulasi dalam tubuh mahluk hidup sehingga diperlukan informasi terbaru mengenai logam berat dalam tubuh kerang hijau.
B. Perumusan Masalah
Aktivitas manusia berupa kegiatan industri, rumah tangga, pertanian dan pertambangan menghasilkan buangan limbah yang tidak digunakan kembali yang menjadi sumber pencemar bagi lingkungan (udara, air dan tanah). Bahan pencemar dari hasil kegiatan ini berupa bahan partikulat, bahan terlarut dan gas-gas. Bahan pencemar ini akan bermuara pada suatu lingkungan perairan. Lingkungan perairan yang tercemar bahan-bahan tersebut akan mengalami penurunan kualitas air yang selanjutnya dapat mengganggu kesetimbangan ekologis yang ada termasuk kehidupan biotanya. Logam berat termasuk salah satu bahan pencemar yang dihasilkan dari kegiatan yang disebutkan di atas. Bahan ini dikategorikan ke dalam limbah bahan beracun berbahaya (B3) karena efek samping yang ditimbulkannya apabila masuk ke dalam tubuh organisme juga kepada manusia.
Teluk Jakarta merupakan salah satu perairan yang telah mengalami penurunan kualitas air, yang diduga disebabkan oleh masuknya 13 sungai yang bermuara ke dalamnya, dan salah satunya adalah Sungai Kamal. Untuk lebih jelas dapat dilihat dari Gambar 1.
Gambar 1. Alur perumusan masalah penelitian Aktivitas manusia
Industri Rumah tangga Pertanian/pertambakan
LImbah
Udara Perairan Tanah
Kualitas air (peningkatan kadar logam Hg,Pb dan Cr)
C. Tujuan
Penelitian ini bertujuan :
1. Menentukan kandungan logam berat Hg, Pb dan Cr pada air, sedimen dan kerang hijau ukuran besar, sedang dan kecil .
II. TINJAUAN PUSTAKA
A. Kerang hijau ( Perna viridis L.)
Kerang hijau (Perna viridis L.) di Indonesia mempunyai nama yang berbeda-beda di setiap daerah, seperti Kijing (Jakarta), Kedaung (Banten) dan Kemudi Kapal (Riau). Di Malaysia dikenal dengan sebutan Siput Kudu, Chay Luan/Tham chay (Singapura), Ta Hong (Philipina) dan Hoi Mong Pong (Thailand) (Kastoro, 1988).
Menurut Vakily (1989) kerang hijau (Green Mussels) diklasifikasikan sebagai berikut :
Filum : Moluska Kelas : Bivalvia
Subkelas : Lamellibranchia Ordo : Anisomyria Famili : Mytilidae Genus : Perna
Spesies : Perna viridis L.
www.dnr.state.sc.us
Gambar 2. Kerang hijau (Perna viridis L.) Sumber : www.dnr.state.sc.us)
Kerang hijau adalah organisme yang dominan pada ekosistem litoral
pasir, dengan cahaya dan pergerakan air yang cukup, serta kadar garam yang tidak terlalu tinggi (Setyobudiandi, 2000).
Persyaratan yang baik menurut Direktorat Jenderal Perikanan (1985) untuk kehidupan kerang hijau adalah perairan bersubstrat lumpur dengan metode bagan rakit tancap, kedalaman 3 -10 m, kecepatan arus 25 cm/detik, salinitas 27 - 35 ‰ dan suhu 26 - 32 ºC.
Berdasarkan cara memperoleh makanannya, moluska bivalvia digolongkan dalam kelompok filter feeder. Apabila makanan diperoleh dengan menyaring fitoplankton dari perairan yang ditempati, maka disebut sebagai suspension feeder. Apabila makanan atau bahan organik diambil dari substratum tempat hidupnya maka disebut sebagai deposit feeder (Setyobudiandi, 2000).
Kerang hijau (Perna viridis L.) de wasa dapat menghasilkan telur lebih kurang 1,2 juta. Pemijahan ini terjadi akibat adanya rangsangan alami seperti perubahan suhu dan salinitas. Sel telur yang telah dibuahi akan berkembang dan menetas menjadi larva. Larva kerang hijau bersifat planktonik, yaitu melayang di air dan terbawa arus selama dua minggu. Larva akan mengalami beberapa kali perubahan bentuk (metamorphosa). Pada akhir stadia larva, kerang hijau akan mengalami perubahan cara hidup dari planktonik menjadi
sessil (tinggal diam dan menempel). Pada saat itu apabila larva tidak mendapatkan substrat maka akan segera mati (Departemen Pertanian, 1985). Kecepatan tumbuh kerang hijau berkisar antara 0,7-1,0 cm per bulan (Direktorat Jenderal Perikanan, 1985).
Menurut Roberts (1976) kelas bivalvia telah digunakan oleh ahli ekologi dalam menganalisis pencemaran air. Hal ini karena sifatnya yang menetap dan cara makan pada umumnya filter feeder, sehingga mempunyai kemampuan mengakumulasi bahan-bahan polutan seperti logam berat.
B. Karakteristik Logam Berat
Logam berasal dari kerak bumi berupa bahan-bahan murni organik dan anorganik. Secara alami siklus perputaran logam adalah dari kerak bumi ke lapisan tanah, ke mahluk hidup, ke dalam air, selanjutnya mengendap dan akhirnya kembali ke kerak bumi (Darmono, 1995).
Meskipun demikian beberapa unsur (boron, silikon, germanium, arsen dan tellurium) yang diketahui sebagai metaloid, mempunyai satu atau lebih sifat-sifat tersebut. Tetapi dalam memisahkan tidak cukup dengan hanya membedakan kekhasan logam dan bukan logam. Lebih jauh, bentuk alotrofik dari beberapa unsur di garis batas mungkin juga memperlihatkan sifat-sifat yang berbeda (Wittman, 1979 in Connell dan Miller, 1995).
Menurut Connell dan Miller (1995), logam berat adalah suatu logam dengan berat jenis lebih besar. Logam ini memiliki karakter seperti berkilau, lunak atau dapat ditempa, mempunyai daya hantar panas dan listrik yang tinggi dan bersifat kimiawi, yaitu sebagai dasar pembentukan reaksi dengan asam. Selain itu logam berat adalah unsur yang mempunyai densitas lebih besar dari 5 gr/cm3, mempunyai nomor atom lebih besar dari 21 dan terdapat di bagian tengah daftar periodik.
Logam berat adalah istilah yang digunakan secara umum untuk kelompok logam dan metaloid dengan densitas lebih besar dari 5 g/cm3, terutama pada unsur seperti Cd, Cr, Cu, Hg, Ni, Pb dan Zn. Unsur-unsur ini biasanya erat kaitannya dengan masalah pencemaran dan toksisitas. Logam berat secara alami ditemukan pada batu-batuan dan mineral lainnya, maka dari itu logam berat secara normal merupakan unsur dari tanah, sedimen, air dan organisme hidup serta akan menyebabkan pencemaran bila konsentrasinya telah melebihi batas normal. Jadi konsentrasi relatif logam dalam media adalah hal yang paling penting (Alloway dan Ayres, 1993).
terhadap toksisitas logam juga bergantung pada daya detoksikasi individu yang bersangkutan, dan faktor kesehatan sangat mempengaruhi (Palar, 1994).
1. Air raksa (Hg)
Logam merkuri bernomor atom 80, berat atom 200,59, titik didih 356,9
o
C, dan massa jenis 13,6 gr/ml (Reilly, 1991). Merkuri dalam perairan dapat berasal dari buangan limbah industri kelistrikan dan elektronik, baterai, pabrik bahan peledak, fotografi, pelapisan cermin, pelengkap pengukur, industri bahan pengawet, pestisida, industri kimia, petrokimia, limbah kegiatan laboratorium dan pembangkit tenaga listrik yang menggunakan bahan baku bakar fosil (Suryadiputra, 1995).
Merkuri terdapat dalam bentuk Hg (murni), Hg anorganik dan Hg organik (Darmono, 1995). Merkuri di alam umumnya terdapat sebagai metil merkuri yaitu bentuk senyawa organik (alkil merkuri atau metil merkuri) dengan daya racun tinggi dan sukar terurai dibandingkan zat asalnya. Bila terakumulasi metil merkuri dalam tubuh, akan mengakibatkan keracunan yang bersifat akut maupun kronis (Darmono, 1995). Akibat dari keracunan akut antara lain adalah mual, muntah-muntah, diare, kerusakan ginjal, bahkan dapat mengakibatkan kematian. Keracunan kronis ditandai oleh peradangan mulut dan gusi, pembengkakan kelenjar ludah dan pengeluaran ludah secara berlebihan, gigi menjadi longgar dan kerusakan pada ginjal. Kadar maksimum merkuri untuk keperluan air baku air minum kurang dari 0,001 mg/l dan untuk kegiatan perikanan yang diperbolehkan kurang dari 0,002 mg/l (Peraturan Pemerintah No. 82 tahun 2001).
dalam organ tersebut terdapat protein yang terdiri dari asam amino sistein (Fardiaz, 1992).
Logam berat Hg berbahaya karena bersifat biomagnifikasi sehingga dapat terakumulasi dalam jaringan tubuh organisme melalui rantai makanan. Organisme yang berada pada rantai yang paling tinggi (top carnivora) memiliki kadar merkuri yang lebih tinggi dibanding organisme di bawahnya. Logam berat dalam jumlah berlebihan dapat bersifat racun. Hal ini disebabkan karena terbentuknya senyawa merkaptida antara logam berat dengan gugus –SH yang terdapat dalam enzim. Akibatnya aktifitas enzim tidak berlangsung. Toksisitas merkuri terhadap organisme perairan tergantung pada jenis, kadar efek sinergis-antagonis dan bentuk fisika kimianya (Hutagalung, 1989).
Merkuri yang paling toksik adalah bentuk alkil merkuri yaitu metil dan etil merkuri yang paling banyak digunakan untuk mencegah timbulnya jamur. Alkil merkuri, terakumulasi dalam hati dan ginjal yang dikeluarkan melalui cairan empedu.
2. Timbal (Pb)
Timbal atau timah hitam adalah sejenis logam lunak berwarna cokelat dengan nomor atom 82, berat atom 207,19, titik cair 327,5º C, titik didih 1725º C, dan berat jenis 11,4 gr/ml (Reilly, 1991). Logam ini mudah dimurnikan sehingga banyak digunakan oleh manusia pada berbagai kegiatan misalnya pertambangan, industri dan rumah tangga. Pada pertambangan timbal berbentuk senyawa sulfida (PbS)
Timbal (Pb) secara alami banyak ditemukan dan tersebar luas pada bebatuan dan lapisan kerak bumi. Di perairan logam Pb ditemukan dalam bentuk Pb2+, PbOH+, PbHCO
3, PbSO4 dan PbCO+ (Perkins, 1977 in Rohilan,
1992). Pb2+ di perairan bersifat stabil dan lebih mendominasi dibandingkan dengan Pb4+ (GESAMP, 1985). Masuknya logam Pb ke dalam perairan melalui proses pengendapan yang berasal dari aktivitas di darat seperti industri, rumah tangga dan erosi, jatuhan partikel-partikel dari sisa proses pemb akaran yang mengandung tetraetil Pb, air buangan dari pertambangan bijih timah hitam dan buangan sisa industri baterai (Palar, 1994).
disertai dengan diare. Sedangkan gejala kronis umumnya ditandai dengan mual, anemia, sakit di sekitar mulut, dan dapat menyebabkan kelumpuhan (Darmono, 2001). Fardiaz (1 992) menambahkan bahwa daya racun dari logam ini disebabkan terjadi penghambatan proses kerja enzim oleh ion-ion Pb2+. Penghambatan tersebut menyebabkan terganggunya pembentukan hemoglobin darah. Hal ini disebabkan adanya bentuk ikatan yang kuat (ikatan kovalen) antara ion-ion Pb2+ dengan gugus sulphur di dalam asam-asam amino. Untuk menjaga keamanan dari keracunan logam ini, batas maksimum timbal dalam makanan laut yang ditetapkan oleh Departemen Kesehatan RI dan FAO adalah sebesar 2,0 ppm. Pada organisme air kadar maksimum Pb yang aman dalam air adalah sebesar 50 ppb (EPA, 1973 in Hutagalung 1984).
3. Khrom (Cr)
Logam kromium bernomor atom 24, berat atom 51,996, titik cair 1875oC, titik didih 2665oC, dan massa jenis 7,19 gr/ml (Reilly, 1991). Kromium merupakan logam yang keras, tahan panas, elektropositif, dan merupakan penghantar panas yang baik. Di alam unsur ini tidak ada dalam bentuk logam murni. Sumber alami kromium sangat sedikit, yaitu batuan chromite (FeCr2O4)
dan chromic oxide (Cr2O3) (Novotny dan Olem, 1994). Di perairan alami
kromium jarang ditemukan dan biasanya dalam bentuk kromium trivalent (Cr3+)
dan kromium hexavalent (Cr6+). Sumber Cr6+ berasal dari industri pelapisan logam dan produksi pigmen. Cr3+ banyak terdapat dalam limbah industri pencelupan tekstil, keramik gelas, dan dari kegiatan penyamakan kulit. Organisme akuatik dapat terpapar oleh Cr melalui media itu sendiri, sedimen maupun makanan (Effendi, 2003).
Toksisitas unsur Cr terhadap organisme perairan tergantung pada bentuk kromium, bilangan oksidasinya, dan pH (Hutagalung, 1991). Penurunan pH dan kenaikan suhu dapat meningkatkan toksisistas Cr6+ terhadap organisme air. Toksisitas Cr6+ lebih besar daripada toksisitas Cr3+. Cr6+ yang larut di dalam air
bagi kehidupan akuatik adalah sekitar 0,05 mg/l (Moore, 1991 in Effendi, 2003). Kadar kromium 0,1 mg/l dianggap berbahaya bagi kehidupan organisme laut (Effendi, 2003). Kadar maksimum kromium untuk keperluan air baku air minum dan kegiatan perikanan menurut Peraturan Pemerintah No. 82 tahun 2001 adalah sebesar 0,05 mg/l.
C. Pencemaran Logam Berat
Menurut keputusan Menteri Negara Kependudukan dan Lingkungan Hidup No.02/MENKLH/I/1988 yang dimaksud dengan polusi atau pencemaran air dan udara adalah masuk dan dimasukannya mahluk hidup, zat, energi dan atau komponen lain ke dalam air/udara dan atau berubahnya tatanan (komposisi) air/udara oleh kegiatan manusia atau proses alam, sehingga kualitas air/udara turun sampai ke tingkat tertentu yang menyebabkan air/udara menjadi kurang atau tidak berfungsi lagi sesuai dengan peruntukannya.
Bahan pencemar (polutan) adalah material atau energi yang dibuang ke lingkungan yang mengakibatkan kerusakan lingkungan baik abiotik maupun biotik (Quano, 1993). Berdasarkan sumber, pencemaran dapat dibagi menjadi dua kelompok (Soegiharto, 1976), yakni :
a. Dari laut, misalnya tumpahan minyak baik dari sumbernya langsung maupun hasil pembuangan kegiatan pertambangan di laut, sampah dan air ballast dari kapal tanker.
b. Kegiatan darat melalui udara dan terbawa oleh arus sungai yang akhirnya bermuara ke laut.
Berdasarkan sifatnya pollutan dibagi menjadi zat yang mudah terurai (biodegradable). Contoh zat yang mudah terurai adalah seperti sampah organik sedangkan zat yang sukar terurai (non biodegradable) contohnya adalah minyak dan logam berat (Odum, 1971).
Menurut Bryan (1976) secara alamiah logam berat juga masuk ke dalam perairan dapat digolongkan sebagai: (1) pasokan dan daerah pantai, yang meliputi masukan dari sungai-sungai dan erosi yang disebabkan oleh gerakan gelombang dan gletser, (2) pasokan dari laut dalam, yang meliputi logam-logam yang dilepaskan gunung berapi di laut dalam dan dari partikel atau endapan oleh adanya proses kimiawi, (3) pasokan yang rnelampaui lingkungan dekat pantai yang meliputi logam yang diangkut ke dalam atmosfer sebagai partikel-partikel debu atau sebagai aerosol dan juga bahan yang dihasilkan oleh erosi gletser di daerah kutub dan diangkut oleh es-es yang mengambang.
Logam berat termasuk sebagai zat pencemar karena sifatnya yang tidak dapat diuraikan secara biologis dan stabil, sehingga dapat tersebar jauh dari tempatnya semula (Dewi, 1996). Selanjutnya dikatakan bahwa ada dua hal yang menyebabkan logam berat digolongkan sebagai pencemar yang berbahaya, yaitu (1) tidak dihancurkan oleh mikroorganisme yang hidup di lingkungan dan (2) terakumulasi dalam komponen-komponen lingkungan, terutama air dengan membentuk senyawa kompleks bersama bahan organik dan anorganik secara adsorpsi dan kombinasi.
1. Logam berat dalam perairan
Banyak logam berat yang bersifat toksik maupun esensial terlarut dalam air dan mencemari air tawar maupun air laut. Sumber pencemaran ini banyak berasal dari pertambangan, peleburan logam dan jenis industri lainnya, dan juga dapat berasal dari lahan pertanian yang menggunakan pupuk atau anti hama yang mengandung logam (Darmono, 2001). Pencemaran logam berat dapat
dapat menjadikan terputusnya satu mata rantai kehidupan. Pada tingkat lanjutan, keadaan tersebut tentu saja dapat menghancurkan satu tatanan ekosistem perairan ( Palar, 1994).
Secara alamiah, unsur logam berat terdapat di seluruh alam, namun dalam kadar yang sangat rendah (Hutagalung,1984). Kadar logam dapat meningkat bila limbah perkotaan, pertambangan, pertanian dan perindustrian yang banyak mengandung logam berat masuk ke dalam perairan alami melalui saluran pembuangan. Logam berat yang sangat beracun ini tahan lama dan sangat banyak terdapat di lingkungan. Logam berat tersebut adalah raksa (Hg), timah hitam (Pb), Arsen (As), Kadmium (Cd), kromium (Cr) dan Nikel (Ni).
Tabel 1. Logam di dalam Hidrosfer
Logam Air Tawar (µµg/l) Air laut (µµg/l)
2. Logam berat dalam sedimen
Hutabarat dan Evans (1985), telah membagi sedimen berdasarkan ukuran diameter butiran, yaitu batuan (boulders), kerikil ( (gravel), pasir sangat kasar
(very coarse sand), pasir kasar (coarse sand), pasir halus (fine sand), pasir sangat halus (very fine sand), pasir (medium sand), lumpur (silt), liat (clay) dan bahan terlarut (dissolved material).
Bahan partikel yang tidak terlarut seperti pasir, lumpur, tanah dan bahan kimia anorganik dan organik menjadi bahan yang tersuspensi di dalam air, sehingga bahan tersebut menjadi penyebab pencemaran tertinggi dalam air. Keberadaan sedimen pada badan air mengakibatkan peningkatan kekeruhan perairan yang selanjutnya menghambat penetrasi cahaya yang dapat menghambat daya lihat (visibilitas) organisme air, sehingga mengurangi kemampuan ikan dan organisme air lainnya untuk memperoleh makanan, pakan ikan menjadi tertutup oleh lumpur. Kekeruhan yang tinggi dapat mengakibatkan terganggunya kerja organ pernapasan seperti insang pada organisme air dan akan mengakumulasi bahan beracun seperti pestisida dan senyawa logam. Pada sedimen terdapat hubungan antara ukuran partikel sedimen dengan kandungan bahan organik. Pada sedimen yang halus, presentase bahan organik lebih tinggi dari pada sedimen yang kasar. Hal ini berhubungan dengan kondisi lingkungan yang tenang, sehingga memungkinkan pengendapan sedimen lumpur yang diikuti oleh akumulasi bahan organik ke dasar perairan. Sedangkan pada sedimen yang kasar, kandungan bahan organiknya lebih rendah karena partikel yang lebih halus tidak mengendap. Demikian pula dengan bahan pencemar, kandungan bahan pencemar yang tinggi biasanya terdapat pada partikel sedimen yang halus. Hal ini diakibatkan adanya daya tarik elektrokimia antara partikel sedimen dengan partikel mineral (Boehm, 1987).
3. Logam berat dalam organisme air
III. METODE PENELITIAN
A. Tempat dan Waktu Penelitian
Penelitian ini dilakukan di Perairan Kamal Muara , Teluk Jakarta Propinsi Daerah Khusus Ibukota Jakarta, dari bulan September sampai dengan bulan Desember 2004. Kegiatan penelitian meliputi pengamatan di lapang dari bulan September sampai dengan bulan November 2004 dan analisa laboratorium dilaksanakan pada bulan Desember 2004. Kegiatan analisis contoh dilakukan di Laboratorium Proling dan Laboratorium Lingkungan Budidaya Perairan, Fakultas Perikanan dan Ilmu Kelautan, serta Laboratorium Terpadu, Fakultas Kedokteran Hewan, Institut Pertanian Bogor.
Pengambilan contoh air, sedimen serta kerang hijau (Perna viridis L.) dlakukan di tiga stasiun Perairan Kamal Muara, Kecamatan Penjaringan, Jakarta Utara. Stasiun-stasiun tersebut adalah stasiun I berada 1000 m (06º 05' 12.0" S dan 106º 43' 51.9" E) dari muara sungai, stasiun II berada 2000 m (06º 05' 01.9" S dan 106º 45' 10.2" E) dari muara sungai dan stasiun III berada pada jarak 3000 m (06º 04' 26.6" S dan 105º 45' 11.6" E) dari muara sungai (Gambar 3).
B. Bahan dan Alat
Bahan-bahan yang digunakan dalam penelitian ini adalah biota air berupa kerang hijau berukuran kecil (< 4 cm), sedang (4 - 6 cm) dan besar (> 6 cm) yang diambil dari setiap stasiun pengamatan, contoh air, sedimen, air destilasi, dan bahan kimia, baik untuk analisis logam berat, analisis kualitas air maupun untuk keperluan pengawetan.
Alat-alat yang digunakan dalam penelitian adalah botol Van Dorn, botol sampel, freezer, peralatan analisis kimia di laboratorium, pH meter, thermometer Hg, alat bedah dan AAS (Atomic Absorption Spectroscopy).
C. Prosedur Kerja
1. Contoh air dan sedimen
Pengambilan contoh air dilakukan dengan menggunakan perahu nelayan yang disesuaikan dengan stasiun pengamatan di lokasi budidaya kerang hijau. Contoh air diambil pada lapisan permukaan dengan menggunakan botol Van Dorn kemudian dimasukkan ke dalam botol polyetilen. Contoh air yang telah diambil dibagi dua botol yaitu botol pertama untuk analisa kekeruhan dan salinitas. Sedangkan botol kedua untuk logam berat yang ditambahkan dengan pengawet HNO3 pekat sebanyak 10 tetes hingga pH contoh air laut berada di
bawah 2.
Pada setiap stasiun pengamatan, selain dilakukan pengambilan contoh air, juga dilakukan pengambilan contoh sedimen. Pengambilan sedimen dilakukan dengan menggunakan Petersen Grab, sedimen yang diambil dibagian tengah dari sisi dinding grab untuk menghindari adanya kontaminasi logam dari penggunaan Petersen Grab. Sedimen dasar diambil sebanyak ± 200 gr dari tiap
stasiun. Kemudian sampel tersebut dimasukan ke dalam kantong plastik dan selanjutnya diukur kandungan logam berat (Hg, Pb dan Cr) dengan menggunakan AAS (Atomic Absorption Spectroscopy) .
2. Contoh kerang hijau
dimasukkan ke dalam kantong plastik untuk mencegah kontaminasi logam selama pengangkutan ke laboratorium dan dimasukkan kedalam ice box.
Kerang hijau dibagi atas tiga kelompok ukuran panjang yaitu, ukuran kecil (< 4 cm), sedang (4 – 6 cm) dan besar (> 6 cm). Penetapan ini berdasarkan pada ukuran kerang yang dikelompokkan di pasar. Pengambilan sampel biota air ini dilakukan untuk melihat kandungan logam berat. Untuk keperluan ini dibutuhkan kerang hijau sebanyak 25 gr daging kerang yang telah dibedah dan dibungkus dengan alumunium, kemudian dimasukkan kedalam freezer pada suhu -29 ºC sampai siap untuk dianalisa. Pengeringan pada suhu rendah bertujuan untuk menghindari penguapan logam berat dan menjaga daging kerang hijau dari kerusakan. Analisis kandungan logam Hg, Pb dan Cr dilakukan di laboratorium dengan menggunakan AAS.
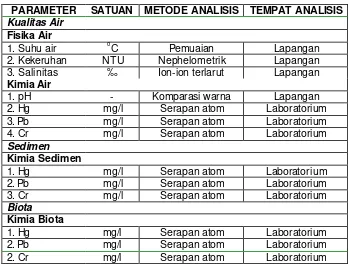
Untuk lebih jelasnya parameter-parameter kualitas air, sedimen dan biota yang diamati, alat yang digunakan dan tempat dilakukan analisis pada penelitian ini dapat dilihat pada Tabel 1.
Tabel 1. Parameter-parameter kualitas air, sedimen dan biota air yang diamati.
PARAMETER SATUAN METODE ANALISIS TEMPAT ANALISIS
Kualitas Air
Fisika Air
1. Suhu air o C Pemuaian Lapangan
2. Kekeruhan NTU Nephelometrik Lapangan
3. Salinitas ‰ Ion-ion terlarut Lapangan
Kimia Air
1. Hg mg/l Serapan atom Laboratorium
2. Pb mg/l Serapan atom Laboratorium
D. Analisis Data
1. Deskriptif
Penggambaran perubahan nilai parameter fisika-kimia dan kandungan logam berat di dalam perairan, di sedimen dan di dalam tubuh kerang hijau yang diperoleh selama pengamatan berlangsung.
2. Faktor bioakumulasi/biokosentrasi
Pendugaan kandungan logam berat dalam daging kerang hijau dengan kandungan logam berat di air, dilakukan dengan mencari Indeks Faktor Kosentrasi (FK) (Van Esch, 1977 in Prartono, 1985) :
Kadar logam berat daging kerang hijau (mg/l) Kadar logam berat dalam air laut (mg/l)
3. Principal Component Analysis (PCA)
Untuk melihat peranan faktor-faktor fisika dan kimia terhadap kandungan logam berat di dalam tubuh kerang hijau digunakan analisis komponen utama (PCA). Analisis komponen utama adalah suatu teknik ordinasi yang memproyeksikan dispersi matriks data multidimensional dalam suatu bidang datar dengan cara mereduksi ruang, maka diperoleh sumbu-sumbu baru yang mempresentasikan secara optimal sebagian besar variabilitas data matriks dimensional, sehingga dapat ditemukan hubungan antara variabel dan hubungan antar objek (Legandre dan Legandre, 1983). Analisis ini membagi matrik korelasi parameter menjadi beberapa komponen, kemudian menyusun keragaman komponen yang bersangkutan dari yang terbesar pada sumbu komponen utama sehingga didapatkan distribusi spasial parameter fisika dan kimia pada stasiun atau lokasi pengamatan.
Menurut Bengen (1998) data matriks (baris = stasiun, kolom = parameter) ditransformasikan dengan rumus,
(
)
∑
= − −= N
j ij ij
ij X X X X
a
1
2
Keterangan : aij = elemen matriks A (setelah sdistandarisasi)
Xij = elemen matriks X (sebelum distandarisasi)
X = rata – rata baris
i = stasiun pengamatan (1, 2 dan 3)
j = nilai parametr fisika-kimia dan kandungan logam berat di di dalam tubuh kerang hijau
IV. HASIL DAN PEMBAHASAN
A. Hasil
1. Parameter fisika dan kimia
a. Suhu
Nilai rata-rata suhu perairan (Gambar 4) di tiap stasiun menunjukkan kisaran antara 31,33 – 31,67 ºC, dengan suhu tertinggi 32 ºC dan terendah 31 ºC. Pengukuran suhu dilakukan mengingat pentingnya parameter ini dalam mempelajari proses-proses fisika, kimia dan biologi. Pada biota atau organisme yang hidup di suatu perairan, suhu mempengaruhi proses-proses metabolisme yang terjadi dalam tubuh kerang hijau. Peningkatan suhu dapat menyebabkan penurunan daya larut oksigen terlarut dan juga akan menaikkan daya racun bahan-bahan tertentu. Suhu air terutama di lapisan permukaan ditentukan oleh pemanasan matahari yang intesitasnya berubah terhadap waktu, oleh karena itu suhu air laut akan seirama dengan perubahan intensitas penyinaran matahari.
Gambar 4. Rata-rata suhu di Perairan Kamal Muara, Teluk Jakarta
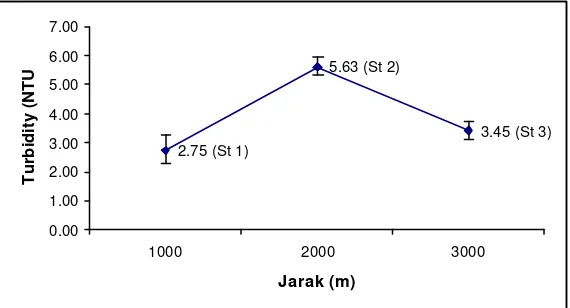
b. Kekeruhan
Nilai rata-rata kekeruhan (turbidity) pada Perairan Kamal Muara, Teluk Jakarta selama pengamatan berkisar antara 2,75 – 5,63 NTU. Nilai kekeruhan tertinggi terdapat pada stasiun 2 yaitu sebesar 5,99 NTU dan terendah pada stasiun 1 yaitu sebesar 2,2 NTU. Pada umumnya perairan laut mempunyai nilai kekeruhan yang rendah dibandingkan dengan perairan tawar (Effendi, 2003).
Kekeruhan menggambarkan sifat optis perairan dalam menyerap sinar matahari yang masuk kedalam perairan. Kekeruhan biasanya disebabkan oleh partikel tersuspensi, partikel koloid, fitoplankton.
Gambar 5. Rata-rata kekeruhan (turbidity) di Perairan Kamal Muara, Teluk Jakarta
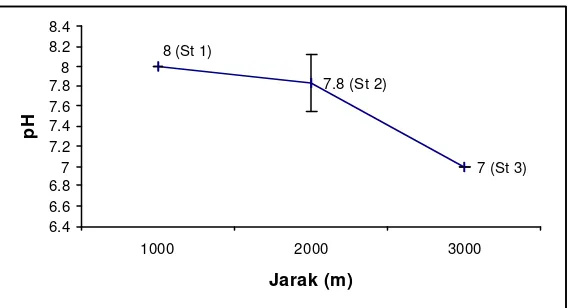
c. pH
Secara umum nilai derajat keasaman (pH) pada Perairan Kamal Muara, Teluk Jakarta di tiap stasiun selama pengamatan tidak berbeda secara signifikan. Hal ini disebabkan sifat dari air laut yang mempunyai sistem buffer atau penyangga, sehingga mampu mengendalikan sifat asam atau basa yang masuk ke dalam perairan. Kisaran nilai derajat keasaman yang diperoleh antara 7 – 8 . Nilai derajat keasaman (pH) ini masih berada pada kadar alamiah untuk perairan laut yaitu 7,0 – 8,0. Kondisi pH pada perairan dapat dijadikan sebagai indikator kualitas perairan. Batasan nilai pH telah ditentukan oleh kantor Kementerian Negara Kependudukan dan Lingkungan hidup No. 51 Tahun 2004 yakni 6,5 – 8.
3.45 (St 3) 5.63 (St 2)
2.75 (St 1)
0.00 1.00 2.00 3.00 4.00 5.00 6.00 7.00
1000 2000 3000
Jarak (m)
Gambar 6. Rata-rata derajat keasaman (pH) di Perairan Kamal Muara, Teluk Jakarta
d. Salinitas
3. Kandungan logam berat Hg, Pb dan Cr di air
Kandungan logam berat Hg, Pb dan Cr di kolom air selama pengamatan dapat di lihat pada Gambar 8 hingga Gambar 10
Gambar 8. Rata-rata kandungan logan berat Hg di kolom Perairan Kamal Muara, Teluk Jakarta
Selama pengamatan kandungan logam berat Hg di Perairan Kamal Muara, Teluk Jakarta mempunyai berkisar antara 0,00004 – 0,00021 mg/l. Rata-rata kandungan logam berat Hg di stasiun 1 sebesar 0,00009 mg/l, di stasiun 2 sebesar 0,000133 mg/l dan di stasiun 3 sebesar 0,000093 mg/l. Pada Gambar 8 terlihat adan ya peningkatan rata-rata kandungan logam berat dari stasiun 1 ke stasiun 2, kemudian mengalami penurunan di stasiun 3. Jika dibandingkan dengan baku mutu yang dikeluarkan oleh Kementerian Negara Lingkungan Hidup No. 51 tahun 2004 nilai ambang batas untuk logam berat Hg di perairan, khususnya untuk biota adalah 0,001 mg/l, maka kandungan logam berat Hg di Perairan Kamal Muara masih di bawah ambang batas.
0.000093 (St 3) 0.000133 (S t 2)
0.00009 (St 1)
0 0.00005 0.0001 0.00015 0.0002
1000 2000 3000
Jarak (m)
Gambar 9. Rata-rata kandungan logam ber at Pb di kolom Perairan Muara Kamal, Teluk Jakarta
Pada Gambar 9 terlihat bahwa kandungan nilai logam berat Pb di Perairan Kamal Muara, Teluk Jakarta berkisar antara 0,004 – 0,056 mg/l. Rata-rata kandungan logam berat Pb di stasiun 1 sebesar 0,006 mg/l, di stasiun 2 sebesar 0,035 mg/l dan di stasiun 3 sebesar 0,006 mg/l. Dari Gambar 8 rata-rata kandungan logam Pb menunjukkan pola yang mirip dengan kandungan logam berat Hg, yakni adanya peningkatan kandungan dari stasiun 1 menuju stasiun 2, kemudian mengalami penurunan pada stasiun 3. Jika dibandingkan dengan baku mutu yang dikeluarkan oleh Kementerian Negara Lingkungan Hidup No. 51 tahun 2004, nilai ambang batas untuk logam berat Pb di perairan, khususnya untuk biota laut adalah 0,008 mg/l. Kandungan Pb yang melampaui ambang batas yaitu pada stasiun 2 dengan nilai rata-rata 0,035 mg/l.
Pada penelitian ini didapatkan kandungan Logam berat Cr pada kolom Perairan Kamal Muara, Teluk Jakarta seperti yang tercantum pada Gambar 10 berkisar nilai antara ttd – 0,032 mg/l. Rata-rata kandungan logam berat Cr di stasiun 1 sebesar 0,011, di stasiun 2 sebesar 0,015 mg/l dan di stasiun 3 sebesar 0,018. Berbeda dengan logam berat Hg dan Pb, logam Cr mempunyai kecenderungan yang meningkat secara rata-rata dari stasiun 1 menuju stasiun 3. Jika dibandingkan dengan baku mutu yang dikeluarkan oleh Kementerian Negara Lingkungan Hidup No. 51 tahun 2004, nilai ambang batas untuk logam berat Cr di perairan, khususnya untuk biota laut adalah sebesar 0,005 mg/l, kandungan logam berat Cr di Perairan Kamal Muara, Teluk Jakarta ini secara umum telah melampaui nilai ambang batas baku mutu Kementerian Negara Lingkungan Hidup No. 51 tahun 2004.
3. Kandungan logam berat Hg, Pb, dan Cr di sedimen.
Kandungan logam berat Hg, Pb, dan Cr di sedimen selama pengamatan dapat dilihat pada Gambar 11 hingga Gambar 13 di bawah ini.
Gambar 11. Rata-rata kandungan logam berat Hg di sedimen Perairan Kamal Muara, Teluk Jakarta
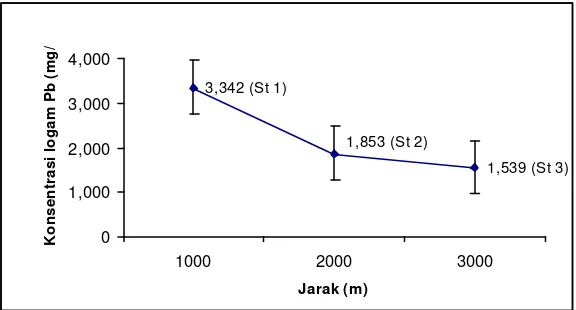
Gambar 12. Rata-rata kandungan logam berat Pb di sedimen Perairan Kamal Muara, Teluk Jakarta
Kandungan logam berat Pb di sedimen Perairan Kamal Muara, Teluk Jakarta mempunyai kisaran 0,101 – 5,555 mg/l. Rata-rata kandungan logam berat Pb di stasiun 1 sebesar 3,342 mg/l, di stasiun 2 sebesar 1,853 mg/l dan di stasiun 3 sebesar 1,539 mg/l. Dari data terlihat bahwa terdapat perbedaan
kecenderungan antara kandungan logam berat Pb dengan logam Pb, yaitu kecenderungan yang terus menurun dari stasiun 1 ke stasiun 3.
Gambar 13. Rata-rata kandungan logam berat Cr di sedimen Perairan Kamal Muara, Teluk Jakarta
4. Kandungan logam berat Hg, Pb dan Cr pada kerang hijau (Perna viridis
L.)
Hasil pengamatan nilai kandungan logam berat Hg, Pb dan Cr pada kerang hijau (Perna viridis L.) ukuran kecil, sedang dan besar selama pengamatan, yakni dari bulan September hingga November dapat dilihat pada Gambar 14 hingga Gambar 22.
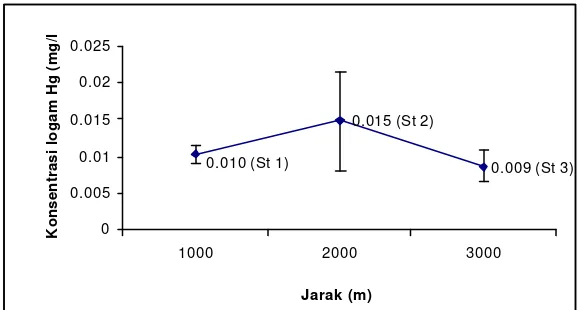
Kandungan logam berat Hg pada kerang hijau ukuran besar (Gambar 14) berkisar antara 0,0062 – 0.02 mg/l. Rata-rata kandungan logam berat Hg pada stasiun 1 sebesar 0,010 mg/l, stasiun 2 sebesar 0,015 dan pada stasiun 3 sebesar 0,009 mg/l. Ada kecenderungan peningkatan kandungan logam Hg dari stasiun 1 ke stasiun 2 dan terjadi penurunan kandungan logam Hg pada stasiun 3.
Gambar 14. Rata-rata kandungan logam berat Hg pada kerang hijau ukuran besar ( > 6 cm)
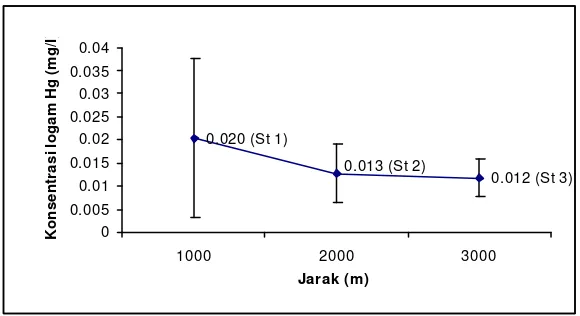
Kandungan logam berat Hg pada kerang hijau ukuran sedang (Gambar 15) berkisar antara 0,0070 – 0,04 mg/l. Rata-rata kandungan logam berat Hg pada stasiun 1 sebesar 0,020 mg/l, stasiun 2 sebesar 0,013 mg/l dan pada stasiun 3 sebesar 0,013 mg/l. Terlihat pada Gambar 15 di bawah ini ada kecenderungan penurunan kandungan logam Hg dari stasiun 1 hingga ke stasiun 3.
0.009 (St 3) 0.015 (St 2)
0.010 (St 1)
0 0.005 0.01 0.015 0.02 0.025
1000 2000 3000
Jarak (m)
Gambar 15. Rata-rata kandungan logam berat Hg pada kerang hijau ukuran sedang ( 4 – 6 cm)
Kandungan logam berat Hg pada kerang hijau ukuran kecil (Gambar 16) berkisar antara 0,0035 – 0,0078 mg/l. Rata-rata kandungan logam berat pada stasiun 1 sebesar 0,006 mg/l, stasiun 2 sebesar 0,005 mg/l dan pada stasiun 3 sebesar 0,007 mg/l. Berbeda dengan kedua ukuran kerang di atas, pada ukuran kerang kecil terlihat adanya kecenderungan peningkatan kandungan logam berat Hg dari stasiun 1 hingga ke stasiun 3, meski penurunan pada stasiun 2 relatif lebih kecil.
Gambar 16. Rata-rata kandungan logam berat Hg pada kerang hijau ukuran kecil (< 4 cm)
Kandungan logam berat Pb pada kerang hijau ukuran besar (Gambar 17) berkisar antara 40,407 – 47,813 mg/l. Rata-rata kandungan logam berat Pb pada stasiun 1 sebesar 45,019 mg/l, stasiun 2 sebesar 46,471 mg/l dan pada stasiun 3 sebesar 40,802 mg/l. Seperti pada logam Hg di atas, untuk kerang hijau ukuran besar pada logam Hg terlihat adanya tendensi peningkatan
kandungan logam berat Pb dari stasiun 1 hingga stasiun 2, dan selanjutnya terjadi penurunan kandungan Logam Pb yang cukup tajam pada stasiun 3.
Gambar 17. Rata-rata kandungan logam berat Pb pada kerang hijau ukuran besar ( > 6 cm)
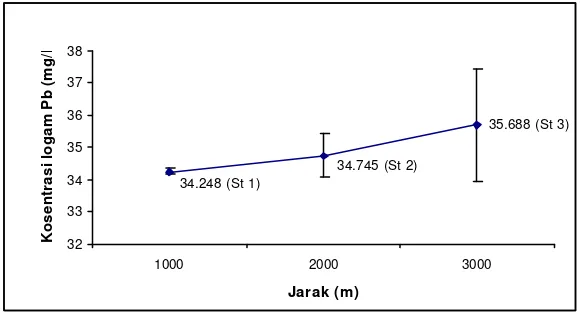
Kandungan logam berat Pb pada kerang hijau ukuran sedang (Gambar 18) berkisar antara 33,699 – 36,829 mg/l. Rata-rata kandungan logam berat pada stasiun 1 sebesar 34.248 mg/l, stasiun 2 sebesar 34,745 mg/l dan pada stasiun 3 sebesar 35, 688 mg/l. Berbeda dengan logam Hg di atas, untuk kerang hijau ukuran sedang pada logam Pb ini cenderung terjadi peningkatan kandungan logam berat Pb dari stasiun 1 hingga stasiun 3.
Gambar 18. Rata-rata kandungan logam berat Pb pada kerang hijau ukuran sedang ( 4 – 6 cm)
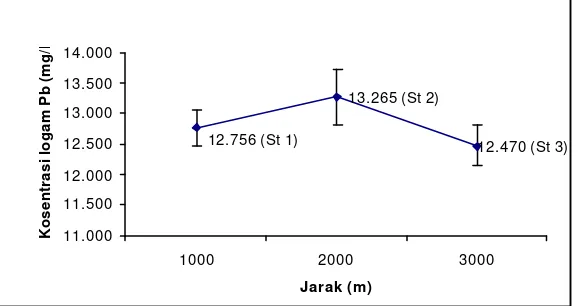
Kandungan logam berat Pb pada kerang hijau ukuran kecil (Gambar 19) berkisar antara 12,135 – 13,656 mg/l. Rata-rata kandungan logam berat pada stasiun 1 sebesar 12,756 mg/l, stasiun 2 sebesar 13,265 mg/l dan pada stasiun 3 sebesar 12,470 mg/l. Pada Gambar 19 di bawah ini pada kerang hijau ukuran
kecil terlihat adanya kecenderungan peningkatan kandungan logam berat Pb dari stasiun 1 hingga stasiun 2, namun terjadi penurunan kandungan logam berat Pb pada stasiun 3.
Gambar 19. Rata-rata kandungan logam berat Pb pada kerang kerang hijau ukuran kecil (< 4 cm)
Kandungan logam berat Cr pada kerang hijau ukuran besar (Gambar 20) berkisar antara 19,039 – 21,195 mg/l. Rata-rata kandungan logam berat Cr pada stasiun 1 sebesar 19,696 mg/l, stasiun 2 sebesar 20,710 mg/l dan pada stasiun 3 sebesar 20,998 mg/l. Berbeda dengan logam Hg dan logam Pb di atas, pada kerang hijau ukuran besar untuk kandungan logam Cr terlihat adanya cenderung terjadi peningkatan kandungan logam berat Cr dari stasiun 1 hingga ke stasiun 3.
Gambar 20. Rata-rata kandungan logam berat Cr pada kerang hijau ukuran besar (> 6 cm)
Kandungan logam berat Cr pada kerang hijau ukuran sedang (Gambar 21) berkisar antara 21,258 – 24,826 mg/l. Rata-rata kandungan logam berat Cr pada stasiun 1 sebesar 22,693 mg/l, stasiun 2 sebesar 23,946 mg/l dan pada stasiun 3 sebesar 21,692 mg/l. Berbeda dengan logam Hg dan logam Pb di atas, pada kerang hijau ukuran sedang, terlihat ada kecenderungan peningkatan kandungan logam berat Cr dari stasiun 1 hingga stasiun 2, namun selanjutnya terjadi penurunan kandungan logam berat Cr pada stasiun 3.
Gambar 21. Rata-rata kandungan logam berat Cr pada kerang hijau ukuran sedang ( 4 – 6 cm)
Kandungan logam berat Cr pada kerang hijau ukuran kecil (Gambar 22) berkisar antara 1,597 – 3,524 mg/l. Rata-rata kandungan logam berat Cr pada stasiun 1 sebesar 3,214 mg/l, stasiun 2 sebesar 3,033 mg/l dan pada stasiun 3 sebesar 1,691 mg/l. Pada Gambar 22 terlihat adanya pola penurunan kandungan logam berat Cr dari stasiun 1 hingga ke stasiun 3.
Gambar 22. Rata-rata kandungan logam berat Pb pada kerang hijau ukuran kecil (< 4 cm)
0
Faktor konsentrasi adalah suatu ukuran nilai dari kemampuan biota atau organisme air dalam mengambil bahan pencemar langsung dari lingkungan yang ada disekitarnya, yaitu kolom air. Faktor konsentrasi logam berat pada kerang hijau menunjukkan adanya kecenderungan biota air tersebut mengakumulasi logam berat. Adapun faktor konsentrasi yang diamati dari September hingga November 2004 ditunjukkan pada Gambar 23 hingga Gambar 25.
Ada tiga kategori yang dikemukakan Van Esch (1977) in Pratono (1985) untuk faktor konsentrasi yaitu, tingkat akumulasi rendah, jika faktor konsentrasi kurang dari 100. Tingkat akumulasi sedang, jika faktor konsentrasi antara 100 hingga 1000. Dan tingkat akumulasi tinggi, jika faktor konsentrasi lebih dari 1000.
Rata-rata faktor konsentrasi pada logam berat Hg (Gambar 23) tertinggi pada kerang hijau yang berukuran sedang (4 – 6 cm), dengan kisaran nilai 133,90 – 288,7. Hal ini menunjukkan bahwa kerang hijau yang berukuran sedang (4 – 6 cm) mempunyai tingkat akumulatif yang sedang terhadap logam berat Hg. Kerang hijau yang berukuran besar (> 6cm) juga mempunyai tingkat akumulatif yang sedang terhadap logam berat Hg dengan nilai kisaran rata-rata 97,66 – 210,01. Untuk kerang hijau yang berukuran kecil (< 4 cm) rata-rata nilai faktor konsentrasi kurang dari 100, yaitu berkisar antara 64,68 – 76,09. Hal ini menunjukkan kerang hijau yang berukuran kecil (< 4 cm) mempunyai tingkat akumulatif yang rendah terhadap logam berat Hg.
0
Faktor konsentrasi logam berat Pb (Gambar 24) cenderung fluktuatif dari stasiun pengamatan 1 hingga stasiun pengamatan 3, namun menurun pada stasiun pengamatan 1 ke stasiun pengamatan 2 dan meningkat dari stasiun pengamatan 2 ke stasiun pengamatan 3. Faktor konsentrasi pada kerang hijau ukuran besar (> 6 cm), rata-rata nilainya melebihi 1000, yaitu berkisar antara 2003,22 – 8396,23. Artinya pada kerang hijau berukuran besar (> 6 cm) mempunyai tingkat akumulasi yang tinggi terhadap logam berat Pb. Pada kerang hijau berukuran sedang (4 – 6 cm) rata-rata nilainya melebihi 1000, yaitu berkisar 1483,17 – 6404,36. Artinya pada kerang hijau ukuran sedang (4 – 6 cm) mempunyai tingkat akumulatif yang tinggi terhadap logam berat Pb. Pada kerang hijau berukuran kecil (> 4 cm), rata-rata nilai faktor konsentrasi berkisar antara 570,96 – 2396,76, dan mempunyai kecenderungan tingkat akumulatif yang tinggi terhadap logam berat Pb, meskipun pada stasiun 2 nilainya kurang dari 1000, yaitu 570,96.
Gambar 24. Rata-rata faktor logam berat Pb pada kerang hijau
0
cenderung tinggi pula terhadap logam berat Cr. Adapun rata-rata faktor konsentrasinya berkisar antara 559,14 – 1035,06.
Gambar 25. Rata-rata faktor logam berat Cr pada kerang hijau
6. Analisis hubungan fisika – kimia dengan kandungan logam berat pada kerang hijau (Perna viridis L.)
Menurut Darmono (2001) faktor-faktor lingkungan ikut mempengaruhi konsentrasi kandungan logam berat dalam tubuh kerang hijau, dalam hal ini konsentrasi kandungan logam berat pada tubuh kerang hijau tergantung pada konsentrasi kandungan logam pada kolom air, konsentrasi kandungan logam pada sedimen, konsentrasi garam, suhu dan pH air serta turbidity (kekeruhan). Untuk melihat pengaruh dari faktor-faktor tersebut digunakan Principal Component Analysis (PCA).
Tabel 3. Hasil analisis Principal Component Analysis (PCA) untuk logam Hg terhadap semua ukuran tubuh kerang hijau
Hasil analisis komponen utama (AKU) atau Principal Component Analysis
(PCA) logam Hg pada kerang hijau ukuran besar didapatkan nilai akar ciri (eigen value) pada sumbu utama (F1) sebesar 68,42 %, sumbu kedua (F2) sebesar 31,58 %. Pada sumbu utama (F1) dicirikan oleh variabel suhu, kekeruhan, konsentrasi logam Hg di air, konsentrasi logam Hg di sedimen dan konsentrasi logam Hg di kerang hijau dan untuk sumbu kedua dicirikan oleh variabel salinitas dan pH (Lampiran 9). Pada kerang hijau ukuran besar, parameter kekeruhan, Hg di air dan Hg di sedimen memberikan peranan positif terhadap kandungan logam berat di dalam tubuh kerang hijau (Lampiran 8). Sedangkan parameter suhu memberikan peranan yang negatif terhadap kandungan logam berat di dalam tubuh kerang hijau besar.
Hasil analisis PCA untuk kerang hijau berukuran sedang nilai akar ciri yang di peroleh dapat menjelaskan sumbu utama (F1) 56,27 % dan pada sumbu kedua (F2) sebesar 43,73 %. Variabel suhu, kekeruhan dan konsentrasi logam Hg di air mencirikan pada sumbu utama (F1), sedangkan pada sumbu kedua (F2) di cirikan variabel salinitas, pH, konsentrasi logam Hg di sedimen dan konsentrasi logam Hg pada kerang hijau (Lampiran 9). Dari matriks korelasi yang diperoleh menunjukkan adanya peranan negatif untuk parameter salinitas terhadap kandungan logam Hg di dalam tubuh kerang hijau ukuran sedang (Lampiran 8).
Tabel 4. Hasil analisis Principal Component Analysis (PCA) untuk logam Pb terhadap semua ukuran tubuh kerang hijau
Logam Pb F1 F2 Korelasi
Pada logam Pb dari hasil analisis PCA yang dilakukan untuk kerang hijau berukuran besar diperoleh nilai akar ciri (eigenvalue) sumbu utama (F1) dapat menjelaskan sebesar 55,92 %, sumbu kedua (F2) dapat menjelaskan sebesar 44,07 %. Pada sumbu utama dicirikan oleh variabel suhu, kekeruhan, konsentrasi Pb di air dan konsentrasi Pb di kerang hijau. Sumbu kedua dicirikan oleh variabel salinitas, pH dan konsentrasi Pb di sedimen (Lampiran 9). Matriks korelasi yang diperoleh terhadap kerang hijau ukuran besar memperlihatkan adanya peranan parameter pH terhadap kandungan dalam tubuh kerang hijau tersebut (Lampiran 8).
Hasil analisis PCA untuk kerang hijau berukuran sedang nilai akar ciri yang diperoleh dari analisis PCA dapat menjelaskan sebesar 52,51 % pada sumbu utama (F1) dan 47,49 % pada sumbu kedua (F2). Pada sumbu utama (F1) dicirikan oleh variabel salinitas, konsentrasi Pb di sedimen dan konsentrasi Pb di kerang hijau dan untuk sumbu kedua (F2) dicirikan oleh variabel suhu, kekeruhan, pH dan konsentrasi Pb di air (Lampiran 9). Terhadap kerang hijau ukuran sedang matriks korelasi yang didapat menunjukkan adanya peranan yang positif oleh parameter salinitas terhadap kandungan logam Pb di dalam tubuh kerang hijau tersebut. Sedangkan untuk parameter pH dan Pb di sedimen memberikan peranan yang negatif terhadap kandungan Pb dalam tubuh kerang hijau (Lampiran 8).
variabel suhu, kkeruhan, koinsentrasi Pb di air, konsentrasi Pb di sedimen dan konsentrasi Pb di kerang hijau dan pada sumbu kedua dicirikan oleh variabel salinitas dan pH (Lampiran 9). Pada kerang hijau ukuran kecil matriks korelasi yang diperoleh memperlihatkan adanya peranan yang positif oleh parameter kekeruhan dan Pb di air, sedangkan parameter suhu memberikan peranan yang negatif (Lampiran 8). Peranan dari parameter-parameter tersebut mempengaruhi kandungan Pb di dalam tubuh kerang hijau kecil.
Tabel 5. Hasil analisis Principal Component Analysis (PCA) untuk logam Cr terhadap semua ukuran tubuh kerang hijau
Logam Cr F1 F2 Korelasi positif Korelasi
Hasil analisis PCA pada logam Cr untuk kerang hijau berukuran besar nilai akar ciri yang di peroleh dapat menjelaskan sumbu utama (F1) sebesar 61,66 %, sumbu kedua (F2) dapa menjelaskan sebesar 38,34 %. Adapun variabel-variabel yang mencirikan sumbu utama (F1) antara lain salinitas, pH, konsentrasi Cr di air, konsentrasi Cr di sedimen dan konsentrasi Cr di kerang hijau. Sumbu kedua (F2) dicirikan oleh variabel suhu dan kekeruhan (Lampiran 9). Pada logam Cr, analisis matriks korelasi yang diperoleh menunjukkan peranan yang positif oleh parameter suhu dan Cr di air terhadap kandungan Cr di dalam tubuh kerang hijau ukuran besar (Lampiran 8).
parameter suhu memberikan peranan yang negatif terhadap kandungan Cr di dalam tubuh kerang hijau ukuran sedang (Lampiran 8).
Hasil analisis PCA. untuk kerang hijau berukuran kecil nilai akar ciri yang diperoleh dapat menjelaskan sumbu utama (F1) sebesar 63,46 % dan pada sumbu kedua sebesar 39,07 %. Variabel pH, konsentrasi Cr di air, konsentrasi Cr di sedimen dan konsentrasi Cr di kerang hijau terdapat pada sumbu utama (F1) dan variabel suhu, salinitas dan kekeruhan pada sumbu kedua (F2). Pada kerang hijau ukuran kecil, peranan positif ditunjukkan oleh parameter pH dan Cr di sedimen terhadap kandungan Cr di dalam tubuhnya dan peranan negatif ditunjukkan oleh logam Cr di air (Lampiran 8).
B. Pembahasan
Pada pengamatan parameter fisika dan kimia yaitu, suhu, kekeruhan, pH dan salinitas secara keseluruhan masih menunjukkan kondisi yang memungkinkan untuk kerang hijau melakukan proses-proses biologis dalam hidupnya, baik untuk pertumbuhan maupun untuk kebutuhan reproduksi. Suhu air selama pengamatan masih menunjukkan kisaran yang normal bagi perkembangan kerang hijau. Hal ini sesuai dengan persyaratan yang dikeluarkan oleh Direktorat Jenderal Perikanan (1985) yang mengatakan bahwa untuk keperluan budidaya kerang hijau disarankan agar suhu perairan ada dalam kisaran 26 – 32 ºC.
Kisaran salinitas pada Perairan Kamal Muara, Teluk Jakarta juga sesuai dengan persyaratan yang dikeluarkan oleh Direktorat Jenderal Perikanan (1985) yaitu dalam kisaran 27 – 35 ‰. Salinitas merupakan faktor yang penting bagi kerang hijau untuk melakukan adaptasi terhadap kondisi perairan, karena salinitas berhubungan langsung dengan proses osmoregulasi yang dilakukan biota yang ada di dalamnya, termasuk kerang hijau.
cenderung berfluktuatif. Hal ini diduga karena adanya pengaruh masukan dari sungai yang bermuara di Perairan Kamal Muara, Teluk Jakarta yang membawa limbah-limbah logam berat dan bergantung pada besar kecilnya konsentrasi logam – logam tersebut yang terbuang ke dalam sungai hingga mencapai Perairan Kamal Muara, Teluk Jakarta. Limbah logam berat ini diduga berasal dari limbah industri dan limbah rumah tangga. Jika dibandingkan dengan baku mutu untuk biota air yang dikeluarkan oleh Kementerian Negara Lingkungan Hidup No. 51 tahun 2004 kondisi kandungan logam berat di Perairan Kamal Muara, Teluk Jakarta untuk logam berat Pb dan Cr telah melampaui ambang batas. Untuk logam berat Pb nilai ambang batasnya adalah 0,008 mg/l dan untuk logam berat Cr nilai ambang batasnya adalah 0,005 mg/l. Berbeda dengan kandungan logam Pb, kandungan logam berat Hg nilainya masih di bawah ambang batas yaitu 0,001 mg/l. Namun demikian konsentrasi yang rendah ini tetap harus diwaspadai karena logam-logam berat yang terlarut dalam kolom perairan pada konsentrasi tertentu dapat berubah fungsi menjadi sumber racun bagi kehidupan perairan (Palar, 1994). Meskipun daya racun yang ditimbulkan oleh satu jenis logam berat terhadap semua biota perairan tidak sama, namun kehancuran dari suatu kelompok dapat menjadikan terputusnya satu mata rantai kehidupan
diendapkan (Lindquist et.al, 1984). Dari hasil pengamatan sedimen di lokasi penelitian jenis sedimen yang didapat berupa lumpur berpasir. Namun hingga saat ini belum ada baku mutu logam berat pada sedimen, sehingga hasil penelitian ini belum bisa dibandingkan dengan standar baku mutu.
Nilai kandungan berat (Hg, Pb dan Cr) yang ada pada kerang hijau lebih tinggi dibanding pada kolom air dan sedimen. Hal ini disebabkan kerang hijau mempunyai kemampuan untuk mengakumulasi logam berat di dalam tubuhnya. Sifat hidupnya yang sessil dan filter feeder, mengakibatkan kerang hijau dapat menyerap logam berat di kolom air dan sedimen melalui proses makan memakan. Hal ini terlihat dari nilai faktor konsentrasi yang telah disebutkan di atas, dalam hal ini kerang hijau mampu menyerap logam berat di kolom air hingga ratusan kali dan bahkan untuk logam berat Pb dan Cr menunjukkan nilai hingga ribuan kali, yang artinya mempunyai tingkat akumulatif yang tinggi terhadap kedua logam tersebut.
Kecenderungan kerang hijau untuk menyimpan atau mengakumulasi logam berat dapat berlangsung dalam jangka waktu yang lama yakni bisa berlangsung selama hidupnya. Hal ini juga dipengaruhi oleh proses fisiologis dalam tubuh kerang hijau itu sendiri. Dalam proses metabolisme tubuhnya akan mengolah atau mentransformasi setiap bahan racun (log am berat) yang masuk, sehingga akan mempengaruhi daya racun atau toksisitas bahan tersebut (logam berat). Logam berat yang telah mengalami bio-transformasi dan tidak dapat diekskresikan atau dikeluarkan oleh tubuh umumnya akan tersimpan dalam organ-organ t ertentu seperti hepatopankreas, ginjal dan gonad.