i
PENGARUH KECEPATAN AGITASI DAN LAMA REAKSI TERHADAP KARAKTERISTIK PRODUK BAHAN BAKU SPREADS HASIL INTERESTERIFIKASI ENZIMATIK MINYAK SAWIT MERAH
Oleh :
MOH TAUFIK F24063110
SKRIPSI
Sebagai salah satu syarat untuk memperoleh gelar
SARJANA TEKNOLOGI PERTANIAN
pada Departemen Ilmu dan Teknologi Pangan
Fakultas Teknologi Pertanian
Institut Pertanian Bogor
2010
FAKULTAS TEKNOLOGI PERTANIAN INSTITUT PERTANIAN BOGOR
ii
ABSTRACT
Moh Taufik. F24063110. Effects of Agitation Speed and Reaction Time on Characteristics of Enzymatic Interesterified Products from Red Palm Oil. Dibawah bimbingan Sugiyono dan Soenar Soekopitojo. 2010.
A blend of red palm olein (RPO)/red palm stearin (RPS) and coconut oil (CNO) (82.5:17.7, wt%) was modified by enzymatic interesterification using immobilized lipase from Candida antartica (Novozyme 435) to produce spreads base. Enzymatic interesterification was carried out at 60 and 10% enzyme of the total weight of substrates. The aim of this research was to study the effects of agitation speed and reaction time on characteristics of enzymatic interesterified products. The effects of agitation speed were studied in two different agitation speeds (100 and 200 rpm). The effects of the reaction time were studied in six different reaction times (1, 2, 4, 8, 16 and 24 hours). Comparison of characteristics were carried out between initial mixtures and enzymatic interesterified products by monitoring their carotene contents, slip melting points (SMP), solid fat contents (SFC), moisture contents and free fatty acids (FFA). Results of this study showed that agitation speed and reaction time had effects on characteristics of enzymatic interesterified products. The increasing of agitation speed decreased carotene content and increased SFC and FFA. The increasing of reaction time decreased carotene content and increased SMP, SFC, moisture content and FFA. The carotene contents of enzymatic interesterified products were 149.62-210.05 ppm and the carotene retentions were 70.51-97.79%. The SMP values of enzymatic interesterified products were 30.1‐35.9 , the moisture contents were 0.104-0.143% and the FFA contents were 1.38-4.54%.
iii RINGKASAN
Moh Taufik. F24063110. Pengaruh Kecepatan Agitasi dan Lama Reaksi terhadap Karakteristik Bahan Baku Spreads Hasil Interesterifikasi Enzimatik Minyak Sawit Merah. Dibawah Bimbingan Sugiyono dan Soenar Soekopitojo. 2010.
Minyak sawit memiliki kandungan β-karoten tinggi yang dapat dijadikan sebagai bahan baku berbagai produk olahan. Kandungan -karoten tersebut banyak hilang selama proses pengolahan minyak sawit. Salah satu produk minyak sawit yang tetap mempertahankan kandungan -karoten adalah minyak sawit merah. Minyak sawit merah dapat dijadikan sebagai bahan baku spreads. Untuk memperbaiki sifat fisik produk bahan baku spreads dari minyak sawit merah, diperlukan pencampuran dengan minyak kelapa yang mempunyai asam lemak jenuh berantai sedang dan pendek melalui reaksi interesterifikasi enzimatik. Reaksi interesterifikasi enzimatik dipengaruhi beberapa faktor diantaranya kecepatan agitasi dan lama reaksi. Untuk melihat pengaruh kecepatan agitasi dan lama reaksi terhadap karakteristik bahan baku spreads hasil interesterifikasi enzimatik maka dilakukan penelitian ini.
Reaksi interesterifikasi enzimatik pada penelitian ini menggunakan enzim lipase dari Candida antartica (Novozyme 435) sebanyak 10% b/b dan suhu reaksi 60 . Pengaruh kecepatan agitasi dipelajari pada dua kecepatan agitasi yang berbeda, yaitu 100 dan 200 rpm. Pengaruh lama reaksi dipelajari pada enam lama reaksi yang berbeda, yaitu 1, 2, 4, 8, 16, dan 24 jam. Analisis yang dilakukan adalah analisis total karoten, slip melting point (SMP), solid fat content (SFC), kadar air, dan asam lemak bebas (ALB)
Hasil penelitian menunjukkan bahwa kecepatan agitasi berpengaruh terhadap karakteristik bahan baku spreads yang dihasilkan. Semakin tinggi kecepatan agitasi, total karoten menjadi semakin rendah, sedangkan SFC dan ALB menjadi semakin tinggi. Hasil penelitian juga menunjukkan bahwa lama reaksi berpengaruh terhadap karakteristik bahan baku spreads yang dihasilkan. Semakin lama reaksi, total karoten menjadi semakin rendah, sedangkan SMP, SFC, kadar air, dan ALB menjadi semakin tinggi. Total karoten setelah interesterifikasi enzimatik berkisar antara 149.62-210.05 ppm dan nilai retensi karotennya berkisar antara 70.51-97.79%. Jika diasumsikan bahan baku spreads
hasil interesterifikasi enzimatik yang digunakan untuk memproduksi spreads
iv Judul Skripsi : Pengaruh Kecepatan Agitasi dan Lama Reaksi terhadap
Karakteristik Bahan Baku Spreads Hasil Interesterifikasi Enzimatik Minyak Sawit Merah
Nama : Moh Taufik
NRP : F24063110
Menyetujui:
Mengetahui:
Ketua Departemen Ilmu dan Teknologi Pangan,
(Dr. Ir. Dahrul Syah) NIP: 19650814 199022 1 001
Tanggal Lulus :
Pembimbing I,
(Dr. Ir. Sugiyono, M.App.Sc.) NIP. 19650729 199002 1 002
Pembimbing II,
v
RIWAYAT HIDUP
Penulis dilahirkan di Sumenep pada tanggal 10 Mei 1987. Penulis adalah anak keempat dari empat
bersaudara, pasangan Maski dan Alwani (alm). Penulis
menyelesaikan pendidikan dasar pada tahun 2000 di SDN
Pinggirpapas 1, kemudian melanjutkan pendidikan
menengah pertama di SMPN 5 Sumenep, hingga tahun
2003. Penulis menamatkan pendidikan menengah atas di
SMA Negeri 1 Sumenep pada tahun 2006. Penulis
melanjutkan pendidikan tinggi di Institut Pertanian Bogor (IPB) pada Departemen
Ilmu dan Teknologi Pangan, Fakultas Teknologi Pertanian melalui jalur USMI
(Undangan Seleksi Masuk IPB) pada tahun 2006.
Selama menjalani pendidikan di IPB, penulis aktif dalam berbagai
organisasi kemahasiswaan, diantaranya menjadi pengurus IKMT (Ikatan Keluarga
Muslim TPB) IPB tahun 2006-2007, GASISMA (Keluarga Mahasiswa Madura)
IPB tahun 2006-2009, FBI FATETA (Forum Bina Islam Fakultas Teknologi
Pertanian) IPB tahun 2007-2008, dan BEM FATETA (Badan Eksekutif
Mahasiswa Fakultas Teknologi Pertanian) IPB tahun 2007-2008, selain itu penulis
juga aktif sebagai tentor di bimbingan belajar NURUL ILMI Bogor dan
PRIMAGAMA Dramaga, Ciomas, dan Bojong Gede. Beberapa prestasi yang
diraih penulis selama pendidikan di IPB adalah penerima beasiswa PEMDA
(Pemerintah Daerah) Sumenep 2006-2008, beasiswa POM (Perkumpulan Orang
Tua Mahasiswa) IPB 2006-2007, dan beasiswa KSE (Karya Salemba Empat) IPB
tahun 2008-2010. Sebagai tugas akhir, penulis melakukan penelitian dengan judul
“Pengaruh Kecepatan Agitasi dan Lama Reaksi terhadap Karakteristik Bahan
vi
KATA PENGANTAR
Puji dan syukur penulis panjatkan kehadirat Allah SWT yang telah
melimpahkan rahmat dan karunia-Nya sehingga penulis dapat menyelesaikan
skripsi ini. Skripsi ini disusun sebagai salah satu syarat untuk memperoleh gelar
Sarjana Teknologi Pertanian pada Departemen Ilmu dan Teknologi Pangan,
Fakultas Teknologi Pertanian, Institut Pertanian Bogor.
Penulisan skripsi yang berjudul “Pengaruh Kecepatan Agitasi dan Lama
Reaksi terhadap Karakteristik Bahan Baku Spreads Hasil Interesterifikasi Enzimatik Minyak Sawit Merah” ini didasarkan pada penelitian yang telah
dilaksanakan sejak Oktober 2009 sampai Mei 2010 di Laboratorium SEAFAST
Center IPB dan Laboratorium Departemen Ilmu dan Teknologi Pangan IPB.
Penghargaan dan ucapan terima kasih penulis sampaikan kepada:
1. Ayahanda Maski dan Ibunda Alwani (alm) atas asuhan, didikan dan kasih
sayang, doa restu yang tulus, dorongan semangat dan motivasi agar ananda
selalu tabah dan tegar menghadapi segala kesulitan selama menempuh
pendidikan di IPB.
2. Dr.Ir.Sugiyono,M.App.Sc. selaku dosen pembimbing pertama atas waktu,
arahan, dan masukan yang diberikan kepada penulis.
3. Ir.Soenar Soekopitojo,M.Si. selaku dosen pembimbing kedua yang dengan
senang hati selalu menyempatkan diri mendengarkan masalah yang penulis
hadapi dan atas semua masukan, nasihat, dan arahan yang diberikan.
4. Dirjen Pendidikan Tinggi Kementerian Pendidikan Nasional yang telah
memberikan dukungan dana melalui Hibah Kompetitif Penelitian Unggulan
Strategi Nasional.
5. Ibu Waysima yang telah memberikan motivasi dan bantuan kepada penulis
selama pendidikan di Departemen Ilmu dan Teknologi Pangan.
6. Bapak/Ibu TPG Gossipin yang telah membantu penulis dalam
menyelesaikan pendidikan di Departemen Ilmu dan Teknologi Pangan.
7. Saudara-saudaraku Masriyani, Amlani dan Marwati (alm) yang telah
memberikan motivasi kepada penulis untuk menjadi manusia yang lebih
vii 8. Ponakan-ponakanku Masodi, Ria, Lisa dan Haidar yang telah memberikan
inspirasi kepada penulis untuk berusaha lebih keras lagi.
9. Kakak iparku Yudiyanto dan Mahad yang telah memberikan motivasi
kepada penulis untuk menjadi manusia yang lebih baik lagi.
10. Teman seperjuanganku Mario dan Pales atas kerjasama, kebersamaan dan
bantuan yang diberikan selama melakukan penelitian.
11. Sahabat-sahabat seperjuangan di kost Perwira 6 (Pak Yazid, Mas Yuli, Mas
Marno, Mba Banun sekeluarga, Mas Bubun, Syahrun, Adit, Pak Wagiman,
Pak Bambang, Pak Ibnu, Pak Prat, Pak Rahmat, Pak Hendra, Rendra, Ian,
Mas Erwin, Mas Yoni, Jay, Mas Reza, Mas Indra, Pak Mustafril dan Pak
Slamat) atas jalinan persaudaraan, motivasi dan kerjasama yang sangat baik
selama ini.
12. Teman-teman Gasisma (Sidiq, Ainol, Mail, Harun, Syamsul, Hendro,
Wahyu dll) atas jalinan persaudaraan dan kerjasamanya.
13. Seluruh teman ITP 43 atas jalinan persahabatan, kerjasama dan kebersamaan
selama menempuh pendidikan di ITP.
Akhirnya kepada semua pihak yang telah membantu dalam melaksanakan
pendidikan dan penelitian ini penulis menyampaikan terima kasih yang tidak
terhingga. Semoga Allah SWT memberikan balasan yang setimpal.
Bogor, Agustus 2010
viii
DAFTAR ISI
Halaman
HALAMAN JUDUL……….. i
ABSTRAK………. ii
RINGKASAN……… iii
HALAMAN PENGESAHAN……… iv
RIWAYAT HIDUP……… v
KATA PENGANTAR………... vi
DAFTAR ISI……...………...……….... viii
DAFTAR TABEL………...………... ix
DAFTAR GAMBAR…….……… xi
DAFTAR LAMPIRAN………….………. xii
I. PENDAHULUAN A. Latar Belakang………... 1
B. Tujuan Penelitian………... 2
C. Manfaat Penelitian………. 3
II. TINJAUAN PUSTAKA A. Minyak Kelapa Sawit….……… 4
B. Minyak Sawit Merah………... 6
C. Karotenoid………... 9
D. Minyak Kelapa………... 11
E. Reaksi Interesterifikasi……….. 14
F. Enzim Lipase….………. 16
G. Spreads………... 17
III.METODOLOGI PENELITIAN A. Bahan dan Alat………... 19
B. Metode Penelitian 1. Penelitian Tahap Pertama……….………...………. 19
2. Penelitian Tahap Kedua………... 20
3. Penelitian Tahap Ketiga……….………... 22
C. Metode Analisis………. 24
IV.HASIL DAN PEMBAHASAN A. Penelitian Tahap Pertama 1. Total Karoten………...……… 27
2. Slip Melting Point dan Solid Fat Content……… 29
3. Kadar Air dan Asam Lemak Bebas……….. 32
B. Penelitian Tahap Kedua 1. Total Karoten………...……… 34
2. Slip Melting Point dan Solid Fat Content……… 36
C. Penelitian Tahap Ketiga 1. Total Karoten………...………...………. 43
2. Slip Melting Point dan Solid Fat Content……… 46
3. Kadar Air dan Asam Lemak Bebas……….. 53
V. KESIMPULAN DAN SARAN A. Kesimpulan……… 56
B. Saran………... 57
ix
DAFTAR TABEL
Halaman
Tabel 1 Komposisi asam lemak minyak sawit kasar, olein, dan stearin.. 5
Tabel 2 Profil trigliserida dari minyak sawit kasar... 5
Tabel 3 Karakteristik RBD minyak sawit dan fraksi-faksinya……….... 6
Tabel 4 Karkteristik minyak sawit merah... 8
Tabel 5 Komposisi karotenoid pada minyak sawit kasar………. 11
Tabel 6 Komposisi asam lemak pada minyak kelapa... 13
Tabel 7 Komposisi trigliserida minyak kelapa………. 13
Tabel 8 Sifat fisik dan kimia minyak kelapa... 14
Tabel 9 Formulasi bahan baku…………... 22
Tabel 10 Perlakuan kecepatan agitasi dan lama reaksi... 23
Tabel 11 Total karoten bahan baku... 27
Tabel 12 Total karoten hasil penelitian Widarta (2008), Hasrini (2008), dan Riyadi (2009)……… 29
Tabel 13 Nilai SMP bahan baku... 29
Tabel 14 Nilai SMP dari bahan baku hasil penelitian Hasrini (2008)…… 30
Tabel 15 Profil SFC formula bahan baku... 31
Tabel 16 Profil SFC bahan baku hasil penelitian Hasrini (2008)………... 31
Tabel 17 Nilai kadar air dan asam lemak bebas bahan baku... 32
Tabel 18 Nilai kadar air dan ALB hasil penelitian Widarta (2008), Hasrini (2008), dan Riyadi (2009)……….………….. 33
Tabel 19 Perbandingan total karoten sebelum dan sesudah interesterifikasi enzimatik (IE)... 35
Tabel 20 Perbandingan total karoten sebelum dan sesudah interesterifikasi enzimatik (IE) hasil penelitian Hasrini (2008)………... 36
x
hasil penelitian Hasrini (2008)……… 38
Tabel 23 Total karoten rata-rata sebelum dan sesudah interesterifikasi
enzimatik (IE)……….. 44
Tabel 24 Nilai AKG sampel sebelum dan sesudah interesterifikasi
enzimatik (IE)……….. 46
Tabel 25 SMP rata-rata sebelum dan sesudah interesterifikasi enzimatik
(IE)………...……… 47
Tabel 26 Kadar air rata-rata sebelum dan sesudah interesterifikasi
enzimatik (IE)……….………...……… 53
Tabel 27 ALB rata-rata sebelum dan sesudah interesterifikasi enzimatik
xi
DAFTAR GAMBAR
Halaman
Gambar 1 Struktur kimia beberapa karoten... 10
Gambar 2 Prinsip reaksi asidolisis, alkoholisis, dan transesterifikasi
(Huyghebaert et al, 1994) ... 15 Gambar 3 Diagram proses fraksinasi (modifikasi Aini et al., 2005)... 20 Gambar 4 Prosedur interesterifikasi enzimatik (modifikasi Zhang et al.,
2001)... 21
Gambar 5 Prosedur interesterifikasi enzimatik (modifikasi Zhang et al.,
2001)... 22
Gambar 6 Profil SFC sebelum dan sesudah interesterifikasi enzimatik (IE)
yang dibandingkan dengan SFC margarin komersial A, margarin
komersial B, margarin komersial target (Fattahi-far et al., 2006), margarin ritel (Pandiangan, 2008), dan margarin industri
(Pandiangan, 2008).)...
41
Gambar 7 Profil SFC sebelum dan sesudah interesterifikasi enzimatik (IE)
hasil penelitian Hasrini (2008)……… 42
Gambar 8 Profil SFC sebelum dan sesudah interesterifikasi enzimatik (IE)
dari perlakuan kecepatan agitasi 100 rpm yang dibandingkan
dengan profil SFC margarin komersial A, margarin komersial B,
margarin komersial target (Fattahi-far et al., 2006), margarin ritel (Pandiangan, 2008), dan margarin industri (Pandiangan,
2008))... 50
Gambar 9 Profil SFC sebelum dan sesudah interesterifikasi enzimatik (IE)
dari perlakuan kecepatan agitasi 200 rpm yang dibandingkan
dengan profil SFC margarin komersial A, margarin komersial B,
margarin komersial target (Fattahi-far et al., 2006), margarin ritel (Pandiangan, 2008), dan margarin industri (Pandiangan,
xii
DAFTAR LAMPIRAN
Halaman
Lampiran 1 Karakteristik bahan baku untuk reaksi interesterifikasi
enzimatik... 64
Lampiran 2 Karakteristik hasil interesterifikasi enzimatik (IE) pada
penelitian tahap kedua... 67
Lampiran 3 Hasil ANOVA dengan uji lanjut Duncan pada karakter total
karoten dari penelitian tahap kedua... 69
Lampiran 4 Hasil ANOVA dengan uji lanjut Duncan pada karakter SMP
dari penelitian tahap kedua... 70
Lampiran 5 Karakteristik margarin komersial A dan margarin komersial B,
margarin komersial target (Fattahi-far et al., 2006), margarin retail (Pandiangan, 2008), dan margarin industri (Pandiangan,
2008)……… 71
Lampiran 6 Karakteristik hasil interesterifikasi enzimatik (IE) pada
penelitian tahap ketiga... 72
Lampiran 7 Hasil ANOVA dengan uji lanjut Duncan pada karakter total
karoten dari penelitian tahap ketiga... 79
Lampiran 8 Hasil ANOVA dengan uji lanjut Duncan pada karakter SMP
dari penelitian tahap ketiga... 81
Lampiran 9 Hasil ANOVA dengan uji lanjut Duncan pada karakter kadar
air dari penelitian tahap ketiga... 82
Lampiran 10 Hasil ANOVA dengan uji lanjut Duncan pada karakter ALB
1
I. PENDAHULUAN
A. Latar Belakang
Indonesia merupakan negara penghasil minyak sawit terbesar di dunia.
Produksi minyak sawit kasar Indonesia dari tahun ke tahun mengalami
peningkatan. Produksi minyak sawit kasar Indonesia sebesar 17.2 juta ton
pada tahun 2007, 19.2 juta ton pada tahun 2008, dan 20.5 juta ton pada tahun
2009. Pemerintah menargetkan produksi minyak sawit kasar sebesar 22 juta
ton pada tahun 2010 (Anonim, 2010).
Minyak sawit dapat dijadikan bahan baku berbagai produk olahan,
seperti minyak goreng, shortening, mayonnaise, dan salad dressing. Pada produk olahan minyak sawit tersebut, kandungan -karoten sudah banyak
hilang akibat proses produksi. Salah satu produk minyak sawit yang tetap
mempertahankan kandungan -karoten di dalamnya adalah minyak sawit
merah. Kandungan -karoten dalam minyak sawit kasar berkisar antara 500
sampai 700 ppm (Unnithan dan Foo, 2001). -karoten sebagai zat gizi mikro
dalam minyak sawit dapat diubah menjadi vitamin A dalam tubuh. Vitamin A
bermanfaat untuk reproduksi, mencegah kebutaan, pemeliharaan sel epitel,
meningkatkan daya tahan tubuh terhadap berbagai macam penyakit, dan
kesehatan kulit (Sianturi, 2002).
Dilihat dari sifat fisiknya, minyak sawit mempunyai stabilitas tinggi
terhadap oksidasi dan bersifat plastis pada suhu ruang, yaitu cenderung
mengandung trigliserida bertitik leleh tinggi (Lida et al., 2002). Sifat fisik dan kandungan karotenoid yang tinggi membuat minyak sawit dapat dijadikan
sebagai ingredient pangan. Salah satu potensi pemanfaatan minyak sawit merah adalah dijadikan sebagai bahan baku spreads. Spreads adalah produk berbentuk semi padat, plastis, mempunyai tekstur yang lembut, dan viskositas
yang cukup rendah, sehingga dapat dengan mudah dioleskan pada suatu
permukaan bahan lain seperti roti dan mampu menyebar (spreadable) (Kristanti, 1989).
2
content) minyak sawit tidak menghasilkan produk yang cepat meleleh di mulut. Sifat kristalisasi minyak sawit yang lambat menghasilkan struktur yang
agak rapuh, pembentukan granula kristal yang rapuh dapat dieleminasi dengan
menurunkan kandungan trigliserida simetri terutama palmitat-oleat-palmitat
(POP) melalui interesterifikasi dengan minyak lain yang mengandung asam
lemak berantai sedang dan pendek. Oleh sebab itu, untuk memperbaiki sifat
sifat leleh dan kristalisasi, minyak sawit dapat dicampur dan diinteresterifikasi
enzimatik dengan minyak kelapa yang mengandung asam lemak berantai
sedang dan pendek (Lida et al., 2002).
Reaksi interesterifikasi merupakan reaksi penyusunan kembali asam
lemak ke dalam molekul trigliserida. Reaksi interesterifikasi dapat dibagi
menjadi tiga jenis yaitu asidolisis, alkoholisis, dan transesterifikasi. Jenis
reaksi interesterifikasi pada penelitian ini adalah reaksi transesterifikasi.
Reaksi transesterifikasi merupakan reaksi pertukaran ester yang dapat terjadi
pada trigliserida yang berbeda atau diantara trigliserida itu sendiri.
Reaksi interesterifikasi enzimatik dipengaruhi oleh beberapa faktor
diantaranya kecepatan agitasi dan lama reaksi. Kecepatan agitasi dapat
memengaruhi hasil interesterifikasi karena kecepatan agitasi menentukan
kecepatan enzim bertemu dengan substrat. Lama reaksi juga memengaruhi
hasil interesterifikasi karena lama reaksi menentukan intensitas reaksi
interesterifikasi enzimatik. Untuk melihat pengaruh kecepatan agitasi dan
lama reaksi terhadap karakteristik bahan baku spreads yang dihasilkan maka dilakukan penelitian ini.
B. Tujuan
Tujuan penelitian ini adalah untuk mengetahui pengaruh kecepatan
3
C. Manfaat
Hasil penelitian ini diharapkan dapat memberikan informasi proses
4
I. TINJAUAN PUSTAKA
A. Minyak Kelapa Sawit
Pohon kelapa sawit dapat dibagi menjadi dua spesies yaitu pohon kelapa
sawit Afrika dan pohon kelapa sawit Amerika. Pohon kelapa sawit Afrika
(Elaeis guineensis) berasal dari Afrika Barat diantara Angola dan Gambia, sedangkan pohon kelapa sawit Amerika (Elaeis oleifera) berasal dari Amerika Tengah dan Amerika Selatan. Di Indonesia, kelapa sawit masuk pada
1848 yang berasal dari Afrika dan pertama kali ditanam di Kebun Raya Bogor
(Naibaho, 1998).
Minyak kelapa sawit dapat dibagi menjadi dua jenis yaitu minyak sawit
kasar (crude palm oil) yang berasal dari bagian mesokarp dan minyak inti sawit (palm kernel oil) yang berasal dari ekstraksi inti kelapa sawit (Somaatmadja, 1981). Minyak sawit kasar mempunyai pigmen yang berwarna
kuning merah, sedangkan minyak inti sawit mempunyai asam kaproat dan
asam kaprilat yang tidak dimiliki oleh minyak sawit kasar (Muchtadi, 1992).
Kadar minyak sawit kasar dan minyak inti sawit yang tertinggi diperoleh dari
buah sawit yang berumur 16 minggu (Muchtadi, 1992 dan Ketaren, 1986).
Minyak sawit kasar terdiri dari dua fraksi yaitu fraksi padat (stearin) dan
fraksi cair (olein). Olein mempunyai nilai ekonomis yang lebih tinggi
dibandingkan dengan stearin karena pada olein terdapat asam-asam lemak
esensial yang lebih tinggi. Selain itu olein lebih mudah difraksinasi dan diubah
menjadi produk pangan dan non pangan (Muchtadi, 1992). Komposisi asam
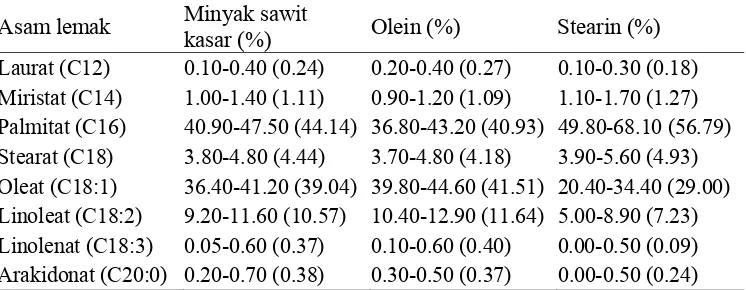
lemak dari minyak sawit kasar, olein, dan stearin dapat dilihat pada Tabel 1. Dari tabel tersebut terlihat asam palmitat merupakan asam lemak dominan
pada minyak sawit kasar dan stearin. Pada olein, asam lemak yang dominan
adalah asam oleat. Variasi struktur dan jumlah karbon dalam rantai asam
5
Tabel 1. Komposisi asam lemak minyak sawit kasar, olein, dan stearin. Asam lemak Minyak sawit
kasar (%) Olein (%) Stearin (%)
Laurat (C12) 0.10-0.40 (0.24) 0.20-0.40 (0.27) 0.10-0.30 (0.18) Miristat (C14) 1.00-1.40 (1.11) 0.90-1.20 (1.09) 1.10-1.70 (1.27) Palmitat (C16) 40.90-47.50 (44.14) 36.80-43.20 (40.93) 49.80-68.10 (56.79) Stearat (C18) 3.80-4.80 (4.44) 3.70-4.80 (4.18) 3.90-5.60 (4.93) Oleat (C18:1) 36.40-41.20 (39.04) 39.80-44.60 (41.51) 20.40-34.40 (29.00) Linoleat (C18:2) 9.20-11.60 (10.57) 10.40-12.90 (11.64) 5.00-8.90 (7.23) Linolenat (C18:3) 0.05-0.60 (0.37) 0.10-0.60 (0.40) 0.00-0.50 (0.09) Arakidonat (C20:0) 0.20-0.70 (0.38) 0.30-0.50 (0.37) 0.00-0.50 (0.24) Keterangan: Nilai dalam tanda kurung adalah nilai tengah
Sumber: Gee (2007)
Asam lemak dapat berikatan dengan gliserol membentuk gliserida.
Gliserida dapat berupa monogliserida, digliserida, dan trigliserida. Profil
trigliserida pada minyak sawit kasar dapat dilihat pada Tabel 2.
Tabel 2. Profil trigliserida dari minyak sawit kasar
Jenuh 1 ikatan
Keterangan: M= Asam miristat; P= Asam palmitat; S= Asam stearat; O= Asam oleat; L= Asam linoleat.
Sumber: Gee (2007)
6 dalam campuran yang diukur pada suhu tertentu. SFC berperan pada banyak
karakteristik produk seperti penampilan umum, kemudahan pengemasan, sifat
organoleptik, dan kemudahan penyebaran (spreading). SMP adalah suhu pada saat lemak dalam pipa kapiler yang berada dalam air menjadi cukup leleh
untuk naik dalam pipa kapiler. Karakteristik refined bleached deodorized
(RBD) minyak sawit yang diteliti oleh Gee (2007) dapat dilihat pada Tabel 3.
Tabel 3. Karakteristik RBD minyak sawit dan fraksi-faksinya Parameter Minyak kelapa
sawit Olein Stearin
Bilangan Iod 50.09-54.91 (52.07) 55.57-61.87 (56.75) 27.84-45.13 (37.74)
Slip melting point
( ) 33.00-39.00 (36.72) 19.20-23.60 (21.45) 46.60-53.80 (51.44) Indeks refraksi 1.45-1.45 (1.45) 1.45-1-1.45 (1.45) 1.44-1-1.45 (1.44)
Apparent density
(g/Ml) 0.88-0.89 (0.88) 0.89-0.89 (0.89) 0.88-0.88 (0.88)
Solid fat content
(%)pada
5 46.1-60.8 (53.7) 23.9-45.5 (38.3) 49.5-84.1 (76.0)
15 33.4-50.8 (39.1) 23.9-45.5 (38.3) 37.2-79.0 (68.9)
20 21.6-31.3 (26.1) 10.7-25.9 (19.9) 25.2-71.2 (60.2)
25 12.1-20.7 (16.3) 0.0-9.0 (5.7) 15.8-63.5 (50.6)
30 6.1-14.3 (10.5) 0.0-4.3 (2.1) 11.2-55.0 (40.4)
35 3.5-11.7 (7.9) 7.2-46.6 (34.3)
40 0.0-8.3 (4.6) 6.1-38.0 (28.1)
45 1.0-32.2 (22.4)
50 0.0-21.3 (12.5)
55 0.0-9.1 (0.6)
Keterangan: Nilai dalam tanda kurung adalah nilai tengah
B. Minyak Sawit Merah
Pengolahan (pemurnian) lebih lanjut terhadap minyak sawit kasar
diperlukan untuk menghasilkan minyak atau lemak yang bermutu tinggi sesuai
7 yaitu pemisahan gum (degumming), netralisasi, pemucatan (bleaching), dan deodorisasi (Allen, 1997).
Minyak sawit merah pada penelitian ini dihasilkan dari pemurnian
minyak sawit kasar melalui proses degumming, netralisasi, deodorisasi, dan fraksinasi. Proses bleaching tidak dilakukan karena bleaching earth (tanah pemucat) yang digunakan pada proses bleaching dapat menyerap karotenoid (Ariana et al. 1996).
Proses degumming bertujuan untuk memisahkan getah atau lendir-lendir yang terdiri dari fosfatida, protein, dan resin tanpa mengurangi asam lemak
bebas dalam minyak (Allen, 1997). Proses degumming cukup penting karena sabun yang terbentuk dari reaksi antara asam lemak bebas dengan soda
kaustik yang digunakan pada proses netralisasi dapat menyerap gum (getah
dan lendir) sehingga menghambat proses pemisahaan sabun (soap stock) dari minyak, dan netralisasi minyak yang masih mengandung lendir mengurangi
jumlah trigliserida yang dihasilkan karena terjadi penambahan partikel emulsi
dalam minyak (Djatmiko dan Ketaren, 1985).
Proses netralisasi dilakukan untuk menghilangkan asam lemak bebas
dalam minyak atau lemak dengan penambahan alkali sehingga terbentuk
sabun (soap stock). Sabun yang terbentuk dari proses netralisasi dapat menyerap kotoran-kotoran lain yang terdapat dalam minyak, sehingga minyak
yang dihasilkan lebih jernih dari “crude oil”-nya (Djatmiko dan Ketaren, 1985). Menurut Johnson (2002), netralisasi harus dilakukan dengan benar atau
beberapa trigliserida akan tersaponifikasi sehingga meningkatkan refining loss.
Proses deodorisasi dilakukan dengan tujuan menghilangkan bau dan rasa
yang tidak enak dalam minyak. Komponen-komponen yang dapat
menimbulkan bau dan rasa dari minyak antara lain aldehida, keton,
hidrokarbon dan minyak esensial yang jumlahnya sekitar 0.1 persen dari berat
minyak (Djatmiko dan Widjaja 1985).
Proses fraksinasi adalah proses pemisahan berbagai trigliserida menjadi
satu atau lebih fraksi dengan menggunakan perbedaan kelarutan trigliserida,
8 dilakukan dengan cara peningkatan suhu sampai 70oC dan penurunan suhu
secara perlahan-lahan hingga tercapai suhu kamar sambil diagitasi. Pada suhu
kamar terjadi kristalisasi fraksi stearin sehingga fraksi olein yang masih
bersifat cair dapat dipisahkan dengan penyaringan vakum (Weiss, 1983).
Minyak sawit kasar mengandung karotenoid sekitar 500-700 ppm (Gee,
2007). Menurut Choo et al. (1993), minyak sawit merah fraksi olein memiliki kandungan karotenoid sebesar 680-760 ppm dan minyak sawit merah fraksi
stearin memiliki kandungan karotenoid sebesar 380-540 ppm. Minyak sawit
merah tidak dianjurkan digunakan sebagai minyak goreng, karena karotenoid
yang terkandung di dalamnya dapat rusak pada suhu tinggi. Minyak sawit
merah biasanya digunakan dalam pembuatan minyak salad, serta dapat
digunakan sebagai bahan fortifikan makanan untuk produk pangan berbasis
minyak/lemak, seperti margarin, selai kacang, dan produk spreads lainnya (Andarwulan et al. 2003). Karakteristik minyak sawit merah dapat dilihat pada Tabel4.
Tabel 4. Karakteristik minyak sawit merah
Parameter Jumlah
Asam lemak bebas 0.04%
Bilangan peroksida 0.10 mekv/kg
Karoten 513 ppm
Tokoferol 707 ppm
Sumber: Choo et al.(1993)
Minyak sawit merah mengalami penurunan mutu selama penyimpanan.
Cahaya, oksigen, kelembaban, dan panas adalah faktor lingkungan yang dapat
berpengaruh buruk terhadap mutu minyak sawit selama pengolahan dan
penyimpanan. Cahaya dapat berperan sebagai pemicu awal terjadinya reaksi
yang menyebabkan kerusakan minyak (Leo, 1983). Oksigen menyebabkan
terbentuknya senyawa hidroperoksida, suatu komponen yang berperan dalam
ketengikan minyak (Osano dan Arowolo, 1990). Kelembaban berperan dalam
9 berperan dalam peningkatan laju reaksi oksidasi dan hidrolisis yang
menyebabkan penurunan mutu pada minyak (Jatmika et al., 1996). Penyimpanan minyak sawit merah pada ruangan gelap bersuhu sekitar 5
memiliki keunggulan dalam hal meminimumkan peningkatan kadar peroksida
dan meminimumkan penurunan kadar karoten. Kadar karoten minyak sawit
merah yang disimpan di ruang gelap, bersuhu rendah, dan ruang yang tidak
terkena sinar matahari langsung relatif tidak berubah (Jatmika dan Guritno,
1997).
C. Karotenoid
Karotenoid merupakan kelompok pigmen yang berwarna kuning, jingga,
merah, dan larut lemak. Menurut Meyer (1966), karotenoid dapat dibagi
menjadi empat golongan yaitu:
1. Karotenoid hidrokarbon (C40H56) seperti α, ß, -karoten, dan likopen.
2. Xantofil dan turunan karoten yang mengandung oksigen dan hidroksil
antara lain kriptosantin, C40H55(OH) dan lutein, C40H54(OH)2.
3. Asam karotenoid yang mengandung gugus karbonil.
4. Ester xantofil asam lemak, misalnya zeasantin.
Karotenoid terdiri dari ikatan hidrokarbon tidak jenuh yang terbentuk
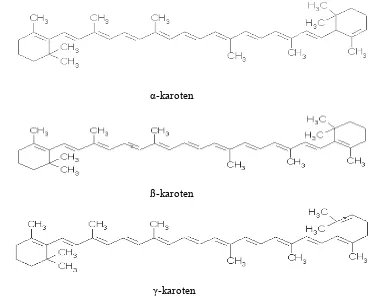
dari 40 atom C dan memiliki 2 buah gugus cincin. Struktur kimia beberapa
karotenoid dapat dilihat pada Gambar 1. Dari Gambar tersebut terlihat perbedaan stuktur antara α, ß, dan -karoten terletak pada letak dan jumlah
ikatan rangkap, serta jenis gugus pada cincin yang memengaruhi aktivitas
10
α-karoten
ß-karoten
-karoten
Gambar 1. Struktur kimia beberapa karoten (Anonim, 2006)
Selain α, ß, dan -karoten, di dalam minyak sawit kasar juga terdapat
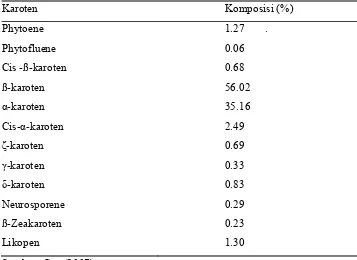
jenis karotenoid yang lain. Komposisi karotenoid dalam minyak sawit kasar
dapat dilihat pada Tabel 3. Dari tabel tersebut terlihat kandungan utama dalam konsentrat karoten adalah α dan -karoten. Kedua jenis karoten ini dapat
dibuat ke dalam berbagai konsentrasi, mulai dari 1 sampai 30% untuk aplikasi
komersial seperti produk pangan, pewarna pangan, nutrasetikal, farmasetikal,
11
Tabel 5. Komposisi karotenoid pada minyak sawit kasar
Karoten Komposisi (%)
Phytoene 1.27 .
Phytofluene 0.06
Cis -ß-karoten 0.68
ß-karoten 56.02
α-karoten 35.16
Cis-α-karoten 2.49
ζ-karoten 0.69
-karoten 0.33
δ-karoten 0.83
Neurosporene 0.29
ß-Zeakaroten 0.23
Likopen 1.30
Sumber: Gee (2007)
Menurut Meyer (1966), karotenoid larut dalam minyak, kloroform,
benzena, karbondisulfida, dan petroleum eter, tidak larut dalam air, methanol,
dan etanol dingin. Karotenoid sangat mudah teroksidasi karena adanya ikatan
ganda (Wafford, 1980). Selain itu, reaksi oksidasi dapat dipicu oleh suhu yang
relatif tinggi. Reaksi oksidasi dapat menyebabkan hilangnya warna karotenoid
dalam makanan (Schwartz dan Elbe, 1996).
Karotenoid lebih tahan tersimpan dalam lingkungan asam lemak tidak
jenuh jika dibandingkan dengan penyimpanan dalam asam lemak jenuh karena
asam lemak tidak jenuh lebih mudah menerima radikal bebas bila
dibandingkan dengan karotenoid. Dengan demikian oksidasi pertama kali
terjadi pada asam lemak dan karotenoid terlindungi dari oksidasi (Chichester
dan Feeters, 1970).
D. Minyak Kelapa
12 berdiri tegak dan tidak bercabang, dan dapat mencapai 10-14 meter lebih.
Daunnya berpelepah, panjangnya dapat mencapai 3-4 meter lebih dengan
sirip-sirip lidi yang menopang tiap helaian. Buahnya terbungkus dengan
serabut dan batok yang cukup kuat sehingga untuk memperoleh buah kelapa
harus dikuliti terlebih dahulu. Kelapa yang sudah besar dan subur dapat
menghasilkan 2-10 buah kelapa setiap tangkainya.
Minyak kelapa merupakan campuran ester dari gliserol dan asam lemak
yang disebut gliserida, larut dalam pelarut minyak atau lemak. Minyak kelapa
lebih tahan terhadap kerusakan oksidatif dibandingkan dengan jenis minyak
lain. Hal ini karena pada minyak kelapa mengandung asam lemak tidak jenuh
lebih sedikit (Canapi et al., 1996). Menurut Fennema (1985), berdasarkan kandungan asam lemaknya, minyak kelapa digolongkan ke dalam minyak
asam laurat (C-12) karena mengandung asam laurat dalam jumlah terbanyak
(40-50%), sedangkan asam lemak berantai C-6, C-8, dan C-10 dalam jumlah
sedang, dan jumlah asam lemak tidak jenuh yang rendah. Komposisi asam
13
Tabel 6. Komposisi asam lemak minyak kelapa
Jenis Asam lemak Jumlah (%)
Asam lemak jenuh
Asam kaproat (C6:0) 0.0- 0.8
Asam kaprilat (C8:0) 5.5-9.5
Asam kaprat (C10:0) 4.5-9.5
Asam laurat (C12:0) 44.0-52.0
Asam miristat (C14:0) 13.0-19.0
Asam palmitat (C16:0) 7.5-10.5
Asam stearat (C18:0) 1.0-3.0
Asam arakidat (C20:4) 0.0-0.4
Asam lemak tidak jenuh
Asam palmitoleat (C16:1) 0.0-1.3
Asam oleat (C18:1) 5.0-8.0
Asam linoleat (C18:2) 1.5-2.5
Sumber: Eckey (1954)
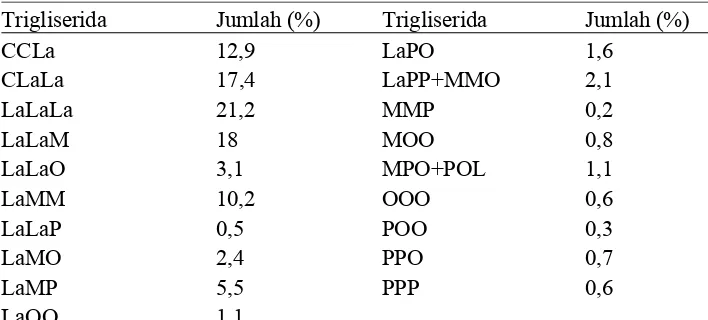
Trigliserida yang dominan pada minyak kelapa adalah trilaurin yaitu
sebesar 21.2%. Komposisi trigliserida pada minyak kelapa dapat dilihat pada
Tabel 7.
Tabel 7. Komposisi trigliserida minyak kelapa
Trigliserida Jumlah (%) Trigliserida Jumlah (%)
CCLa 12,9 LaPO 1,6
Keterangan: TAG: triasilgliserol; C: kaprat; La: laurat; M: miristat; P: palmitat; O: oleat; L: linoleat
14 Dalam minyak kelapa terdapat tokoferol sebesar 0.003%, senyawa
tokoferol tidak dapat disabunkan, dan berfungsi sebagai antioksidan (Ketaren,
1986). Menurut Eckey (1954), fungsi tokoferol sebagai antiokisidan adalah
dengan memperpanjang periode induksi atau periode jangka waktu mulai
terjadinya proses oksidasi sampai timbul bau tengik. Minyak kelapa berwujud
cair pada suhu ruang karena mempunyai titik cair dikisaran suhu ruang yaitu
24-27 ºC. Beberapa sifat fisik dan kimia dari minyak kelapa dapat dilihat di
Tabel 8..
Tabel 8. Sifat fisik dan kimia dari minyak kelapa
Sifat fisiko kimia Selang
Bilangan penyabunan (mg KOH/g CNO) 250-264
Bilangan Iod (g I2/100 g CNO) 7.5-10.5
Bilangan asam (mg NaOH/g CNO) 0.01
Bobot jenis (25 ) 0.919
Titik cair ) 24-27
Keterangan: CNO= coconut oil. Sumber: Swern (1979)
E. Reaksi Interesterifikasi
Reaksi interesterifikasi merupakan reaksi penyusunan kembali
asam-asam lemak ke dalam molekul trigliserida. Reaksi interesterifiksai tidak
mengubah sifat dan profil asam lemak tetapi mengubah profil lemak atau
minyak karena memiliki susunan trigliserida yang berbeda dari trigliserida
awalnya (Tombs, 1995).
Reaksi interesterifikasi melibatkan penggantian dan pendistribusian
ulang grup asil di dalam trigliserida. Menurut Swern (1979) proses
penggantian asam lemak itu sendiri meliputi tiga tipe reaksi yaitu:
1. Reaksi asidolisis, reaksi asidolisis adalah reaksi yang terjadi antara ester
dengan asam lemak. Reaksi ini merupakan cara yang efektif untuk
15 2. Reaksi alkoholisis, reaksi alkoholisis merupakan reaksi antara lemak dan
alkohol untuk menghasilkan ester. Jika alkohol yang digunakan adalah
gliserol maka disebut reaksi gliserolisis.
3. Reaksi pertukaran ester (transesterifikasi), pertukaran ester dapat terjadi
pada trigliserida yang berbeda atau diantara trigliserida itu sendiri.
Pertukaran ester dapat meningkatkan sifat fisik lemak (misalnya titik
leleh) karena terjadi perubahan susunan grup asil pada trigliserida tersebut.
Reaksi transesterifikasi dapat digunakan untuk produksi lemak seperti
margarin, mentega, dan shortening (Swern, 1979). Reaksi transesterifikasi dapat dilakukan secara enzimatik dengan menggunakan enzim. Reaksi
transesterifikasi enzimatik merupakan reaksi utama pada penelitian ini. Prinsip
reaksi asidolisis, alkoholisis, dan transesterifikasi dapat dilihat pada Gambar 2.
1. Asidolisis
2. Alkoholisis
3. Transesterifikasi
16
F. Enzim Lipase
Enzim lipase adalah jenis enzim hidrolase yang mengkatalisis sejumlah
reaksi meliputi hidrolisis, alkoholisis, esterifikasi, dan interesterifikasi
(Nurhasanah, 2008). Cara kerja enzim lipase berbeda-beda, tergantung dari
jenis mikroorganisme dan sumber penghasilnya. Spesifisitas kerjanya
tergantung pada posisi atau lokasi ester, asam lemak, dan asilgliserol (Macrae,
1983).
Lipase mikrobial dapat dibagi menjadi dua kelompok berdasarkan
spesifikasi kerjanya, yaitu lipase non-spesifik dan lipase spesifik sn-1,3 atau
sn-2. Dalam reaksi interesterifikasi, lipase non-spesifik menyusun kembali
asam-asam lemak dari ketiga posisi ikatan trigliserida. Lipase spesifik
menyusun kembali asam lemak pada ikatan sn-1,3 atau sn-2.
Enzim lipase yang digunakan pada penelitian kali ini adalah enzim
Lipozyme TL IM dan Novozyme 435. Lipozyme TL IM yang merupakan
salah satu jenis enzim lipase komersial terimobilisasi yang berasal dari
Thermomyces lanuginosa yang mempunyai kespesifitasan posisional molekul trigliserida yaitu pada posisi primer (sn-1,3). Lipozyme TL IM ini
terimobilisasi dalam bentuk metode penjebakan, yaitu enzim dijebak di dalam
matriks silika gel atau dibungkus di dalam membran semipermiabel dengan
erat sehingga enzim menjadi tidak bebas dalam menjalankan fungsi
katalitiknya di dalam kisi-kisi polimer tersebut (Hasrini, 2008). Aktivitas
enzim terimobilisasi lebih rendah dari enzim bebas karena enzim imobil
secara spesifik terbatas atau terlokalisasi dalam suatu area tertentu tetapi
masih mempertahankan aktivitas kinetiknya dan dapat digunakan secara
berulang dan kontinu (Chibata, 1978). Dibandingkan dengan enzim yang
masih dalam bentuk bebas, imobilisasi enzim Lipozyme TL IM memberikan
manfaat yaitu reusabilitas, penghentian yang lebih cepat dari reaksi, biaya
yang lebih rendah, pembentukan produk yang terkontol, dan produk lebih
mudah dipisahkan dari reaktannya.
Enzim Novozyme 435 merupakan enzim lipase komersial terimobilisasi
17 (termostabil). Novozyme 435 biasanya digunakan dalam reaksi esterase untuk
memproduksi ester-ester tertentu pada suhu proses yang rendah (60-70oC).
Enzim ini juga dapat digunakan untuk meresintesis lemak (trigliserida) dari
gliserol dan asam-asam lemak bebas. Suhu proses untuk Novozyme 435 yang
relatif rendah dapat mencegah pembentukan hasil sampingan sehingga dapat
menurunkan biaya purifikasi produk akhir (Novozyme, 2010). Menurut
Criado et al. (2007a), enzim Novozyme 435 mempunyai kadar air yang lebih rendah dari Lipozyme TL IM. Lipozyme TL IM mengandung kadar air sekitar
5% (Farmani et al., 2006), sedangkan Novozyme 435 mengandung kadar air sebesar 1-2% (Kapucu et al., 2003).
Aktivitas lipase dipengaruhi oleh kondisi lingkungan, diantaranya adalah
kadar air, pH, suhu, konsentrasi produk, dan kandungan lipase. Suhu optimum
untuk lipase imobil adalah antara 30-62oC, sedangkan pH optimum untuk
aktivitas lipase adalah antara 7-9. Kadar air optimum untuk lipase adalah
antara 0.04-11% (b/v), walaupun kebanyakan reaksi interesterifikasi
membutuhkan kadar air kurang dari 1% (Willis dan Marangoni, 2002).
G. Spreads
Spreads adalah produk olahan lemak untuk olesan yang memiliki kadar lemak 10-90%. Spreads dibagi menjadi dua kelompok, yaitu fat spreads
yang memiliki kadar lemak kurang dari 80%, dan margarin yang memiliki
kadar lemak lebih dari atau sama dengan 80% (Codex, 2007). Menurut
Kristanti (1989), spreads adalah produk berbentuk semi padat, plastik, mempunyai tekstur yang lembut dan viskositas yang cukup rendah sehingga
dapat dengan mudah dioles ke suatu pernukaan bahan makanan lain seperti
roti dan mampu menyebar.
Kristal-kristal lemak pada spreads membentuk jaringan tiga dimensi yang memberikan struktur semi padat pada produk dan menahan bagian cair
lemak. Struktur yang terintegritas ini terbentuk terutama karena adanya ikatan
kimia (ikatan primer) yang sangat kuat antara kristal-kristal lemak yang
berdekatan dan ikatan sekunder Van der Waals yang lemah di antara
18 tersebut tidak dapat dibangun kembali apabila putus akibat adanya kerja
mekanik, sedangkan ikatan sekunder bersifat reversibel (deMan, 1999).
Menurut Moran (1994), fungsi lemak spreads adalah meningkatkan palatabilitas produk roti dan kue seperti meminyaki (lubrication) roti ketika dimakan, sebagai sumber energi, vitamin, dan asam lemak esensial, serta
memberikan flavor pangan, berkontribusi pada rasa dingin ketika dimakan, dan membentuk struktur produk. Karakteristik produk spreads dilihat dari daya oles (spreadability), oiliness, dan sifat lelehnya (Chrysam, 1996) :
1. Daya oles (spreadability) adalah satu sifat paling penting pada spreads,
mungkin kedua setelah flavor.
2. Pengeluaran minyak (oiliness) pada margarin terjadi jika matriks kristal lemak berubah ukuran. Ini masalah serius untuk produk batangan, minyak
dapat bocor keluar dari kemasan.
3. Margarin meja berkualitas tinggi meleleh dengan cepat dengan sensasi
dingin pada langit-langit mulut. Komponen flavor dan garam pada fase mengandung air dengan cepat diterima oleh indra perasa, dan tidak
meninggalkan tekstur berlemak.
Spreads harus bersifat plastis sehingga mempunyai kemampuan untuk dioles pada suatu permukaan. Menurut Gaman dan Sherrington (1992),
plastisitas lemak disebabkan karena lemak merupakan campuran trigliserida
yang masing-masing mempunyai titik leleh sendiri-sendiri, hal ini berarti pada
suhu tertentu sebagian lemak mencair dan sebagian lagi dalam bentuk kristal
19
II. METODOLOGI PENELITIAN
A. Bahan dan Alat Penelitian
Bahan-bahan yang digunakan adalah minyak sawit merah netral
(neutralized deodorized red palm oil/NDRPO) dari SEAFAST Center IPB, minyak kelapa (coconut oil/CNO) merk Barco, lipase Thermomyces lanuginosa imobil spesifik sn-1,3 (Lipozyme TL IM), dan lipase Candida antartica imobil non-spesifik (Novozyme 435).
Bahan-bahan untuk analisis kimia adalah heksana p.a., etanol 95%
netral, indikator fenoftalein 1%, NaOH 0.25 N, aseton, gas N2, dan air
destilata. Alat-alat yang digunakan pada penelitian ini adalah shaker, sentrifus,
nuclear magnetic resonance (NMR), spektrofotometer, refrigerator, timbangan analitik, oven, hot plate, desikator, termometer, labu ukur, corong, erlenmeyer, cawan alumunium, stirer, vortex, filter 0.45 µm, buret, kertas
putih, kertas tissue, pengelim plastik, label kertas, kertas saring, dan alat-alat gelas untuk analisis.
B. Metode Penelitian
Penelitian ini dibagi menjadi tiga tahap. Penelitian tahap pertama yaitu
karakterisasi bahan baku. Penelitian tahap kedua yaitu pemilihan formula
bahan baku, sedangkan penelitian tahap ketiga yaitu pengaruh kecepatan
agitasi dan lama reaksi terhadap karakteristik produk bahan baku spreads hasil interesterifikasi enzimatik minyak sawit merah.
1. Penelitian Tahap Pertama: Karakterisasi Bahan Baku
Penelitian tahap pertama bertujuan untuk mengetahui kondisi awal
dari bahan baku sehingga dapat diketahui peluangnya untuk proses
interesterifikasi enzimatik. Sebelum karakterisasi, dilakukan terlebih
dahulu proses fraksinasi dan formulasi. Proses fraksinasi dilakukan
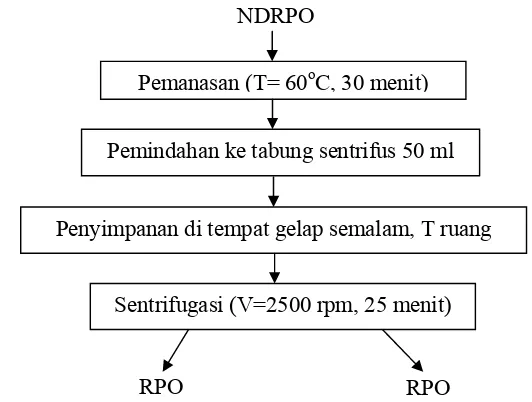
20 metode Aini et al. (2005) yang dimodifikasi Hasrini (2008). Proses fraksinasi dapat dilihat pada Gambar 3.
Gambar 3. Diagram proses fraksinasi (modifikasi Aini et al., 2005)
Prosedur lengkapnya yaitu NDRPO dipanaskan pada suhu 60
selama 30 menit, lalu NDRPO tersebut dipindahkan ke dalam tabung
sentrifus 50 ml dan didiamkan semalam (±16 jam). Pemisahan RPO dan
RPS dilakukan dengan sentrifus pada kecepatan 2500 rpm selama 25
menit. Setelah proses fraksinasi, dilakukan proses formulasi terhadap
RPO, RPS, dan CNO. Proses formulasi dilakukan dengan cara
mencampurkan RPO/RPO (1:1) dan CNO dengan rasio 75:25, 77.5:22.5,
dan 82.5:17.5. Karakteristik yang dianalisis pada penelitian tahap ini
adalah total karoten, slip melting point, solid fat content, kadar air, dan asam lemak bebas.
2. Penelitian Tahap Kedua: Pemilihan Formula Bahan Baku
Penelitian tahap kedua bertujuan untuk memilih satu formula bahan
baku. Pemilihan formula bahan baku dilakukan terhadap tiga formula hasil
penelitian Hasrini (2008) yang menghasilkan karakter fisik paling
mendekati margarin ritel dan industri. Enzim yang digunakan pada NDRPO
Sentrifugasi (V=2500 rpm, 25 menit) Pemindahan ke tabung sentrifus 50 ml
RPO RPO
Pemanasan (T= 60oC, 30 menit)
21 penelitian tahap ini adalah Lipozyme TL IM. Prosedur interesterifikasi
enzimatik menggunakan metode Zhang et al. (2001) yang dimodifikasi Hasrini (2008). Prosedur kerja interesterifikasi enzimatik dapat dilihat
pada Gambar 4
Gambar 4. Prosedur interesterifikasi enzimatik (modifikasi Zhang et al.,
2001)
Prosedur lengkapnya yaitu RPO/RPS (1:1) ditambahkan CNO
masing-masing dengan rasio sesuai perlakuan sebanyak 10 g. Sampel
tersebut lalu dimasukkan ke dalam tabung erlenmeyer 25 ml, diagitasi
dengan menggunakan shaker pada kecepatan 200 rpm dan suhu 60 . Setelah mencapai suhu 60 dan sampel telah meleleh sempurna,
kemudian dimasukkan enzim Lipozyme TL IM sebanyak 10% b/b dan
diagitasi kembali selama 4 jam. Hasil interesterifikasi tersebut diangkat
dan Lipozyme TL IM disaring. Sampel kemudian disimpan dalam botol
kaca gelap, dihembus N2, ditutup dan disimpan dalam refrigerator.
Analisis yang dilakukan terhadap produk hasil interesterifikasi enzimatik
adalah total karoten, slip melting point, dan solid fat content. Tiga formula bahan baku yang digunakan dalam interesterifikasi enzimatik dapat dilihat
pada Tabel 9.
Hasil interesterifikasi enzimatik Agitasi selama 4 jam (V= 200 rpm, T= 60ºC)
Penyaringan enzim
Penambahan enzim Lipozyme TL IM 10% b/b Agitasi sampai suhu mencapai 60ºC (V= 200 rpm)
Pemasukan ke dalam erlenmeyer Penambahan CNO sesuai perlakuan
22
Tabel 9. Formula bahan baku
Sampel Kode Sampel
RPO/RPS (1:1):CNO 75:25 M75
77.5:22.5 M77
82.5:17.5 M82
3. Penelitian Tahap Ketiga: Pengaruh Kecepatan Agitasi dan Lama Reaksi terhadap Karakteristik Produk Bahan Baku Spreads Hasil Interesterifikasi Enzimatik Minyak Sawit Merah.
Penelitian tahap ketiga bertujuan untuk melihat pengaruh kecepatan
agitasidan lama reaksi terhadap karakteristik produk hasil interesterifikasi
enzimatik. Satu formula bahan baku dari penelitian tahap kedua digunakan
sebagai formula terpilih pada penelitian tahap ketiga. Tahapan kerja
interesterifikasi enzimatik dapat dilihat pada Gambar 5.
Gambar 5. Prosedur interesterifikasi enzimatik (modifikasi Zhang et al.,
2001)
Prosedur lengkapnya yaitu RPO/RPS (1:1) ditambahkan CNO sesuai
perlakuan sebanyak 15 g. Sampel tersebut lalu dimasukkan ke dalam
tabung erlenmeyer 25 ml, diagitasi dengan menggunakan shaker pada Penambahan CNO sesuai perlakuan
RPO/RPS (1:1)
Penambahan enzim Novozyme 435 10% b/b Agitasi sampai suhu mencapai 60 ºC (V= 100, 200 rpm)
Pemasukan sampel ke dalam erlenmeyer
Agitasi selama 0, 1, 2, 4, 8, 16, 24 jam (V= 100, 200 rpm, T= 60 )
23 kecepatan sesuai perlakuan dan suhu 60 . Setelah mencapai suhu 60
dan sampel telah meleleh sempurna, kemudian dimasukkan enzim
Novozyme 435 sebanyak 10% b/b dan diagitasi kembali sesuai dengan
lama reaksi yang telah ditentukan. Hasil interesterifikasi tersebut diangkat
dan Novozyme 435 disaring. Sampel kemudian disimpan dalam botol kaca
gelap, dihembus N2, ditutup, dan disimpan dalam refrigerator. Analisis
yang dilakukan pada tahap ini adalah total karoten, slip melting point,
solid fat content, kadar air, dan asam lemak bebas.
Kecepatan agitasiyang digunakan pada tahap ini adalah 100 dan 200
rpm, sedangkan lama reaksi yang digunakan adalah 0, 1, 2, 4, 8, 16, dan
24 jam. Sampel dengan lama reaksi 0 jam merupakan sampel yang tidak
mengalami reaksi interesterifikasi enzimatik (initial mixtures). Perlakuan
kecepatan agitasidan lama reaksi dapat dilihat pada Tabel 10.
Tabel 10. Perlakuan kecepatan agitasidan lama reaksi
Kecepatan agitasi (rpm) Lama reaksi (jam) Kode sampel
100
0 A0 1 A1 2 A2 4 A4 8 A8 16 A16 24 A24
200
24
C. Metode Analisis
Metode analisis yang digunakan untuk menganalisis total karoten, slip melting point, solid fat content, kadar air, dan kadar asam lemak bebas adalah:
1. Total Karoten (PORIM p2.6, 1995)
Sampel dilelehkan dan dihomogenasi. Kemudian sampel sebanyak
0.1 g dilarutkan dengan heksana p.a. ke dalam labu takar 25 ml sampai
tanda tera, lalu dikocok hingga benar-benar homogen. Selanjutnya
absorbansi diukur dengan spektrofotometer pada panjang gelombang 446
nm. Total karotenoid dihitung dengan menggunakan rumus:
Total karotenoid ppm Berat sampel g x 5 x 8 x absorbansi
2. Slip Melting Point (SMP) (AOCS Official Method Cc 3-25, 1990)
Pipa kapiler yang berdiameter 1 mm dan panjang 10 cm dicelupkan
dalam sampel minyak yang sudah dipanaskan setinggi ± 1 cm, lalu bagian
luar pipa kapiler dibersihkan dengan tissue. Pipa kapiler disimpan dalam
refrigerator (suhu 4-10 ºC) selama 16 jam (semalam). Kemudian dipasangkan pada termometer dengan diikat karet sejajar dengan ujung
termometer. Termometer dicelupkan ke dalam gelas piala di atas hot plate
berisi air dengan suhu 8-10 di bawah SMP sampel. Hot plate dinyalakan dengan kenaikan suhu 1 per menit. Air dalam gelas piala naik suhunya,
pada suhu tertentu sampel minyak dalam kapiler mencair yang ditandai
dengan naiknya sampel tersebut. Selang suhu termometer saat sampel
minyak mulai naik sampai sampel minyak berada di atas batas 1 cm
dicatat.
3. Solid Fat Content (SFC) (IUPAC 2.150 ex 2.323, 1987)
Pre-25
treatment atau prosedur stabilisasi sangat menentukan jumlah dan tipe kristal lemak yang terbentuk, dan konsekuensinya terhadap kandungan
padatan (solid content) yang diukur dengan NMR. Prosedur stabilisasi dan tempering untuk pengukuran SFC margarin, sesuai dengan yang
dikeluarkan oleh Bruker (Typical Applications for Industry: Minispec Application Note 8).
Sampel diisikan ke dalam tabung NMR setinggi ± 2,5 cm. Sebelum
dianalisis, sampel dipanaskan pada suhu 80 agar meleleh sempurna
untuk meyakinkan homogenitasnya. Kemudian sampel yang telah meleleh
dipertahankan pada suhu 60 selama 5 menit. Selanjutnya sampel
disimpan pada suhu 0 selama 60 menit. Sebelum dianalisis SFC, sampel
dipertahankan dulu pada masing-masing suhu pengukurannya yaitu 10, 20,
25, 30, 35, dan 40oC selama 30-35 menit.
4. Kadar Air (AOAC, 1995)
Sejumlah ± 5.0 g sampel dimasukkan ke dalam cawan yang telah
diketahui beratnya. Kemudian cawan dimasukkan ke dalam oven bersuhu
100oC hingga diperoleh berat yang konstan. Perhitungan kadar air
dilakukan dengan menggunaan rumus:
Kadar air (%) = x 100%
Keterangan : a = berat cawan dan sampel (g)
b = berat cawan dan sampel akhir (g)
c = berat sampel awal (g)
5. Kadar Asam Lemak Bebas (AOCS Official Method Ca 5a-40, 1990)
Sampel sebanyak 7.05 ± 0.05 g dilarutkan dalam 75 ml alkohol 95%
netral, dipanaskan selama 10 menit dalam hot plate sambil diaduk, lalu ditambahkan 3-5 tetes indikator fenoftalein 1%. Setelah itu sampel
26 muda tetap. Asam lemak bebas dinyatakan sebagai persen asam lemak,
dihitung sampai dua desimal dengan menggunakan rumus:
Kadar asam lemak bebas (%)=
(%)
Keterangan: M= Bobot molekul asam lemak (269.74 untuk minyak sawit,
266.38 untuk fraksi stearin minyak sawit, 270.54 untuk
fraksi olein minyak sawit, dan 212.23 untuk minyak
kelapa)
V= Volume NaOH yang diperlukan dalam peniteran (ml)
T= Normalitas NaOH (N)
m= Bobot contoh (g)
D. Analisis Data
Data total karoten, slip melting point (SMP), kadar air, dan asam lemak bebas yang diperoleh dari penelitian tahap kedua dan penelitian tahap ketiga
diuji secara statistik. Pengolahan data untuk uji statistik menggunakan
program SPSS 12.0. Data yang diperoleh terlebih dahulu dilakukan analisis
ragam dengan ANOVA untuk mengetahui apakah data tersebut berbeda nyata.
Setelah diketahui bahwa data yang diperoleh berbeda nyata, selanjutnya
dilakukan uji lanjut Duncan. Hasil uji lanjut Duncan menunjukkan antar data
27
IV. HASIL DAN PEMBAHASAN
A. Penelitian Tahap Pertama: Karakterisasi Bahan Baku
Karakterisasi dilakukan untuk mengetahui kondisi awal dari bahan baku
sehingga dapat diketahui peluangnya untuk proses interesterifikasi enzimatik.
Sebelum karakterisasi, dilakukan terlebih dahulu proses fraksinasi dan
formulasi. Proses fraksinasi dilakukan terhadap neutralized deodorized red palm oil (NDRPO) untuk mendapatkan red palm olein (RPO) dan red palm stearin (RPS). Proses formulasi dilakukan dengan cara mencampurkan RPO/RPS (1:1) dan coconut oil (CNO) dengan rasio 75:25, 77.5:22.5, dan 82.5:17.5. Karakteristik bahan baku yang dianalisis adalah total karoten, slip melting point, solid fat content, kadar air, dan asam lemak bebas. Hasil analisis terhadap karakteristik tersebut terdapat pada Lampiran 1.
1. Total Karoten
Minyak sawit merah merupakan sumber yang kaya karoten alami.
Menurut Naibaho (1990), minyak sawit merah mengandung total karoten
600–1000 ppm dengan persentase α-karoten 36.2%, β-karoten 54.4%, δ
-karoten 3.3%, likopen 3.8%, dan xantofil 2.2%. Hasil analisis total -karoten
dari bahan baku ditunjukkan pada Tabel 11.
Tabel 11. Total karoten dari bahan baku
Sampel Kode sampel Total karoten (ppm)
NDRPO 376.47 ± 3.65
RPO 351.36 ± 12.07
RPO/RPS 343.27 ± 7.89
(RPO/RPS):CNO
75:25 M75 262.42 ± 6.80
77.5:22.5 M77 265.01 ± 12.66
82.5:17.5 M82 269.02 ± 8.73
Keterangan: Data ± Standar deviasi; NDRPO= Neutralized deodorized red palm oil; RPO= Red palm olein; RPS= Red palm stearin; CNO= Coconut oil.
Total karoten NDRPO lebih tinggi dari total karoten RPO dan
28 fraksinasi, sehingga menyebabkan turunnya total karoten. Menurut Chen
et al. (1994), adanya ikatan ganda menyebabkan karoten peka terhadap panas, cahaya, oksigen, dan degradasi asam.
RPO mempunyai total karoten lebih tinggi dari total karoten
RPO/RPS. Menurut Gee (2007), selama proses fraksinasi, digliserida,
skualan, karoten, tokoferol, dan tokotrienol lebih banyak terdistribusi pada
olein, sedangkan monogliserida, sterol, dan fosfolipid lebih banyak
terdistribusi pada stearin.
Setelah proses formulasi, sampel M82 mempunyai total karoten
tertinggi dan sampel M75 mempunyai total karoten terendah. Total
karoten yang tinggi pada sampel M82 karena sampel tersebut mempunyai
rasio RPO/RPS yang besar. Semakin besar rasio RPO/RPS, total karoten
menjadi semakin tinggi karena RPO/RPS merupakan sumber karoten.
Minyak sawit merah yang digunakan pada penelitian ini berasal dari
minyak sawit yang telah dinetralisasi oleh Widarta (2008) dan
dideodorisasi oleh Riyadi (2009). Selain itu, minyak sawit juga digunakan
oleh Hasrini (2008) untuk membuat bahan spreads dengan cara diinteresterifikasi enzimatik dengan minyak kelapa. Total karoten hasil
penelitian Widarta (2008), Hasrini (2008), dan Riyadi (2009) dapat dilihat
pada Tabel 12.
Berdasarkan Tabel 12 terlihat sampel yang digunakan pada penelitian ini mempunyai total karoten yang lebih rendah dibandingkan
total karoten hasil penelitian Widarta (2008), Riyadi (2009), dan Hasrini
(2008). Rendahnya total karoten diduga karena terjadi kerusakan karoten
selama penyimpanan sebelum digunakan. Faktor lingkungan seperti
cahaya, oksigen, kelembaban, dan panas dapat menyebabkan menurunnya
mutu minyak selama pengolahan dan penyimpanan. Menurut Klau dan
Bauernfeind (1981), faktor utama yang memengaruhi karoten selama
pengolahan dan penyimpanan adalah oksidasi oleh oksigen maupun
29
Tabel 12. Total karoten hasil penelitian Widarta (2008), Hasrini (2008), dan Riyadi (2009)
Sampel Kode
sampel
Total karoten (ppm) Widarta
Keterangan: CPO= Crude palm oil; NRPO= Neutralized red palm oil; NDRPO= Neutralized deodorized red palm oil; RPO= Red palm olein; RPS= Red palm stearin; CNO= Coconut oil.
2. Slip Melting Point dan Solid Fat Content
Slip melting point (SMP) merupakan temperatur pada saat lemak dalam pipa kapiler yang berada dalam air menjadi cukup leleh untuk naik
dalam pipa kapiler. Menurut Karabulut et al. (2004), SMP dari lemak atau minyak dipengaruhi oleh panjang rantai asam lemak, rasio ketidakjenuhan,
jumlah asam lemak trans, dan posisi asam lemak pada gliserol. SMP biasanya digunakan untuk mengkarakterisasi sifat fisik minyak atau lemak
seperti hardness dan solidifikasi/tingkah laku pelelehan (Goh dan Ker, 1991). Rata-rata kisaran nilai SMP bahan baku dapat dilihat pada Tabel 13.
Tabel 13. Nilai SMP dari bahan baku
Sampel Kode sampel SMP ( )
(RPO/RPS):CNO 75:25 M75 34.1±0.9
77.5:22.5 M77 35.6±0.5
82.5:17.5 M82 36.5±0.4
Keterangan: Data ± Standar deviasi; RPO= Red palm olein; RPS= Red palm stearin; CNO= Coconut oil
30 stearat yang semakin tinggi dengan semakin besar rasio RPO/RPS. Asam
stearat termasuk asam lemak jenuh bertitik leleh tinggi, yaitu sebesar 70 .
Semakin besar derajat ketidakjenuhan asam lemak maka semakin rendah
titik leleh minyak, begitu juga sebaliknya (Swern, 1979).
Nilai SMP bahan baku hasil penelitian Hasrini (2008) dapat dilihat
pada Tabel 14. Dari tabel tersebut terlihat nilai SMP hasil penelitian Harsini (2008) lebih kecil dari hasil penelitian tahap ini. Hal ini diduga
karena perbedaan tahapan dalam proses pemurnian (refining) minyak sawit sehingga menghasilkan karakteristik SMP yang berbeda. Hasrini
(2008) melakukan proses pemurnian dengan tahapan degumming, netralisasi, dan fraksinasi. Minyak sawit yang digunakan pada penelitian
ini dihasilkan dari proses pemurnian dengan tahapan degumming, netralisasi, deodorisasi, dan fraksinasi. Proses deodorisasi dapat berfungsi
untuk menghilangkan asam lemak bebas karena dalam proses ini
digunakan suhu tinggi dan tekanan vakum (Ketaren, 1986). Asam lemak
bebas dapat menyebabkan kenaikan atau penurunan SMP.
Tabel 14: Nilai SMP dari bahan baku hasil penelitian Hasrini (2008)
Sampel Kode sampel SMP ( )
(RPO/RPS):CNO 75:25 M75 31.15±0.23
77.5:22.5 M77 33.34±0.78
82.5:17.5 M82 36.19±0.28
Keterangan: Data ± Standar deviasi; RPO= Red palm olein; RPS= Red palm stearin; CNO= Coconut oil
Solid fat content (SFC) adalah jumlah kristal lemak yang terdapat dalam campuran minyak/lemak yang menentukan karakteristik produk
seperti pelelehan maupun sifat organoleptik. Pada penelitian ini, nilai SFC
diukur pada suhu 10 sampai 40 . Hasil analisis SFC disajikan pada Tabel 15. Dari tabel tersebut terlihat nilai SFC meningkat berturut-turut pada sampel M75, M77, dan M82. Peningkatan nilai SFC pada ketiga sampel
tersebut diduga karena kandungan RPS yang semakin besar. Menurut
31 mempunyai titik leleh tinggi, sehingga potensial untuk digunakan sebagai
bahan margarin dan shortening.
Tabel 15. Profil SFC bahan baku
Sampel SFC (%)
10 oC 20 oC 25 oC 30 oC 35 oC 40 oC
NDRPO 40.26 18.92 8.96 7.71 5.96 3.28
RPO 32.93 10.03 4.90 1.47 1.33 1.17
RPS 52.26 34.96 25.29 21.40 17.80 13.22
RPO/RPS 47.38 26.58 20.78 11.57 9.18 6.04
CNO 69.50 29.84 7.36 2.26 1.24 1.04
M75 37.86 14.86 14.31 7.48 6.40 3.52
M77 41.41 16.53 12.65 9.88 7.50 4.92
M82 42.99 17.23 16.49 11.76 8.31 5.15
Keterangan: NDRPO= Neutralized deodorized red palm oil; RPO= Red palm olein; RPS= Red palm stearin; CNO= Coconut oil; M75= Rasio (RPO/RPS):CNO 75:25; M77= Rasio (RPO/RPS):CNO 77.5:22.5; M82= Rasio (RPO/RPS):CNO 82.5:17.5.
Tabel profil SFC bahan baku hasil penelitian Hasrini (2008) dapat
dilihat pada Tabel 16. Dari tabel tersebut terlihat nilai SFC hasil penelitian Hasrini (2008) cenderung lebih tinggi dari nilai SFC hasil penelitian tahap
ini. Hal ini diduga karena perbedaan tahapan dalam proses pemurnian
(refining) minyak sawit sehingga menghasilkan karakteristik SFC yang berbeda.
Tabel 16. Profil SFC bahan baku hasil penelitian Hasrini (2008)
Sampel SFC (%)
10 oC 20 oC 25 oC 30 oC 35 oC 40 oC
M75 45.78 23.52 20.13 14.11 11.23 8.12
M77 46.47 23.46 20.46 14.18 11.28 8.29
M82 46.90 41.37 22.62 16.14 12.59 9.63
32
3. Kadar Air dan Asam Lemak Bebas
Menurut Willis dan Marangoni (2002), kadar air optimum untuk
interesterifikasi enzimatik berkisar antara 0.04 sampai 11% (b/v). Hasil
analisis kadar air dan asam lemak bebas disajikan pada Tabel 17. Dari tabel tersebut terlihat sampel M75, M77, dan M82 dapat digunakan untuk
reaksi interesterifikasi enzimatik karena mempunyai kadar air pada kisaran
kadar air optimum.
Asam lemak bebas (ALB) terbentuk karena adanya reaksi hidrolisis.
Hidrolisis merupakan reaksi yang memisahkan asam lemak dari gliserol
pada molekul minyak (trigliserida) akibat adanya air (Murano, 2003).
Menurut Ketaren (1986), proses hidrolisis dibantu oleh adanya asam,
alkali, uap air, panas, enzim lipolitik (lipase), dan logam katalis seperti Cu
dan Fe.
Tabel 17. Nilai kadar air dan asam lemak bebas bahan baku
Sampel Kode sampel Kadar air (%) Asam Lemak
Bebas (%)
NDRPO 0.065±0.004 1.33±0.01
RPO 0.093±0.001 1.30±0.00
RPO/RPS 0.105±0.003 1.40±0.05
CNO 0.029±0.002 0.33±0.00
(RPO/RPS):CNO
75:25 M75 0.083±0.000 1.00±0.01
77.5:22.5 M77 0.086±0.000 1.15±0.04
82.5:17.5 M82 0.093±0.002 1.26±0.03
Keterangan: Data ± Standar deviasi; NDRPO= Neutralized deodorized red palm oil; RPO=Red palm olein; RPS= Red palm stearin; CNO= Coconut oil.
Dari Tabel 17 terlihat terjadi peningkatan ALB berturut-turut pada sampel M75, M77, dan M82. Peningkatan ALB ini diduga disebabkan
kadar air yang semakin tinggi. Kadar air yang tinggi dapat menyebabkan
hidrolisis yang mengubah minyak menjadi asam lemak bebas sehingga
dapat menyebabkan ketengikan (Ketaren, 1986).
Kadar air dan ALB hasil penelitian Widarta (2008), Hasrini (2008),
33 Riyadi (2009) lebih kecil dari hasil penelitian tahap ini. Hal ini disebabkan
oleh terjadinya kerusakan minyak sawit selama penyimpanan sehingga
menyebabkan kenaikan kadar air dan ALB. Menurut Hartley (1977), ALB
sudah terdapat di dalam minyak sejak bahan tersebut mulai dipanen dan
jumlahnya terus bertambah selama proses pengolahan dan penyimpanan.
Tabel 18. Nilai kadar air dan ALB hasil penelitian Widarta (2008), Hasrini (2008), dan Riyadi (2009)
Sampel Kadar air (%)
Widarta (2008) Hasrini (2008) Riyadi (2009)
CPO 0.14 ± 0.01 - -
NRPO 0.58 ± 0.11 0.035±0.003 0.34 ± 0.31
NDRPO - - 0.00 ± 0.00
RPO - 0.015±0.001 -
RPO/RPS - 0.016±0.001 -
CNO - 0.002±0.000 -
Asam lemak bebas (%)
Widarta (2008) Hasrini (2008) Riyadi (2009)
CPO 3.62 ± 0.21 - -
NRPO 0.13 ± 0.02 0.64±0.04 0.484 ± 0.15
NDRPO - - 0.490 ± 0.15
RPO - 0.51±0.02 -
RPO/RPS - 0.79±0.03 -
CNO - 0.13±0.01 -
34
B. Penelitian Tahap Kedua: Pemilihan Formula Bahan Baku
Penelitian tahap kedua bertujuan untuk memilih satu formula bahan
baku. Pemilihan formula bahan baku dilakukan terhadap tiga formula hasil
penelitian Hasrini (2008) yaitu campuran antara RPO/RPS (1:1) dan CNO
dengan rasio 75:25, 77.7:22.5, dan 82.5:17.5. Ketiga formula tersebut
merupakan formula yang menghasilkan karakteristik mendekati profil bahan
baku margarin ritel dan margarin industri sesudah diinteresterifikasi enzimatik
(Hasrini, 2008). Dari ketiga formula tersebut terlihat rasio RPO/RPS lebih
tinggi dari rasio CNO. Hal ini berhubungan dengan slip melting point yang ingin dihasilkan. Slip melting point minyak sawit cenderung sedikit lebih tinggi dari suhu mulut yaitu 36.72 (Gee, 2007), sehingga diperlukan
pencampuran dengan minyak kelapa dalam jumlah kecil supaya nilai slip melting point-nya berada dalam kisaran suhu tubuh. Interesterifikasi enzimatik pada tahap ini menggunakan enzim Lipozyme TL IM yang merupakan enzim
spesifik (sn-1,3). Karakteristik hasil interesterifikasi enzimatik yang dianalisis
adalah total karoten, slip melting point, dan solid fat content. Hasil analisis terhadap karakteristik tersebut terdapat pada Lampiran 2.
1. Total Karoten
Hasil ANOVA menunjukkan bahwa total karoten sampel berbeda
nyata. Uji lanjut Duncan menunjukkan bahwa total karoten sebelum dan
sesudah interesterifikasi enzimatik pada sampel M75, M77, dan M82
berbeda nyata. Uji lanjut Duncan juga menunjukkan bahwa total karoten
sesudah interesterifikasi enzimatik antara sampel M75, M77, dan M82
tidak berbeda nyata (Lampiran 3). Perbandingan total karoten sebelum dan sesudah interesterifikasi enzimatik dapat dilihat Tabel 19. Dari tabel tersebut terlihat terjadi penurunan total karoten sesudah interesterifikasi