METODE SPEKTROFOTOMETRI
SKRIPSI
TRESNA NAIBAHO
050802048
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
UNIVERSITAS SUMATERA UTARA
METODE SPEKTROFOTOMETRI
SKRIPSI
Diajukan untuk melengkapi tugas dan memenuhi syarat mencapai gelar sarjana Sains
TRESNA NAIBAHO
050802048
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
UNIVERSITAS SUMATERA UTARA
PERSETUJUAN
Judul : PENGARUH KONSENTRASI DAN LAMA PENYIMPANAN LARUTAN KITOSAN TERHADAP ADSORPSI ION Fe DENGAN METODE SPEKTROFOTOMETRI
Kategori : SKRIPSI
Nama : TRESNA NAIBAHO Nomor Induk Mahasiswa : 050802048
Program Studi : SARJANA (S1) KIMIA Departemen : KIMIA
Fakultas : MATEMATIKA DAN ILMU PENGETAHUAN ALAM (FMIPA) UNIVERSITAS SUMATERA UTARA
Disetujui di Medan, Januari 2010
Komisi Pembimbing :
Pembimbing 2 Pembimbing 1
Prof.Dr.Zul Alfian,M.Sc Prof.Dr.Harry Agusnar,M.Sc.,M.Phill NIP. 131 273 465 NIP. 131 273 466
Diketahui/Disetujui oleh
Departemen Kimia FMIPA USU Ketua,
PERNYATAAN
PENGARUH KONSENTRASI DAN LAMA PENYIMPANAN LARUTAN KITOSAN TERHADAP ADSORPSI ION Fe DENGAN METODE
SPEKTROFOTOMETRI
SKRIPSI
Saya mengakui bahwa skripsi ini adalah hasil kerja saya sendiri, kecuali beberapa kutipan dan ringkasan yang masing-masing disebutkan sumbernya.
Medan, Januari 2010
PENGHARGAAN
Segala puji syukur penulis panjatkan kepada Tuhan Yesus Kristus, berkat kasih dan karunia-Nya dalam setiap pimpinan-Nya setiap saat. Dalam masa-masa tersulit maupun terberat Tuhan tetap teguhkan penulis hingga akhirnya penulis dapat menyelesaikan penelitian dan penyusunan skripsi ini.
Dengan kerendahan hati penulis menyampaikan ucapan terima kasih yang sebesar-besarnya kepada Bapak Prof.Dr.Harry Agusnar,M.Sc.,M.Phill selaku pembimbing 1 dan Bapak Prof.Dr.Zul Alfian,M.Sc selaku pembimbing 2 yang telah meluangkan waktunya untuk memberikan bimbingan dan saran kepada penulis selama melakukan penelitian dan penyusunan skripsi ini dan kepada Bapak Prof.Dr.Harlem Marpaung selaku Kepala Laboratorium bidang Kimia Analitik FMIPA USU yang telah memberikan dorongan dan saran-saran kepada penulis. Ucapan terima kasih juga ditujukan kepada Ketua dan Sekretaris Departemen Kimia FMIPA USU, Ibu Dr.Rumondang Bulan Nst,M.Sc dan Bapak Drs.Firman Sebayang,MS, Ibu Andriayani,S.Pd.,M.Si selaku dosen wali yang telah membimbing penulis selama mengikuti perkuliahan di FMIPA USU Medan. Kepada seluruh asisten Laboratorium Kimia Analitik, rekan-rekan angkatan 2005, terkhusus teman-temanku yang setia selalu memberikan dukungannya kepada penulis Mariati, Novriana, Evi Sitopu, Beldina, Natalia, serta sahabat-sahabatku di violet, Indah, Ika, Nora yang telah memberikan dukungan dan perhatian kepada penulis. Akhirnya penulis juga mengucapkan terima kasih yang tak terhingga untuk Papa tersayang T.Naibaho dan Mama tercinta L.Sianipar dan adik-adik tersayang: Handini Naibaho, Dewi Naibaho, Ingrid Clairine Naibaho serta seluruh keluarga buat doa dan kasihnya. Semoga Tuhan Yesus Kristus selalu menyertai kita semua.
Penulis menyadari bahwa skripsi ini masih banyak kekurangan, karena keterbatasan penulis baik dalam literatur maupun pengetahuan. Oleh karena itu, Penulis mengharapkan kritik dan saran yang membangun demi kesempurnaan skripsi ini, dan semoga skripsi ini bermanfaat bagi kita semua.
Medan, Januari 2010
ABSTRAK
THE INFLUENCE OF CONCENTRATION AND STOCKING TIMES OF
CHITOSAN SOLUTION FOR THE ADSORPTION OF ION Fe2+ BY USING
METHOD OF SPECTROPHOTOMETRY
ABSTRACT
DAFTAR ISI
1.2 Permasalahan 2
1.3 Pembatasan Masalah 2
1.4 Tujuan Penelitian 3
1.5 Manfaat Penelitian 3
1.6 Metodologi Penelitian 3
1.7 Lokasi Penelitian 3
BAB 2 TINJAUAN PUSTAKA 4
2.1 Kitosan 4
2.1.1 Kitin dan Kitosan 4
2.1.2 Sifat-Sifat Kitosan 5
2.2 Pemanfaatan Kitosan 6
2.3 Interaksi Kitosan dengan Ion Logam 7
2.4 Mekanisme Serapan Kitosan 7
2.5 Viskositas 8
2.5.1 Viskosimeter Ostwald 8
2.5.2 Penentuan Massa Molekul Polimer 9
2.6 Besi 12
2.6.1 Sifat-Sifat Logam Besi 12
2.6.2 Logam Besi dalam Air 12
2.6.3 Toksisitas Besi 13
2.7 Spektrofotometri Visible 14
2.7.1 Instrumentasi Spektrofotometer UV-Vis 14 2.7.2 Prinsip Dasar Spektrofotometri Visible 16
2.8 Analisa Fe secara Spektrofotometri 17
2.8.1 Metode 1,10-fenantrolina 17
BAB 3 BAHAN DAN METODE PENELITIAN 20
3.1 Alat-Alat 20
3.2 Bahan- bahan 20
3.3 Prosedur Penelitian 21
3.3.1 Pembuatan Larutan Pereaksi 21
3.3.2 Pembuatan Larutan induk 21
3.3.2.1 Pembuatan Larutan Induk Besi (Fe) 1000 mg/L 21 3.3.2.2 Pembuatan Larutan Standar Besi (Fe) 100 mg/L 22 3.3.2.3 Pembuatan Larutan Standar Besi (Fe) 10 mg/L 22 3.3.2.4 Pembuatan Larutan Seri Standar Besi (Fe)
0,6; 0,8; 1,0; 1,2; dan 1,4 mg/L 22
3.3.3 Pembuatan Larutan Kitosan 22
3.3.4 Penentuan Kadar Fe secara Spektrofotometri 22
3.3.4.1 Penentuan λ Maksimum 22
3.3.4.2 Penentuan Waktu Operasi 23
3.3.4.3 Penentuan Kurva Kalibrasi 23
3.3.4.4 Penentuan Konsentrasi Fe setelah Penambahan
Larutan Kitosan untuk Variasi Konsentrasi 23 3.3.4.5 Penentuan Konsentrasi Fe setelah Penambahan
Larutan Kitosan untuk Variasi Lama Penyimpanan
pada Suhu -230C 24
3.3.4.6 Penentuan Konsentrasi Fe setelah Penambahan Larutan Kitosan untuk Variasi Lama Penyimpanan
Pada Suhu Kamar 24
3.3.5 Pengukuran Waktu Alir Larutan Kitosan pada Penentuan
Viskositas 25
3.4 Bagan Penelitian 26
3.4.1 Penentuan Adsorpsi Larutan Kitosan untuk Variasi
Konsentrasi 26
3.4.2 Penentuan Adsorpsi Larutan Kitosan untuk Variasi Lama
Penyimpanan pada Suhu -230C 27
3.4.3 Penentuan Adsorpsi Larutan Kitosan untuk Variasi Lama
Penyimpanan pada Suhu Kamar 28
3.4.4 Penentuan Viskositas Larutan Kitosan 29
BAB 4 HASIL DAN PEMBAHASAN 30
4.1 Hasil Penelitian 30
4.2 Pengolahan Data 31
4.2.1 Penurunan Persamaan Garis Regresi dengan Metode
Kurva Kalibrasi 31
4.2.2 Penurunan Persamaan Garis Regresi 32
4.2.3 Koefisien Korelasi 33
4.2.4 Penentuan Batas Deteksi 35
4.2.5 Penentuan Kadar Besi (Fe) setelah Penambahan
Kitosan 36
4.2.6 Persentasi (%) Penurunan Konsentrasi Ion Besi (Fe) 38
BAB 5 KESIMPULAN DAN SARAN 42
5.1 Kesimpulan 42
5.2 Saran 42
DAFTAR PUSTAKA 43
DAFTAR TABEL
Halaman
Tabel 1. Penentuan Panjang Gelombang Maksimum dari Larutan
Standar 0,6 mg/L Besi 44
Tabel 2. Penentuan Waktu Operasi dari Larutan Standar 0,6 mg/L Besi 44 Tabel 3. Penentuan Kurva Kalibrasi Standar Besi (Fe) 44 Tabel 4. Data Penurunan Kadar Besi (Fe) untuk Variasi Konsentrasi
Larutan Kitosan 45
Tabel 4.1. Data Hasil Pengukuran Transmitansi Ion Besi (Fe) untuk Variasi
Konsentrasi Larutan Kitosan ` 30
Tabel 4.2. Data Hasil Pengukuran Transmitansi Ion Besi (Fe) untuk Variasi
Lama Penyimpanan Larutan Kitosan pada Suhu -230C 31 Tabel 4.3. Data Hasil Pengukuran Trasmitansi Ion Besi (Fe) untuk Variasi
Lama Penyimpan Larutan Kitosan pada Suhu Kamar 31 Tabel 4.4. Hasil Penurunan Persamaan Regresi untuk Fe 32 Tabel 4.5. Data Hasil Perhitungan Korelasi untuk Besi 33 Tabel 5. Data absorbansi Ion Besi (Fe) untuk Variasi Lama Penyimpanan
Larutan Kitosan pada Suhu -23 oC 46
Tabel 6. Data absorbansi Ion Besi (Fe) untuk Variasi Lama Penyimpanan
Larutan Kitosan pada Suhu Kamar 47
DAFTAR GAMBAR
Halaman
Gambar 2.1 Struktur Kitin 5
Gambar 2.2 Struktur Kitosan 5
Gambar 5.1 Viskosimeter Ostwald 9
Gambar 8.1 Sistem Optis Spectronic 20 Bausch and Lomb 18 Gambar 1. Kurva Standar Larutan Standar Besi (Fe) dengan
ABSTRAK
THE INFLUENCE OF CONCENTRATION AND STOCKING TIMES OF
CHITOSAN SOLUTION FOR THE ADSORPTION OF ION Fe2+ BY USING
METHOD OF SPECTROPHOTOMETRY
ABSTRACT
BAB 1
PENDAHULUAN
1.1 Latar Belakang
Kitosan merupakan salah satu senyawa turunan kitin yang diperoleh melalui proses
deasetilasi. Kitin yang merupakan bahan baku kitosan adalah salah satu komponen
penyusun utama limbah cangkang rajungan. Kitosan dapat dimanfaatkan untuk
berbagai keperluan salah satunya, yang sedang marak diteliti saat ini, adalah
pemanfaatan kitosan sebagai penyerap (adsorben) logam.
Kitosan merupakan senyawa turunan dari kitin yang memiliki struktur
(1,4)-2-Amino-2-Deoksi-β-D-Glukosa. Sumber kitosan yang sangat potensial adalah kerangka
Crustaceae. Kitin dan kitosan dapat berinteraksi dengan ion logam. Kitosan dapat
mengikat logam melalui pertukaran ion, adsorpsi dan pembentukan chelat
(Muzarelli,R.A.A,1977).
Kitosan memiliki kegunaan yang beragam, antara lain sebagai koagulan untuk
proses penjernihan air, mengkoagulasi minyak /lemak, proses pengawetan serta dapat
digunakan sebagai adsorben untuk mendegradasi logam berat. Kitosan mempunyai
kemampuan untuk mengadsorpsi logam dan membentuk kompleks kitosan dengan
logam.
Berdasarkan sudut pandang toksikologi, logam Fe termasuk dalam logam berat
esensial, dimana keberadaannya dalam jumlah tertentu sangat dibutuhkan, namun
dalam jumlah berlebihan dapat menimbulkan efek racun, bergantung pada bagian
mana logam berat itu terikat pada tubuh.
Besi, sebagai elemen esensial untuk nutrisi, tubuh, batasan penggunaannya
air dan garam ferri kadang-kadang digunakan untuk menjernihkan air
(Dean,B.Robert,1981).
Defisiensi besi dalam tubuh berpengaruh luas terhadap kualitas sumber daya
manusia, yaitu terhadap kemampuan belajar dan produktivitas kerja. Kelebihan besi
dapat menimbulkan efek racun bagi tubuh. Gejalanya seperti muntah, diare bahkan
denyut jantung meningkat (Almatsier,S,2003). Selain itu, kadar logam besi yang
tinggi juga merugikan, karena dapat menimbulkan rasa besi/logam, air teh menjadi
hitam, warna air pun menjadi kuning atau cokelat, sehingga merugikan jika dipakai
dalam produksi maupun untuk aktivitas sehari-hari.
1.2 Permasalahan
Bagaimanakah pengaruh konsentrasi dan lama penyimpanan larutan kitosan terhadap
adsorpsi ion Fe pada larutan standar besi.
1.3 Pembatasan Masalah
1. Penelitian dibatasi hanya untuk menganalisa kadar ion Fe pada larutan standar
Fe sebelum dan sesudah penambahan larutan kitosan.
2. Variasi konsentrasi larutan kitosan yang ditambahkan pada larutan standar Fe
adalah 0,2%; 0,4%; 0,6%; 0,8% dan 1%
3. Variasi lama penyimpanan larutan kitosan adalah hari pertama sampai hari
kelima.
4. Parameter yang dinalisis yaitu kadar Fe dan diukur dengan spektrofotometer
visible pada λ = 510 nm
Penelitian ini bertujuan untuk menentukan pengaruh konsentrasi dan lama
penyimpanan larutan kitosan terhadap adsorpsi ion Fe pada larutan standar besi.
1.5 Manfaat Penelitian
Diharapkan hasil yang diperoleh dari penelitian ini memberikan suatu informasi
ilmiah mengenai karakterisasi kitosan dalam mengadsorpsi ion Fe untuk jumlah yang
optimal, sehingga dapat diaplikasikan untuk menyerap besi seperti sebagai alternatif,
untuk mengurangi kadar ion Fe dalam air.
1.6 Metodologi Penelitian
Penelitian ini bersifat ekperimen laboratorium yaitu melihat pengaruh konsentrasi dan
lama penyimpanan larutan kitosan terhadap adsorpsi ion Fe. Kitosan dilarutkan
didalam asam asetat 1%, dan dibuat dalam variasi konsentrasi 0,2%; 0,4%; 0,6%;
0,8% dan 1%. Variasi hari yang digunakan adalah hari pertama sampai hari kelima.
Larutan stok disimpan dalam lemari pendingin pada suhu -23°C maupun pada suhu
kamar. Larutan kitosan ini kemudian digunakan sebagai adsorben untuk mengadsorpsi
Fe dengan waktu kontak 30 menit . Kadar Fe sebelum dan sesudah diadsorpsi,
dianalisa dengan metode Spektrofotometri UV-Visible.
1.7 Lokasi Penelitian
Penelitian ini dilakukan di Laboratorium Kimia Analitik Fakultas Matematika dan
BAB 2
TINJAUAN PUSTAKA
2.1 Kitosan
2.1.1 Kitin dan Kitosan
Kitin merupakan polisakarida rantai linier dengan rumus β (1-4)
2-asetamida-2-deoksi-D-glucopyranosa (Muzzarelli,R.A.A,1977) dan kitin sebagai prekursor kitosan
pertama kali ditemukan pada tahun 1811 oleh orang Prancis bernama Henri Braconnot
sebagai hasil isolasi dari jamur. Sedangkan kitin dari kulit serangga ditemukan pada
tahun 1820 (Rismana, 2004).
Kitin tersebar luas di alam dan dijumpai sebagai bahan pembentuk kerangka
luar (eksoskleton) kelompok hewan krustacea, insekta, moluska, dan dinding sel
jamur tertentu dan ditaksir dihasilkan di alam sekitar 109 hingga 1010 ton pertahunnya
(Kumar, 2000).
Kitosan merupakan senyawa turunan dari kitin yang memiliki struktur
(1,4)-2-Amino-2-Deoksi-β-D-Glukosa. Sumber kitosan yang sangat potensial adalah kerangka
Crustaceae (Muzarelli,R.A.A,1977). Kitosan merupakan polimer alami dengan
struktur molekul yang menyerupai selulosa (serat pada sayur-sayuran dan
buah-buahan) bedanya terletak pada gugus rantai 2 di mana gugus hidroksi (OH) pada
C-2 digantikan oleh amina (NH2) (Hardjito, 2006).
Kitosan ditemukan oleh Routget (1859). Beliau menemukan bahwa kitin yang
telah didihkan pada larutan KOH, juga dapat diperlakukan dengan NaOH dan
dipanaskan, maka terjadi pelepasan gugus asetil yang terikat pada atom nitrogen
O O
Kitin murni mengandung gugus asetamida (NH-COCH3), dan kitosan murni
mengandung gugus amino (NH2). Perbedaan gugus ini akan mempengaruhi sifat-sifat
kimia senyawa tersebut (Roberts,G.A.F,1992).
Gambar 2.1 Struktur Kitin
Gambar 2.2 Struktur Kitosan
2.1.2 Sifat-Sifat Kitosan
Kitosan adalah padatan amorf putih yang tidak larut dalam alkali dan asam mineral
kecuali pada keadaan tertentu. Keterlarutan kitosan yang paling baik ialah dalam
larutan asam asetat 1%, asam format 10% dan asam sitrat 10%. Kitosan tidak dapat
larut dalam asam piruvat, asam laktat dan asam-asam anorganik pada pH tertentu,
walaupun setelah dipanaskan dan diaduk dengan waktu yang agak lama. Keterlarutan
kitosan dalam larutan asam format ataupun asam asetat dapat membedakan kitosan
Kitosan dibedakan dari kitin oleh kelarutannya dalam larutan asam encer.
Kitosan bermuatan positif karena kelompok amina pada pH asam, yang besarannya
tergantung pada tingkat deasetilasi, dan dengan demikian kitosan diklasifikasikan
sebagai polielektrolit kationik, sedangkan polisakarida yang lain memberikan muatan
netral ataupun anionik (Hwang dan Shin, 2001).
Kitosan memiliki sifat unik yang dapat digunakan dalam berbagai cara serta
memiliki kegunaan yang beragam, antara lain sebagai perekat, aditif untuk kertas dan
tekstil, penjernihan air minum, serta untuk mempercepat penyembuhan luka, dan
memperbaiki sifat pengikatan warna. Kitosan merupakan pengkelat yang kuat untuk
ion logam transisi. Kitosan mempunyai kemampuan untuk mengadsorpsi logam dan
membentuk kompleks kitosan dengan logam (Robert,G.A.F,1992).
Peningkatan kelarutan berbanding lurus dengan peningkatan derajat
deasetilasi. Hal ini disebabkan gugus asetil pada kitin yang dipotong oleh proses
deasetilasi akan menyisakan gugus amina. Ion H pada gugus amina menjadikan
kitosan mudah berinteraksi dengan air melalui ikatan hidrogen. Sifat kitosan hanya
dapat larut dalam asam encer, seperti asam asetat, asam format, asam sitrat kecuali
kitosan yang telah disubstitusi dapat larut air. Adanya gugus karboksil dalam asam
asetat akan memudahkan pelarutan kitosan karena terjadinya interaksi hidrogen antara
gugus karboksil dengan gugus amina dari kitosan (Dunn et al,1997).
2.2 Pemanfaatan Kitosan
Kitosan banyak digunakan oleh berbagai industri antara lain industri farmasi,
kesehatan, biokimia, bioteknologi, pangan, pengolahan limbah, kosmetik,
agroindustri, industri tekstil, industri perkayuan, industri kertas dan industri
elektronika. Aplikasi khusus berdasarkan sifat yang dipunyainya antara lain untuk
pengolahan limbah cair terutama bahan sebagai bersifat resin penukar ion untuk
meminimalisasi logam-logam berat, mengkoagulasi minyak/lemak, serta mengurangi
2.3 Interaksi Kitosan dengan Ion Logam
Muzzarelli(1973) menyatakan bahwa kitosan mengikat logam melalui pertukaran ion,
penyerapan dan pengkhelatan. Ketiga proses tersebut bergantung pada ion logam
masing-masing. Untuk Ca, pertukaran ion merupakan proses yang paling dominan,
dibanding dengan logam lain, penyerapan dengan proses pengkhelat yang lebih
dominan. Interaksi antara ion logam transisi periode pertama dengan kitosan disertai
dengan pembentukan warna pada setiap contoh. Merah untuk Titanium, hijau untuk
Cr3+, kuning kecoklatan dengan Fe2+, hijau kekuningan dengan Fe3+, merah jambu
dengan Co, hijau dengan Ni, dan biru dengan Cu. Warna ini akan lebih kuat dengan
kitosan daripada dengan kitin (Muzzarelli,R.A.A,1977).
Kemampuan kitosan untuk mengikat logam dengan cara pengkelat adalah
dihubungkan dengan kadar nitrogen yang tinggi pada rantai polimernya. Kitosan
mempunyai satu kumpulan amino linier bagi setiap unit glukosa. Kumpulan amino ini
mempunyai sepasang elektron yang dapat berkoordinat atau membentuk ikatan-ikatan
aktif dengan kation-kation logam. Unsur nitrogen pada setiap monomer kitosan
dikatakan sebagai gugus yang aktif berkoordinat dengan kation logam
(Hutahaean,S.Ida,2001).
2.4 Mekamisme Serapan Kitosan
Pada umunya mekanisme serapan kitosan terhadap logam dapat dirumuskan pada tiga
cara,yaitu :
1. Secara pengkhelat, dimana terbentuknya ikatan aktif antara nitrogen kitosan
Dengan kation logam,dalam hal ini nitrogen dari kitosan bertindak sebagai basa
lewis yang menyumbang sepasang elektron untuk berkoordinat dengan logam.
2. Secara pertukaran ion, yaitu berlaku pertukaran antara proton dari kitosan dengan
kation logam.
3. Secara memperangkap, dimana ion logam terperangkap dalam lingkaran rantai
2.5 Viskositas
Viskositas menyatakan ukuran kekentalan suatu cairan atau fluida. Kekentalan
merupakan sifat cairan yang berhubungan erat dengan hambatan untuk mengalir.
Viskositas cairan akan menimbulkan gesekan antara bagian-bagian atau
lapisan-lapisan cairan yang bergerak satu terhadap yang lain. Hambatan atau gesekan yang
terjadi ditimbulkan oleh gaya kohesi dalam zat cair.
Setiap fluida mempunyai viskositas yang berbeda-beda yang harganya
bergantung pada jenis cairan dan suhu. Pada kebanyakan cairan, viskositasnya turun
dengan naiknya suhu. Menurut ’teori lubang’ terdapat kekosongan dalam cairan dan
molekul bergerak secara kontinyu ke dalam kekosongan ini, sehingga kekosongan
akan bergerak keliling. Proses ini menyebabkan aliran, tetapi memerlukan energi
karena ada energi pengaktifan yang harus dipunyai suatu molekul agar dapat bergerak
ke dalam kekosongan. Energi pengaktifan lebih mungkin terdapat pada suhu yang
lebih tinggi dan dengan demikian cairan lebih mudah mengalir (Yazid,Estein,2005).
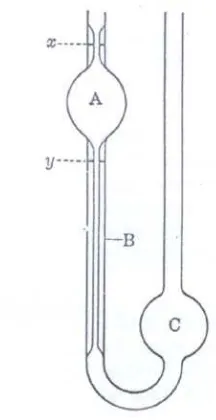
2.5.1 Viskometer Ostwald
Metode ini ditentukan berdasarkan hukum Poiseuille menggunakan alat viskosimeter
Ostwald. Penetapannya dilakukan dengan mengukur waktu yang diperlukan untuk
mengalirnya cairan dalam pipa kapiler dari x ke y. Cairan yang akan diukur
viskositasnya dimasukkan ke dalam viskosimeter yang diletakkan pada termostat.
Cairan kemudian dihisap dengan pompa ke dalam bola A sampai diatas tanda x.
Cairan dibiarkan mengalir ke bawah dan waktu yang diperlukan dan x ke y dicatat
Gambar 5.1 Viskosimeter Ostwald
Viskosimeter Ostwald terdiri dari bola dengan nilai batas atas (x)dan (y), yang
terkait dengan tabung kapiler B dan bola tempat cuplikan C. Volume cairan awal
dimasukkan ke dalam bola C, kemudian dihisap ke A dan kemudian dilihat waktu alir
dari cairan yang berada di antara x dan y. Kemudian perlakukan diulang untuk cairan
yang lain. Tekanan yang terjadi selama mengalirnya cairan melalui kapiler B adalah
sebanding dengan hgp, dimana h adalah perbedaan tinggi diantara bola tempat
mengalirnya cairan. Sebagai nilai awal dan nilai akhir sama tiap kasus, dimana
bergatung pada tekanan dan juga densitas cairan.
2 1
ηη = 2 2 1 1
t t
ρρ
Dimana t1 dan t2 adalah waktu alir (Glastone,Samuel,1959).
2.5.2 Penentuan Massa Molekul Polimer
Bilamana bahan polimer bercampur dengan suatu pelarut (cairan berbobot molekul
rendah) terlebih dahulu akan terjadi peristiwa penggembungan, dengan molekul
interaksi antar sesama rantai polimer menjadi semakin lemah dan akhirnya lepas sama
sekali membentuk larutan polimer. Bobot molekul polimer dapat ditentukan dengan
cara pengamatan sifat fisik larutannya, seperti ultrasentrifugasi, metode viskositas, dan
teknik Kromatografi Permeasi Gel (GPC).
Salah satu karakteristik dari larutan polimer berbobot molekul tinggi
dibandingkan dengan pelarut murninya adalah kenaikan viskositas larutannya oleh
pertambahan konsentrasi. Karena berat/ukurannya yang besar, molekul polimer dalam
larutan akan menurunkan mobilitas dan mempengaruhi sifat aliran campuran yang
sebanding dengan jumlah molekul terlarut. Karena itu, pengamatan perubahan
viskositas ini dapat digunakan untuk menentukan bobot molekul polimer tersebut
(Wirjosentono,B, 1995).
Tabel 2.5.2 Pembagian Viskositas Larutan Encer
Istilah Umum Istilah IUPAC Simbol dan defenisi
Viskositas relatif Rasio viskositas η= η/ηo = t/to
Viskositas spesifik - ηsp = η - ηo/ ηo
Viskositas tereduksi Bilangan viskositas ηred= ηsp/C
Viskositas inheren Billangan viskositas
Logaritma
ηinh= ln (ηrel)/C
Viskositas intrinsik Bilangan viskositas
terbatas
Viskositas intrinsik paling bermafaat dan mudah dipakai karena bisa
dihubungkan ke berat molekul oleh persamaan empiris Mark-Houwink,
[η] = K. Ma
K dan a adalah tetapan karakteristik polimer-pelarut pada suhu tertentu
(Stevens,M.P,2001).
Viskositas dari suatu larutan kitosan diukur menggunakan viskometer.
t - to
η sp =
to
η sp = viskositas spesifik (detik)
t = waktu yang diperlukan untuk mengalirnya larutan sampel (detik)
to = waktu yang diperlukan untuk mengalirnya larutan solvent (detik)
Dengan cara ini akan diperoleh viskositas spesifik, yang tidak mempunyai satuan.
Viskositas spesifik digunakan nilainya untuk penentuan viskositas intrinsik dan berat
molekul.
Berat molekul kitosan ditentukan berdasarkan viskositas intrinsik menurut
persamaan Mark-Houwink berikut ini :
[η] = KMa
[η] = viskositas intrinsik ( ml/g)
K = Konstanta untuk pelarut (ml/g)
a = konstanta
M = berat molekul
Viskositas intrinsik kitosan dapat ditentukan apabila nilai K dan a untuk pelarut yang
digunakan telah diketahui.
(Http://
resources.unpad.ac.id/unpad-content/upload/publikasi_dosen/makalah-6.viskositas)
Persamaan Mark-Houwink dengan harga tetapan yang bersangkutan hanya
berlaku untuk polimer rantai lurus. Hubungan viskositas intrinsik dengan bobot
molekul untuk polimer cabang dan kopolimer memerlukan persamaan yang lebih
rumit. Percabangan pada rantai polimer akan menaikkan rapatan segmen dalam
gulungan, sehingga rantai ini mempunyai volume-hidrodinamis yang lebih kecil.
Akibatnya, mobilitas molekul rantai cabang akan lebih besar (mempunyai viskositas
intrinsik lebih kecil) dibanding dengan rantai lurus berbobot molekul sama
2.6 Besi
2.6.1 Sifat-Sifat Logam Besi
Besi mempunyai semua karakteristik sifat-sifat dari unsur-unsur transisi. Jadi, besi
berbentuk logam berat yang memiliki titik didih yang tinggi. Sifat fisika besi: besi
murni merupakan logam berwarna abu-abu dengan densitas 7,8; titik leburnya 1527°,
dan mendidih jika ditanur pada suhu 3235°. Dalam laboratorium, ferro sulfat yang
biasa digunakan adalah Ferro ammonium sulfat, (NH4)2Fe(SO4)2.6H2O, karena itu,
garam ganda ini dan lebih mudah dimurnikan, dan dalam larutan tidak mudah
mengalami oksidasi oleh udara (Lowry,T.M,1958).
Jarang terdapat besi komersial yang murni; biasanya besi mengandung
sejumlah kecil karbida, silisida, fosfida, dan sulfida dari besi,serta sedikit grafit.
Gara-garam besi(II) diturunkan dari besi(II) oksida, FeO. dalam larutan, Gara-garam-Gara-garam ini
mengadung kation Fe2+ dan berwarna sedikit hijau. Ion besi (II) dapat mudah
dioksidasikan menjadi besi(III), maka merupakan zat pereduksi yang kuat. Semakin
kurang asam larutan itu, semakin nyatalah efek ini; dalam suasana netral atau basa
bahkan oksigen dari atmosfer akan mengoksidasikan ion besi (II). Maka larutan
besi(II) harus sedikit asam bila ingin disimpan untuk waktu yang agak lama
(Vogel,1990).
2.6.2 Logam Besi dalam Air
Besi merupakan salah satu elemen kimia yang dapat ditemui pada hampir setiap
tempat di bumi, pada semua lapisan geologis dan semua badan air, besi yang ada di
dalam air dapat bersifat :
1. Terlarut sebagai Fe2+(fero) atau Fe3+(feri)
2. tersuspensi sebagai butir koloidal
3. tergabung dengan zat organis atau zat padat yang inorganis atau seperti tanah
Pada air permukaan jarang dijumpai kadar Fe yang lebih besar dari 1 mg/L,
tetapi didalam air tanah kadar Fe dapat jauh lebih tinggi. Pada air yang tidak
mengandung oksigen (O2) seperti sering kali air tanah, besi berada sebagai Fe2+ yang
cukup larut (Alaerts,G,1987).
Pada air permukaan, konsentrasi besi jarang mencapai 1 mg/L. Beberapa air
tanah dan permukaan yang sedikit asam memungkinkan untuk mengandung besi yang
lebih banyak. Besi didalam air dapat menyebabkan bintik/noda pada pakaian dan
porselen. Rasa air yang sedikit manis kadang dapat dideteksi oleh beberapa orang
pada kadar dibawah 1 mg/L (Standard method,1980).
Kadar besi pada perairan yang mendapat cukup aerasi (aerob) hampir tidak
pernah lebih dari 0,3 mg/L. Kadar besi > dari 1,0 mg/L dianggap membahayakan
kehidupan organisme akuatik. Air yang diperuntukkan bagi air minum sebaiknya
memiliki kadar besi kurang dari 0,3 mg/L. Kadar besi yang berlebihan dapat
mengakibatkan karat pada peralatan yang terbuat dari logam, serta dapat memudarkan
bahan celupan dan tekstil (Effendi,2003).
Kadar besi maksimum yang dianjurkan terletak antara 0,05 dan 1 mg/L untuk
menghindarkan noda bintik pada pakaian ( Dean,B.Robert,1981).
2.6.3 Toksisitas Besi
Besi merupakan mineral mikro yang paling banyak terdapat didalam tubuh manusia
yaitu sebanyak 3-5 gram di dalam tubuh manusia dewasa. Mineral mikro terdapat
dalam jumlah sangat kecil di dalam tubuh, namun mempunyai peranan esensial untuk
kehidupan, kesehatan dan reproduksi. Besi mempunyai beberapa fungsi esensial di
dalam tubuh: sebagai alat angkut oksigen dari paru-paru ke jaringan tubuh, sebagai
alat angkut elektron di dalam sel dan sebagai bagian terpadu berbagai reaksi enzim di
Mineral yang sering berada dalam air dengan jumlah besar adalah kandungan
Fe. Apabila Fe tersebut berada dalam jumlah yang banyak akan memunculkan
gangguan. Efek toksik dari logam mampu menghalangi kerja enzim sehingga
mengganggu metabolisme tubuh, menyebabkan alergi, bersifat mutagen, teratogen
atau karsinogenik bagi manusia maupun hewan. Fe berperan penting dalam sistem
imunitas. Seseorang dengan kadar Fe rendah akan memiliki daya tahan tubuh rendah
terhadap infeksi (Widowati,W,2008).
2.7 Spektrofotometri Visible
Jika suatu berkas sinar dilewatkan melalui suatu kuvet yang berisi cairan, maka radiasi
yang dihasilkan akan lebih lemah dari sinar masuk. Hal ini disebabkan karena adanya
kehilangan yang disebabkan pantulan pada permukaan dan hamburan oleh adanya
partikel suspensi, tetapi pada larutan yang jernih dapat ditentukan dari absorbsi energi
radiasi oleh larutan itu.
Jika energi yang diserap besar untuk suatu panjang gelombang sinar tampak,
maka akan memperlihatkan warna. Warna yang tampak dari larutan itu biasanya
merupakan warna komplemen dari warna yang diabsorbsi. Suatu substansi yang tidak
berwarna atau berwarna lemah umumnya ditentukan dengan menambahkan suatu
reagen yang akan mengubahnya menjadi suatu campuran yang memiliki warna yang
kuat.
Spektrofotometer untuk ultraviolet dan visible umumnya berada pada panjang
gelombang antara 165 nm dan 210 nm. Batas maksimumnya tidak kurang dari 650
nm, dan banyak juga diperluas sampai 1000 nm dan selanjutnya (Ewing,W.G,1975).
2.7.1 Instrumentasi Spektrofotometer UV-Vis
SR M SK D A VS
Keterangan:
SR = Sumber radiasi D = Detektor
M = Monokromator A = Amplifier atau penguat
SK = Sampel kompartemen VS = Visual display atau meter
1. Sumber radiasi
Beberapa macam sumber radiasi yang dipakai pada spektrofotometer UV-Vis adalah
lampu deuterium, lampu tungsten, dan lampu merkuri. Sumber radiasi deuterium
dapat dipakai pada daerah panjang gelombang 190 nm sampai 380 nm (daerah
ultraviolet dekat). Sumber radiasi tungsten merupakan campuran dari filamen tungsten
dan gas iodin (halogen). Ini digunakan pada spektrofotometer UV-Vis sebagai sumber
radiasi pada daerah pengukuran sinar tampak dengan rentangan panjang gelombang
380 – 900 nm. Sumber radiasi merkuri dipakai untuk mengecek atau mengkalibrasi
panjang gelombang pada spektrofotometer UV-Vis pada daerah ultraviolet, sekaligus
mengecek resolusi dari monokromator.
2. Monokromator
Monokromator pada spektrofotometer UV-Vis biasanya terdiri dari susunan celah
(slit) masuk-filter-prisma-kisi(grating)-celah keluar. Monokromator ini berfungsi
untuk mendapatkan radiasi monokromatis dari sumber radiasi yang memancar radiasi
polikromatis.
3. Sel atau kuvet
Kuvet atau sel merupakan wadah sampel yang akan dianalisis. Ditinjau dari
pemakaiannya kuvet ada 2 macam yaitu kuvet yang permanen terbuat dari bahan gelas
atau leburan silika dan kuvet disposibel untuk satu kali pemakaian yang terbuat dari
teflon atau plastik.
4. Detektor
Peranan detektor penerima adalah memberikan respon terhadap cahaya pada berbagai
5. amplifier
Untuk memperkuat sinyal yang dihasilkan oleh detektor.
6. Visual display atau meter
Sinyal-sinyal elektronik yang dihasilkan pada detektor oleh visual display kemudian
dibaca dalam bentuk transmitansi (Mulja,1999).
2.7.2 Prinsip Dasar Spektrofotometri Visible
Bila cahaya (monokromatik maupun campuran) jatuh pada suatu medium homogen,
sebgaian sinar masuk akan dipantulkan, Sebagian diserap dalam medium itu,dan
sisanya diteruskan. Jika intensitas sinar masuk dinyatakan oleh Io, Ia intensitas sinar yang diserap, It intensitas sinar terteruskan, Ir intensitas sinar terpentulkan, maka:
Io =Ia + It + Ir
Lambert seringkali dianggap berjasa dalam menyelidiki serapan cahaya
sebagai fungsi ketebalan medium, meskipun sebenarnya ia hanya memperluas konsep
yang pada mulanya dikembangkan oleh Bouguer. Beer kemudian menerapkan
eksperimen serupa pada larutan dengan konsentrasi yang berlainan. Kedua hukum
yang terpisah yang mengatur absorbsi itu biasanya dikenal sebagai hukum Lambert
dan hukum Beer. Dalam gabungan, hukum ini dikenal sebagai hukum Beer-Lambert.
Hukum Lambert menyatakan bahwa bila cahaya monokromatik melewati
medium tembus cahaya, laju berkurangnya intensitas oleh bertambahnya ketebalan,
berbanding lurus dengan intensitas cahaya. Ini setara dengan menyatakan bahwa
intensitas cahaya yang dipancarkan berkurang secara eksponensial dengan
bertambahnya ketebalan medium yang menyerap.
A = log Io/It
Hukum Beer mengkaji efek konsentrasi penyusun yang berwarna dalam larutan,
terhadap transmisi maupun absorbsi cahaya (Vogel,1994).
2.8 Analisa Fe secara Spektrofotometri
Melalui pembentukan ion kompleks dengan 1,10 fenantrolin, tiga molekul fenantrolin
bergabung dengan Fe2+ membentuk ion kompleks berwarna orange-merah. Sistem
warna tersebut mengikuti hukum Beer : Sinar cahaya dengan panjang gelombang yang
tertentu yaitu 510 nm, akan diabsorbsi secara proporsional dengan jarak perjalanannya
di dalam larutan dan dengan kadar kompleks yang berwarna orange-merah ini.
Sianida, nitrit dan polifosfat dalam analisa Fe yang dapat mengganggu reaksi
dapat diatasi melalui pendidihan sampel. Krom dan seng (jika konsentrasinya 10 kali
konsentrasi besi), kobalt, dan tembaga (jika > 5 mg/L) dan nikel (jika >2 mg/L)
semuanya dapat mengganggu walaupun keadaan tersebut hanya ditemui misalnya
pada air limbah industri yang mengandung logam tersebut, gangguan ini dapat
dihindarkan dengan penambahan hidroksilamin. Bismut, kadmium, air raksa, molibdat
dan perak dapat mengendapkan fenantrolin. Dalam kasus ini konsentrasi fenantrolin
harus dinaikkan (Alaert,G,1987).
2.8.1 Metode 1,10-Fenantrolina
Besi (II) bereaksi dengan 1,10-fenantrolina membentuk kompleks jingga-merah
[ C12H8N2)3Fe]2+. Intensitas warnanya tak bergantung pada keasaman dalam jangka
pH 2-9, dan stabil untuk waktu yang lama. Besi (III) dapat direduksi dengan
hidroksilamonium klorida atau dengan hidrokuinon. Perak, bismut, tembaga, nikel dan
kobalt mengganggu dengan serius, seperti juga perklorat, sianida, molibdat dan
tungstat. Kompleks besi-fenantrolina diukur pada 515 nm terhadap blanko reagensia.
besi(II) jingga-kemerahan menyerap pada 515 nm, dan baik kompleks besi(II)
maupun besi(III) yang berwarna kuning mempunyai absorbsi identik pada 396 nm,
dengan absorbans aditif. Larutan yang sedikit bersifat asam oleh asam sulfat, diolah
dengan 1,10-fenantrolina, dan dibuffer dengan kalium hidrogen ftalat pada 3,9;
pembacaan pada 396 nm menghasilkan besi total dan pembacaan pada 515 nm besi
(II) (Vogel,1994).
2.8.2 Spectronic 20 Bausch and Lomb
Instrument ini pada hakekatnya terdiri dari monokromator kisi-difraksi dan sistem
deteksi elektronik, amlifikasi dan pengukuran. Panjang gelombangnya berjangka 375
nm ke 650 nm, dan dapat diperluas ke 950 nm dengan menambahkan sebuah filter
merah. Sistem optisnya dipaparkan dalam gambar 8.1.
Gambar 8.1 sistem optis Spectronic 20 Bausch and Lomb
Cahaya putih dari lampu wolfram difokuskan oleh lensa A ke celah masuk;
lensa B mengumpulkan cahaya dari celah masuk itu dan memfokuskan kembali ke
celah keluar setelah dipantulkan dan didispersikan oleh kisi difraksi untuk
memperoleh berbagai panjang gelombang. Kisi itu diputar dengan pertolongan suatu
lengan yang digerakkan bila roda sisirnya diputar. Cahaya monokromatik yang
ke dalam berkas cahaya sehingga kendali penguat dapat disesuaikan. Kuvet atau
tabung uji kecil yang khusus digunakan sebagai wadah untuk contoh.
Kendali pengganda disesuaikan agar pengukur menunjuk nol pada skala
Transmitans Persen atau pada skala Absorbans. Tabung uji atau kuvet yang
mengandung air atau pelarut lain kemudian dimasukkan ke dalam pemegang contoh.
Kendali cahaya kemudian diputar sampai pengukur menunjukkan ’100’ atau ’0’.
Larutan contoh kemudian dimasukkan menggantikan blanko dan transmitansi persen
BAB 3
BAHAN DAN METODE PENELITIAN
3.1 Alat-alat
- Timbangan elektrik Mettler PM 400
- Peralatan gelas Pyrex
- Hot plate stirrer PMC
- Shaker Stuart
- Lemari pendingin
- Magnetik bar
- Spektrofotometer Spektronik 20
- Kuvet
- Mikro pipet Pyrex
- Kertas saring Whatman no.1
3.2 Bahan-bahan
- Kitosan
- CH3COOH glasial p.a (E.Merck)
- Fe(NH4)2(SO4)2.6H2O p.a (E.Merck)
- H2SO4 98% p.a(E.Merck)
- NH2OH.HCl p.a(E.Merck)
- NaCH3COO.3H2O p.a(E.Merck)
- 1,10-phenanthroline monohidrat p.a(E.Merck)
- HCl 37% p.a(E.Merck)
3.3 Prosedur Penelitian
3.3.1 Pembuatan Larutan Pereaksi
a. Larutan Asam Asetat 1%
Sebanyak 10 mL asam asetat glasial dimasukkan kedalam labu takar 1000 mL.
Kemudian diencerkan dengan akuadest sampai garis tanda, kemudian dihomogenkan.
b. Larutan Hidroksilamin
Sebanyak 10 g NH2OH.HCl dilarutkan dengan 100 mL akuades dalam labu takar 100
mL sampai garis tanda, kemudian dihomogenkan.
c. Larutan Natrium Asetat
Sebanyak 25 g NaCH3COO. 3H2O dilarutkan dengan 100 mL akuades dalam labu
takar 100 mL sampai garis tanda, kemudian dihomogenkan.
d. Larutan 1,10-fenantrolin
Sebanyak 100 mg 1,10-phenantroline monohidrat (C12H8N2.H2O) dilarutkan dengan
100 mL akuades yang telah di tambahkan 2 tetes HCl pekat, dalam labu takar 100 mL
sampai garis tanda, kemudian dihomogenkan.
3.3.2 Pembuatan Larutan Induk
3.3.2.1 Pembuatan Larutan Induk Fe 1000 mg/L
Didalam labu takar 1 L diisi 50 mL air suling, kemudian ditambahkan dengan hati-hati
20 mL H2SO4 pekat, kemudian larutkan kedalamnya sebanyak 7,0225 g Fe(NH4)2
(SO4)2.6H2O. Tambahkan larutan KMnO4 0,1 N sedikit demi sedikit sampai sampai
warna merah muda. diencerkan dengan aquadest sampai garis tanda kemudian
3.3.2.2 Pembuatan Larutan Standar Fe 100 mg/L
Sebanyak 5 mL larutan induk Fe 1000 mg/L dimasukkan dalam labu takar 50 mL lalu
diencerkan dengan akuades sampai garis tanda dan dihomogenkan.
3.3.2.3 Pembuatan Larutan Standar Fe 10 mg/L
Sebanyak 5 mL larutan induk Fe 100 mg/L dimasukkan dalam labu takar 50 mL lalu
diencerkan dengan akuades sampai garis tanda dan dihomogenkan.
3.3.2.4 Pembuatan Larutan Seri Standar Fe 0,6; 0,8; 1,0; 1,2; 1,4 mg/L
Sebanyak 3,4,5,6,7 mL larutan standar Fe 10 mg/L dimasukkan kedalam 5 labu takar
50 mL kemudian diencerkan dengan akuades sampai garis tanda dan dihomogenkan
sehingga diperoleh larutan standar Fe 0,6; 0,8; 1,0; 1,2; dan 1,4 mg/L.
3.3.3 Pembuatan Larutan Kitosan
Sebanyak 0,2; 0,4; 0,6; 0,8; 1,0 g kitosan ditimbang dan dimasukkan ke dalam gelas
beaker dan dilarutkan dengan 100 mL asam asetat 1%, dan distirer selama ± 30 menit
3.3.4 Penentuan Kadar Fe secara Spektrofotometri
3.3.4.1 Penentuan Panjang Gelombang Maksimum (λ maks)
Sebanyak 50 mL larutan standar Fe 0,6 mg/L dimasukkan ke dalam erlenmeyer dan
ditambahkan 1 mL hidroksilamin kemudian diaduk hingga homogen, lalu
ditambahkan dengan 1 mL larutan natrium asetat lalu dihomogenkan, kemudian
ditambahkan dengan 10 mL larutan 1,10-fenantrolin dan diaduk kembali hingga
homogen. Larutan didiamkan selama 10 menit hingga pembentukan warna sempurna.
Selanjutnya transmitansi larutan diukur dengan spektrofotometer sinar tampak pada
3.3.4.2 Penentuan Waktu Operasi
Sebanyak 50 mL larutan standar Fe 0,6 mg/L dimasukkan ke dalam erlenmeyer dan
ditambahkan 1 mL hidroksilamin kemudian diaduk hingga homogen, lalu
ditambahkan dengan 1 mL larutan natrium asetat lalu dihomogenkan, kemudian
ditambahkan dengan 10 mL larutan 1,10-fenantrolin dan diaduk kembali hingga
homogen. Larutan didiamkan selama 10 menit sehingga di peroleh kompleks yang
berwarna merah jingga. Selanjutnya transmitansi larutan diukur dengan
spektrofotometer sinar tampak pada panjang gelombang 510 nm dengan variasi
waktu 5, 10, 15, 20, 25 menit.
3.3.4.3 Penentuan Kurva Kalibrasi
Sebanyak 50 mL larutan standar Fe 0,2 mg/L; 0,4 mg/L; 0,6 mg/L; 0,8 mg/L dan 1
mg/L dimasukkan secara terpisah ke dalam 5 buah gelas Erlenmeyer dan dalam setiap
larutan ditambahkan 1 mL hidroksilamin kemudian diaduk hingga homogen, lalu
ditambahkan dengan 1 mL larutan natrium asetat lalu dihomogenkan, kemudian
ditambahkan dengan 10 mL larutan 1,10-fenantrolin dan diaduk kembali hingga
homogen. Larutan didiamkan selama 10 menit sehingga di peroleh kompleks yang
berwarna merah jingga. Selanjutnya transmitansi larutan diukur dengan
spektrofotometer sinar tampak pada panjang gelombang 510 nm.
3.3.4.4 Penentuan Konsentrasi Fe setelah Penambahan Larutan Kitosan untuk
Variasi Konsentrasi
Sebanyak 80 mL larutan standar Fe 1 mg/L dimasukkan kedalam 5 buah gelas
Erlenmeyer berbeda dan ditambahkan 20 mL larutan kitosan dengan variasi
konsentrasi 0,2%; 0,4%; 0,6%; 0,8% dan 1% kemudian diaduk dengan kecepatan 200
Sebanyak 50 mL filtrat dimasukkan ke dalam erlenmeyer dan ditambahkan 1
mL hidroksilamin kemudian diaduk hingga homogen, lalu ditambahkan dengan 1 mL
larutan natrium asetat lalu dihomogenkan, kemudian ditambahkan dengan 10 mL
larutan 1,10-fenantrolin dan diaduk kembali hingga homogen. Larutan didiamkan
selama 10 menit sehingga di peroleh kompleks yang berwarna merah
jingga.Selanjutnya transmitansi larutan diukur dengan spektrofotometer sinar tampak
pada panjang gelombang 510 nm.
3.3.4.5 Penentuan Konsentrasi Fe setelah Penambahan Larutan Kitosan untuk
Variasi Lama Penyimpanan pada Suhu -230C
Larutan stok kitosan dengan konsentrasi 0,6% yang disimpan selama 1,2,3,4 dan 5
hari pada suhu -230C lalu kemudian dikondisikan pada suhu kamar. Sebanyak 80 mL
larutan standar Fe 1 mg/L dimasukkan kedalam Erlenmeyer, ditambahkan 20 mL
larutan stok kitosan, kemudian diaduk dengan kecepatan 200 rpm selama ± 30 menit.
Didiamkan selama 1 jam, kemudian disaring.
Sebanyak 50 mL filtrat dimasukkan ke dalam erlenmeyer dan ditambahkan 1
mL hidroksilamin kemudian diaduk hingga homogen, lalu ditambahkan dengan 1 mL
larutan natrium asetat lalu dihomogenkan, kemudian ditambahkan dengan 10 mL
larutan 1,10-fenantrolin dan diaduk kembali hingga homogen. Larutan didiamkan
selama 10 menit sehingga diperoleh kompleks yang berwarna merah jingga.
Selanjutnya transmitansi larutan diukur dengan spektrofotometer sinar tampak pada
panjang gelombang 510 nm.
3.3.4.6 Penentuan Konsentrasi Fe setelah Penambahan Larutan Kitosan untuk
Variasi Lama Penyimpanan pada Suhu Kamar
Sebanyak 80 mL larutan standar Fe 1 mg/L dimasukkan kedalam Erlenmeyer,
hari pada suhu kamar, kemudian diaduk dengan kecepatan 200 rpm selama ± 30
menit. Didiamkan selama 1 jam, kemudian disaring.
Sebanyak 50 mL filtrat dimasukkan ke dalam erlenmeyer dan ditambahkan 1
mL hidroksilamin kemudian diaduk hingga homogen, lalu ditambahkan dengan 1 mL
larutan natrium asetat lalu dihomogenkan, kemudian ditambahkan dengan 10 mL
larutan 1,10-fenantrolin dan diaduk kembali hingga homogen. Larutan didiamkan
selama 10 menit sehingga diperoleh kompleks yang berwarna merah jingga.
Selanjutnya transmitansi larutan diukur dengan spektrofotometer sinar tampak pada
panjang gelombang 510 nm.
3.3.5 Pengukuran Waktu Alir Larutan Kitosan pada Penentuan Viskositas
Untuk menentukan viskositas larutan digunakan alat Viskosimeter Ostwald,
pengukuran dilakukan pada suhu kamar.
1. Viskosimeter dibersihkan dan dikeringkan
2. Dimasukkan cairan kedalam viskosimeter
3. Cairan dihisap melalui pipa kapiler, sehingga cairan naik sampai batas atas
4. Penghisap dilepaskan,cairan dibiarkan turun, stopwatch dihidupkan pada saat
cairan berada pada garis batas atas, dan dihentikan pada saat permukaan tepat
melalui garis batas bawah
5. Waktu yang diperlukan cairan untuk mengalir dari batas atas ke batas bawah di
catat sebagai waktu alir
3.4 Bagan Penelitian
3.4.1 Penentuan Adsorpsi Larutan Kitosan untuk Variasi Konsentrasi
Larutan kitosan dengan konsentrasi
0,2%; 0,4%; 0,6%; 0,8%; 1,0%
Diukur 20 mL
Dimasukkan ke dalam erlenmeyer yang berisi
80 mL larutan standar Fe 1 mg/L
Diaduk dengan kecepatan 200 rpm selama
30 menit
Didiamkan selama 1 jam
Disaring
(Mat,B.Zakaria,1995)
Filtrat Residu
Diukur sebanyak 50 mL dan dimasukkan ke dalam erlenmeyer
Ditambahkan 1 mL hidroksilamin
Ditambahkan 1 mL larutan natrium asetat
Ditambahkan 10 mL 1,10-fenantrolin
Diaduk hingga homogen
Larutan merah jingga
Didiamkan selama 10 menit
Diukur dengan spektrofotometer visible pada λ= 510 nm
(Standar method,1980)
3.4.2 Penentuan Adsorpsi Larutan Kitosan untuk Variasi Lama Penyimpanan
pada Suhu -230C
Larutan kitosan konsentrasi 0,6 %
dengan lama penyimpanan 1,2,3,4 dan 5 hari
Dikondisikan pada suhu kamar
Diukur 20 mL
Dimasukkan ke dalam erlenmeyer yang berisi
80 mL larutan standar Fe 1 mg/L
Diaduk dengan kecepatan 200 rpm selama
30 menit
Didiamkan selama 1 jam
Disaring
Filtrat Residu
Diukur sebanyak 50 mL dan dimasukkan ke dalam erlenmeyer
Ditambahkan 1 mL hidroksilamin
Ditambahkan 1 mL larutan natrium asetat
Ditambahkan 10 mL 1,10-fenantrolin
Diaduk hingga homogen
Larutan merah jingga
Didiamkan selama 10 menit
Diukur dengan spektrofotometer visible pada λ= 510 nm
3.4.3 Penentuan Adsorpsi Larutan Kitosan untuk Variasi Lama Penyimpanan
pada Suhu Kamar
Larutan kitosan konsentrasi 0,6 %
dengan lama penyimpanan 1,2,3,4 dan 5 hari
Diukur 20 mL
Dimasukkan ke dalam erlenmeyer yang berisi
80 mL larutan standar Fe 1 mg/L
Diaduk dengan kecepatan 200 rpm selama
30 menit
Didiamkan selama 1 jam
Disaring
Filtrat Residu
Diukur sebanyak 50 mL dan dimasukkan ke dalam erlenmeyer
Ditambahkan 1 mL hidroksilamin
Ditambahkan 1 mL larutan natrium asetat
Ditambahkan 10 mL 1,10-fenantrolin
Diaduk hingga homogen
Larutan merah jingga
Didiamkan selama 10 menit
Diukur dengan spektrofotometer visible pada λ= 510 nm
3.4.4 Penentuan Viskositas Larutan Kitosan
(Yazid,Estein.2005)
Larutan kitosan
Diukur 10 mL
Dimasukkan ke dalam viskosimeter ostwald
Dihisap larutan melalui pipa kapiler, sehingga
naik sampai batas atas
Dilepaskan penghisap dan dihidupkan stopwatch
saat larutan mengalir batas atas sampai batas
bawah
Dicatat waktu alirnya
BAB 4
HASIL DAN PEMBAHASAN
4.1 Hasil Penelitian
Data hasil penentuan panjang gelombang, waktu operasi dan pengukuran absorbansi
dari suatu seri larutan standar besi diplotkan terhadap konsentrasi larutan standar
dapat dilihat pada tabel 1,2 dan 3 pada lampiran.
Data hasil pengukuran absorbansi ion Besi(Fe) untuk variasi konsentrasi dan lama
penyimpanan larutan kitosan dapat dilihat pada tabel 4.1, tabel 4.2 dan tabel 4.3.
Tabel 4.1 Data Hasil Pengukuran Transmitansi Ion Besi (Fe) untuk Variasi
Konsentrasi Larutan Kitosan
No Konsentrasi Larutan Kitosan
Transmitansi
%T1 %T2 %T3 % T A (2 – log%T)
1 0,2% 73 74 73 73,33 0,1347
2 0,4% 74 74 75 74,33 0,1288
3 0,6% 75 75 74 74,67 0,1269
4 0,8% 74 72 73 73 0,1367
Tabel 4.2 Data Hasil Pengukuran Trasmitansi Ion Besi (Fe) untuk Variasi Lama
Tabel.4.3. Data Hasil Pengukuran Transmitansi Ion Besi (Fe) untuk Variasi Lama
Penyimpanan Larutan Kitosan pada Suhu Kamar
4.2 Pengolahan Data
4.2.1 Penurunan Persamaan Garis Regresi dengan Metode Kurva Kalibrasi
Hasil pengukuran transmitansi dari suatu seri larutan standar besi yang digunakan
A = 2 – log %T
Selanjutnya absorbansi dialurkan terhadap konsentrasi larutan standar sehingga
diperoleh suatu kurva kalibrasi berupa garis linier (gambar 1) dapat dilihat pada
lampiran. Persamaan garis regresi untuk kurva kalibrasi ini dapat diturunkan dengan
metode Least Square sebagai berikut :
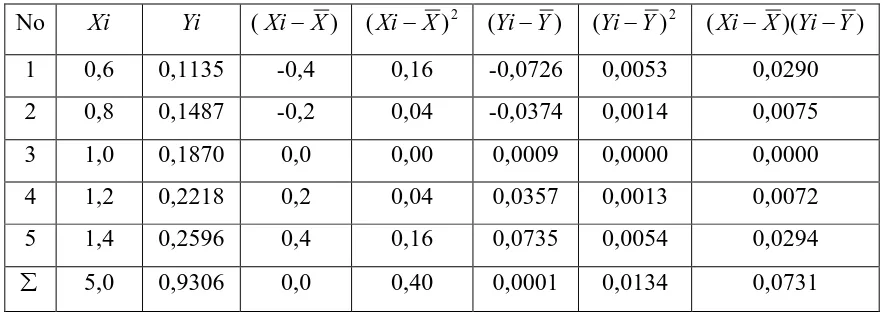
Tabel 4.4 Data Hasil Penurunan Persamaan Regresi untuk Fe
No Xi Yi (Xi−X) (Xi−X)2 (Yi−Y) (Yi−Y)2 (Xi−X)(Yi−Y)
Dimana harga X rata-rata :
n
4.2.2 Penurunan Persamaan Garis Regresi
Persamaan garis regresi untuk kurva kalibrasi dapat diturunkan dari persamaan garis :
y = ax + b
Sehingga diperoleh harga a :
Harga intersept (b) diperoleh melalui substitusi harga (a) ke persamaan berikut :
y = ax + b
b = y – ax
= 0,1861- (0,1828 x 1)
= 0,0033
Maka persamaan garis regresi yang diperoleh adalah :
y = 0,1828 x + 0,0033
4.2.3 Koefisien Korelasi
Koefisien korelasi (r) dapat ditentukan sebagai berikut :
r =
Dengan mensubstitusi harga konsentrasi larutan standar (Xi) ke persamaan garis
regresi maka diperoleh harga Y yang baru (Y )seperti tercantum dalam tabel :
Tabel 4.5. Data Hasil Perhitungan Korelasi untuk Besi
Dari perhitungan pada tabel diatas maka dapat ditentukan deviasi standar untuk
intersept (Sb) yaitu dengan persamaan:
Sb =
Harga Sb dihitung untuk menentukan batas kepercayaan nilai intersept yaitu b ± t
(Sb), dimana t diperoleh dari tabel t-distribusi dengan derajat kepercayaan 95% dan
derajat kebebasan (n-2) = 5-2 = 3 diperoleh p = 0,05 dan t = 3,18 sehingga batas
kepercayaan untuk nilai intersept adalah :
0,0033 ± (3,18)(1,4915 x 10-3)
0,0033 ± 4,7430 x 10-3
0,0033 ± 0,0047
Sa =
Sesuai dengan cara untuk menentukan batas kepercayaan nilai intersept maka
kepercayaan nilai slope adalah a ± t (Sa),
0,1828 ± (3,18)(1,5502 x 10-3)
0,1828 ± 4,9296 x 10-3
0,1828 ± 0,0049
4.2.4 Penentuan Batas Deteksi
Batas deteksi dapat dihitung dengan persamaan :
3Sb = Y – Yb
atau, Y = 3Sb + Yb
Dimana : Y = signal pada batas kadar deteksi
Sb = standar deviasi
Yb = Intersept kurva kalibrasi
Persamaan kurva kalibrasi, Y = 0,1828 x + 0,0033
Dimana, Yb = 0,0033
Sb =
x
Maka dengan mensubstitusikan harga Yb dan Sb pada persamaan Y = 3Sb + Yb dapat
diperoleh harga untuk batas deteksi :
Y = 3Sb + Yb
= 3(0,9434 x 10-3) + 0,0033
= 0,0028 + 0,0033
= 0,0061
Dengan mensubstitusi nilai Y terhadap persamaan :
Y = 0,1828x + 0,0033
0,0061 = 0,1828x + 0,0033
0,0028 = 0,1828x
x = 0,0153 mg/L
Jadi, batas deteksi pengukuran besi untuk penelitian ini adalah 0,0153 mg/L.
4.2.5 Penentuan Kadar Besi (Fe) setelah Penambahan Kitosan
Kadar Besi dapat ditentukan dengan menggunakan metode kurva kalibrasi dengan
mensubstitusikan nilai Y (absorbansi) yang diperoleh dari hasil pengukuran terhadap
persamaan garis regresi dari kurva kalibrasi.
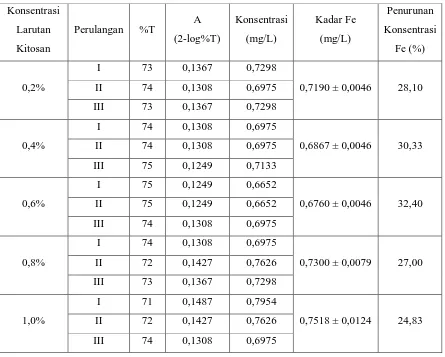
Dari data pengukuran % transmitansi Besi untuk variasi konsentrasi larutan kitosan
0,2%, diperoleh sebagai berikut :
%T1 =73 A1 = 0,1367
%T2 = 74 A2 = 0,1308
%T3 = 73 A3 = 0,1367
Dengan mensubstitusikan nilai Y (absorbansi) ke persamaan garis regresi berikut :
X1 = 0,7298
X2 = 0,6975
X3 = 0,7298
Dengan demikian kadar Besi untuk variasi konsentrasi larutan kitosan 0,2% adalah :
n Xi
X =Σ = 0,7190
Kemudian dihitung deviasi standar sebagai berikut :
2
Dari data hasil distribusi t student untuk n=3, derajat kebebasan (dk) = n-1 = 2
Untuk derajat kepercayaan 95% (p=0,05), t=4,30.
Maka, d = t(0,05xn−1)Sx
d = 4,30 x 0,1 x 0,0108
d = 0,0046
Dari data hasil pengukuran kadar Besi untuk variasi konsentrasi larutan kitosan 0,2%
adalah sebesar:
Dengan cara yang sama dapat ditentukan konsentrasi ion Besi (Fe) untuk variasi
konsentrasi dan lama penyimpanan larutan kitosan. Data dapat dilihat pada tabel 4,
tabel 5 dan tabel 6 pada lampiran.
4.2.6 Persentasi (%) Penurunan Konsentrasi Ion Besi (Fe)
Data hasil percobaan yang diperoleh ditunjukkan dalam tabel 4, tabel 5 dan tabel 6
dalam lampiran.
Persen penurunan kadar besi diperoleh dari hasil perhitungan dengan rumus sebagai
berikut :
Persen penurunan =
[ ] [
]
[ ]
x100% awal4.3 Pembahasan
Dari hasil penelitian yang dilakukan diperoleh panjang gelombang maksimum (λ maks) dari pembentukan warna kompleks merah jingga untuk larutan standar 0,6
mg/L besi sebesar 510 nm. Metode penentuan panjang gelombang maksimum larutan standar besi dilakukan pada λ = 510 nm.
Pengukuran dengan spektrofotometer sinar tampak perlu dilakukan
pengukuran khusus untuk menentukan waaktu operasi yaitu pada saat mana suatu
larutan berwarna mencapai transmitansi minimum atau absorbansi maksimum. Waktu
operasi kompleks warna dari larutan standar 0,6 mg/L besi diperoleh dengan waktu 10
menit. Jadi waktu operasi ini merupakan selang waktu antara saat penambahan
pereaksi hidroksilamin, larutan natrium asetat dan 1,10-fenantrolin dengan waktu saat
intensitas warna mencapai maksimum.
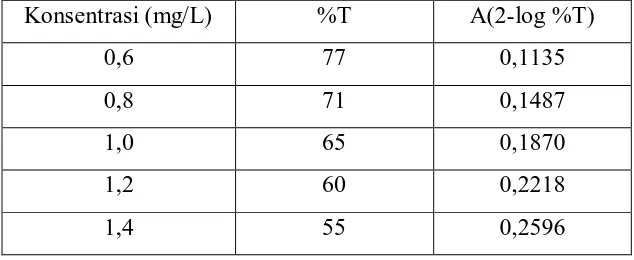
Kurva kalibrasi larutan standar besi (Tabel 3), dibuat dengan memvariasikan
konsentrasi larutan standar besi dengan menggunakan persamaan Least Square
diperoleh persamaan garis Y =0,1828X +0,0033 dengan grafik pada gambar 1.
Dalam penentuan apakah suatu penelitian memiliki titik yang sejajar pada
kurva kalibrasi dengan harga slope positif dapat dilihat dari perhitungan koefisien
korelasi (r). Dalam data statistik diperoleh harga koefisien korelasi sebesar 0,9986.
Hal ini menunjukkan adanya hubungan atau korelasi positif antara konsentrasi dengan
absorbansi. Pada penelitian analitik, grafik kurva kalibrasi yang baik ditunjukkan
dengan harga r ≥0,99 (Miller J.C.,Miller,J.N,1986).
Penentuan batas deteksi dari pengukuran kadar besi dalam penelitian ini
adalah 0,0153 mg/L. Hal ini menunjukkan batas pengukuran alat spektrofotometer
untuk kadar besi dalam sampel hanya dapat dilakukan jika konsentrasi besi diatas
0,0153 mg/L.
Dari hasil penelitian yang dilakukan terjadi penurunan kadar besi setelah
larutan kitosan, dimana konsentrasi awal larutan standar besi yang digunakan adalah 1
mg/L. Setelah penambahan larutan kitosan dengan variasi konsentrasi 0,2%; 0,4%;
0,6%; 0.8% dan 1 % diperoleh konsentrasi akhir larutan besi masing-masing sebesar
0,7190 mg/L; 0,6867 mg/L; 0,6760 mg/L; 0,7300 mg/L dan 0,7518 mg/L. Dengan
persen penurunan masing-masing sebesar 28,10%; 30,33%; 32,40%; 27,00% dan
24,83%. Dari data diperoleh bahwa penyerapan optimum dari larutan kitosan adalah
pada penambahan kitosan dengan konsentrasi 0,6% yakni sebesar 32,40%.
Penurunan konsentrasi besi setelah penambahan kitosan disebabkan karena
kitosan mengikat logam melalui pertukaran ion, penyerapan dan pengkhelatan
(Muzarelli,R.A.A,1977). Kitosan mempunyai satu kumpulan amino linier untuk setiap
unit glukosa. Kumpulan amino ini mempunyai sepasang elektron yang dapat
berkoordinat atau membentuk ikatan-ikatan aktif dengan kation-kation logam. Unsur
nitrogen dari setiap monomer kitosan dikatakan sebagai gugus aktif berkoordinat
dengan logam (Hutahaean,S.Ida,2001).
Besi merupakan akseptor elektron yang menurut lewis digolongkan sebagai
asam. Ditinjau dari kekuatan asam, Pearson dalam teori HSAB (Hard Soft Acid Base),
besi digolongkan kedalam asam antara artinya logam ini akan mampu berinteraksi
dengan baik terhadap basa kuat seperti OH-,RNH2 dan R-OH (Hancock dan
Martel,1996). Dengan demikian memungkinkan pengambilan Fe(II) atau Fe(III)
melalui mekanisme adsorpsi dengan adsorben yang memiliki gugus fungsional dan
bersifat basa lewis seperti yang dimiliki oleh kitosan.
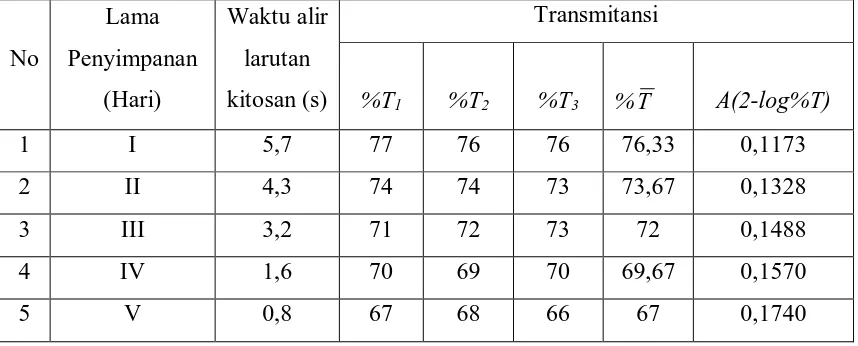
Untuk penambahan larutan kitosan dengan variasi lama penyimpanan pada
hari I, II, III, IV dan V dalam lemari pendingin pada suhu -23oC untuk konsentrasi
optimumnya, diperoleh konsentrasi akhir masing-masing sebesar 0,6236 mg/L; 0,6548
mg/L; 0,7083 mg/L; 0,7517 mg/L dan 0,7958 mg/L. Dengan persen penurunan
sebesar 37,64%; 34,52%; 29,17%; 24,83% dan 20,42% . Sedangkan pada suhu kamar,
diperoleh konsentrasi larutan besi yang tersisa adalah 0,6236 mg/L; 0,7082 mg/L;
0,7626 mg/L; 0,8408 mg/L dan 0,9336 mg/L. Dengan persen penurunan
Dari data diperoleh bahwa larutan kitosan didapati menurun setelah pada
hari-hari berikutnya, baik ketika larutan kitosan tersebut disimpan pada suhu -23oC
maupun pada suhu kamar. Pada larutan kitosan yang disimpan pada suhu kamar
terjadi penurunan viskositas maupun daya adsorpsi yang cukup besar dari kitosan
dibanding pada suhu -230C. Hal ini terjadi karena larutan kitosan yang disimpan pada
suhu kamar lebih mudah terdegradasi dibanding pada suhu -230c.
Kelarutan kitosan dalam larutan asam asetat dipengaruhi oleh suhu. Adanya
gugus karboksil(-COOH) dalam asam asetat akan memudahkan pelarutan kitosan
karena terjadinya interaksi hidrogen antara gugus karboksil dengan gugus amina dari
kitosan. (Dunn el al.1997). Dalam suasana ini, gugus amina bebas sangat cocok
sebagai polikationik untuk mengekelat logam. Semakin lama kitosan kontak dengan
asam asetat memungkinkan gugus amina dari kitosan akan terprotonasi membentuk
gugus amino kationik (NH3+), sehingga muatan positif kitosan juga akan semakin
banyak. Dalam larutan, tingginya muatan positif akan menghasilkan gaya tolak
menolak. Suhu rendah dapat menghambat terprotonasinya gugus amina di dalam
BAB 5
KESIMPULAN DAN SARAN
5.1 Kesimpulan
Dari data yang diperoleh pada penelitian ini, didapat bahwa konsentrasi larutan
kitosan yang paling optimal untuk adsorpsi besi adalah pada konsentrasi larutan
kitosan 0,6% dimana yang teradsorpsi adalah sebesar 32,40%. Lama penyimpanan
larutan kitosan mempengaruhi daya adsorpsinya terhadap logam, dimana semakin
lama waktu penyimpanan larutan kitosan maka viskositas larutan kitosan tersebut
akan semakin menurun seiring kemampuannya untuk mengadsorpsi besi semakin
lama juga semakin kecil. Hal ini ditunjukkan dengan persentasi (%) adsorpsi besi
setiap harinya semakin lama semakin kecil, baik yang disimpan pada suhu -230C
maupun pada suhu kamar.
5.2 Saran
Perlu adanya penelitian lebih lanjut untuk membandingkan bagaimana daya adsorpsi
kitosan terhadap logam lainnya selain dari besi, jika divariasikan konsentrasi maupun
DAFTAR PUSTAKA
Alaert,G. 1987. Metoda Penelitian Air. Surabaya : Usaha Nasional. Almatsier,S. 2003. Prinsip Dasar Ilmu Gizi. Yakarta : UI Press.
Dean,R.B. 1981. Water Reuse: problem and solution. London: Academic Press Inc. Dunn,ET.EW. Grandmaison dan MFA. Goosen. 1997. Aplication and Properties of
Chitosan. Di dalam MFA. Goosen (ed). Applications of Chitin and Chitosan. Technomic Pub,Basel.
Effendi,H. 2003. Telaah Kualitas Air. Yogyakarta: Penerbit Kanisius.
Ewing,G.W. 1975. Instrumental Methods of Chemical Analysis.New York: Mc.Graw- Hill.
Glastone,S. 1959. Physical Chemistry. Second Edition. New York: Van Nostrand Company Inc.
(Http:// resources.unpad.ac.id/unpad-content/upload/publikasi_dosen/makalah 6. Viskositas).Diakses 10 juni,2009.
Hardjito,L. 2006. Chitosan Sebagai Bahan Pengawet Pengganti Formalin.Majalah Pangan : Media Komunikasi dan Informasi. No 46/XV/Januari/2006. Hutahaean,I.S. 2001. Penggunaan Kitosan Sebagai Penyerap Logam Zinkum(Zn2+)
Dan Logan Kromium(Cr3+) dengan Metode Spektrofotometri Serapan atom. Skripsi. Medan: Jurusan Kimia FMIPA USU.
Jae Kwan Hwang dan Hae Hun Shin. 2001. Rheological Properties of Chitosan Solutions. Korea-Australia Rheology Jurnal.
Kumar,M.N.V.R. 2000. A Review of Chitin and Chitosan Applications. India: Department of Chemistry, University of Roorkee.
Lowry,T.M. 1958. Intermediate Chemistry. London: Macmillan & CO LTD. Mat,B.Zakaria. 1995.Chitin and Chitosan. University Kebangsaan Malaysia.
Miller,J.C.,Miller,J.N.1986.Statistika untuk kimia analitik.Edisi Kedua. Bandung: ITB Press.
Mulja.1999.analisis Instrument. Jakarta : Erlangga.
Muzzarelly, R.A.A. 1977. Chitin. New York. Oxford: Perngamon Press. Rismana, E. 2004. Serat Kitosan Mengikat Lemak.
Diakses tanggal 29 Februari, 2009.
Robert,G.A.F. 1992. Chitin Chemistry.London : The Macmillan Press.
Stevens,M.P. 2001.Kimia Polimer. Cetakan pertama. Jakarta: Pradnya Paramita. Standard Methods for the Examination of Water and Wastewater. 1980. Washington: APHA,AWWA,WPCF. 15th ed.
Vinvogadro,A.P. 1971. Elementary Chemical Composition of Marine Organism. Moscow: A.V.USSR.
Vogel. 1990. Analisis Anorganik Kualitatif Makro dan Semimikro. Jakarta : PT. Kalman Media Pusaka.
Vogel. 1994. Kimia Analisis Kuantitatif Anorganik. Edisi 4. Jakarta : Penerbit Buku Kedokteran.
Widowati,W. 2008. Efek toksik Logam. Yogyakarta : Penerbit ANDI. Wirjosentono, B. 1995. Analisis dan Karakteristik Polimer. Edisi Pertama.
Tabel 1. Penentuan Panjang Gelombang Maksimum dari Larutan Standar 0,6 mg/L Besi
Panjang Gelombang
(nm) %T A(2-log %T)
480 80 0,0969
490 78 0,1079
500 77 0,1135
510 76 0,1191
520 78 0,1079
Tabel 2. Penentuan Waktu Operasi dari Larutan Standar 0,6 mg/L Besi
Waktu (menit) %T A(2-log %T)
5 83 0,0809
10 77 0,1135
15 78 0,1079
20 81 0,0915
25 82 0,0861
Tabel 3. Penentuan Kurva Kalibrasi Standar Besi (Fe)
Konsentrasi (mg/L) %T A(2-log %T)
0,6 77 0,1135
0,8 71 0,1487
1,0 65 0,1870
1,2 60 0,2218