PEMANFAATAN LIMBAH TANDAN KOSONG
KELAPA SAWIT DAN AZOLA MENJADI
KOMPOS PUPUK TABLET
TESIS
Oleh :
AHMAD DAHYAR
087006008 / KM
ILMU KIMIA
SEKOLAH PASCA SARJANA
UNIVERSITAS SUMATERA UTARA
PEMANFAATAN LIMBAH TANDAN KOSONG
KELAPA SAWIT DAN AZOLLA MENJADI
KOMPOS PUPUK TABLET
TESIS
Diajukan Sebagai Salah Satu Syarat Untuk Memperoleh Gelar Magister Sains Dalam Program Studi Ilmu Kimia Pada Fakultas Matematika Dan Ilmu Pengetahuan Alam
Universitas Sumatera Utara
Oleh
AHMAD DAHYAR
087006008/KIM
PROGRAM PASCASARJANA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS SUMATERA UTARA
Judul : PEMANFAATAN LIMBAH TANDAN KOSONG KELAPA SAWIT DAN AZOLLA MENJADI KOMPOS PUPUK TABLET
Nama Mahasiswa : AHMAD DAHYAR
N I M : 087006008
Program Studi : Magister Ilmu Kimia
Menyetujui Komisi Pembimbing :
(Dr. Hamonangan Nainggolan, MSc) (Dra. Emma Zaidar, Msi)
Ketua Anggota
Mengetahui,
Ketua Program Studi Dekan FMIPA USU
(Prof. Basuki Wirjosentono, MS, Ph.D) (Prof. Dr. Eddy Marlianto, M.Sc)
Telah diuji pada Tanggal 17 Mei 2010
Panitia Penguji Tesis
Ketua : Dr. Hamonangan Nainggolan, M.Sc Anggota : 1. Dra. Emma Zaidar, M.Si
2. Prof. Basuki WIrjosentono, MS. Ph.D 3. Prof. Dr. Harry Agusnar, M.Sc.M,Phil 4. Dr. Minto Supeno, MS
PERNYATAAN
PEMANFAATAN LIMBAH TANDAN KOSONG
KELAPA SAWIT DAN AZOLLA MENJADI
KOMPOS PUPUK TABLET
TESIS
Dengan ini saya menyatakan bahwa dalam tesis ini tidak terdapat karya yang
pernah diajukan untuk memperoleh gelar kesarjanaan di suatu Perguruan Tinggi dan
sepanjang pengetahuan saya juga tidak terdapat karya atau pendapat yang pernah
ditulis atau diterbitkan oleh orang lain, kecuali secara tertulis diacu dalam naskah dan
disebutkan dalam daftar pustaka.
Medan, Mei 2010 Penulis
PEMANFAATAN LIMBAH TANDAN KOSONG KELAPA SAWIT DAN AZOLLA MENJADI KOMPOS PUPUK TABLET
ABSTRAK
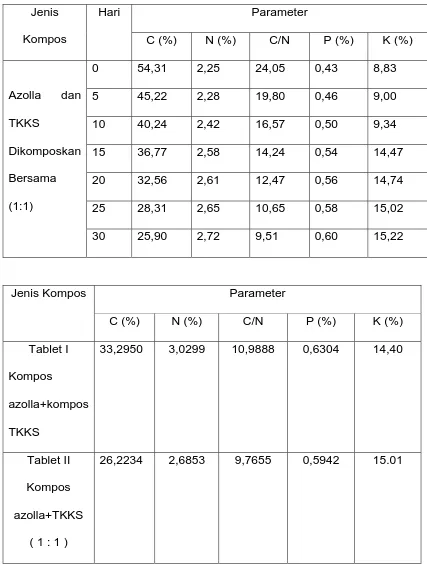
Telah dilakukan penelitian tentang pemanfaatan Tandan Kosong Kelapa Sawit (TKKS) dan azolla menjadi kompos pupuk tablet.Penelitian dilakukan dengan mengkomposkan masing-masing TKKS dan azolla, selama 30 hari dengan menggunakan activator EM4 ( effective microopganisms 4 ). Untuk mengetahui kadar unsur hara C, N, P dan K kompos dilakukan analisa selama berlangsungnya pengomposan dengan variasi waktu 0, 5, 10, 15, 20, 25, dan 30 hari. Dari analisa tablet kompos C/N kompos azolla + kompos TKKS adalah 10,9888, Kadar C=33,2950%, Kandungan hara makro N=3,0299%, P=0,6304%, dan K=14,405% menunjukkan tablet kompos ini telah memenuhi Standar Nasional Indonesia SNI 19-7030-2004. Untuk analisa tablet kompos azolla + TKKS (1:1 ) C/N = 9,7655, kandungan unsure hara N=2,6853%, P=0,5942%, dan K=15,01%. Dari rasio C/N sedikit dibawah Standar Nasional Indonesia SNI 19-7030-2004.
Kata Kunci :Tandan Kosong Kelapa Sawit, Azolla, Kompos, Pupuk Tablet,
Effective Microorgansms, rasio C/N.
THE USES OF PALM OIL EMPTY BUNCHES
AND AZOLLA BECOME TABLET COMPOST
ABSTRACT
It has been conducted a research on the uses of palm-oil empty bunches (TKKS) and the azolla to become compost fertilizer on tablet. The research was done by composting each TKKS and azolla for 30 days there using EM4 (Effective micro-organism 4) activator. In order to measure the content of manure element C, N, P and K compost there were conducted an analysis during the compost taking place with the time variety of 0, 5, 10, 15, 20, 25, and 30 days. By the compost tablet analysis C/N compost azolla + TKKS compost noted 10.9888, its content C=33.2950%, the content of macro manure N=3.0299%, P=0.6304%, and K=14.405% showed this compost table has already fulfilled the Indonesian National Standard Rate SNI 19-7030-2004. For analysis of compost table azolla + TKKS (1:1) C/N = 9.7655, the content of manure element N=2.6853%, P=0.5942%, and K=15.01%. For the C/N ratio is noted lower under Indonesian National Standard rate SNI 19-7030-2004.
Keywords : Palm-oil empty bunches, Azolla, Compost, pellet fertilizer,
KATA PENGANTAR AR
Puji dan syukur penulis panjatkan kehadirat Tuhan Yang Maha Kuasa atas
segala Rahmat dan Karunia yang telah diberikannya kepada penulis sehingga tesis ini
dapat diselesaikan.
Puji dan syukur penulis panjatkan kehadirat Tuhan Yang Maha Kuasa atas
segala Rahmat dan Karunia yang telah diberikannya kepada penulis sehingga tesis ini
dapat diselesaikan.
Penulis mengucapkan terimakasih yang sebesar-besarnya kepada Pemerintah
Provinsi Sumatera utara c.q. BAPEDA Sumatera Utara, Pemerintah Kota medan dan
Dinas Pendidikan Kota Medan yang telah memberikan bantuan finansial dan surat
izin belajar bagi penulis selama mengikuti perkuliahan hingga menyelasaikan tesis
ini.
Penulis mengucapkan terimakasih yang sebesar-besarnya kepada Pemerintah
Provinsi Sumatera utara c.q. BAPEDA Sumatera Utara, Pemerintah Kota medan dan
Dinas Pendidikan Kota Medan yang telah memberikan bantuan finansial dan surat
izin belajar bagi penulis selama mengikuti perkuliahan hingga menyelasaikan tesis
ini.
Penulis juga mengucapkan terimakasih yang sebesar-besarnya kepada : Rektor
Universitas Sumatera Utara, Bapak Prof.Dr.dr. Syahril Pasaribu DTM & H. M.Sc
(CTM), Sp.A(K) atas kesempatan dan fasilitas yang diberikan kepada penulis untuk
menyelesaikan Program magister. Ucapan terimakasih juga penulis sampaikan
kepada Dekan FMIPA USU Bapak Prof. DR.Eddy Marlianto, M.Sc, dan Direktur
Sekolah Pascasarjana, Ibu Prof. Dr. Ir. T.Chairunnisa B, serta ketua program studi
kimia, Bapak Prof. Basuki Wirjosentono,MS, PhD. Atas kesempatan yang telah
diberikan kepada penulis untuk menjadi Mahasiswa Program Magister pada sekolah
Pascasarjana Universitas Sumatera Utara.
Penulis juga mengucapkan terimakasih yang sebesar-besarnya kepada : Rektor
Universitas Sumatera Utara, Bapak Prof.Dr.dr. Syahril Pasaribu DTM & H. M.Sc
(CTM), Sp.A(K) atas kesempatan dan fasilitas yang diberikan kepada penulis untuk
menyelesaikan Program magister. Ucapan terimakasih juga penulis sampaikan
kepada Dekan FMIPA USU Bapak Prof. DR.Eddy Marlianto, M.Sc, dan Direktur
Sekolah Pascasarjana, Ibu Prof. Dr. Ir. T.Chairunnisa B, serta ketua program studi
kimia, Bapak Prof. Basuki Wirjosentono,MS, PhD. Atas kesempatan yang telah
diberikan kepada penulis untuk menjadi Mahasiswa Program Magister pada sekolah
Pascasarjana Universitas Sumatera Utara.
Terimakasih yang sebesar-besarnya dan yang setinggi-tingginya penulis ucapkan
kepada :
Terimakasih yang sebesar-besarnya dan yang setinggi-tingginya penulis ucapkan
kepada :
1. Bapak Dr. Hamonangan Naingolan, MSc. Selaku dosen pembimbing Utama dan
ibu Dra. Emma Zaidar, MSi. Selaku anggota pembimbing utama yang setiap saat
dengan penuh perhatian dan selalu menyediakan waktu untuk memberikan
bimbingan,saran dan motivasi sehingga tesis ini dapat terselesaikan.
1. Bapak Dr. Hamonangan Naingolan, MSc. Selaku dosen pembimbing Utama dan
ibu Dra. Emma Zaidar, MSi. Selaku anggota pembimbing utama yang setiap saat
dengan penuh perhatian dan selalu menyediakan waktu untuk memberikan
bimbingan,saran dan motivasi sehingga tesis ini dapat terselesaikan.
2. Bapak Prof.Basuki Wirjosentono, MS. PhD, Bapak Prof.Dr.Harry Agusnar,
Bapak Dr.Minto Supeno, MS Selaku dosen pembanding yang telah banyak
memberikan saran dan masukan dalam penulisan tesis ini
2. Bapak Prof.Basuki Wirjosentono, MS. PhD, Bapak Prof.Dr.Harry Agusnar,
Bapak Dr.Minto Supeno, MS Selaku dosen pembanding yang telah banyak
memberikan saran dan masukan dalam penulisan tesis ini
3. Ibu dan mertua serta saudara-saudara penulis yang telah memberikan dukungan
kepada penulis selama mengikuti perkuliahan pada program magister di Sekolah
Pascasarjana USU.
4. Istri Saya Dra.Alfita Hanim Lubis, yang dengan penuh kesabaran memberi
semangat ,dorongan dengan setia mendampingi penulis dan juga kedua buah hati
penulis ananda tercinta Aisyah Putri Nabilah dan Muhammad Dzakwan Habibi
yang merupakan semangat dan motivator bagi penulis selama mengikuti program
Pascasarjana.
5. Bapak dan ibu dosen Program Pascasarjana, jurusan kimia yang telah banyak
memberikan ilmu dan motivasi bagi penulis.
6. Bapak kepala sekolah SMA 3 negeri Medan, Drs. Sahlan Daulay.MPd, yang telah
memberikan rekomendasi dan motvasi kepada penulis selama mengikuti program
Pascasarjana di USU
7. Rekan-rekan guru SMAN 3 medan khususnya Bapak Drs.Simon Manurung, MSi
dan teman-teman yang mengikuti program Pascasarjana di USU Medan.
Penulis menyadari bahwa tesis ini masih banyak kekurangan dan masih jauh dari
sempurna, oleh karena itu sangat mengharapkan kritik dan saran demi kesempurnaan
tesis ini. Akhirnya penulis berharap bahwa tesis ini dapat bermanfaat bagi penelitian
dan kemajuan ilmu pengetahuan.Amin.
Hormat Penulis
RIWAYAT HIDUP HIDUP
Penulis dilahirkan di Desa Tanggabosi, Kecamatan Siabu, Kabupaten
Mandailing Natal pada tanggal 2 Pebruari 1964, anak ke delapan dari 9 bersaudara
pasangan dari Imam Mahiddin Nasution dan Hj.Satiah Batubara.Penulis mempunyai
2 anak sebagai buah hati yaitu Aisyah Putri Nabilah Nasution dan Muhammad
Dzakwan Habibi Nasution hasil pernikahan dengan istri tercinta Dra. Alfita Hanim
Lubis.
Penulis dilahirkan di Desa Tanggabosi, Kecamatan Siabu, Kabupaten
Mandailing Natal pada tanggal 2 Pebruari 1964, anak ke delapan dari 9 bersaudara
pasangan dari Imam Mahiddin Nasution dan Hj.Satiah Batubara.Penulis mempunyai
2 anak sebagai buah hati yaitu Aisyah Putri Nabilah Nasution dan Muhammad
Dzakwan Habibi Nasution hasil pernikahan dengan istri tercinta Dra. Alfita Hanim
Lubis.
Penulis menjalani masa pendidikan di SD Negeri no 2 Tanggabosi tamat tahun 1976,
SMP Negeri Huraba tamat tahun 1980, SMA Negeri Medan tamat tahun
1983.Kemudian melanjutkan pendidikan pada IKIP negeri medan jurusan
Pendidikan Kimia FPMIPA dan tamat tahun 1989.
Penulis menjalani masa pendidikan di SD Negeri no 2 Tanggabosi tamat tahun 1976,
SMP Negeri Huraba tamat tahun 1980, SMA Negeri Medan tamat tahun
1983.Kemudian melanjutkan pendidikan pada IKIP negeri medan jurusan
Pendidikan Kimia FPMIPA dan tamat tahun 1989.
Setelah tamat dari IKIP , penulis mengajar di sekolah SMA swasta di Yayasan
Perguruan Islam Sutan Oloan Medan dari tahun 1989 sampai tahun 1998.Penulis di
angkat jadi guru Pegawai negeri Sipil golongan III / A di SMA negeri 1 Bohorok 1
desember 1995 sampai tahun 2007.
Setelah tamat dari IKIP , penulis mengajar di sekolah SMA swasta di Yayasan
Perguruan Islam Sutan Oloan Medan dari tahun 1989 sampai tahun 1998.Penulis di
angkat jadi guru Pegawai negeri Sipil golongan III / A di SMA negeri 1 Bohorok 1
desember 1995 sampai tahun 2007.
Pada April 2007 penulis mutasi tugas ke SMAN 3 medan sampai dengan sekarang.
Pada bulan Juli tahun 2008, penulis melanjutkan pendidikan program magister di
sekolah Pasca sarjana Universitas Sumatera Utara yang di biayai oleh Pemerintah
Provinsi Sumatera Utara melalui BAPEDA Sumatera utara.
Pada April 2007 penulis mutasi tugas ke SMAN 3 medan sampai dengan sekarang.
Pada bulan Juli tahun 2008, penulis melanjutkan pendidikan program magister di
sekolah Pasca sarjana Universitas Sumatera Utara yang di biayai oleh Pemerintah
Provinsi Sumatera Utara melalui BAPEDA Sumatera utara.
2.7.2. Parameter yang Dapat Diamati Sebagai Petunjuk
Sempurnanya Proses Pengomposan Sebagai Berikut 12
2.7.3. Proses Pengomposan 13
2.7.4. Menentukan Kematangan Kompos 15
2.7.5. Meningkatkan Kesuburan Tanah 16
3.3.2. Penyediaan Sampel Tandan Kosong Kelapa Sawit (TKKS) 20
3.3.3 Pembuatan Starter Effective Microorganism 4 (EM4) 21
3.3.4. Pembuatan Kompos 21
3.3.4.1 Kompos Azolla 21
3.3.4.2. Kompos TKKS 21
3.3.4.3. Kompos Azolla + TKKS (1:1) 22
3.3.4.4. Pembuatan Tabel Kompos 22
3.3.5 Pembuatan Pereaksi dan Larutan Standar 23
3.3.5.1.Pembuatan Pereaksi dan Larutan standar untuk
penentuan Posfor sebagai P2O5 Metode
Spektrofotometri 23
3.3.5.2 Pembuatan Pereaksi untuk Penentuan C – Organik 24
3.3.5.3 Pembuatan Pereaksi untuk Penentuan Nitrogen
Metode Kjehldahl 25
3.3.5.4 Pembuatan Pereaksi Untuk Penentuan Kalium
sebagai K2O Dengan Metode 27
3.3.6. Penentuan P-Total Metode spektrofometri 27
3.3.6.1 Preparasi Sampel 27
3.3.6.2 Pembuatan Kurva Kalibrasi 28
3.3.6.3 Penentuan Kadar Posfor pada Sampel 28
3.3.7. Penentuan Kadar C -Organik dengan metode
Walkey Black 28
3.3.8 Pengukuran Nitrogen dengan Metode Kjehdahl 29
3.3.9 Penentuan Kalium sebagai K2O Dengan Metode
Spektrofotometer Serapan Atom (SSA) 30
3.4 Bagan Penelitian 31
3.4.1 Pembuatan Kompos 31
3.4.1.1.Pembuatan Starter EM4 31
3.4.1.2 Pembuatan kompos Azolla 32
3.4.1.3 Pembuatan kompos TKKS 33
3.4.1.4 Pembuatan tablet kompos azolla dan kompos TKKS 34
3.4.1.5. Bagan Pembuatan Kompos Azolla + TKKS (1:1)
Serta Pembuatan Tablet 35
3.4.2 Penentuan C – Organik 36
3.4.3. Penentuan Posfor sebagai P2O5 Metode Spektrofotometri 37
3.4.3.1 Pengekstrakan Azolla 37
3.4.2.2.Pengukuran Absorbansi dari Larutan Standar P
untuk kurva Kalibrasi Untuk Larutan standar 2 ppm 38
3.4.2.3 Pengukuran Absorbansi untuk Ekstrak Azola 39
3.4.4 Penentuan Kadar Nitrogen Azolla 40
3.4.5 Penentuan Kalium sebagai K2O dengan Metode
Spektrofotometer Serapan Atom 41
BAB IV HASIL DAN PEMBAHASAN
4.1 Hasil Penelitian 42
4.1.1 Data Analisa Pengomposan Azolla 42
4.1.2 Data Analisa Pengomposan TKKS 44
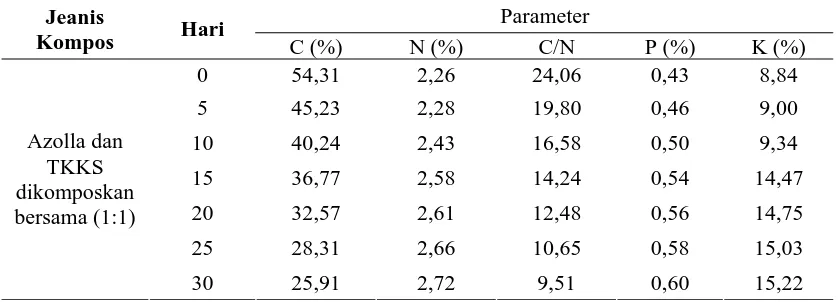
4.1.3 Data Analisa Pengomposan Azolla dan TKKS (1:1) 46
BAB V KESIMPULAN DAN SARAN
5.1 Kesimpulan 49
5.2 Saran 49
DAFTAR PUSTAKA LAMPIRAN - LAMPIRAN
DAFTAR GAMBAR
Gambar 4.1. Kurva Perubahan Konsetrasi C, N, C/N. P dan K dari Azolla Gambar 4.1. Kurva Perubahan Konsetrasi C, N, C/N. P dan K dari Azolla
Selama Pengomposan 43
Selama Pengomposan 43
Gambar 4.2. Kurva Perubahan Konsetrasi C, N, C/N. P dan K dari TKKS Gambar 4.2. Kurva Perubahan Konsetrasi C, N, C/N. P dan K dari TKKS
Selama Pengomposan 45
Selama Pengomposan 45
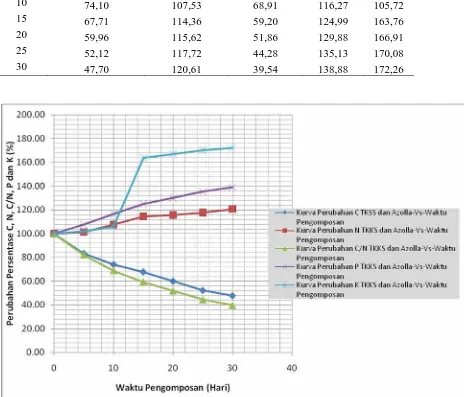
Gambar 4.3. Kurva Perubahan Konsetrasi C, N, C/N. P dan K dari TKKS Dan Gambar 4.3. Kurva Perubahan Konsetrasi C, N, C/N. P dan K dari TKKS Dan
Azolla Dikomposkan bersama (1:1) Selama Pengomposan 47 Azolla Dikomposkan bersama (1:1) Selama Pengomposan 47
DAFTAR TABEL
Tabel 2.3. Komposisi Bahan Organic pada Serat dan Tandan Kosong 10 Tabel 2.3. Komposisi Bahan Organic pada Serat dan Tandan Kosong 10
Tabel 2.4. Analisis Kimia Kompos 17
Tabel 2.4. Analisis Kimia Kompos 17
Tabel 4.1. Pengomposan Azolla 42
Tabel 4.1. Pengomposan Azolla 42
Tabel 4.2. Persentase Perubahan Konsentrasi C, N, C/N, P dan K dari Azolla Tabel 4.2. Persentase Perubahan Konsentrasi C, N, C/N, P dan K dari Azolla
Selama Pengomposan 43
Selama Pengomposan 43
Tabel 4.3. Pengomposan TKKS 44
Tabel 4.3. Pengomposan TKKS 44
Tabel 4.4. Persentase Perubahan Konsentrasi C, N, C/N, P dan K dari TKKS Tabel 4.4. Persentase Perubahan Konsentrasi C, N, C/N, P dan K dari TKKS
Selama Pengomposan 45
Selama Pengomposan 45
Tabel 4.5. Pengomposan Bersama Azolla dan TKKS (1:1) 46 Tabel 4.5. Pengomposan Bersama Azolla dan TKKS (1:1) 46
Tabel 4.6. Persentase Perubahan Konsentrasi C, N, C/N, P dan K dari TKKS Tabel 4.6. Persentase Perubahan Konsentrasi C, N, C/N, P dan K dari TKKS
Dan Azolla yang Dikomposkan Bersama Selama Pengomposan 47 Dan Azolla yang Dikomposkan Bersama Selama Pengomposan 47
Tabel 4.7. Analisa Tablet Kompos 48
Tabel 4.7. Analisa Tablet Kompos 48
17
DAFTAR LAMPIRAN
RAN
Nomor Judul Halaman
Nomor Judul Halaman
Lampiran 1. Data Analisa Pengomposan Azolla, TKKS, Lampiran 1. Data Analisa Pengomposan Azolla, TKKS,
dan Azolla + TKKS (1:1) 52
dan Azolla + TKKS (1:1) 52
Lampiran 2. Data Perhitungan N-Total Pengomposan Azolla dan TKKS 54 Lampiran 2. Data Perhitungan N-Total Pengomposan Azolla dan TKKS 54
Lampiran 3. Data Perhitungan P Pengomposan Azolla dan TKKS 55 Lampiran 3. Data Perhitungan P Pengomposan Azolla dan TKKS 55
Lampiran 4. Data Perhitungan K Pada Pengomposan Azolla dan TKKS 56 Lampiran 4. Data Perhitungan K Pada Pengomposan Azolla dan TKKS 56
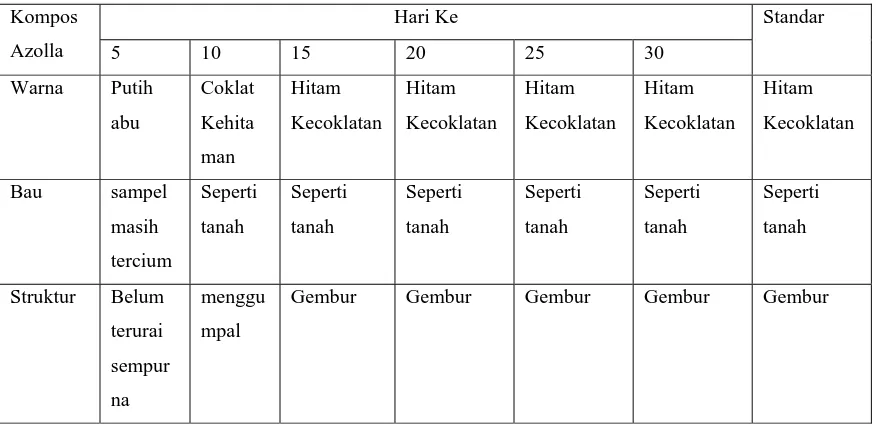
Lampiran 5. Hasil Pengomposan Azolla, TKKS, Azolla + TKKS (1:1) 57 Lampiran 5. Hasil Pengomposan Azolla, TKKS, Azolla + TKKS (1:1) 57
Lampiran 6. Standar Kualitas Kompos (SNI 19-7030-2004) 59 Lampiran 6. Standar Kualitas Kompos (SNI 19-7030-2004) 59
PEMANFAATAN LIMBAH TANDAN KOSONG KELAPA SAWIT DAN AZOLLA MENJADI KOMPOS PUPUK TABLET
ABSTRAK
Telah dilakukan penelitian tentang pemanfaatan Tandan Kosong Kelapa Sawit (TKKS) dan azolla menjadi kompos pupuk tablet.Penelitian dilakukan dengan mengkomposkan masing-masing TKKS dan azolla, selama 30 hari dengan menggunakan activator EM4 ( effective microopganisms 4 ). Untuk mengetahui kadar unsur hara C, N, P dan K kompos dilakukan analisa selama berlangsungnya pengomposan dengan variasi waktu 0, 5, 10, 15, 20, 25, dan 30 hari. Dari analisa tablet kompos C/N kompos azolla + kompos TKKS adalah 10,9888, Kadar C=33,2950%, Kandungan hara makro N=3,0299%, P=0,6304%, dan K=14,405% menunjukkan tablet kompos ini telah memenuhi Standar Nasional Indonesia SNI 19-7030-2004. Untuk analisa tablet kompos azolla + TKKS (1:1 ) C/N = 9,7655, kandungan unsure hara N=2,6853%, P=0,5942%, dan K=15,01%. Dari rasio C/N sedikit dibawah Standar Nasional Indonesia SNI 19-7030-2004.
Kata Kunci :Tandan Kosong Kelapa Sawit, Azolla, Kompos, Pupuk Tablet,
Effective Microorgansms, rasio C/N.
THE USES OF PALM OIL EMPTY BUNCHES
AND AZOLLA BECOME TABLET COMPOST
ABSTRACT
It has been conducted a research on the uses of palm-oil empty bunches (TKKS) and the azolla to become compost fertilizer on tablet. The research was done by composting each TKKS and azolla for 30 days there using EM4 (Effective micro-organism 4) activator. In order to measure the content of manure element C, N, P and K compost there were conducted an analysis during the compost taking place with the time variety of 0, 5, 10, 15, 20, 25, and 30 days. By the compost tablet analysis C/N compost azolla + TKKS compost noted 10.9888, its content C=33.2950%, the content of macro manure N=3.0299%, P=0.6304%, and K=14.405% showed this compost table has already fulfilled the Indonesian National Standard Rate SNI 19-7030-2004. For analysis of compost table azolla + TKKS (1:1) C/N = 9.7655, the content of manure element N=2.6853%, P=0.5942%, and K=15.01%. For the C/N ratio is noted lower under Indonesian National Standard rate SNI 19-7030-2004.
Keywords : Palm-oil empty bunches, Azolla, Compost, pellet fertilizer,
BAB I PENDAHULUAN
1.1. Latar Belakang
Indonesia adalah sebuah negara agraris yang selalu didengung-dengungkan.
Hal ini tentu harus diikuti dengan produktifitas yang sesuai dengan yang diharapkan
seperti swasembada pangan dan lain sebagainya.Berbagai kendala yang belum dapat
diatasi secara berkesinambungan dalam berbagai langkah utuk menanggulangi
ataupun mendapatkan sistem pertanian yang baik sehingga menghasilkan produk
yang benar-benar menguntungkan dari segi hasil yang diperoleh. Pemerintah juga
telah melakukan upaya-upaya mulai dari sistem mebuat benih yang baik, irigasi,
penanggulangan hama, pendistribusian pupuk bersubsidi untuk mengatasi
kelangkaaan ataupun mahalnya harga pupuk untuk petani.
Pupuk merupakan bahan tambahan yang diberikan pada tanaman yang berfungsi
mengubahan keadaan fisik, komposisi kimia dan biologi tanah sesuai dengan
kebutuhan unsur hara yang diperlukan oleh tanaman. Sedangkan pemupukan
dimaksudkan sebagai pemberian zat makan yang diperlukan untuk pertumbuhan serta
meningkatkan hasil tanaman. Secara umum dapat dikatakan manfaat pupuk adalah
untuk menyediakan unsur hara yang kurang atau tidak tersedia didalam tanah untuk
mendukung pertumbuhan tanaman.
Pemakaian pupuk pabrik (bahan Anorganik) tidak dianjurkan diterapkan terus
menerus tanpa digabung dengan bahan organik. Pemberian bahan anorganik dalam
jangka panjang pada tanah sawah menyebabkan keseimbangan hara disawah
terganggu. Bahan anorganik dalam tanah bersifat meracuni bagi kehidupan mikroba
tanah, mikroba yang peka akan mati sedangkan yang tahan akan berkurang
kemampuannya untuk menguraikan bahan organik, dalam jangka panjang berakibat
tanah kehilangan mikroba yang berguna dan akibatnya tanah sawah akan kurang
subur sehingga mengeras dan pada musim kemarau akan retak-retak (Ikip, L.K. et.
al. 2004).Untuk menjaga tingkat kesuburan tanah yang berkelanjutan dan
memanfaatkan limbah industri serta menjaga kelestarian lingkungan sangat
diperlukan teknologi yang mudah diterapkan dilapangan membuat pupuk organik
yang sesuai dan praktis penggunaannya.
Azolla adalah tumbuhan paku air yang termasuk ordo Salviniales, famili Azollaceae.
Sangat mudah berkembang terkadang dianggap petani sebagai gulma, di Indonesia
ada yang menamakannya kiambang. Pemanfatan azolla sebagai pupuk pengganti
urea telah banyak dilaporkan oleh karena dapat mengikat nitrogen yang cukup besar.
Pabrik kelapa sawit banyak menghasilkan limbah padat terutama tandan kosong
kelapa sawit, dimana setelah proses perebusan dan diikuti penebahan maka buah
kelapa sawit akan terpisah dari tandannya dan selanjutnya buah akan diproses
menjadi crude palm oil (CPO) sedangkan tandan kosongnya akan dikirim ke tungku
pembakaran (insenerator). Sebahagian pabrik ada yang memanfaatkannya untuk
diproses menjadi pupuk oleh karena jumlah tandan kosong ini cukup banyak yaitu
sebanyak 20% dari jumlah tandan buah sawit yang di olah serta kandungan kalium
Manfaat dari penggunaan pupuk terhadap sifat fisis tanah yaitu memperbaiki struktur
tanah\dari padat menjadi gembur. Dengan pemberian pupuk pada tanah akan dapat
memperbaiki struktur tanah dimana akan tersedia ruang-ruang pada tanah, dimana
ruang yang akan terbentuk dapat digunakan bakteri aerob yang berada pada akar
untuk mendukung pertumbuhan dan mengurangi erosi permukaan tanah. Penyediaan
unsur-unsur yang diperlukan oleh tanaman dapat terpenuhi baik unsur hara makro
(N, P, K) dan unsur mikro yang diperlukan. Dimana pemupukan dengan bahan
organik unsur-unsur makro ini tidak mudah hilang atau menguap, sehingga tanaman
dapat menyerap dalam jangka waktu lama. (Marsono, 2001). Pupuk organic
merangsang mikroorganisme tanah yang diperlukan terutama untuk mengubah
senyawa-senyawa organik yang terdapat dalam pupuk seperti nitosomonas yang akan
mengubah NO2 menjadi N2 sehingga mudah diserap oleh akar dan rhizobium,
mikoriza adalah bakteri yang dapat menguraikan pospat atau kalium.
Menurut PT Cipta Visi Sinar Kencana (CVSK) Bandung sebagai produsen pupuk
formula NPK tablet Gramafix ® Padi, pupuk organic bentuk tablet mempunyai
banyak keuntungan antara lain, memperoleh bentuk yang padu, tidak mudah larut,
dan tidak mudah hancur, serta tepat dosis.Pupuk organic dalam bentuk tablet juga
mengatasi masalah pemborosan pupuk majemuk akibat mudah tercuci dan
penguapan, serta mempermudah dan menghemat biaya distribusi pupuk. Disamping
itu aplikasi pupuk bentuk tablet dapat mengurangi tumbuhnya gulma dan rumput
penganggu karena pupuk tablet dibenamkan 5 cm – 10 cm. Dengan rendahnya
biaya pemeliharaan tanaman padi. Untuk lahan basah pupuk tablet juga dapat
memperbaiki struktur tanah dan menperlambat pelepasan hara.
1.2. Permasalahan
Apakah Tandan Kosong Kelapa Sawit dan Azolla dapat dijadikan pupuk
Kompos
1.3. Pembatasan Masalah
Penelitian ini dititik beratkan pada pengomposan bahan-bahan limbah yang
banyak mengandung unsur hara makro terutama azola dan tandan kosong kelapa
sawit.
1.4. Tujuan Penelitian
Untuk pemanfaatan Tandan Kosong Kelapa Sawit dan Azolla sebagai kompos
pupuk tablet.
1.5. Manfaat Penelitian
Untuk membantu petani mendapatkan pupuk yang murah, praktis dan sesuai
kebutuhan tanaman sesuai Standar Nasional Indonesia (SNI).
1.6. Metodologi Penelitian
5
2. Sampel Azolla diambil dari Sei Tuan pantai Labu Deli Serdang dan sampel
TKKS dari PKS di Turange, kec.Selapian, Langkat.
3. Pengomposan dilakukan dengan penambahan EM4 terhadap masing-masing
Azolla dan TKKS, juga terhadap campuran Azolla + TKKS (1:1) dengan
waktu pengomposan bervariasi yaitu 5 sampai 30 hari dengan interval
pengomposan 5 hari.
4. Penentuan C - Organik dilakukan dengan metode walkey Black,
5. Penentuan Nitrogen dilakukan dengan metode Kjehldahl.
6. Penentuan Posfor (P) sebagai P2PO5 dengan spektrofotometri.
7. Penentuan Kalium (K) sebagai K2O yang larut dalam asam klorida 25%.
1.7. Lokasi Penelitian
Penelitian dilakukan di Laboratorium Pusat Penelitian (PUSLIT) dan
BAB II
TINJAUAN PUSTAKA
2.1 Azolla
Azolla adalah asal kata dari bahasa latin yaitu azollaceae, yang merupakan
tumbuhan paku air yang termasuk ordo Salviniales, famili Azollaceae. dan
mempunyai enam spesies. Sangat mudah berkembang terkadang dianggap petani
sebagai gulma atau limbah pertanian di daerah Sumatera umumnya disebut kiambang.
Azolla pada daerah persawahan akan mengambang diatas permukaan air dan bila air
surut akan menempel pada tanah yang lembab. Pemanfatan azolla sebagai pupuk
pengganti urea telah banyak dilaporkan oleh karena dapat mengikat nitrogen yang
cukup besar. Spesies yang banyak terdapat di Indonesia terutama di pulau Jawa
adalah Azolla.pinnata, dan biasa tumbuh bersama-sama padi di sawah. (Lumpkin dan
Plucknett. 1982).
Meski sudah diperkenalkan dan dipopulerkan sejak awal tahun 1990-an, ternyata
belum banyak petani yang memanfaatkan tanaman azolla ( Azolla pinnata) untuk
usaha taninya. Padahal manfaat tanaman air yang satu ini cukup banyak. Selain biasa
untuk pupuk dan media tanaman biasa, azolla juga bisa dimanfaatkan untuk pakan
ternak dan ikan.
Di Bali, azolla biasa dan sering dijumpai terapung di perairan sawah dan kolam ikan,
karena dianggap gulma, para petani lantas menyingkirkannya. Ditumpuk dan dibuang
begitu saja. Padahal, bila dimanfaatkan sebagai pupuk tanaman padi di sawah, azolla
2.2. Kandungan Nutrisi Azolla.
Berikut susunan hara dan asam amino yang terkandung didalam azolla.
Tabel 2.1. Susunan hara azolla (%) berdasarkan berat kering.
Unsur Kandungan Unsur Kandungan
Abu 10.50 Magnesium 0.5 – 0.6
Sumber : Maffuchah, 1998
2.3. Pengganti Urea
Pemanfaatan azolla sebagai pupuk ini memang memungkinkan.Bila dihitung
dari berat keringnya dalam bentuk kompos (azolla kering) mengandung unsure
Nitrogen (N) 3-5%, Phosphor (P) 0.5-0.9% dan Kalium (K) 2-4.5%. Sedangkan hara
mikronya berupa Calsium (Ca) 0.4-1%, Magnesium (Mg) 0.5-0.6%, Ferum(Fe)
0.06-0.26% dan Mangaan(Mn) 0.11-0.16%.
Berdasarkan komposisi kimia tersebut, bila digunakan untuk pupuk mempertahankan
kesuburan tanah, setiap hektar areal memerlukan azolla sejumlah 20 ton dalam
keadaan kering. Bila azolla diberikan secara rutin setiap musim tanam, maka suatu
saat tanah itu tidak memerlukan pupuk buatan lagi.
Hal itu dimungkinkan, karena pana penebaran pertama ¼ bagian unsure yang
dikandung azolla langsung dimanfaatkan oleh tanah. Seperempat bagian ini, setara
dengan 65 Kg pupuk Urea. Pada musim tanam ke-2 dan ke-3, azolla mensubsitusikan
Dibanding pupuk buatan, azolla memang lebih ramah lingkungan. Cara kerjanya juga
istimewa, karena azolla mampu mengikat Nitrogen langsung dari udara.
2.4. Untuk Media Tanam
Penggunaan sebagai pupuk, selain dalam bentuk segar, baik juga dalam
bentuk kering dan kompos. Dalam bentuk kompos ini, azolla juga baik untuk media
tanam aneka jenis tanaman hias mulai dari bonsai, suplir, kaktus sampai mawar.
Untuk media tanaman hias, selain digunakan secara langsung. Kompos azolla ini juga
dicampur dengan pasir dan tanah kebun dengan perbandingan 3 : 1 : 1. untuk
membuat kompos azolla, caranya cukup mudah. Buat saja lubang ukuran (PxLxD)
3x2x2 meter. Kemudian azolla segar dimasukkan ke dalam lubang. Seminggu, azolla
yang sudah terfermentasi tersebut lama dijemur. Setelah agak kering, baru dikemas
dalam kantong plastik atau langsung digunakan sebagai media tanam.
2.5. Tandan Kosong Kelapa Sawit
Tandan buah sawit yang diolah dipabrik akan menghasilkan minyak sawit, inti
sawit, cangkang, serat dan tandan kosong. Dalam proses pengolahan terdapat bahan
yang tidak termanfaatkan seperti tandan kosong dan air buangan pabrik. Karena
kapasitas pabrik yang cukup besar yaitu antara 10 s/d 60 ton TBS/jam maka bahan
buangan tersebut dapat mempengaruhi lingkungan biotik dan abiotik.
Perkembangan areal perkebunan kelapa sawit yang diikuti dengan pembangunan
pabrik yang cukup pesat akan mempengaruhi lingkungan sekitar terutama lingkungan
sawit yang mengacu pada undang-undang no.4 tahun 1982 dan peraturan pemerintah,
maka pengendalian limbah pabrik kelapa sawit dapat dilakukan dengan cara
pemanfaatan, pengurangan volume limbah dan pengawasan mutu limbah.
Pembangunan instalasi pengendalian limbah dilakukan bersamaan dengan
pembangunan pabrik kelapa sawit dengan sistem yang didasarkan kepasa kapasitas
dan kualitas limbah yang diinginkan.
2.6. Karateristik Limbah Pabrik 2.6.1 Limbah Padat
Limbah padat yang dihasilkan oleh pabrik pengolah kelapa sawit ialah tandan
kosong, serat dan tempurung.Lihat tabel 2.2
Tabel 2.2 Rendemen limbah padat.
Jenis Persentase terhadap TBS
Basah Kering Hasil prosses
Tandan Kosong 21 – 23 10 – 12 Bantingan
Serat 8 – 11 5 – 8 Screw press
Tempurung 5 4 Shell Separator
Sumber : Naibaho. P.S.1998
Limbah padat tandan kosong kadang-kadang mengandung buah tidak lepas dSi antara
celah – celah ulir dibagian dalam. Kejadian ini timbul, bila perebusan dan bantingan
yang tidak sempurna sehingga pelepasan buah sangat sulit. Hal ini sering terjadi di
pabrik – pabrik yang tekanan kerja ketel rebusan di bawah 2,8 kg disertai produksi
uap yang tidak mencukupi kebutuhan. Perebusan yang tidak sempurna menghasilkan
Serat yang merupakan hasil pemisahan dari fibre cyclone mempunyai kandungan
cangkang, minyak dan inti. Kandungan tersebut tergantung pada proses ekstraksi di
screw press dan pemisahan pada fibrecyclone. Kualitas asap pembakaran pada dapur
ketel uap dipengaruhi oleh komposisi serat tersebut. Ampas serat sekarang ini telah
habis terpakai di pabrik sehingga dampak yang mungkin ditimbulkan pada
lingkungan ialah polusi udara.Tempurung yang dihasilkan dari kernel plant yaitu
shell separator masih mengandung biji bulat dan inti sawit. Bila bahan ini digunakan
sebagai bahan bakar pada dapur ketel akan menghasilkan gas-gas yang tidak terbakar
sempurna. Hal ini timbul karena udara yang display adalah untuk kebutuhan
cangkang, sehingga timbul pembakaran yang tidak sempurna.
Tandan kosong dan serat merupakan bahan organic dengan komposisi sebagai
berikut.
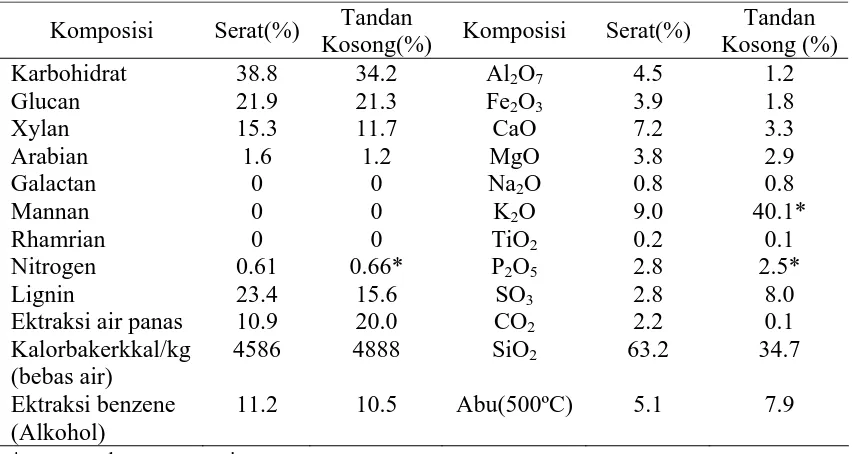
Tabel 2.3. Komposisi bahan organic pada serat dan tandan kosong
Komposisi Serat(%) Tandan
Kosong(%) Komposisi Serat(%)
Tandan
* unsur makro yang penting.
2.7. Kompos
Kompos merupakan hasil aksir suatu proses fermentasi tumpukan sampah,
serasah tanaman ataupun bangkai binatang. Ciri – ciri kompos yang baik adalah
berwarna coklat, berstruktur remah, berkonsistensi gembur dan berbau daun lapuk.
Tumpukan bahan mentah ( serasah, sisa tanaman, sampah dapur dan lain sebagainya )
bisa menjadi kompos akibat proses pelapukan dan penguraian.dengan kata lain terjadi
perubahan dari sifat fisik yang baru. Perubahan itu sebagian besar muncul oleh karena
adanya kegiatan jasad renik sehubungan dengan kebutuhan hidup organisme itu. Apa
yang diikat oleh jasad renik demi mencukupi kebutuhan hidupnya, kelak akan
dikembalikan lagi apabila jasad renik itu mati. Terjadi proses penguraian, pengikatan
dan pembebasan berbagai zat atau unsur hara selama berlangsungnya proses
pembentukan kompos.
Penjelasan lengkap meengenai proses yang terjadi adalah sebagai berikut ;
a. Hidrat arang (selulosa, hemiselulosa, dan lain- lain ) diurai menjadi CO2 dan air
atau Ch4 dan H2.
b. Zat putih telur diurai menjadi amida, asam amino, amoniak, CO2 air.
c. Berbagai jenis unsure hara, terutama N, di samping P,K dan yang lain sebagai
hasil penguraian,akan terikat dalam tubuh jasad renik. Sebagain yang tidak terikat
akan menjadi persediaan di dalam tanah. Yang terikat dalam tubuh jasad renik
d. Juga ada unsur hara dari senyawa organik yang akan terbebas menjadi senyawa
an-organik sehingga menjadi persediaan di dalam tanah bagi keperluan
pertumbuhan dan perkembangan tanaman.
e. Lemak dan lilin akan terurai menjadi CO2 dan air.
Selama berlangsungnya proses tersebut akan terjadi perubahan berat dan isi
dari bahan-bahan pembuatanya. Terjadi penguranagan berat karena adanya
penguapan dan pencucian. Sebagaian besar senyawa hidrat arang akan hilang ke
udara selama penguapan.
2.7.1 Syarat Pembuatan Kompos
a. Campuran kompos harus homogen agar kadar N dan kecepatan fermentasi
dapat merata dan tetap. Oleh karena itu bahan menttah perlu dipotong-potong
hingga menjadi bagian-bagaian kecil.
b. Temperatur awal harus tiinggi untuk membunuh pathogen, biji
rumput-rumputan, lalat dan telurnya, serta larva hama lain beserta penyakit
(cendawan) yang terbawa ke dalam tumpukan. (Nurheti Yuliarti, 2009).
2.7.2 Parameter yang dapat diamati sebagai petunjuk sempurnanya proses pengomposan sebagai berikut:
1. Selama proses pengomposan, dari hari pertama temperatur akan meningkat
secara bertahap. Proses pengomposan dianggap selesai apabila temperature
kompos turun mendekati temperatur awal. Pengamatan ini dapat dilakukan
2. Pengamatan terhadap penyusutan tumpukan kompos dilakukan pada akhir
pengomposan (untuk bahan lunak) dan setiap minggu (untuk bahan keras).
2.7.3 Proses pengomposan
Campuran bahan yang sudah ditambah bioakttivator difermentasi dengan cara
menutupnya menggunakan terval dan membiarkannya selama 5 – 7 hari. Pada hari
kedua atau ketiga, temperatur bahan kompos akan meningkat menjadi 40 – 60o C.
Jika temperatur meningkat, tumpukan bahan tersebut harus dibalik, kemudian ditutup
lagi. Tiga hari kemudian temperatur akan turun kembali dan berangsur – angsur
stabil. Jika temperatur sudah stabil, bahan tersebut sudah menjadi kompos dan siap
dikemas atau digunakan. ( Sofian, 2006).
Sumber bahan organik tanah adalah jaringan tanaman baik yang berupa serasah atau
sisa tanaman yang berrupa batang , akar daun yang kemudian dirombak oleh
mikroorganisme tananh, atau sisa hewan yang berupa kotoran maupun bangkai
hewan. Secara kimiawi bahan organic tanah tersususn atas karbohidrat, protein lignin
dan sejumlah senyawa kecil seperti lemak, lilin dan sebagainya, salah satu hasil
perombakan bahan organik adalah humus, yang mempunyai kapasitas pengikatan
unsure hara dan air yang sangat tinggi, memiliki kekhususan koloidal dan mampu
mengikat air 80-90% dari berat keringnya, bandingkan dengan tanah liat yang hanya
mampu mengikat air 15-20% saja. Humus memberi warna tanah menjadi agak
kehitaman dan sangat bermanfaat bagi pertanian karena mempengaruhi struktur
Bahan organik dalam tanah sangat berhubungan dengan kecepatan pelapukan tanah.
Bahan organic yang mempunyai C/N rasio yang rendah akan lebih cepat melapuk
disbanding bahan organik yang mempunyai C/N rasio yang tinggi. Untuk cepat lapuk
maka perlu penambahan nitrogen tanah yaitu dengan menambahkan bahan organic
yang cepat lapuk. Walaupun demikian peran oksigen yang terkandung dalam tanah
sangat penting, karena berkurangnya kadar oksigen juga berpengaruh pada aktivitas
mikroorganisme dalam penguraian. Ini berkaitan dengan ketersediaan unsure hara
dari bahan organik yang bisa diserap tanaman. ( M, Isnaini, 2006 )
Reaksi - reaksi yang terjadi pada proses pengomposan yaitu :
Reduksi sulfat :
CH3CHOHCOOH + SO42- 2CH3COOH + H2S + 2OH -
4H2 + SO42- 2H2O + H2S + 2OH-
Reduksi karbon organik secara anaerobik :
CH3COOH CH4 + CO2
4CH3OH 3CH4 + CO2 + 2H2O
C6H12O6 bakteri 3CH3COOH
C6H12O6 kapang 2CH3CH2OH + 2CO2
Reduksi karbon dioksida :
2CH3CH2OH + 2CO2 2CH3COOH + CH4
4H2 + CO2 CH4 + 2H2O
Reduksi oksidasi sempurna :
CH3COOH + 2O2 CO2 + 2H2O
2H2 + O2 2H2O
CH4 + 2O2 CO2 + 2H2O
( M. Judoamidjojo, A.A. Darwis dan E.G. Said ).
Reaksi aminasi :
Protein proses enzimatik senyawa asam amino komplek + O2 + amina
R NH2 + H2O hidrolisa enzim R OH + NH3 + energi
Reaksi amonifikasi :
2NH3 + H2CO3 (NH4)2CO3 2NH4+ + CO3
2-Reaksi nitrifikasi :
2NH4+ + 3O2 NO2- + 2H2O + 4H+ + Energi
2NO2- + O2 2NO3- + Energi
( Mul Yulyani Sutedjo, 2002 )
2.7.4. Menentukan Kematangan Kompos
Kompos dikatakan bagus dan Siap diaplikasikan jira tingkat kematangannya
sempurna, dan bisa dilihat dari keadaan bentuk fisiknya, sebagai berikut :
1. Jika diraba, suhu tumpukan bahan yang dikomposkan sudah dingin, mendekati
suhu ruang.
2. Tidak mengeluarkan bau busuk lagi.
4. Jika dilarutkan ke dalam air, kompos yang sudah matang tidak akan larut.
5. Strukturnya remah, tidak menggumpal.
( Simamora, Suhut dan Salundik. 2006. Meningkatkan Kualitas Kompos )
2.7.5 Meningkatkan Kesuburan Tanah
Produksi tanaman akan terhalang jika unsur hara yang terkandung di dalam
tanah kurang atau tidak seimbang, terutama di daerah yang kadar unsur haranya
buruk atau tanahnya terlalu asam atau basa. Meningkatkan jumlah produksi
komoditas pertanian di Indonesia dapat dilakukan dengan cara meningkatkan kualitas
tanah yang sudah mulai menurun kesuburannya.
Upaya yang dapat dilakukan untuk membatasi hilangnya unsur hara dan
mengembalikan kesuburan tanah dilakukan dengan cara mendaur ulang limbah
organik, seperti limbah dari kandang peternakan, kotoran manusia, sisa tanaman atau
sisa pengolahan tanaman. Hasil daur ulang limbah organik tersebut dikembalikan ke
lahan baik secara langsung ataupun setelah diolah menjadi kompos atau
difermentasikan. Dengan memanfaatkan pupuk organik tersebut, unsur hara dalam
tanah akan bisa diperbaiki. Sehingga kehilangan unsur hara akibat terbawa air hujan /
leaching dapat diatasi.
Pemupukan menggunakan kompos mengakibatkan tanah yang strukturnya ringan
(berpasir atau ringan) menjadi lebih baik, daya ikat air menjadi lebih tinggi.
Sementara itu,tanah yang berat (tanah liat) menjadi lebih optimal dalam mengikat air.
Kompos dapat meningkatkan kapasitas tukar kation (KTK) tanah dan dapat
Unsur hara yang dibutuhkan tanaman tersedia di dalam tanah dan pupuk, serta akan
diserap dengan rambut akar dalam bentuk ion. Tanah yang memiliki kapasitas tukar
kation (KTK) rendah hanya memiliki sedikit unsur hara di dalamnya yang dapat
diserap tanaman.
Unsur hara yang dibutuhkan tanaman dibagi menjadi dua yaitu unsur hara
makro dan unsur hara mikro. Unsur hara makro antara lain Nitrogen (N), Fosfor (P),
Kalium (K), Kalsium (Ca), Magnesium (Mg), dan Sulfur (S). Sedangkan unsur hara
mikro antara lain Zat besi (Fe), Mangan (Mn), Tembaga (Cu), dan seng (Zn).
Komponen kompos yang semakin berpengaruh terhadap sifat kimia tanah adalah
kandungan humusnya. Humus dalam kompos mengandung unsur hara yang
dibutuhkan tanaman. Humus yang menjadi asam humat dapat melarutkan zat besi dan
aluminium sehingga fosfat yang terikat besi dan alminium akan lepas dan dapat
diserap oleh tanaman. Selain itu humus merupakan penyangga kation yang dapat
mempertahankan unsur hara sebagai bahan makanan untuk tanaman. Kandungan
kimia kompos terlihat pada table di bawah ini :
Tabel 2.4. Analisis Kimia Kompos
Sumber : http : // www.kompos.go.id/htmt
18
Kompos juga berfungsi sebagai pemasok makanan bagi organisme di dalam tanah
seperti kapang, bakteri, actinomycetes, dan protozoa sehingga dapat meningkatkan
dan mempercepat proses dekomposisi bahan organik.( http:// www.kompos.go.id/
BAB III
METODE PENELITIAN
3.1 Alat – alat yang digunakan
Alat – alat yang dipergunakan dalam penelitian ini adalah :
• Buret Pyrex
• Statif • Klemp
• Alat destilasi Quickfit
• Labu Erlenmeyer Pyrex
• Gelas beaker 250 mL Pyrex
• Pipet volumentri 10 mL Pyrex
• Pipet volumentri 5 mL Pyrex
• Labu takar 100 mL Pyrex
• Pipet Skala 5 mL Pyrex
3.2 Bahan – bahan yang digunakan
Bahan – bahan yang dipergunakan dalam penelitian ini adalah ;
• Tumbuhan Azolla
• Tandan Kosong Kelapa Sawit
• H2SO4(p) p.a E. Merck
• (NH4)2Fe(SO4)2.6H2O p.a E. Merck
• K2Cr2O7 p.a E. Merck
• NaOH p.a E. Merck
• Fenolftalein p.a E. Merck
• Metil Merah p.a E. Merck
• Metal Biru p.a E. Merck
• H2C2O4.2H2O p.a E. Merck
• HCI p.a E. Merck
• H3BO3 p.a E. Merck
• H3PO4 p.a E. Merck
• Indikator difenilamin p.a E. Merck
• Selenium p.a E. Merck
• Akuades
• Bakteri EM4
3.3. Prosedur Penelitian
3.3.1. Penyediaan Sampel Azolla
Azolla yang diambil secara acak, dikeringkan dibawah sinar matahari selama
3 hari, selanjutnya dihaluskan jadi tepung.
3.3.2. Penyediaan Sampel Tandan Kosong Kelapa Sawit ( TKKS )
TKKS yang diambil secara acak dirajang menjadi potongan – potongan kecil
sekitar 2 milimeter, kemudian dikeringkan dibawah sinar matahari selama 3 hari,
3.3.3. Pembuatan starter Effective Microoganism 4 (EM4)
Kedalam gelas beaker dimasukkan EM4 sebanyak 5 ml,kemudian
ditambahkan aquades sebanyak 1 L, selanjutkan ditambahkan gula pasir sebanyak ½
sendok makan,diaduk sampai homogen dan dibiarkan selama 24 jam.
3.3.4 Pembuatan Kompos 3.3.4.1 Kompos Azolla
Ditimbang sebanyak 500 g sampel yang sudah dihaluskan dimasukkan ke
dalam ember plastik, kemudian ditambahkan starter EM4 yang telah diencerkan
sedikit demi sedikit hingga kandungan air 30 – 40%, kandungan air yang diinginkan,
diuji dengan tidak menetesnya air bila bahan digenggam dan akan mekar jika
genggaman bahan dilepas.Dihomogenkan, ditutup dan disimpan pada tempat yang
telah disterilkan, dibiarkan sampai 30 hari, dilakukan pengadukan sekali dalam 48
jam untuk mengeluarkan gas gas yang terbentuk dan menjaga suhu adonan.
Ditentukan kadar Kalium, Posfos, C-Organik dan Nitrogen untuk setiap variasi
pengomposan 0-5-10-15-20-25 dan 30 hari.
3.3.4.2 Kompos TKKS
Ditimbang sebanyak 500 g sampel yang sudah dihaluskan dimasukkan
kedalam ember plastik, kemudian ditambahkan starter EM4 yang telah diencerkan
sedikit demi sedikit hingga kandungan air 30 – 40% kandungan air yang diinginkan
,diuji dengan tidak menetesnya air bila bahan digenggam dan tidak menetesnya air
jika genggaman bahan dilepas.Dihomogenkan,ditutup dan disimpan pada tempat
48 jam untuk mengeluarkan gas gas yang terbentuk dan menjaga suhu adonan.
Ditentukan kadar Kalium, Posfos, C-Organik dan Nitrogen untuk setiap variasi
pengomposan 5-10-15-20-25 dan 30 hari.
3.3.4.3 Kompos Azolla +TKKS ( 1 : 1 )
Ditimbang sebanyak 500 g sampel azolla dan 500 g TKKS ( 1 : 1 ) yang
sudah di haluskan, lalu dimasukkan ke dalam ember plastik dicampur sampai
homogen,bahan diaduk terus sehingga campuran benar-benar merata, kemudian
ditambahkan starter EM4 yang telah diencerkan sedikit demi sedikit hingga
kandungan air 30 – 40 % yang ditandai dengan tidak menetesnya air jika bahan
digenggam dan akan mekar jika genggaman bahan dilepas.Kemudian ditutup dan
disimpan dibiarkan selama 30 hari, dilakukan pengadukan sekali dalam 48 jam untuk
mengeluarkan gas gas yang terbentuk dan menjaga suhu adonan. Ditentukan kadar
Kalium, Posfor, C-oraganik dan Nitrogen setiap variasi pengomposan 5,10,15,20,25
dan 30 hari.
3.3.4.4 . Pembuatan tablet kompos
Kompos yang sudah matang masing masing diayak untuk dibuat tablet
kompos.
Tablet 1. Kompos azolla 50 g + kompos TKKS 50 g dicampur homogen lalu di
tambah larutan kanji 2 gram / 50 ml sehingga berbentuk adonan yang liat, selanjutnya
di cetak menjadi tablet kompos, dikeringanginkan lalu dianalisa kandungan hara
Tablet 2. Kompos azolla + TKKS (1:1) 100 g di tambah larutan kanji 2 gram / 50 ml
dibuat adonan yang liat selanjutnya dicetak menjadi tablet kompos, dikeringanginkan
lalu dianalisa kandungan hara makro C,N,PdanK.
3.3.5 Pembuatan Pereaksi dan Larutan Standar
3.3.5.1 Pembuatan Pereaksi dan Larutan standar untuk penentuan Posfor sebagai P2O5 Metode Spektrofotometri
a. Larutan HCl 25%
Dipipet 173,6 ml HCl (p), dimasukkan ke dalam labu takar 250 ml, diencerkan
dengan akuades hingga garis tanda dan dihomogenkan.
b. Larutan Standar 100 P 100 ppm
Ditimbang 0,2195 g kristal KH2PO4 secara kuantitatif, dimasukkan ke dalam
gelas piala 250 ml, dilarutkan dengan akuades secukupnya, dimasukkan kedalam labu
takar 500 ml, diencerkan dengan akuades hingga garis tanda dan dihomogenkan.
c. Larutan Amonium Molibdat 4%
Ditimbang 1,883 g kristal (NH4)6Mo7O24.4H2O, dimasukkan ke dalam gelas
piala 50 ml, dilarutkan dengan akuades secukupnya, dimasukkan kedalam labu takar
50 ml, diencerkan dengan akuades hingga garis tanda, dan dihomogenkan.
d. Larutan Asam Askorbat 0,1 M
Ditimbang 0,880 g kristal C6H8O6, dimasukkan ke dalam gelas piala 50 ml,
dilarutkan dengan akuades secukupnya, dimasukkan kedalam labu takar 50 ml,
e. Larutan Kalium antimonil Tartarat 1mg Sb/ml
Ditimbang 0,105 g kristal KSbOC4H4O6.1/2 H2O, dimasukkan ke dalam gelas
piala 50 ml, dilarutkan dengan akuades secukupnya, dimasukkan kedalam labu takar
50 ml, diencerkan dengan akuades hingga garis tanda, dan dihomogenkan.
f. Larutan Seri Standar P dalam ekstrak HCl 0,95 N
Dipipet masing – masing 20 ml akuades dan 11,7 ml HCl 25% ke dalam labu
takar 100 ml, dipipet 2ml, 4ml, 6ml, 8ml,10 ml larutan standar 100 ppm secara
kuantitatif, diencerkan dengan akuades hingga garis tanda , dan dihomogenkan.
g. Larutan H2SO4 5 N
Dipipet 13,72 ml H2SO4 (p),dimasukkan ke dalam labu takar 100 ml yang telah
berisi 20 akuades, diencerkan dengan akuades hingga garis tanda, didinginkan dan
dihomogenkan
h. Pembuatan Larutan Campuran Pengkompleks
Dipipet 25 ml H2SO4 5 N ke dalam labu takar 50 ml, ditambahkan 7,5 ml
larutan (NH4)6Mo7O24. 4%, ditambahkan 15 ml larutan asam askorbat 0,1 M,
ditambahkan 2,5 ml larutan KSbOC4H4O6 0,1 M, dan dihomogenkan.
3.3.5.2 Pembuatan Pereaksi untuk Penentuan C – Organik a. Larutan K2Cr2O7 1 N
Ditimbang secara kuantitatif kristal K2Cr2O7 sebanyak 12,257 g, dimasukkan
ke dalam gelas piala 250 ml, dilarutkan dengan akuades secukupnya, dimasukkan
b.Larutan FeSO4 1 N
Ditimbang secara kuantitatif kristal FeSO47H2O sebanyak 69,505 g,
dimasukkan ke dalam gelas piala 250 ml, dilarutkan dengan akuades secukupnya,
ditambahkan 37,5 ml H2SO4 pekat secara perlahan – lahan , diaduk hingga larut,
dimasukkan ked lam labu takar 250 ml, ditambahakan akuades hingga garis tanda,
didinginkan dan dihomogenkan.
c. Larutan Difenilamin ( (C6H5)2NH4 )
Ditimbang 0,5 g kristal difenilamin, dilarutkan dengan 20 ml akuades dalam
gelas piala 250 ml, ditambahkan dengan 100 ml H2SO4 pekat secara perlahan – lahan
dengan merendam gelas beaker dalam air es, dan diaduk hingga larut seluruhnya.
3.3.5.3 Pembuatan Pereaksi untuk Penentuan Nitrogen Metode Kjehldahl a. Larutan NaOH 40%
Ditimbang sebanyak 40 g kristal NaOH, dimasukkan kedalam gelas piala 250
ml, kemudian dilarutkan dengan akuades, dimasukkan kedalam labu takar 100 ml,
diencerkan hingga garis tanda dan dihomogenkan.
b. Larutan Indikator fenolftalein
Dimasukkan kedalam labu takar 100 ml, diencerkan hingga garis tanda, dan
dihomogenkan.
c. Larutan H3BO3 3%
Ditimbang H3BO3 sebanyak 3 g, dimasukkan kedalam gelas piala 250 ml,
dilarutkan dengan akuades, dimsukkan kedalam labu takar 100 ml,diencerkan hingga
d. Larutan Indikator Campuran
Sebanyak 2 bagian indikator metil biru 0,1% (b/v) dan 1 bagian indikator
metil merah 0,2% (b/v) dalam etanol.
e. Larutan H2C2O4 0,01 N
Ditimbang kristal H2C2O4.2H2O secara kuantitatif sebanyak 0,63 g,
dimasukkan kedalam gelas piala 250 ml, dilarutkan dengan akuades, dimasukkan ke
dalam labu takar 1000 ml, diencerkan hingga garis tanda, dan dihomogenkan.
f. Larutan NaOH 0,01 N
Ditimbang secara kuantitatif kristal NaOH sebanyak 0,4 g, dimasukkan ke
dalam gelas piala 250 ml, dilarutkan dengan akuades, dimasukkan ke dalam labu
takar 1000 ml, diencerkan hingga garis tanda, dan dihomogenkan.
g. Larutan HCl 0,01 N
Sebanyak 0,83 ml HCl 37% dipipet ke dalam labu takar 1000 ml, diencerkan
hingga garis tanda dengan akuades, dan dihomogenkan.
h. Standarisasi Larutan NaOH 0,01 N
- Dipipet 10 ml larutan H2C2O4 0,01 N dimasukkan ke dalam gelas erlenmeyer
- Ditambahkan 3 tetes indikator Fenolftalein
- Dititrasi dengan NaOH hingga terjadi perubahan warna menjadi merah
lembayung
- Dilakukan hal yang sama sebanyak 3 kali.
i. Standarisasi HCl 0,01 N
- Dipipet 10 ml larutan HCl 0,01 N dimasukkan ke dalam gelas erlenmeyer
- Dititrasi dengan NaOH yang telah distandarisasi hingga terjadi perubahan
warna biru menjadi hijau kekuningan
- Dilakukan hal yang sama sebanyak 3 kali.
3.3.5.4 Pembuatan Pereaksi Untuk Penentuan Kalium sebagai K2O Dengan
Metode Spektrofotometer Serapan Atom (SSA) a. Larutan HCl 25%
Dipipet 173,6 ml HCl (p), dimasukkan ke dalam labu takar 250 ml, diencerkan
dengan akuades hingga garis tanda dan dihomogenkan
b. Larutan Kalium 100 ppm
Dilarutkan 1,907 g KCl p.a. dengan akuades dalam labu takar 1000 ml hingga
garis tanda . Larutan ini mengandung 1 mg K/L.
c. Larutan Standar Kalium 100 ppm
Sebanyak 10 ml larutan standar kalium 1000 ppm diencerkan dengan akuades
dalam labu takar 100 ml hingga garis tanda.
d. Larutan Seri Standard Kalium untuk kalibrasi (0,0 - 5 - 10 - 15 - 20 ppm) Dari larutan standar 100 ppm kalium masing – masing dipipet 0,0; 5; 10; 15;
20, ml, kemudian masing-masing diencerkan dengan akuades dalam labu takar 100
ml hingga garis tanda. Masing – masing larutan adalah 0,0; 5; 10; 15; 20 ppm kalium.
3.3.6. Penentuan P-Total Metode spektrofometri 3.3.6.1 Preparasi Sampel
Ditimbang 1 g sampel yang telah dikeringkan dibawah sinar matahari,
25%, dikocok dengan mesin pengocok selama 2 jam, disaring kertas saring no. 40,
ditampung ekstrak sampel ke dalam labu takar 100 ml, diencerkan dengan akuades
hingga garis tanda, dan dihomogenkan.
3.3.6.2 Pembuatan Kurva Kalibrasi
Dipipet 1 ml masing – masing larutan standar ke dalam tabung reaksi,
ditambahkan 5 ml akuades,ditambahkan 1 ml larutan campuran,didiamkan selama 15
menit, diukur absorbansinya dengan spektrofotometer, pada λ= 710 nm, dibuat
kurva kalibrasi dengan memplotkan konsentrasi terhadap absorbansi.
3.3.6.3 Penentuan Kadar Posfor pada Sampel
Dipipet ekstrak sampel ke dalam tabung reaksi, ditambahkan 5 ml akuades,
ditambahkan 1 ml larutan campuran, didiamkan selama 15 menit , diukur
absorbansinya dengan spektrofotometer, pada λ = 710 nm.
3.3.7. Penentuan Kadar C -Organik dengan metode Walkey Black
- Ditimbang secara kuantitatif sebanyak 0,1 g sampel yang telah dihaluskan dan
kering udara dimasukkan ke dalam erlenmeyer 500 ml
- Ditambahkan 10 ml larutan K2Cr2O7 1 N
- Ditambahkan 5 ml H2SO4 pekat secara perlahan
- Diaduk selama 1 menit
- Dididamkan selama 30 menit
- Ditambahkan 200 ml akuades
- Dititrasi dengan larutan FeSO4 hingga terjadi perubahan warna dari ungu
menjadi hijau
- Catatan : terlebih dahulu dilakukan hal yang sama pada blanko untuk
standarisasi FeSO4
3.3.8 Pengukuran Nitrogen dengan Metode Kjehdahl
- Ditimbang secara kuantitatif sebanyak 0,1 g sampel dimasukkan kedalam labu
Kjehldahl
- Ditambahkan 0,3 g selenium dan 25 ml H2SO4 pekat
- Didekstruksi sampel hingga sampel berubah menjadi larutan coklat kehitaman
- Dipindahkan ke dalam labu destilasi dan ditambahkan 50 mll akuades
- Ditambahkan 3 tetes indikator Fenolftalein dan NaOH 40% sehingga
berwarna merah lembayung
- Disediakan penampung untuk hasil destilat berupa labu Erlenmeyer yang
berisi 50 ml H3BO3 3% dan 3 tetes indikator campuran
- Dipasang tabung destilasi pada alat destilasi, kemudian diletakkan paada
tempatnya
- Dilakukan destilasi hingga diperoleh wwarna hijau muda
- Destilat kemudian dititrasi dengan HCl 0,01 N sampai terbentuk merah
lembayung
- Dicatat volume titran ditentukan % N
3.3.9 Penentuan Kalium sebagai K2O Dengan Metode Spektrofotometer
Serapan Atom (SSA)
- Dipanaskan gelas timbangan ke dalam oven pada suhu 105 0C dipanaskan
selama 15 menit lalu didinginkan dalam desikator selama 30 menit
- Ditimbang sebanyakl 5 g sampel kering lalu dimasukkan ke dalam erlenmeyer
100 ml
- Ditambahkan 12,5 ml HCl 25% ke dalam erlenmeyer 100 ml yang berisi
sampel
- Larutan dibiarkan selama 1 malam
- Kemudian dikocok dengan mesin pengocok bolak-balik selama 2 jam sampai
terbentuk suspensi
- Larutan disaring ke dalam labu takar 100 ml dengan menggunakan kertas
saring whatman No. 40, sambil dicuci sebanyak 3 kali dengan akuades
- Kemudian labu ukur dipenuhkan dengan akuades sampai garis tanda
- Filtrat disimpan didalam botol plastik untuk penetapan kadar kalium
- Konsentrasi kalium di dalam larutan diukur dengan menggunakan
3.4 Bagan Penelitian 3.4.1 Pembuatan Kompos 3.4.1.1.Pembuatan Starter EM4
Dimasukkan kedalam gelas beaker 1 L
Ditambahkan 1 L akuades
Ditambahkan ½ sendok makan gula pasir
Diaduk sampai homogen
Dibiarkan selama 24 jam 5 mL EM4
3.4.1.2.Pembuatan kompos azolla
Dirajang kecil-kecil sampai halus
Dikeringkan dibawah sinar matahari selama 3 hari
Dibuat jadi tepung
Ditentukan kadar C,N,P dan K
Ditimbang 500 gram
Dimasukkan ke dalam ember plastik
Ditambah starter EM4 sedikit demi sedikit hingga kandungan air
30 sampai 40 %
Ditutup rapat ember plastik yang telah dilobangi
Disimpan pada tempat yang steril
Dilakukan pengadukan sekali 48 jam untuk mengeluarkan gas –
gas yang terbentuk dan menjaga suhu adonan
Dibiarkan selama sampai 30 hari
Ditentukan kadar P sebagai P2O5, C – organic, Nitrogen dan
kalium sebagai K2O masing-masing kompos dengan variasi
3.4.1.3. Pembuatan kompos TKKS
Dipotong kecil kecil 1 – 2 cm
Dikeringkan dibawah sinar matahari selama 3 hari
Dihaluskan
Ditentukan kadar C,N,P dan K
Ditimbang sebanyak 500 g
Dimasukkan ke dalam ember plastik
Ditambahkan starter EM4 sedikit demi sedikit hingga kandungan air
30 sampai 40 %
Ditutup rapat ember plastik yang dilobangi
Disimpan pada tempat yang steril
Dilakukan pengadukan sekali 48 jam untuk mengeluarkan gas – gas
yang terbentuk dan menjaga suhu adonan
Dibiarkan selama 0 sampai 30 hari
Ditentukan kadar P sebagai P2O5, C – organic, Nitrogen dan kalium
sebagai K2O masing-masing kompos dengan variasi waktu
5,10,15,20,25 dan 30 hari Hasil
Kompos TKKS 500 g serbuk TKKS
3.4.1.4. Pembuatan tablet kompos azolla dan kompos TKKS
Kompos Azolla 50 g
Dihaluskan dan diayak
Kompos TKKS 50 g
Dihomogenkan dengan larutan kanji 2 gr/ 50 ml air menjadi
adonan yang liat Dicetak
Dikeringanginkan
Dianalisa kadar C,N,P dan K
3.4.1.5.Bagan Pembuatan Kompos Azolla + TKKS (1:1) Serta Pembuatan Tablet
Dimasukkan ke dalam ember plastik
Ditambah starter EM4 sedikit demi
sedikit sambil diaduk hingga
kandungan air 30-40%
Ditutup rapat ember plastik yang
dilobangi
Disimpan pada tempat yang steril
Dilakukan pengadukan sekali 48 jam
untuk mengeluarkan gas – gas yang
terbentuk dan menjaga suhu adonan
Disimpan dibiarkan selama 30 hari
Dianalisa Kadar C,N,P,K setiap variasi hari pengomposan 5,10,20,25
dan 30 hari
Diayak
Ditimbang 100 g
Dihomogenkan dengan larutan
kanji 2 gr/ 50 ml air menjadi adonan
yang liat
3.4.2 Penentuan C – Organik
Ditambahkan 10 ml K2Cr2O7
Ditambahkaan 20 ml H2SO4 pekat
Diaduk selama 1 menit
Didiamkan selama 30 menit
Ditambahkan 100 ml akuades
Ditambahkan 5 ml H3PO4 85 %
Ditambahkan 1 ml larutan difenilamin
Dititrasi dengan FeSO4 0,8987 N hingga warna berubah
menjadi hijau
Dicatat volume FeSO4 0,8987 N yang terpakai
Hasil
Larutan ungu
Larutan hijau kekuningan 0,1 g Azolla
Catatan : Prosedur ini dilakukan dengan cara yang sama untuk TKKS Prosedur ini dilakukan untuk masing – masing kompos Azolla
dan TKKS sesudah pengomposan dengan variasi waktu 5,10,15,20,25
dan 30 hari
Pengukuran dilakukan sebanyak 3 kali dan disajikan sebagai nilai rata –
3.4.3. Penentuan Posfor sebagai P2O5 Metode Spektrofotometri
3.4.3.1 Pengekstrakan Azolla
Ditambahkan 12,5 ml HCl 25%
Dikocok selama 2 jam dengan mesin pengocok dengan kecepatan
20 rpm
Disaring dengan kertas saring whatman no.40
Dimasukkan ke dalam labu takar 100 ml
Diencerkan dengan akuades hingga garis tanda
Dihomogenkan
Ekstrak azolla encer Ekstrak
Ekstrak Azolla Residu
1 g serbuk Azolla yang telah
dikeringkan dibawah sinar matahari
Catatan : Prosedur ini dilakukan untuk masing – masing kompos Azolla dan daun TKKS sesudah pengomposan dengan variasi waktu 5,10,15,20,25,dan 30
3.4.2.2. Pengukuran Absorbansi dari Larutan Standar P untuk kurva Kalibrasi Untuk Larutan standar 2 ppm
Dimasukkan ke dalam tabung reaksi
Ditambahkan 5 ml akuades
Ditambahkan 1 ml larutan campuran pengkompleks
Didiamkan 15 menit
Diukur absorbansinya dengan spektorfotometer pada λ= 710 nm Hasil
Larutan berwarna biru 1 ml larutan standar 2 ppm
3.4.2.3 Pengukuran Absorbansi untuk Ekstrak Azola
Dimasukkan ke dalam tabu ng reaksi
Ditambahkan 5 ml akuades
Ditambahakan 1 ml larutan campuran pengkompleks
Didiamkan 15 menit 1 ml ekstrak azolla
Diukur absorbansinya dengan spektrofotometer pada λ= 710 nm
Larutan berwarna biru
Hasil
Catatan : Prosedur ini dilakukan untuk masing – masing kompos azolla dan TKKS sesudah pengomposan dengan variasi waktu 5,10,15,20.25 dan 30 hari
3.4.3 Penentuan Kadar Nitrogen Azolla
ditambahkan 0,3 gselenium dan H2SO4 pekat
didekstruksi hingga menjadi larutan coklat kehitaman
Dipindahkan ke dalam labu destilasi
Ditambahkan 50 ml akuades
Ditambahakan 3 tetes indikator fenoltalein
Ditambahkan NaOH 40% sampai berwarna merah lembayung
Didestilasi
Ditampung destilat ke dalam gelas erlenmeyer yang berisi 50
ml H3BO3 3% dan 3 tetes indikator campuran hingga berwarna
hijau Larutan coklat kehitaman 0,1 g serbuk Azolla yang telah
dikeringkan
Ditampung di dalam gelas erlenmeyer yang berisi 50 ml
H3BO3 3% dan 3 tetes indikator campuran
Dititrasi dengan HCl 0,01 N
Ditentukan % N
Catatan : prosedur ini dilakukan untuk masing – masing kompos azolla dan TKKS sesudah pengomposan dengan variasi waktu 5,10,15,20,25 dan 30 hari Larutan merah muda
Hasil
Destilat berwarna hijau
41
3.4.4 Penentuan Kalium sebagai K2O dengan Metode Spektrofotometer
Serapan Atom
Didinginkan dalam desikator selama 30 menit
Dimasukkan ke dalam erlenmeyer 100 ml
Dilarutkan dengan 12,5 ml HCl 25%
Didesktruksi selama 3 jam
didiamkan selama 1 malam
Didinginkan, lalu disaring pada labu takar 100 ml dengan
kertas saring whatman no. 40
Diencerkan dengan akuades sampai garis
Didinginkan pada suhu kamar
Didiamkan selama 12 jam
Disaring dengan kertas saring Whatman No. 42
Cawan dicuci tiga kali dengan akuades
Kertas saring dicuci akuades tiga kali dengan akuades
Dibuat pH ± 3 dengan penambahan NH4OH 20% tetes demi
tetes
Diencerkan dengan akuades hingga garis tanda
Konsentrasi K diukur dengan Spektrofotometer Serapan Atom
Di dalam gelas timbangan
Larutan
Filtrat (dalam labu takar 100 ml)
Konsentrasi kalium
BAB IV
HASIL DAN PEMBAHASAN
4.1. Hasil Penelitian
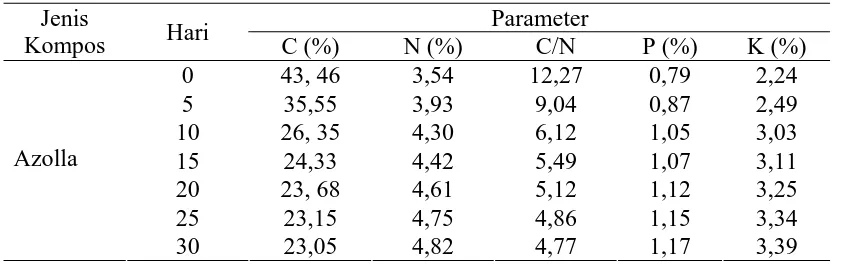
4.1.1 Data Analisa Pengomposan Azolla Tabel 4.1. Pengomposan Azolla
Parameter
Dari data analisa Pengomposan Azolla seperti tabel 4.1 terlihat Perubahan
Konsentrasi C, N, C/N, P, K sebagai berikut :
Pada pengomposan 10 hari penurunan konsentrasi karbon makin rendah dan stabil
sampai hari ke 30. Sedangkan Konsentarsi N, P, dan K terjadi kenaikan tajam sampai
dengan hari ke 10, setelah hari ke sepuluh perubahan konsentrasi N, P, dan K tetap
menunjukkan kenaikan. Dengan demikian diperoleh data C/N sebanding dengan
penurunan konsentarsi C, artinya pada hari ke 10 dapat dikatakan rasio yang paling
baik untuk untuk pengomposan Azolla. Untuk melihat perubahan yang terjadi
pengomposan terus diamati hingga hari ke 30. Perubahan konsentrasi ini dapat dilihat
seperti yang ditunjukkan pada tabel 4.1. Perubahan konsentrasi C, N, C/N, P dan K
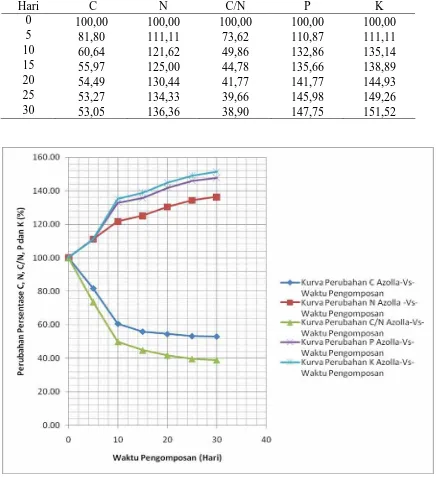
Tabel 4.2. Persentase Perubahan Konsentrasi C, N, C/N, P dan K dari Azolla Selama Pengomposan
Hari C N C/N P K
0 100,00 100,00 100,00 100,00 100,00
5 81,80 111,11 73,62 110,87 111,11
10 60,64 121,62 49,86 132,86 135,14
15 55,97 125,00 44,78 135,66 138,89
20 54,49 130,44 41,77 141,77 144,93
25 53,27 134,33 39,66 145,98 149,26
30 53,05 136,36 38,90 147,75 151,52
4.1.2 Data Analisa Pengomposan TKKS Tabel 4.3 Pengomposan TKKS
Parameter
Pada pengomposan TKKS sampai hari ke 10 terjadi pengurangan konsentrasi
karbon yang lambat , namun setelah hari ke 10 perubahan konsentrasi makin cepat
sampai hari ke 30. Untuk N dan P, mengalami perubahan laju konsentrasi yang relatif
sama. Kenaikan laju konsentrasi N dan P lambat sampai hari ke 15 dan naik cepat
mulai hari ke 15 sampai hari ke 30. Konsentrasi K mengalami perubahan konsentrasi
yang cukup tinggi mulai hari ke 10 sampai dengan hari ke 15 dan terjadi penurunan
konsentrasi K setelah hari ke 15, perubahan relatif stabil sampai hari ke 30. Rasio
C/N terlihat mengikuti perubahan konsentarsi Karbon. Pada hari ke 10 rasio C/N
adalah 61,84 dengan persentase perubahan 93,94 % dan pada hari ke 30 rasio C/N
adalah 33,54 dengan persentase perubahan 50, 96 %. Dilihat dari rasio C/N pada hari
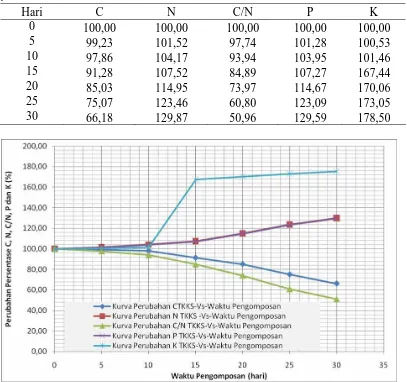
Tabel 4.4. Persentase Perubahan Konsentrasi C, N, C/N, P dan K dari TKKS Selama Pengomposan
.
Hari C N C/N P K
0 100,00 100,00 100,00 100,00 100,00
5 99,23 101,52 97,74 101,28 100,53
10 97,86 104,17 93,94 103,95 101,46
15 91,28 107,52 84,89 107,27 167,44
20 85,03 114,95 73,97 114,67 170,06
25 75,07 123,46 60,80 123,09 173,05
30 66,18 129,87 50,96 129,59 178,50