79
Lampiran 2. Kurva aktivitas antioksidan terhadap Vitamin C Data pengamatan Vitamin C
% Hambatan IC50 4 µg/ml 6 µg/ml 8 µg/ml 10 µg/ml 12 µg/ml 14 µg/ml
39,5788 40,0871 42,4110 44,5171 49,4553 53,8126 12,4724 µg/ml
y = 1.4483x + 31.942 R² = 0.9295
0 10 20 30 40 50 60
0 2 4 6 8 10 12 14 16
P
ers
en
ta
se
h
am
ba
ta
n
(
%
)
Lampiran 3. Data pengamatan analisis kadar air (%) dan Tabel sidik ragam kadar air (%)
Data pengamatan analisis kadar air (%)
Perlakuan Ulangan Total Rataan
1 2
S1K1 12,5182 15,8438 28,3620 14,1810 S1K2 13,6703 11,4077 25,0781 12,5390 S1K3 12,2398 12,0756 24,3153 12,1577 S1K4 11,2658 11,3652 22,6310 11,3155 S2K1 18,0299 19,0096 37,0396 18,5198 S2K2 14,7459 16,5920 31,3379 15,6690 S2K3 11,9978 10,8484 22,8462 11,4231 S2K4 17,1978 11,1682 28,3660 14,1830 S3K1 16,7041 16,3976 33,1017 16,5508 S3K2 17,7873 17,7750 35,5623 17,7812 S3K3 19,2761 16,1460 35,4222 17,7111 S3K4 16,7254 15,0404 31,7658 15,8829 S4K1 18,5763 18,2205 36,7968 18,3984 S4K2 16,4408 15,8774 32,3182 16,1591 S4K3 18,4114 18,8105 37,2219 18,6110 S4K4 17,6111 17,1977 34,8088 17,4044
Total 495,9737
Rataan 15,5304
Tabel sidik ragam kadar air (%)
SK db JK KT F Hit F 0,05 F 0,01
81
Lampiran 4. Data pengamatan analisis kadar vitamin C (mg/100g) dan Tabel sidik ragam vitamin C (mg/100g)
Data pengamatan analisis kadar vitamin C (mg/100g)
Perlakuan Ulangan Total Rataan
1 2
Tabel sidik ragam kadar vitamin C (mg/100g)
Lampiran 5. Data pengamatan analisis total asam (%) dan Tabel sidik ragam total asam (%)
Data pengamatan analisis total asam (%)
Perlakuan Ulangan Total Rataan
1 2
Tabel sidik ragam total asam (%)
SK db JK KT F hit. F 0,05
83
Lampiran 6. Data pengamatan analisis total soluble solid (oBrix) dan Tabel sidik ragam total soluble solid (oBrix)
Data pengamatan analisis total soluble solid (oBrix)
Perlakuan Ulangan Total Rataan
1 2
Tabel sidik ragam Total Soluble Solid (oBrix)
SK db JK KT F hit. F 0,05
Lampiran 7. Data pengamatan analisis kadar abu (%) dan Tabel sidik ragam kadar abu (%)
Data pengamatan analisis kadar abu (%)
Perlakuan Ulangan Total Rataan
1 2
Tabel sidik ragam kadar abu (%)
SK db JK KT F Hit F 0,05 F 0,01
85
Lampiran 8. Data pengamatan analisis nilai warna L dan Tabel sidik ragam nilai warna L
Data pengamatan analisis nilai warna L
Perlakuan Ulangan Total Rataan
1 2
S1K1 29,93 31,76 61,69 30,85 S1K2 31,13 30,35 61,48 30,74 S1K3 30,50 28,50 59,00 29,50 S1K4 29,04 26,59 55,63 27,82 S2K1 34,63 31,49 66,12 33,06 S2K2 31,04 30,75 61,79 30,90
S2K3 31,16 28,29 59,45 29,73
S2K4 30,76 28,07 58,83 29,42 S3K1 34,51 38,30 72,81 36,41 S3K2 33,32 30,24 63,56 31,78 S3K3 31,94 28,90 60,84 30,42 S3K4 30,57 30,32 62,89 31,45 S4K1 34,93 38,31 73,24 36,62 S4K2 30,74 33,96 64,70 32,35 S4K3 31,51 31,34 62,85 31,43 S4K4 33,05 31,86 64,91 32,46
Total 1007,79
Rataan 31,49
Tabel sidik ragam nilai warna L
Lampiran 9. Data pengamatan analisis nilai warna a dan Tabel sidik ragam nilai warna a
Data pengamatan analisis nilai warna a
Perlakuan Ulangan Total Rataan
1 2
Tabel sidik ragam nilai warna a
SK db JK KT F Hit F 0,05 F 0,01 Galat 16 53,7581 3,3599
Total 31 1502,2586 48,4600 Keterangan :
FK = 31.738,77 tn = tidak nyata KK = 5,493%
87
Lampiran 10. Data pengamatan analisis nilai warna b dan Tabel sidik ragam nilai warna b
Data pengamatan analisis nilai warna b
Perlakuan Ulangan Total Rataan
1 2
Tabel sidik ragam nilai warna b
Lampiran 11. Data pengamatan analisis hedonik warna dan Tabel sidik ragam hedonik warna
Data pengamatan analisis hedonik warna
Perlakuan Ulangan Total Rataan
1 2
S1K1 3,4000 3,3333 6,7333 3,3667
S1K2 3,0000 2,9333 5,9333 2,9667
S1K3 3,4667 3,0667 6,5333 3,2667
Tabel sidik ragam analisa hedonik warna
89
Lampiran 12. Data pengamatan analisis hedonik aroma dan Tabel sidik ragam hedonik aroma
Data pengamatan analisis hedonik aroma
Perlakuan Ulangan Total Rataan
1 2
Tabel sidik ragam hedonik aroma
Lampiran 13. Data pengamatan analisis hedonik rasa dan Tabel sidik ragam hedonik rasa
Data pengamatan analisis hedonik rasa
Perlakuan Ulangan Total Rataan
1 2
Tabel sidik ragam hedonik rasa
91
Lampiran 14. Data pengamatan analisis hedonik tekstur dan Tabel sidik ragam hedonik tekstur
Data pengamatan analisis hedonik tekstur
Perlakuan Ulangan Total Rataan
1 2
S1K1 3,7333 3,6000 7,3333 3,6667
S1K2 3,8667 3,6000 7,4667 3,7333
S1K3 3,6667 3,8667 7,5333 3,7667
S4K4 2,0000 1,8000 3,8000 1,9000
Total 97,6000
Rataan 3,0500
Tabel sidik ragam hedonik tekstur
Lampiran 15. Data pengamatan analisis skor tekstur dan Tabel sidik ragam skor tekstur
Data pengamatan analisis skor tekstur
Perlakuan Ulangan Total Rataan
1 2
Tabel sidik ragam skor tekstur
SK db JK KT F Hit F 0,05 F 0,01
93
Lampiran 16. Data pengamatan gula reduksi permen jelly dengan perlakuan terbaik.
S2K3 = Sorbitol : Sari Ubi Jalar Ungu (60% : 40%), Konsentrasi Karagenan (3%) U1 = Ulangan pertama
Lampiran 17. Data pengamatan aktivitas antioksidan permen jelly dengan
S2K3U1 0,0504 31,1547 32,6071 33,3333 37,8359 41,0312 46,6231 52,3602 56,2092 184,6535 µg/ml S2K3U2 0,0515 31,2273 31,7357 32,5345 36,3834 39,6514 46,5505 51,2709 55,8460 190,6863 µg/ml Rataan 187,6699 µg/ml
Keterangan:
S2K3 = Sorbitol : Sari Ubi Jalar Ungu (60% : 40%), Konsentrasi Karagenan (3%) U1 = Ulangan pertama
95
Lampiran 18. Spesifikasi sorbitol cair
Spesifikasi sorbitol 70% Batch original : 503031770
Ex : PT. Sorini Agro Asia Corp. (Cargill) Mfg date : 03/2015
Expire date : 03/2017 pH : 5,.0 – 7,0 Brix : 65,0 – 70,0 indeks bias : 1, 455 – 1,465
97
Lampiran 20. Foto produk permen jelly
Sari ubi jalar ungu Sari jeruk nipis
Foto produk dari semua kombinasi perlakuan
S1K1 S1K2 S1K3 S1K4
Keterangan :
S1K1 = Perbandingan konsentrasi sorbitol dengan sari ubi jalar ungu 50% : 50% dan konsentrasi karagenan 1%
S1K2 = Perbandingan konsentrasi sorbitol dengan sari ubi jalar ungu 50% : 50% dan konsentrasi karagenan 2%
S1K3 = Perbandingan konsentrasi sorbitol dengan sari ubi jalar ungu 50% : 50% dan konsentrasi karagenan 3%
99
S2K1 S2K2 S2K3 S2K4
Keterangan :
S2K1 = Perbandingan konsentrasi sorbitol dengan sari ubi jalar ungu 60% : 40% dan konsentrasi karagenan 1%
S2K2 = Perbandingan konsentrasi sorbitol dengan sari ubi jalar ungu 60% : 40% dan konsentrasi karagenan 2%
S2K3 = Perbandingan konsentrasi sorbitol dengan sari ubi jalar ungu 60% : 40% dan konsentrasi karagenan 3%
S3K1 S3K2 S3K3 S3K4
Keterangan :
S3K1 = Perbandingan konsentrasi sorbitol dengan sari ubi jalar ungu 70% : 30% dan konsentrasi karagenan 1%
S3K2 = Perbandingan konsentrasi sorbitol dengan sari ubi jalar ungu 70% : 30% dan konsentrasi karagenan 2%
S3K3 = Perbandingan konsentrasi sorbitol dengan sari ubi jalar ungu 70% : 30% dan konsentrasi karagenan 3%
101
S4K1 S4K2 S4K3 S4K4
Keterangan :
S4K1 = Perbandingan konsentrasi sorbitol dengan sari ubi jalar ungu 80% : 20% dan konsentrasi karagenan 1%
S4K2 = Perbandingan konsentrasi sorbitol dengan sari ubi jalar ungu 80% : 20% dan konsentrasi karagenan 2%
S4K3 = Perbandingan konsentrasi sorbitol dengan sari ubi jalar ungu 80% : 20% dan konsentrasi karagenan 3%
S4K4 = Perbandingan konsentrasi sorbitol dengan sari ubi jalar ungu 80% : 20% dan konsentrasi karagenan 4%
DAFTAR PUSTAKA
Adina, A.B., F.F. Handoko, I.I. Setyarini, dan E. Sulistyorini. 2014. Jeruk nipis (Citrus aurantifolia). http://ccrc.farmasi.ugm.ac.id (12 November 2015). Agustin, F. dan Putri, W. 2014. Pembuatan jellydrink Averrhoa blimbi L. (Kajian
proporsi belimbing wuluh : air dan konsentrasi karagenan). Jurnal Pangan dan Agroindustri, 2(3): 1-9.
AOAC. 1995. Official Methods of Analysis of The Association of Official Analytical Chemists. AOAC, Washington.
Apriliyanti, T. 2010. Kajian sifat fisikokimia dan sensori tepung ubi jalar ungu (Ipomoea batatas blackie) dengan variasi proses pengeringan. Skripsi Program Studi Teknologi Hasil Pertanian Fakultas Pertanian Universitas Sebelas Maret, Surakarta.
Apriyantono, A., D. Fardiaz, N. L. Puspitasari, Sedarwati, dan S. Budiyanto, 1989. Petunjuk Laboratorium Analisa Pangan. Pusat Antar Universitas Pangan Dan Gizi, Institut Pertanian Bogor.
Atmaka, W., B. Sigit dan C. Monris. 2013. Pengaruh berbagai konsentrasi sorbitol terhadap karakteristik sensoris, kimia dan kapasitas antioksidan getuk ubi jalar ungu (Ipomoea Batatas) selama penyimpanan. Jurnal Teknosains Pangan. 2 (3):43-50.
Bangun, M. K. 1991. Perancangan Percobaan. USU-Press, Medan.
Belitz, H. D., dan W. Grosch. 1987. Food Chemistry. Translation from the second German edition by D. Hadziyev. Department of food science University of Alberta, Canada.
Buckle, K. A., R. A. Edwards, G.H. Fleet dan M. Wootton. 1987. Ilmu Pangan. Penerjemah H. Purnomo dan Adiono, UI-Press, Jakarta.
Departemen Kesehatan RI., 1996. Daftar Komposisi Bahan Makanan. Bhratara Karya Aksara, Jakarta.
Dianitami, R. 2009. Efek rumput laut Eucheuma sp. terhadap kadar glukosa darah dan jumlah trombosit tikus Wistar yang diinduksi aloksan. Laporan akhir penelitian karya tulis ilmiah. Fakultas Kedokteran Universitas Diponegoro, Semarang.
74
Dwivedi, B. K. 1991. Sorbitol dalam L. O. Nabors & R. C. Gelardi (Ed). 1991. Alternative Sweeteners. 2nd edition. Marcel Dekker Inc, New York.
Estiasih, T dan K. Ahmadi. 2009. Teknologi Pengolahan Pangan. PT Bumi Aksara, Jakarta.
Furia, T. E. 1992. CRC Handbook of Food Additives. CRC Press, Boston.
Garrow, J.S. dan W.P.T. James. 1993. Human Nutrition and Dietetics. Longman Singapore, Singapore.
Goldberg, I. 1994. Functional Foods. Chapmann Hall, New York.
Haq, G. T., A. Permanasari, dan H. Sholihin. 2010. Efektivitas penggunaan sari buah jeruk nipis terhadap ketahanan nasi. Jurnal Sains dan Teknologi Kimia. 1 (1) : 44-58.
Harijono, J. Kusnadi, dan S.A. Mustikasari. 2001. Pengaruh kadar karagenan dan total padatan terlarut sari buah apel muda terhadap aspek kualitas permen
jelly. Jurnal Teknologi Pertanian. 2(2): 110 – 116.
Hidayat, N. dan I. Ken. 2004. Membuat Permen Jelly. Penerbit Trubus Agrisarana. Surabaya.
Houwink B.1993. Ilmu Kedokteran Gigi Pencegahan. Gadjah Mada University Press ,Yogyakarta.
Hutchings, J. B. 1999. Food Color and Appearance, 2nd editions. Springer,
Maryland.
Indrati, R., dan M. Gardjito. 2014. Pendidikan Konsumsi Pangan; Aspek Pengolahan dan Keamanan. Kencana, Jakarta.
Jaya, E. F. P. 2013. Pemanfaatan antioksidan dan betakaroten ubi jalar ungu pada pembuatan minuman non-beralkohol. Media Gizi Masyarakat Indonesia. 2(2):54-57.
Juanda, D. dan B. Cahyono. 2000. Ubi Jalar Budi Daya dan Analisis Usaha Tani. Penerbit Kanisius,Yogyakarta.
Kamal, N. 2010. Pengaruh bahan aditif CMC (Carboxyl methyl cellulose) terhadap beberapa parameter pada larutan sukrosa. Jurnal Teknologi. 1(17): 78-84.
Kobori, M. 2003. In vitro screening for cancer suppressive effect of food components. JARQ 37(3): 159–165.
Kusumaningsih, T. 1999. Hubungan antar indeks keparahan karies dengan jumlah
Lactobacillus sp. di dalam saliva anak taman kanak-kanak. Majalah Kedokteran Gigi FKG Unair. 32(4): 291-6.
Lingga, P., B. Sarwono, F. Rahardi, C. Raharja, J. J. Anfiastini, W. Rini, dan W. H. Apriadji. 1986. Bertanam Umbi-umbian. PT. Penebar Swadaya, Jakarta.
Liur, I. J., A. F. Musfiroh, M. Mailoa, R. Bremeer, V. P. Bintoro, dan Kusrahayu. 2013. Potensi penerapan tepung ubi jalar dalam pembuatan bakso sapi. Jurnal Aplikasi Teknologi Pangan. 2(1): 40-42.
Lukas A., W. Purwanto dan A.Y. Ridwam. 2011. Soft candy dari bahan aktif oleoresin temulawak (Curcuma xanthorhiza Roxb.). Jurnal Sains dan Teknologi Indonesia. 13(3):151-158.
Milani, J. dan Maleki, G. 2012. Food Industrial Processes – Methods and Equipment. InTech, Croatia.
Murdinah. 2010. Pemanfaatan rumput laut dan fitokoloid untuk produk pangan dalam rangka penelitian nilai tambah dan diversifikasi pangan. Penelitian. Balai Besar Riset. Pengolahan Produk dan Bioteknologi Kelautan dan Perikanan.
Pietrasik, Z. dan A. Jarmolouk. 2003. Effect of sodium caseinate and k-carrageenan on binding and textural properties of pork muscle gels enhanced by microbial transglutaminase addition. Journal of Food Engineering. 6 (3): 285-294.
Pokamy, J., N. Yanishlieva, dan M. Gordon. 2001. Antioxidant in Food; Practical and Application. CRC Press, New York.
Ramadhan, W. 2011. Pemanfaatan agar-agar tepung sebagai texturizer pada formulasi selai jambu biji merah (Psidium guajava L.) lembaran dan pendugaan umur simpannya. Skripsi. IPB. Bogor.
Ranganna, S. 1978. Manual of Analysis for Fruit and Vegetable Products. Mc. Graw Hill Publishing Company Limited, New Delhi.
Rozi, F. dan R. Krisdiana. 2005. Prospek Ubi Jalar Berdaging Ungu Sebagai Makanan Sehat dalam Mendukung Ketahanan Pangan. Laporan Penelitian. Balai Penelitian Tanaman Kacang-kacangan dan Umbi-umbian, Malang.
76
Sarwono, B. 2001. Khasiat dan Manfaat Jeruk Nipis. PT AgroMedia Pustaka, Jakarta.
Sidi, N. C., E. Widowati, dan A .Nursiwi. 2014. Pengaruh penambahan karagenan pada karakteristik fisikokimia dan sensoris fruit leather nanas (Ananas Comosus L. Merr.) dan wortel (Daucus Carota). Jurnal Aplikasi Teknologi Pangan 3 (4): 122-127.
Soekarto, S.T. 1985. Penilaian Organoleptik Untuk Pangan dan Hasil Pertanian. Bhratara Karya Aksara, Jakarta.
Soerarti, W., N. Rasita, dan E. R. Himawati. 2004. Pengaruh jenis humektan terhadap pelepasan asam sitrat dari basis gel secara in vitro. J. Phar. 4 (2) ISSN: 0852-1050.
Soesilo D., R. E. Santoso dan I. Diyatri. 2005. Peranan sorbitol dalam mempertahankan kestabilan pH saliva pada proses pencegahan karies. Maj. Ked. Gigi. (Dent. J.). 38(1): 25–28.
Standar Nasional Indonesia (SNI). 1994. Kadar Abu. SNI 01-3451-1994. Dewan Standarisasi Indonesia.
Standar Nasional Indonesia (SNI). 2008. Permen Jelly. SNI 3547-02-2008. Dewan Standarisasi Indonesia.
Sudarmanto. 1990. Bahan Pewarna Alami dalam Tanaman Pangan. PAU Pangan dan Gizi. UGM. Yogyakarta.
Sudaryati, H. P. dan Mulyani, T. 2003. The manufacture of lemon jelly candy by the addition of gelatine & glucose-sucrose proportion. Seminar Nasional dan Perhimpunan Ahli Teknologi Pangan Indonesia, Yogyakarta. (1156-1162).
Suismono. 2001. Teknologi Pembuatan Tepung dan Pati Ubi-Ubian untuk menunjang Ketahanan Pangan. Majalah pangan nomor: 37/X/Juli/2001 Hal. 37-49.
Sumarny, R., Djamil, R., dan Afrilia, I. S. 2012. Kadar kurkumin dan potensi antioksidan ekstrak etanol rimpang temu putih (Curcuma zedoaria (Berg) Roscoe), temu mangga (Curcuma mangga Val et Zyp) dan temu lawak (Curcuma xanthorrhiza Roxb). Prosiding Seminar Nasional Pokjanas TOI XLII. 1(1): 1-9.
Syafutri, M. I., E. Lidiasari, dan H. Indawan. 2010. Karakteristik permen jelly timun suri (Cucumis melo L.) dengan penambahan sorbitol dan ekstrak Kunyit (Curcuma domestika Val.). Jurnal Gizi dan Pangan . 5(2): 78 – 86. Tarigan, R. 1993. Karies gigi. Cetakan ke-3. Hipokrates, Jakarta.
Tarwiyati. 2007. Desain dan uji kinerja pasteurisasi non thermal menggunakan sinar ultraviolet (Kajian pada nira kelapa dengan pengujian dosis sinar ultraviolet). Universitas Brawijaya. Malang.
Willett, N.P, R.R White, dan S. Rose. 1991. Essential Dental Microbiology. Connecticut. Prentice-Hall, New York.
Winarno, F. G. 1990. Teknologi Pengolahan Rumput Laut. Pustaka Sinar Harapan, Jakarta.
Winarno, F. G. 1992. Kimia Pangan dan Gizi. Gramedia Pustaka Utama, Jakarta.
Winarsi, H. 2008. Antioksidan Alami dan Radikal Bebas: Potensi dan Aplikasinya dalam Kesehatan. Kanisius, Yogyakarta.
Winarti , S. 2010. Makanan fungsional. Graha ilmu, Yogyakarta.
BAHAN DAN METODE
Waktu dan Tempat Penelitian
Penelitian dilaksanakan di Laboratorium Teknologi Pangan dan di
Laboratorium Analisa Kimia Bahan Pangan, Fakultas Pertanian Universitas
Sumatera Utara. Waktu penelitian dilakukan pada bulan Juni hingga Juli 2015.
Bahan Penelitian
Bahan yang digunakan dalam penelitian ini adalah ubi jalar ungu dan jeruk
nipis yang diperoleh dari pasar tradisional yang berada di Medan. Bahan lain yaitu
sorbitol cair 70% dari PT. Brataco, karagenan komersil (ekstrak dari rumput laut)
dari Lansida, dan CMC.
Reagensia
Reagensia yang digunakan dalam penelitian ini adalah indikator
phenolphtalein 1%, NaOH 0,01 N, alkohol 80%, larutan DNS (1,3
Dinitrosalisilat), larutan Dye (Di-klorofenil indofenol), asam askorbat, asam
oksalat, akuades, metanol pro analisis, dan larutan DPPH
(1,1-difenil-2-pikrilhidrazil).
Alat Penelitian
Alat yang digunakan dalam penelitian ini adalah untuk membuat permen
jelly yaitu baskom, pisau stainless steel, talenan, panci kukus stainless steel,
sendok pengaduk, timbangan, cetakan jelly, loyang, oven blower, thermometer,
kain saring, dan blender. Peralatan yang digunakan untuk mengetahui mutu
Jepang), alat gelas laboratorium, kertas saring, kapas, cawan porselen, tanur,
desikator, handrefractometer, incubator, danspektrofotometer UV (Genesys 20).
Metode Penelitian
Penelitian ini dilakukan dengan menggunakan rancangan acak lengkap
(RAL), yang terdiri dari dua faktor, yaitu:
Faktor I : Perbandingan konsentrasi sorbitol dan sari ubi jalar ungu (S) :
S1 = 50% :50%
S2 = 60%: 40%
S3 = 70% :30%
S4 = 80% :20%
Faktor II : Konsentrasi karagenan (K) :
K1 = 1%
K2 = 2%
K3 = 3%
K4 = 4%
Banyaknya kombinasi perlakuan atau Treatment Combination (Tc) adalah 4x4 =
16, dengan jumlah ulangan sebanyak 2 kali, sehingga jumlah sampel keseluruhan
adalah 32 sampel.
Model Rancangan (Bangun, 1991)
Penelitian ini dilakukan dengan Rancangan Acak Lengkap (RAL) faktorial
dengan model :
17
Keterangan:
ijk : Hasil pengamatan dari faktor S pada taraf ke-i dan faktor K pada taraf ke-j
dengan ulangan ke-k
µ : Efek nilai tengah
αi : Efek dari faktor S pada taraf ke-i
βj : Efek dari faktor K pada taraf ke-j
(αβ)ij : Efek interaksi faktor S pada taraf ke-i dan faktor K pada taraf ke-j
εijk : Efek galat dari faktor S pada taraf ke-i dan faktor K pada taraf ke-j dalam
ulangan ke-k
Apabila diperoleh hasil yang berbeda nyata atau sangat nyata maka
dilanjutkan dengan uji LSR (Least Significant Range).
Pelaksanaan Penelitian
Pembuatan sari ubi jalar ungu
Ubi jalar ungu disortasi, dikupas, dicuci bersih, dipotong-potong,
diblansing dengan uap pada suhu 80 oC selama 5 menit, dan diblender dengan
penambahan air, perbandingan ubi jalar ungu dan air sebesar 1:2, kemudian
disaring dengan menggunakan kain saring sehingga diperoleh sari ubi jalar ungu.
Skema pembuatan sari ubi jalar ungu dapat dilihat pada Gambar 4.
Pembuatan sari jeruk nipis
Jeruk nipis disortasi, dicuci, dipotong-potong dan diperas, kemudian
disaring sehingga diperoleh sari jeruk nipis. Skema pembuatan sari jeruk nipis
Pembuatan permen jelly
Sorbitol dan sari ubi jalar ungu ditimbang dan dicampur berdasarkan taraf
perlakuan (50%:50%, 60%:40%, 70%:30%, 80%:20%) sebanyak 200 g.
Dilakukan penambahan karagenan sesuai taraf perlakuan (1%, 2%, 3%, 4%),
CMC 2% dan sari jeruk nipis 10% dari berat bahan kemudian dilarutkan.
Dilakukan pemasakan dan pengadukan hingga suhu mencapai 80 oC kemudian api
dimatikan. Kemudian diangkat, dicetak, dan didinginkan pada suhu ruang.
Selanjutnya dikeringkan dengan oven blower pada suhu 50 oC selama 48 jam.
Permen jelly dikemas dan disimpan selama 3 hari kemudian dilakukan
pengamatan dan pengukuran data berupa penentuan kadar air, kadar vitamin C,
total asam, total soluble solid (TSS), kadar abu, nilai warna L, a, b, serta uji
organoleptik warna, aroma, rasa dan tekstur. Perlakuan terbaik dilakukan
pengujian gula reduksi dan aktivitas antioksidan. Skema pembuatan permen jelly
dapat dilihat pada Gambar 6.
Pengamatan dan Pengukuran Data
Pengamatan dan pengukuran data dilakukan dengan cara analisis terhadap
parameter sebagai berikut :
Penentuan kadar air
Kadar air ditentukan dengan metode AOAC (1995) yang dimodifikasi.
Sampel sebanyak 5 g dimasukkan ke dalam cawan alumunium yang telah
dikeringkan selama satu jam pada suhu 80 oC dan telah diketahui beratnya.
Sampel tersebut dipanaskan pada suhu 80 oC selama enam jam, kemudian
didinginkan dalam desikator selama 15 menit, kemudian ditimbang. Pemanasan
19
Kadar Air = Berat sampel awal (g) – Berat sampel akhir (g) x 100% Berat sampel awal (g)
Penentuan kadar vitamin C
Kadar vitamin C dilakukan berdasarkan metode spektrofotometer yang
telah dimodifikasi. Pembuatan larutan Dye yaitu ditimbang 100 mg
2,6-diklorofenol dan 84 mg sodium bikarbonat. Dilarutkan dengan akuades kemudian
dimasukkan ke dalam labu ukur 100 ml dan ditambahkan akuades sampai batas
tera, disaring dengan menggunakan kertas saring. Dipipet larutan sebanyak 25 ml
dan diterakan pada labu ukur 500 ml.
Ditimbang bahan 5 g ditambahkan asam oksalat 6% sampai 50 ml, diambil
5 ml ditambahkan asam oksalat 6% sampai 100 ml. Diambil 5 ml ekstrak sampel
kemudian dimasukkan ke dalam kuvet atau tabung reaksi kering. Ditambahkan 10
ml larutan Dye, kemudian dikocok dan segera dilakukan pengukuran absorbansi
larutan pada panjang gelombang 518 nm.
Pembuatan kurva standar dilakukan dengan membuat larutan asam
askorbat. Ditimbang asam askorbat 100 mg dan ditambahkan asam oksalat 6%
hingga batas tera 100 ml. Diambil 4 ml larutan asam askorbat kemudian
ditambahkan asam oksalat 6% sampai volume 100 ml. Dipipet masing-masing 1
ml, 2 ml, 3 ml, 4 ml, dan 5 ml larutan ke dalam tabung reaksi. Diencerkan dengan
asam oksalat6% sampai volume 5 ml. Ditambahkan dengan cepat 10 ml larutan
Dye, kemudian dikocok dan segera dilakukan pengukuran absorbansi larutan pada
panjang gelombang 518 nm (Apriyantono, dkk., 1989). Kurva standar asam
askorbat dapat dilihat pada Lampiran 1.
Vitamin C (mg/100g) =
Berat sampel awal (g) – Berat sampel akhir (g) x 100% Berat sampel awal (g)
Penentuan total asam
Ditimbang sampel sebanyak 10 g, dihaluskan dan dimasukkan ke dalam
labu ukur dan ditambahkan akuades sampai volume 100 ml. Diaduk hingga
merata dan disaring dengan kertas saring. Diambil filtrate-nya sebanyak 10 ml dan
dimasukkan ke dalam Erlenmeyer lalu ditambahkan phenolphtalein 2-3 tetes
kemudian dititrasi dengan menggunakan NaOH 0,01 N. Titrasi dihentikan setelah
timbul warna merah jambu yang stabil (Ranganna, 1978).
ml NaOH x N NaOH x BM asam dominan x FP x 100% Total asam (%) =
Berat sampel (g) x 1000 x valensi
Keterangan :
BM = Berat molekul asam sitrat (C6H8O7) yaitu 192 valensi 3.
FP = Faktor Pengencer
Penentuan total soluble solid
Diambil sampel yang telah dihaluskan sebanyak 5 g dan dimasukkan ke
dalam beaker glass. Ditambahkan akuades hingga volume 15 ml kemudian diaduk
hingga merata. Diambil satu tetes larutan dan diteteskan dalam handrefractometer
lalu dilihat angka di titik terang dan gelapnya (Ranganna, 1978).
Total padatan terlarut (oBrix) = angka handrefractometer x FP
Keterangan :
FP = Faktor pengencer
Penentuan kadar abu
Sampel sebanyak 5 g dimasukkan ke dalam cawan porselin kering yang
telah diketahui beratnya (yang terlebih dulu dibakar dalam tanur dan didinginkan
dalam desikator). Kemudian sampel dipijarkan diatas pembakar mecker kira-kira ml NaOH x N NaOH x BM asam dominan x FP x 100%
21
1 jam, mula-mula api kecil dan selanjutnya api dibesarkan secara perlahan-lahan
sampai terjadi perubahan contoh menjadi arang. Arang dimasukkan ke dalam
tanur dengan suhunya 500 oC sampai terbentuk abu. Setelah itu cawan yang berisi
abu didinginkan sampai mencapai suhu kamar dan selanjutnya ditimbang beratnya
(SNI-01-3451-1994). Kadar abu dihitung dengan rumus sebagai berikut:
Kadar abu = Bobot abu (g) x 100% Bobot sampel (g)
Penentuan nilai warna L, a dan b (Metode Hunter)
Pengujian warna dilakukan dengan menggunakan kromameter Konika
Minolta (tipe CR-400, Jepang). Sejumlah sampel ditempatkan pada wadah yang
datar. Pengukuran menghasilkan nilai L, a, dan b dari sampel dengan kisaran 0
(hitam) sampai ± 100 (putih). L menyatakan parameter kecerahan. Warna
kromatik campuran merah hijau ditunjukkan oleh nilai a dengan nilai “+a”
(positif) dari 0 sampai + 80 untuk warna merah dan nilai “–a “ (negatif) dari 0
sampai – 80 untuk warna hijau. Warna kromatik campuran biru kuning
ditunjukkan oleh nilai b dengan nilai nilai “+b” (positif) dari 0 sampai + 80 untuk
warna kuning dan nilai “–b “ (negatif) dari 0 sampai – 80 untuk warna biru.
(Hutchings, 1999).
Uji organoleptik warna, aroma, rasa dan tekstur
Organoleptik terhadap warna, aroma, rasa dan tekstur ditentukan dengan
uji hedonik dan uji skor untuk organoleptik tekstur. Caranya contoh yang telah
diberi kode diuji secara acak oleh 15 panelis. Pengujian dilakukan secara indrawi
(organoleptik) yang ditentukan berdasarkan skala numerik dan skor
(Soekarto, 1985). Untuk skala hedonik warna, aroma, rasa, dan tekstur dapat
Tabel 4. Skala hedonik warna, aroma, rasa, dan tekstur
Skala hedonik warna Skala numerik
Sangat suka
Tabel 5. Skala skor tekstur
Skala skor tekstur Skala numerik
Prinsip metode ini adalah dalam suasana alkali gula pereduksi akan
mereduksi 3,5-dinitrosalisilat (DNS) membentuk senyawa yang dapat diukur
absorbansinya pada panjang gelombang 550 nm. Persiapan pereaksi DNS dibuat
dengan melarutkan 10,6 g asam 3,5-dinitrosalisilat dan 19,8 g NaOH ke dalam
1416 ml air ditambahkan ke dalam larutan tersebut 106 g NaK-tartarat. 7,6 ml
fenol (cairkan pada suhu 50ºC) dan 8,3 g Na-metabisulfit, dicampur merata.
Dilakukan standarisasi dengan melakukan titrasi 3 ml pereaksi DNS dengan HCL
0,1 N dan indikator fenolftalein. Dibutuhkan 5-6 ml HCL 0,1 N, jika kurang dari
itu ditambahkan 2 g NaOH untuk setiap kekurangan 0,1 ml HCL 0,1 N.
Penentuan kurva standar dibuat dengan mengukur nilai gula pereduksi
pada glukosa pada selang 0,2-0,5 mg/ml. Masing-masing konsentrasi sebanyak 1
ml ditambahkan dengan 3 ml pereaksi DNS. Ditempatkan dalam air mendidih
selama 15 menit. Dibiarkan dingin sampai suhu ruang. Selanjutnya intensitas
23
panjang gelombang 550 nm. Kurva standar dibuat dengan memplot konsentrasi
glukosa terhadap absorbansinya.
Penetapan gula reduksi pada sampel yaitu ditimbang sampel sebanyak 2 g
yang telah dihaluskan dimasukkan ke dalam beaker glass 100 ml, lalu
ditambahkan alkohol 80% 50 ml, kemudian distirer selama 1 jam. Kemudian
disaring ke dalam labu ukur 250 ml dan ditambahkan akuades sampai batas tera.
Dipanaskan dalam waterbath selama 1 jam untuk menghilangkan alkohol. Setelah
dingin ditambahkan akuades sampai batas tera kemudian distiter. Diambil 1 ml
dan 9 ml aquadest yang kemudian dimauskkan ke dalam tabung reaksi dan
digojog dengan vortex. Setelah itu diambil 1 ml larutan tersebut dan dimasukkan
ke dalam tabung reaksi tertutup. Dilakukan penambahan DNS sebanyak 3 ml dan
digojog dengan vortex. Kemudian dipanaskan selama 15 menit dan didinginkan
selama 30 menit. Ukur absorbansi dengan spektrofotometer pada panjang
gelombang 550 nm (Apriyantono dkk., 1989).
Konsentrasi gula (mg/ml) x Faktor pengencer
Kadar gula reduksi = x 100% Bobot Sampel (g) x 1000
Uji aktivitas antioksidan dengan metode DPPH (Sumarny, dkk., 2012)
1. Pembuatan larutan DPPH (0,4 mM)
Ditimbang lebih kurang 15,8 mg DPPH (1,1-difenil-2-pikrilhidrazil),
kemudian dilarutkan dengan metanol pro analisis hingga 100 ml pada labu ukur,
ditempatkan dalam botol gelap.
2. Pembuatan larutan blanko (larutan DPPH)
Dipipet 1 ml larutan DPPH (0,4 mM) ke dalam labu ukur 5 ml dan
3. Pembuatan larutan uji
Ditimbang 5,0 mg sampel kemudian dilarutkan dalam 5 ml metanol pro
analisis (1000 bpj), larutan ini merupakan larutan induk. Dipipet 25 µl, 50 µl, 125
µl, 250 µl, 500 µl, 750 µl, 1000 µl, dan 1500 µl larutan induk (triplo) ke dalam
labu ukur 5 ml untuk mendapatkan konsentrasi sampel 5, 10, 25, 50, 100, 150,
200, dan 300 µg/ml. Ke dalam masing-masing labu ukur ditambahkan 1 ml
larutan DPPH, ditambahkan dengan metanol pro analisis sampai tanda tera,
kemudian dihomogenkan.
4. Pembuatan larutan vitamin C
Ditimbang 5 mg vitamin C kemudian dilarutkan dalam 5 ml metanol pro
analisis (1000 bpj), larutan ini merupakan induk. Dipipet 20 µl, 30 µl, 40 µl, 50
µl, 60 µl, dan 70 µl larutan induk (triplo) ke dalam labu ukur 5 ml untuk
mendapatkan konsentrasi sampel 4, 6, 8, 10, 12, dan 14 µg/ml ke dalam
masing-masing labu ukur ditambahkan 1 ml larutan DPPH dan ditambahkan dengan
metanol pro analisis sampai tanda tera kemudian dihomogenkan.
5. Uji aktivitas antioksidan
Larutan uji dan larutan vitamin C dengan beberapa konsentrasi diinkubasi
pada suhu 37 ºC selama tepat 30 menit, serapan diukur pada panjang gelombang
maksimum 517 nm menggunakan spektrofotometri UV-VIS. Persentase inhibisi
dihitung menggunakan rumus sebagai berikut :
% hambatan = Absorbansi blanko – absorbansi sampel x 100%
Absorbansi blanko
Perhitungan nilai IC50 dengan memasukkan nilai dari konsentrasi larutan
uji (sumbu x) dan % hambatan terhadap DPPH (sumbu y) ke dalam persamaan Absorbansi blanko (larutan DPPH) – absorbansi sampel x 100%
25
garis regresi. Semakin rendah nilai IC50 berarti semakin tinggi aktivitas
antioksidan sebagai peredam radikal bebas. Aktivitas suatu senyawa dikatakan
memiliki aktivitas tinggi jika mempunyai nilai IC50 di bawah 20 bpj, aktivitas
sedang jika mempunyai nilai IC50 21 – 100 bpj, aktivitas rendah jika mempunyai
nilai IC50 101 – 200 bpj dan tidak aktif jika mempunyai nilai IC50 di atas 200 bpj.
Gambar 4. Skema pembuatan sari ubi jalar ungu
Gambar 5. Skema pembuatan sari jeruk nipis Disortasi, dikupas, dicuci dan dipotong-potong
Diblansing dengan uap pada suhu 80 oC
selama 5 menit
Disaring dengan kain saring
Sari ubi jalar ungu
Diblender dengan perbandingan buah dan air 1: 2
Ubi jalar ungu
Jeruk nipis
Disortasi dan dicuci
Dipotong-potong dan diperas
Disaring
27
Gambar 6. Skema pembuatan permen jelly
Ditimbang sorbitol dan sari ubi jalar ungu
sebanyak 200 g
Dicetak dan didinginkan pada suhu ruang
Parameter yang diuji:
- Penentuan kadar air
- Penentuan kadar vitamin C
- Penentuan total asam
- Penentuan total soluble solid (TSS)
- Penentuan kadar abu
- Penentuan nilai warna L, a, dan b
- Uji organoleptik terhadap warna, aroma, rasa, dan tekstur
Perbandingan
Dipanaskan dan diaduk hingga mencapai
suhu 80 oC kemudian api dimatikan
Ditambahkan karagenan, CMC 2%, sari jeruk nipis 10% diaduk hingga larut Konsentrasi
Dikeringkan dengan oven blower dengan suhu 50 oC selama 48 jam
Perlakuan terbaik
Permen jelly
Parameter yang diuji:
- Penentuan gula reduksi
- Penentuan aktivitas antioksidan
HASIL DAN PEMBAHASAN
Hasil penelitian yang dilakukan pada permen jelly menunjukkan adanya
pengaruh perbandingan konsentrasi sorbitol dengan sari ubi jalar ungu dan
konsentrasi karagenan terhadap parameter yang diamati yaitu sebagai berikut.
Pengaruh Perbandingan Konsentrasi Sorbitol dengan Sari Ubi Jalar Ungu terhadap Parameter yang Diamati
Berdasarkan penelitian yang telah dilakukan, perbandingan sorbitol dengan
sari ubi jalar ungu pada produk permen jelly memberikan pengaruh terhadap
parameter kadar air (%), kadar vitamin C (mg/100g), total asam(%), total soluble
solid (oBrix), kadar abu (%), nilai warna L, a, b, nilai hedonik warna, aroma, rasa, tekstur dan nilai skor tekstur dapat dilihat pada Tabel 6.
Tabel 6. Pengaruh perbandingan sorbitol dengan sari ubi jalar ungu terhadap parameter yang diamati.
Parameter
Perbandingan konsentrasi sorbitol dengan sari ubi jalar ungu (S)
29
Pengaruh Konsentrasi Karagenan terhadap Parameter yang Diamati
Hasil penelitian menunjukkan bahwa penambahan karagenan memberikan
pengaruh terhadap parameter yang diuji yaitu kadar air (%), kadar vitamin C
(mg/100g), total asam (%), total soluble solid (oBrix), kadar abu (%), nilai warna
L, a, b, nilai hedonik warna, aroma, rasa, tekstur serta nilai skor tekstur seperti
pada Tabel 7.
Tabel 7. Pengaruh konsentrasi karagenan terhadap parameter yang diamati.
Parameter
Kadar vitamin C (mg/100g) Total asam (%)
Pengaruh perbandingan konsentrasi sorbitol dengan sari ubi jalar ungu terhadap kadar air permen jelly
Kadar air permen jelly dari perbandingan konsentrasi sorbitol dengan sari
ubi jalar ungu memberikan pengaruh yang berbeda sangat nyata (P<0,01) dapat
dilihat dari daftar sidik ragam (Lampiran 3). Hasil uji LSR pengaruh
perbandingan konsentrasi sorbitol dengan sari ubi jalar ungu dapat dilihat pada
Tabel 8. Uji LSR efek utama pengaruh konsentrasi sorbitol dengan sari ubi jalar
ungu terhadap kadar air permen jelly
Jarak LSR Perbandingan sorbitol Rataan
(%)
Keterangan : Notasi huruf berbeda menunjukkan pengaruh yang berbeda nyata pada taraf 5% (huruf kecil) dan berbeda sangat nyata pada taraf 1% (huruf besar)
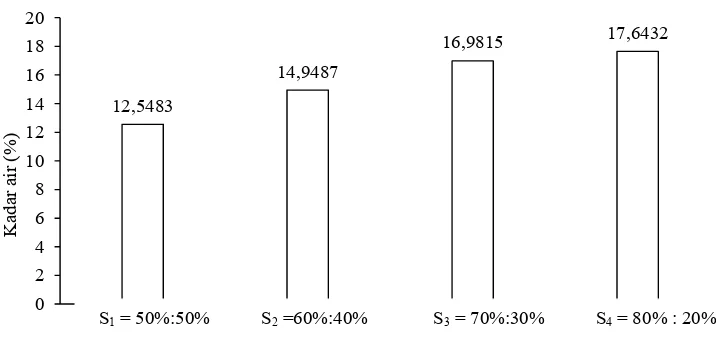
Dari Tabel 8, dapat dilihat bahwa kadar air tertinggi terdapat pada
perlakuan S4 (80% : 20%) yaitu sebesar 17,6432% dan terendah terdapat pada
perlakuan S1 (50% : 50%) yaitu sebesar 12,5483%. Hubungan konsentrasi sorbitol
dengan sari ubi jalar ungu dengan kadar air permen jelly dapat dilihat pada
Gambar 7.
Gambar 7. Hubungan konsentrasi sorbitol dengan sari ubi jalar ungu dengan kadar
air permen jelly
Berdasarkan Gambar 7, menunjukkan bahwa semakin tinggi konsentrasi
sorbitol yang ditambahkan maka semakin tinggi kadar air pada permen jelly. Hal
ini disebabkan sorbitol yang bersifat sebagai humektan. Menurut Soerarti, 12,5483
Konsentrasi sorbitol : sari ubi jalar ungu (%)
31
dkk., (2004), humektan merupakan suatu bahan yang dapat mempertahankan
kelembaban sehingga kadar air dapat dipertahankan serta dapat menurunkan aktivitas
air (aw) sehingga dapat melindungi produk dari pemanasan dan menjaga kesegaran
produk. Syafutri, dkk., (2010) menyatakan bahwa semakin tinggi konsentrasi
sorbitol maka semakin banyak air yang terikat sehingga penguapan air semakin
kecil yang menyebabkan kadar air bahan tinggi.
Pengaruh konsentrasi karagenan terhadap kadar air permen jelly
Hasil sidik ragam (Lampiran 3) memberikan pengaruh berbeda nyata
(P<0,05) terhadap kadar air permen jelly. Hasil uji LSR pengaruh konsentrasi
karagenan terhadap kadar air permen jelly dapat dilihat pada Tabel 9.
Tabel 9. Uji LSR efek utama pengaruh konsentrasi karagenan terhadap kadar air
permen jelly
Jarak LSR Konsentrasi
karagenan
Rataan (%)
Notasi
0,05 0,05
- - K1= 1% 16,9125 a
2 1,5873 K2= 2% 15,5371 ab
3 1,6646 K3= 3% 14,9757 b
4 1,7128 K4= 4% 14,6964 b
Keterangan : Notasi huruf berbeda menunjukkan pengaruh yang berbeda nyata pada taraf 5% (huruf kecil)
Berdasarkan Tabel 9, dapat dilihat bahwa kadar air tertinggi terdapat pada
perlakuan K1 (1%) yaitu sebesar 16,9125% dan terendah terdapat pada perlakuan
K4 (4%) yaitu sebesar 14,6964%. Hubungan antara konsentrasi karagenan dengan
Gambar 8. Hubungan antara konsentrasi karagenan dengan kadar air permen jelly Berdasarkan Gambar 8, menunjukkan semakin banyak konsentrasi
karagenan yang digunakan maka kadar air pada permen jelly semakin rendah. Hal
ini disebabkan karagenan memiliki kemampuan dalam membentuk metrik gel
tiga dimensi yang dapat mengikat air. Pietrasik dan Jarmolouk (2003)
menjelaskan bahwa penambahan karagenan semakin tinggi akan meningkatkan
ikatan matrik gel dan memperkecil struktur berongga. Semakin kuat ikatan matrik
gel yang terbentuk maka air akan terikat semakin banyak sedangkan air bebas
akan semakin sedikit sehingga penguapan air semakin kecil yang menyebabkan
kadar air produk rendah.
Pengaruh interaksi antara perbandingan konsentrasi sorbitol dengan sari ubi jalar ungu dan konsentrasi karagenan terhadap kadar air permen jelly
Dari daftar sidik ragam (Lampiran 3) dapat dilihat bahwa interaksi antara
perbandingan konsentrasi sorbitol dengan sari ubi jalar ungu dan konsentrasi
karagenan memberikan pengaruh berbeda tidak nyata (P>0,05) terhadap kadar air
permen jelly yang dihasilkan sehingga uji LSR tidak dilanjutkan.
33
Kadar Vitamin C (mg/100g)
Pengaruh perbandingan konsentrasi sorbitol dengan sari ubi jalar ungu terhadap kadar vitamin C permen jelly
Kadar vitamin C permen jelly dari perbandingan konsentrasi sorbitol
dengan sari ubi jalar ungu jika dilihat dari daftar sidik ragam (Lampiran 4)
memberikan pengaruh berbeda sangat nyata (P<0,01) terhadap kadar vitamin C
permen jelly yang dihasilkan. Hasil uji LSR pengaruh perbandingan konsentrasi
sorbitol dengan sari ubi jalar ungu terhadap kadar vitamin C permen jelly dapat
dilihat pada Tabel 10.
Tebel 10. Uji LSR efek utama pengaruh konsentrasi sorbitol dengan sari ubi jalar
ungu terhadap kadar vitamin C permen jelly
Jarak
LSR Perbandingan sorbitol
Rataan (mg/100g)
Notasi
0,05 0,01 dengan sari ubi Jalar
ungu 0,05 0,01
- - - S1 = 50% : 50% 25,6854 a A
2 1,5235 2,0993 S2 = 60% : 40% 24,8744 a A
3 1,5977 2,1892 S3 = 70% : 30% 22,3644 b B
4 1,6440 2,2487 S4 = 80% : 20% 21,5072 b B
Keterangan : Notasi huruf berbeda menunjukkan pengaruh yang berbeda nyata pada taraf 5% (huruf kecil) dan berbeda sangat nyata pada taraf 1% (huruf besar)
Kadar vitamin C tertinggi terdapat pada perlakuan S1 (50% : 50%) yaitu
sebesar 25,6854 mg/100g dan terendah pada perlakuan S4 (80% : 20%) yaitu
sebesar 21,5072 mg/100g. Hubungan konsentrasi sorbitol dengan sari ubi jalar
Gambar 9. Hubungan konsentrasi sorbitol dengan sari ubi jalar ungu dengan kadar
vitamin C permen jelly
Semakin rendah konsentrasi sari ubi jalar ungu yang ditambahkan maka
semakin rendah kandungan vitamin C pada permen jelly yang dihasilkan. Menurut
Winarti (2010) ubi jalar ungu mengandung vitamin C sebesar 22 mg/100 g bahan.
Hal ini didukung berdasarkan pengujian Departemen Kesehatan RI (1996),
kandungan vitamin C ubi jalar ungu sebesar 21,43 (mg/100g) bahan.
Pengaruh konsentrasi karagenan terhadap kadar vitamin C permen jelly
Dari daftar sidik ragam (Lampiran 4) dapat dilihat bahwa konsentrasi
karagenan memberikan pengaruh berbeda tidak nyata (P>0,05) terhadap kadar
vitamin C permen jelly yang dihasilkan sehingga uji LSR tidak dilanjutkan.
Pengaruh interaksi antara perbandingan konsentrasi sorbitol dengan sari ubi jalar ungu dan konsentrasi karagenan terhadap kadar vitamin C permen jelly
Dari daftar sidik ragam (Lampiran 4) dapat dilihat bahwa interaksi antara
perbandingan konsentrasi sorbitol dengan sari ubi jalar ungu dan konsentrasi 25,6854 24,8744
Konsentrasi sorbitol : sari ubi jalar ungu (%)
35
karagenan memberikan pengaruh berbeda tidak nyata (P>0,05) terhadap kadar
vitamin C permen jelly yang dihasilkan sehingga uji LSR tidak dilanjutkan.
Total Asam (%)
Pengaruh perbandingan konsentrasi sorbitol dengan sari ubi jalar ungu terhadap total asam permen jelly
Total asam permen jelly dari perbandingan konsentrasi sorbitol dengan sari
ubi jalar ungu, jika dilihat pada daftar sidik ragam (Lampiran 5) memberikan
pengaruh yang berbeda sangat nyata (P<0,01). Hasil uji LSR pengaruh
perbandingan konsentrasi sorbitol dengan sari ubi jalar ungu terhadap total asam
permen jelly dapat dilihat pada Tabel 11.
Tabel 11. Uji LSR efek utama pengaruh perbandingan konsentrasi sorbitol dengan
sari ubi jalar ungu terhadap total asam permen jelly
Jarak
LSR Perbandingan sorbitol
Rataan
Keterangan : Notasi huruf yang berbeda menunjukkan pengaruh yang berbeda nyata pada taraf 5% (huruf kecil) dan berbeda sangat nyata pada taraf 1% (huruf besar)
Berdasarkan Tabel 11, total asam tertinggi terdapat pada perlakuan S1
(50% : 50%) yaitu sebesar 0,2701% dan terendah pada perlakuan S4 (80% : 20%)
yaitu sebesar 0,1863%. Semakin tinggi sorbitol yang ditambahkan maka total
asam permen jelly semakin rendah. Menurut Atmaka, dkk., (2013), penggunaan
sorbitol yang semakin tinggi cenderung menurunkan ion H+ pada bahan yang
dihasilkan. Hal ini didukung dengan pernyataan Syafutri, dkk., (2010) bahwa
sehingga menurunkan total asam bahan. Hubungan konsentrasi sorbitol dengan
sari ubi jalar ungu dengan total asam permen jelly dapat dilihat pada Gambar 10.
Gambar 10. Hubungan konsentrasi sorbitol dengan sari ubi jalar ungu dengan total
asam permen jelly
Pengaruh konsentrasi karagenan terhadap total asam permen jelly
Berdasarkan daftar sidik ragam (Lampiran 5) dapat dilihat bahwa
konsentrasi karagenan memberikan pengaruh berbeda sangat nyata (P<0,01)
terhadap total asam permen jelly yang dihasilkan. Hasil uji LSR pengaruh
konsentrasi karagenan terhadap total asam permen jelly dapat dilihat pada Tabel
12.
Tabel 12. Uji LSR efek utama pengaruh konsentrasi karagenan terhadap total
asam permen jelly
Jarak LSR Konsentrasi Rataan
(%)
Keterangan : Notasi huruf yang berbeda menunjukkan pengaruh yang berbeda nyata pada taraf 5%
(huruf kecil) dan berbeda sangat nyata pada taraf 1% (huruf besar)
Konsentrasi sorbitol : sari ubi jalar ungu (%)
37
Total asam tertinggi terdapat pada perlakuan K1 yaitu sebesar 0,2581%
dan terendah terdapat pada perlakuan K4 yaitu sebesar 0,2138%. Hubungan antara
konsentrasi karagenan dengan total asam permen jelly dapat dilihat pada Gambar
11.
Gambar 11. Hubungan antara konsentrasi karagenan dengan total asam permen jelly
Berdasarkan Gambar 11, semakin tinggi konsentrasi karagenan maka total
asam permen jelly semakin rendah. Penurunan total asam terjadi pada konsentrasi
karagenan kurang dari 2% sedangkan pada konsentrasi karagenan lebih dari 2%
penurunan total asam terjadi secara tidak nyata. Menurut Agustin dan Putri
(2014), terjadinya penurunan total asam disebabkan karagenan yang memiliki
gugus OH- yang relatif banyak serta kandungannya yang berupa kalsium,
potassium, natrium dan magnesium yang dapat bereaksi dengan asam membentuk
garam sehingga menurunkan keasaman. Gugus OH- pada karagenan akan
berikatan dengan asam yang merupakan H+ sehingga semakin banyak karagenan
yang ditambahkan maka akan menurunkan total asam.
Pengaruh interaksi antara perbandingan konsentrasi sorbitol dengan sari ubi jalar ungu dan konsentrasi karagenan terhadap total asam permen jelly
Berdasarkan tabel sidik ragam (Lampiran 5) dapat dilihat bahwa interaksi
antara perbandingan konsentrasi sorbitol dengan sari ubi jalar ungu dan
konsentrasi karagenan memberikan pengaruh yang berbeda sangat nyata (P<0,01)
terhadap total asam pemen jelly yang dihasilkan. Hasil uji LSR pengaruh interaksi
antara perbandingan konsentrasi sorbitol dengan sari ubi jalar ungu dan
konsentrasi karagenan terhadap total asam dapat dilihat pada Tabel 13.
Tabel 13. Uji LSR pengaruh interaksi antara perbandingan konsentrasi sorbitol dengan sari ubi jalar ungu dan konsentrasi karagenan terhadap total
asam permen jelly.
Keterangan : Notasi huruf berbeda menunjukkan pengaruh yang berbeda nyata pada taraf 5% (huruf kecil) dan berbeda sangat nyata pada taraf 1% (huruf besar)
Berdasarkan Tabel 13, dapat diketahui bahwa total asam tertinggi terdapat
pada perlakuan S1K1 yaitu sebesar 0,2788% dan terendah pada perlakuan S4K4
39
dengan sari ubi jalar ungu dan konsentrasi karagenan dengan total asam permen
jelly dapat dilihat pada Gambar 12.
Gambar 12. Hubungan interaksi perbandingan konsentrasi sorbitol dengan sari ubi
jalar ungu dan konsentrasi karagenan dengan total asam permen jelly
Berdasarkan Gambar 12, dapat dilihat bahwa semakin tinggi konsentrasi
sorbitol dan semakin tinggi konsentrasi karagenan maka semakin rendah total
asam pada permen jelly. Menurut Agustin dan Putri (2014) dan Syafutri, dkk.,
(2010) menyatakan, hal ini disebabkan sorbitol dan karagenan sama sama
memiliki gugus OH- yang dapat mengikat gugus H+ sehingga dapat menurunkan
total asam pada permen jelly yang dihasilkan.
Total Soluble Solid (oBrix)
Pengaruh perbandingan konsentrasi sorbitol dengan sari ubi jalar ungu terhadap total soluble solid permen jelly
Berdasarkan daftar sidik ragam (lampiran 6) dapat dilihat bahwa
perbandingan konsentrasi sorbitol dengan sari ubi jalar ungu memberikan
pengaruh berbeda sangat nyata (P<0,01) terhadap total soluble solid permen jelly
yang dihasilkan. Hasil uji LSR pengaruh perbandingan konsentrasi sorbitol
dengan sari ubi jalar ungu terhadap total soluble solid dapat dilihat pada Tabel 14.
Tabel 14. Uji LSR efek utama pengaruh perbandingan konsentrasi sorbitol dengan
sari ubi jalar ungu terhadap total soluble solid permen jelly
Jarak
LSR Perbandingan sorbitol
Rataan
Keterangan : Notasi huruf berbeda menunjukkan pengaruh yang berbeda nyata pada taraf 5% (huruf kecil) dan berbeda sangat nyata pada taraf 1% (huruf besar)
Berdasarkan Tabel 14, dapat diketahui bahwa total soluble solid tertinggi
terdapat pada perlakuan S4 (80% : 20%) yaitu sebesar 70,8741 oBrix dan terendah
terdapat pada perlakuan S1 (50% : 50%) yaitu sebesar 55,7270 oBrix. Hubungan
antara konsentrasi sorbitol dengan sari ubi jalar ungu dengan total soluble solid
dapat dilihat pada Gambar 13.
Gambar 13. Hubungan antara konsentrasi sorbitol dengan sari ubi jalar ungu
dengan total soluble solid permen jelly.
55.7270 58.0042
Konsentasi sorbitol : sari ubi jalar ungu (%)
41
Berdasarkan Gambar 13, menunjukkan semakin tinggi sorbitol yang
ditambahkan maka semakin tinggi total soluble solid permen jelly yang
dihasilkan. Sorbitol cair 70% memiliki nilai oBrix yaitu 65-70 (Lampiran 18).
Buckle, dkk., (1987) menyatakan bahwa kadar gula pada produk menunjukkan
tingginya total padatan terlarut sehingga semakin tinggi kadar gula yang diberikan
maka total padatan terlarut pada produk akan semakin besar.
Pengaruh konsentrasi karagenan terhadap total soluble solid permen jelly
Berdasarkan daftar sidik ragam (Lampiran 6) dapat dilihat bahwa
konsentrasi karagenan memberikan pengaruh berbeda tidak nyata (P>0,05)
terhadap total soluble solid permen jelly yang dihasilkan sehingga uji LSR tidak
dilanjutkan.
Pengaruh interaksi antara perbandingan konsentrasi sorbitol dengan sari ubi jalar ungu dan konsentrasi karagenan terhadap total soluble solid permen jelly
Berdasarkan daftar sidik garam (Lampiran 6) dapat dilihat bahwa interaksi
antara perbandingan konsentrasi sorbitol dengan sari ubi jalar ungu dan
konsentrasi karagenan memberikan pengaruh berbeda nyata (P<0,05) terhadap
total soluble solid permen jelly yang dihasilkan. Hasil uji LSR pengaruh interaksi antara perbandingan konsentrasi sorbitol dengan sari ubi jalar ungu dan
konsentrasi karagenan terhadap total soluble solid permen jelly dapat dilihat pada
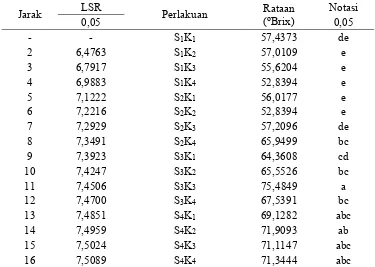
Tabel 15. Berdasarkan tabel 15, dapat diketahui bahwa total soluble solid tertinggi
terdapat pada perlakuan S3K3 yaitu sebesar 75,4849 oBrix dan terendah pada
Tabel 15. Uji LSR pengaruh interaksi antara perbandingan konsentrasi sorbitol
dengan sari ubi jalar ungu dan konsentrasi karagenan terhadap total
soluble solid permen jelly
Jarak LSR Perlakuan Rataan
Keterangan : Notasi huruf berbeda menunjukkan pengaruh yang berbeda nyata pada taraf 5% (huruf kecil)
Semakin tinggi penambahan sorbitol dan karagenan maka total soluble
solid yang dihasilkan akan semakin tinggi. Tarwiyati (2007) menyatakan nilai total padatan terlarut menunjukkan nilai total gula secara keseluruhan dengan
satuan oBrix. Pada lampiran 18 menunjukkan bahwa sorbitol cair 70% memiliki
padatan terlarut sebesar 65-70 oBrix. Estiasih dan Ahmadi (2009) juga
menyatakan bahwa karagenan dapat menstabilkan bahan dalam bentuk suspensi
dan dapat mengikat gula-gula, sehingga padatan terlarut yang ada pada produk
dapat diikat dan dipertahankan. Hubungan interaksi perbandingan konsentrasi
sorbitol dengan sari ubi jalar ungu dan konsentrasi karagenan dengan total soluble
43
Gambar 14. Hubungan interaksi perbandingan konsentrasi sorbitol dengan sari ubi
jalar ungu dan konsentrasi karagenan dengan total soluble solid
permen jelly
Kadar Abu (%)
Pengaruh perbandingan konsentrasi sorbitol dengan sari ubi jalar ungu terhadap kadar abu permen jelly
Berdasarkan daftar sidik ragam (Lampiran 7), bahwa perbandingan
konsentrasi sorbitol dengan sari ubi jalar ungu memberikan pengaruh berbeda
sangat nyata (P<0,01) terhadap kadar abu permen jelly yang dihasilkan. Hasil uji
LSR pengaruh perbandingan konsentrasi sorbitol dengan sari ubi jalar ungu
terhadap kadar abu permen jelly dapat dilihat pada Tabel 16. Berdasarkan Tabel
16, dapat dilihat bahwa kadar abu tertinggi terdapat pada perlakuan S1 (50% :
50%) yaitu sebesar 1,4571% dan terendah terdapat pada perlakuan S4 (80% :
20%) yaitu sebesar 1,1378%.
Tabel 16. Uji LSR efek utama pengaruh perbandingan konsentrasi sorbitol dengan
sari ubi jalar ungu terhadap kadar abu permen jelly
Jarak
LSR Perbandingan sorbitol
Rataan
Keterangan : Notasi huruf berbeda menunjukkan pengaruh yang berbeda nyata pada taraf 5% (huruf kecil) dan berbeda sangat nyata pada taraf 1% (huruf besar)
Semakin rendah konsentrasi sari ubi jalar ungu yang digunakan pada
permen jelly maka kadar abu yang dihasilkan semakin rendah. Penurunan kadar
abu pada perlakuan S1, S2, dan S3 memberikan pengaruh tidak nyata namun
penurunan kadar abu pada perlakuan S4 memberikan pengaruh sangat nyata.
Menurut Liur, dkk., (2013) dalam penelitiannya kadar abu ubi jalar ungu sebesar
2,03%. Terjadinya penurunan kadar abu diduga karena penambahan sari ubi jalar
ungu yang semakin sedikit sehingga mempengaruhi kadar abu pada permen jelly
yang dihasilkan. Hubungan antara konsentrasi sorbitol dengan sari ubi jalar ungu
dengan kadar abu permen jelly dapat dilihat pada Gambar 15.
Konsentrasi sorbitol : sari ubi jalar ungu (%)
S1 = 50%:50% S2 =60%:40% S3 = 70%:30% S4 = 80% : 20%
Gambar 15. Hubungan antara konsentrasi sorbitol dengan sari ubi jalar ungu
45
Pengaruh konsentrasi karagenan terhadap kadar abu permen jelly
Berdasarkan daftar sidik ragam (Lampiran 7) dapat dilihat bahwa
konsentrasi karagenan memberikan pengaruh berbeda sangat nyata (P<0,01)
terhadap kadar abu permen jelly yang dihasilkan. Hasil uji LSR pengaruh
konsentrasi karagenan terhadap kadar abu permen jelly dapat dilihat pada Tabel
17.
Tabel 17. Uji LSR efek utama pengaruh konsentrasi karagenan terhadap kadar abu
permen jelly
Jarak LSR Konsentrasi Rataan
(%)
Keterangan : Notasi huruf berbeda menunjukkan pengaruh yang berbeda nyata pada taraf 5% (huruf kecil) dan berbeda sangat nyata pada taraf 1% (huruf besar)
Tabel 17, dapat dilihat bahwa kadar abu tertinggi terdapat pada perlakuan
K4 (4%) yaitu sebesar 1,7424% dan terendah terdapat pada perlakuan K1 (1%)
yaitu sebesar 0,8473%. Hubungan antara konsentrasi karagenan dengan kadar abu
permen jelly dapat dilihat pada Gambar 16.
Berdasarkan Gambar 16, menunjukkan semakin tinggi karagenan yang
ditambahkan maka kadar abu permen jelly yang dihasilkan semakin tinggi.
Menurut Sidi, dkk., (2014) dan Santoso, dkk., (2004), peningkatan kadar abu pada
bahan disebabkan oleh kandungan kadar abu yang terdapat pada kappa karagenan
berupa kandungan mineral yang cukup tinggi. Milani dan Maleki (2012)
menambahkan bahwa karagenan mampu membentuk jala tiga dimensi. Jala tiga
dimensi ini dapat mengikat kandungan mineral pada produk sehingga mineral
yang terkandung dapat dipertahankan.
Pengaruh interaksi antara perbandingan konsentrasi sorbitol dengan sari ubi jalar ungu dan konsentrasi karagenan terhadap kadar abu permen jelly
Berdasarkan daftar sidik ragam (Lampiran 7) dapat dilihat bahwa interaksi
antara perbandingan konsentrasi sorbitol dengan sari ubi jalar ungu dan
konsentrasi karagenan memberikan pengaruh berbeda sangat nyata (P<0,01)
terhadap kadar abu permen jelly yang dihasilkan. Hasil uji LSR pengaruh interaksi
antara perbandingan konsentrasi sorbitol dengan sari ubi jalar ungu dan
konsentrasi karagenan terhadap kadar abu permen jelly dapat dilihat pada Tabel
18. Berdasarkan Tabel 18, dapat diketahui bahwa kadar abu tertinggi terdapat
pada perlakuan S1K4 yaitu sebesar 1,9148% dan terendah pada perlakuan S4K1
yaitu sebesar 0,6986%. Semakin tinggi konsentrasi sari ubi jalar ungu yang
digunakan serta semakin tinggi karagenan yang ditambahkan maka kadar abu
permen jelly yang dihasilkan semakin tinggi. Menurut Liur, dkk., (2013) dalam
47
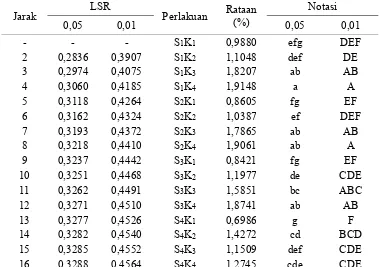
Tabel 18. Uji LSR pengaruh interaksi antara perbandingan konsentrasi sorbitol dengan sari ubi jalar ungu dan konsentrasi karagenan terhadap kadar
abu permen jelly
Jarak LSR Perlakuan Rataan
(%)
Notasi
0,05 0,01 0,05 0,01
- - - S1K1 0,9880 efg DEF
2 0,2836 0,3907 S1K2 1,1048 def DE
3 0,2974 0,4075 S1K3 1,8207 ab AB
4 0,3060 0,4185 S1K4 1,9148 a A
5 0,3118 0,4264 S2K1 0,8605 fg EF
6 0,3162 0,4324 S2K2 1,0387 ef DEF
7 0,3193 0,4372 S2K3 1,7865 ab AB
8 0,3218 0,4410 S2K4 1,9061 ab A
9 0,3237 0,4442 S3K1 0,8421 fg EF
10 0,3251 0,4468 S3K2 1,1977 de CDE
11 0,3262 0,4491 S3K3 1,5851 bc ABC
12 0,3271 0,4510 S3K4 1,8741 ab AB
13 0,3277 0,4526 S4K1 0,6986 g F
14 0,3282 0,4540 S4K2 1,4272 cd BCD
15 0,3285 0,4552 S4K3 1,1509 def CDE
16 0,3288 0,4564 S4K4 1,2745 cde CDE
Keterangan : Notasi huruf berbeda menunjukkan pengaruh yang berbeda nyata pada taraf 5% (huruf kecil) dan berbeda sangat nyata pada taraf 1% (huruf besar)
Milani dan Maleki (2012) menambahkan bahwa karagenan mampu
membentuk jala tiga dimensi. Jala tiga dimensi ini dapat mengikat kandungan
mineral pada produk sehingga mineral yang terkandung dapat dipertahankan.
Hubungan interaksi perbandingan konsentrasi sorbitol dengan sari ubi jalar ungu
dan konsentrasi karagenan dengan kadar abu permen jelly dapat dilihat pada
Gambar 17. Hubungan interaksi perbandingan konsentrasi sorbitol dengan sari ubi
jalar ungu dan konsentrasi karagenan dengan kadar abu permen jelly
Nilai Warna L
Pengaruh perbandingan konsentrasi sorbitol dengan sari ubi jalar ungu terhadap nilai warna L permen jelly
Nilai warna L dari perbandingan konsentrasi sorbitol dengan sari ubi jalar
ungu dapat dilihat pada Lampiran 8. Hasil analisis ragam pada Lampiran 8
menunjukkan bahwa perbandingan konsentrasi sorbitol dengan sari ubi jalar ungu
memberikan pengaruh berbeda sangat nyata (P<0,01) terhadap nilai warna L
permen jelly. Hasil uji LSR pengaruh perbandingan konsentrasi sorbitol dengan
sari ubi jalar ungu terhadap nilai warna L permen jelly dapat dilihat pada Tabel
19. Dari Tabel 19, dapat dilihat bahwa nilai warna L tertinggi terdapat pada
perlakuan S4 (80% : 20%) yaitu sebesar 33,21 dan terendah pada perlakuan S1
49
Tabel 19. Uji LSR efek utama pengaruh perbandingan konsentrasi sorbitol dengan
sari ubi jalar ungu terhadap nilai warna L permen jelly
Jarak
LSR Perbandingan sorbitol
Rataan
Notasi
0,05 0,01 dengan sari ubi jalar
ungu 0,05 0,01
- - - S1 = 50% : 50% 29,73 c B
2 1,8337 2,5267 S2 = 60% : 40% 30,77 bc AB
3 1,9230 2,6349 S3 = 70% : 30% 32,26 ab A
4 1,9786 2,7065 S4 = 80% : 20% 33,21 a A
Keterangan : Notasi huruf berbeda menunjukkan pengaruh yang berbeda nyata pada taraf 5% (huruf kecil) dan berbeda sangat nyata pada taraf 1% (huruf besar)
Semakin rendah konsentrasi sari ubi jalar ungu maka nilai warna L atau
tingkat kecerahan dari permen jelly semakin tinggi sedangkan pada permen jelly
yang lebih banyak sari ubi jalar ungu memiliki warna yang lebih pekat atau keruh.
Hal ini disebabkan adanya kandungan pigmen warna yaitu antosianin yang tinggi
serta adanya pati pada sari ubi jalar ungu yang tergelatinisasi oleh adanya
pemanasan yang menyebabkan kekeruhan pada permen jelly yang dihasilkan.
Sudarmanto dkk., (1990) menambahkan bahwa peningkatan kadar gula juga akan
mengurangi kandungan pigmen, sehingga semakin sedikit sari ubi jalar ungu yang
ditambahkan maka warna permen jelly menjadi lebih cerah atau tingkat
kekeruhannya semakin berkurang. Hubungan antara konsentrasi sorbitol dengan
sari ubi jalar ungu dengan nilai warna L permen jelly dapat dilihat pada Gambar
Gambar 18. Hubungan antara konsentrasi sorbitol dengan sari ubi jalar ungu
dengan nilai warna L permen jelly
Pengaruh konsentrasi karagenan terhadap nilai warna L permen jelly
Dari daftar sidik ragam (Lampiran 8) dapat dilihat bahwa konsentrasi
karagenan memberi pengaruh berbeda sangat nyata (P<0,01) terhadap nilai warna
L permen jelly yang dihasilkan. Hasil uji LSR pengaruh konsentrasi karagenan
terhadap nilai warna L permen jelly dapat dilihat pada Tabel 20.
Tabel 20. Uji LSR efek utama pengaruh konsentrasi karagenan terhadap nilai
warna L permen jelly
Jarak LSR Konsentrasi Rataan Notasi
0,05 0,01 karagenan 0,05 0,01
- - - K1= 1% 34,23 a A
2 1,8337 2,5267 K2= 2% 31,44 b B
3 1,9230 2,6349 K3= 3% 30,27 b B
4 1,9786 2,7065 K4= 4% 30,03 b B
Keterangan : Notasi huruf berbeda menunjukkan pengaruh yang berbeda nyata pada taraf 5% (huruf kecil) dan berbeda sangat nyata pada taraf 1% (huruf besar)
Berdasarkan Tabel 20, dapat dilihat bahwa nilai warna L tertinggi terdapat
pada perlakuan K1 (1%) yaitu sebesar 34,23 dan terendah terdapat pada perlakuan
K4 (4%) yaitu sebesar 30,03. Hubungan konsentrasi karagenan dengan nilai warna
L permen jelly dapat dilihat pada Gambar 19. Aaaaaaaaaaaaaaaaaaaaaaaaaaaaaaa
29.73 30.77 32.26 33.21
Konsentrasi sorbitol : sari ubi jalar ungu (%)
51
Gambar 19. Hubungan antara konsentrasi karagenan dengan nilai warna L
permen jelly
Berdasarkan Gambar 19, dapat dilihat semakin tinggi konsentrasi
karagenan yang ditambahkan maka semakin rendah nilai warna L yang dihasilkan.
Hal ini disebakan warna karagenan memiliki warna putih kekuningan yang
menyebabkan semakin banyak konsentrasi karagenan yang ditambahkan ke dalam
permen jelly menyebabkan kecerahan permen jelly menjadi semakin menurun
nilainya. Harijono dkk., (2001) menyatakan dalam penelitiannya penambahan
konsentrasi karagenan yang tinggi akan menghasilkan permen jelly yang kokoh
namun intensitas warna yang dihasilkan akan semakin berkurang.
Pengaruh interaksi antara perbandingan konsentrasi sorbitol dengan sari ubi jalar ungu dan konsentrasi karagenan terhadap nilai warna L permen
jelly
Dari daftar sidik ragam (Lampiran 8) dapat dilihat bahwa interaksi antara
perbandingan konsentrasi sorbitol dengan sari ubi jalar ungu dan konsentrasi
karagenan memberikan pengaruh berbeda tidak nyata (P>0,05) terhadap nilai
warna L permen jelly yang dihasilkan sehingga uji LSR tidak dilanjutkan.
Nilai Warna a
Pengaruh perbandingan konsentrasi sorbitol dengan sari ubi jalar ungu terhadap nilai warna a permen jelly
Nilai warna a dari perbandingan konsentrasi sorbitol dengan sari ubi jalar
ungu dapat dilihat pada Lampiran 9. Hasil analisis ragam pada Lampiran 9
menunjukkan bahwa perbandingan konsentrasi sorbitol dengan sari ubi jalar ungu
memberikan pengaruh berbeda sangat nyata (P<0,01) terhadap nilai warna a
permen jelly. Hasil uji LSR pengaruh perbandingan konsentrasi sorbitol dengan
sari ubi jalar ungu terhadap indeks warna a permen jelly dapat dilihat pada Tabel
21. Dari Tabel 21, dapat dilihat bahwa nilai warna a tertinggi terdapat pada
perlakuan S4 (80% : 20%) yaitu sebesar 27,97 dan terendah pada perlakuan S1
(50% : 50%) yaitu sebesar 13,49.
Tabel 21. Uji LSR efek utama pengaruh perbandingan konsentrasi sorbitol dengan
sari ubi jalar ungu terhadap nilai warna a permen jelly
Jarak
LSR Perbandingan Sorbitol
Rataan
Notasi
0,05 0,01 dengan Sari Ubi Jalar
Ungu 0,05 0,01
- - - S1 = 50% : 50% 13,49 c C
2 1,9429 2,6771 S2 = 60% : 40% 13,77 c C
3 2,0375 2,7919 S3 = 70% : 30% 24,68 b B
4 2,0965 2,8677 S4 = 80% : 20% 27,97 a A
Keterangan : Notasi huruf berbeda menunjukkan pengaruh yang berbeda nyata pada taraf 5% (huruf kecil) dan berbeda sangat nyata pada taraf 1% (huruf besar)
Semakin sedikit sari ubi jalar ungu yang ditambahkan maka warna merah
dari permen jelly yang dihasilkan semakin merah cerah sedangkan semakin
banyak sari ubi jalar ungu yang ditambahkan maka warna yang dihasilkan akan
menjadi merah gelap. Hal ini disebabkan karena kandungan pigmen warna
antosianin yang cukup tinggi sehingga mempengaruhi tingkat kecerahan warna
53
disebabkan kandungan pigmen antosianin yang terdapat pada ubi jalar ungu yang
mengalami perubahan dari berwarna ungu menjadi berwarna merah. Winarno
(1992), menyatakan pigmen antosianin akan berwarna merah jika dalam kondisi
asam atau pH rendah, ungu pada pH netral dan berwarna biru jika dalam kondisi
pH tinggi. Hubungan antara konsentrasi sorbitol dengan sari ubi jalar ungu
dengan nilai warna a permen jelly dapat dilihat pada Gambar 20.
Gambar 20. Hubungan antara konsentrasi sorbitol dengan sari ubi jalar ungu
dengan nilai warna a permen jelly
Pengaruh konsentrasi karagenan terhadap nilai warna a permen jelly
Dari daftar sidik ragam (Lampiran 9) dapat dilihat bahwa konsentrasi
karagenan memberi pengaruh berbeda sangat nyata (P<0,01) terhadap nilai warna
a permen jelly yang dihasilkan. Hasil uji LSR pengaruh konsentrasi karagenan
terhadap indeks warna a permen jelly dapat dilihat pada Tabel 22.
13.49 13.77
Konsentrasi sorbitol : sari ubi jalar ungu (%)