SULFONASI ONGGOK SEBAGAI SUPERABSORBEN
PRIMASTI RAMADHANI
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
ABSTRAK
PRIMASTI RAMADHANI. Pembuatan Produk Sulfonasi Onggok Sebagai
Superabsorben. Dibimbing oleh ANWAR NUR dan
MOHAMMAD KHOTIB
.
Onggok merupakan hasil samping dari industri tapioka. Penelitian ini
memanfaatkan onggok yang awalnya memiliki nilai jual yang rendah menjadi suatu
produk yang berpotensi memiliki nilai jual lebih tinggi. Pembuatan penyerap air dari
onggok singkong melalui metode sulfonasi. Proses pembuatan penyerap air diawali
dengan proses oksidasi menggunakan senyawa NaIO
4dengan ragam waktu 210, 270, dan
330 menit. Kemudian proses dilanjutkan dengan dilarutkan dalam larutan yang
mengandung NaHSO
3dengan bobot 15, 20, dan 35 gram pada suhu 22 ºC dengan ragam
selama 60, 120, dan 180 menit. Onggok yang telah teroksidasi kemudian disulfonasi
dengan NaHSO
3dengan ragam konsentrasi dan ragam waktu sulfonasi. Produk yang
dihasilkan adalah onggok tersulfonasi dengan 3 parameter. Kemampuan absorbsi onggok
tersulfonasi diujikan dengan perendaman produk pada air distilat selama 4 jam dan
dihitung kapasitas pengembangannya. Modifikasi onggok singkong tersulfonasi
menghasilkan 27 komposisi produk dari 3 parameter yang di buat beragam. Kapasitas
absorbsi terbesar diperoleh dari komposisi 330 menit oksidasi, 340 menit sulfonasi dan
15 gram bisulfit sebesar 44.06 gram cairan per gram sampel. Proses oksidasi yang
dilakukan memungkinkan senyawa bisulfit teradisi ke dalam gugus karbonil pada onggok
banyaknya rantai karbon yang terputus saat oksidasi dengan NaIO
4menentukan
banyaknya ion bisulfit yang yang pada rantai karbon. Gugus [SO
3]
2-berinteraksi melalui
ikatan hidrogen dengan senyawa H
2O. Analisis spektrometer inframerah tranformasi
fourier membuktikan adanya gugus [SO
3]
2-yang terikat pada onggok.
ABSTRACT
PRIMASTI RAMADHANI. Sulfonation of waste cassava to produce superabsorbent.
Under supervision of
ANWAR NUR and
MOHAMMAD KHOTIB.
Onggok is a waste product of tapioca industries which has low economical value.
The aim of this research is to find a way to increase the added value of onggok by
transforming it into a superabsorbent. The making of superabsorbent from onggok was
preparated through sulfonation and preceded by oxidation. In this experiment the
oxidation was carried out with 3 levels of reaction time, i.e. 210, 270, and 330 minutes.
While sulfonation was carried out with 3 levels of concentration of NaHSO
3, that are 15,
20 and 35 g and 3 levels of sulfonation time of 120, 180 and 240 minutes. The absorption
capacity of the product was evaluated through their absorption capacity, carried out by
immersing the product for 4 hours in a known volume of distill water. Its absorptive
capacity is calculated based on its sample weight increases due to water absorption. The
results show that the highest absorption capacity was indicated by the sample with 270
minutes of oxidation, 240 minutes of sulfonation time and 20 g of NaHSO
3. Its absorption
SULFONASI ONGGOK SEBAGAI SUPERABSORBEN
PRIMASTI RAMADHANI
Skripsi
sebagai salah satu syarat untuk memperoleh gelar Sarjana Sains pada
Departemen Kimia
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
Judul
: Sulfonasi Onggok sebagai Superabsorben
Nama : Primasti Ramadhani
NIM
: G44204083
Menyetujui,
Pembimbing I,
Pembimbing II,
Prof. (em) Dr. Ir. H. M. Anwar Nur, M.Sc
NIP 19781018 200701 1 002
M. Khotib, S.Si
Mengetahui,
Dekan Fakultas Matematika dan Ilmu Pengetahuan Alam
Institut Pertanian Bogor
Dr. Drh. Hasim, DEA
NIP 19610328 198601 1 002
PRAKATA
Puji dan syukur penulis panjatkan kepada Allah SWT yang telah melimpahkan
rahmat, karunia, iman, kekuatan, dan kecerdasan kepada penulis, sehingga laporan
hasil penelitian ini berhasil diselesaikan. Shalawat dan salam semoga selalu
tercurah kepada Nabi Muhammad SAW beserta keluarga.
Terima kasih penulis ucapkan kepada Prof. (em) Dr. Ir. H. M. Anwar Nur,
M.Sc dan M Khotib S.Si selaku pembimbing yang telah memberikan motivasi dan
arahan untuk kelancaran penelitian ini.
Ungkapan terima kasih tidak lupa penulis haturkan kepada kepada Ibu, Nyomo,
Aryo, dan keluarga tercinta; Dede dan sahabat-sahabatku; Drs Ahmad Syahriza,
Dra Armi Wulanawati dan Drs Farid untuk bimbingannya, seluruh staf Lab
Terpadu; Bisma, Ciwaluya 26, Pak Sabur, teman-teman di laboratorium kimia
organik, teman-teman Kimia angkatan 41 atas doa dan dukungannya.
Semoga laporan hasil penelitian ini dapat bermanfaat.
Bogor, 4 September 2009
RIWAYAT HIDUP
Penulis dilahirkan di Jakarta pada tanggal 25 Mei 1986. Anak pertama dari 2
bersaudara merupakan anak dari pasangan Bapak Djoko Sunaryo dan Ibu
Musarofah.
Penulis menyelesaikan pendidikan tingkat pertama di tahun 2001 di SLTPN
09 Jakarta Timur. Tahun 2004 penulis menyelesaikan pendidikan menengah atas
di SMAN 39, Jakarta. Penulis diterima sebagai mahasiswi Departemen Kimia,
Fakultas Matematika Dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor pada
tahun yang sama melalui jalur Seleksi Penerimaan Mahasiswa Baru (SPMB).
Selama
mengikuti
perkuliahan
penulis
aktif
dalam
organisasi
kemahasiswaan Ikatan Mahasiswa Kimia (Imasika) IPB pada tahun 2005/2006,
asisten kimia TPB matrikulasi pada tahun 2008 dan kimia fisik ITP 2008-2009.
Kegiatan praktik lapangan yang dilakukan penulis mengenai Analisis
Cooling
DAFTAR ISI
Halaman
DAFTAR TABEL ...
viii
DAFTAR GAMBAR ...
viii
DAFTAR LAMPIRAN ...
ix
PENDAHULUAN ...
1
TINJAUAN PUSTAKA
Singkong (Manihot esculenta.)...
1
Onggok
...
2
Polisakarida ...
2
Perlakuan Pendahuluan ...
3
Sulfonasi ...
3
Superabsorben ...
3
BAHAN DAN METODE
Bahan dan Lingkup Kerja ...
4
Lingkup Kerja ...
4
HASIL DAN PEMBAHASAN
Perlakuan Pendahuluan Asam (Marshall et. all)...
6
Perlakuan Pendahuluan Asam ...
6
Kondisi Sulfonasi Onggok Terhadap Kapasitas Absorbsi ...
7
Pencirian Onggok ...
8
SIMPULAN DAN SARAN
Simpulan ...
10
Saran ...
10
DAFTAR PUSTAKA ...
10
DAFTAR TABEL
Halaman
1 Komposisi kimia onggok singkong...
2
2 Rancangan Percobaan
screening
Sulfonasi Onggok ...
6
3 Kadar sulfur total ...
9
4 Vibrasi ulur dan tekuk dari onggok awal, sampel O
1S
2W
1dan O
3S
1W
3.
..
9
DAFTAR GAMBAR
Halaman
1 Umbi singkong
...
1
2 Onggok awal
...
2
3 Struktur amilosa
...
2
4 Struktur amilopektin
...
2
5 Struktur selulosa
...
3
6 Reaksi sulfonasi polisakarida (Ramakant, 1997)
...
3
7 Mekanisme hidrasi polimer superabsorben
...
3
8 Proses pembengkakan polimer superabsorben
...
6
9 Proses pembengkakan superabsorben onggok ...
6
10 Kurva hubungan waktu perlakuan pendahuluan dengan asam dan
kapasitas absorbsi ...
7
11 Hubungan kapasitas absorbsi dengan t
oksidasidan t
sulfonasisampel ...
7
12 Hubungan kapasitas absorbsi dengan t
oksidasidan bobot NaHSO
3...
8
13 Hubungan kapasitas absorbsi dengan t
sulfonasidan bobot NaHSO
3...
8
DAFTAR LAMPIRAN
Halaman
1
Kerangka optimasi onggok singkong ...
12
2 Diagram proses pembuatan tepung tapioka pada industri kecil ...
13
3 Onggok tersulfonasi
(Ramakant, 1996)
...
14
4 Perhitungan uji proksimat onggok ...
15
5 Data pengukuran kapasitas absorbsi awal dengan pra perlakuan ...
16
6 Data ulangan pengukuran kapasitas absorbsi (QH
2O) ...
17
7 Analisis Annova untuk
screening
sulfonasi onggok menggunakan
Software
Statistica
V.6 ...
18
8 Grafik pengaruh setiap variabel bebas terhadap Q ...
19
9 Gambar pengaruh interaksi antar variabel-variabel bebas (x) terhadap Q ..
20
10 Grafik hubungan antara data prediksi dengan data pengamatan ...
21
PENDAHULUAN
Singkong disebut juga ubi kayu atau ketela pohon. Singkong memiliki kandungan pati yang tinggi sebagai sumber karbohidrat dan terutama diolah menjadi tepung tapioka
banyak diekspor. Produk samping
pembuatan tepung tapioka berupa onggok (ampas) dalam jumlah besar. Onggok biasanya digunakan untuk bahan baku industri saus, campuran kerupuk, obat
nyamuk bakar, dan pakan ternak.
Kandungan terbesar dalam onggok ialah selulosa dan pati (Djarir 1982). Kandungan karbohidrat dan air yang tinggi dari onggok mempermudah aktivitas mikrobe pengurai menghasilkan senyawa amonia (NH3 dan
H2S) yang menimbulkan bau tidak sedap
(Pudjiastuti et al. 1999). Oleh karena itu, pemanfaatan onggok untuk produk-produk yang memiliki nilai jual perlu dikembangkan lebih banyak lagi (Enie 1989).
Polimer alam berupa serat, termasuk di dalamnya selulosa telah banyak dimodifikasi
melalui modifikasi kimia seperti
karboksimetilasi, sulfatilasi, ataupun fosforilasi. Modifikasi selulosa dapat meningkatkan kapasitas absorpsi. Hasil modifikasi tersebut biasanya dimanfaatkan
dalam banyak bidang, di antaranya
pembungkus makanan, teknik konstruksi, industri kimia, pengolahan limbah, dan bahan pembuat sensor (Jian 2008).
Bahan utama absorben umumnya adalah
poliakrilamida. Namun poliakrilamida
mempunyai kekurangan dalam hal kekuatan fisik dan kestabilan pada suhu. Pembuatan komposit polimer absorben dengan mineral alam seperti bentonit, zeolit, sepiolit merupakan jenis komposit yang termasuk baru dikembangkan. Pembuatan komposit polimer absorben dapat dilakukan dengan proses sambung polimer dengan mineral alam dan proses penggabungan monomer
dengan mineral alam lalu diikuti
polimerisasi. Komposit polimer absorben dengan mineral alam seperti bentonit, zeolit, sepiolit merupakan jenis komposit yang
termasuk baru dikembangkan
(Kiatkamjorwong 2002).
Ramakant (1996) telah melakukan
modifikasi pulp kertas secara sulfonasi.
Awalnya modifikasi ini bertujuan
meningkatkan kekuatan tarik dalam kondisi basah (wet strength) dari pulp kertas, tetapi modifikasi ini juga dapat meningkatkan kapasitas absorpsi pulp kertas hingga 16 kali bobot awalnya. Selain itu nitrasi selulosa
onggok singkong juga dapat meningkatkan
daya serap pada senyawa-senyawa
kurkuminoid temulawak sehingga dapat memperbesar jumlah eluat hasil elusi kolom. Hal ini dapat dilihat dari hasil analisis
spektroskopi UV-Vis. Filtrat hasil
pengocokan onggok bekas elusi kolom
dengan etanol membuktikan adanya
senyawa-senyawa yang tertahan pada fase diam onggok (Maretta 2006).
Penelitian ini melaporkan keberhasilan
pembuatan superabsorben dari materi
berbahan dasar onggok. Terdapat 27 ragam
perlakuan dari 3 parameter untuk
mengetahui faktor yang paling
mempengaruhi kapasitas absorpsi dalam penelitian ini (Lampiran 1 ).
TINJAUAN PUSTAKA
Singkong
Singkong termasuk tumbuhan berbatang pohon lunak atau getas (mudah patah). Ubi kayu berbatang bulat dan bergerigi yang terjadi dari bekas pangkal tangkai daun dan bagian tengahnya bergabus. Ubi kayu bisa
mencapai ketinggian 1–4 meter.
Pemeliharaannya mudah dan produktif. Daun ubi kayu memiliki tangkai panjang dan helaian daunnya menyerupai telapak tangan, dan tiap tangkai mempunyai daun sekitar 3-8 lembar. Tangkai daun tersebut
berwarna kuning, hijau, atau merah.
Singkong merupakan makanan pokok di beberapa negara Afrika. Singkong dapat tumbuh subur di daerah yang berketinggian 1200 meter di atas permukaan air laut dan merupakan tumbuhan yang produktif (Alves 2000). Di samping sebagai bahan makanan, singkong juga dapat digunakan sebagai pakan ternak dan bahan baku industri pembuatan tepung tapioka (Gambar 1).
SULFONASI ONGGOK SEBAGAI SUPERABSORBEN
PRIMASTI RAMADHANI
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
ABSTRAK
PRIMASTI RAMADHANI. Pembuatan Produk Sulfonasi Onggok Sebagai
Superabsorben. Dibimbing oleh ANWAR NUR dan
MOHAMMAD KHOTIB
.
Onggok merupakan hasil samping dari industri tapioka. Penelitian ini
memanfaatkan onggok yang awalnya memiliki nilai jual yang rendah menjadi suatu
produk yang berpotensi memiliki nilai jual lebih tinggi. Pembuatan penyerap air dari
onggok singkong melalui metode sulfonasi. Proses pembuatan penyerap air diawali
dengan proses oksidasi menggunakan senyawa NaIO
4dengan ragam waktu 210, 270, dan
330 menit. Kemudian proses dilanjutkan dengan dilarutkan dalam larutan yang
mengandung NaHSO
3dengan bobot 15, 20, dan 35 gram pada suhu 22 ºC dengan ragam
selama 60, 120, dan 180 menit. Onggok yang telah teroksidasi kemudian disulfonasi
dengan NaHSO
3dengan ragam konsentrasi dan ragam waktu sulfonasi. Produk yang
dihasilkan adalah onggok tersulfonasi dengan 3 parameter. Kemampuan absorbsi onggok
tersulfonasi diujikan dengan perendaman produk pada air distilat selama 4 jam dan
dihitung kapasitas pengembangannya. Modifikasi onggok singkong tersulfonasi
menghasilkan 27 komposisi produk dari 3 parameter yang di buat beragam. Kapasitas
absorbsi terbesar diperoleh dari komposisi 330 menit oksidasi, 340 menit sulfonasi dan
15 gram bisulfit sebesar 44.06 gram cairan per gram sampel. Proses oksidasi yang
dilakukan memungkinkan senyawa bisulfit teradisi ke dalam gugus karbonil pada onggok
banyaknya rantai karbon yang terputus saat oksidasi dengan NaIO
4menentukan
banyaknya ion bisulfit yang yang pada rantai karbon. Gugus [SO
3]
2-berinteraksi melalui
ikatan hidrogen dengan senyawa H
2O. Analisis spektrometer inframerah tranformasi
fourier membuktikan adanya gugus [SO
3]
2-yang terikat pada onggok.
ABSTRACT
PRIMASTI RAMADHANI. Sulfonation of waste cassava to produce superabsorbent.
Under supervision of
ANWAR NUR and
MOHAMMAD KHOTIB.
Onggok is a waste product of tapioca industries which has low economical value.
The aim of this research is to find a way to increase the added value of onggok by
transforming it into a superabsorbent. The making of superabsorbent from onggok was
preparated through sulfonation and preceded by oxidation. In this experiment the
oxidation was carried out with 3 levels of reaction time, i.e. 210, 270, and 330 minutes.
While sulfonation was carried out with 3 levels of concentration of NaHSO
3, that are 15,
20 and 35 g and 3 levels of sulfonation time of 120, 180 and 240 minutes. The absorption
capacity of the product was evaluated through their absorption capacity, carried out by
immersing the product for 4 hours in a known volume of distill water. Its absorptive
capacity is calculated based on its sample weight increases due to water absorption. The
results show that the highest absorption capacity was indicated by the sample with 270
minutes of oxidation, 240 minutes of sulfonation time and 20 g of NaHSO
3. Its absorption
SULFONASI ONGGOK SEBAGAI SUPERABSORBEN
PRIMASTI RAMADHANI
Skripsi
sebagai salah satu syarat untuk memperoleh gelar Sarjana Sains pada
Departemen Kimia
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
Judul
: Sulfonasi Onggok sebagai Superabsorben
Nama : Primasti Ramadhani
NIM
: G44204083
Menyetujui,
Pembimbing I,
Pembimbing II,
Prof. (em) Dr. Ir. H. M. Anwar Nur, M.Sc
NIP 19781018 200701 1 002
M. Khotib, S.Si
Mengetahui,
Dekan Fakultas Matematika dan Ilmu Pengetahuan Alam
Institut Pertanian Bogor
Dr. Drh. Hasim, DEA
NIP 19610328 198601 1 002
PRAKATA
Puji dan syukur penulis panjatkan kepada Allah SWT yang telah melimpahkan
rahmat, karunia, iman, kekuatan, dan kecerdasan kepada penulis, sehingga laporan
hasil penelitian ini berhasil diselesaikan. Shalawat dan salam semoga selalu
tercurah kepada Nabi Muhammad SAW beserta keluarga.
Terima kasih penulis ucapkan kepada Prof. (em) Dr. Ir. H. M. Anwar Nur,
M.Sc dan M Khotib S.Si selaku pembimbing yang telah memberikan motivasi dan
arahan untuk kelancaran penelitian ini.
Ungkapan terima kasih tidak lupa penulis haturkan kepada kepada Ibu, Nyomo,
Aryo, dan keluarga tercinta; Dede dan sahabat-sahabatku; Drs Ahmad Syahriza,
Dra Armi Wulanawati dan Drs Farid untuk bimbingannya, seluruh staf Lab
Terpadu; Bisma, Ciwaluya 26, Pak Sabur, teman-teman di laboratorium kimia
organik, teman-teman Kimia angkatan 41 atas doa dan dukungannya.
Semoga laporan hasil penelitian ini dapat bermanfaat.
Bogor, 4 September 2009
RIWAYAT HIDUP
Penulis dilahirkan di Jakarta pada tanggal 25 Mei 1986. Anak pertama dari 2
bersaudara merupakan anak dari pasangan Bapak Djoko Sunaryo dan Ibu
Musarofah.
Penulis menyelesaikan pendidikan tingkat pertama di tahun 2001 di SLTPN
09 Jakarta Timur. Tahun 2004 penulis menyelesaikan pendidikan menengah atas
di SMAN 39, Jakarta. Penulis diterima sebagai mahasiswi Departemen Kimia,
Fakultas Matematika Dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor pada
tahun yang sama melalui jalur Seleksi Penerimaan Mahasiswa Baru (SPMB).
Selama
mengikuti
perkuliahan
penulis
aktif
dalam
organisasi
kemahasiswaan Ikatan Mahasiswa Kimia (Imasika) IPB pada tahun 2005/2006,
asisten kimia TPB matrikulasi pada tahun 2008 dan kimia fisik ITP 2008-2009.
Kegiatan praktik lapangan yang dilakukan penulis mengenai Analisis
Cooling
DAFTAR ISI
Halaman
DAFTAR TABEL ...
viii
DAFTAR GAMBAR ...
viii
DAFTAR LAMPIRAN ...
ix
PENDAHULUAN ...
1
TINJAUAN PUSTAKA
Singkong (Manihot esculenta.)...
1
Onggok
...
2
Polisakarida ...
2
Perlakuan Pendahuluan ...
3
Sulfonasi ...
3
Superabsorben ...
3
BAHAN DAN METODE
Bahan dan Lingkup Kerja ...
4
Lingkup Kerja ...
4
HASIL DAN PEMBAHASAN
Perlakuan Pendahuluan Asam (Marshall et. all)...
6
Perlakuan Pendahuluan Asam ...
6
Kondisi Sulfonasi Onggok Terhadap Kapasitas Absorbsi ...
7
Pencirian Onggok ...
8
SIMPULAN DAN SARAN
Simpulan ...
10
Saran ...
10
DAFTAR PUSTAKA ...
10
DAFTAR TABEL
Halaman
1 Komposisi kimia onggok singkong...
2
2 Rancangan Percobaan
screening
Sulfonasi Onggok ...
6
3 Kadar sulfur total ...
9
4 Vibrasi ulur dan tekuk dari onggok awal, sampel O
1S
2W
1dan O
3S
1W
3.
..
9
DAFTAR GAMBAR
Halaman
1 Umbi singkong
...
1
2 Onggok awal
...
2
3 Struktur amilosa
...
2
4 Struktur amilopektin
...
2
5 Struktur selulosa
...
3
6 Reaksi sulfonasi polisakarida (Ramakant, 1997)
...
3
7 Mekanisme hidrasi polimer superabsorben
...
3
8 Proses pembengkakan polimer superabsorben
...
6
9 Proses pembengkakan superabsorben onggok ...
6
10 Kurva hubungan waktu perlakuan pendahuluan dengan asam dan
kapasitas absorbsi ...
7
11 Hubungan kapasitas absorbsi dengan t
oksidasidan t
sulfonasisampel ...
7
12 Hubungan kapasitas absorbsi dengan t
oksidasidan bobot NaHSO
3...
8
13 Hubungan kapasitas absorbsi dengan t
sulfonasidan bobot NaHSO
3...
8
DAFTAR LAMPIRAN
Halaman
1
Kerangka optimasi onggok singkong ...
12
2 Diagram proses pembuatan tepung tapioka pada industri kecil ...
13
3 Onggok tersulfonasi
(Ramakant, 1996)
...
14
4 Perhitungan uji proksimat onggok ...
15
5 Data pengukuran kapasitas absorbsi awal dengan pra perlakuan ...
16
6 Data ulangan pengukuran kapasitas absorbsi (QH
2O) ...
17
7 Analisis Annova untuk
screening
sulfonasi onggok menggunakan
Software
Statistica
V.6 ...
18
8 Grafik pengaruh setiap variabel bebas terhadap Q ...
19
9 Gambar pengaruh interaksi antar variabel-variabel bebas (x) terhadap Q ..
20
10 Grafik hubungan antara data prediksi dengan data pengamatan ...
21
PENDAHULUAN
Singkong disebut juga ubi kayu atau ketela pohon. Singkong memiliki kandungan pati yang tinggi sebagai sumber karbohidrat dan terutama diolah menjadi tepung tapioka
banyak diekspor. Produk samping
pembuatan tepung tapioka berupa onggok (ampas) dalam jumlah besar. Onggok biasanya digunakan untuk bahan baku industri saus, campuran kerupuk, obat
nyamuk bakar, dan pakan ternak.
Kandungan terbesar dalam onggok ialah selulosa dan pati (Djarir 1982). Kandungan karbohidrat dan air yang tinggi dari onggok mempermudah aktivitas mikrobe pengurai menghasilkan senyawa amonia (NH3 dan
H2S) yang menimbulkan bau tidak sedap
(Pudjiastuti et al. 1999). Oleh karena itu, pemanfaatan onggok untuk produk-produk yang memiliki nilai jual perlu dikembangkan lebih banyak lagi (Enie 1989).
Polimer alam berupa serat, termasuk di dalamnya selulosa telah banyak dimodifikasi
melalui modifikasi kimia seperti
karboksimetilasi, sulfatilasi, ataupun fosforilasi. Modifikasi selulosa dapat meningkatkan kapasitas absorpsi. Hasil modifikasi tersebut biasanya dimanfaatkan
dalam banyak bidang, di antaranya
pembungkus makanan, teknik konstruksi, industri kimia, pengolahan limbah, dan bahan pembuat sensor (Jian 2008).
Bahan utama absorben umumnya adalah
poliakrilamida. Namun poliakrilamida
mempunyai kekurangan dalam hal kekuatan fisik dan kestabilan pada suhu. Pembuatan komposit polimer absorben dengan mineral alam seperti bentonit, zeolit, sepiolit merupakan jenis komposit yang termasuk baru dikembangkan. Pembuatan komposit polimer absorben dapat dilakukan dengan proses sambung polimer dengan mineral alam dan proses penggabungan monomer
dengan mineral alam lalu diikuti
polimerisasi. Komposit polimer absorben dengan mineral alam seperti bentonit, zeolit, sepiolit merupakan jenis komposit yang
termasuk baru dikembangkan
(Kiatkamjorwong 2002).
Ramakant (1996) telah melakukan
modifikasi pulp kertas secara sulfonasi.
Awalnya modifikasi ini bertujuan
meningkatkan kekuatan tarik dalam kondisi basah (wet strength) dari pulp kertas, tetapi modifikasi ini juga dapat meningkatkan kapasitas absorpsi pulp kertas hingga 16 kali bobot awalnya. Selain itu nitrasi selulosa
onggok singkong juga dapat meningkatkan
daya serap pada senyawa-senyawa
kurkuminoid temulawak sehingga dapat memperbesar jumlah eluat hasil elusi kolom. Hal ini dapat dilihat dari hasil analisis
spektroskopi UV-Vis. Filtrat hasil
pengocokan onggok bekas elusi kolom
dengan etanol membuktikan adanya
senyawa-senyawa yang tertahan pada fase diam onggok (Maretta 2006).
Penelitian ini melaporkan keberhasilan
pembuatan superabsorben dari materi
berbahan dasar onggok. Terdapat 27 ragam
perlakuan dari 3 parameter untuk
mengetahui faktor yang paling
mempengaruhi kapasitas absorpsi dalam penelitian ini (Lampiran 1 ).
TINJAUAN PUSTAKA
Singkong
Singkong termasuk tumbuhan berbatang pohon lunak atau getas (mudah patah). Ubi kayu berbatang bulat dan bergerigi yang terjadi dari bekas pangkal tangkai daun dan bagian tengahnya bergabus. Ubi kayu bisa
mencapai ketinggian 1–4 meter.
Pemeliharaannya mudah dan produktif. Daun ubi kayu memiliki tangkai panjang dan helaian daunnya menyerupai telapak tangan, dan tiap tangkai mempunyai daun sekitar 3-8 lembar. Tangkai daun tersebut
berwarna kuning, hijau, atau merah.
Singkong merupakan makanan pokok di beberapa negara Afrika. Singkong dapat tumbuh subur di daerah yang berketinggian 1200 meter di atas permukaan air laut dan merupakan tumbuhan yang produktif (Alves 2000). Di samping sebagai bahan makanan, singkong juga dapat digunakan sebagai pakan ternak dan bahan baku industri pembuatan tepung tapioka (Gambar 1).
Onggok
Onggok adalah hasil samping
pengolahan singkong menjadi tapioka yang berupa limbah padat utama setelah proses pengepresan (Gambar 2). Pada industri tapioka yang sudah maju, limbah padat kebanyakan hanya mengandung serat kasar, sedangkan sisa pati yang terikat sangat kecil. Lain halnya dengan limbah padatan yang dihasilkan oleh pengrajin tapioka (industri kecil) pada umumnya onggok masih
mengandung pati yang lebih tinggi
(Darmadjati 1985).
Gambar 2 Onggok awal.
Tabel 1 menunjukkan komposisi kimia
onggok. Komposisi kimia onggok
dipengaruhi oleh varietas singkong,
kandungan mineral serta kadar air media tanam dan cara ekstraksi pati singkong. Kadar air onggok yang tinggi menyebabkan onggok perlu segera diolah lebih lanjut sebelum mengalami pembusukan (Golief 2002).
Tabel 1 Komposisi kimia onggok singkong
Komposisi Kadar (%)
Air 12.7
Abu 9.1
Serat Kasar 8.1
Protein 2.5
Lemak 1.0
Karbohidrat 65.9
Sumber: Rinaldy 1987
Onggok segar mengandung air yang cukup tinggi (10-20%) sehingga perlu
dikeringkan terlebih dahulu sebelum
dimodifikasi (BPOM 2004). Di sisi lain kadar protein dan lemak onggok yang rendah memungkinkan onggok dimodifikasi tanpa menghilangkan lemak dan proteinnya terlebih dahulu.
Polisakarida
Polisakarida merupakan polimer
molekul-molekul berantai lurus atau
bercabang yang dapat dihidrolisis dengan enzim-enzim yang spesifik kerjanya.Derajat polimerisasi (DP) selulosa sebesar 7000– 15000. Hasil hidrolisis sebagian polisakrida akan menghasilkan oligosakarida dan dapat dipakai untuk menentukan struktur molekul polisakarida (Winarno 1984). Polisakarida
berbeda dalam kandungan unit
monosakaridanya, panjang rantainya, dan dalam tingkat percabangannya. Terdapat dua jenis polisakarida yaitu homopolisakarida (mengandung hanya satu jenis monomer) dan heteropolisakarida (mengandung dua atau lebih jenis unit monosakarida yang berbeda). Contoh homopolisakarida adalah pati dan selulosa.
Pati merupakan homopolimer glukosa dengan ikatan α-glikosidik. Berbagai macam pati tidak sama sifatnya, bergantung pada panjang rantai C-nya, serta apakah lurus atau bercabang rantai molekulnya. Pati terdiri atas 2 fraksi yang dapat dipisahkan dengan air panas. Fraksi terlarut disebut amilosa (Gambar 3) dan fraksi tidak terlarut disebut
amilopektin (Gambar 4). Amilosa
memberikan sifat keras (pera) sedangkan amilopektin menyebabkan sifat lengket (Winarno 1984).
Gambar 3 Struktur amilosa
Gambar 4 Struktur amilopektin
Selulosa merupakan senyawa organik yang terdapat pada dinding sel bersama lignin yang berperan dalam mengokohkan
struktur jaringan tumbuhan. Selulosa
satu sama lain dengan ikatan-ikatan glikosida (1,4). Molekul selulosa (Gambar 5) seluruhnya berbentuk linear dan memiliki kecenderungan kuat membentuk ikatan hidrogen baik inter- maupun intramolekuler.
Gambar 5 Struktur selulosa
Selulosa mempunyai potensi yang cukup besar untuk dijadikan sebagai penyerap karena gugus –OH yang terikat dapat berinteraksi dengan komponen absorbat. Keberadaan gugus –OH. pada selulosa dan hemiselulosa menyumbang polaritas pada polimer tersebut. Dengan demikian selulosa dan hemiselulosa akan menyerap senyawa yang bersifat polar daripada yang kurang polar.
Perlakuan Pendahuluan
Perlakuan pendahuluan dapat dilakukan
dengan memberikan perlakuan kimia,
seperti direaksikan dengan asam dan basa
atau dengan perlakuan fisik seperti
pencucian (Marshall 1996). Perlakuan
pendahuluan yang digunakan dalam
penelitian ini adalah menggunakan asam nitrat. Tujuan perlakuan pendahuluan ini adalah untuk membersihkan onggok dari
pengotor, lemak, dan protein yang
terkandung didalamnya (aktivasi
permukaan).
Sulfonasi
Salah satu metode untuk memodifikasi
sifat fungsional polisakarida adalah
sulfonasi. Sulfonasi pada dasarnya
merupakan reaksi antara polisakarida dan suatu bisulfit. Perlakuan ini bertujuan mengadisikan gugus sulfonat pada karbonil dari unit dialdehid glukosa polisakarida.
Awalnya sulfonasi digunakan dalam industri untuk meningkatkan kekuatan bahan dalam keadaan basah (wet strength) yang
memberikan hasil yang cukup baik
(Ramakan 1996). Reaksi sulfonasi selulosa dilakukan dengan mengoksidasi polisakarida terlebih dahulu menggunakan oksidator periodat, Dialdehida oksiselulosa yang dihasilkan kemudian direaksikan dengan
NaHSO3 atau campuran NaOH-SO2. Reaksi
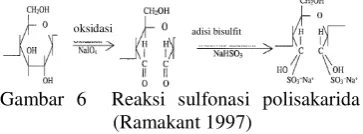
sulfonasi polisakarida dapat dilihat pada Gambar 6.
Gambar 6 Reaksi sulfonasi polisakarida (Ramakant 1997)
Superabsorben
Superabsorben adalah suatu polimer yang dapat mengabsorpsi sejumlah besar air, larutan garam, dan cairan denganya serap mulai 10 hingga 1000 kali dari bobot awalnya. Superabsorben dapat menyimpan
cairan lebih dari berat bahan yang
diserapnya dan tidak melepas cairan tersebut
(Kiatkamjornwong 2002). Penggunaan
polimer absorben sangat banyak, di
antaranya digunakan sebagai bahan
pengolahan limbah, media tumbuh tanaman, bahan untuk mengurangi gesekan dalam pipa, bahan pelapis antibocor, pelindung
jaringan kabel bawah tanah, bahan
pembuatan kemasan barang, dan bahan pemadam kebakaran.
Gambar 7 menunjukkan ikatan utama suatu polimer absorben yang mengandung gugus hidrofilik karena terdiri atas gugus bisulfit (SO3-) yang bersifat hidrofilik.
Ketika polimer absorben dimasukkan dalam air atau pelarut akan terjadi interaksi antara polimer dan molekul air. Interaksi yang terjadi adalah hidrasi. Mekanisme hidrasi terjadi karena ion dari zat terlarut dalam polimer seperti SO3- dan Na+ berikatan
dengan molekul polar air melalui ikatan hidrogen. (Chang 1999).
Gambar 7 Mekanisme hidrasi polimer superabsorben
Berdasarkan morfologinya, absorben diklasifikasikan menjadi absorben serbuk, partikel, bola, serat, membran, dan emulsi. Ditinjau dari jenis bahan penyusunnya terdiri atas polimer absorben makromolekul alam, semipolimer sintetis dan polimer sintetis sedangkan dilihat dari proses
SO3
) % 100 ( 100 air kadar
-pembuatannya dapat dibedakan atas polimer cangkokan dan ikatan silang (Dayo 2003).
BAHAN DAN LINGKUP
KERJA
Bahan dan Alat
Bahan-bahan yang digunakan adalah onggok kering dari daerah Tanah Baru Bogor, NaIO4, dan NaHSO3.
Alat-alat yang dipakai adalah
spektroskopi inframerah transformasi fourier (FTIR) Bruker jenis Tentor 37.
Lingkup Kerja
Uji Proksimat
Penentuan Kadar Air (AOAC 1999)
Sebanyak 0.1 g onggok yang telah dihaluskan ditempatkan dalam cawan petri yang telah dikeringkan dalam oven dan telah diketahui bobot kosongnya. Cawan petri berisi sampel dikeringkan dalam oven pada suhu 105 °C selama 3 jam dan didinginkan. Setelah dingin, cawan petri berisi sampel tersebut disimpan dalam desikator, lalu ditimbang. Pengeringan dilakukan beberapa kali selama 1 jam sampai diperoleh bobot yang tetap. % 100 ´ = awal sampel bobot air bobot air Kadar
Kadar abu (AOAC 1999)
Sampel ditimbang sebanyak 1-5 gram, lalu dimasukkan ke dalam cawan poselen yang sudah diketahui bobot tetapnya. Sampel dipanaskan diatas bunsen dengan nyala api kecil hingga berasap, selanjutnya sampel dimasukkan ke dalam tanur pada suhu 500°C sampai menjadi abu bewarna putih. Cawan yang berisi abu didinginkan dalam desikator dan dilakukan penimbangan hingga diperoleh bobot tetap. Kadar abu dapat dihitung dengan rumus:
% 100 ) ( ) ( (%) = ´ g Sampel Berat g Abu Berat Abu Kadar
Kadar Protein (AOAC 1999)
Sampel ditimbang sebanyak 0.5-3 gram lalu dimasukkan ke dalam labu Kjeldahl dan didestruksi dengan menggunakan 20 ml asam sulfat pekat dengan pemanasan sampai terbentuk larutan berwarna jernih. Larutan hasil destruksi diencerkan dan didistilasikan
dengan penambahan 10 ml NaOH 10%. Destilat ditampung dalam 25 ml larutan H3BO3 3%. Larutan H3BO3 dititrasi dengan
HCl standar menggunakan merah metil sebagai indikator. Dari hasil titrasi, total nitrogen dapat diketahui dengan rumus
% 100 14 (%)= ´ ´ ´ ´ Sampel Bobot fk HCL N titran ml Nitrogen Total
Fk = faktor koreksi kadar air =
Kadar Lemak (AOAC 1999)
Labu lemak yang ukurannya sesuai dengan alat ekstraksi Soxhlet dikeringkan dalam oven. Kemudian didinginkan dalam desikator dan ditimbang hingga bobot tetap. Sebanyak 5 g sampel dibungkus dengan kertas saring, kemudian ditutup dengan kapas wool yang bebas lemak. Kertas saring yang berisi sampel tersebut dimasukkan dalam alat ekstraksi soklet.
Pelarut dietil eter dituangkan ke dalam labu lemak secukupnya. Sampel kemudian direfluks selama kurang lebih 5 jam atau hingga pelarut yang turun kembali ke labu lemak tidak berwarna. Pelarut yang ada dalam labu didistilasi dan ditampung. Labu lemak yang berisi hasil ekstraksi kemudian dipanaskan dalam oven pada suhu 105°C.
Labu selanjutnya didinginkan dalam
desikator dan dilakukan penimbangan
hingga bobot tetap.
% 100 ) ( ) ( ´ = g Sampel Bobot g Lemak Bobot Lemak Kadar
Perlakuan Pendahuluan sampel onggok dengan asam (Marshall et al 1999)
Ampas onggok dibersihkan dengan air keran untuk menghilangkan bau dan kotoran yang tersisa dari pengolahan singkong.
Onggok kemudian dicuci kembali
menggunakan air hangat (50–60 ºC) dengan perbandingan onggok:air 1:3 sambil diaduk selama 30 menit. Pencucian dilakukan 3 kali. Sampel onggok sebanyak 5 g dimasukkan ke dalam gelas piala dan ditambah 33 mL asam. Asam yang digunakan adalah HNO3 0.6 M. Campuran
Onggok Tersulfonasi (Ramakant, 1996)
Oksidasi onggok diawali dengan
dilarutkannya 30 g KIO4 dalam 425 ml air
distilat dengan ragam waktu masing-masing 210, 270, dan 330 menit. Larutan dijaga pada pH 4 dengan penambahan asam sulfat. Suhu reaksi ditingkatkan antara 35–40 ºC. Setelah reaksi oksidasi selesai, pulp onggok dicuci dengan merendam pulp dalam 100 ml air distilat selama 5 menit (pH air 6). Sampel
kemudian diagitasi selama 15 menit
kemudian disaring. Tahap pencucian ini diulang hingga 3 kali.
Pulp teroksidasi kemudian direaksikan dengan 100 ml larutan yang mengandung NaHSO3 dengan ragam bobot 15, 20, dan
35 g pada suhu 22 ºC dan ragam waktu 60, 120, dan 180 menit.
Onggok tersulfonasi kemudian dicuci dengan 100 ml etanol p.a selama 5 menit kemudian disaring dan didispersikan dalam 50 ml aseton p.a. selama 5 menit lalu dikeringudarakan pada suhu 22 ºC.
Pengukuran Kapasitas Penyerapan (Kiatkamjorwong 2002)
Material superabsorben ditimbang
sebanyak 0.1 gram kemudian dilarutkan dalam air destilat selama kurang lebih 4 jam pada suhu ruang hingga mencapai bobot
pembengkakan equilibrium. Sisa air
dipisahkan menggunakan kertas saring yang kemudian digantung selama 15 menit. Potongan kertas saring kering ditempatkan pada sampel untuk memastikan tidak adanya air bebas Kapasitas penyerapan QHO
2 dari
sampel absorben dihitung menggunakan persamaan Kering Sampel Bobot Kering Sampel Bobot Mengembang Sampel Bobot QHO
-=
2
Analisis Spektroskopi FTIR
Sebanyak 2 mg sampel yang halus dicampurkan ke dalam 198 mg KBr. Campuran ini digerus dan dibentuk menjadi pelet untuk dianalisis dengan FTIR.
Analisis Sulfur Total (Pusat Penelitian Balai Tanah 2005)
Timbang 0.05 g onggok ke dalam tabung digestion blok. Kemudian tambahkan 5 ml HNO3 p.a. dan 0.5 ml HClO4 p.a. lalu
dibiarkan 1 malam. Besoknya sampel dipanaskan dalam digestion blok dengan suhu 100 °C selama 1 jam, lalu suhu ditingkatkan menjadi 150 °C. Setelah uap
kuning habis suhu digestion blok
ditingkatkan menjadi 200 °C. Destruksi selesai setelah keluar asap putih dan sisa ekstrak kurang lebih 0.5 ml. Tabung diangkat dan dibiarkan dingin. Ekstrak diencerkan dengan air bebas ion hingga volume tepat 50 ml dan kocok dengan pengocok tabung hingga homogen.
Sebanyak 1 ml ekstrak dan deret standar S dipipet ke dalam tabung reaksi. Ditambahkan masing-masing 7 ml asam campur (campuran dari 50 ml CH3COOH
glasial p.a., 20 ml HCl pekat p.a., dan 20 ml H3PO4 pekat p.a., dan 2.5 ml larutan BaCl2
kemudian kocok dengan pengocok tabung hingga homogen. Biarkan 30 menit dan tkemudian diukur dengan spektrofotometer pada panjang gelombang 432 nm.
Kadar S =
100
1000
´
´
ml
ekstrak
ml
kurva
ppm
Desain Faktorial Tiga Tingkat (3k)
Rancangan faktorial (factorial design) merupakan salah satu cara yang digunakan dalam melakukan suatu percobaan untuk melihat efek dari dua faktor atau lebih terhadap hasil yang diperoleh. Dengan
menggunakan rancangan faktorial,
didefinisikan bahwa setiap percobaan yang dilakukan adalah kombinasi percobaan yang mungkin untuk setiap ragam dalam faktor
yang dicoba. Rancangan faktorial
merupakan solusi paling efisien, karena semua kemungkinan kombinasi tiap ragam dari faktor-faktor dapat diselidiki secara lengkap. Kelebihan desain faktorial adalah (i) lebih efisien dibandingkan dengan metode one-factor-at-a-time, (ii) mampu menunjukkan efek interaksi antar faktor, (iii) dapat memberikan perkiraan efek dari suatu faktor pada kondisi ragam yang berbeda-beda dari suatu faktor lain. Salah satu jenis
perancangan percobaan dengan
menggunakan faktorial desain adalah 3k faktorial desain. Dalam desain menggunakan 3kfaktorial desain ini, dilakukan penyusunan faktorial untuk k faktor pada 3 ragam (Mattjik 2002).
faktor-faktor lain diluar faktor-faktor yang sedang diteliti, dan dalam percobaan ini setiap unit percobaan diacak secara sempurna, tanpa dibatasi oleh blok.
Tabel 2 Rancangan percobaan screening
Sulfonasi onggok.
Bobot Bisulfit
tOksidasi tSulfonasi W1 W2 W3
O1 S1 O1S1W1 O1S1W2 O1S1W3
S2 O1S2W1 O1S2W2 O1S2W3
S3 O1S3W1 O1 S3W2 O1S3W3
O2 S1 O2S1W1 O2S1W2 O2S1W3
S2 O2S2W1 O2S2W2 O2S2W3
S3 O2S3W1 O2 S3W2 O2 S3W3
O3 S1 O3S1W1 O3S1W2 O3S1W3
S2 O3S2W1 O3S2W2 O3S2W3
S3 O3S3W1 O3S3W2 O3S3W3
HASIL DAN PEMBAHASAN
Onggok sebagai bahan baku pembuatan superabsorben dihaluskan hingga berukuran 100–200 mesh untuk meningkatkan luas permukaan sehingga reaksi lebih sempurna. Ion periodat digunakan sebagai agen pengoksidasi karena dapat bereaksi dengan
selulosa tanpa memutuskan rangkaian
polimernya, tetapi bekerja spesifik
memutuskan rantai 1,2 diol (Fessenden 1982). pH reaksi diatur antara 3 dan 4.5 dengan asam sulfat pekat. Pengaturan pH
dilakukan selain untuk meningkatkan
kelarutan KIO4, juga untuk menstabilkan
reaksi oksidasi dan mempercepat reaksi sulfonasi. Setelah reaksi sulfonasi selesai, sampel kemudian didispersikan dalam etanol p.a. dengan tujuan untuk mengeluarkan air yang terserap dalam sampel. Setelah itu, sampel didispersikan kembali dalam aseton p.a. untuk menjerap sisa etanol yang tertinggal dalam sampel. Aseton merupakan senyawa bipolar yang dapat menyerap pelarut yang bersifat polar dan nonpolar karena memiliki gugus yang bersifat hidrofobik sekaligus hidrofilik.
Polimer superabsorben yang telah
dihasilkan ditentukan kapasitas absorpsinya. Uji kapasitas absorpsi dilakukan dengan cara memasukan polimer absorben ke dalam
pelarut air. Polimer absorben akan
mengalami penggembungan seperti pada Gambar 8.
Gambar 8 Proses pembengkakan polimer superabsorben.
Air akan terdifusi dalam polimer
superabsorben karena adanya gugus
hidrofilik. Setelah mencapai tahap
kesetimbangan, atom hidrogen dar air akan membentuk ikatan hidrogen dengan ion SO32- yang terikat pada karbon selulosa.
Pada akhirnya air yang terserap akan tetap
tertahan pada polimer superabsorben
sehingga polimer mengalami
pembengkakan. Gambar 9 menunjukkan pembengkakan sampel onggok tersulfonasi. Saat terjadi pembengkakan, air terikat
melalui ikatan hidrogen sehingga
membentuk gel atau hidrokoloid. Penelitian ini menunjukkan bahwa reaksi sulfonasi dapat meningkatkan kapasitas absorbsi dari onggok yang awalnya sebesar 2.22 g/g meningkat hingga menjadi 44.06 g/g.
Gambar 9 Proses pembengkakan
superabsorben onggok.
Perlakuan Pendahuluan Asam
Nilai kapasitas penyerapan (
Q
HO2 ) yang tidak berbeda antara onggok yang diberi dan
tanpa perlakuan pendahuluan asam
2 2.5 3 3.5 4 4.5
15 30 45 60 75
Waktu Praperlakuan K ap as ita s A b so rb si
Pretreatmen 1 Pretreatment 2 Pretreatment 3 Rerata onggok awal
Gambar 10 Hubungan antara waktu pra perlakuan asam dan kapasitas absorbsi.
Kondisi Sufonasi Onggok Terhadap Kapasitas Absorbsi
Hasil analisis statistik untuk desain RAL faktorial lengkap dari proses sulfonasi onggok menggunakan perangkat lunak statistika V.6 menghasilkan persamaan;
Q = 25.61+14.47*O+5.064*O2+3.99*
S-2.21*S2+2.80*W-2.04*W21.14*O*S
+0.38*O*S2-3.47*O2*S+0.69*O2*S2 -1.23*O*W-1.92*O*W2-1.13O2W -2.10*O2*W2-0.33*S*W+0.17*S*W2+ 0.11*S2*W-1.48*S2*W
Dengan nilai koefisien R2 = 89.74%
Persamaan ini menunjukkan bahwa dengan data variable bebas (waktu oksidasi, waktu sulfonasi, dan bobot bisulfit), dalam penelitian ini dengan memasukkan data kapasitas absorpsi kedalam persamaan akan dapat mempredikisi daya serap produk dengan tingkat kepercayaan 89% dari yang seharusnya. Hasil analisis Anova (Lampiran 7) menunjukkan bahwa nilai probabilitas, baik pengaruh liniear atau kuadratik dari variable waktu oksidasi lebih kecil dari 0.05
(P =0.05), artinya waktu oksidasi
berpengaruh nyata terhadap nilai Q
(kapasitas absorpsi) pada tingkat
kepercayaan 95%. Kesempurnaan oksidasi dengan periodat akan memberikan peluang terbentuknya dialdehida pada C2 dan C3 dari selulosa sehingga adisi ion bisulfit berlangsung lebih banyak dan mudah. Dari data tersebut dapat disimpulkan bahwa
waktu oksidasi merupakan variabel
penentu, atau tahap paling kritis yaitu tidak terjadi sulfonasi jika tidak tersedia karbon yang mudah diadisi seperti gugus aldehida. Semakin banyak karbon yang teroksidasi,
semakin banyak kemungkinan yang
tersulfonsi, dan semakin besar daya
absorpsinya.
Reaksi oksidasi dalam prosesnya
dilakukan dengan pemanasan yang
memengaruhi banyaknya rantai karbon yang terputus pada monomer selulosa onggok. Semakin lama waktu oksidasi maka semakin banyak rantai yang terputus yang
dapat meningkatkan adisi bisulfit.
Banyaknya jumlah bisulfit yang teradisi pada karbon onggok dapat meningkatkan jumlah H2O yang terikat melalui ikatan
hidrogen.
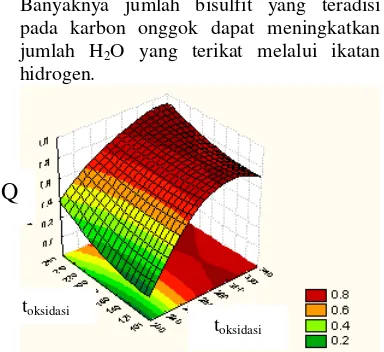
Gambar 11 Hubungan antara kapasitas absorbsi dengan toksidasi dan
tsulfonasi sampel
Ragam waktu sulfonasi yang digunakan adalah 120, 180 dan 240 menit. Lampiran 8 menunjukkan bahwa perpanjangan waktu
sulfonasi mmenurunkan kapasitas
penyerapan. Hal ini dipengaruhi oleh viskositas sampel pada saat disulfonasi. Pada sulfonasi 120 menit sampel lebih mudah diaduk sehingga homogenitasnya tinggi. Saat reaksi sulfonasi memasuki waktu 240 menit pengadukan, terpaksa dilanjutkan secara manual karena tingginya viskositas sampel.
Pada visualisasi Gambar 11 interaksi waktu oksidasi dan waktu sulfonalasi menunjukkan bahwa kondisi optimal akan tercapai dengan menambah waktu oksidasi dan sulfonasi. Pada waktu oksidasi 300 menit dan waktu sulfonasi 120–140, menit kapasitas absorpsinya mendekati optimum. Kondisi optimum dapat dicapai dengan memperpanjang waktu oksidasi. Hal ini didukung dari visualisasi interaksi bobot bisulfit dan waktu sulfonasi (Gambar 13) yang menunjukkan nilai kapasitas absorpsi yang tinggi juga dicapai pada waktu sulfonasi dan bobot bisulfit yang rendah. Namun, nilai kapasitas absorpsi optimum yang diperoleh dari bobot bisulfit dan waktu
toksidasi
toksidasi
sulfonasi rendah lebih kecil dibandingkan dengan nilai kedua faktor ditingkatkan.
Bobot NaHSO3 yang digunakan belum
menemukan titik optimumnya (Lampiran 8). Peningkatan jumlah bisulfit dalam penelitian ini meningkatkan kapasitas penyerapan onggok. namun ketika diusahakan untuk
mencapai nilai Q optimum ternyata
terhambat oleh mengentalnya sampel.
Demikian juga interaksi waktu oksidasi dan bobot bisulfit yang ditunjukkan oleh Gambar 12 bahwa kondisi optimal dapat dicapai dengan memperpanjang waktu oksidasi tanpa menambah bobot bisulfit.
Gambar 12 Hubungan kapasitas absorbsi dengan toksidasi dan bobot NaHSO3
Hal ini memperkuat dugaan bahwa faktor yang paling menentukan daya absorpsi onggok tersulfonasi adalah waktu oksidasi. Selain itu gambar 13 juga dapat memprediksi peningkatan waktu oksidasi dan bobot bisulfit dapat meningkatkan nilai Q. Adanya penurunan nilai Q pada variabel
O3 pada waktu 330 menit sehingga
viskositas sampel yang tinggi menyebabkan sampel menjadi sulit diaduk ditunjukkan pada lampiran 8 Namun sedikitnya dapat digambarkan apabila waktu oksidasi dan
jumlah bisulfit ditingkatkan, dapat
memberikan pengaruh pada peningkatan nilai
Q
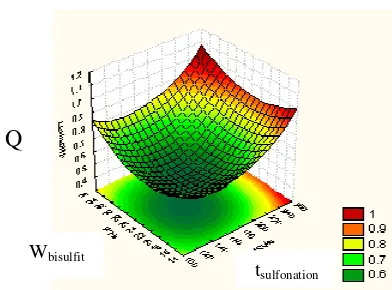
HO2 . Visualisasi interaksi bobot bisulfit dan waktu sulfonasi (Gambar 13) yang menunjukkan nilai kapasitas absorpsi yang tinggi juga dicapai pada waktu sulfonasi dan bobot bisulfit yang rendah. Akan tetapi, nilai kapasitas absorpsi optimum yang diperoleh dari bobot bisulfit dan waktu sulfonasi yang rendah lebih kecil
dibandingkan dengan semua faktor
ditingkatkan.
Q
H2O dapat mencapai nilaioptimumnya apabila jumlah bisulfit yang ditambahkan rendah namun mengalami waktu sulfonasi yang lebih lama lagi. Namun hubungan kedua variabel ini tidak terlalu signifikan terhadap nilai
Q
HO2 dilihat dari sedikitnya peluang yang ada.
Gambar 13 Hubungan kapasitas penyerapan dan tsulfonasi dan bobot NaHSO3
Hasil O2S1W3 dapat menunjukkan dari
total senyawa NaHSO3 yang ditambahkan
sebanyak 35 gram hanya 10.76 gram senyawa NaHSO3 yang dapat bereaksi
dengan sampel atau sekitar 68.78% senyawa NaHSO3 yang hilang, hal ini dapat terjadi
saat dispersi sampel dalam etanol dan aseton untuk mengikat pelarut, dalam hal ini ion bisulfit yang tidak bereaksi dengan sampel akan terlarut dalam pelarut dan terbuang saat dispersi. penelitian ini menghasilkan
Q
HO2 tanpa ulangan sebesar 44.06 g/g.
Pencirian Onggok
Tabel 3 menunjukkan adanya
peningkatan kadar sulfur total sebanyak 167 kali, dari onggok awal dengan kadar sulfur 0.02 menjadi 3.36% setelah disulfonasi. Adanya peningkatan kadar sulfur total,
mengindikasikan adanya bisulfit yang
teradisi pada sampel. Viskositas sampel juga
dipengaruhi oleh banyaknya senyawa
bisulfit yang digunakan. Pada produk absorben, sulfur dalam bentuk ion bisulfit dapat membentuk ikatan hidrogen dengan air sehingga dapat meningkatkan kapasitas absorbsi suatu sampel (Ramakant 1996). Sampel yang digunakan dalam pengukuran
toksidasi
Wbisulfit
tsulfonation
Q
Q
kadar sulfur total adalah sampel onggok awal dan sampel onggok tersulfonasi jumlah bisulfit terbanyak. Hal ini bertujuan untuk
membandingkan total sulfur yang
terkandung dalam sampel, sebelum dan sesudah reaksi.
Tabel 3 Kadar sulfur total
Sampel Kadar Sulfur Total (%) Kadar Sulfonat(%) Derajat Subtitusi
Onggok 0.02 0.50 0.01
Sampel 3.36 8.40 1.68
Pencirian dilakukan pada sampel yang belum mendapat perlakuan dan sampel dengan waktu oksidasi dan jumlah bisulfit terendah (O1S2W1), serta sampel dengan
waktu oksidasi dan jumlah bisulfit tertinggi (O3S1W3) (Lampiran 11). Hal ini bertujuan
membandingkan spektrum sebelum dan
sesudah perlakuan dengan 2 kondisi
berbeda. Spektrum FTIR tidak menunjukkan adanya adanya reaksi sulfonasi karena serapan gugus SO32- belum ditunjukkan pada
kedua sampel yang telah diberi perlakuan. Namun hasil analisis FTIR bukanlah suatu hasil yang pasti dalam penelitian ini karena hasil analisis sulfur menunjukkan adanya peningkatan kadar sulfur total dalam sampel. Spektrum FTIR dari onggok O1S2W1 dan
O3S1W3, memperlihatkan pita serapan dari
beberapa gelombang yang menunjukkan gugus yang terkandung dalam sampel. Salah satu pita serapan tersebut adalah pita serapan dari gugus –OH dan –CH. Karakteristik vibrasi ulur –OH terlihat pada daerah
bilangan gelombang 3550–3200 cm-1,
sedangkan vibrasi ulur –CH terdapat pada
bilangan gelombang 3000–2840cm-1
(Silverstein et al).
Spektrum FTIR dari sampel O3S1W3
pada daerah 3700–3500 cm-1 yang
merupakan vibrasi ulur gugus –OH yang intensitasnya menurun apabila dibandingkan dengan onggok awal Serapan pada bilangan gelombang 3000-2840 cm-1 merupakan vibrasi ulur C-H. Serapan pada daerah
bilangan gelombang 1205-1124 cm-1
merupakan serapan dari vibrasi ulur C-O dari alkohol sekunder yang mulai hilang pada sampel yang telah di sulfonasi. Serapan pada daerah bilangan gelombang 1150–1000 cm-1 terdapat ulur –CO dari aklohol sekunder, pada daerah ini juga terdapat banyak pita lain, yang menandakan besar kemungkinan senyawa yang diidentifikasi adalah senyawa karbohidrat. Pita –CO
adalah pita yang memiliki penurunan intensitas yang paling drastis hal ini dapat membuktikan adanya pemutusan antara rantai karbon 1 dan 5. Selain itu pita-pita berintensitas sangat lemah di daerah ini yang mengindikasikan hilangnya gugus –CO pada sampel O1S2W1 dan O3S1W3, gugus –CO
pada sampel telah teradisi dengan ion –SO3
sehingga berubah menjadi gugus hidroksil. Pada daerah 800–900cm-1 terdapat serapan dari vibrasi senyawaan nitro yang terdapat pada asam amino atau protein singkong.
Tabel 4 Vibrasi ulur dan tekuk dari onggok awal, sampel O1S2W1 dan O3S1W3
A (3700-3500) ulur -OH terikat dari karbohidrat B (3000–2500) C-H terisolasi, runcing dari
karbon polisakarida
C (1400-1600) Tekuk NH+, diduga berasal dari asam amino atau proteinnya D (1300-1100) vibrasi ulur C-O dari alkohol
sekunder
E (1150-1000) Ulur –CO diduga berasal dari CH2O-CH2
F (800-900) -NH2 yang diduga terdapat pada protein
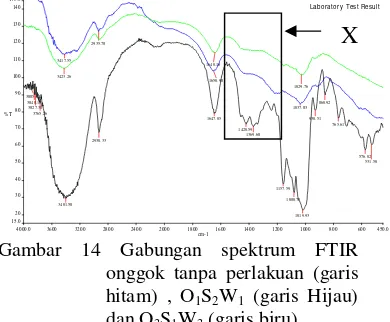
Serapan gugus –OH dan –CH yang menurun ketajamannya disebabkan adanya reaksi oksidasi pada gugus –OH yang memutus rantai (Gambar 14). Adanya perubahan intensitas sulfur akibat adisi gugus SO3- kurang tampak. Serapan gugus – OH dan –CH yang melemah disebabkan adanya reaksi oksidasi pada gugus –OH yang memutus rantai yang menyebabkan putusnya gugus hidroksil. Meskipun masih terdapat juga –OH dan –CH yang tidak putus.
4000.0 3600 3200 2800 2400 2000 1800 1600 1400 1200 1000 800 600 450.0 15.0 20 30 40 50 60 70 80 90 100 110 120 130 140 145.0 cm-1 %T
Laborat ory Test Result
3417.55 2935.78 1650.98 1037.83 3885.83 3848.16 3827.30 3765.26 3401.58 2930.33 1647.05 1420.59 1369.68 1157.59 1080.70 1019.93 930.51 860.92 765.61 576.02 531.50 3423.26 1640.16 1029.76
Gambar 14 Gabungan spektrum FTIR onggok tanpa perlakuan (garis hitam) , O1S2W1 (garis Hijau)
dan O3S1W3 (garis biru).
F
SIMPULAN DAN SARAN
Simpulan
Pemberian perlakuan pendahuluan asam pada onggok tidak memberikan perubahan signifikan pada kapasitas absorbsi onggok, sehingga dalam penelitian ini onggok awal tidak diberi perlakuan pendahuluan. Hasil penelitian menunjukkan bahwa onggok dapat ditingkatkan kapasitas absorbsinya melalui reaksi sulfonasi. Dari ketiga parameter yang diamati ternyata faktor oksidasi adalah penentu pada peningkatan kapasitas absorpsi Nilai kapasitas absorpsi tertinggi dihasilkan sampel O3S3W1 (waktu
oksidasi 330 menit, waktu sulfonasi 240 menit, dan jumlah pereaksi bisulfit sebanyak 15 g) yang memiliki rerata nilai kapasitas absorbsi sebesar 38.54 g/g. nilai ini meningkat cukup tinggi dari kapasitas absorbsi onggok awal sebesar 2.22 g/g.
Analisis data menunjukkan bahwa
kapasitas absorbsi onggok belum mencapai kapasitas penyerapan optimumnya hal ini dapat dilihat dari bentuk kurva yang belum mencapai titik maksimumnya. Hasil analisis
sulfur total menunjukkan adanya
peningkatan jumlah sulfur total pada sampel O3S1W3 (sampel dengan
Q
H2Otertinggikeempat) sebanyak 167 kali dari sulfur total pada onggok awal.
Saran
Perlu diadakan penelitian lanjutan untuk meningkatkan kapasitas penyerapan air pada onggok. factor oksidasi sebaiknya lebih diperhatikan seperti jenis, konsentrasi, waktu pengoksidasi disamping pengkajian yang lebih teliti pada perlakuan
DAFTAR PUSTAKA
Adam RS, Johnson JR. 1949. Laboratory experiments in Organic Chemistry. Ed ke-4. The Macmillan.
Anonim. 2008. Pengolahan pangan.
[Terhubung Berkala].
http://www.iptek.net.id. [23 Maret 2009].
[BPOM] Badan Pengawas Obat Dan
Makanan. 2004. Monografi Ekstrak
Tumbuhan Obat Indonesia. Jakarta: BPOM RI.
Darmadjati D.S. 1985. Strategi Penelitian Limbah Ubi Kayu di Indonesia. Di dalam F.G. Winarno (ed) Monografi Limbah Pertanian. Kantor menteri muda Urusan Peningkatan Produksi Pangan.
David J. 2007. Kajian Nisbah Lignin-NaHSO3 dan Ph Pada Reaksi Sulfonasi
Lignin Kraft Untuk Menghasilkan
Natrium Lignosulfonat [Skripsi]. Bogor: Fakultas Teknologi Pertanian, IPB.
Dayo G. 2003, ”Superabsorbent Polymer Composite (SAPC) Materials and their Industrial and High-Tech Applications”, Dissertation, Der Technischen U ät Bergakademie Fiberg University.
Erdener K. O¨ mer Barýs_ zu¨m, Dursun
Saraydýn, Olgun Gu¨ven, 2006,
“Swelling characterization of
gamma-radiation induced crosslinked
acrylamide/maleic acid hydrogels in urea solutions” Materials and Design Journals 27.
Gritter RJ, Bobbitt JM, Schwarting AE. 1991. Pengantar Kromatografi. Ed ke-2.Kosasih Padmawinata, penerjemah. Bandung: Penerbit ITB. Terjemahan dari: Introduction to Chromatograph.
Hwang JK, Penemu: LG Household & Healthcare. 24 feb 2004. Antibacterial Composition Having Xanthorrizol. US patent 6 696 404.
Jenie B.S.L dan Fachda.1991. Pemanfaatan Onggok Singkong dan Dedak Padi Untuk Produksi Pigmen Angkik oleh
Monescus Purpureus. Pertemuan Ilmiah Tahunan. Perhimpunan Mikrobiologi Indonesia.
Ketaren, S. 1988. Penentuan Komponen Utama Minyak Atsiri Temulawak (Curcuma xanthorrhiza Roxb.) [Skripsi]. Bogor: Fakultas Teknologi Pertanian, IPB.
Lehninger AL. 1982. Dasar-Dasar
Biokimia. Maggy Thenawijaya, Penerjemah. Jakarta: Penerbit Erlangga.
Terjemahan dari: Principles of
Lembaga Penelitian Tanah. 2005. Penuntun Analisis Kimia Tanah Dan Tanaman. Bogor: Balai Penelitian Tanah.
Marshall WE, Wartelle LH, Boler DE. 1999.
Enhanced Metal Adsorption by Soybean Hulls Modified with Citric Acid. Biores Technol 69: 263-268.
Netty, MR. Pemanfaatan Onggok Singkong Ternitrasi dan Terasetilasi Sebagai Fase Diam Kromatografi Kolom. [skripsi].
Fakultas Matematika dan Ilmu
Pengetahian Alam. IPB.
Pakpahan A, Pasaribu SM, Djauhari A, Nasution A.1993. Cassava Marketing System In Indonesia. IARD-J.15:52-59.
Pudjiastuti L, Suwarno N, Nurhatika S. 1999. Pemanfaatan limbah padat industri tepung tapioka menjadi etanol dalam usaha minimasi pencemaran lingkungan [Laporan Penelitian]. Surabaya: Pusat
Penelitian Kementrian Lingkungan
Hidup, Institut Teknologi Sepuluh
Nopember.
Rinaldy W. 1987. Pemanfaatan onggok singkong (Manihot esculenta Crantz)
sebagai bahan pembuatan etanol [Tesis]. Bogor: Fakultas Teknologi Pertanian, Institut Pertanian Bogor.
Santi. 2006. Onggok Sagu Termodifikasi Sebagai Fase Diam dalam Kromatografi
Kolom [skripsi]. Fakultas Matematika dan Ilmu Pengetahian Alam. IPB.
Sherma J, Fried B, editor. 2001. Handbook of Thin Layer Chromatography. Ed ke-2. New York: Marcel Dekker.
Shet Ramakan T, Penemu; Kimberly-Clark Coorperation. 4 Jun, 1996. Sulfonated Cellulose and Method of Preparation. US patent 5 522 967.
Sidik, Mulyono MW, Mutadi A. 1995.
Temulawak (Curcuma xanthorriza Roxb). Jakarta: Phyto Medika.
Skoog DA, Holler FJ, Nieman TA. 1998.
Principles of Instrumental Analysis. Ed ke-5. Philadelphia: Harcourt Brace.
Suda K, Kanlaya M, Manit S, 2002. ”Synthesis and Property Characterization of Cassava Starch Grafted Polyacrylamide-Maleic Acid Superabsorbent via Gamma Irradiation”, Polymer Journal 43.
Tjokroadikoesoemo, S. 1986. HFS dan
Industri Ubi Kayu Lainnya. Gramedia. Jakarta.
Lampiran 1 Diagram Pembuatan Onggok Tersulfonasi
10 gram
20 gram
30 gram
10 gram
20 gram
30 gram 10 gram
20 gram
30 gram
Onggok
10 gram
20 gram
30 gram
120 menit
180 menit
240 menit
10 gram
20 gram
30 gram 10 gram
20 gram
30 gram
10 gram
20 gram
30 gram
10 gram
20 gram
30 gram 10 gram
20 gram
30 gram
120 menit
180 menit
240 menit
210 menit
270 menit
330 menit
120 menit
180 menit
Lampiran 2 Diagram proses pembuatan tepung tapioka pada industri kecil
Singkong
Pengupasan Kulit
(manusia) Kulit dan Kotoran
Pencucian Air Buangan
Pemarutan (mesin)
Bubur Singkong
Pemerasan dan Penyaringan
(manusia)
Pemerasan dan Penyaringan
(mesin) Manusia
Air Pompa
Ampas (Onggok) dikeringkan Ampas (Onggok)
dikeringkan
Pengendapan Pati Limbah Cair
Limbah Cair
(dibuang ke lingkungan) Pengeringan
Penggilingan dan Pengayakan
Pengepakan
Tapioka Pengendapan
Limbah Cair (dibuang ke lingkungan)
Lindur Elot
Pengeringan
Lampiran 3 Diagram pembuatan onggok tersulfonasi
(Ramakant, 1996)
100 g pulp
onggok
30 gram NaIO
4dalam
425ml air destilat
t = 38 ºC, T = 210 menit
rendam onggok dalam 400 ml air
destilat (pH = 6), agitasi 15 menit.
saring. Ulangan 2 kali
pencucian
20 gram NaHSO
3dalam 400 liter air
destilat. T = 37.5 ºC, t= 120 menit
Pencucian kembali.
Cuci dalam 100 ml ethanol anhidrat,
selama 15 menit, saring dan kering
udarakan.
Cuci dalam 50 ml aseton anhidrat,
selama 15 menit, saring dan keringkan
Lampiran 4 Perhitungan uji proksimat onggok
Kadar air
Ulangan
1
2
Bobot Cawan kosong (g)
85.6735
82.4882
bobot cawan kosong + sampel (g)
95.3116
95.1757
Bobot sampel (g)
9.6381
12.6878
Bobot cawan kosong + sampel ( setelah oven) (g)
940.8420
93.5281
Bobot Sampel Setelah Oven (g)
8.4107
11.0399
Kadar air (%)
12.73
12.99
rerata (%)
12.86
Contoh Perhitungan
%
73
.
12
%
100
6381
.
9
2274
.
1
%
100
=
´
=
´
=
g
g
awal
sampel
bobot
air
bobot
air
Kadar
Kadar Abu
Ulangan
1
2
Bobot Cawan kosong (g)
33.3302
34.6598
bobot cawan kosong + sampel (g)
35.3972
37.8705
Bobot sampel (g)
2.0670
3.2107
Bobot cawan kosong + abu ( setelah oven) (g)
33.3526
34.6938
Bobot abu (g)
0.0224
0.0340
Kadar abu (%)
1.08
1.06
rerata (%)a
1.07
Contoh Perhitungan
% 08 . 1 % 100 067 . 2 0224 . 0 % 100 ) ( ) ( (%) = ´ = ´ = g g g Sampel Berat g Abu Berat Abu KadarKadar Lemak
Bobot (g)
Sampel
11.4915
Labu + lemak
76.7889
Labu + lemak
76.7729
Lemak
0.0160
Lampiran 5 Data pengukuran kapasitas absorbsi Onggok awal dan onggok dengan
perlakuan pendahuluan
Onggok Awal
Ulangan
Bobot (g)
QH
2O (g/g)
Awal
Akhir
1
1.0045
3.1240
2.11
2
1.0002
2.9905
1.99
3
1.0030
3.5706
2.56
Rerata
2.22
Praperlakuan Ulangan 1
Bobot (g)
Waktu (menit)
awal
akhir
QH
2O (g/g)
15
1.0030
3.6740
2.66
30
1.0932
4.2274
2.87
45
1.0357
4.4040
3.25
60
1.0870
4.2521
2.91
75
1.1087
5.7639
4.20
Praperlakuan Ulangan 2
Bobot (g)
Waktu (menit)
awal
akhir
QH
2O (g/g)
15
1.0058
3.9343
2.91
30
1.0021
3.5692
2.56
45
1.0341
4.5863
3.44
60
1.0097
4.0853
3.05
75
1.0511
4.7545
3.52
Praperlakuan Ulangan 3
Bobot (g)
QH
2O (g/g)
Waktu (menit)
awal
akhir
15
1.0045
3.9075
2.89
30
1.0648
3.9504
2.71
45
1.0025
4.4009
3.39
60
1.0362
4.6007
3.44
Lampiran 6 Kapasitas absorbsi (QH
2O) untuk semua perlakuan dengan 3 kali ulangan
Ulangan 1 20 juni Ulangan 2 21 juni Ulangan 3 24 juni
Bobot
QH2O
Bobot Bobot rerata
Awal Akhir Awal Akhir QH2O Awal Akhir QH2O Ulangan 1 Ulangan 2 Ulangan 3 Rerata
O1S1W1 0.1139 1.192 9.45 0.1005 1.6311 15.23 0.1174 2.4924 20.23 9.45 15.23 20.23 14.97
O1S1W2 0.1102 1.172 9.63 0.177 2.2602 11.77 0.1403 1.8477 12.17 9.63 11.77 12.17 11.19
O1S1W3 0.1577 1.8731 10.88 0.1095 1.902 16.37 0.1565 2.7137 16.34 10.88 16.37 16.34 14.53
O1S2W1 0.1048 1.1708 10.17 0.1732 2.6742 14.44 0.1284 2.1147 15.47 10.17 14.44 15.47 13.36
O1S2W2 0.1011 1.007 8.22 0.1303 2.7584 20.17 0.2139 3.6812 16.21 8.22 20.17 16.21 14.9
O1S2W3 0.1285 2.6445 19.58 0.1806 3.5505 18.66 0.123 2.2312 17.14 19.58 18.66 17.14 14.46
O1S3W1 0.1199 1.3538 10.34 0.2642 4.3821 15.58 0.1175 1.1756 13.95 10.34 15.58 13.95 13.29
O1 S3W2 0.1686 3.3298 18.75 0.1256 3.2354 24.76 0.1004 2.6445 25.34 18.75 24.76 25.34 22.95
O2S1W3 0.1778 5.2682 28.63 0.1694 4.6771 26.61 0.1678 4.4802 25.7 28.63 26.61 25.7 26.98
O2S1W1 0.1054 3.4276 31.52 0.1226 3.7233 29.37 0.1077 3.0586 27.4 31.52 29.37 27.4 29.43
O2S1W2 0.1825 4.8088 25.35 0.1884 5.7763 29.66 0.1403 4.1444 28.54 25.35 29.66 28.54 27.85
O1S3W3 0.1695 5.2612 30.04 0.1343 4.824 34.92 0.1047 3.2163 29.72 30.04 34.92 29.72 31.56
O2S2W1 0.1117 3.6916 32.05 0.1216 4.065 32.43 0.1762 4.6358 25.31 32.05 32.43 25.31 29.93
O2S2W2 0.1373 3.1057 21.62 0.184 4.6699 24.38 0.1039 2.5403 23.45 21.62 24.38 23.45 23.15
O2S2W3 0.1172 4.3117 35.79 0.1756 4.9027 26.92 0.1122 3.4905 30.11 35.79 26.92 30.11 30.94
O2S3W1 0.1476 4.503 29.51 0.1362 4.2521 30.22 0.3292 10.8076 31.83 29.51 30.22 31.83 30.52
O3S1W2 0.1243 3.3946 26.31 0.1213 3.6402 29.01 0.1263 2.7293 20.61 26.31 29.01 20.61 25.31
O2 S3 W3 0.1007 3.169 30.47 0.2006 5.9377 28.6 0.3764 13.4337 34.69 30.47 28.6 34.69 31.26
O3S1W1 0.1225 3.4483 27.15 0.2891 6.6897 22.14 0.1664 5.5993 26.64 27.15 22.14 26.64 25.32
O3S1W2 0.4217 12.0437 27.56 0.1205 3.8078 30.6 0.0876 2.6954 29.77 27.56 30.6 29.77 29.29