DAFTAR PUSTAKA
Agusnar, H. 2007.Kimia Lingkungan. USU Press. Medan.
Alfial,Z. 2004.Analisis Kadar Fe dalam Minuman Ringan Kemasan Kaleng Dengan
Menggunakan Spektrofotometri Serapan Atom. Jurnal Sains Kimia.Vol 8. No.1 ISSN: 0854-3054
Albert,D.S.2012.Pengaruh Variasi Tekanan Terhadap Konstanta Kisi Debu Vulkanik Gunung Sinabung. Skripsi Departemen Fisika USU.
Azwar, A.1996. Pengantar Kesehatan Lingkungan.Penerbit Buku Kedokteran EGC.
Jakarta.
Chandra, B. 2005. Pengantar Kesehatan Lingkungan. Penerbit Buku Kedokteran
EGC. Jakarta.
Darmono, B. 1995. Logam Dalam Sistem Biologi Makhluk Hidup. UI Press. Jakarta.
Effendi, H. 2003. Telaah Kualitas Air Bagi Pengolahan Sumber Daya dan
Lingkungan Perairan. Penerbit Kanisius. Yogyakarta.
Khopkar, S. M. 2008. Konsep Dasar Kimia Analitik. UI Press. Jakarta.
Palar, H. 2004. Pencemaran Dan Toksikologi Logam Berat. Cetakan 2. Rineka Cipta.
Jakarta.
Rohman, A. 2007. Kimia Farmasi Analisis. Cetakan 1. Pustaka Pelajar. Yogyakarta.
Slamet, J.S. 2009. Kesehatan Lingkungan. Gadjah Mada University Press.
Yogyakarta.
Standard Methods For the Examination of Water and Watewater . 1899. Fifteenth Edition. American Public Health Association 1015 Fiffteen Street NW
Washington, DC 20005.
Surbakti, P. 2011, Analisis Logam Berat Cadmium (Cd), Cuprum (Cu), Cromium
Sutrisno, C,T. 2004. Teknologi Penyediaan Air Bersih. PT Rineka Cipta. Jakarta.
Wardhana, W. A. 2004. Dampak Pencemaran Lingkungan. Andi. Yogyakarta.
Widowati, W. Astiana Sastiono. Rymond Jusuf Rumampuk. 2008. Efek Toksik
Logam. Andi. Yogyakarta.
Badan Standarisasi Nasional. Cara Uji Kadmium (Cd) dengan Spektrofotometri
Serapan Atom (SSA)-nyala. SNI 6989.16:2009
Badan Standarisasi Nasional. Cara Uji Mangan (Mn) dengan Spektrofotometri
Serapan Atom (SSA)-nyala. SNI 6989.2:2009
Badan Standarisasi Nasional. Cara Uji Besi (Fe) dengan Spektrofotometri Serapan
Atom (SSA)-nyala. SNI 6989.4:2009
Darmono. 1995. Logam Dalam Sistem Mahkluk Hidup. Jakarta : UI Press
Darmono. 2001. Lingkungan Hidup dan Pencemaran. Jakarta : UI Press
Effendi, H. 2003. Telaah Kualitas Air Bagi Pengelolaan Sumber Daya dan
Lingkungan Periran. Yogyakarta : Kanisius
Haswell, S. J. 1991. Atomic Absorption Spectrometry Theory, Design and
Application. Amsterdam : Elsevier.
Jovita, T M. 2003. Kandungan Logam Berat Pada Kerang Darah (Anadara
Montgomery, J. M. 1985. Water Treatment Principles and Design. New York : John
Wiley and Sons
Mulja, M. 1995. Analisis Instrumental. Surabaya : Airlangga University Press
Mulyanto, H. R. 2007. Ilmu Lingkungan. Yogyakarta : Graha Ilmu
Palar, H. 2004. Pencemaran dan Toksikologi Logam Berat. Jakarta : Rineka Cipta
Rohman, A. 2007. Kimia Farmasi Analisis. Yogyakarta : Pustaka Pelajar.
Sartono. 2002. Racun dan Keracunan. Jakarta : Widya medika
Underwood, D.A.1998.Analisa Kimia Kuantitatif.Jakarta. Erlangga
Wikipedia A, 2010, Gunung Berapi, (http://id.wikipedia.org/wiki/Gunung_berapi)
diakses tanggal 29 maret 2015.
Wikipedia B, 2010.GunungSinabung(http://id.wikipedia.org/wiki/Gunung_Sinabung)
di akses tanggal 02 Maret 2015.
Vogel, A.I.1994. Buku Teks Anorganik Kualitatif Makro dan Semi Mikro.Edisi
BAB 3
METODE PENELITIAN
3.1 Alat dan Bahan penelitian 3.1.1 Alat-alat penelitian
- Gelas Beaker Pyrex 1000 ml
- Gelas Beaker Pyrex 250 ml
- Gelas Ukur pyrex 100 ml
- Labu Takar Pyrex 50 ml
- Pipet Tetes
- Hotplate Cimarec
- Kertas Saring Whatman No 42
- Spektofotometer Serapan Atom (SSA) GBC AVANTA
VER.2.02
- Corong kaca
- Pipet Volume Fisherbrand 5mL
- Botol Aquadest
- Botol Sampel
- Bola Karet
- Neraca analitis AND
- Oven
- pH meter
3.1.2. Bahan-bahan penelitian
- Sampel Sedimen dan Air sungai desa Guru kinayan kec.Naman teran
- HNO3(p) p.a (E.Merck)
- Larutan Standar Fe 1000 mg/L p.a (E.Merck)
- Larutan Standar Mn 1000 mg/L p.a (E.Merck)
- Larutan Standar Cd 1000 mg/L p.a (E.Merck)
- Akuades.
3.2 Pesedur Penelitian
3.2.1. Metode Pengambilan sampel
Metode Pengambilan Sampel dilakukan dengan Metode Grab Sampel. Tititk titk
sampel diambil yaitu pada hulu dan hilir. Jarak antara hulu sungai dengan hilir sungai
yaitu ± 3 km. Sedimen dan Air diambil dengan menggunakan metode sederhana
dengan alat penampung plastik. Alat tersebut diturunkan ke dasar sungai yang
dalamnya sekitar 1 meter. Kemudian alat tersebut diangkat dan ditarik ke permukaan.
sampel yang diperoleh dimasukkan kedalam botol yg terbuat dari plastik. Selanjutnya
sampel dibawa ke laboratorium kimia LIDA USU. Kemudian diberi label dan tanda.
3.2.2. Pengawetan dan Preparasi Sampel
Sampel ditambahkan HNO3(p) sampai pH ± 4. Di pisahkan antara sampel sedimen
dengan sampel air. Yaitu dengan cara di saring menggunakan kertas saring whatman
no 42. Air yang tersaring di masukkan kedalam botol sampel dan diberi tanda dan
sampel Air diambil sebanyak 100 mL sampel kemudian dimasukkan ke dalam beaker
glass dan ditambahkan 5 mL HNO3(p). Dipanaskan sampai hampir kering, kemudian
ditambahkan 50 mL akuades dan dimasukkan kedalam labu takar 100 mL melalui
kertas saring. Diencerkan dengan akuades sampai garis tanda dan diaduk sampai
homogen.
3.2.3. Pembuatan Larutan Standar Besi (Fe) 100 mg/L
Sebanyak 5 mL larutan induk Besi (Fe) 1000 mg/L dimasukkan kedalam labu takar
50 mL lalu diencerkan dengan larutan pengencer sampai garis tanda dan diaduk
sampai homogen.
3.2.4. Pembuatan Larutan Standar Besi (Fe) 10 mg/L
Sebanyak 5 mL larutan induk standar 100 mg/L dimasukkan kedalam labu takar 50
mL lalu diencerkan dengan larutan pengencer sampai garis tanda dan diaduk sampai
homogen.
3.2.5. Pembuatan Larutan Standar Besi (Fe) 1 mg/L
Sebanyak 5 mL larutan induk standar 10 mg/L dimasukkan kedalam labu takar 50 mL lalu diencerkan dengan larutan pengencer sampai garis tanda dan diaduk sampai
homogen.
3.2.6. Pembuatan Larutan Seri Standar Besi (Fe) 0,0; 0,2; 0,4; 0,6 dan 0,8 mg/L Sebanyak 0; 10; 20; 30 dan 40 mL larutan standar Besi (Fe) 1 mg/L dimasukkan
kedalam labu takar 50 mL lalu diencerkan dengan larutan pengencer sampai garis
tanda dan diaduk sampai homogen.
3.2.7. Pembuatan Kurva Kalibrasi Besi (Fe)
Larutan seri standar Besi (Fe) 0,2 mg/L diukur dengan menggunakan
sebanyak tiga kali. Dilakukan hal yang sama untuk larutan seri standar 0,4; 0,6; 0,8,
1,0 mg/L dan blanko.
3.2.8. Pengukuran Kadar Besi (Fe) dalam Sampel
Absorbansi diukur dengan Spektrofotometer Serapan Atom (SSA) pada �spesifik =
248,3 nm. Perlakuan dilakukan sebanyak 3 kali untuk setiap sampel
3.2.9. Pembuatan Larutan Standar Kadmium (Cd) 100 mg/L
Sebanyak 5 mL larutan induk Kadmium (Cd) 1000mg/L dimasukkan kedalam labu
takar 50 mL lalu diencerkan dengan larutan pengencer sampai garis tanda dan diaduk
sampai homogen.
3.2.10. Pembuatan Larutan Standar Kadmium (Cd) 10 mg/L
Sebanyak 5 mL larutan standar 100 mg/L dimasukkan kedalam labu takar 50 mL lalu
diencerkan dengan larutan pengencer sampai garis tanda dan diaduk sampai
homogen.
3.2.11. Pembuatan Larutan Standar Kadmium (Cd) 1 mg/L
Sebanyak 5 mL larutan standar 10 mg/L di masukkan kedalam labu takar 50 mL lalu
di encerkan dengan larutan pengencer sampai garis tanda dan diaduk sampai
homogen.
3.2.12. Pembuatan Larutan Seri Standar Kadmium (Cd) 0,000; 0,001; 0,002; 0,003; 0,004 dan 0,005 mg/L
Sebanyak 0,00; 0,05; 0,10; 0,15; 0,20 dan 0,25 mL larutan standar Kadmium (Cd) 1
mg/L dimasukkan kedalam labu takar 50 mL lalu diencerkan dengan larutan
3.2.13. Pembuatan Kurva Kalibrasi Kadmium (Cd)
Larutan seri standar Kadmium (Cd) 0.001 mg/L diukur absorbansinya dengan
menggunakan Spektrofotometer Serapan Atom (SSA) pada �spesifik = 228,8 nm.
Perlakuan dilakukan sebanyak tiga kali. Dilakukan hal yang sama untuk larutan seri
standar 0,002; 0,003; 0,004 dan 0,005 mg/L
3.2.14. Pengukuran Kadar Kadmium (Cd) dalam Sampel
Absorbansi diukur dengan Spektrofotometer Serapan Atom (SSA) pada �spesifik =
228,8 nm. Perlakuan dilakukan sebanyak 3 kali untuk setiap sampel.
3.2.15. Pembuatan Larutan Standar Mangan (Mn) 100 mg/L
Sebanyak 5 mL larutan induk Mangan (Mn) 1000 mg/L dimasukkan kedalam labu
takar 50 mL lalu diencerkan dengan larutan pengencer sampai garis tanda dan diaduk
sampai homogen.
3.2.17. Pembuatan Larutan Standar Mangan (Mn) 10 mg/L
Sebanyak 5 mL larutan induk Mangan (Mn) 100 mg/L dimasukkan kedalam labu
takar 50 mL lalu diencerkan dengan larutan pengencer sampai garis tanda dan diaduk
sampai homogen.
3.2.18. Pembuatan Larutan Standar Mangan (Mn) 1 mg/L
Sebanyak 5 mL larutan induk Mangan (Mn) 10 mg/L dimasukkan kedalam labu takar
50 mL lalu diencerkan dengan larutan pengencer sampai garis tanda dan diaduk
sampai homogen.
3.2.19. Pembuatan Larutan Seri Standar Mangan (Mn) 0,0; 0,5; 1,0; 1,5; 2,0 dan 2,5 mg/L
Dipipet sebanyak 0,0; 25 mL larutan standar Mangan 1 mg/L dan juga dipipet
sebanyak 7,5; 10 dan 12,5 mL larutan standar Mangan 10 mg/L kemudian di
3.2.20. Pembuatan Kurva Kalibrasi Mangan (Mn)
Larutan seri standar Mangan (Mn) 0,5 mg/L diukur dengan menggunakan
Spektrofotometri Serapan Atom (SSA) pada�spesifik = 279,5 nm. Perlakuan dilakukan
sebanyak tiga kali. Dilakukan hal yang sama untuk larutan seri standar 1,0; 1,5; 2,0,
3.2.21. Pengukuran Kadar Mangan (Mn) dalam Sampel
Absorbansi diukur dengan Spektrofotometer Serapan Atom (SSA) pada �spesifik=
3.3 Bagan Penelitian
3.3.1 Pembuatan Larutan Seri Standar Besi (Fe)0,0; 0,2; 0,4; 0,6; 0,8 dan 1,0 mg/L dan Pembuatan Kurva Kalibrasi Besi (Fe)
(SNI 6989.4:2009)
Larutan Standar Besi 1000 mg/L
Dipipet sebanyak 5 mL larutan standar Besi kemudian dimasukkan
kedalam labu takar 50 mL.
Diencerkan dengan akuades sampai garis tanda
Diaduk hingga homogen
Larutan Standar Besi 100 mg/L
Dipipet sebanyak 5 mL larutan standar Besi kemudian dimasukkan
kedalam labu takar 50 mL
Diencerkan dengan akudes sampai garis tanda
Diaduk hingga homogen
Larutan Standar Besi 10 mg/L
Dipipet sebanyak 5 mL larutan standar Besi kemudian dimasukkan
kedalam labu takar 50 mL
Diencerkan dengan akudes sampai garis tanda
Diaduk hingga homogen
Larutan Standar Besi 1 mg/L
Dipipet sebanyak 0;10; 20; 30 dan 40 mL larutan standar Besi
kemudian dimasukkan kedalam labu takar 50 mL
Diencerkan dengan akudes sampai garis tanda
Diaduk hingga homogen
Larutan Seri Standar Besi 0,0; 0,2; 0,4; 0,6
dan 0,8 mg/L
Diukur absorbansinya dengan Spektrofotometer Serapan Atom
3.3.2. Pembuatan Larutan Seri Standar Kadmium (Cd) 0,000; 0,001; 0,002; 0,003; 0,004 dan 0,005 mg/L dan Pembuatan Kurva Kalibrasi Kadmium (Cd) (SNI 6989.16:2009)
Larutan Standar Kadmium 1000 mg/L
Dipipet sebanyak 5 mL larutan standar Kadmium kemudian di
masukkan kedalam labu takar 50 mL.
Diencerkan dengan akuades sampai garis tanda
Diaduk hingga homogen
Larutan Standar Kadmium100 mg/L
Dipipet sebanyak 5 mL larutan standar kadmium kemudian di
masukkan kedalam labu takar 50 mL
Diencerkan dengan akudes sampai garis tanda
Diaduk hingga homogen
Larutan Standar Kadmium 10 mg/L
Dipipet sebanyak 5 mL larutan standar kadmium kemudian di
masukkan kedalam labu takar 50 mL
Diencerkan dengan akudes sampai garis tanda
Diaduk hingga homogen
Larutan Standar Kadmium 1 mg/L
Dipipet sebanyak 0,0; 0,05; 0,1; 0,15; 0,20 dan 0,25 mL larutan
standar Kadmium kemudian di masukkan kedalam labu takar 50 mL
Diencerkan dengan akuades sampai garis tanda
Diaduk hingga homogen
Larutan Seri Standar kadmium 0,0; 0,001;
0,002; 0,003; 0,004 dan 0,005 mg/L
Diukur absorbansinya dengan Spektrofotometer Serapan Atom
(SSA) dengan �spesifik = 228,8 nm
3.3.3. Pembuatan Larutan Seri Standar Mangan (Mn) 0,0; 0,5; 1,0; 1,5; 2,0 dan 2,5 mg/L dan Pembuatan Kurva Kalibrasi Mangan (Mn)
(SNI 6989.41:2005)
Larutan Standar Mangan 1000 mg/L
Dipipet sebanyak 5 mL larutan standar Mangan kemudian di
masukkan kedalam labu takar 50 mL.
Diencerkan dengan akuades sampai garis tanda
Diaduk hingga homogen
Larutan Standar Mangan 100 mg/L
Dipipet sebanyak 5 mL larutan standar Mangan kemudian di
masukkan kedalam labu takar 50 mL
Diencerkan dengan akudes sampai garis tanda
Diaduk hingga homogen
Lrutan Standar Mangan 10 mg/L
Dipipet sebanyak 5 mL larutan standar Mangan kemudian di
masukkan kedalam labu takar 50 mL
Diencerkan dengan akudes sampai garis tanda
Diaduk hingga homogen
Larutan Standar Mangan 1 mg/L
Dipipet sebanyak 0,0; 25 mL larutan standar Mangan 1 mg/L dan
juga dipipet sebanyak 7,5; 10 dan 12,5 mL larutan standar Mangan
10 mg/L kemudian di masukkan kedalam labu takar 50 mL
Diencerkan dengan akuades sampai garis tanda
Diaduk hingga homogen
Larutan seri standar Mangan 0,5; 1,5;
2,0 dan 2,5 mg/L
Diukur absorbansinya dengan Spektrofotometer Serapan Atom
(SSA) dengan �spesifik = 279,5 nm
3.3.4. Pemisahan sampel sedimen dan sampel air.
Sampel Air sungai dan sedimen.
Disaring dengan kertas saring whatman no 44
(Residu) Sampel sedimen.
(Filtrat) Sampel air
3.3.5 Penentuan Kadar Unsur Besi (Fe) pada Sampel sedimen (Darmono,1995)
Dikeringkan 3 hari
Digerus
Dioven hingga suhu 105o C ± 6 jam
Ditimbang 1 gram
Ditambahkan 40 ml HNO3(P)
Dipanaskan hingga suhu 80o C hingga
HNO3(P)
menguap
Didinginkan
Diencerkan dengan aquades hingga
volume 100 ml
Disaring dengan kertas saring Whatman
no.42
Diukur pH 4
Dimasukkan kedalam labu takar 50 ml
hingga garis tanda.
Diukur absorbansinya dengan alat SSA
3.3.6 Penentuan Kadar Mangan (Mn) pada Sampel sedimen (Darmono,1995)
Dikeringkan 3 hari
Digerus
Dioven hingga suhu 105o C ± 6 jam
Ditimbang 1 gram
Ditambahkan 40 ml HNO3(P)
Dipanaskan hingga suhu 80o C hingga
HNO3(P)
menguap
Didinginkan
Diencerkan dengan aquades hingga
volume 100 ml
Disaring dengan kertas saring Whatman
no.42
Diukur pH 4
Dimasukkan kedalam labu takar 50 ml
hingga garis tanda.
Diukur absorbansinya dengan alat SSA
pada λspesifik 279,5 nm Sampel sedimen
3.3.7 Penentuan Kadar Kadmium (Cd) pada Sampel sedimen (Darmono,1995)
Dikeringkan 3 hari
Digerus
Dioven hingga suhu 105o C ± 6 jam
Ditimbang 1 gram
Ditambahkan 40 ml HNO3(P)
Dipanaskan hingga suhu 80o C hingga
HNO3(P)
menguap
Didinginkan
Diencerkan dengan aquades hingga
volume 100 ml
Disaring dengan kertas saring Whatman
no.42
Diukur pH 4
Dimasukkan kedalam labu takar 50 ml
hingga garis tanda.
Diukur absorbansinya dengan alat SSA
3.3.8. Penentuan Kadar Besi (Fe) pada Sampel Air (SNI 6989.4:2009)
Dimasukkan kedalam beaker glass 100 mL
Ditambahkan dengan 5 mL HNO3(p)
Dipanaskan perlahan diatas hotplate hingga sisa volume 15 mL
Ditambahkan dengan 50 mL akuades
Dimasukkan kedalam labu takar 100 mL melalui kertas saring
Diencerkan dengan akuades sampai garis tanda
Dihomogenkan
Diukur absorbansinya dengan Spektrofotometri Serapan atom
(SSA) pada �spesifik = 248,3 nm Sampel Air
3.3.8. Penentuan Kadar Mangan (Mn) pada Sampel Air (SNI 6989.41:2005)
Dimasukkan kedalam beaker glass 100 mL
Ditambahkan dengan 5 mL HNO3(p)
Dipanaskan perlahan diatas hotplate hingga sisa volume 15 mL
Ditambahkan dengan 50 mL akuades
Dimasukkan kedalam labu takar 100 mL melalui kertas saring
Diencerkan dengan akuades sampai garis tanda
Dihomogenkan
Diukur absorbansinya dengan Spektrofotometri Serapan atom
(SSA) pada �spesifik = 279,5 nm
Hasil
3.3.8. Penentuan Kadar Kadmium (Cd) pada Sampel Air (SNI 6989.16:2004)
Dimasukkan kedalam beaker glass 100 mL
Ditambahkan dengan 5 mL HNO3(p)
Dipanaskan perlahan diatas hotplate hingga sisa volume 15 mL
Ditambahkan dengan 50 mL akuades
Dimasukkan kedalam labu takar 100 mL melalui kertas saring
Diencerkan dengan akuades sampai garis tanda
Dihomogenkan
Diukur absorbansinya dengan Spektrofotometri Serapan atom
(SSA) pada �spesifik = 228,8 nm
Hasil
BAB 4
HASIL DAN PEMBAHASAN
4.1. Hasil Penelitian 4.1.1. Logam Besi (Fe)
Pada pengukuran Logam Besi (Fe) dengan menggunakan alat Spektrofotometer
Serapan Atom (SSA) komdisi alat dapat dilihat pada tabel 4.1
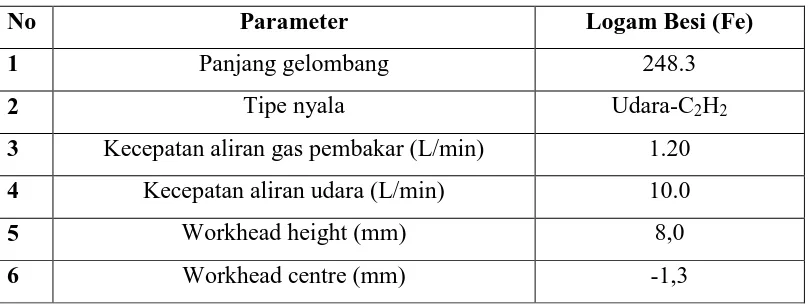
Tabel 4.1. Kondisi alat Atomic Absorbtion Spectrophotometer (AAS) merk GBC AVANTA VER. 2.02
No Parameter Logam Besi (Fe)
1 Panjang gelombang 248.3
2 Tipe nyala Udara-C2H2
3 Kecepatan aliran gas pembakar (L/min) 1.20
4 Kecepatan aliran udara (L/min) 10.0
5 Workhead height (mm) 8,0
6 Workhead centre (mm) -1,3
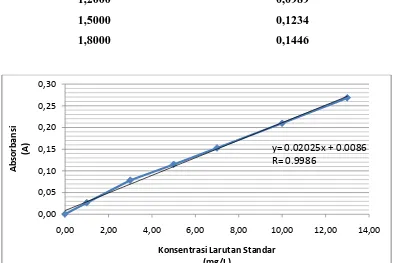
Pembuatan kurva larutan standar unsur Besi (Fe) dilakukan dengan menyiapkan
larutan standar dengan berbagai konsentrasi yaitu pada pengukuran 0,0000; 0,3000;
0,6000; 0,9000; 1,2000; 1,5000; dan 1,8000 mg/L, kemudian diukur absorbansinya
dengan alat SSA. Data absorbansi untuk larutan standar Besi (Fe) dapat dilihat pada
Tabel 4.2. Data absorbansi larutan standar Besi (Fe)
Konsentrasi (mg/L) Absorbansi Rata – Rata (Ā)
0,0000 0,0002
Gambar 4.1. Kurva Larutan Standar Logam Besi (Fe) 0,00
0,00 2,00 4,00 6,00 8,00 10,00 12,00 14,00
4.1.2. Pengolahan Data Logam Besi (Fe)
4.1.2.1. Penurunan Persamaan Garis Regresi Dengan Metode Least Square Hasil pengukuran absorbansi larutan seri standar logam Besi (Fe) pada tabel 4.2. di
plotkan terhadap konsentrasi sehingga diperoleh kurva berupa garis linear. Persamaan
garis regresi untuk kurva ini dapat diturunkan dengan metode Least Square dengan
data pada tabe 4.3
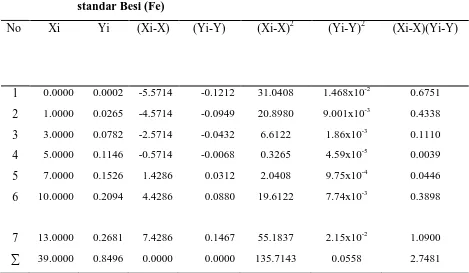
Tabel 4.3 Penurunan persamaan garis regresi untuk penentuan konsentrasi Logam Besi (Fe) berdasarkan pengukuran absorbansi larutan standar Besi (Fe)
No Xi Yi (Xi-X) (Yi-Y) (Xi-X)2 (Yi-Y)2 (Xi-X)(Yi-Y)
1 0.0000 0.0002 -5.5714 -0.1212 31.0408 1.468x10-2 0.6751
2 1.0000 0.0265 -4.5714 -0.0949 20.8980 9.001x10-3 0.4338
3 3.0000 0.0782 -2.5714 -0.0432 6.6122 1.86x10-3 0.1110
4 5.0000 0.1146 -0.5714 -0.0068 0.3265 4.59x10-5 0.0039
5 7.0000 0.1526 1.4286 0.0312 2.0408 9.75x10-4 0.0446
6 10.0000 0.2094 4.4286 0.0880 19.6122 7.74x10-3 0.3898
7 13.0000 0.2681 7.4286 0.1467 55.1837 2.15x10-2 1.0900
�= ∑��� = 39.000
7 =5.5714
�= ∑��
� = 0.8496
7 =0.1214
Persamaan garis regresi untuk kurva dapat di turunkan dari persamaan garis :
�= ��+�
Dimana :
a = slope
b = intersept
Selanjutnya harga slope dapat ditentukan dengan menggunakan metode least square
sebagai berikut :
� = ∑(�� − �)(�� − �)
∑(�� − �)2
�= � − ��
Dengan mensubstitusikan harga – harga yang tercantum pada tabel 4.2 pada
persamaan di atas maka diperoleh :
� = 2.7481
135.7143 =0.02025
b = 0,1214– (0,02025 x 5,5714)
= 0,1214−0,1128
= 0,0086
Maka persamaan garis yang diperoleh adalah :
4.1.2.2. Koefisien Korelasi
Koefisien korelasi dapat ditentukan dengan menggunakan persamaan sebagai berikut
:
�= ∑(�� − �)(�� − �) [∑(�� − �)2 ∑(�� − �)2]½
�= 2,7481
[(135,7143)(0,0558)]½
�= 2,7481
[7,5728]½
�= 2,7481
2,7518
�= 0,9986
4.1.2.3. Penentuan Konsentrasi logam Besi (Fe)
Untuk menghitung konsentrasi dari logam Besi (Fe), maka diambil data hasil
pengukuran absorbansi logam Besi (Fe) dalam air sungai dan sedimen (padatan total)
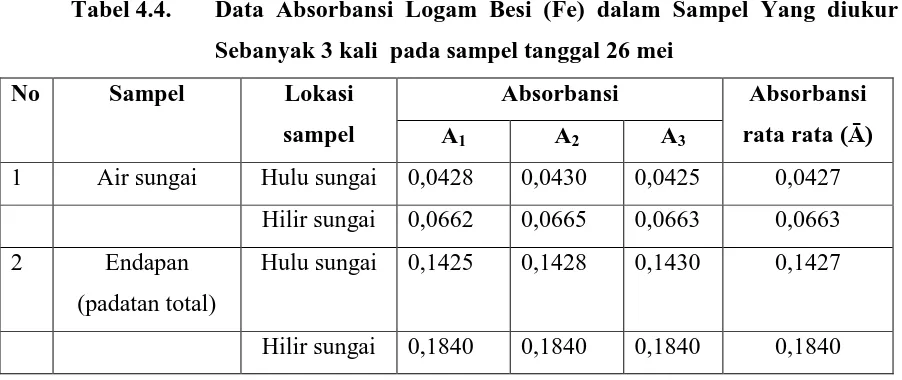
Tabel 4.4. Data Absorbansi Logam Besi (Fe) dalam Sampel Yang diukur Sebanyak 3 kali pada sampel tanggal 26 mei
No Sampel Lokasi sampel
Absorbansi Absorbansi rata rata (Ā) A1 A2 A3
1 Air sungai Hulu sungai 0,0428 0,0430 0,0425 0,0427
Hilir sungai 0,0662 0,0665 0,0663 0,0663
2 Endapan
(padatan total)
Hulu sungai 0,1425 0,1428 0,1430 0,1427
Hilir sungai 0,1840 0,1840 0,1840 0,1840
Konsentrasi logam Besi (Fe) dalam sampel dapat di ukur dengan mensubstitusikan
nilai Y (absorbansi) logam Besi (Fe) ke persamaan :
Tabel 4.5. Analisis data statistik penentuan konsentrasi Logam Besi (Fe) dari air hulu sungai lau borus.
No Xi (Xi-X)2
1 1,6930 2,6678x10-6
2 1,7029 1,3308x 10-4
3 1,6782 1,7336x 10-4
∑ 5,0741
N X = 1,6913 ∑ (Xi-X)2 = 3,0904x 10-4
�� =�∑ (Xi−X)
2
� −1
=�3,0904 �10
−4
2
= 0,015
Konsentrasi Logam Besi (Fe) dari hulu sungai lau Borus kecamatan naman teran
=� ±��
Tabel 4.6. Analisis data statistik penentuan konsentrasi Logam Besi (Fe) air dari hilir sungai lau borus.
No Xi (Xi-X)2
Konsentrasi Logam Besi (Fe) dari hilir sungai lau Borus kecamatan naman teran
=� ±��
= 2,8580 ± 0,0075 (mg/L)
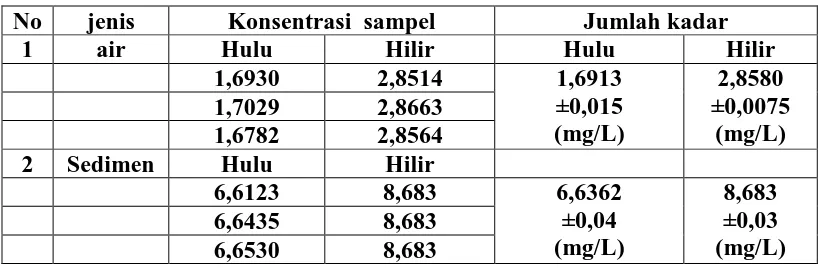
Tabel 4.7. hasil penentuan kadar logam Besi (Fe) dari air sungai Lau Borus No jenis Konsentrasi sampel Jumlah kadar
4.1.3. Logam Mangan (Mn)
Pada pengukuran Logam Mangan (Mn) dengan menggunakan alat Spektrofotometer Serapan Atom (SSA) komdisi alat dapat dilihat pada tabel 4.xx
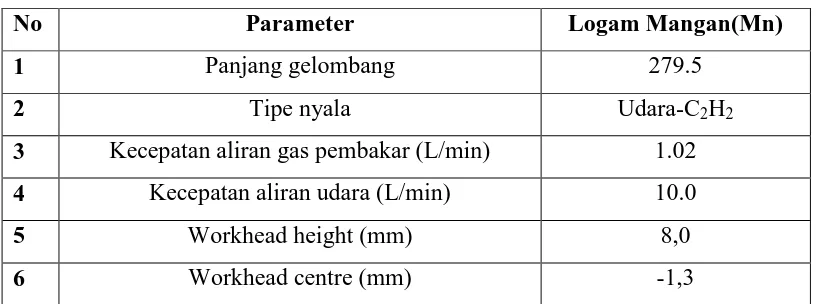
Tabel 4.8. Kondisi alat Atomic Absorbtion Spectrophotometer (AAS) merk GBC AVANTA VER. 2.02
No Parameter Logam Mangan(Mn)
1 Panjang gelombang 279.5
2 Tipe nyala Udara-C2H2
3 Kecepatan aliran gas pembakar (L/min) 1.02
4 Kecepatan aliran udara (L/min) 10.0
5 Workhead height (mm) 8,0
6 Workhead centre (mm) -1,3
Pembuatan kurva larutan standar Logam Mangan (Mn) dilakukan dengan
menyiapkan larutan standar dengan berbagai konsentrasi yaitu pada pengukuran
0,0000; 0,2000; 0,4000; 0,6000; 8000; 1,0000 dan 1,2000 mg/L, kemudian diukur
absorbansinya dengan alat SSA (kondisi alat pada lampiran 2). Data absorbansi untuk
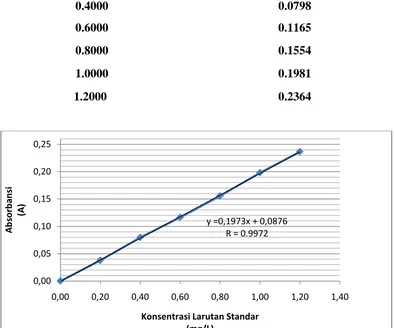
Tabel 4.9. Data absorbansi larutan standar Mangan (Mn)
Konsentrasi (mg/L) Absorbansi Rata – Rata (Ā)
0.0000 0.0002
Gambar 4.2. Kurva Larutan Standar logam Mangan (Mn)
4.1.4. Pengolahan Data Unsur Mangan (Mn)
4.1.4.1. Penurunan Persamaan Garis Regresi dengan Metode Least Square Hasil pengukuran absorbansi larutan seri standar Logam Mangan (Mn) pada Tabel
y =0,1973x + 0,0876
0,00 0,20 0,40 0,60 0,80 1,00 1,20 1,40
Persamaan garis regresi untuk kurva ini dapat diturunkan dengan metode Least
Square dengan data pada tabel 4.6
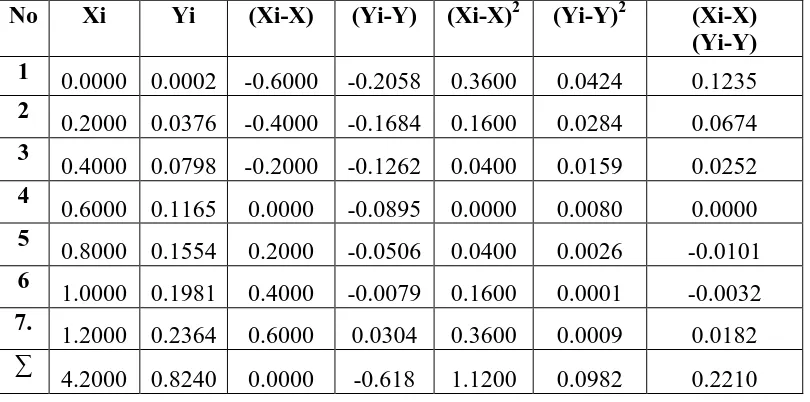
Tabel 4.10. Penurunan persamaan garis regresi untuk penentuan konsentrasi Logam Mangan (Mn) berdasarkan pengukuran absorbansi larutan standar Mangan (Mn)
Persamaan garis regresi untuk kurva dapat di turunkan dari persamaan garis :
�= ��+�
Dimana :
a = slope
b = intersept
Selanjutnya harga slope dapat ditentukan dengan menggunakan metode least square
sebagai berikut :
� = ∑(�� − �)(�� − �)
∑(�� − �)2
�= � − ��
Dengan mensubstitusikan harga – harga yang tercantum pada tabel 4.6. pada
persamaan di atas maka diperoleh :
� =0,2210
1,1200= 0,1973
b = 0,2060– (0,1973 x 0,6000)
= 0,2060−0,1184
= 0,0876
Maka persamaan garis yang diperoleh adalah :
�= 0,1973�+ 0,0876
4.1.4.2. Koefisien Korelasi
�= ∑(�� − �)(�� − �)
4.1.4.3. Penentuan Konsentrasi logam Mangan (Mn)
Untuk menghitung konsentrasi dari unsur Mangan (Mn), maka diambil data hasil
pengukuran absorbansi unsur Mangan (Mn) dalam air sumur bor. Data selengkapnya
pada tabel 4.7
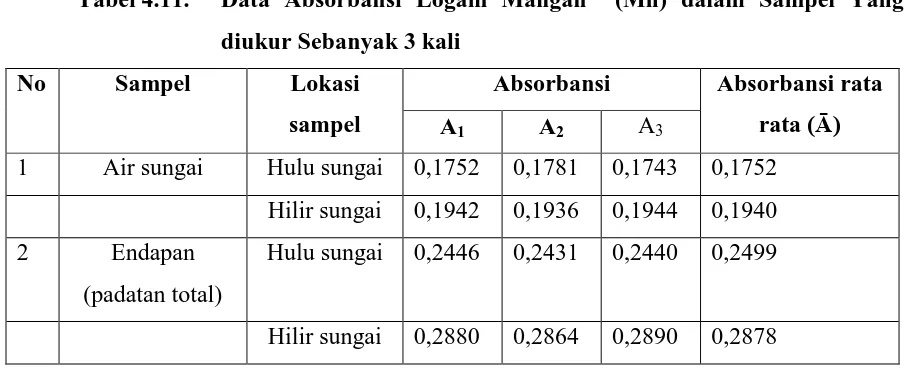
Tabel 4.11. Data Absorbansi Logam Mangan (Mn) dalam Sampel Yang diukur Sebanyak 3 kali
No Sampel Lokasi sampel
Absorbansi Absorbansi rata rata (Ā)
Konsentrasi unsur Mangan (Mn) dalam sampel dapat diukur dengan
Tabel 4.12. Analisis data statistik penentuan konsentrasi Logam Mangan (Mn) dari air hulu sungai lau borus.
No Xi (Xi-X)2
1 0,4446 2,77 x 10-8
2 0,4593 2,21x 10-4
3 0,4294 2,22x 10-4
∑ 1,3333
n X = 0,4444 ∑ (Xi-X)2 = 447x10-4
�� =�∑ (Xi−X)
2
� −1
=�447x10
−4
2
= 0,02
Konsentrasi Logam Besi (Fe) dari hulu sungai lau Borus kecamatan naman teran
=� ±��
= 0,4444 ± 0,02(mg/L)
Tabel 4.13. Analisis data statistik penentuan konsentrasi Logam Mangan (Mn) dari air hilir sungai lau borus.
No Xi (Xi-X)2
1 0,5411 5.37x 10-7
2 0,5380 5,6x 10-6
∑ 1,6211
Konsentrasi Logam Mangan (Mn) dari hulu sungai lau Borus kecamatan naman teran
=� ±��
= 0,5403 ± 0,0044 (mg/L)
Tabel 4.14 Hasil penentuan kadar logam Mangan (Mn) dari air sungai Lau Borus
No jenis Konsentrasi sampel Jumlah kadar
4.1.5. Logam Kadmium (Cd)
Pada pengukuran Logam Kadmium (Cd) dengan menggunakan alat Spektrofotometer
Serapan Atom (SSA) komdisi alat dapat dilihat pada tabel 4.1
Tabel 4.15. Kondisi alat Atomic Absorbtion Spectrophotometer (AAS) merk GBC AVANTA VER. 2.02
No Parameter Logam Kadmium (Cd)
1 Panjang gelombang 228.8
2 Tipe nyala Udara-C2H2
3 Kecepatan aliran gas pembakar (L/min) 1.10
4 Kecepatan aliran udara (L/min) 10.0
5 Workhead height (mm) 8,0
6 Workhead centre (mm) -1,3
Pembuatan kurva larutan standar Logam Kadmium (Cd) dilakukan dengan
menyiapkan larutan standar dengan berbagai konsentrasi yaitu pada pengukuran
0,0000; 0,0200; 0,0400; 0,0600; 0,0800 dan 0,1000 mg/L, kemudian diukur
absorbansinya dengan alat SSA. Data absorbansi untuk larutan standar Kadmium
(Cd) dapat dilihat pada tabel 4.13. di bawah ini.
Tabel 4.16. Data absorbansi larutan standar Kadmium (Cd)
Konsentrasi (mg/L) Absorbansi Rata – Rata (Ā)
0.0000 0.0003
0.0200 0.0134
0.0400 0.0324
0.0600 0.0480
0.0800 0.0650
Gambar 4.3. Kurva larutan standar Kadmium (Cd)
4.1.5. Pengolahan Data Logam Kadmium (Cd)
4.1.5.1. Penurunan Persamaan Garis Regresi dengan Metode Least Square Hasil pengukuran absorbansi larutan seri standar Logam Kadmium (Cd) pada Tabel
4.17. diplotkan terhadap konsentrasi sehingga diperoleh kurva berupa garis linier.
Persamaan garis regresi untuk kurva ini dapat diturunkan dengan metode Least
Square dengan data pada tabel 4.18.
y = 0.8157x - 0.0006
0,000 0,020 0,040 0,060 0,080 0,100 0,120
Tabel 4.17. Penurunan persamaan garis regresi untuk penentuan konsentrasi Logam (Cd) berdasarkan pengukuran absorbansi larutan standar Kadmium (Cd)
Persamaan garis regresi untuk kurva dapat di turunkan dari persamaan garis :
�= ��+�
Dimana :
a = slope
b = intersept
Selanjutnya harga slope dapat ditentukan dengan menggunakan metode least square
sebagai berikut :
� = ∑(�� − �)(�� − �)
∑(�� − �)2
Dengan mensubstitusikan harga – harga yang tercantum pada tabel 4.14. pada
persamaan di atas maka diperoleh :
� =5,71� 10
−3
0,007 = 0,8157
b = 0,0401 – (0,8157 x 0,05)
= 0,0401−0,0407
=−0,0006
Maka persamaan garis yang diperoleh adalah :
�= 0,8157� −0,0006
4.1.5.2. Koefisien Korelasi
Koefisien korelasi dapat ditentukan dengan menggunakan persamaan sebagai berikut
:
�= ∑(�� − �)(�� − �) [∑(�� − �)2 ∑(�� − �)2]½
�= 5,71�10
−3
[(0,007)(4,671�10−3)]½
�= 5,71�10
−3
[3,269�10−5]½
�= 5,71�10
−3
5,718�10−3
Untuk menghitung konsentrasi logam Kadmium (Cd), maka diambil data hasil
pengukuran absorbansi logam Kadmium (Cd) dalam air sungai dan sedimen (padatan
total) Data selengkapnya pada tabel 4.19
Tabel 4.18. Data Absorbansi Logam Kadmium (Cd) dalam Sampel Yang diukur Sebanyak 3 kali pada sampel tanggal 26 mei
No Sampel Lokasi sampel
Absorbansi Absorbansi rata rata (Ā) A1 A2 A3
1 Air sungai Hulu sungai 0,0121 0,0124 0,0125 0,0123
Hilir sungai 0,0135 0,0134 0,0136 0,0135
2 Endapan
(padatan total)
Hulu sungai 0,1425 0,1428 0,1430 0,1427
Hilir sungai 0,1522 0,1520 0,1523 0,0521
Konsentrasi Logam Kadmium (Cd) dalam sampel dapat di ukur dengan
mensubstitusikan nilai Y (absorbansi) Kadmium (Cd) ke persamaan :
Tabel 4.19. Analisis data statistik penentuan konsentrasi Logam Kadmium (Cd) dari air hulu sungai lau borus.
No Xi (Xi-X)2
1 0,0155 5,377x10-7
2 0,0159 5,60x 10-6
3 0,0160 2,667x 10-6
∑ 1,6211
n X = 0,5404 ∑ (Xi-X)2 = 8,80x 10-6
�� =�∑ (Xi−X)
2
� −1
=�8,80 �10
−6
2
= 0,004
Konsentrasi Logam Kadmium (Cd) dari hulu sungai lau Borus kecamatan naman teran =� ±��
Tabel 4.20. Analisis data statistik penentuan konsentrasi Logam Kadmium (Cd) dari air hilir sungai lau borus.
No Xi (Xi-X)2
1 0,0173 0
2 0,0172 1x 10-8
3 0,0174 1x 10-8
∑ 0,0519
n X = 0,0173 ∑ (Xi-X)2 = 2x 10-8
�� =�∑ (Xi−X)
2
� −1
=�2 �10
−8
2
= 0,0001
Konsentrasi Logam Kadmium (Cd) dari hulu sungai lau Borus kecamatan naman teran =� ±��
Tabel 4.21. Hasil penentuan kadar logam Kadmium (Cd) dari air sungai Lau Borus
No jenis Konsentrasi sampel Jumlah kadar
1 Air Hulu Hilir Hulu Hilir
0,0155 0,0173 0,0158 ±0,004 (mg/L)
0,0173 ±0,0001
(mg/L) 0,0159 0,0172
0,0160 0,0174 2 Sedimen Hulu Hilir
0,1754 0,1873 0,1756 ±0,005 (mg/L)
0,1872 ±0,0004
(mg/L) 0,1757 0,1870
Tabel 4.22. Hasil penentuan konsentrasi Logam Besi (Fe) , Mangan (Mn), dan Kadmium (Cd) dalam Sampel air
Jenis logam : titik lokasi Fe
Tabel 4.23. Hasil penentuan konsentrasi Logam Besi (Fe) , Mangan (Mn), dan Kadmium (Cd) dalam Sampel sedimen
Jenis logam : titik lokasi Fe
Tabel 4.24. Hasil penentuan konsentrasi Logam Besi (Fe) , Mangan (Mn), dan Kadmium (Cd) dalam Sampel total .
Jenis logam : titik lokasi Fe
4.2. Pembahasan.
Pencemaran air sungai khusus yang disebabkan oleh komponen – komponen
anorganik yang berasal dari Bencana alam (Natural Desaster) seperti gunung
meletus/erupsi dan kebanjiran diantaranya melepaskan berbagai logam berat
berbahaya.
Penentuan kadar logam Besi (Fe), Mangan (Mn), dan Kadmium (Cd) dalam air
sungai dan sedimen (Padatan Total) dari air sungai Lau Borus kecamatan Naman
teran aliran lahar dingin gunung sinabung. dilakukan dengan mengasamkan sampel
dengan HNO3 dan diukur pH. kemudian disaring dan dipisahkan antara sampel
terlarut yaitu filtrat dengan sampel tidak larut (padatan total) yaitu residu.kemudian
sampel di destruksi dengan HNO3(p). kemudian diukur nilai absorbansi dan
konsentrasi dari sampel tersebut menggunakan alat spektrofotometer serapan atom
pada panjang gelombang (λ) untuk Besi (Fe) λspesifik 248,3 nm, Mangan (Mn), λspesifik 279,5 nm dan Kadmium (Cd) λspesifik 228,8 nm.
Dari hasil penelitian diperoleh bahwa kadar logam Besi (Fe), Mangan (Mn) dan
Kadmium (Cd) pada Daerah Hilir sungai lebih tinggi dibandingkan dengan kadar
logam pada Daerah Hulu sungai yaitu kadar Logam besi (Fe) sebesar 1,6913 mg/L,
logam Mangan (Mn) sebesar 0,4444 mg/L, dan Kadmium sebesar 0,0158 mg/L untuk
air dan logam besi (Fe) sebesar 6,6362 mg/L, logam Mangan (Mn) sebesar 0,7933
mg/L, dan Kadmium sebesar 0,1756 mg/L untuk sampel sedimen.
Pada daerah hilir sungai memiliki kadar yang lebih tinggi dibandingkan dengan
kadar logam daerah hulu. Hal ini disebabkan oleh adanya pengaruh aliran air sungai
yang dapat membuat logam logam dari lahar dingin gunung sinabung melarut serta
tingginya debet air pada daerah hilir dapat mempercepat terjadinya pelarutan dalam
lahar dingin yang dibawa dari hulu atau sumber erupsi. Abu vulkanik yang di
yang dapat dilihat pula ialah daerah hulu yang merupakan titik yang lebih dekat
dengan sumber erupsi memiliki aliran yang lambat dan tidak terjadi pengenceran
serta teralirkan sehingga mineral mineral yang dikeluarkan dalam lahar dingin
tersebut tidak sampai masuk kedalam badan air secara maksimal sehingga dengan
adanya aliran arus sungai maka logam logam akan terakumulasi di daerah hilir
sungai.
Sementara untuk sedimen karena sulit untuk terlarut didalam air, pergerakan air
sangat mempengaruhi banyaknya jumlah logam didalam badan air. Disamping itu
sedimen mudah tersuspensi karena pergerakan massa air yang akan melarutkan
kembali logam yang terkandung di dalam air, sehingga sedimen menjadi sumber
pencemar potensial dalam skala waktu tertentu yang panjang.
Dari hasil penelitian tersebut dapat diketahui bahwa air sungai Lau Borus tersebut
sudah tercemar. Yaitu kadarnya telah melewati ambang batas normal berdasarkan PP
No 82 tahun 2001 untuk semua golongan air pada semua lokasi baik di hulu maupun
di hilir sungai tersebut dimana kadar logam yang di perbolehkan yaitu untuk logam
Besi (Fe) 0,3 mg/L, logam Mangan (Mn) 0,1 mg/L,dan Kadmium (Cd) 0,01 mg/L.
sementara untuk kadar logam yang ada dalam sedimen (padatan total) parameter baku mutu tidak secara khusus di terbitkan oleh instansi pemerintah, sehingga tidak
ada patokan secara khusus yang penulis dapatkan untuk membandingkan apakah
BAB 5
KESIMPULAN DAN SARAN
5.1. Kesimpulan
Dari penelitian dan analisis data yang telah dilakukan pada air sungai dan sedimen
(padatan total) sungai Lau Borus yang berasal dari aliran lahar dingin gunung
sinabung pasca erupsi diperoleh kadar logam Besi (Fe) 1,6913 mg/L, Mangan (Mn)
0,444 mg/L,dan Kadmium (Cd) 0,0158 mg/L untuk air pada daerah hulu sungai. dan
logam Besi (Fe) 2,8580 mg/L, Mangan (Mn) 0,5403 mg/L,dan Kadmium (Cd) 0,0173
mg/L untuk air pada daerah hilir sungai, kemudian kadar logam Besi (Fe) 6,6362
mg/L, Mangan (Mn) 0,7933 mg/L,dan Kadmium (Cd) 0,1756 mg/L untuk sedimen
pada daerah hulu sungai. dan logam Besi (Fe) 8,683 mg/L, Mangan (Mn) 1,062
mg/L,dan Kadmium (Cd) 0,1872 mg/L untuk sedimen pada daerah hilir sungai,
dimana pada konsentrasi Besi (Fe) Mangan (Mn) dan Kadmium (Cd) pada sampel air
di hulu maupun di hilir melewati ambang batas maksimal untuk kualitas air.
Berdasarkan Peraturan Pemerintah (PP) No 82 Tahun 2001. Sedangkan untuk sedimen (Padatan total) konsentrasi logam beratnya tidak memiliki ambang batas
yang di keluarkan oleh pemerintah atau standar nasional (SNI) sehingga tingkat
5.2. Saran
- Air sungai Lau Borus yang merupakan aliran lahar dingin Gunung sinabung
telah tercemar logam berat Besi (Fe), Mangan (Mn) dan Kadmium (Cd) yang
berada di atas ambang batas kualitas air berdasarkan Peraturan Pemerintah
(PP) No 82 Tahun 2001.
- Perlu dilakukan penelitian lebih lanjut terhadap kandungan logam berat lain
seperti Raksa (Hg), Arsen (As), Plumb (Pb) akibat debu erupsi gunung
sinabung pada beberapa sungai yang berada di kaki gunung sinabung.
- Perlu adanya Standart Nasional Indonesia (SNI) atau peraturan pemerintah
secara resmi untuk menentukan kadar logam dalam sedimen
-BAB 2
TINJAUAN PUSTAKA
2.1. Gunung Berapi.
Gunung berapi atau gunung api secara umum adalah istilah yang dapat di defenisikan
sebagai suatu sistem saluran fluida panas (batuan dalam wujud cair atau lava) yang
memanjang dari kedalaman sekitar 10 km dibawah permukaan bumi sampai
kepermukaan bumi, termasuk endapan hasil akumulasi material yang dikeluarkan
pada saat gunung meletus. Lebih lanjut, istilah gunung api ini juga dipakai untuk
menamai fenomena pembentukan. Ice volcanoes atau gunung api es dan mud
volcanoes atau gunung api lumpur. Gunung api es biasa terjadi di daerah yang
mempunyai musim dingin bersalju, sedangkan gunung api lumpur dapat kita lihat di
daerah kuwu, grobogan, Jawa Tengah yang populer sebagai bledug kuwu.
Gunung berapi terdapat di seluruh dunia, tetapi lokasi gunung berapi yang
paling dikenali adalah gunung berapi yang berada di sepanjang busur cincin api
pasifik (pacific ring of fire). Busur Cincin Api Pasifik merupakan garis bergesernya
antara dua lempengan tektonik. Gunung berapi terdapat dalam beberapa bentuk sepanjang masa hidupnya. Gunung berapi yang aktif mungkin berubah menjafi
separuh aktif, istirahat, sebelum akhirnya menjadi tidak aktif atau mati.
Bagaimanapun gunung berapi mampu istirahat dalam waktu 610 tahun sebelum
berubah menjadi aktif kembali. Oleh karena itu, sulit untuk menentukan keadaan
sebenarnya dari suatu gunung berapi itu. Apakah gunung berapi itu berada dalam
keadaan istirahat atau telah mati.
Apabila gunung berapi meletus, magma yang terkandung di dalam kamar
magma di bawah gunung berapi meletus keluar sebagai lahar atau lava. Selain
daripada aliran lava, kehancuran oleh gunung berapi disebabkan oleh berbagai cara
seperti berikut:
• Aliran lava
• Aliran lumpur
2.1.1 Klasifikasi Gunung Berapi di Indonesia
Kalanagan vulkanologi Indonesia mengelompokkan gunung merapi kedalam 3 tipe
berdasarkan catatan sejarah letusan erupsinya.
Gunung api tipe A
Gunung berapi yang tercatat pernah mengalami erupsi magnetic sekurang kurangnya
satu kali sesudah tahun 1600.
Gunung api tipe B
Gunung berapi yang sesudah tahun 1600 belum tercatat lagi mengadakan erupsi
magmatik namun masih memeperlihatkan gejala kegiatan vulkanik seperti kegiatan
sofatara.
Gunung api tipe C
Gunung berapi yang sejarah erupsinya tidak diketahui dalam catatan manusia, namun
masih terdapat tanda tanda kegiatan masa lampau berupa lapangan solfatara/fumarola
pada tingkat lemah. (Albert,2012).
2.2. Erupsi gunung Merapi
Pada tanggal 13 februari 2014, gunung kelud meletus. Gunung yang terletak di perbatasan antara kabupaten Kediri, kabupaten Blitar, dan kabupaten Malang telah
berstatus siaga sejak 2 februari 2014 dan ditingkatkan statusnya menjadi waspada 8
hari kemudian. Letusan yang sangat besar menimbulkan suara yang terdengar hingga
radius puluhan kilometer. Walaupun saat ini aktivitasnya cenderung turun, namun
Bencana yang sama sebelumnya juga terjadi di Gunung Sinabung pada 2013
lalu. Letusannya melepaskan awan panas dan abu vulkanik yang menjangkau
kawasan sibolangit dan berastagi. Guguran lava pijar dan semburan awan panas
masih terus dihasilkan sampai 3 januari 2014 dan hingga kini rentetan gempa,
letusan, dan luncuran awan panas masih terjadi secara terus menerus. Sampai saat ini,
letusan kecil masih terjadi di gunung sinabung mencapai kota Medan yang jaraknya
sekitar 30 km dari pusat letusan. Korban jiwa pun berjatuhan, terutama akibat terkena
sapuan awan panas, yang mencapai 17 orang. (Suryani,2014)
Debu vulkanik terdiri dari partikel-partikel batuan vulkanik terfragmentasi. Hal ini
terbentuk selama ledakan gunung berapi, dari longsoran panas batuan yang mengalir
menuruni sisi gunung berapi, atau dari merah-panas cair lava semprot. Debu
bervariasi dalam penampilan tergantung pada jenis gunung berapi dan bentuk letusan
(Wikipedia B,2010).
2.3. Tinjauan umum tentang Air. 2.3.1. Air
Air merupakan sumber daya alam yang diperlukan untuk hajat hidup orang banyak, bahkan oleh semua mahkluk hidup. Oleh karena itu, sumber daya air harus dilindungi
agar tetap dapat dimanfaatkan dengan baik oleh manusia serta makluk hidup yang
lain. Pemanfaatan air untuk berbagai kepentingan harus dilakukan secara bijaksana,
dengan memperhitungkan kepentingan generasi sekarang maupun generasi
mendatang. Saat ini, masalah utama yang dihadapi oleh sumber daya air meliputi
kuantitas air yang sudah tidak mampu memenuhi kebutuhan yang terus meningkat
dan kualitas air untuk keperluan domestik yang semakin menurun. Kegiatan industri,
domestik, dan kegiatan lain berdampak negatif terhadap sumber daya air, antara lain
Air merupakan senyawa yang paling melimpah di permukaan bumi. Sifat-sifat
dari air memiliki pengaruh yang berarti untuk penyediaan air, kualitas air dan teknik
pengolahan air (Montgomery, 1985).
Makhluk hidup yang ada di bumi ini tidak dapat terlepas dari kebutuhan akan
air. Air merupakan kebutuhan utama bagi proses kehidupan di bumi ini. Tidak akan
ada kehidupan seandainya di bumi ini tidak ada air. Air yang relatif bersih
didambakan oleh manusia, baik untuk keperluan hidup sehari – hari, untuk keperluan
industri, untuk keperluan sanitasi kota, maupun untuk keperluan pertanian, dan lain
sebagainya.
Dewasa ini air menjadi masalah yang perlu mendapat perhatian yang seksama
dan cermat. Untuk mendapatkan air yang baik, sesuai dengan standar tertentu, saat ini
menjadi barang yang mahal karena air sudah banyak tercemar oleh bermacam –
macam limbah dari hasil kegiatan manusia, baik limbah dari kegiatan rumah tangga,
limbah dari kegiatan industri dan kegiatan – kegiatan lainnya.
Untuk mendapatkan standar air yang bersih tidaklah mudah, karena
tergantung pada banyak faktor penentu. Faktor penentu tersebut adalah:
1) Kegunaan air:
a) Air untuk minum
b) Air untuk keperluan rumah tangga
c) Air untuk industri
d) Air untuk mengairi sawah
e) Air untuk kolam perikanan, dll.
2) Asal sumber air:
a) Air dari mata air di pegunungan
b) Air danau
c) Air sungai
Air yang ada di bumi ini tidak pernah terdapat dalam keadaan murni bersih,
tetapi selalu ada senyawa atau mineral (unsur) lain yang terlarut di dalamnya. Hal ini
tidak berarti bahwa semua air di bumi telah tercemar. Sebagai contoh, air yang di
ambil dari mata air di pegunungan dan air hujan. Keduanya dapat dianggap sebagai
yang bersih, namun senyawa atau mineral (unsur) yang terdapat didalamnya berlainan
(Wardhana, 2004).
2.3.2 Penggolongan Air
Peraturan Pemerintah No. 20 tahun 1990 mengelompokkan kualitas air menjadi
beberapa golongan menurut peruntukannya. Adapun penggolongan air menurut
peruntukannya adalah sebagai berikut :
1) Golongan A, yaitu air yang dapat digunakan sebagai air minum secara
langsung, tanpa pengolahan terlebih dahulu
2) Golongan B, yaitu air yang dapat digunakan sebagai air baku air minum
3) Golongan C, yaitu air yang dapat digunakan untuk keperluan perikanan dan
peternakan
4) Golongan D, yaitu air yang dapat digunakan untuk keperluan pertanian, usaha
di perkotaan, industri, dan pembangkit listrik tenaga air (Effendi, 2003).
2.3.3 Macam dan Sumber Air
Jika membicarakan tentang macam air yang dikaitkan dengan sumber atau
asalnya, maka air dapat dibedakan atas :
1) Air hujan, embun ataupun salju, yakni air yang didapat dari angkasa, karena
terjadinya proses presipitasi dari awan, atmosfir yang mengandung uap air
2) Air permukaan tanah, dapat berupa air tergenang atau air yang mengalir,
3) Air dalam tanah, yakni air permukaan tanah yang meresap ke dalam tanah,
jadi telah mengalami penyaringan oleh tanah ataupun batu-batuan. Air dalam
tanah ini sekali waktu juga akan menjadi air permukaan, yakni dengan
mengalirnya air tersebut menuju ke laut.
Ditinjau dari segi kesehatan, ketiga macam air ini tidaklah selalu memenuhi
syarat kesehatan, karena ketiga-tiganya mempunyai kemungkinan untuk dicemari.
Embun, air hujan atau salju misalnya, yang berasal dari angkasa, ketika turun ke bumi
dapat menyerap abu, gas ataupun materi-materi berbahaya lainnya. Demikian pula air
permukaan, karena dapat terkontaminasi dengan berbagai zat-zat berbahaya untuk
kesehatan. Air dalam tanah demikian pula halnya, karena sekalipun telah terjadi
proses penyaringan, namun tetap saja ada kemungkinan terkontaminasi dengan
zat-zat mineral ataupun kimia yang mungkin membahayakan kesehatan. Adapun
perbandingan antara ketiga macam air tersebut sebagai berikut:
Tabel 2.1 Perbandingan antara embun, air hujan, dan salju, air permukaan tanah, dan
air tanah dalam
Embun, air hujan dan
salju
Air permukaan tanah Air dalam tanah
Pada umumnya jika belum
terkontaminasi air bersifat
bersih, steril, murni, hanya
saja mudah merusak
dan zat kimia, kaya akan
O2, CO2 serta mengandung
bersih, bebas dari bakteri.
Hanya saja kemungkinan
mengandung zat mineral
cukup besar, karena itu
sering berwarna, berbau
dan mempunyai rasa
yang tidak nyaman
Air yang diperuntukkan bagi konsumsi manusia harus berasal dari sumber
yang bersih dan aman. Batasan – batasan sumber air yang bersih dan aman tersebut,
antara lain :
1) Bebas dari kontaminasi kuman atau bibit penyakit
2) Bebas dari substansi kimia yang berbahaya dan beracun
3) Tidak berasa dan berbau
4) Dapat dipergunakan untuk mencakupi kebutuhan domestik dan rumah tangga
5) Memenuhi standar minimal yang ditentukan oleh WHO atau Departemen
Kesehatan RI.
Air dikatakan tercemar bila mengandung bibit penyakit, parasit, bahan – bahan kimia
yang berbahaya, dan sampah atau limbah industri (Chandra, 2005).
2.4. Logam
Dalam kehidupan sehari – hari, kita tidak terpisah dari benda – benda yang bersifat
logam. Benda ini kita gunakan sebagai alat perlengkapan rumah tangga seperti
sendok, garpu, pisau dan lain – lain (logam biasa), sampai pada tingkat perhiasan
mewah yang tidak dapat dimiliki oleh semua orang seperti emas, perak, dan lain –
lain (logam mulia). Secara gamblang, dalam konotasi kesehatan kita beranggapan
bahwa logam diidentikkan dengan besi, padat, berat, keras dan sulit dibentuk.
Logam berat masih termasuk golongan logam dengan kriteria – kriteria yang
sama dengan logam – logam lain. Perbedaannya terletak dari pengaruh yang
dihasilkan bila logam berat ini berikatan dan atau masuk ke dalam tubuh organisme
hidup.
Sebagai contoh, bila unsur logam besi (Fe) masuk ke dalam tubuh, meski
dalam jumlah yang agak berlebihan, biasanya tidaklah menimbulkan pengaruh yang
tenbaga (Cu), bila masuk kedalam tubuh dalam jumlah berlebihan akan menimbulkan
pengaruh - pengaruh buruk terhadap fungsi fisiologis tubuh. Jika yang masuk ke
dalam tubuh organisme hidup adalah unsur logam beracun seperti hidragyrum (Hg)
atau disebut juga air raksa, maka dapat dipastikan bahwa organisme tersebut akan
langsung keracunan.
Berbeda dengan logam biasa, logam berat biasanya menimbulkan efek – efek
khusus pada makhluk hidup. Dapat dikatakan bahwa semua logam berat dapat
menjadi bahan beracun yang akan meracuni makhluk hidup. Sebagai contoh adalah
logam air raksa (Hg), kadmium (Cd), timah hitam (Pb), dan khrom (Cr). Namun
demikian, meski logam berat dapat mengakibatkan keracunan atas makhluk hidup,
sebagian dari logam – logam berat tersebut tetap dibutuhkan oleh makhluk hidup.
Kebutuhan tersebut berada dalam jumlah yang sangat sedikit. Tetapi bila
kebutuhan dalam jumlah yanga sangat kecil itu tidak terpenuhi, maka dapat berakibat
fatal terhadap kelangsungan hidup dari setiap makhluk hidup. Karena tingkat
kebutuhan sangat dipentingkan maka logam – logam tersebut juga dinamakan sebagai logam – logam atau mineral –mineral essensial tubuh.
Ternyata kemudian, bila jumlah dari logam – logam essesnsial ini masuk
kedalam tubuh dalam jumlah berlebihan, maka akan berubah fungsi menjadi zat
racun bagi tubuh. Contoh dari logam – logam berat essensial ini adalah tembaga (Cu),
seng (Zn), dan nikel (Ni) (Palar, 2004).
2.5. Pengaruh Logam Berat terhadap Kesehatan 2.5.1. Besi
Besi dibutuhkan oleh tubuh dalam pembentukan HB, banyaknya Fe dikendalikan
pada fase absorbsi. Fe2+ mempunyai fungsi esensial tubuh sebagai alat angkut
oksigen dari paru – paru ke seluruh tubuh , sebagai alat angkut e- dalam sel sebagai
jenis obat-obatan tertentu yang tidak larut dalam air (Widowati, 2008) , berperan
dalam katalis reaksi oksidasi dalam sistem biologi dan berperan dalam transport gas.
Apabila Fe berada dalam jumlah yang banyak akan muncul berbagai gangguan
lingkungan. Simpanan Fe tinggi bisa menyebakan kanker. Fe dalam dosis besar pada
manusia bersifat toksik karena fero bisa bereaksi dengan peroksida dan menghasilkan
radikal bebas. Fe bersifat toksik bila jumlah transferin melebihi kebutuhan sehingga
mengikat Fe bebas. Toksisitas kronis Fe bisa mengakibatkan gangguan fungsi hati,
gangguan fungsi endokrin dan penyakit kardiovaskular. Toksisitas kronis Fe pada
tingkat sel akan meningkatkan peroksidasi lipid sehingga merusak membrane sel,
mitokondria, mikrosom, dan organel sel lainnya.
Perlakuan toksisitas akut Fe per oral bisa mengakibatkan muntah, gangguan alat
pencernaan dan shock. Inhalasi debu Fe oksida bisa mengakibatkan deposisi Fe
dalam paru-paru yang berdasarkan hasil x-ray menunjukkan kemiripan dengan
silikosis. Beberapa hasil penelitian menunjukkan adanya keterkaitan antara Fe
berlebih yang bisa mengakibatkan diabetes, kanker, meningkatkan resiko infeksi,
reumatik, juga meningkatkan resiko terhadap penyakit jantung. Kadar Fe yang terlalu
tinggi bisa mengakibatkan kerusakan sel akibat radikal bebas. Pasien mengalami dialisis ginjal bila diberi Fe melalui injeksi yang akhirnya mengakibatkan stress.
Salah satu penyebab serangan jantung adalah tingginya kadar Fe dalam tubuh. Wanita
pre-menopause kurang beresiko terserang penyakit jantung karena mampu
mengurangi kelebihan Fe saat menstruasi, sementara itu waanita menopause lebih
beresiko terserang penyakit jantung koroner.
Dosis yang melebihi 20 mg/kg berat pada manusia menyebabkan toksisitas dengan
LD50 Fe 60 mg/kg. Konsumsi suplemen Fe melebihi 45mg/hari bisa menimbulkan
iritasi lambung, anak-anak dapat meninggal bila terpapar per oral sebesar 200mg
sampai 5,85gr Fe. Salah satu kekurangan tubuh manusia adalah tidak terdapatnya
mekanisme kontrol pembuangan Fe di dalam tubuh (Widowati, 2008).
Tubuh manusia tidak dapat mengeksresikan besi. Karenanya mereka yang
usus. Kematian sering disebabkan oleh rusaknya dinding usus ini. Debu Fe juga dapat
diakumulasikan didalam alveoli dan menyebabkan berkurangnya fungsi paru paru.
Pada umumnya besi yang larut dalam tanah sangat rendah dibandingkan
dengan kadar besi total. Namun pada tanah tergenang seperti sawah Fe3+ (feri)
direduksi menjadi Fe2+ (fero) sehingga besi yang larut meningkat. Kelarutan besi
yang tinggi dapat menimbulkan keracunan yang sering dialami oleh padi sawah dan
kedele yang ditanam setelah padi sawah di mana tanahnya masih terlalu basah.
Keracunan besi dapat menghambat berbagai kegiatan seperti respirasi,
fotosintesa,reduksi nitrat dan sintensisklorofil.
2.5.2. Mangan
Keracunan sering kali bersifat kronis sebagai akibat inhalasi debu dan uap logam ,
gejala yang timbul , berupa gejala susunan saraf : insomnia , lemah pada kaki dan otot
muka sehingga ekspresi muka menjadi beku dan muka tampak seperti topeng (mask)
bila pemaparan berlanjut maka bicaranya melambat dan monoton terjadi hiper
refleksi, clonus pada platela dan tumit dan berjalan seperti Parkinson, penggumpalan
darah, gangguan kulit, menurunkan kadar kolestrol, perubahan warna rambut, dan
kerusakan otak.
Logam Mn merupakan salah satu logam dengan jumlah sangat besar di dalam
tanah, dalam bentuk oksida maupun hidroksida. Senyawa Mn secara alami berbentuk
padat di lingkungan dan hanya sebagian kecil yang berada dalam air dan di udara
sebagai debu. Bila kadar Mn relatif tinggi dalam air maka kualitas air menurun
sehingga tidak layak digunakan baik untuk industri maupun keperluan rumah tangga.
Beberapa organisme seperti diatome, moluska, dan sepon mengakumulasikan
Mn. Ikan mampu mengakumulasikan hingga 5 ppm, hewan mamalia mampu
mengakumulasikan hingga 3 ppm dalam jaringan sehingga kadar normal dalam
jaringan adalah 1 ppm.
Syarat air minum kadar mangan diperbolehkan 0,1 ppm, sedangkan untuk air
bersih 0,5 ppm. Tanaman mahoni dan kembang sepatu mampu mengakumulasikan
logam berat Cu, Zn, Cd, Pb, dan Mn secara fisiologis unsur tersebut digunakan oleh
pembentukan organ tumbuhan. Kadar Mn yang tinggi dalam tanah bisa bersifat toksik
dan pH rendah pada tanah dapat menyebabkan defisiensi Mn pada tanaman.
Tingginya konsentrasi Mn pada tanah bisa mengakibatkan pembengkakan dinding
sel, mengeringkan daun, dan munculnya bercak coklat pada daun.
Paparan Mn dalam debu tidak boleh melebihi 5mg/m3, dalam waktu singkat
akan menimbulkan toksisitas seperti infeksi saluran pernafasan. Paparan Mn lewat
kulit bisa mengakibatkan tremor, kegagalan koordinasi, dan dapat mengakibatkan
munculnya tumor. Konsumsi Mn melebihi 11mg/hari menunjukkan gejala gangguan
sistem syaraf (Widowati, 2008)
2.5.3. Kadmium (Cd)
Kadmium (Cd) adalah logam berwarna putih perak, lunak, mengkilap, tidak larut
dalam basa. Cd memiliki nomor atom 40, berat atom 112,4 g/mol; titik leleh 321°C,
dan titik didih 767°C. Kadmium bersifat lentur, tahan terhadap tekanan. Keberadaan
kadmium (Cd) bisa mencemari lingkungan dan bisa berada di atmosfer, tanah, dan
perairan (Widowati, 2008).
Logam kadmium (Cd) sangat banyak digunakan dalam kehidupan sehari – hari manusia. Logam ini telah digunakan semenjak tahun 1950 dan total produksi
dunia adalah sekitar 15.000 – 18.000 per tahun. Prinsip dasar atau prinsip utama
dalam penggunaan kadmium adalah sebagai bahan ‘stabilitasi’ sebagai bahan
pewarna dalam industri plastik dan pada elektroplating. Namun sebagian dari
substansi logam kadmium ini juga digunakan untuk solder dan alloy – alloynya
digunakan pula untuk baterai (Palar, 2004).
Kadmium (Cd) dalam konsentrasi rendah banyak digunakan dalam industri
pada proses pengolahan roti, pengolahan ikan, pengolahan minuman, serta industri
Banyak logam baik bersifat toksik maupun esensial terlarut dalam air dan mencemari
air tawar maupun laut. Logam sendiri adalah senyawa anorganik di alam. Untuk
kepentingan biologi, logam dapat dibagi menjadi tiga kelompok:
a. Logam ringan, yang biasanya diangkut sebagai kation aktif di dalam larutan
encer.
b. Logam transisi, diperlukan dalam konsentrasi rendah, tetapi dapat menjadi
racun dalam konsentrasi tinggi.
c. Logam berat dan metalloid, umumnya tidak diperlukan dalam kegiatan
metabolisme dan bertindak sebagai racun bagi sel dalam konsentrasi yang
rendah.
Istilah logam berat sebetulnya telah dipergunakan secara luas terutama dalam
perpustakaan ilmiah, sebagai suatu istilah yang menggambarkan dari logam tertentu.
Berbeda dengan logam biasa, logam berat adalah istilah yang digunakan untuk
kelompok logam berat dan metalloid yang densitasnya lebih tinggi dari 5 g/cm3.
Logam berat dalam kadar tertentu merupakan unsur yang penting bagi tubuh. Jika
dikonsumsi oleh makhluk hidup diatas batas aman, maka logam berat akan menjadi
masalah bagi kesehatan.
Logam berat di perairan terdapat dalam bentuk terlarut dan tersuspensi.
Logam berat terletak di sudut kanan bawah dalam sistem periodik unsur, memiliki
afinitas yang tinggi terhadap unsur S dan biasanya bernomor atom 22 sampai 92 dari
periode keempat sampai dengan periode ketujuh. Biasanya mempunyai daya hantar
listrik yang tinggi dan merupakan bahan pencemar lingkungan yang tahan urai.
Unsur-unsur logam berat tersebut biasanya erat kaitannya dengan masalah
pencemaran dan toksisitas. Berdasarkan sifat fisika dan kimianya, tingkat atau daya
racun logam berat terhadap hewan dan air dapat di urutkan dari tinggi ke rendah
sebagai berikut: Hg, Cu, Cd, Zn, Sn, Al, Ni, Fe, Be, Mn, Li, Co, K, Ca, Sr, Mg, dan
Na (Santoso, 2012; Putra 2002).
Pencemaran yang disebabkan logam berat sangat perlu mendapat perhatian
karena adanya sifat-sifat logam berat yang tahan terhadap pelapukan. Selain itu,
dalam jangka waktu yang lama sebagai racun yang terakumulasi (Putra, 2002). Dalam
penelitian yang penulis laksanakan i ini logam yang diamati adalah Fe, Cu dan Ni.
Sehingga, perlu dibahas sifat sifat dan karakteristik logam-logam tersebut.
2.7. Proses Kontaminasi Logam Dalam Air.
Pencemaran logam berat merupakan permasalahan yang sangat serius untuk
ditangani, karena merugikan lingkungan dan ekosistem secara umum. Sejak kasus
merkuri di Minamata Jepang pada 1953, pencemaran logam berat semakin sering
terjadi dan semakin banyak dilaporkan. Agen Lingkungan Amerika Serikat (EPA)
melaporkan, terdapat 13 elemen logam berat yang diketahui berbahaya bagi
lingkungan. Diantaranya arsenik (As), timbal (Pb), merkuri (Hg), dan kadmium (Cd).
Logam berat yang masuk ke sistem perairan, baik di sungai maupun lautan
akan dipindahkan dari badan airnya melalui tiga proses yaitu pengendapan, adsorbsi,
dan absorbsi oleh organisme-organisme perairan (Bryan, 1976 dalam Purnomo,
2008). Pada saat buangan limbah industri masuk ke dalam suatu perairan maka akan
terjadi proses pengendapan dalam sedimen. Hal ini menyebabkan konsentrasi bahan
pencemar dalam sedimen meningkat. Logam berat yang masuk ke dalam lingkungan
perairan akan mengalami pengendapan, pengenceran dan dispersi, kemudian diserap oleh organisme yang hidup di perairan tersebut. Pengendapan logam berat di suatu
perairan terjadi karena adanya anion karbonat hidroksil dan klorida (Hutagalung,
1984 dalam Purnomo, 2008). Logam berat mempunyai sifat yang mudah mengikat
bahan organik dan mengendap di dasar perairan dan bersatu dengan sedimen
sehingga kadar logam berat dalam sedimen lebih tinggi dibanding dalam air
2.8. Spektrofotometri serapan atom
Peristiwa serapan atom pertama kali diamati oleh Fraunhofer, ketika menelaah garis –
garis hitam pada spektrum matahari. Sedangkan yang memanfaatkan prinsip serapan
atom pada bidang analisis adalah seorang Australia bernama Alan Walsh di tahun
1955. Sebelumnya ahli kimia banyak bergantung pada cara – cara spektrofotometrik
atau metode analisis spektrografik. Beberapa cara ini yang sulit dan memakan waktu,
kemudian segera digantikan dengan spektorskopi serapan atom atau Atomic
Absorption Spectroscopy (AAS) (Khopkar, 2008).
Spektrofotometri Serapan Atom adalah suatu metode pengukuran kuantitatif
suatu unsur yang terdapat dalam suatu cuplikan berdasarkan penyerapan cahaya pada
panjang gelombang tertentu oleh atom-atom fase gas dalam keadaan dasar.
Metode spektrofotometri serapan atom pertama kali dikembangkan oleh
Walsh, A., (1955) yang ditujukan untuk analisis logam renik dalam sampel yang
dianalisis. Sampai saat ini metode spektrofotometri serapan atom telah berkembang
dengan pesat dan hampir mencapai sejumlah 70 unsur yang dapat di tentukan dengan
metode ini (Mulja, 1995)
2.8.1 Prinsip Dasar Spektrofotometri Serapan Atom
Jika cahaya dengan panjang gelombang resonansi dilewatkan nyala dengan
mengandung atom-atom bersangkutan, maka sebagian cahaya itu akan diserap, dan
jauhnya penyerapan akan berbanding lurus denga banyaknya atom keadaan dasar
yang berada dalam nyala. Hal ini merupakan dasar penentuan kuantitatif
logam-logam dengan menggunakan SSA (Walsh, 1995)
Komponen penting yang membentuk spektrofotometer serapan atom diperlihatkan
1 2 3 4 5 6 7
.
Motor
Sumber bahan bakar oksigen
tenaga sampel
Gambar 2.2. Komponen-komponen spektrofotometer serapan atom (Underwood, 1988).
Keterangan :
1. Tabung Katoda Berongga
2. Pemotong Berputar
3. Nyala
4. Monokromator
5. Detektor
6. Penguat Arus
Sumber sinar yang lazim dipakai adalah lampu katoda berongga. Lampu ini terdiri
atas tabung kaca tertutup yang mengandung suatu katoda dan anoda. Katoda sendiri
berbentuk silinder berongga yang terbuat dari logam atau dilapisi dengan logam
tertentu. Tabung logam ini diisi dengan gas mulia (neon atau argon) dengan tekanan
rendah. Neon biasanya lebih disukai karena memberikan intensitas pancaran lampu
yang lebih rendah.
2. Tempat Sampel
Dalam analisis dengan spektrofotometri serapan atom, sampel yang akan dianalisis
harus diuraikan menjadi atom-atom netral yang masih dalam keadaan asas. Ada
berbagai macam alat yang dapat digunakan untuk mengubah suatu sampel menjadi
uap atom-atom yaitu dengan :
a. Nyala (flame)
Nyala digunakan untuk mengubah sampel yang berupa padatan atau cairan menjadi
bentuk uap atomnya, dan juga berfungsi untuk atomisasi. Suhu yang dapat dicapai
oleh nyala tergantung pada gas-gas yang digunakan, misalnya untuk gas
batubara-udara, suhunya kira-kira sebesar 1800OC; gas alam-udara 1700OC; gas asetilen-udara 2200OC dan gas asetilen-dinitrogen oksida (N2O) sebesar 3000OC (Rohman, 2007).
3. Monokromator
Monokromator memisahkan, mengisolasi dan mengontrol intensitas dari radiasi
energi yang mencapai detektor. Pada hakekatnya mungkin saja dapat dianggap
sebagai suatu saringan yang dapat disesuaikan dengan suatu daerah yang spesifik,
monokromator harus mampu memisahkan garis resonansi. Karena ada beberapa
unsur yang mudah dan ada beberapa unsur yang sulit (Haswell, 1991).
4. Detektor
Detektor pada spektrofotometer serapan atom berfungsi mengubah intensitas radiasi
yang datang menjadi arus listrik. Pada spektrofotometer serapan atom yang umum
dipakai sebagai detektor dalah tabung penggandaan foton (PMT = Photo Multi Tube
Detector) (Mulja, 1995).
5. Sistem Pencatat (Sistem Read-Out)
Sistem read-out yang digunakan pada instrumental spektrofotometer serapan atom
adalah untuk mengubah sinyal yang diterima menjadi sinyal digital, yaitu dalam
satuan absorbansi. Dengan pengubahan dalam bentuk digital beratri read-out
mencegah atau mengulangi kesalahn dalam pembacaan skala secara paralaks,
kesalahan interplasi di antara pembagian skala dan sebagainya serta menyeragamkan
tampilan datanya (yaitu dalam satuan absorbansi). Sistem read-out) untuk instrument
SSA sekarang ini dilengkapi dengan satuan mikroprosesor (komputer) sehingga memungkinkan pembacaan langsung konsentrasi analit di dalam sampel yang di
analisa (Haswell, 1991).
2.8.2.Nyala Pembakar
Sejauh susunan nyala itu dipentingkan, dapatlah dicatat bahwa suatu
campuran asetilena-udara sesuai untuk penetapan sekitar tiga puluh logam, tetapi
suatu nyala propilena-udara haruslah dipilih untuk logam yang mudah untuk diubah
menjadi keadaan uap atom. Untuk logam seperti Alumunium dan titanium yang
membentuk oksida tahan api, temperatur nyala asetilena-nitrogen oksida yang lebih
tinggi itu mutlak perlu dan nyala kepekaan bertambah bila nyala kaya akan asetilena.