PENEPUNGAN
I WAYAN KUKUH FERYANA
SEKOLAH PASCASARJANA INSTITUT PERTANIAN BOGOR
Dengan ini saya menyatakan bahwa tesis yang berjudul Karakterisasi dan Pemurnian Minyak Ikan Makerel (Scomber japonicus) Hasil Samping Penepungan adalah benar karya saya dengan arahan dari komisi pembimbing dan belum diajukan dalam bentuk apa pun kepada perguruan tinggi mana pun. Sumber informasi yang berasal atau kutipan dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir tesis ini.
Dengan ini saya melimpahkan hak cipta dari karya tulis saya kepada Institut Pertanian Bogor.
Bogor, September 2015
I Wayan Kukuh Feryana
Makerel (Scomber japonicus) Hasil Samping Penepungan. Dibimbing oleh SUGENG HERI SUSENO dan NURJANAH.
Ikan makerel (Scomber japonicus) merupakan sumber nutrisi potensial terutama omega-3. Pemanfaatan ikan makerel di Indonesia sebagai bahan baku ikan kaleng dan hasil sampingnya digunakan sebagai bahan baku produksi tepung ikan. Hasil samping proses penepungan diketahui mengandung nutrisi yang potensial yaitu minyak ikan. Penelitian ini bertujuan untuk meningkatkan kualitas minyak ikan dari hasil samping penepungan. Metode yang digunakan yaitu netralisasi alkali (NaOH) dengan 3 konsentrasi yang berbeda (19,70%; 17,87%; dan 16,09%) dan penambahan adsorben (kitosan dan atapulgit) dengan konsentrasi masing-masing yaitu 3%, 4% dan 5%. Ikan makerel mengandung lemak yang tinggi yaitu 9,23±0,32%; residu logam berat kadmium (Cd) sebesar 0,02±0,005 ppm; timbal (Pb) 0,65±0,093 ppm.
Hasil analisis menunjukkan bahwa minyak ikan makerel kasar tanpa perebusan memiliki nilai oksidasi lebih rendah dibandingkan dengan minyak ikan makerel kasar dengan perebusan dengan nilai peroksida (PV) 28,06±1,38 meq/kg; nilai anisidin (AnV) 19,19±1,36 meq/kg; bilangan asam (AV) 31,52±0,14 mg KOH/kg; persentase asam lemak bebas (FFA) 15,88±0,06%; total oksidasi (TOTOX) 75,31±2,06 meq/kg. Perlakuan konsentrasi NaOH terbaik adalah 17,87% (24oBe) dan menghasilkan nilai peroksida (PV) 5,60±0,42 meq/kg; nilai anisidin (AnV) 14,31±0,15 meq/kg; bilangan asam (AV) 4,30±0,49 mg KOH/kg; persentase asam lemak bebas (FFA) 2,16±0,25%; total oksidasi (TOTOX) 25,53±0,71 meq/kg.
Jenis dan konsentrasi adsorben terbaik untuk proses pemurnian adalah atapulgit 5% dan menghasilkan nilai peroksida (PV) 3,52±0,16 meq/kg; nilai anisidin (AnV) 5,36±1,86 meq/kg; bilangan asam (AV) 2,32±0,63 mg KOH/kg; persentase asam lemak bebas (FFA) 1,17±0,32%; total oksidasi (TOTOX) 12,4±0,32 meq/kg. Kandungan PUFA pada bahan baku penepungan adalah 17,21% (3,90% EPA: 9,91% DHA); kandungan PUFA pada minyak kasar tanpa perebusan adalah 29,74% (7,86% EPA :17,38% DHA); kandungan PUFA pada minyak kasar dengan perebusan adalah 29,33% (7,73% EPA:17,04% DHA); kandungan PUFA pada minyak ikan hasil netralisasi adalah 33,48% (8,86% EPA:20,33% DHA); kandungan PUFA pada minyak ikan hasil penambahan adsorbenadalah 33,79% (8,95% EPA : 20,31% DHA).
(Scomber japonicus) Fish Oil from Fishmeal Processing Byproduct. Supervised by SUGENG HERI SUSENO andNURJANAH.
Mackerel is a potential source of nutrition especially ω-3. Utilization of mackerel in Indonesia as canning raw material and it's byproduct used as material of fish meal production. The fishmeal byproduct known still contain potential nutrition such fish oil. This study aims were to improve quality of fish oil from fish meal processing byproduct. The method used were neutralization with three different NaOH concentration (19,70%; 17,87%; and 16,09%) and refining with two different adsorbent (attapulgite and chitosan) in three concentration (3%, 4% and 5%).
Mackerel contained high fat of 9.23±0.32%, residue of cadmium and lead were 0.02±0.005 ppm and 0.65±0.093 ppm. The oxidation values of fresh was lower compare to boiled crude fish oil with PV 28.06±1.38 meq/kg; AnV 19.19±1.36 meq/kg; AV 31.52±0.14 mg KOH/kg; FFA 15.88±0.06%; TOTOX 75.31 meq/kg. The best concentration of NaOH was 17.87% (24oBe) with PV 5.60±0.42 meq/kg; AnV 14.31±0.15 meq/kg; AV 4.30±0.49 mg KOH/kg; FFA 2.16±0.25%; TOTOX 25.53±0.71 meq/kg.
The concentration of choosen adsorbent were attapulgite 5% with PV 3.52±0.16 meq/kg; AnV 5.36±1.86 meq/kg; AV 2.32±0.63 mg KOH/kg; FFA 1.17±0.32%;TOTOX 12.4±0.32 meq/kg. PUFA recovered were 17.21% (3.90% EPA: 9.91% DHA) of raw material; 29.74% (7.86% EPA :17.38% DHA) of crude fish oil; 29.33% (7.73% EPA:17.04% DHA) of crude boiled fish oil; 33.48% (8.86% EPA:20.33% DHA) of neutralized fish oil; 33.79% (8.95% EPA : 20.31% DHA) of adsorbent refined fish oil. Thus the best purification were using NaOH 17.87% and attapulgite 5%.
© Hak Cipta Milik IPB, Tahun 2015
Hak Cipta Dilindungi Undang-Undang
Dilarang mengutip sebagian atau seluruh karya tulis ini tanpa mencantumkan atau menyebutkan sumbernya. Pengutipan hanya untuk kepentingan pendidikan, penelitian, penulisan karya ilmiah, penyusunan laporan, penulisan kritik, atau tinjauan suatu masalah; dan pengutipan tersebut tidak merugikan kepentingan IPB
PENEPUNGAN
I WAYAN KUKUH FERYANA
Tesis
sebagai salah satu syarat untuk memperoleh gelar Magister Sains
pada
Program Studi Teknologi Hasil Perairan
SEKOLAH PASCASARJANA INSTITUT PERTANIAN BOGOR
Judul : Karakterisasi dan Pemurnian Minyak Ikan Makerel (Scomber japonicus) Hasil Samping Penepungan
Nama : I Wayan Kukuh Feryana NRP : C351124031
Disetujui oleh
Komisi Pembimbing
Dr Sugeng Heri Suseno, SPi, MSi Prof Dr Ir Nurjanah, MS
Ketua Anggota
Diketahui Oleh
Ketua Program Studi
Teknologi Hasil Perairan Dekan Sekolah Pascasarjana
Dr Ir Wini Trilaksani, MSc Dr Ir Dahrul Syah, MScAgr
rahmat dan karuniaNya, sehingga penyusunan tesis ini dapat terselesaikan. Judul yang dipilih dalam penelitian ini adalah Karakterisasi dan Pemurnian Minyak Ikan Makerel (Scomber japonicus) Hasil Samping Penepungan.
Keberhasilan penulis mengikuti pendidikan di Sekolah Pascasarjana IPB tidak lepas dari dukungan berbagai pihak. Penulis menyampaikan banyak terimakasih yang setulusnya kepada:
1. Dr Sugeng Heri Suseno, SPi, MSi selaku ketua komisi pembimbing dan Prof Dr Ir Nurjanah, MS sebagai anggota komisi pembimbing atas kesediaan waktu untuk membimbing, memberikan arahan dan masukan selama penyusunan tesis ini.
2. Prof Dr Ir Joko Santoso, MSi selaku penguji luar komisi.
3. Dr Wini Trilaksani, MSc selaku ketua Program Studi Teknologi Hasil Perairan.
4. Keluarga besar penulis teruntuk Ayahanda I Wayan Tusta dan Ibunda Ni Luh Simpen serta adik adik tercinta Ni Kadek Fera Yunika Atmajayani, I Komang Tangguh Widyalaksana dan Ni Luh Putu Febri Satriani atas motivasi, doa, semangat dan dukungan baik moril maupun material selama penulis menempuh studi.
5. Pimpinan dan staf PT. Maya Food Industries yang telah berkenan memberikan bantuan sampel penelitian.
6. Teman-teman S2 THP 2011, 2012 dan 2013 atas kerjasama yang baik selama studi.
7. Semua pihak yang telah membantu tersusunnya tesis ini
Penulis menyadari bahwa tesis ini masih banyak kekurangan. Semoga karya ilmiah ini membawa manfaat bagi seluruh civitas IPB khususnya dan masyarakat Indonesia umumnya.
Bogor, September 2015
DAFTAR TABEL xii
DAFTAR GAMBAR xii
DAFTAR LAMPIRAN xii
1 PENDAHULUAN 1
Latar Belakang 1
Perumusan Masalah 3
Tujuan 3
Manfaat 3
Ruang Lingkup 3
Luaran 4
2 METODOLOGI PENELITIAN 5
Waktu dan Tempat 5
Bahan dan Alat 5
Prosedur 5
Analisis Data 9
3 HASIL DAN PEMBAHASAN 15
Karakteristik Bahan Baku 15
Residu Logam Berat Bahan Baku dan Minyak Ikan Makerel 16
Karakteristik Parameter Oksidasi 17
Profil Asam Lemak 24
4 SIMPULAN DAN SARAN 28
Simpulan 28
Saran 28
DAFTAR PUSTAKA 29
LAMPIRAN 35
1 Konsentrasi NaOH dengan berbagai derajat Baumé (Hodgum 1995) 6
2 Proporsi ikan makerel 15
3 Proksimat bahan baku penepungan ikan makerel 15 4 Residu logam berat bahan baku penepungan dan minyak ikan hasil
samping penepungan 16
5 Karakteristik parameter oksidasi minyak ikan makerel 17 6 Karakteristik parameter oksidasi minyak ikan makerel pada tiap
perlakuan konsentrasi NaOH 19
7 Profil asam lemak bahan baku penepungan dan minyak ikan makerel 25
DAFTAR GAMBAR
1 Diagram alir proses karakterisasi bahan baku dan minyak ikan makerel 6 2 Diagram alir proses netralisasi minyak ikan makerel hasil samping
penepungan 7
3 Struktur kimia atapulgit 7
4 Struktur kimia kitosan 8
5 Diagram alir proses pemurnian minyak ikan makerel hasil netralisasi
dengan penambahan adsorben 8
6 Reaksi safonifikasi (http//: asuhankakseto.blogspot.com) 19 7 Nilai peroksida minyak ikan makerel dengan jenis dan perlakuan
adsorben yang berbeda ( =atapulgit ; = kitosan; huruf superscript
menunjukkan nilai yang berbeda nyata) 21
8 Persentase asam lemak bebas minyak ikan makerel dengan jenis perlakuan adsorben yang berbeda ( =atapulgit ; = kitosan; huruf
superscript menunjukkan nilai yang berbeda nyata) 22 9 Bilangan asam minyak ikan makerel dengan jenis dan perlakuan
adsorben yang berbeda ( =atapulgit ; = kitosan; huruf superscript
menunjukkan nilai yang berbeda nyata 22
10 Nilai p-anisidin minyak ikan makerel dengan jenis dan perlakuan adsorben yang berbeda ( =atapulgit ; = kitosan; huruf superscript
menunjukkan nilai yang berbeda nyata) 23
11 Nilai total oksidasi minyak ikan makerel dengan jenis dan perlakuan adsorben yang berbeda ( =atapulgit; = kitosan; huruf superscript
2 Karakteristik atapulgit (NCBI 2015) 36
samping penepungan tanpa perebusan 37
6 Kromatogram Gas Chromatography minyak ikan makerel kasar hasil
samping penepungan dengan perebusan 38
7 Kromatogram Gas Chromatography minyak ikan makerel hasil
perlakuan netralisasi terbaik 38
11 ANOVA nilai anisidin minyak ikan makerel pada tiap perlakuan
konsentrasi NaOH 39
12 Uji lanjut (LSD) nilai anisidin minyak ikan makerel pada tiap
perlakuan konsentrasi NaOH 40
13 ANOVA bilangan asam minyak ikan makerel pada tiap perlakuan
konsentrasi NaOH 40
19 ANOVA rendemen minyak ikan makerel pada tiap perlakuan
konsentrasi NaOH 41
20 Uji lanjut (LSD) rendemen minyak ikan makerel pada tiap perlakuan
konsentrasi NaOH 41
21 ANOVA nilai peroksida minyak ikan makerel pada tiap perlakuan
jenis dan konsentrasi adsorben 41
22 Uji lanjut (LSD) nilai peroksida minyak ikan makerel pada tiap
perlakuan jenis dan konsentrasi adsorben 42
23 ANOVA nilai anisidin minyak ikan makerel pada tiap perlakuan
jenis dan konsentrasi adsorben 42
24 Uji lanjut (LSD) nilai anisidin minyak ikan makerel pada tiap
perlakuan jenis dan konsentrasi adsorben 43 27 ANOVA persentase asam lemak bebas minyak ikan makerel pada
tiap perlakuan jenis dan konsentrasi adsorben 43 28 Uji lanjut (LSD) persentase asam lemak bebas minyak ikan makerel
pada tiap perlakuan jenis dan konsentrasi adsorben 43 29 ANOVA total oksidasi minyak ikan makerel pada tiap perlakuan
jenis dan konsentrasi adsorben 43
30 Uji lanjut (LSD) total oksidasi minyak ikan makerel pada tiap perlakuan
jenis dan konsentrasi adsorben 44
1 PENDAHULUAN
Latar Belakang
Ikan makerel (Scomber japonicus) adalah jenis ikan pelagis yang termasuk dalam keluarga Scombridae yang merupakan perenang cepat dan predator. Ikan makerel merupakan salah satu ikan yang bernilai ekonomis tinggi. Produk olahan ikan makerel berupa fillet, ikan kaleng, ikan beku, ikan kering dan ikan asap. Pemanfaatan ikan makerel di Indonesia sebagai bahan baku ikan kaleng. Pengalengan ikan merupakan salah satu pengolahan ikan yang memiliki prospek usaha yang tinggi. Produksi olahan ikan kaleng Indonesia pada tahun 2014 tercatat 77.253 ton. Data impor ikan beku tahun 2014 yaitu 94.329 ton dengan nilai US$ 29,811 juta (KKP 2015).
Proses pengalengan ikan memanfaatkan bagian daging (chub) sebagai bahan baku utama, sedangkan bagian kepala, jeroan dan ekor dimanfaatkan sebagai bahan baku penepungan. Proses penepungan dilakukan dengan perebusan bahan baku kemudian dilakukan pengepresan. Proses tersebut menghasilkan produk utama berupa tepung ikan dan minyak yang bercampur air sebagai produk samping. Junker et al. (2006) menyatakan bahwa hasil samping pengolahan ikan masih banyak mengandung senyawa organik yang baik untuk kesehatan yaitu asam lemak ɷ-3. Penelitian produksi minyak ikan dari by-product hasil perikanan telah banyak dilakukan, antara lain ikan makerel (Fuadi et al. 2014), ikan patin (Arifianto et al. 2013), ikan lele (Kalalo et al. 2013), ikan sarden (Suseno et al.
2012), ikan walleye pollock (Wu et al. 2009), ikan herring (Aidos et al. 2002), dan ikan tuna (Chantachum et al. 2000). Permasalahan minyak dari hasil by-product tersebut yaitu kualitas yang rendah sehingga masih perlu usaha peningkatan mutu.
Proses penepungan melalui beberapa tahapan pengolahan, yaitu pengukusan, pengepresan, perebusan dan penyimpanan selama beberapa waktu sebelum dipasarkan. Proses ekstraksi dilakukan dengan steaming/pengukusan (wet rendering) dan pengepresan sehingga menghasilkan hasil berupa fraksi padat (tepung ikan) dan fraksi cair (campuran minyak dan air). Tepung ikan merupakan produk utama dari proses ekstraksi tersebut, sedangkan campuran minyak dan air merupakan hasil samping ekstraksi. Fraksi cair (minyak dan air) kemudian direbus dengan cara mengalirkan udara panas sehingga dapat menguapkan air pada minyak. Proses ekstraksi yang dilakukan saat penepungan menggunakan suhu yang tinggi sehingga mempengaruhi kualitas dari asam lemak yang terkandung.
dalam minyak kasar yaitu senyawa hidroperoksida, aldehid dan keton dapat berdampak buruk pada kesehatan manusia. Senyawa hasil oksidasi merupakan radikal bebas yang dapat menyebabkan penyakit degeneratif yaitu kanker dan penyakit jantung koroner (Sidhu et al 2003). Pemurnian minyak ikan dapat dilakukan dengan metode fisik ataupun kimia. Metode pemurnian secara kimia salah satunya dilakukan dengan proses netralisasi alkali sedangkan secara fisik dilakukan dengan penambahan adsorben.
Penggunaan agen netralisasi dikarenakan memiliki beberapa kelebihan, salah satunya mudah didapat dengan harga terjangkau. Metode ini mudah diaplikasikan secara massal untuk meningkatkan kualitas minyak ikan dengan mengurangi kandungan bahan pengotor (impurities) yang terkandung dalam minyak (Huang et al. 2010). Pemurnian minyak ikan dengan alkali yang telah dilakukan antara lain dengan NaOH (Huang et al. 2010; Pestana-Bauer et al.
2012; Estiasih et al. 2013), KOH (Haas et al. 2000). NaOH efektif sebagai alkali pilihan dalam pemurnian karena terbukti mampu menurunkan nilai asam lemak bebas (FFA) (Pestana-Bauer et al. 2012; Estiasih et al. 2013). Huang dan Sathivel (2010) melaporkan penurunan asam lemak bebas (FFA) sebesar 96,57% pada minyak ikan salmon dengan perlakuan NaOH.
Pemurnian minyak ikan dapat dilakukan secara fisika yaitu dengan perlakuan sentrifugasi dan penambahan adsorben. Adsorben merupakan zat padat yang dapat menyerap komponen tertentu dari suatu fase fluida (Singh et al. 2007). Adsorben secara umum merupakan bahan yang berpori dan memiliki daya serap tinggi. Mekanisme adsorpsi yang terjadi antara adsorben dengan senyawa oksidasi berupa ikatan kovalen pada sisi aktif adsorben dengan senyawa oksidasi, selain itu mekanisme adsorpsi juga dapat terjadi akibat pembentukan ikatan hidrogen antara gugus silanol (Si-OH) dengan senyawa hidrogen peroksida (Lewandowski et al.
2014). Senyawa oksidasi menempel pada permukaan adsorben dengan ikatan kovalen selain itu trigliserida dan asam oleat berikatan secara fisik dengan magnesium silika melalui ikatan hidrogen pada gugus karbonil dengan permukaan silanol (Si-OH). Asam oleat juga secara kimia diserap melalui ikatan ionik antara ion karboksilat (COO-) dan logam oksida (Yates et al. 1997; Suseno et al. 2014). Minyak ikan yang telah dicampurkan adsorben kemudian di sentrifugasi untuk memisahkan adsorben dengan minyak. Atapulgit merupakan salah satu jenis adsorben magnesium silika yang umum dimanfaatkan sebagai bahan baku obat diare. Atapulgit layak digunakan sebagai bahan pemurnian minyak karena nilai ekonomis yang rendah dan mudah diperoleh. Jenis adsorben lain yang banyak tersedia yaitu kitosan. Kitosan merupakan jenis adsorben alami yang diperoleh melalui ekstraksi kitin (karapas crustacean). Penggunaan kitosan sebagai adsorben dilakukan sebagai usaha penerapan zerowaste system pada pengolahan produk perikanan.
Adsorben yang ditambahkan dalam minyak dapat menghilangkan senyawa oksidasi, pigmen, residu logam berat, dan mencerahkan warna (Suseno et al.
aktif) pada pemurnian minyak ikan salmon. Attapulgit merupakan jenis adsorben sintetik yang efektif menurunkan 85% nilai peroksida dan 56,08% nilai p-anisidin (Tambunan et al. 2014).
Perumusan Masalah
Minyak ikan makerel hasil samping penepungan memiliki kualitas buruk berupa kandungan bahan pengotor dan nilai oksidasi yang tinggi, sehingga tidak layak untuk dikonsumsi manusia. Minyak ikan makerel mengandung asam lemak tidak jenuh (PUFA) yang tinggi sehingga perlu dilakukan usaha untuk peningkatan kualitas. Solusi yang diperlukan yaitu metode pemurnian yang tepat untuk menghasilkan minyak dengan kualitas yang baik dan memiliki nilai ekonomis. NaOH digunakan sebagai agen netralisasi pemurnian minyak karena efektif menghilangkan impurities dan dapat diaplikasikan secara massal. Adsorben kitosan dan atapulgit digunakan untuk memurnikan minyak ikan karena dapat menghilangkan senyawa oksidasi serta bau (odor) pada minyak ikan makerel.
Tujuan
Tujuan penelitian ini adalah untuk mendapatkan karakteristik bahan baku penepungan dan minyak ikan makerel kasar hasil samping penepungan, serta untuk menentukan metode pemurnian minyak ikan dengan proses netralisasi dan penambahan adsorben terbaik sehingga diperoleh minyak ikan dengan kualitas sesuai IFOS.
Manfaat
Manfaat dari penelitian ini yaitu mendapatkan teknologi untuk pemurnian minyak ikan hasil samping penepungan sehingga dapat meningkatkan kualitas minyak hasil samping penepungan sehingga dimanfaatkan sebagai sumber omega-3.
Ruang Lingkup
Luaran
2 METODOLOGI PENELITIAN
Waktu dan Tempat
Penelitian ini dilaksanakan pada bulan Juli sampai Desember 2014. Tempat yang digunakan dalam penelitian ini adalah Laboratorium Bahan Baku Hasil Perairan, Departemen Teknologi Hasil Perairan; Laboratorium Terpadu Fakultas Peternakan; Laboratorium Pusat Rekayasa Pangan Pusat Antar Universitas Institut Pertanian Bogor dan Laboratorium Kimia Terpadu Sekolah Pascasarjana Institut Pertanian Bogor.
Bahan dan Alat
Bahan-bahan yang digunakan dalam penelitian ini adalah ikan makerel bahan baku penepungan, minyak hasil samping penepungan makerel dari PT Maya Food Industries, Pekalongan, larutan standar pengujian parameter oksidasi asam lemak seperti kloroform, asam asetat, KI jenuh, ethanol, trimetylpenthane, natrium thiosulfat, KOH, air, p-anisidine, indikator PP.
Alat-alat yang digunakan adalah jerigen, gelas ukur, beaker glass, erlenmeyer, labu takar, tabung reaksi, pipet, timbangan analitik, thermometer, penangas, panci, stopwatch, perangkat titrasi (buret dan statif), spektrofotometer merk Agilent 8453 dan alat-alat yang digunakan untuk analisis proksimat antara lain oven, kjeldahl sistem, soxlet, alat titrasi, cawan porselen, gegep, tanur, destilator. Alat-alat yang digunakan untuk analisis logam berat antara lain alat destruksi, labu destruksi, Atomic Absorption Spectrophotometer (AAS) merk Aanalyst 100 Perkin Elmer HGA 850, Massachusetts USA dan perangkat kromatografi gas (gas chromatography) Shimadzu GC 2010 Plus, Kyoto Japan untuk pengujian profil asam lemak.
Prosedur
Bahan baku penepungan dan minyak kasar hasil samping penepungan diperoleh dari PT. Maya Food Industries, Pekalongan, Jawa Tengah. Proses pengumpulan sampel dilakukan segera setelah proses penepungan selesai. Bahan baku penepungan yang digunakan sebagai bahan uji adalah ikan makerel utuh beku. Sampel minyak yang telah dikoleksi ditampung dengan jerigen kemudian diletakan dalam kardus dan dibawa ke laboratorium. Sampel disaring untuk memisahkan bahan pengotor berupa sisa penepungan yang masih tertinggal dalam minyak dan disimpan dalam freezer dengan suhu -10 °C.
dianalisis proksimat, residu logam berat dan profil asam lemak. Minyak ikan pada setiap tahapan dianalisis kualitasnya yang meliputi parameter oksidasi, residu logam berat dan profil asam lemak.
Prosedur tahap karakterisasi bahan baku dan minyak ikan makerel hasil samping penepungan sebelum dan setelah perebusan. Analisis yang dilakukan yaitu analisis proksimat, analisis logam berat, profil asam lemak dan analisis parameter oksidasi yang meliputi nilai peroksida (PV), nilai p-anisidin (AnV), bilangan asam (AV), persentase asam lemak bebas (FFA), dan nilai total oksidasi (TOTOX). Diagram alir proses penelitian dapat dilihat pada Gambar 1.
Gambar 1 Diagram alir proses karakterisasi bahan baku dan minyak ikan makerel
Proses netralisasi minyak ikan makerel dilakukan menggunakan larutan NaOH. Minyak terpilih pada tahap pertama yaitu minyak ikan kasar segar dinetralisasi dengan larutan NaOH dengan derajat Baume (konsentrasi NaOH) yang berbeda. Kebutuhan larutan NaOH dihitung berdasarkan konsentrasi NaOH dilihat pada Tabel 1.
Tabel 1 Konsentrasi NaOH dengan berbagai derajat Baumé (Hodgum 1995) Derajat Boume pada suhu 15oC Konsentrasi larutan NaOH (%)
16 11,06
Analisis Logam Berat, Parameter Oksidasi, dan Profil Asam Lemak Ekstraksi wet
rendering
Kebutuhan jumlah NaOH dihitung dengan rumus berikut :
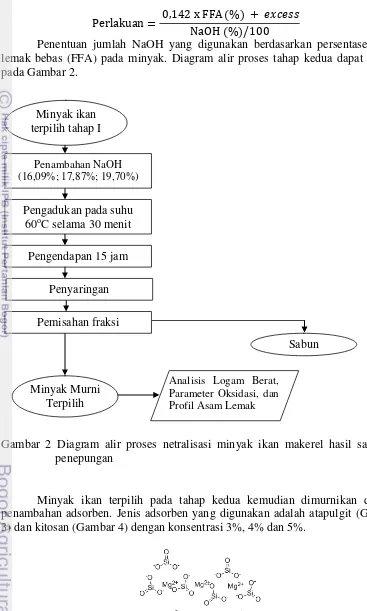
Perlakuan = 0,142 x FFA (%) + ���� NaOH (%)/100
Penentuan jumlah NaOH yang digunakan berdasarkan persentase asam lemak bebas (FFA) pada minyak. Diagram alir proses tahap kedua dapat dilihat pada Gambar 2.
Gambar 2 Diagram alir proses netralisasi minyak ikan makerel hasil samping penepungan
Minyak ikan terpilih pada tahap kedua kemudian dimurnikan dengan penambahan adsorben. Jenis adsorben yang digunakan adalah atapulgit (Gambar 3) dan kitosan (Gambar 4) dengan konsentrasi 3%, 4% dan 5%.
Gambar 3 Struktur kimia atapulgit Minyak ikan
terpilih tahap I
Pengendapan 15 jam Pengadukan pada suhu
60oC selama 30 menit
Analisis Logam Berat, Parameter Oksidasi, dan Profil Asam Lemak Minyak Murni
Terpilih
Penambahan NaOH (16,09%; 17,87%; 19,70%)
Sabun Pemisahan fraksi
Gambar 4 Struktur kimia kitosan
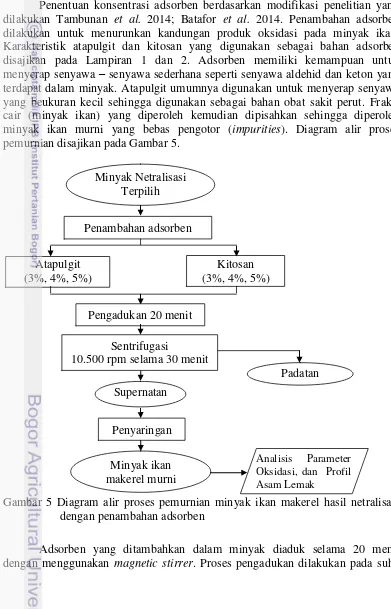
Penentuan konsentrasi adsorben berdasarkan modifikasi penelitian yang dilakukan Tambunan et al. 2014; Batafor et al. 2014. Penambahan adsorben dilakukan untuk menurunkan kandungan produk oksidasi pada minyak ikan. Karakteristik atapulgit dan kitosan yang digunakan sebagai bahan adsorben disajikan pada Lampiran 1 dan 2. Adsorben memiliki kemampuan untuk menyerap senyawa – senyawa sederhana seperti senyawa aldehid dan keton yang terdapat dalam minyak. Atapulgit umumnya digunakan untuk menyerap senyawa yang beukuran kecil sehingga digunakan sebagai bahan obat sakit perut. Fraksi cair (minyak ikan) yang diperoleh kemudian dipisahkan sehingga diperoleh minyak ikan murni yang bebas pengotor (impurities). Diagram alir proses pemurniandisajikan pada Gambar 5.
Gambar 5 Diagram alir proses pemurnian minyak ikan makerel hasil netralisasi dengan penambahan adsorben
Adsorben yang ditambahkan dalam minyak diaduk selama 20 menit dengan menggunakan magnetic stirrer. Proses pengadukan dilakukan pada suhu
Supernatan Atapulgit
(3%, 4%, 5%)
Sentrifugasi
10.500 rpm selama 30 menit
Penyaringan
Minyak ikan makerel murni
Analisis Parameter Oksidasi, dan Profil Asam Lemak
Padatan Minyak Netralisasi
Terpilih
Kitosan (3%, 4%, 5%) Penambahan adsorben
ruang menyebabkan terjadinya ikatan fisik antara adsorben dengan adsorbat (pengotor). Adsorpsi dengan ikatan fisik terjadi akibat gaya van der waals antara molekul adsorben dengan molekul pengotor. Karakteristik proses adsorpsi secara fisik terjadi pada suhu dibawah 100 ºC. Ikatan yang terbentuk antara adsorben dan adsorbat tidak terlalu kuat dan ikatan fisik yang terbentuk bersifat reversible
(Patterson 2009; Suseno et al. 2014).
Analisis Data
Penelitian ini menggunakan analisis Rancangan Acak Lengkap (RAL) dengan perlakuan diulang sebanyak 3 kali dan jika berpengaruh nyata maka diuji lanjut menggunakan uji Duncan (Steel dan Torrie 1993). Analisis data dilakukan pada tahapan penelitian kedua dan ketiga. Pada penelitian tahap kedua dilakukan analisis ragam dengan faktor konsentrasi NaOH yaitu 16,09%; 17,87%; 19,70%). Pada tahapan penelitian ketiga dilakukan analisis ragam untuk 2 jenis adsorben yaitu kitosan dan atapulgit dengan taraf konsentrasi adsoben yaitu 3%, 4% dan 5%.
Analisis proksimat
Analisis proksimat merupakan suatu analisis yang dilakukan untuk memprediksi komposisi kimia suatu bahan, termasuk di dalamnya analisis kadar air, abu, lemak dan protein.
Kadar air (AOAC 2005)
Tahap pertama yang dilakukan untuk menganalisis kadar air adalah mengeringkan cawan porselen dalam oven pada suhu 105 oC selama 1 jam. Cawan tersebut diletakkan ke dalam desikator (kurang lebih 15 menit) dan dibiarkan sampai dingin kemudian ditimbang. Cawan tersebut ditimbang kembali hingga beratnya konstan, sebanyak 5 g contoh dimasukkan ke dalam cawan tersebut, kemudian dikeringkan dengan oven pada suhu 105 oC selama 5 jam atau hingga beratnya konstan. Setelah selesai proses pengeringan kemudian cawan tersebut dimasukkan ke dalam desikator dan dibiarkan sampai dingin dan selanjutnya ditimbang kembali.
Perhitungan kadar air :
Kadar air % = B−C
B−A× 100%
Keterangan : A = Berat cawan kosong (g)
B = Berat cawan yang diisi dengan sampel (g)
C = Berat cawan dengan sampel yang sudah dikeringkan (g)
Kadar abu (AOAC 2005)
Perhitungan kadar abu:
Kadar abu % = C−A
B−A× 100%
Keterangan : A = Berat cawan porselen kosong (gram) B = Berat cawan dengan sampel (gram)
C = Berat cawan dengan sampel setelah dikeringkan (gram)
Kadar protein (AOAC 2005)
Tahapan yang dilakukan dalam analisis protein terdiri atas tiga tahap yaitu destruksi, destilasi, dan titrasi. Pengukuran kadar protein dilakukan dengan metode mikro Kjeldahl. Sampel ditimbang sebanyak 0,25 g, kemudian dimasukkan ke dalam labu Kjeldahl 100 mL, lalu ditambahkan 0,25 g selenium dan 3 mL H2SO4 pekat. Contoh didestruksi pada suhu 410oC selama kurang lebih 1 jam sampai larutan jernih lalu didinginkan. Setelah dingin, ke dalam labu Kjeldahl ditambahkan 50 mL akuades dan 20 mL NaOH 40%, kemudian dilakukan proses destilasi dengan suhu destilator 100 oC. Hasil destilasi ditampung dalam labu Erlenmeyer 125 mL yang berisi campuran 10 mL asam borat (H3BO3) 2% dan 2 tetes indikator bromcresol green-methyl red yang berwarna merah muda. Setelah volume destilat mencapai 40 mL dan berwarna hijau kebiruan, maka proses destilasi dihentikan. Destilat dititrasi dengan HCl 0,1 N sampai terjadi perubahan warna merah muda. Volume titran dibaca dan dicatat. Larutan blanko dianalisis seperti contoh.
Kadar protein dihitung dengan rumus sebagai berikut :
N % = mL HCl−mL blanko × N HCl × 14,007
berat sampel × faktor koreksi alat × 100%
Ket : *) Faktor koreksi alat = 2,5
% Kadar protein = % N x faktor konversi * *) Faktor konversi = 6,25
Kadar Karbohidrat (AOAC 2005)
Analisis karbohidrat dilakukan secara by difference, yaitu hasil pengurangan dari 100 % dengan kadar air, kadar abu, kadar protein dan kadar lemak, sehingga kadar karbohidrat tergantung pada faktor pengurangannya. Hal ini karena karbohidrat sangat berpengaruh terhadap zat gizi lainnya.
Analisis kadar karbohidrat dapat dihitung dengan persamaan berikut:
Karbohidrat (%) = 100% - (kadar air + kadar abu + kadar lemak + kadar protein)
Kadar lemak (AOAC 2005)
dalam selongsong lemak, kemudian sampel yang telah dibungkus dimasukkan ke dalam labu lemak yang sudah ditimbang berat tetapnya (W2) dan disambungkan dengan tabung soklet. Selongsong lemak dimasukkan ke dalam ruang ekstraktor tabung soxhlet dan disiram dengan pelarut lemak (n-heksana), kemudian dilakukan refluks selama 6 jam. Pelarut lemak yang ada dalam labu lemak didestilasi hingga semua pelarut lemak menguap. Pada saat destilasi pelarut akan tertampung di ruang ekstraktor, pelarut dikeluarkan sehingga tidak kembali ke
dalam labu lemak, selanjutnya labu lemak dikeringkan dalam oven pada suhu 105 oC, setelah itu labu didinginkan dalam desikator sampai beratnya konstan (W3).
Perhitungan kadar lemak :
Kadar lemak % =W3−W2
W3 × 100%
Keterangan : W1= Berat sampel (gram)
W2= Berat labu lemak kosong (gram) W3= Berat labu lemak dengan lemak (gram)
Analisis logam berat Cd, Pb, Hg, Ni dan As (BSN 2009)
Analisis dilakukan menggunakan 1 gram contoh, kemudian dimasukkan ke dalam labu destruksi 100 mL, dengan ditambahkan 15 mL HNO3 pekat dan 5 mL HClO4, kemudian didiamkan 24 jam. Sampel didestruksi hingga jernih, didinginkan, dan ditambahkan 10-20 mL air bebas ion, dilakukan pemanasan ±10 menit, diangkat, dan didinginkan. Larutan tersebut dipindahkan ke dalam labu takar 100 mL (labu dekstruksi dibilas dengan air bebas ion dan dimasukkan ke dalam labu takar). Larutan ditambahkan air sampai batas tanda tera. Kemudian dikocok dan disaring dengan kertas saring Whatman no.4. Sampel dipreparasi dan dianalisis sesuai dengan pengujian logam berat (Cd, Pb, Hg, Ni, As) pada analisis air (APHA 3110 untuk logam Cd, Pb, dan Ni; metode 3114 untuk As; dan metode 3112 untuk Hg). Filtrat dianalisis menggunakan Atomic Absorption Spectrophotometer (AAS).
Analisis residu logam dapat dihitung dengan persamaan berikut:
Residu logam ppm = konsentrasi kurva standar µg/mL × V pelarutan berat sampel
Analisis Bilangan Peroksida/Peroxide Value (PV) (AOAC 2005)
Metode penentuan bilangan peroksida menggunakan prinsip titrasi iodin yang dilepaskan dari senyawa kalium iodida oleh peroksida dengan menggunakan standar larutan thiosulfat sebagai titran dan larutan pati sebagai indikator. Metode ini mendeteksi semua zat yang mengoksidasi kalium iodida dalam kondisi asam.
ditambahkan 30 mL aquades. Selanjutnya dilakukan titrasi larutan dengan 0,01 N natrium tiosulfat(Na2S2O3) hingga larutan berubah warna menjadi kuning, setelah itu ditambahkan 0,5 mL larutan indikator kanji 1% yang akan mengubah warna larutan menjadi biru, titrasi kemudian dilanjutkan bersamaan dengan terus mengocok larutan hingga berubah warna menjadi biru muda yang menandakan pelepasan iodin dari lapisan kloroform, dilanjutkan titrasi dengan hati-hati hingga warna biru pada larutan hilang.
Perhitungan nilai peroksida dilakukan dengan persamaan berikut:
Nilai Peroksida (PV) = S × M × 1000 berat sampel (g)
S = Jumlah natrium tiosulfat (mL) M = Konsentrasi natrium tiosulfat (0,01)
Analisis Nilai p-anisidin/Anisidine Value (AnV) (Watson 1994)
Penentuan nilai p-anisidin dilakukan dengan membandingkan nilai absorbansi dua larutan uji. Larutan uji 1 dibuat dengan cara melarutkan 0,5 g sampel kedalam 25 mL trimethylpentane. Larutan uji 1 diukur nilai absorbansinya pada panjang gelombang 350 nm dengan menggunakan trimethylpentane sebagai larutan kompensasi. Larutan uji 2 dibuat dengan cara menambahkan 1 mL larutan
p-anisidine (2,5 g/L) kedalam 5 mL larutan uji 1, kemudian dikocok dan dihindarkan dari cahaya. Larutan referensi uji 2 dibuat dengan cara menambahkan 1 mL larutan p-anisidine (2,5 g/L) ke dalam 5 mL larutan trimethylpentane, kemudian dikocok dan dihindarkan dari cahaya. Pengujian absorbansi larutan uji 2 dilakukan pada panjang gelombang 350 nm tepat 10 menit setelah larutan disiapkan.
Nilai anisidine ditetapkan dengan persamaan berikut:
Nilai anisidin (AnV) =25 × (1,2 A2−A1) m
A1 = Absorbansi larutan uji 1 A2 = Absorbansi larutan uji 2
m = Massa sampel yang digunakan pada larutan uji 1
Analisis Asam Lemak Bebas/ Free Fatty Acid (FFA) (AOAC 1995)
Persentase FFA dihitung berdasarkan persamaan berikut:
FFA (%) =A x N x M 10G
A = Jumlah titrasi KOH (mL) N = Normalitas KOH
G = Berat sampel
M = Bobot molekul asam lemak dominan (282,5)
Analisis bilangan asam/acid value (AV) (Wrolstad et al. 2005)
Penentuan bilangan asam dilakukan dengan cara titrasi KOH terhadap sampel, yang menggunakan prinsip jumlah KOH yang diperlukan (mg) untuk menetralkan 1 g lemak. berikut persamaan untuk mendapatkan derajat kejernihan (mg KOH/ mL lipid)
Bilangan asam AV = V × N × M G
V = Jumlah KOH yang diperlukan untuk titrasi (mL) N = Normalitas KOH (mg/mL)
M = Berat molekul KOH (56,1) G = Berat sampel (g)
Penentuan Nilai Total Oksidasi (Perrin 1996)
Penentuan nilai total oksidasi (TOTOX) dilakukan dengan metode Perrin (1996) dengan persamaan dibawah ini:
Nilai Total Oksidasi = (2PV + AV)
PV = Nilai bilangan peroksida AV = Nilai p-anisidin
Analisis Profil Asam Lemak (AOAC 2005)
Asam-asam lemak diubah menjadi ester-ester metil atau alkil yang lainnya sebelum disuntikkan ke dalam kromatografi gas. Metilasi dilakukan dengan merefluks lemak di atas penangas air dengan pereaksi berturut-turut NaOH-metanol 0,5 N, BF3 dan n-heksana. Sebanyak 0,02 g minyak dari sampel dimasukkan ke dalam tabung reaksi dan ditambahkan 5 mL NaOH-metanol 0,5 N lalu dipanaskan dalam penangas air selama 20 menit pada suhu 80 ºC. Larutan kemudian didinginkan. Sebanyak 5 mL BF3 ditambahkan ke dalam tabung lalu tabung dipanaskan kembali pada waterbath dengan suhu 80ºC selama 20 menit dan didinginkan. Kemudian ditambahkan 2 mL NaCl jenuh dan dikocok. Selanjutnya, ditambahkan 5 mL isooktan, kemudian dikocok dengan baik. Larutan isooktan di bagian atas larutan dipindahkan dengan bantuan pipet tetes ke dalam tabung reaksi. Sampel lemak sebanyak 1 μL diinjeksikan ke dalam gas chromatography. Asam lemak yang ada dalam metil ester akan diidentifikasi oleh
flame ionization detector (FID) atau detektor ionisasi nyala dan respon yang ada akan tercatat melalui kromatogram (peak).
Identifikasi asam lemak dilakukan dengan menginjeksikan metil ester pada alat kromatografi gas dengan kondisi sebagai berikut : jenis alat kromatografi gas yang digunakan adalah Shimadzu GC 2010 Plus, gas yang digunakan sebagai fase bergerak adalah gas nitrogen dengan laju alir 30 mL/menit dan sebagai gas pembakar adalah hidrogen dan oksigen, kolom yang digunakan adalah capilary column merk Quadrex dengan diameter dalam 0,25 mm.
Analisis kuantitatif asam lemak dihitung dengan rumus :
Asam Lemak (%) = � � � � �
100− � � � � � X 100%
Kondisi alat GC pada saat analisis:
a) Kolom = Cyanopropil methyl sil (capilary column) b) Dimensi kolom = P = 60 m, Ø dalam = 0,25 mm, 0,25 μm film
Tickness
c) Laju alir N2 = 30 mL/menit d) Laju alir H2 = 40 mL/menit e) Laju alir udara = 400 mL/menit f) Suhu injektor = 220 °C
3 HASIL DAN PEMBAHASAN
Karakteristik Bahan Baku
Ikan makerel di Indonesia digunakan sebagai bahan baku ikan kaleng. Ukuran ikan yang digunakan sebagai bahan baku berkisar antara 196,67±19,04 g dengan panjang 26±1 cm. Persentase bagian ikan yang digunakan sebagai bahan baku ikan kaleng 67,80% dari bobot utuh ikan atau 133,33±13,79 g per ekor. Hasil samping (by-product) dari pengalengan ikan makerel yaitu kepala, jeroan dan ekor (63,33±12,23 g) atau sebanyak 32,20% digunakan sebagai bahan baku pembuatan tepung ikan. Data berat bagian/proporsi ikan makerel dapat dilihat pada Tabel 2.
Tabel 2 Proporsi ikan makerel
Morfometrik Ikan Makerel
Bagian Berat (g) Proporsi (%)
Utuh 196,67 ± 19,04 100,00
Daging 133,33 ± 13,79 67,80
Kepala 38,00 ± 6,08 19,32
Jeroan 20,67 ± 4,62 10,51
Ekor 4,67 ± 1,53 2,37
Komposisi kimia dari bahan baku penepungan (kepala, ekor dan jeroan) yang meliputi analisis kandungan lemak, protein, lemak, karbohidrat, kadar abu dan kadar air dapat dilihat pada Tabel 3. Proksimat menunjukkan persentase kandungan gizi dari bahan baku hasil penepungan. Persentase kadar air tertinggi yaitu 69,38±0,53%, kemudian protein dengan persentase 18,67±0,27%. Kandungan lemak memiliki persentase yang tinggi yaitu 9,23±0,32%. Hasil uji sejalan dengan yang dilaporkan oleh Lim (2012) yang menganalisis kandungan lemak ikan makerel yaitu 9,04% dan Fuadi (2014) dengan kadar lemak 9,93% pada bagian daging.
Tabel 3 Proksimat bahan baku penepungan ikan makerel
Komposisi Persentase (%)
Protein 18,00 ± 0,31
Karbohidrat 1,22 ± 0,32
Lemak 9,23 ± 0,32
Abu 2,18 ± 0,24
Air 69,38 ± 0,53
Persentase kandungan lemak pada sampel yang diuji lebih tinggi dibandingkan dengan hasil yang dilaporkan Osako et al. (2006) yaitu kandungan lemak pada viscera makerel Scomber australasicus sebesar 8,1%. Suseno et al.
(2014) juga melaporkan kandungan lemak yang lebih rendah pada viscera ikan
Karacam (2011) menambahkan bahwa spesifik spesies dan perbedaan lokasi penangkapan juga mempengaruhi kandungan proksimat ikan makerel. Kadar karbohidrat dan abu bahan baku yaitu 0,55±0,26% dan 2,17±0,24%.
Residu Logam Berat Bahan Baku dan Minyak Ikan Makerel
Hasil analisis residu logam berat menunjukkan bahwa pada bahan baku penepungan terdapat residu kadmium (Cd) sebesar 0,02 ppm dan timbal (Pb)
sebesar 0,65 ppm. Hasil analisis residu Pb berada diatas ambang IFOS yaitu ≤0,1
ppm. Minyak ikan yang dihasilkan dari proses penepungan juga masih mengandung residu logam berat yaitu kadmium (Cd) sebesar 0,002 ppm dan timbal (Pb) sebesar 0,022 ppm. Konsentrasi residu logam berat Cd dan Pb pada minyak kasar mengalami penurunan dibandingkan pada bahan baku penepungan. Residu logam berat bahan baku dan minyak hasil samping penepungan dapat
Keterangan : TTD = tidak terdeteksi; Cd =kadmium; Pb =timbal; Hg =raksa; N/i=nikel; As =arsen Netralisasi merupakan salah satu metode untuk menghilangkan bahan pengotor yang terdapat dalam minyak. Logam berat merupakan salah satu bahan pengotor yang umum terdapat dalam hasil perikanan. Pengujian residu logam berat sangat penting dilakukan terkait keamanan bahan pangan. Residu logam berat minyak ikan makerel kasar dan hasil netralisasi disajikan pada Tabel 4.
Karakteristik Parameter Oksidasi
Karakteristik minyak ikan makerel kasar
Proses penepungan ikan menghasilkan produk utama berupa tepung ikan dan produk samping berupa minyak ikan. Minyak ikan yang dihasilkan oleh perusahaan melalui beberapa tahapan, yaitu proses ekstraksi wet rendering, dekantasi dan perebusan. Proses dekantasi dilakukan untuk mengendapkan komponen non minyak yang terdapat dalam hasil ekstraksi dan proses perebusan
dilakukan untuk menguapkan kadar air pada minyak. Produk sampingan (by-product) berupa minyak ikan kasar umumnya memiliki kualitas yang kurang
baik sehingga hanya dimanfaatkan untuk bahan baku pakan hewan (feed). Karakteristik parameter oksidasi minyak ikan makerel kasar dapat dilihat pada Tabel 5.
Tabel 5 Karakteristik parameter oksidasi minyak ikan makerel
Parameter Minyak Ikan Standar
Kasar segar Kasar rebus IFOS IFOMA IFOMA. Nilai peroksida (PV) minyak ikan berkaitan dengan faktor kesegaran bahan baku yang digunakan (Aidos et al. 2003). Batista et al. (2009) melaporkan bahwa minyak ikan sarden kasar dari hasil samping memiliki nilai peroksida yang tinggi yaitu 45,3 – 68,3 meq/kg dan memiliki warna gelap yang mengindikasikan bahwa minyak tersebut telah teroksidasi. Ikan makarel yang digunakan sebagai bahan baku merupakan ikan impor yang diasumsikan telah mengalami penyimpanan yang lama sehingga menyebabkan kualitas minyak yang dihasilkan kurang baik. Faktor lain yang mempengaruhi tingginya hidroperoksida adalah suhu (Aidos et al. 2003; Rabiei et al. 2011; Capitani et al. 2011). Proses penepungan menggunakan suhu tinggi untuk ekstraksi dan proses perebusan sehingga dapat menyebabkan tingginya nilai peroksida minyak kasar dan minyak kasar hasil perebusan. Proses perebusan minyak ikan kasar dilakukan dengan mengalirkan udara panas pada minyak untuk menguapkan air yang terkandung. Proses ini menyebabkan terjadinya proses autoooksidasi minyak. Suhu tinggi dapat mengkatalis reaksi oksigen menjadi radikal dan mempengaruhi ikatan pada minyak sehingga terbentuk radikal bebas berupa senyawa hidroperoksida.
alkali yang digunakan untuk menghilangkan sabun pada proses netralisasi (Crexi
et al. 2010; Sathivel et al. 2003).
Bilangan asam merupakan parameter kualitas untuk menentukan adanya asam lemak bebas atau asam non lipid lain dalam minyak. Bilangan asam dipengaruhi oleh beberapa faktor yaitu komposisi minyak, prosedur ekstraksi dan kesegaran bahan baku (Rubio-Rodriguez et al. 2008). Hasil uji bilangan asam minyak ikan kasar tanpa perebusan (31,52±0,14mg KOH/kg) dan minyak ikan dengan perebusan (33,92±0,72 mg KOH/kg) tidak memenuhi standar (IFOS dan IFOMA).
Nilai p-anisidin (AnV) merupakan parameter oksidasi sekunder yang berhubungan dengan penyimpanan dari minyak ikan yang disebabkan oleh degradasi lemak lanjutan yang diinisiasi oleh hidroperoksida. Proses ini menghasilkan produk akhir berupa komponen non volatile sekunder (Aidos et al.
2003). Hasil analisis nilai p-anisidin menunjukkan minyak ikan kasar dan hasil perebusan yaitu 19,19±1,36 meq/kg dan 21,40±0,78 meq/kg, nilai tersebut masih memenuhi standar IFOMA namun tidak memenuhi standar IFOS. Hasil tersebut lebih rendah dibandingkan hasil pengujian nilai p-anisidin minyak ikan herring
hasil samping yang dilaporkan oleh Mohanarangan et al. (2012) yaitu 56,93-69,83 meq/kg. Nilai anisidin merupakan parameter ketengikan minyak. Minyak ikan yang memiliki nilai anisidin diatas standar (IFOS) dianggap telah mengalami ketengikan. Kosoko et al. (2009) menyatakan bahwa nilai anisidin meningkat seiring dengan meningkatnya suhu. Nilai anisidin digunakan sebagai indikator kandungan aldehid dalam minyak dan akan meningkat secara drastis seiring dengan dekomposisi senyawa oksidasi primer (Crapiste et al. 1999).
Nilai total oksidasi pada minyak ikan merupakan hasil penjumlahan dua kali nilai peroksida ditambah nilai anisidin. Hasil analisis total oksidasi minyak ikan makerel kasar tidak memenuhi standar kualitas minyak (IFOS dan IFOMA) yaitu minyak kasar tanpa perebusan (75,31±2,06 meq/kg) dan minyak ikan makerel kasar (89,98±2,96 meq/kg). Hasil yang didapatkan pada penelitian ini masih lebih tinggi dari rekomendasi Bimbo (1998) yang menyatakan nilai TOTOX untuk minyak layak konsumsi berkisar antara 10-60 meq/Kg. IFOS menyatakan minyak layak konsumsi harus memiliki nilai TOTOX dibawah 20 meq/kg.
Karakteristik minyak ikan makerel hasil netralisasi
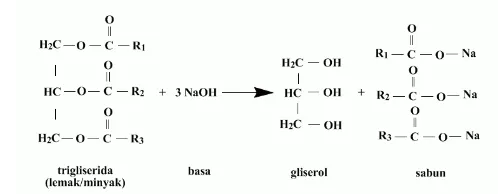
tersabunkan (Estiasih et al. 2004; Pigott 1996). Fraksi non minyak yang terikat dalam minyak antara lain asam lemak bebas dan pigmen. Konsentrasi NaOH tinggi yang digunakan menyebabkan asam lemak bebas berikatan dengan ion Na+ dan menjadi sabun. Reaksi saponifikasi yang terjadi juga mengikat komponen pigmen sehingga warna minyak hasil netralisasi lebih cerah dibandingkan minyak kasar. Karakteristik parameter oksidasi minyak ikan setelah perlakuan konsentrasi NaOH disajikan pada Tabel 6.
Tabel 6 Karakteristik parameter oksidasi minyak ikan makerel pada tiap perlakuan konsentrasi NaOH
Keterangan : huruf superscript yang berbeda pada baris yang sama menunjukkan adanya
perbedaan nyata (p<0,05); R22 = persentase penurunan perlakuan 22oBe; R24 = persentase penurunan perlakuan 24oBe; R26 = persentase penurunan
perlakuan 26oBe.
Pembentukan senyawa peroksida merupakan tanda terjadinya proses oksidasi primer pada minyak ikan. Senyawa hidroperoksida terbentuk dalam minyak disebabkan oleh berbagai faktor diantaranya faktor kesegaran bahan dan suhu perlakuan (Aidos et al. 2003). Hasil analisis nilai peroksida pada awal dan setelah perlakuan netralisasi menunjukkan penurunan yang signifikan. Nilai peroksida minyak ikan makerel terbaik pada perlakuan 26oBe dengan nilai 3,60±0,42 meq/kg dan yang paling rendah pada perlakuan 22oBe dengan nilai 8,15±0,84 meq/kg. Reaksi saponifikasi (Gambar 6) yang terjadi pada pemurnian menjadi faktor yang menyebabkan turunnya nilai peroksida. Senyawa hidroperoksida yang terdapat dalam minyak berikatan dengan sabun yang terbentuk dalam reaksi tersebut (Huang dan Sathivel 2010).
Gambar 6 Reaksi saponifikasi (http//: asuhankakseto.blogspot.com)
15,88±0,06% sehingga diperlukan jumlah konsentrasi NaOH yang tinggi. Hasil pengujian persentase asam lemak bebas menunjukkan bahwa semakin tinggi konsentrasi NaOH yang digunakan maka akan semakin rendah nilai persentase asam lemak bebas dalam minyak. Nilai asam lemak bebas paling rendah diperoleh pada perlakuan 26oBe (1,93±0,25%) sedangkan persentase paling tinggi pada 22oBe (2,68%±0,17%). Uji statistik menunjukkan adanya perbedaan yang nyata antara tiap perlakuan (P<0,05), namun pada perlakuan 24oBe dan 26oBe tidak berbeda nyata (P>0,05). Perlakuan 24oBe dipilih sebagai perlakuan terbaik karena dapat menurunkan asam lemak bebas secara efektif dan tidak berbeda nyata dengan perlakuan 26oBe, persentase penurunan asam lemak bebas dari perlakuan yang terpilih dapat mencapai 86,35%. Alasan lain yaitu dari sisi ekonomi, penggunaan NaOH dengan jumlah lebih sedikit akan mengurangi biaya produksi perusahaan. Parameter oksidasi primer dan sekunder berhubungan erat dengan warna, bau, rasa dan pengotor lain dalam minyak ikan (Suseno et al. 2012). Asam lemak bebas dalam minyak merupakan parameter dalam penentuan kualitas minyak. Minyak yang memiliki persentase asam lemak bebas yang tinggi akan memiliki aroma dan rasa yang kurang baik (Sathivel et al. 2003). Asam lemak bebas dalam minyak akan mudah teroksidasi sehingga produk turunan misalnya aldehid dan keton akan mudah terbentuk dan menyebabkan minyak menjadi lebih mudah tengik.
Nilai bilangan asam berkaitan erat dengan jumlah KOH yang digunakan untuk menetralkan 1 g minyak. Hasil analisis statistik menunjukkan perbedaan yang nyata (P<0,05) antara tiap perlakuan. Bilangan asam paling rendah diperoleh pada perlakuan 26oBe (3,84±0,51 mg KOH/kg) dan paling tinggi pada 22oBe (5,32±0,34 mg KOH/kg).
Nilai p-anisidin merupakan salah satu parameter pengukuran oksidasi sekunder pada minyak. Senyawa p-anisidin merupakan turunan dari senyawa hidroperoksida pada oksidasi primer berupa senyawa aldehid dan keton. Senyawa tersebut yang menyebabkan perubahan bau dari minyak ikan dan menjadi tengik. Hasil analisis nilai p-anisidin menunjukkan perbedaan yang nyata antar tiap perlakuan konsentrasi NaOH. Nilai p-anisidin paling tinggi ditemukan pada perlakuan 26oBe (19,71±0,18 meq/kg) dan paling rendah pada perlakuan 22oBe (7,82±0,24 meq/kg). Waktu penyimpanan merupakan faktor yang menyebabkan pembentukan senyawa p-anisidin disamping pengaruh kandungan antioksidan alami yang terkandung dalam minyak ikan. Proses netralisasi menyebabkan terpisahnya antioksidan alami kedalam fraksi padat (sabun) sehingga minyak akan lebih mudah teroksidasi. Huang dan Sathivel (2010) melaporkan bahwa proses netralisasi secara signifikan menghilangkan pigmen karotenoid dalam minyak. Karotenoid merupakan pigmen alami yang terdapat dalam minyak ikan, dan berfungsi sebagai antioksidan alami. Tanaka et al. (1977) melaporkan bahwa karotenoid merupakan pigmen yang terdapat pada minyak ikan tuna. Kandungan antioksidan alami pada minyak dengan perlakuan 22oBe diduga paling tinggi dibandingkan dengan perlakuan yang lain sehingga menyebabkan minyak tersebut tidak mudah teroksidasi dan memiliki nilai p-anisidin yang paling rendah.
lanjut menunjukkan bahwa perlakuan 24oBe adalah perlakuan konsentrasi NaOH terbaik. Nilai total oksidasi ini juga menunjukkan kestabilan yang lebih baik dibandingkan dengan perlakuan yang lain. Bimbo (1998) menyatakan nilai TOTOX untuk minyak layak konsumsi berkisar antara 10-60 meq/kg. IFOS menyatakan minyak layak konsumsi harus memiliki nilai TOTOX dibawah 20 meq/kg, data analisis TOTOX pada tiap perlakuan tidak memenuhi IFOS sehingga diperlukan pemurnian lanjutan.
Karakteristik minyak ikan dengan penambahan adsorben
Senyawa hidroperoksida merupakan senyawa yang terbentuk akibat degradasi asam lemak yang disebabkan oleh proses autooksidasi. Analisis nilai peroksida (PV) minyak ikan makerel dengan penambahan adsorben disajikan pada Gambar 7.
Gambar 7 Nilai peroksida minyak ikan makerel dengan jenis dan perlakuan adsorben yang berbeda ( =atapulgit ; = kitosan; huruf superscript menunjukkan nilai yang berbeda nyata)
Analisis nilai peroksida pada minyak ikan dengan penambahan adsorben menunjukkan hasil yang berbeda nyata (P<0,05). Hasil nilai peroksida terbaik yaitu 3,52±0,16 meq/kg diperoleh pada pelakuan adsorben atapulgit dengan konsentrasi 5%. Penambahan atapulgit 5% sebagai adsorben dapat menurunkan nilai peroksida sebesar 37,14%, sedangkan perlakuan lain yaitu atapulgit 4% (31,61%); atapulgit 3% (22,32%); kitosan 5% (29,82%); kitosan 4% (18,21%); kitosan 3% (13,04%) menunjukkan persentase penurunan nilai peroksida yang lebih rendah. Atapulgit merupakan mineral alam yang mengandung silika dan magnesium. Kandungan silika dalam atapulgit mampu mengikat senyawa peroksida karena bersifat phorous (Suseno et al. 2013). Kitosan merupakan turunan kitin yang memiliki gugus amina (NH3+) yang dapat berikatan dengan senyawa hasil oksidasi. Atapulgit memiliki kemampuan adsorpsi senyawa peroksida lebih baik dibandingkan dengan kitosan, hal ini disebabkan oleh gugus silanol (Si-OH) yang terdapat pada atapulgit (El-mofty et al. 2008).
Asam lemak bebas merupakan hasil degradasi trigliserida yang mengalami reaksi hidrolisis. Analisis persentase asam lemak bebas (FFA) minyak ikan makerel dengan penambahan adsorben disajikan pada Gambar 8. Analisis persentase asam lemak bebas pada minyak ikan dengan penambahan adsorben menunjukkan hasil yang berbeda nyata (P<0,05). Persentase asam lemak bebas terendah yaitu 1,17±0,32% diperoleh pada pelakuan adsorben atapulgit dengan
konsentrasi 5%. Penambahan atapulgit 5% dapat menurunkan persentase asam lemak bebas secara signifikan dibandingkan dengan perlakuan lain.
Gambar 8 Persentase asam lemak bebas minyak ikan makerel dengan jenis perlakuan adsorben yang berbeda ( =atapulgit ; = kitosan; huruf superscript menunjukkan nilai yang berbeda nyata)
Penambahan atapulgit 5% sebagai adsorben dapat menurunkan persentase asam lemak bebas sebesar 45,83%, sedangkan perlakuan lain yaitu atapulgit 4% (40,74%); atapulgit 3% (27,78%); kitosan 5% (40,74%); kitosan 4% (25,00%); kitosan 3% (8,33%) memiliki persentase penurunan asam lemak bebas yang lebih rendah. Mekanisme yang terjadi pada proses penambahan adsorben yaitu senyawa pengotor akan menempel dan tersaring pada adsorben. Komponen silanol (ikatan Si-OH) yang terdapat pada atapulgit diduga lebih reaktif dibandingkan dengan gugus amina (NH3+) pada kitosan, sehingga dapat menyerap asam lemak bebas dalam minyak. Luas permukaan juga berpengaruh terhadap hasil adsorpsi oleh adsorben (Tambunan et al. 2014; Suseno et al. 2011)
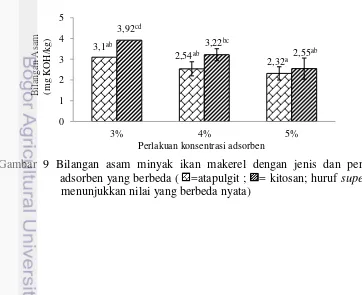
Ketengikan minyak ikan dimulai saat trigliserida terpecah menjadi asam lemak dan gliserol yang akan meningkatkan bilangan asam (Mohanaranngan 2012). Analisis bilangan asam (AV) minyak ikan makerel dengan penambahan adsorben disajikan pada Gambar 9.
Analisis bilangan asam pada minyak ikan dengan penambahan adsorben menunjukkan hasil yang berbeda nyata (P<0,05). Bilangan asam terendah didapatkan dari perlakuan adsorben atapulgit 5% dengan nilai 2,32±0,63 mg KOH/kg. Bilangan asam minyak ikan makerel menurun secara signfikan setelah penambahan atapulgit 5%. Penambahan atapulgit 5% sebagai adsorben dapat menurunkan bilangan asam sebesar 46,05%, sedangkan perlakuan lain yaitu atapulgit 4% (40,93%); atapulgit 3% (27,91%); kitosan 5% (40,70%); kitosan 4% (25,12%); kitosan 3% (8,84%) memiliki persentase penurunan bilangan asam yang lebih rendah.Bilangan asam merupakan parameter kualitas minyak yang berhubungan langsung dengan persentase asam lemak bebas. Adeniyi dan Bawa (2006) melaporkan hasil bilangan asam minyak ikan makerel hasil pemurnian yaitu 2,27 mg KOH/kg.
Analisis nilai p-anisidin (AnV) minyak ikan makerel dengan penambahan adsorben disajikan pada Gambar 10.
Gambar 10 Nilai p-anisidin minyak ikan makerel dengan jenis dan perlakuan adsorben yang berbeda ( =atapulgit ; = kitosan; huruf superscript menunjukkan nilai yang berbeda nyata)
Analisis nilai p-anisidin pada minyak ikan dengan penambahan adsorben menunjukkan hasil yang berbeda nyata (P<0,05). Nilai p-anisidin terendah didapatkan pada perlakuan adsorben atapulgit 5% dengan nilai 5,36±1,86meq/kg. Penambahan atapulgit 5% dapat menurunkan nilai anisidin secara signifikan (P<0,05) dibandingkan dengan perlakuan lain. Penambahan atapulgit 5% sebagai adsorben dapat menurunkan nilai anisidin sebesar 62,57%, sedangkan perlakuan lain yaitu atapulgit 4% (50,70%); atapulgit 3% (31,08%); kitosan 5% (59,71%); kitosan 4% (48,46%); kitosan 3% (17,67%) memiliki persentase penurunan nilai p-anisidin yang lebih rendah. Mekanisme yang terjadi pada saat penambahan adsorben yaitu senyawa anisidin yang terdapat pada minyak ikan akan terserap dan menempel pada permukaan adsorben (Garcia-Moreno et al. 2012).
Nilai totox adalah hubungan oksidasi primer dan sekunder yang didapatkan dengan penjumlahan dua kali nilai peroksida dan nilai anisidin. Analisis total oksidasi (TOTOKS) minyak ikan makerel dengan penambahan adsorben disajikan pada Gambar 11.
Gambar 11 Nilai total oksidasi minyak ikan makerel dengan jenis dan perlakuan
adsorben yang berbeda ( =atapulgit; = kitosan; huruf superscript
menunjukkan nilai yang berbeda nyata)
Analisis total oksidasi pada minyak ikan dengan penambahan adsorben menunjukkan hasil yang berbeda nyata (P<0,05). Nilai total oksidasi terendah didapatkan pada perlakuan adsorben atapulgit 5% dengan nilai 12,4±1,53 meq/kg. Nilai total oksidasi minyak ikan makerel menurun secara signfikan setelah penambahan atapulgit 5%. Penambahan atapulgit 5% sebagai adsorben dapat menurunkan nilai anisidin sebesar 51,43%, sedangkan perlakuan lain yaitu atapulgit 4% (42,34%); atapulgit 3% (23,35%); kitosan 5% (46,61%); kitosan 4% (35,25%); kitosan 3% (15,67%) memiliki persentase penurunan nilai total oksidasi yang lebih rendah. Nilai total oksidasi dapat digunakan untuk mengukur progresivitas dari proses deteriorasi yang terjadi pada minyak dan menyediakan informasi mengenai pembentukan produk oksidasi primer serta sekunder (Hamilton and Rossell 1986).
Profil Asam Lemak
Minyak ikan hasil samping proses pengolahan hasil perikanan diketahui
banyak mengandung omega-3 (Junker et al. 2006; Estiasih et al. 2013). Fuadi et al. (2014) melaporkan bahwa ikan makerel mengandung DHA dalam
jumlah yang tinggi yaitu 19,22%. Proses penepungan ikan menghasilkan minyak kasar dengan jumlah yang tinggi namun memiliki kualitas yang rendah.
Penentuan profil asam lemak dilakukan untuk menentukan kandungan asam lemak berupa asam lemak jenuh/Saturated Fatty Acid (SFA), asam lemak tidak jenuh tunggal/Mono Unsaturated Fatty Acid (MUFA) dan asam lemak tak jenuh majemuk/Poly Unsaturated Fatty Acid (PUFA). Profil asam lemak bahan baku dan minyak ikan makerel disajikan pada Tabel 7.
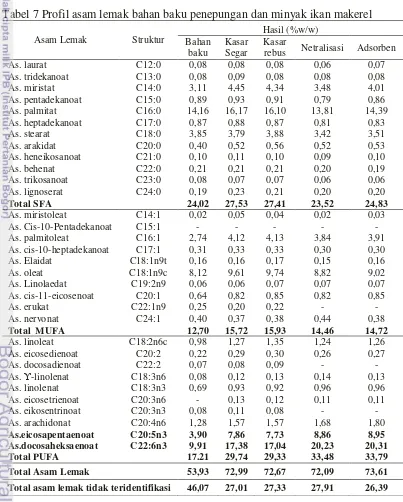
Data yang tersaji menunjukkan bahwa kandungan asam lemak jenuh pada bahan baku yaitu 24,02% sedangkan pada minyak kasar tanpa dan dengan perebusan memiliki total SFA yaitu 27,53% dan 27,41%. Asam lemak dominan pada jenis asam lemak jenuh bahan baku dan minyak kasar yaitu asam palmitat dengan persentase 14,16%; 16,17%; 17,10%. Kandungan asam lemak jenuh pada minyak sebelum netralisasi yaitu 27,53% sedangkan pada minyak setelah netralisasi total SFA menurun menjadi 23,52%.
Penurunan persentase SFA minyak ikan setelah netralisasi diduga disebabkan oleh proses netralisasi yang dilakukan. Proses saponifikasi
menghilangkan asam lemak yang memiliki rantai C yang lebih pendek dibandingkan dengan asam lemak yang memiliki rantai lebih panjang. Data yang diperoleh sesuai dengan hasil penelitian yang dilakukan oleh Sahena et al. (2010) yang menunjukkan bahwa asam palmitat (C16:0) merupakan asam lemak yang dominan pada jenis asam lemak jenuh pada ikan Indian Mackerel. Hasil serupa juga dilaporkan oleh Guil-Guerrero et al. (2011) yaitu persentase SFA pada ikan makerel Atlantik (Scomber scombrus) sebesar 23,3%. Kandungan SFA pada minyak sebelum dan setelah penambahan adsorben yaitu 23,52% dan 24,83%. Asam lemak dominan pada jenis asam lemak jenuh minyak sebelum dan setelah penambahan adsorben yaitu asam palmitat dengan persentase 13,81% dan 14,39%
Tabel 7 Profil asam lemak bahan baku penepungan dan minyak ikan makerel
Asam Lemak Struktur
rebus Netralisasi Adsorben As. laurat
Total Asam Lemak 53,93 72,99 72,67 72,09 73,61
Hasil uji menunjukkan bahwa jenis asam lemak dominan pada kelompok asam tidak jenuh tunggal (MUFA) adalah kandungan asam oleat (C18:1n9c). Persentase MUFA pada bahan baku dan minyak kasar (segar dan dengan perebusan) yaitu 12,70%; 15,72% dan 15,93%. Kandungan MUFA ikan laut umumnya didominasi oleh asam oleat (Guil-Guerrero et al. 2011). Persentase MUFA pada minyak ikan makerel sebelum dan setelah netralisasi yaitu 15,72% dan 14,46%. Asam oleat yang terdeteksi pada minyak ikan makerel sebelum dan setelah netralisasi yaitu 9,61% dan 8,82%, sedangkan hasil pada penambahan adsoben yaitu 9,02%. Persentase MUFA pada minyak ikan makerel sebelum dan setelah penambahan adsorben yaitu 14,46% dan 14,72%.
Kandungan PUFA pada bahan baku dan minyak kasar yaitu 17,21%, 29,74% dan 29,33%. Bahan baku penepungan memiliki kandungan PUFA rendah yang disebabkan oleh komposisi asam lemak yang tidak teridentifikasi. Komponen asam lemak yang tidak teridentifikasi mempengaruhi persentase PUFA dalam perbandingan dengan total asam lemak. Komposisi asam lemak ikan dipengaruhi banyak faktor. Orban et al. (2011) mengungkapkan bahwa waktu, daerah, dan musim penangkapan dapat mempengaruhi komposisi asam lemak. Ikan makerel memiliki rasio kandungan omega-3 yang paling tinggi dibandingkan dengan komposisi asam lemak yang lain seperti atlantic cod, shortfin mako,
forkbeard, dan bluewhiting. Tercatat bahwa sekitar 80-87% dari total asam lemak merupakan omega-3 (Orban et al. 2011; Orban et al. 2008; Orban et al. 2007; Orban et al. 2006). Asam dokosaheksanoat (DHA) merupakan asam lemak yang dominan terdapat pada ikan makerel. Kandungan DHA pada bahan baku yaitu 9,91%, sedangkan pada minyak kasar (segar dan direbus) yaitu 17,38% dan 17,04%. Persentase kandungan DHA pada minyak ikan kasar meningkat dibandingkan dengan bahan baku karena jumlah asam lemak total yang teridentifikasi persentasenya juga meningkat. Peningkatan kandungan DHA disebabkan proses ektraksi. Proses ekstraksi soxhlet digunakan untuk mengekstrak bahan baku, sedangkan untuk ekstraksi minyak kasar di perusahaan digunakan metode wet rendering. Suhu tinggi yang digunakan pada metode soxhlet diduga berpengaruh terhadap total asam lemak yang teridentifikasi pada minyak. Total asam lemak yang teridentifikasi pada bahan baku dan minyak kasar (tanpa dan dengan perebusan) yaitu 53,93%, 72,99%, dan 72,67%. Total asam
lemak tersebut berpengaruh terhadap persentase kandungan asam lemak. Shim et al. (2004) melaporkan hasil pengujian kandungan omega-3 pada bahan
baku ikan kaleng (makerel dan tuna) didominasi oleh DHA pada kelompok asam lemak tidak jenuh majemuk dengan persentase 6,4-7,4%.
Kandungan PUFA pada minyak ikan makerel sebelum dan setelah netralisasi yaitu 29,74% dan 33,48%. Kandungan DHA pada minyak ikan makerel sebelum netralisasi adalah 17,38%, sedangkan pada minyak ikan makerel setelah netralisasi yaitu 20,23%. Hasil ini sejalan dengan hasil yang diperoleh oleh Fuadi
et al. (2014) dengan kandungan DHA dan EPA minyak ikan makerel hasil netralisasi yaitu 20,58% dan 7,65% dengan total PUFA yaitu 32,83%. Kandungan
DHA ikan makerel dipengaruhi variasi musim dan lokasi penangkapan (Osako et al. 2003; Lim et al. 2012; Bae dan Lim 2013). Konsentrasi PUFA pada
terikat pada proses saponifikasi (Huang dan Sathivel 2010; Sathivel dan Priyanwiwatkul 2004). Mohanarangan et al. (2012) menyatakan bahwa peningkatan konsentrasi pada PUFA akan menurunkan konsentrasi MUFA dan SFA.
Kandungan PUFA pada minyak ikan makerel sebelum dan setelah penambahan adsorben yaitu 33,48% dan 33,79%. Kandungan DHA pada minyak ikan makerel sebelum penambahan adsorben adalah 20,23%, sedangkan pada minyak ikan makerel setelah penambahan adsorben yaitu 20,31%. Proses penambahan adsorben meningkatkan konsentrasi PUFA, namun tidak terlalu tinggi. Hal ini disebabkan karena pada proses penambahan adsorben menyerap senyawa berukuran kecil seperti senyawa oksidasi (primer dan sekunder), pigmen, asam lemak bebas (Suseno et al. 2013). PUFA memiliki rantai panjang dan ikatan rangkap sehingga tidak dapat terikat pada adsorben yang digunakan.
4 SIMPULAN DAN SARAN
Simpulan
Persentase kepala, jeroan dan ekor sebagai bahan baku penepungan didapatkan 32,20% dari bobot tubuh ikan. Ikan makerel termasuk golongan ikan berlemak tinggi dengan kadar lemak 9,23±0,32%. Residu logam berat dalam ikan makerel yaitu kadmium (Cd) 0,02±0,005 ppm dan timbal (Pb) 0,65±0,093 ppm. Karakteristik parameter oksidasi minyak ikan makerel kasar tanpa perebusan lebih baik dibandingkan minyak ikan makerel yang direbus. Terjadi penurunan logam berat pada minyak kasar yaitu sebesar 90% untuk kadmium (Cd) dan timbal (Pb) sebesar 66,15%. Perlakuan konsentrasi NaOH terbaik adalah 24oBe (17,87%). Perlakuan adsorben terbaik yaitu atapulgit 5% menghasilkan minyak ikan dengan karakteristik sebagai berikut yaitu PV 3,52±0,16 meq/kg; AV 2,32±0,63 mg KOH/kg; FFA 1,17±0,32%; AnV 5,36±1,86 meq/kg; TOTOKS 12,4±1,53 meq/kg dengan PUFA 33,79% EPA 8,95% DHA 20,31%. Persentase reduksi senyawa oksidasi yaitu PV 37,14%; AnV 62,57; AV 46,05%; FFA 45,83%; TOTOKS 51,43%.
Saran
DAFTAR PUSTAKA
Ackman RG. 1989. Nutritional composition of fats in sea foods. Progress in Food Nutrition Science 13: 161-289.
Adeniyi OD, Bawa AA. 2006. Mackerel (ScomberScrombrus) oil extraction and evaluation as raw materials for industrial utilization. Leonardo Journal of Sciences. 8:33-42
Ahmadi K, Mushollaeni W. 2009. Aktivasi kimiawi zeolit alam untuk pemurnian minyak ikan dari hasil samping penepungan ikan lemuru (Sardinella longiceps). Jurnal Teknologi Pertanian. 8(2):71–79
Aidos I, Jacobsen C, Jensen B, Luten JB, van der Padt A, Boom RM, 2002. Volatile oxidation products formed in crude Heerring oil under accelerated oxidation conditions.Journal Lipid Science Technology. 4:148–161 .
Aidos I, Schelvus-Smit R, Veldnan MB, Luten J, Padt AVD, Broom RM. 2003. Chemical and sensory evaluation of crude oil extracted from Heerring by-product from different processing operations. Journal of Agricultural and Food Chemistry 50. 1897 – 1903.
Arifianto TB. 2013. Karakterisasi bahan dan ekstraksi minyak ikan dari hasil samping ikan patin (Pangasius hypoptalmus) [tesis]. Bogor (ID): Institut Pertanian Bogor.
[AOAC] Association of Official Analytical Chemist. 2005. Official Method of Analysis of the Association of Official Analytical of Chemist. Arlington. Virginia (US): The AOAC Inc.
[AOCS] American Oil Chemists’ Society. 1998. Official Methods and
Recommended Practices of the American Oil Chemists’ Society. 5th ed., Champaign (US): AOCS Press.
Bae JH, Yoon SH, Lim SY. 2011. Heavy metal contents and chemical compositions of the atlantic (Scomber scombrus), blue (Scomber australasicus), and chub (Scomber japonicus) mackerel muscles. Food Science Biotechnology. 20:709-714.
Bae JH, Lim SY. 2012. Effects of season on the heavy metal contents and chemical compositions of chub mackerel (Scomber japonicus) muscle. Journal of Food Science. 77: T52-T57.
Bae JH, Lim SY. 2013. Comparative study of the concentration of mercury and lead and the chemical characteristics of Japanese and Korean chub mackerel
(Scomber japonicus Houttuyn, 1782) in the East China Sea. Journal of Agricultur Resousces. 8(3):269-273
Batafor YMJ. 2014. Peningkatan kualitas minyak ikan sardin (Sardinella sp.) dengan sentrifugasi dan adsoben [tesis]. Bogor (ID): Institut Pertanian Bogor.
Batista I, Ramos C, Mendonça R, Leonor-Nunes M. 2009. Enzymatic hydrolysis of sardine (Sardina pilchardus) by-products and lipid recovery. Journal of Aquatic Food Product Technology. 18:120–134