INFRAMERAH
MUHAMAD FARID
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
Dengan ini saya menyatakan bahwa tesis yang berjudul Pengukuran Derajat Grafting Akrilamida pada Matriks Polisakarida dengan Spektrometri Inframerah adalah karya saya dengan arahan dari komisi pembimbing dan belum diajukan dalam bentuk apa pun kepada perguruan tinggi mana pun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam daftar pustaka di bagian akhir tesis ini.
Bogor, September 2011
Muhamad Farid
MUHAMAD FARID. Grafting degree Measurement of acrylamide onto polysaccharide using Infrared Spectrometry. Under direction of ZAINAL ALIM MAS’UD and H.M. ANWAR NUR.
Utilization of carbohydrate-based agricultural wastes has been carried out with the manufacture of derivatives by grafting and crosslinking with acrylamide. The success of the process is monitored by setting the levels of nitrogen in the product. This research work is trying to look for possible use of spectrometry Fourier Transform Infrared technique to determine level of nitrogen in the products. Preparation of powder with a reflectance technique gives satisfactory results for grafting product, also for saponified products very satisfactory. ANOVA test of the PLS for each processing the data on IR spectral of the grafted-crosslinked product and its saponified showed a smaller probability value of 0.05, it is indicate the model developed by the independent variable (wave number) is significant effect on nitrogen content at 95% confidence level. Results of Partial Least Square (PLS) model for each treatment to give the coefficient of determination (R2) ranged from 0.961-0.998, it is the model with the wave number of independent variables can predict nitrogen content as well. Results of PLS analysis also provide information that the processing of IR spectrum data does not affect the difference between the predictions and the values of the nitrogen content.
MUHAMAD FARID. Pengukuran Derajat Grafting Akrilamida pada Matriks Polisakarida dengan Spektrometri Inframerah. Dibimbing oleh ZAINAL ALIM MAS’UD dan H.M. ANWAR NUR.
Indonesia sebagai negara agraris yang merupakan negara penghasil singkong. Salah satu produk turunan singkong adalah tepung tapioka. Proses produksi tapioka dari singkong akan menghasilkan produk samping yang disebut onggok. Salah satu kandungan utama dalam onggok adalah karbohidrat, dalam bentuk selulosa dan pati. Sebagai pakan ternak pun, onggok tidak bisa langsung digunakan, melainkan harus difermentasi terlebih dahulu. Untuk meningkatkan nilai tambah dari onggok, maka harus dilakukan proses modifikasi kandungan utamanya sehingga diperoleh turunan yang mempunyai nilai jual tinggi.
Modifikasi tepung singkong (tepung tapioka) dapat dilakukan melalui reaksi pencangkokan dan penautanulang akrilamida membentuk super adsorben yang ramah lingkungan. Keberhasilan proses pencangkokan dan penautan ulang bisa dipantau dengan menentukan kandungan nitrogen dalam produk reaksi. Kandungan nitrogen ditentukan menggunakan metode klasik yaitu Kjeldahl. Untuk menghasilkan data dengan metode Kjeldahl membutuhkan bahan kimia, energi, waktu (sekitar 4 jam) dan kehatian-hatian yang tinggi.
Teknik pengukuran spektrum inframerah dekat (Near infrared, NIR) telah banyak digunakan dalam analisis kuantitatif nondestruktif yang cepat. Dengan mengukur spekrum inframerah sejumlah tertentu bahan yang analog yang sudah diketahui kadar analatnya dengan metoda lain, kemudian dilakukan pengolahan data analisis komponen utama (Principal Componen Analysis, PCA) dan pengolahan data kuadrat terkecil parsial (Partial Least Square, PLS) maka dapat dibuat model kalibrasi hubungan antara serapan pada bilangan gelombang tertentu serta kandungan analat yang dicari.
Kuantifikasi hubungan antara besaran serapan inframerah pada bilangan gelombang tertentu dengan kandungan nitrogen menggunakan analisis statistik PLS dalam rangka menunjang proses pengambilan keputusan yang cepat berkaitan dengan kondisi sintesis suatu reaksi. Sampel yang digunakan dalam pemodelan sebanyak 47 sampel yang terdiri dari 34 sampel dari produk pencangkokan dan penautan silang dan 13 sampel dari produk saponifikasinya.
Uji ANOVA dari PLS untuk setiap pengolahan data pada spektrum IR dari produk pencangkokan menunjukkan nilai probabilitas lebih kecil dari 0,05, yang berarti model yang dikembangkan dengan variabel bebas (bilangan gelombang) secara bersama-sama berpengaruh nyata terhadap kadar nitrogen pada tingkat kepercayaan 95%. Model hasil PLS untuk setiap pengolahan memberikan nilai koefisien determinasi (R2) berkisar 0,961 – 0,998, yang berarti model dengan variabel bebas bilangan gelombang dapat memprediksi kadar nitrogen dengan baik dan hasil prediksi memberikan hasil yang tidak berbeda (berimpit) dengan nilai aktual. Hasil analisis PLS juga memberikan informasi bahwa pengolahan data spektrum IR tidak berpengaruh terhadap perbedaan antara prediksi dan nilai aktual dari kadar nirogen.
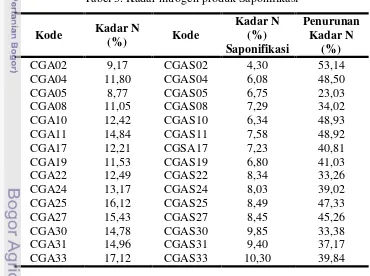
Produk saponifikasi mengandung nitrogen 4,30% – 10,30%, dan proses saponifikasi menurunkan kadar nitrogen produk pencangkokan-penautan berkisar 23,03% – 53,14%. Pada semua spektrum selain terlihat serapan karakteristik
Uji ANOVA dari PLS untuk setiap pengolahan data pada spektrum IR dari produk pencangkokan menunjukkan nilai probabilitas lebih kecil dari 0,05, yang berarti model yang dikembangkan dengan variabel bebas (bilangan gelombang) secara bersama-sama berpengaruh nyata terhadap kadar nitrogen pada tingkat kepercayaan 95%. Model hasil PLS untuk setiap pengolahan memberikan nilai koefisien determinasi (R2) berkisar 0,961 – 0,998, yang berarti model dengan variabel bebas bilangan gelombang dapat memprediksi kadar nitrogen dengan baik dan hasil prediksi memberikan hasil yang tidak berbeda (berimpit) dengan nilai aktual. Hasil analisis PLS juga memberikan informasi bahwa pengolahan data spektrum IR tidak berpengaruh terhadap perbedaan antara prediksi dan nilai aktual dari kadar nirogen.
© Hak Cipta milik IPB, tahun 2011 Hak Cipta dilindungi Udang-Undang
Dilarang mengutip sebagian atau seluruh karya tulis ini tanpa mencantumkan atau menyebutkan sumbernya. Pengutipan hanya untuk kepentingan pendidikan, penelitian, penulisan karya ilmiah, penyusunan laporan, penulisan kritik, atau tinjauan suatu masalah; dan pengutipan tersebut tidak merugikan kepentingan yang wajar IPB
NIM : G451 06 0041 Program Studi : Kimia
Disetujui
Komisi Pembimbing
Dr. Zainal Alim Mas’ud, DEA Ketua
Prof. (em) Dr. Ir. H. M. Anwar Nur, M.Sc Anggota
Diketahui
Ketua Program Studi Kimia
Dekan Sekolah Pascasarjana IPB
Prof.Dr. Dra. Purwantiningsih, MS. Dr.Ir. Dahrul Syah, MSc.Agr.
Puji dan Syukur penulis panjatkan kepada Allah SWT atas segala Rahmat dan Karunia-Nya sehingga karya ilmiah ini berhasil diselesaikan. Penelitian dengan judul Pengukuran Derajat Grafting Akrilamida pada Matriks Polisakarida dengan Spektrometri Inframerah diselesaikan selama 9 bulan sejak Januari sampai September 2011 bertempat di Laboratorium Terpadu IPB.
Terima kasih penulis ucapkan kepada berbagai pihak yang telah membantu dalam penyelesaian karya ilmiah ini, antara lain Dr. Zainal Alim Mas’ud, DEA dan Prof. (emeritus) Dr. Ir. H. M. Anwar Nur, M.Sc selaku komisi pembimbing, kepada Prof. Dr. Ir. Purwantiningsih, MS selaku Ketua Program Studi Kimia Sekolah Pascasarjana IPB, dan kepada Prof. Dr. Ir. Tun Tedja Irawadi, MS selaku Ketua Departemen Kimia IPB. Terima kasih kepada segenap staf dan pegawai di Laboratorium Terpadu IPB dan Departemen kimia yang telah memberikan dukungannya sehingga penulis dapat menyelesaikan studi di Sekolah Pascasarjana IPB.
Bogor, September 2011
Penulis dilahirkan di Bogor pada tanggal 25 Mei 1964 dari pasangan Bapak H. Muhamad Sidik dan Ibu (almh) R. Nani Surjani. Penulis merupakan anak ketiga dari sembilan bersaudara
INFRAMERAH
MUHAMAD FARID
Tesis
sebagai salah satu syarat untuk memperoleh gelar Magister Sains pada
Program Studi Kimia
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
DAFTAR ISI
Modifikasi Struktural Poli (akrilamida) ... 9
Spektrometer Inframerah Transformasi Fourier ... 11
Kuadrat Terkecil Parsial (Partial Least Square) ... 12
METODE ... 14
Bahan Dan Peralatan ... 14
Preparasi Onggok ... 15
Pencangkokan dan Penautan Silang Akrilamida ... 15
Saponifikasi hasil pencangkokan dan penautan silang ... 15
Penentuan Kadar Nitrogen Kjeldahl ... 16
Standarisasi Larutan HCl 0,1N ... 16
Perhitungan Redemen Grafting dan Efisiensi Grafting ... 17
Pengambilan Spektrum Inframerah Transformasi Fourier ... 17
Pengolahan data ... 18
HASIL DAN PEMBAHASAN ... 19
Hasil pencangkokan dan penautan silang... 19
Hasil analisis kadar nitrogen Kjeldahl produk pencangkokan dan penautan silang ... 19 Hasil pengukuran serapan inframerah produk pencangkokan dan penautan silang ... 20 PLS Pengukuran Serapan inframerah produk pencangkokan dan penautan silang ... 22 Hasil saponifikasi ... 24
Hasil analisis kadar nitrogen Kjeldahl produk saponifikasi ... 24
Hasil pengukuran serapan inframerah produk saponifikasi ... 24
SIMPULAN ... 28
DAFTAR PUSTAKA ... 29
LAMPIRAN ... 33
DAFTAR TABEL
Halaman 1 Komposisi kimia singkong dan onggok tapioka ... 32 Kadar nitrogen produk sintesis ... 19
3 Kadar nitrogen produk Saponifikasi ... 24
DAFTAR GAMBAR
Halaman 1 Pola percabangan polisakarida ... 42 Struktur molekul amilosa ... 5
3 Struktur molekul amilopektin ... 5
4 Struktur molekul selulosa ... 6
5 (A). Diagram skematik (I) fisisosorpsi, (II) “mencangkok untuk”, (III) “mencangkok dari”. (B). Diagram skematik (I) “tautan silang antarmolekul” dan (II) “tautan silang intramolekular” ... 9 6 Hidrolisis basa dan asam poliakrilamid ... 10
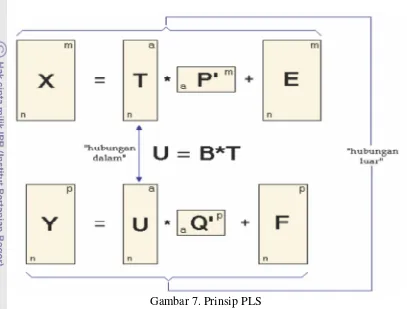
7 Prinsip PLS ... 13
8 Spektrum inframerah hasil pencangkokan dan penautan silang ... 20
9 Spektrum inframerah hasil pencangkokan dan penautan silang
akrilamida pada tepung singkong dan produk saponifikasinya ... 21
10 Spektrum inframerah hasil pencangkokan dan penautan silang
akrilamida pada tepung singkong dengan berbagai perbandingan ... 21
11 Plot antara kadar nitrogen aktual dan hasil prediksi model Manipulasi produk pencangkokan dan penautan silang ...
23
12 Regresi linier kadar nitrogen aktual dan hasil prediksi model manipulasi produk pencangkokan dan penautan silang ...
23
13 Spektrum inframerah hasil saponifikasi ... 25
14 Plot kadar nitrogen aktual dan hasil prediksi pada berbagai produk saponifikasi...
26
15 Regresi linier kadar nitrogen aktual dan hasil prediksi model manipulasi produk saponifikasi...
3 Saponifikasi Graftized Crosslinked acrylamide Onggok (Nakason et al 2010) ...
PENDAHULUAN
Latar Belakang
Indonesia sebagai negara agraris pada tahun 2008 menghasilkan singkong
(Manihot esculenta) sebesar 21.593.100 MT dengan nilai US$ 1.524.288.000, dan merupakan negara peringkat 3 dunia penghasil singkong (FAOSTAT). Salah satu
produk turunan singkong adalah tepung tapioka. Proses produksi tapioka dari
singkong akan menghasilkan produk samping yang disebut onggok. Setiap 1 ton
singkong akan menghasilkan 160 kg onggok (Dit PPHP DitJen BPHH Deptan,
2005; Bank Indonesia. 2005). Onggok mempunyai nilai jual rendah (Rp. 1800,- –
2300,-/kg). Salah satu kandungan utama dalam onggok adalah karbohidrat, dalam
bentuk selulosa dan pati. Onggok selama ini digunakan sebagai pengisi saos,
pembuatan obat nyamuk bakar, dan salah satu komponen pakan ternak. Sebagai
pakan ternak pun, onggok tidak bisa langsung digunakan, melainkan harus
difermentasi terlebih dahulu. Untuk meningkatkan nilai tambah dari onggok,
maka harus dilakukan proses modifikasi kandungan utamanya sehingga diperoleh
turunan yang mempunyai nilai jual tinggi.
Lanthong et al. (2006) dan Nakason et al. (2010) telah melakukan modifikasi tepung singkong (tepung tapioka) melalui reaksi pencangkokan dan
penautanulang akrilamida membentuk super adsorben yang ramah lingkungan.
Nur et al. (2011) melakukan riset yang analog dengan bahan baku onggok. Hasil penelitiannya menunjukkan bahwa keberhasilan proses pencangkokan dan
penautan ulang bisa dipantau dengan menentukan kandungan nitrogen dalam
produk reaksi. Kandungan nitrogen ditentukan menggunakan metode klasik yaitu
Kjeldahl.
Teknik pengukuran spektrum inframerah dekat (Near infrared, NIR) telah banyak digunakan dalam analisis kuatitatif nondestruktif yang cepat. Dengan
mengukur spekrum inframerah sejumlah tertentu bahan yang analog yang sudah
diketahui kadar analatnya dengan metoda lain, kemudian dilakukan pengolahan
data Partial Least Square (PLS) maka dapat dibuat model kalibrasi hubungan antara serapan pada bilangan gelombang tertentu serta kandungan analat yang
Tujuan Penelitian
Penelitian ini bertujuan mengkuantifikasi hubungan antara besaran serapan
inframerah pada bilangan gelombang karakteristik gugus fungsi amida produk
penautan ulang dan saponifikasi dengan kandungan nitrogen menggunakan teknik
analisis statistik PLS.
Hipotesis
Serapan inframerah pada daerah bilangan gelombang karakteristik gugus
fungsi amida (1450 – 1780 cm–1 dan 3030 – 3450 cm–1) dari hasil pencangkokan
dan penautansilang akrilamida serta produk turunan hasil saponifikasinya
TINJAUAN PUSTAKA
Onggok Tapioka
Onggok merupakan hasil samping proses produksi tapioka dari singkong.
Proses tersebut merupakan proses esktraksi pati dari singkong, sehingga
kandungan karbohidrat yang tidak larut (serat kasar) akan meningkat pada
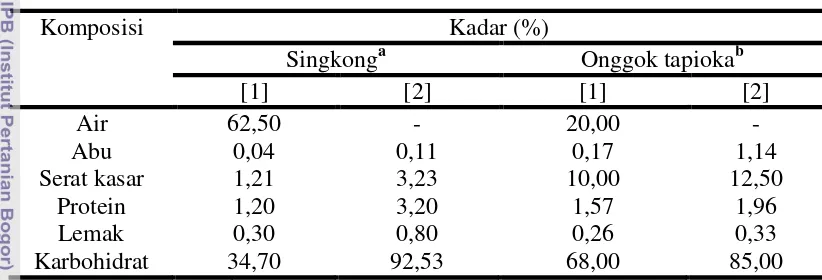
onggok. Hasil analisis kimia pada singkong dan onggok tertera pada Tabel 1.
Tabel 1 Komposisi kimia singkong dan onggok tapioka
Komposisi Kadar (%)
tidak perlu dilakukan proses deproteinasi dan pengawalemakan terlebih dahulu
sebelum dilakukan modifikasi.
Polisakarida
Polisakarida dengan rumus umum (C6H10O5)n adalah polimer alami yang
bila dihidrolisis menghasilkan banyak molekul monosakarida. Dalam nomenklatur
kimia, polisakarida merupakan glikan dan sebagai terdiri dari unit glikosil.
Polisakarida dibagi lagi menjadi 2 golongan, yaitu homopolisakarida dan
heteropolisakarida. Homopolisakarida bila dihidrolisis hanya menghasilkan satu
jenis monosakarida, misalnya pati dan selulosa. Heteropolisakarida bila
menghasilkan lebih dari satu jenis mono-sakarida, misalnya inulin (BeMiller
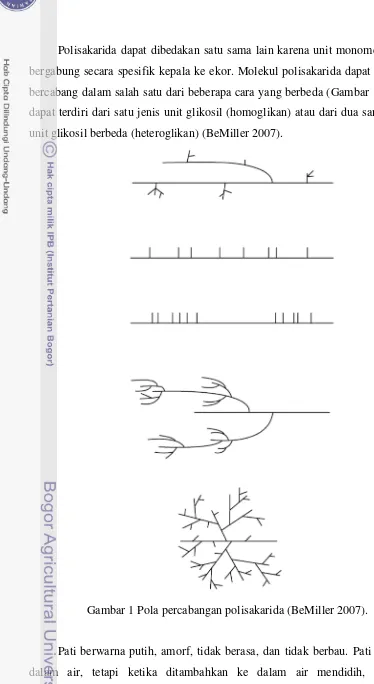
Polisakarida dapat dibedakan satu sama lain karena unit monomer individu
bergabung secara spesifik kepala ke ekor. Molekul polisakarida dapat linear atau
bercabang dalam salah satu dari beberapa cara yang berbeda (Gambar 1). Mereka
dapat terdiri dari satu jenis unit glikosil (homoglikan) atau dari dua sampai enam
unit glikosil berbeda (heteroglikan) (BeMiller 2007).
Gambar 1 Pola percabangan polisakarida (BeMiller 2007).
Pati berwarna putih, amorf, tidak berasa, dan tidak berbau. Pati tidak larut
dalam air, tetapi ketika ditambahkan ke dalam air mendidih, butirannya
dipanaskan pada suhu 200°C–250°C akan membentuk dekstrin. Pada suhu yang lebih tinggi akan mengalami pengarangan. Pati bila dididihkan dengan asam encer
akan menghasilkan glukosa sebagai produk utama. Pati dapat dibagi menjadi 2
struktur umum yaitu struktur linear amilosa dan struktur bercabang amilopektin.
Amilosa bereaksi dengan larutan iod encer akan menghasilkan warna biru, yang
menghilang bila dipanaskan, dan timbul kembali bila didinginkan. Amilopektin,
bereaksi dengan larutan iod encer menghasilkan warna coklat. Berat molekul
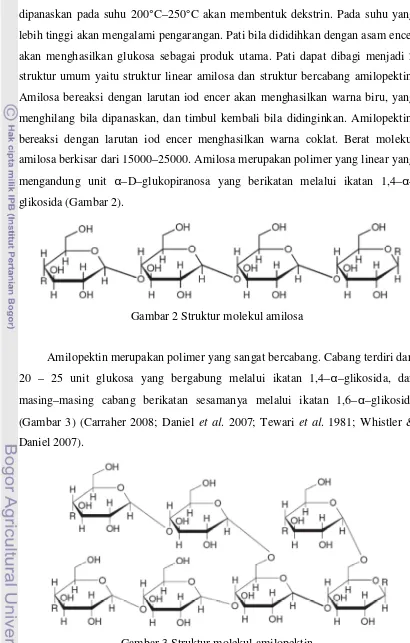
amilosa berkisar dari 15000–25000. Amilosa merupakan polimer yang linear yang
mengandung unit α–D–glukopiranosa yang berikatan melalui ikatan 1,4–α–
glikosida (Gambar 2).
Gambar 2 Struktur molekul amilosa
Amilopektin merupakan polimer yang sangat bercabang. Cabang terdiri dari 20 – 25 unit glukosa yang bergabung melalui ikatan 1,4–α–glikosida, dan masing–masing cabang berikatan sesamanya melalui ikatan 1,6–α–glikosida (Gambar 3) (Carraher 2008; Daniel et al. 2007; Tewari et al. 1981; Whistler & Daniel 2007).
Selulosa berupa padatan tidak berwarna, tidak larut dalam air, tapi larut
dalam larutan tembaga (II) hidroksida amoniakal (Pereaksi Schweitzer). Selulosa
juga larut dalam larutan seng klorida dalam asam klorida. Selulosa akan larut bila
direaksikan dengan asam sulfat pekat. Bila larutan ini diencerkan akan
menghasilkan bahan seperti pati, amiloid. Bila selulosa dididihkan dengan asam
sulfat encer, akan terhidrolisis sempurna menjadi glukosa. Bila selulosa
direaksikan dengan larutan NaOH 20% selulosa akan menjadi halus dan berkilau.
Selulosa mempunyai unit glukosa, yang tiga gugus hidroksinya bebas untuk
diesterkan. Selulosa bereaksi dengan asam nitrat pekat dan asam sulfat pekat
membentuk campuran selulosa mono, di dan trinitrat. Selulosa bereaksi dengan
campuran anhidrida asetat dan asam asetat glasial membentuk campuran selulosa
mono, di dan triasetat (Carraher 2008; French et al. 2007; Krässig et al. 2004; Tewari et al. 1981).
Selulosa bila dihidrolisis sempurna akan menghasilkan glukosa dalam
bentuk β–D–glukopiranosa sebagai produk utama. Selulosa merupakan polimer
linear dengan unit β–D– glukopiranosa yang berikatan melalui 1,4–β–glikosida
(Gambar 4) (Carraher 2008; French et al. 2007; Krässig et al. 2004; Tewari et al.
1981).
Gambar 4 Struktur molekul selulosa
Akrilamida
Akrilamida (CH2=CHCONH2, 2–propenamida, CAS No. 79–06–1), padatan
berwarna putih yang stabil pada suhu ambien hingga suhu titik lelehnya (tanpa
ada cahaya). Diatas suhu titik lelehnya, akrilamida segera mengalami reaksi
polimerisasi adisi sambil membebaskan panas yang besar. Akrilamida merupakan
monomer bifungsional, memiliki gugus alkena (CH2=CH–) dan amida (–CONH2),
menunjukkan karakter asam lemah dan basa lemah. Gugus penarik elektron amida
mengaktivasi ikatan rangkap, dan segera bereaksi dengan pereaksi nukleofilik.
Nu:H + CH2=CHCONH2 → Nu–CH2CH2CONH2
Hadirnya basa memungkinkan penambahan merkaptan, sulfida, keton,
nitroalkana, dan alkohol ke akrilamida. Akrilamida bereaksi dengan alkohol
polimerik seperti poli (vinil alkohol), selulosa, dan pati. Dalam kondisi basa hasil
reaksi hidrolisis parsial amida berupa campuran karbamoiletil dan karboksietil.
Sebagian besar akrilamida (94%) digunakan untuk membuat poliakrilamida.
Poliakrilamida digunakan sebagai pereaksi pengolahan air (56%), produksi pulp
dan kertas (24%), pemrosesan mineral (10%), pembuatan monomer N–
metilakrilamid dan monomer lainnya (6%), dan lain–lain (4%) (Habermann,
2007).
Modifikasi Polimer
Meskipun jenis polimer sangat banyak, kadang-kadang mereka tidak dapat
memenuhi suatu keperluan. Modifikasi pada polimer sangat penting karena akan
memperluas ruang lingkup aplikasi. Ada dua pendekatan utama, yaitu
mengkonstruksi molekul baru dengan mengatur komposisi molekular hingga
dicapai sifat yang diinginkan, atau modifikasi polimer yang sudah ada
(Bhattacharya & Ray 2009; Carraher 2008; Ebewele 2000; Hamielec & Tobita
2005; Swift et al. 1997).
Terdapat 4 teknik modifikasi polimer, yaitu grafting (cangkok), crosslinking
(ikatan silang), blending (campuran), dan pembentukan komposit. Kopolimer cangkok dilakukan dengan cara mencangkokkan polimer lain yang berbeda
jenisnya dengan polimer kerangka utamanya. Penautan silang diperoleh bila
digunakan monomer yang memiliki dua atau lebih gugus fungsi yang dapat
membentuk ikatan. Campuran homogen makroskopik dari dua atau lebih polimer
yang berbeda dapat didefinisikan sebagai campuran polimer. Campuran polimer
ini menggabungkan sifat yang berguna dari semua konstituen dan merupakan
sarana untuk memproduksi bahan-bahan baru. Komposit dibuat dengan
menggabungkan dua atau lebih bahan yang berbeda sedemikian rupa sehingga
Komponen-komponen ini tidak mengambil bagian dalam reaksi kimia dan
juga tidak larut atau benar-benar bergabung dengan satu sama lain. Meskipun
demikian, mereka tetap sangat terikat bersama-sama sambil mempertahankan
sebuah antarmuka antara satu sama lain dan memberikan kinerja yang lebih baik.
Dalam komposit polimer, polimer yang merupakan komponen utama
mengandung bahan penguat yang berbeda seperti serat kaca, serat karbon, silika,
atau mika sebagai komponen kecil. Hasil penguatan berupa meningkatnya kuat
regang, kelenturan, kompresi, kekuatan dampak, kekakuan, ukuran stabilitas,
ketahanan api, tahan korosi, sifat listrik, dan kemudahan diproses. Komposit
polimer memiliki aplikasi serbaguna dari sektor konstruksi untuk bahan
komoditas (Bhattacharya & Ray 2009; Carraher 2008; Ebewele 2000; Hamielec &
Tobita 2005; Swift et al. 1997).
Asosiasi monomer dan polimer dijelaskan dengan cara "fisisosorpsi,"
"mencangkok" dan "mentaut-silang. Istilah fisisorpsi berkaitan dengan gaya tarik
menarik fisik. Proses fisisorpsi dapat balik, dan dicapai dengan ujung polimer
terfungsionalisasi pada permukaan padat atau perakitan mandiri polimer
surfaktan. "Mencangkok" dapat digambarkan sebagai proses lampiran kovalen
dan tidak dapat balik. Pencangkokan dapat dilakukan dengan cara pendekatan
"mencangkok untuk" atau "mencangkok dari". Dalam pendekatan "mencangkok
untuk", monomer terfungsionalisasi bereaksi dengan polimer kerangka utama
untuk membentuk satu cangkokkan. Di sisi lain, "mencangkok dari" dicapai
dengan memperlakukan substrat dengan metode tertentu untuk menghasilkan
inisiator yang diimobilisasi lalu diikuti dengan polimerisasi. Pencangkokan
polimer densitas tinggi dapat dilakukan dengan menggunakan teknik ini.
Presentasi skematis dari semua proses yang digambarkan dalam Gambar 5 (A).
"tautan silang" adalah asosiasi dari polimer melalui ikatan kimia. Dalam
Gambar 5 (A). Diagram skematik (I) fisisosorpsi, (II) “mencangkok untuk”, (III) “mencangkok dari”. (B). Diagram skematik (I) “tautan silang antarmolekul” dan (II) “tautan silang intramolekular” (Bhattacharya & Ray 2009)
Modifikasi Struktural Poli (akrilamida)
Poli (akrilamida) (PAM) adalah polimer organik yang relatif stabil. Namun,
PAM dapat terdegradasi (misalnya, penurunan berat molekul) dalam kondisi
tertentu. Fungsi amida secara alamiah bersifat asam dan mampu menjalani
sebagian besar reaksi kimia amida primer. Akibatnya polimer akrilamida dapat
difungsionalisasikan melalui pasca-polimerisasi. Untuk mendapatkan turunan
anionik, PAM dapat dihidrolisis dengan basa. PAM ter-sulfometilasi dapat dibuat
dengan mereaksikan PAM dengan formaldehida dan natrium bisulfit dalam
suasana asam. PAM bereaksi dengan hidroksilamin dalam kondisi basa
menghasilkan PAM hidroksamat. Sebagai contoh dari turunan kationik,
Mannich-dasar PAM dapat diperoleh dengan mereaksikan PAM dengan formaldehida dan
dimetilamin untuk menghasilkan polimer kationik bermuatan tergantung pH.
Sebagai contoh dari turunan nonionik, PAM dapat bereaksi dengan glioksal
menghasilkan fungsi liontin aldehida. Poliakrilamida yang diubah secara
struktural ini merupakan produk komersial yang sukses (Huang et al. 2007; Swift
Hidrolisis dari poli (akrilamida) berlangsung lancar melalui berbagai pH.
Pada pH basa, kinetika reaksi tiga konstanta telah diuraikan, k0, k1, dan k2.
Subskrip mencirikan jumlah gugus karboksilat tetangga sebelah gugus amida
yang terhidrolisis. Para k0 laju konstan adalah untuk tidak ada tetangga
karboksilat, k1 adalah untuk satu tetangga karboksilat, dan k2 untuk dua tetangga
karboksilat. Bukti tidak langsung telah menunjukkan bahwa k0 > k1 > k2. Dalam
kondisi basa, laju hidrolisis poli (akrilamida) menurun dengan konversi
meningkat. Tolakan elektrostatik dari meningkatnya jumlah gugus karboksilat
dalam polimer kerangka utama menghalangi ion hidroksil mendekat. Akibatnya
hidrolisis lebih lanjut akan sangat sukar. Hanya sekitar 80% dari kelompok amida
dapat dihidrolisis dengan ion hidroksida berlebih bahkan pada suhu yang tinggi
(Huang et al. 2007).
Hidrolisis dari poli (akrilamida) berlangsung perlahan dalam kondisi asam.
Kelompok-kelompok asam karboksilat yang tidak terdisosiasi terprotonasi
merupakan spesies netral dalam kondisi ini. Katalisis intramolekul dari gugus –
CO2H terdisosiasi pada pH rendah diduga sebagai mekanisme utama. Struktur
imida diduga sebagai bentuk antara pada hidrolisis pH rendah poli (akrilamida),
dan menghasilkan penghalang pendek gugus karboksil yang terdistribusi
sepanjang rantai polimer (Gambar 6). Untuk saat ini, telah ada aplikasi terbatas
dari struktur kopolimer blok ini, dan yang mempunyai berat molekul tinggi belum
dikomersialkan (Huang et al. 2007; Nakason et al. 2010).
Spektrometer Inframerah Transformasi Fourier
Radiasi IR berada pada kisaran panjang gelombang 0.78 – 1000 µm atau
bilangan gelombang 12800 – 10 cm–1. Spektrumnya terbagi atas radiasi
inframerah dekat (12 800 – 4000 cm–1), menengah (4000 – 200 cm–1), dan jauh
(200 – 10 cm–1). Daerah spektrum yang paling banyak digunakan untuk berbagai
keperluan praktis seperti analisis dalam bidang industri, bahan pertanian, dan
kendali mutu adalah pada bilangan gelombang 4000 – 670 cm–1 atau daerah IR
tengah (Rouessac & Rouessac 2007; Skoog et al. 1998).
Energi radiasi IR digunakan terbatas hanya pada transisi molekul yang
melibatkan vibrasi dan rotasi. Efek dari vibrasi ini menyebabkan perubahan
momen dipol. Radiasi medan listrik yang berubah-ubah akan berinteraksi dengan
molekul dan akan menyebabkan perubahan amplitudo dari salah satu gerakan
molekul. Dalam padatan dan cairan berotasi secara terbatas sedangkan dalam gas
tidak). Perwujudan interaksi tersebut menghasilkan serapan yang khas dari setiap
komponen atau struktur molekul. Serapan grup fungsional berada pada kisaran
bilangan gelombang 4000 – 1500 cm–1 sedangkan fenomena intra-molekular yang
bersifat sangat spesifik untuk setiap materi antara 1500 cm–1 – 400 cm–1 (daerah
sidik jari) (Khopkar 2002; Rouessac & Rouessac 2007).
Berbeda dengan spektrometer klasik, FTIR tidak mengukur panjang
gelombang satu demi satu, melainkan dapat mengukur intensitas transmitans pada
berbagai panjang gelombang secara serempak. Pada FTIR, monokromator
digantikan dengan interferometer. Interferometer ini mengatur intensitas sumber
sinar inframerah dengan cara mengubah posisi cermin pemantul yang
memantulkan sinar dari sumber sinar ke contoh. Jadi, keberadaan interferometer
membuat spektrometer mampu mengukur semua frekuensi optik secara serempak
dengan mengatur intensitas dari semua frekuensi tunggal sebelum sinyal
mencapai detektor. Hasil scanning interferometer yang berupa interferogram (pengaluran antara intensitas dan posisi cermin) ini tidak dapat diinterpretasikan
dalam bentuk aslinya. Proses matematika transformasi fourier akan mengubah
interferogram menjadi spektrum antara intensitas dan frekuensi (Skoog et al.
Analisis kuantitatif spektrum IR rumit karena adanya tumpang tindih
spektrum serapan dari molekul-molekul dalam sampel. Untuk dapat
mengekstraksi informasi dari data spektrum IR yang rumit tersebut, diperlukan
suatu metode kemometrik berupa analisis multivariat (Stchur et al. 2002).
Analisis multivariat menyediakan metode untuk mengurangi data berukuran
besar yang diperoleh dari instrumen, seperti spektrofotometer. Metode kalibrasi
multivariat dapat berupa multiple linear regression, principal component
regression, PLS, dan artificial neural network (ANN) (Brereton 2003).
Kuadrat Terkecil Parsial (Partial Least Square)
Kuadrat terkecil parsial digunakan untuk memperkirakan serangkaian
peubah tidak bebas (respons) dari peubah bebas (prediktor) yang jumlahnya
sangat banyak, memiliki struktur sistematik linear atau nonlinear, dengan atau
tanpa data yang hilang, dan memiliki kolinearitas yang tinggi (Hervé 2007).
Metode ini membentuk model dari peubah-peubah yang ada untuk membentuk
serangkaian respons dengan menggunakan regresi kuadrat terkecil dalam bentuk
matriks (Lindblom 2004).
Bila jumlah prediktor X jauh lebih besar dibandingkan dengan jumlah
pengamatan Y, pendekatan regresi akan sulit diterapkan karena adanya
multikolinearitas pada data. Permasalahan ini diatasi dengan menentukan
komponen utama dari matriks X, yang selanjutnya digunakan sebagai regresor
pada Y. Peubah-peubah X yang memiliki korelasi yang tinggi dengan peubah
respons diberi bobot lebih karena akan lebih efektif dalam perkiraan (Miller &
Miller 2005).
Parameter-parameter dalam PLS sebagai metode kalibrasi adalah factors,
loadings, dan scores. Model PLS berdasar pada komponen utama dari data
independen X dan data dependen Y. Inti dari PLS adalah untuk menghitung nilai
(scores) dari matriks X dan Y dan untuk membuat model regresi antara nilai-nilai
tersebut (Dieterle 2003).
Gambar 7 menunjukkan bahwa matriks X diuraikan menjadi matriks T
(matriks scores), matriks P′ (matriks loading) dan matriks error E, sedangkan
matriks Y diuraikan menjadi U dan Q dan error F. Kedua persamaan ini disebut
dan Q mendekati konsentrasi sebenarnya. Tujuan dari algoritma PLS adalah untuk
meminimumkan F dengan terus menjaga korelasi antara X dan Y dalam
‘hubungan dalam’ U=BT (Fundamental Of Statistic).
METODE
Bahan Dan Peralatan
Bahan yang digunakan yaitu limbah padat tapioka (onggok tapioka) dari
sekitar Kecamatan Bogor Utara, akuades, gas nitrogen [N2, berkemurnian tinggi
(high purity), Brin's Oxygen Company Gases Indonesia (BOC Gases Indonesia)], akrilamida [AA, CH2=CHCONH2, CAS No. 79–06–1, Merck], amonium persulfat
[APS, (NH4)2S2O8, CAS No. 7727–54–0, Merck), N,N–Metilenediakrilamid
Merck),asam borat (H3BO3, CAS No. 10043–35–3, Merck), dinatrium tetraborat
dekahidrat (boraks, Na2B4O7. 10 H2O; CAS No. 1303–96–4, Merck).
Alat-alat yang digunakan ialah neraca dengan ketelitian 0,1 mg, neraca
dengan ketelitian 0,01 g, labu leher tunggal, labu leher dua, labu leher tiga, mantel
pemanas, lempeng pemanas berpengaduk magnet (hotplate with magnetic stirer),
overheadstirrer, kondensor, termometer, corong tambah cairan dengan ekualisasi tekanan, gelas ukur 100 mL, gelas piala 1000 mL, gelas piala 2000 mL, gelas
piala PP 1000 mL, gelas piala PP 2000 mL, corong tambah padatan dengan
ekulisasi tekanan, klem dan statif, sistem pendingin sirkular, kertas timbang,
spatula, sendok PP, pipet Mohr 25 mL, labu Kjeldahl 100 mL dan 500 mL,
pembakar Bunsen, labu ukur 100 mL & 1000 mL, botol semprot plastik 500
mL, peralatan destilasi Kjeldahl, Erlenmeyer 250 mL, buret 50 mL, corong kaca,
batang pengaduk, oven (Memert), dan Spektrometer FTIR Shimadzu Prestige
Preparasi Onggok
Onggok tapioka kasar dicuci dengan air sampai air hasil pencucian jernih
kemudian dikering-udarakan. Onggok tapioka bersih dan kering ini dihaluskan
hingga lolos ayakan 100 mesh.
Pencangkokan dan Penautan Silang Akrilamida
Sintesis pencangkokan dan panautan silang akrilamida dilakukan dengan
menvariasikan jumlah monomer akrilamida (15 – 30 g), onggok (0 – 15 g), penaut
ulang (8 – 25 mg) dan inisiator (160 – 330 mg), dan diberi kode “CGA01” hingga
“CGA34”. Kondisi sintesis lainnya dibuat sama.
Onggok tapioka bersih, kering dan halus ditimbang dan dimasukkan ke
dalam di dalam labu leher tiga yang telah dilengkapi dengan kondensor, sistem
embusan gas nitrogen, termometer, dan overhead stirrer. Ke dalam labu dimasukkan 150 mL air, kemudian diaduk dan dipanaskan hingga suhu 95°C. Aliran gas nitrogen dihidupkan selama 30 menit.
Selanjutnya suhu diturunkan menjadi 60°C−65°C, lalu ditambahkan sejumlah inisiator APS dalam 12,5 mL air sambil diaduk selama 15 menit.
Kemudian ditambahkan 200 mL larutan campuran AA dan MBA secara perlahan dalam waktu 20 – 30 menit, dan selama penambahan suhu dijaga minimal 55°C sambil tetap diaduk. Setelah penambahan selesai, suhu reaksi dinaikkan menjadi 70°C dan direaksikan selama 3 jam.
Produk yang dihasilkan diendapkan dengan metanol dan etanol. Setelah itu produk direfluks dengan aseton selama 1 jam. Lalu dikeringkan dengan suhu 60°C hingga bobot produk konstan. Produk kering digiling dan disaring hingga
terbentuk partikel kecil berukuran 80-100 mesh. Produk ini dinamakan Graftized Crosslinked Onggok. Bagan alir tahapan preparasi dan pencangkokan dan penautan silang akrilamida disajikan pada Lampiran 2.
Saponifikasi hasil pencangkokan dan penautan silang
Tidak semua hasil pencangkokan dan penautan silang disaponifikasi.
Sebanyak 13 produk pencangkokan dan penautan silang akrilamida selanjutnya di
Sebanyak 40 gram Graftized Crosslinked Onggok, dimasukkan ke dalam labu 500 mL. Ke dalam labu ditambahkan 100 mL larutan NaOH 1M dan 100 mL air suling dan direfluks pada suhu 90°C pada beberapa kisaran waktu. Hasil refluks kemudian dinetralkan dengan larutan HCl 1 M, lalu dikoagulasi dan diendapkan dengan metanol. Hasil saponifikasi dikeringkan pada suhu 60°C, lalu digiling dan disaring hingga terbentuk partikel lolos ayakan 80 mesh. Produk ini
dinamakan Saponified Graftized Crosslinked Onggok. Bagan alir tahapan saponifikasi hasil pencangkokan dan penautan silang disajikan pada Lampiran 3.
Penentuan Kadar Nitrogen Kjeldahl (Kenkel, 2003; Carter & Gregorich, 2005;
Pansu & Gautheyrou, 2005; Sulaeman et al. 2005).
Ditimbang menggunakan neraca analitik (ketelitian 0,1 mg) 0,1 g contoh,
dan kemudian dimasukkan ke dalam labu Kjeldahl 100 mL. Ditambahkan 2 g
campuran selen dan 10 mL H2SO4 pekat. Dipanaskan di atas api atau pembakar
Bunsen sampai mendidih dan larutan menjadi jernih kehijau-hijauan. Dibiarkan
hingga mendingin di udara terbuka. Disiapkan alat destilasi untuk penetapan
nitrogen. Pada bagian penampung, disiapkan 20 mL larutan asam borat 2%
(selama proses penyulingan, ujung pipa kondensor harus selalu tercelup dalam
larutan borat). Dipindahkan larutan hasil destruksi ke labu Kjeldahl 500 mL, dan
dibilas dengan 150 mL air suling dan 50 mL NaOH 40%, segera dihubungkan
dengan alat destilasi Kjeldahl. Dijalankan proses destilasi hingga volume larutan
dalam penampung detilasi sekitar 100 mL. Dientikan proses destilasi. Diilas
bagian dalam kondensor dan ujung pipa dengan air suling. Dititar hasil destilasi
dengan larutan HCl 0,1 N hingga titik akhir tercapai (warna larutan berubah dari
hijau menjadi merah muda). Dikerjakan penetapan blanko.
Kadar Nitrogen (%)
=
VB = Volume HCl 0,1 N yang dipergunakan pada penitaran blanko (mL )
NHCl = Normalitas HCl
Standarisasi Larutan HCl 0,1N (Jeffery et al. 1989)
Ditimbang menggunakan neraca analitik (ketelitian 0,1 mg) 0,2 g boraks
(dinatrium tetraborat dekahidrat, Na2B4O7. 10 H2O; CAS No. 1303–96–4, Mr =
381,37). Dilarutkan ke dalam erlenmeyer 100 mL . Ditambahkan 2 tetes indikator
merah metil 0,1%, dihomogenkan. Dititar larutan ini dengan larutan HCl 0,1 N
sampai titik akhir tercapai yang ditandai dengan perubahan warna dari kuning ke
merah. Dicatat volume HCl yang terpakai. Dihitung normalitas HCl hingga 4
VS = Volume larutan HCl yang digunakan untuk standarisasi
Titrasi diualangi 2 x, dan hasilnya dirata-ratakan.
Perhitungan rendemen grafting dan efisiensi grafting
Rendemen dan efisiensi grafting dihitung menurut Nakason et al (2010), yaitu:
Rendemen grafting =
100× %N100 × CH2=CHCONH2N
100- %N100 × CH2=CHCONH2N ×100
Efisiensi grafting = Rendemen graftingberat monomer berat onggok
Pengambilan Spektrum Inframerah Transformasi Fourier
Serbuk halus onggok tapioka yang bersih, kering, dan halus, Graftized Crosslinked Onggok, dan Saponified Graftized Crosslinked Onggok diukur serapan inframerahnya menggunakan Spektrometer Shimadzu IR Prestige 21.
Pengolahan data
Data mentah hubungan antara bilangan gelombang (ν, cm–1) vs transmitas (%T) dengan piranti lunak IRsolution diolah terlebih dahulu dengan manipulasi Kubelka-Munk (KM), kombinasi Kubelka-Munk dengan garis dasar nol
(KM+BL), kombinasi Kubelka-Munk dengan Normalisasi (KM+Norm),
kombinasi garis dasar nol dengan Kubelka-Munk (BL+KM), kombinasi garis
dasar nol (dengan koreksi Lambert Beer) dengan Kubelka-Munk (BL+LB+KM),
dan kombinasi Normalisasi dengan Kubelka-Munk (Norm+KM). Data mentah
tidak dimanipulasi dengan koreksi atmosferik. Data hasil manipulasi selanjutnya
diekspor kedalam bentuk format notepad (*.txt). Data bentuk *.txt (notepad), untuk selanjutnya dipindahkan ke format *.xls (Microsoft excel 2010).
Data FTIR (bilangan gelombang (ν, cm–1) vs absorbans hasil manipulasi) bersama data kadar nitrogen dilakukan analisis PLS menggunakan perangkat
lunak Minitab 14 sistem operasi Windows 7. Analisis PLS dilakukan untuk
pembentukan model prediksi kadar nitrogen dilakukan oleh PLS dengan
melibatkan variabel “x” (absorbans hasil pengukuran FTIR) dan variabel “y”
HASIL DAN PEMBAHASAN
Hasil pencangkokan dan penautan silang
Jumlah produk pencangkokan dan penautan silang yang diperoleh sebanyak
34 prototipe, yang diberi kode “CGA01” hingga “CGA34”, berupa padatan
berwarna putih.
Hasil analisis kadar nitrogen Kjeldahl produk pencangkokan dan penautan
silang
Keberhasilan sintesis ditunjukkan dengan hadirnya nitrogen pada produk.
Kandungan nitrogen pada produk pencangkokan dan penautan silang ditetapkan
secara Kjeldahl titrimetri, dan disajikan pada Tabel 2. Produk pencangkokan dan
penautan silang mengandung nitrogen 5,84% hingga 16,12% yang ekuivalen
dengan efisiensi grafting 7,99% hingga 47,15%.
Tabel 2. Kadar nitrogen produk sintesis
Hasil pengukuran serapan inframerah produk pencangkokan dan penautan
silang
Produk pencangkokan dan penautan silang diukur spektrum inframerahnya.
Hasilnya disajikan pada Gambar 8.
Gambar 8. Spektrum inframerah hasil pencangkokan dan penautan silang
Pada semua spektrum terlihat serapan pada bilangan gelombang 3360 –
3340 cm–1 (regangan NH2 amida primer), 3190 – 3170 cm–1 (regangan simetrik
NH2 amida), 1680 – 1660 cm–1 (regangan C=O amida primer), 1650 – 1620 cm–1
(tekuk NH2 amida primer) dan 1560 – 1530 cm–1 (regangan C–N) (Stuart, 2004).
Penelitian yang dilakukan oleh Nakasone (2010) juga menunjukan hasil
yang serupa baik untuk produk pencangkokan dan penautan silang serta hasil
Gambar 9. Spektrum inframerah hasil pencangkokan dan penautan silang akrilamida pada tepung singkong dan produk saponifikasinya
Nakason (2010) juga menunjukan bahwa perbandingan reaktan (akril amida
dan tepung singkong) sangat mempengaruhi intensitas spektrum inframerahnya.
Berdasarkan vibrasi molekul yang spesifik untuk amida, maka dilakukan ekstraksi
data (bilangan gelombang dan absorban) pada bilangan gelombang 1450 – 1780
cm–1 dan 3030 – 3450 cm–1 untuk selanjutnya dilakukan analisis statistik dengan
PLS menggunakan perangkat lunak Minitab 14.
PLS Pengukuran Serapan inframerah produk pencangkokan dan penautan
silang
Uji ANOVA dari PLS untuk setiap manipulasi data {Kubelka-Munk (KM),
kombinasi Munk dengan garis dasar nol (KM+BL), kombinasi
Kubelka-Munk dengan Normalisasi (KM+Norm), kombinasi garis dasar nol dengan
Kubelka-Munk (BL+KM), kombinasi garis dasar nol (dengan koreksi Lambert
Beer) dengan Kubelka-Munk (BL+LB+KM), dan kombinasi Normalisasi dengan
Kubelka-Munk (Norm+KM)} pada spektrum IR dari produk pencangkokan dan
penautan menunjukkan nilai probabilitas lebih kecil dari 0.05, yang berarti model
yang dikembangkan dengan variabel bebas (bilangan gelombang) secara
bersama-sama berpengaruh nyata terhadap kadar nitrogen pada tingkat kepercayaan 95%.
Model hasil PLS untuk setiap pengolahan memberikan nilai koefisien determinasi
(R2) berkisar 0.961-0.998, yang berarti model dengan variabel bebas bilangan
gelombang dapat memprediksi kadar nitrogen dengan baik. Hasil analisis PLS
juga memberikan informasi bahwa pengolahan data spektrum IR tidak
berpengaruh terhadap perbedaan antara prediksi dan nilai aktual dari kadar
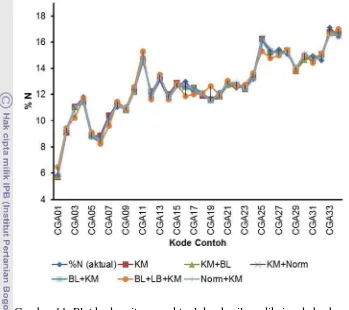
nitrogen. Plot antara kadar nitrogen aktual dan hasil prediksi model untuk produk
Gambar 11. Plot kadar nitrogen aktual dan hasil prediksi pada berbagai produk pencangkokan dan penautan silang
Hasil saponifikasi
Dari 34 produk pencangkokan dan penautan silang, 13 diantaranya
disaponifikasi menghasilkan 13 produk, yang diberi kode “CGASxx” (“xx”
merupakan nomor pencangkokan dan penautan silang awalnya), berupa padatan
berwarna kecoklatan.
Hasil analisis kadar nitrogen Kjeldahl produk saponifikasi
Keberhasilan saponifikasi ditunjukkan dengan dibebaskannya amoniak
(berbau khas) dan turunannya kadar nitrogen pada produk. Kandungan nitrogen
pada produk saponifikasi ditetapkan secara Kjeldahl titrimetri, dan disajikan pada
Tabel 3. Produk saponifikasi mengandung nitrogen 4,30% -10,30%.
Tabel 3. Kadar nitrogen produk Saponifikasi
Kode Kadar N
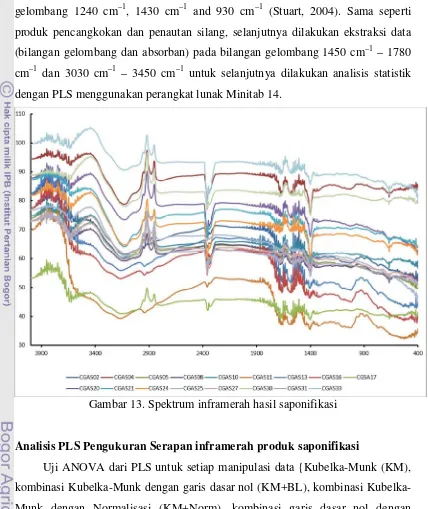
Hasil pengukuran serapan inframerah produk saponifikasi
Produk saponifikasi diukur spektrum inframerahnya. Hasilnya disajikan
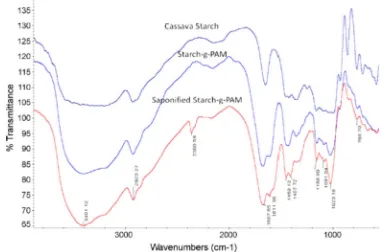
pada Gambar 15. Pada semua spektrum selain terlihat serapan karakteristik amida,
juga terlihat pita regangan yang kuat dan lebar pada kisaran bilangan gelombang
3300 – 2500 cm–1 yang khas untuk asam karboksilat. Pita regangan C=O teramati
C–O dalam bidang dan keluar bidang pita tekuk O–H berturut turtu pada bilangan
gelombang 1240 cm–1, 1430 cm–1 and 930 cm–1 (Stuart, 2004). Sama seperti
produk pencangkokan dan penautan silang, selanjutnya dilakukan ekstraksi data
(bilangan gelombang dan absorban) pada bilangan gelombang 1450 cm–1 – 1780
cm–1 dan 3030 cm–1 – 3450 cm–1 untuk selanjutnya dilakukan analisis statistik
dengan PLS menggunakan perangkat lunak Minitab 14.
Gambar 13. Spektrum inframerah hasil saponifikasi
Analisis PLS Pengukuran Serapan inframerah produk saponifikasi
Uji ANOVA dari PLS untuk setiap manipulasi data {Kubelka-Munk (KM),
kombinasi Munk dengan garis dasar nol (KM+BL), kombinasi
Kubelka-Munk dengan Normalisasi (KM+Norm), kombinasi garis dasar nol dengan
Kubelka-Munk (BL+KM), kombinasi garis dasar nol (dengan koreksi Lambert
Beer) dengan Kubelka-Munk (BL+LB+KM), dan kombinasi Normalisasi dengan
Kubelka-Munk (Norm+KM)} pada spektrum IR dari produk saponifikasi
menunjukkan nilai probabilitas lebih kecil dari 0.05, yang berarti model yang
dikembangkan dengan variabel bebas (bilangan gelombang) secara bersama-sama
hasil PLS untuk setiap pengolahan memberikan nilai koefisien determinasi (R2)
berkisar 0.961-0.998, yang berarti model dengan variabel bebas bilangan
gelombang dapat memprediksi kadar nitrogen dengan baik. Hasil analisis PLS
juga memberikan informasi bahwa pengolahan data spektrum IR tidak
berpengaruh terhadap perbedaan antara prediksi dan nilai aktuan dari kadar
nitrogen. Plot antara kadar nitrogen aktual dan hasil prediksi model untuk produk
saponifikasi disajikan pada Gambar 16 – Gambar 21.
SIMPULAN
Teknik pengukuran FTIR model reflektansi pada rentang bilangan
gelombang karakteristik gugus fungsi amida (1450 – 1780 cm–1 dan 3030 – 3450
cm–1) dapat digunakan untuk menduga kandungan nitrogen dalam produk
pencangkokan penautansilang akrilamida dan saponifikasi menggunakan teknik
analisis PLS dengan koefisien determinasi (R2) berkisar 0,96-0,998. Pengolahan
data spektrum IR yang sesuai manual tidak mempengaruhi nilai koefisien
determinasi. Model kuantitatif PLS antara besaran serapan infra merah (“x”)
dengan kadar nitrogen (“y”) berpengaruh nyata secara signifikan pada tingkat
keprcayaan 95%, sehingga model dapat digunakan untuk memprediksi kadar
DAFTAR PUSTAKA
[BI] Bank Indonesia. 2005. Pola Pembiayaan Usaha Kecil (PPUK) Pengolahan Tepung Tapioka. Jakarta: Bank Indonesia.
[Dit PPHP DitJen BPHH Deptan] Direktorat Pengolahan Dan Pemasaran Hasil Pertanian Direktorat Jenderal Bina Pengolahan Dan Pemasaran Hasil Pertanian Departemen Pertanian. 2005. Pengembangan Usaha Pengolahan Tepung Tapioka. Jakarta: Dit PPHP, DitJen BPHH, Deptan.
[IUPAC] International Union Of Pure And Applied Chemistry Organic Chemistry Division. 1995. Glossary Of Class Names Of Organic Compounds And Reactive Intermediates Based On Structure. Pure App Chem 67 (8/9): 1307 – 1365.
BeMiller JN. 2007. Carbohydrates. Di dalam: Kroschwitz JI, editor. Kirk-Othmer Encyclopedia Of Chemical Technology, Ed 5th, Vol : 4. John Wiley and Sons, Inc. hlm 696–732.
Bhattacharya A, Ray P. 2009. Intoduction. Di dalam: Bhattacharya A, Rawlins, JW, Ray P. editor. Polymer Grafting And Crosslinking. Hoboken, New Jersey: John Wiley & Sons, Inc. hlm 1–6.
Brereton RG. 2003. Chemometrics : data analysis for the laboratory and chemical plant. West Sussex: John Wiley & Sons Ltd.
Carraher, CE. 2008. Seymour/Carraher’s polymer chemistry, Ed–7th. Boca Raton, FL: CRC Taylor & Francis.
Carter MR, Gregorich EG. 2005. Soil Sampling and Methods of Analysis, Ed ke-2. Boca Raton, FL : CRC Press Taylor & Francis Group, hlm 239–250.
Chan H T , JR. 1983. Handbook of Tropical Foods. New York and Bassel: Marcel Dekker Inc.
Daniel JR, Whistler RL, Röper H, Elvers B. 2007. Starch. Di dalam: Matthias B, Jeffrey BC, Boy C, editor. Ullmann's Encyclopedia of Industrial Chemistry, Ed 7th, Vol : 34. John Wiley and Sons, Inc. hlm 1348–1372.
Dieterle F. 2003. Multianalyte Quantifications by Means of Integration of Artificial Neural Networks, Genetic Algorithms and Chemometrics for Time-Resolved Analytical Data [Disertasi]. Tubungen: Institute of Physical and Theoretical Chemistry (IPTC) at the University of Tübingen.
FAOSTAT [Production] [About] [Country by Commodity] [Selected item] [Cassava]. http://faostat.fao.org/site/339/default.aspx. [ 1 Mei 2011]
French AD., et al. 2007. Cellulose. Di dalam: Kroschwitz JI, editor. Kirk-Othmer Encyclopedia Of Chemical Technology, Ed 5th, Vol : 5. John Wiley and Sons, Inc. hlm 360–393.
Fundamental Of Statistic. http://www.statistics4u.com/fundstat_eng [ 1 Mei 2011]
Habermann CE. 2007. Acrylamide. Di dalam: Kroschwitz JI, editor. Kirk-Othmer Encyclopedia Of Chemical Technology, Ed 5th, Vol : 1. John Wiley and Sons, Inc. hlm 288–303.
Hamielec AE, Tobita H. 2005. Polymerization Processes. Di dalam: Matthias B, Jeffrey BC, Boy C, editor. Ullmann's Encyclopedia of Industrial Chemistry, Ed 7th, Vol : 34. John Wiley and Sons, Inc. hlm 1348–1372.
Herve A. 2007. Partial least square regression (PLS regression). Di dalam: Salkind NJ (editor): Encyclopedia of Measurement and Statistics. Thousand Oaks (CA): Sage. hlm. 740–744.
Huang SY, Lipp DW, Farinato RS. 2007. Acrylamide Polymers. Di Dalam: Kroschwitz JI (editor). Kirk-Othmer Encyclopedia Of Chemical Technology, Ed 5th, Vol : 10. John Wiley and Sons, Inc. hal. 304–342.
Jeffery GH, Basset J, Mendham J, Denney RC. 1989. Vogel’s Textbook Of Quantitative Chemical Analysis, Ed ke-5. London : Longman Scientific & Technical , hlm 262–268, 286–289, 300–303.
Kenkel J. 2003. Analytical Chemistry for Technicians, Ed ke-3. Boca Raton, FL : CRC Press, hlm 109–112, 136–137.
Khopkar SM. 2002. Konsep Dasar Kimia Analitik. Saptorahardjo A, penerjemah; Jakarta: UI Press. Terjemahan dari: Basic Concepts of Analytical Chemistry.
Krässig et al. 2004. Cellulose. Di dalam: Matthias B, Jeffrey BC, Boy C, editor.
Ullmann's Encyclopedia of Industrial Chemistry, Ed 7th, Vol : 7. John Wiley and Sons, Inc.
Lanthong P, Nuisin R, Kiatkamjornwong S. 2006. Graft copolymerization, characterization, and degradation of cassava starch-g-acrylamide/itaconic acid superabsorbents. Carbohydrate Polymers66 (02): 229–245.
Miller JN, Miller JC. 2005. Statistics and chemometrics for analytical chemistry. Essex : Pearson Education Limited.
Nakason et al (2010). Preparation of cassava starch-graft-polyacrylamide superabsorbents and associated composites by reactive blending. Carbohydrate Polymers81 (02): 348–357.
Nur MA, Mas’ud ZA, dan Sjahreza A. 2011. Rekayasa biopolimer hasil samping pabrik tapioka sebagai enriched soil conditioner. Program Insentif Riset, MenRisTek.
Ohara et al. 2003. Acrylic Acid and Derivatives. Di dalam: Matthias B, Jeffrey BC, Boy C, editor. Ullmann's Encyclopedia of Industrial Chemistry, Ed 7th, Vol : 1. John Wiley and Sons, Inc.
Pansu M, Gautheyrou J. 2005. Handbook of Soil Analysis : Mineralogical, Organic and Inorganic Methods. New York: Springer Berlin Heidelberg, hlm 344–349.
Rinaldy W. 1987. Pemanfaatan onggok singkong (Manihot esculenta Crantz) sebagai bahan pembuatan etanol [Tesis]. Bogor: Fakultas Teknologi Pertanian, Institut Pertanian Bogor.
Rouessac F, and Rouessac A. 2007. Chemical Analysis Modern Instrumentation Methods and Techniques. Ed-2. Chichester, West Sussex: John Wiley & Sons Ltd.
Skoog DA, Holler FJ, Nieman TA. 1998. Principles of Instrumental Analysis. Ed-5. Philadelphia: Saunders College Publishing.
Stchur P, Cleveland D, Zhou J, Michel RG. 2002. A review of recent applications of near infrared spectroscopy, and the characteristics of a novel PbS CCD array - based near infrared spectrometer. Appl Spect Rev37 (4) : 383–428.
Stuart B. 2004. Infrared Spectroscopy: Fundamentals and Applications. Philadelphia: Saunders College Publishing.
Sulaeman, Suparto, Eviati. 2005. Petunjuk Teknis Analisis Kimia Tanah, Tanaman, Air, Dan Pupuk. Bogor: Balai Penelitian Tanah, hlm 104–106.
Swift G, Carraher, Jr., CE, Bowman CN. 1997. Polymer Modification. New York: Plenum Press.
Lampiran 1 Diagram alir penelitian
Onggok tapioka
• Pencangkokan dan penautan
Polimer Prototipe I
• Saponifikasi
Polimer Prototipe II Analisis Kadar N
Kjeldahl (Peubah “y”)
Spektrum FTIR (Peubah “x”)
Spektrum FTIR (Peubah “x”) Analisis Kadar N
Kjeldahl (Peubah “y”) PLS
PCA
PLS
Lampiran 2 Sintesis Onggok ter-grafting dan crosslinking akril amida (Graftized Crosslinked Onggok)
Onggok tapioka kasar
• Dicuci dengan air • Dikeringudarakan
• Dihaluskan hingga lolos ayakan 100 mesh
Onggok tapioka bersih & halus
• Dimasukkan ke dalam labu leher tiga • (+) 150 mL air, diaduk (overhead stirer) • Dipisahkan antara padatan dan cairan
Graftized Crosslinked Onggok
• (+) 150 – 200 ml aseton, direfluks selama 1 jam • Dipisahkan antara padatan dan cairan
MeOH + EtOH
Graftized Crosslinked Onggok Homopolimer PAA
• Dikeringkan di oven pada suhu 60°C
Graftized Crosslinked Onggok
Fasa padat Fasa cair
Lampiran 3 Saponifikasi Graftized Crosslinked acrylamide Onggok (Nakason et al 2010)
Graftized Crosslinked Onggok (40g)
• (+) 100 ml NaOH 1M • (+) 100 ml air destilata • Refluks (T=90oC)
• (+) HCl 1M sampai netral
• (+) MeOH sampai mengendap sempurna • Dipisahkan antara padatan dan cairan
• Dikeringkan pada suhu 60o
C (di oven) • Dihaluskan
Saponified Graftized Crosslinked Onggok (40g)
H–Saponified Graftized Crosslinked Onggok
Padatan Cairan
MeOH + NaCl(aq)
MUHAMAD FARID. Grafting degree Measurement of acrylamide onto polysaccharide using Infrared Spectrometry. Under direction of ZAINAL ALIM MAS’UD and H.M. ANWAR NUR.
Utilization of carbohydrate-based agricultural wastes has been carried out with the manufacture of derivatives by grafting and crosslinking with acrylamide. The success of the process is monitored by setting the levels of nitrogen in the product. This research work is trying to look for possible use of spectrometry Fourier Transform Infrared technique to determine level of nitrogen in the products. Preparation of powder with a reflectance technique gives satisfactory results for grafting product, also for saponified products very satisfactory. ANOVA test of the PLS for each processing the data on IR spectral of the grafted-crosslinked product and its saponified showed a smaller probability value of 0.05, it is indicate the model developed by the independent variable (wave number) is significant effect on nitrogen content at 95% confidence level. Results of Partial Least Square (PLS) model for each treatment to give the coefficient of determination (R2) ranged from 0.961-0.998, it is the model with the wave number of independent variables can predict nitrogen content as well. Results of PLS analysis also provide information that the processing of IR spectrum data does not affect the difference between the predictions and the values of the nitrogen content.
PENDAHULUAN
Latar Belakang
Indonesia sebagai negara agraris pada tahun 2008 menghasilkan singkong
(Manihot esculenta) sebesar 21.593.100 MT dengan nilai US$ 1.524.288.000, dan merupakan negara peringkat 3 dunia penghasil singkong (FAOSTAT). Salah satu
produk turunan singkong adalah tepung tapioka. Proses produksi tapioka dari
singkong akan menghasilkan produk samping yang disebut onggok. Setiap 1 ton
singkong akan menghasilkan 160 kg onggok (Dit PPHP DitJen BPHH Deptan,
2005; Bank Indonesia. 2005). Onggok mempunyai nilai jual rendah (Rp. 1800,- –
2300,-/kg). Salah satu kandungan utama dalam onggok adalah karbohidrat, dalam
bentuk selulosa dan pati. Onggok selama ini digunakan sebagai pengisi saos,
pembuatan obat nyamuk bakar, dan salah satu komponen pakan ternak. Sebagai
pakan ternak pun, onggok tidak bisa langsung digunakan, melainkan harus
difermentasi terlebih dahulu. Untuk meningkatkan nilai tambah dari onggok,
maka harus dilakukan proses modifikasi kandungan utamanya sehingga diperoleh
turunan yang mempunyai nilai jual tinggi.
Lanthong et al. (2006) dan Nakason et al. (2010) telah melakukan modifikasi tepung singkong (tepung tapioka) melalui reaksi pencangkokan dan
penautanulang akrilamida membentuk super adsorben yang ramah lingkungan.
Nur et al. (2011) melakukan riset yang analog dengan bahan baku onggok. Hasil penelitiannya menunjukkan bahwa keberhasilan proses pencangkokan dan
penautan ulang bisa dipantau dengan menentukan kandungan nitrogen dalam
produk reaksi. Kandungan nitrogen ditentukan menggunakan metode klasik yaitu
Kjeldahl.
Teknik pengukuran spektrum inframerah dekat (Near infrared, NIR) telah banyak digunakan dalam analisis kuatitatif nondestruktif yang cepat. Dengan
mengukur spekrum inframerah sejumlah tertentu bahan yang analog yang sudah
diketahui kadar analatnya dengan metoda lain, kemudian dilakukan pengolahan
data Partial Least Square (PLS) maka dapat dibuat model kalibrasi hubungan antara serapan pada bilangan gelombang tertentu serta kandungan analat yang
Tujuan Penelitian
Penelitian ini bertujuan mengkuantifikasi hubungan antara besaran serapan
inframerah pada bilangan gelombang karakteristik gugus fungsi amida produk
penautan ulang dan saponifikasi dengan kandungan nitrogen menggunakan teknik
analisis statistik PLS.
Hipotesis
Serapan inframerah pada daerah bilangan gelombang karakteristik gugus
fungsi amida (1450 – 1780 cm–1 dan 3030 – 3450 cm–1) dari hasil pencangkokan
dan penautansilang akrilamida serta produk turunan hasil saponifikasinya
TINJAUAN PUSTAKA
Onggok Tapioka
Onggok merupakan hasil samping proses produksi tapioka dari singkong.
Proses tersebut merupakan proses esktraksi pati dari singkong, sehingga
kandungan karbohidrat yang tidak larut (serat kasar) akan meningkat pada
onggok. Hasil analisis kimia pada singkong dan onggok tertera pada Tabel 1.
Tabel 1 Komposisi kimia singkong dan onggok tapioka
Komposisi Kadar (%)
tidak perlu dilakukan proses deproteinasi dan pengawalemakan terlebih dahulu
sebelum dilakukan modifikasi.
Polisakarida
Polisakarida dengan rumus umum (C6H10O5)n adalah polimer alami yang
bila dihidrolisis menghasilkan banyak molekul monosakarida. Dalam nomenklatur
kimia, polisakarida merupakan glikan dan sebagai terdiri dari unit glikosil.
Polisakarida dibagi lagi menjadi 2 golongan, yaitu homopolisakarida dan
heteropolisakarida. Homopolisakarida bila dihidrolisis hanya menghasilkan satu
jenis monosakarida, misalnya pati dan selulosa. Heteropolisakarida bila
menghasilkan lebih dari satu jenis mono-sakarida, misalnya inulin (BeMiller
Polisakarida dapat dibedakan satu sama lain karena unit monomer individu
bergabung secara spesifik kepala ke ekor. Molekul polisakarida dapat linear atau
bercabang dalam salah satu dari beberapa cara yang berbeda (Gambar 1). Mereka
dapat terdiri dari satu jenis unit glikosil (homoglikan) atau dari dua sampai enam
unit glikosil berbeda (heteroglikan) (BeMiller 2007).
Gambar 1 Pola percabangan polisakarida (BeMiller 2007).
Pati berwarna putih, amorf, tidak berasa, dan tidak berbau. Pati tidak larut
dalam air, tetapi ketika ditambahkan ke dalam air mendidih, butirannya
dipanaskan pada suhu 200°C–250°C akan membentuk dekstrin. Pada suhu yang lebih tinggi akan mengalami pengarangan. Pati bila dididihkan dengan asam encer
akan menghasilkan glukosa sebagai produk utama. Pati dapat dibagi menjadi 2
struktur umum yaitu struktur linear amilosa dan struktur bercabang amilopektin.
Amilosa bereaksi dengan larutan iod encer akan menghasilkan warna biru, yang
menghilang bila dipanaskan, dan timbul kembali bila didinginkan. Amilopektin,
bereaksi dengan larutan iod encer menghasilkan warna coklat. Berat molekul
amilosa berkisar dari 15000–25000. Amilosa merupakan polimer yang linear yang
mengandung unit α–D–glukopiranosa yang berikatan melalui ikatan 1,4–α–
glikosida (Gambar 2).
Gambar 2 Struktur molekul amilosa
Amilopektin merupakan polimer yang sangat bercabang. Cabang terdiri dari 20 – 25 unit glukosa yang bergabung melalui ikatan 1,4–α–glikosida, dan masing–masing cabang berikatan sesamanya melalui ikatan 1,6–α–glikosida (Gambar 3) (Carraher 2008; Daniel et al. 2007; Tewari et al. 1981; Whistler & Daniel 2007).
Selulosa berupa padatan tidak berwarna, tidak larut dalam air, tapi larut
dalam larutan tembaga (II) hidroksida amoniakal (Pereaksi Schweitzer). Selulosa
juga larut dalam larutan seng klorida dalam asam klorida. Selulosa akan larut bila
direaksikan dengan asam sulfat pekat. Bila larutan ini diencerkan akan
menghasilkan bahan seperti pati, amiloid. Bila selulosa dididihkan dengan asam
sulfat encer, akan terhidrolisis sempurna menjadi glukosa. Bila selulosa
direaksikan dengan larutan NaOH 20% selulosa akan menjadi halus dan berkilau.
Selulosa mempunyai unit glukosa, yang tiga gugus hidroksinya bebas untuk
diesterkan. Selulosa bereaksi dengan asam nitrat pekat dan asam sulfat pekat
membentuk campuran selulosa mono, di dan trinitrat. Selulosa bereaksi dengan
campuran anhidrida asetat dan asam asetat glasial membentuk campuran selulosa
mono, di dan triasetat (Carraher 2008; French et al. 2007; Krässig et al. 2004; Tewari et al. 1981).
Selulosa bila dihidrolisis sempurna akan menghasilkan glukosa dalam
bentuk β–D–glukopiranosa sebagai produk utama. Selulosa merupakan polimer
linear dengan unit β–D– glukopiranosa yang berikatan melalui 1,4–β–glikosida
(Gambar 4) (Carraher 2008; French et al. 2007; Krässig et al. 2004; Tewari et al.
1981).
Gambar 4 Struktur molekul selulosa
Akrilamida
Akrilamida (CH2=CHCONH2, 2–propenamida, CAS No. 79–06–1), padatan
berwarna putih yang stabil pada suhu ambien hingga suhu titik lelehnya (tanpa
ada cahaya). Diatas suhu titik lelehnya, akrilamida segera mengalami reaksi
polimerisasi adisi sambil membebaskan panas yang besar. Akrilamida merupakan
monomer bifungsional, memiliki gugus alkena (CH2=CH–) dan amida (–CONH2),
menunjukkan karakter asam lemah dan basa lemah. Gugus penarik elektron amida
mengaktivasi ikatan rangkap, dan segera bereaksi dengan pereaksi nukleofilik.
Nu:H + CH2=CHCONH2 → Nu–CH2CH2CONH2
Hadirnya basa memungkinkan penambahan merkaptan, sulfida, keton,
nitroalkana, dan alkohol ke akrilamida. Akrilamida bereaksi dengan alkohol
polimerik seperti poli (vinil alkohol), selulosa, dan pati. Dalam kondisi basa hasil
reaksi hidrolisis parsial amida berupa campuran karbamoiletil dan karboksietil.
Sebagian besar akrilamida (94%) digunakan untuk membuat poliakrilamida.
Poliakrilamida digunakan sebagai pereaksi pengolahan air (56%), produksi pulp
dan kertas (24%), pemrosesan mineral (10%), pembuatan monomer N–
metilakrilamid dan monomer lainnya (6%), dan lain–lain (4%) (Habermann,
2007).
Modifikasi Polimer
Meskipun jenis polimer sangat banyak, kadang-kadang mereka tidak dapat
memenuhi suatu keperluan. Modifikasi pada polimer sangat penting karena akan
memperluas ruang lingkup aplikasi. Ada dua pendekatan utama, yaitu
mengkonstruksi molekul baru dengan mengatur komposisi molekular hingga
dicapai sifat yang diinginkan, atau modifikasi polimer yang sudah ada
(Bhattacharya & Ray 2009; Carraher 2008; Ebewele 2000; Hamielec & Tobita
2005; Swift et al. 1997).
Terdapat 4 teknik modifikasi polimer, yaitu grafting (cangkok), crosslinking
(ikatan silang), blending (campuran), dan pembentukan komposit. Kopolimer cangkok dilakukan dengan cara mencangkokkan polimer lain yang berbeda
jenisnya dengan polimer kerangka utamanya. Penautan silang diperoleh bila
digunakan monomer yang memiliki dua atau lebih gugus fungsi yang dapat
membentuk ikatan. Campuran homogen makroskopik dari dua atau lebih polimer
yang berbeda dapat didefinisikan sebagai campuran polimer. Campuran polimer
ini menggabungkan sifat yang berguna dari semua konstituen dan merupakan
sarana untuk memproduksi bahan-bahan baru. Komposit dibuat dengan
menggabungkan dua atau lebih bahan yang berbeda sedemikian rupa sehingga