SKRIPSI
OLEH:
KAREN DARMAWAN
090305026/ILMU DAN TEKNOLOGI PANGAN
PROGRAM STUDI ILMU DAN TEKNOLOGI PANGAN
FAKULTAS PERTANIAN
UNIVERSITAS SUMATERA UTARA
MEDAN
SKRIPSI
Oleh:
KAREN DARMAWAN
090305026/ILMU DAN TEKNOLOGI PANGAN
Skripsi penelitian sebagai salah satu syarat untuk memperoleh gelar sarjana di Fakultas Pertanian
Universitas Sumatera Utara
PROGRAM STUDI ILMU DAN TEKNOLOGI PANGAN
FAKULTAS PERTANIAN
UNIVERSITAS SUMATERA UTARA
MEDAN
Nim : 090305026
Program Studi : Ilmu dan Teknologi Pangan
Disetujui oleh Komisi Pembimbing
Ir. Rona J Nainggolan, SU
Ketua Anggota
Ir. Lasma Nora Limbong
Mengetahui,
Ketua Program Studi Dr. Ir. Herla Rusmarilin, MP
Pektin dari Kulit Durian. Dibimbing oleh RONA J. NAINGGOLAN dan LASMA NORA LIMBONG.
Penelitian ini dilakukan untuk mengetahui metode pencucian dan jumlah lapisan penyaringan yang tepat pada ekstraksi pektin dari kulit durian dan meningkatkan nilai ekonomis limbah kulit durian. Penelitian ini dilakukan dengan menggunakan rancangan acak lengkap dua faktor, yaitu metode pencucian dengan dan tanpa alkohol dan jumlah lapisan penyaringan yaitu 1 lembar, 2 lembar, 3 lembar, 4 lembar, 5 lembar, dan 6 lembar. Parameter yang dianalisis adalah rendemen, kadar air, kadar abu, berat ekivalen, kandungan metoksil, kadar galakturonat, dan uji organoleptik warna.
Hasil penelitian menunjukkan bahwa metode pencucian memberikan pengaruh berbeda sangat nyata terhadap rendemen, kadar air, dan warna dan memberikan pengaruh yang nyata terhadap kadar abu serta pengaruh tidak nyata terhadap berat ekivalen, kandungan metoksil, dan kadar galakturonat. Jumlah lapisan penyaringan memberikan pengaruh yang berbeda sangat nyata terhadap rendemen, kadar air, kadar abu, berat ekivalen, kandungan metoksil, dan kadar galakturonat. Interaksi metode pencucian dan jumlah lapisan penyaringan memberikan pengaruh yang berbeda sangat nyata terhadap rendemen dan warna serta berbeda nyata terhadap kadar abu dan memberikan pengaruh berbeda tidak nyata terhadap kadar air, berat ekivalen, kandungan metoksil, dan kadar galakturonat. Metode pencucian dengan alkohol dan jumlah lapisan penyaringan 6 lembar menghasilkan mutu pektin kulit durian yang terbaik.
Kata kunci: kulit durian, pektin, metode pencucian, jumlah lapisan penyaringan
ABSTRACT
KAREN DARMAWAN: Washing Methods and Filtration on the Extraction of Durian Peel Pectin, supervised by Rona J. Nainggolan and Lasma Nora Limbong. This research was aimed to know the washing methods and filtration thickness on the quality of pectin extracted from durian peel and to increase economic value on durian peel waste. This research was conducted using a completely randomized design with two factors, namely the washing methods; washed and unwashed with alcohol and filtration thickness: 1 piece, 2 pieces, 3 pieces, 4 pieces, 5 pieces, and 6 pieces. The parameters analyzed were yield, water content, ash content, equivalent weight, methoxyl content, galacturonic content and color.
The results showed that the washing methods had highly significant effect on yield, water content, and colors and had significant effect on ash content and provided no effect on equivalent weight, methoxyl content, galacturonic content. Filtration thickness gave highly significant effect on yield, water content, ash content, equivalent weight, methoxyl content and galacturonic content. Interactions of the two factors gave highly significant effect on yield and color and had significant effect on ash content and provided no effect on water content, equivalent weight, methoxyl content and galacturonic content. Washing with alcohol and filtration thickness of 6 pieces produce the best quality of durian peel pectin.
Keywords: durian peel, pectin, washing methods, filtration thickness. i
Penulis dilahirkan di Jakarta pada tanggal 9 Agustus 1991 dari ayah Wong Tonny Darmawan dan ibu Tjiong Sioe Bing. Penulis merupakan putri bungsu dari
tiga bersaudara.
Tahun 2009 penulis lulus dari SMA Kristen III BPK Penabur, Jakarta dan
pada tahun yang sama masuk ke Fakultas Pertanian USU melalui jalur Ujian Masuk Bersama Perguruan Tinggi Negeri. Penulis memilih program studi Ilmu dan Teknologi Pangan.
Selama mengikuti perkuliahan, penulis aktif sebagai anggota Ikatan Mahasiswa Ilmu dan Teknologi Pangan (IMITP) serta Keluarga Kristen Ilmu dan
Teknologi Pangan (KKITP).
Penulis melaksanaan praktek kerja lapangan (PKL) di PT. Niramas Utama (INACO) yang bertempat di Bekasi, Jawa Barat dari tanggal 9 Juli sampai 8
Agustus 2012.
Puji dan syukur penulis panjatkan kepada Tuhan Yesus Kristus, atas segala rahmat dan karuniaNya sehingga penulis dapat menyelesaikan skripsi yang berjudul “Metode Pencucian dan Penyaringan pada Ekstraksi Pektin dari Kulit
Durian”.
Pada kesempatan ini penulis menghaturkan pernyataan terima kasih
sebesar-besarnya kepada kedua orang tua penulis yang telah membesarkan, memelihara dan mendidik penulis selama ini. Penulis menyampaikan ucapan terima kasih kepada Ir. Rona J. Nainggolan, SU dan Ir. Lasma Nora Limbong
selaku ketua dan anggota komisi pembimbing yang telah membimbing dan memberikan berbagai masukan berharga kepada penulis dari mulai menetapkan
judul, melakukan penelitian, sampai pada ujian akhir. Khusus untuk Bapak penjual durian di Ucok Durian Medan, penulis menyampaikan banyak terima kasih atas bantuannya selama penulis mengumpulkan kulit durian.
Di samping itu, penulis juga mengucapkan terima kasih kepada semua staf pengajar dan pegawai di Program Studi Ilmu dan Teknologi Pangan, teman-teman
ITP’09 serta semua rekan mahasiswa yang tak dapat disebutkan satu per satu di sini yang telah membantu penulis dalam menyelesaikan skripsi ini. Penulis berharap semoga skripsi ini bermanfaat bagi yang membacanya.
Medan, Oktober 2013
Penulis
Hal
Struktur dan komposisi kimia pektin ... 10
Proses produksi pektin ... 11
Peranan pektin ... 12
Proses Ekstraksi Pektin Kulit Durian ... 13
Rendemen ... 22 Pengaruh jumlah lapisan penyaringan terhadap parameter yang diamati ... 26
Pengaruh metode pencucian terhadap parameter yang diamati ... 27
Rendemen Pengaruh jumlah lapisan penyaringan terhadap rendemen ... 28
Pengaruh metode pencucian terhadap rendemen ... 30
Pengaruh interaksi antara jumlah lapisan penyaringan dan metode pencucian terhadap rendemen ... 31
Kadar Air Pengaruh jumlah lapisan penyaringan terhadap kadar air ... 33
Pengaruh metode pencucian terhadap kadar air ... 34
Pengaruh interaksi antara jumlah lapisan penyaringan dan metode pencucian terhadap kadar air ... 36
Kadar Abu Pengaruh jumlah lapisan penyaringan terhadap kadar abu ... 37
Pengaruh metode pencucian terhadap kadar abu ... 38
Pengaruh interaksi antara jumlah lapisan penyaringan dan metode pencucian terhadap kadar abu ... 39
Berat Ekivalen Pengaruh jumlah lapisan penyaringan terhadap berat ekivalen .... 41
Pengaruh metode pencucian terhadap berat ekivalen ... 43
Pengaruh interaksi antara jumlah lapisan penyaringan dan metode pencucian terhadap berat ekivalen ... 43
Kandungan Metoksil Pengaruh jumlah lapisan penyaringan terhadap kandungan metoksil ... 44
Pengaruh metode pencucian terhadap kandungan metoksil ... 45
Pengaruh interaksi antara jumlah lapisan penyaringan dan metode pencucian terhadap kandungan metoksil ... 45
Kadar Galakturonat Pengaruh jumlah lapisan penyaringan terhadap kadar galakturonat ... 46
Pengaruh metode pencucian terhadap kadar galakturonat ... 47
Pengaruh interaksi antara jumlah lapisan penyaringan dan metode pencucian terhadap kadar galakturonat ... 48
Pengaruh interaksi antara jumlah lapisan penyaringan dan
metode pencucian terhadap warna ... 49
KESIMPULAN DAN SARAN Kesimpulan ... 52
Saran ... 53
DAFTAR PUSTAKA ... 54
LAMPIRAN ... 57
No. Hal
1. Provinsi penghasil durian terbesar di Indonesia ... 4
2. Komposisi kimia kulit durian ... 5
3. Faktor mutu pektin menurut standar mutu SI ... 7
4. Spesifikasi mutu pektin pangan komersial... 8
5. Sifat kimia etanol ... 16
6. Pengaruh jumlah lapisan penyaringan terhadap parameter yang diamati ... 26
7. Pengaruh metode pencucian terhadap parameter yang diamati ... 27
8. Uji LSR efek utama pengaruh jumlah lapisan penyaringan terhadap rendemen (%) ... 29
9. Uji LSR efek utama pengaruh metode pencucian terhadap rendemen (%) ... 30
10. Uji LSR interaksi jumlah lapisan penyaringan dan metode pencucian terhadap rendemen (%) ... 32
19. Uji LSR efek utama pengaruh metode pencucian terhadap warna ... 49 20. Uji LSR interaksi jumlah lapisan penyaringan dan metode pencucian
terhadap warna ... 50
No. Hal
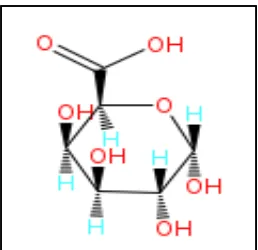
1. Struktur kimia asam α-galakturonat ... 10
2. Struktur kimia asam poligalakturonat ... 11
3. Struktur fungsional pektin ... 11
4. Mekanisme reaksi esterifikasi ... 16
5. Skema ekstraksi pektin dari kulit durian ... 25
6. Hubungan jumlah lapisan penyaringan yang berbeda dengan rendemen ... 30
7. Hubungan metode pencucian yang berbeda dengan rendemen ... 31
8. Interaksi jumlah lapisan penyaringan dan metode pencucian terhadap rendemen (%) ... 33
9. Hubungan jumlah lapisan penyaringan yang berbeda dengan kadar air ... 34
10. Hubungan metode pencucian yang berbeda dengan kadar air ... 36
11. Hubungan jumlah lapisan penyaringan yang berbeda dengan kadar abu ... 38
12. Hubungan metode pencucian yang berbeda dengan kadar abu ... 39
13. Interaksi jumlah lapisan penyaringan dan metode pencucian terhadap kadar abu (%) ... 41
14. Hubungan jumlah lapisan penyaringan yang berbeda dengan berat ekivalen ... 43
15. Hubungan jumlah lapisan penyaringan yang berbeda dengan kandungan metoksil ... 45
16. Hubungan jumlah lapisan penyaringan yang berbeda dengan kadar galakturonat ... 47
17. Hubungan metode pencucian yang berbeda dengan warna ... 49
18. Interaksi jumlah lapisan penyaringan dan metode pencucian terhadap warna ... 51
No. Hal
1. Data pengamatan rendemen ... 57
2. Data pengamatan kadar air ... 58
3. Data pengamatan kadar abu ... 59
4. Data pengamatan berat ekivalen ... 60
5. Data pengamatan kandungan metoksil ... 61
6. Data pengamatan kadar galakturonat ... 62
7. Data pengamatan uji organoleptik warna ... 63
8. Foto pengolahan pektin dari kulit durian ... 64
Pektin dari Kulit Durian. Dibimbing oleh RONA J. NAINGGOLAN dan LASMA NORA LIMBONG.
Penelitian ini dilakukan untuk mengetahui metode pencucian dan jumlah lapisan penyaringan yang tepat pada ekstraksi pektin dari kulit durian dan meningkatkan nilai ekonomis limbah kulit durian. Penelitian ini dilakukan dengan menggunakan rancangan acak lengkap dua faktor, yaitu metode pencucian dengan dan tanpa alkohol dan jumlah lapisan penyaringan yaitu 1 lembar, 2 lembar, 3 lembar, 4 lembar, 5 lembar, dan 6 lembar. Parameter yang dianalisis adalah rendemen, kadar air, kadar abu, berat ekivalen, kandungan metoksil, kadar galakturonat, dan uji organoleptik warna.
Hasil penelitian menunjukkan bahwa metode pencucian memberikan pengaruh berbeda sangat nyata terhadap rendemen, kadar air, dan warna dan memberikan pengaruh yang nyata terhadap kadar abu serta pengaruh tidak nyata terhadap berat ekivalen, kandungan metoksil, dan kadar galakturonat. Jumlah lapisan penyaringan memberikan pengaruh yang berbeda sangat nyata terhadap rendemen, kadar air, kadar abu, berat ekivalen, kandungan metoksil, dan kadar galakturonat. Interaksi metode pencucian dan jumlah lapisan penyaringan memberikan pengaruh yang berbeda sangat nyata terhadap rendemen dan warna serta berbeda nyata terhadap kadar abu dan memberikan pengaruh berbeda tidak nyata terhadap kadar air, berat ekivalen, kandungan metoksil, dan kadar galakturonat. Metode pencucian dengan alkohol dan jumlah lapisan penyaringan 6 lembar menghasilkan mutu pektin kulit durian yang terbaik.
Kata kunci: kulit durian, pektin, metode pencucian, jumlah lapisan penyaringan
ABSTRACT
KAREN DARMAWAN: Washing Methods and Filtration on the Extraction of Durian Peel Pectin, supervised by Rona J. Nainggolan and Lasma Nora Limbong. This research was aimed to know the washing methods and filtration thickness on the quality of pectin extracted from durian peel and to increase economic value on durian peel waste. This research was conducted using a completely randomized design with two factors, namely the washing methods; washed and unwashed with alcohol and filtration thickness: 1 piece, 2 pieces, 3 pieces, 4 pieces, 5 pieces, and 6 pieces. The parameters analyzed were yield, water content, ash content, equivalent weight, methoxyl content, galacturonic content and color.
The results showed that the washing methods had highly significant effect on yield, water content, and colors and had significant effect on ash content and provided no effect on equivalent weight, methoxyl content, galacturonic content. Filtration thickness gave highly significant effect on yield, water content, ash content, equivalent weight, methoxyl content and galacturonic content. Interactions of the two factors gave highly significant effect on yield and color and had significant effect on ash content and provided no effect on water content, equivalent weight, methoxyl content and galacturonic content. Washing with alcohol and filtration thickness of 6 pieces produce the best quality of durian peel pectin.
Keywords: durian peel, pectin, washing methods, filtration thickness. i
Latar Belakang
Sumatera Utara adalah salah satu provinsi penghasil buah durian terbesar di Indonesia dengan angka sebesar 79.659 ton pada tahun 2011 (BPS, 2013) dan terus semakin meningkat pada tahun-tahun selanjutnya. Seiring dengan semakin
meningkatnya jumlah durian tersebut, tidak dapat dihindari bahwa durian akan menghasilkan limbah atau buangan berupa biji dan kulit durian yang semakin
banyak. Kulit durian merupakan penyusun terbesar dari buah durian dengan angka 57% dari bobot buah tersebut. Artinya, bobot kulit itu setara dengan 45.405 ton kulit durian yang dihasilkan di Sumatera Utara saja.
Jawa Barat dan di banyak provinsi lainnya yang merupakan penghasil buah durian, telah ditemukan pemanfaatan limbah kulit durian seperti untuk pembuatan obat anti nyamuk, biogas, dan kerajinan tangan atau barang kesenian
tetapi di Sumatera Utara, dengan limbah yang begitu melimpah belum terdapat pengolahan yang bernilai ekonomi. Pengolahan yang ada selama ini hanya dalam
skala menjadikan kulit durian tersebut sebagai pupuk. Pemanfaatan limbah kulit durian menjadi pupuk adalah pengolahan limbah yang masih sederhana dan belum maksimal pemanfaatannya.
Kulit durian, seperti pada kulit buah lainnya, mengandung pektin. Pektin merupakan suatu senyawa yang umumnya terdapat dalam buah, namun banyak
juga terdapat pada kulit buah karena fungsinya yang merupakan elemen struktural pada pertumbuhan jaringan dan komponen utama dari lamella tengah pada tanaman dan juga berperan sebagai perekat dan menjaga stabilitas jaringan dan
sel. Pektin banyak dimanfaatkan pada industri pangan, contohnya digunakan
sebagai bahan perekat dan stabilizer agar tidak terbentuk endapan. Pektin digunakan sebagai pembentuk gel dan pengental dalam pembuatan jelly,
marmalade, makanan rendah kalori dan dalam bidang farmasi digunakan untuk obat diare.
Permintaan akan pektin terus meningkat setiap tahunnya. Hingga tahun
2011, seluruh pektin yang digunakan di industri-industri Indonesia adalah barang impor. Jumlah impor pektin cukup besar, yaitu lebih besar dari 100 ton per tahun
dan harganya sangat mahal, membuat biaya impor pektin berdampak terhadap pengurangan devisa negara yang besar pula (Hanum, dkk., 2012). Selain itu, harga pektin di pasaran sangat mahal yakni bisa mencapai Rp. 200.000 - 300.000/kg.
Dan bukan hanya itu, pektin yang lazim dipakai selama ini berasal dari kulit jeruk atau kulit apel sementara kulit durian belum dimanfaatkan dalam pembuatan pektin skala industri semacam itu. Padahal kulit durian sangat berlimpah di
Indonesia khususnya daerah Sumatera Utara.
Proses ekstraksi pektin pada umumnya melalui beberapa tahap. Di
antaranya adalah pencucian dan penyaringan. Biasanya pada tahap pencucian, pektin basah akan dicuci dengan alkohol untuk mencerahkan warnanya. Lalu pada tahap penyaringan akan kembali disaring dengan kain saring yang dirangkapkan
beberapa lembar untuk menghilangkan asamnya. Oleh karena itu, ekstraksi pektin dari kulit durian dengan memvariasikan metode pencucian dengan jumlah lapisan
dibandingkan dengan kualitas pektin komersial pada umumnya. Untuk itu perlu
dilakukan penelitian dengan judul “Metode Pencucian dan Penyaringan pada Ekstraksi Pektin dari Kulit Durian”.
Perumusan Masalah
Pemanfaatan limbah dari kulit durian merupakan cara inovasi dengan harapan dapat meningkatkan nilai ekonomi kulit durian dan perlakuan metode
pencucian dapat mencerahkan warna pektin serta dengan jumlah lapisan penyaringan dapat meningkatkan kemurnian pektin.
Tujuan Penelitian
Adapun tujuan dari penelitian ini adalah untuk mengetahui pengaruh
metode pencucian dan jumlah lapisan penyaringan terhadap mutu pektin kulit durian.
Kegunaan Penelitian
Sebagai sumber informasi bagi masyarakat dan sebagai sumber data dalam penyusunan skripsi di Program Studi Ilmu dan Teknologi Pangan, Fakultas Pertanian, Universitas Sumatera Utara, Medan.
Hipotesa Penelitian
Tinjauan Umum Buah Durian
Sumatera Utara adalah salah satu provinsi penghasil buah durian terbesar di Indonesia dengan angka sebesar 79.659 ton pada tahun 2011. Durian (Durio zibethinus) adalah salah satu komoditas buah yang terkenal dari Sumatera Utara
dan di beberapa negara lain seperti Malaysia, Thailand. Selama musim panen durian, kulit durian banyak yang terbuang dan dapat menyebabkan masalah pada
lingkungan. Tabel 1 berikut ini menunjukkan data tentang provinsi penghasil buah durian terbesar di Indonesia.
Tabel 1. Provinsi penghasil durian terbesar di Indonesia
(Sumber: BPS, 2013)
Polisakarida larut air yang diekstrak dari kulit durian mengandung banyak
pektin yang nantinya dapat dimanfaatkan untuk keperluan industri (Hokputsa, dkk., 2004). Pada pH 3 dan kadar gula 65% pektin kulit durian dapat membentuk
gel kuat sehingga dapat dimanfaatkan sebagai agen pembentuk gel (Easa, 2005 dalam Wong, dkk., 2008). Pektin juga mengandung komponen non gula, khususnya methanol, asam asetat, asam fenolat dan terkadang gugus amida.
Reaksi esterifikasi asam galakturonat dengan methanol atau asam asetat merupakan reaksi yang akan menentukan karakteristik struktur pektin yang
dihasilkan(Kurniasari, dkk., 2012).
Provinsi Durian (ton)
Jawa Barat 157.030
Jawa Timur 111.207
Sumatera Utara 79.659
Lampung 42.550
Komposisi Kimia Kulit Durian
Kulit durian merupakan penyusun terbesar dari buah durian dengan angka 57% dari bobot buah tersebut. Dengan angka itu artinya bobot kulit itu setara
dengan 332.712 ton kulit durian yang dihasilkan, hanya dari Sumatera Utara saja (Medan Bisnis, 2013). Kulit durian terdiri atas beberapa senyawa seperti pati, ethanol, lemak, dan lain-lain. Data penjelasan tentang komposisi kimia kulit
durian pada Tabel 2 berikut ini.
Tabel 2. Komposisi kimia kulit durian
(Sumber: Dewati, dkk., 2011).
Kandungan kimia kulit durian yang dapat dimanfaatkan adalah pektin.
Kulit durian secara proporsional mengandung unsur selulosa yang tinggi (50-60%) dan kandungan lignin (5%) serta kandungan pati yang rendah (5%) sehingga
dapat diindikasikan bahan tersebut bisa digunakan sebagai campuran bahan baku papan olahan serta produk lainnya yang dimampatkan. Hasil penelitian menunjukkan bahwa nilai kalor kulit durian yang diperoleh menunjukkan angka
sebesar 3786,95 kal/gram dengan kadar abu rendah yaitu 4% (Novita, 2013).
Komposisi Persentase (%)
Pati 18,50
Gula Total 1,85
Ethanol 0,16
Lemak 0,22
Protein 0,35
Serat Kasar 19,40
Pektin
Pengertian dan sumber pektin
Pektin berasal dari bahasa Latin “pectos” yang berarti pengental atau yang
membuat sesuatu menjadi keras/padat. Pektin adalah substansi alami yang terdapat pada sebagian besar tanaman pangan. Selain sebagai elemen struktural pada pertumbuhan jaringan dan komponen utama dari lamella tengah pada
tanaman, pektin juga berperan sebagai perekat dan menjaga stabilitas jaringan dan sel. Pektin ditemukan oleh Vauquelin dalam jus buah sekitar 200 tahun yang lalu.
Pada tahun 1790, pektin belum diberi nama. Nama pektin pertama kali digunakan tahun 1824, yaitu ketika Braconnot melanjutkan penelitian yang dirintis oleh Vauquelin. Braconnot menyebut substansi pembentuk gel tersebut sebagai asam
pektat (Herbstreith dan Fox, 2005).
Pektin merupakan senyawa polisakarida dengan bobot molekul tinggi yang banyak terdapat pada tumbuhan. Pektin digunakan sebagai pembentuk gel dan
pengental dalam pembuatan jelly, marmalade, makanan rendah kalori dan dalam bidang farmasi digunakan untuk obat diare (National Research Development
Corporation, 2004). Pektin adalah konstituen dari jaringan tanaman dan merupakan molekul yang kompleks dan besar. Pektin paling sering ditemukan di dinding sel primer, namun ada juga yang terdapat di antara dinding sel. Pektin
adalah polimer linier dari D-galakturonat yang berikatan dengan α-1,4-glikosida (Vaclavik dan Christian, 2008).
termasuk ke dalam golongan serat. Ada dua golongan serat, yaitu yang tidak dapat
larut dan yang dapat larut dalam air. Serat yang tidak dapat larut dalam air adalah selulosa, hemiselulosa, dan lignin. Serat yang larut dalam air adalah pektin, gum,
mukilase, glukan, dan algae. Pektin, gum, mukilase terdapat di sekeliling dan di dalam sel tumbuh-tumbuhan. Ikatan-ikatan ini mengembang atau larut dalam air, sehingga membentuk gel. Oleh karena itu, di dalam industri pangan digunakan
sebagai bahan pengental, emulsifier, dan stabilizer. Adapun syarat mutu pektin yang tergolong memenuhi standar mutu Standard Internasional (SI) ada pada
Tabel 3 dan menjadi acuan dalam menentukan apakah pektin kulit durian ini layak untuk menjadi pektin komersial berskala internasional. Sedangkan kualitas pektin untuk pangan menurut Food Chemical Codex menunjukkan pada Tabel 4.
Tabel 3. Faktor mutu pektin menurut standar mutu SI
Faktor Mutu Standar Mutu (SI)
Kekuatan Gel
Kandungan Metoksil
• Pektin metoksil tinggi
• Pektin metoksil rendah Kadar Asam Galakturonat Kadar Air
Kadar Abu
Derajat Esterifikasi, untuk :
• Pektin ester tinggi
• Pektin ester rendah Kandungan logam berat :
Tabel 4. Spesifikasi mutu pektin pangan komersial
(Sumber: Food Chemical Codex, 1996 dalam Hariyati, 2006).
Sifat-sifat pektin
Sifat penting pektin adalah kemampuannya membentuk gel. Pektin metoksil tinggi membentuk gel dengan gula dan asam, yaitu dengan konsentrasi gula 58 - 75% dan pH 2,8 - 3,5. Pembentukan gel terjadi melalui ikatan hidrogen
di antara gugus karboksil bebas dan di antara gugus hidroksil. Pektin bermetoksil rendah tidak mampu membentuk gel dengan asam dan gula tetapi membentuk gel
dengan adanya ion-ion kalsium (Sari, dkk., 2012).
Pektin dapat digolongkan menjadi dua kelompok, yaitu :
a. Pektin berester tinggi yaitu mempunyai lebih besar dari 50% gugus karboksil
yang teresterkan.
b. Pektin berester rendah yaitu mempunyai lebih kecil dari 50% gugus karboksil yang teresterkan.
Berdasarkan banyaknya gugus karboksil yang mengalami esterifikasi, maka pektin dapat dibedakan menjadi dua golongan, yaitu :
a. High Methoxy Pectin (HMP), yaitu pektin yang mengandung gugus metoksil sekurang-kurangnya 7 - 8%. HMP mengandung 50-58% gugus karboksil yang teresterifikasi. HMP hanya dapat membentuk gel dengan gula dan asam pada
Karakteristik Nilai
Kadar air (maksimum) 12 %
Kadar abu (maksimum) 1 %
Pektin bermetoksil tinggi (minimum) 7 %
Pektin bermetoksil rendah (maksimum) 7 %
Asam galakturonat (minimum) 65 % (bk)
kadar gula 60 – 65%, oleh karena itu HMP dapat dimanfaatkan dalam pembuatan
jelly.
b. Low Methoxy Pectin (LMP), yaitu pektin yang mengandung gugus metoksil
kurang dari 7% (biasanya 3 – 5%). Pada LMP, hanya 20-40% gugus karboksil yang teresterifikasi. LMP dapat membentuk gel pada kadar gula 10 – 20% dan dengan ion bivalen yaitu kalsium (Vaclavik dan Christian, 2008).
Pektin yang umum terdapat pada limbah pertanian adalah pektin jenis HMP. Pektin jenis ini akan membentuk gel pada pH rendah dan dengan adanya
padatan terlarut dalam jumlah besar. Gel yang terbentuk akan mudah larut dalam air sehingga praktis pektin jenis HMP tidak bisa digunakan sebagai adsorben logam berat. Semakin rendah kadar metoksil pektin maka sifat pembentukan
jellinya akan semakin berkurang, sehingga jenis pektin yang dapat digunakan sebagai adsorben adalah LMP. LMP dapat dihasilkan dari HMP dengan proses demetilasi. (Kurniasari, dkk., 2012).
Kadar abu dalam pektin semakin meningkat dengan meningkatnya konsentrasi asam, suhu, dan waktu ekstraksi. Hal ini disebabkan oleh kemampuan
asam untuk melarutkan mineral alami dari bahan yang diekstrak yang semakin meningkat dengan meningkatnya konsentrasi asam, suhu, dan waktu reaksi. Mineral yang terlarut akan ikut mengendap bercampur dengan pektin pada saat
pengendapan dengan alkohol (Kalapathy dan Proctor, 2001 dalam Hariyati, 2006). Berat ekivalen merupakan ukuran terhadap kandungan gugus asam
esterifikasi. Asam pektat murni memiliki berat ekivalen 176. Tingginya derajat
esterifikasi antara asam galakturonat dengan methanol menunjukkan semakin rendahnya jumlah asam bebas yang berarti semakin tingginya berat ekivalen
(Rouse, 1977) dalam (Hariyati, 2006). Semakin tinggi berat ekivalen, semakin tinggi kadar metoksil (Perina, dkk., 2007). Semakin besar berat ekivalen, semakin rendah kadar galakturonatnya (Hariyati, 2006).
Struktur dan komposisi kimia pektin
Pada tahun 1924, Smolenski adalah yang pertama kali berasumsi bahwa pektin merupakan polimer asam galakturonat. Tahun 1930, Meyer dan Mark
menemukan formasi rantai dari molekul pektin, kemudian Schneider dan Bock pada tahun 1937 membentuk formula tersebut (Herbstreith dan Fox, 2005). Pektin
tersusun atas molekul asam galakturonat yang berikatan dengan ikatan α-
(1-4)-glikosida sehingga membentuk asam poligalakturonat. Gugus karboksil sebagian teresterifikasi dengan methanol dan sebagian gugus alkohol sekunder terasetilasi
(Herbstreith dan Fox, 2005). Gambar 1 di bawah ini menunjukkan struktur kimia
unit asam α-galakturonat.
Pektin merupakan asam poligalakturonat yang mengandung metil
ester. Pektin diekstraksi secara komersial dari kulit buah jeruk dan apel dalam kondisi asam. Masing-masing cincin merupakan suatu molekul dari asam α -galakturonat, dan ada 300 – 1000 cincin seperti itu dalam suatu tipikal molekul pektin, yang dihubungkan dengan suatu rantai linier (Hoejgaard, 2004).
Gambar 2. Struktur kimia asam poligalakturonat
Selain asam D-galakturonat sebagai komponen utama, pektin juga
memiliki D-galaktosa, L-arabinosa, dan L-ramnosa dalam jumlah yang bervariasi. Komposisi kimia pektin sangat bervariasi tergantung pada sumber dan kondisi yang dipakai dalam isolasinya (Willats, dkk., 2006). Pada
Gambar 3 berikut adalah gambar struktur fungsional pektin.
Proses produksi pektin
Bagian dalam kulit buah durian ditimbang 460 g dan ditambahkan akuades sebanyak 4,14 L dan dihaluskan menggunakan blender, kemudian ditambahkan
dengan larutan HCl 1N hingga pH 2, kemudian dipanaskan pada suhu 90°C selama 4 jam. Selanjutnya disaring menggunakan kain saring. Filtratnya diambil dan didinginkan pada suhu ruang dan ditambahkan 13,36 L etanol asam dan
biarkan selama 1 jam. Kemudian disaring menggunakan kain saring sehingga diperoleh bagian gelnya yang kemudian ditambahkan 1,28 L akuades, lalu
ditambahkan lagi 3 L etanol 95% dan disaring kembali menggunakan kain saring, sehingga diperoleh pektin basah. Pektin basah kemudian dikeringkan pada suhu 25°C. Kemudian pektin kering digerus hingga halus dan diayak menggunakan
saringan 60 mesh (Wong, dkk., 2008).
Kualitas pektin komersial ditentukan oleh sifat-sifat fisik pektin. Sifat fisik tersebut diantaranya warna dan cita rasa yang cocok, kelarutan (untuk pektin
padat), derajat gel, kecepatan membeku, serta tidak mengandung bahan atau zat berbahaya bagi kesehatan. Sifat fisik tersebut dipengaruhi oleh sifat kimia pektin
(Hariyati, 2006).
Peranan pektin
Pektin seperti juga pembentukan gel lainnya, tidak larut dalam suatu media
yang biasanya terjadi penjedalan. Pektin akan semakin sulit larut jika telah terdapat banyak bahan padatan pada suatu medium. Untuk memudahkan pelarutan, pektin dapat dicampur dengan padatan yang mudah larut seperti
cepat. Karena pektin mempunyai sifat koloid yang menyebabkan rasa sentuhan di
mulut yang dikehendaki dalam air buah. Pektin dapat juga ditambahkan pada rekonstitusi air buah untuk memperoleh konsistensi seperti keadaan aslinya
(Cahyadi, 2006).
Pektin memiliki banyak kegunaan yang dapat kita manfaatkan dalam kehidupan sehari-hari. Di bidang farmasi pektin dikenal sebagai bahan yang
bersifat potensiator dan memperpanjang pengaruh antibiotik, hormon-hormon dan obat-obatan sulfat dan analgesik-analgesik. Pektin juga digunakan sebagai
emulsifier bagi preparat cair dan sirup, obat diare pada anak-anak, obat penawar racun logam, bahan penurun daya racun dan meningkatkan daya larut obat sulfa, memperpanjang kerja hormon dan antibiotika, bahan pelembar perban (pembalut
luka) guna menyerap kotoran dan jaringan yang rusak serta bahan kosmetik, oral atau injeksi untuk mencegah pendarahan (Chahyaditha, 2011).
Pektin juga berfungsi sebagai biosorben logam berat dimana pektin
merupakan salah satu komponen pada tumbuhan yang banyak mengandung gugus aktif, yaitu komponen yang berperan penting dalam proses biosorpsi. Pektin yang
dapat diaplikasikan sebagai biosorben logam berat adalah pektin bermetoksil rendah (LMP) yang gapat langsung diambil dari tanaman yang mengandung LMP atau dari HMP yang mengalami proses demetilasi. Beberapa penelitian
Proses Ekstraksi Pektin Kulit Durian
Ekstraksi
Pektin dapat diekstraksi dengan pemanasan selama 4 jam pada suhu 90°C
dengan penambahan asam klorida hingga pH 2. Filtrat yang diperoleh diendapkan dengan menggunakan etanol asam (HCl 4% dalam etanol 95%) dan kemudian dicuci beberapa kali menggunakan etanol 95% (Wong, et al., 2008). Lamanya
waktu ekstraksi yang dilakukan mempengaruhi berat pektin yang didapat, semakin lama waktu ekstraksi yang dilakukan maka semakin besar pula berat
pektin yang diperoleh dan kenaikan berat pektin sejalan dengan peningkatan suhu pada proses ekstraksi (Akhmalludin dan Kurniawan, 2009).
Penggunaan asam dalam ekstraksi pektin adalah untuk menghidrolisis
protopektin menjadi pektin yang larut dalam air ataupun membebaskan pektin dari ikatan dengan senyawa lain, misalnya selulosa. Protopektin menjadi pektin merupakan makromolekul yang merupakan berat molekul tinggi, terbentuk
antara rantai molekul pektin satu sama lain atau dengan polimer lain. Protopektin tidak larut karena dalam bentuk garam kalsium-magnesium pektinat. Proses
pelarutan protopektin menjadi pektin terjadi karena adanya penggantian ion kalsium dan magnesium oleh ion hidrogen ataupun karena putusnya ikatan antara pektin dan selulosa. Semakin tinggi konsentrasi ion hidrogen (pH) makin rendah
kemampuan menggantikan ion kalsium dan magnesium ataupun memutus ikatan dengan selulosa akan semakin tinggi pula dan pektin yang larut akan bertambah
Berikut adalah karakteristik dari Asam Klorida (HCl):
Berat molekul : 36,5 kg/kmol
Densitas : 1.180 kg/m³
Titik didih : 110°C
Spesifik gravity : 1,2
Kapasitas panas : 0,191 kkal/kgoC (pada 25oC)
Viskositas : 1,9 mPa.s (pada 25oC) (Tanjung, 2011). Pektin bersifat hidrofilik (suka akan air) dikarenakan gugus hidroksil polar
yang besar dan bergabung dengan gugus karboksil yang terdapat pada molekulnya. Ketika pektin terpisah dalam air, gugus asam akan terionisasi dan air akan mengikat kedua gugus tersebut pada molekulnya. Gugus negatif akan
mengisi molekul pektin5bersama dengan terikatnya air membuat mereka bergabung sehingga mereka dapat membentuk sol yang stabil (Vaclavik dan Christian, 2008).
Berikut adalah karakteristik kimia dari air (H2O): Berat molekul : 18 kg/kmol
Densitas : 997,0479 kg/m³
Titik didih : 100°C
Spesifik gravity : 1
Kapasitas panas : 75,28 J/mol.K (pada 25oC)
Pengendapan
Pengendapan merupakan proses pemisahan pektin dari larutan dengan cara
pengendapan senyawa pektinnya. Biasanya dilakukan dengan spray drying,
salting out dan dengan penambahan bahan pelarut organik seperti alkohol dan
aseton. Spray drying jarang dilakukan karena mahal. Pengendapan dengan salting out juga tidak banyak dilakukan karena kesulitan untuk memisahkan pektin yang
dihasilkan dan garam yang digunakan. Pengendapan dengan alkohol merupakan cara yang pertama kali digunakan, menghasilkan pektin yang kurang murni karena
alkohol tidak hanya mengendapkan pektin, tetapi juga senyawa lain seperti dekstrin dan hemiselulosa. Pengendapan dengan aseton lebih disukai karena dapat membentuk endapan yang tegar sehingga mudah dipisahkan dari asetonnya
(Akhmalludin dan Kurniawan, 2009).
Pada proses ekstraksi pektin kulit durian ini menggunakan etanol baik sebagai cairan pengendap maupun pencuci. Etanol merupakan nama IUPAC dari
alkohol. Beberapa sifat-sifat kimia yang dimiliki etanol tercantum dalam Tabel 5 berikut.
Tabel 5. Sifat kimia etanol
(Sumber: Ilmu Kimia, 2013).
Alkohol umumnya berwujud cair dan memiliki sifat mudah menguap
(volatil) tergantung pada panjang rantai karbon utamanya (semakin pendek rantai C, semakin volatil). Pembentukan ester dari alkohol dapat dilakukan dengan
mereaksikan alkohol dengan asam karboksilat. Dalam reaksi ini akan dihasilkan
Rumus Struktur CH3CH2OH
Nama IUPAC Etanol
Nama Umum Etil alkohol
Titik Leleh (oC) -114,7
Titik Didih (oC) 78,5
air dan ester. Molekul air dibentuk dari gugus -OH yang berasal dari karboksilat
dan hidrogen yang berasal dari gugus alkohol. Mekanisme reaksi esterifikasi secara umum ditunjukkan pada Gambar 4.
Gambar 4. Mekanisme reaksi esterifikasi (Chemistry, 2010).
Pencucian
Proses ini dimaksudkan agar pektin dapat bebas dari senyawa-senyawa
lain. Pencucian pektin dengan alkohol menghasilkan jumlah pektin yang tidak terlalu jauh dengan pencucian tanpa menggunakan alkohol, namun pektin yang
dihasilkan memberikan warna yang jauh lebih baik yaitu putih kekuningan. Warna putih kekuningan ini didapat dari pektin kulit cokelat (Akhmalludin dan Kurniawan, 2009).
Pektin masam ditambah dengan alkohol 95 % kemudian diaduk. Setiap 1 liter pektin masam ditambah dengan 1,5 liter alkohol 95 %. Setelah itu dilakukan
penyaringan dengan kain saring. Hal ini bertujuan agar pektin yang disaring nantinya tidak akan masam lagi. Semakin banyak lembaran dari kain saring tersebut akan semakin baik. Namun, lembaran kain saring yang optimal adalah
kain saring empat lembar. Setelah disaring, hasil yang diperoleh disebut pektin basah. Adapun pektin yang tidak bereaksi asam ialah pektin yang tidak berwarna
merah bila ditambah dengan indikator phenolftalein (Ristek, 2007).
Pengeringan
Pektin basah dijemur sampai kering atau dikeringkan dengan pengeringan pada suhu 40-60oC selama 6-10 jam sampai kadar air di bawah 9 %. Hasil yang diperoleh disebut pektin kering (Ristek, 2007). Parameter-parameter yang
digunakan untuk menentukan kualitas pektin antara lain seperti kadar air, kadar impurities, kadar asam galakturonat dan kadar esterifikasi pektin. Total produksi
pektin di seluruh dunia setiap tahunnya diperkirakan sebanyak 80.000 ton dengan nilai ekonomi lebih dari 300 juta dollar Amerika Serikat. Dimana konsumsi negara-negara Eropa Barat sebanyak 36%, Amerika Serikat 32%, Asia 25% dan
Waktu dan Tempat Penelitian
Penelitian ini dilaksanakan di Laboratorium Teknologi Pangan
Fakultas Pertanian Universitas Sumatera Utara. Penelitian dilakukan pada bulan Juni sampai Juli 2013.
Bahan Penelitian
Bahan baku yang digunakan dalam penelitian ini adalah limbah kulit durian yang diperoleh dari pedagang buah durian “Ucok Durian” yang berada di Jalan Iskandar Muda, Medan.
Reagensia Penelitian
Reagensia yang digunakan dalam penelitian ini adalah asam klorida (HCl) pekat 37% (PA), etanol teknis 96% yang dibutuhkan dalam pengendapan dan
pencucian, natrium hidroksida (NaOH) dengan konsentrasi 0,1478N dan 0,25N, indikator phenolphtalein serta aquadest.
Alat Penelitian
Adapun alat yang digunakan dalam penelitian ini yaitu blender, kain
saring, oven, timbangan, tanur, pH meter, gelas ukur, desikator, hot plate, beaker glass, water bath, statis, buret, dan peralatan lainnya.
Metode Penelitian
Penelitian ini dilakukan dengan menggunakan rancangan acak lengkap (RAL)
yang terdiri dari dua faktor, yaitu :
Faktor I : Metode pencucian (M), terdiri dari 2 taraf, yaitu :
M1 = Dengan Alkohol
M2 = Tanpa Alkohol
Faktor II : Jumlah Lapisan Penyaringan (T), terdiri dari 6 taraf, yaitu:
T1 = 1 lembar
T2 = 2 lembar
T3 = 3 lembar
T4 = 4 lembar
T5 = 5 lembar
T6 = 6 lembar
Banyaknya kombinasi perlakuan atau Treatment Combination (Tc) adalah
2 x 6 = 12, maka jumlah ulangan (n) minimum adalah sebagai berikut :
Tc (n-1) ≥ 15
12 (n-1) ≥ 15
12 n ≥ 27
n ≥ 2,25 ... dibulatkan menjadi 3
Jadi, untuk ketelitian dalam penelitian ini dilakukan ulangan sebanyak 3 kali.
Model Rancangan (Bangun, 1991)
Penelitian ini dilakukan dengan model rancangan acak lengkap (RAL) dua
faktorial dengan model sebagai berikut :
Ŷijk= µ + αi+ βj+ (αβ)ij+ εijk
dimana:
Ŷijk : Hasil pengamatan dari faktor M pada taraf ke-i dan faktor T pada taraf
ke-j dalam ulangan ke-k
µ : Efek nilai tengah
αi : Efek faktor M pada taraf ke-i
βj : Efek faktor T pada taraf ke-j
(αβ)ij : Efek interaksi faktor M pada taraf ke-i dan faktor T pada taraf ke-j
εijk : Efek galat dari faktor M pada taraf ke-i dan faktor T pada taraf ke-j
dalam ulangan ke-k
Apabila diperoleh hasil yang berbeda nyata dan sangat nyata maka uji
dilanjutkan dengan uji beda rataan, menggunakan uji Least Significant Range
(LSR).
Pelaksanaan Penelitian
Kegiatan yang akan dilakukan dalam penelitian ini terdiri dari dua tahap, yaitu :
Tahap 1 : Preparasi Sampel
a. Preparasi Sampel
Sampel yang digunakan adalah durian dari Jl. Iskandar Muda Medan. Bagian
kulit yang digunakan adalah bagian kulit dalam yang berwarna putih dengan cara
mengiris kulit bagian terluar. Kemudian bagian dalam kulit tersebut dicuci bersih
Tahap 2 : Ekstraksi Pektin
a. Ekstraksi
Kulit durian bagian dalam yang telah dikupas kulit bagian luarnya ditimbang
500 gram dan dipotong-potong. Kemudian ditambahkan air 1 : 3 untuk
mempermudah dalam pemblenderan. Dihaluskan bahan dengan blender,
kemudian ditambahkan dengan larutan HCl 5% hingga pH 2, kemudian
dipanaskan pada suhu 90oC selama 4 jam dengan memanaskannya sampai suhu
90oC dan ketika suhunya telah tercapai maka api akan dikecilkan dan
dipertahankan agar suhunya tetap. Selanjutnya disaring menggunakan kain saring
60 mesh dengan 6 taraf berbeda yaitu 1 lembar, 2 lembar, 3 lembar, 4 lembar, 5
lembar, dan 6 lembar. Filtratnya diambil dan didinginkan pada suhu ruang.
b. Pengendapan
Pengendapan dilakukan dengan penambahan pengendap etanol dengan
konsentrasi etanol 95% masing-masing 1 : 1 dari filtrat yang diambil dan
didiamkan dengan waktu 14 jam. Kemudian disaring menggunakan kain saring
sehingga diperoleh bagian gelnya.
c. Pencucian
Setelah diperoleh gelnya dilakukan pencucian dengan 2 taraf berbeda, yaitu
dengan alkohol 95% dan tanpa alkohol. Serta disaring dan diperas kembali untuk
mengeringkannya dari alkohol.
d. Pengeringan
Setelah didapat pektin basah, dikeringkan pada suhu 40oC selama 7 jam.
Kemudian pektin kering diblender hingga halus dan diayak dengan menggunakan
Pengamatan dan pengukuran data
Pengamatan dan pengukuran data dilakukan dengan cara analisa. Pada pektin kulit
durian tadi dilakukan pengujian rendemen, kadar air, kadar abu, berat ekivalen,
kandungan metoksil, kadar galakturonat, dan warna pektin yang dihasilkan.
1. Rendemen
Menimbang hasil pektin yang telah dikeringkan dari masing-masing perlakuan
dan membandingkannya dengan kulit durian yang telah dikupas dari bagian yang
tajam.
massa pektin kering
% Rendemen = x 100%
massa kulit durian (bagian putih)
2. Kadar air (Ranganna, 1977)
Sebanyak 1 gram contoh dikeringkan di dalam oven pada suhu 105oC, selama
4 jam. Selanjutnya didinginkan dalam desikator dan ditimbang sampai diperoleh
bobot yang tetap.
berat awal - berat akhir
% Kadar Air (bb) = x 100%
berat awal
3. Kadar abu (Sudarmadji, dkk., 1989)
Penentuan kadar abu dilakukan dengan menggunakan muffle. Bahan ditimbang sebanyak 5 g, kemudian dikeringkan dalam oven terlebih dahulu selama 5 jam
dengan suhu 105oC.Didinginkan dalam desikator selama 15 menit. Bahan yang sudah kering dimasukkan ke dalam muffle dengan suhu 100oC selama 1 jam,
desikator selama 15 menit lalu ditimbang beratnya. Kadar abu dihitung dengan
rumus:
berat abu (g)
Kadar Abu (%) = x 100% berat sampel (g)
4. Berat ekivalen (Ranganna, 1977)
Pektin sebanyak 0,5 gram dibasahi dengan 5 ml etanol dan dilarutkan dalam
100 ml air suling bebas karbonat yang berisi 1 gram NaCl. Larutan hasil
campuran tersebut dititrasi perlahan-lahan dengan 0,1 N NaOH memakai
indikator fenol merah sampai terjadi perubahan menjadi merah kekuningan
(pH 7,5) yang bertahan sedikitnya 30 detik.
bobot pektin (mg)
Berat Ekivalen (BE) =
ml NaOH
5. Kandungan metoksil (Ranganna, 1977)
Larutan netral dari penentuan BE ditambah 25 ml larutan 0,25 N NaOH,
dikocok dan dibiarkan selama 30 menit pada suhu kamar dalam keadaan tertutup.
Selanjutnya ditambahkan 25 ml larutan 0,25 N HCl dan dititrasi dengan larutan
0,1 N NaOH dengan indikator fenol merah sampai titik akhir seperti pada
penentuan BE.
ml NaOH x 31 x N NaOH
Kandungan metoksil (%) = x 100%
Bobot contoh (mg)
Nilai 31 didapatkan dari bobot molekul metoksil yang berupa CH3O
6. Kadar galakturonat (McCready, 1965)
Kadar galakturonat dihitung dari mek (miliekivalen) NaOH yang diperoleh dari
mek (BE + metoksil) x 176
Kadar galakturonat (%) = x 100%
bobot contoh (mg)
Nilai 176 diperoleh dari berat ekivalen terendah asam pektat
7. Warna
Dilakukan dengan melihat warna tepung pektin yang dihasilkan dengan parameter
Gambar 5. Skema ekstraksi pektin dari kulit durian
Dipanaskan 90oC selama 4 jam
Filtrat didinginkan pada suhu ruang Diblender dengan penambahan air 1:3
Ditambahkan HCl 5% hingga pH 2
Ditambahkan etanol 95% Disaring dengan kain Diendapkan selama 14 jam
Diberi perlakuan
Dikeringkan pada suhu 40oC selama 7 jam Disaring gel dengan kain saring
Jumlah Lapisan
Diblender hingga halus
Pektin kering kulit Pektin basah
Disaring
Gel
Diayak menggunakan ayakan 80 mesh
Pengaruh jumlah lapisan penyaringan terhadap parameter yang diamati
Secara umum hasil penelitian yang dilakukan menunjukkan bahwa teknik pencucian memberikan pengaruh terhadap rendemen, kadar air, kadar abu, berat
ekivalen, kandungan metoksil, kadar galakturonat, dan warna pada pektin kulit durian seperti pada Tabel 6 berikut ini.
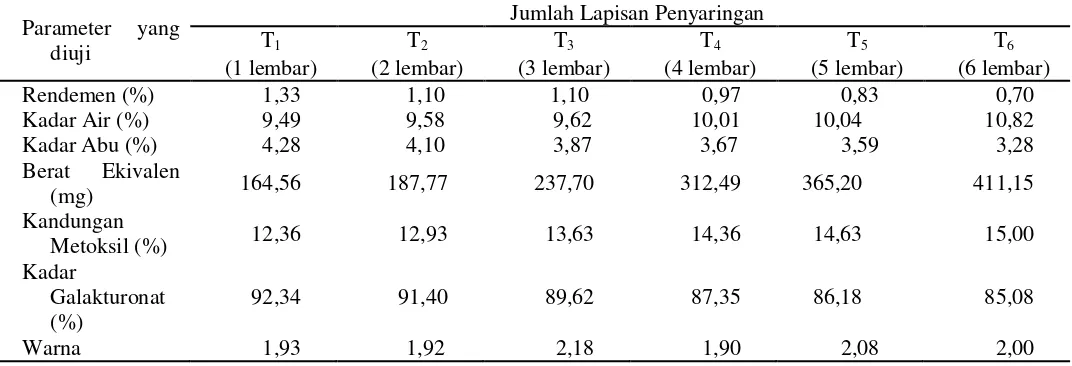
Tabel 6. Pengaruh jumlah lapisan penyaringan terhadap parameter yang diamati
Parameter yang diuji
Jumlah Lapisan Penyaringan
T1 T2 T3 T4 T5 T6
(1 lembar) (2 lembar) (3 lembar) (4 lembar) (5 lembar) (6 lembar)
Rendemen (%) 1,33 1,10 1,10 0,97 0,83 0,70
Kadar Air (%) 9,49 9,58 9,62 10,01 10,04 10,82
Kadar Abu (%) 4,28 4,10 3,87 3,67 3,59 3,28
Berat Ekivalen
(mg) 164,56 187,77 237,70 312,49 365,20 411,15
Kandungan
Tabel 6 menunjukkan bahwa jumlah lapisan penyaringan memberikan
pengaruh terhadap parameter yang diuji. Pada Tabel 6 menunjukkan bahwa rendemen tertinggi terdapat pada perlakuan T1 (1 lembar) yaitu sebesar 1,33% dan
terendah terdapat pada T6 (6 lembar) yaitu sebesar 0,70%. Kadar air tertinggi terdapat pada perlakuan T6 (6 lembar) yaitu sebesar 10,82% dan terendah terdapat pada T1 (1 lembar) yaitu sebesar 9,49%. Kadar abu tertinggi terdapat pada
perlakuan T1 (1 lembar) yaitu sebesar 4,28% dan terendah terdapat pada perlakuan T6 (6 lembar) yaitu sebesar 3,28%. Berat ekivalen tertinggi terdapat pada
perlakuan T6 (6 lembar) yaitu sebesar 411,15 mg dan terendah terdapat pada perlakuan T1 (1 lembar) yaitu sebesar 164,56 mg. Kandungan metoksil tertinggi
terdapat pada perlakuan T6 (6 lembar) yaitu sebesar 15,00% dan terendah terdapat
pada perlakuan T1 (1 lembar) yaitu sebesar 12,36%. Kadar galakturonat tertinggi terdapat pada perlakuan T1 (1 lembar) yaitu sebesar 92,34% dan terendah terdapat
pada perlakuan T6 (6 lembar) yaitu sebesar 85,08%. Uji organoleptik warna tertinggi terdapat pada T3 (3 lembar) yaitu sebesar 2,18 dan terendah terdapat pada T4 (4 lembar) yaitu 1,90.
Pengaruh metode pencucian terhadap parameter yang diamati
Hasil penelitian menunjukkan bahwa metode pencucian pada pektin kulit durian yang dihasilkan memberikan pengaruh terhadap rendemen, kadar air, kadar
abu, berat ekivalen, kandungan metoksil, kadar galakturonat, dan warna seperti pada Tabel 7 berikut ini.
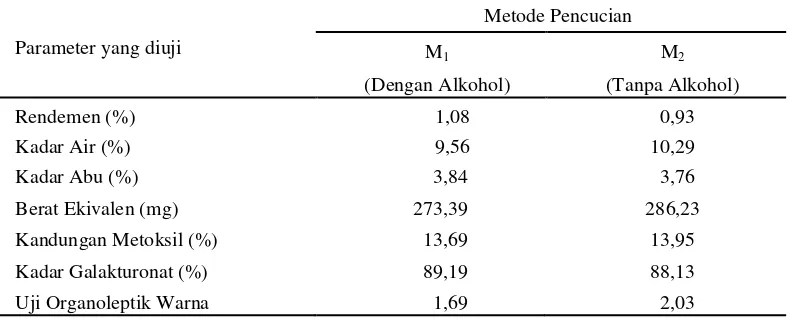
Tabel 7. Pengaruh metode pencucian terhadap parameter yang diamati
Parameter yang diuji
Metode Pencucian
M1 M2
(Dengan Alkohol) (Tanpa Alkohol) Rendemen (%) 1,08 0,93
Tabel 7 menunjukkan bahwa metode pencucian memberikan pengaruh
terhadap parameter yang diuji. Tabel 7 menunjukkan bahwa rendemen tertinggi terdapat pada perlakuan M1 (dengan alkohol) yaitu sebesar 1,08% dan terendah terdapat pada perlakuan M2 (tanpa alkohol) yaitu sebesar 0,93%. Kadar air
abu tertinggi terdapat pada perlakuan M1 (dengan alkohol) yaitu sebesar 3,84%
dan terendah terdapat pada perlakuan M2 (tanpa alkohol) yaitu sebesar 3,76%. Berat ekivalen tertinggi terdapat pada perlakuan M2 (tanpa alkohol) yaitu sebesar
286,23 mg dan terendah terdapat pada perlakuan M1 (dengan alkohol) yaitu sebesar 273,39 mg. Kandungan metoksil tertinggi terdapat pada perlakuan M2 (tanpa alkohol) yaitu sebesar 13,95% dan terendah terdapat pada perlakuan M1
(dengan alkohol) yaitu sebesar 13,69%. Kadar galakturonat tertinggi terdapat pada perlakuan M1 (dengan alkohol) yaitu sebesar 89,19% dan terendah terdapat pada
perlakuan M2 (tanpa alkohol) yaitu sebesar 88,13%. Uji organoleptik warna tertinggi terdapat pada perlakuan M2 (tanpa alkohol) yaitu sebesar 2,03 artinya warna pektin semakin tua dan terendah terdapat pada perlakuan M1 (dengan
alkohol) yaitu sebesar 1,69 artinya warna pektin semakin cerah/muda.
Rendemen
Pengaruh jumlah lapisan penyaringan terhadap rendemen
Daftar sidik ragam (Lampiran 1) menunjukkan bahwa jumlah lapisan penyaringan memberikan pengaruh yang berbeda sangat nyata (P<0,01) terhadap rendemen pektin kulit durian yang dihasilkan. Hasil pengujian dengan LSR
Keterangan: Notasi huruf yang berbeda menunjukkan pengaruh yang berbeda nyata pada taraf 5% (huruf kecil) dan berbeda sangat nyata pada taraf 1% (huruf besar).
Tabel 8 menunjukkan bahwa perlakuan T1 berbeda sangat nyata dengan T2, T3, T4, T5, dan T6. Perlakuan T2 tidak berbeda nyata dengan T3,namun berbeda
sangat nyata dengan T4, T5, dan T6. Perlakuan T3 berbeda sangat nyata dengan T4, T5, dan T6. Perlakuan T4 berbeda sangat nyata dengan T5 dan T6, serta perlakuan
T5 berbeda sangat nyata dengan T6. Rendemen tertinggi terdapat pada perlakuan T1 (1 lembar) yaitu sebesar 1,333% dan terendah terdapat pada perlakuan T6 (6 lembar) yaitu sebesar 0,7%. Terjadinya penurunan rendemen ini disebabkan
karena semakin banyak tingkat lembaran saringan yang ada, maka akan semakin banyak pektin basah yang masih terhambat di saringannya sehingga menjadi tidak
efektif. Hubungan jumlah lapisan penyaringan yang berbeda dengan rendemen ditunjukkan pada Gambar 6.
Tabel 8. Uji LSR efek utama pengaruh jumlah lapisan penyaringan terhadap rendemen (%)
Jarak LSR Jumlah lapisan
penyaringan Rataan
Notasi
0,05 0,01 0,05 0,01
- - - T1 = 1 lembar 1,333 a A
2 0,0688 0,0933 T2 = 2 lembar 1,100 b B
3 0,0724 0,0973 T3 = 3 lembar 1,100 b B
4 0,0745 0,0999 T4 = 4 lembar 0,967 c C
5 0,0761 0,1018 T5 = 5 lembar 0,833 d D
Gambar 6. Hubungan jumlah lapisan penyaringan yang berbeda dengan rendemen
Pengaruh metode pencucian terhadap rendemen
Daftar sidik ragam (Lampiran 1) menunjukkan bahwa metode pencucian memberikan pengaruh yang berbeda sangat nyata (P<0,01) terhadap rendemen pektin kulit durian yang dihasilkan. Hasil pengujian dengan LSR menunjukkan
pengaruh metode pencucian terhadap rendemen tiap-tiap perlakuan yang ditunjukkan pada Tabel 9.
Tabel 9. Uji LSR efek utama pengaruh metode pencucian terhadap rendemen (%)
Jarak LSR Metode pencucian Rataan Notasi
0,05 0,01 0,05 0,01
- - - M1 = Dengan Alkohol 1,078 a A
2 0,0397 0,0539 M2 = Tanpa Alkohol 0,933 b B
Keterangan: Notasi huruf yang berbeda menunjukkan pengaruh yang berbeda nyata pada taraf 5% (huruf kecil) dan berbeda sangat nyata pada taraf 1% (huruf besar).
Tabel 9 menunjukkan bahwa perlakuan M1 berbeda sangat nyata terhadap
M2. Rendemen tertinggi terdapat pada perlakuan M1 (dengan alkohol) yaitu sebesar 1,078% dan rendemen terendah terdapat pada perlakuan M2 (tanpa alkohol) yaitu sebesar 0,933%. Perlakuan pencucian dengan alkohol ini pada
1,33
1 lembar 2 lembar 3 lembar 4 lembar 5 lembar 6 lembar
kenyataannya dapat membuat pektin basah menggumpal menjadi satu sehingga
pada akhirnya didapat kontur pektin basah yang lebih konsisten dan lebih kering, walaupun perbedaannya tidak terlalu jauh. Hal ini sesuai dengan Akhmalludin dan
Kurniawan (2009) yang menyatakan bahwa pencucian pektin dengan alkohol menghasilkan jumlah pektin yang tidak terlalu jauh dibandingkan dengan pencucian tanpa menggunakan alkohol. Hubungan metode pencucian yang
berbeda dengan rendemen ditunjukkan pada Gambar 7.
Gambar 7. Hubungan metode pencucian yang berbeda dengan rendemen
Pengaruh interaksi jumlah lapisan penyaringan dan metode pencucian terhadap rendemen
Daftar sidik ragam (Lampiran 1) menunjukkan bahwa interaksi jumlah
lapisan penyaringan dan metode pencucian memberikan pengaruh yang berbeda sangat nyata (P<0,01) terhadap rendemen pektin kulit durian yang dihasilkan. Hasil pengujian dengan LSR menunjukkan pengaruh interaksi jumlah lapisan
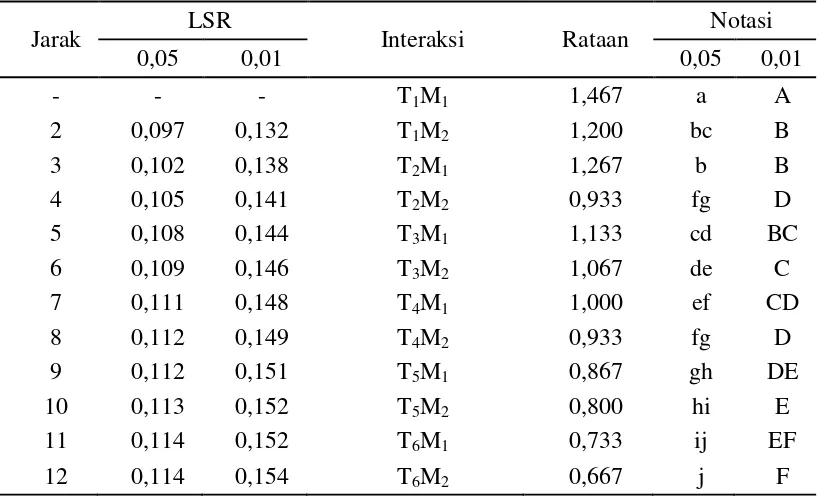
penyaringan dan metode pencucian terhadap rendemen tiap-tiap perlakuan yang ditunjukkan pada Tabel 10.
Keterangan: Notasi huruf yang berbeda menunjukkan pengaruh yang berbeda nyata pada taraf 5% (huruf kecil) dan berbeda sangat nyata pada taraf 1% (huruf besar).
Tabel 10 menunjukkan bahwa kombinasi perlakuan antara jumlah lapisan penyaringan dan metode pencucian memberikan pengaruh yang berbeda sangat nyata terhadap rendemen. Rendemen tertinggi diperoleh dari kombinasi perlakuan
T1M1 yaitu sebesar 1,467% dan terendah diperoleh dari kombinasi perlakuan T6M2 yaitu sebesar 0,667%. Hal ini diakibatkan karena semakin banyak tingkat
lembaran saringan yang ada, maka akan semakin banyak pektin basah yang masih terhambat di saringannya sehingga menjadi tidak efektif serta pencucian dengan alkohol yang dapat meningkatkan rendemen (Akhmalludin dan Kurniawan, 2009).
Interaksi jumlah lapisan penyaringan dan metode pencucian terhadap rendemen ditunjukkan pada Gambar 8.
Gambar 8. Interaksi jumlah lapisan penyaringan dan metode pencucian terhadap rendemen
Kadar Air
Pengaruh jumlah lapisan penyaringan terhadap kadar air
Daftar sidik ragam (Lampiran 2) menunjukkan bahwa jumlah lapisan penyaringan memberikan pengaruh yang berbeda sangat nyata (P<0,01) terhadap
kadar air pektin kulit durian yang dihasilkan. Hasil pengujian dengan LSR menunjukkan pengaruh teknik pencucian terhadap kadar air tiap-tiap perlakuan
yang ditunjukkan pada Tabel 11.
Keterangan: Notasi huruf yang berbeda menunjukkan pengaruh yang berbeda nyata pada taraf 5% (huruf kecil) dan berbeda sangat nyata pada taraf 1% (huruf besar).
0,00
Tabel 11. Uji LSR efek utama pengaruh jumlah lapisan penyaringan terhadap kadar air (%)
Jarak LSR Jumlah lapisan
Tabel 11 menunjukkan bahwa perlakuan T1 tidak berbeda nyata dengan T2
dan T3, namun berbeda sangat nyata dengan T4, T5, dan T6. Perlakuan T2 tidak berbeda nyata dengan T3,namun berbeda nyata dengan T4, T5, dan berbeda sangat
nyata dengan T6. Perlakuan T3 berbeda nyata dengan T4, T5, dan berbeda sangat nyata dengan T6. Perlakuan T4 tidak berbeda nyata dengan T5, namun berbeda sangat nyata dengan T6. Perlakuan T5 berbeda sangat nyata dengan T6. Kadar air
tertinggi terdapat pada perlakuan T6 (6 lembar) yaitu sebesar 10,818% dan terendah terdapat pada perlakuan T1 (1 lembar) yaitu sebesar 9,485%. Terjadinya
peningkatan kadar air ini disebabkan karena semakin banyak lembaran saringan yang ada, maka akan semakin banyak pektin basah yang masih terhambat di saringannya sehingga kadar air pada pektin pun akan semakin meningkat.
Hubungan jumlah lapisan penyaringan yang berbeda dengan kadar air ditunjukkan pada Gambar 9.
Gambar 9. Hubungan jumlah lapisan penyaringan yang berbeda dengan kadar air
1 lembar 2 lembar 3 lembar 4 lembar 5 lembar 6 lembar
Pengaruh metode pencucian terhadap kadar air
Daftar sidik ragam (Lampiran 2) menunjukkan bahwa metode pencucian memberikan pengaruh yang berbeda sangat nyata (P<0,01) terhadap kadar air
pektin kulit durian yang dihasilkan. Hasil pengujian dengan LSR menunjukkan pengaruh metode pencucian terhadap kadar air tiap-tiap perlakuan menunjukkan pada Tabel 12.
Tabel 12. Uji LSR efek utama pengaruh metode pencucian terhadap kadar air (%)
Jarak LSR Metode pencucian Rataan Notasi
0,05 0,01 0,05 0,01
- - - M1 = Dengan Alkohol 9,562 b B
2 0,194 0,263 M2 = Tanpa Alkohol 10,288 a A
Keterangan: Notasi huruf yang berbeda menunjukkan pengaruh yang berbeda nyata pada taraf 5% (huruf kecil) dan berbeda sangat nyata pada taraf 1% (huruf besar).
Tabel 12 menunjukkan bahwa perlakuan M1 berbeda sangat nyata terhadap
M2. Kadar air tertinggi terdapat pada perlakuan M2 (tanpa alkohol) yaitu sebesar 10,288% dan terendah terdapat pada perlakuan M1 (dengan alkohol) yaitu sebesar 9,562%. Perlakuan pencucian dengan alkohol ini pada kenyataannya dapat
membuat pektin basah menggumpal menjadi satu sehingga pada akhirnya didapat kontur pektin basah yang lebih konsisten dan lebih kering sehingga pektin basah
yang mengalami pencucian dengan alkohol kadar airnya semakin rendah dan sebaliknya yang tidak mengalami pencucian akan lebih tinggi kadar airnya. Hubungan metode pencucian yang berbeda dengan kadar air ditunjukkan pada
Gambar 10. Hubungan metode pencucian yang berbeda dengan kadar air
Pengaruh interaksi jumlah lapisan penyaringan dan metode pencucian terhadap kadar air
Daftar sidik ragam (Lampiran 2) menunjukkan bahwa interaksi jumlah
lapisan penyaringan dan metode pencucian memberikan pengaruh yang berbeda tidak nyata (P>0,05) terhadap kadar air pektin kulit durian yang dihasilkan,
sehingga hasil uji LSR tidak dilanjutkan.
Kadar Abu
Pengaruh jumlah lapisan penyaringan terhadap kadar abu
Daftar sidik ragam (Lampiran 3) menunjukkan bahwa jumlah lapisan
penyaringan memberikan pengaruh yang berbeda sangat nyata (P<0,01) terhadap kadar abu pektin kulit durian yang dihasilkan. Hasil pengujian dengan LSR
menunjukkan pengaruh jumlah lapisan penyaringan terhadap kadar abu tiap-tiap perlakuan yang ditunjukkan pada Tabel 13.
Keterangan: Notasi huruf yang berbeda menunjukkan pengaruh yang berbeda nyata pada taraf 5% (huruf kecil) dan berbeda sangat nyata pada taraf 1% (huruf besar)
Tabel 13 menunjukkan bahwa perlakuan T1 berbeda sangat nyata dengan
T2, T3, T4, T5, dan T6. Perlakuan T2 berbeda sangat nyata dengan T3,T4, T5, dan T6. Perlakuan T3 berbeda sangat nyata dengan T4, T5, dan T6. Perlakuan T4 tidak
berbeda nyata dengan T5 namun berbeda sangat nyata T6, serta perlakuan T5 berbeda sangat nyata dengan T6. Kadar abu tertinggi terdapat pada perlakuan T1 (1 lembar) yaitu sebesar 4,282% dan terendah terdapat pada perlakuan T6 (6 lembar)
yaitu sebesar 3,280%. Terjadinya penurunan kadar abu ini adalah karena jumlah lapisan penyaringan yang semakin banyak sehingga mengakibatkan peningkatan
kadar air dan penurunan kadar abu pada pektin. Hubungan jumlah lapisan penyaringan yang berbeda dengan kadar abu ditunjukkan pada Gambar 11.
Jarak LSR Jumlah lapisan
penyaringan Rataan
Notasi
0,05 0,01 0,05 0,01
- - - T1 = 1 lembar 4,282 a A
2 0,085 0,115 T2 = 2 lembar 4,098 b B
3 0,089 0,120 T3 = 3 lembar 3,870 c C
4 0,091 0,123 T4 = 4 lembar 3,668 d D
5 0,094 0,125 T5 = 5 lembar 3,590 de DE
Gambar 11. Hubungan jumlah lapisan penyaringan yang berbeda dengan kadar abu
Pengaruh metode pencucian terhadap kadar abu
Daftar sidik ragam (Lampiran 3) menunjukkan bahwa metode pencucian memberikan pengaruh yang berbeda nyata (P<0,05) terhadap kadar abu pektin
kulit durian yang dihasilkan. Hasil pengujian dengan LSR menunjukkan pengaruh metode pencucian terhadap kadar abu tiap-tiap perlakuan yang ditunjukkan pada Tabel 14.
4,28
4,10
3,87
3,67 3,59
3,28
2,00 2,50 3,00 3,50 4,00 4,50
1 lembar 2 lembar 3 lembar 4 lembar 5 lembar 6 lembar
K
ada
r A
bu (
%)
Keterangan: Notasi huruf yang berbeda menunjukkan pengaruh yang berbeda nyata pada taraf 5% (huruf kecil) dan berbeda sangat nyata pada taraf 1% (huruf besar).
Tabel 14 menunjukkan bahwa perlakuan M1 berbeda nyata terhadap M2. Kadar abu tertinggi terdapat pada perlakuan M1 (dengan alkohol) yaitu sebesar
3,838% dan terendah terdapat pada perlakuan M2 (tanpa alkohol) yaitu sebesar 3,758%. Kadar abu pada perlakuan M1 lebih tinggi daripada M2 karena dengan pencucian dengan alkohol, mineral asam akan terlarut bersama dengan pektin
sehingga menambah kadar abu pektin. Hal ini dapat dianalogikan dengan pernyataan Kalapathy dan Proctor (2001) dalam Hariyati (2006) yang menyatakan
bahwa mineral yang terlarut akan ikut mengendap bercampur dengan pektin pada saat pengendapan dengan alkohol. Dapat terlihat jelas bahwa penambahan alkohol akan meningkatkan kadar abu. Hubungan metode pencucian yang berbeda dengan
kadar abu ditunjukkan pada Gambar 12.
Gambar 12. Hubungan metode pencucian yang berbeda dengan kadar abu
3,84
Tabel 14. Uji LSR efek utama pengaruh metode pencucian terhadap kadar abu (%)
Jarak LSR Metode pencucian Rataan Notasi
0,05 0,01 0,05 0,01
- - - M1 = Dengan Alkohol 3,838 a A
Pengaruh interaksi jumlah lapisan penyaringan dan metode pencucian terhadap kadar abu
Daftar sidik ragam (Lampiran 3) menunjukkan bahwa interaksi jumlah lapisan penyaringan dan metode pencucian memberikan pengaruh yang berbeda nyata (P<0,05) terhadap kadar abu pektin kulit durian yang dihasilkan. Hasil
pengujian dengan LSR menunjukkan pengaruh interaksi jumlah lapisan penyaringan dan metode pencucian terhadap kadar abu tiap-tiap perlakuan yang
ditunjukkan pada Tabel 15.
Keterangan: Notasi huruf yang berbeda menunjukkan pengaruh yang berbeda nyata pada taraf 5% (huruf kecil) dan berbeda sangat nyata pada taraf 1% (huruf besar).
Tabel 15 menunjukkan bahwa kombinasi perlakuan antara jumlah lapisan
penyaringan dan metode pencucian memberikan pengaruh yang berbeda nyata terhadap kadar abu. Kadar abu tertinggi diperoleh dari kombinasi perlakuan T1M1 yaitu sebesar 4,367% dan terendah diperoleh dari kombinasi perlakuan T6M2 yaitu
sebesar 3,237%. Hal ini disebabkan oleh teknik pelembaran yang akan Tabel 15. Uji LSR interaksi jumlah lapisan penyaringan dan metode pencucian
terhadap kadar abu (%)
mengurangi asam, sehingga jika pelembarnya lebih banyak, maka asam akan
semakin menurun. Dengan kata lain, asam semakin meningkat menandakan kadar abu akan mengalami peningkatan juga. Begitu juga dengan penambahan alkohol,
alkohol akan melarutkan mineral yang ada pada pektin sehingga kadar abu pektin akan meningkat.
Sebenarnya kadar abu pektin komersial yang seharusnya maksimum
hanya 1% menurut Food Chemical Codex (1996) dalam Hariyati (2006), namun pada SI diperbolehkan maksimum hingga 10% dan pada kenyataannya diperoleh
hasil yaitu sekitar 3%. Hal ini dipengaruhi oleh kadar abu pada kulit durian adalah 4% (Novita, 2013) dan metode ekstraksi yang belum maksimal sehingga mengakibatkan masih tingginya kadar abu pada pektin yang dihasilkan dan
menjadikan pektin kulit durian ini belum memenuhi standar sebagai pektin dalam pembuatan makanan. Interaksi jumlah lapisan penyaringan dan metode pencucian terhadap kadar abu ditunjukkan pada Gambar 13.
Gambar 13. Interaksi jumlah lapisan penyaringan dan metode pencucian terhadap kadar abu (%)
Pengaruh jumlah lapisan penyaringan terhadap berat ekivalen
Daftar sidik ragam (Lampiran 4) menunjukkan bahwa jumlah lapisan
penyaringan memberikan pengaruh yang berbeda sangat nyata (P<0,01) terhadap berat ekivalen pektin kulit durian yang dihasilkan. Hasil pengujian dengan LSR menunjukkan pengaruh jumlah lapisan penyaringan terhadap berat ekivalen
tiap-tiap perlakuan yang ditunjukkan pada Tabel 16.
Keterangan: Notasi huruf yang berbeda menunjukkan pengaruh yang berbeda nyata pada taraf 5% (huruf kecil) dan berbeda sangat nyata pada taraf 1% (huruf besar).
Tabel 16 menunjukkan bahwa perlakuan T1 tidak berbeda nyata dengan
T2, namun berbeda sangat nyata dengan T3, T4, T5, dan T6. Perlakuan T2 berbeda sangat nyata dengan T3,T4, T5, dan T6. Perlakuan T3 berbeda sangat nyata dengan T4, T5, dan T6. Perlakuan T4 berbeda sangat nyata dengan T5 dan T6, serta
perlakuan T5 tidak berbeda nyata dengan T6. Berat ekivalen tertinggi terdapat pada perlakuan T6 (6 lembar) yaitu sebesar 411,15 mg dan terendah terdapat pada perlakuan T1 (1 lembar) yaitu sebesar 164,56 mg. Terjadinya peningkatan berat
ekivalen ini karena pelembaran yang semakin banyak menyebabkan jumlah asam
pada pektin berkurang. Hal ini sesuai dengan Rouse (1977) dalam Hariyati (2006)
yang menyatakan bahwa semakin rendahnya jumlah asam bebas berarti semakin tinggi berat ekivalen. Hubungan jumlah lapisan penyaringan yang berbeda dengan
berat ekivalen ditunjukkan pada Gambar 14.
Gambar 14. Hubungan jumlah lapisan penyaringan yang berbeda dengan berat
ekivalen
Pengaruh metode pencucian terhadap berat ekivalen
Daftar sidik ragam (Lampiran 4) menunjukkan bahwa metode pencucian memberikan pengaruh yang berbeda tidak nyata (P>0,05) terhadap berat ekivalen pektin kulit durian yang dihasilkan, sehingga hasil uji LSR tidak
dilanjutkan.Pengaruh interaksi jumlah lapisan penyaringan dan metode pencucian terhadap berat ekivalen
1 lembar 2 lembar 3 lembar 4 lembar 5 lembar 6 lembar
Interaksi jumlah lapisan penyaringan dan metode pencucian terhadap berat ekivalen
Daftar analisis sidik ragam (Lampiran 4) menunjukkan bahwa interaksi jumlah lapisan penyaringan dan metode pencucian memberikan pengaruh yang berbeda tidak nyata (P>0,05) terhadap berat ekivalen pektin kulit durian yang
dihasilkan, sehingga hasil uji LSR tidak dilanjutkan.
Kandungan Metoksil
Pengaruh jumlah lapisan penyaringan terhadap kandungan metoksil
Daftar sidik ragam (Lampiran 5) menunjukkan bahwa jumlah lapisan penyaringan memberikan pengaruh yang berbeda sangat nyata (P<0,01) terhadap kandungan metoksil pektin kulit durian yang dihasilkan. Hasil pengujian dengan
LSR menunjukkan pengaruh jumlah lapisan penyaringan terhadap kandungan metoksil tiap-tiap perlakuan yang ditunjukkan pada Tabel 17.
Keterangan: Notasi huruf yang berbeda menunjukkan pengaruh yang berbeda nyata pada taraf 5% (huruf kecil) dan berbeda sangat nyata pada taraf 1% (huruf besar).
Tabel 17 menunjukkan bahwa perlakuan T1 tidak berbeda nyata dengan T2, namun berbeda sangat nyata dengan T3, T4, T5, dan T6. Perlakuan T2 tidak
berbeda nyata dengan T3, namun berbeda sangat nyata dengan T4, T5 dan T6. Tabel 17. Uji LSR efek utama pengaruh jumlah lapisan penyaringan terhadap
kandungan metoksil (%)
Jarak LSR Jumlah lapisan
Perlakuan T3 tidak berbeda nyata dengan T4, namun berbeda sangat nyata dengan
T5, dan T6. Perlakuan T4 tidak berbeda nyata dengan T5 dan T6, serta perlakuan T5 tidak berbeda nyata dengan T6. Kandungan metoksil tertinggi terdapat pada
perlakuan T6 (6 lembar) yaitu sebesar 15,002% dan terendah terdapat pada perlakuan T1 (1 lembar) yaitu sebesar 12,358%. Kandungan metoksil berhubungan dengan berat ekivalen. Semakin besar berat ekivalen, maka semakin
tinggi kandungan metoksilnya (Perina, dkk., 2007). Kandungan metoksil pektin ini sudah sesuai dengan standar yang ada yaitu pektin bermetoksil tinggi adalah
pektin yang mempunyai kandungan metoksil minimal 7% menurut Food Chemical Codex (1996) dalam Hariyati (2006) dan pektin dari limbah pertanian memang pektin bermetoksil tinggi (Kurniasari, dkk., 2012). Hubungan jumlah
lapisan penyaringan yang berbeda dengan kandungan metoksil ditunjukkan pada Gambar 15.
Gambar 15. Hubungan jumlah lapisan penyaringan yang berbeda dengan kandungan metoksil
1 lembar 2 lembar 3 lembar 4 lembar 5 lembar 6 lembar
Pengaruh metode pencucian terhadap kandungan metoksil
Daftar analisis sidik ragam (Lampiran 5) menunjukkan bahwa metode pencucian memberikan pengaruh yang berbeda tidak nyata (P>0,05) terhadap
kandungan metoksil pektin kulit durian yang dihasilkan, sehingga hasil uji LSR tidak dilanjutkan.
Pengaruh interaksi jumlah lapisan penyaringan dan metode pencucian terhadap kandungan metoksil
Daftar sidik ragam (Lampiran 5) menunjukkan bahwa interaksi jumlah
lapisan penyaringan dan metode pencucian memberikan pengaruh yang berbeda tidak nyata (P>0,05) terhadap kandungan metoksil pektin kulit durian yang dihasilkan, sehingga hasil uji LSR tidak dilanjutkan.
Kadar Galakturonat
Pengaruh jumlah lapisan penyaringan terhadap kadar galakturonat
Daftar sidik ragam (Lampiran 6) menunjukkan bahwa jumlah lapisan
penyaringan memberikan pengaruh yang berbeda sangat nyata (P<0,01) terhadap kadar galakturonat pektin kulit durian yang dihasilkan. Hasil pengujian dengan LSR menunjukkan pengaruh jumlah lapisan penyaringan terhadap kadar