ANALI
STRA
DiajuISIS KAN
MAGNE
AWBERR
SPEKT
ukan untuk gelarPROGRA
UNIV
NDUNGA
ESIUM DA
RY (
Fraga
ROFOTO
k melengka Sarjana Fa Univers MIC NAM EKST
FAKU
VERSITA
AN MINER
AN NATR
aria anan
OMETRI
SKRIPSapi salah sa armasi pad sitas Suma OLEH: CA FARAD NIM 111524
TENSI SA
ULTAS FA
AS SUMA
MEDAN
2014
RAL KAL
RIUM PA
nassa
Duc
I SERAPA
SI
ANALI
STRA
DiajuISIS KAN
MAGNE
AWBERR
SPEKT
ukan untuk gelarPROGRA
UNIV
NDUNGA
ESIUM DA
RY (
Fraga
ROFOTO
k melengka Sarjana Fa Univers MIC NAM EKST
FAKU
VERSITA
AN MINER
AN NATR
aria anan
OMETRI
SKRIPSapi salah sa armasi pad sitas Suma OLEH: CA FARAD NIM 111524
TENSI SA
ULTAS FA
AS SUMA
MEDAN
2014
RAL KAL
RIUM PA
nassa
Duc
I SERAPA
SI
PENGESAHAN SKRIPSI
ANALISIS KANDUNGAN MINERAL KALIUM, KALSIUM,
MAGNESIUM DAN NATRIUM PADA BUAH
STRAWBERRY (
Fragaria ananassa
Duchesne.) SECARA
SPEKTROFOTOMETRI SERAPAN ATOM
OLEH:
MICA FARADILLA NIM 111524071
Dipertahankan di Hadapan Panitia Penguji Skripsi Fakultas Farmasi Universitas Sumatera Utara
Pada Tanggal: Disetujui Oleh:
Pembimbing I, Panitia Penguji,
Drs. Ismail, M.Si., Apt. Dr. Ginda Haro, M.Sc., Apt. NIP 195006141980031001 NIP 195108161980031002 Pembimbing II,
Drs. Ismail, M.Si., Apt.
NIP 195006141980031001
Dr. Muchlisyam, M.Si., Apt. NIP 195006221980021001
Dra. Tuty Roida Pardede, M.Si., Apt.
NIP 195401101980032001
Dra. Saleha Salbi, M.Si., Apt.
NIP 194909061980032001
Medan, Januari 2014
Fakultas Farmasi
Universitas Sumatera Utara
Dekan,
KATA PENGANTAR
Alhamdulillah, penulis haturkan ke hadirat Allah Yang Maha Kuasa yang telah melimpahkan rahmat, hidayah dan kemudahan kepada penulis sehingga dapat menyelesaikan penelitian dan penulisan skripsi ini.
Skripsi ini disusun untuk melengkapi salah satu syarat mencapai gelar Sarjana Farmasi pada Fakultas Farmasi Universitas Sumatera Utara, dengan judul Analisis Kandungan Mineral Kalium, Kalsium, Magnesium dan Natrium Pada buah Strawberry (Fragaria ananassa Duchesne.) Secara Spektrofotometri Serapan Atom.
Ibu Dra. Masfria, M.S., Apt., selaku Kepala Laboratorium Kimia Farmasi Kualitatif Fakultas Farmasi USU dan Bapak Prof. Dr. rer. nat. Effendy De Lux Putra, S.U., Apt., selaku Koordinator Laboratorium Penelitian Fakultas Farmasi USU yang telah memberikan izin dan fasilitas untuk penulis sehingga dapat mengerjakan dan menyelesaikan penelitian.
Penulis juga mengucapkan terima kasih dan penghargaan yang tiada terhingga kepada Ayahanda Zairuddin, Ibunda Khairani, serta saudaraku Khalik Fazduani, yang telah memberikan cinta kasih yang tidak ternilai dengan apapun, doa yang tulus serta pengorbanan baik materi maupun non-materi atas segala doa, kasih sayang, dan memberikan semangat. Buat sahabatku Muhammad Habib S dan Juli Handayani P, S.Farm serta Teman-Teman Ekstensi Farmasi USU 2011, terima kasih untuk perhatian, semangat, doa dan kebersamaannya selama ini, serta seluruh pihak yang telah ikut membantu penulis yang tidak dapat disebutkan satu persatu.
Penulis menyadari sepenuhnya bahwa dalam penulisan skripsi ini masih jauh dari kesempurnaan, oleh karena itu penulis menerima kritik dan saran demi kesempurnaan skripsi ini. Akhirnya, penulis berharap semoga skripsi ini dapat memberi manfaat bagi kita semua.
Medan, Januari 2014 Penulis
ANALISIS KANDUNGAN MINERAL KALIUM, KALSIUM, MAGNESIUM DAN NATRIUM PADA BUAH STRAWBERRY
(Fragaria ananassa Duchesne.) SECARA SPEKTROFOTOMETRI SERAPAN ATOM
ABSTRAK
Strawberry merupakan tanaman yang dapat tumbuh dikawasan pegunungan. Tanaman ini sangat bermanfaat bagi tubuh karena mengandung vitamin dan mineral yang diperlukan untuk pertumbuhan dan kesehatan. Tanaman ini mengandung mineral antara lain kalium, kalsium, natrium dan magnesium. Tujuan penelitian ini untuk mengetahui kadar mineral kalium, kalsium, natrium, dan magnesium pada strawberry (Fragaria ananassa Duchesne.).
Metode penelitian yang dilakukan secara destruksi kering terhadap strawberry (Fragaria ananassa Duchesne.) dan penetapan kadar mineral kalium, kalsium, magnesium dan natrium dilakukan dengan menggunakan spektrofotometer serapan atom dengan panjang gelombang 766,50 nm untuk kalium, pada panjang gelombang 422,7 nm untuk kalsium pada panjang gelombang 285,20 nm untuk magnesium dan pada panjang gelombang 589,00 nm untuk natrium.
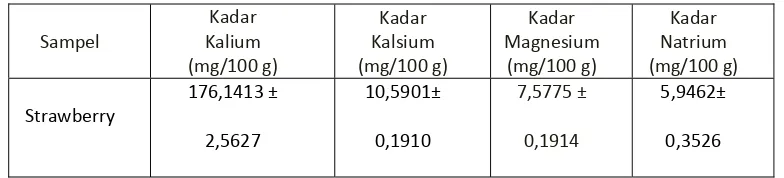
Hasil penelitian menunjukkan bahwa buah strawberry mengandung kalium dengan kadar (176,1413 ± 2,5627) mg/100 g, kalsium dengan kadar (10,5901 ± 0,1910) mg/100 g, magnesium dengan kadar (7,5775 ± 0,1914) mg/100 g dan natrium dengan kadar (5,9462 ± 0,3526) mg/100 g.
Kata kunci: Strawberry (Fragaria ananassa Duchesne.), Kalium (K), Kalsium (Ca) Natrium (Na), Magnesium (Mg), Spektrofotometer Serapan Atom.
ANALYSIS MINERALS CONTENT OF POTASSIUM, CALCIUM MAGNESIUM AND SODIUM STRAWBERRY (Fragaria ananassa Duchesne.) BY ATOMIC ABSORPTION SPECTROPHOTOMETRY
ABSTRACT
Strawberry is a plant that can grow in the mountainous region. This plant is very beneficial for the body because it contains vitamins and minerals needed for growth and health. It contains minerals such as potassium, calcium, sodium, and magnesium. The purpose of this study to determine the mineral content of potassium, calcium, sodium, and magnesium in strawberry (Fragaria ananassa Duchesne.).
This research is used with dry destruction to strawberry (Fragaria ananassa Duchesne.) and the determination of potassium, calcium, magnesium and sodium are using the atomic absorption spectrophotometer with 766.50 nm for potassium, 422.7 nm for calcium, 285.20 nm for magnesium and 589.00 nm for sodium.
The results of study indicated that the strawberry (Fragaria ananassa Duchesne.) contained potassium (176.1413 ± 2.5627) mg/100 g, calcium (10.5901 ± 0.1910) mg/100 g, magnesium (7.5775 ± 0.1914) mg/100 g and sodium (5.9462 ± 0.3526) mg/100 g.
DAFTAR ISI
Halaman
JUDUL i
HALAMAN PENGESAHAN iii
KATA PENGANTAR iv
ABSTRAK vi
ABSTRACT vii
DAFTAR ISI viii
DAFTAR TABEL xii
DAFTAR GAMBAR xiii
DAFTAR LAMPIRAN xiv
BAB I PENDAHULUAN 1
1.1 Latar Belakang 1
1.2 Perumusan Masalah 3
1.3 Hipotesis 3
1.4 Tujuan Penelitian 3
1.5 Manfaat Penelitian 3
BAB II TINJAUAN PUSTAKA 4
2.1 Uraian Sampel 4
2.1.1 Strawberry (Fragaria ananassa Duchesne) 4 2.1.2 Deskripsi Tanaman Strawberry 5 2.1.3 Kandunga Gizi Strawberry 6
2.2.1 Kalium 6
2.2.2 Kalsium 7
2.2.3 Natrium 7
2.2.4 Magnesium 8
2.3 Spektrofotometri Serapan Atom 8
2.4 Validasi Metode Analisis 13
BAB III METODE PENELITIAN 16
3.1 Tempat dan Waktu Penelitian 16
3.2 Bahan-Bahan 16
3.2.1 Sampel 16
3.2.2 Pereaksi 16
3.3 Alat-Alat 16
3.4 Pembuatan Pereaksi 17
3.4.1 Larutan Asam Pikrat 1% b/v 17 3.4.2 Larutan Kuning Titan 0,1% b/v 17 3.4.3 Larutan Natrium Hidroksida 2 N 17 3.4.4 Larutan Asam Nitrat 5 N 17 3.4.5 Larutan Asam Sulfat 1 N 17
3.5 Prosedur Penelitian 17
3.5.1 Pengambilan Sampel 17
3.5.2 Penyiapan Sampel 17
3.5.5 Analisis Kualitatif 19 3.5.5.1 Uji Nyala Ni/Cr Pada Kalium, Kalsium Dan
Natrium 19
3.5.5.2 Uji Kristal Pada Kalium, Kalsium Dan
Natrium 19
3.5.5.3 Magnesium Dengan Larutan
Titan yellow 0,1% b/v 20
3.5.6 Analisis Kuantitatif 20
3.5.6.1 Penentuan Panjang Gelombang Maksimum 20 3.5.6.2 Penetapan Kadar Mineral dalam Sampel 22 3.5.7 Analisis Data Secara Statistik 24 3.5.7.1 Penolakan Hasil Pengamatan 24 3.5.8 Validasi Metode Analisis 26 3.5.8.1 Uji Perolehan Kembali 26 3.5.8.2 Simpangan Baku Relatif 27 3.5.8.3 Penentuan Batas Deteksi dan Batas
Kuantitasi 28
BAB IV HASIL DAN PEMBAHASAN 29
4.1 Identifikasi Kalium, Kalsium, Magnesium dan Natrium
Pada Sampel 29
4.2 Penetapan Kadar Kalium, Kalsium, Magnesium dan
Natrium Pada Sampel 31
4.2.1 Kurva Kalibrasi Kalium, Kalsium, Magnesium dan
Natrium 31
4.2.2 Pengukuran Kadar Kalium, Kalsium, Magnesium
4.3 Validasi Metode Analisis 35 4.3.1 Uji perolehan Kembali (Recovery) 35
4.3.2 Simpangan Baku Relatif 36
4.3.3 Batas Deteksi dan Batas Kuantitasi 36
BAB V KESIMPULAN DAN SARAN 38
5.1 Kesimpulan 38
5.2 Saran 38
DAFTAR PUSTAKA 39
DAFTAR TABEL
Halaman
Tabel 1 Nilai Q kritis Pada Taraf Kepercayaan 95% 25 Tabel 2 Hasil Analisa Kualitatif Kalium, Kalsium, Magnesium
dan Natrium 29
Tabel 3 Hasil Analisis Kuantitatif Kalium, Kalsium, Magnesium
DAFTAR GAMBAR
DAFTAR LAMPIRAN
Halaman Lampiran 1 Hasil Identifikasi Tanaman 41
Lampiran 2 Sampel yang Digunakan 42
Lampiran 3 Hasil Analisis Kualitatif Kalium, Kalsium, Natrium,
Magnesium 43
Lampiran 4 Bagan Alir Proses Destruksi Kering pada Sampel 45 Lampiran 5 Bagan Alir Pembuatan Larutan Sampel 46 Lampiran 6 Data Kalibrasi Kalium dengan Spektrofotometer
Serapan Atom dan Perhitungan Persamaan Regresi 47 Lampiran 7 Data Kalibrasi Kalsium dengan Spektrofotometer
Serapan Atom dan Perhitungan Persamaan Regresi 48 Lampiran 8 Data Kalibrasi Magnesium dengan Spektrofotometer
Serapan Atom dan Perhitungan Persaman Regresi 49 Lampiran 9 Data Kalibrasi Natrium dengan Spektrofotometer
Serapan Atom dan Perhitungan Persaman Regresi 50 Lampiran 10 Hasil Analisis Kadar Mineral Kalium, Kalsium,
Natrium dan Magnesium dalam Sampel 51 Lampiran 11 Contoh Perhitungan Kadar Kalium, Kalsium, Natrium
dan Magnesium dalam Sampel 52
Lampiran 12 Perhitungan Statistik Kadar Kalium, Kalsium, Natrium
dan Magnesium dalam Sampel 54
Lampiran 13 Perhitungan Simpangan Baku Relatif (RSD) Kadar Kalium, Kalsium, Natrium dan Magnesium dalam
Sampel 58
Lampiran 14 Perhitungan Batas Deteksi dan Batas Kuantitasi 62 Lampiran 15 Hasil Uji Perolehan Kembali Kalium, Kalsium,
Natrium dan Magnesium Setelah Penambahan
Lampiran 16 Contoh Perhitungan Uji Perolehan Kembali Kalium
Kalsium, Natrium dan Magnesium dalam Sampel 68 Lampiran 17 Gambar Alat Alat yang Digunakan 72
Lampiran 18 Tabel Distribusi t 73
ANALISIS KANDUNGAN MINERAL KALIUM, KALSIUM, MAGNESIUM DAN NATRIUM PADA BUAH STRAWBERRY
(Fragaria ananassa Duchesne.) SECARA SPEKTROFOTOMETRI SERAPAN ATOM
ABSTRAK
Strawberry merupakan tanaman yang dapat tumbuh dikawasan pegunungan. Tanaman ini sangat bermanfaat bagi tubuh karena mengandung vitamin dan mineral yang diperlukan untuk pertumbuhan dan kesehatan. Tanaman ini mengandung mineral antara lain kalium, kalsium, natrium dan magnesium. Tujuan penelitian ini untuk mengetahui kadar mineral kalium, kalsium, natrium, dan magnesium pada strawberry (Fragaria ananassa Duchesne.).
Metode penelitian yang dilakukan secara destruksi kering terhadap strawberry (Fragaria ananassa Duchesne.) dan penetapan kadar mineral kalium, kalsium, magnesium dan natrium dilakukan dengan menggunakan spektrofotometer serapan atom dengan panjang gelombang 766,50 nm untuk kalium, pada panjang gelombang 422,7 nm untuk kalsium pada panjang gelombang 285,20 nm untuk magnesium dan pada panjang gelombang 589,00 nm untuk natrium.
Hasil penelitian menunjukkan bahwa buah strawberry mengandung kalium dengan kadar (176,1413 ± 2,5627) mg/100 g, kalsium dengan kadar (10,5901 ± 0,1910) mg/100 g, magnesium dengan kadar (7,5775 ± 0,1914) mg/100 g dan natrium dengan kadar (5,9462 ± 0,3526) mg/100 g.
Kata kunci: Strawberry (Fragaria ananassa Duchesne.), Kalium (K), Kalsium (Ca) Natrium (Na), Magnesium (Mg), Spektrofotometer Serapan Atom.
ANALYSIS MINERALS CONTENT OF POTASSIUM, CALCIUM MAGNESIUM AND SODIUM STRAWBERRY (Fragaria ananassa Duchesne.) BY ATOMIC ABSORPTION SPECTROPHOTOMETRY
ABSTRACT
Strawberry is a plant that can grow in the mountainous region. This plant is very beneficial for the body because it contains vitamins and minerals needed for growth and health. It contains minerals such as potassium, calcium, sodium, and magnesium. The purpose of this study to determine the mineral content of potassium, calcium, sodium, and magnesium in strawberry (Fragaria ananassa Duchesne.).
This research is used with dry destruction to strawberry (Fragaria ananassa Duchesne.) and the determination of potassium, calcium, magnesium and sodium are using the atomic absorption spectrophotometer with 766.50 nm for potassium, 422.7 nm for calcium, 285.20 nm for magnesium and 589.00 nm for sodium.
The results of study indicated that the strawberry (Fragaria ananassa Duchesne.) contained potassium (176.1413 ± 2.5627) mg/100 g, calcium (10.5901 ± 0.1910) mg/100 g, magnesium (7.5775 ± 0.1914) mg/100 g and sodium (5.9462 ± 0.3526) mg/100 g.
BAB I PENDAHULUAN
1.1 Latar Belakang
Tanaman strawberry dibudidayakan di daerah subtropika seluruh dunia. Tanaman ini sangat bermanfaat bagi tubuh karena mengandung vitamin (A, B6, B12, C) dan mineral (Ca, Fe, Mg, K, Na). Tanaman strawberry merupakan salah satu tanaman buah buahan yang mempunyai nilai ekonomi yang tinggi. Daya pikatnya terletak pada warna buah yang merah mencolok, menarik serta rasa yang manis segar. Strawberry mengandung ellagic acid sebagai antioksidan. Ellagic acid terbukti dapat menghalangi pertumbuhan tumor dalam paru-paru (Kristanti, 2010).
Peranan kalsium tidak saja sebagai pembentukan tulang dan gigi tetapi juga memegang peranan penting pada berbagai proses fisiologik dan biokhemik didalam tubuh, fungsi lain yaitu iritabilitas syaraf otot dan memberikan kekerasan dan ketahanan terhadap pengeroposan. Kalium adalah mineral penting yang diperlukan tubuh dalam pengaturan keseimbangan cairan tubuh yang membantu menjaga tekanan osmotik. Natrium dalam tubuh berperan untuk mempertahankan keseimbangan tubuh. Magnesium dalam tubuh berfungsi membantu mengurangi getaran otot dan meningkatkan tekanan osmotik (Budiyanto, 2001).
Metode yang dipilih untuk penetapan kadar kalsium, kalium, magnesium dan natrium adalah metode Spektrofotometri Serapan Atom, pemilihan ini didasarkan pada ketelitian alat, kecepatan analisis, bahan yang digunakan sedikit, dan spesifik untuk setiap logam tanpa dilakukan pemisahan terlebih dahulu dan dapat menetukan kadar suatu unsur dengan konsentrasi yang rendah (Khopkar, 1985).
1.2 Perumusan Masalah
1. Apakah kandungan mineral kalium, kalsium, magnesium dan natrium pada strawberry dapat diidentifikasi dengan reaksi kimia kualitatif ? 2. Berapakah kadar mineral kalium, kalsium, magnesium dan natrium
1.3Hipotesis
1. Kandungan mineral kalium, kalsium, magnesium dan natrium pada strawberry dapat diidentifikasi dengan reaksi kimia kualitatif.
2. Kadar mineral kalium, kalsium, magnesium dan natrium pada strawberry berada dalam jumlah tertentu.
1.4Tujuan Penelitian
1. Untuk mengidentifikasi kandungan kalium, kalsium, magnesium dan natrium pada buah strawberry dengan reaksi kimia.
2. Untuk mengetahui kadar kalium, kalsium, natrium dan magnesium dalam buah strawberry.
1.5 Manfaat Penelitian
BAB II
TINJAUAN PUSTAKA
2.1 Uraian Sampel 2.1.1 Strawberry
Menurut Tim Karya Tani Mandiri (2010) strawberry dikenal dengan nama arbei yang bersal dari bahasa belanda, aardbhei yaitu sebuah genus tumbuhan dalam keluarga Rosaceae. Di Indonesia buah ini disebut “strawberry”. Dalam sistematika tumbuh-tumbuhan (taksonomi) strawberry diklasifikasikan sebagai berikut:
Kingdom : Plantae
Divisi : Spermatophyta Class : Dicotyledoneae Ordo : Rosales
Famili : Rosaceae Genus : Fragaria
Spesies : Fragaria ananassa Duchesne.
hibrid yang merupakan strawberry modern (komersil) Fragaria x ananassa var Duchesne (Tim Karya Tani Mandiri, 2010).
2.1.2 Deskripsi Tanaman Strawberry
Strawberry adalah tanaman subtropis yang dapat beradaptasi dengan baik di dataran tinggi tropis yang memiliki temperatur optimum antara 22-28 o
C, kelembapan yang baik untuk pertumbuhan tanaman strawberry 80-90% dan sinar matahari yang tidak terlalu kuat dengan lama penyinaran cahaya matahari yang dibutuhkan dalam pertumbuhan adalah 8-10 jam setiap harinya (Tim Karya Tani Mandiri, 2010).
2.1.3 Kandungan gizi strawberry
Kandungan gizi strawberry dalam 100 g adalah 30 kkal energi; 0,6 g protein; 0,4 g lemak; 7 g karbohidrat; 0,5 g serat; 0,4 g abu; 14 mg kalsium; 19 mg fosfor; 0,4 mg zat besi; 1 mg natrium; 166 mg kalium; 92 g air; 10 mg magnesium dan 56,7 mg vitamin C (Hancock, 1999).
2.2 Mineral
Mineral merupakan bagian dari tubuh dan memegang peranan penting dalam pemeliharaan fungsi tubuh, baik pada tingkat sel, jaringan, organ, maupun fungsi tubuh secara keseluruhan. Mineral digolongkan ke dalam mineral makro dan mineral mikro. Mineral makro adalah mineral yang dibutuhkan tubuh dalam jumlah lebih dari 100 mg sehari, sedangkan mineral mikro adalah mineral yang dibutuhkan tubuh dalam jumlah kurang dari 100 mg sehari. Yang termasuk mineral makro antara lain natrium, klorida, kalium, kalsium, fosfor, dan magnesium. Sedangkan yang termasuk mineral mikro antara lain besi, mangan zink, dan tembaga (Almatsier, 2004).
2.2.1 Kalium
Kalium merupakan salah satu mineral makro yang berperan dalam pengaturan keseimbangan cairan tubuh. Sebanyak 95% kalium berada di dalam cairan intraseluler. Kalium terdapat di dalam semua makanan berasal dari tumbuh-tumbuhan dan hewan. Sumber utamanya adalah makanan mentah/segar, terutama buah, sayuran dan kacang-kacangan (Almatsier, 2004).
menyebabkan lemah lesu tetapi jarang terjadi, sepanjang seseorang cukup makan sayuran dan buah segar. Kebutuhan minimum akan kalium ditaksir sebanyak 2000 mg sehari (Almatsier, 2004).
2.2.2 Kalsium
Kalsium merupakan mineral yang paling banyak terdapat di dalam tubuh, yaitu 1,5 – 2% dari berat badan orang dewasa atau kurang lebih sebanyak 1 kg. Peningkatan kebutuhan akan kalsium terjadi pada masa pertumbuhan, kehamilan dan menyusui. Jumlah kalsium yang dianjurkan per hari untuk bayi adalah 300-400 mg, remaja 600-700 mg, dewasa 500-800 mg, dan ibu hamil dan menyusui sebesar 1200 mg (Almatsier, 2004). Sumber kalsium tinggi pada milk dan hasil olahannya, serealia, kacang-kacangan, telur, ikan dan buah-buahan, sedangkan yg sedikit adalah gula, pati dan minyak (Sudarmadji., dkk, 1996).
Kekurangan kalsium pada masa pertumbuhan dapat menyebabkan gangguan pertumbuhan seperti tulang kurang kuat, mudah bengkok dan rapuh. Pada orang dewasa, terutama sesudah usia 50 tahun akan kehilangan kalsium dari tulangnya. Ini yang dinamakan osteoporosis (Almatsier, 2004).
2.2.3 Natrium
nafsu makan (Tjay dan Rahardja, 2007). Kebutuhan natrium untuk orang dewasa ditaksir sebanyak 500 mg sehari (Almatsier, 2004).
2.2.4 Magnesium
Hampir 60% magnesium dalam tubuh terdapat pada tulang, 26% dalam otot, dan sisanya ada dalam jaringan lunak serta cairan tubuh. Magnesium memegang peranan penting dalam lebih dari tiga ratus sistem enzim di dalam tubuh (Almatsier, 2004).
Di dalam cairan sel ekstraseluler, magnesium memegang peranan penting dalam relaksasi otot. Kadar magnesium yang normal dapat mempertahankan tonus otot polos dan berimplikasi terhadap kontrol tekanan darah (Barasi, 2007). Kekurangan magnesium menyebabkan kurang nafsu makan, kejang atau tetanus, gangguan sistem syaraf pusat, halusinasi, koma. Konsumsi magnesium dengan banyak dapat menyebabkan gagal ginjal. Orang dewasa membutuhkan magnesium sekitar 250-280 mg sehari (Almatsier, 2004).
2.3 Spektrofotometri Serapan Atom.
Spektrofotometri serapan atom digunakan untuk analisis kuantitatif unsur-unsur logam dalam jumlah sekelumit (trace) dan sangat sekelumit (ultratrace). Cara analisis ini memberikan kadar unsur logam tertentu dalam suatu sampel. Cara ini cocok untuk analisis sekelumit logam karena mempunyai kepekaan yang tinggi, pelaksanaanya relatif sederhana, dan interferensinya sedikit. Spektrofotometri serapan atom didasarkan pada penyerapan energi sinar oleh atom-atom netral dalam bentuk gas (Ganjar dan Rohman, 2007).
Proses yang terjadi ketika dilakukan analisis dengan menggunakan spektrofotometri serapan atom dengan cara absorbsi yaitu penyerapan energi radiasi oleh atom-atom yang berada pada tingkat dasar. Atom-atom tersebut menyerap radiasi pada panjang gelombang tertentu, tergantung pada sifat atom tersebut. Sebagai contoh kalium menyerap radiasi pada panjang gelombang 766,50 nm, kalsium pada 422,7 nm, natrium pada 589 nm, dan magnesium menyerap radiasi pada panjang gelombang 285,20 nm. Dengan menyerap radiasi, maka atom akan memperoleh energi sehingga suatu atom pada keadaan dasar dapat ditingkatkan menjadi ke tingkat eksitasi (Ganjar dan Rohman, 2007).
(Resonance line). Garis-garis resonansi ini akan dibaca dalam bentuk angka oleh Readout (Ganjar dan Rohman, 2007).
Menurut Ganjar dan Rohman (2007) instrumentasi spektrofotometer serapan atom adalah sebagai berikut :
a. Sumber Radiasi
Sumber radiasi yang digunakan adalah lampu katoda berongga (hollow cathode lamp). Lampu ini terdiri atas tabung kaca tertutup yang mengandung suatu katoda dan anoda. Katoda berbentuk silinder berongga yang dilapisi dengan logam tertentu sesuai dengan logam yang diperiksa.
b. Sumber atomisasi
Sumber atomisasi dibagi menjadi dua yaitu sistem nyala dan sistem tanpa nyala. Kebanyakan instrumen sumber atomisasinya adalah nyala dan sampel diintroduksikan dalam bentuk larutan. Sampel masuk ke nyala dalam bentuk aerosol. Aerosol biasa dihasilkan oleh nebulizer (pengabut) yang dihubungkan ke nyala oleh ruang penyemprot (chamber spray).
1. Dengan nyala (Flame)
2. Tanpa nyala (Flameless)
Pengatoman dilakukan dalam tungku dari grafit. Sejumlah sampel diambil sedikit lalu diletakkan dalam tabung grafit, kemudian tabung tersebut dipanaskan dengan sistem elektris dengan cara melewatkan arus listrik pada grafit. Akibat pemanasan ini, maka zat yang akan dianalisis berubah menjadi atom-atom netral dan pada fraksi atom ini dilewatkan suatu sinar yang berasal dari lampu katoda berongga sehingga terjadilah proses penyerapan energi radiasi yang memenuhi kaidah analisis kuantitatif.
c. Monokromator
Monokromator merupakan alat untuk memisahkan dan memilih spektrum sesuai dengan panjang gelombang yang digunakan dalam analisis yang dihasilkan lampu katoda berongga.
d. Detektor
Detektor digunakan untuk mengukur intensitas cahaya yang melewati tempat pengatoman.
e. Amplifier
Amplifier merupakan suatu alat untuk memperkuat signal yang diterima dari detektor sehingga dapat dibaca alat pencatat hasil (Readout).
f. Readout
Me pada saat gangguan a. Gangg Ga yang buka atomik da penggangg atomik ini b. Gangg di dal Menu keadaan a - Di ter aka Gambar 2 enurut Ganj t dilakukan itu antara la guan oleh p angguan in an berasal apat diseba gu yang be i adalah bek guan kimia lam nyala. urut Ganjar
zas di dalam sosiasi se rbentuknya
an mengura
2.1. Kompon jar dan Roh n analisis d
ain adalah: penyerapan ni terjadi a
dari atom-abkan adan erada di da kerja pada p a yang dapa
dan Rohm m nyala seri enyawa-seny senyawa re angi jumlah nen Spektro hman (2007 dengan ala non-atomik akibat peny -atom yang nya penyera
alam nyala. panjang gelo at mempeng
man (2007) p ing tergangg yawa yan efraktorik (s h atom netra
ofotometer 7), gangguan
at spektrofo
k
yerapan ca g akan dian
apan cahay . Cara men ombang yan garuhi juml
pembentuk gu oleh dua ng tidak sukar diuraik al yang ada d
Serapan Ato n-gangguan otometer se
haya dari nalisis. Peny ya oleh par ngatasi peny ng lebih bes
ah atau ban
atom-atom a peristiwa k
sempurna kan dalam a di dalam ny
om
n dapat terja erapan ato sumber sin nyerapan no artikel-partik nyerapan no sar. nyaknya ato
- Ionisasi atom-atom di dalam nyala akibat suhu yang digunakan terlalu tinggi. Prinsip analisis dengan spektrofotometer serapan atom adalah mengukur absorbansi atom-atom netral yang berada dalam keadaan azas. Jika terbentuk ion maka akan mengganggu pengukuran absorbansi atom netral karena spektrum absorbansi atom-atom yang mengalami ionisasi tidak sama dengan spektrum atom dalam keadaan netral sehingga akan mempengaruhi hasil.
2.4 Validasi Metode Analisis
Menurut Harmita (2004), validasi metode analisis adalah suatu tindakan penilaian terhadap parameter tertentu berdasarkan percobaan laboratorium untuk membuktikan bahwa parameter tersebut memenuhi persyaratan untuk penggunaannya. Beberapa parameter analisis yang harus dipertimbangkan dalam validasi metode analisis adalah sebagai berikut :
a. Kecermatan
Kecermatan adalah ukuran yang menunjukkan derajat kedekatan hasil analisis dengan kadar analit yang sebenarnya. Kecermatan dinyatakan sebagai persen perolehan kembali (recovery) analit yang ditambahkan. Kecermatan ditentukan dengan dua cara, yaitu:
- Metode simulasi
dianalisis dan hasilnya dibandingkan dengan kadar analit yang ditambahkan (kadar yang sebenarnya).
- Metode penambahan baku
Metode penambahan baku (standard addition method) merupakan metode yang dilakukan dengan cara menambahkan sejumlah baku dengan konsentrasi tertentu pada sampel yang diperiksa, lalu dianalisis dengan metode yang akan divalidasi. Hasilnya dibandingkan dengan sampel yang dianalisis tanpa penambahan sejumlah baku. Persen perolehan kembali ditentukan dengan menentukan berapa persen baku yang ditambahkan ke dalam sampel dapat ditemukan kembali.
Menurut Ermer (2005), suatu metode dikatakan teliti jika nilai recoverynya antara 80-120%. Recovery dapat ditentukan dengan menggunakan metode standar adisi.
b. Keseksamaan (presisi)
c. Selektivitas (Spesifisitas)
Selektivitas atau spesifisitas suatu metode adalah kemampuannya yang hanya mengukur zat tertentu secara cermat dan seksama dengan adanya komponen lain yang ada di dalam sampel.
d. Linearitas dan rentang
Linearitas adalah kemampuan metode analisis yang memberikan respon baik secara langsung maupun dengan bantuan transformasi matematika, menghasilkan suatu hubungan yang proporsional terhadap konsentrasi analit dalam sampel. Rentang merupakan batas terendah dan batas tertinggi analit yang dapat ditetapkan secara cermat, seksama dan dalam linearitas yang dapat diterima.
e. Batas deteksi dan batas kuantitasi
BAB III
METODE PENELITIAN
3.1 Tempat dan Waktu Penelitian
Penelitian ini dilakukan di Laboratorium Kimia Farmasi Kualitatif Fakultas Farmasi Universitas Sumatera Utara dan di Laboratorium Penelitian Fakultas Farmasi Universitas Sumatera Utara Medan pada bulan Juli 2013 - Oktober 2013.
3.2 Bahan-bahan 3.2.1 Sampel
Sampel yang digunakan dalam penelitian ini adalah buah strawberry (Fragaria ananassa Duchesne.) yang diambil di daerah Brastagi, Provinsi Sumatera Utara.
3.2.2 Pereaksi
Bahan yang digunakan adalah pro analisis keluaran E. Merck yaitu asam nitrat pekat 65% b/v, asam pikrat 99% b/v, Titan yellow 0,1% b/v, natrium hidroksida 99% b/v, aqua bidestilata (Ikapharmindo Putramas), larutan baku kalium 1000 mcg/ml, larutan baku kalsium 1000 mcg/ml, larutan baku magnesium 1000 mcg/ml dan larutan baku natrium 1000 mcg/ml (Laboratorium Penelitian Fakultas Farmasi USU).
3.3Alat-alat
oberol), hotplate, kertas saring Whatman no. 42, neraca analitik, pisau stainless stell, krus porselen dan spatula.
3.4 Pembuatan Pereaksi 3.4.1 Asam Pikrat 1% b/v
Sebanyak 1 gram asam pikrat dilarutkan dalam aquabides hingga 100 ml.
3.4.2 Titan yellow 0,1% b/v
Larutan kuning titan 0,1% b/v dibuat dengan cara melarutkan 0,1 g titan yellow dalam 100 ml aquabides.
3.4.3 Larutan Natrium Hidroksida 2 N
Sebanyak 80,02 gram natrium hidroksida dilarutkan dengan aquabides hingga 1000 ml (Ditjen POM, 1979).
3.5 Prosedur Penelitian 3.5.1 Pengambilan sampel
Sampel yang digunakan adalah buah strawberry yang diambil di daerah Brastagi, Provinsi Sumatera Utara. Metode pengambilan sampel dilakukan dengan cara sampling purposif, yaitu sampel ditentukan atas dasar pertimbangan bahwa sampel yang diambil dapat mewakili populasi (Sudjana, 2005).
3.5.2 Penyiapan Sampel
3.5.3 Proses Destruksi
3.5.3.1 Proses Destruksi Kering
Sampel yang telah dihaluskan ditimbang sebanyak 10 gram dimasukkan kedalam krus porselen, lalu diabukan di tanur dengan temperatur awal 100oC dan perlahan-lahan temperatur dinaikkan menjadi 500oC dengan interval 25oC setiap 5 menit. Pengabuan dilakukan selama 24 jam dan dibiarkan dingin lalu dipindahkan ke desikator. Abu dibasahi dengan 10 tetes aquabides dan ditambahkan 5 ml HNO
3 (1 : 1) secara hati-hati. Kemudian kelebihan HNO3 diuapkan pada hot plate dengan suhu 100-120oC sampai kering. Krus porselen dimasukkan kembali kedalam tanur dan diabukan selama 1 jam dengan suhu 500oC, kemudian didinginkan (Helrich, 1990).
3.5.4 Pembuatan Larutan Sampel
3.5.5 Analisis Kualitatif
3.5.5.1 Uji nyala Ni/Cr Pada Kalium, Kalsium dan Natrium
Bersihkan kawat Ni/Cr dengan HCl pekat lalu dipijar pada api bunsen sampai tidak memberikan warna khusus pada nyala bunsen. Kedalam tabung masukkan larutan sampel dan tambahkan NaOH, endapannya kemudian di saring, cek pH (pH 13) lalu celupkan kawat pada hasil saringan tersebut lalu dipijar pada api bunsen, amati warna yang terjadi pada nyala bunsen. Jika terdapat kalsium, akan terbentuk warna merah bata pada nyala bunsen. Kedalam tabung tambahkan larutan sampel, celupkan kawat lalu dipijar pada api bunsen, amati warna yang terjadi, jika terdapat kalium akan terbentuk warna merah ungu pada nyala bunsen. Kedalam tabung tambahkan larutan sampel, celupkan kawat lalu dipijar pada api bunsen, amati warna yang terjadi, jika terdapat natrium akan terbentuk warna kuning pada nyala bunsen (Vogel, 1979).
3.5.5.2 Uji Kristal Pada Kalsium, Kalium dan Natrium
3.5.5.3 Magnesium
3.5.5.3.1 Reaksi Kualitatif dengan Larutan Kuning Titan 0,1% b/v
Kedalam tabung reaksi dimasukkan 2 ml larutan sampel, ditambah 5-6 tetes NaOH 2 N dan 3 tetes pereaksi Titan yellow. Dihasilkan endapan atau larutan warna merah terang (Vogel, 1979).
3.5.6 Analisis Kuantitatif
3.5.6.1 Penentuan Panjang Gelombang Maksimum
Terlebih dahulu dilakukan penentuan panjang gelombang maksimum kalium 766,5 nm, kalsium 477,2 nm, magnesium 285,2 nm dan natrium 589,0 nm untuk mengetahui apakah panjang gelombang yang terdapat pada alat sesuai dengan yang tercantum diliteratur dengan menggunakan lampu katoda masing-masing mineral.
3.5.6.1.1 Pembuatan Kurva Kalibrasi Kalium
Larutan baku kalium (1000 µg/ml) dipipet sebanyak 5 ml, dimasukkan ke dalam labu tentukur 50 ml dan dicukupkan hingga garis tanda dengan aquabides (konsentrasi 100µg/ml), kemudian dipipet 5 ml dimasukkan ke dalam labu tentukur 50 ml dan dicukupkan hingga garis tanda dengan aquabides (konsentrasi 10 µg/ml).
aquabides (larutan ini mengandung (0,5; 1,0; 2,0; 3,0 dan 4,0)µg/ml dan diukur pada panjang gelombang 766,5 nm dengan nyala udara-asetilen.
3.5.6.1.2 Pembuatan Kurva Kalibrasi Kalsium
Larutan baku kalsium (1000 µg/ml) dipipet sebanyak 5 ml, dimasukkan ke dalam labu tentukur 50 ml dan dicukupkan hingga garis tanda dengan aquabides (konsentrasi 100µg/ml), kemudian dipipet 5 ml dimasukkan ke dalam labu tentukur 50 ml dan dicukupkan hingga garis tanda dengan aquabides (konsentrasi 10 µg/ml).
Larutan untuk kurva kalibrasi kalsium dibuat dengan memipet (1,25; 2,5; 5,0; 7,5; dan 10) ml larutanbaku 10 µg/ml, masing-masing dimasukkan ke dalam labu tentukur 25 ml dan dicukupkan hingga garis tanda dengan aquabides (larutan ini mengandung (0,5; 1,0; 2,0; 3,0 dan 4,0) µg/ml) dan diukur pada panjang gelombang 422,7 nm dengan nyala udara-asetilen.
3.5.6.1.3 Pembuatan Kurva Kalibrasi Magnesium
Larutan baku magnesium (1000 µg/ml) dipipet sebanyak 5 ml, dimasukkan ke dalam labu tentukur 50 ml dan dicukupkan hingga garis tanda dengan aquabides (konsentrasi 100µg/ml), kemudian dipipet 5 ml dimasukkan kedalam labu tentukur 50 ml dan dicukupkan hingga garis tanda dengan aquabides (konsentrasi 10 µg/ml), kemudian dipipet 5 ml dimasukkan ke dalam labu tentukur 50 ml dan dicukupkan hingga garis tanda dengan aquabides (konsentrasi 1µg/ml).
dalam labu tentukur 25 ml dan dicukupkan hingga garis tanda dengan aquabides (larutan ini mengandung (0,05; 0,1; 0,2; 0,3; dan 0,4) µg/ml) dan diukur pada panjang gelombang 285,2 nm dengan nyala udara-asetilen.
3.5.6.1.4 Pembuatan Kurva Kalibrasi Natrium
Larutan baku natrium (1000 µg/ml) dipipet sebanyak 1 ml, dimasukkan kedalam labu tentukur 100 ml dan dicukupkan hingga garis tanda dengan aquabides (konsentrasi 10 µg/ml).
Larutan untuk kurva kalibrasi natrium dibuat dengan memipet (0,75; 1; 1,5; 2 dan 2,5) ml larutan baku 10 µg/ml, masing-masing dimasukkan ke dalam labu tentukur 50 ml dan dicukupkan hingga garis tanda dengan aquabides (larutan ini mengandung (0,15; 0,2; 0,3; 0,4; 0,5) µg/ml) dan diukur pada panjang gelombang 589,0 nm dengan nyala udara-asetilen.
3.5.6.2 Penetapan Kadar Mineral dalam Sampel 3.5.6.2.1. Penetapan Kadar Kalium
3.5.6.2.2 Penetapan Kadar Kalsium
Larutan sampel strawberry diambil sebanyak 5 ml dimasukkan kedalam labu tentukur 25 ml dan diencerkan dengan aquabides hingga garis tanda (Faktor Pengenceran = 25/5 = 5 kali). Diukur absorbansinya dengan menggunakan spektrofotometer serapan atom pada panjang gelombang 422,7 nm. Nilai absorbansi yang diperoleh harus berada dalam rentang kurva kalibrasi larutan baku kalsium. Konsentrasi kalsium dalam sampel ditentukan berdasarkan persamaan garis regresi dari kurva kalibrasi.
3.5.6.2.3 Penetapan Kadar Magnesium
Larutan sampel strawberry diambil sebanyak 0,5 ml dimasukkan kedalam labu tentukur 25 ml dan diencerkan dengan aquabides hingga garis tanda (Faktor Pengenceran = (25/0,5 = 50 kali). Diukur absorbansi dengan menggunakan spektrofotometer serapan atom pada panjang gelombang 285,2 nm. Nilai absorbansi yang diperoleh harus berada dalam rentang kurva kalibrasi larutan baku magnesium. Konsentrasi magnesium dalam sampel ditentukan berdasarkan persamaan garis regresi dari kurva kalibrasi.
3.5.6.2.4 Penetapan Kadar Natrium
kalibrasi larutan baku natrium. Konsentrasi natrium dalam sampel ditentukan berdasarkan persamaan garis regresi dari kurva kalibrasi.
Menurut Harmita (2004), kadar kalium, kalsium, magnesium dan natrium dihitung dengan mensubstitusikan absorbansi ke dalam persamaan
regresi yang diperoleh dari kurva kalibrasi seperti di bawah ini:
Y = aX + b
Dimana :
Y = Absorbansi sampel a = Slope
X = Konsentrasi sampel b = Intersep
Menurut Harmita (2004), kadar kalium, kalsium, natrium, dan magnesium dalam sampel dapat dihitung dengan cara sebagai berikut:
(g) Sampel Berat
n pengencera xFaktor
(ml) xVolume (mcg/ml)
i Konsentras (mcg/g)
Atom
Kadar
3.5.7 Analisis Data SecaraStatistik 3.5.7.1 Penolakan Hasil Pengamatan
Kadar mineral kalium, kalsium, magnesium dan natrium yang diperoleh dari hasil pengukuran masing-masing larutan sampel dianalisis secara statistik.
Menurut Sudjana (2005), standar deviasi dapat dihitung dengan rumus:
SD =
1 -n
Keterangan :
Xi = Kadar sampel
X = Kadar rata-rata sampel n = jumlah pengulangan
Kadar kalium, kalsium, magnesium dan natrium yang diperoleh dari hasil pengukuran masing-masing keenam larutan sampel, diuji secara statistik dengan uji Q.
Q =
terendah Nilai
tertinggi Nilai
terdekat yang
Nilai dicurigai
yang Nilai
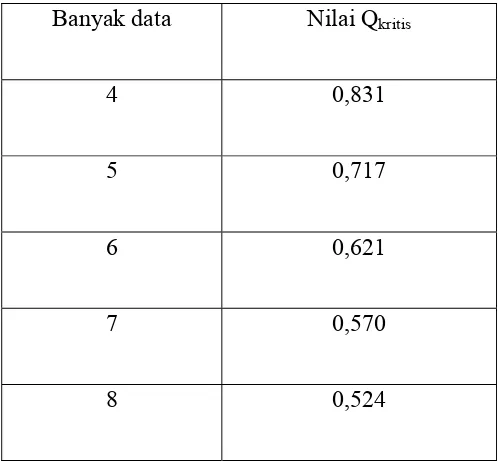
[image:42.595.117.366.457.688.2]Hasil pengujian atau nilai Q yang diperoleh ditinjau terhadap daftar harga Q padaTabel 1 apabila Q>Qkritis maka data tersebut ditolak (Gandjar dan Rohman, 2007)
Tabel 1. Nilai Qkritis pada Taraf Kepercayaan 95%
Banyak data Nilai Qkritis
4 0,831
5 0,717
6 0,621
7 0,570
Menurut Sudjana (2005), Untuk menentukan kadar kalium, kalsium, magnesium dan natrium didalam sampel dengan interval kepercayaan 95%; α = 0.05; dk = n - 1, dapat digunakan rumus:
µ = X ± (t(α/2, dk) x SD/√n
Keterangan :
µ = interval kepercayaan X = kadar rata-rata sampel
dk = derajat kebebasan (dk = n-1) t = harga t tabel sesuai dengan dk = n-1 α = tingkat kepercayaan
SD = standar deviasi n = jumlah pengulangan
3.5.8 Validasi Metode Analisis
3.5.8.1 Uji Perolehan Kembali (Recovery)
Uji perolehan kembali (recovery) dilakukan dengan metode penambahan larutan standar (standard addition method). Dalam metode ini, kadar mineral dalam sampel ditentukan terlebih dahulu, selanjutnya dilakukan penentuan kadar mineral dalam sampel setelah penambahan larutan baku dengan konsentrasi tertentu (Ermer, 2005).
baku magnesium (konsentrasi 100 mcg/ml) dan 6 ml larutan baku natrium (konsentrasi 100 mcg/ml), kemudian dilanjutkan dengan prosedur destruksi kering seperti yang telah dilakukan sebelumnya. Prosedur pengukuran uji perolehan kembali dilakukan sama dengan prosedur penetapan kadar dalam sampel.
Menurut Harmita (2004), persen perolehan kembali dapat dihitung dengan rumus di bawah ini:
% Perolehan Kembali =
A A F
C C C
*
x 100%
Keterangan:
CA = Kadar logamdalamsampelsebelumpenambahanbaku CF = Kadar logamdalamsampelsetelahpenambahanbaku C*A = Kadar larutan baku yang ditambahkan
3.5.8.2 Simpangan Baku Relatif
Keseksamaan atau presisi merupakan ukuran yang menunjukkan derajat kesesuaian antara hasil uji individual ketika suatu metode dilakukan secara berulang untuk sampel homogen. Adapun uji ketelitian yaitu koefisien variasi atau Relative Standard Deviation (%RSD) (Harmita, 2004).
Menurut Harmita (2004), harga persentase koefisien variasi (%RSD) ditentukan dengan rumus sebagai berikut:
RSD = x100%
x SD
Keterangan:
X = Kadar rata-rata sampel SD = Standar Deviasi
RSD = Relative Standard Deviation
3.5.8.3 Penentuan Batas Deteksi dan Batas Kuantitasi
Batas deteksi merupakan jumlah terkecil analit dalam sampel yang dapat dideteksi yang masih memberikan respon signifikan, sedangkan batas kuantitasi merupakan kuantitas terkecil analit dalam sampel yang masih dapat memenuhi kriteria cermat dan seksama (Harmita, 2004).
Menurut Harmita (2004), batas deteksi dan batas kuantitasi ini dapat dihitung dengan rumus sebagai berikut:
Simpangan Baku (SB) =
22
n Yi Y
Batas deteksi (LOD) =
slope SB x
3
Batas kuantitasi (LOQ) =
slope SB x
10
BAB IV
HASIL DAN PEMBAHASAN
4.1 Identifikasi Kalium, Kalsium, Magnesium dan Natrium pada Sampel Analisis kualitatif dilakukan sebagai analisis pendahuluan untuk mengetahui ada atau tidaknya kalium, kalsium, magnesium dan natrium dalam sampel yang akan dianalisis secara kuantitatif dengan menggunakan spektrofotometer serapan atom. Hasil analisis kualitatif kalium, kalsium, magnesium dan natrium dapat dilihat pada Tabel 2.
Tabel 2. Hasil Analisis Kualitatif Kalium, Kalsium, Magnesium dan Natrium Pada Sampel
No Mineral yang
dianalisis Pereaksi Hasil Reaksi Keterangan
1. Kalium
Asam pikrat 1% b/v Kristal jarum + Reaksi Nyala
menggunakan kawat Nikel-Krom
Warna nyala lembayung
+
2. Kalsium
Asam sulfat 1 N Kristal jarum besar
+
Reaksi Nyala Menggunakan kawat
Nikel-Krom
Warna nyala merah bata
+
3. Natrium
Asam pikrat 1% b/v Kristal jarum halus
+ Reaksi Nyala
Menggunakan kawat Nikel-Krom
Warna nyala Kuning keemasan
+
4. Magnesium Kuning titan 0,1% b/v dan NaOH 2 N
Warna endapan merah
terang
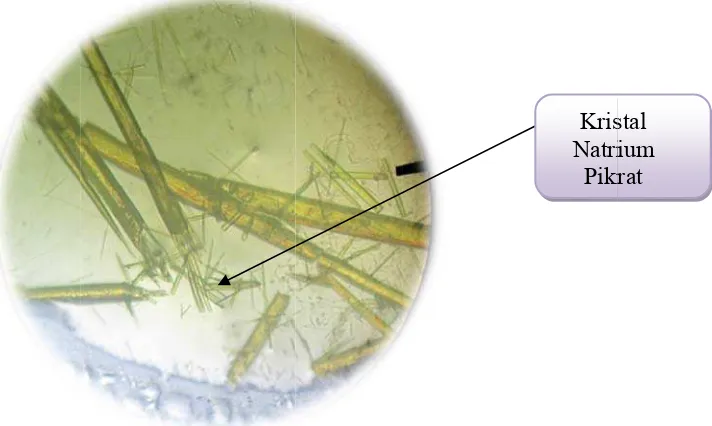
Pada Tabel 2 menunjukkan bahwa strawberry mengandung mineral kalium, kalsium, magnesium dan natrium. Sampel dikatakan positif mengandung mineral kalium karena menghasilkan kristal jarum kalium pikrat pada saat penambahan asam pikrat 1% b/v serta memberikan warna nyala lembayung pada uji nyala dengan kawat nikel-krom. Sampel dikatakan positif mengandung mineral kalsium karena menghasilkan kristal jarum besar kalsium sulfat pada saat penambahan asam sulfat 1 N serta memberikan warna nyala merah bata pada uji nyala dengan kawat nikel-krom. Sampel dikatakan positif mengandung mineral natrium karena menghasilkan kristal jarum halus natrium pikrat pada saat penambahan asam pikrat 1% b/v serta dikatakan positif mengandung mineral natrium karena memberikan warna nyala kuning keemasan pada uji nyala dengan kawat nikel-krom. Dikatakan positif mengandung mineral magnesium karena menghasilkan endapan merah terang dengan penambahan larutan Titan yellow 0,1% b/v dan natrium hidroksida 2 N (Vogel, 1979).
4.2 Penetapan Kadar Kalium, Kalsium, Magnesium dan Natrium pada Sampel
4.2.1 Kurva Kalibrasi Kalium, Kalsium, Magnesium dan Natrium
Kurva kalibrasi kalium diperoleh dengan cara mengukur absorbansi
dari larutan baku kalium pada panjang gelombang 766,50 nm sehingga diperoleh persamaan garis regresi Y = 0,0347X+0,0012 dengan koefisien
korelasi (r) = 0,9995 (Data dan perhitungan persamaan garis regresi dapat dilihat pada Lampiran 6, halaman 47).
Berdasarkan hasil pengukuran tersebut diperoleh kurva kalibrasi larutan
baku kalium yang dapat dilihat pada Gambar 4.1.
Gambar 4.1 Kurva Kalibrasi Larutan Baku Kalium
Kurva kalibrasi kalsium diperoleh dengan cara mengukur absorbansi
dari larutan baku kalsium pada panjang gelombang 422,7 nm sehingga diperoleh persamaan garis regresi Y = 0,0306X+0,0027 dengan koefisien
korelasi (r) = 0,9985 (Data dan perhitungan persamaan garis regresi dapat dilihat pada Lampiran 7, halaman 48).
Berdasarkan hasil pengukuran tersebut diperoleh kurva kalibrasi larutan
baku kalsium yang dapat dilihat pada Gambar 4.2.
y = 0,0347X +0,0012 r = 0,9995
‐0,05 0 0,05 0,1 0,15
0 1 2 3 4 5
Absorbansi
Gambar 4.2 Kurva Kalibrasi Larutan Baku Kalsium
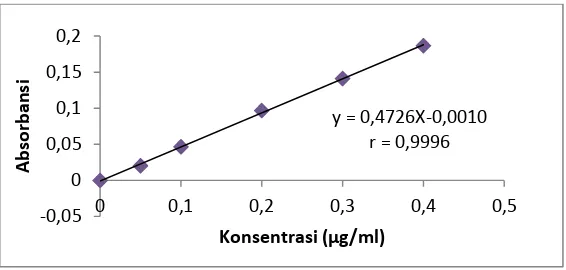
Kurva kalibrasi magnesium diperoleh dengan cara mengukur absorbansi
dari larutan baku magnesium pada panjang gelombang 285,20 nm sehingga
diperoleh persamaan garis regresi Y = 0,4726X – 0,0010 dengan koefisien
korelasi (r) = 0,9996 (Data dan perhitungan persamaan garis regresi dapat dilihat pada Lampiran 8, halaman 49).
Berdasarkan hasil pengukuran tersebut diperoleh kurva kalibrasi larutan
baku magnesium yang dapat dilihat pada Gambar 4.3.
Gambar 3.3 Kurva Kalibrasi Larutan Baku Magnesium
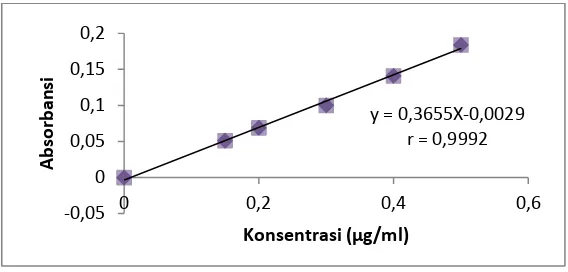
Kurva kalibrasi natrium diperoleh dengan cara mengukur absorbansi dari
larutan baku natrium pada panjang gelombang 589,00 nm sehingga diperoleh
persamaan garis regresi Y = 0,3655X - 0,0029 dengan koefisien korelasi (r) =
y = ,0,0306X+ 0,0027 r = 0,9985 0
0,05 0,1 0,15
0 2 4 6
Absorbansi
Konsentrasi (µg/ml)
y = 0,4726X‐0,0010 r = 0,9996
‐0,05 0 0,05 0,1 0,15 0,2
0 0,1 0,2 0,3 0,4 0,5
Absorbansi
[image:49.595.163.446.461.596.2]0,9992. (Data dan perhitungan persamaan garis regresi dapat dilihat pada Lampiran 9, halaman50).
Berdasarkan hasil pengukuran tersebut diperoleh kurva kalibrasi larutan
baku natrium yang dapat dilihat pada Gambar 4.4.
[image:50.595.168.452.208.344.2]
Gambar 4.4 Kurva Kalibrasi Larutan Baku Natrium
Berdasarkan kurva kalibrasi dari keempat mineral diatas diperoleh hubungan yang linear antara konsentrasi dengan absorbansi, dengan koefisien korelasi (r) untuk kalium sebesar 0,9995; untuk kalsium sebesar 0,9985; untuk magnesium sebesar 0,9996 dan untuk natrium sebesar 0,9992. Nilai r ≥ 0,97 menunjukkan adanya korelasi linier yang menyatakan adanya hubungan antara X (konsentrasi) dan Y (absorbansi) (Ermer, 2005).
4.2.2 Pengukuran Kadar Kalium, Kalsium, Natrium, dan Magnesium dalam Sampel
Pada pengukuran sampel yang dilakukan secara spektrofotometri serapan atom, terlebih dahulu dikondisikan alat dengan baik dan benar. Setelah itu, dilakukan pengenceran terhadap sampel. Pengenceran yang dilakukan yaitu sebesar 100 kali (25/0,25) untuk kalium; 5 kali (25/5) untuk kalsium; 50 kali
y = 0,3655X‐0,0029 r = 0,9992
‐0,05 0 0,05 0,1 0,15 0,2
0 0,2 0,4 0,6
Absorbansi
(25/0,5) untuk magnesium dan 50 kali (25/0,5) untuk natrium. Selain itu, karena sampel memiliki kadar mineral yang cukup tinggi sehingga agar diperoleh nilai absorbansi yang berada dalam rentang kalibrasi maka sampel harus diencerkan. Konsentrasi kalium, kalsium, magnesium dan natrium dalam sampel ditentukan berdasarkan persamaan garis regresi kurva kalibrasi larutan baku kalium, kalsium, magnesium dan natrium. (Data dan contoh perhitungan dapat dilihat pada Lampiran 10, halaman 51 dan Lampiran 11, halaman 52-53.
[image:51.595.109.501.394.483.2]Analisis dilanjutkan dengan perhitungan statistik (Perhitungan dapat dilihat pada Lampiran 12, halaman 54-57). Hasil analisis kuantitatif kalium, kalsium, natrium, dan magnesium pada sampel dapat dilihat pada Tabel 3. Tabel 3. Kadar Kalium, Kalsium, Magnesium dan Natrium Pada Sampel
Sampel
Kadar Kalium (mg/100 g)
Kadar Kalsium (mg/100 g)
Kadar Magnesium
(mg/100 g)
Kadar Natrium (mg/100 g)
Strawberry
176,1413 ±
2,5627
10,5901±
0,1910
7,5775 ±
0,1914
5,9462±
0,3526
Setelah dilakukan uji Q dengan taraf kepercayaan 95% terhadap kadar sampel menunjukkan bahwa kadar masing-masing mineral kalium, kalsium, magnesium dan natrium yang terdapat dalam sampel yaitu kadar kalium sebesar 176,1413 ± 2,5627 mg/100 g, kadar kalsium sebesar 10,5901 ± 0,1910mg/100 g, kadar magnesium sebesar 7,5775 ± 0,1914mg/100 g dan kadar natriumnya sebesar 5,9462 ± 0,3526 mg/100 g. Hasil penelitian menunjukkan bahwa kadar kalium, kalsium, magnesium dan natrium lebih
untuk natrium (Hancock, 1990). Hal ini disebabkan berbagai faktor diantaranya dipengaruhi oleh keadaan tanah, letak geografis, tempat tumbuh dan keadaan musim (Tim Karya Tani Mandiri, 2010).
4.3 Validasi Metode Analisis
4.3.1 Uji Perolehan Kembali (Recovery)
Hasil uji perolehan kembali (recovery) kadar kalium, kalsium, magnesium dan natrium setelah penambahan masing-masing larutan baku dapat dilihat pada Lampiran 15, halaman 66-67. Contoh perhitungannya pada Lampiran 16, halaman 68-71.
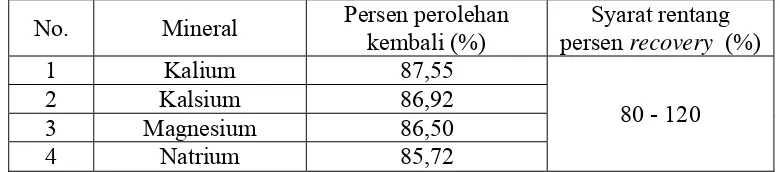
[image:52.595.109.499.472.558.2]Persen perolehan kembali (recovery) kadar mineral kalium, kalsium, magnesium dan natrium dalam sampel dapat dilihat pada Tabel 4.
Tabel 4. Persen Uji Perolehan Kembali (recovery) Kalium, Kalsium, Magnesium dan Natrium dalam Sampel
No. Mineral Persen perolehan kembali (%)
Syarat rentang persen recovery (%)
1 Kalium 87,55
80 - 120
2 Kalsium 86,92
3 Magnesium 86,50
4 Natrium 85,72
memberikan ketepatan pada pemeriksaan kadar mineral dalam sampel. Menurut Ermer (2005), suatu metode dikatakan teliti jika nilai perolehan kembalinya antara 80-120%.
4.3.2 Simpangan Baku Relatif
Dari perhitungan yang dilakukan terhadap data hasil pengukuran kadar mineral kalium, kalsium, magnesium dan natrium pada buah strawberry (Fragaria ananassa Duchesne.) diperoleh nilai Simpangan Baku (SD) sebesar 6,6802 untuk mineral kalium; 0,2961 untuk mineral kalsium; 0,2965 untuk mineral magnesium; 0,3661 untuk mineral natrium dan nilai Simpangan Baku Relatif (RSD) sebesar 2,05% untuk mineral kalium; 1,53% untuk mineral kalsium; 2,04% untuk mineral magnesium; 3,30% untuk mineral natrium.
Menurut Harmita (2004), nilai Simpangan Baku Relatif (RSD) untuk analit dengan kadar part per million (ppm) adalah ≤ 16%. Dari hasil yang diperoleh menunjukkan bahwa metode yang dilakukan memiliki presisi yang baik. Data perhitungan Simpangan Baku Relatif (RSD) kadar mineral kalium, kalsium, magnesium dan natrium dapat dilihat pada Lampiran 13, halaman 58-61.
4.3.3 Batas Deteksi dan Batas Kuantitasi
Berdasarkan data kurva kalibrasi kalium, kalsium, magnesium dan natrium diperoleh batas deteksi dan batas kuantitas untuk keempat mineral tersebut.
Dari hasil perhitungan diperoleh batas deteksi untuk mineral kalium, kalsium,
mineral kalium, kalsium, magnesium dan natrium masing-masing sebesar
0,0182 mcg/ml; 0,9447 mcg/ml; 0,0461 mcg/ml dan 0,0823 mcg/ml.
Dari hasil perhitungan dapat dilihat bahwa semua hasil yang diperoleh pada
pengukuran sampel berada diatas batas deteksi dan batas kuantitasi.
Perhitungan batas deteksi dan batas kuantitasi mineral kalium, kalsium,
BAB V
KESIMPULAN DAN SARAN
5.1 Kesimpulan
Berdasarkan hasil pemeriksaan kandungan kalium, kalsium, magnesium dan natrium pada strawberry yang diuji dengan reaksi kualitatif menunjukkan hasil yang positif bahwa kandungan mineral kalium, kalsium, magnesium dan natrium pada strawberry dapat diuji dengan reaksi kualitatif.
Hasil analisis mineral kalium, kalsium, magnesium dan natrium pada strawberry secara kuantitatif dengan menggunakan spektrofotometer serapan atom menunjukkan bahwa masing-masing kadar mineral kalium, kalsium, magnesium dan natrium pada strawberry adalah (176,1413 ± 2,5627) mg/100 g, (10,5901 ± 0,1910) mg/100 g, (7,5775 ± 0,1914) mg/100 g dan (5,9462 ± 0,3526) mg/100 g.
5.2 Saran
DAFTAR PUSTAKA
Achadi, L.E. (2007). Gizi dan Kesehatan Masyarakat. Edisi I. Departemen Gizi dan Kesehatan Masyarakat Fakultas Kesehatan Masyarakat, Universitas Indonesia. Jakarta: PT. Raja Grafindo Persada. Halaman 94.
Almatsier, S. (2004). Prinsip Dasar Ilmu Gizi. Jakarta: PT. Gramedia Pustaka Utama. Halaman 228-229, 233-237, 242-247.
Barasi, M. (2007). Nutrition at a Glance. Penerjemah: Hermin. (2009). At a Glance: Ilmu Gizi. Jakarta: Penerbit Erlangga. Halaman 52.
Budiyanto, M.A.K. (2001). Dasar Dasar Ilmu Gizi. Edisi Kedua. Cetakan I. Malang: UMM- Press. Halaman 59.
Ditjen POM. (1979). Farmakope Indonesia. Edisi Ketiga. Jakarta: Departemen Kesehatan RI. Halaman 744,748.
Ermer, J. (2005). Method Validation in Pharmaceutical Analysis. Weinheim: Wiley-Vch Verlag GmbH & Co. KGaA. Halaman171.
Gandjar, I.G., dan Rohman, A.(2007). Kimia Farmasi Analisis. Cetakan I. Yogyakarta: PustakaPelajar. Halaman 298-312.
Harmita. (2004). Petunjuk Pelaksanaan Validasi Metode dan Cara Perhitungannya. Review Artikel. Majalah Ilmu Kefarmasian. 1(3): 117-119, 121-122, 127-128, 130.
Helrich, K. (1990). Official Methods of the Association of Official Analytical Chemist. Edisi kelimabelas. Virginia: AOAC International. Hal. 42
Khopkar, S.M. (1985). Basic Concepts of Analytical Chemistry. Penerjemah: Saptorahardjo.(2003). Konsep Dasar Kimia Analitik. Jakarta: UI-Press. Halaman 283.
Kristanti, H. (2010). Penyakit Akibat Kelebihan & Kekurangan Vitamin, Mineral & Elektrolit. Cetakan I. Yogyakarta: Citra Pustaka. Halaman 146,152.
Sudarmadji, S., Bambang, H., dan Suhardi. (1996). Analisis Bahan Makanan Dan Pertanian. Yogyakarta: Universitas Gadjah Mada. Halaman 151.
Tan, T.H., dan Rahardja, K. (2007). Obat-Obat Penting. Edisi VI. Jakarta: PT Elex Media Komputindo. Halaman 867-868.
Tim Karya Tani Mandiri. (2010). Pedoman Bertanam Stroberi. Cetakan I. Bandung: Nuansa Aulia. Halaman 1-3, 105- 112.
Lampiran 2. Sampel yang digunakan
Lampiran
Gambar 2
Gambar 3
n 3. Hasil A Magne Duche
2. Hasil ana pada bua
3. Hasil ana pada bu
Analisis Kua esium Pada esne.)
alisis kualita ah strawberr
alisis kualita uah strawber
alitatif Kaliu Buah straw
atif kalium d ry (Fragaria
atif natrium rry (Fragar
um, Kalsium wberry (Frag
dengan asam a ananassa
m dengan asa ria ananassa
m, Natrium, garia anana
m pikrat 1% Duchesne.)
am pikrat 1 a Duchesne Kalium
Kris Natri Pikr
, dan assa
% b/v )
% b/v e.) m pikrat
[image:60.595.121.477.473.686.2]Gambar 4
Gambar 5
4. Hasil ana pada bua
5. Hasil reak 0,1% b/v N
alisis kualita ah strawber
ksi kualitati v pada buah
Akuabides + NaOH + Kuning
Titan 0,1%
atif kalsium rry (Fragari
if magnesiu h strawberry Samp
+ Ku
m dengan asa ia ananassa
um dengan l y (Fragaria
el + NaOH uning Titan
0,1%
am sulfat 1 N a Duchesne.
larutan Titan ananassa D Ka
N .)
[image:61.595.187.414.393.637.2]Lampiran 4. Bagan Alir Proses Destruksi Kering
Buah strawberry
Ditimbang 10 gram di atas krus Diarangkan di atas hot plate
Diabukan dalam tanur dengan temperatur awal 100oCdan perlahan – lahan temperatur dinaikkan hingga suhu 500oC dengan interval 25oC setiap 5 menit
Dibasahi dengan 10 tetes akuabides Ditambahkan 5 ml HNO3(1:1)
Diuapkan pada hot platesampai kering
Hasil
Dilakukan selama 24 jam dan dibiarkan hingga dingin pada desikator
Abu
Dilakukan selama 1 jam dan dibiarkan hingga dingin pada desikator
Dibersihkan dari pengotoran
Dimasukkan kembali ke dalam tanur dengan temperatur awal 100oCdan perlahan – lahan temperatur dinaikkan hingga suhu 500oC dengan interval 25oC setiap 5 menit.
Dicuci bersih
Lampiran 5. Bagan Alir Proses Pembuatan Larutan Sampel
Sampel yang telah didestruksi
Dilarutkan dengan 5 ml HNO3 (1:1) dalam k
Dituangkan ke dalam labu tentukur 50 ml Diencerkan dengan akuabides hingga garis tanda
Dimasukkan ke dalam botol Larutan sampel
Disaring dengan kertas saring Whatman No.42 42N 42
Filtra t
Dibuang 5 ml untuk menjenuhkan kertas saring
Dilakukan analisis kualitatif
Dilakukan analisis kuantitatif dengan Spektrofotometer Serapan atom pada 766,5 nm untuk logam kalium, 422,7 nm untuk logam kalsium, 589,00 nm untuk logam natrium dan 285,2 nm untuk logam magnesium
Lampiran 6. Data Kalibrasi Kalium dengan Spektrofotometer Serapan Atom dan Perhitungan Persamaan Garis Regresi dan Koefisien Korelasi N o. Konsentrasi (mg/l) (X) Absorbansi (Y)
1. 0,0000 -0,0002
2. 0,5000 0,0181
3. 1,0000 0,0362
4. 2,0000 0,0725
5. 3,0000 0,1069
6. 4,0000 0,1375
No. X Y XY X2 Y2x10-4
1. 0,0000 -0,0002 0,0000 0,0000 0,0004
2. 0,5000 0,0181 0,0091 0,2500 3,2761
3. 1,0000 0,0362 0,0362 1,0000 13,1044
4. 2,0000 0,0725 0,1450 4,0000 52,5625
5. 3,0000 0,1069 0,3207 9,0000 114,2761
6. 4,0000 0,1375 0,5512 16,0000 189,8884
10,500
X =1,7500
0,3713
Y = 0,0619
1,0622 30,2500 373,1079
a =
X
nX n Y X XY / / 2 2
=
10,5000
/6 2500 , 30 6 / ) 3713 , 0 ( 5000 , 10 0622 , 1 2 = 0,0347
Y = a X + b b = Y aX
= 0,0619 – (0,0347)(1,7500) = 0,0012
Maka persamaan garis regresinya adalah: Y = 0,0347X + 0,0012
=
30,2500 10,5000 /6
373,1079x10-4
0,3713
/6
6 / ) 3713 , 0 ( 5000 , 10 0622 , 1 2 2 = 4126 , 0 4124 , 0 = 0,9995Lampiran 7. Data Kalibrasi Kalsium dengan Spektrofotometer Serapan Atom dan Perhitungan Persamaan Garis Regresi dan Koefisien Korelasi (r)
No. Konsentrasi (mg/l)
(X)
Absorbansi (Y)
1. 0,0000 0,0002
2. 0,5000 0,0166
3. 1,0000 0,0357
4. 2,0000 0,0671
5. 3,0000 0,0954
6. 4,0000 0,1222
No. X Y XY X2 Y2x10-4
1. 0,0000 0,0002 0,0000 0,0000 0,0004
2. 0,5000 0,0166 0,0083 0,2500 2,7556
3. 1,0000 0,0357 0,0357 1,0000 12,7449
4. 2,0000 0,0671 0,1342 4,0000 45,0241
5. 3,0000 0,0954 0,2862 9,0000 91,0116
6. 4,0000 0,1222 0,4888 16,0000 149,3284
10,5000
X = 1,7500
0,3372
Y = 0,0562
0,9532 30,2500 300,865
a =
X
nX n Y X XY / / 2 2
=
10,5000
/6 2500 , 30 6 / 3372 , 0 5000 , 10 9532 , 0 2 = 0,0306
Y = a X + b b = Y aX
Maka persamaan garis regresinya adalah: Y = 0,0306X + 0,0027
=
30,2500 10,5000 /6
300,8650x10-4
0,3372
/6
6 / 3372 , 0 5000 , 10 9532 , 0 2 2 = 0,3636 3631 , 0= 0,9985
Lampiran 8. Data Kalibrasi Magnesium dengan Spektrofotometer Serapan Atom dan Perhitungan Persamaan Garis Regresi dan Koefisien Korelasi. N o. Konsentrasi (mg/l) (X) Absorbansi (Y)
1. 0,0000 -0,0004
2. 0,0500 0,0201
3. 0,1000 0,0464
4. 0,2000 0,0967
5. 0,3000 0,1411
6. 0,4000 0,1866
No. X Y XY X2 Y2x10-4
1. 0,0000 -0,0004 0,0000 0,0000 0,0016
2. 0,0500 0,0201 0,0011 0,0025 4,0401
3. 0,1000 0,0464 0,0046 0,01 21,5296 4. 0,2000 0,0967 0,0193 0,04 93,5089 5. 0,3000 0,1411 0,0423 0,09 199,0921 6. 0,4000 0,1866 0,0746 0,16 348,1956
1,0500
X =0,1750
0,4905
Y = 0,0818
0,1419 0,3025 666,3679
a =
X
nX n Y X XY / / 2 2
=
1,0500
/6 3025 , 0 6 / ) 4905 , 0 ( 0500 , 1 1419 , 0 2 = 0,4726
Y = a X + b b = Y aX
= 0,0818 – (0,4726)(0,1750) = -0,0010
Maka persamaan garis regresinya adalah: Y = 0,4726X – 0,0010
=
0,3025 1,0500 /6
666,3679x10-4
0,4905
/6
6 / ) 4905 , 0 ( 0500 , 1 1419 , 0 2 2 = 05613 , 0 05611 , 0 = 0,9996Lampiran 9. Data Kalibrasi Natrium dengan Spektrofotometer Serapan Atom Dan Perhitungan Persamaan Garis Regresi dan Koefisien
Korelasi. N o. Konsentrasi (mg/l) (X) Absorbansi (Y)
1. 0,0000 -0,0001
2. 0,1500 0,0511
3. 0,2000 0,0690
4. 0,3000 0,1046
5. 0,4000 0,1410
6. 0,5000 0,1839
No. X Y XY X2 Y2x10-4
1. 0,0000 -0,0001 0,0000 0,0000 0,0001
2. 0,1500 0,0511 0,0076 0,0225 26,1121
3. 0,2000 0,0690 0,0138 0,04 47,6100
4. 0,3000 0,1046 0,0313 0,09 109,4116
5. 0,4000 0,1410 0,0564 0,16 198,8100
6. 0,5000 0,1839 0,0919 0,25 338,1921
1,5500
X = 0,2583
0,5495
Y = 0,0915
0,2011 0,5625 720,1359
a =
X
n=
1,55 /6 5625 , 0 6 / ) 5495 , 0 ( 5500 , 1 2011 , 0 2 = 0,3655
Y = a X + b b = Y aX
= 0,0915 – (0,3655)(0,2583) = -0,0029
Maka persamaan garis regresinya adalah: Y = 0,3655X – 0,0029
=
0,5625 1,5500 /6
720,1359x10-4
0,5495
/6
6 / ) 5495 , 0 ( 5500 , 1 2011 , 0 2 2 = 05929 , 0 05924 , 0 = 0,9992Lampiran 10. Hasil Analisis Kadar Kalium, Kalsium, Magnesium dan Natrium Dalam Sampel.
1. Hasil Analisis Kalium
No Sampel Berat Sampel (g) Absorbansi (A) Konsentrasi (mcg/ml) Kadar (mg/100 g) 1. 2. 3. 4. 5. 6.
2. Hasil Analisis Kalsium
3.Hasil Analisis Magnesium
4. Hasil Analisis Natrium
Lampiran 11. Contoh Perhitungan Kadar Kalium, Kalsium, Magnesium dan Natrium Dalam Sampel.
1. Contoh Perhitungan Kadar Kalium
Berat sampel yang ditimbang = 10,0386 g Absorbansi (Y) = 0,0630
X = 0347 , 0 0012 , 0 0630 , 0 = 1,8501 Konsentrasi Kalium = 1,8501 mcg/ml
(g) Sampel Berat n pengencera Faktor x (ml) Volume x (mcg/ml) i Konsentras (mcg/g) Kalium
Kadar
= g x ml x ml mcg 0386 , 10 ) 25 , 0 / 25 ( 100 / 1,8501
= 1842,9860 mcg/g = 184,29860 mg/100 g 2. Contoh Perhitungan Kadar Kalsium
Berat sampel yang ditimbang = 10,0116 g Absorbansi (Y) = 0,0613
Persamaan Regresi: Y = 0,0306 X + 0,0027 X =
0306 , 0 0027 , 0 0613 , 0 = 2,0915 Konsentrasi Kalium = 2,0915 mcg/ml
(g) Sampel Berat n pengencera Faktor x (ml) Volume x (mcg/ml) i Konsentras (mcg/g) Kalisum
Kadar
= g x ml x ml mcg 0386 , 10 5 100 / 2,0915
= 104,1728 mcg/g = 10,41728 mg/100 g
3. Contoh Perhitungan Kadar Natrium Berat sampel yang ditimbang = 25,020 g
Absorbansi (Y) = 0,0640
(g) Sampel Berat n pengencera Faktor x (ml) Volume x (mcg/ml) i Konsentras (mcg/g) Na
Kadar
= g mlx mlx mcg 020 , 25 50 100 / 1671 , 0
= 83,3832 mcg/g = 8,3383 mg/100g 4. Contoh Perhitungan Kadar Magnesium Berat sampel yang ditimbang = 10,0386 g
Absorbansi (Y) = 0,0743
Persamaan Regresi: Y = 0,4726 X - 0,0010 X = 4726 , 0 0010 , 0 0743 , 0 = 0,1550 Konsentrasi Magnesium = 0,1550 mcg/ml
(g) Sampel Berat n pengencera Faktor x (ml) Volume x (mcg/ml) i Konsentras (mcg/g) Mg
Kadar
= g mlx mlx mcg 0386 , 10 50 100 / 0,1550
= 77,2020 mcg/g = 7,72020 mg/100g
Lampiran 12. Perhitungan Statistik Kadar Kalium, Kalsium, Magnesium dan Natrium Dalam Sampel
1. Perhitungan Statistik Kadar Kalium Dalam Sampel
No. X
(Kadar mg/100 g ) X - X (X - X) 2
1 184,2986 8,1573 66,5415
2 176,1556 0,0143 0,0002
3 170,2820 -5,8593 34,3313
4 168,7246 -7,4167 55,0074
5 180,5853 4,444 19,7491
6 176,8021 0,6608 0,4366
∑X = 1056,8482
X = 176,1413 ∑(X - X)
2
Dari 6 data yang diperoleh data ke-3 adalah yang paling menyimpang sehingga diuji dengan uji Q.
170,2820–168,7246 Q = = 0,1 184,2986–168,7246
Nilai Q yang diperoleh tidak melebihi nilai Q0,95 yaitu 0,621 sehingga semua data diterima.
SD=
1 -n
X -Xi 2
SD = 2,4225
5 29,3443
Rata-rata kadar kalium dengan selang kepercayaan 95% dengan nilai α = 0,05; n = 6; dk = 5, dari tabel distribusi t diperoleh nilai t tabel = 2,5706
= X ± (t (α/2, dk) x SD / √n )
= 176,1413 mg/100 g ± ((2,5706 x 2,4225 )/√6) mg/100 g = (176,1413± 2,5627) mg/100 g
2. Perhitungan Statistik Kadar Kalsium Dalam Sampel
No. X
(Kadar mg/100g ) X - X (X - X) 2
1 10,4172 -0,1729 0,0298
2 10,7879 0,1978 0,0391
3 10,5991 0,009 0,000081
4 10,7886 0,1985 0,0394
5 10,5979 0,0078 0,000060
6 10,3504 0,2397 0,0574
∑X = 63,5411
X = 10,5901 ∑(X - X)
2
= 0,1658
25,1632–24,3064
Q = = 1,9552 10,7886–10,3504
Nilai Q yang diperoleh tidak melebihi nilai Q0,95 yaitu 0,621 sehingga semua data diterima.
SD=
1 -n
X -Xi 2
SD = 0,1820 5
0,1658
Rata-rata kadar kalsium dengan selang kepercayaan 95% dengan nilai α = 0,05; n = 6; dk = 5, dari tabel distribusi t diperoleh nilai t tabel = 2,5706
= X ± (t (α/2, dk) x SD / √n )
= 10,5901 mg/100 g ± ((2,5706 x 0,1820)/√6) mg/100 g = (10,5901± 0,1910) mg/100 g
3. Perhitungan Statistik Kadar Natrium Dalam Sampel
No. X
(Kadar mg/100 g) X - X (X - X) 2
1 5,6930 -0,2532 0,0641
2 6,3925 0,4463 0,1991
3 5,5850 -0,3612 0,1304
4 5,7401 0,2061 0,0424
5 5,9623 0,0161 0,00025
6 6,3047 0,3585 0,1285
∑X = 35,6776
X = 8,4679 ∑(X – X) 2
= 0,5647
Dari 6 data yang diperoleh data ke-4 adalah yang paling menyimpang sehingga diuji dengan uji Q.
5,9623 – 5,7401
Nilai Q yang diperoleh tidak melebihi nilai Q0,95 yaitu 0,621 sehingga semua data diterima.
SD =
1 -n
X -Xi 2
SD = 0,3360 5
5647 ,
0
Rata-rata kadar natrium dengan selang kepercayaan 95% dengan nilai α = 0,05; n = 6; dk = 5, dari tabel distribusi t diperoleh nilai t tabel = 2,5706
= X ± (t (α/2, dk) x SD / √n )
= 5,9462 mg/100 g ± ((2,5706 x 0,3360)/√6) mg/100 g = (5,9462 ± 0,3526) mg/100 g
4. Perhitungan Statistik Kadar Magnesium Dalam Sampel
No. X
(Kadar mg/100 g) X – X (X - X) 2
1 7,7202 0,1427 0,0203
2 7,3115 -0,266 0,0707
3 7,3886 -0,1889 0,0356
4 7,6253 0,0478 0,0022
5 7,6736 0,0961 0,0092
6 7,7462 0,1687 0,0284
∑X = 45,4654
X =7,5775 ∑(X - X) 2
= 0,1664
Dari 6 data yang diperoleh, data ke-2 adalah yang paling menyimpang sehingga diuji dengan uji Q.
7,3115 - 7,3886
Nilai Q yang diperoleh tidak melebihi nilai Q0,95 yaitu 0,621 sehingga semua data diterima.
SD =
1 -n
X -Xi 2
SD = 0,1824 5
0,1664
Rata-rata kadar natrium dengan selang kepercayaan 95% dengan nilai α = 0,05; n = 6; dk = 5, dari tabel distribusi t diperoleh nilai t tabel = 2,5706
= X ± (t (α/2, dk) x SD / √n )
= 7,5775 mg/100 g ± ((2,5706 x 0,1824)/√6) mg/100 g = (7,5775 ± 0,1914) mg/100 g
Lampiran 13. Perhitungan Simpangan Baku Relatif (RSD) Kadar Kalium, Kalsium, Natrium dan Magnesium pada Sampel