i
UIN SYARIF HIDAYATULLAH JAKARTA
PEMBUATAN MIKROPARTIKEL
DILTIAZEM HIDROKLORIDA MENGGUNAKAN
METODE PENGUAPAN PELARUT
SKRIPSI
EVI NURUL HIDAYATI
1111102000131
FAKULTAS KEDOKTERAN DAN ILMU KESEHATAN
PROGRAM STUDI FARMASI
ii
UIN SYARIF HIDAYATULLAH JAKARTA
PEMBUATAN MIKROPARTIKEL
DILTIAZEM HIDROKLORIDA MENGGUNAKAN
METODE PENGUAPAN PELARUT
SKRIPSI
Diajukan sebagai salah satu syarat memperoleh gelar Sarjana Farmasi
EVI NURUL HIDAYATI
1111102000131
FAKULTAS KEDOKTERAN DAN ILMU KESEHATAN
PROGRAM STUDI FARMASI
vi Nama : Evi Nurul Hidayati Program Studi : Farmasi
Judul Penelitian : Pembuatan Mikopartikel Diltiazem Hidroklorida Menggunakan Metode Penguapan Pelarut
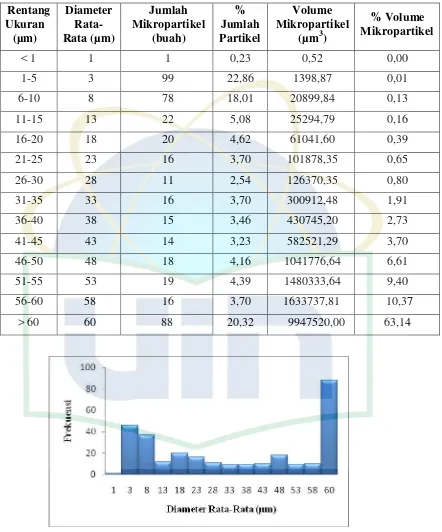
Mikropartikel merupakan salah satu sistem penghantaran obat yang berpotensi untuk dikembangkan karena sistem ini dapat menjadi alternatif penghantaran beberapa sediaan konvensional. Metode penguapan pelarut adalah metode pembuatan mikropartikel yang sederhana dan efektif untuk menghasilkan mikropartikel. Metode yang digunakan pada penelitian ini adalah metode penguapan pelarut menggunakan sistem emulsi minyak/air. Tujuan penelitian ini adalah formulasi dan karakterisasi mikropartikel diltiazem hidroklorida. Bahan yang digunakan adalah etil selulosa, diltiazem hidroklorida dan polivinil alkohol. Mikropartikel dibuat dalam dua formula yaitu F1 dan F2 dengan variasi pada konsentrasi surfaktan. Konsentrasi surfaktan yang digunakan untuk F1 dan F2 berturut-turut adalah 0,8% dan 1%. Mikropartikel yang terbentuk dianalisa apakah berpotensi untuk dihantarkan melalui paru-paru. Berikutnya dilakukan karakterisasi mikropartikel, yaitu ukuran mikropartikel, kadar obat, efisiensi penjerapan, perolehan kembali, dan pelepasan obat. Hasil karakterisasi mikropartikel F1 dan F2 berturut-turut yaitu perolehan kembali 77,51% dan 57,51%. Rentang ukuran yaitu sebesar 0,680-159,740 µm dan 0,340-117,674 µm. Kadar obat yaitu 3,51±0,02 % dan 3,91±0,01 %. Efisiensi penjerapan yaitu 9,57±0,02 % dan 7,87±0,01 %. Hasil disolusi selama 8 jam mencapai 7,44±0,32% pada F1 dan 6,94±0,05% pada F2. Apabila dianalisa dari hasil karakterisasi mikropartikel, metode ini belum bisa menghasilkan mikropartikel yang sesuai untuk sistem penghantaran obat melalui paru-paru.
vii Name : Evi Nurul Hidayati
Major : Pharmacy
Title : Formulation Microparticle of Diltiazem Hydrochloride using Solvent Evaporation Methode
Microparticle is a drug delivery system that has potential to be developed because this system can be an alternative to deliver some conventional dosages. Solvent evaporation method is a microparticle preparation method that is simple and effective to produce microparticles. The method that was used for this study is solvent evaporation method using o/w system. The purpose of this study is to formulate and characterize diltiazem hydrochloride microparticles. Materials used in this study are ethyl cellulose, diltiazem hydrochloride and polyvinyl alcohol. Microparticle were formulated in two formulas termed F1 and F2 with variation in surfactant concentration. Surfactant concentration used for F1 and F2 respectively 0,8% and 1%. Microparticles from this method is analyzed whether it has potential to be delivered through the pulmonary drug delivery system. Microparticles was characterized with various parameters such us, the microparticle size, drug loading, drug entrapment efficiency, % yield, and drug release. The characterization results of microparticle F1 and F2 were respectively 77.51% and 57.51%. The size range was 0.680 to 159.740 μm and 0.340 to
117.674 μm. The drug contentwas3.51 and 3.91 ± 0.02% ± 0.01%. The drug
entrapment efficiency was 0.02% ± 9.57 and 7.87 ± 0.01%. The dissolution results for 8 hours reached 7.44 ± 0.32%for F1 and 6.94 ± 0.05% for F2. If its analyzed from the microparticle characterization, this method can not produce sufficient microparticle for pulmonary drug delivery system.
viii
Alhamdulillahirobbil’alamin, puji dan syukur penulis ucapkan kepada
Allah SWT yang telah melimpahkan rahmat, ridho dan hidayah-Nya sehingga
penulis dapaat menyelesaikan penyusunan skripsi ini hingga selesai. Penulisan
skripsi berjudul “Pembuatan Mikropartikel Diltiazem Hidroklorida Menggunakan Metode Penguapan Pelarut” bertujuan untuk memenuhi persyaratan guna mendapatkan gelar Sarjana Farmasi pada Fakultas Kedokteran dan Ilmu
Kesehatan Universitas Islam Negeri Syarif Hidayatullah Jakarta.
Pada kesempatan ini penulis menyadari bahwa tanpa bantuan dan
bimbingan dari berbagai pihak, sejak masa perkuliahan hingga penyusunan skripsi
ini, sangat sulit bagi penulis untuk menyelesaikan skripsi ini. Oleh karna itu,
penulis mengucapkan terima kasih dan penghargaan sebesar-besarnya kepada:
1. Ibu Yuni Anggraeni, M.Farm., Apt dan Ibu Nelly Suryani, Ph.D., Apt, selaku
dosen pembimbing yang telah banyak memberikan bimbingan, wakt, tenaga,
saran, dan dukungan dalam penyusunan skripsi ini.
2. Bapak Dr. H. Arif Sumantri, SKM.,M.Kes selaku Dekan Fakultas Kedokteran
dan Ilmu Kesehatan Uiniversitas Isalam Negeri Syarif Hidayatullah Jakarta
3. Bapak Yardi, Ph.D., Apt selaku ketua program studi Fakultas Kedokteran dan
Ilmu Kesehatan Uiniversitas Isalam Negeri Syarif Hidayatullah Jakarta
4. Seluruh dosen di Program Studi Farmasi Fakultas Kedokteran dan Ilmu
Kesehatan Universitas Islam Negeri Syarif Hidayatullah Jakarta atas ilmu
pengetahuan yang telah diberikan kepada saya.
5. Kedua orang tua, ayahanda Drs. Abd. Rochim dan ibunda Dra. Elik
Zunniaroh yang senantiasa memberikan doa, semangat dan kasih sayang yang
tidak pernah putus, serta dukungan moril maupun materil. Sungguh besar jasa
beliau, tidak ada apapun di dunia ini yang mampu membalas pengorbanan
beliau. Semoga Allah selalu memberikan keberkahan, kesehatan,
keselamatan, perlindungan, rahmat kepada kedua orang tua hamba.
6. Kedua kakak saya, Muhammad Syaifuddin Zuhri dan Nurur Rahmawati yang
telah memberikan doa, semangat, kasih sayang, dan dukungan moril maupun
ix
8. Kakak-kakak laboran FKIK, kak Eris, kak Rahmadi, mba Rani, kak Tiwi, kak
Lisna atas dukungan dan kerjasamanya selama kegiatan penelitian
9. Lela Laelatu R, Athiyah, Silvia Aryani, Annisa Tiana S.P, Annisa Nurul
Azzahra serta teman-teman seperjuangan yang telah memberikan semangat
dan kebersamaannya, terima kasih atas kerjasama dalam penelitian ini
10. Teman-teman seperjuangan farmasi angkatan 2011 atas dukungan dan
kebersamaannya
11. Serta pihak-pihak lain yang tidak dapat disebutkan satu persatu, yang telah
memberikan dukungan hingga terwujudnya skripsi ini.
Penulis menyadari bahwa penelitian ini masih jauh dari sempurna, namun
penulis berharap semoga hasil penelitian ini dapat bermanfaat bagi perkembangan
ilmu pengehtahuan pada umumnya, dan ilmu farmasi pada khususnya. Akhir kata
penulis berharap Allah SWT berkenan membalas segala kebaikan semua pihak
yang telah membantu penulis dalam menyelesaikan penelitian ini.
Ciputat, 2 Juli 2015
xi DAFTAR ISI
HALAMAN JUDUL ... ii
HALAMAN PERSETUJUAN PEMBIMBING ... iii
DAFTAR ISI ... iv
2.2.1 Presipitasi Partikel dengan Penambahan Bukan Pelarut (Koaservasi) ... 8
2.2 2 Presipitasi Partikel dengan Partisis Pelarut ... 9
2.2 3 Semprot Kering (Spray Drying) ... 10
2.2 4 Metode Ekstraksi Cairan Superkritis... 11
2.2 5 Metode Penguapan Pelarut ... 12
2.2 5.1 Proses Emulsi Tunggal ... 13
2 5.1.2 Proses Emulsi Ganda ... 16
2.3 Pembuatan Mikropartikel Menggunakan Metode Penguapan Pelarut ... 18
2.3 1 Material ... 18
2.3 1.1 Fase Dispersi ... 18
2.3 1.1 Fase Kontinyu ... 22
2.3.2 Kondisi dalam Pembuatan Mikropartikel Menggunakan Metode Penguapan Pelarut ... 23
xii
3.3.2 Pembuatan Mikropartikel ... 33
3.3.3 Penentuan Perolehan Kembali ... 33
3.3.4 Penentuan Ukuran Partikel Mikropartikel ... 34
3.3 5 Pembuatan Panjang Gelombang Maksimum dan Kurva Kalibrasi ... 34
3.3 6 Penentuan Kadar Obat dan Efisiensi Penjerapan ... 34
3.3 7 Pelepasan Obat Secara In Vitro ... 35
BAB 4. HASIL DAN PEMBAHASAN ... 36
4.1 Formulasi Mikropartikel ... 36
4.2 Perolehan Kembali ... 36
4.3 Ukuran Mikropartikel ... 37
xiii
DAFTAR GAMBAR
Gambar 2.1. Variasi Formula Mikropartikel ... 5
Gambar 2.2. Skema Empat Prinsip Proses Dalam Pembuatan Mikrosfer Menggunakan Penguapan Pelarut (Minyak/Air) ... 14
Gambar 2.3. Enkapsulasi Menggunakan Teknik Emulsi Minyak Dalam Air ... 14
Gambar 2.4. Skema empat proses utama pada proses penguapan/ekstraksi pelarut (Air/Minyak/Air) ... 18
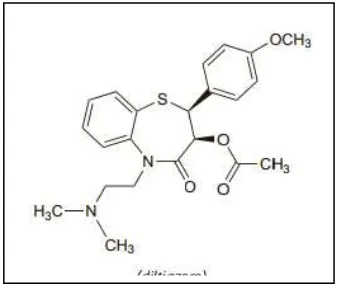
Gambar 2.5. Struktur Kimia Diltiazem Hidroklorida ... 28
Gambar 2.6. Stuktur Kimia Etil Selulosa ... 29
Gambar 2.7. Stuktur Kimia Polivinil Alkohol ... 31
Gambar 4.1. Diagram Distribusi Frekuensi Mikropartikel F1 ... 39
Gambar 4.2. Diagram Distribusi Frekuensi Mikropartikel F2 ... 40
Gambar 4.3. Kurva kalibrasi Diltiazem Hidroklorida dalam Dapar Fosfat pH 7,4 ... 41
xiv
DAFTAR TABEL
Tabel 3.1. Formula Mikropartikel Diltiazem Hidroklorida ... 33
Tabel 4.1. Efek Variabel Konsentrasi Surfaktan pada Mikropartikel Diltiazem Hidroklorida ... 37
Tabel 4.2. Efek Variabel Konsentrasi Surfaktan pada Ukuran Mikropartikel ... 37
Tabel 4.3. Distribusi Ukuran Mikropartikel F1 ... 39
Tabel 4.4. Distribusi Ukuran Mikropartikel F2 ... 40
Tabel 4.5 Efisiensi Penjerapan dan Kadar Obat Mikropartikel ... 42
xv
DAFTAR LAMPIRAN
Lampiran 1. Alur Penelitian ... 58
Lampiran 2. Pembuatan Dapar Fosfat ... 58
Lampiran 3. Scanning Panjang Gelombang Maksimum DIltiazem Hidroklorida Medium Dapar Fosfat pH 7,4 ... 59
Lampiran 4. Data Absorbansi Kurva Standar Diltiazem Hidroklorida Medium Dapar Fosfat pH 7,4 ... 59
Lampiran 5. Hasil Mikropartikel Diltiazem Hidroklorida ... 60
Lampiran 6. Hasil Uji Perolehan Kembali (PK) ... 60
Lampiran 7. Hasil Uji Disolusi pada Mikropartikel... 60
Lampiran 8. Bobot dan Persentase Terdisolusi F1 ... 61
Lampiran 9. Bobot dan Persentase Terdisolusi F2 ... 61
Lampiran 10. Gambar Alat ... 62
Lampiran 11. Contoh Perhitungan Nilai Efisiensi Penjerapan dan Kadar Obat . 62 Lampiran 12. Contoh Perhitungan Persentase Disolusi ... 62
Lampiran 13. Contoh Perhitungan Persentase Disolusi ... 64
Lampiran 14. Contoh Perhitungan Volume Mikropartikel ... 66
Lampiran 15. Sertifikat Analisis Etil Selulosa ... 67
Lampiran 16. SertifikatAnalisis Poli Vinil Alkohol ... 68
UIN Syarif Hidayatullah Jakarta
BAB 1 PENDAHULUAN
1.1.Latar Belakang
Sediaan mikropartikel adalah sediaan dengan ukuran partikel sebesar
1-1000 µm. Mikropartikel dapat menjadi penghantaran obat yang akurat,
mengurangi konsentrasi obat pada target dan memberikan sistem penghantaran
yang efektif untuk zat aktif yang sedikit larut dalam air. Selain itu sediaan
mikropartikel dapat melepaskan lebih dari 80% zat aktif dalam waktu 10 menit.
Mikropartikel dapat digunakan untuk memproduksi obat amorf dengan karakter
fisik yang diinginkan dan dapat mengurangi efek samping lokal, misalnya iritasi
saluran pencernaan pada pemberian oral (Parida, K et al., 2013). Mikropartikel
merupakan salah satu sistem penghantaran yang dapat diberikan melalui oral,
transdermal, intramuskular, intraperitonial, dan paru-paru.
Salah satu syarat penghantaran obat melalui paru-paru adalah ukuran
partikel sediaan tidak boleh lebih dari 10 µm (Hillery, A.M et al., 2005). Apabila
ukuran sediaan melebihi 10 µm, sediaan akan terdeposit pada saluran nafas atas
dan dapat dengan cepat terlepas karena batuk, tertelan dan proses pembersihan
mukus. Partikel dengan ukuran lebih kecil dari 0,5 µm akan dikeluarkan dari
paru-paru melalui proses ekspirasi sebelum terjadi sedimentasi (Taylor, G., Kellawa, I.,
2001).
Obat yang dapat dihantarkan melalui paru-paru dapat berupa obat dengan
efek lokal atau efek sistemik. Karakteristik obat dengan efek sistemik yang dapat
dihantarkan melalui paru-paru di antaranya obat yang memiliki kekurangan
apabila diberikan melalui oral, misalnya obat yang memiliki bioavaibilitas rendah
dan memiliki efek samping terkait saluran pencernaan ketika diberikan melalui
oral. Salah satu obat tersebut adalah diltiazem hidroklorida.
Terdapat beberapa metode pembuatan mikropartikel, diantaranya
penguapan pelarut (solvent evaporation), gelasi ionik, semprot kering, koaservasi,
ekstraksi cairan superkritis (Muhaimin, 2013). Adapun metode yang digunakan
pada penelitian ini adalah metode penguapan pelarut. Metode ini memiliki
UIN Syarif Hidayatullah Jakarta
beberapa keunggulan diantaranya reprodusibilitas bagus, waktu pembuatan yang
tidak lama dan alat yang digunakan mudah digunakan (Tiwari, S., P, Verma.,
2011). Beberapa hal yang dapat mempengaruhi ukuran mikropartikel
menggunakan metode penguapan pelarut adalah kecepatan pengadukan, volume
fase encer eksternal dan konsentrasi polimer. Pada faktor konsentrasi surfaktan,
semakin besar konsentrasinya maka dihasilkan ukuran mikropartikel yang lebih
kecil (Muhaimin, 2013).
Berdasarkan uraian di atas, maka dalam penelitian ini akan dibuat
mikropartikel diltiazem hidroklorida menggunakan metode penguapan pelarut.
Bahan yang digunakan pada metode penguapan pelarut ini diantaranya polimer,
pelarut yang mudah menguap, surfaktan dan zat aktif. Polimer yang digunakan
pada penelitian ini adalah etil selulosa. Etil selulosa adalah polimer hidrofilik
yang pada penelitian sebelumnya diketahui bahwa mikropartikel etil selulosa
dengan zat aktif natrium diklofenak menunjukan pola pelepasan lepas lambat
(Giri, T.K et al., 2012). Adapun pelarut yang digunakan pada formulasi diltiazem
hidroklorida ini adalah diklorometan. Diklorometan adalah pelarut yang paling
banyak digunakan untuk enkapsulasi menggunakan metode penguapan pelarut
karena volatilitas yang tinggi, titik didih rendah dan ketidakbercampuran dengan
air yang tinggi (Li et al., 2008 dalam Muhaimin, 2013). Bahan selanjutnya adalah
poli vinil alkohol (PVA) sebagai surfaktan. Fungsi surfaktan disini untuk
menurunkan tegangan permukaan antara dua fase (Li et al., 2008 dalam
Muhaimin, 2013). Berdasarkan penelitian Pandav, S., A, Lokhande., J, Naikk
(2013), PVA terbukti lebih mampu menghasilkan mikropartikel dengan stabilitas
lebih baik daripada Tween 80. Komponen berikutnya adalah zat aktif. Zat aktif
yang digunakan sebagai sampel dalam pembuatan mikropartikel ini adalah
diltiazem hidroklorida. Tujuan penggunaan zat aktif ini dalam pembuatan
mirkopartikel untuk meningkatkan bioavaibilitas zat aktif melalui sistem lepas
lambat.
Pada penelitian ini akan dibuat dua formula mikropartikel dengan variasi
pada konsentrasi surfaktan. Adapaun evaluasi yang akan dilakukan adalah
perolehan kembali, ukuran mikropartikel, efisiensi penjerapan, kadar obat, dan
UIN Syarif Hidayatullah Jakarta
1.2. Rumusan Masalah
a. Bagaimana karakteristik mikropartikel diltiazem hidroklorida menggunakan
metode penguapan pelarut?
b. Berapa nilai perolehan kembali, efisiensi penjerapan, kadar obat, dan pelepasan
obat secera in vitro dari mikropartikel diltiazem hidroklorida yang telah
diformulasi?
c. Apakah ukuran mikropartikel diltiazem hidroklorida yang terbentuk sudah
memenuhi syarat untuk sediaan penghantaran obat melalui paru-paru?
1.3.Tujuan
a. Mengetahui karakteristik mikropartikel diltiazem hidroklorida menggunakan
metode penguapan pelarut
b. Mengetahui nilai perolehan kembali, efisiensi penjerapan, kadar obat, dan
pelepasan obat secera in vitro mikropartikel diltiazem hidroklorida
c. Mengetahui apakah mikropartikel yang dihasilkan memenuhi syarat sediaan
penghantaran obat melalui paru-paru
1.4. Manfaat
Penelitian ini dapat memberikan informasi tentang formulasi dan
karakteristik mikropartikel diltiazem hidroklorida menggunakan metode
penguapan pelarutyang berguna untuk pengobatan angina pektoris, hipertensi dan
UIN Syarif Hidayatullah Jakarta
BAB 2
TINJAUAN PUSTAKA
2.1. Mikropartikel
Mikropartikel adalah sediaan dengan ukuran partikel antara 1-1000 µm.
Mikropartikel umumnya diberikan melalui intraperitonial, intramuskular,
subkutan atau langsung ke organ target. Mikropartikel merupakan sistem
penghantaran yang dapat digunakan untuk lepas lambat. Obat dilepaskan secara
perlahan melalui mekanisme erosi dan difusi dari partikel. Kecepatan pelepasan
dapat ditingkatkan dengan menurunkan berat molekul polimer, ukuran partikel
dan mengontrol polimer alam (Parida et al., 2013). Mikropartikel diklasifikasi
menjadi dua, yaitu mikropkapsul dan mikrosfer. Mikrokapsul adalah sistem
reservoir mikrometik. Pada mikrokapsul obat terpusat dalam kulit polimer dengan
ketebalan tertentu dan pelepasannya dikontrol melalui proses disolusi, difusi atau
keduanya. Mikrokapsul dengan dinding tebal umumnya melepas obat dengan
mengikuti orde nol. Mikrosfer berbentuk padat dan hampir berbentuk sistem
matriks mikrometik sferis (Parida et al., 2013). Selain itu, menurut Muhaimin
(2013), mikrosfer adalah mikropartikel sferis sedangkan mikropkapsul adalah
mikropartikel dengan inti yang dikelilingi oleh material berbeda secara nyata dari
inti tersebut. Inti dapat bersifat padatan, cairan ataupun gas. Mikropartikel juga
dideskripsikan sebagai sediaan yang terdiri dari campuran homogen dari polimer
dan zat aktif.
Gambar 2.1. Varasi Formula Mikropartikel [sumber : Birnbaum and Peppas, 2004]
UIN Syarif Hidayatullah Jakarta
Mikrosfer dapat menjaga konsentrasi obat dalam darah untuk tetap konstan
sehingga dapat meningkatkan kepatuhan pasien, menurunkan dosis dan
menurunkan kemungkinan terjadinya toksisitas. Selain itu mikrosfer juga dapat
melindungi obat dari reaksi enzimatik dan pemutusan fotolitik sehingga bentuk
sediaan ini dapat digunakan untuk penghantaran protein (Tiwari, S., P, Verma.,
2012). Mekanisme pelepasan obat dari sediaan mikrosfer menurut Tiwari, S., P,
Verma (2012) adalah sebagai berikut:
a. Sistem monolitik degradasi terkontrol
Pada sistem ini, obat larut dalam matriks dan pelepasannya tergantung pada
degradasi matriks polimer. Difusi obat lebih pelan apabila dibandingkan
dengan degradasi matriks.
b. Sistem monolitik difusi terkontrol
Obat dilepaskan melalui proses difusi sebelum atau saat degradasi matriks
polimer.
c. Sistem reservoir difusi terkontrol
Disini zat aktif dienkapsulasi dengan membran pengontrol kecepatan pelepasan
dimana obat akan berdifusi melewati membran ini. Membran polimer akan
terkikis hanya jika penghantaran obat sudah sempurna.
d. Erosi
Bahan polimer pelapis seperti beeswax dan stearil alkohol dipengaruhi oleh
hidrolisisi enzimatik dan pH.
Alasan pemilihan mikroenkapsulasi diantaranya dapat menutupi rasa dan
bau obat, obat dalam bentuk cairan dapat dirubah menjadi bentuk serbuk yang
mengalir bebas, mencegah inkompatibilitas antar obat, dan dapat mengubah
tempat absorpsi protein (Tiwari, S., P, Verma., 2012).
Mikropartikel dibuat dari polimer biocompatable dan biodegradable
misalnya Polylactic acid (PLA), dan Polylactid-co-glycolic (PLGA). Polimer
alam seperti gelatin dan albumin juga digunakan dalam pembuatan mikrosfer.
Mikropartikel memberikan penghantaran akurat untuk obat poten, mengurangi
konsentrasi obat pada target dan menjadi sistem penghantaran yang efektif untuk
zat aktif yang sedikit larut dalam air. Selain itu mikropartikel dapat
UIN Syarif Hidayatullah Jakarta
menghantarkan lebih dari 80% zat aktif dalam 10 menit. Misalnya nimesulid
(Parida et al., 2013).
Menurut Muhaimin (2013), sistem penghantaran obat dengan pelepasan
terkontrol telah dikembangkan untuk mengatasi kesulitan pemberian obat secara
tradisional. Penghantaran obat dengan pelepasan terkontrol menggunakan device
(alat) seperti piringan berbasis polimer, rod, pil atau mikropartikel yang
mengenkapsulasi obat dan pelepasan obat ini terjadi dengan kecepatan terkontrol
selama periode waktu tertentu. Sistem ini memberikan beberapa keuntungan
apabila dibandingkan dengan pemberian obat dengan metode tradisional. Adapun
keuntungan itu adalah sebagai berikut:
a. Kecepatan pelepasan obat dapat digunakan untuk aplikasi spesifik
b. Sistem pelepasan terkontrol dapat melindungi obat, terutama protein yang
mudah rusak ketika berada di tubuh
c. Sistem pelepasan terkontrol dapat meningkatkan kepatuhan pasien.
Ketika berbagai alat digunakan untuk penghantaran obat dengan pelepasan
terkontrol, mikropartikel berbasis polimer adalah tipe yang paling umum
digunakan karena memiliki beberapa keuntungan. Mikropartikel dapat
mengenkapsulasi berbagai obat dengan molekul kecil, vaksin, protein, dan asam
nukleat (Azevedo., et al, 2006; Feng., et a.l, 2006; Little., et al, 2005 dalam
Muhaimin, 2013). Mikropartikel dapat menghantarkan makromolekul, berbagai
faktor diantaranya tipe polimer, berat molekul polimer, komposisi kopolimer, sifat
eksipien yang ditambahkan pada formula mikropartikel, dan ukuran mikropartikel
dapat memberikan efek pada kecepatan penghantaran (Muhaimin, 2013).
Polimer dapat digunakan untuk mengontrol kecepatan pelepasan obat dari
formulasi. Polimer dapat mengikat partikel dari bentuk sediaan dan mengubah
sifat aliran. Aplikasi polimer pada penghantaran obat telah meningkat karena
polimer memberikan sifat unik yang saat ini masih belum dimiliki oleh material
lain. Polimer adalah makromolekul yang memiliki ikatan yang besar, memiliki
berbagai gugus fungsi, dapat dicampur dengan material dengan berat molekul
yang besar atau kecil. Pemahaman mengenai konsep dasar polimer diperlukan
untuk pemahaman lebih jauh mengenai produk obat dan model sistem
UIN Syarif Hidayatullah Jakarta
peluang untuk penggunaan berbagai polimer sebagai sistem penghantaran obat
(Leong and Langer, 1988; Wang et al., 2002 dalam Muhaimin, 2013).
Pelepasan terkontrol teofilin telah berhasil dibuat dengan pengembangan
formula untuk penghantaran chronotherapeutic menggunakan guar gum,
mikrosfer teofilin dibuat dengan teknik emulsifikasi. Pelapisan mikrosfer
menggunakan metode penguapan pelarut dengan polimer Eudragit® yang sensitif
dengn pH. Chronotherapeutic berbasis sistem penghantaran obat teofilin dengan
target usus besar memanfaatkan sifat sensitif pH enzim dibuat untuk menghindari
serangan asma episodik pada pagi hari. Kelarutan bergantung pH dai Eudragit dan
sifat gel guar gum berperan dalam penundaan pelepasan (Soni et al., 2011).
Chronotherapeutic adalah metode pengobatan dimana ketersediaan obat secara in
vivo diberikan batas waktu untuk menyesuaikan dengan ritme penyakit sehingga
dapat mengoptimalkan hasil terapi dan meminimalisir efek samping (Sajan, J et
al., 2009).
2.2. Metode Pembuatan Mikropartikel
Terdapat banyak metode dalam pembuatan mikropartikel yang digunakan
dalam berbagai aplikasi. Metode ini digunakan untuk mengenkapsulasi obat
dalam polimer (Jalil and Nixon, 1990a, 1990b dalam Muhaimin, 2013). Metode
pembuatan ini harus memiliki syarat tertentu, diantaranya stabilitas dan aktivitas
biologi obat tidak boleh terpengaruh oleh parameter proses yang digunakan dalam
produksi mikropartikel yang mengandung obat. Selain itu hasil mikropartikel
harus memiliki ukuran partikel yang diinginkan dan efisiensi enkapsulasi obat
harus tinggi. Syarat berikutnya adalah kualitas partikel dan profil pelepasan obat
harus reprodusibel (Muhaimin, 2013).
2.2.1. Presipitasi Partikel dengen Penambahan Bukan Pelarut (Koaservasi) Pada metode ini mikropartikel dibuat dengan mendispersikan partikel
kristal padat atau larutan encer obat dalam larutan organik yang mengandung
polimer, diikuti dengan pemisahan fase dengan penambahan pelarut organik
kedua dimana polimer tidak larut (yang didefinisikan disini sebagai bukan
UIN Syarif Hidayatullah Jakarta
DL-PLG menggunakan metode ini (Sanders et al., 1984, 1985 dalam Muhaimin,
2013). Larutan encer obat diemulsifikasi dalam larutan polimer DL-PLG dan
diklorometan untuk memproduksi emulsi air/minyak. Penambahan bukan pelarut
menghasilkan presipitasi polimer di sekitar larutan encer obat untuk membentuk
mikropartikel. Penambahan bukan pelarut dalam volume besar melengkapi proses
ekstraksi pelarut polimer dan pengerasan mikrosfer. Metode yang sama telah
digunakan pada obat oksitetrasiklin, tetapi pada proses ini partikel obat padat
dicampurkan pada larutan polimer organik (Vidmar et al., 1984 dalam Muhaimin,
2013). Partikel yang diproduksi dengan metode ini memiliki distribusi ukuran
yang luas dimana hal ini tidak diinginkan untuk penggunaan klinis. Mikropartikel
yang diproduksi dengan metode ini juga memiliki kecenderungan besar untuk
teragregasi. Hasil dari metode ini dapat dirubah dengan perubahan parameter
penyiapan misalnya obat, rasio polimer, pelarut polimer, kecepatan pengadukan,
suhu, volume bukan pelarut, dan tipe bukan pelarut (Muhaimin, 2013).
2.2.2. Presipitasi Partikel dengan Partisi Pelarut
Pada metode ini, larutan atau suspensi obat dalam larutan polimer/pelarut
organik dimasukan pada aliran minyak mineral secara perlahan. Pelarut organik
larut dalam minyak, tetapi obat dan polimer tidak larut dalam minyak,
kopresipitasi obat dan polimer terjadi sebagai partisi campuran dalam minyak.
Hasil pada metode ini tergantung pada kelarutan obat. Apabila obat larut dalam
larutan polimer, obat dan polimer akan terpresipitasi bersama. Apabila obat
dicampurkan dalam larutan polimer, polimer akan terpresipitasi mengelilingi
partikel obat padat (Muhaimin, 2013).
Hidrokortison telah berhasil diformulasi dalam mikropartikel polimer
polilaktida menggunakan metode ini. Namun mikropartikel yang terbentuk relatif
lebih besar. Ukuran partikel berkisar antara 144 µm-412 µm, bergantung pada
kecepatan aliran dan diameter jarum suntik dimana campuran obat/polimer
dimasukan (Leelarasamee et al., 1988 dalam Muhaimin, 2013). Dengan metode
ini, parameter penyiapan yang memberikan efek terhadap ukuran mikropartikel
adalah diameter jarum suntik, rasio obat:polimer, kecepatan aliran minyak
UIN Syarif Hidayatullah Jakarta
2.2.3. Semprot Kering (Spray Drying)
Semprot kering adalah perubahan bentuk emulsi, suspensi atau suatu
dispersi menjadi bentuk kering melalui atomisasi produk dan pendispersian bahan
pada udara panas. Teknik ini merubah cairan menjadi serbuk kering dalam satu
langkah. Selain itu metode ini mudah dilakukan untuk proses scale up
mikroenkapsulasi. Akhir-akhir ini di dunia industri, metode ini digunakan
memproduksi berbagai macam makanan, kosmetik dan industi farmasi untuk
memproduksi serbuk obat dan sediaan kering lainnya. Bahan yang larut air atau
larut dalam pelarut organik dapat dikeringkan melalui proses semprot kering.
Proses semprot kering terdiri dari tiga tahap, yaitu atomisasi, pengeringan, dan
pengumpulan serbuk. Mula-mula cairan didispersikan ke dalam atomizer dan
akan terdispersi menjadi droplet dalam udara hangat atau gas inert dalam
chamber kering. Hal ini menyebabkan luas permukaan partikel besar sehingga
tahapan penguapan pelarut terjadi dengan cepat. Setelah itu partikel kering
melewati putaran udara dan terjadi pemisahan partikel berdasarkan energi
sentrifugasi. Partikel yang terbentuk umumnya memiliki rentang distribusi ukuran
yang sempit antara satu dan beberapa mikron tergantung pada kondisi proses dan
formula awal. Obat hidrofobik dan hidrofilik dapat dienkapsulasi ke dalam
polimer melalui semprot kering (Patel, H.V. et al., 2013).
Pada pembuatan mikropartikel menggunakan metode ini, parameter yang
harus dipertimbangkan adalah suhu inlet, kapasitas aspirator dan kapasitas pompa.
Suhu inlet adalah parameter penting yang mempengaruhi dimensi dan hasil
partikel. Suhu inlet yang digunakan harus sesuai dengan bahan (obat dan polimer)
dan pelarut. Aspirator udara dapat mempengaruhi pengubahan droplet nebulizer
menjadi partikel padat. Pompa peristaltik mempengaruhi waktu dan efikasi proses
pengeringan (Patel, A.S., T. Soni., V. Thakkar., T Gandhi., 2012)
Keuntungan teknik ini adalah senyawa larut air dan senyawa tidak larut air
dapat dimasukan pada bulatan mikropartikel. Hal ini berbeda dengan sistem
penguapan dengan emulsi tunggal minyak/air dimana metode ini tidak cocok
untuk senyawa yang larut air. Progesteron dan teofilin telah berhasil dimasukan
dalam mikropartikel polilaktida menggunakan metode semprot kering (Bodmeier
UIN Syarif Hidayatullah Jakarta
Akan tetapi sistem ini memiliki beberapa kekurangan, misalnya kristal
berbentuk jarum dibentuk ketika kafein dimasukan menggunakan metode ini ke
dalam polimer polilaktida. Hal ini memungkinkan terjadinya inkompatibilitas
antara obat dan polimer (Bodmeier and Chen, 1988 dalam Muhaimin, 2013).
Begitu pula pada serat yang dapat terbentuk karena kekuatan dispersi yang tidak
cukup untuk memtuskan larutan polimer. Pemilihan pelarut organik menjadi
penting, polimer harus larut dalam pelarut, misalnya metilen klorida, etil asetat
atau hexafluoroisopropanol, karena pelarut dapat menguap dengan cepat dalam
udara panas pada fase pengeringan. Selain itu polimer yang digunakan juga
biasanya tidak larut dalam pelarut organik (Muhaimin, 2013).
Pada metode ini, selama tahap ekstraksi partikel dipaparkan pada udara
panas dengan volume besar sehingga stabilitas obat termolabil atau obat sensitif
oksidasi dapat berubah. Meskipun nitrogen akan mencegah proses oksidasi obat
apabila digunakan untuk menggantikan udara pada fase ini, kemampuan konduksi
nitrogen lebih kecil dari udara sehingga akan mempengaruhi hasil mikropartikel
yang terbentuk. Pembuatan mikroparikel dengan metode ini mengasilkan partikel
dengan ukuran diameter 5 sampai 125 µm (Muhaimin, 2013).
2.2.4. Metode Ekstraksi Cairan Superkritis
Mikronisasi dan pengurangan ukuran partikel adalah hal menarik dalam
teknologi farmasetik yang telah digunakan untuk menyelesaikan masalah
kelarutan atau penargetan obat. Metode pengurangan ukuran partikel
konvensional memerlukan proses kirstalisasi substansi sebelum proses dimulai.
Selama fase ini, ukuran kristal tidak terkontrol. Ketika tenaga mekanis digunakan
untuk mengurangi ukuran kristal, partikel yang terbentuk sering memiliki muatan
permukaan dan menjadi lebih kohesif. Kekurangan lain yang berhubungan dengan
kristalisasi diantaranya memerlukan biaya dan waktu yang besar, distribusi ukuran
partikel bersifat polidispersi dengan jarak ukuran yang besar, dan pelarut organik
yang bersifat toksik digunakna pada proses kristalisasi serta residu pelarut dalam
proses rekristalisasi obat mungkin dapat melebihi batas yang diizinkan
UIN Syarif Hidayatullah Jakarta
Penggunaan cairan superkritis sebagai media ekstraksi merupakan
alternatif dalam pembuatan mikropartikel obat dan eksipien farmasi (Eckert et
al., 1996; Fredriksen et al., 1997; Hanna et al., 1995; Marr and Gamse, 1999;
McHugh and Krukonis, 1994; Subramaniam et al., 1997; York, 1999 dalam
Muhaimin 2013). Penelitian yang memelopori pembuatan mikropartikel dari
polimer biodegradabel menggunakan metode ekstraksi cairan superkritis sudah
dilaporkan (Bleich et al., 1993, 1996; Bodmeier et al., 1995; Pablo et al., 1993;
Thies and Müller, 1998; Tom et al., 1993 dalam Muhaimin 2013). Terdapat dua
alasan utama dalam penggunaan teknik ini. Alasan pertama adalah cairan
superkritis mampu melarutkan secara selektif sehingga dapat memungkinkan
untuk memisahkan komponen tertentu dari campuran multikomponen. Alasan
berikutnya adalah sifat perpindahan massa yang mneguntungkan dan kelarutan
pelarut yang tinggi dalam cairan superkritis membuat proses pengeringan
mikropartikel lebih cepat dan efisien dengan jumlah residu pelarut yang rendah
(Folker et al., 1996 ; Shariati and Peters, 2003 dalam Muhaimin 2013).
CO2 superkritis adalah cairan superkritis yang banyak digunakan karena
memiliki kondisi kritis yang rendah (Tc = 31,1oC, Pc = 7,38 MPa), nontoksik,
tidak mudah terbakar, dan memiliki hargayang murah. Teknik yang digunakan
untuk pembentukan partikel menggunakan CO2 superkritis diantaranya
penyebaran cepat larutan superkritis, berbagai macam proses antipelarut misalnya
antipelarut gas, sistem ekstraksi pelarut, partikel dari larutan gas jenuh, proses
antipelarut superkritis, dan disperse peningkat kelarutan melalui cairan superkritis
(Kang,Yunqing et al., 2008)
2.2.5. Metode Penguapan Pelarut
Metode penguapan pelarut banyak digunakan pada pebuatan mikropartikel
polimer yang mengandung obat yang berbeda (Jalil and Nixon, 1990a; Lewis
et al., 1984; Suzuki and Price, 1985; Wang et al., 1999 dalam Muhaimin, 2013).
Beberapa variable yang dapat mempengaruhi mikropartikel telah diteliti
diantaranya kelarutan obat, morfologi internal, tipe pelarut, kecepatan difusi,
suhu, komposisi polimer, viskositas polimer, dan muatan obat (Benoit et al., 1996;
UIN Syarif Hidayatullah Jakarta
1990a, 1990b; Jaraswekin et al., 2007 dalam Muhaimin, 2013). Efektivitas
metode penguapan pelarut untuk memproduksi mikrosfer tergantung pada
keberhasilan penjerapan zat aktif dalam mikropartikel. Proses ini paling berhasil
pada obat yang tidak larut atau sulit larut dalam medium cairan yang mengandung
fase kontinyu (Bodmeier and McGinity, 1987 dalam Muhaimin, 2013). 1993 dalam Muhaimin, 2013). Terdapat perbedaan metode dalam membuat
mikropartikel menggunakan metode penguapan pelarut. Peningkatan efisiensi
enkapsulasi obat bergantung pada hidrofilisitas dan hidrofobisitas obat
(Muhaimin, 2013).
2.2.5.1. Proses Emulsi Tunggal
Menurut Muhaimim (2013), proses ini melibatkan emulsifikasi minyak
dalam air (minyak/air). Sistem emulsi minyak/air terdiri dari fase organik yang
mengandung pelarut mudah menguap dengan polimer terlarut dan obat yang telah
terenkapsulasi, kemudian diemulsifikasi dalam fase cairan yang mengandung
larutan surfaktan. Untuk obat yang tidak larut atau sulit larut dalam air, sering
digunakan metode minyak dalam air. Metode ini adalah metode paling sederhana
daripada metode lain. Metode ini terdiri dari 4 tahapan utama, yaitu:
a. Disolusi obat hidrofobik dalam pelarut organik yang mengandung polimer
b. Emulsifikasi fase organik, yang disebut fase dispersi, dalam fase encer yang
disebut fase kontinyu
c. Ekstraksi pelarut dari fase dispersi menggunakan fase kontinyu, diiringi
penguapan pelarut, proses perubahan droplet dari fase dispersi menjadi partikel
padat
d. Proses recovery (perolehan kembali) dan pengerinagn mikrosfer untuk
UIN Syarif Hidayatullah Jakarta
Gambar 2.2. Skema Empat Prinsip Proses Dalam Pembuatan Mikrosfer Menggunakan Penguapan Pelarut (Minyak/Air)
(sumber : Muhamin, 2013)
Sebagian besar sistem emulsi minyak dalam air digunakan untuk
pembuatan mikropartikel yang mengandung fase organik yang terdiri dari pelarut
mudah menguap dengan polimer terlarut dan obat yang terenkapsulasi kemudian
diemulsifikasi dalam fase encer yang mengandung surfaktan terlarut (gambar 2.3).
Surfaktan dimasukan pada fase kontinyu untuk mencegah koalesen droplet
organik ketika terbentuk droplet (Muhamimin, 2013).
Gambar 2.3. Enkapsulasi Menggunakan Teknik Emulsi Minyak Dalam Air (sumber : Birnbaum and Peppas, 2004)
Larutan polimer-pelarut-obat diemulsifikasi (dengan kecepatan dan suhu
tertentu) untuk menghasilkan emulsi minyak/air. Emulsi ini terbentuk dengan
menggunakan baling-baling atau bar magnetic untuk mencampur fase organik dan
fase kontinyu. Seperti yang terlihat pada gambar 3, surfaktan digunakan untuk
UIN Syarif Hidayatullah Jakarta
mencegah terjadinya koalesen. Surfaktan besifat ampifatik di alam dan akan
mengelilingi permukaan droplet untuk menstabilkan pembentukan droplet melalui
pengurangan energi bebas pada interfase diantara dua fase. Surfaktan juga
menyebabkan resistensi untuk terjadinya koalesen dan flokulasi mikrosfer. PVA
adalah salah satu surfaktan yang banyak digunakan untuk memproduksi
mikropartikel polimer biodegradabel dan non biodegradabel. Ketika emulsi
terbentuk, kemudian dilakukan penghilangan pelarut melalui penguapan dan
ekstraksi untuk memadatkan droplet polimer. Pada proses penghilangan pelarut
melalui penguapan, emulsi dijaga pada tekanan rendah atau tekanan asmosfer dan
kecepatan pengadukan dikurangi sehingga pelarut volatil dapat menguap
(Muhaimin, 2013).
Pelarut organik larut dari droplet menuju fase kontinyu eksternal sebelum
menguap pada interfase air-udara. Pada proses ekstraksi, emulsi berpindah
menuju air dalam jumlah besar atau medium lain, dimana pelarut dapat
dikeluarkan dari droplet minyak. Kecepatan penghilangan pelarut melalui
ekstraksi tergantung pada suhu medium, rasio volume emulsi dengan medium dan
sifat kelarutan polimer, pelarut, dan medium dispersi. Hasil ekstraksi yang tinggi
akan menyebabkan pembentukan partikel dengan porositas yang tinggi sehingga
dapat menimbulkan profil pelepasan obat yang tidak dikehendaki (Arshady, 1991;
Jeyanthi, 1996 dalam Muhaimin, 2013). Metode penghilangan pelarut melalui
ekstraksi lebih cepat terjadi (umumnya kurang dari 30 menit) daripada proses
penguapan dan hasil mikrosfer yang terbentuk dengan metode ekstraksi sering
lebih berpori daripada menggunakan metode penguapan pelarut. Salah satu
kekurangan proses emulsi minyak/air adalah efisiensi enkapsulasi yang rendah
pada obat dengan kelarutan sedang dalam air. Obat berdifusi atau memisah dari
fase terdispersi minyak menuju fase kontinyu dan fragmen mikrokristalin obat
hidrofilik terdeposit pada permukaan mikrosfer (Cavalier et al., 1986 Muhaimin,
2013) serta terdispersi dalam matriks polimer. Hal ini menyebakan rendahnya
penjerapan obat hidrofilik dan pelepasan awal obat yang cepat (efek ledakan/burst
effect) (Jalil and Nixon, 1990b; Jones et al., 1995 Muhaimin, 2013). Proses
emulsifikasi minyak/air banyak digunakan untuk enkapsulasi obat larut lemak.
UIN Syarif Hidayatullah Jakarta
minyak dalam minyak (Tsai, 1986). Pada metode ini, obat dapat terlarut atau
bercampur pada fase minyak sebelum didispersikan dalam fase minyak lainnya.
Pelarut organik yang dapat bercampur dengan air, seperti asetonitril digunakan
untuk melarutkan obat dalam PLGA atau PLA. Kemudian larutan ini
didispersikan dalam minyak seperti minyak mineral ringan dengan ditambahkan
surfaktan larut lemak seperti sorvitan oleat (Span) untuk menghasilkan emulsi
minyak/minyak. Setelah itu mikropartikel didapatkan dengan penguapan atau
ekstraksi pelarut organik dari droplet minyak terdispersi dan minyak yang dicuci
dengan pelarut seperti n-heksan. Proses ini juga disebut metode emulsi air dalam
minyak (Jalil and Nixon, 1λλ0a; O’Hagan et al., 1994 Muhaimin, 2013).
2.2.5.1.Proses Emulsi Ganda
Metode minyak dalam air sesuai untuk enkapsulasi obat hidrofilik tinggi
karena terdapat dua alasan utama. Alasan pertama adalah obat hidrofilik tidak
larut dalam pelarut organik. Alasan berikutnya adalah obat akan berdifusi menuju
fase kontinyu selama proses emulsi yang dapat menyebabkan kehilangan obat
yang tinggi. Terdapat empat alternatif untuk membuat obat hidrofilik dapat
dienkapsulasi adalah:
a. Metode emulsi ganda air/minyak/air: larutan encer obat hidrofilik
diemulsifikasi dengan fase organik (emulsi air/minyak) kemudian emulsi ini
terdispersi menuju larutan encer kedua untuk membentuk emulsi kedua.
b. Metode kosolven minyak/air: ketika obat tidak larut dalam pelarut organik
utama, pelarut kedua atau yang disebut kosolven diperlukan untuk melarutkan
obat.
c. Metode dispersi minyak/air: obat didispersikan pada serbuk padat dalam
larutan polimer dan pelarut organik
d. Metode penguapan pelarut bukan kontinyu minyak/minyak: fase kontinyu
digantikan dengan bukan air (misalnya minyak mineral) (Li et al., 2008 dalam
Muhaimin, 2013)
Proses emulsi ganda biasa digunakan untuk obat yang tidak larut dalam
pelarut organik. Proses emulsi padat minyak/air dapat digunakan untuk
UIN Syarif Hidayatullah Jakarta
Kristal dengan ukuran yang lebih kecil dapat disitribusikan secara homogen
selama pembentukan droplet organik pada emulsi. Obat hidrofilik (cisplatin,
doxorubicin) telah dienkapsulasi menggunakan metode ini. Masalah dalam
enkapsulasi obat hidrofilik adalah kehilangan obat pada fase kontinyu eksternal
selama pembentukan mikropartikel. Adanya kehilangan obat pada fase eksternal
menyebabkan sisa obat akan bermigrasi ke permukaan droplet sebelum proses
pemadatan. Untuk meminimalisisr masalah ini, droplet organik perlu dipadatkan
menjadi mirkopartikel secepat mungkin (Thies, 1992 dalam Muhaimin, 2013).
Hal ini dapat dicapai dengan menggunakan larutan organik polimer yang kental
dan meningkatkan volume sekunder air sehingga dapat menarik pelarut organik
menuju fase encer dengan cepat. Setelah itu terbentuk mikropartikel dengan obat
yang telah terenkapsulasi di dalamnya. Fase dispersi yang kental dapat
mengurangi volume pelarut organik, memfasilitasi penghilangan pelarut organik
secara cepat dari droplet, juga dapat menghalangi partikel/kristal obat padat untuk
berpindah ke permukaan. Hal ini mengakibatkan distribusi obat dalam partikel
menjadi lebih homogen (Muhaimin, 2013).
Alternatif lain untuk mengenkapsulasi obat hidrofilik adalah dengan
menggunakan proses emulsi air-minyak-air (gambar 4). Larutan encer obat
ditambahkan pada fase organik yang mengandung polimer dan pelarut organik
dengan pengadukan untuk membentuk emulsi pertama yaitu emulsi minyak dalam
air. Emulsi ini kemudian didispersikan ke fase kontinyu yang mengandung
surfaktan untuk membentuk emulsi kedua yaitu emulsi air/minyak/air. Beberapa
obat hidrofilik seperti peptida leuprolida asetat (Okada, 1994; Toguchi, 1992),
vaksin (Azevedo et al., 2006; Feng et al., 2006; Little et al., 2005; O'Hagan et
al., 1991; Singh, 1995;), protein/peptida dan molekul konvensional telah
berhasil dienkapsulasi menggunakan metode ini. Masalah dalam tipe emulsi ini
terjadi ketika emulsi dalam tidak stabil sehingga menyebabkan kehilangan droplet
encer yang mengandung obat menuju fase kontinyu. Pemilihan surfaktan yang
dapat digunakan untuk menstabilkan emulsi terbatas pada material yang akan
terlarut dalam pelarut organik. Biasanya ester asam lemak dari polioksietilen atau
sorbiton digunakan untuk obat dengan kelarutan tinggi pada pelarut organik dan
UIN Syarif Hidayatullah Jakarta
Gambar 2.4. Skema empat proses utama pada proses penguapan/ekstraksi pelarut (Air/Minyak/Air)
(sumber : Muhaimin, 2013)
2.3. Pembuatan Mikropartikel Menggunakan Metode Penguapan Pelarut Pembuatan mikropartikel menggunakan metode penguapan pelarut
memerlukan beberapa bahan dan kondisi agar mikropartikel yang dihasilkan
memiliki karakteristik yang ditargetkan.
2.3.1. Material
Material yang digunakan pada pembuatan mikropartikel menggunakan
metode ini terdiri dari dua fase, yaitu fase dispersi dan fase kontinyu.
2.3.1.1. Fase Dispersi
Fase disperse pada metode ini terdiri dari polimer, pelarut dan komponen
lain yang perlu diperhatikan oleh peneliti agar mikropartikel yang terbentuk sesuai
dengan yang ditargetkan.
a. Polimer
Metode pembuatan mikropartikel adalah faktor penting dalam enkapsulasi
dan pelepasan obat. Penyiapan bahan termasuk tipe polimer, berat polimer,
komposisi kopolimer, sifat eksipien yang ditambahkan pada formula
mikropartikel, dan ukuran mikropartikel dapat berpengaruh besar pada kecepatan
penghantaran obat (Muhaimin, 2013).
Tipe dan mekanisme polimer degradasi dapat mempengaruhi kecepatan
pelepasan. Berdasarkan kecepatan terhidrolisis pada gugus fungsional, polimer
dapat dikategorikan menjadi dua tipe, yaitu surface eroding (pengikisan
permukaan) dan bulk eroding (pengikisan bulk) (Burkersroda et al., 2002; Kang et
UIN Syarif Hidayatullah Jakarta
Wagdare et al., 2011 dalam Muhaimin, 2013). Polimer tipe pengikisan bulk
seperti PLG, dapat menyebar pada air kemudian menjadi matriks polimer dan
terdegradasi pada seluruh matriks mikropartikel. Berbeda dengan polimer
pengikisan permukaan seperti polianhidrida yang mengandung monomer
hidrofobik dengan ikatan lemah. Tipe polimer ini mencegah agar air tidak
berpenetrasi ke dalam polimer bulk, dimana akan terdegradasi secara cepat
menjadi oligomer dan monomer pada interfase polimer/air melalui proses
hidrolisis (Saltzman, 2001 Muhaimin, 2013).
Mikropartikel polimer pengikisan bulk sering terjadi obat pecah sebesar
50% dari total obat yang terdapat dalam mikropartikel tersebut (O’Donnell and
McGinity, 1997 dalam Muhaimin, 2013). Pelepasan obat terjadi selama inkubasi
pada beberapa jam pertama, diikuti dengan difusi pelepasan obat terkontrol secara
pelan dan kadang-kadang fase ketiga dimana obat tersisa akan dilepaskan secara
cepat. Hal ini terjadi akibat degradasi matriks polimer yang parah. Pada
mikropartikel yang mengandung polimer pengikisan permukaan, obat dilepaskan
pada permukaan ketika polimer pecah. Erosi pada polimer ini umumnya terjadi
dengan kecepatan konstan (Gopferich and Langer, 1993; Kanjickal et al., 2004
Muhaimin, 2013). Apabila obat yang diinginkan terdispersi secara homogen
dalam mikropartikel, kecepatan pelepasan yang tinggi akan terjadi pada awalnya.
Seiring berjalannya waktu, area permukaan sferis dan kecepatan pelepasan akan
menurun secara asimtomatis (Muhaimin, 2013).
Polimer dengan berat molekul besar dapat mempengaruhi degradasi
polimer dan kecepatan pelepasan obat. Peningkatan berat molekul dapat
menurunkan kemampuan difusi dan mengurangi kecepatan pelepasan obat
(Alonso et al., 1994; Katou et al., 2008; Le Corre et al., 1994; Liggins and Burt,
2001; Mabuchi et al., 1994; Yang et al., 2001dalam Muhaimin, 2013).
Mekanisme utama pelepasan obat adalah difusi melalui pori yang terisi air.
Degradasi polimer menghasilkan monomer dan oligomer yang larut sehingga
dapat berdifusi keluar dari partikel. Produk yang lebih kecil akan dihasilkan oleh
degradasi cepat dari polimer dengan berat molekul yang lebih rendah. Penurunan
kecepatan pelepasan yang sejalan dengan kenaikan berat molekul polimer
UIN Syarif Hidayatullah Jakarta
Mehta et al., 1996 dalam Muhaimin, 2013). Akan tetapi pada mikrosfer
polianhidrida (polimer tipe pengikisan permukaan), berat molekul hanya
memberikan efek kecil pada pelepasan obat (Hanes et al., 1996; Tabata and
Langer, 1993dalam Muhaimin, 2013). Rasio kopolimer pada berbagai kopolimer
juga dapat memberikan efek pada kecepatan pelepasan. Selain itu peningkatan
bahan yang dapat mempercepat degradasi monomer dapat meningkatkan
kecepatan pelepasan (Lin et al., 2000; Shen et al., 2002; Spenlehauer et al., 1989
dalam Muhaimin, 2013). Ketika pelepasan obat dikontrol dengan polimer
pengikis, kecepatan pelepasan dapat meningkat sejalan dengan tingginya
konsentrasi monomer yang larut atau monomer yang lebih kecil (Tabata and
Langer, 1993 dalam Muhaimin, 2013). Efek komposisi polimer dapat menjadi
kompleks dengan adanya perbedaan fase polimer atau termodinamik obat yang
terenkapsulasi (Kipper et al., 2002 dalam Muhaimin, 2013).
b. Pelarut
Sifat pelarut yang sesuai digunakan dalam pembuatan mikropartikel
menggunakan metode penguapan pelarut adalah dapat melarutkan polimer yang
digunakan, sedikit larut pada fase kontinyu, volatilitas tinggi, titik didih rendah,
dan toksisitas rendah (Li et al., 2008 dalam Muhaimin, 2013)
Sebelumnya kloroform sering digunakan, akan tetapi karena toksisitas dan
tekanan uap yang rendah, pelarut ini digantikan oleh diklorometan. Diklorometan
(metilen klorida) adalah pelarut yang paling banyak digunakan untuk enkapsulasi
menggunakan metode penguapan pelarut karena volatilitas yang tinggi, titik didih
rendah dan ketidakbercampuran dengan air yang tinggi (Li et al., 2008 dalam
Muhaimin, 2013).
Selain itu etil asetat juga berpotensi digunakan karena memiliki toksisitas
yang lebih rendah dari diklorometan. Akan tetapi kebercampuran parsial etil asetat
dalam air (4,5 kali lebih tinggi dari diklorometan), mikrosfer tidak dapat terbentuk
apabila fase terdispersi dikenali secara langsung oleh fase kontinyu. Ekstraksi
mendadak etil asetat dari fase terdispersi menyebabkan polimer terpresipitasi
menjadi serat seperti aglomerat (Freytag et al, 2000 dalam Muhaimin, 2013).
UIN Syarif Hidayatullah Jakarta
menggunakan tiga metode,yaitu larutan encer dijenuhkan terlebih dahulu dengan
pelarut (Bahl and Sah, 2000 dalam Muhaimin, 2013). Metode kedua dengan
mengemulsifikasikan fase dispersi dengan sedikit larutan encer. Setelah
pembentukan droplet, emulsi ini dimasukan ke dalam larutan encer dalam jumlah
besar (Freytag et al, 2000 dalam Muhaimin, 2013). Metode terakhir adalah
mengemulsikan fase dispersi dengan sedikit larutan encer kemudian larutan
diagitasi dan pelarut menguap sehingga terjadi pemadatan mikrosfer (Sah, 1997
dalam Muhaimin, 2013).
Kesimpulannya, pelarut dengan toksisitas rendah telah diuji dan
menunjukan bahwa pelarut tersebut dapat digunakan untuk pembuatan
mikropartikel. Akan tetapi belum ada hasil yang cukup untuk membandingkan
kualitas mikrosfer dengan pelarut yang berbeda. Diklorometan masih menjadi
pelarut yang paling banyak digunakan karena cepat menguap, efisiensi
enkapsulasi obat tinggi, menghasilkan bentuk mikrosfer yang sferis dan lebih
seragam (Muhaimin, 2013).
c. Komponen Lain
Pada beberapa kasus, bahan lain yang ditambahkan pada fase dispersi
seperti kosolven dan generator penyerap (Muhaimin, 2013). Kosolven digunakan
untuk melarutkan obat yang tidak larut dalam pelarut pada fase dispersi (Graves et
al., 2006; Hsu and Lin, 2005; Li et al., 2008; Luan et al., 2006; Reithmeier et
al., 2001 dalam Muhaimin, 2013).
Generator penyerap atau yang disebut porosigen atau porogen digunakan
untuk menghasilkan pori di dalam mikropartikel sehingga dapat meningkatkan
kecepatan degradasi polimer dan meningkatkan kecepatan pelepasan obat (Li et
al, 2008 dalam Muhaimin, 2013). Pelarut organik seperti heksan yang tidak
melarutkan poli asam laktat dan poli asam laktat koglikol dapat dicampurkan ke
dalam mikrosfer untuk membentuk pori (Li et al., 2008; Spenlehauer et al,
1986 dalam Muhaimin, 2013). Penggabungan Sephadex (sambung silang gel
dekstran) dalam mikrosfer insulin-PLA dapat meningkatkan porositas mikrosfer
secara signifikan (Li et al, 2008; Watts et al, 1990 dalam Muhaimin, 2013).
UIN Syarif Hidayatullah Jakarta
etilselulosa/diklorometan untuk enkapsulasi aspirin, juga untuk meningkatkan
porositas obat. Akan tetapi pemberian n-heptan yang berlebihan menyebabkan
mikrosfer memiliki porositas tinggi sehingga menyebabkan efisiensi enkapsulasi
obat rendah (Li et al, 2008; Yang et al, 2000a dalam Muhaimin, 2013).
2.3.1.2. Fase Kontinyu a. Surfaktan
Surfaktan atau juga disebut agen tensioaktif sering digunakan untuk
mendispersikan satu fase ke fase lain yang tidak bercampur dan menstablikan
emulsi. Surfaktan dapat mengurangi tegangan permukaan fase kontinyu,
menghindari koalesen dan aglomerasi droplet dan menstabilkan emulsi. Surfaktan
yang sesuai dapat menghasilkan mikropartikel dengan ukuran umum dan
distribusi ukuran partikel yang kecil. Selain itu surfaktan dapat menjamin
pelepasan obat untuk menjadi lebih terprediksi dan stabil. Sebelum memilih tipe
dan konsentrasi surfaktan, perlu terlebih dahulu mengetahui polaritas kedua fase
tidak bercampur, ukuran mikropartikel yang diinginkan dan sferisitas
mikropartikel. Surfaktan untuk emulsi bersifat ampifilik. Salah satu bagian
molekul memiliki afinitas untuk menjadi zat terlarut yang polar seperti air dan
bagian lain memiliki afinitas menjadi zat tidak polar seperti hidrokarbon
(hidrofobik). Ketika surfaktan dicampurkan dalam emulsi, surfaktan akan
menutupi permukaan droplet dengan bagian hidrofobiknya dalam droplet dan
bagian hidrofilik terdapat dalam air (Li et al, 2008 dalam Muhaimin, 2013).
Terdapat empat klasifikasi surfaktan berdasarkan bagian hidrofilik dalam
molekulnya, yaitu anionik, kationik, amfoterik, dan non ionik. Surfaktan anioik
menghasilkan muatan negatif pada larutan kontinyu. Surfaktan ini memiliki HLB
atau hydrophilic-lipophile balance (keseimbangan hidrofilikk-lipofilik) tinggi
karena surfaktan jenis ini memiliki kecenderungan bersifat hidrofil. Tipe kedua
adalah surfaktan kationik. Surfaktan ini memberikan muatan positif pada larutan
encer. Tipe selanjutnya adalah surfaktan amfoterik. Surfaktan amfoterik bersifat
anionik pada pH basa dan bersifat kationik pada pH asam. Tipe terakhir adalah
surfaktan non ionik. Surfaktan non ionik tidak memiliki muatan (Li et al., 2008
UIN Syarif Hidayatullah Jakarta
Sebagian besar emulsi diklorometan/air, menggunakan beberapa tipe
surfaktan. Pertama adalah tipe non ionik misalnya PVA (Polivinil Alkohol)
terhidrolisis sebagian, metil selulosa (Berchane et al., 2006; Lee et al., 1999
dalam Muhaimin, 2013), tweenn (Yang et al., 2000 dalam Muhaimin, 2013)
dan span (Jalil and Nixon., 1990a dalam Muhaimin, 2013). Tipe kedua adalah
tipe anionik, misalnya SDS atau sodiun dodecyl sulphate (natrium dodesil sulfat)
(Muhaimin, 2013). Tipe selanjutnya adalah tipe kationik: CTAB atau
cetyltrimethyl ammonium bromide (setiltrimetil amonium bromida) (Muhaimin,
2013)
Dari kesekian surfaktan ini, yang paling umum digunakan adalah PVA
karena PVA dapat menghasilkan ukuran mikrosfer yang paling kecil (Jeffery et
al., 1991 dalam Muhaimin, 2013). Peningkatan konsentrasi surfaktan dapat
mengurangi ukuran mikropartikel (Pachuau, L., B, Mazumder, 2009).
Penambahan surfaktan dapat menurunkan tegangan permukaan fase kontinyu
sehingga dapat mengurangi ukuran partikel. Akan tetapi selama konsentrasi misel
kritis atau critical micelle concentration (CMC), tegangan permukaan tidak dapat
menurun. Ketika konsentrasi surfaktan mencapai level tertentu, permukaan larutan
dapat diisi secara sempurna. Penambahan surfaktan lebih lanjut dapat
menyebabkan terbentuknya misel dan tegangan permukaan fase encer tidak akan
menurun lagi (Li et al, 2008 dalam Muhaimin, 2013).
b. Antifoam (Antibusa)
Selain surfaktan, antibusa terkadang ditambahkan pada fase kontinyu
ketika dilakukan agitasi yang kuat karena busa dapat mengganggu pembentukan
mikrosfer. Ketika kecepatan pengadukan ditingkatkan, udara akan banyak masuk
dan membentuk busa. Antibusa yang digunakan dapat berupa silika atau nonsilika
dan digunakan saat kecepatan dinaikan dimana gelembung udara sudah tidak
teratur (Berchane et al, 2006; Li et al, 2008; Torres et al, 1998 dalam Muhaimin,
UIN Syarif Hidayatullah Jakarta
2.3.2. Kondisi dalam Pembuatan Mikropartikel Menggunakan Metode Penguapan Pelarut
Faktor lain yang perlu diperhatikan oleh peneliti pada pembuatan mikropartikel menggunakan metode penguapan pelarut adalah kondisi dalam
pembuatan mikropartikel. Kondisi tersebut adalah agitasi, prediksi ukuran, suhu,
dan tekanan.
2.3.2.1. Agitasi dan Prediksi Ukuran
Agitasi adalah salah satu parameter paling penting untuk mengontrol
ukuran mikropartikel selain sifat fisikokimia material yang digunakan. Banyak
faktor yang berhubungan dengan agitasi yang dapat memberikan efek pada ukuran
mikropartikel, misalnya geometri wadah, dorongan, posisi dorongan, dan rasio
diameter dorongan apabila dibandingkan dengan diameter wadah (Li et al, 2008;
Maa and Hsu, 1996 dalam Muhaimin, 2013). Terdapat beberapa korelasi yang
dapat memprediksi ukuran dan distribusi droplet dalam emulsi dua cairan tidak
bercampur (Maa and Hsu, 1996 dalam Muhaimin, 2013). Korelasi ini memiliki
dua aspek, yaitu:
a. Sifat fisik bahan, seperti masa jenis fase kontinyu dan tegangan antarmuka
b. Faktor yang berhubungan dengan agitasi (Li et al. 2008 dalam Muhaimin,
2013)
Peningkatan kecepatan agitasi dapat menurunkan rata-rata ukuran
mikropartikel (Mateovic et al., 2002; Yang et al.,2000b dalam Muhaimin,
2013). Disisi lain dilaporkan bahwa peningakatan volume fase dispersi dapat
menurunkan ukuran mikropartikel (Jeffery et a., 1991, 1993; Jeyanthi et al, 1997;
Li et al, 2008 dalam Muhaimin, 2013), namun pada studi lain tidak ada pengaruh
yang diteliti (Sansdrap and Moës, 1993 dalam Muhaimin, 2013).
2.3.2.2. Suhu dan tekanan
Kecepatan penguapan pelarut dapat dipercepat dengan peningkatan suhu
fase kontinyu (Li, 1994; Li et al., 2008; Miyazaki et al., 2006 dalam Muhaimin,
2013) atau dengan mengurangi tekanan wadah atau reaktor (Izumikawa et al.,
1991; Chung et al., 2001, 2002; Meng et al., 2004 dalam Muhaimin, 2013).
UIN Syarif Hidayatullah Jakarta
massa total perolehan kembali, perubahan distribusi ukuran menjadi lebih besar,
penurunan efisiensi enkapsulasi obat, dan morfologi menjadi lebih kasar (Freitas
et al., 2005 dalam Muhaimin, 2013). Suhu yang digunakan tidak boleh terlalu
tiggi supaya obat tetap bersifat alami dan agar pelarut dapat mencapai titik didih.
Oleh karena itu pengurangan tekanan menjadi pilihan yang lebih baik (Li et al,
2008 dalam Muhaimin, 2013).
Studi yang dilakukan oleh Meng et al (2004), pengisian hemoglobin bovin
pada mikrosfer PELA atau poly(d,l-lactic acid)-co-poly(ethylene glycol) (poli
asam laktat kopolietilen glikol) dibuat menggunakan metode emulsi
air/minyak/air dengan kondisi tekanan atmosfir dan kondisi penurunan tekanan
(30 kPa). Waktu pemadatan mikropartikel menurun dari 240 menit menjadi 40
menit akibat penurunan tekanan. Pengurangan tekanan dapat meningkatkan
efisiensi enkapsulasi pada beberapa kasus (Li et al., 2008 dalam Muhaimin,
2013). Progesteron yang dimasukan pada mikrosfer polilaktida menggunakan
teknik penguapan pelarut minyak/air, didapatkan hasil bahwa efisensi enkapsulasi
lebih besar pada mikrosfer yang dibuat menggukan metode penguapan pelarut
dengan penurunan tekanan, yaitu 200 mmHg lebih rendah daripada tekanan
atmosfir mula-mula yaitu 760 mmHg. Akan tetapi penelitian lain menunjukan
hasil yang berbeda (Izumikawa et al., 1991 dalam Muhaimin, 2013). Efisiensi
enkapsulasi lidokain (Chung et al., 2001 dalam Muhaimin, 2013) atau albumin
(Chung et al., 2002 dalam Muhaimin, 2013) pada mikrosfer PLA yang dibuat
dengan penurunan tekanan lebih rendah daripada mikropartikel yang dibuat
menggunakan tekanan atmosfir. Morfologi permukaan mikrosfer yang diukur
menggunakan scanning electron microscopy pada mikrosfer yang dibuat
menggunakan metode tekanan atmosfir menunjukan permukaan yang berpori dan
keras (Izumikawa et al., 1991 dalam Muhaimin, 2013). Sementara mikrosfer yang
dibuat menggunakan metode pengurangan tekanan memiliki permukaan yang
halus. Mikrosfer yang dibuat dengan tekanan yang berbeda memiliki ukuran yang
mirip dengan penelitian Meng et al (2004). Hasil ini berbeda dengan hasil
penelitian Chung et al (2001, 2002) dimana mikrosfer yang dibuat menggunakan
UIN Syarif Hidayatullah Jakarta
menggunakan tekanan atmosfir. Pengaruh tekanan pada ukuran mikrosfer masih
belum jelas karena penelitian yang masih kurang (Muhaimin, 2013).
Penurunan tekanan dapat meningkatkan kecepatan penguapan sehingga
tekanan yang digunakan sebaiknya serendah mungkin. Namun apabila tekanan
lebih rendah dari tekanan uap jenuh pelarut pada suhu tertentu, pelarut akan
mendidih. Pembentukan gelembung dapat merusak droplet fase dispersi, jadi
pengurangan tekanan perlu dijaga agar tidak melebihi tekanan uap jenuh pelarut
pada suhu tertentu. Analisi lain menunjukan bahwa suhu harus dijaga pada titik
didih saat dilakukan pengurangan tekanan (Li et al, 2008 dalam Muhaimin, 2013).
2.4. Penghantaran Obat Melalui Paru-Paru
Pengembangan terapi inhalasi yang memiliki efikasi dan keamanan yang
tinggi tidak hanya dipengaruhi oleh sifat farmakologi zat aktif, tetapi juga sistem
penghantaran dengan desain dan formulasi yang baik. Optimasi keseluruhan
sistem, yaitu obat, formulasi obat dan device (alat) perlu dilakukan untuk
mengembangkan terapi inhalasi, baik untuk terapi penyakit lokal maupun
penyakit sistemik. Kombinasi obat-alat harus dapat membuat kondisi aerosol obat
dengan distribusi ukuran partikel yang tepat dan konsentrasi untuk meningkatkan
optimasi deposisi serta dosis pada area paru-paru yang diinginkan (Labiris, N.R.,
MB, Dolovich., 2003).
Penghantaran obat melalui paru-paru sudah digunakan semenjak ribuat
tahun yang lalu. Awal mula terapi inhalasi adalah 4000 tahun yang lalu dimana
masyarakat India menghirup asap tanaman Atropa belladonna untuk mengobati
batuk. Pada abad ke 19 dan ke 20, sigaret asma yang mengandung serbuk
stramonium dengan campuran rokok untuk mengobati penyakit asma
dikembangkan. Pengembangan alat inhalasi modern dapat dibagi menjadi tiga
kategori yaitu nebulizer, MDI (Metered Dose Inhaler), dan DPI (Dry Powder
Inhaler) (Labiris,N.R.,MB, Dolovich., 2003).
a. Nebulizer
Nebulizer telah digunakan selama beberapa tahun yang lalu untuk





![Gambar 2.6. Struktur Kimia Etil Selulosa [sumber : Rowe, Paul., Marian, 2009]](https://thumb-ap.123doks.com/thumbv2/123dok/1172193.769721/43.595.230.401.602.711/gambar-struktur-kimia-etil-selulosa-sumber-rowe-marian.webp)