PEMANFAATAN PEKTIN YANG DIMODIFIKASI
DARI KULIT MARKISA KUNING (Passiflora edulis
flavicarpa) UNTUK MENYERAP LOGAM Pb(II)
SKRIPSI
Oleh
YUSRO ALHUSNA
100405005
DEPARTEMEN TEKNIK KIMIA
FAKULTAS TEKNIK
PEMANFAATAN PEKTIN YANG DIMODIFIKASI
DARI KULIT MARKISA KUNING (Passiflora edulis
flavicarpa) UNTUK MENYERAP LOGAM Pb(II)
SKRIPSI
Oleh
YUSRO ALHUSNA
100405005
SKRIPSI INI DIAJUKAN UNTUK MELENGKAPI SEBAGIAN
PERSYARATAN MENJADI SARJANA TEKNIK
DEPARTEMEN TEKNIK KIMIA
FAKULTAS TEKNIK
i
PERNYATAAN KEASLIAN SKRIPSI
Saya menyatakan dengan sesungguhnya bahwa skripsi dengan judul:
PEMANFAATAN PEKTIN YANG DIMODIFIKASI DARI KULIT MARKISA
KUNING (Passiflora edulis flavicarpa) UNTUK MENYERAP LOGAM Pb(II)
dibuat untuk melengkapi sebagian persyaratan menjadi Sarjana Teknik pada
Departemen Teknik Kimia Fakultas Teknik Universitas Sumatera Utara. Skripsi ini
adalah hasil karya saya kecuali kutipan-kutipan yang telah saya sebutkan sumbernya.
Demikian pernyataan ini diperbuat, apabila dikemudian hari terbukti bahwa karya ini
bukan karya saya atau merupakan hasil jiplakan maka saya bersedia menerima sanksi
sesuai dengan aturan yang berlaku.
Medan, September 2015
Yusro Alhusna
iii
PRAKATA
Puji dan syukur penulis panjatkan kehadirat Allah SWT atas limpahan rahmat dan
karunia-Nya sehingga skripsi ini dapat diselesaikan. Tulisan ini merupakan skripsi
dengan judul “Pemanfaatan Pektin Yang Dimodifikasi Dari Kulit Markisa Kuning
(Passiflora edulis flavicarpa) Untuk Menyerap Logam Pb(II)”, berdasarkan hasil
penelitian yang penulis lakukan di Departemen Teknik Kimia Fakultas Teknik
Universitas Sumatera Utara. Skripsi ini merupakan salah satu syarat untuk
mendapatkan gelar sarjana teknik.
Hasil penelitian ini diharapkan dapat memberikan gambaran kepada dunia industri
tentang pembuatan biosorben dari limbah kulit buah markisa untuk menyerap limbah
logam Pb.
Selama melakukan penelitian sampai penulisan skripsi ini penulis mengucapkan
terimakasih dan penghargaan yang sebesar – besarnya kepada:
1. Ibu Prof. Dr. Ir. Setiaty Pandia, selaku Dosen Pembimbing yang telah
bersedia meluangkan waktu untuk memberi pengarahan, diskusi dan
bimbingan serta persetujuan sehingga skripsi ini dapat selesai dengan baik.
2. Bapak Prof. Dr. Ir. M. Turmuzi, MS dan Bapak Dr. Eng. Rondang Tambun,
ST, MT, selaku Dosen Penguji yang telah memberikan saran dan masukan
yang membangun dalam penulisan skripsi ini.
3. Bapak Dr. Eng. Ir. Irvan, MT., selaku ketua Departemen Teknik Kimia,
Fakultas Teknik, Universitas Sumatera Utara.
4. Ibu Ir. Renita Manurung, MT., selaku koordinator penelitian.
Penulis menyadari bahwa skripsi ini masih jauh dari sempurna oleh karena itu
penulis mengharapkan saran dan masukan demi kesempurnaan skripsi ini. Semoga
skripsi ini memberikan manfaat bagi pengembangan ilmu pengetahuan.
Medan, September 2015
Penulis
iv
DEDIKASI
v
RIWAYAT HIDUP PENULIS
Nama: Yusro Alhusna
NIM: 100405005
Tempat/Tanggal Lahir: Bangkinang / 25 Maret 1993
Nama Orang Tua: Hj. Ir. Nurmita Permata Farma
Alamat Orang Tua: Kec. Bangkinang, Kab. Kampar,
Riau
Asal Sekolah
TK ABA Melati Medan tahun 1997 – 1998 SD Muhammadiyah 30 Medan tahun 1998 – 2004 SMP Negeri 1 Bangkinang tahun 2004 – 2007 SMA Negeri 1 Bangkinang tahun 2007 – 2010 Pengalaman Organisasi / Kerja
Himpunan Mahasiswa Islam (HMI) periode 2010 – 2011 sebagai Anggota PA Himpunan Mahasiswa Islam (HMI) periode 2011 – 2012 sebagai Anggota PA Himpunan Mahasiswa Islam (HMI) periode 2012 – 2013 sebagai Wakil Bendahara Umum
Ikatan Pemuda dan Mahasiswa Kampar Sumatera Utara (IPMK-SU) periode 2012 – 2013 sebagai Sekretaris Umum
Himpunan Mahasiswa Teknik Kimia (HIMATEK) periode 2013 – 2014 sebagai Sekretaris Bidang HUMAS
vi
ABSTRAK
Penelitian ini bertujuan untuk mengetahui efisiensi biosorben dari pektin yang dimodifikasi pada proses biosorpsi logam Pb(II) dengan massa, ukuran partikel, dan waktu kontak yang paling baik. Bahan-bahan yang digunakan antara lain timbal (II) sulfat, kulit markisa kuning, asam klorida, etanol 96%, natrium hidroksida, aseton,
dan aquadest. Variabel-variabel yang diamati antara lain waktu kontak dengan pektin
non-modifikasi dan pektin modifikasi, serta bobot dan ukuran partikel pada pektin modifikasi pada proses biosorpsi logam Pb(II). Ekstraksi kulit markisa kuning dilakukan dengan HCl 0,5 N dan aquadest dengan perbandingan 1:15 (w/v) pada pH 2 dan suhu 60 – 70oC selama 2 jam. Pektin diendapkan dengan alkohol 96 %. Setelah itu dilanjutkan dengan pencucian pektin dengan alkohol asam, alkohol 70% dan terakhir alkohol 96%. Setelah itu pektin dikeringkan dalam oven 40oC selama 24 jam. Proses modifikasi pektin dilakukan dengan menggunakan NaOH 3 N, HCl 3 N dan pengendapan dengan alkohol 96%. Lalu dikeringkan dalam oven vakum pada suhu 25oC selama 8 jam dan diayak menggunakan ayakan 60 dan 100 mesh. Hasil analisa gugus fungsi dengan menggunakan spektrofotometri FTIR menunjukkan adsorben mempunyai gugus karboksil yang dapat menyerap logam. Pektin tanpa modifikasi dan dengan modifikasi di kontakkan dengan larutan tunggal dengan cara mengontakkan 1 gr pektin dengan 50 ml larutan tunggal Pb(II) dengan pengadukan menggunakan magnetic stirrer 200 rpm selama waktu kontak selama 30, 60, 90 dan 120 menit. Waktu kontak terbaik digunakan sebagai acuan waktu pada variabel bobot 0,25; 0,5; 0,75 dan 1 gram. Waktu kontak terbaik dan bobot terbaik digunakan sebagai acuan untuk variasi ukuran partikel 60 dan 100 mesh. Waktu kontak terbaik pada biosorpsi logam Pb(II) pada pektin tanpa modifikasi adalah 120 menit (99,52%) dan dengan modifikasi adalah 90 menit (99.92%), bobot terbaik adalah 1 gram (99.92%) dan ukuran terbaik adalah 100 mesh (100%). Hal ini menunjukkan bahwa pektin dari kulit markisa kuning yang dimodifikasi sebagai biosorben sangat efektif dalam menurunkan konsentrasi Pb(II).
vii
ABSTRACT
The purpose of this research is to study efficiency of biosorbent from modified pectin at biosorption of Pb(II) by the best parameter of biosorbent weight, particle size, and contact time. Materials that use in this research are lead (II) sulfide, yellow passion fruit peel, hydrocholric acid, 95% ethanol, sodium hydroxide, acetone, and aquadest. Observed variables are contact time of non-modified pectin and modified pectin, biosorbent weight and particle size of modified pectin at biosorption of Pb(II). Yellow passion fruit rind was extracted with HCl 0,5 N and water with solid-liquid ratio 1 : 15 at pH 2 and temperature 60-70oC for 2 hours. Pectin was precipitated using 96% alcohol. Then pectin was washed with acidified alcohol, 70% alcohol, and last 96% alcohol. Pectin was dried in oven at 40oC for 24 hours. Modified pectin was done with NaOH 3N, HCl 3N and precipitated with 96% alcohol. Then pectin was dried in vacuum oven at 25oC for 8 hours and sieved at 60 and 100 mesh. The result of FTIR analysis indicate that pectin has a carboxyl group to absorb metal. Non-modified pectin and Non-modified pectin were compared with single solution by means 1 gr pectin was compared with 50 ml of Pb(II) single solution and stirred using magnetic stirrer 200 rpm for contact time 30, 60, 90, and 120 minutes. The optimum condition of contact time is used as reference on variable of weight 0,25; 0,5; 0,75; and 1 gram. The optimum condition of contact time and weight is used as reference on variable of particle size 60 and 100 mesh. The optimum condition for non-modified pectin as biosorbent of Pb(II) is at 120 minutes (99,52%) and non-modified pectin is at 90 minutes (99,92%), optimum weight condition for modified pectin is at 1 gram (99,92%) and optimum particle size condition is at 100 mesh (100%). The result show that modified pectin from passion fruit peel pectin as biosorbent is effective to decrease concentration of Pb(II).
viii
DAFTAR ISI
Halaman
PERNYATAAN KEASLIAN SKRIPSI i
PENGESAHAN ii
PRAKATA iii
DEDIKASI iv
RIWAYAT HIDUP PENULIS v
ix
3.3.1 Persiapan Analisis dan Kimia 17
3.3.2 Ekstraksi Pektin 17
3.3.3 Modifikasi Pektin 18
3.3.4 Penentuan Waktu Optimum 18
3.3.5 Pengaruh Bobot Biosorben 19
3.3.6 Pengaruh Ukuran Partikel Biosorben 19
3.3.7 Analisa Isoterm Adsorpsi Freundlich dan Langmuir 20
3.3.8 Analisa FTIR (Fourier Transform Infra Red) 20
3.3.9 Penentuan Derajat Esterifikasi Pektin 20
3.4 FLOWCHART PENELITIAN 22
3.4.1 Persiapan Analisis dan Kimia 22
3.4.2 Flowchart Ekstraksi Pektin 23
3.4.3 Flowchart Modifikasi Pektin 24
3.4.4 Flowchart Penentuan Waktu Optimum 25
3.4.5 Flowchart Pengaruh Bobot Biosorben 26
3.4.6 Flowchart Pengaruh Ukuran Partikel Biosorben 27
3.4.7 Flowchart Analisa Isoterm Langmuir dan Freundlich 28
3.4.8 Flowchart Penentuan Derajat Esterifikasi Pektin 29
BAB IV HASIL DAN PEMBAHASAN 30
4.1 EKSTRAKSI PEKTIN 30
4.2 MODIFIKASI PEKTIN 31
4.3 PENENTUAN WAKTU OPTIMUM 32
4.4 PENGARUH BOBOT BIOSORBEN 34
4.5 PENGARUH UKURAN BIOSORBEN 35
x
4.7 ANALISA FTIR 39
4.8 ANALISA PENENTUAN DERAJAT ESTERIFIKASI
PEKTIN MODIFIKASI DAN NONMODIFIKASI 42
BAB V KESIMPULAN DAN SARAN 44
5.1 KESIMPULAN 44
5.2 SARAN 44
DAFTAR PUSTAKA 45
LAMPIRAN 1 52
LAMPIRAN 2 57
xi
Gambar 3.7 Flowchart Analisa Isoterm Langmuir dan Freundlich 28
Gambar 3.8 Flowchart Penentuan Derajat Esterifikasi Pektin 29
Gambar 4.1 Hasil Ekstraksi Pektin Kulit Buah Markisa 30
Gambar 4.2 Hasil Modifikasi Pektin Kulit Buah Markisa 31
Gambar 4.3 Pengaruh Waktu Optimum Biosorpsi Pb(II) Terhadap
Persentase Penyerapan 33
Gambar 4.4 Pengaruh Bobot Biosorben Terhadap Persentase
Penyerapan Pb(II) 34
Gambar 4.5 Pengaruh Ukuran Biosorben Terhadap Persentase
Penyerapan Pb(II) 35
Gambar 4.6 Pola Isoterm Adsorpsi Pektin Kulit Buah Markisa
Terhadap Ion Logam Pb(II) 36
Gambar 4.7 Kurva Isoterm Langmuir Pektin Kulit Buah Markisa
Terhadap Ion Logam Pb(II) 38
Gambar 4.8 Kurva Isoterm Freundlich Pektin Kulit Buah Markisa
Terhadap Ion Logam Pb (II) 38
Gambar 4.9 Hasil Spektrum FTIR Untuk Pektin Non-Modifikasi 40
Gambar 4.10 Hasil Spektrum FTIR Untuk Pektin Modifikasi 41
Gambar L1.1 Hasil Uji FTIR Pektin Non-Modifikasi 53
xii
Gambar L2.1 Kurva Isoterm Adsorpsi Langmuir Pektin Kulit Buah
Markisa Terhadap Ion Logam Pb2+ 58
Gambar L2.2 Kurva Isoterm Adsorpsi Freundlich Pektin Kulit Buah
Markisa Terhadap Ion Logam Pb2+ 59
Gambar L3.1 Kulit Markisa Kuning Kering 61
Gambar L3.2 Ekstraksi Kulit Markisa Kuning 61
Gambar L3.3 Penyaringan Filtrat Pektin 62
Gambar L3.4 Hasil Penyaringan Filtrat Pektin 62
Gambar L3.5 Pengendapan Pektin 62
Gambar L3.6 Penyaringan Gel Pektin 63
Gambar L3.7 Pencucian Gel Pektin 63
Gambar L3.8 Gel Pektin 63
Gambar L3.9 Pektin Kering 64
Gambar L3.10 Hasil Pelarutan Pektin dan Pengaturan pH 64
Gambar L3.11 Pengendapan Dengan Etanol 95% 64
Gambar L3.12 Peninkubasian Pektin Dengan Es Batu 65
Gambar L3.13 Penyaringan Pektin 65
Gambar L3.14 Pencucian Pektin Dengan Aseton 66
Gambar L3.15 Pektin Hasil Penyaringan 66
Gambar L3.16 Pektin Kering 66
Gambar L3.17 Proses Pengkontakan Pektin Dengan Logam 67
Gambar L3.18 Penyaringan Pektin dan Endapan Pengotor 67
Gambar L3.19 Hasil Larutan Logam yang Telah Diadsorpsi 68
Gambar L3.20 Alat Analisa Uji AAS 68
xiii
DAFTAR TABEL
Halaman
Tabel 2.1 Standar Mutu Pektin Berdasarkan Standar Mutu
International Pectin Producers Association 8
Tabel 2.2 Perhitungan Biaya Pembelian Bahan Baku 14
Tabel 2.3 Perhitungan Biaya Kebutuhan Listrik 14
Tabel L1.1 Data Hasil Percobaan Penentuan Waktu Optimum 52
Tabel L1.2 Data Hasil Percobaan Pengaruh Bobot Biosorben 52
Tabel L1.3 Data Hasil Percobaan Pengaruh Ukuran Biosorben 53
Tabel L1.4 Data Hasil Percobaan Analisa Isoterm Adsorpsi 53
Tabel L1.5 Data Hasil Analisa Penentuan Derajat Esterifikasi Pektin 54
Tabel L1.6 Data Hasil Perhitungan Penentuan Waktu Optimum 55
Tabel L1.7 Data Hasil Perhitungan Pengaruh Bobot Biosorben 55
Tabel L1.8 Data Hasil Perhitungan Pengaruh Ukuran Biosorben 55
Tabel L1.9 Data Hasil Perhitungan Analisa Isoterm Adsorpsi 56
Tabel L1.10 Data Hasil Perhitungan Analisa Penentuan Derajat
Esterifikasi Pektin 56
xiv
DAFTAR LAMPIRAN
Halaman
LAMPIRAN 1 DATA HASIL PERCOBAAN 52
L1.1 DATA HASIL PERCOBAAN 52
L1.1.1 Data Hasil Percobaan Penentuan Waktu
Optimum 52
L1.1.2 Data Hasil Percobaan Pengaruh Bobot
Biosorben 52
L1.1.3 Data Hasil Percobaan Pengaruh Ukuran
Biosorben 53
L1.1.4 Data Hasil Percobaan Analisa Isoterm
Adsorpsi 53
L1.1.5 Data Hasil Analisa FTIR (Fourier
Transform Infra Red) 53
L1.1.6 Data Hasil Analisa Penentuan Derajat
EsterifikasiPektin 54
L1.2 DATA HASIL PERHITUNGAN 55
L1.2.1 Data Hasil Perhitungan Penentuan Waktu
Optimum 55
L1.2.2 Data Hasil Perhitungan Pengaruh Bobot
Biosorben 55
L1.2.3 Data Hasil Perhitungan Pengaruh Ukuran
Biosorben 55
L1.2.4 Data Hasil Perhitungan Analisa Isoterm
Adsorpsi 56
L1.2.5 Data Hasil Perhitungan Analisa Derajat
Esterifikasi 56
LAMPIRAN 2 CONTOH HASIL PERHITUNGAN 57
L2.1 PERHITUNGAN PERSENTASE PENYERAPAN 57
xv
L2.3 PERHITUNGAN DERAJAT ESTERIFIKASI 60
LAMPIRAN 3 FOTO HASIL PERCOBAAN 61
L3.1 EKSTRAKSI PEKTIN 61
L3.2 MODIFIKASI PEKTIN 64
L3.3 PROSES BIOSORPSI DENGAN LOGAM Pb 67
xvi
DAFTAR SINGKATAN
HMP High Methoxyl Pectin
LMP Low Methoxyl Pectin
DE Degree of Esterification
HG Homogalaturonat
pH power of Hydrogen
AAS Atomic Absorption Spechtrophotometry
FTIR Fourier Transform Infra Red
ppm part per million
xvii
DAFTAR SIMBOL
Simbol Keterangan Dimensi
Pb Timbal / Plumbum
NaOH Natrium Hidroksida
HCl Asam Klorida
C3H6O Aseton
Pb2SO4 Timbal (II) Sulfat
% Efisiensi Efisiensi logam Pb(II) yang terserap %
C1 Konsentrasi larutan Pb(II) awal ppm
C2 Konsentrasi larutan Pb(II) akhir ppm
R2 Koefisien korelasi
Ce Konsentrasi adsorbat pada kesetimbangan pada fasa
cair mg/L
qm Kapasitas adsorpsi optimum mg/g
bqm Konstanta kesetimbangan isotherm Langmuir
T Temperatur K
k Konstanta adsorpsi untuk isotherm Freundlich
vi
ABSTRAK
Penelitian ini bertujuan untuk mengetahui efisiensi biosorben dari pektin yang dimodifikasi pada proses biosorpsi logam Pb(II) dengan massa, ukuran partikel, dan waktu kontak yang paling baik. Bahan-bahan yang digunakan antara lain timbal (II) sulfat, kulit markisa kuning, asam klorida, etanol 96%, natrium hidroksida, aseton,
dan aquadest. Variabel-variabel yang diamati antara lain waktu kontak dengan pektin
non-modifikasi dan pektin modifikasi, serta bobot dan ukuran partikel pada pektin modifikasi pada proses biosorpsi logam Pb(II). Ekstraksi kulit markisa kuning dilakukan dengan HCl 0,5 N dan aquadest dengan perbandingan 1:15 (w/v) pada pH 2 dan suhu 60 – 70oC selama 2 jam. Pektin diendapkan dengan alkohol 96 %. Setelah itu dilanjutkan dengan pencucian pektin dengan alkohol asam, alkohol 70% dan terakhir alkohol 96%. Setelah itu pektin dikeringkan dalam oven 40oC selama 24 jam. Proses modifikasi pektin dilakukan dengan menggunakan NaOH 3 N, HCl 3 N dan pengendapan dengan alkohol 96%. Lalu dikeringkan dalam oven vakum pada suhu 25oC selama 8 jam dan diayak menggunakan ayakan 60 dan 100 mesh. Hasil analisa gugus fungsi dengan menggunakan spektrofotometri FTIR menunjukkan adsorben mempunyai gugus karboksil yang dapat menyerap logam. Pektin tanpa modifikasi dan dengan modifikasi di kontakkan dengan larutan tunggal dengan cara mengontakkan 1 gr pektin dengan 50 ml larutan tunggal Pb(II) dengan pengadukan menggunakan magnetic stirrer 200 rpm selama waktu kontak selama 30, 60, 90 dan 120 menit. Waktu kontak terbaik digunakan sebagai acuan waktu pada variabel bobot 0,25; 0,5; 0,75 dan 1 gram. Waktu kontak terbaik dan bobot terbaik digunakan sebagai acuan untuk variasi ukuran partikel 60 dan 100 mesh. Waktu kontak terbaik pada biosorpsi logam Pb(II) pada pektin tanpa modifikasi adalah 120 menit (99,52%) dan dengan modifikasi adalah 90 menit (99.92%), bobot terbaik adalah 1 gram (99.92%) dan ukuran terbaik adalah 100 mesh (100%). Hal ini menunjukkan bahwa pektin dari kulit markisa kuning yang dimodifikasi sebagai biosorben sangat efektif dalam menurunkan konsentrasi Pb(II).
vii
ABSTRACT
The purpose of this research is to study efficiency of biosorbent from modified pectin at biosorption of Pb(II) by the best parameter of biosorbent weight, particle size, and contact time. Materials that use in this research are lead (II) sulfide, yellow passion fruit peel, hydrocholric acid, 95% ethanol, sodium hydroxide, acetone, and aquadest. Observed variables are contact time of non-modified pectin and modified pectin, biosorbent weight and particle size of modified pectin at biosorption of Pb(II). Yellow passion fruit rind was extracted with HCl 0,5 N and water with solid-liquid ratio 1 : 15 at pH 2 and temperature 60-70oC for 2 hours. Pectin was precipitated using 96% alcohol. Then pectin was washed with acidified alcohol, 70% alcohol, and last 96% alcohol. Pectin was dried in oven at 40oC for 24 hours. Modified pectin was done with NaOH 3N, HCl 3N and precipitated with 96% alcohol. Then pectin was dried in vacuum oven at 25oC for 8 hours and sieved at 60 and 100 mesh. The result of FTIR analysis indicate that pectin has a carboxyl group to absorb metal. Non-modified pectin and Non-modified pectin were compared with single solution by means 1 gr pectin was compared with 50 ml of Pb(II) single solution and stirred using magnetic stirrer 200 rpm for contact time 30, 60, 90, and 120 minutes. The optimum condition of contact time is used as reference on variable of weight 0,25; 0,5; 0,75; and 1 gram. The optimum condition of contact time and weight is used as reference on variable of particle size 60 and 100 mesh. The optimum condition for non-modified pectin as biosorbent of Pb(II) is at 120 minutes (99,52%) and non-modified pectin is at 90 minutes (99,92%), optimum weight condition for modified pectin is at 1 gram (99,92%) and optimum particle size condition is at 100 mesh (100%). The result show that modified pectin from passion fruit peel pectin as biosorbent is effective to decrease concentration of Pb(II).
1
BAB I
PENDAHULUAN
1.1 LATAR BELAKANG
Kontaminasi logam berat merupakan masalah serius yang dihadapi saat ini
karena logam berat merupakan unsur logam yang sangat berbahaya. Jika tanah
terkontaminasi oleh logam berat dengan kadar yang tinggi, maka akan merusak
rantai makanan dan pada akhirnya akan membahayakan kehidupan manusia [1].
Penggunaan logam Pb yang cukup luas saat ini seperti pengaplikasian pada
baterai, bensin, cat, dan lain-lain menyebabkan tingginya kemungkinan terjadinya
pencemaran oleh logam Pb. Logam timbal bersifat beracun pada sistem syaraf,
hometologic, dan mampu mempengaruhi kinerja ginjal [2].
Untuk mengontrol pencemaran lingkungan oleh logam berat, perlu dibatasi
kandungan maksimum logam dalam suatu limbah yang boleh dibuang ke
lingkungan. Dari Lampiran Peraturan Menteri Negara Lingkungan Hidup Nomor
03 Tahun 2010 Tentang Baku Mutu Air Limbah Bagi Kawasan Industri,
kandungan timbal yang diizinkan yaitu dengan kadar maksimum 1 mg/L [3].
Dikarenakan efek logam yang sangat berbahaya bagi manusia, maka
dilakukan beberapa penelitian untuk mengembangkan berbagai metode alternatif
dalam penanganan limbah. Beberapa proses pengambilan logam berat yang telah
ada diantaranya adalah pengendapan secara kimia, ion exchange, pemisahan
dengan membran, elektrolisa dan ekstraksi dengan solvent [4]. Namun, proses-
proses tersebut memiliki kelemahan, diantaranya adalah efisiensi yang rendah,
kondisi operasi yang sensitif, dan limbah lumpur yang tinggi [5]. Selain itu,
proses-proses diatas umumnya memerlukan biaya tinggi serta kurang efektif bila
diaplikasikan pada konsentrasi limbah yang rendah [6].
Terdapat beberapa bahan-bahan biologis yang dapat diaplikasikan sebagai
alternatif bahan baku biosorben, diantaranya adalah alga, fungi dan bakteri.
Namun penggunaan organisme hidup sebagai biosorben memiliki beberapa
kendala diantaranya adalah perlunya pemberian nutrisi tambahan dan terdapat
2
Selain mikroorganisme, bahan baku biosorben dapat diperoleh dari limbah
pertanian. Limbah pertanian merupakan limbah organik yang dapat ditemukan
dalam jumlah besar. Keuntungan penggunaan limbah pertanian ini adalah selain
mampu mengurangi volume limbah juga dapat memberdayakan limbah sehingga
memiliki nilai jual yang tinggi. Salah satu limbah pertanian yang dapat digunakan
adalah jerami padi, kentang, kulit buah-buahan serta daun dan ranting
tanaman-tanaman tertentu [8].
Sumatera Utara merupakan salah satu daerah sentral produksi markisa
(Passiflora edulis) di Indonesia. Limbah yang dihasilkan oleh industri pengolahan
buah markisa adalah berupa kulit buah markisa dengan produksi limbah kulit
buah markisa sebanyak 2,5–4 ton per hari [9].
Menurut penelitian yang dilakukan oleh Kurniasari, dkk [8] pektin dapat
digunakan sebagai salah satu alternatif sumber biosorben karena banyak
mengandung gugus aktif. Namun pektin yang terdapat pada limbah organik
umumnya adalah jenis HMP (High Methoxyl Pectin) sehingga untuk dapat
diaplikasikan sebagai logam berat, pektin harus didemetilasi atau dimodifikasi
terlebih dahulu.
Pektin merupakan campuran polisakarida dengan komponen utama polimer
α-D-asam galakturonat yang mengandung gugus metal ester pada konfigurasi atom C-2 [10]. Beberapa kelompok karboksilat dari molekul asam galakturonat
dalam rantai pektin adalah metil esterifikasi dan persentase kelompok
teresterifikasi dinyatakan sebagai DE (Degree of Esterification). Tergantung pada
derajat metoksilasi, pektin dibagi menjadi dua kelompok besar: pektin dengan
kadar metoksil tinggi, dengan DE 50 – 80% dan pektin dengan kadar metoksil rendah, dengan DE 25 – 50% [11].
Beberapa penelitian telah dilakukan guna mengembangkan berbagai bahan
baku yang dapat digunakan. Wong, dkk. [12] menggunakan pektin durian
termodifikasi dapat menghilangkan logam Pb dengan persentase penghilangan
logam 57,86%. Penelitian lain tentang penggunaan pektin sebagai biosorben
logam berat dilakukan oleh Mata, dkk. [13] dengan menggunakan pektin dari
pulpa gula bit. Pektin digunakan untuk biosorpsi logam Cu(II), Cd(II) dan Pb(II)
3
logam berat dengan pektin mengikuti susunan ; Cu>Pb>Cd. Penelitian oleh
Rajawane [14] memperlihatkan bahwa kulit buah kakao yang mengandung pektin
dan selulosa berpotensi sebagai adsorben logam Pb(II) dari limbah industri aki
dengan kapasitas adsorpsi 724.90 μg/g adsorben. Penelitian lain juga dilakukan oleh Balaria dan Silke [15] menggunakan citrus pectin untuk menyerap logam
Pb(II). Dari penelitian ini disimpulkan bahwa LMP dan HMP dapat
menghilangkan Pb hampir 90% pada jumlah pektin 0,1 g/L dan konsentrasi Pb 0,1
mM. Penelitian oleh Pavan, dkk. [16] menggunakan pektin dari ponkan peel untuk
menyerap logam Pb(II). Dari penelitian ini dapat disimpulkan bahwa pH optimum
pektin adalah 5, waktu rata-rata yang penyerapan logam yang paling cepat adalah
pada 60 menit, dan maksimum kapasitas penyerapan logam oleh ponkan peel
adalah pada 112,1 mg/g.
Oleh karena kulit buah markisa mengandung pektin yang cukup tinggi yakni
27,8% basis kering [17] dan juga ketersediaan bahan baku yang cukup tinggi,
maka dilakukan penelitian dengan menggunakan kulit buah markisa yang telah
dimodifikasi yang dapat dimanfaatkan sebagai penyerap ion logam berat timbal
(Pb).
1.2 PERUMUSAN MASALAH
Adapun perumusan masalah dalam penelitian ini adalah sejauh mana
pengaruh massa, ukuran, dan waktu biosorben dari pektin yang dimodifikasi
terhadap adsorpsi ion logam Pb(II).
1.3 TUJUAN PENELITIAN
Adapun tujuan dari penelitian ini adalah untuk mengetahui efisiensi
biosorben dari pektin yang dimodifikasi (massa, ukuran partikel, dan waktu)
terhadap adsorpsi ion logam Pb(II).
1.4 MANFAAT PENELITIAN
Manfaat dari penelitian ini adalah:
1. Untuk memperoleh informasi mengenai pemanfaatan pektin dari kulit
4
2. Untuk memberikan informasi dasar kelayakan penggunaan pektin dari kulit
markisa sebagai adsorben logam berat.
1.5 RUANG LINGKUP PENELITIAN
Adapun ruang lingkup dari penelitian ini adalah:
1. Bahan baku yang digunakan sebagai biosorben adalah pektin dari kulit
markisa.
2. Ekstraksi dilakukan pada pH 2 dan suhu 60 – 70oC selama 2 jam [18-19] 3. Modifikasi pektin dilakukan dengan menggunakan modifikasi pH dan
temperatur. pH pektin ditingkatkan menjadi basa hingga pH 10 dengan
menggunakan NaOH, didinginkan hingga temperatur kamar dan diasamkan
kembali dengan menggunakan HCl hingga pH 3 [12].
4. Sampel limbah yang digunakan sebagai aplikasi biosorben adalah logam
tunggal Pb(II).
5. Metode adsorpsi dilangsungkan dengan memvariasikan tiga variabel sebagai
berikut:
- Waktu adsorpsi: 30, 60, 90, dan 120 menit [20]
- Bobot biosorben: 0,25; 0,50; 0,75; dan 1 gr untuk 50 ml larutan tunggal
Pb (II) [20]
- Ukuran partikel adsorben: 60 dan 100 mesh [20]
6. Analisa yang dilakukan adalah:
- Analisa isotherm adsorpsi Freundlich dan Langmuir dengan variasi
konsentrasi logam 15, 18, 21, 24 dan 27 ppm.
- Analisa FTIR pada rentang gelombang 500 – 4000 cm-1.
- Analisa derajat esterifikasi pektin menggunakan cara titrasi dengan NaOH
5
BAB II
TINJAUAN PUSTAKA
2.1 MARKISA KUNING (Passiflora edulis flavicarpa)
Markisa kuning merupakan salah satu kelompok markisa asam tergolong
dalam famili Passifloraceae atau disebut buah Rola (Yellow Passion Fruit).
Markisa kuning dapat dibudidayakan di daerah dataran rendah hingga pada
ketinggian 600 m dpl., curah hujan antara 2.000 – 3.000 mm/tahun, dan suhu 22 – 32oC Berikut adalah ciri-ciri markisa kuning:
1. Merupakan tanaman herba atau berkayu, dan memiliki sulur.
2. Ruas batang lebih panjang dari pada markisa ungu 7-10 cm dengan sulur
muda berwarna kecoklatan.
3. Bentuk daun menjari dengan ukuran daun lebih besar dan lebih tebal daripada
markisa ungu, panjang daun 10 – 13 cm, dan lebar 9 – 12 cm, daun muda berwarna hijau, sedangkan tangkai berwarna hijau kecoklatan.
4. Ukuran bunga besar dengan mahkota tambahan berbentuk benang dan
memencar berwarna ungu dengan ujung putih.
5. Buah muda berwarna hijau, sedangkan buah masak berwarna kuning muda
dengan kulit yang tebal dan agak keras. Buah berbentuk bulat agak lonjong
atau oval dengan sari buah berwarna kuning, rasanya asam manis dengan
aroma seperti jambu biji [21].
Penelitian invitro di University of Florida menemukan bahwa ekstrak buah
markisa kuning banyak mengandungsenyawa kimia yang mampu membunuh sel
kanker. Kandungan senyawa kimia tersebut antara lain polifenol dan karotenoid.
Sedangkan kandungan gizinyaantara lain: lemak, protein, serat, mineral, kalsium,
fosfor, zat besi, karoten, tiamin, riboflavin, niasin, asam askorbat, dan asam sitrat
6
Gambar 2.1 Buah Markisa [23]
Klasifikasi markisa kuning menurut Rukmana [23] adalah sebagai berikut:
Kingdom : Plantae
Divisi : Spermatophyta
Subdivisio : Angiospermae
Kelas : Dicotyledonae
Ordo : Passiflorae
Famili : Passifloraceae
Genus : Passiflora
Spesies : Passiflora edulis var. flavicarpa
Dalam proses pengolahan markisa untuk menghasilkan sari buah markisa,
juga dihasilkan limbah. Makin meningkatnya produksi pengolahan markisa berarti
akan meningkat pula limbah yang dihasilkan. Bila dikaitkan dengan produksi
markisa Indonesia pada tahun 2010 dan 51% dari buah markisa terdiri dari kulit,
maka terdapat limbah kulit markisa sebanyak 67.314 ton yang belum
dimanfaatkan. Padahal kulit markisa mengandung pektin yang tinggi yaitu sebesar
14% [24].
2.2 PEKTIN
Pektin adalah polimer linier dari asam D-galakturonat yang berikatan
dengan ikatan 1,4-α-glikosidik [25] [26]. Polisakarida, homogalakturonat, i-ramnogalakturonat adalah 3 jenis pektin yang terdapat pada dinding sel tanaman.
Homogalakturonat (HG) adalah rantai linier dari ikatan 1,4-α-glikosidik, yang beberapa dari gugus karboksilnya adalah metil teresterifikasi [27]. Gambar 2.2
7
Gambar 2.2 Rantai Molekul Pektin [10]
Pektin pertama kali diisolasi tahun 1825 oleh Heneri Bracannot. Kegunaan
utamanya adalah sebagai gelling agent dan stabilizer pada berbagai industri
pangan [28]. Selain dibidang pangan, pektin juga banyak digunakan pada bidang
farmasi dan kedokteran misalnya sebagai penggumpal pada terapi darah [29].
Senyawa penyusun pektin yaitu:
1. Asam pektat, adalah pektin yang tidak mengandung gugus metil ester.
Senyawa ini biasanya terdapat pada sayuran dan buah yang busuk atau yang
terlalu matang.
2. Asam pektina (pektin), adalah asam poligalakturonat, yaitu asam yang
mengandung gugus metil ester, dapat terikat dengan air membentuk jelly dan
gula dalam suasana asam.
3. Protopektin, adalah komponen yang tidak larut dalam air, dapat dihirolisa dan
terdispersi menjadi pektin dan pektinat [30].
Hasil ekstraksi pektin adalah berbentuk bubuk berwarna putih hingga
coklat terang. Pada proses ekstraksi, sebagian gugus karboksil pada polimer
pektin akan mengalami metilasi menjadi gugus metoksil. Senyawa hasil ekstraksi
inilah yang disebut dengan asam pektinat (pektin). Nilai derajat metilasi
menentukan suhu pembentukan gel, yakni semakin tinggi derajat metilasi maka
suhu pembentukan gelnya juga akan semakin tinggi [31].
Sifat fisik pektin tergantung pada karakteristik kimianya. Pada pektin
dengan kadar metoksil rendah, kemampuan membentuk gel dengan gula dan asam
hilang. Namun sebaliknya, pektin dengan kadar metoksil rendah ini justru mampu
membentuk gel dengan penambahan ion kalsium. Sedangkan pada pektin dengan
kadar metoksil tinggi, pembentukan gelnya terjadi melalui ikatan hidrogen
8
Tabel 2.1 menunjukkan standar mutu pektin berdasarkan standar mutu
International Pectin Producers Association.
Tabel 2.1 Standar Mutu Pektin Berdasarkan Standar Mutu Internasional Pectin
Producers Association [33]
Faktor Mutu Kandungan
Kekuatan gel, grade min 150
Kandungan metoksil:
Pektin metoksil tinggi, %
Pektin metoksil rendah, %
>7,12
2,5 – 7,12
Kadar asam galakturonat, % min 35
Kadar air, % maks 12
Kadar abu, % maks 10
Derajat esterifikasi untuk:
Pektin ester tinggi, % min
Pektin ester rendah, % maks
50
50
Bilangan asetil, % 0,15 – 0,45
Berat ekivalen 600 - 800
2.3 EKSTRAKSI PEKTIN
Ekstraksi merupakan suatu proses pemisahan satu atau beberapa bahan dari
satu padatan atau cairan, dengan menggunakan bahan pelarut pada suhu tertentu.
Pada proses ekstraksi pektin, bahan baku dipanaskan dalam larutan asam encer
untuk menghidrolisa protopektin yang tidak larut menjadi pektin yang larut [34].
Kondisi ekstraksi pektin berpengaruh terhadap karakteristik pectin, dan sifat
fisik pektin tergantung dari karakteristik kimia pektin. Jika waktu ekstraksi pektin
terlalu lama maka akan menyebabkan terjadinya hidrolisis pektin menjadi asam
galakturonat. Pada kondisi asam, ikatan glikosidik gugus metil ester dari pektin
cenderung terhidrolisis menghasilkan asam galakturonat [35] [36].
Beberapa perlakukan selama proses ekstraksi mempengaruhi hasil pektin
yang diperoleh. Lama waktu ekstraksi mempengaruhi berat pektin yang didapat,
yakni semakin lama waktu ekstraksi maka akan semakin besar pula berat pektin
9
suhu selama proses ekstraksi. Sedangkan untuk proses pencucian pektin,
pencucian dengan alkohol tidak mempengaruhi banyaknya jumlah pektin yang
diperoleh, namun akan memberikan warna yang lebih baik yaitu putih kekuningan
[37].
Pektin yang lebih mudah larut dalam air dapat diperoleh dengan
memodifikasi pH dan suhu pada metode ekstraksi. Pektin yang diperoleh dengan
cara ini memiliki rantai lebih pendek dan tidak bercabang sehingga akan lebih
mudah larut dibandingkan pektin yang memiliki rantai yang lebih panjang [12].
2.4 BIOSORPSI
Proses penyerapan yang menggunakan material biologi (biomaterial)
sebagai sorben disebut biosorpsi. Biosorpsi didefenisikan sebagai proses
penggunaan bahan alami untuk mengikat logam berat [38]. Proses ini terjadi
ketika ion logam berat mengikat dinding sel dengan dua cara yang berbeda,
pertama pertukaran ion dimana ion monovalent dan divalent seperti Na, Mg, dan
Ca pada dinding sel digantikan oleh ion-ion logam berat; dan kedua adalah
pembentukan kompleks antara ion-ion logam berat dengan fungsional grup seperti
karbonilm amini, thiol, hidroksi, posfat, dan hidroksi-karboksil yang berada pada
dinding sel [39].
Proses biosorpsi logam berat dengan adsorben hayati merupakan proses
yang kompleks dan mekanismenya bisa bervariasi tergantung bahan baku
adsorbennya. Bila bahan baku biosorpsi adalah dari limbah pertanian, maka
mekanisme yang mungkin adalah yang tidak tergantung pada metabolisme sel.
Mekanisme biosorpsi pada bahan-bahan ini umumnya didasarkan pada interaksi
kimia fisika antara ion logam dengan gugus fungsional yang ada pada permukaan
sel. [40].
Tahap perpindahan yang terjadi adalah:
1. Perpindahan ion logam dari bagian larutan ke film pembatas yang ada di
sekitar dinding sel.
2. Perpindahan ion logam dari film pembatas ke permukaan sel.
10
4. Fase penyerapan yang terdiri dari pengikatan, pengompleksan, dan
pengendapan didalam membran biomaterial [41].
2.5 LOGAM BERAT
Logam berat merupakan komponen alami tanah yang tidak dapat
didegradasi maupun dihancurkan. Logam berat menjadi berbahaya dikarenakan
sistem bioakumulasi, yaitu adanya peningkatan konsentrasi unsur kimia didalam
tubuh mahluk hidup [42]. Beberapa jenis logam berat yang sering menimbulkan
pencemaran adalah mercuri (Hg), khrom (Cr), kadmium (Cd), timbal (Pb) dan
arsen (As) [1].
Logam berat umumnya bersifat racun, walaupun ada beberapa diantaranya
dibutuhkan oleh tubuh dalam jumlah yang sangat kecil. Logam berat mampu
terdistribusi ke bagian tubuh manusia melalui udara, makanan, dan air yang
terkontaminasi oleh logam berat. Kontaminasi logam berat dalam jangka waktu
yang panjang dapat mencapai jumlah yang membahayakan kesehatan manusia
[43].
2.5.1 Timbal (Pb)
Timbal sering juga disebut sebagai timah hitam atau plumbum yang
disimbolkan dengan Pb. Timbal pada tabel periodik unsur kimia termasuk dalam
kelompok logam golongan IV-A dengan nomor atom (NA) 82 dan berat atom
(BA) 207,2. Timbal merupakan suatu logam berat berwarna kelabu kebiruan
dengan titik leleh 327oC dan titik didih 1.725oC. Pada suhu 550 – 600oC timbal menguap dan membentuk oksigen dalam udara lalu membentuk timbal oksida.
[44].
Timbal biasanya ditemukan di dalam batu - batuan, tanah, tumbuhan dan
hewan. Timbal 95% bersifat anorganik yang tersedia dalam bentuk garam
anorganik yang umumnya kurang larut dalam air dan selebihnya berbentuk timbal
organik. Timbal organik dapat ditemukan dalam bentuk senyawa Tetra Ethyl Lead
(TEL) dan Tetra Methyl Lead (TML). Kedua jenis senyawa ini hampir tidak larut
dalam air, namun dapat dengan mudah larut dalam pelarut organik misalnya lipid
11
Timbal pernah diaplikasikan sebagai tambahan pada bahan bakar yang
bertujuan untuk meningkatkan nilai oktan dari suatu bahan bakar karena harga
timbal relatif lebih murah. Jenis timbal yang digunakan adalah TEL yang
dipercaya mampu menjaga dudukan katup mobil dari keausan sehingga lebih awet
dan tahan lama. Namun kemudian ditemukan fakta bahwa penggunaan timbal
pada bahan bakar dapat menjadi racun sehingga semakin lama penggunaannya
semakin berkurang [46].
Timbal menyebabkan racun pada sistem saraf, hemetologic, hemetotoxic,
dan mempengaruhi kerja ginjal. Konsumsi mingguan elemen ini yang
direkomendasikan oleh WHO toleransinya bagi orang dewasa adalah 50 μg/kg berat badan dan untuk bayi atau anak-anak 25 μg/kg berat badan. Depkes RI membatasi kandungan Pb maksimum dalam makanan adalah 4 ppm, dan FAO
membatasi maksimum 2 ppm. Gejala keracunan kronis timbal ditandai dengan
rasa mual, anemia, sakit di sekitar perut dan dapat menyebabkan kelumpuhan.
[47].
2.6 ISOTERM ADSORPSI
Hubungan kesetimbangan antara potensial kimia adsorbat dalam gas atau
cairan dan potensial kimia adsorbat di permukaan adsorben pada suhu tetap
dikatakan sebagai isoterm adsorpsi. Kesetimbangan tercapai jika laju pengikatan
adsorben terhadap adsorbat sama dengan laju pelepasannya [48].
2.6.1 Isoterm Freundlich
Isoterm Freundlich mengasumsikan suatu permukaan adsorpsi yang
heterogen dan perbedaan energi pada tapak aktif [48]. Selain itu model isoterm ini
juga mengasumsikan bahwa terdapat lebih dari satu lapisan permukaan
(multilayer) [47].
Persamaan Freundlich adalah sebagai berikut [50]:
(2.1)
12
Model Isoterm Langmuir menunjukkan bahwa kesetimbangan terjadi
apabila kecepatan adsorpsi sama dengan kecepatan desorpsi [51]. Menurut
Ribeiro, et al [52], isoterm Langmuir mengasumsikan bahwa setiap tapak adsorpsi
adalah ekuivalen dan kemampuan partikel untuk terikat di tapak tersebut tidak
bergantung pada ditempati atau tidak ditempatinya tempat yang berdekatan.
Dengan kata lain, permukaan adsorpsi digambarkan homogen.
Model kinetika Langmuir dapat ditunjukkan sebagai berikut [53]:
= ( ) Ce + (2.3)
Produksi biosorben guna penyerapan logam berat akan meningkat seiring
dengan meningkatnya aplikasi penggunaan logam berat dengan menghasilkan
limbah yang berbahaya bagi lingkungan. Kulit buah markisa adalah limbah yang
dihasilkan dari limbah industri pangan serta limbah rumah tangga. Limbah kulit
buah markisa yang dibuang memiliki nilai ekonomis yang rendah karena tidak
13
menangani limbah kulit buah markisa adalah dengan cara mengubahnya menjadi
suatu produk yang lebih berharga dengan proses yang efektif dan efisien.
Salah satu cara untuk meningkatnya nilai yang tinggi pada limbah kulit buah
markisa adalah dengan membuat biosorben dari kulit buah markisa. Biosorben ini
nantinya dapat diaplikasikan guna penyerapan dan penurunan konsentrasi limbah
logam berat cair.
Produksi biosorben dari limbah kulit buah markisa dilakukan dengan
tahapan sebagai berikut:
1. Mengeringkan kulit buah markisa lalu memperkecil ukuran untuk
mempermudah proses ekstraksi.
2. Penambahan aquadest dengan perbandingan 1 : 15 (w/v), lalu pH diubah
menjadi 2 dengan penambahan HCl 0,5 N.
3. Ekstraksi dilakukan dengan memanaskan larutan pada suhu 60 – 70oC sambil diaduk selama 2 jam
4. Penyaringan filtrat dan pendinginan filtrat sampai suhu kamar
5. Pengendapan filtrat pektin dengan menggunakan alkohol 1 : 2 (v/v)
selama 16 jam.
6. Penyaringan gel pektin.
7. Pencucian gel pektin dengan alkohol asam, etanol 70% sampai pH
netral, dan terakhir dengan etanol 96%.
8. Pengeringan untuk memperoleh pektin kering.
Pada penelitian ini dilakukan pemodifikasian hasil pektin yang diperoleh
guna meningkatkan kemampuan dalam penyerapan logam berat. Proses
modifikasi dilakukan dengan cara sebagai berikut:
1. Pektin kering dilarutkan dalam aquadest sampai 1,5%.
2. pH pektin ditingkatkan menjadi 10 dengan NaOH 3N dan dilakukan
inkubasi pada suhu 50 – 60oC selama 1 jam.
3. Larutan didinginkan hingga temperatur kamar, kemudian pH diturunkan
menjadi 3 dengan 3N HCl dan disimpan semalaman.
4. Pengendapan pektin menggunakan etanol 95% dan diinkubasi dalam
wadah berisi es batu selama 2 jam.
14
6. Pengeringan pektin untuk memperoleh pektin kering.
Berikut merupakan rincian biaya pembuatan bisorben dari limbah kulit buah
markisa yang telah dilakukan selama penelitian. Perhitungan analisis ekonomi
dapat dilihat pada tabel 2.2 dan 2.3 dibawah ini
Tabel 2.2 Perhitungan Biaya Pembelian Bahan Baku
No. Biaya bahan baku Harga
Tabel 2.3 Perhitungan Biaya Kebutuhan Listrik
No. Alat Harga/ kWh Kebutuhan
kebutuhan listrik + biaya transportasi
+ biaya lain-lain
= Rp. 71.472 + Rp. 9.619,48 + Rp.
30.000,00 + Rp. 9.000,00
= Rp 120.091,48
- Harga jual pektin modifikasi =
(Rp 120.091,48/2 )
15
Berdasarkan proses yang dilakukan pada penelitian ini didapat pektin
sebanyak 2 gram dengan biaya produksi Rp. 120.091,48. Sehingga dapat
diestimasi harga jual pektin seharga Rp. 60.045,74 / gram.
Nilai ekonomi yang dimiliki pektin cukup tinggi. Indonesia masih
mengimpor pektin dengan harga eceran tepung pektin berkisar antara Rp 200.000
– Rp 300.000/kg [36]. Jika dibandingkan harga penjualan pektin kulit markisa kuning modifikasi ini dengan harga jual jual karbon aktif di pasaran, harga jual
pektin dari proses ini lebih mahal. Namun pembuatan pektin modifikasi dengan
proses ini layak dipertimbangkan, mengingat dengan proses ini dapat mengurangi
limbah kulit markisa kuning dan dapat menghasilkan efisiensi penyerapan yang
cukup tinggi.
Adapun keuntungan penggunaan biosorben pektin dari limbah kulit buah
markisa antara lain:
1. Mengurangi pencemaran limbah pertanian
2. Meningkatkan nilai jual limbah pertanian.
3. Dapat mengurangi efek pencemaran lingkungan akibat limbah logam
berat.
4. Mampu menghilangkan kadar limbah dengan efisiensi penyerapan yang
16
BAB III
METODOLOGI PENELITIAN
3.1 LOKASI DAN WAKTU PENELITIAN
Penelitian dilakukan di Laboratorium Kimia Organik, Departemen Teknik
Kimia, Fakultas Teknik, Universitas Sumatera Utara, Medan. Penelitian ini
dilakukan selama lebih kurang 8 bulan.
3.2 BAHAN DAN PERALATAN
3.2.1 Bahan Penelitian
Pada penelitian ini bahan yang digunakan adalah:
1. Kulit markisa kuning dari beberapa pasar buah di Medan, Sibolangit dan
Peralatan yang digunakan dalam penelitian ini adalah:
17
17. Atomic Absorption Spectrophotometry (AAS)
18. Fourier Transform Infra Red (FTIR)
3.3 PROSEDUR PENELITIAN
3.3.1 Persiapan Analisis dan Kimia
a. Buah markisa dicuci dan dipisahkan dari dagingnya.
b. Kulit buah markisa dikeringkan dengan oven pada 105oC.
c. Kulit kering lalu diblender sampai halus.
3.3.2 Ekstraksi Pektin
Prosedur ekstraksi pektin diadopsi dari prosedur yang dilakukan Liew, dkk.
[18] dan Simmaky dan Jaanaki [19] dengan sedikit modifikasi :
1. Tepung kulit markisa kering yang telah diperoleh ini kemudian ditambahkan
air dengan perbandingan 1 : 15 (w/v) lalu campuran diaduk.
2. Campuran ditambahkan HCl 0,5 N sampai pH 2.
3. Campuran tersebut di panaskan diatas magnetic stirer pada kisaran suhu 60 – 70 oC selama 2 jam.
4. Campuran disaring dengan kain saring dan filtrat dibiarkan dingin sampai
temperatur kamar.
5. Setelah itu ditambahkan alkohol 96 % dengan perbandingan 1 : 2 (v/v) dan
dibiarkan selama 16 jam.
6. Campuran di saring dan didapatkan pektin basah.
7. Dicuci pertama dengan alkohol asam yang dibuat dengan cara 960 ml alkohol
96% ditambah HCl 4N sampai volumenya 1000 ml, lalu pencucian kedua
18
1. Pektin dilarutkan dalam air suling sampai 1,5%.
2. pH ditingkatkan menjadi 10,0 dengan NaOH (3N) lalu diinkubasi pada 50 – 60oC selama 1 jam.
3. Lalu didinginkan hingga temperatur kamar.
4. pH disesuaikan menjadi 3 dengan 3N HCl dan disimpan semalaman.
5. Sampel diendapkan dengan 95% etanol dan diinkubasi dengan es batu selama
2 jam
6. Lalu disaring dan dicuci dengan aseton.
7. Dikeringkan pada oven vakum pada 25oC selama 8 jam.
8. Lalu diayak untuk mendapatkan ukuran 60 dan 100 mesh.
9. Selanjutnya ini diberi nama pektin dengan modifikasi.
3.3.4 Penentuan Waktu Optimum
Prosedur penentuan jumlah logam Pb(II) yang terjerap dalam biosorben
dengan variasi waktu pengadukan dilakukan dengan mengadopsi prosedur yang
dilakukan oleh Sunarya [20] yaitu:
1. 1 gr biosorben dimasukkan dalam 50 ml larutan tunggal Pb(II) dengan
konsentrasi 15 ppm.
2. Campuran diaduk dengan magnetic stirrer 200 rpm selama selang waktu
tertentu (30, 60, 90, dan 120 menit).
3. Disaring dan dianalisa dengan AAS pada panjang gelombang 283,3 nm.
4. Efisiensi Pb(II) yang terjerap oleh setiap gram sampel dapat dihitung dengan
19 Keterangan :
% Efisiensi = Efisiensi logam Pb(II) yang terjerap (%)
C1 = konsentrasi larutan Pb(II) awal (ppm)
C2 = konsentrasi larutan Pb(II) akhir (ppm)
3.3.5Pengaruh Bobot Biosorben
Prosedur penentuan jumlah logam Pb(II) yang terjerap dalam biosorben
dengan variasi bobot biosorben dilakukan dengan mengadopsi prosedur yang
dilakukan oleh Sunarya [20] yaitu:
1. Sejumlah massa (0,25; 0,50; 0,75 dan 1 gr) biosorben dimasukkan dalam 50
ml tunggal Pb(II) dengan konsentrasi 15 ppm.
2. Campuran diaduk dengan magnetic stirrer 200 rpm selama waktu optimum.
3. Disaring dan dianalisa dengan AAS pada panjang gelombang 283,3 nm.
4. Efisiensi Pb(II) yang terjerap oleh setiap gram sampel dapat dihitung dengan
rumus sebagai berikut:
% Efisiensi = Efisiensi logam Pb(II) yang terjerap (%)
C1 = konsentrasi larutan Pb(II) awal (ppm)
C2 = konsentrasi larutan Pb(II) akhir (ppm)
3.3.6 Pengaruh Ukuran Partikel Biosorben
Prosedur penentuan jumlah logam Pb(II) yang terjerap dalam biosorben
dengan variasi ukuran partikel biosorben dilakukan dengan mengadopsi prosedur
yang dilakukan oleh Sunarya [20] yaitu:
1. 1 gr biosorben dengan ukuran partikel yang berbeda (60 dan 100 mesh)
masing-masing dimasukkan dalam 50 ml tunggal Pb(II) dengan konsentrasi
15 ppm.
2. Campuran diaduk dengan magnetic stirrer 200 rpm selama waktu optimum.
20
4. Efisiensi Pb(II) yang terjerap oleh setiap gram sampel dapat dihitung dengan
rumus sebagai berikut:
% Efisiensi = Efisiensi logam Pb(II) yang terjerap (%)
C1 = konsentrasi larutan Pb(II) awal (ppm)
C2 = konsentrasi larutan Pb(II) akhir (ppm)
3.3.7 Analisa Isoterm Adsorpsi Freundlich dan Langmuir
Analisa isoterm adsorpsi dilakukan dengan menggunakan
persamaan-persamaan yang berlaku pada isoterm adsorpsi Freundlich dan Langmuir. Analisa
dilakukan dengan menvariasikan konsentrasi yaitu 15, 18, 21, 24, dan 27 ppm dan
diuji dengan AAS pada panjang gelombang 283,3 nm.
3.3.8 Analisa FTIR (Fourier Transform Infra Red)
Analisa FTIR dilakukan untuk mengetahui gugus fungsi yang terdapat pada
pektin modifikasi dan dilakukan perbandingan dengan pektin non-modifikasi.
3.3.9 Penentuan Derajat Esterifikasi Pektin
Prosedur derajat esterifikasi pektin dilakukan dengan mengadopsi prosedur
yang dilakukan oleh Liew, dkk. [18] yaitu:
1. 0,2 gram pektin kering di basahi dengan etanol dan dilarutkan dengan
aquades dan diaduk sampai larut sepenuhnya.
2. Lalu campuran ditambahkan 3 tetes phenoftalein dan dititrasi dengan NaOH
0,1 N. Hasil titrasi dicatat dan di sebut dengan initial titration.
3. Lalu sampel ditambahkan 10 ml 0,1 N NaOH untuk menetralkan
polygalacturonic acid dan sampel sampel dikocok kuat, setelah itu didiamkan
sselama 2 jam pada temperatur kamar untuk de-esterify.
4. Setelah itu sampel ditambahkan HCl 0,1 N untuk menetralkan natrium
21
5. Lalu sampel ditambahkan 3 tetes phenoftalein lagi dan dititrasi dengan
NaOH 0,1 N dicatat volume yang digunakan dan disebut dengan final
titration.
6. Berat jenis (densitas) adsorben dapat dihitung dengan rumus:
DE = (3.4)
Keterangan :
DE = Derajat Esterifikasi (%)
Final Titration = jumlah NaOH yang digunakan pada titrasi terakhir (ml)
22 3.4 FLOWCHART PENELITIAN
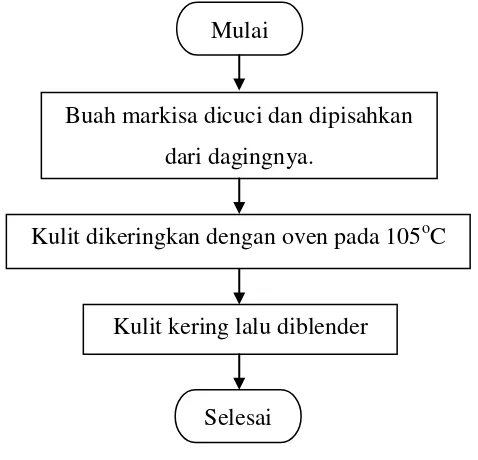
3.4.1 Persiapan Analisis dan Kimia
Gambar 3.1 menunjukkan flowchart persiapan analisis dan kimia kulit
markisa.
Gambar 3.1 Flowchart Persiapan Analisis dan Kimia Mulai
Buah markisa dicuci dan dipisahkan
dari dagingnya.
Kulit dikeringkan dengan oven pada 105oC
Kulit kering lalu diblender
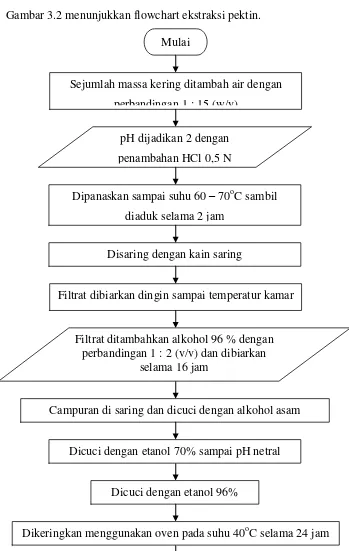
23 3.4.2 Flowchart Ekstraksi Pektin
Gambar 3.2 menunjukkan flowchart ekstraksi pektin.
Gambar 3.2 Flowchart Ekstraksi Pektin Mulai
Sejumlah massa kering ditambah air dengan
perbandingan 1 : 15 (w/v)
pH dijadikan 2 dengan
penambahan HCl 0,5 N
Dipanaskan sampai suhu 60 – 70oC sambil diaduk selama 2 jam
Disaring dengan kain saring
Filtrat dibiarkan dingin sampai temperatur kamar
Campuran di saring dan dicuci dengan alkohol asam
Dicuci dengan etanol 70% sampai pH netral
Dicuci dengan etanol 96%
Dikeringkan menggunakan oven pada suhu 40oC selama 24 jam
Diblender dan diayak 60 mesh
Selesai
Filtrat ditambahkan alkohol 96 % dengan perbandingan 1 : 2 (v/v) dan dibiarkan
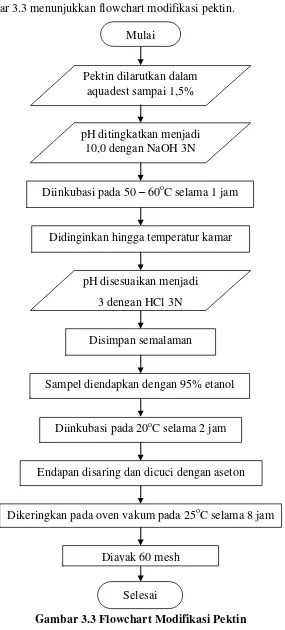
24 3.4.3 Flowchart Modifikasi Pektin
Gambar 3.3 menunjukkan flowchart modifikasi pektin.
Gambar 3.3 Flowchart Modifikasi Pektin Mulai
Pektin dilarutkan dalam aquadest sampai 1,5%
pH ditingkatkan menjadi 10,0 dengan NaOH 3N
Diinkubasi pada 50 – 60oC selama 1 jam
Didinginkan hingga temperatur kamar
pH disesuaikan menjadi
3 dengan HCl 3N
Disimpan semalaman
Sampel diendapkan dengan 95% etanol
Diinkubasi pada 20oC selama 2 jam
Endapan disaring dan dicuci dengan aseton
Dikeringkan pada oven vakum pada 25oC selama 8 jam
Diayak 60 mesh
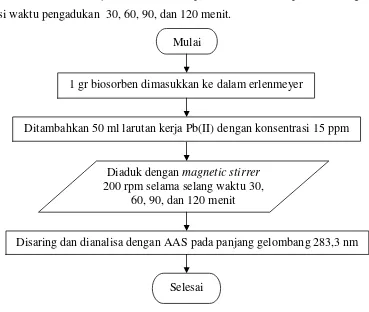
25 3.4.4 Flowchart Penentuan Waktu Optimum
Gambar 3.4 menunjukkan flowchart penentuan waktu optimum dengan
variasi waktu pengadukan 30, 60, 90, dan 120 menit.
Gambar 3.4 Flowchart Penentuan Waktu Optimum Mulai
1 gr biosorben dimasukkan ke dalam erlenmeyer
Ditambahkan 50 ml larutan kerja Pb(II) dengan konsentrasi 15 ppm
Diaduk dengan magnetic stirrer 200 rpm selama selang waktu 30,
60, 90, dan 120 menit
Disaring dan dianalisa dengan AAS pada panjang gelombang 283,3 nm
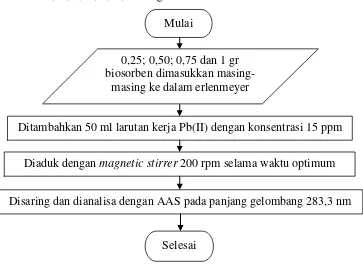
26 3.4.5 Flowchart Pengaruh Bobot Biosorben
Gambar 3.5 menunjukkan flowchart pengaruh bobot biosorben dengan
variasi bobot 0,25; 0,50; 0,75; dan 1 gr.
Gambar 3.5 Flowchart Pengaruh Bobot Biosorben Mulai
0,25; 0,50; 0,75 dan 1 gr biosorben dimasukkan
masing-masing ke dalam erlenmeyer
Ditambahkan 50 ml larutan kerja Pb(II) dengan konsentrasi 15 ppm
Diaduk dengan magnetic stirrer 200 rpm selama waktu optimum
Disaring dan dianalisa dengan AAS pada panjang gelombang 283,3 nm
27
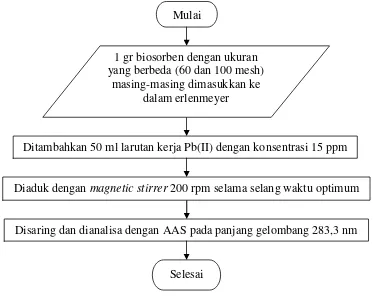
3.4.6 Flowchart Pengaruh Ukuran Partikel Biosorben
Gambar 3.6 menunjukkan flowchart pengaruh ukuran partikel biosorben
dengan variasi ukuran 60 dan 100 mesh.
Gambar 3.6 Flowchart Pengaruh Ukuran Partikel Biosorben Mulai
Ditambahkan 50 ml larutan kerja Pb(II) dengan konsentrasi 15 ppm
Disaring dan dianalisa dengan AAS pada panjang gelombang 283,3 nm
Selesai
Diaduk dengan magnetic stirrer 200 rpm selama selang waktu optimum 1 gr biosorben dengan ukuran
yang berbeda (60 dan 100 mesh) masing-masing dimasukkan ke
28
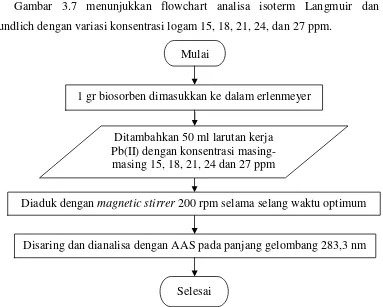
3.4.7 Flowchart Analisa Isoterm Langmuir dan Freundlich
Gambar 3.7 menunjukkan flowchart analisa isoterm Langmuir dan
Freundlich dengan variasi konsentrasi logam 15, 18, 21, 24, dan 27 ppm.
Gambar 3.7 Flowchart Analisa Isoterm Langmuir dan Freundlich Mulai
1 gr biosorben dimasukkan ke dalam erlenmeyer
Disaring dan dianalisa dengan AAS pada panjang gelombang 283,3 nm
Selesai
Ditambahkan 50 ml larutan kerja Pb(II) dengan konsentrasi masing-masing 15, 18, 21, 24 dan 27 ppm
29
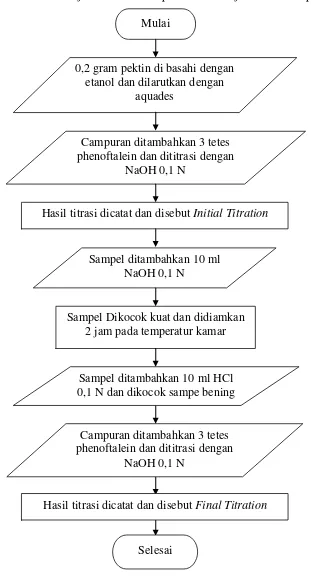
3.4.8 Flowchart Penentuan Derajat Esterifikasi Pektin
Gambar 3.8 menunjukkan flowchart penentuan derajat esterifikasi pektin.
Gambar 3.8 Flowchart Penentuan Derajat Esterifikasi Pektin Mulai
0,2 gram pektin di basahi dengan etanol dan dilarutkan dengan
aquades
Campuran ditambahkan 3 tetes phenoftalein dan dititrasi dengan
NaOH 0,1 N
Hasil titrasi dicatat dan disebut Initial Titration
Sampel ditambahkan 10 ml NaOH 0,1 N
Sampel Dikocok kuat dan didiamkan 2 jam pada temperatur kamar
Selesai
Sampel ditambahkan 10 ml HCl 0,1 N dan dikocok sampe bening
Campuran ditambahkan 3 tetes phenoftalein dan dititrasi dengan
NaOH 0,1 N
30
BAB IV
HASIL DAN PEMBAHASAN
4.1 EKSTRAKSI PEKTIN
Albido dari kulit buah markisa dikeringkan dengan oven pada suhu 105oC
lalu diblender sampai halus. Tepung kulit markisa ini ditambahkan air dengan
perbandingan 1 : 15 (w/v), kemudian pH larutan diatur menjadi 2 dengan HCl 0,5
N. Ekstraksi dilakukan untuk mengambil kandungan pektin yang terdapat di
dalam kulit, yang dilakukan pada suhu 60 – 70oC selama 2 jam. Hasil ekstraksi pektin kemudian disaring untuk diambil filtratnya. Filtrat kemudian didinginkan
hingga suhu kamar. Pengendapan pektin dilakukan dengan menambahkan alkohol
96% dengan perbandingan 1 : 2 (v/v) lalu didiamkan selama 16 jam. Hasil
pengendapan disaring untuk diambil gelnya. Kemudian gel pektin dicuci pertama
dengan alkohol asam yang dibuat dengan cara 960 ml alkohol 96% ditambah HCl
4N sampai volumenya 1000 ml, lalu pencucian kedua dilakukan dengan alkohol
70% dan terakhir dengan alkohol 96%. Pektin kemudian dikeringkan dengan oven
pada suhu 40oC selama 24 jam dan diayak 60 mesh.
Gambar 4.1 menunjukkan hasil yang diperoleh dari ekstraksi pektin dari
kulit buah markisa.
31
Dari gambar diatas dapat dilihat bahwa hasil ekstraksi pektin diperoleh gel
berwarna kuning keputihan. Sedangkan hasil pengeringan diperoleh pektin kering
sebanyak 1,5 – 2,5 gr. Menurut Akhmalludin dan Arie [37], pencucian pektin dengan alkohol tidak mempengaruhi banyaknya pektin yang dihasilkan, namun
pektin yang dihasilkan memberikan warna yang lebih baik yaitu kuning
keputihan.
4.2 MODIFIKASI PEKTIN
Pektin kering yang diperoleh dari hasil ekstraksi lalu dimodifikasi yang
berguna untuk meningkatkan kemampuan pektin dalam menyerap logam.
Modifikasi pektin dilakukan dengan menggunakan modifikasi pH dan temperatur.
pH pektin ditingkatkan menjadi basa hingga pH 10 dengan menggunakan NaOH,
didinginkan hingga temperatur kamar dan diasamkan kembali dengan
menggunakan HCl hingga pH 3. Hasil modifikasi ini nantinya diharapkan akan
menghasilkan pektin dengan kadar metoksil yang lebih rendah.
Gambar 4.2 menunjukkan hasil yang diperoleh dari modifikasi pektin kulit
buah markisa.
32
Hasil pektin yang diperoleh dari modifikasi adalah pektin berwarna coklat
dan tidak terbentuk gel. Dapat dilihat perbedaan hasil banyak gel pektin yang
diperoleh dari pektin non modifikasi dan pektin modifikasi. Pektin modifikasi
memiliki gel yang lebih sedikit bahkan hampir tidak terlihat sama sekali
dibandingkan dengan pektin non modifikasi. Pektin dengan kandungan metoksil
rendah adalah pektin dengan derajat esterifikasi kurang dari 50%. Kekuatan
pembentukan gel suatu senyawa akan lebih tinggi bila residu asam
galakturonatnya dalam molekul juga besar, atau dengan kata lain pektin dengan
kadar metoksil yang tinggi akan menghasilkan gel yang lebih banyak
dibandingkan dengan pektin metoksil rendah [54]. Hal ini diperkuat oleh
Kurniasari, dkk. [8] bahwa semakin rendah kadar metoksil pektin maka sifat
pembentukan jellinya akan semakin berkurang.
Pektin bekerja pada pH 2 – 5 untuk menyerap logam. Jika pH lebih dari 5, maka banyaknya jumlah ion logam yang diserap akan menurun [55]. Modifikasi
pektin dengan menggunakan alkali dan asam pernah diteliti oleh Annadurai, dkk.
[56] dengan menggunakan HNO3 dan NaOH untuk menyerap logam Pb2+.
Hasilnya menunjukkan bahwa perlakukan asam menunjukkan kapasitas adsorpsi
yang lebih baik jika diikuti dengan perlakuan alkali dan air diawal treatment. Oleh
karena itu modifikasi pektin dilakukan dengan perlakuan asam menggunakan HCl
yang diikuti dengan perlakuan alkali diawal treatment. pH akhir pektin adalah 3
karena pektin bekerja pada pH asam yakni 2 – 5.
4.3 PENENTUAN WAKTU OPTIMUM
Biosorben pektin dari kulit buah markisa digunakan untuk mengadsorpsi
larutan tunggal Pb(II). Konsentrasi larutan tunggal yang digunakan adalah 15
ppm sebanyak 50 ml dan ukuran partikel biosorben adalah 60 mesh sebanyak 1 gr.
Sedangkan variasi waktu pengadukan yang digunakan untuk menentukan waktu
optimum adalah 30, 60, 90, dan 120 menit.
Waktu kontak optimum dicari untuk mengetahui waktu yang dibutuhkan
dalam proses adsorpsi ion Pb2+ oleh biosorben hingga tercapai titik maksimum
dan mencapai titik kesetimbangan. Selain itu waktu kontak juga digunakan
33
tidak lagi mampu menyerap ion logam Pb2+ [57]. Pada saat persentase penyerapan
logam mencapai nilai optimum, maka lama proses biosorpsi tersebut diambil
sebagai waktu optimum biosorpsi.
Gambar 4.3 menunjukkan grafik pengaruh waktu biosorpsi terhadap
persentase penyerapan ion logam Pb2+.
Gambar 4.3 Pengaruh Waktu Optimum Biosorpsi Terhadap Persentase
Penyerapan Pb(II)
Dari gambar 4.3 dapat dilihat bahwa untuk pektin modifikasi selama selang
waktu 30, 60, dan 90 menit terjadi peningkatan persentase penyerapan. Hal ini
disebabkan oleh karena masih banyak gugus dari biosorben yang belum
berinteraksi secara optimum dengan biosorbat. Pada menit ke 90 persentase
penyerapan diperoleh sebesar 99,92%. Selanjutnya terjadi penurunan pada waktu
120 menit yang menunjukkan bahwa biosorben sudah mengalami titik kejenuhan.
Hal ini menunjukkan bahwa pada waktu 90 menit telah terjadi kondisi
kesetimbangan antara ion logam yang terlepas dan terikat kembali [57].
Dari hasil penelitian dapat disimpulkan bahwa waktu optimum biosorpsi
logam Pb2+ oleh modifikasi pektin kulit buah markisa adalah 90 menit. Sedangkan
untuk pektin nonmodifikasi peningkatan persentase penyerapan terus terjadi
hingga menit ke 120. Pada menit ke 120 persentase penyerapan adalah 99,52%
sehingga dapat disimpulkan bahwa waktu optimum untuk pektin nonmodifikasi
34 4.4 PENGARUH BOBOT BIOSORBEN
Biosorben pektin dari kulit buah markisa digunakan untuk mengadsorpsi
larutan tunggal Pb(II). Konsentrasi larutan tunggal yang digunakan adalah 15 ppm
sebanyak 50 ml, ukuran partikel biosorben adalah 60 mesh, dan waktu
pengadukan diambil dari waktu optimum yakni 90 menit. Sedangkan variasi
bobot biosorben yang digunakan adalah 0,25;0,50;0,75; dan 1 gr
Gambar 4.4 menunjukkan grafik pengaruh bobot biosorben terhadap
persentase penyerapan ion logam Pb2+.
Gambar 4.4 Pengaruh Bobot Biosorben Terhadap Persentase Penyerapan Pb(II)
Dari gambar 4.4 dapat dilihat bahwa semakin besar bobot biosorben maka
persentase penyerapannya akan semakin besar.
Jika bobot biosorben dinaikkan, sedangkan waktu kontak dan konsentrasi
biosorbat tetap, peningkatan jumlah tapak aktif akan meningkatkan penyebaran
biosorbat, sehingga waktu yang dibutuhkan untuk mencapai kesetimbangan lebih
lama. Oleh sebab itu, kapasitas biosorpsi semakin rendah dengan meningkatnya
bobot biosorben [58]. Hal ini juga diperkuat oleh Junior, dkk. [59] yang
menyatakan bahwa pada saat ada sebuah peningkatan bobot biosorben, maka ada
35 4.5 PENGARUH UKURAN BIOSORBEN
Biosorben pektin dari kulit buah markisa digunakan untuk mengadsorpsi
larutan tunggal Pb(II). Konsentrasi larutan tunggal yang digunakan adalah 15 ppm
sebanyak 50 ml, dan waktu pengadukan diambil dari waktu optimum yakni 90
menit. Ukuran partikel yang digunakan 60 mesh dan 100 mesh, dimana ukuran 60
mesh adalah hasil ayakan yang lolos pada ukuran 60 mesh tetapi tertahan pada
ukuran 80 mesh dan ukuran 100 mesh merupakan hasil ayakan yang lolos pada
ukuran 100 mesh tetapi tertahan pada ayakan 140 mesh.
Gambar 4.5 menunjukkan grafik pengaruh ukuran biosorben terhadap
persentase penyerapan ion logam Pb2+.
Gambar 4.5 Pengaruh Ukuran Biosorben Terhadap Persentase Penyerapan Pb(II)
Dari gambar 4.5 dapat dilihat bahwa semakin kecil ukuran biosorben maka
persentase penyerapannya juga akan semakin besar. Hal ini dikarenakan semakin
kecil ukuran partikel per satuan volume bisorben, maka semakin luas
permukaannya, sehingga ion-ion akan lebih banyak terserap pada permukaan
biosorben tersebut [20]. Pada grafik juga menunjukkan hasil yang tidak terlalu
jauh berbeda antara 60 mesh dan 100 mesh yakni 99,92% dan 100%. Hal ini
mungkin disebabkan pada saat pengayakan jenis partikel yang lolos yang
digunakan untuk percobaan pada variabel 60 dan 100 mesh terdapat ukuran
36 4.6 ANALISA ISOTERM ADSORPSI
Kelayakan dan efisiensi suatu proses biosorpsi tidak hanya bergantung pada
sifat biosorben, tetapi juga pada konsentrasi larutan ion logam [60]. Setiap
adsorben yang menyerap suatu zat satu dengan zat lain mempunyai pola isoterm
adsorpsi yang berbeda. Hal ini dikarenakan terdapat faktor-faktor yang
mempengaruhi dalam proses adsorpsi antara lain yaitu jenis adsorben, jenis zat
yang diserap, luas permukaan adsorben, konsentrasi zat yang diadsorpsi dan suhu.
[61].
Data kesetimbangan biasanya digambarkan dalam bentuk kurva isoterm
adsorpsi. Pendekatan dengan model terhadap kurva isoterm dapat membantu
menganalisis karakteristik isoterm berupa kapasitas, afinitas, selektifitas serta
mekanisme interaksi adsorpsi [62].
Gambar 4.6 menunjukkan grafik pola isoterm adsorpsi terhadap logam ion
Pb.
Gambar 4.6 Pola Isoterm Adsorpsi Pektin Kulit Buah Markisa Terhadap Ion
Logam Pb2+
Model isoterm adsorpsi Langmuir dan Freudlich umum digunakan untuk
menentukan parameter adsorpsi pada adsorpsi cairan dengan konsentrasi rendah.
Model isoterm Langmuir dibuat berdasarkan asumsi bahwa binding sites
terdistribusi secara homogen di seluruh permukaan adsorben, dimana adsorpsi
37
berdasarkan asumsi bahwa ada permukaan heterogen dengan beberapa tipe pusat
adsorpsi yang aktif. Model ini sering digunakan untuk menggambarkan adsorpsi
senyawa organik dan inorganik dalam larutan. [63].
Model kinetika Langmuir dapat ditunjukkan sebagai berikut [53]:
= ( ) Ce +
dimana:
Ce = konsentrasi adsorbat pada kesetimbangan pada fasa cair (mg/L)
qe = konsentrasi adsorbat pada fasa padat/adsorben (mg/s)
1/qm = kemiringan atau sensitifitas
qm = kapasitas adsorpsi optimum (mg/g)
1/(bqm) = intersep
bqm = konstanta kesetimbangan
Model kinetika Freundlich dapat ditunjukkan sebagai berikut [50]:
dimana:
Ce = konsentrasi adsorbat pada kesetimbangan pada fasa cair (mg/L)
qe = konsentrasi adsorbat pada fasa padat/adsorben (mg/s)
k = konstanta kesetimbangan