VIRULENSI NUCLEAR POLYHEDROSIS VIRUS (NPV) TERHADAP ULAT GRAYAK (Spodoptera litura F.) (Lepidoptera : Noctuidae) PADA
TANAMAN TEMBAKAU DELI DI RUMAH KACA
S K R I P S I
Oleh:
ADE SARTIKA RIMADHANI 080302004
HPT
PROGRAM STUDI AGROEKOTEKNOLOGI FAKULTAS PERTANIAN
UNIVERSITAS SUMATERA UTARA MEDAN
VIRULENSI NUCLEAR POLYHEDROSIS VIRUS (NPV) TERHADAP ULAT GRAYAK (Spodoptera litura F.) (Lepidoptera : Noctuidae) PADA
TANAMAN TEMBAKAU DELI DI RUMAH KACA
S K R I P S I
Oleh:
ADE SARTIKA RIMADHANI 080302004
HPT
Skripsi Sebagai Salah Satu Syarat Untuk Dapat Memperoleh Gelar Sarjana di Program Studi Agroekoteknologi Fakultas Pertanian
Universitas Sumatra Utara, Medan.
Disetujui Oleh: Dosen Pembimbing
(Prof. Dr. Ir. Darma Bakti, M.S) (Prof. Dr. Dra. Maryani Cyccu Tobing, M.S
Ketua
Anggota
)
PROGRAM STUDI AGROEKOTEKNOLOGI FAKULTAS PERTANIAN
UNIVERSITAS SUMATERA UTARA MEDAN
ABSTRACT
Ade Sartika Rimadhani, ”The Virulence of Nuclear Polyhedrosis Virus
(NPV) of Larvae Tobacco Caterpillar (Spodoptera litura F.) (Lepidoptera : Noctuidae) On Deli Tobacco In Glasshouse”, under supervised by
Darma Bakti and Maryani Cyccu Tobing. This research was to study the virulence of NPV of larvae S. litura on Deli tobacco in Glasshouse. This research was
carried out at Central Research Deli Tobacco Sampali PTPN II Medan since May-September 2012. The method of this research was Randomized Complete
Design Factorial which consists stages of larvae (2nd and 4th instar) and the number of virus suspenses (10, 20, and 30 larvae infected virus/1 l water) with three replication.
The result showed that highest percentage mortality (91,67%) was found in treatment 2nd instar with suspense 30 larvae infected virus/1 l water and the lowest percentage (0%) on control. The highest percentage of damage intensity (33,06%) was control and the lowest percentage (15,58%) on suspense 30 larvae infected virus/1 l water. The fastest incubation period (1,67 days) in the treatment 4th instar are 1,67 days and suspense of 30 larvae infected virus/1 l water are 1,83 days and the lowest in the treatment 2nd instar are 2,58 days and control didn’t showed symptoms infection.
ABSTRAK
Ade Sartika Rimadhani, “Virulensi Nuclear Polyhedrosis Virus (NPV) Terhadap Ulat Grayak (Spodoptera litura F.) (Lepidoptera : Noctuidae) Pada Tanaman Tembakau Deli di Rumah Kaca”, di bawah bimbingan Darma Bakti dan Maryani Cyccu Tobing. Penelitian ini bertujuan untuk mengetahui virulensi Nuclear Polyhedrosis Virus (NPV) terhadap ulat grayak pada tanaman tembakau Deli di rumah kaca. Penelitian ini dilaksanakan di Balai Penelitian Tembakau Deli PTPN II Sampali Medan pada bulan Mei-September 2012. Metode yang digunakan adalah Rancangan Acak Lengkap (RAL) Faktorial terdiri dari stadia larva (Instar 2 dan 4), dan banyaknya suspensi larva terinfeksi virus (10, 20, dan 30 ekor larva terinfeksi virus/1 liter air) dengan tiga ulangan.
Hasil penelitian menunjukkan persentase mortalitas tertinggi (91,67%)
terdapat pada perlakuan instar 2 dengan suspensi 30 ekor larva terinfeksi virus/1 liter air dan terendah pada perlakuan kontrol (0%). Intensitas serangan
tertinggi (33,06%) pada perlakuan kontrol dan terendah pada perlakuan suspensi 30 ekor larva terinfeksi virus/1 liter air (15,58%). Periode inkubasi tercepat pada perlakuan instar 4 yaitu 1,67 hari dan suspensi 30 ekor larva terinfeksi virus/1 liter air yaitu 1,83 hari sedangkan paling lama pada perlakuan instar 2 yaitu 2,58 hari dan kontrol tidak ada menunjukkan gejala.
RIWAYAT HIDUP
Ade Sartika Rimadhani, lahir pada tanggal 31 Maret 1990 di Tanjung
Balai, putri dari Ayahanda Hermanto dan Ibunda Fitrinasari Siregar. Penulis
merupakan anak pertama dari empat bersaudara.
Pendidikan dan Pengalaman
1. Lulus dari Sekolah Dasar Negeri 112265 Damuli Kebun pada tahun 2002
2. Lulus dari SMP Negeri 2 Kualuh Selatan pada tahun 2005
3. Lulus dari SMA Negeri 1 Kualuh Selatan pada tahun 2008
4. Pada tahun 2008 diterima di Fakultas Pertanian Universitas Sumatera
Utara, Departemen Agroekoteknologi melalui jalur PMP.
5. Tercatat sebagai anggota IMAPTAN (Ikatatan Mahasiswa Perlindungan
Tanaman) Departemen FP-USU tahun 2008-2012
6. Tahun 2010/2011, 2011/2012 sebagai asisten Laboratorium Dasar
Perlindungan Tanaman Sub Hama Departemen Ilmu Hama dan Penyakit
Tumbuhan FP USU.
7. Pernah mengikuti seminar seperti:
- Anggota Komunikasi Muslim HPT (KOMUS HPT) 2008-2012
- Seminar nasional dan Rapat Tahunan BKS-PTN Wilayah Barat Bidang
Ilmu Pertanian tahun 2012
- Seminar Pengembangan Perkebunan Kelapa Sawit Berkelanjutan,
- Seminar optimalisasi Sistem Pertanian Untuk Menekan Dampak
Perubahan Iklim Guna Terwujudnya Pertanian Berkelanjutan tahun
2010
- Seminar Ketahanan Pangan Nasional di Medan pada tahun 2011.
- Seminar Police Goes To Campus di USU Medan tahun 2011.
- Mengikuti Praktek Kerja Lapang (PKL) di PT PP London Sumatera
Unit Kebun Bah Lias Kab. Simalungun pada bulan Juli 2011.
- Melaksanakan penelitian skripsi di Balai Penelitian Tembakau Deli
KATA PENGANTAR
Puji dan syukur penulis ucapkan kehadirat Tuhan Yang Maha Esa atas
berkat dan rahmat-Nya penulis dapat menyelesaikan skripsi ini tepat pada
waktunya.
Adapun judul skripsi ini adalah “Virulensi Nuclear Polyhedrosis Virus Terhadap Ulat Grayak (Spodoptera litura F.) (Lepidoptera : Noctuidae) Pada Tanaman Tembakau Deli di Rumah Kaca” yang merupakan salah satu
syarat untuk dapat meraih gelar sarjana di Program Studi Agroekoteknologi
Fakultas Pertanian Universitas Sumatra Utara, Medan.
Pada kesempatan ini penulis mengucapkan terima kasih kepada
Komisi Pembimbing Prof. Dr. Ir. Darma Bakti, M. S., selaku Ketua dan
Prof. Dr. Dra. Maryani Cyccu Tobing, M. S., selaku Anggota
yang telah membantu penulis dalam menyelesaikan skripsi ini.
Penulis juga tidak lupa mengucapkan terima kasih kepada seluruh staf
Balai Penelitian Tembakau Deli (BPTD) PT. Perkebunan Nusantara 2 Sampali,
yang telah memberikan tempat dan fasilitas untuk pelaksanaan penelitian ini.
Penulis menyadari bahwa skripsi ini masih jauh dari sempurna. Oleh karena
itu penulis mengharapkan kritik dan saran yang bersifat membangun demi
kesempurnaan tulisan ini.
Akhir kata penulis mengucapkan terima kasih. Semoga skripsiini dapat
bermanfaat bagi pihak yang membutuhkan.
Medan, Oktober 2012
DAFTAR ISI
Mekanisme Infeksi dan Gejala Serangan Serta Penyebaran NPV ... 11
Faktor-Faktor Yang Mempengaruhi Keberhasilan Virus ... 14
BAHAN DAN METODE Tempat dan Waktu Percobaan ... 16
Bahan dan Alat ... 16
Metode Penelitian ... 16
Pelaksanaan Penelitian ... 18
Periode Inkubasi Larva (Hari) ... 22
HASIL DAN PEMBAHASAN
Persentase Mortalitas (%) ... 23 Intensitas Serangan (%) ... 26 Periode Inkubasi Virus Dalam Tubuh Larva (Hari) ... 28
KESIMPULAN DAN SARAN
Kesimpulan ... 30 Saran ... 31
DAFTAR TABEL
No. Judul Hlm
1. Beda Uji Rataan Pengaruh Stadia Larva Terhadap Persentase
Mortalitas (%) ... 22
2. Beda Uji Rataan Pengaruh Banyaknya Suspensi Larva Yang
Terinfeksi Virus Terhadap Persentase Mortalitas (%) ... 23
3. Beda Uji Rataan Persentase Interaksi Antara Stadia Larva dan
Banyaknya Suspensi Larva Yang Terinfeksi Virus ... 24
4. Beda Uji Rataan Pengaruh Banyaknya Supensi Larva Yang Terinfeksi Virus Terhadap Intensitas Serangan (%) ... 26
5. Beda Uji Rataan Pengaruh Stadia Larva Terhadap Periode Inkubasi Virus dalam Tubuh Larva ... 24
6. Beda Uji Rataan Pengaruh Banyaknya Suspensi Larva Yang
DAFTAR GAMBAR
No. Judul Hlm
1. Telur S. litura ... 5
2. Larva S. litura ... 6
3. Pupa S. litura ... 6
4. Imago S.litura ... 7
5. Gejala serangan S. litura ... 7
6. Diagram inclusion bodies NPV ... 8
7. Mekanisme infeksi NPV ... 9
DAFTAR LAMPIRAN
No. Judul Hlm
1. Bagan Penelitian ... 33
2. Deskripsi Tanaman Tembakau Deli ... 34
3. Foto Penelitian ... 35
4. Persentase Mortalitas ... 38
5. Intensitas Serangan ... 42
ABSTRACT
Ade Sartika Rimadhani, ”The Virulence of Nuclear Polyhedrosis Virus
(NPV) of Larvae Tobacco Caterpillar (Spodoptera litura F.) (Lepidoptera : Noctuidae) On Deli Tobacco In Glasshouse”, under supervised by
Darma Bakti and Maryani Cyccu Tobing. This research was to study the virulence of NPV of larvae S. litura on Deli tobacco in Glasshouse. This research was
carried out at Central Research Deli Tobacco Sampali PTPN II Medan since May-September 2012. The method of this research was Randomized Complete
Design Factorial which consists stages of larvae (2nd and 4th instar) and the number of virus suspenses (10, 20, and 30 larvae infected virus/1 l water) with three replication.
The result showed that highest percentage mortality (91,67%) was found in treatment 2nd instar with suspense 30 larvae infected virus/1 l water and the lowest percentage (0%) on control. The highest percentage of damage intensity (33,06%) was control and the lowest percentage (15,58%) on suspense 30 larvae infected virus/1 l water. The fastest incubation period (1,67 days) in the treatment 4th instar are 1,67 days and suspense of 30 larvae infected virus/1 l water are 1,83 days and the lowest in the treatment 2nd instar are 2,58 days and control didn’t showed symptoms infection.
ABSTRAK
Ade Sartika Rimadhani, “Virulensi Nuclear Polyhedrosis Virus (NPV) Terhadap Ulat Grayak (Spodoptera litura F.) (Lepidoptera : Noctuidae) Pada Tanaman Tembakau Deli di Rumah Kaca”, di bawah bimbingan Darma Bakti dan Maryani Cyccu Tobing. Penelitian ini bertujuan untuk mengetahui virulensi Nuclear Polyhedrosis Virus (NPV) terhadap ulat grayak pada tanaman tembakau Deli di rumah kaca. Penelitian ini dilaksanakan di Balai Penelitian Tembakau Deli PTPN II Sampali Medan pada bulan Mei-September 2012. Metode yang digunakan adalah Rancangan Acak Lengkap (RAL) Faktorial terdiri dari stadia larva (Instar 2 dan 4), dan banyaknya suspensi larva terinfeksi virus (10, 20, dan 30 ekor larva terinfeksi virus/1 liter air) dengan tiga ulangan.
Hasil penelitian menunjukkan persentase mortalitas tertinggi (91,67%)
terdapat pada perlakuan instar 2 dengan suspensi 30 ekor larva terinfeksi virus/1 liter air dan terendah pada perlakuan kontrol (0%). Intensitas serangan
tertinggi (33,06%) pada perlakuan kontrol dan terendah pada perlakuan suspensi 30 ekor larva terinfeksi virus/1 liter air (15,58%). Periode inkubasi tercepat pada perlakuan instar 4 yaitu 1,67 hari dan suspensi 30 ekor larva terinfeksi virus/1 liter air yaitu 1,83 hari sedangkan paling lama pada perlakuan instar 2 yaitu 2,58 hari dan kontrol tidak ada menunjukkan gejala.
PENDAHULUAN
Latar Belakang
Tembakau Deli saat ini masih menjadi primadona tembakau cerutu, yang
kegunaannya lebih diutamakan untuk pembungkus cerutu. Daun tembakau Deli
dikenal sebagai pembungkus cerutu nomor satu di dunia, sehingga tetap
dibutuhkan oleh pabrik penghasil cerutu berkualitas tinggi (Erwin, 2000).
Gangguan hama dan penyakit pada tembakau Deli merupakan salah satu
masalah penting yang senantiasa dihadapi pada setiap musim tanam tembakau.
Gangguan ini dapat menimbulkan kerugian yang cukup besar, tidak saja terhadap
produksi tetapi juga terhadap kualitas tembakau itu sendiri. Seperti di ketahui
bahwa tembakau Deli harus dapat memenuhi beberapa persyaratan kualitas
anatara lain daun harus utuh, memiliki rasa dan aroma yang baik, warna terang
dan rata dengan daya bakar yang baik. Untuk memenuhi persyaratan di atas,
sangat bergantung pada banyak faktor, antara lain faktor lingkungan yaitu iklim
dan tanah dan faktor teknis yang perlu mendapat perhatian terus adalah
pengendalian hama dan penyakit (Abidin, 2004).
Tembakau cerutu merupakan komoditas strategis bagi Indonesia. Adanya
serangan hama seperti pemakan daun, Helicoverpa spp., Spodoptera litura, dan
Myzus persicae, dapat menghilangkan hasil di Deli sebesar 30-40% dan di Besuki sebesar 15-25%. Pengendalian hama secara kimia dengan penyemprotan
Ulat grayak (S. litura) (Lepidoptera : Noctuidae) merupakan salah satu hama daun penting tembakau karena mempunyai kisaran inang yang luas
(polypagus) dan menjadi hama penting di India (Trang dan Chaudari, 2002).
Sampai saat ini, sebagian besar petani mengendalikan ulat grayak
dengan mengandalkan insektisida yang diaplikasikan dengan dosis yang
cenderung berlebihan sehingga berpotensi menimbulkan dampak negatif
terhadap lingkungan. Oleh karena itu, pemerintah telah mencanangkan
arah kebijakan peningkatan keseimbangan ekosistem dan Pengendalian
Hama Terpadu (PHT) dengan menerapkan teknologi pengendalian hama
berwawasan lingkungan, antara lain dengan memanfaatkan patogen
serangga (Kemtan, 2009).
Pengurangan penggunaan pestisida di areal pertanian menuntut
tersedianya cara pengendalian lain yang aman dan ramah lingkungan, diantaranya
dengan memanfaatkan musuh alami, seperti entomopatogen, serangga predator,
dan parasitoid (Trizelia dkk, 2011).
Pengendalian Hama Terpadu (PHT) merupakan pendekatan ekosistem
terhadap produksi dan perlindungan tanaman yang menggabungkan strategi
pengendalian yang berbeda dan praktek untuk menanam tanaman yang sehat
dengan meminimalkan penggunaan pestisida (FAO, 2012).
Pengendalian hayati merupakan salah satu metode pengendalian hama
yang diminati akhir- akhir ini karena memiliki keunggulan. Diantaranya adalah
sifatnya yang ramah lingkungan, dapat menghemat biaya dan diharapkan dapat
Beberapa keuntungan pengendalian hama dengan menggunakan agens hayati
seperti yang dikemukakan oleh Steinhaus (1956) dalam Hall (1973) antara lain: 1) patogen serangga tidak mencemari lingkungan, 2) sebagian besar patogen
tingkat spesifikasinya relatif tinggi sehingga cenderung melindungi serangga
berguna, 3) beberapa patogen dapat bersifat sinergis, 4) relatif lebih murah
dibandingkan insektisida sintetis dan beberapa patogen dapat diproduksi sendiri,
5) pengaruh mikrobial patogen terhadap resistensi inangnya lambat dan 6) dosis
yang dibutuhkan dalam pengendalian rendah (Trisnaningsih dan Arifin, 2008).
Beberapa patogen serangga (jamur, bakteri, virus dan nematoda) telah
digunakan untuk mengendalikan ulat grayak pada tanaman kedelai, tembakau dan
kapas (Trisnaningsih dan Arifin, 2008).
Virus entomopatogen sebagian besar masuk kedalam 5 genera virus yaitu
Baculovirus, Poxvirus, Iridovirus, Enterovirus, dan Rhabdovirus. Dari kelima
genera ini genus Baculovirus yang terpenting karena termasuk didalamnya
kelompok virus terbesar yaitu NPV (Nuclear Polyhedrosis Virus) yang banyak
digunakan sebagai agens hayati (Untung, 1993).
NPV merupakan patogen yang berpotensi tinggi dan berpeluang besar
untuk dikembangkan sebagai bioinsektisida yang ramah lingkungan dan efektif
(Arifin dan Desti, 2001)
NPV dapat dijadikan sebagai agensia pengendalian hayati, sesuai dengan
prinsip PHT karena (a) memiliki inang spesifik terutama ulat grayak dan beberapa
jenis serangga Noctuidae lainnya, (b) tidak mempengaruhi predator dan
parasitoid, dan tidak membahayakan serangga bukan sasaran, manusia, dan
insektisida kimia (Starnes dkk, 1993). Berdasarkan potensi biotik dan manfaat
NPV tersebut, maka NPV layak untuk dikembangkan sebagai insektisida mikrobia
(Arifin, 1994).
Tujuan Penelitian
Untuk mengetahui virulensi NPV terhadap ulat grayak pada tanaman
tembakau Deli di rumah kaca.
Hipotesis Penelitian
NPV efektif untuk menginfeksi dan mengendalikan larva ulat grayak pada
instar tertentu.
Kegunaan Penelitian
1. Sebagai salah satu syarat untuk dapat melakukan penelitian di Program Studi
Agroekoteknologi Fakultas Pertanian Universitas Sumatera Utara, Medan.
TINJAUAN PUSTAKA
Biologi Spodoptera litura (Lepidoptera : Noctuidae)
Ulat grayak (Spodoptera litura F.) merupakan salah satu hama daun yang penting karena mempunyai kisaran inang yang luas meliputi kedelai, kacang
tanah, kubis, ubi jalar, kentang, dan lain-lain. S. litura menyerang tanaman budidaya pada fase vegetatif yaitu memakan daun tanaman yang muda sehingga
tinggal tulang daun sajaa (Laoh dkk, 2003).
Kerusakan yang disebabkan oleh ulat grayak pada tanaman tembakau
mencapai 40 – 50% atau tanaman tembakau tidak bisa dipanen daunnya
(BPTD, 2004).
Telur diletakkan secara berkelompok pada helaian daun sebelah bawah
dengan jumlah 250-300 butir. Telur ditutupi jaringan halus warna putih
kekuningan. Koloni telur berwarna cokelat kekuningan (Gambar 1).
Gambar 1. Telur S. Litura
Sumber: Foto Langsung
Larva yang baru keluar dari kelompok telur pada mulanya bergerombol
sampai instar ketiga. Larva berwarna hijau kelabu hitam. Larva terdiri 5-6 instar.
(Gambar 2) (BPTD, 2004).
a. b.
Gambar 2. Larva S. Litura a. Instar 2 dan b. Instar 4 Sumber: Foto Langsung
Lama stadia larva 17-26 hari, yang terdiri dari larva instar 1 antara
5-6 hari, instar 2 antara 3-5 hari, instar 3 antara 3-6 hari, instar 4 antara 2-4 hari,
dan instar 5 antara 3-5 hari (Cardona dkk, 2007).
Pupa berada di dalam tanah atau pasir. Pupa berbentuk oval memanjang
dan berwarna cokelat mengkilat. Pupa memiliki panjang dan lebar antara
22,29 + 0,7 mm dan 7,51 + 0,36 mm, lama stadia pupa 9-14 hari
(Cardona dkk, 2007) (Gambar 3).
Gambar 3. Pupa S. Litura
Imago jantan dan betina memiliki rambut harus pada tubuhnya. Betina
berwarna coklat pucat sedangkan jantan berwarna lebih gelap. Ukuran tubuh
betina lebih besar dengan abdomen yang besar sedangkan jantan lebih sempit
dengan bagian ujung abdomen runcing (Gambar 4) (Cardona dkk, 2007).
a b
Gambar 4. Imago S. Litura a. Betina dan b. Jantan
Sumber
Ngengat aktif pada malam hari dan serangga betina bila meletakkan telur
dalam bentuk paket dan satu paket bisa mencapai 200-300 butir. Seekor betina
bisa meletakkan telur mencapai 800-1000 butir. Dan lama masa hidup imago 5-9
hari. Lama siklus dari hama ini adalah 24-41 hari (Subandrijo dkk, 1992).
Gejala Serangan S. litura
Hama ini merusak tanaman tembakau pada stadia larva, yang memakan
daun tembakau mulai dari bibitan sampai ke pertanaman di lapangan. Serangan
hama ini berlangsung pada malam hari. Akibat serangan ini daun-daun akan
berlubang-lubang sehingga daun tembakau menjadi tidak utuh, dan secara
langsung akan menurunkan rendemen cerutu dari setiap daun yang rusak
(Abidin, 2004). Kerusakan daun yang diakibatkan larva yang masih kecil merusak
daun dengan meninggalkan sisa-sisa epidermis bagian atas, transparan dan tinggal a
tulang-tulang daun saja. Larva instar lanjut merusak tulang daun. Pada serangan
berat menyebabkan gundulnya tanaman (Gambar 5) (Sudarmo, 1992)
Gambar 5. Gejala serangan S. Litura
Sumber: Foto Langsung
Serangan yang ditimbulkan akan kelihatan daun transparan karena daging
daun habis dimakan. Pada instar ke-4 dan ke-5 larva menyebar ketanaman
didekatnya terutama bila daun untuk dimakan sudah berkurang (BPTD, 2004).
Nuclear Polyhedrosis Virus (NPV)
Famili Baculoviridae terdiri dari dua generaasi yaitu Nucleopolyhedrosis
virus biasanya dikenal dengan NPV dan Granular Virus biasanya dikenal dengan
GV. NPV saat ini mempunyai lebih dari 100 isolat dan sangat efektif tetapi
sebatas hanya untuk serangga-serangga Lepidoptera (Hall dan Menn, 1999). NPV
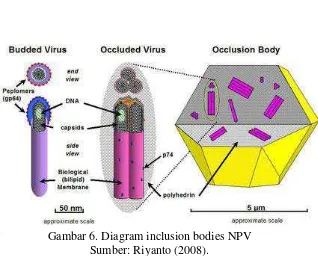
berbentuk batang dan terdapat di dalam inclusion bodies yang disebut polihedra. Polihedra berbentuk kristal bersegi banyak dan terdapat di dalam inti sel yang
rentan dari serangga inang, seperti hemolimfa, hipodermis, dan matriks trakea.
Polihedra berukuran 0,5-15 µm dan mengandung partikel virus yang disebut
virion. Virion berbentuk batang, berukuran 40-70 nm X 250-400 nm, dan berisi
yang mengandung beberapa nukleokapsid disebut multiply-enveloped NPV (Payne dan Kelly 1981). Morfologi polihedra dan virion dapat dilihat di bawah
mikroskop elektron dengan pengecatan negatif atau dengan teknik irisan jaringan
yang terinfeksi NPV (Gambar 6) (Arifin, 2011).
Pembentukan Occlusion body yang umum dalam virus serangga yang
spesifik (Baculovirus dan Cypovirus), dan struktur ini berfungsi untuk melindungi
partikel virus dari lingkungan ekstrim selama masa transmisi. Sehingga NPV
berpotensi sebagai agens pengendalian hayati (Miller dan Andrew, 1998).
Rekombinan NPV merupakan vektor yang efisien untuk tingkat tinggi
ekspresi gen asing dalam penelitian dasar dan aplikasi medis
(Kamita dan Maeda, 1993). NPV adalah salah satu jenis virus patogen yang
berpotensi sebagai agensia hayati dalam mengendalikan ulat grayak, karena
bersifat spesifik, selektif, efektif untuk hama-hama yang telah resisten terhadap
insektisida dan aman terhadap lingkungan. Hasil penelitian di lapangan
menunjukkan bahwa kerusakan buah kapas akibat hama Helicoverpa armigera
mampu ditekan sampai 5,6% setelah diplikasikan di NPV dibandingkan dengan
kontrol mencapai 11,53% (Gothamdkk, 1990 ; Indrayani dkk, 1998). Efektivitas
NPV dalam mengendalikan S. litura dipengaruhi oleh beberapa faktor salah satunya adalah perbedaan tingkat instar S. litura Okada (1977 dalam Soekarna 1985). Masing-masing tingkat larva S. litura mempunyai kerentanan yang berbeda terhadap NPV (Laoh dkk, 2003).
NPV pada umumnya menyerang paling banyak pada ordo Lepidoptera
(86%) dan sedikit pada ordo Hymenoptera (7%) serta ordo Diptera (3%).
Berbagai virus NPV mempunyai prospek untuk digunakan dalam pengendalian
hayati. NPV telah diisolasi dari berbagai semua serangga seperti Spodoptera,
Helicoverpa (Heliothis), Trichoplusia, Plusia, Pectinophora, Neodiprion,
Melacosoma, Agrotis, Chilo, dll. Genus serangga tersebut merupakan hama
penting pada berbagai tanaman di Indonesia (Untung, 1993). Aizawa (1987 dalam
Sutarya 1995), membuktikan bahwa aplikasi virus yang semakin tinggi
konsentrasinya akan mengakibatkan makin banyaknya polihedra virus yang
tertelan dan akan makin banyak jaringan larva yang terinfeksi virus sehingga akan
mempercepat kematian larva. Sebaliknya pada konsentrasi virus yang rendah akan
memperpanjang periode laten bagi virus dalam tubuh serangga (Laoh dkk, 2003).
Virus memperbanyak diri dalam tubuh di dalam sel inang atau dalam
tubuh larva dengan memanfaatkan protein yang terdapat dalam tubuh larva yang
dihasilkan melalui sintesa metabolisme dan bahan organik didalam sel. Virus
khususnya famili Baculoviridae peka terhadap faktor fisik yaitu UV dan suhu
tinggi. NPV merupakan salah satu patogen berstatus musuh alami yang
antara lain (a) memiliki inang spesifik, (b) tidak membahayakan serangga bukan
sasaran, manusia, dan lingkungan, (c) dapat mengatasi masalah keresistensian ulat
grayak terhadap insektisida, dan (d) kompatibel dengan komponen PHT lainnya,
termasuk insektisida (Arifin, 2011).
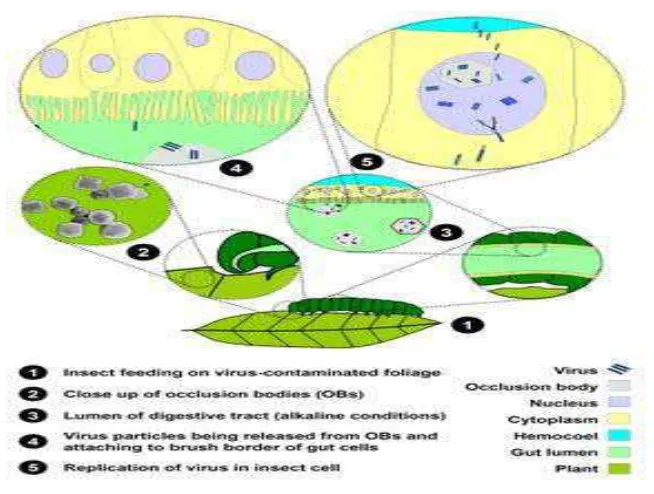
Mekanisme Infeksi dan Gejala Serangan Serta Penyebaran NPV
Proses infeksi NPV dimulai dari tertelannya polihedra oleh larva bersama
pakan. Di dalam saluran pencernaan yang bersuasana alkalis (pH 9,0 - 10,5),
selubung polihedra larut, sehingga membebaskan virion. Virion menembus
dinding saluran pencernaan untuk masuk ke rongga tubuh, kemudian menginfeksi
sel-sel yang rentan (Gambar 7). Replikasi virion terjadi di dalam inti sel
(Arifin, 2011).
Gambar 7. Mekanisme infeksi NPV Sumber: Riyanto (2008)
Dalam waktu 1-2 hari setelah polihedra tertelan, hemolimfa yang semula
integumen yang membengkak dan perubahan warna tubuh menjadi pucat
kemerahan, terutama pada bagian abdomen. Kemampuan makannya menurun,
sehingga pertumbuhannya lambat. Larva cenderung merayap ke pucuk tanaman
kemudian mati menggantung dengan posisi terbalik dengan tungkai semu bagian
akhir pada tanaman (Gambar 8) (Irfan dkk, 2007).
Gambar 8. Gejala NPV pada larva S. litura
Sumber: Foto Langsung
Integumen larva yang mati mengalami lisis dan disintegrasi, sehingga
sangat rapuh. Apabila integumen robek, dari dalam tubuh larva keluar cairan
hemolimfa berwarna putih kecoklatan yang mengandung polihedra. Larva muda
(instar 1-3) mati dalam 2 hari, sedangkan larva tua (instar 4-6) dalam 4-9 hari
setelah polihedra tertelan (Arifin, 2011).
Apabila virus telah masuk ke dalam tubuh serangga polihedra NPV akan
larut dan pecah serta melepaskan partikel-partikel virus yang kemudian memasuki
sel-sel bagian perut serangga dan kemudian memperbanyak diri. Setiap sel yang
terinfeksi virus nukleusnya membengkak dan dipenuhi oleh masa padat yang
disebut viroplan. Proses perbanyakan nukleokapsid berjalan dengan cepat
tubuh serangga sampai dipenuhinya sel-sel tubuh serangga oleh virus berjalan
antara 4 hari sampai 3 minggu tergantung pada jenis NPV, jenis serangga inang,
jumlah polihedra yang masuk, instar larva yang mulai terinfeksi dan keadaan suhu
(Untung, 1993).
Larva ulat grayak instar 1 sampai 3 lebih peka terhadap NPV daripada
larva instar 4 dan 5. Larva instar 5 menunjukkan ketahanan 100 kali lebih besar
dari pada larva instar 1 (Arifin dan Waskitoe, 2001).
Semakin tinggi konsentrasi virus yang digunakan maka persentase
kematian larva semakin tinggi dan kemampuan larva merusak daun juga menurun
(Poinar dan Gerard, 1984).
NPV tertular melalui kontaminasi pada makanan larva, polihedra dari
larva yang yang terinfeksi virus hancur dan jatuh pada daun kemudian daun
tersebut termakan oleh larva lain. NPV juga terdapat pada larva dewasa jika larva
terserang NPV. Penularan NPV juga dapat terjadi secara transovarial, artinya
induk yang terinfeksi NPV dapat menghasilkan telur yang terkontaminasi NPV
(Laoh dkk, 2003). Larva yang terserang NPV dapat dilihat dari gejala serangan
yang antara lain terlihat larva semakin malas bergerak, pertumbuhannya, kulit
berganti warna semakin pucat dan larva bergerak ke pucuk tanaman. Larva yang
mati karena virus posisi tubuhnya seperti patah dan menggantung pada bagian
tanaman (Untung, 1993).
Adanya kenyataan bahwa NPV berdaya bunuh lambat membawa
konsekuensi kemungkinan terjadinya kerusakan daun. Menurut Tanada dan Kaya
(1993), tingkat kerusakan daun karena NPV ditentukan oleh kemampuan makan,
tertelan oleh larva, makin besar peluang terjadinya infeksi, dan semakin
cepat larva mati. Apabila tingkat kematian larva tinggi, maka total luas daun yang
dimakan larva berkurang, sehingga tingkat kerusakan daun menjadi rendah
(Arifin dan Desti, 1999).
Virus memperbanyak diri di dalam sel inang atau dalam tubuh larva
dengan memanfaatkan protein yang terdapat dalam tubuh larva yang dihasilkan
melalui sintesa metabolisme dan bahan organik didalam sel. Virus khususnya
Baculoviridae peka terhadap faktor fisik yaitu UV dan suhu tinggi
(Drieche dan Bellows, 1996).
Faktor-Faktor yang Mempengaruhi Keberhasilan Virus
Faktor-faktor yang mempengaruhi keberhasilan virus antara lain:
a. Jenis Inang
Kebanyakan virus yang digunakan untuk mengendalikan hama antara lain
NPV dan GV. Virus tersebut telah diuji tetapi hanya efektif pada Lepidoptera
dan tidak efektif pada hewan bertulang belakang. Virus yang telah diuji lebih
jauh tidak secara langsung menginfeksi atau tidak membahayakan parasitoid
hama karena hanya efektif pada inang yang sesuai. Virus yang menyerang
serangga secara khusus menyerang inang yang hanya dari satu genus atau
berhubungan dari genera dari satu famili yang dapat diinfeksi
(Drieche dan Bellows, 1996).
Variabel kemanjuran SlNPV dan mortalitas larva S. litura pada tanaman inang yang berbeda dapat berhubungan dengan metabolit sekunder, enzim,
b. Umur dan Tingkat Instar
Salah satu faktor yang mempengaruhi keberhasilan NPV sebagai pengendali
ini adalah umur atau tingkat instar serangga sasaran tersebut. Okada
(1977 dalam Soekarna 1985) yang melakukan penelitian di Jepang pada
tahun 1977 menemukan perbedaan kepekaan antar instar larva S. litura dan
Leucania separata terhadap NPV. Dari hasil penelitian tersebut dijelaskan bahwa instar I dan II dari kedua jenis larva lebih rentan dibandingkan dengan
instar III, IV, V dan VI (Laoh dkk, 2003).
c. Suhu
NPV relatif tahan terhadap suhu tinggi. Suspensi NPV pada suhu 65OC
selama 20 menit tidak menurun aktivitasnya. Aktivitas NPV mulai menurun
pada suhu 70OC dan menjadi inaktif pada suhu 85OC setelah 5 menit. Suhu
lapang (<45OC) tidak berpengaruh terhadap stabilitas NPV. Meskipun
demikian, replikasi virus mulai dihambat pada suhu 40OC. NPV sebaiknya
disimpan pada suhu rendah. Aktivitas suspensi NPV yang disimpan pada
suhu -20O dan 5OC sangat stabil dan tidak menurun setelah 15 tahun. NPV
yang disimpan pada suhu 37OC selama 4 minggu masih menunjukkan
aktivitasnya(Arifin, 1993).
Untuk penyimpanan jangka pendek (menit atau jam) selama percobaan di
laboratorium atau rumah kaca, adalah inokulum virus dianjurkan disimpan di
atau dekat 00C. Ini biasanya dilakukan dengan tabung berisi inokulum dalam
BAHAN DAN METODE
Tempat dan Waktu Percobaan
Penelitian ini dilaksanakan di Rumah Kaca BPTD (Balai Penelitian
Tembakau Deli), PT. Perkebunan Nusantara II, Sumatera Utara, Medan. Dengan
ketinggian tempat ± 25 m di atas permukaan laut. Penelitian dilaksanakan pada
bulan Mei sampai dengan selesai.
Bahan dan Alat
Bahan yang digunakan dalam penelitian ini antara lain daun tembakau,
Nuclear Polyhedrosis Virus (NPV) yang berasal dari BPTD, larva ulat grayak
(S. litura), akuades, media tanam 3 : 2 : 1 (tanah humus : pasir : pupuk kompos), dan bibit tanaman tembakau varietas F1 – 45 bahan lain yang mendukung
penelitian.
Alat yang digunakan dalam penelitian ini antara lain blender, stoples,
beaker glass, kain muslin, handsprayer, timbangan, polibag, alat tulis dan alat lain
yang mendukung penelitian.
Metode Penelitian
Penelitian ini menggunakan Rancangan Acak Lengkap (RAL) faktorial
yang terdiri dari 2 faktor yaitu:
Faktor I : Stadia Larva
I1 = Larva instar 2
Faktor II : Suspensi larva terinfeksi virus
V0 = Kontrol (Tanpa Perlakuan)
V1 = Suspensi 10 ekor larva terinfeksi virus/liter air
V2 = Suspensi 20 ekor larva terinveksi virus/liter air
V3 = Suspensi 30 ekor larva terinveksi virus/ liter air
Kombinasi perlakuan adalah :
I1V0 I2V0
I1V1 I2V1
I1V2 I2V2
I1V3 I2V3
Banyak ulangan dari masing-masing perlakuan adalah :
t1 (t2 - 1) r ≥ 15
2 (4 – 1) r ≥ 15
6 r ≥ 15
r ≥ 15/6
r ≥ 2,5 r = 3 ulangan
Banyak ulangan adalah 3 ulangan
Kombinasi perlakuan : 8 perlakuan
Jumlah perlakuan : 8 x 3 = 24 perlakuan
Jumlah tanaman per plot : 4 tanaman
Data dianalisis dengan sidik ragam menggunakan model linier :
Yijk = µ + αi + βj+ αβij + ∑ijk
Yijk = Respon atau nilai pengamatan pada perlakuan ke-i dan kelompok ke-j.
µ = Nilai tengah umum
αi = Nilai pengamatan pengaruh perlakuan ke-i
βj = Nilai pengamatan pengaruh kelompok ke-j
αβij = interaksi dari faktor a pada taraf ke i dan faktor b pada taraf ke j
∑ijk = Efek eror karena pengaruh perlakuan pada taraf ke-i, faktor b pada taraf
ke-j dan pada ulangan ke-k
Pelaksanaan Penelitian Perbanyakan Ulat Grayak
Perbanyakan ulat grayak dilakukan dengan cara mengambil sebanyak
mungkin kelompok telur dari pertanaman tembakau. Kelompok telur tersebut
diambil bersamaan dengan daun tembakau. Telur-telur yang menempel pada daun
tembakau tersebut diletakkan pada tempat perbanyakan, kemudian kelompok telur
dibiakkan di tempat tersebut. Perbanyakan hama dilakukan untuk mendapatkan
larva dengan instar yang sama.
Persiapan Pembibitan
Persemaian dibuat dengan bedengan dengan ukuran 1 x 6 m dengan arah
Utara-Selatan. Naungan pembibitan dibuat dengan arah Timur-Barat dan tinggi
Sebelum benih disemaikan tanah diolah sampai gembur kemudian
dibiarkan selama satu minggu. Pada persemaian ditaburkan kompos sebanyak
10 kg secara merata di atas permukaan tanah.
Persiapan Media
Sementara melaksanakan pembibitan, areal pertanaman dibersihkan dari
sisa-sisa tanaman kemudan dibuang. Disiapkan polibag dengan ukuran 15 kg,
kemudian polibag diisi dengan tanah yang sudah disterilkan. Seterusnya dibuat
plot percobaan.
Penanaman
Setelah areal pertanaman selesai dibersihkan dan bibit telah berumur 40
hari maka bibit tersebut dipindahkan ke polibag. Bibit dipindahkan dari
pembibitan, dan waktu penanaman bibit, tanah ditekan sedikit agar tegak
pertumbuhannya dan tidak rebah.
Pemeliharaan
Penyiraman dilakukan setiap hari yaitu pagi hari. Hal ini dilakukan karena
tanaman tembakau pada fase pembibitan memerlukan cukup air untuk
perumbuhannya. Penyiraman dilakukan sampai tahap pertumbuhan.
Penyisipan dilakukan pada tanaman di dalam polybag yang mengalami
kegagalan pertumbuhan. Penyisipan dilakukan pada sore hari yang diambil dari
plot tanaman yang dikhususkan untuk tanaman sisipan. Waktu penyisipan
selambat-lambatnya 2 MST.
Penyiangan gulma dilakukan satu minggu sekali tergantung pada keadaan
Pemupukan yang dilakukan sesuai dengan rekomendasi BPTD
(Balai Penelitian Tanaman Tembakau Deli) Medan yaitu pupuk mixed
(NPK 12,5 : 7,5 : 10), KNO3 dengan dosis 10 gr/tanaman yang diberikan dua kali,
pertama pada saat bibit tembakau akan ditanam ke polibag yang diberikan pada
lubang tanam sebanyak 1/3 (10 gram/lubang tanam), pemupukan kedua dilakukan
pada saat tambah media 1x pada umur 7-10 hari sebanyak 1/3 (10 g/tan) ditabur di
sekitar tanaman (melingkar). Pupuk KNO3 diberikan pada umur tanaman 16-20
hari (pada saat tambah media 2x) sebanyak 1/3 (10 g/tan) diberikan dengan cara
ditabur di sekitar tanaman (dibuat melingkar).
Perbanyakan Virus
Daun tembakau dicelupkan kedalam larutan NPV
(100 gr NPV/liter air). Setelah itu daun tembakau di keringanginkan dalam stoples
berukuran besar, kemudian dimasukkan larva ulat grayak ke dalam stoples. Larva
yang terinfeksi NPV dapat dilihat dari gejala serangan antara lain terlihat larva
berganti warna semakin pucat, larva malas bergerak, nafsu makan menurun
kemudian larva akan mati. Untuk selanjutnya digunakan sebagai sumber virus
bagi larva ulat grayak berikutnya.
Aplikasi Virus
Larva yang terinveksi NPV kemudian disimpan dalam lemari pendingin
sebagai persediaan bahan pembuatan larutan NPV untuk keperluan perlakuan
dalam percobaan. Larva yang terinfeksi diambil sesuai perlakuan kemudian
dihaluskan dengan blender lalu dicampur air 100 ml, disaring dengan kain muslin.
masing-masing tanaman diletakkan 5 ekor larva. Aplikasi virus dilakukan terhadap larva
instar 2 dan 4.
Peubah Amatan
Persentase Mortalitas (%)
Pengamatan terhadap ulat grayak yang mati dilakukan setiap hari setelah
satu hari aplikasi. Persentase mortalitas dilakukan dengan menghitung larva yang
mati dengan menggunakan rumus:
M
=
aa+b
�
100%
Keterangan:
M = Persentase mortalitas Larva S. litura
a = Jumlah S. litura yang mati b =Jumlah S. litura yang hidup
(Laoh dkk, 2003)
Intensitas Serangan (%)
Pengamatan dilakukan dengan mengamati persentase serangan hama dari
ulat grayak dengan menggunakan rumus :
IS
=
∑(nxv )NxZ
�
100%
Dimana:
IS = Intensitas Serangan hama (%)
n = Jumlah daun rusak tiap kategori serangan
v = Nilai skala tiap kategori terserang
Z = Nilai skala tertinggi kategori serangan
Nilai skala dapat dikategorikan sebagai berikut:
0 = Daun sehat tidak ada serangan
1 = > 0-25 % yang terserang dari jumlah daun yang diamati
2 = > 25-50 % yang terserang dari jumlah daun yang diamati
3 = > 50-75 % yang terserang dari jumlah daun yang diamati
4 = > 75-100% yang terserang dari jumlah daun yang diamati
(BPTD, 2004).
Periode Inkubasi Virus Dalam Tubuh Larva (Hari)
Pengamatan dilakukan setiap hari dengan menghitung waktu yang
HASIL DAN PEMBAHASAN
1. Persentase Mortalitas Larva S. litura (%)
Dari hasil sidik ragam dapat dilihat bahwa stadia larva yang diaplikasikan
sangat berpengaruh nyata terhadap persentase mortalitas larva (%). Hal ini dapat
dilihat pada Tabel 1 dan Lampiran 1.
Tabel 1. Persentase mortalitas larva S. litura dari dua instar yang berbeda (%)
Perlakuan Rataan
I1 (larva instar 2) 49,08 a
I2 (larva nstar 4) 16,25 b
Keterangan: Angka yang diikuti oleh notasi huruf yang berbeda menunjukkan data berbeda nyata menurut Uji Jarak Duncan pada taraf 5%.
Tabel 1 menunjukkan bahwa persentase mortalitas larva tertinggi
(49,08%) terdapat pada perlakuan I1 (larva instar 2) dan persentase terendah
(16,25%) terdapat pada perlakuan I2 (larva instar 4). Perbedaan persentase
mortalitas ini menunjukkan bahwa larva instar 2 lebih peka terhadap perlakuan
dengan NPV dibandingkan dengan larva instar 4. Hasil penelitian ini tidak
berbeda dengan penelitian yang dilakukan oleh Laoh dkk (2003) bahwa tingginya
mortalitas larva pada instar 2 dibandingkan dengan instar 3 dan 4 karena larva
instar 2 lebih muda sehingga lebih rentan terhadap NPV dibandingkan dengan
instar larva 3 dan 4. Selanjutnya, Salama dan Sharaby (1986 dalam
Gothama dkk 1990) menyatakan bahwa pada organ tubuh larva muda, terutama
saluran pencernaan bagian tengah yang merupakan sasaran utama karena masih
lemah, sehingga NPV lebih mudah menembus organ tersebut dan merusak sel-sel
yang rentan. Sedangkan pada larva instar tua kepekaan larva berkurang sejalan
pertumbuhan larva, organ-organ dan jaringan tubuh larva mengalami
perkembangan dan diferensiasi. Saluran pencernaan, lapisan kitin peritrofik dan
integumen makin tebal dan kuat, sehingga makin sulit ditembus oleh NPV.
Dari hasil sidik ragam dapat dilihat bahwa banyaknya suspensi larva
S. litura yang terinfeksi virus NPV sangat berpengaruh nyata terhadap persentase mortalitas larva S. litura (%). Hal ini dapat dilihat pada Tabel 2 dan Lampiran 1. Tabel 2. Banyaknya suspensi larva S. litura yang terinfeksi virus NPV
Perlakuan Rataan
V0 (kontrol) 0 d
V1 (suspensi 10 ekor larva terinfeksi virus/liter air) 28,33 c
V2 (suspensi 20 ekor larva terinfeksi virus/liter air) 38,17 b
V3 (suspensi 30 ekor larva terinfeksi virus/liter air) 64,17 a
Keterangan: Angka yang diikuti oleh notasi huruf yang berbeda menunjukkan data berbeda nyata menurut Uji Jarak Duncan pada taraf 5%.
Tabel 2 menunjukkan bahwa banyaknya suspensi larva yang terinfeksi
virus terhadap persentase mortalitas larva yang tertinggi (64,17%) terdapat pada
perlakuan V3 (suspensi 30 ekor larva terinfeksi virus/liter air) dan persentase
terendah (0%) terdapat pada perlakuan V0 (kontrol). Hal ini menunjukkan bahwa
perlakuan V3 (suspensi 30 ekor larva terinfeksi virus/liter air) lebih efektif
dibandingkan dengan perlakuan lain karena pada perlakuan tersebut konsentrasi
virus/liter air tinggi sehingga semakin tinggi konsentrasi virus semakin tinggi
kematian larva hal ini disebabkan banyaknya polyhedra virus yang tertelan oleh
larva. Hal ini sesuai dengan pernyataan Aizawa (1977 dalam Arifin, 2011) membuktikan bahwa aplikasi virus yang semakin tinggi konsentrasinya akan
mengakibatkan makin banyaknya polihedra virus yang tertelan dan akan makin
larva. Sebaliknya pada konsentrasi virus yang rendah akan memperpanjang
periode laten bagi virus dalam tubuh serangga.
Dari hasil sidik ragam dapat dilihat bahwa interaksi antara stadia larva
S. litura dengan banyaknya suspensi larva S. litura yang terinfeksi virus NPV sangat berpengaruh nyata terhadap persentase mortalitas larva (%). Hal ini dapat
dilihat pada Tabel 3 dan Lampiran 1.
Tabel 3. Persentase interaksi stadia larva S. litura dan banyaknya suspensi larva terinfeksi virus NPV (%)
Perlakuan Rataan
I1V0 dan I2V0 (kontrol) 0 g
I1V1(suspensi 10 ekor larva yang terinfeksi virus terhadap instar 2) 45,00 c
I1V2(suspensi 20 ekor larva yang terinfeksi virus terhadap instar 2) 59,67 b
I1V3(suspensi 30 ekor larva yang terinfeksi virus terhadap instar 2) 91,67 a
I2V1(suspensi 10 ekor larva yang terinfeksi virus terhadap instar 4) 11,67 f
I2V2(suspensi 20 ekor larva yang terinfeksi virus terhadap instar 4) 16,67 e
I2V3(suspensi 30 ekor larva yang terinfeksi virus terhadap instar 4) 36,67 d
Keterangan: Angka yang diikuti oleh notasi huruf yang berbeda menunjukkan data berbeda nyata menurut Uji Jarak Duncan pada taraf 5%.
Tabel 3 menunjukkan bahwa persentase mortalitas tertinggi (91,67%) dari
interaksi stadia larva dengan banyaknya suspensi larva yang terinfeksi virus
terdapat pada perlakuan I1V3 (suspensi 30 ekor larva yang terinfeksi virus
terhadap instar 2) dan persentase terendah (0%) terdapat pada perlakuan I1V0 dan
I2V0 (kontrol) sebesar 0%. Hal ini dapat terjadi karena konsentrasi virus pada
perlakuan I1V3 (suspensi 30 ekor larva yang terinfeksi virus terhadap instar 2)
lebih tinggi dibandingkan dengan perlakuan yang lain, dan pada perlakuan ini
stadia larva yang diaplikasikan virus adalah instar 2 yang memiliki daya tahan
lebih rendah dalam menanggapi patogen NPV. NPV dengan konsentrasi tinggi
rendah terhadap larva instar 4, terbukti pada perlakuan I1V3 (suspensi 30 ekor
larva yang terinfeksi virus terhadap instar 2). Hal ini sesuai dengan pernyataan
Poinar dan Gerard (1984) bahwa semakin tinggi konsentrasi virus yang digunakan
maka persentase kematian larva semakin tinggi. Selanjutnya, Arifin (2011)
menyatakan bahwa larva instar 1 sampai 3 lebih peka terhadap NPV dari pada
larva instar 4 dan 5, sedangkan larva instar 5 menunjukkan ketahanan 100 kali
lebih besar daripada larva instar 1.
2. Intensitas Serangan (%)
Dari hasil sidik ragam dapat dilihat bahwa banyaknya suspensi larva
S. litura yang terinfeksi virus NPV sangat berpengaruh nyata terhadap intensitas serangan (%). Hal ini dapat dilihat dari Tabel 4 dan Lampiran 2.
Tabel 4. Banyaknya suspensi larva S. litura yang terinfeksi virus NPV
Perlakuan Rataan
V0 (kontrol) 33,06 a
V1 (suspensi 10 ekor larva terinfeksi virus/liter air) 25,25 b
V2 (suspensi 20 ekor larva terinfeksi virus/liter air) 20,07 c
V3 (suspensi 30 ekor larva terinfeksi virus/liter air) 15,58 d
Keterangan: Angka yang diikuti oleh notasi huruf yang berbeda menunjukkan data berbeda nyata menurut Uji Jarak Duncan pada taraf 5%.
Tabel 4 menunjukkan intensitas serangan hama S. litura tertinggi (33,06%) terdapat pada perlakuan V0 (kontrol) dan terendah (15,58%) dalam
perlakuan V3 (suspensi 30 ekor larva yang teinfeksi virus/liter air). Perlakuan V0
(kontrol) bisa mencapai nilai tertinggi karena pada perlakuan V0 (kontrol) tidak
diaplikasikan virus sehingga larva yang diaplikasikan dapat tumbuh dengan baik
dan dapat memakan daun tembakau lebih banyak tanpa ada yang terinfeksi virus.
nilai intensitas yang rendah. Hal ini dikarenakan dalam perlakuan V3 (suspensi 30
ekor larva terinfeksi virus/liter air) konsentrasi virus yang terkandung/liter air
sangat tinggi sehingga apabila termakan larva akan terinfeksi virus. Sehingga
perlakuan V3 (suspensi 30 ekor larva terinfeksi virus/liter air) lebih efektif dalam
menurunkan kerusakan pada daun. Hal ini sesuai dengan pernyataan
Trisnaningsih dan Arifin (2008) bahwa NPV yang efektif dan efisien ditentukan
berdasarkan kriteria: tingkat kematian larva minimal yang mencapai 70%, dan
tingkat kerusakan daun yang diakibatkan oleh larva yang bertahan hidup relatif
rendah. Selanjutnya, Arifin dan Desti (1999) menyatakan bahwa makin banyak
polihedra yang tertelan larva, makin besar peluang terjadinya infeksi, dan semakin
cepat larva mati. Apabila tingkat kematian larva tinggi, maka total luas daun yang
dimakan larva berkurang, sehingga tingkat kerusakan daun menjadi rendah.
3. Periode Inkubasi (Hari)
Dari analisis sidik ragam dapat dilihat bahwa stadia larva S. litura sangat berpengaruh nyata terhadap waktu munculnya gejala infeksi awal atau periode
inkubasi (hari). Hal ini dapat dilihat pada Tabel 5 dan Lampiran 2.
Tabel 5. Periode inkubasi pada stadia larva S. litura yang berbeda (hari)
Perlakuan Rataan
I1 (larva instar 2) 2.58 a
I2 (larva instar 4) 1.67 a
Keterangan: Angka yang diikuti oleh notasi huruf yang berbeda menunjukkan data berbeda nyata menurut Uji Jarak Duncan pada taraf 5%.
Tabel 5 menunjukkan hari muncul gejala awal larva terinfeksi virus
tercepat (1,67 hari) terdapat pada perlakuan I2 (larva instar 4) sedangkan paling
lama (2,58 hari) terdapat pada perlakuan I1 (larva instar 2). Perbedaan waktu
sedikit memakan daun dibandingkan dengan instar 4. Hasil penelitian ini tidak
berbeda dengan penelitian yang dilakukan dengan Laoh dkk (2003) bahwa larva
instar 2 lebih sedikit memakan daun yang mengandung NPV dibandingkan larva
instar 3 dan 4, sehingga konsentrasi virus di dalam tubuh larva instar 2 ini juga
lebih rendah. Pada konsentrasi virus yang rendah ini belum mampu untuk
membunuh larva instar 2.
Dari hasil pengamatan juga dapat dilihat bahwa gejala larva yang
terinfeksi NPV mengalami perubahan warna menjadi hijau pucat, tidak mau
makan, biasanya larva yang terinfeksi menggantung dengan posisi terbalik di
bagian ujung tanaman dan mengalami kematian setelah 2-3 hari setelah aplikasi.
Hal ini sesuai dengan pernyataan Irfan dkk (2007) bahwa dalam waktu 1-2 hari
setelah polihedra tertelan, hemolimfa yang semula jernih berubah menjadi keruh.
Kemampuan makannya menurun, sehingga pertumbuhannya lambat. Ulat
cenderung merayap ke pucuk tanaman kemudian mati menggantung dengan posisi
terbalik dengan tungkai semu bagian akhir pada tanaman
Dari analisis sidik ragam dapat dilihat bahwa banyaknya suspensi larva
S. litura yang terinfeksi virus/liter air sangat berpengaruh nyata terhadap waktu munculnya gejala infeksi awal atau periode inkubasi (hari). Hal ini dapat dilihat
pada Tabel 6 dan Lampiran 2.
Tabel 6. Banyaknya suspensi larva S. litura yang terinfeksi virus NPV
Perlakuan Rataan
V0 (kontrol) 0 c
V1 (suspensi 10 ekor larva terinfeksi virus/liter air) 4,00 a
V2 (suspensi 20 ekor larva terinfeksi virus/liter air) 2,67 b
Keterangan: Angka yang diikuti oleh notasi huruf yang berbeda menunjukkan data berbeda nyata menurut Uji Jarak Duncan pada taraf 5%.
Tabel 6 menunjukkan bahwa hari munculnya gejala awal atau periode
inkubasi tercepat (1,83 hari) terdapat pada perlakuan V3 (suspensi 30 ekor larva
terinfeksi virus/liter air) sedangkan pada perlakuan V0 (kontrol) tidak ada
menunjukkan gejala infeksi virus. Hal ini menunjukkan bahwa semakin tinggi
konsentrasi virus yang diaplikasikan maka semakin tinggi konsentrasi virus dalam
tubuh larva. Perlakuan V0 (kontrol) tidak menunjukkan gejala infeksi virus,
sedangkan pada perlakuan V1 (suspensi 10 ekor larva terinfeksi virus/liter air)
menunjukkan waktu yang cukup lama untuk menunjukkan gejala hal ini
dikarenakan konsentrasi virus rendah sehingga waktu menunjukkan gejala juga
lama. Hal ini sesuai dengan pernyataan Arifin dan Wahyoe (2001) bahwa hasil
penelitian mengenai tingkat dan waktu kematian larva tersebut menunjukkan
bahwa tingkat dan waktu kematian larva tergantung pada konsentrasi polihedra.
Semakin tinggi konsentrasi polihedra semakin tinggi dan cepat pula tingkat
kematian ulat. Selanjutnya, Aizawa (1977 dalam Laoh dkk, 2003) bahwa aplikasi virus yang semakin tinggi konsentrasinya akan mengakibatkan makin banyaknya
polihedra virus yang tertelan dan akan makin banyak jaringan larva yang
KESIMPULAN DAN SARAN
Kesimpulan
1. Persentase mortalitas tertinggi pada pengamatan stadia larva terdapat
pada perlakuan I1 (larva instar 2) yaitu sebesar 49,08% dan terendah
terdapat pada perlakuan I2 (larva instar 4) yaitu 16,25%.
2. Persentase mortalitas tertinggi pada pengamatan banyaknya suspensi
larva yang terinfeksi virus terdapat pada perlakuan V3 (suspensi 30
ekor larva terinfeksi virus/liter air) yaitu sebesar 64,17% dan terendah
terdapat pada perlakuan V0 (kontrol) yaitu 0%.
3. Intensitas serangan tertinggi terdapat pada perlakuan V0 (kontrol) yaitu
sebesar 33,06% dan yang terendah terdapat pada perlakuan V3
(suspensi 30 ekor larva terinfeksi virus/liter air) yaitu sebesar 15,58%.
4. Periode inkubasi tercepat pada pengamatan stadia larva terdapat pada
perlakuan I2 (larva instar 4) yaitu selama 1,67 hari dan yang terlama
terdapat pada perlakuan I1 (larva instar 2) yaitu selama 2,58 hari.
5. Periode inkubasi tercepat pada pengamatan banyaknya suspensi larva
terinfeksi virus terdapat pada perlakuan V3 (suspensi 30 ekor larva
terinfeksi virus/liter air) yaitu selama 1,83 hari dan pada V0 (kontrol)
Saran
1. Sebaiknya aplikasi NPV dilakukan dari mulai awal munculnya telur
S. litura pada tanaman tembakau Deli dan aplikasi dilakukan pada sore hari.
2. Larva yang terinfeksi NPV dapat digunakan untuk perbanyakan virus
selanjutnya.
3. Perlu dilakukan penelitian tentang banyaknya virus yang terkandung
DAFTAR PUSTAKA
Abidin, Z. 2004. Pengendalian Hama dan Penyakit Utama Pada Tanaman Tembakau.Balai Penelitian Tembakau Deli. Medan.
Arifin, M. 1994. Pemanfaatan SlNPV sebagai Agensia Pengendalian Hayati. Balai Penelitian Tanaman Pangan. Bogor.
dan D. Nuzullianti. 1999. Keefektifan bioinsektisida NPV pada berbagai macam bahan perangsang makan terhadap ulat grayak kedelai, Spodoptera litura (F.). Dalam Prosiding Nasional Pertanian Organik, Bogor 2-4 September 1994.
dan W. I. S. Waskitoe. 2001. Balai Penelitian Tanaman Pangan. Bogor.
.2011. Teknik Produksi dan Pemanfaatan Bioinsektisida NPV untuk Pengendalian Ulat Grayak Kedelai. Balai Penelitian Bioteknologi Tanaman Pangan. Bogor.
Cardona, E. V., C. S. Ligat., dan M. P. Subang. 2007. Life History Of Common Cutworm, Spodoptera litura Fabricius (Noctuidae : Lepidoptera) In Benguet.Progress Report. BSU Research In- House Review.
BPTD. 2004. Strategi Pengendalian Hama dan Penyakit Tanaman Tembakau. BPTD PTP Nusantara II. Medan.
Driesche, R. G. V., dan T. S. Belows. 1996. Biological Control. Chapman and Hall Dept. BC. 115 fifth Avenue, New York.
Erwin. 2000. Hama dan Penyakit Tembakau Deli. Balai Penelitian Tembakau Deli PTPN II (Persero). Medan.
FAO. 2012. Integreted Pest Management. Food and Agriculture Organization Of The United Nations.
Hall, F. R., dan J. J. Menn. 1999. Biopesticides. Humana Press. Totawa, New Jersey.
Haryani. 2005. Resistensi Spodoptera litura F. (Lepidoptera : Noctuidae) Pada Tanaman Tembakau Deli. Dalam Prosiding Nasional Perlindungan Tanaman. Bandung, 12-13 Februari 2005.
Kalshoven, L. G. E. 1981. The Pest of Crop In Indonesia. P. A. Vander Laan dan PT Ichtiar Baru-Van Hoeve. Jakarta.
Kamita, S. G., dan S. Maeda. 1993. Inhibiting Bombyx mori Nuclear Ployhedrosis Virus (NPV) Replication by The Putative DNA Helicase Gene Of
Authgrapha californica NPV. J. Virology 67 : (6239-6245).
Kemtan (Kementerian Pertanian). 2009. Rancangan Rencana Strategis Kementerian Pertanian Tahun 2010-2014. Kementerian Pertanian, Jakarta.
Miller, L. K. dan L. A, Ball. 1998. The Insect Viruses. Plenum Press. New York.
Laoh, J. H., F. Puspita., dan Hendra. 2003. Kerentanan Larva Spodoptera litura
Terhadap Nuclear Plyhedrosis Virus. J. Natur Indon. 5(2): 145-151.
Oka, I. N. 1995. Pengendalian Hama Terpadu dan Implementasinya Di Indonesia. Gadjah Mada University press. Yogyakarta.
Poinar G. O., dan G. M. Thomas. 1984. Laboratory Guide to Insect Pathogens and Parasites. Plenum Press. New York.
Purnama, H. A. 2003. Hama dan Penyakit Tembakau Deli. BPTD PTPP Nusantara II. Medan.
Ravishankar, B. S., dan M. G. Venkatesha. 2010. Effectiveness of SlNPV of
Spodoptera litura (Fab.) (Lepidoptera: Noctuidae) on different host plants.
J. Biopestisida 3 : (168-171).
Riyanto. 2008. Potensi Agen Hayati Spodoptera Litura Nuclear Polyherosis Virus (SlNPV) untuk Pengendalian Spodoptera Litura Fabricus. FORUM MIPA, ISSN 1410-1262.
Subandrijo, S. H., Istdijoso., dan Suwarso. 1992. Pengendalian Serangga Hama Tembakau Besuki Oogst. Badan Penelitian dan Pengembangan Tembakau dan Tanaman Serat. Malang.
Sudarmo, S. 1992. Tembakau. Penerbit Kanisius. Yogyakarta.
Susilo, 2007. Pengendalian Hayati dengan Memberdayakan Musuh Alami Hama Tanaman. Graha ilmu: Yogyakarta.
Trang, T. T. K., dan S. Chaudri. 2002. Bioassay of Nuclear Polyhedrosis Virus (NPV) and in combination with insecticide on Spodoptera litura (Fab).Omonrice (10): 45-53.
Trizelia, M. Syahrawati, dan A. Mardiah. 2011. Patogenitas Beberapa Isolat Cendawan Entomopatogen Metarhizium Spp. Terhadap Telur Spodoptera litura Fabricius (Lepidoptera: Noctuidae). J. Entomol. Indon. 8 (1): 45-54. Untung, K. 1993. Pengantar Pengelolaan Hama Terpadu. Gadjah Mada University. Yogyakarta.
BAGAN PENELITIAN
Keterangan:
I1V0 : Kontrol
I1V1 : Suspensi 10 ekor larva/1 liter air terhadap larva instar 2
I1V2 : Suspensi 20 ekor larva/1 liter air terhadap larva instar 2
I1V3 : Suspensi 30 ekor larva/1 liter air terhadap larva instar 2
I2V0 : Kontrol
I2V1 : Suspensi 10 ekor larva/1 liter air terhadap larva instar 5
I2V2 : Suspensi 20 ekor larva/1 liter air terhadap larva instar 5
I2V3 : Suspensi 30 ekor larva/1 liter air terhadap larva instar 5
DESKRIPSI TANAMAN TEMBAKAU DELI (Nicotianae tabacum L.)
Varietas : F1-45
Bentuk Permukaan Daun : Ovalis / rata
Urat Daun : Halus
Tepi daun : Rata
Warna Daun : Hijau Terang
Panjang Daun Pasir (cm) : 38,6
Panjang Daun Kaki I (cm) : 48,23
Panjang Daun Kaki II (cm) : 19,12
Lebar Daun Kaki I (cm) : 22,43
Lebar Daun Kaki II (cm) : 28,61
Tebal Daun Pasir (cm) : 0,38
Tebal Daun Kaki I (cm) : 0,29
Tebal Daun Kaki II (cm) : 0,28
Tinngi Tanaman (cm) : 215
Diameter Batang (cm) : 2,3
Intermedia (cm) : 7,5
Jumlah Daun Per pokok (hl) : 42
Jumlah Daun Produksi (hl) : 26
Mulai Tanaman Berbunga (hr) : 55 – 60
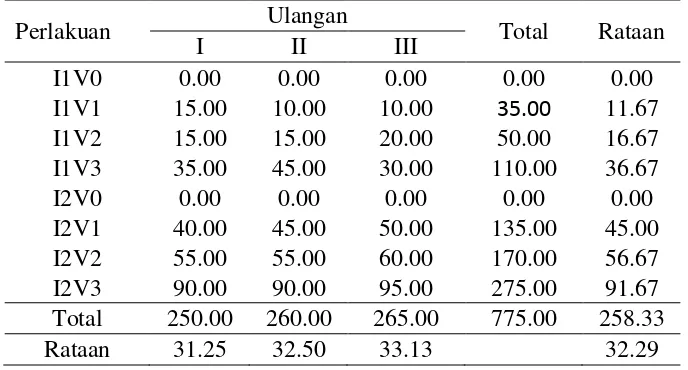
Lampiran 1. Persentase mortalitas (%)
Perlakuan Ulangan Total Rataan
Transformasi Arc Sin
Perlakuan Ulangan Total Rataan
Uji Jarak Duncan
I X V
SY 0.53
-1.60 -1.68 9.95 14.91 35 43.20 57.86 89.85
T 2 3 4 5 6 7 8 9
SSR 0,05 3.00 3.15 3.23 3.30 3.34 3.37 3.39 3.41 LSR 0,05 1.60 1.68 1.72 1.76 1.78 1.80 1.81 1.82 Perlakuan I2V0 I1V0 12V1 I2V2 I2V3 I1V1 I1V2 I1V3
Rataan 0.00 0.00 11.67 16.67 36.67 45.00 59.67 91.67 a. b.
c. d.
e. f.
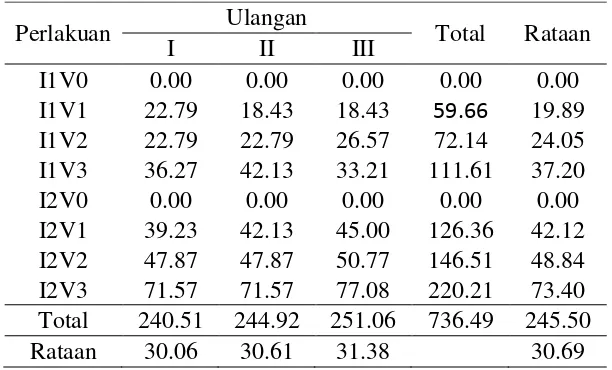
Lampiran 2. Intensitas Serangan (%)
Perlakuan Ulangan Total Rataan
I II III
suspensi larva terinfeksi virus Total Rataan
V0 V1 V2 V3
I1 28.72 24.84 20.07 15.61 89.25 22.31 I2 37.39 25.66 20.07 15.56 98.68 24.67 Total 66.12 50.50 40.15 31.17 187.93
Transformasi Arc Sin
Perlakuan Ulangan Total Rataan
Lampiran 3. Periode Inkubasi Vrus Dalam Tubuh Larva (Hari)
Perlakuan Ulangan Total Rataan
I II III
suspensi larva terinfeksi virus Total Rataan
V0 V1 V2 V3
suspensi larva terinfeksi virus Total Rataan
V0 V1 V2 V3
I1 0.00 4.67 3.33 2.33 10.33 2.58
I2 0.00 3.33 2.00 1.33 6.67 1.67
Total 0.00 8.00 5.33 3.67 17.00
Transformasi Arc Sin
Perlakuan Ulangan Total Rataan
Beda uji rataan pengaruh stadia larva terhadap persentase mortalitas (%)
Beda Uji Rataan Pengaruh Stadia Larva
Terhadap Persentase Moralitas (%)
Beda uji rataan pengaruh banyaknya ssuspensi larva yang terinfeksi virus terhadap persentase mortalitas (%)
Perlakuan Rataan
V0 (Kontrol) 0
V1 (Suspensi 10 ekor larva terinfeksi virus dalam 1 liter air) 28,33
V2 (Suspensi 20 ekor larva terinfeksi virus dalam 1 liter air) 38,17
V3 (Suspensi 30 ekor larva terinfeksi virus dalam 1 liter air) 64,17
0
Beda Uji Rataan Pengaruh Banyaknya
Suspensi Larva Yang Terinfeksi Virus
Terhadap Persentase Mortalitas (%)
Beda uji rataan Pengaruh Interaksi Antara Stadia Larva dengan Banyaknya suspensi Suspensi Larva terinveksi virus Terhadap Persentase Mortalitas (%)
Perlakuan Rataan
I1V0 dan I2V0 (Kontrol) 0
I1V1(Suspensi 10 ekor larva yang terinfeksi virus terhadap instar 2) 45,00
I1V2(Suspensi 20 ekor larva yang terinfeksi virus terhadap instar 2) 59,67
I1V3(Suspensi 30 ekor larva yang terinfeksi virus terhadap instar 2) 91,67
I2V1(Suspensi 10 ekor larva yang terinfeksi virus terhadap instar 4) 11,67
I2V2(Suspensi 20 ekor larva yang terinfeksi virus terhadap instar 4) 16,67
I2V3(Suspensi 30 ekor larva yang terinfeksi virus terhadap instar 4) 36,67
0
I1V0 I1V1 I1V2 I1V3 I2V0 12V1 I2V2 I2V3
P
Interaksi antara stadia larva dengan banyaknya suspensi larva terinfeksi virus
Beda Uji Rataan Pengaruh Interaksi Antara
Stadia Larva dengan Banyaknya Suspensi
Larva Terinfeksi Virus (%)
Beda uji rataan pengaruh banyaknya suspensi larva yang terinfeksi virus terhadap intensitas serangan (%)
Perlakuan Rataan
V0 (Kontrol) 33,06
V1 (Suspensi 10 ekor larva terinfeksi virus dalam 1 liter air) 25,25
V2 (Suspensi 20 ekor larva terinfeksi virus dalam 1 liter air) 20,07
V3 (Suspensi 30 ekor larva terinfeksi virus dalam 1 liter air) 15,58
0
Beda Uji Rataan Pengaruh Banyaknya
Suspensi Larva Yang Terinfeksi Virus
Terhadap Intensitas Serangan
Beda uji rataan pengaruh stadia larva terhadap periode inkubasi (Hari)
Beda uji rataan pengaruh stadia larva
terhadap periode inkubasi
I1
Beda uji rataan pengaruh banyaknya suspensi Larva yang terinfeksi virus terhadap periode inkubasi (Hari)
Perlakuan Rataan
V0 (Kontrol) 0
V1 (Suspensi 10 ekor larva terinfeksi virus dalam 1 liter air) 4,00
V2 (Suspensi 20 ekor larva terinfeksi virus dalam 1 liter air) 2,67
V3 (Suspensi 30 ekor larva terinfeksi virus dalam 1 liter air) 1,83