Lampiran 4. Bagan alir proses dekstruksi kering pada Sampel
Ditambahkan 5 mL HNO3 (1:1)
Diuapkan pada hot plate sampai kering Dimasukkan kembali kedalam tanur
dengan temperatur awal 100oC dan perlahan-
lahan temperatur dinaikkan menjadi 500oC
dengan interval 25oC setiap 5 menit
Dilakukan selama 1 jam dan dibiarkan dingin pada desikator
Hasil Abu
Ditimbang sebanyak 25 g di atas krus porselen
Diarangkan diatas hotplate
Diabukan di tanur dengan temperature awal
100oC dan perlahan-lahan temperatur dinaikkan menjadi 500oC dengan interval 25oC setiap 5
Menit
Dilakukan selama 48 jam dan dibiarkan dingin pada desikator
Sampel yang telah dirajang
Dibersihkan dari pengotoran Dicuci bersih dengan air
Ditiriskan dan dikeringkan dengan cara diangin- anginkan
Dirajang
Lampiran 5. Bagan Alir Pembuatan Larutan Sampel
Hasi destruksi kering
Dilarutkan dalam 5 mL HNO3, hingga diperoleh
larutan bening.
Dimasukkan ke dalam labu tentukur 50 mL Dibilas Krus porselen dengan akua demineralisata
sebanyak 3 kali
Dicukupkan volumenya dengan akua
demineralisata sampai garis tanda
Disaring dengan kertas Whatman No.42 dengan membuang 5 mL larutan pertama hasil
penyaringan Larutan Sampel
Dilakukan analisis kualitatif
Dilakukan analisis kuantitatif dengan spektrofotometer serapan atom pada λ 766,5 nm untuk kalium.
Lampiran 6. Hasil analisis Kualitatif kalium
Lampiran 7. Data dan Perhitungan Persamaan Garis Regresi 1. Perhitungan Persamaan Garis Regresi Kalium
No. X Y XY X2 Y2
1. 0,0000 0,0001 0,0000 0,0000 0,00000001 2. 2,0000 0,0589 0,1178 4,0000 0,00346921 3. 4,0000 0,1154 0,4616 16,0000 0,01331716 4. 6,0000 0,1663 0,9978 36,0000 0,02765569 5. 8,0000 0,2294 1,8352 64,0000 0,05262436 6. 10,0000 0,2889 2,889 100,0000 0,08346321
∑ 30,0000 5,0000 = X 0,8590 0,143166 = Y
6,3014 220,0000 0,18052964
02866 , 0 6 ) 30 ( 220 6 ) 8590 , 0 )( 30 ( 3014 , 6 ) ( 2 2 2 = − − = ∑ − ∑ ∑ ∑ − ∑ = n X X n Y X XY a
0,000134
) 5 )( 02866 , 0 ( 143166 , 0 − = − = − = + = X a Y b X a Y
Lampiran 7. (Lanjutan)
{
}{
}
{
}{
}
9997 , 0 0071 , 2 0064 , 2 6 / ) 8590 , 0 ( ) 18052964 , 0 ( 6 / ) 30 ( ) 220 ( 6 / ) 8590 , 0 )( 30 ( ) 3014 , 6 ( / ) ( / ) ( / 2 2 2 2 2 2 = = − − − = − − ∑ ∑ − ∑ =∑
∑
∑
X∑
X n Y Y nLampiran 8. Hasil Penetapan Kadar Mineral Kalium pada Sampel A. Sampel Buah Oyong
No. Sampel Berat Sampel (g) Absorbansi (A) Konsentrasi (µg/mL) Kadar (µg / g)
Kadar (mg/100 g)
1 . 25,0341 0,0852 2,9774 2973,344 297,3344 2. 25,0235 0,0851 2,9739 2971,107 297,1107 3. 25,0146 0,0838 2,9286 2926,890 292,6890 4. 25,0214 0,0850 2,9704 2967,859 296,7859 5. 25,0345 0,0852 2,9774 2973,346 297,3346 6. 25,0415 0,0854 2,9844 2979,454 297,9454
B. Sampel Daun Alpukat No. Sampel Berat Sampel . (g) Absorbansi (A) Konsentrasi (µg/mL) Kadar (µg / g)
Kadar (mg/100 g)
1. 25,0368 0,1252 4,3731 4366,672 436,6672 2. 25,0452 0,1260 4,4010 4393,057 439,3057 3. 25,0457 0,1262 4,4080 4399.956 439,9956 4. 25,0341 0,1243 4,3417 4335,785 433,5785 5 25,0361 0,1253 4,3766 4370,289 437,0289 6. 25,0351 0,1247 4,3556 4349,493 434,9493
C. Sampel Herba Pecut Kuda No. Sampel Berat Sampel (g) Absorbansi (A) Konsentrasi (µg/mL) Kadar (µg / g)
Kadar (mg/100 g)
Lampiran 9. Contoh Perhitungan Kadar Mineral Kalium pada Sampel A. Contoh Perhitungan Kadar Mineral Kalium pada Buah Oyong Berat sampel yang ditimbang = 25,0341 g
Absorbansi (Y) = 0,0852
Persamaan Regresi : Y = 0,02866X – 0,000134
X = 2,9774µg/mL
2866 0,0 000134 , 0 0852 0, = +
Konsentrasi Kalium = 2,9774µg/mL
B.Contoh Perhitungan Kadar Mineral Kalium pada Daun Alpukat Berat sampel yang ditimbang = 25,0368 g
Absorbansi (Y) = 0,1252
Persamaan Regresi: Y = 0,02866 X – 0,000134
X = 4,3731µg/mL
2866 0,0 000134 , 0 02866 0, = +
Konsentrasi Kalium = 4,3731 µg/mL
Lampiran 9. (Lanjutan)
C. Contoh Perhitungan Kadar Mineral Kalium pada Pecut Kuda Berat sampel yang ditimbang = 25,0208 g
Absorbansi (Y) = 0,1223
Persamaan Regresi : Y = 0,02866 X – 0,000134
X = 4,2719µg/mL
2866 0,0 000134 , 0 1223 0, = +
Konsentrasi Kalium = 4,2719 µg/mL
Lampiran 10. Perhitungan Statistik Kadar Mineral Kalium pada Buah Oyong 1. Perhitungan Statistik Kadar Mineral Kalium pada Buah Oyong
No. Xi
Kadar (mg/100 g) Xi−X
2
) (Xi−X
1 297,3344 0,0201 0,00040401
2 297,1107 0,2438 0,05943844
3 297,6161 0,2616 0,06843456
4 296,7859 0,5686 0,32330596
5 297,3346 0,0199 0,00039601
6 297,9454 0,5909 0,34916281
∑ 296,5333 2 , 1779 = X 0,80114179
0,4002mg/100g 1 -6 80114179 , 0 1 -) -( 2
∑
= = = n X Xi SDPada interval kepercayaan 95% dengan nilai α = 0,05 dk = n - 1 = 5 diperoleh
nilai ttabel= α/2, dk = 2,5706. Data diterima jika thitung < ttabel
t
hitung =n SD X Xi / −
t
hitung 1 = 0,12316 / 4002 , 0 0201 , 0 =
t
hitung 2 = 1,49296 / 4002 , 0 2438 , 0 =
t
hitung 3 = 1,6019Lampiran 10. (Lanjutan)
t
hitung 4 = 3,4819 (dataditolak)6 / 4002 , 0 5658 , 0 =
t
hitung 5 = 0,12186 / 4002 , 0 0199 , 0 =
t
hitung 6 = 3,6184 (dataditolak)6 / 4002 , 0 5909 , 0 =
Dari hasil uji statistik diatas, diketahui bahwa kadar no 4 dan no 6 ditolak,
sehingga dilakukan kembali uji statistik tanpa mengikutsertakan data no 4 dan
6, g 100 / mg 2082 , 0 1 -4 13004277 , 0 1 -) -( 2
∑
= = = n X Xi SDPada interval kepercayaan 95% dengan nilai α = 0,05 dk = n – 1 = 3 diperoleh
nilai ttabel= α/2, dk = 3,1824. Data diterima jika thitung < ttabel
t
hitung =n SD X Xi / −
No, Kadar (mg/100 g) Xi Xi - X (Xi - X)2
1 297,3344 -0,0145 0,00021025
2 297,1107 -0,2382 0,05673924
3 297,6161 0,0412 0,00169744
5 297,3346 0,2672 0,07139584
∑X = 1189,3958 ∑ = 0,13004277
t
hitung 1 = 0,13924 / 2082 , 0
0,0145
-=
t
hitung 2 = 2,28814 / 2082 , 0
0,2382
-=
t
hitung 3 = 0,39574 / 2082 , 0
0,0412 =
t
hitung 5 = 2,56674 / 2082 , 0
0,2672 =
Dari hasil perhitungan diatas diperoleh semua thitung < ttabel, maka semua
data tersebut diterima. Kadar mineral kalium sebenarnya pada buah oyong
adalah:
n / SD x t
( ± X =
μ (a/2,dk)
= X= 297,3489 ± 3,1824 x 0,2082/ 4
Lampiran 11. Perhitungan Statistik Kadar Mineral Kalium pada Daun Alpukat
1. Perhitungan Statistik Kadar Mineral Kalium pada Daun Alpukat
No. Xi
Kadar (mg/100 g) Xi−X
2
) (Xi−X
1 436,6672 -0,3036 0,09217296
2 439,3057 2,3349 5,45175801
3 439,9956 3,0248 9,14941504
4 433,5785 -3,3923 11,50769929
5 437,0289 0,0581 0,00337561
6 434,9493 -2,0215 4,08646225
∑ 2621,8252 436,9708 = X 30,29088316 g mg/100 4613 , 2 1 -6 29088316 , 30 1 -) -( 2
∑
= = = n X Xi SDPada interval kepercayaan 95% dengan nilai α = 0,05 dk = n – 1 = 5 diperoleh
nilai ttabel= α/2, dk = 2,5706 Data diterima jika
t
hitung< t
tabel.t
hitung =n / SD X -Xi
t
hitung 1 = 0,30216 / 4613 , 2 3036 , 0 =
t
hitung 2 = 2,3237Lampiran 11. (Lanjutan)
t
hitung 3 = 3,0103 (dataditolak)6 / 4613 , 2 0248 , 3 =
t
hitung 4 = 3,3760 (dataditolak)6 / 4613 , 2 3923 , 3 = −
t
hitung 5 = 0,05786 / 4613 , 2 0581 , 0 =
t
hitung 6 = 2,01186 / 4613 , 2 0215 , 2 = −
Dari hasil uji statistik diatas, diketahui bahwa kadar no 3 dan no 4 ditolak,
sehingga dilakukan kembali uji statistik tanpa mengikutsertakan data no 3 dan
4, g mg/100 5613 , 5 1 -4 9,63258769 1 -) -( 2
∑
= = = n X Xi SDPada interval kepercayaan 95% dengan nilai α = 0,05; dk = n - 1 = 3; diperoleh nilai ttabel= α/2, dk = 3,1824 Data diterima jika thitung < ttabel,
No, Kadar (mg/100 g) Xi Xi - X (Xi - X)2
1 436,6672 -0,3205 0,10272025
2 439,3057 2,318 5,3731
5 437,0289 0,0412 0,00169744
6 434,9493 -2,0384 4,15507
∑X = 1747,9511 ∑ = 9,63258769
thitung =
t
hitung 1 = 0,11524 / 5613 , 5 0,3205 -=
t
hitung 2 = 0,83364 / 5613 , 5 2,318 =
t
hitung 5 = 0,01484 / 5613 , 5 0,0412 =
t
hitung 6 = 0,73314 / 5613 , 5 2,0384 -=
Dari hasil perhitungan diatas diperoleh semua thitung < ttabel, maka semua data
tersebut diterima. Kadar mineral kalium sebenarnya pada Daun Alpukat adalah:
) n / SD x ) dk , 2 / α ( t ( ± x = μ
= 436,9877 ± 3,1824 x 5,5613/ 4
Lampiran 12. Perhitungan Statistik Kadar Mineral Kalium pada Herba Pecut Kuda
1. Perhitungan Statistik Kadar Mineral Kalium pada Herba Pecut Kuda
No. Xi
Kadar (mg/100 g) Xi−X
2
) (Xi−X
1 426,8348 -4,1336 17,08664896
2 425,8334 -5,1350 26,368225
3 425,8470 -5,1214 26,22873796
4 432,3946 1,4262 2,03404644
5 431,3883 0,4199 0,17631601
6 443,5124 12,544 157,351936
∑ 2585,8105 9684 , 430 = X 229,2459104 g 100 / mg 7712 , 6 1 -6 4 229,245910 1 -) -( 2
∑
= = = n X Xi SDPada interval kepercayaan 95% dengan nilai α = 0,05 dk = n – 1 = 5 diperoleh
nilai ttabel= α/2, dk = 2,5706. Data diterima jika thitung < ttabel
t
hitung =n SD X Xi / −
t
hitung 1 = 1,49506 / 7712 , 6 13336 , 4 =
t
hitung 2 = 1,8575Lampiran 12. (Lanjutan)
t
hitung 3 = 1,85256 / 7712 , 6 1214 , 5 =
t
hitung 4 = 0,51596 / 7712 , 6 4262 , 1 =
t
hitung 5 = 0,15186 / 7712 , 6 0,4199 =
t
hitung 6 = 4,5376(dataditolak)6 / 7712 , 6 12,544 =
Dari hasil uji statistik diatas, diketahui bahwa kadar no, 6 ditolak,
sehingga dilakukan kembali uji statistik tanpa mengikutsertakan data no 6,
g 100 / mg 1785 , 3 4 41240333 , 40 1 -) -( 2
∑
= = = n X Xi SDPada interval kepercayaan 95% dengan nilai α = 0,05 dk = n - 1 = 4 diperoleh
nilai ttabel= α/2, dk = 2,7765 Data diterima jika thitung < ttabel
No, Kadar (mg/100 g) Xi Xi - X (Xi - X)2
1 426,8348 -1,6212 2,62828944
2 425,8334 -2,6262 6,89692644
3 425,8470 -2,6126 6,82567876
4 432,3946 3,935 15,484225
5 431,3883 2,9287 8,57728369
∑X = 2142,2981 ∑ = 40,41240333
Lampiran 12. (Lanjutan)
t
hitung =n SD X Xi / −
t
hitung 1 = 1,14055 / 1785 , 3 6212 , 1 =
t
hitung 2 = 1,84765 / 1785 , 3 6262 , 2 =
t
hitung 3 = 1,83805 / 1785 , 3 6126 , 2 =
t
hitung 4 = 2,76835 / 1785 , 3 935 , 3 =
t
hitung 5 = 2,06045 / 1785 , 3 9287 , 2 =
Karena thitung < ttabel, maka semua data tersebut diterima, Kadar kalium
sebenarnya (µ) dalam Herba Pecut Kuda:
µ = X ± (t(α/2), dk) x SD/
= 426,1717mg/100 g ± (2,7765 x 3,1785/ 5) mg/100 g
Lampiran 13. Rekapitulasi Data Kadar Mineral Kalium pada buah oyong, daun alpukat dan herba pecut kuda sebelum usji-t.
Mineral Sampel No
Berat Sampel
(g)
Absorbansi Konsentrasi (µg/mL)
Kadar (µg/g)
Kadar (mg/100g)
Kalium
Buah Oyong
1. 25,0341 0,0852 2,9774 2973,344 297,3344 2. 25,0235 0,0851 2,9739 2971,107 297,1107 3. 25,0146 0,0838 2,9286 2926,890 292,6890 4. 25,0214 0,0850 2,9704 2967,859 296,7859 5. 25,0345 0,0852 2,9774 2973,346 297,3346 6. 25,0415 0,0854 2,9844 2979,454 297,9454
Rata-rata 2965,333 296,5333
SD 0,4002
Kalium
Daun Alpukat
1. 25,0368 0,1252 4,3731 4366,672 436,6672 2. 25,0452 0,1260 4,4010 4393,057 439,3057 3. 25,0457 0,1262 4,4080 4399,956 439,9956 4. 25,0341 0,1243 4,3417 4399,956 439,5785 5. 25,0361 0,1253 4,3766 4370,289 437,0289 6. 25,0351 0,1247 4,3556 4349,493 434,9493
Rata-rata 4369,708 437,9208
SD 2,4613
Kalium
Herba Pecut Kuda
1. 25,0208 0,1223 4,2719 4268,348 426,8348 2. 25,0186 0,1220 4,2614 4258,334 425,8334 3. 25,0172 0,1220 4,2614 4258,470 425,8470 4. 25,0217 0,1239 4,3277 4323,946 432,3946 5. 25,0198 0,1236 4,3173 4313,883 431,3883 6. 25,0214 0,1271 4,4394 4435,124 443,5124
Rata-rata 4284,596 430,9684
Lampiran 14. Validasi Metode Analisis
1. Validasi Metode Analisis Kalium
Berat
Sampel
(g)
Absorbansi Konsentrasi (µg/mL)
CA
(µg/mL)
CF
(µg/mL)
% Recovery
25,0345 0,1416 4,9503 2,9774 4,9453 98,395%
25,0415 0,1419 4,9608 2,9914 4,9558 98,22%
25,0214 0,1412 4,9363 2,9739 4,9314 97,875%
25,0341 0,1415 4,9468 2,9844 4,9418 97,87%
25,0398 0,1418 4,9578 2,9704 4,9523 99,095%
25,0235 0,1414 4,9433 2,9879 4,9383 97,52% ∑ = 588,975%
X= 98,1625%
Keterangan:
CF : Kosenterasi logam dalam sampel setelah penambahan baku (µ g/mL)
CA : Kosenterasi rata-rata logam dalam sampel sebelum penambahan baku
(µg/mL)
Lampiran 15. Perhitungan Batas Deteksi (LOD) dan Batas Kuantitasi (LOQ) Kalium
1. Perhitungan Batas Deteksi (LOD) dan Batas Kuantitasi (LOQ) Kalium Y = 0,02866X – 0,000134
Slope = 0,02866 X
No.
Konsentrasi (µg/mL)
X
Absorbansi
Y Yi Y-Yi
(Y-Yi)2 ( x 10-6)
1. 0,0000 0,0001 -0,000134 0,000234 0,18
2. 2,0000 0,0589 0, 0571 0,0018 3,24
3. 4,0000 0,1154 0,1145 0,0009 0,81
4. 6,0000 0,1663 0,1718 -0,0055 30,25
5. 8,0000 0,2294 0,2291 0,0003 0,09
6. 10,0000 0,2889 0,2864 0,0025 6,25
∑= 40,82 x 10-6
Lampiran 16. Perhitungan Persen Perolehan Kembali (Recovery) Kadar Mineral Kalium pada Sampel.
Sampel 1
Persamaan Regresi : Y = 0,02866 X - 0,000134
9453 , 4 02866 , 0 000134 , 0 1416 0, )
(CF = + =
X
Konsentrasi kalium setelah ditambahkan larutan baku = 4,9453µg/mL
konsentrasi sampel sebelum ditambah larutan standar (CA) = 2,9774 µg/mL
Berat sampel rata-rata uji recovery = 25,03247 g
Kadar larutan standar yang ditambahkan (C *A) = 2 µg/mL
% 395 , 98 % 100 µg/mL 2 µg/mL 9774 , 2 -µg/mL 9453 , 4 % 100 * -Kalium Kembali Perolehan 0 0 = = = x x C CA C A F Sampel 2
Persamaan Regresi : Y = 0,02866 X - 0,000134
9558 , 4 02866 , 0 000134 , 0 1419 0, )
(CF = + =
X
Konsentrasi kalium setelah ditambahkan larutan baku = 4,9558µg/mL
konsentrasi sampel sebelum ditambah larutan standar (CA) = 2,9914 µg/mL
Berat sampel rata-rata uji recovery = 25,03247 g
Lampiran 16. (Lanjutan) % 22 , 98 % 100 µg/mL 2 µg/mL 9914 , 2 -µg/mL 9558 , 4 % 100 * -Kalium Kembali Perolehan 0 0 = = = x x C CA C A F Sampel 3
Persamaan Regresi : Y = 0,02866 X - 0,000134
9314 , 4 02866 , 0 000134 , 0 1412 0, )
(CF = + =
X
Konsentrasi kalium setelah ditambahkan larutan baku = 4,9314µg/mL
konsentrasi sampel sebelum ditambah larutan standar (CA) = 2,9739 µg/mL
Berat sampel rata-rata uji recovery = 25,03247 g
Kadar larutan standar yang ditambahkan (C *A) = 2 µg/mL
% 875 , 97 % 100 µg/mL 2 µg/mL 9739 , 2 -µg/mL 9314 , 4 % 100 * -Kalium Kembali Perolehan 0 0 = = = x x C CA C A F Sampel 4
Persamaan Regresi : Y = 0,02866 X - 0,000134
9418 , 4 02866 , 0 000134 , 0 1415 0, )
(CF = + =
X
Konsentrasi kalium setelah ditambahkan larutan baku = 4,9418µg/mL
konsentrasi sampel sebelum ditambah larutan standar (CA) = 2,9844 µg/mL
Lampiran 16. (Lanjutan)
Kadar larutan standar yang ditambahkan (C *A) = 2 µg/mL
% 87 , 97 % 100 µg/mL 2 µg/mL 9844 , 2 -µg/mL 9418 , 4 % 100 * -Kalium Kembali Perolehan 0 0 = = = x x C CA C A F Sampel 5
Persamaan Regresi : Y = 0,02866 X - 0,000134
9523 , 4 02866 , 0 000134 , 0 1418 0, )
(CF = + =
X
Konsentrasi kalium setelah ditambahkan larutan baku = 4,9523µg/mL
konsentrasi sampel sebelum ditambah larutan standar (CA) = 2,9704 µg/mL
Berat sampel rata-rata uji recovery = 25,03247 g
Kadar larutan standar yang ditambahkan (C *A) = 2 µg/mL
% 095 , 99 % 100 µg/mL 2 µg/mL 9704 , 2 -µg/mL 9523 , 4 % 100 * -Kalium Kembali Perolehan 0 0 = = = x x C CA C A F Sampel 6
Persamaan Regresi : Y = 0,02866 X - 0,000134
9418 , 4 02866 , 0 000134 , 0 1414 0, )
(CF = + =
X
Konsentrasi kalium setelah ditambahkan larutan baku = 4,9383µg/mL
Lampiran 16. (Lanjutan)
Berat sampel rata-rata uji recovery = 25,03247 g
Kadar larutan standar yang ditambahkan (C *A) = 2 µg/mL
% 52 , 97
% 100 µg/mL
2
µg/mL 9879 , 2 -µg/mL 9383 , 4
% 100 *
-Kalium Kembali
Perolehan
0 0
= = =
x x
C CA C
A F
Lampiran 17. Perhitungan Simpangan Baku Relatif (RSD) Kalium pada Sampel
1. Perhitungan Simpangan Baku Relatif (RSD) Kalium pada Sampel
No.
konsentrasi % Perolehan Kembali
(Xi)
( Xi-X ) ( Xi-X )2
1. 4,9453 0,0012 0,00000144
2. 4,9558 0,0117 0,00013689
3. 4,9314 -0,0127 0,00016129
4. 4,9418 0,0023 0,00000529
5. 4,9523 0,0082 0,00006724
6. 4,9383 -0,0059 0,00003481
∑ 29,2356 0,00040696
X 4,9441 0,0000678267
Lampiran 18. Pengujian Beda Nilai Rata-Rata Kadar Kalium Dalam Buah Oyong dan Daun Alpukat
No. Buah Oyong Daun Alpukat
1. X1 = 297,3489 X2 = 436,9877
2. S1 = 0,2082 S2 =5,5613
Dilakukan uji F dengan taraf kepercayaan 95% untuk mengetahui apakah variasi kedua populasi sama (σ1 = σ2) atau bebeda (σ1 ≠ σ2 ).
− Ho : σ1 = σ2
H1 : σ1 ≠ σ2
− Nilai kritis F yang diperoleh dari tabel (F0,05/2 (3,3))adalah = 15,44
Daerah kritis penerimaan : -15,44 ≤ F
o≤ 15,44
Daerah kritis penolakan : F
o < -15,44 dan Fo> 15,44
Fo = 2 2 2 1 S S
Fo = 2
2
5,5613
0,2082
Fo = 0,0014
− Dari hasil ini menunjukkan bahwa Ho diterima dan H1 ditolak sehingga
disimpulkan bahwa σ1 = σ2 .simpangan bakunya adalah :
Sp =
2 ) 1 ( ) 1 ( 2 1 2 2 2 2 1 1 − ++ − − n n S n S n = 2 4 4 5,5613 1 4 2082 , 0 1
4 2 2
− − − + ) ( + ) ( = 6,1299
− Ho : µ1 = µ2
− Dengan menggunakan taraf kepercayaan 95% dengan nilai α = 5% → t0,05/2 = ± 2,4469 untuk df = 4 + 4 – 2 = 6
− Daerah kritis penerimaan : -2,4469 ≤ to ≤ 2,4469
Daerah kritis penolakan : to< -2,4469 dan to> 2,4469
=
(
)
2 1
2 1
/ 1 / 1
x -x
n n
s +
=
(
)
4 1 4 1 6,1299
436,9877
-297,3489 +
= -45,5598
Karena to = -45,5598 < -2,4469 maka hipotesis ditolak. Berarti terdapat
perbedaan yang signifikan rata-rata kadar kalium dalam buah Oyong
Lampiran 19. Pengujian Beda Nilai Rata-Rata Kadar Kalium Dalam Daun Alpukat dan Herba Pecut Kuda
No. Daun Alpukat Herba Pecut Kuda
1. X1 = 436,9877 X2 = 426,1717
2. S1 =5,5613 S2 = 3,1785
Dilakukan uji F dengan taraf kepercayaan 95% untuk mengetahui apakah variasi
kedua populasi sama (σ1 = σ2) atau bebeda (σ1 ≠ σ2 ).
− Ho : σ1 = σ2
H1 : σ1 ≠ σ2
− Nilai kritis F yang diperoleh dari tabel (F0,05/2 (3,4))adalah = 9,98
Daerah kritis penerimaan : - 9,98≤ F
o≤ 9,98
Daerah kritis penolakan : F
o < -9,98dan Fo> 9,98
Fo = 2 2 2 1 S S
Fo = 2
2
3,1785
5,5613
Fo = 3,0613
− Dari hasil ini menunjukkan bahwa Ho diterima dan H1 ditolak sehingga
disimpulkan bahwa σ1 = σ2 .simpangan bakunya adalah :
Sp =
2 ) 1 ( ) 1 ( 2 1 2 2 2 2 1 1 − ++ − − n n S n S n =
2
5
4
3,1785
1
5
5613
,
5
1
4
2 2−
−
−
+
)
(
+
)
(
= 4,3621− Ho : µ1 = µ2
− Dengan menggunakan taraf kepercayaan 95% dengan nilai α = 5% → t0,05/2 = ± 2,3646 untuk df = 4 + 5 – 2 = 7
− Daerah kritis penerimaan : -2,3646 ≤ to ≤ 2,3646
Daerah kritis penolakan : to< -2,3646 dan to> 2,3646
=
(
)
2 1
2 1
/ 1 / 1
x -x
n n
s +
=
(
)
5 1 4 1 4,3621
426,1717
-436,9877 +
= 3,6962
Karena to = 3,6962 > 2,3646 maka hipotesis ditolak. Berarti terdapat
perbedaan yang signifikan rata-rata kadar kalium dalam daun alpukat
Lampiran 20. Pengujian Beda Nilai Rata-Rata Kadar Kalium Dalam Buah Oyong dan Herba Pecut Kuda
No. Buah Oyong Herba Pecut Kuda
1. X1 = 297,3489 X2 = 426,1717
2. S1 = 0,2082 S2 = 3,1785
Dilakukan uji F dengan taraf kepercayaan 95% untuk mengetahui apakah variasi
kedua populasi sama (σ1 = σ2) atau bebeda (σ1 ≠ σ2 ).
− Ho : σ1 = σ2
H1 : σ1 ≠ σ2
− Nilai kritis F yang diperoleh dari tabel (F0,05/2 (3,4))adalah = 9,98
Daerah kritis penerimaan : - 9,98≤ F
o≤ 9,98
Daerah kritis penolakan : F
o < -9,98dan Fo> 9,98
Fo = 2 2 2 1 S S
Fo = 2
2
3,1785
2082
,
0
Fo = 0,004
− Dari hasil ini menunjukkan bahwa Ho diterima dan H1 ditolak sehingga
disimpulkan bahwa σ1 = σ2 .simpangan bakunya adalah :
Sp =
2 ) 1 ( ) 1 ( 2 1 2 2 2 2 1 1 − ++ − − n n S n S n =
2
5
4
3,1785
1
5
2082
,
0
1
4
2 2−
−
−
+
)
(
+
)
(
= 2,4065− Ho : µ1 = µ2
− Dengan menggunakan taraf kepercayaan 95% dengan nilai α = 5% → t0,05/2 = ± 2,3646 untuk df = 4 + 5 – 2 = 7
− Daerah kritis penerimaan : -2,3646 ≤ to ≤ 2,3646
Daerah kritis penolakan : to< -2,3646 dan to> 2,3646
=
(
)
2 1
2 1
/ 1 / 1
x -x
n n
s +
=
(
)
5 1 4 1 2,4065
426,1717
-297,3489 +
= -79,7995
Karena to = -79,7995 < -2,3646 maka hipotesis ditolak. Berarti terdapat
perbedaan yang signifikan rata-rata kadar kalium dalam buah oyong
Lampiran 23. Hasil Identifikasi Tanaman
Lampiran 24. Gambar Alat yang Digunakan
Alat Spektrofotometer Serapan Atom Hitachi (Z-2000
DAFTAR PUSTAKA
Almatsier, S. (2004). Prinsip Dasar Ilmu Gizi. Jakarta: PT. Gramedia Pustaka Utama. Hal. 228, 233, 234, 235, 241, 242, 243.
Arukwe, U., Amadi, B.A., Duru, M.K. (2012). Chemical composition of persea
americana leaf, fruit and seed. IJRRAS. 2012;11(2): 346- 349.
Astawan, M. (2008). Sehat dengan Buah. Jakarta : PT. Dian Rakyat. Hal. 19.
Bassett, J., Denney, R.C., Jeffery, G.H., dan Mendham, J. (1991). Vogel’s
Textbook of Quantitative Inorganic Analysis Including Elementary Instrumental Analysis. Penerjemah: Ahmad Hadiyana Pudjaatmaka dan
Lukman Setiono. (1994). Buku Ajar Vogel Kimia Analisis Kuantitatif
Anorganik. Edisi Keempat. Jakarta: Penerbit Buku Kedokteran EGC. Hal
372.
Budiyanto, M.A.K. (2001). Dasar-dasar Ilmu Gizi. Edisi Kedua. Cetakan Pertama. Malang: UMM. Press. Hal. 59.
Dalimarta, S. (2005). Atlas Tumbuhan Obat Indonesia. Volume Kedua. Hal. 129.
Damayanti, L., Trisunuwati, P., dan Murwani, S. (2013). Efek Perasan Daun dan Tangkai Semanggi Air (Marsilea crenata) Terhadap Kualitas Urin Pada Hewan Model Urolithiasis Tikus Putih (Rattus norvegicus). Student
Journal. 1(3): 11.
Depkes RI. (2008). Farmakope Herbal Indonesia. Edisi Kesatu. Jakarta: Departemen Kesehatan Republik Indonesia. Hal. 4-5.
Ditjen POM. (1989). Materia Medika Indonesia. Edisi Kelima. Jakarta: Departemen Kesehatan RI. Hal. 315, 455..
Ditjen POM. (1979). Farmakope Indonesia. Edisi Ketiga. Jakarta: Departemen Kesehatan RI. Hal. 744,748.
Ermer, J. (2005). Method Validation in Pharmaceutical Analysis. Weinheim: Wiley-VchVerlag GmbH & Co. KGaA. Hal. 171.
Gandjar, I.G., dan Rohman, A. (2009). Kimia Farmasi Analisis. Cetakan Keempat. Yogyakarta: Pustaka Pelajar. Hal. 298-299.
Harris, D.C. (2007). Quantitative Chemistry Analysis. USA: Craig Bleyer. Hal. 455.
Harmita. (2004). Petunjuk Pelaksanaan Validasi Metode dan Cara Perhitungannya. Review Artikel. Majalah Ilmu Kefarmasian. 1(3). Hal. 117-119, 121-122, 127-128, 130.
Horwitz, K. (2000). Official Methods of the Association Official Analytical
Chemist. Edisi Ketujuh Belas. Arlington: AOAC International. Hal. 43.
Khan, I.A., dan Abourashed, E.A. (2010). Leung’s Encyclopedia of Common
Natural Ingredients: Used in Food, Drugs and Cosmetics. Edisi Ketiga.
N.J.: John Wiley & Sons Inc. Hal. 671.
Khopkar, S.M. (1985). Basic Concepts of Analytical Chemistry. Penerjemah: Saptorahardjo, A. (2008). Konsep Dasar Kimia Analitik. Jakarta: UI-Press. Hal. 298.
Listiowati., Wiranti, S.R., Pri Iswati, U. (2011). Analisis Cemaran Tembaga dalam Air Sumur Industri Pelapisan Emas di Kota Tegal dengan Metode Spektrofotometri Serapan Atom. Jurnal Pharmacy. 8(3): 75.
Maryati, S., Fidrianny I, Ruslan K. (2007). Telaah kandungan kimia daun alpukat (persea americana mill.) skripsi. Bandung : Sekolah Farmasi, Intsitut Teknologi Bandung.
Nuraini, D. (2011), Aneka Manfaat Biji-bijian. Yogyakarta: Penerbit Gava Media, Hal. 11-12.
Ojewole, J.A., Kamadyaapa, D.R., Gondwe, M.M., Moodley, K., Musabayane, C.T. (2007). Cardiovascular effects of Persea americana Mill (Lauraceae) (avocado) aqueous leaf extract in experimental animals.
Cardiovasc. J. Afr. 18: 69–76.
Owolabi, MA., Jaja, SI., Coker, HA. (2005). Vasorelaxant action of aqueous extract of the leaves of Persea americana on isolated thoracic rat aorta.
Fitoterapia (76): 567–573.
Rahman, A.H.M.M., Anisuzzaman, M., Ahmad, Ferdaos., Islam, A.K.M., Rafiul, dan Naderuzzaman, A.T.M. (2008). Study Of Nutritive Value and Medical Uses of Cultivated Cucurbits. Journal Of applied Sciences Research, 4(5): 555-558.
Rodriguez, SM., dan Castro, O. (1996). Evaluation Farmacologica quimica de Stachytarpheta jamaicensis (Verbenacea). Revista de Bivl Trop. 44(1): 353-359.
Stephens, J. M. (2003). Gourd, Luffa-Luffa cylindrica (L.) Roem., Luffa aegyptica
Mill and Luffa acutangula L. Roxb. Florida. Hal. 1-2.
Sudjana. (2005). Metode Statistika. Edisi Keenam. Bandung: Tarsito. Hal. 93, 168, 239.
Tjay, T.H., dan Rahardja, K. (2007). Obat-obat Penting Khasiat, Penggunaan dan
Efek-efek Sampingnya. Edisi Ketujuh. Cetakan. Pertama. Jakarta: PT Elex
Media Komputindo Kelompok Kompas-Gramedia. Hal. 625, 698, 840.
V., Jyothi., Ambati, Srinath., dan V., Asha Jyothi. (2010). The Pharmacognostic, Phytochemical and Pharmacological Profile of Luffa acutangula.
International Journal Of Pharmacy & Technology, 2(4): 512-524.
Vogel, A.I. (1979). Textbook of Macro and Semimicro Qualitative Inorganic
Analysis. Penerjemah: Setiono dan Hadyana Pudjaaatmaka. (1990). Vogel: Buku Teks Analisis Anorganik Kualitatif Makro dan Semimikro. Bagian
Pertama. Jakarta: Kalman Media Pustaka. Hal. 308.
Wibowo, S. (2013). Herbal Ajaib tumpas macam-macam penyakit, Cetakan. Pertama. Pustaka Makmur. Hal. 17.
Wijayakusuma, H. (1994). Tanaman Berkhasiat Obat di Indonesia, Jilid kedua. Pustaka Kartini, Jakarta. Hal. 20, 45, 46, 50.
BAB III
METODE PENELITIAN
Metode penelitian ini dilakukan secara deskriptif yaitu suatu metode
penelitian dimana peneliti menggambarkan atau menganalisis suatu hasil yang ada
di masyarakat tanpa memberikan kontrol atau perlakuan terhadap sampel.
3.1 Tempat dan Waktu Penelitian
Penelitian ini dilakukan di Laboratorium Kimia Farmasi Kualitatif dan di
Laboratorium Penelitian Fakultas Farmasi Universitas Sumatera Utara pada bulan
Maret sampai Juni 2015.
3.2 Bahan-bahan 3.2.1 Sampel
Sampel yang digunakan dalam penelitian ini adalah buah oyong (Luffa
acutangula (L.) Roxb.), daun alpukat (Persea americana Mill.) dan herba pecut
kuda (Stachytarpheta jamaicensis (L.) Vahl.) yang diambil secara purposif di
kota Pematang Siantar, Kecamatan Siantar Utara di daerah Parluasan.
3.2.2 Pereaksi
Bahan yang digunakan adalah pro analisis produksi E. Merck kecuali
HNO3 65%, asam pikrat, larutan baku kalium 1000 µg/ml dan aqua demineralisata
3.3 Alat-alat
Spektrofotometer Serapan Atom (Hitachi Z-2000) lengkap dengan lampu
katoda kalium, tanur (Stuart), hot plate, kertas saring Whatman No. 42, neraca
analitik, krus porselen, spatula dan alat-alat gelas.
3.4 Identifikasi Sampel
Identifikasi sampel dilakukan oleh bagian Herbarium Bogoriense Bidang
Botani Pusat Penelitian Biologi-LIPI Bogor.
3.5 Pembuatan Pereaksi 3.5.1 Larutan HNO3 (1:1)
Diencerkan sebanyak 50 mL larutan HNO3 65% dengan 50 mL air suling
(Ditjen, POM., 1979).
3.5.2 Larutan Asam Pikrat 1% b/v
Larutan asam pikrat 1 % dibuat dengan melarutkan 1 g asam pikrat dalam
aqua demineralisata hingga 100 mL (Ditjen, POM., 1979).
3.6 Prosedur Penelitian 3.6.1 Pengambilan Sampel
Sampel yang digunakan adalah buah oyong, daun alpukat dan herba pecut
kuda yang diambil di daerah Parluasan Pematang Siantar, Provinsi Sumatera
Utara. Metode pengambilan sampel dilakukan dengan cara purposif sampling,
yaitu sampel ditentukan atas dasar pertimbangan bahwa sampel yang diambil
3.6.2 Penyiapan Sampel
Masing-masing sampel (buah oyong, daun alpukat, herba pecut kuda)
segar dibersihkan dari pengotoran, dicuci dengan akua demineralisata, lalu
ditiriskan dan dikeringkan dengan cara diangin-anginkan kemudian dirajang.
3.6.3 Proses Destruksi Kering
Masing-masing Sampel (buah oyong, daun alpukat, herba pecut kuda)
yang telah dirajang ditimbang sebanyak 25 g (buah oyong, daun alpukat, herba
pecut kuda), dimasukkan ke dalam krus porselen, kemudian diarangkan di atas hot
plate selama 10 jam. didinginkan, lalu diabukan dalam tanur dengan temperatur
awal 1000C dan perlahan-lahan temperatur dinaikkan hingga suhu 5000C dengan
interval 250C setiap 5 menit. Pengabuan dilakukan selama 60 jam dan setelah itu
di biarkan hingga dingin, kemudian dipindahkan ke desikator. Ditambahkan 5 mL
HNO3 (1:1) ke dalam abu, kemudian diuapkan pada hot plate sampai kering. Krus
porselen dimasukkan kembali ke dalam tanur dengan temperatur awal 1000C dan
perlahan-lahan temperature dinaikkan hingga suhu 5000C dengan interval 250C
setiap 5 menit. Pengabuan dilakukan selama 1 jam dan dibiarkan hingga dingin
dan dipindahkan ke desikator (Horwitz, 2000).
3.6.4 Pembuatan Larutan Sampel
Hasil destruksi dilarutkan dalam 5 mL HNO3 (1:1) hingga diperoleh
larutan bening. Kemudian dimasukkan ke dalam labu tentukur 50 mL dan krus
porselen dibilas dengan aqua demineralisata sebanyak 3 kali. Hasil pembilasan
dimasukkan ke dalam labu tentukur. Setelah itu dicukupkan volumenya dengan
aqua demineralisata hingga garis tanda. Lalu disaring dengan kertas saring
selanjutnya ditampung ke dalam botol (Horwitz, 2000). Larutan ini digunakan
untuk uji kualitatif dan kuantitatif kalium.
3.6.5 Analisa Kualitatif Kalium 3.6.5.1 Uji Nyala Ni/Cr
Bersihkan kawat Ni/Cr dengan HCl pekat lalu dipijar pada api bunsen
sampai tidak memberikan warna khusus pada nyala bunsen. Kemudian celupkan
kawat pada sampel lalu dipijar pada api bunsen, amati warna yang terjadi pada
nyala bunsen. Jika terdapat kalium, akan terbentuk warna ungu pada nyala
bunsen.
3.6.5.2 Uji Kristal Kalium dengan Asam Pikrat
Larutan sampel diteteskan 1-2 tetes pada objek glass kemudian ditetesi
dengan larutan asam pikrat, dibiarkan ± 5 menit lalu diamati di bawah mikroskop.
Jika terdapat kalium, akan terlihat kristal berbentuk jarum kasar (Vogel, 1979).
3.6.6 Analisa Kuantitatif
3.6.6.1 Pembuatan Kurva Kalibrasi Kalium
Larutan baku kalium (1000 µg/mL) dipipet sebanyak 5 mL, dimasukkan
ke dalam labu tentukur 50 mL dan dicukupkan hingga garis tanda dengan akua
demineralisata (konsentrasi 100 µg/mL). Larutan untuk kurva kalibrasi kalium
dibuat dengan memipet (0,5; 1; 1,5; 2 dan 2,5) mL larutan baku 100 µg/mL,
masing-masing dimasukan ke dalam labu tentukur 25 mL dan dicukupkan hingga
garis tanda dengan akua demineralisata (konsentrasi larutan 2,0; 4,0; 6,0; 8,0 dan
10,0 µg/mL) dan diukur pada panjang gelombang 766,5 nm dengan nyala
3.6.6.2 Penetapan Kadar Kalium
Larutan sampel hasil destruksi dari (buah oyong, daun alpukat, dan herba
pecut kuda) sebanyak 0,1 mL, dimasukkan ke dalam labu tentukur 50 mL (faktor
pengenceran = 500 kali) dan dicukupkan dengan akua demineralisata hingga garis
tanda. Lalu diukur absorbansinya dengan menggunakan spektrofotometer serapan
atom yang telah dikondisikan dan diatur metodenya, dimana pengujian kadar
kalium dilakukan pada panjang gelombang 766,5 nm. Nilai absorbansi yang
diperoleh harus berada dalam rentang kurva kalibrasi larutan baku kalium.
Konsentrasi kalium dalam sampel ditentukan berdasarkan persamaan garis regresi
dari kurva kalibrasi.
3.6.7 Analisis Data Secara Statistik 3.6.7.1 Penolakan Hasil Pengamatan
Kadar mineral kalium yang diperoleh dari hasil pengukuran
masing-masing larutan sampel dianalisis secara statistik.Menurut Sudjana (2005), standar
deviasi dapat dihitung dengan rumus:
SD =
( )
1 -n
X -Xi 2
∑
Keterangan :
Xi = Kadar sampel
X = Kadar rata-rata sampel n = jumlah perulangan (replikasi)
Kadar kalium yang diperoleh dari hasil pengukuran masing-masing ke
Untuk mengetahui data ditolak atau diterima dilakukan dengan uji t yang
dapat dihitung dengan rumus:
thitung =
Hasil pengujian atau nilai thitung yang diperoleh ditinjau terhadap tabel distribusi t,
apabila thitung > ttabel maka data tersebut ditolak.
Menurut Sudjana (2005), untuk menentukan kadar kalium di dalam sampel
dengan tingkat kepercayaan 95%,
α = 0,05, dk = n-1, dapat digunakan rumus:
µ = X ± t (½α,dk) x (SD/ )
Keterangan :
µ = kadar sebenarnya (mg/100 g) X = kadar rata-rata sampel (mg/100 g) t = harga t tabel sesuai dengan dk = n-1
α = tingkat kepercayaan SD = standar deviasi (mg/100 g)
n = jumlah perulangan
3.6.8 Validasi Metode Analisis
3.6.8.1 Penentuan Batas Deteksi dan Batas Kuantitasi
Batas deteksi merupakan jumlah terkecil analit dalam sampel yang dapat
dideteksi yang masih memberikan respon signifikan. Sedangkan batas kuantitasi
merupakan kuantitas terkecil analit dalam sampel yang masih dapat memenuhi
kriteria cermat dan seksama.
Menurut (Harmita, 2004) batas deteksi dan batas kuantitasi ini dapat
Simpangan baku =
Batas Deteksi (LOD) =
Batas Kuantitasi (LOQ) =
3.6.8.2 Uji Akurasi (Recovery)
Uji akurasi (recovery) dilakukan dengan metode penambahan larutan standar
(standard addition method). Dalam metode ini, kadar mineral dalam sampel
ditentukan terlebih dahulu, selanjutnya dilakukan penentuan kadar mineral dalam
sampel setelah penambahan larutan baku dengan konsentrasi tertentu (Ermer,
2005).
Sampel buah oyong yang telah diketahui kadarnya, dirajang dan ditimbang
secara seksama sebanyak 25 g, lalu ditambahkan 1 mL larutan baku kalium
(konsentrasi 100 µg/mL), kemudian dilanjutkan dengan prosedur destruksi kering
seperti yang telah dilakukan sebelumnya. Prosedur pengukuran uji perolehan
kembali dilakukan sama dengan prosedur penetapan kadar dalam sampel.
Menurut Harmita (2004), persen perolehan kembali dapat dihitung dengan
rumus di bawah ini:
% Perolehan Kembali = A
A F
C C C
*
− x 100%
Keterangan:
CA = Kosenterasi logam dalam sampel sebelum penambahan baku
CF = Kosenterasi logam dalam sampel setelah penambahan baku
3.6.8.3 Uji Presisi
Keseksamaan atau presisi diukur sebagai simpangan baku relatif atau
koefisien variasi. Keseksamaan atau presisi merupakan ukuran yang menunjukkan
derajat kesesuaian antara hasil uji individual ketika suatu metode dilakukan secara
berulang untuk sampel yang relatif. Nilai simpangan baku relatif yang memenuhi
persyaratan menunjukkan adanya keseksamaan metode yang dilakukan.
Menurut Harmita (2004), rumus untuk menghitung simpangan baku relatif
adalah sebagai berikut:
RSD = ×100% X
SD
Keterangan : X = Kadar rata-rata sampel (mg/100 g) SD = Standar Deviasi (mg/100 g)
BAB IV
HASIL DAN PEMBAHASAN
4.1 Identifikasi Tumbuhan
Identifikasi tumbuhan dilakukan di Herbarium Bogoriense Bidang Botani
Pusat Penelitian Biologi LIPI Bogor. Hasil identifikasi dapat dilihat pada Tabel
4.1 dan Lampiran 20 halaman 67.
Tabel 4.1 Hasil Identifikasi Tanaman
Sampel Jenis Suku
Buah oyong Luffa acutangula (L.) Roxb. Cucurbitaceae
Daun alpukat Persea americana Mill. Lauraceae Herba Pecut kuda Stachytarpheta jamaicensis (L.) Vahl Lamiaceae
4.2 Analisis Kualitatif
Analisis kualitatif dilakukan sebagai analisis pendahuluan untuk
[image:50.595.113.523.590.748.2]mengidentifikasi mineral kalium. Data hasil analisis kualitatif dapat dilihat pada
[image:50.595.108.534.591.749.2]Tabel 4.2 dan Lampiran 6 halaman 42.
Tabel 4.2 Hasil Analisis Kualitatif Ion yang
dianalisis
Pereaksi Hasil Reaksi Hasil
BO HPK DA
Kalium Uji Nyala menggunakan
kawat Ni/Cr
Warna Nyala Ungu
+ + +
Asam pikrat 1% b/v
Kristal jarum
kasar + + +
Hasil pada Tabel 4.2 menunjukkan bahwa buah oyong, daun alpukat dan
herba pecut kuda positif mengandung kalium. Sampel dinyatakan positif
mengandung mineral kalium karena menghasilkan endapan kuning dengan
penambahan asam pikrat 1% b/v, kemudian diamati secara mikroskopis berupa
kristal bentuk jarum kasar serta memberikan nyala warna ungu setelah dilakukan
uji nyala dengan menggunakan kawat Nikel-Krom (Vogel, 1979).
Hasil serapan dengan spektrofotometer serapan atom juga menunjukkan
adanya serapan pada panjang gelombang kalium 766,50 nm dengan menggunakan
lampu katoda kalium. Hal ini juga membuktikan secara kualitatif bahwa sampel
mengandung mineral kalium.
4.3 Analisis Kuantitatif
4.3.1 Kurva Kalibrasi Kalium
Kurva kalibrasi kalium diperoleh dengan cara mengukur absorbansi dari
beberapa konsentrasi larutan baku kalium pada panjang gelombang 766,50 nm.
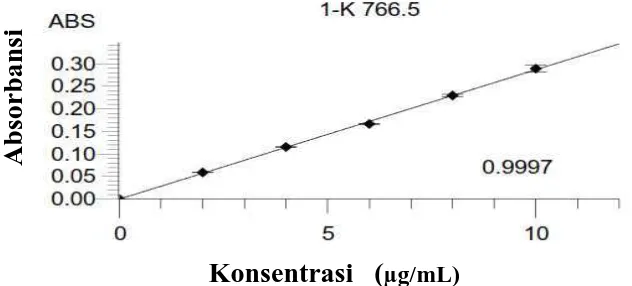
Dari pengukuran kurva kalibrasi diperoleh persamaan regresi yaitu Y = 0,02866 X
[image:51.595.123.439.561.704.2]– 0,000134. Kurva Kalibrasi kalium dapat dilihat pada Gambar 4.1.
Gambar 4.1. Kurva kalibrasi kalium
Ab
sor
b
an
si
Berdasarkan kurva di atas diperoleh hubungan yang linear antara
konsentrasi dengan absorbansi, dengan koefisien korelasi (r) kalium sebesar
0,9997. Menurut Erner dan McB. Miller, 2005, Nilai r ≥ 0,997 menunjukkan
adanya korelasi linear antara X (konsentrasi) dan Y (absorbansi). dilihat pada
Lampiran 7 halaman 43-44.
4.3.2 Kadar Kalium Dalam Buah Oyong, Daun Alpukat dan Herba Pecut Kuda
Konsentrasi mineral kalium pada sampel ditentukan berdasarkan persamaan
garis regresi pada kurva kalibrasi mineral tersebut. Data hasil penetapan kadar
kalium pada sampel secara kuantitatif ini dapat dilihat pada Lampiran 8 halaman
45. Contoh perhitungan dapat dilihat pada Lampiran 9 halaman 46-47. Pengujian
dilanjutkan dengan perhitungan statistik yang dapat dilihat pada Lampiran 10 – 12
[image:52.595.110.524.485.600.2]halaman 48-50. Hasil pengukuran kadar kalium pada sampel dapat dilihat pada
Tabel 4.3.
Tabel 4.3. Hasil pengukuran kadar kalium pada sampel
No Sampel Kadar Kalium (mg/100 g)
1. Buah Oyong 297,3489 ± 0,2675
2. Daun Alpukat 436,99877 ± 7,1479
4. Herba Pecut Kuda 426,1717 ± 0,8522
Berdasarkan hasil analisis kadar mineral kalium yang tercantum pada Tabel
4.3 daun alpukat mengandung kalium yang paling tinggi dibandingkan buah
oyong dan herba pecut kuda. Daun alpukat memiliki kandungan kalium yang
tinggi. Kalium diperlukan untuk keseimbangan elektrolit dan mengontrol tekanan
mengobati kencing batu, darah tinggi, sakit kepala, nyeri syaraf, sakit pinggang,
nyeri lambung, saluran nafas membengkak, dan menstruasi tidak teratur (Hariana,
2009).
4.3.3 Perbandingan kadar kalium buah oyong, daun alpukat dan herba pecut kuda.
Perbandingan kadar kalium buah oyong, daun alpukat dan herba pecut
[image:53.595.117.511.261.463.2]kuda dapat dilihat pada Gambar 4.2 dibawah ini.
Gambar 4.2. Perbandingan kadar kalium buah oyong, daun alpukat dan herba pecut kuda.
4.4 Validasi Metode
4.4.1 Batas Deteksi dan Batas Kuantitasi
Berdasarkan data kurva kalibrasi kalium diperoleh batas deteksi 0,3343
µg/mL dan batas kuantitasi 1,1146 µg/mL untuk ketiga sampel tersebut. Dari hasil
perhitungan dapat dilihat bahwa semua hasil yang diperoleh pada pengukuran
sampel berada di atas batas deteksi dan batas kuantitasi. Perhitungan batas deteksi
4.4.2 Uji Akurasi (Recovery)
Rata-rata hasil uji akurasi (recovery) untuk kalium 98,16 %. Persen
perolehan kembali tersebut menunjukkan kecermatan kerja yang memuaskan pada
saat pemeriksaan kadar kalium dalam sampel. Hasil yang diperoleh dari uji
akurasi memberikan ketepatan pada pemeriksaan kadar kalium dalam sampel.
Menurut Ermer (2005), suatu metode dikatakan teliti jika nilai recoverynya antara
95-105%. Perhitungan persen perolehan kembali dapat dilihat pada Lampiran 16
halaman 60-63.
4.4.3 Uji Presisi
Nilai simpangan baku (SD) untuk kalium adalah sebesar 0,0090 sedangkan
uji presisi untuk kalium sebesar 0,18%. Perhitungan simpangan baku dapat dilihat
pada Lampiran 17 Halaman 64. Menurut Harmita (2004), nilai simpangan baku
relatif (RSD) untuk analit dengan kadar part per million (ppm) adalah tidak lebih
dari 16% dan untuk analit dengan kadar part per billion (ppb) RSD nya adalah
tidak lebih dari 32%. Dari hasil yang diperoleh menunjukkan bahwa metode yang
BAB V
KESIMPULAN DAN SARAN
5.1 Kesimpulan
a. Hasil analisis kuantitatif dengan menggunakan spektrofotometer serapan
atom menunjukkan bahwa kadar kalium paling tinggi terdapat pada daun
alpukat. Kadar kalium dalam buah oyong, daun alpukat dan herba pecut
kuda masing-masing (297,3489 ± 0,2675) mg/100 g, daun alpukat sebesar
(436,99877 ± 7,1479) mg/100 g dan herba pecut kuda (426,1717 ± 0,8522)
mg/100 g.
b. Hasil penelitian menunjukkan adanya perbedaan pada kadar kalium yang
terdapat dalam buah oyong dengan daun alpukat dan herba pecut kuda,
kadar kalium paling tinggi terdapat pada daun alpukat.
5.2 Saran
Disarankan kepada peneliti selanjutnya untuk menentukan kadar kalium dari
buah oyong, daun alpukat dan herba pecut kuda dalam air rebusan dari buah
BAB II
TINJAUAN PUSTAKA
2.1 Oyong (Gambas)
Tumbuhan oyong (gambas) berasal dari India kemudian menyebar ke
berbagai negara yang beriklim tropis. Tumbuhan oyong (gambas) berbatang lunak
dengan bentuk segi lima, tumbuh merambat atau menjalar, serta mempunyai sulur
yang digunakan sebagai alat untuk merambat. Sulur muncul dari ketiak daun,
berbentuk spiral dan mempunyai bulu yang lebih panjang dari pada bulu-bulu
batang. Daunnya tunggal berwarna hijau tua, bentuk lonjong (silindris) dengan
pangkal mirip bentuk jantung, puncak daun meruncing dan permukaan daun
kasar. Daun berukuran panjang 10 cm - 25 cm dan bertangkai sepanjang 5 cm - 10
cm, tulang daun menonjol pada permukaan bawah. Bunganya berkelamin satu
(monoecus) yaitu bunga jantan dan betina terdapat dalam satu tanaman. Bunganya
berwarna kuning, dapat menyerbuk sendiri (self pollination) dan menyerbuk
silang (cross pollination). Buah gambas berbentuk bulat panjang dengan bagian
pangkal kecil. Buah berukuran panjang 15 cm - 60 cm, lebar 5 cm - 12 cm dengan
diameter 5 cm - 8 cm. Tiap buah berbiji banyak dan tiap biji berukuran 11 - 13
mm x 7 - 9 mm dengan struktur kulit agak keras (Rukmana, 2000). Buah yang
sudah tua berwarna hijau kecoklatan hingga kuning coklat, dan kulit biji berwarna
hitam dan keras. Buah yang sudah tua mengandung serat-serat kasar yang sering
dipergunakan sebagai spons (Stephens, 2003).
Menurut Herbarium Bogoriense (2015), taksonomi Buah Oyong adalah
Kingdom : Plantae
Divisi : Spermatophyta
Sub Divisi : Angiospermae
Kelas : Dicotyledoneae
Ordo : Cucurbitales
Famili : Cucurbitaceae
Genus : Luffa
Spesies : Luffa acutangula (L.) Roxb.
Kandungan kimia buah oyong termasuk karbohidrat, karoten, lemak,
protein, asam amino, alanine, arginine, sistin, asam glutamate, glisin,
hidroksiprolin, serin, triptofan, asam pipekolat, flavonoid dan saponin. Dalam
buah oyong juga terdapat kandungan senyawa yang memberikan rasa pahit yakni
lufein (V., Jyothi, dkk. 2010). Secara tradisional buah oyong digunakan untuk
memperlancar aliran darah dan memfasilitasi aliran energi dalam tubuh serta
memiliki efek anti inflamasi, menurunkan demam, dapat bermanfaat dalam
detoksifikasi racun. Buah oyong juga dapat digunakan mengatasi rematik, nyeri
sendi, otot, nyeri dada dan memperbanyak asi serta menghilangkan jaringan kulit
mati (Khan dan Abourashed, 2010). Buah oyong secara empiris diketahui
memiliki efek diuretik yang dapat membantu menurunkan tekanan darah
(Rahman, dkk., 2008).
2.2 Alpukat
Pohon buah alpukat berasal dari Amerika tengah, tumbuh liar di
gembur dan subur serta tidak tergenang air. Pohon kecil, tinggi 3 - 10 m, berakar
tunggang, batang berkayu, bulat, warnanya coklat kotor, banyak bercabang,
ranting berambut halus. Daun tunggal, bertangkai yang panjangnya 1,5 - 5 cm,
kotor, letaknya berdesakan di ujung ranting, bentuknya jorong sampai bundar
telur memanjang, tebal seperti kulit ujung dan pangkal yang runcing. Tepi rata
kadang agak menggulung keatas, betulang menyirip, panjang 10 - 20 cm, lebar 3 -
10 cm, daun muda warnanya kemerahan dan berambut rapat, daun tua warnaya
hijau dan gundul (Depkes, RI, 2010).
Menurut Herbarium Bogoriense (2015), taksonomi alpukat adalah sebagai
berikut:
Kingdom : Plantae
Divisi : Spermatophyta
Sub Divisi : Angiospermae
Kelas : Dicotyledoneae
Ordo : Laurales
Famili : Lauraceae
Genus : Persea
Spesies : Persea americana Mill.
Daun alpukat memiliki elemen mineral yang penting manfaatnya bagi
kesehatan. Tanaman ini memiliki kandungan natrium, kalium, kalsium,
magnesium, fosfor dan mineral lainnya (Arukwe, dkk, 2012). Buah dan daun buah
alpukat mengandung saponin, alkaloida, flavonoida dan tanin. daun alpukat
Berdasarkan penelitian, daun alpukat memiliki aktifitas antioksidan dan
membantu dalam mencegah atau memperlambat kemajuan berbagai oksidatif stres
yang berhubungan dengan penyakit. Konsumsi ekstrak daun alpukat diketahui
dapat menurunkan tekanan darah pada penderita hipertensi secara signifikan,
menurunkan kadar glukosa darah serta dapat menurunkan kadar ureum dan
kreatinin pada ginjal (Owolabi, dkk., 2010). Dalam penelitian yang dilakukan oleh
Ojewole, dinyatakan bahwa daun alpukat berpengaruh terhadap penurunan
tekanan darah melalui efek vasorelaksan yang dimilikinya (Ojewole, dkk., 2007).
Daun alpukat berkhasiat untuk kencing batu, darah tinggi dan sakit kepala, nyeri
saraf, nyeri lambung, saluran nafas membengkak dan menstrusasi tidak teratur
(Yuniarti, 2008).
2.3 Pecut Kuda
Pecut kuda merupakan suatu tumbuhan liar di tepi jalan, tanah lapang dan
tempat terlantar lainnya. tanaman yang dari Amerika tropis ini dapat ditemukan di
daerah cerah, terlindung dari sinar matahari dan pada ketinggian 1-1500 m.
Tumbuh tegak, tinggi 20-90 cm. Daun tunggal, bertangkai, letak berhadapan.
Helaian daun berbentuk bulat telur, pangkal menyempit, ujung runcing, tepi
bergerigi, permukaan jelas berlekuk-lekuk, panjang 4-8 cm, lebar 3-6 cm,
berwarna hijau tua. Bunga majemuk tersusun dalam poros bulir yang memanjang,
seperti pecut, panjangnya 1-20 cm. Bunga mekar dalam waktu yang berbeda,
ukuran kecil, berwarna ungu. Buah berbentuk garis, berbiji dua. Biji berbentuk
Menurut Herbarium Bogoriense (2015), taksonomi pecut kuda adalah
sebagai berikut:
Kingdom : Plantae
Divisi : Spermatophyta
Sub Divisi : Angiospermae
Kelas : Dicotyledoneae
Ordo : Lamiales
Famili : Lamiaceae
Genus : Stachytarpheta
Spesies : Stachytarpheta jamaicensis (L.) Vahl
Pecut kuda mengandung glikosida, flavonoid dan alkaloid. Tanaman ini
rasanya pahit dan sifatnya dingin sering digunakan untuk mengobati infeksi dan
batu saluran kemih, (sakit tenggorokan karena radang (faringitis), batuk, rematik,
pebersih darah, keputihan dan hepatitis A (Dalimarta, 2005).
2.4 Kalium
Kalium adalah logam putih perak yang lunak. Logam ini melebur pada
63,5˚C. kalium tetap tidak berubah dalam udara kering, tetapi dengan cepat
teroksidasi dalam udara lembab, menjadi tertutup dengan suatu lapisan biru.
Garam – garam kalium mengandung kation monovalent K+, biasanya larut dan
membentuk larutan tidak berwarna, kecuali jika anionnya berwarna (vogel, 1979).
Kalium merupakan salah satu mineral makro yang berperan dalam
pengaturan keseimbangan cairan tubuh. Sebanyak 95% kalium berada di dalam
pemeliharaan keseimbangan cairan dan elektrolit serta keseimbangan asam basa
serta isotonis sel, selain itu kalium juga mengaktivasi banyak reaksi enzim dan
proses fisiologi, seperti transmisi impuls di saraf dan otot, kontraksi otot dan
metabolism karbohidrat (Tjay dan Rahardja, 2007).
Kalium diabsorpsi dengan mudah dalam usus halus. Sebanyak 80-90%
kalium yang dimakan diekskresikan melalui urin, selebihnya dikeluarkan melalui
feses, keringat dan cairan lambung. Taraf kalium normal darah dipelihara oleh
ginjal melalui kemampuannya menyaring, mengabsorbsi kembali dan
mengeluarkan kalium dibawah pengaruh aldosterone. Kalium dikeluarkan dalam
bentuk ion dengan menggantikan ion natrium melalui mekanisme pertukaran
didalam ginjal (Almatsier, 2004).
Konsumsi kalium dalam jumlah yang tinggi dapat melindungi individu
dari hipertensi. Konsumsi kalium yang banyak akan meningkatkan konsentrasinya
di dalam cairan intraselular, sehingga cenderung menarik cairan dari bagian
ekstraselular dan menurunkan tekanan darah. Rasio kalium dan natrium dalam
diet berperan dalam mencegah dan mengendalikan hipertensi (Muliyati, dkk.,
2011). Kekurangan kalium dapat terjadi karena terjadinya kehilangan melalui
saluran cerna dan ginjal. Kekurangan kalium menyebabkan lemah, lesu,
kehilangan nafsu makan, dan konstipasi. Kelebihan kalium akut dapat terjadi bila
konsumsi tidak diimbangi oleh kenaikan ekskresi (Winarno, 1992).
Bahan pangan yang mengandung kalium baik dikonsumsi oleh penderita
darah tinggi (Budiyanto, 2004). Konsumsi kalium yang banyak akan
meningkatkan konsentrasinya di dalam cairan intraseluler sehingga cenderung
(Astawan, 2008). Kebutuhan minimum akan kalium kurang lebih 2000 mg sehari
(Almatsier, 2004).
2.5 Spektrofotometri Serapan Atom
2.5.1 Prinsip dasar spektrofotometri serapan atom
Spektrofotometri serapan atom didasarkan pada penyerapan energi sinar
oleh atom-atom netral, dan sinar yang diserap biasanya sinar tampak atau sinar
ultraviolet (Gandjar dan Rohman, 2007). Spektrofotometri serapan atom
digunakan untuk kuantitatif unsur-unsur mineral dalam jumlah sekelumit (trace)
dan sangat sekelumit (ultratrace). Cara ini cocok untuk analisis logam karena
mempunyai kepekaan yang tinggi (batas deteksi kurang dari 1 ppm),
pelaksanaannya relatif sederhana, dan interferensinya sedikit (Gandjar dan
Rohman, 2007).
Metode spektrofotometri serapan atom berprinsip pada absorbsi cahaya
oleh atom. Atom-atom akan menyerap cahaya pada panjang gelombang tertentu
tergantung pada sifat unsurnya. Sebagai contoh kalium menyerap cahaya pada
panjang gelombang 766,5 nm. Cahaya pada panjang gelombang ini mempunyai
cukup energi untuk mengubah tingkat elektronik suatu atom. Dengan menyerap
suatu energi, maka atom akan memperoleh energi sehingga suatu atom pada
keadaan dasar dapat dinaikkan tingkat energinya ke tingkat eksitasi (Gandjar dan
Rohman, 2007).
Interaksi materi dengan berbagai energi seperti energi panas, energi
radiasi, energi kimia, dan energi listrik selalu memberikan sifat-sifat yang spesifik
jumlah unsur atau persenyawaan yang terdapat didalamnya. Proses interaksi ini
mendasari analisis spektrofotometri atom yang dapat berupa emisi dan absorpsi
(Gandjar dan Rohman, 2007).
2.5.2 Instrumentasi spektrofotometri serapan atom
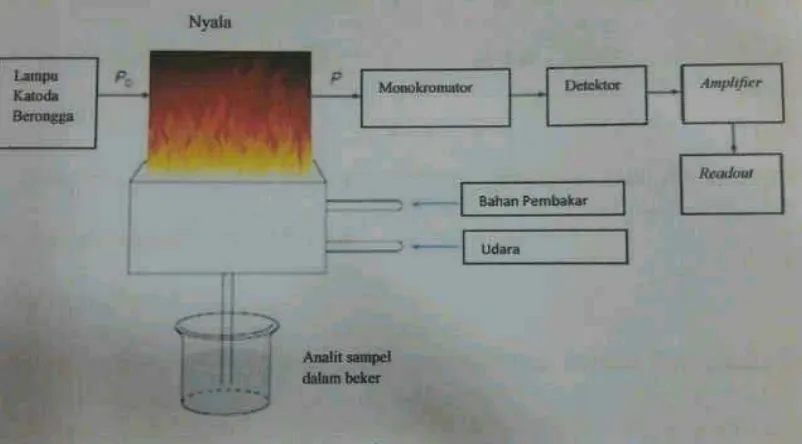
[image:63.595.114.515.251.473.2]Sistem peralatan spektrofotometer serapan atom dapat dilihat pada Gambar 2.1.
Gambar 2.1 Komponen Spektrofotometer Serapan Atom (Harris, 2007) a. Sumber sinar
Sumber sinar yang umum dipakai adalah lampu katoda berongga (hollow
cathode lamp). Lampu ini terdiri atas tabung kaca tertutup yang mengandung
suatu katoda dan anoda. Katoda berbentuk silinder berongga yang terbuat dari
unsur atau dilapisi unsur yang sama dengan unsur yang akan dianalisis. Tabung
logam ini diisi dengan gas mulia dengan tekanan rendah yang jika diberikan
tegangan pada arus tertentu, katoda akan memancarkan elektron-elektron yang
bergerak menuju anoda dengan kecepatan dan energi yang tinggi. Elektron dengan
kehilangan elektron dan menjadi ion bermuatan positif. Ion gas mulia bermuatan
positif akan bergerak menuju katoda dengan kecepatan dan energi yang tinggi
sehingga menabrak unsur-unsur yang terdapat pada katoda. Akibat tabrakan ini,
unsur-unsur akan terlempar ke luar permukaan katoda dan mengalami eksitasi ke
tingkat energi elektron yang lebih tinggi (Gandjar dan Rohman, 2007).
b. Tempat sampel
Dalam analisis dengan spektrofotometri serapan atom, sampel yang akan
dianalisis harus diuraikan menjadi atom-atom netral. Ada berbagai macam alat
yang dapat digunakan untuk mengubah suatu sampel menjadi uap atom-atom
yaitu dengan nyala (flame) dan tanpa nyala (flameless) (Gandjar dan Rohman,
2007).
Teknik atomisasi dengan nyala bergantung pada suhu yang dapat dicapai
oleh gas-gas yang digunakan. Untuk gas batubara-udara suhunya kira-kira sebesar
1800ºC, gas alam-udara 1700ºC, gas udara 2200ºC, dan gas
asetilen-dinitrogen oksida sebesar 3000ºC. Sumber nyala yang paling banyak digunakan
adalah campuran asetilen sebagai bahan pembakar dan udara sebagai pengoksidasi
(Gandjar dan Rohman, 2007).
Teknik atomisasi tanpa nyala dapat dilakukan dengan meletakkan
sejumlah sampel didalam tungku dari grafit kemudian dipanaskan dengan sistem
elektris dengan cara melewatkan arus listrik pada tabung grafit. Akibat pemanasan
ini, zat yang akan dianalisis akan berubah menjadi atom-atom netral dan
dilewatkan suatu sinar yang berasal dari lampu katoda berongga sehingga terjadi
c. Monokromator
Pada spektrofotometri serapan atom, monokromator berfungsi untuk
memisahkan dan memilih panjang gelombang yang digunakan untuk analisis. Di
dalam monokromator, terdapat suatu alat yang digunakan untuk memisahkan
panjang gelombang yang disebut dengan chopper (Gandjar dan Rohman, 2007).
d. Detektor
Detektor digunakan untuk mengukur intensitas cahaya yang melalui
tempat pengatoman (Gandjar dan Rohman, 2007).
e. Readout
Readout merupakan suatu alat penunjuk atau dapat juga diartikan sebagai
sistem pencatatan hasil. Pencatatan hasil dilakukan dengan suatu alat yang telah
terkalibrasi untuk pembacaan suatu transmisi atau absorbsi. Hasil pembacaan
dapat berupa angka atau kurva dari suatu alat perekam yang menggambarkan
absorbansi atau intensitas emisi (Gandjar dan Rohman, 2007).
2.5.3 Gangguan-gangguan pada spektrofotometri serapan atom
Gangguan-gangguan (interference) pada Spektrofotometri Serapan Atom
adalah peristiwa-peristiwa yang menyebabkan pembacaan absorbansi unsur yang
dianalisis menjadi lebih kecil atau lebih besar dari nilai yang sesuai dengan
konsentrasinya dalam sampel (Gandjar dan Rohman, 2007).
Menurut Gandjar dan Rohman (2007), gangguan-gangguan yang terjadi
pada spektrofotometri serapan atom adalah:
1. Gangguan yang berasal dari matriks sampel yang mana dapat mempengaruhi
2. Gangguan kimia yang dapat mempengaruhi jumlah atau banyaknya atom
yang terjadi di dalam nyala.
3. Gangguan oleh absorbansi yang disebabkan bukan absorbansi atom yang
dianalisis, yakni absorbansi oleh molekul-molekul yang terdisosiasi di dalam
nyala.
4. Gangguan oleh penyerapan non-atomik.
2.6 Validasi Metode Analisis
Validasi metode analisis adalah suatu tindakan penilaian terhadap
parameter tertentu, berdasarkan percobaan laboratorium, untuk membuktikan
bahwa parameter tersebut memenuhi persyaratan untuk penggunaannya. Tindakan
ini dilakukan untuk menjamin bahwa metode analisis akurat, spesifik,
reprodusibel, dan tahan akan kisaran analit yang akan dianalisis (Harmita, 2004).
Beberapa parameter analisis yang harus dipertimbangkan dalam validasi
metode analisis adalah sebagai berikut:
1. Kecermatan (accuracy)
Kecermatan adalah ukuran yang menunjukkan derajat kedekatan hasil
analis dengan kadar analit yang sebenarnya. Kecermatan dinyatakan sebagai
persen perolehan kembali (recovery) analit yang ditambahkan. Untuk mencapai
kecermatan yang tinggi, dapat dilakukan dengan berbagai cara seperti
menggunakan peralatan yang telah dikalibrasi, menggunakan pereaksi dan pelarut
yang baik, pengontrolan suhu, dan pelaksanaannya yang cermat, taat asas sesuai
− Metode simulasi (spiked-placebo recovery)
Dalam metode simulasi, sejumlah analit bahan murni ditambahkan ke
dalam campuran bahan pembawa sediaan farmasi lalu campuran tersebut
dianalisis dan hasilnya dibandingkan dengan kadar analit yang ditambahkan
(kadar yang sebenarnya) (Harmita, 2004).
− Metode penambahan baku (standard addition method)
Dalam metode penambahan baku, sampel dianalisis lalu sejumlah tertentu
analit yang diperiksa ditambahkan ke dalam sampel, dicampur dan dianalisis lagi.
Selisih kedua hasil dibandingkan dengan kadar yang sebenarnya (hasil yang
diharapkan) (Harmita, 2004).
Dalam kedua metode tersebut, persen perolehan kembali dinyatakan
sebagai rasio antara hasil yang diperoleh dengan hasil yang sebenarnya. Metode
adisi dapat dilakukan dengan menambahkan sejumlah analit dengan konsentrasi
tertentu pada sampel yang diperiksa, lalu dianalisis dengan metode tersebut.
Persen perolehan kembali ditentukan dengan menentukan berapa persen analit
yang ditambahkan tadi dapat ditemukan (Harmita, 2004).
2. Keseksamaan (precision)
Keseksamaan adalah ukuran yang menunjukkan derajat kesesuaian antara
hasil uji individual, diukur melalui penyebaran hasil individual dari rata-rata jika
prosedur diterapkan secara berulang pada sampel-sampel yang diambil dari
campuran yang homogen. Presisi merupakan ukuran keterulangan metode analisis
dan biasanya dinyatakan sebagai simpangan baku relatif dari sejumlah sampel
3. Selektivitas (Spesifisitas)
Selektivitas atau spesifisitas suatu metode adalah kemampuan suatu
metode mengukur zat tertentu saja secara cermat dan seksama dengan adanya
komponen lain yang mungkin ada dalam matriks sampel. Selektivitas biasanya
dinyatakan sebagai derajat penyimpangan metode yang dilakukan terhadap
sampel yang mengandung bahan yang ditambahkan berupa cemaran, hasil urai,
senyawa sejenis, dan senyawa lain yang dibandingkan terhadap hasil analisis
sampel yang tidak mengandung bahan lain yang ditambahkan (Harmita, 2004).
4. Linearitas dan Rentang
Liniearitas merupakan kemampuan suatu metode untuk memperoleh
hasil-hasil uji yang secara langsung proporsional dengan konsentrasi analit pada kisaran
yang diberikan. Linearitas suatu metode merupakan ukuran seberpa baik kurva
kalibrasi yang menghubungkan antara absorbansi (y) dengan konsentrasi (x).
Liniearitas dapat diukur dengan melakukan pengukuran tunggal pada konsentrasi
yang berbeda-beda. Rentang metode adalah pernyataan batas terendah dan
tertinggi analit yang sudah ditunjukkan dapat ditetapkan dengan kecermatan,
keseksamaan, dan linearitas yang dapat diterima (Harmita, 2004).
5. Batas Deteksi dan Batas Kuantitasi
Batas deteksi adalah jumlah analit terkecil dalam sampel yang dapat
dideteksi. Batas kuantitasi merupakan parameter pada analisis dan diartikan
sebagai kuantitas analit terkecil dalam sampel yang masih dapat memenuhi
kriteria cermat dan seksama (Harmita, 2004). Batas deteksi dan kuantitasi dapat
dihitung secara statistik melalui garis regresi linier dari kurva kalibrasi larutan
6. Ketangguhan Metode (Ruggedness)
Ketangguhan metode adalah derajat ketertiruan hasil uji yang diperoleh
dari analisis sampel yang sama dalam berbagai kondisi uji normal, seperti
laboratorium, analisis, instrumen, bahan pereaksi, suhu, dan hari yang berbeda.
Ketangguhan metode dinyatakan sebagai tidak adanya pengaruh perbedaan
operasi atau lingkungan kerja terhadap hasil uji (Harmita, 2004).
7. Kekuatan (Robustness)
Kekuatan merupakan kemampuan metode untuk tetap tidak terpengaruh
oleh adanya variasi parameter metode yang kecil. Kekuatan suatu metode adalah
dengan membuat variasi parameter-parameter penting dalam suatu metode secara
sistematis lalu mengukur pengaruhnya pada pemisahan (Gandjar dan Rohman,
BAB I PENDAHULUAN 1.1Latar Belakang
Buah oyong (Luffa acutangula) atau disebut juga gambas, tanaman ini
termasuk dalam famili Cucurbitaceae, berasal dari India, namun telah beradaptasi
dengan baik di Asia Tenggara termasuk Indonesia. Buahnya dapat dibuat sayur
lodeh, sop, sayur bening, dikukus dan dilalap. Buah oyong mengandung zat gizi
penting, diantaranya : protein, karbohidrat, lemak, kalsium, fosfor, zat besi,
vitamin A, vitamin B1, vitamin C, serat, kalium, sodium, Vitamin K, dan masih
mineral penting lainnya. Kadar kalium yang terdapat dalam buah oyong 453 mg/
100 gram (V., Jyothi, dkk., 2010). Buah oyong secara empiris diketahui memiliki
efek diuretik yang dapat membantu menurunkan tekanan darah (Rahman, dkk.,
2008)
Daun alpukat merupakan alternatif yang baik mengingat persebarannya
yang luas di masyarakat sehingga mudah didapatkan dan harganya tidak