AKTIVITAS ANTIOKSIDAN DAN MUTU SENSORI
FORMULASI MINUMAN FUNGSIONAL SAWO (Achras sapota
L.) DAN KAYU MANIS (Cinnamomum burmannii)
FATHONAH NUR ANGGRAINI
PROGRAM STUDI KIMIA
FAKULTAS SAINS DAN TEKNOLOGI
UNIVERSITAS ISLAM NEGERI SYARIF HIDAYATULLAH
JAKARTA
AKTIVITAS ANTIOKSIDAN DAN MUTU SENSORI FORMULASI
MINUMAN FUNGSIONAL SAWO (Achras sapota L.) DAN KAYU MANIS
(Cinnamomum burmannii)
Oleh:
FATHONAH NUR ANGGRAINI NIM 109096000023
SKRIPSI
Sebagai Salah Satu Syarat untuk Memperoleh Gelar Sarjana Sains
Program Studi Kimia
Fakultas Sains dan Teknologi
Universitas Islam Negeri Syarif HidayatullahJakarta
PROGRAM STUDI KIMIA
FAKULTAS SAINS DAN TEKNOLOGI
UNIVERSITAS ISLAM NEGERI SYARIF HIDAYATULLAH
JAKARTA
AKTIVITAS ANTIOKSIDAN DAN MUTU SENSORI FORMULASI
MINUMAN FUNGSIONAL SAWO (Achras sapota L.) DAN KAYU MANIS
(Cinnamomum burmannii)
SKRIPSI
Sebagai Salah Satu Syarat untuk Memperoleh Gelar Sarjana Sains
Program Studi Kimia
Fakultas Sains dan Teknologi
Universitas Islam Negeri Syarif HidayatullahJakarta
Oleh:
Fathonah Nur Anggraini 109096000023
Menyetujui
Pembimbing I Pembimbing II
Anna Muawanah, M.Si. NIP : 19740508 199903 2 002
Drs. Dede Sukandar, M. Si NIP. 19650104 199103 1 004
Mengetahui,
Ketua Program Studi Kimia
PENGESAHAN UJIAN
Skripsi yang berjudul “Aktivitas Antioksidan dan Mutu Sensori Formulasi Minuman Fungsional Sawo (Achras sapota L.) dan Kayu Manis (Cinnamomum Burmannii) telah diuji dan dinyatakan lulus pada sidang Munaqosyah Fakultas Sains dan Teknologi, Universitas Islam Negeri Syarif Hidayatullah Jakarta pada hari Jum’at, 21 Maret 2014. Skripsi ini telah diterima sebagai salah satu syarat untuk memperoleh gelar Sarjana Strata Satu (S1) Program Studi Kimia.
Menyetujui,
Penguji I Penguji II
Sandra Hermanto, M.Si. NIP : 19750810 200501 1 005
Nurhasni, M. Si NIP. 19740618 200501 2 005
Pembimbing I Pembimbing II
Anna Muawanah, M.Si. NIP : 19740508 199903 2 002
Drs. Dede Sukandar, M. Si NIP. 19650104 199103 1 004
Mengetahui,
Dekan
Fakultas Sains dan Teknologi Ketua Program Studi Kimia
Dr. Agus Salim, M.Si. NIP : 19720816 199903 1 003
PERNYATAAN
DENGAN INI SAYA MENYATAKAN BAHWA SKRIPSI INI ADALAH HASIL KARYA SENDIRI YANG BELUM PERNAH DIAJUKAN SEBAGAI SKRIPSI ATAU KARYA ILMIAH PADA PERGURUAN TINGGI ATAU LEMBAGA MANAPUN
Jakarta, Maret 2014
ABSTRAK
FATHONAH NUR ANGGRAINI, Aktivitas Antioksidan dan Mutu Sensori Formulasi Minuman Fungsional Sawo (Achras sapota L) dan Kayu Manis (Cinnamomum burmannii). Di bawah bimbingan ANNA MUAWANAH dan
DEDE SUKANDAR.
Penelitian mengenai aktivitas antioksidan dan mutu sensori formulasi minuman fungsional sawo (Achras sapota L) dan kayu manis (Cinnamomum burmannii) telah dilakukan. Tujuan dari penelitian ini adalah mengetahui formulasi minuman yang paling disukai berdasarkan uji organoleptik dan aktivitas antioksidannya serta kualitasnya berdasarkan standar mutu sari buah SNI 01-3719-1995. Penelitian ini terdiri dari tiga tahap yaitu penentuan formulasi minuman fungsional, analisis antioksidan yang meliputi aktivitasnya (IC50), serta komponen
antioksidan vitamin C dan total fenolik, dan terakhir analisis produk meliputi sifat fisik, sifat kimia, cemaran logam dan cemaran mikroba. Hasil penelitian menunjukkan bahwa formula 561 merupakan produk yang paling disukai panelis berdasarkan uji organoleptik. Formulasi 561 menunjukkan aktivitas antioksidan (IC50) 54,1 μL/mL, yang berbeda nyata dengan aktivitas antioksidan (IC50)
komponen penyusunnya sawo 72,04 μL/mL pada taraf signifikansi 5%. Kandungan total fenolik formulasi 561 yaitu sebesar 459,69 (mg/L) EAG, vitamin C 70,4 mg/100 mL, kadar air 88,32 % (b/b), pH 3,94, total padatan terlarut 10 %, total asam 7,68 %, dan kadar abu 0,48 % (b/b), logam Zn 0,95 mg/L, logam Cu 0,285 mg/L serta total mikroba kurang dari 1,0 × 101 koloni/mL. Formulasi 561 memiliki kualitas yang sesuai dengan standar SNI sari buah (SNI 01-3719-1995).
ABSTRACT
FATHONAH NUR ANGGRAINI, Antioxidant Activity and Sensory Quality In Sapota (Achras sapota L) and Cinnamon (Cinnamomum burmannii) Functional Drink Formulation. Advisor ANNA MUAWANAH dan DEDE SUKANDAR.
The antioxidant activity and sensory quality in sapota (Achras sapota L) and cinnamon (Cinnamomum burmannii) functional drink formulation was studied. The objective of this study was to determine the most preffered formulation based on organoleptic, to determine antioxidant activity and quality of sapota-cinammon functional drink formulation based on SNI 01-3719-1995. The research consisted of three stages, which were determinating of sapota-cinammon drink formulation, analysis of antioxidant covering the activity (IC50) and the component of
antioxidant were asorbic acid and phenolic total compounds, and lastly analysis of products covering the physical properties, chemical properties, metal contaminations and microbial contamination. The results showed that the 561 formula was the most preferred formulation by panelists based on the organoleptic test. In the formulation 561 indicates antioxidant activity (IC50) of 54,1 μL/mL
which were significantly different to antioxidant activity (IC50) the constituent
components sapota of 72,04 μL/mL on level of significance 5%. Phenolic total content the 561 formula of 459,69 (mg/L) EAG, asorbic acid content of 70,4 mg/100 ml, moisture 88,32 % (w/w), pH 3,94, TSS of 10%, acid total acidity of 7,68 %, level of ash 0,48 % (w/w), Zn level of 0,95 mg/L, Cu level of 0,285 mg/L, and total microbial was less than 1,0 × 101 colony/mL of product. The quality of 561 formulation heve met the standards of SNI (SNI 01-3719-1995).
vii
KATA PENGANTAR
Puji syukur penulis haturkan pada Allah SWT karena berkat rahmat dan
hidayah-Nya penulis dapat menyelesaikan skripsi yang berjudul “Aktivitas
Antioksidan dan Mutu Sensori Formulasi Minuman Fungsional Sawo
(Achras sapota L.) dan Kayu Manis (Cinnamomum burmannii)”yang disusun
dalam rangka memenuhi mata kuliah tugas akhir sebagai syarat untuk
memperoleh gelar Sarjana Sains Program Studi Kimia di Fakultas Sains dan
Teknologi Universitas Islam Negeri Syarif hidayatullah Jakarta.
Dalam kesempatan ini, penulis ingin mengucapkan terimakasih kepada
semua pihak yang telah membantu secara ikhlas dalam penyelesaian skiripsi ini,
yakni kepada:
1. Ibu Anna Muawanah, M.Si., selaku pembimbing I yang telah dengan sabar
membimbing dan memberikan saran kepada penulis selama proses penulisan
skripsi ini.
2. Bapak Drs. Dede Sukandar, M.Si., selaku pembimbing II dan juga selaku
Ketua Program Studi Kimia Fakultas Sains dan Teknologi Universitas Islam
Negeri Syarif Hidayatullah Jakarta yang telah memberikan perhatian dan
bimbingannya kepada penulis.
3. Dr. Agus Salim, M.Si., selaku dekan Fakultas Sains dan Teknologi UIN Syarif
Hidayatullah Jakarta.
4. Bapak Dr.Thamzil Laz selaku penasihat akademik yang selalu memberikan
viii 5. Ayah, Bunda, dan juga Kakak yang tidak pernah mengenal lelah dalam
memberikan perhatian dan dukungannya kepada penulis sampai sekarang.
6. Keluargaku di Solo Mbah Putri, Pakde, Om, Bulek, Sepupu yang senantiasa
selalu mendoakan penulis dalam setiap kesulitan dan perjuangan. Semoga
Allah SWTmembalas kebaikan kalian.
7. Ade, Diah, Lina, Ayya, Nur, Dita, Adaw, Puput, Chitta, Rafi, Hafiz serta
teman-teman kimia 2009 yang sudah banyak partisipasinya, dalam membantu
penulis baik secara langsung maupun tidak langsung.
8. Kak pipit selaku laboran kimia yang telah sabar membantu dan mendukung
dalam proses penelitian.
9. Adik- adik kimia angkatan 2010 dan 2011 yang juga telah membantu dalam
proses penelitian.
Penulis menyadari skripsi ini masih jauh dari kesempurnaan. Oleh karena
itu, penulis mengharapkan kritik dan saran yang bersifat membangun dari
berbagai pihak. Semoga skripsi ini dapat bermanfaat dan memberikan
pengetahuan bagi para pembacanya. Aamiin.
Akhirnya, hanya kepada Allah SWT penulis berserah diri,
mudah-mudahan semua bentuk perhatian, bantuan dan partisipasi yang sudah diberikan
mendapatkan pahala yang setimpal dari-Nya.
Jakarta, Januari 2014
ix
DAFTAR ISI
Hal
KATA PENGANTAR ... vii
DAFTAR ISI ... ix
DAFTAR GAMBAR ... xii
DAFTAR TABEL ... xiv
DAFTAR LAMPIRAN ... xv
BAB I PENDAHULUAN 1.1. Latar Belakang ... 1
1.2. Perumusan Masalah ... 3
1.3. Tujuan Penelitian ... 3
1.4. Hipotesis Penelitian ... 4
1.5. Manfaat Penelitian ... 4
BAB II TINJAUAN PUSTAKA 2.1. Sawo Manila ... 5
2.2. Kayu Manis... 11
2.3. Pangan Fungsional ... 14
2.4. Minuman Sari Buah ... 15
2.4.1. Komposisi Sari Buah ... 19
2.5. Antioksidan ... 22
2.6. Analisis Sensori ... 28
x
2.7.1. Spektrofotometri Serapan Atom... 30
2.7.2. Spektrofotometri UV-Vis ... 32
BAB III METODE PENELITIAN 3.1. Waktu dan Tempat Penelitian... 35
3.2. Alat dan Bahan ... 35
3.3. Prosedur Penelitian ... 36
3.3.1. Pembuatan Minuman Fungsional ... 36
3.3.2. Analisis Sensori ... 37
3.3.3. Analisis antioksidan ... 38
3.3.4. Uji Sifat Fisik dan Kimia ... 39
3.3.5. Uji Cemaran Logam ... 42
3.3.6. Uji Cemaran Mikroba... 42
3.3.7. Analisis Data ... 44
BAB IV HASIL DAN PEMBAHASAN 4.1. Analisis Sensori ... 45
4.2. Analisis Antioksidan ... 57
4.3. Uji Sifat Fisik dan Kimia ... 67
4.4. Uji Cemaran Logam ... 70
xi
BAB V PENUTUP
5.1. Kesimpulan ... 74
5.2. Saran ... 75
DAFTAR PUSTAKA ... 76
xii
DAFTAR GAMBAR
Hal
Gambar 1. Sawo Manila (Achras Sapota L) ... 5
Gambar 2. Struktur Beberapa Fenolat ... 9
Gambar 3. Kulit Dan Bubuk Kayu Manis ... 11
Gambar 4. Sukrosa ... 21
Gambar 5. Mekanisme Antioksidan Primer ... 23
Gambar 6. Asam Askorbat ... 24
Gambar 7. Mekanisme Reaksi Asam Askorbat dan Ion Superoksida Dan Hidrogen Peroksida ... 26
Gambar 8. Reduksi DPPH dari Senyawa Peredam Radikal Bebas ... 27
Gambar 9. Skema Peralatan SSA ... 31
Gambar 10. Komponen Spektrofotometer UV-Vis ... 33
Gambar 11. Histogram Rata-Rata Skor Hedonik Warna ... 46
Gambar 12. Formulasi Minuman Fungsional ... 47
Gambar 13. Reaksi Antara dalam Pembentukan Melanin ... 49
Gambar 14. Reaksi Pembentukan Melanin dari O-Kuinon atau O-Difenol ... 50
Gambar 15. Histogram Rata-Rata Skor Hedonik Aroma ... 51
Gambar 16. Histogram Rata-Rata Skor Hedonik Rasa Manis dan Asam ... 54
Gambar 17. Skema Teori Kemanisan ... 55
Gambar 18. Histogram Rata-Rata Skor Hedonik Penerimaan Keseluruhan ... 57
xiii
Gambar 20. Kurva Korelasi Aktivitas Antioksidan dengan Kadar Fenolik
Total Buah Sawo, Kayu Manis, dan Jeruk Nipis ... 62
Gambar 21. Mekanisme Kerja Antioksidan Golongan Fenol ... 64
Gambar 22. Mekanisme Kerja Vitamin C Sebagai Antioksidan ... 65
Gambar 23. Mekanisme Reaksi Asam Askorbat dan Ion Superoksida dan
xiv
DAFTAR TABEL
Hal
Tabel 1. Kandungan Sawo dalam 100 g Sawo Masak Segar ... 8
Tabel 2. Standar Mutu Minuman Sari Buah (SNI 01-3719-1995) ... 16
Tabel 3. Formulasi Minuman Sari Buah Sawo ... 37
Tabel 4. Hasil Pengujian Organoleptik Minuman Fungsional ... 45
Tabel 5. Kandungan Total Fenolik, Vitamin C, dan Antioksidan pada Sawo, Kayu Manis, dan Jeruk Nipis ... 58
Tabel 6. Kandungan Total Fenolik, Vitamin C, dan Antioksidan pada Minuman Fungsional 561 ... 63
Tabel 7. Sifat Kimia dan Fisik Minuman Fungsional Tersukai... 67
xv
DAFTAR LAMPIRAN
Hal
Lampiran 1. Bagan Skema Penelitian ... 88
Lampiran 2. Bagan Proses Pembuatan Minuman Fungsional Sawo-Kayu Manis ... 89
Lampiran 3. Formulir Uji Organoleptik ... 90
Lampiran 4. Skor Hedonik Panelis Terhadap Minuman Fungsional Sawo-Kayu Manis ... 91
Lampiran 5. Hasil SPSS Warna ... 96
Lampiran 6. Hasil SPSS Aroma ... 97
Lampiran 7. Hasil SPSS Rasa Manis ... 98
Lampiran 8. Hasil SPSS Rasa Asam ... 99
Lampiran 9. Hasil SPSS Penerimaan Keseluruhan ... 100
Lampiran 10. Hasil Uji T-Student Aktivitas Antioksidan Perasan Sawo dan Minuman Formula 561 ... 101
Lampiran 11. Hasil Uji T-Student Kandungan Total Fenolik Perasan Sawo dan Minuman Formula 561 ... 102
Lampiran 12. Pengujian Aktivitas Antoksidan Sawo, Kayu Manis, dan Jeruk Nipis ... 103
Lampiran 13. Perhitungan Minuman Fungsional 561 ... 104
Lampiran 14. Hasil Analisis Total Fenol ... 105
Lampiran 15. Hasil Uji Logam... 106
1
BAB I
PENDAHULUAN
1.1. Latar Belakang
Buah sawo (Achras sapota L.) selama ini dianggap sebagai buah asli
Indonesia karena sudah lama dikenal dan ditanam di Indonesia terutama di Pulau
Jawa. Buah sawo disukai karena memiliki rasa yang manis dan biasa dikonsumsi
sebagai buah segar dalam keadaan matang (Rukmana, 1997). Namun, buah sawo
sebagai produk hortikultura merupakan komoditas yang mudah rusak terutama
setelah pemanenan. Kerusakan yang terjadi dapat berupa kerusakan fisik,
mekanis, maupun mikrobiologis (Ratule, 1999), sehingga tidak dapat disimpan
lama dan umumnya hanya dapat bertahan selama lima sampai tujuh hari jika
disimpan pada kondisi normal (Aryati, 2006). Kondisi buah sawo yang demikian,
maka diperlukan teknologi pengolahan sehingga buah sawo tidak hanya
dikonsumsi dalam bentuk segar, melainkan dapat dimanfaatkan menjadi bahan
olahan lain yang memiliki nilai tambah. Pengolahan ini merupakan salah satu cara
untuk mempertahankan mutu produk dan memperpanjang masa simpan buah
sawo (Aryati, 2006). Salah satu bentuk pengolahan yang dapat dijadikan sebagai
alternatif yaitu diolah menjadi pangan fungsional berupa minuman fungsional sari
buah.
Pangan fungsional merupakan pangan yang mempunyai efek fisiologis
bagi tubuh, seperti dapat menurunkan tekanan darah, meningkatkan kondisi umum
2 digunakan untuk menyembuhkan beberapa penyakit (Astawan, 2003; Siro et al.,
2008). Efek fisiologis tersebut karena adanya komponen aktif yang terkandung
didalam bahan pangan tersebut (Winarti et al., 2005).
Komponen aktif yang terkandung didalam buah sawo dan bermanfaat bagi
kesehatan yaitu vitamin C, fenolik, dan karotenoid yang diketehui memilik efek
antioksidan (Kulkarni et al.,2006). Antioksidan adalah senyawa yang mempunyai
struktur molekul yang dapat memberikan elektronnya kepada molekul radikal
bebas dan dapat memutus reaksi berantai dari radikal bebas (Kumalaningsih,
2006). Radikal bebas yang berlebih dapat menyerang senyawa apa saja terutama
yang rentan seperti lipid dan protein dan berimplikasi pada timbulnya berbagai
penyakit degeneratif (Middleton, 2000).
Pengolahan sawo selain untuk mempertahankan mutu dan memperpanjang
masa simpan, juga dapat menghasilkan minuman fungsional yang dapat dijadikan
sebagai sumber gizi terutama sumber antioksidan. Selain itu, pembuatan minuman
fungsional dapat juga dipadukan dengan bahan lain seperti kayu manis sebagai
flavor dalam formulasi minuman. Kayu manis merupakan tanaman rempah yang
telah lama dimanfaatkan sebagai pewangi atau peningkat cita rasa pada makanan
atau minuman (Rismunandar et al.,2001). Komponen-komponen bioaktif dalam
kayu manis, seperti sinamaldehid, asam sinamat, dan sineol diketahui memiliki
aktivitas antioksidan yang bermanfaat bagi kesehatan (Jayapprakasha, 2003).
Dengan demikian, perpaduan antara sawo dengan rempah-rempah dalam
formulasi diharapkan akan menghasilkan suatu formulasi yang dapat diterima dari
3
1.2. Rumusan Masalah
a. Apakah formulasi minuman fungsional sawo-kayu manis berpengaruh
terhadap tingkat kesukaan panelis berdasarkan pengujian organoleptik?
b. Bagaimana aktivitas antioksidan formulasi minuman fungsional
sawo-kayu manis yang tersukai?
c. Apakah kualitas formulasi minuman fungsional sawo-kayu manis
tersukai telah memenuhi standar mutu sari buah sesuai SNI
01-3719-1995.
1.3. Tujuan Penelitian
Tujuan dari penelitian ini yaitu:
a. Mendapatkan formulasi minuman fungsional sawo-kayu manis yang
paling disukai oleh panelis berdasarkan pengujian organoleptik.
b. Mengetahui aktivitas antioksidan formulasi minuman fungsional
sawo-kayu manis yang paling disukai.
c. Mengetahui kualitas formulasi minuman fungsional sawo-kayu manis
4
1.4. Hipotesis
a. Terdapat pengaruh formulasi minuman fungsional sawo-kayu manis
terhadap tingkat kesukaan panelis berdasarkan pengujian
organoleptik.
b. Formulasi minuman fungsional sawo-kayu manis yang tersukai
memiliki aktivitas antioksidan yang tinggi.
c. Kualitas formulasi minuman fungsional sawo-kayu manis telah
memenuhi standar mutu sari buah sesuai SNI 01-3719-1995.
1.5. Manfaat Penelitian
Penelitian ini diharapkan dapat memberikan informasi yang bermanfaat
kepada masyarakat mengenai pemanfaatan buah sawo sebagai bahan baku
alternatif minuman fungsional yang memiliki aktivitas antioksidan, bermanfaat
bagi kesehatan dan juga sebagai upaya dalam peningkatan mutu produk buah
5
BAB II
TINJAUAN PUSTAKA
2.1. Sawo Manila (Achras sapota L)
Sawo manila, Achras sapota L.yang biasa dikenal sebagai chikku
merupakan salah satu buah lezat daerah tropis yang merupakan keluarga dari
Sapotaceae. Sawo disukai karena rasanya yang manis dan lezat. Sawo biasa
dikonsumsi sebagai makanan pencuci mulut (Hiremath et al., 2012).
Tanaman sawo diduga berasal dari daerah Amerika Tengah, terutama
kawasan Guatemala. Namun, tanaman sawo selama ini dianggap sebagai tanaman
asli Indonesia karena sudah lama dikenal dan ditanam di Indonesia terutama di
Pulau Jawa (Rukmana,1997). Sawo diketahui merupakan salah satu tanaman buah
utama di India, Meksiko, Guatemala, dan Venezuela (Kulkarni et al., 2006; Maya
et al., 2003). Bentuk tanaman dan buah sawo dapat dilihat pada gambar 1.
Gambar 1. Sawo Manila ( Candra, 2011)
Di Indonesia, sawo merupakan tanaman buah-buahan yang berbuah tanpa
musim. Tanaman sawo ini dapat tumbuh dan bereproduksi dengan baik mulai dari
dataran rendah sampai ketinggian 700 meter diatas permukaan laut. Tanaman
6 (Rukmana, 1997). Buah sawo yang cukup tua memiliki ukuran buah yang
maksimal, kulit buah berwarna coklat muda, daging buah agak lembek, bila
dipetik mudah terlepas dari tangkainya, serta bergetah relatif sedikit (Aryati,
2006).
Matangnya buah dapat diberi batasan sebagai perubahan berturut-turut
warna buah, aroma, tekstur kearah kondisi buah yang siap untuk dikonsumsi
(Kartasapoetra, 1989). Sawo tidak dapat disimpan lama dan umumnya buah hanya
dapat bertahan selama lima sampai tujuh hari jika disimpan pada kondisi biasa
(Aryati, 2006). Buah sawo umumnya dikonsumsi sebagai buah segar dalam
keadaan matang atau biasa dinamakan buah meja (Rukmana, 1997).
Sawo memiliki beberapa nama umum lainnya yang berbeda pada setiap
negara, seperti sawo manila (Indonesia), baramasi (Bengal dan Bihar), buah chiku
(Malaya, India), chicle (Meksiko), chico (Filipina), korob (Kosta Rika), Mespil
(Virgin Islands), muy (Guatemala), muyozapot (El Salvador), neeseberry (British
West Indies), nispero (Puerto Rico, Amerika Tengah), nispero quitense (Ekuador),
sapotí (Brasil), sapotille (French West Indies), zapota (Venezuela)(Morton, 1987).
Menurut Heyne (1987), tanaman sawo manila (gambar 1) memiliki
taksonomi sebagai berikut.
Kingdom : Plantae
Divisi : Magnoliophyta
Kelas : Magnoliopsida
Ordo : Ericales
Famili : Sapotaceae
Genus : Chrysophyllum
7 Menurut Rukmana (1997), sawo termasuk buah klima-terik yaitu buah
yang proses fisiologisnya berlangsung terus walau sudah dipetik atau dipanen.
Proses fisiologis yang dimaksud yaitu akan mengadakan perubahan dari tua
(mature) setelah panen menjadi masak (ripening) dan akan berlanjut ke fase lewat
matang (decaying) atau pembusukan juga disertai terbentuk aroma khas. Oleh
karena itu, buah sawo sebagai produk hortikultura merupakan komoditas yang
mudah rusak terutama setelah pemanenan. Kerusakan yang terjadi dapat berupa
kerusakan fisik, mekanis, maupun mikrobiologis (Ratule, 1999), sehingga tidak
dapat disimpan lama dan umumnya buah hanya dapat bertahan selama 5-7 hari
jika disimpan pada kondisi biasa (Aryati, 2006). Kondisi buah sawo yang
demikian, perlu diperkenalkan kepada petani khususnya dan masyarakat
umumnya mengenai teknologi pengolahannya sehingga buah sawo tidak hanya
dikonsumsi dalam bentuk segar, melainkan dapat dimanfaatkan menjadi bahan
olahan lain yang memiliki nilai tambah besar. Selain itu, pengolahan merupakan
salah satu cara untuk mempertahankan mutu produk pertanian (Aryati, 2006).
.Tanaman sawo, selain menghasilkan buah yang rasanya manis dan
menyegarkan, juga mengandung gizi cukup tinggi dengan komposisi lengkap
8
Tabel 1.Kandungan Sawo dalam 100 g Sawo Masak Segar oleh Direktorat Gizi Depkes (1981).
No Kandungan Gizi Jumlah
1. Kalori 92.00 kal
Buah sawo juga diketahui mengandung flavonoid, saponin, dan tanin
(Sukandar et al., 2012). Selain itu, sawo diketahui merupakan sumber yang baik
dari asam askorbat, karetenoid, dan fenolik yang dilaporkan memiliki banyak
manfaat pada kesehatan (Kulkarni et al., 2006). Hasil penelitian Sukandar et al
(2012) menunjukkan ekstrak etanol buah sawo memiliki aktivitas antioksidan
yang cukup tinggi yaitu dengan IC50 sebesar 29,20 ppm, sedangkan Kulkarni et al
(2006) menyebutkan dalam penelitiannya perasan sari sawo memiliki aktivitas
antioksidan (IC50) sebesar 87,53 μL/mL.
Buah sawo dilaporkan juga mengandung gula (Siddappa et al., 1954),
asam (Shanmugavelu et al.,1973), protein, asam amino (Selvaraj et al.,1984),
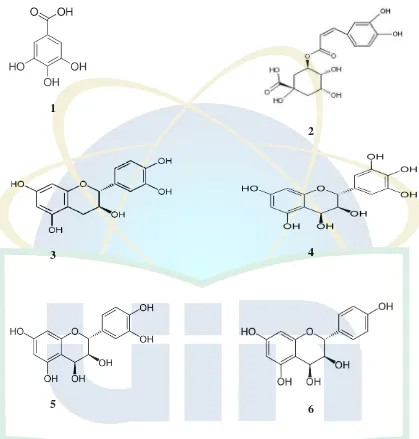
fenolat (gambar 2), yaitu, asam galat (1), asam chlorogenic (2), catechin (3),
leucodelphinidin (4), leucocyanidin (5).dan leucopelargonidin (6) (Mathew et
al.,1969), karotenoid, asam askorbat, dan mineral seperti kalium, kalsium dan zat
9
1
3
5
2
4
6
Gambar 2. Struktur Beberapa Fenolat
Shanmugavelu et al (1973) menyebutkan buah sawo juga merupakan
sumber yang baik dari gula yang dapat dicerna, yaitu berkisar antara 12 sampai 20
persen dan juga memiliki banyak kandungan mineral seperti zat besi dan kalsium.
Buah juga memiliki jumlah yang cukup protein, lemak, kalsium, serat, fosfor,
karoten, zat besi, dan vitamin C. Selain itu, sawo diketahui kaya akan bio-besi
10 Sumeru (1995) menyebutkan buah sawo adalah buah berdaging buah tebal
dengan rasa manis yang memiliki kandungan gula sebesar 14%, sakarosa 7,02%,
dektrosa 3,7%, levulosa 3,4%, dan mengandung sedikit asam serta abu 1%. Selain
itu, sawo mengandung gizi cukup tinggi dengan komposisi lengkap, yaitu kalori
92,0 kkal, protein 0,5 gram, lemak 0,10 gram, karbohidrat 26,4 gram dan vitamin
sekitar 60,00 SI (Rukmana, 1997). Buah sawo memiliki kandungan mineral cukup
baik. Buah ini merupakan sumber kalium yang baik, yaitu 193 mg/100 g. Di lain
pihak, sawo juga memiliki kadar natrium yang rendah, 12 mg/100g. Perbandingan
kandungan kalium dan natrium yang mencapai 16:1 menjadikan sawo sangat baik
untuk jantung dan pembuluh darah (Candra, 2010).
Logam transisi, besi, tembaga, dan seng, juga merupakan nutrisi penting
yang terkandung dalam sawo (Kulkarni et al., 2006). Kekurangan ion logam ini
dilaporkan telah menjadi gangguan defisiensi gizi yang paling umum terjadi di
dunia yang mempengaruhi sekitar dua milyar orang, sebagian besar mereka
tinggal di negara berkembang (Lynch, 2005). Menurut Kulkarni et al (2006)
dalam Kwong et al (2004), kekurangan zat besi memiliki dampak yang merusak
yakni menurunnya imunitas sel dan menyebabkan perubahan perilaku dan
kognitif. Kekurangan tembaga juga telah dikaitkan dengan gangguan metabolisme
karbohidrat (Davis et al.,1987), sedangkan kekurangan seng menyebabkan
kekurangan atau ketidak sempurnaan dari pertumbuhan, kematangan seksual,
11
2.2. Kayu Manis
Menurut Heyne (1987), pohon kayu manis merupakan tumbuhan asli Asia
Selatan, Asia Tenggara dan daratan Cina, Indonesia termasuk didalamnya.
Tumbuhan ini termasuk famili Lauraceae yang memiliki nilai ekonomi dan
merupakan tanaman tahunan yang memerlukan waktu lama untuk diambil
hasilnya. Hasil utama kayu manis (gambar 3) adalah kulit batang dan dahan,
sedang hasil samping adalah ranting dan daun. Komoditas ini selain digunakan
sebagai rempah, hasil olahannya seperti minyak atsiri dan oleoresin banyak
dimanfaatkandalam industri-industri farmasi, kosmetik, makanan, minuman,
rokok, dan lain-lain.
Gambar 3. Kulit dan Bubuk Kayu Manis (Rusli et al., 1988).
Dari 54 spesies kayu manis (Cinnamomum sp.) yang dikenal di dunia, 12
di antaranya terdapat di Indonesia. Tiga jenis kayu manis yang menonjol di pasar
dunia yaitu Cinnamomum burmannii (di Indonesia) yang produknya dikenal
dengan nama cassiavera, Cinnamomum zeylanicum (di Sri Lanka dan Seycelles)
dan Cinnamomum cassia (di China) yang produknya dikenal dengan Cassia
China. Jenis-jenis tersebut merupakan beberapa tanaman rempah yang terkenal di
pasar dunia. Tanaman kayu manis yang selama ini banyak dikembangkan di
12 terutama diusahakan di Sumatera Barat, Jambi dan Sumatera Utara. Jenis
Cburmanii BL atau cassiavera ini merupakan produk ekspor tradisional yang
masih dikuasai Indonesia sebagai negara pengekspor utama di dunia.Tanaman
kayu manis memiliki klasifikasi sebagai berikut:
Kerajaan : Plantae
Divisio : Magnoliophyta
Kelas : Magnoliopsida
Ordo : Laurales
Suku : Lauraceae
Marga : Cinnamomum
Spesies : Cinnamomum burmanii Bl
Tanaman kayu manis merupakan jenis tanaman rempah yang tergolong
dalam famili Lauraceae, yaitu salah satu famili dari ordo Ranales. Famili ini
memiliki 45 genera dan 1100 spesies. Pertanaman kayu manis umumnya
merupakan perkebunan rakyat, terutama tersebar di daerah Sumatera Barat,
Kerinci, dan Tapanuli Selatan. Dewasa ini kayu manis juga sudah mulai
dikembangkan di Jawa, Kalimantan, Flores, dan Lombok. Jenis tanaman yang
diusahakan sebagaian besar adalah Cinnamomum burmannii BI. dan sedikit
Cinnamomum zeylanicum BI. dan Cinnamomum cassia BI, terutama di daerah
Jawa Barat (Rusliet al., 1985). Kulit kayu manis kering yang bermutu baik pada
umumnya mengandung minyak atsiri, pati, getah, resin, fixed oil, tanin, selulosa,
13 Komponen utama flavor dalam kayu manis adalah sinamaldehid gmbar
struktur, yang bukan merupakan fenol. Tetapi komponen minor flavor, kumarin
mengandung gugus fenol dan penting untuk memberi ciri khas flavor alami kayu
manis (Ho et al., 1992).
Eugenol yang merupakan komponen utama flavor cengkeh, juga
ditemukan pada kayu manis dalam jumlah kecil. Eugenol ditemukan pada kayu
manis sebesar 0,04-0,2 %, pada oleoresin kayu manis sebesar 2-6 %, dan pada
minyak kayu manis sebesar 70-90 % (Ho et al., 1992). Kayu manis dapat berperan
sebagai antioksidan karena mengandung senyawa tanin dan eugenol (King, 2000).
Selain sebagai rempah, hasil olahan kulit kayu manis seperti minyak atsiri
dan oleoresin banyak digunakan dalam industri-indusri farmasi, kosmetik,
makanan dan minuman, rokok, dan sebagainya. Tanaman ini juga digunakan
sebagai tanaman penghijauan dan konservasi tanah-tanah yang miring pada daerah
aliran sungai. Cinnamomum burmannii juga banyak ditanam sebagai tanaman hias
karena warna pucuknya yg merah terlihat indah (Rusli et al., 1985).
Minyak atsiri kayu manis sudah sejak lama dimanfaatkan sebagai
antiseptik. Minyak kayu manis ini juga memiliki efek untuk mengeluarkan angin
(karminatif), membangkitkan selera atau menguatkan lambung (stomakik),
sebagai obat sariawan, encok, masuk angin, dan sebagai antidiare. Untuk
pengolahan makanan dan minuman, minyak kayu manis sudah lama dimanfaatkan
sebagai pewangi atau peningkat citarasa, diantaranya untuk minuman keras,
minuman ringan, agar-agar, kue, kembang gula, bumbu gulai, dan sup
14
2.3. Pangan Fungsional
Menurut Badan POM (2011), pangan fungsional adalah pangan olahan
yang mengandung satu atau lebih komponen pangan yang berdasarkan kajian
ilmiah mempunyai fungsi fisiologis tertentu diluar fungsi dasarnya, terbukti tidak
membahayakan dan bermanfaat bagi kesehatan. Menurut Winarti & Nurdjanah
(2005), berbagai jenis pangan fungsional telah beredar di pasaran, mulai dari
produk susu probiotik tradisional seperti yoghurt, kefir dan coumiss sampai
produk susu rendah lemak siap dikonsumsi yang mengandung serat larut.
Berbagai minuman telah tersedia dan berkhasiat menyehatkan tubuh yang
mengandung komponen aktif rempah-rempah seperti kunyit asam, minuman sari
jahe, sari temulawak, beras kencur, serbat, dan bandrek.
Pangan fungsional dikonsumsi layaknya makanan atau minuman,
mempunyai karakteristik sensori berupa penampakan, warna, tekstur, dan cita rasa
yang dapat diterima oleh konsumen, serta tidak memberikan kontraindikasi dan
tidak memberikan efek samping terhadap metabolisme zat gizi lainnya jika
digunakan pada jumlah penggunaan yang dianjurkan. Meskipun mengandung
senyawa yang bermanfaat bagi kesehatan, pangan fungsional tidak berbentuk
kapsul, tablet atau bubuk yang berasal dari senyawa alami (Winarti et al.,2005
dalam Badan Pengawasan Obat dan Makanan (BPOM), 2001).
Pangan fungsional mempunyai tiga fungsi dasar antara lain sensory
(warna dan penampilan menarik, citarasanya enak), nutritional (bernilai gizi), dan
physiological (memberikan pengaruh fisiologis, menguntungkan bagi tubuh).
15 yang berhubungan dengan konsumsi pangan, b) meningkatkan daya tahan tubuh
(regulating bio-defensiveness), c) meregulasi rithme kondisi fisik tubuh, d)
memperlambat proses penuaan (aging), dan e) penyehatan kembali (recovery)
tubuh setelah menderita penyakit tertentu (Muchtadi, 2004).
Dewasa ini produk pangan fungsional yang bermanfaat bagi kesehatan
mulai banyak diminati oleh konsumen karena kesadaran akan pentingnya hidup
sehat semakin meningkat. Senyawa fitokimia sebagai senyawa kimia yang
terkandung dalam tanaman mempunyai peranan yang sangat penting bagi
kesehatan termasuk fungsinya dalam pencegahan terhadap penyakit degeneratif.
Beberapa senyawa fitokimia yang diketahui mempunyai fungsi fisiologis adalah
karotenoid, fitosterol, saponin, glikosinolat, polifenol, inhibitor protease,
monoterpen, fitoestrogen, sulfide dan asam fitat (Winarti et al., 2005). Komponen
fenolik dalam tanaman diketahui dapat menghambat pertumbuhan kanker dan
mempunyai aktivitas antimutagenik. Pertumbuhan kanker yang dapat ditekan oleh
senyawa fenolik antara lain kanker usus, payudara, paru-paru, dan kulit (Craig,
1999).
2.4. Minuman Sari Buah
Minuman sari buah adalah minuman ringan yang dibuat dari sari buah dan
air minum dengan atau tanpa penambahan gula dan bahan tambahan makanan
yang diizinkan (SNI 01-3719-1995). Minuman sari buah yang diproduksi harus
memiliki mutu yang sesuai dengan yang ada dalam SNI 01-3719-1995 yang
16
Tabel 2. Standar Mutu Minuman Sari Buah (SNI 01-3719-1995)
No Kriteria Uji Satuan Persyaratan
1. Keadaan:
3. Bahan tambahan makanan:
3.1 Pemanis buatan - tidak boleh ada
3.2 Pewarna tambahan sesuai SNI 01-0222-1987*)
3.3 Pengawet sesuai SNI 01-0222-1987*)
4. Cemaran logam:
6.4 Salmonella koloni/25ml Negatif
6.5 S.Aureus koloni/ml 0
6.6 Vibrio.sp koloni/ml Negatif
6.7 Kapang koloni/ml maks. 50
6.8 Khamir koloni/ml maks. 50
CATATAN: *) dan revisinya
**) untuk yang dikemas dalam
kaleng
Menurut Pollard et al (1974), sari buah merupakan hasil pengepresan atau
ekstraksi buah yang sudah disaring. Buah yang digunakan sebagai sari buah harus
dalam keadaan matang dan mempunyai cita rasa yang enak. Buah-buahan yang
17 berasal dari daerah penanaman yang sama. Sedangkan faktor yang mempengaruhi
cita rasa sari buah adalah perbandingan antara gula dan asam, jenis dan jumlah
komponen aroma, serta jenis vitamin (Kusumawati, 2008).
Menurut Makfoeld (1982), tahap-tahap pengolahan sari buah secara umum
adalah pemilihan dan penentuan kematangan buah, pencucian dan sortasi,
ekstraksi, homogenisasi, penyaringan, deaerasi, pengawetan, dan pengemasan.
Untuk buah-buahan tertentu, dapat dilakukan modifikasi terhadap proses
pengolahan tersebut, bergantung pada sifat buah dan sari buah yang diinginkan
(Kusumawati, 2008).
Pemilihan bahan merupakan hal yang penting dalam pembuatan formulasi
minuman ini, karena bahan yang baik akan menghasilkan kualitas minuman yang
baik pula. Pemilihan buah dilakukan berdasarkan bentuk buah, ukuran, warna, dan
banyak sedikitnya noda yang merupakan faktor dari kerusakan.
Penghancuran sari buah dilakukan dengan blender dan ekstraksi dilakukan
dengan cara pengepresan secara manual atau dengan pengepres alat dan kain
saring. Ekstraksi yang baik dapat menghindarkan tercampurnya kotoran dan
jaringan buah sehingga flavornya baik (Muchtadi, 1979).
Penambahan pengawet berperan penting dalam pembuatan sari buah untuk
meminimalkan pertumbuhan mikroorganisme. Salah satu pengawet yang dapat
digunakan yaitu natrium benzoat. Batas maksimum pengawet yang diperbolehkan
Menkes di dalam minuman yaitu 600 mg/kg (PP No. 722/ Menkes/ Per/ IX/
1988).Natrium benzoat dipilih sebagai pengawet minuman karena efektif mampu
18 natrium benzoat bekerja sebagai pengawet yaitu pada bahan pangan yang
memiliki pH ≤ 4.0 (Jay, 1978; Dunn, 1957). Oleh karena itu, perlu ditambahkan
asidulan atau zar pengatur keasaman yang berfungsi untuk menurunkan pH pada
minuman. Asidulan yang dapat ditambahkan yaitu asidulan alami seperti jeruk
nipis. Asidulan alami dapat dipilih agar meminimalkan penggunaan bahan
tambahan pangan (BTP) sintetis ke dalam minuman (Herold, 2007).
Pengemasan yang merupakan bagian penting dalam suatu proses
pembuatan produk pangan. Menurut Dwiari (2008), fungsi paling mendasar dari
kemasan adalah mewadahi dan melindungi produk dari kerusakan-kerusakan
sehingga lebih mudah disimpan, diangkut, dan dipasarkan. Jenis kemasan yang
digunakan dalam penelitian ini yaitu botol. Botol merupakan kemasan berbahan
gelas yang memiliki beberapa keuntungan, yaitu bersifat inert terhadap bahan
kimia, tahan terhadap tekanan dari dalam, tahan panas, dan relatif murah. Selain
itu, botol gelap yang digunakan dalam penelitian ini merupakan kemasan yang
tahan cahaya, tidak transparan atau tidak tembus cahaya, sehingga menghindarkan
produk dari reaksi oksidasi akibat terkena cahaya langsung yang dapat
menyebabkan kerusakan pada produk.
Setalah dilakukan proses pengemasan, dilakukan proses pasteurisasi.
Pasteurisasi adalah suatu proses pemanasan yang dapat membunuh atau
memusnahkan sebagian tetapi tidak semua mikroba yang ada dalam bahan dan
biasanya menggunakan suhu di bawah 100℃. Pasteurisasi membunuh semua
mikroorganisme mesofilik dan sebagian yang bersifat termofilik (Winarno, 1993).
19 patogen atau pembusuk, maka produk pangan yang sudah dipasteurisasi umumnya
masih mengandung mikroba lain seperti bakteri tidak berspora dari genera
Streptoccocus dan Lactobacillus, serta kapang dan khamir (Fardiaz, 1996).
Penyimpanan dingin (chilling storage) merupakan cara penyimpanan
bahan atau produk pangan di bawah suhu 15°C dan di atas titik beku
bahan/produk. Penyimpanan dingin merupakan salah satu cara menghambat
turunnya mutu sari buah, disamping penambahan zat-zat pengawet kimia dan
konsentrasi gula yang tinggi. Pendinginan akan menurunkan laju pertumbuhan
mikroba pada bahan/produk yang disimpan. Penurunan ini disebabkan terjadinya
denaturasi enzim dan penghambatan sintesa enzim yang dibutuhkan mikroba.
Menurut Pollard & Timberlake (1974), suhu penyimpanan yang ideal bagi sari
buah adalah 35-40°F (1.67-4.44°C) (Kusumawati, 2008)..
2.4.1. Komposisi Sari Buah
Dalam penelitian ini, minuman fungsional sari buah dibuat dengan
beberapa komposisi diantaranya yaitu, buah sawo, kayu manis, air, gula pasir,
jeruk nipis, dan natrium benzoat.
Air merupakan komponen penting dalam bahan makanan karena air dapat
mempengaruhi penampakan, tekstur, serta cita rasa makanan (Winarno, 1992). Air
yang digunakan dalam penelitian ini untuk mengekstraksi komponen-komponen
kimia dalam buah sawo hingga menjadi sari buah. Namun, air dalam
penggunaanya harus memenuhi beberapa persyarataan agar dapat digunakan,
20 a. Syarat fisik. Air tersebut bening (tak berwarna), tidak berasa, dan suhu
dibawah suhu diluarnya.
b. Syarat bakteriologis. Air harus terbebas dari segala macam bakteri, terutama
bakteri patogen. Untuk mengetahuinya dengan memeriksa melalui sampel
air, dalam per 100 ml sampel tidak dibolehkan terkandung bakteri E.Coli
dan total bakteri koliform (PMK No.492 tentang persyaratan kualitas air
minum).
c. Syarat kimia. Air tidak boleh mengandung zat-zat kimia berbahaya yang
dapat mempengaruhi kesehatan.
Gula atau sukrosa (gambar 4) adalah oligosakarida yang memiliki peran
penting dalam pengolahan makanan dan banyak terdapat pada tebu, bit,
siwalan,dan kelapa kopyor. Untuk industri-industri makanan biasa digunakan
sukrosa dalam bentuk kristal halus atau kasar dan dalam jumlah yang banyak
dipergunakan dalam bentuk cairan sukrosa (sirup). Pada pembuatan sirup, gula
pasir (sukrosa) dilarutkan dalam air dan dipanaskan, sebagian sukrosa akan terurai
menjadi glukosa dan fruktosa, yang disebut gula invert (Winarno, 1992). Menurut
Buckle et al (1987), sukrosa dalam pembuatan makanan berfungsi untuk memberi
rasa manis dan sebagai pengawet dimana dalam konsentrasi tinggi dapat
menghambat pertumbuhan mikroorganisme dan menurunkan aktivitas air dalam
21
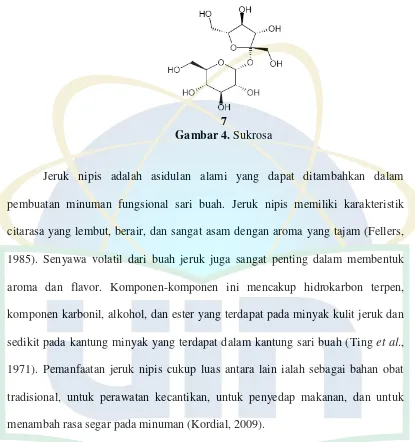
7
Gambar 4. Sukrosa
Jeruk nipis adalah asidulan alami yang dapat ditambahkan dalam
pembuatan minuman fungsional sari buah. Jeruk nipis memiliki karakteristik
citarasa yang lembut, berair, dan sangat asam dengan aroma yang tajam (Fellers,
1985). Senyawa volatil dari buah jeruk juga sangat penting dalam membentuk
aroma dan flavor. Komponen-komponen ini mencakup hidrokarbon terpen,
komponen karbonil, alkohol, dan ester yang terdapat pada minyak kulit jeruk dan
sedikit pada kantung minyak yang terdapat dalam kantung sari buah (Ting et al.,
1971). Pemanfaatan jeruk nipis cukup luas antara lain ialah sebagai bahan obat
tradisional, untuk perawatan kecantikan, untuk penyedap makanan, dan untuk
menambah rasa segar pada minuman (Kordial, 2009).
Natrium benzoat merupakan butiran atau sebuk putih tidak berbau dan
bahan ini dapat ditambahkan langsung ke dalam makanan atau dilarutkan terlebih
dahulu di dalam air atau pelarut-pelarut lainnya. Dalam penggunaanya, asam
benzoat kurang kelarutannya dalam air dibandingkan dalam bentuk garamnya,
sehingga pemakaiannya sering digunakan dalam bentuk garamnya yaitu natrium
22 Natrium benzoat merupakan pengawat sintetis yang biasa ditambahkan
pada makanan atau minuman. Aturan menteri kesehatan menyebutkan bahwa
batas penggunaan natrium benzoat pada yaitu600 mg/kg, PP No. 722/ Menkes/
Per/ IX/ 1988. Mekanisme kerja natrium benzoat sebagai pengawet yaitu
berdasarkan permeabilitas membran sel mikroba terhadap molekul-molekul asam
benzoat tidak terdisosiasi. Molekul-molekul asam benzoat tersebut dalam suasana
asam dapat mencapai sel mikroba yang membran selnya mempunyai sifat
permeabel terhadap molekul-molekul asam benzoat yang tidak terdisosiasi. Sel
mikroba yang mempunyai pH cairan sel netral akan dimasuki molekul-molekul
asam benzoat, maka molekul asam benzoat akan berdisosiasi dan menghasilkan
ion-ion H+, sehingga akan menurunkan pH mikroba tersebut. Hal ini
mengakibatkan metabolisme sel akan terganggu dan akhirnya sel mikroba tersebut
mati (Winarno dan Laksmi, 1974)
2.5. Antioksidan
Menurut Kochhar & Rossel (1990), antioksidan sebagai senyawa yang
dapat menunda, memperlambat, dan mencegah proses oksidasi lipid. Dalam arti
khusus, antioksidan adalah zat yang dapat menunda atau mencegah terjadinya
reaksi antioksidasi radikal bebas dalam oksidasi lipid.
Menurut Winarno (1997), antioksidan dibagi menjadi dua ketegori yaitu
antioksidan primer dan antioksidan sekunder. Antioksidan primer merupakan zat
yang dapat bereaksi dengan radikal bebas atau mengubahnya menjadi produk
yang stabil, sedangkan antioksidan sekunder atau antioksidan preventif dapat
23 primer (AH) bekerja dengan mekanisme seperti pada gambar 5. Antioksidan
primer (AH) bereaksi dengan oksida lipid dengan cara memberikan atom hidrogen
secara terus-menerus kepada radikal lipida (reaksi 1 dan 2). Reaksi berikutnya
berkompetisi dengan rantai reaksi propagasi (reaksi 5 dan 6).
(1) ROO*+AH ROOH + A*
(2) RO*+ AH ROH + A*
(3) ROO*+ A*ROOA
(4) RO*+ A*ROA
(5) RO*+ RH ROOH + R*
(6) ROO*+ RH R*+ ROOH
Gambar 5. Mekanisme Antioksidan Primer
Berdasarkan fungsinya, menurut Siagian (2002) antioksidan dapat dibagi
menjadi 4 tipe, yaitu:
a. Tipe pemutus rantai reaksi pembentuk radikal bebas, dengan menyumbangkan
atom H, misalnya vitamin E.
b. Tipe pereduksi, dengan mentransfer atom H atau oksigen, atau bersifat
pemulung, misalnya vitamin C.
c. Tipe pengikat logam, mampu mengikat zat peroksidan, seperti Fe2+ dan Cu2+,
misalnya flavonoid.
d. Antioksidan sekunder, mampu mendekomposisi hidroperoksida menjadi
24
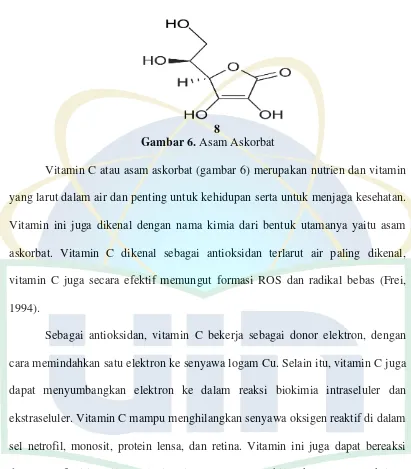
8
Gambar 6. Asam Askorbat
Vitamin C atau asam askorbat (gambar 6) merupakan nutrien dan vitamin
yang larut dalam air dan penting untuk kehidupan serta untuk menjaga kesehatan.
Vitamin ini juga dikenal dengan nama kimia dari bentuk utamanya yaitu asam
askorbat. Vitamin C dikenal sebagai antioksidan terlarut air paling dikenal,
vitamin C juga secara efektif memungut formasi ROS dan radikal bebas (Frei,
1994).
Sebagai antioksidan, vitamin C bekerja sebagai donor elektron, dengan
cara memindahkan satu elektron ke senyawa logam Cu. Selain itu, vitamin C juga
dapat menyumbangkan elektron ke dalam reaksi biokimia intraseluler dan
ekstraseluler. Vitamin C mampu menghilangkan senyawa oksigen reaktif di dalam
sel netrofil, monosit, protein lensa, dan retina. Vitamin ini juga dapat bereaksi
dengan Fe-ferritin. Diluar sel, vitamin C mampu menghilangkan senyawa oksigen
reaktif, mencegah terjadinya LDL teroksidasi, mentransfer electron ke dalam
tokoferol teroksidasi dan mengabsorpsi logam dalam saluran pencernaan (Levine,
et al., 1995).
Askorbat dapat langsung menangkap radikal bebas oksigen, baik dengan
atau tanpa katalisator enzim. Secara tidak langsung, askorbat dapat meredam
25 terhadap senyawa oksigen reaktif lebih cepat dibandingkan dengan komponen
lainnya. Askorbat juga melindungi makromolekul penting dari oksidatif. Reaksi
terhadap radikal hidroksil terbatas hanya melalui proses difusi.
Vitamin C bekerja secara sinergis dengan vitamin E. Vitamin E yang
teroksidasi radikal bebas dapat bereaksi dengan vitamin C kemudian akan berubah
menjadi tokoferol setelah mendapat ion hidrogen dari vitamin C
(Belleville-Nabeet,1996)
Sebagai zat penyapu radikal bebas, vitamin C dapat langsung bereaksi
dengan anion superoksida, radikal hidroksil, oksigen singlet dan lipid peroksida.
Sebagai reduktor asam askorbat akan mendonorkan satu elektron membentuk
semidehidroaskorbat yang tidak bersifat reaktif dan selanjutnya mengalami reaksi
disproporsionasi membentuk dehidroaskorbat yang bersifat tidak stabil.
Dehidroaskorbat akan terdegradasi membentuk asam oksalat dan asam treonat.
Oleh karena kemampuan vitamin C sebagai penghambat radikal bebas, maka
peranannya sangat penting dalam menjaga integritas membran sel (Suhartono et
al., 2007).
Menurut Asada (1992) reaksi askorbat dengan superoksida secara fisologis
mirip dengan kerja enzim SOD dan reaksi dengan hidrogen peroksida dikatalisis
26
Gambar 7. Mekanisme Reaksi Asam Askorbat dan Ion Superoksida (Atas) danHidrogen Peroksida (Bawah) (Asada, 1992)
Askorbat ditemukan dalam kloroplas, sitosol, vakuola, dan kompartemen
ekstraseluler. Kloroplas mengandung semua enzim yang berfungsi untuk
meregenerasi askorbat tereduksi dan produk-produk terioksidasi. Hidrogen
peroksida juga dihancurkan dalam kloroplas melalui reaksi redoks askorbat dan
pemanfaatan kembali glutation. Superoksida diubah menjadi hidrogen peroksida
secara spontan melalui reaksi dismutasi atau oleh enzim SOD. Hidrogen
peroksida ditangkap oleh askorbat dan enzim askorbat peroksidase (Asada, 1992).
Dalam hal ini monodehiroaskorbat memiliki 2 jalur regenerasi. Salah satunya
melalui monodehidrosiaskorbat reduktase, yang lainnya melalui dehidroaskorbat
reduktase dan glutation, sementara yang berperan sebagai donor elektron adalah
NADPH. Jalur ini juga memberikan 2 manfaat, yaitu detoksifikasi hidrogen
peroksida yang didiga berperan dalam reaksi Feton dan oksidasi NADPH.
Salah satu uji untuk menentukan aktivitas antioksidan penangkap radikal
adalah metode DPPH (1,1-Diphenyl-2-picrylhidrazyl).Metode DPPH memberikan
27 memberikan serapan kuat pada panjang gelombang 517 nm dengan warna violet
gelap. Penangkap radikal bebas menyebabkan elektron menjadi berpasangan yang
kemudian menyebabkan penghilangan warna yang sebanding dengan jumlah
elektron yang diambil (Sunarni, 2005).
Molekul 1,1-diphenyl-2-picrylhidrazil (DPPH) pada gambar 8, yang
bereaksi dengan atom hidrogen yang dilepaskan satu molekul komponen sampel
(antioksidan), pelepasan satu molekul sampel akan membentuk senyawa
1,1-diphenyl-2-21 picrylhidrazine dan radikal antioksidan yang menyebabkan
terjadinya peluruhan warna DPPH dari ungu ke kuning. Reaksi antara antioksidan
dengan molekul DPPH (Prakash, 2001).
N
Gambar8. Reaksi Radikal DPPHdengan Senyawa Antioksidan
Antioksidan alami yang paling umum adalah flavonoid (flavanol,
isoflavon, flavon, katekin, dan flavanon), turunan dari asam sinamat, kumarin,
tokoferol, dan asam organik polifungsional (Pratt et al.,1990). Secara alami,
28 bahan pangan tersebut diolah maka antioksidan yang terkandung di dalamnya
dapat mengalami degradasi kimia atau fisik sehingga fungsinya berkurang
(Fardiaz, 1980).
2.6. Analisis Sensori
Analisis sensori atau pengujian organoleptik penting dilakukan untuk
mendapatkan formulasi minuman yang tersukai sehingga dapat diketahui apakah
suatu produk dapat diterima oleh konsumen atau tidak (Muawanah et al., 2012).
Analisis sensori atau pengujian organoleptik adalah identifikasi, pengukuran
ilmiah, analisis, dan interpretasi dari karakteristik (atribut) produk berdasarkan
penerimaan melalui kelima indera manusia yaitu penglihatan, penciuman,
pencicipan, perabaan, dan pendengaran. Atribut sensori yang dianalisis dengan
pengindraan ini antara lain adalah penampilan, aroma, tekstur dan konsistensi,
citarasa, serta suara (Meilgaard, 1999).
Metode pengujian sensori melibatkan panelis dalam menilai suatu produk
pangan. Panelis adalah orang atau sekelompok orang yang menilai dan
memberikan tanggapan terhadap produk yang diuji. Panelis dapat dipilih dari
konsumen awam pengguna produk sampai seorang yang sangat ahli dalam
menilai menilai kualitas sensori. Penggunaan panelis diharapkan dapat
menjelaskan sensasi dan persepsi citarasa yang diterima oleh indra manusia
(Setyaningsih et al., 2010).
Citarasa (flavor) merupakan kompleks sensasi yang ditimbulkan oleh
berbagai indra (penciuman, pengecap, penglihatan, peraba, dan pendengaran)
29 ditimbulkan dapat berupa sensasi rasa (manis, asam, asin, dan pahit) oleh papila
lidah (taste buds), sensasi aroma oleh rongga hidung (nasal cavity), dan sensasi
pain (sepat, panas atau pedas (pungency), dingin) oleh saraf-saraf trigeminal.
Sensasi tidak langsung, seperti penampakan, suara, dan emosi juga turut
berpengaruh terhadap persepsi citarasa makanan dan minuman yang dikonsumsi.
Oleh karena itu, sensasi tersebut dapat mempengaruhi aspek penerimaan
konsumen secara keseluruhan (Lindsay, 1996).
Secara umum, Meilgaard (1999) mengklasifikasikan analisis sensori
menjadi tiga bagian yaitu, uji pembedaan, uji deskripsi, dan uji afektif.
a. Uji Pembedaan
Uji pembedaan yaitu uji yang digunakan untuk mengetahui perbedaan
diantara dua atau lebih contoh. Uji pembedaan biasanya digunakan dalam
konteks pengawasan mutu produk, studi umur simpan, dan investigasi bau atau
flavor asing.
b. Uji Deskriptif
Uji deskriptif yaitu uji yang digunakan untuk menentukan atau mengukur
karakter dan instensitas perbedaan dalam suatu produk. Uji ini lebih tepat
digunakan untuk pengembangan produk, reformulasi produk, dan untuk meneliti
perbedaan produk percobaan dengan produk komersial. Panelis yang digunakan
dalam uji ini yaitu yang sudah terlatih yang telah melalui proses seleksi dan
30 c. Uji Afektif
Uji afektif yaitu uji yang digunakan untuk mengetahui respon individu
berupa penerimaan ataupun kesukaan dari konsumen terhadap produk yang sudah
ada, produk baru, atau karakteristik khusus dari produk yang diuji. Menurut Poste
(1991), hasil uji afektif mengindikasikan pilihan, kesukaan, atau penerimaan suatu
produk. Secara umum terdapat dua macam uji afektif yaitu uji afektif kualitatif
dan uji afektif kuantitatif. Metode uji afektif kualitatatif terdiri dari focus group,
focus panel, dan wawancara personal. Sedangkan, metode uji afektif kuantitatif
terdiri dari uji kesukaan atau uji hedonik dan uji penerimaan (Meilgaard, 1999).
Menurut Poste (1991), uji kesukaan atau uji hedonik merupakan metode
pengujian yang paling umum dilakukan untuk mengukur kesukaan suatu sampel
bila dibandingkan sampel lain. Skala hedonik kemudian digunakan utnuk
menunjukkan tingkat kesukaan atau ketidaksukaan terhadap suatu produk. Skala
yang dapat digunakan pada uji hedonik yaitu skala yang berkisar antara 1 sampai
5 antara 1 sampai 5, dimana (5) Sangat Suka, (4) Suka, (3) Agak Suka, (2) Tidak
Suka, dan (1) Sangat Tidak Suka (Akhtar et al., 2010).
2.7. Instrumentasi
2.7.1. Spektrofotometri Serapan Atom (SSA)
Spektrometri serapan atom adalah bagian dari spektroskopi. Teknik
spektroskopi didasarkan pada emisi atau absorbsi radiasi elektromagnetik yang
merupakan sifat khas dari perubahan energi tertentu dalam suatu molekul atau
atom. Perubahan energi ini berupa tingkatan energi yang terkuantisasi yang
31 radiasi elektromagnetik, energi dari foton dapat dipindahkan ke atom atau
molekul sehingga dapat mengubah tingkatnya dari keadaan dasar ke keadaan
tereksitasi. Proses ini dikenal sebagai absorpsi (Anwar et al., 1989). Dalam garis
besarnya prinsip spektrofotometri serapan atom sama saja dengan
spektrofotometri sinar tampak dan ultraviolet. Perbedaan terletak pada bentuk
spektrum, cara pengerjaan sampel dan peralatannya (Rohman, 2007).
Metode spektrofotometri serapan atom, berprinsip pada absorbansi cahaya
oleh atom. Atom-atom menyerap cahaya tersebut pada panjang gelombang
tertentu, tergantung pada sifat unsurnya. Cahaya pada panjang gelombang tersebut
memiliki energi yang cukup untuk mengubah tingkat energi elektronik suatu
atom. Dengan absorpsi energi, berarti memperoleh lebih banyak energi, suatu
atom pada keadaan dasar dinaikkan tingkat energinya ke tingkat eksitasi
(Khopkar, 2003). Skema peralatan AAS (gambar 9) yaitu:
32 1. Sumber radiasi, yaitu berupa lampu katoda berongga (hollow cathoda
lamp). Lampu ini terdiri atas tabung kaca tertutuo yang mengandung suatu
katida dan anoda.
2. Atomizer,yaitu yang terdiri dari pengabut dan pembakar.
3. Monokromator, yaitu untuk memisahkan dan memilih panjang gelombang
yang digunakan dalam analisis.
4. Detektor, yaitu untuk mengukur intensitas cahaya yang melalui tempat
pengatoman.
5. Rekorder, yaitu suatu alat penunjuk atau dapat juga diartikan sebagai
sistem pencatatan hasil (Rohman, 2007).
2.7.2. Spektrofotemetri UV-VIS
Spektrofotometri merupakan suatu metode pengukuran yang digunakan
untuk mempelajari interaksi antara atom atau molekul dengan radiasi
elektromagnetik, dimana substansi kimia secara selektif menghamburkan
(scatter), menyerap atau mengemisi energi elektromagnetik pada panjang
gelombang yang digunakan dalam range ultraviolet (200-400 nm), sinar tampak
(400-700 nm), atau cahaya yang mendekati inframerah (Khopkar, 2003).
Prinsip spektrofotometri UV-Vis yakni radiasi pada rentang panjang
gelombang 200-800 nm dilewatkan melalui suatu larutan senyawa.
Elektron-elektron pada ikatan didalam molekul menjadi tereksitasi sehingga menempati
keadaan kuantum yang lebih tinggi dan dalam proses menyerap sejumlah energi
yang melewati larutan tersebut. Dua hukum empiris telah diformulasikan tentang
33 tidak tergantung terhadap intensitas sumber sinar. Hukum Beer’s menyatakan
bahwa serapan tergantung jumlah molekul yang terserap. Dari kedua hukum
tersebut dapat disajikan ke dalam persamaan berikut (Supratman, 2010):
A = log Io
I = kcb
Dimana :
A = absorbansi Io = intensitas sinar awal
I = intensitas sinar yang diteruskan c = konsentrasi sampel
b = tebal selyang dilalui sampel (cm) k = koefisien ekstingsi
Hukum Beer menyatakan bahwa absorbans berbanding langsung dengan
tebal larutan dan konsentrasi larutan. Dimana apabila suatu berkas radiasi dengan
intensitas Io dilewatkan melalui suatu larutan dalam wadah transparan setebal b
yang berisi sejumlah n partikel (atom, ion, atau molekul) maka sebagian radiasi
akan diserap sehingga intensitas radiasi yang diteruskan I menjadi lebih kecil dari
pada Io. Dimana berkurangnya intensitas radiasi tergantung dari luas penampang
yang menyerap partikel, dan luas penampang ini sebanding dengan jumlah
partikel (n). Ini menunjukkan bahwa larutan tersebut menyerap sejumlah sinar.
34 Sebuah spektrofotometer memiliki lima bagian penting (gambar 10), yaitu:
1. Sumber cahaya, untuk UV umumnya digunakan lampu deuterium (D2O),
untuk visibel digunakan lampu tungsten xenon (Auc).
2. Monokromator, suatu alat yang berfungsi mengubah cahaya polikromatik
menjadi cahaya monokromatik.
3. Sel penyerap / wadah pada sampel, cell dalam spektrofotometer disebut juga
dengan kuvet.
4. Photodetector, berfungsi untuk mengubah energi cahaya menjadi energi
listrik.
5. Analyzer (pengolah data), untuk spektrofotometer modern biasanya dilengkapi
35
BAB III
METODE PENELITIAN
3.1. Waktu dan Tempat Penelitian
Penelitian ini dilaksanakan di Pusat Laboratorium Terpadu (PLT) Kimia
Universitas Islam Negeri Syarif Hidayatullah Jakarta. Penelitian inidilaksanakan
pada bulan Mei 2013 sampai November 2013.
3.2. Alat dan Bahan
3.2.1. Alat
Alat-alat yang digunakan pada penelitianini antara lain yaitu pisau, juice
extractor, alat penyaring, botol gelas, timbangan analitik, hot plate, tanur listrik,
peralatan gelas kimia, pH meter, refraktometri, spektrofotometer UV-Vis
(Lambda 25 merk Perkin Elmer), dan spektrofotometer serapan atom (Perkin
Elmer Analyst 800).
3.2.2. Bahan
Bahan-bahan utama yang digunakan adalah buah sawo, kayu manis, jeruk
nipis, C6H3COONa, dan C12H22O11 yang didapatkan dari Pasar Tradisional
Ciputat, Tangerang Selatan. Bahan-bahan lainnnya yaitu Na2CO3, C7H6O5 (asam
galat), reagen Folin-Cicalteau, KI, I2, NaOH, HNO3, CH3OH, DPPH, PCA dan
36
3.3. Prosedur Penelitian
3.3.1. Pembuatan minuman fungsional
Pembuatan minuman fungsional dilakukan dalam beberapa tahapan yaitu,
pemilihan bahan, ekstraksi, penambahan larutan gula, natrium benzoat, dan jeruk
nipis, pengemasan, dan pasteurisasi. Buah sawo dipilih berdasarkan bentuk buah,
ukuran, warna, banyak sedikitnya noda yang merupakan faktor dari kerusakan.
Buah yang memiliki gumpalan getah dan gorasan pada kulitnya tidak dipilih
karena menandakan kematangan buah yang tidak merata atau rusaknya buah.
Sortasi atau pemilihan ulang dilakukan yang bertujuan agar didapatkan hasil yang
seragam, lalu dilakukan pembersihan dan pencucian. Kemudian, dilakukan
ekstraksi untuk mendapatkan sari buah yang diinginkan dengan menggunakan alat
juice extractor. Dilakukan penyaringan dengan penyaring dan kainuntuk
memisahkan ampas dan sari buahnya. Selanjutnya, dilakukan ekstraksi kayu
manis dengan menggunakan airselama 15 menit yang dilakukan di dalam wadah
tertutup untuk meminimalkan teruapkannya komponen volatil. Selanjutnya,
minuman fungsional dibuat dengan lima macam formulasi (tabel 3) yaitu dengan
mencampurkan perasan sari sawo, ekstrak kayu manis 0,8 % (b/v), larutan gula 30
% (b/v), jeruk nipis, dan larutan natrium benzoat (konsentrasi akhir 500 ppm).
(Aturan Menkes batas maksimum pengawetyaitu 600 mg/kg, PP No. 722/
Menkes/ Per/ IX/ 1988).Minuman dibuat dalam volume total 100 mL untuk
37
Tabel 3. Formulasi minuman sari buah sawo
Bahan Komposisi per 100 mL
829 561 401 952 733
Sari sawo (mL) 40 45 50 55 60
Ekstrak kayu manis 0,8 % b/b 40 35 30 25 20
Larutan gula 30 % (b/b) 15 15 15 15 15
Larutan Na-Benzoat (konsentrasi akhir
500 ppm) 1 1 1 1 1
Jeruk nipis (mL) 4 4 4 4 4
Minuman fungsional yang telah diformulasi lalu dikemas ke dalam botol
kaca yang sebelumnya telah disterilkan. Setelah itu, botol di pasteurisasi didalam
penangas air selama 30 detik.
3.3.2. Analisis Sensori
Analisis sensori atau uji organoleptik dilakukan melalui uji hedonik yang
mengindikasikan pilihan, kesukaan, atau penerimaan suatu produk. Parameter uji
yang digunakan yaitu parameter warna, aroma, rasa manis, rasa asam, dan
penerimaan keseluruhan. Pengujian dilakukan terhadap 20 orang panelis semi
terlatih, yaitu panelis yang bukan ahli dan juga yang bukan awam yang tidak bisa
mengenali ciri-ciri organoleptik. Pengujian dilakukandalam sebuah kuesioner
(lampiran 3) dengan menggunakan skala hedonik yang berkisar antara 1 sampai 5,
dimana (5) Sangat Suka, (4) Suka, (3) Agak Suka, (2) Tidak Suka, dan (1) Sangat
Tidak Suka (Akhtar et al., 2010). Data yang didapatkan kemudian dianalisis
dengan menggunakan software SPSS versi 17 untuk menentukan formulasi yang
paling disukai panelis. Formulasi tersukai kemudian dianalisis antioksidannya
yang meliputi pengujian aktivitas antioksidan serta komponen kimia antioksidan,
38
3.3.3. Analisis Antioksidan
Analisis antioksidan meliputi pengujian aktivitas antioksidan dan
komponen kimia antioksidan yaitu pengujian total fenolik dan kandungan vitamin
C.
3.3.3.1.Uji Aktivitas Antioksidan (Kekuda et al., 2010)
Aktivitas penghambatan radikal sampel dilakukan berdasarkan
penghambatannya pada radikal bebas 1,1-diphenyl-2-picrylhydrazil (DPPH).
Disiapkan larutan sampel pada varian konsentrasi (0,19 �L sampai 100 �L/mL)
dalam metanol. Dimasukkan masing-masing larutan sampel sebanyak 2 mL ke
dalam tabung reaksi. Setelah itu ditambahkan 2 mL larutan DPPH 0,002 % (dalam
metanol). Dilakukan inkubasi didalam ruang gelap selama 30 menit, lalu diukur
absorbansi sampel dengan spektrofotometer UV-Vis (panjang gelombang=518
nm). Besarnya aktivitas antioksidan diukur dengan parameter persen inhibisi lalu
diukur (IC50).
Persen inhibisi= � � − �
� � × 100 %
Nilai IC50 ditentukan dengan menggunakan rumus persamaan regresi
linear, dengan ekstrapolasi persen inhibisi sebagai ordinat (y) dan konsentrasi
sebagai absis (x).
3.3.3.2.Analisis Total Fenol (Heilerova et al., 2003 )
Pengukuran total fenol dilakukan dengan menggunakan reagen
Folin-Ciocalteu dan asam galat sebagai standar. Pertama-tama 0,2 mL sampeldiambil
dan kemudian ditambahkan 1 mL reagen Folin Ciocalteu 10 % (dalam air).
39 ditambahkan 3 mL larutan Na2CO32 % (dalam air). Sampel diinkubasi selama 1
jam dalam tempat gelap. Lalu absorsorbansinya diukur pada panjang gelombang
765 nm dengan spektrofotometer UV-Vis. Total fenolik ditentukan dalam
(�g/mL) berat ekuivalen asam galat (EAG) dengan menggunakan persamaan
regresi dari kurva standar asam galat (0–32 �g/mL).
3.3.3.3.Analisis Kadar Vitamin C (AOAC, 1999)
Kadar vitamin C ditentukan dengan cara titrasi Iod. Sebanyak 5 ml sampel
dimasukkan ke dalam erlenmeyer 100 ml. Ditambahkan 20 ml air destilat dan
beberapa tetes larutan pati sebagai indikator. Selanjutnya dititrasi dengan larutan
Iod 0,01 N sampai larutan berwarna biru. Tiap ml larutan Iod equivalen dengan
0,88 mg asam askorbat. Kadar vitamin C dapat dihitung sebagai asam askorbat
dengan rumus sebagai berikut :
=ml Iod 0,01 N x 0,88 x P x 100
dimana, merupakan mg asam askorbat per 100 ml sari buah dan P merupakan
faktor pengenceran.
3.3.4. Uji Sifat Kimia dan Fisik
Analisis sifat kimia dan fisik bertujuan untuk mengetahui komposisi nilai
gizi dari produk pangan. Uji sifat kimia dan fisik meliputi analisis kadar air, kadar
abu, pH, total padatan terlarut, dan total asam.
3.3.4.1. Kadar Air (AOAC, 2005)
Tahap pertama yang dilakukan untuk menganalisis kadar air adalah
mengeringkan cawan porselen dalam oven pada suhu 105°C selama 1 jam. Cawan