PROFIL KROMATOGRAFI LAPIS TIPIS PRODUK FRAKSINASI DINGIN CAMPURAN CPO(CRUDE PALM OIL)DAN PKO (PALM KERNEL OIL)
(Skripsi)
Oleh
MUHAMMAD FERDIANSYAH MULYA HARAHAP
FAKULTAS PERTANIAN UNIVERSITAS LAMPUNG
ABSTRAK
PROFIL KROMATOGRAFI LAPIS TIPIS PRODUK FRAKSINASI DINGIN CAMPURAN CPO (Crude Palm Oil)DAN PKO (Palm Kernel Oil)
Oleh
MUHAMMAD FERDIANSYAH MULYA HARAHAP
Industri pengolahan buah kelapa sawit menghasilkan produk minyak sawit mentah (Crude Palm Oil/CPO) dan minyak inti sawit (Palm Kernel Oil/PKO). Produk turunan hasil olahan buah sawit yang banyak dimanfaatkan sebagai emulsifier dan antimikroba adalah produk monogliserida (MG) dan digliserida (DG). Penelitian sebelumnya menunjukkan bahwa produk hasil fraksinasi dingin campuran CPO-PKO diketahui memiliki sifat antibakteri dan emulsifier yang baik. Penelitian ini bertujuan untuk mengetahui nilai rendemen, pola pemisahan dan aktivitas antimikroba senyawa komponen terpisah. Teknik identifikasi yang digunakan adalah kromatografi lapis tipis (KLT) silica gel. Metode penelitian dilakukan secara deskriptif dengan faktor tunggal dengan tiga ulangan. Faktor tunggal perlakuan adalah campuran eluen heksana, dietil eter, dan asam formiat 80:20:2 (v/v) sebanyak 30 ml dalam chamber, selanjutnya dilakukan pengamatan pola sebaran berdasarkan nilai Rf, nilai rendemen, dan uji aktivitas antimikroba dengan metode difusi agar sumur terhadap Escherecia coli, Staphylococcus aureus, dan Saccaromhyces cerevisiae. Hasil pemurnian produk fraksinasi dingin campuran CPO dan PKO menghasilkan lima fraksi komponen terpisah yang ditentukan berdasarkan nilai Rf yaitu MG, DG, asam lemak bebas (ALB), dan trigliserida (TG). Rendemen fraksi komponen terpisah MG, DG, etil ester (EE), ALB, dan TG sisa secara berurutan adalah 24,75%, 24,89%, 12,45%, 24,63%, dan 13,27%. Total rendemen gabungan MG dan DG rata-rata 49,65%. Komposisi MG-DG tertinggi produk fraksinasi dingin (52,54%) dengan TG sisa (12,48%).
ABSTRACT
THIN LAYER CHROMATOGRAPHY PROFILES FROM COLD FRACTIONATION PRODUCTS MIXTURE CPO (Crude Palm Oil) AND
PKO (Palm Kernel Oil)
By
MUHAMMAD FERDIANSYAH MULYA HARAHAP
Oil palm fruit processing industry produce crude palm oil (CPO) and palm kernel oil (PKO). Products derived oil palm fruit as an emulsifier and antimicrobial is a monoglycerides (MG) and diglycerides (DG). The research previously, reported that cold fractionation products mix CPO-PKO known to have antibacterial properties and good emulsifier. This study aims to determine the value of the yield, the pattern of separation and antimicrobial activity of compounds separate components. Identification technique have used the Thin Layer Chromatography (TLC) silica gel. The research methods have used single factor with three repetitions. The single factor used mixture of hexane, diethyl ether, and formic acid = 80:20:2 (v/v) 30 ml in the chamber. The observed distribution patterns based on the Rf value, the value of yield and antimicrobial activity test by the method agar diffusion on Eschercia coli, Staphylococcus aureus, and Saccaromhyces cerevisiae. The results purification of cold fractionation product mix CPO and PKO have produced five separate component fractions determined based on the value of Rf is monogliserydes (MG), dilgiserydes (DG), free faty acid (FFA/ALB), and trigliserydes (TG). The yield of fraction separate components MG, DG, ethyl ester (EE), FFA/ALB, and TG rest have produced by 24.75%, 24.89%, 12.45%, 24.63%, and 13.27%. The total yield combined of MG and DG have averaged of 49.65%. The highest composition MG-DG cold fractionation products (52.54%) with TG rest (12.48%).
KAJIAN PROFIL KROMATOGRAFI LAPIS TIPIS PRODUK FRAKSINASI DINGIN DARI CAMPURAN CPO (CRUDE PALM OIL ) DAN PKO (PALM KERNEL OIL )
Oleh
MUHAMMAD FERDIANSYAH MULYA HARAHAP
Skripsi
Sebagai Salah Satu Syarat untuk Mencapai Gelar SARJANA TEKNOLOGI PERTANIAN
Pada
Jurusan Teknologi Hasil Pertanian Fakultas Pertanian Universitas Lampung
FAKULTAS PERTANIAN UNIVERSITAS LAMPUNG
RIWAYAT HIDUP
Penulis dilahirkan di Bandar Lampung pada tanggal 2 Juli 1990, sebagai anak pertama dari dua bersaudara dari pasangan Bapak Bonardin Saleh Harahap (alm) dan Ibu Nurmaulina Siregar.
Pendidikan penulis diawali di Taman Kanak-kanak Kedaton Way Galih Bandar Lampung yang diselesaikan pada tahun 1996, kemudian dilanjutkan ke Sekolah Dasar Al-Azhar 1 Way Halim Bandar Lampung yang diselesaikan tahun 2002, melanjutkan Sekolah Menengah Pertama di SMP Negeri 1 Bandar Lampung, diselesaikan pada tahun 2005, dan Sekolah Menengah Atas di SMA Negeri 2 Bandar Lampung yang diselesaikan pada tahun 2008.
SANWACANA
Puji syukur penulis ucapkan ke hadirat Allah SWT, karena atas rahmat dan kuasa-Nya skripsi dengan judul“Profil Kromatografi Lapis Tipis Produk Fraksinasi
Dingin Campuran CPO (Crude Palm Oil) dan PKO (Palm Kernel Oil)”adalah salah satu syarat untuk memperoleh gelar Sarjana Teknologi Pertanian di Universitas Lampung dapat diselesaikan.
Dalam kesempatan ini penulis mengucapka terima kasih kepada:
1. Bapak Prof. Dr. Ir. Wan Abbas Zakaria, M.S., selaku Dekan Fakultas Pertanian Universitas Lampung;
2. Ibu Ir. Susilawati, M.S., selaku Ketua Jurusan Teknologi Hasil Pertanian Fakultas Pertanian Universitas Lampung atas izin penelitian yang diberikan; 3. Bapak Dr. Ir. Murhadi, M.Si. selaku Pembimbing Satu skripsi yang telah
banyak memberikan pengarahan, saran dan masukan dalam menyelesaikan skripsi ini;
5. Ibu Ir. Sri Setyani, M.S. selaku Penguji yang telah memberikan saran-saran guna terselesaikanya skripsi ini;
6. Ayah (alm), Ibu, Adik, semua keluarga besar dan Gista yang telah memberikan dukungan, motivasi, dan kasih sayang yang selalu menyertai penulis dalam doa dan pendampingan;
7. Teman angkatan 2008 jurusan Teknologi Hasil Pertanian (THP) yang selalu memberikan dukungan serta adik-adik dan kakak-kakak keluarga besar HMJ THP FP Unila atas kebersamaan dan persahabatan yang luar biasa.
Penulis berharap semoga Allah SWT membalas kebaikan mereka dan semoga laporan skripsi ini dapat bermanfaat bagi kita semua.
Bandar Lampung, 13 April 2015 Penulis
DAFTAR ISI
Halaman
DAFTAR TABEL ... iv
DAFTAR GAMBAR ... v
I. PENDAHULUAN ... 1
1.1. Latar Belakang dan Masalah ... 1
1.2. Tujuan Penelitian ... 3
1.3. Kerangka Pemikiran ... 3
II. TINJAUAN PUSTAKA ... 7
2.1. Tanaman Kelapa Sawit ... 7
2.1.1. Minyak sawit mentah (CPO) ... 8
2.1.2. Minyak inti sawit (PKO) ... 11
2.2. Etanolisis Trigliserida ... 14
2.3. Fraksinasi ... 16
2.4. Antimikroba ... 19
2.5. Kromatografi Lapis Tipis ... 20
2.5.1. Fase diam (penjerap) ... 21
2.5.2. Fase gerak (pelarut pengembang) ... 22
2.5.3. Nilai Rf ... 22
2.5.4. Kromatografi lapis tipis preparatif ... 23
2.6. Karakteristik Bakteri Uji ... 24
2.6.1. Staphylococcus aureus ... 24
2.6.2. Escherichia coli ... 25
III. BAHAN DAN METODE ... 27
3.1. Tempat dan Waktu ... 27
3.2. Bahan dan Alat ... 27
3.3. Metode Penelitian ... 28
3.4. Pelaksanaan Penelitian ... 28
3.4.1. Persiapan bahan utama ... 29
3.4.2. Persiapan pelarut etanol-NaOH 1% ... 29
3.4.3. Produksi etanolisis kasar ... 30
3.4.4. Fraksinasi ... 30
3.4.5. Identifikasi komponen gliserdia ... 31
3.5. Pengamatan ... 31
3.5.1. Nilai Rf dan pola sebaran komponen terpisah ... 32
3.5.2. Rendemen fraksi massa komponen terpisah ... 33
3.5.3. Pengujian aktivitas antimikroba ... 34
IV. HASIL DAN PEMBAHASAN ... 37
4.1. Fraksinasi Kromatografi Lapis Tipis Produk Etanolisis ... 37
4.2. Nilai Rf dan Pola Sebaran Produk Fraksinasi Dingin ... 38
4.3. Rendemen Fraksi Komponen Terpisah ... 42
4.4.. Aktivitas Antimikroba ... 45
4.4.1. Staphylococcus aureus ... 46
4.4.2. Escherecia coli ... 48
4.4.3. Saccahromyces cerevisiae ... 50
V. KESIMPULAN DAN SARAN ... 51
5.1. Simpulan ... 51
5.2. Saran ... 51
DAFTAR PUSTAKA ... 53
DAFTAR GAMBAR
Gambar
Halaman
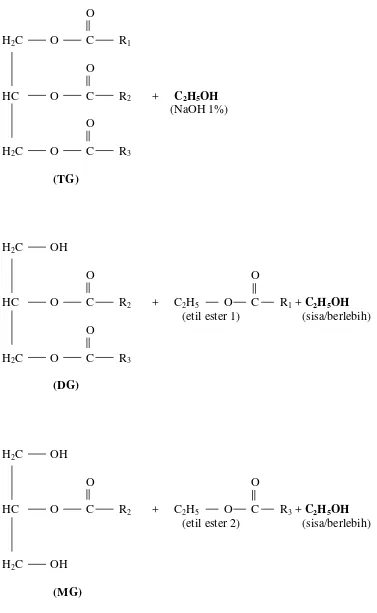
1. Tahapan reaksi etanolisis trigliserida (TG) menghasilkan digliserida
(DG), monogliserida (MG), dan etil ester asam lemak ... 15
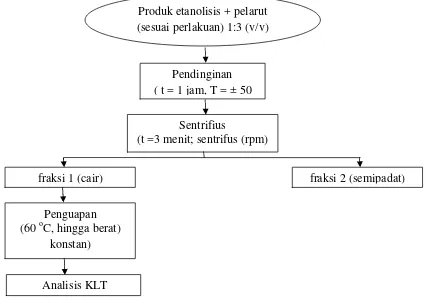
2. Diagram alir fraksinasi dingin produk etanolisis kasar dari campuran CPO dan PKO ... 31
3. Preparasi sampel pada lempeng KLT... 32
4. Pengamatan spot pada lempeng KLT... 33
5. Hasil etanolisis campuran CPO dan PKO ... 37
6. Fraksi cair dan semipadat hasil fraksinasi dingin... 38
7. Hasil pemisahan fraksi-fraksi komponen terpisah produk fraksinasi dingin etanolisis dari campuran CPO dan PKO menggunakan KLT ... 41
8. Zona hambat anti-Staphylococcus aureuspada MG dan DG dengan menggunakan pelarut etanol... 46
9. Nilai diameter zona hambat anti-Staphylococcus aureus komponen terpisah hasil fraksinasi KLT produk fraksinasi dingin etanolisis campuran CPO-PKO dengan pelarut etanol... 47
11. Nilai diameter zona hambat anti-Escherichia coli komponen terpisah hasil fraksinasi KLT produk fraksinasi dingin campuran CPO-PKO
dengan pelarut etanol ... 49
12. Proses etanolisis CPO-PKO ... 63
13. Proses fraksinasi dingin ... 64
DAFTAR TABEL
Tabel Halaman
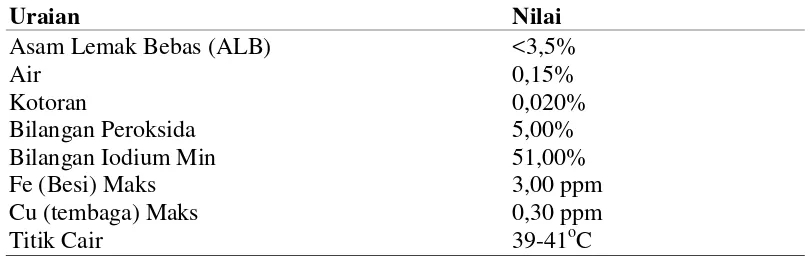
1. Kualitas CPO yang dihasilkan PTPN XIII ... 9
2. Komposisi minyak sawit mentah (CPO) dan minyak inti sawit (PKO)... 10
3. Sifat kimia minyak sawit mentah ... 10
4. Sifat fisika minyak sawit mentah ... 10
5. Kandungan inti sawit di PTPN XIII ... 12
6. Sifat-sifat fisik PKO ... 12
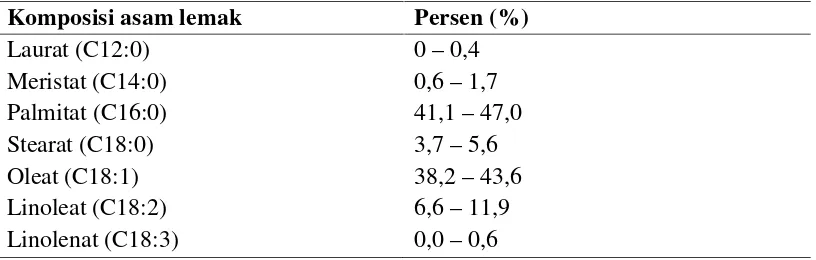
7. Komposisi asam lemak jenuh... 13
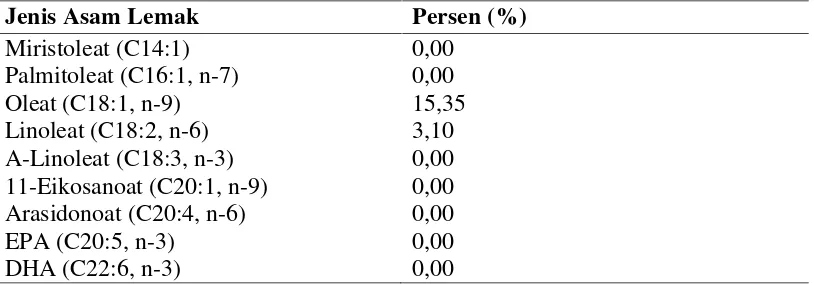
8. Komposisi asam lemak tidak jenuh PKO... 13
9. Nilai Rf komponen terpisah dari masing-masing produk fraksinasi dingin CPO-PKO... 38
10. Nilai Rf komponen terpisah dari masing-masing produk etanolisis kasar PKO pada penelitian sebelumnya ... 39
11. Rendemen fraksi komponen terpisah dari masing-masing produk fraksinasi dingin CPO-PKO ... 41
13. Berat masing-masing fraksi komponen terpisah hasil fraksinasi KLT
produk etanolisis campuran CPO dan PKO ... 59 14. Rendemen fraksi komponen terpisah hasil fraksinasi KLT produk
etanolisis campuran CPO dan PKO... 60 15. Perhitungan nilai diameter zona hambat komponen fraksi terpisah
dengan etanol padaEscherecia coli... 61 16. Perhitungan nilai diameter zona hambat komponen fraksi terpisah
I. PENDAHULUAN
1.1. Latar Belakang dan Masalah
Propinsi Lampung merupakan salah satu daerah paling potensial untuk menghasilkan produk-produk dari buah sawit. Tahun 2008 total luas areal perkebunan kelapa sawit di Provinsi Lampung mencapai 75.150 Ha (Perkebunan Besar Negara 11.379 Ha dan Perkebunan Besar Swasta 63.771 Ha) belum termasuk yang diusahakan rakyat (Perkebunan Rakyat/PR), terutama di lima Kabupaten, yaitu: Tulang Bawang, Way Kanan, Lampung Tengah, Lampung Utara, dan Lampung Barat (Anonim, 2009). Industri pengolahan buah kelapa sawit (Elaeis guineensis Jacq) dapat menghasilkan produk utama berupa minyak sawit mentah (crude palm oil/CPO) dan minyak inti sawit (palm kernel oil/PKO). Minyak kelapa sawit diperoleh dari pengolahan buah kelapa sawit (Murhadi dan Suharyono, 2008).
2
terutama minyak inti sawit adalah produk monogliserida (MG) dan digliserida (DG). Produk MG-DG dapat bermanfaat sebagai emulsifier dan berfungsi sebagai antibakteri (Lestari dan Murhadi, 2008). MG umumnya dibuat dari reaksi langsung gliserol dengan asam lemak bebas (reesterifikasi) atau dengan hidrolisis lemak (trigliserida atau digliserida) di dalam suatu katalisator bersifat alkali. Metode produksi MG-DG yang dinilai cukup potensial adalah dengan reaksi etanolisis (Murhadi dan Zuidar, 2009).
3
1.2. Tujuan
Tujuan penelitian ini untuk mengetahui profil kromatofrafi lapis tipis (nilai Rf pola sebaran komponen terpisah dan rendemen fraksi massa) serta diameter zona hambat aktivitas antimikroba komponen terpisah hasil fraksinasi dingin campuran CPO dan PKO.
1.3. Kerangka Pemikiran
Minyak sawit mengandung senyawa-senyawa aktif diantaranya adalah asam lemak yang berada dalam bentuk trigliserida. Trigliserida akan dipisahkan seacara langsung dari minyak sawit dengan menggunakan teknik transesterifikasi Proses transesterifikasi pada penelitian ini menggunakan pelarut etanol dengan katalis basa pada suhu pemanasan 400C selama 8 menit.
4
Menurut Gunstone et al., (1997), fraksinasi merupakan proses thermomechanical dimana bahan dasar (raw material) dipisahkan menjadi dua atau lebih fraksi. Proses ini dilakukan dalam dua tahap yaitu proses kristalisasi dengan cara mengatur kondisi suhu, dan tahap dua memisahkan fraksi MDAG (mono-diasil gliserida) tersebut dengan cara penyaringan. Fraksinasi yang dilakukan secara berulang (double fractionation) akan menghasilkan fraksi minyak yang lebih beragam untuk diaplikasikan ke dalam berbagai produk pangan (Gunstone et al., 1994).
Monogliserida (MG) adalah ikatan ester umumnya pada posisi 1, 3 atau 2 suatu asam lemak tertentu pada gliserol yang memiliki sifat semipolar atau relatif polar tergantung dari jenis asam yang teresterkan. Asam-asam lemak yang memiliki rantai karbon panjang jenuh (C16:0 dan C18:0) lebih berkontribusi kepada sifat
semipolar menuju nonpolar, sedangkan asam-asam lemak dengan rantai karbon pendek sampai sedang (C8:0 sampai C12:0) menyebabkan produk MG yang
dihasilkan bersifat semipolar menuju relatif polar. Nilai kepolaran produk MG ini yang menentukan sifat kepolarannya pada beberapa pelarut organik dan memiliki sifat kepolaran yang berbeda dengan trigliserida.
5
perlakuan pelarut etanol dengan kecepatan dengan sentrifus 3000 rpm yaitu sebesar 15,01 mm untuk Staphylococcus aureus dan pada perlakuan pelarut etil asetat dengan sentrifus 1000 rpm yaitu sebesar 11,52 mm untuk kultur mikroba alami. Fraksi 1 pada penelitiannya menghasilkan daya aktivitas antimikroba dan emulsifier yang cukup baik. Hal ini diduga adanya monogliserida dan digliserida (asam lemak dengan rantai pendek seperti laurat) yang bersifat relatif polar, larut dalam pelarut etanol dan etil asetat yang memiliki sifat kapilaritas masing-masing yaitu polar dan semi-polar.
MG dan DG yang dominan diisi oleh asam lemak rantai panjang diduga akan menunjukkan Rf (Retention factor) yang berbeda dengan MG dan DG yang dominan diisi oleh asam lemak rantai pendek. Nilai Rf merupakan parameter karakteristik kromatografi lapis tipis dan kromatografi kertas. Nilai Rf didefinisikan sebagai pervandingan antara jarak senyawa dari titik awal dan jarak titik tengah noda dari titik awal/jarak tepi muka pelarut dari titik awal. Beberapa faktor yang menentukan harga Rf yaitu pelarut, suhu, ukuran dari bejana, kertas dan sifat campuran.
6
heksan dan eter merupakan pelarut non-polar sehingga dapat melarutkan trigliserida dan asam lemak bebas dengan sangat baik.
II. TINJAUAN PUSTAKA
2.1. Tanaman Kelapa Sawit
Kelapa sawit (Elaeis guineensis Jacq) adalah tumbuhan industri penting penghasil minyak goreng, minyak industri maupun bahan bakar (biodiesel). Buah sawit mempunyai warna bervariasi dari hitam, ungu, hingga merah tergantung bibit yang digunakan. Minyak dihasilkan oleh buah. Kandungan minyak bertambah sesuai kematangan buah. Setelah melewati fase matang, kandungan asam lemak bebas (FFA) akan meningkat dan buah akan rontok dengan sendirinya. Buah terdiri dari tiga lapisan:
a. Eksokarp, bagian kulit buah berawarna kemerahan dan licin. b. Mesokarp, serabut buah.
c. Endokarp, cangkang pelindung inti. Inti sawit (kernel, yang sebetulnya adalah biji) merupakan endosperma dan embrio dengan kandungan minyak inti berkualitas tinggi
8
sawit yang terdapat pada kernel. Kedua jenis minyak ini berbeda dalam komposisi asam lemak dan sifat fisiko-kimianya. Kandungan karoten dapat mencapai 1000 ppm atau lebih, tetapi pada minyak jenis tenera lebih kurang 500-700 ppm, kandungan tokoferol bervariasi dan dipengaruhi oleh penanganan selama produksi (Ketaren, 2005).
2.1.1. Minyak sawit mentah (CPO)
Minyak sawit mentah (CPO) mengandung sekitar 500-700 ppm karoten dan merupakan bahan pangan sumber karoten alami terbesar. Oleh karena itu CPO berwarna merah jingga dan jumlahnya juga cukup tinggi. Minyak sawit ini diperoleh dari mesokarp buah kelap sawit melalui ektraksi dan mengandung sedikit air serta serat halus yang berwarna kuning sampai merah dan berbentuk semi solid pada suhu ruang. Dengan adanya alur dan serat halus tersebut menyebabkan minyak sawit mentah tidak dapat langsung digunakan sebagai bahan pangan maupun non-pangan (Naibaho, 1988).
9
menghasilkan produk minyak sawit CPO rata–rata 1000-1100 ton/hari dengan norma kualitas sebagai berikut yang disajikan pada Tabel 1.
Tabel 1. Kualitas CPO yang dihasilkan PTPN XIII
Uraian Nilai
Asam Lemak Bebas (ALB) <3,5%
Air 0,15%
Kotoran 0,020%
Bilangan Peroksida 5,00%
Bilangan Iodium Min 51,00%
Fe (Besi) Maks 3,00 ppm
Cu (tembaga) Maks 0,30 ppm
Titik Cair 39-41oC
Sumber : (PUSINFO, 2011)
Sifat-sifat minyak kelapa sawit dipengaruhi oleh ikatan kimia unsur C dan jumlah atom C yang membangun asam lemak tersebut, sedangkan sifat-sifat fisik dipengaruhi oleh sifat-sifat kimianya. Minyak merupakan gliserida yang terdiri dari berbagai asam lemak, sedangkan titik cair gliserida tersebut tergantung pada kejenuhan asam. Semakin jenuh asam lemaknya semakin tinggi titik cair dari
10
Tabel 2. Komposisi asam lemak minyak sawit mentah (CPO)
Komposisi asam lemak Persen (%)
Tabel 3. Sifat kimia minyak sawit mentah
Parameter Batas Nilai
Bilangan iodin (mg I2/1000 g) 52-54
Bilangan penyabunan (mg KOH/g) 198-205
Mengandung zat warna alfa dan beta karotenoit (0,05-0,2%) Kandungan karoten 297-313
Sumber: (Ketaren, 1986)
Tabel 4. Sifat fisika minyak sawit mentah
Parameter Batas Nilai
Specific gravity(250C/15,50C) 0,917-0,919
Density(g/ml) 0,8910
Massa jenis 0,9
Indeks bias 1,4565-1,0445
Berat molekul 200,31
Melting point(0C) 33-39
Boiling point(0C), P =10 mm Hg 170
11
Kegunaan minyak sawit mentah CPO selain minyak goreng kelapa sawit, dapat dijadikan margarine, shortening, vanaspati (vegetable ghee), ice creams, bakery fats, instans noodle, sabun dan detergent, cocoa butter extender, chocolate dan coatings, specialty fats, dry soap mixes, sugar confectionary, biskuit cream fats,
filled milk, lubrication, textiles oils dan bio diesel. Khusus untuk biodiesel, permintaan akan produk ini pada beberapa tahun mendatang akan semakin meningkat, terutama dengan diterapkannya kebijaksanaan di beberapa negara Eropa dan Jepang untuk menggunakanrenewable energy(Anonim, 2010).
CPO mengandung asam palmitat dan oleat yang tinggi (sekitar 86%) yang diharapkan akan berkontribusi pada penguatan sifat emulsifier serta kandungan asam laurat dan miristat (sekitar 65%) yang telah terbukti sebagai substansi antibakteri dan antikhamir. Produk etanolisis dari campuran PKO dan CPO (berbasis sawit) dimungkinkan sebagai produk baru Bahan Tambahan Pangan (BTP) yang berperan fungsional, baik sebagai pengemulsi maupun sebagai pengawet pangan bagi beberapa produk pangan hasil pabrik.
2.1.2. Minyak inti sawit (PKO)
12
48.2% dan 16,2%. Bilangan iod minyak inti sawit adalah 35-40 g/100g minyak dengan titik leleh sekitar 35oC (Weiss, 1985). PKO ini berupa minyak putih kekuning-kuningan yang diperoleh dari proses ekstraksi inti buah tanaman kelapa sawit. Standar mutu PKO di Indonesia tercantum di dalam Standar Produksi (SP 10-1975). Adapun syarat mutu PKO adalah kadar minyak minimun 48%; kadar air maksimum 8,5%; kontaminan maksimum 4,0%; kadar inti pecah maksimum 15%, warna maksimum 40%, dan asam lemak bebas maksimum 0,1% (Liang, 2009). PTPN XIII menghasilkan produk inti sawit/palm kernel rata-rata 210-220 ton/hari dengan norma yang disajikan pada Tabel 5 dan adapun sifat-sifat fisika PKO seperti terlihat pada Tabel 6.
Tabel 5. Kandungan inti sawit di PTPN XIII
13
Asam oleat dapat dihasilkan dari fraksinasi asam lemak yang diperoleh dari proses pengubahan minyak menjadi asam lemak. Asam oleat dapat dihasilkan dari fraksinasi asam lemak yang diperoleh dari hidrolisis lemak. Dalam industri asam oleat banyak digunakan sebagai surface active, emulsifier, dan dalam produk-produk kosmetika. Kegunaan produk-produk ini (asam oleat) adalah sebagai berikut: industri minuman, seperti pembuatan susu; industri sabun dan detergen; industri kosmetik; industri minyak goring, dan industri bahan makanan. Adapun komposisi asam lemak asam lemak lainya pada PKO disajikan pada Tabel 7 dan Tabel 8.
Tabel 7. Komposisi asam lemak jenuh PKO
Jenis Asam Lemak Persen (%)
Tabel 8. Komposisi asam lemak tidak jenuh PKO
14
2.2. Etanolisis Trigliserida
Etanolisis merupakan salah satu metode reaksi yang digunakan untuk menghasilkan produk monogliserida (MG) dan digliserida (DG) dari trigliserida (TG) minyak nabati. Reaksi etanolisis pada minyak nabati khususnya trigliserida (TG) melalui tiga tahapan raksi, yaitu: (1) Trigleserida bereaksi dengan etanol dalam suasana basa menghasilkan digliserida dan etil ester pertama dari posisi asam lemak ke-1/ sn-1, (2) digliserida selanjutnya bereaksi dengan sisa etanol berlebih dalam suasana basa menghasilkan monogliserida dan etil ester kedua dari posisi asam lemak ke-3/ sn-3, dan (3) jika reaksi berlanjut, monogliserida akan bereaksi dengan sisa etanol berlebih dalam suasana basa menghasilkan gliserol dan etil ester dari posisi asam lemak ke-2/sn-2 (Hassanudinet al., 2003).
15
O
H2C O C R1
O
HC O C R2 + C2H5OH
(NaOH 1%) O
H2C O C R3
(TG)
H2C OH
O O
HC O C R2 + C2H5 O C R1+C2H5OH (etil ester 1) (sisa/berlebih) O
H2C O C R3
(DG)
H2C OH
O O
HC O C R2 + C2H5 O C R3+C2H5OH
(etil ester 2) (sisa/berlebih)
H2C OH
(MG)
16
Menurut Murhadi (2005), minyak disusun oleh turunan karboksilat dari ester gliserol yang disebut gliserida. Gliserida terdiri dari sebagian besar trigliserida (TG) yang ketiga gugus OH(-)dari gliserol diesterkan oleh asam karboksilat berantai panjang C12 sampai C24). TG merupakan senyawa ester 3 asam lemak dengan gliserol yang disebut minyak netral dan merupakan komponen utama dari storage lipidpada hewan dan tumbuhan yang bersifat hidrofobik atau nonpolar. TG terdiri dari TG sederhana (tristearin, tripalmitin, dan triolein) dan TG campuran.
Digliserol merupakan senyawa 2 ester asam lemak dengan gliserol. Digliserol (DG) dihasilkan dari hasil hidrolisis TG oleh panas dan katalis atau enzim lipase. DG bersifat relatig semipolar dan dapat berfungsi sebagai emulsifier, karena memiliki gugus polar dan nonpolar. Monogliserol (MG) merupakan senyawa 1 ester asam lemak dengan gliserol. MG dihasilkan dari hidrolisis TG atau DG atau dari reaksi re-esterifikasi antara ALB dengan gliserol. MG bersifat semipolar atau polar, dapat berfungsi sebagai antimikroba terutama jika asam lemak yang
teresterkan merupakan asam lemak laurat (Murhadi, 2005).
2.3. Fraksinasi
17
dan digliserida, dan turunan minyak lainnya, untuk menghasilkan fraksi dengan sifat yang diinginkan untuk aplikasinya dalam industri pangan, industri sabun, industri oleokimia dan farmasi (O’Brienet al., 2000)
Secara umum proses fraksinasi dilakukan dalam dua tahap yaitu proses kristalisasi dengan cara mengatur kondisi suhu, dan tahap kedua memisahkan fraksi tersebut dengan cara penyaringan (filtrasi). Menurut Breeding dan Marshal (1995), proses kristalisasi biasanya menggunakan suhu rendah dan proses filtrasinya menggunakan membran press filter. Menurut Winarno (1997), bila suatu lemak didinginkan, hilangnya panas akan memperlambat gerakan partikel-partikel dalam molekul, sehingga jarak antara molekul lebih kecil.
18
trigliserida tertentu, dan pemisahan menjadi dua fraksi untuk aplikasi yang lebih luas, misalnya fraksinasi minyak kelapa sawit menjadi fraksi olein dan stearin. Menurut O’Brien et al., (2000), ada tiga prinsip dasar yang berbeda dalam
fraksinasi antara lain fraksinasi kering (dry fractionation), fraksinasi dengan pelarut (solvent fractionation), dan fraksinasi menggunakan deterjen atau bahan kimia lain (detergent fractionation).
19
berlangsung dalam suspensi cair. Kemudian dilakukan sentrifugasi agar fraksi olein dan stearin terpisah. Fraksi olein kemudian dicuci dengan air panas untuk menghilangkan sisa deterjen lalu dikeringkan dengan vaccum dryer. Olein yang diperoleh mencapai 80% (Moran dan Rajah, 1994).
Penurunan suhu, fraksi stearin yang memiliki titik leleh tinggi (48-50 oC) lebih mudah membeku, sedangkan fraksi olein yang memiliki titik leleh rendah (18-20
o
C) tetap berbentuk cair dan sebagian besar karotenoid yang larut minyak ikut terlarut ke dalam fraksi olein (Gunstone dan Noris, 1983). Fraksi olein berwarna merah sedangkan fraksi stearin berwarna kuning pucat. Warna merah pada olein disebabkan kandungan karotenoid yang terlarut di dalamnya sedangkan fraksi stearin hanya sedikit mengandung karotenoid.
2.4. Antimikroba
Senyawa antimikroba didefinisikan sebagai senyawa biologis atau kimia yang dapat menghambat pertumbuhan dan aktivitas mikroba (Pelzcar dan Reid, 1979). Beberapa jenis senyawa yang mempunyai aktivitas antimikroba adalah sodium benzoate, senyawa fenol, asam-asam organik, asam lemak rantai medium dan esternya, sorbet, sulfur dioksida, sulfit, nitrit, surfaktan, dimetil karbonat dan metal askorbat (Davidson dan Branen, 1993).
20
lisis, penghambatan system metabolisme dalam sel dengan cara menghambat kerja enzim intraseluler, dan merusak membran sel (Pelzcar dan Reid, 1979). Kerusakan membran sel oleh senyawa antimikroba mengakibatkan terjadinya kebocoran sel yang ditandai dengan keluarnya berbagai komponen penting dalam sel bakteri, seperti proten, asam nukleat, nukleutida dan lain-lain (Vincent, 1987).
Aktivitas antimikroba asam-asam lemak dari sumber minyak/lemak tanaman. Lemak (trigliserida) tidak memiliki penghambatan terhadap mikroba, kecuali yang mengandung asam-asam lemak berantai karbon rendah-sedang terutama dalam bentuk monogliserida. Secara umum, asam lemak jenuh yang paling efektif sebagai senyawa antibakteri adalah asam laurat (12:0) dalam bentuk monolaurin, sedangkan untuk asam lemak tidak jenuh tunggal dan asam lemak tidak jenuh ganda, masing-masing adalah asam palmitoleat (16:1) dan asam linolenat (18:3) relatif tidak memiliki sifat antimikroba. Jumlah ikatan rangkap pada asam lemak C12-C22 lebih mempengaruhi aktivitas antimikroba asam lemat tersebut. Konfigurasi geometri stuktur asam lemak yang aktif sebagai antimikroba adalah bentukcis, sedangkan bentuk isomer trans tidak aktif. Asam lemak dalam bentuk ester alkohol monohidrat mengakibatkan inaktivasi antibakteri, sementara itu dalam bentuk ester polizol dan gliserol dapat meningkatkan aktivitas bakterinya (Kabara, 1984)
2.5. Kromatografi Lapis Tipis
21
larutan yang di totolkan baik berupa bercak ataupun pita. Setelah plat atau lapisan dimasukkan ke dalam bejana tertutup rapat yang berisi larutan pengembang yang cocok (fase gerak), pemisahan terjadi selama perambatan kapiler (pengembangan). Selanjutnya senyawa yang tidak berwarna harus ditampakkan (Stahl, 1985).
Pendeteksian bercak hasil pemisahan dapat dilakukan dengan beberapa cara. Untuk senyawa tak berwarna cara yang paling sederhana adalah dilakukan pengamatan dengan sinar ultraviolet. Beberapa senyawa organik bersinar atau berfluoresensi jika disinari dengan sinar ultraviolet gelombang pendek (254 nm) atau gelombang panjang (366 nm). Jika dengan cara itu senyawa tidak dapat dideteksi maka harus dicoba disemprot dengan pereaksi yang membuat bercak tersebut tampak yaitu pertama tanpa pemanasan, kemudian bila perlu dengan pemanasan (Gritteret al., 1991).
2.5.1 Fase diam (lapisan penjerap)
Pada kromatografi lapis tipis, fase diam berupa lapisan tipis yang terdiri atas bahan padat yang dilapiskan pada permukaan penyangga datar yang biasanya terbuat dari kaca, dapat pula terbuat dari plat polimer atau logam. Lapisan melekat pada permukaan dengan bantuan bahan pengikat, biasanya kalsium sulfat atau amilum (pati). Penjerap yang umum dipakai untuk kromatografi lapis tipis adalah silika gel, alumina, kieselgur, dan selulosa (Gritteret al., 1991).
22
Ukuran partikel yang biasa digunakan adalah 1-25 mikron. Partikel yang butirannya sangat kasar tidak akan memberikan hasil yang memuaskan dan salah satu cara untuk memperbaiki hasil pemisahan adalah dengan menggunakan fase diam yang butirannya lebih halus. Butiran yang halus memberikan aliran pelarut yang lebih lambat dan resolusi yang lebih baik (Sastrohamidjojo, 1985).
2.5.2. Fase gerak (pelarut pengembang)
Fase gerak ialah medium angkut yang terdiri atas satu atau beberapa pelarut. Jika diperlukan sistem pelarut multi komponen, harus berupa suatu campuran sesederhana mungkin yang terdiri atas maksimum tiga komponen (Stahl, 1985). Dalam pemisahan senyawa organik selalu menggunakan pelarut campur. Tujuan menggunakan pelarut campur adalah untuk memperoleh pemisahan senyawa yang baik. Kombinasi pelarut adalah berdasarkan atas polaritas masing-masing pelarut, sehingga dengan demikian akan diperoleh sistem pengembang yang cocok. Pelarut pengembang yang digunakan dalam kromatografi lapis tipis antara lain: n-heksana, karbontetraklorida, benzena, kloroform, eter, etilasetat, piridian,
aseton, etanol, metanol dan air (Gritteret al., 1991).
2.5.3. Nilai Rf
23
dan kerataan dari lapisan penjerap, pelarut dan derajat kemurniannya, derajat kejenuhan uap pengembang dalam bejana, teknik percobaan, jumlah cuplikan yang digunakan, suhu, dan kesetimbangan (Sastrohamidjojo, 1985).
2.5.4. Kromatografi lapis tipis preparatif
Kromatografi Lapis Tipis (KLT) preparatif merupakan salah satu metode pemisahan dengan menggunakan peralatan sederhana. Ketebalan penjerap yang sering dipakai adalah 0,5-2 mm. ukuran plat kromatografi biasanya 20x20 cm. Pembatasan ketebalan lapisan dan ukuran plat sudah tentu mengurangi jumlah bahan yang dapat dipisahkan dengan KLT preparatif. Penjerap yang paling umum digunakan adalah silika gel.
Penotolan cuplikan dilakukan dengan melarutkan cuplikan dalam sedikit pelarut. Cuplikan ditotolkan berupa pita dengan jarak sesempit mungkin karena pemisahan tergantung pada lebar pita. Penotolan dapat dilakukan dengan pipet tetapi lebih baik dengan penotol otomatis. Pelarut yang baik untuk melarutkan cuplikan adalah pelarut yang atsiri. Pengembangan plat KLT preparatif dilakukan dalam bejana kaca yang dapat menampung beberapa plat. Bejana dijaga tetap jenuh dengan pelarut pengembang dengan bantuan kertas saring yang diletakkan berdiri disekeliling permukaan bagian dalam bejana (Hostettmannet al.,1995).
24
dengan cara menutup plat dengan sepotong kaca lalu menyemprot kedua sisi dengan penyemprot (Hostettmannet al., 1995).
Setelah pita ditampakkan dengan cara yang tidak merusak maka senyawa yang tidak berwarna dengan penjerap dikerok dari plat kaca. Cara ini berguna untuk memisahkan campuran beberapa senyawa sehingga diperoleh senyawa murni (Gritteret al., 1991).
2.6. Karakteristik Bakteri Uji
2.6.1.Staphylococcus aureus
Staphylococcus aureus adalah bakteri gram positif dan jika diamati di bawah mikroskop akan tampak dalam bentuk bulat tunggal atau berpasangan, atau berkelompok seperti buah anggur. S. aureus termasuk dalam famili Staphylococcaceae, berukuran diameter 0,5-1,5 µm dan membentuk pigmen
kuning keemasan. Bakteri ini tidak membentuk spora, bersifat aerob atau anaerob fakultatif, non-motil, koagulase dan katalase positif, mampu memfermentasi manitol seta mampu menjalankan dua macam metabolisme respirasi maupun fermentasi.
25
KeberadaanS. aureusdalam bahan pangan erat kaitannya dengan sanitasi pekerja serta kebersihan lingkungan dan peralatan pengolahan. Pangan yang dilaporkan dalam berbagai kejadian luar biasa S. aureus umumnya diolah dengan proses pemotongan, pemarutan, dan penggilingan yang melibatkan pekerja yang terkontaminasi. S. aureus terdapat luas di alam dan pada bahan baku pangan sehingga penganan yang kurang tepat dapat meningkatkan risiko keracunan pangan akibatS. aureus(Robinsonet al.,2000).
S.aureus memiliki beberapa jenis faktor virulensi yang mendukung terjadinya penyakit pada tubuh manusia, salah satunya adalah protein permukaan yang membantu kolonisasi pada jaringan inang. Untuk mendukung penyebarannya pada jaringan, bakteri ini menghasilkan invasin, seperti leukosidin, kinase dan hyarulonidase. Leukosidin adalah sitotoksin yang dapat membunuh leukosit, sedangkan hyarulonidase adalah enzim yang dapat mendegradasi asam hyaluronat sehingga meningkatkan permeabilitas jaringan (Todar, 2008).
KontaminasiS.aureus pada makanan dapat menyebabkan keracunan (intoksikasi). Hal ini disebabkan karena bakteri tersebut mampu menghasilkan toksin yang berupa enterotoksin di dalam saluran pencernaan. Enterotoksin dapat diproduksi apabila kondisi lingkungan mendukung untuk pertumbuhan dan perkembangan bakteri tersebut, seperti pH dan suhu (Miliotis dan Bier, 2003).
2.6.2. Escherichia coli
26
dalam famili Enterobactericeae (Fardiaz, 1989).E. coli adalah bakteri berbentuk batang dengan ukuran panjang 2,0–6,0 mikron dan lebar 1,1-1,5 mikron, terdapat dalam bentuk Flagela peritikous, tumbuh pada suhu 10-40 oC dengan suhu optimum 37oC dan pH optimum 7,0-7,5 dengan nilai aktivitas air (Aw) minimum adalah 0,96 (Fardiaz, 1983).
E. coli enteropatogenik merupakan bakteri patogen yang dapat menimbulkan penyakit pada manusia dan hewan melalui dua cara, yaitu dengan cara memproduksi enterotoksi (tidak bersifat invasif atau menembus) dengan gejala diare tanpa demam, dan dengan cara invasif atau penetrasi pada sel-sel mukosa usus disertai gejala infeksi seperti menggigil, demam dan diare (Fardiaz, 1983).
2.6.3.Sacharomyces cerevisiae
Saccharomyces crevisiaetermasuk ke dalam kelasAscomycetes, selnya berbentuk bulat panjang 6-8 µm (Pelzcaret al.,1993).S. cerevisiae merupakan jenis khamir yang memiliki suhu pertumbuhan optimum 33-35 oC, suhu minimum 4-13oC dan suhu pertumbuhan maksimum adalah 38-39oC, sedangkan Aw pertumbuhan 0,89.
III. BAHAN DAN METODE
3.1. Tempat dan Waktu Penelitian
Penelitian ini dilaksanakan di Laboratorium Mikrobiologi Hasil Pertanian dan Laboratorium Analisis Kimia Hasil Pertanian Jurusan Teknologi Hasil Pertanian Fakultas Pertanian Universitas Lampung pada bulan Juli-Oktober tahun 2014.
3.2. Bahan dan Alat
Bahan utama dalam penelitian ini adalah minyak sawit mentah (CPO) dan minyak inti sawit (PKO) PTPN VII Bekri Lampung. Bahan kimia terdiri dari: heksana, etanol, NaOH, HCl 35%, natrium sulfat anhidrat, dietil eter, asam formiat, etil asetat, iodium kristal, dan sejumlah bahan kimia penunjang analisis. Kultur mikroba yang digunakan dalam penelitian ini adalah Escherichia coli, Staphylococcus aureus, dan Sacharomyces cerevisiae. Media yang digunakan adalah NA (Nutrient Agar), NB (Nutrient Broth), PDB (Potato Dextrrose Broth), dan PDA (Potato Dextrose).
Alat-alat yang digunakan pada penelitian ini adalah hotplate-magnetic stirrer, centrifuge, labu pemisah, kertas saring, oven, corong Buchner, plat kromatografi lapis tipis silika gel 60 F254 20x20 cm, chamber, autoklaf, mikropipet, inkubator,
28
3.3. Metode Penelitian
Penelitian ini dilakukan dengan perlakuan tunggal yaitu pemurnian dengan metode kromatografi lapis tipis dengan komposisi eluen heksana/dietil eter/asam formiat (80:20:2) sebanyak 30 ml dan pengujian aktivitas antimikroba sebanyak 3 ulangan. Produk yang diujikan yaitu 10 produk terbaik dari fraksinasi produk etanolisis campuran CPO dan PKO dari penelitian sebelumnya yaitu pelarut etil asetat dengan sentrifus (1000, 1500, 2000, 3000 rpm); pelarut etanol dengan sentrifus (2000, 3000, 3500 rpm); pelarut etanol-etil asetat dengan sentrifus (1500, 2500, 3500 rpm). Data dianalisis dan disajikan secara deskriptif dalam bentuk tabel, grafik dan gambar.
3.4. Pelaksanaan Penelitian
29
3.4.1. Persiapan bahan utama
Bahan utama berupa CPO dan PKO segar yang diperoleh dari Perusahaan Persero (PT) Perkebunan Nusantara VII Unit Usaha Bekri, Lampung Tengah. Selajutnya masing-masing CPO dan PKO disaring menggunakan kertas saring dan ditampung dalam erlenmeyer, dikeringkan menggunakan oven (80oC) seharian hingga kandungan air dalam CPO atau PKO berkurang, lalu diwadahi dalam (jerigen plastik) terpisah dan disimpan ditempat yang sejuk, gelap, dan kering, sebagai stok CPO dan PKO untuk pelaksanaan penelitian (Murhadi dan Zuidar, 2009 dengan modifikasi).
3.4.2. Persiapan pelarut etanol-NaOH 1%
30
3.4.2. Produksi produk etanolisis kasar
Reaksi etanolisis dilakuan mengikuti metode yang telah dilakukan pada penelitan sebelumnya (Murhadi dan Suharyono, 2008 dengan modifikasi). Sejumlah 256 ml etanol 96% yang telah mengandung NaOH 1% (b/b CPO-PKO) ditambahkan 160 g CPO-PKO (nisbah = 0,8; b/b) di dalam Erlenmeyer 1000 ml dengan total volume reaksi etanolisis kurang lebih 420 ml (nisbah = 1,6; v/b), lalu diletakkan diatas hotplate-magnetic stirrer dengan sentrifus 1000 rpm selama 8 menit pada suhu 40oC. Reaksi dihentikan dengan meneteskan sebanyak 42 tetes larutan HCL 35%. Campuran produk reaksi, dimasukan kedalam labu pemisah dan dibiarkan selama 15-30 menit, sehingga telah terlihat jelas pemisahan antar lapisan atas dan lapisan bawah.. Produksi produk etanolisis ini dilakukan sebanyak 1 kali untuk medapatkan produk etanolisis kasar yang cukup untuk penelitian tahap selanjutnya.
3.4.3. Fraksinasi
31
fraksi 2 (semipadat)
Analisis KLT
digunakan untuk pengujiaan pola sebaran komponen gliserida pdengan metode kromatografi lapis tipis. Diagram alir proses fraksinasi dingin produk etanolisis kasar campuran CPO dan PKO disajikan pada Gambar 2.
Gambar 2. Diagram alir fraksinasi dingin produk etanolisis kasar dari campuran CPO dan PKO
Sumber : Ranggaet al.(2005) dengan modifikasi.
3.4.5. Identifikasi komponen gliserida
Identifikasi pola sebaran komponen gliserida diamati menggunakan metode kromatografi lapis tipis (Mappiratu, 1999). Seluruh produk (10) hasil fraksinasi dingin sebanyak ±0,5 µl dalam spotting capiler diaplikasikan pada lempeng kromatografi lapis tipis (KLT) silika gel 60 F254(20x20 cm) dalam batch. Jarak
Penguapan (60oC, hingga berat)
konstan) fraksi 1 (cair)
Sentrifius
(t =3 menit; sentrifus (rpm) Pendinginan
32
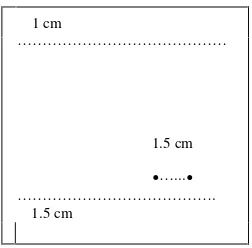
antar spot adalah 2 cm. Jarak batas bawah adalah 1,5 cm dan jarak batas atas 1 cm seperti terlihat pada Gambar 3.
1 cm
………
1.5 cm
.
…....
……….1.5 cm
Gambar 3. Preparasi sampel pada lempeng KLT
Setelah spotting selesai dilakukan, lempeng KLT kemudian dikembangkan atau dielusi menggunakan eluen berupa campuran heksana/dietil eter/asam formiat, 80:20:2 (v/v/v) yang sebelumnya telah dijenuhkan di dalamchamber.Proses elusi berjalan dimulai dari bergeraknya eluen dari bagian bawah lempeng KLT dan dihentikan hingga eluen mencapai garis batas atas lempeng KLT. Waktu yang diperlukan untuk mengelusi ±1,5 jam. Lempeng kemudian dikeluarkan dari dalam chamberdan didiamkan selama beberapa menit sampai uap yang masih tertinggal hilang. Identifikasi komponen terpisah pada lempeng KLT ditampakan dengan zat penampak uap iodium hingga membentuk spot bewarna kuning.
3.5. Pengamatan
3.5.1. Nilai Rf dan pola sebaran komponen terpisah
33
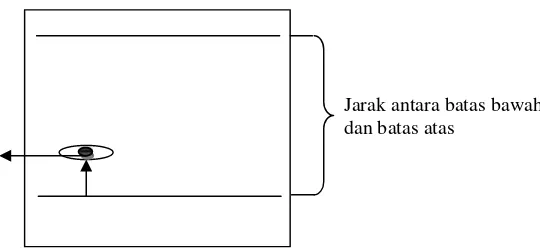
Jarak antara batas bawah dan batas atas
Jarak antara batas bawah dengan titik tengah spot
Gambar 4. Rencana pengamatan spot pada lempeng KLT
Nilai Rf dapat dicari dengan menggunakan rumus sebagai berikut:
=
Keterangan :
Jarak X : Jarak antara garis batas bawah KLT dengan titik tengah spot Jarak total : Jarak antara garis bawah KLT dengan garis batas atas KLT
Selanjutnya identifikasi pola sebaran komponen gliserida ditentukan dari nilai Rf yang kurang lebih mendekati pada penelitian sebelumnya (Murhadi dan Zuidar, 2010). Spot pada lempeng KLT yang memiliki nilai Rftertinggi sampai terendah
berturut-turut adalah TG, ALB, DG, dan MG (Mappiratu, 1999).
3.5.2. Rendemen fraksi massa komponen terpisah
34
masing-masing komponen terpisah (TG, ALB/EE, DG, dan MG) dihitung dengan membagi berat (mg) semua komponen yang terpisah pada KLT, lalu dikali 100%. Fraksi massa setiap spot dihitung berdasarkan persamaan berikut :
(%) = × 100
Keterangan :
Berat X : Berat masing-masing spot produk etanolisis Berat total : Berat keseluruhan spot produk etanolisis
3.5.3. Pengujian aktivitas antimikroba
35
mm. Ke dalam tiap lubang, diinokulasi dengan 60 µL fraksi produk etanolisis kasar dari campuran CPO dan PKO.
Zona penghambatan yang diukur adalah radius (r, mm) penghambatan berupa areal bening di sekitar sumur uji, setelah diinkubasi selama 24 jam dengan suhu 37oC. Pengukuran jari-jari (r, mm) zona hambat di sekeliling sumur uji dilakukan dengan cara mengukur jarak dari tepi sumur uji ke batas lingkaran zona hambat menggunakan jangka sorong (ketelitian 0.01 mm) pada beberapa sisi sumur uji, lalu dirata-ratakan. Selanjutnya dengan asumsi tinggi atau tebal media agar di dalam cawan petri uji adalah sama (9,0 cm) dan volume media agar cair yang ditambahkan sama (20 ml), maka perhitungan diameter zona hambat riil dapat menggunakan konsep dimensi luas lingkaran (dua dimensi). Perhitungannya sebagai berikut (Murhadi, 2010b):
1. Dihitung luas kotor (L1,mm2) lingkaran areal bening akibat daya hambat
bakteri uji disekeliling sumur uji dengan persamaan luas : L1= π. r12, dimana r1= rp+ rs
rp = jarak dari lingkaran luar sumur ke lingkaran terluar
areal bening di sekeliling sumur uji (mm), rs= jari-jari sumur uji (mm),
π = 3,14
2. Dihitung luas kontrol (L2, mm2) areal bening akibat daya hambat pelarut
36
rk = jarak dari lingkaran luar sumur ke lingkaran terluar
areal bening di sekeliling sumur uji (mm) akibat daya hambat/pengencer organik,
rs= jari-jari sumur uji (mm), π = 3,14
3. Dihitung luas bersih (L3,mm2) dengan persamaan : L3= L1- L2
4. Dihitung jari-jari zona hambat riil (rr, mm) dengan persamaan :
rr=√(L3/3,14)
5. Dihitung nilai diameter zona hambat riil (dr, mm) dengan persamaan :
dr= 2. rr
6. Akhirnya dapat dihitung nilai diameter zona hambat hasil konversi (dc,
V. SIMPULAN DAN SARAN
5.1. Simpulan
Berdasarkan penelitian yang telah dilakukan dapat disimpulkan bahwa:
1. Pemurnian produk fraksinasi dingin campuran CPO dan PKO menggunakan metode kromatografi lapis tipis menghasilkan 5 fraksi komponen terpisah yang ditentukan berdasarkan nilai Rf yaitu monogliserida (MG), digliserida (DG), etil ester/senyawa biodiesel (EE), asam lemak bebas (ALB), dan trigliserida (TG).
2. Rendemen rata-rata fraksi komponen MG, DG, EE, ALB, TG sisa dan komposisi MG-DG hasil penelitian ini secara berurutan sebesar 24,75%, 24,89%, 12,45%, 24,63%, 13,27%, dan 49,65%.
3. Komposisi MG-DG tertinggi pada produk fraksinasi dingin E1C5 (52,54%) dengan TG sisa (12,48%).
4. MG dan DG dari campuran CPO dan PKO memiliki sifat antibakteri yang relatif kuat dalam penelitian ini.
5.2. Saran
52
DAFTAR PUSTAKA
Ahmad, R. Zainuddin. 2006. Pemanfaatan Khamir Saccharomyces cerevisiae Untuk Ternak. Balai Penelitian Veteriner. Bogor 16114.
Anonim. 2009. Lampung Dalam Angka 2009. BPS Provinsi Lampung. CV. Mulya Abadi. Bandar Lampung.
Anonim. 2010. Produk turunan CPO. https://umyiffahcollection.wordpress.com
/2014/10/30/kelapa-sawit-sebagai-salah-satu-komoditi-ekspor-indonesia-dan-hasil pengolahannya diakses pada tanggal 15 Oktober 2014.
Anonim. 2011. Pusat Informasi BUMN Perkebunan (PUSINFO). Kualitas CPO pada PTPN XIII. http://www.lpp.ac.id/ptpn.php?id=247. Diakses pada tanggal 15 Oktober 2014
Branden, A. L. and P. M. Davidson. 1983. Antimicrobials in Foods. Marcel Dekker, Inc. New york.
Breeding, C.J. and R.T Marshall. 1995. Crystallization of Butter Oil and Separation by Filter Centrifugation. JAOCS. 72(4):449-553.
Buckle, K. A., R. A. Edwards, G.H. Fleet, and M. Wootton. 1987. Ilmu Pangan. Diterjemahkan oleh Purnomo dan Aldino. UI-Press. Jakarta, 365 hlm.
Choo, Y. M., S. C. Yap, A. S. H. Ong, C. K. Ooi and S. H. Gog. 1989. Palm Oil Carotenoid: Chemistry and Technology. Proc. Of Int. Palm Oil Conf. PORIM, Kuala Lumpur.
Davis W. W. dan T. R. Stout. 1971. Disc Plate Method Of Microbilogical Antibiotic Assay:I.Factors Influencing Variability An Error I.Aook Microbiol:22(4) : 659-665.
Fardiaz, S. 1983. Keamanan Pangan. Jilid I: Bakteriologi. Jurusan Ilmu dan Teknologi Pangan. Institut Pertanian Bogor. Bogor. 110 hlm.
54
Fardiaz. 1998. Panduan Pengolahan Pangan Yang Baik Bagi Industri RumahTangga. Badan Pengawas Obat dan Makanan Deput Bidang PengawasKeamanan Pangan dan Bahan Berbahaya. Jakarta.
Gritter, R. J., J. M. Bobbit, A. E. Scwharting. 1991. Pengantar Kromatografi (terjemahan Kosasih Padmawinata), edisi 2, penerbit ITB, Bandung, 107 hlm.
Gunstone, F. D., J. L. Harwood and F. B. Padley. 1994.The Lipid Handbook. Chapman and Hall. London.
Gunstone, F. D dan F. B Padley. 1997. Lipids Technologies and Applications. Marcel Dekker Inc., New York.
Hamilton, R. I. 1995.Development in Oil and Fats. Chapman and Hall, New York.
Hasanuddin, A., Mappiratu, dan G. S. Hutomo. 2003.Pola Perubahan Mono dan Diasilgliserol dalam Reaksi Etanolisis Minyak Sawit Mentah. Jurnal Teknologi dan Industri Pangan. XIV(3):241-246.
Herlianti, N. 2010. Pra Rancangan Pabrik Pembuatan Asam Oleat dari CPO dengan Kapasitas 1000 Ton/Hari.Jurnal Jurusan Teknik Kimia.Univesitas Sumatera Utara.
Hostettmann, K., Marston A., dan Wolfender J. L. 1995. Strategy in The Search For New Biologically Active Plant Constitutents, in: Hostettmann K, Marston A, Maillard M, Hamburger M, eds, Phytochemistry of Plants Used in Traditional Medicine, Proceedings of the Phytochemical Society of Europe. Oxford, Oxford Science Publications, pp. 18–45. Khasbullah, F. 2010. Pola Sebaran dan Rendemen Produk Gliserolisis PKO. Teknologi Hasil
Pertanian.Universitas Lampung. Bandar Lampung. 40 hlm.
Ketaren, S. 1986. Pengantar Teknologi Minyak dan Lemak Pangan. Cetakan Pertama. Jakarta: UI-Press.
Ketaren, S. 2005. Minyak dan Lemak Pangan. Jakarta. UI-Press.
Lestari, M. dan Murhadi. 2008.Pengaruh Nisbah Etanol-PKO dan Waktu Reaksi terhadap Rendemen dan Aktivitas Produk Etanolisis Minyak Inti Sawit.
Liang, T. 2009. Seluk Beluk Kelapa Sawit-Bab VIII. Produk dan Standarisasi. PT. Harapan Sawit Lestari, Kab. Ketapang. Kalimantan Barat. 15 hlm.
Kabara, J.J. 1984.Antimicrobial agents derved from fatty acids. J. Am. Oil. Chem. Soc. 61:397-403.
55
Mappiratu. 1999. Penggunaan Biokatalis Dedak Padi dalam Biosintesis Antimikroba Monoasilgliserol dari Minyak Kelapa. Disertasi S3. PPs IPB. Bogor.
Maulidha, N. 2014. Kajian Fraksinasi Dingin Terhadap Aktivitas Antimikroba dan Daya Emulsi Fraksi Produk Etanolisis dari Campuran CPO dan PKO. (Skripsi). Teknologi Hasil Pertanian. Universitas Lampung. Bandar Lampung.
Monday, S. R. and R. W. Bennet. 2003. Staphylococcus aureus. Di dalam: Miliotis M.D.dan J.W. Bier. International Handbook of Foodborne Pathogenes. Marcel Dekker,New York. Moran, D. P. J. dan K. K. Rajah. 1994. Fats in Food Products. Blackie Academic and
Professional, Glasgow.
Murhadi. 2005. Kimia. Diktat Ajar Kimia Hasil Pertanian. Fakultas Pertanian. Jurusan Teknologi Hasil Pertanian. Universitas Lampung. Bandar Lampung. 244 hlm.
Murhadi dan AS. Suharyono. 2008. Kajian Aktivitas Antibakteri Produk Etanolisis dari Campuran Minyak Inti Sawit (Elaeis guineensis Jacq.) dan Minyak Biji Mengkudu (Morinda citrifolia L.). Jurnal Teknologi dan Industri Hasil Pertanian. Universitas Lampung. Bandar Lampung. Hlm 47-58.
Murhadi dan A. S. Zuidar. 2009.Penganekaragaman Bahan Tambahan Pangan (BTP) Berbasis Minyak Inti Sawit. Laporan Akhir HB Tahun Pertama. Lembaga Penelitian UNILA. Bandar Lampung.
Murhadi. 2010a. The Emulsion Stability of Coconut (Cocos nucifera L.) Milk Added with Ethanolysis Product from Palm Kernel Oil (Elaeis guineensis Jacq). International Seminar on Horticulture to Support Food Security. Bandar Lampung. Pages B-223-B-229.
Murhadi. 2010b. Antimikroba dari Tanaman; Golongan Senyawa, Sumber dan Aktivitasnya. Lembaga Penelitian. Universitas Lampung.
Murhadi dan A. S. Zuidar. 2010. Nilai Rf dan Rendemen Massa Fraksi-fraksi Komponen Antibakteri Produk Etanolisis Kasar dari Palm Kernel Oil (PKO). Jurusan Teknologi Hasil Pertanian Fakultas Pertanian.Universitas Lampung.
Naibaho, P.M. 1988. Pemisahan Karotena (Provitamin A) Minyak Sawit dengan Metode Adsorpsi. Disertasi S3, FPS. Institut Pertanian Bogor. Bogor
Nikolova, Boryana dan Damyanova. 2002. Lipids Analysis by Thin Layer Chromatography. Encyclopedia of Chromatography.
56
Pelzcar, M. J. and R. D. Reid. 1979. Food of Microbiology. Tata McGraw Hill Book Co.Inc, Kogunha Co. Ltd, Tokyo.
Pelzcar, M. J. and E. C. S. Chan. 1986.Microbiology. Mc.Graw-Hill Book Co New York.
Rangga, A., Murhadi, F. Nuraeni, dan Pitutur. 2005. Produksi dan Kajian Aktivitas Antibakteri Produk Gliserolisis dari Minyak Inti Sawit (PKO). Makalah Seminar Nasional Research and Studies TPSDP Dikti Depdiknas. Mei 2005. Yogyakarta.
Robinson, B. W., D. S. Wilson, A. S. Margosian. 2000. A Plurastic Analysis of Character Release In Pumpkinseed Sunfish (Lepomis Gibbosus). Ecology 81: 2799-2812.
Sastrohamidjojo, H. 1985. Kromatografi. Edisi I. Cetakan I. Yogyakarta: Liberty. Stahl, E. 1985. Analisis obat secara Kromatografi dan Mikroskop, ITB, Bandung.
Todar, K. 2008.Staphylococcus aureusdanStaphylococcal Disease.USA: Winconsin, Madison. Available from http://textbookofbacteriology.net/staph.html.
Vincent, G. 1987. Farmakologi dan Terapi. Edisi ke-3. Bagian Farmakologi Fakultas Kedokteran UI. Jakarta.
Winarno, F.G. 1997. Kimia Pangan dan Gizi. Gramedia. Jakarta.