Lampiran 2. Gambar tumbuhan dan simplisia daun beluntas (Pluchea indica (L.) Less.)
Tumbuhan beluntas
Lampiran 3. Gambar mikroskopik serbuk simplisia daun beluntas (Pluchea indica (L.) Less.
Keterangan : 1. Stomata tipe anomositik
2. Pembuluh kayu berpenebalan spiral 3. Rambut penutup
1 2
Lampiran 4. Bagan Penelitian
1. Pembuatan serbuk simplisia, karakterisasi simplisia dan skrining fitokimia
Lampiran 4. (Lanjutan)
2. Pembuatan ekstark etanol , fraksi n-heksana, fraksi etilasetat dan fraksi air daun beluntas (Pluchea indica (L.) Less.)
Dimaserasi dengan etanol 96 %
Diuapkan dengan rotary evaporator Dikeringkan dengan freeze dryer
Ditimbang 30 g untuk fraksinasi Dilarutkan dengan aquadest Difraksinasi dengan n-heksana
Dipekatkan
Dipekatkan Difraksinasi dengan etilasetat
Dipekatkan
Dipekatkan Serbuk simplisia 400 g
Maserat
Ekstrak etanol kental 50,51 g
Uji aktivitas antibakteri
Fraksi n-heksana Fraksi air
Fraksi n-heksana kental 6,80 g
Fraksi etilasetat
Fraksi air (sisa) Fraksi etilasetat kental 6,28 g
Uji aktivitas antibakteri
Fraksi air kental 8,25 g
Lampiran 4. (Lanjutan)
3. Pengujian aktivitas antibakteri
Diambil dengan jarum ose steril Ditanam pada media NA miring
Diinkubasi pada suhu 35 + 2oC selama 18-24 jam
Diambil 1 ose
Disuspensikan ke dalam 10 ml nutrient broth Diukur kekeruhan suspense bakteri menggunakan spektrofotometer pada panjang gelombang 580 nm sampai diperoleh nilai transmitan 25-27%
Dimasukkan 0,1 ml inokulum ke dalam cawan petri Dituang 20 ml media NA steril ke dalam cawan petri Dihomogenkan dan dibiarkan hingga memadat
Diletakkan beberapa pencadang kertas yang telah direndam dalam ekstrak dengan berbagai konsentrasi Diinkubasi pada suhu 35 + 2oC selama 18-24 jam Diukur diameter hambat di sekitar pencadang kertas Biakan murni bakteri
Stok kultur bakteri
Inokulum bakteri
Media padat
Lampiran 5. Perhitungan hasil penetapan kadar
a. Perhitungan penetapan kadar air
Lampiran 5. (Lanjutan)
b. Perhitungan penetapan kadar sari yang larut dalam air
Kadar sari larut dalam air = Berat sari 100 Berat simplisia 20
1. Kadar sari larut dalam air I
Berat sampel = 5,009 g
Berat sari = 0,214 g
Kadar sari larut dalam air = 0,214100 5,009 20
= 21,361 % 2. Kadar sari larut dalam air II
Berat sampel = 5,007 g
Berat sari = 0,193 g
Kadar sari larut dalam air = 0,193100 5,007 20
= 19,273 % 3. Kadar sari larut dalam air III
Berat sampel = 5,042 g
Berat sari = 0,214 g
Kadar sari larut dalam air = 0,214100 5,042 20
= 21,221 %
Lampiran 5. (Lanjutan)
c. Perhitungan penetapan kadar sari yang larut dalam etanol
1. Kadar sari larut dalam etanol I
Berat Cawan = 49,700 g
Berat Sampel = 5,015 g
Berat sari = 0,176 g
Kadar sari larut dalam etanol = 0,176100 5,015 20 = ,, x x 100%
= 17,547 % 2. Kadar sari larut dalam etanol II
Berat Sampel = 5,069 g
Berat sari = 0,143 g
Kadar sari larut dalam etanol = 0,143100 5,069 20
= 14,105 % 3. Kadar sari larut dalam etanol III
Berat Sampel = 5,009 g
Berat sari = 0,173 g
Kadar sari larut dalam etanol = 0,173100 5,009 20 = 17,268 %
Lampiran 5. (Lanjutan)
d. Perhitungan penetapan kadar abu total
1. Sampel I
Kadar abu total rata-rata = 6,389%+6,8879%+7,028% 3
= 6,7459 % Kadar abu total= Berat abu total
Berat simplisia
Lampiran 5. (Lanjutan)
e. Perhitungan Penetapan Kadar Abu Tidak Larut Dalam Asam
1. Sampel I
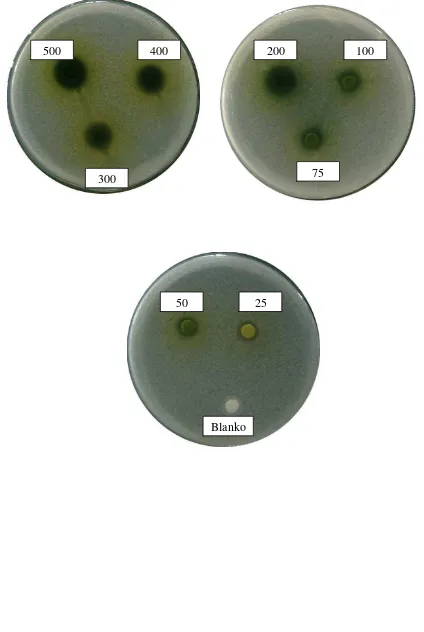
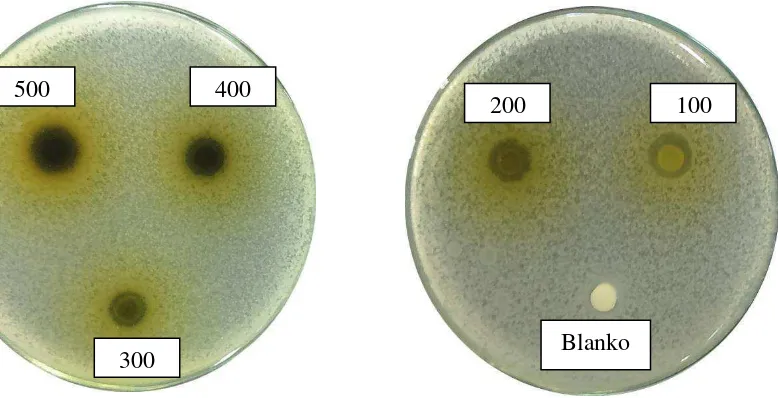
Lampiran 6. Gambar hasil uji aktivitas antibakteri ekstrak etanol daun beluntas terhadap bakteri Eschericia coli
500 400
300
200 100
75
50 25
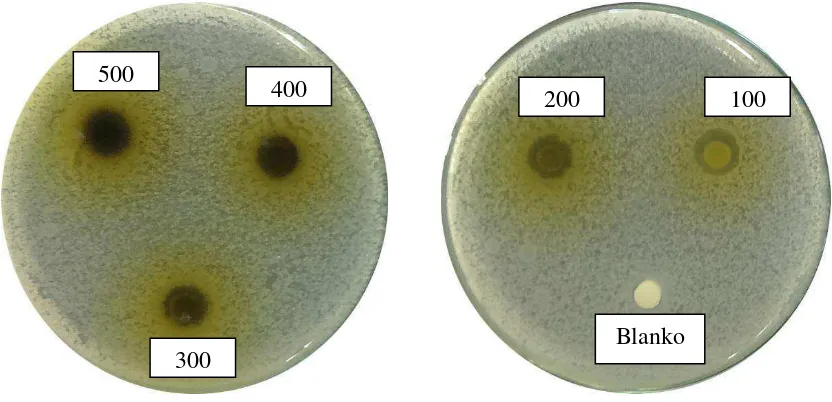
Lampiran 7. Gambar hasil uji aktivitas antibakteri ekstrak etanol daun beluntas terhadap bakteri Bacillus subtilis
500 400
300
200
100
75
50 25
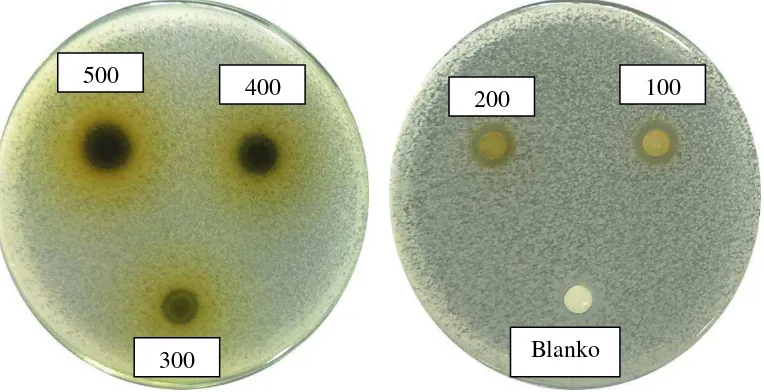
Lampiran 8. Gambar hasil uji aktivitas antibakteri fraksi etilasetat daun beluntas terhadap bakteri Eschericia coli
500
400
300
200 100
75
50
25
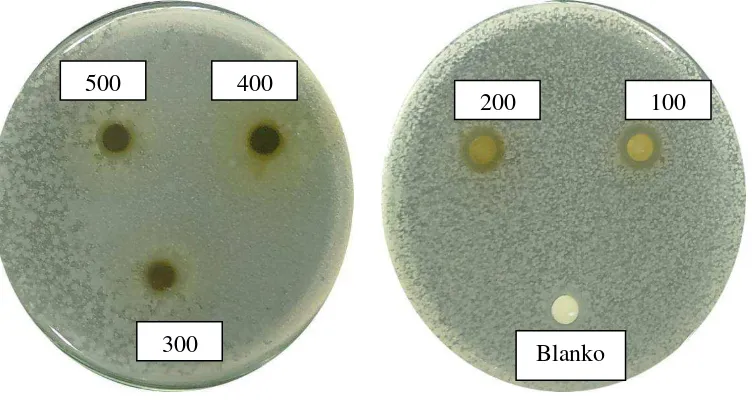
Lampiran 9. Gambar hasil uji aktivitas antibakteri fraksi etilasetat daun beluntas terhadap bakteri Bacillus subtilis
500
400
300
200 100
75
50
25
Lampiran 10. iGambar hasil uji aktivitas antibakteri fraksi n-heksana daun beluntas terhadap bakteri Eschericia coli
500
400
300
200 100
Lampiran 11. iGambar hasil uji aktivitas antibakteri fraksi n-heksana daun beluntas terhadap bakteri Bacillus subtilis
500 400
300
200 100
Lampiran 12.iGambar hasil uji aktivitas antibakteri fraksi air daun beluntas terhadap bakteri Eschericia coli
400
300
200 100
Lampiran 13.iGambar hasil uji aktivitas antibakteri fraksi air daun beluntas terhadap bakteri Bacillus subtilis
500 400
300
200 100
Lampiran 14. Hasil Uji Aktivitas Antibakteri Ekstrak Etanol DaunBeluntas dan Fraksinya Terhadap Bakteri Escherichia coli Kons.
mg/ml
Diameter Daerah Hambatan (mm)
Ekstrak etanol Fraksi n- heksana Fraksi etilasetat Fraksi air
D1 D2 D3 D* D1 D2 D3 D* D1 D2 D3 D* D1 D2 D3 D*
500 16 16 16,05 16 10,25 12 11,10 11,11 17,75 18 19,50 18,41 12 12,10 12,20 12,10
400 14,05 14,75 14,35 14,38 10 10,25 9,30 9,85 17,10 17,75 17,80 17,55 11,50 11 10,75 11,08
300 13,95 12,95 13,25 13,38 9 8,75 8,90 8,88 17,10 17,50 17,20 17,26 10 9,75 9,75 9,83
200 12 12,35 12,75 12,36 8,75 8 8,50 8,41 17,50 17 17 17,16 9 9 8,75 8,92
100 11,70 11 10,55 11,08 8,40 8,30 8 8,23 15,25 15 16 15,42 8,25 8 7,75 8
75 10 9,50 10 9,83 - - - - 12,30 12 12,50 12,27 - - - -
50 8,75 9 8 8,58 - - - - 11,50 11 10,25 10,92 - - - -
25 8 8 8 8 - - - - 8 9,50 9 8,83 - - - -
Blanko - - - -
Lampiran 15. Hasil Uji Aktivitas Antibakteri Ekstrak Etanol Daun Beluntas dan Fraksinya Terhadap Bakteri Bacillus subtilis Kons.
mg/ml
Diameter Daerah Hambatan (mm)
Ekstrak etanol Fraksi n- heksana Fraksi etilasetat Fraksi air
D1 D2 D3 D* D1 D2 D3 D* D1 D2 D3 D* D1 D2 D3 D*
500 17,70 17,10 17,15 17,31 11 10,50 10,20 10,56 18,10 18 18 18,03 9,10 8,75 8,75 8,87
400 14,05 14,75 14,35 15,05 10,10 10,20 9,10 9,80 17,50 17,50 17,75 17,50 8,50 7,50 7,50 7,83
300 13,95 12,95 13,25 14,47 9,5 9,75 9,70 9,55 17 17,75 17,25 17,33 7,25 7,50 7,50 7,41
200 12 12,35 12,75 12,76 9 9,30 9,50 9,26 16,20 16 17 16,40 7,10 7,25 7,25 7,38
100 11,70 11 10,55 10,43 8 8,20 8,30 8,16 14,10 14,20 14 14,10 7 7,05 7,05 7,03
75 10 9,50 10 9,13 - - - - 11,30 12,50 11,25 11,68 - - - -
50 8,75 9 8 8,5 - - - - 10 9,50 11,25 10,25 - - - -
25 8 8 8 8 - - - - 8,65 9 9 8,88 - - - -
Blanko - - - -
DAFTAR PUSTAKA
Ardiansyah. 2005. Daun Beluntas Sebagai Bahan Antibakteri dan Antioksidan.http://www.beritaiptek.com. [17 November 2015]
Basset, J., Denney, R.C., Jeffrey, G. H., dan Mendham, J. (1994). Buku Ajar Vogel: Kimia Analisis Kuantitatif Anorganik. Edisi 4. Jakarta: EGC. Halaman 165.
Cowan, M. (1999). Plant Product as Antimicrobial Agent. Clinical Microbiology Reviews, 12(4): 564-582.
Dalimartha, S. (1999). Atlas Tumbuhan Obat Indonesia. Jilid I. Jakarta: Permata Bunda. Halaman 19.
Depkes RI. (1979). Materia Medika Indonesia. Jilid III. Jakarta: Departemen Kesehatan RI. Halaman 321-326.
Depkes RI. (1995). Materia Medika Indonesia. Jilid VI. Jakarta:Departemen Kesehatan RI. Halaman 321-326.
Depkes RI. (2000). Parameter Standar Umum Ekstrak Tumbuhan Obat. Jakarta: Departemen Kesehatan RI. Halaman. 1, 10-11.
Dirjen POM. (1979). Farmakope Indonesia. Edisi III. Jakarta: Departemen
Dwidjoseputro, D. (1987). Dasar-Dasar Mikrobiologi. Jakarta: Djambatan. Halaman 104-106.
Fardiaz, S. (1992). Mikrobiologi Pangan I. Jakarta: Penerbit PT. Gramedia Pustaka Utama. Halaman 143
Ferawaty, A.S., Agus, S.,dan Delianis, P. (2012). Potensi Antibakteri Rumput Laut Terhadap Bakteri Penyakit Kulit Pseudomonas aeruginosa, Staphylococcus epidermidis dan Micrococcus luteus. Jornal of Marine Research. 1(2): 152-160.
FKUI. (1993). Mikrobiologi Kedokteran. Bogor: Penerbit Binrupa Aksara. Halaman 125.
Ganiswara, S. (1995). Farmakologi dan Terapi. Edisi 4. Jakarta: Penerbit Universitas Indonesia. Halaman 571-573
Handa, S., Suman, P.S.K., Gennaro, L., dan Dev, D.R.. (2008). Extraction Technologies For Medicinal And Aromatic Plants. Italy: International Centre For Science and High Technology. Halaman: 22.
Harborne, J.B. (1984). Metode Fitokimia, Penuntun Cara Modern Menganalisa Tumbuhan.Terjemahan K. Padmawinata. Edisi II. Bandung: ITB Press. Halaman: 76.
Irianto, K. (2006). Mikrobiologi Menguak Dunia Mikroorganisme. Jilid Satu. Bandung: Penerbit Yrama Widya. Halaman 35, 75-78, 159-161,170-172. Jawetz, E. (2001). Mikrobiologi Kedokteran. Penerjemah: Eddy Mudihardi,
Kuntaman dan Lindawati Alimsardjono. Jakarta: Penerbit Salemba Medika. Halaman 317-318, 352-360.
Madigan, M. (2005). Brock Biology of Microorganisms (11th ed).San Francisco:
Prentice Hall
Manu, R.R.S. (2013). Aktivitas Antibakteri Ekstrak Etanol Daun Beluntas (Pluchea indicaL.) Terhadap Staphylococcus aureus, Bacillus subtilis dan Pseudomonas aeruginosa.Jurnal Ilmiah Mahasiswa Universitas Surabaya. 2 (1): 8.
Oxoid. (1982). The Oxoid Manual of Culture Media, Ingredients and Other Laboratory Services. Fifth Edition. Hampsshire: Oxoid Limited. Halaman 223, 224.
Pratiwi, S.T. (2008). Mikrobiologi Farmasi. Jakarta: Penerbit Erlangga. Halaman 6,22-24, 105-117, 154-160.
Pujowati, P. (2006). “Pengenalan Ragam Tanaman Lanskap Asteraceae (Compositae)”. Tesis. Bogor: Departemen ArsitekturLanskap Fakultas Pertanian ITB.
Robinson, T. (1995). Kandungan Organik Tumbuhan Tinggi. Edisi VI. Diterjemahkan oleh Kosasih Padmawinata. Bandung: Penerbit ITB. Halaman 154.
Rohman, A. (2007). Kimia Farmasi Analisis. Yogyakarta: Pustaka Pelajar. Halaman 46-47.
Sirait, M. (2007). Penuntun Fitokimia Dalam Farmasi. Bandung: Penerbit ITB. Halaman 129-130.
Suryanto, D., dan Erman, M. (2006). Mikrobiologi. Medan: Departemen Biologi FMIPA Universitas Sumatera Utara. Halaman 10-11
BAB III
METODOLOGI PENELITIAN
Penelitian ini menggunakan metode eksperimental dengan tahapan penelitian yaitu pengambilan bahan tumbuhan, identifikasi, pembuatan simplisia, pemeriksaan mikroskopik, skrining fitokimia, pembuatan ekstrak dan pembuatan fraksi. Pengujian aktivitas antibakteri denganmetode difusi menggunakan kertas cakram (Uji Kirby-Bauer). Parameter yang diamati yaitu besarnya diameter daerah hambat pertumbuhan bakteri. Analisa data diolah menggunakan analisa data SPSS. Penelitian dilakukan di Laboratorium Farmakognosi dan Laboratorium Mikrobiologi Fakultas Farmasi Universitas Sumatera Utara.
3.1. Alat-alat
Alat-alat yang digunakan dalam penelitian ini adalah alat-alat gelas, autoklaf (Fisons), blender (Panasonic), desikator, hot plate (Fisons),inkubator (Fiber Scientific), jarum ose, jangka sorong, kamera digital (Sony), krus porcelin, lemari pendingin (Glacio), mikroskop (Olympus),mikro pipet (Eppendorf), neraca listrik (Mettler Tolledo),neraca kasar, oven (Memmert),penangas air, pinset, rotary evaporator (Haake D), seperangkat alat penetapan kadar air,statif dan klem, spatula, spekrofotometer visibel (Dynamica) dan tanur (Nabertherm).
3.2. Bahan-bahan
25922, nutrient agar (NA), nutrient broth (NB) dan simplisia daun beluntas. Bahan kimia yang digunakan berkualitas pro analisis, kecuali dinyatakan lain, yaitu air suling, alfa naftol, amil alkohol, asam klorida pekat, asam asetat anhidrida, asam nitrat, asam sulfat pekat, besi (III) klorida, benzen, bismuth (III) nitrat, dimetilsulfoksida (DMSO), etanol, eter, etilasetat, iodium, isopropanol, kalium klorida, kloroform, n-heksana, natrium sulfat anhidrida, raksa (II) klorida, serbuk magnesium, serbuk zinkum, timbal (II) asetat dan toluena.
3.3. Persiapan Bahan
3.3.1. Pengambilan bahan tumbuhan
Pengambilan sampel dilakukan secara purposif yaitu tanpa membandingkan dengan tumbuhan yang sama dari daerah lain. Bahan tumbuhan yang digunakan adalah daun beluntasyang berwarna hijau dan masih segar, yang diperoleh dariDesa Labuhan Deli, Kecamatan Medan Marelan, Kota Madya Medan, Provinsi Sumatera Utara.
3.3.2. Identifikasi tumbuhan
Identifikasi tumbuhan dilakukan di Herbarium Bogoriense, Bidang Botani Pusat Penelitian dan Pengembangan Biologi (LIPI), Bogor.
3.3.3. Pembuatan simplisia
menjadi serbuk dan disimpan dalam wadah plastik yang tertutup rapat (Depkes, RI., 1979).
3.4. Pembuatan Pereaksi 3.4.1. Pereaksi Bouchardat
Sebanyak 4 g kalium iodida P dilarutkan dalam air suling secukupnya kemudian ditambahkan 2 g iodida sedikit demi sedikit, cukupkan dengan air suling sampai 100 ml (Depkes, RI., 1979).
3.4.2. Pereaksi Dragendorff
Larutan bismut (III) nitrat P 40% b/v dalam asam nitrat P sebanyak 20 ml kemudian dicampurkan dengan 50 ml larutan kalium iodida, didiamkan sampai memisah sempurna. Larutan jernih diambil dan diencerkan dengan air suling secukupnya hingga 100 ml (Depkes, RI., 1979).
3.4.3.Pereaksi Mayer
Larutan raksa (II) klorida P 2,266% b/v sebanyak 60 ml dicampur dengan 10 ml larutan kalium iodida P 50% b/v. Kedua larutan dicampurkan dan ditambahkan air suling hingga diperoleh larutan 100 ml (Depkes, RI., 1979). 3.4.4.Pereaksi besi (III) klorida 1%
Sebanyak 1 g besi (III) klorida dilarutkan dalam air suling sampai 100 ml (Depkes, RI., 1979).
3.4.5.Perekasi Molisch
Sebanyak 3 g α-naftol dilarutkan dalam asam nitrat 0,5 N hingga 100 ml (Depkes, RI., 1979).
3.4.6.Pereaksi timbal (II) asetat 0,4 M
3.4.7.Pereaksi asam klorida 2 N
Sebanyak 17 ml asam klorida pekat diencerkan dengan air suling sampai 100 ml (Depkes, RI., 1979).
3.4.8.Pereaksi natrium hidroksida 2 N
Sebanyak 8,002 g pellet natrium hidroksida ditimbang, kemudian dilarutkan dalam air suling hingga 100 ml (Depkes, RI., 1979).
3.4.9.Pereaksi asam sulfat 2 N
Larutan asam sulfat pekat sebanyak 9,8 ml ditambahkan air suling sampai 100 ml (Depkes, RI., 1979).
3.4.10.Pereaksi Liebermann-Burchard
Campur secara perlahan 5 ml asam asetat anhidrida dengan 5 ml asam sulfat pekat tambahkan etanol hingga 50 ml (Harborne, 1984).
3.4.11.Larutan kloralhidrat
Sebanyak 50 g kloralhidrat ditimbang lalu dilarutkan dalam 20 ml air suling (Dirjen, POM., 1979).
3.5. Pemeriksaan Karakteristik Simplisia
Pemeriksaan karakteristik simplisia meliputi pemeriksaan makroskopik, mikroskopik, penetapan kadar air, penetapan kadar sari larut dalam air, penetapan kadar sari larut dalam etanol, penetapan kadar abu total, penetapan kadar abu yang tidak larut dalam asam.
3.5.1. Pemeriksaan makroskopik
3.5.2. Pemerikasaan mikroskopik
Pemeriksaan mikroskopik dilakukan terhadap serbuk simplisia. Serbuk simplisia ditaburkan diatas objek glass yang telah ditetesi larutan kloralhidrat dan ditutup dengan kaca penutup dan diamati di bawahmikroskop (WHO., 1998). 3.5.3.Penetapan kadar air
Penetapan kadar air dilakukan dengan metode Azeotropi (destilasi toluen). Alat terdiri dari labu alas bulat 500 ml, alat penampung, pendingin, tabung penyambung dan tabung penerima. Cara penetapannya, yaitu:
Pada labu bulat dimasukkan 200 ml toluena dan 2 ml air suling, didestilasi selama 2 jam. Destilasi dihentikan dan dibiarkan dingin selama 30 menit, kemudian volume air di dalam tabung penerima dibaca dengan ketelitian 0,05 ml. Labu yang berisi toluen jenuh tersebut dimasukkan 5 g serbuk simplisia yang telah ditimbang saksama, lalu dipanaskan hati-hati selama 15 menit, setelah toluen mulai mendidih, kecepatan tetesan diatur lebih kurang 2 tetes per detik hingga sebagian air tersuling. Kecepatan dinaikkan hingga 4 tetes per detik, kemudian setelah semua air tersuling, bagian dalam pendingin dibilas dengan toluena. Destilasi dilanjutkan selama 5 menit, kemudian tabung penerima dibiarkan mendingin sampai suhu kamar, setelah air dan toluen memisah sempurna, volume air dibaca dengan ketelitian 0,05 ml. Selisih kedua volume air yang dibaca sesuai dengan kandungan air yang terdapat dalam bahan yang diperiksa. Kadar air dihitung dalam persen (WHO., 1998).
3.5.4.Penetapan kadar sari larut dalam air
sambil sesekali dikocok selama 6 jam pertama, dibiarkan selama 18 jam, kemudian disaring. Diuapkan 20 ml filtrat sampai kering dalam cawan penguap yang berdasar rata yang telah dipanaskan dan ditara. Sisa dipanaskan pada suhu 105oC sampai bobot tetap. Kadar dalam air dihitung terhadap bahan yang telah dikeringkan diudara (Depkes, RI., 1979).
3.5.5.Penetapan kadar sari larut dalam etanol
Sebanyak 5 g serbuk simplisia, dimaserasi selam 24 jam dalam etanol 96% dalam labu bersumbat sambil sesekali dikocok selama 6 jam pertama, dibiarkan selama 18 jam, kemudian disaring. Diuapkan 20 ml filtrat sampai kering dalam cawan penguap yang berdasar rata yang telah dipanaskan dan ditara. Sisa dipanaskan pada suhu 105oC sampai bobot tetap. Kadar sari larut dalam etanol dihitung terhadap bahan yang telah dikeringkan (Depkes, RI., 1979).
3.5.6.Penetapan kadar abu total
Sebanyak 2 g serbuk simplisia yang telah digerus dan ditimbang seksama dimasukkan dalam krus porcelin yang telah dipijar dan ditara, kemudian diratakan. Krus dipijar perlahan-lahan sampai arang habis, pemijaran dilakukan pada suhu 600oC selama 3 jam. Didinginkan dan ditimbang sampai diperoleh bobot tetap. Kadar abu dihitung terhadap bahan yang telah dikeringkan di udara (Depkes, RI., 1979).
3.5.7.Penetapan abu tidak larut dalam asam
3.6. Skrining Fitokimia
Skrining fitokimia simplisia, ekstrak dan fraksi-fraksi meliputi pemeriksaan senyawa golongan alkaloida, glikosida, steroid/triterpenoida, flavonoid, saponin, tanin dan antrakinon.
3.6.1. Pemeriksaan alkaloida
Serbuk simplisia ditimbang sebanyak 0,5 g kemudian dimasukkan ke dalam tabung reaksi lalu ditambahkan 1 ml asam klorida 2 N dan 9 ml air suling, dipanaskan di atas penangas air selama 2 menit, didinginkan lalu disaring (Depkes, RI., 1979). Filtrat dipakai untuk percobaan berikut:
a. Filtrat sebanyak 3 tetes ditambahkan 2 tetes larutan Mayer akan terbentuk endapan bewarna putih atau kuning
b. Filtrat sebanyak 3 tetes ditambahkan 2 tetes larutan Bouchardat akan terbentuk endapan bewarna coklat hitam
c. Filtrat sebanyak 3 tetes ditambahkan 2 tetes larutan Dragendorff akan terbentuk endapan bewarna merah atau jingga.
Alkaloid dinyatakan positif jika terjadi endapan atau paling sedikit dua atau tiga dari percobaan diatas. Hal yang sama dilakukan juga untuk ekstrak etanol dan fraksinya.
3.6.2. Pemeriksaan flavonoida
3.6.3. Pemeriksaan glikosida
Serbuk simplisia ditimbang sebanyak 3 g kemudian disari dengan 30 ml campuran 7 bagian volume etanol 96% dan 3 bagian volume air suling, selanjutnya ditambahkan 10 ml HCl 2 N, direfluks selama 10 menit, didinginkan dan disaring. Pada 30 ml filtrat ditambahkan 25 ml air suling dan 25 ml timbal (II) asetat 0,4 M, dikocok, didiamkan selama 5 menit lalu disaring. Filtrat disari sebanyak 3 kali, tiap dengan 20 ml campuran 3 bagian volume kloroform dan 2 bagian isopropanol. Diambil lapisan air kemudian ditambahkan 2 ml air dan 5 tetes pereaksi Molisch, ditambahkan hati-hati 2 ml asam sulfat pekat terbentuk cincin ungu pada batas kedua cairan menunjukkan adanya gula. Hal yang sama dilakukan juga untuk ekstrak etanol dan fraksinya (Depkes, RI., 1979).
3.6.4. Pemeriksaan tanin
Sebanyak 0,5 g serbuk simplisia disari dengan 10 ml air suling, disaring lalu filtratnya diencerkan dengan air suling sampai tidak berwarna. Diambil 2 ml larutan lalu ditambahkan 1 sampai 2 tetes pereaksi besi (III) klorida 1 %. Terjadi warna biru atau hijau kehitaman menunjukkan adanya tanin. Hal yang sama dilakukan juga untuk ekstrak etanol dan fraksinya(Depkes, RI., 1979).
3.6.5.Pemeriksaan saponin
3.6.6.Pemeriksaan steroid/triterpenoida
Sebanyak 1 g serbuk simplisia dimaserasi dengan 20 ml n-heksan selama 2 jam, lalu disaring. Filtrat diuapkan dalam cawan penguap. Pada sisa dalam cawan penguap ditambahkan 2 tetes asam asetat anhidrida dan 1 tetes asam sulfat pekat. Timbul warna ungu atau merah kemudian berubah menjadi hijau biru menunjukkan adanya steroida-triterpenoida. Hal yang sama dilakukan juga untuk ekstrak etanol dan fraksinya(Harbone, 1984).
3.6.7. Pemeriksaan antrakinon
Sebanyak 0,2 g serbuk simplisia ditimbang, kemudian ditambahkan 5 ml asam sulfat 2 N, dipanaskan sebentar, setelah dingin ditambahkan 10 ml benzena, dikocok dan didiamkan. Lapisan benzena dipisahkan dan disaring, kocok lapisan benzena dengan 2 ml NaOH 2 N, didiamkan. Lapisan air berwarna merah dan lapisan benzena tidak berwarna menunjukkan adanya antrakinon. Hal yang sama dilakukan juga untuk ekstrak etanol dan fraksinya(Depkes, RI., 1979).
3.7. Pembuatan Ekstrak Daun Beluntas 3.7.1. Pembuatan ekstrak etanol
Sebanyak 200 g serbuk simplisia dimaserasi dengan etanol 96 % dalam wadah dan ditutup rapat. Dibiarkan pada suhu kamar selama 5 hari terlindung dari cahaya matahari sambil diaduk, kemudian disaring dan ampas dimaserasi kembali sampai maserat jernih. Maserat yang diperoleh dipekatkan dengan menggunakan rotary evaporator pada temperatur ±40oC sampai diperoleh ekstrak kental dan dimasukkan ke dalam freezer (± 1 minggu) (Depkes, RI., 1995).
3.7.2. Pembuatan fraksi-fraksi dari ekstrak etanol
etanol ditambahkan 5 ml etanol dan 10 ml air suling, lalu dimasukkan ke dalam corong pisah,kemudian ditambahkan 20 ml n-heksana, dikocok, didiamkan
sampai 2 lapisan n-heksana (lapisan atas) diambil dengan cara dekantasi dan fraksinasi dilakukan sampai warna lapisan n-heksana jernih, kemudian ditambahkan 20 ml etilasetat pada lapisan air, dikocok, didiamkan sampai terdapat 2 lapisan yang terpisah, lapisan etilasetat (lapisan atas) diambil dengan cara dekantasi dan fraksinasi dilakukan sampai warna lapisan etilasetat jernih, kemudian semua fraksi yang diperoleh diuapkan sampai diperoleh ekstrak kental. Masing-masing fraksi yang diperoleh dilakukan uji aktivitas antibakteri. Dilakukan 6 kali pengulangan (Rohman, 2007).
3.8. Uji Aktivitas Antibakteri 3.8.1. Sterilisasi alat
Alat-alat yang digunakan dalam uji aktivitas antimikroba ini disterilkan terlebih dahulu sebelum dipakai. Alat-alat gelas disterilkan di dalam oven pada suhu 170oC selama 1-2 jam. Media disterilkan di autoklaf pada suhu 121oC selama 15 menit. Jarum ose dan pinset dengan lampu Bunsen (Dirjen, POM., 1995).
3.8.2. Pembuatan media a. Media nutrient agar (NA)
Komposisi: ‘Lab-Lemco’ Powder 1 g
Yeast Extract 2 g
Peptone 5 g
Sodium chloride 5 g
Agar 15 g
kemudian disterilkan di dalam autoklaf pada suhu 121oC selama 15 menit (Oxoid, 1982).
b. Media nutrient broth (NB)
Komposisi: ‘Lab-Lemco’ Powder 1 g
Yeast Extract 2 g
Peptone 5 g
Sodium chloride 5 g
Cara pembuatannya, yaitu: sebanyak 13 g nutrient broth (NB) dimasukkan ke dalam erlemenyer masukkan air suling 1 L, lalu dipanaskan sampai larut kemudian disterilkan di dalam autoklaf pada suhu 121oC selama 15 menit (Oxoid, 1982).
3.8.3. Pembuatan media agar miring
Sebanyak 3 ml media nutrient agar yang sudah dicairkan dimasukkan ke dalam tabung reaksi steril, didiamkan pada temperatur kamar sampai memadat pada posisi miring membentuk sudut 30-45o. Disimpan dalam lemari pendingin pada suhu 5oC.
3.8.4. Pembuatan stok kultur
Biakan bakteri Escherichia coli dari strain utama diambil dengan jarum ose lalu diinokulasikan pada permukaan media nutrient agar miring dengan cara menggores, kemudian diinkubasi dalam inkubator pada suhu 35±2oC selama 18-24 jam. Hal yang sama dilakukan pada biakan bakteri Bacillus subtilis(Dirjen, POM., 1995).
3.8.5. Penyiapan inokulum
3.8.6. Pembuatan Larutan Uji Ekstrak Etanol, Fraksi N-Heksana Dan Etilasetat Daun Beluntas (Pluchea indica (L.) Less.)Dengan Berbagai Konsentrasi
Ekstrak etanol daun beluntas ditimbang sebanyak 3 g kemudian dilarutkan dalam dimetilsulfoksida (DMSO) dicukupkan sampai 6 ml. Konsentrasi ekstrak adalah 500 mg/ml kemudian dibuat pengenceran. Larutan tersebut diencerkan kembali dengan pelarut DMSO dengan konsentrasi 400 mg/ml; 300 mg/ml; 200 mg/ml; 100 mg/ml; 75 mg/ml; 50 mg/ml dan 25 mg/ml. Hal yang sama dilakukan terhadap fraksi n-heksana, fraksi etilasetat dan fraksi air.
3.8.7. Pengujian aktivitas antibakteri secara in vitro
BAB IV
HASIL DAN PEMBAHASAN
4.1. Identifikasi Tumbuhan
Hasil identifikasi tumbuhan telah dilakukan di Herbarium Bogoriense, Bidang Botani Pusat Penelitian Biologi LIPI-Bogor adalah Daun Beluntas (Pluchea indica (L.) Less.) suku Compositae. Hasil dapat dilihat pada Lampiran 1, halaman 41.
4.2. Pemeriksaan Karakteristik
Hasil pemeriksaan organoleptik terhadap simplisia daun beluntas yaitu bau khas, rasa agak pahit dan agak kelat.
Hasil pemeriksaan makroskopik simplisia daun beluntas tunggal bertangkai, rapuh, berwarna hijau kekuningan sampai hijau tua, bentuk bundar telur sampai jorong, panjang 4-8 cm lebar 3-5 cm, ujung daun meruncing, pinggir daun bergerigi, tulang daun menyirip. Hasil dapat dilihat pada Lampiran 2, halaman 42.
Hasil pemeriksaan mikroskopik serbuk simplisia pada daun beluntas adanya stomata tipe anomositik, rambut penutup dan pembuluh kayu penebalan spiral. Hasil dapat dilihat pada Lampiran 3, halaman 43.
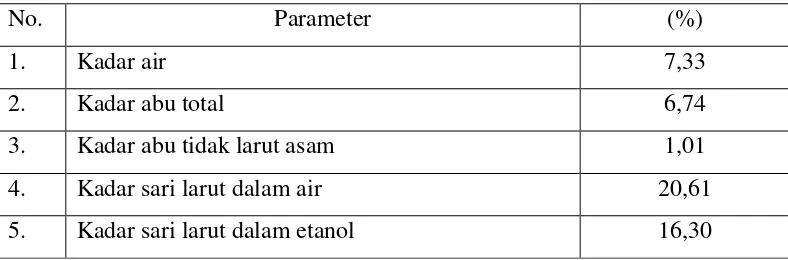
Hasil pemeriksaan karakteristik simplisia daun beluntas dapat dilihat pada Lampiran 5, halaman 47-51 dan Tabel 4.1.
Tabel 4.1. Pemeriksaan karakteristik simplisia daun beluntas
No. Parameter (%)
1. Kadar air 7,33
2. Kadar abu total 6,74
3. Kadar abu tidak larut asam 1,01
4. Kadar sari larut dalam air 20,61
5. Kadar sari larut dalam etanol 16,30
Hasil yang diperoleh dari pemeriksaan kadar air yaitu 7,33% berarti standarisasi simplisia memenuhi persyaratan.Apabila kadar air simplisia lebih besar dari 10% maka simplisia tersebut akan mudah ditumbuhi kapang pada saat penyimpanan sehingga mutu simplisia akan menurun. Kadar sari yang larut dalam air adalah 20,61% memenuhi persyaratan MMI yaitu tidak kurang dari 20%, sedangkan kadar sari yang larut dalam etanol 16,30% memenuhi persyaratan MMI yaitu tidak kurang dari 5%. Berdasarkan hasil penetapan kadar sari menunjukkan bahwa simplisia daun beluntas lebih banyak mengandung senyawa yang larut dalam air daripada yang larut dalam etanol. Penetapan kadar sari dilakukan untuk mengetahui kadar senyawa yang bersifat polar, sedangkan kadar sari larut dalam etanol untuk mengetahui senyawa yang terlarut dalam etanol baik polar maupun non polar. Senyawa yang bersifat polar dan larut dalam air akan tersari oleh air. Senyawa-senyawa yang tidak larut dalam air dan larut dalam etanol akan tersari oleh etanol (WHO., 1998).
ada pada simplisia dengan cara melarutkan abu total dalam asam klorida (WHO., 1998).
Simplisia daun beluntas 400 g diekstraksi dengan cara maserasi menggunakan pelarut etanol 96%. Hasilnya diperoleh ekstrak etanol daun beluntas 51,51 g. Dilakukan ekstarksi cair-cair secara berturut-turut menggunakan pelarut n-heksana, dan etilasetat. Dari 30 g ekstrak etanol diperoleh fraksi n-heksana 6,80 g, fraksi etilasetat 6,38 g dan fraksi air 8,25 g.
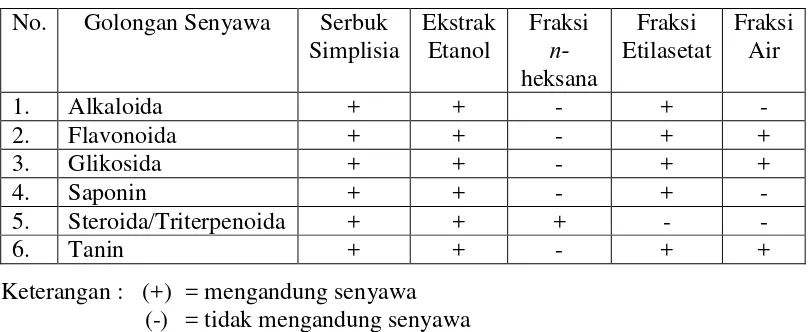
4.3. Skrining Fitokimia
Hasil skrining fitokimia terhadap serbuk simplisia, ekstrak etanol, fraksi n-heksana, fraksi etilasetat dan fraksi air daun beluntas terdapat golongan-golongan senyawa kimia yang memberikan hasil positif. Data dapat dilihat pada Tabel 4.2. Tabel 4.2.Skrining fitokimia dari simplisia, ekstrak etanol daun beluntasdan
fraksinya.
No. Golongan Senyawa Serbuk Simplisia
Keterangan : (+) = mengandung senyawa (-) = tidak mengandung senyawa
buih yang mantap setinggi 1-10 cm. Senyawa steroid/triterpenoid positif karena menghasilkan warna ungu atau hijau. Senyawa tanin positif karena menghasilkan warna hijau pada pengujiannya.
4.4. Uji Aktivitas Antibakteri Ekstrak Etanol, Fraksi N-Heksana dan Etilasetat Daun Beluntas (Pluchea indica (L.) Less.)
Hasil pengujianaktivitas antibakteri ekstrak etanol, fraksi n-heksana dan etilasetat daun beluntas (Pluchea indica (L.) Less.)terhadap bakteri Escherichia coli dan Bacillus subtilis dengan metode difusi agarmenunjukkan bahwa ekstrak etanol, fraksi n-heksana, etilasetat, dan air dapat menghambat pertumbuhan bakteri Escherichia coli dan Bacillus subtilis. Hasil pengukuran zona hambat ekstrak etanol, fraksi n-heksana, etilasetat dan air daun beluntas dapat dilihat pada Tabel 4.3-4.4dan pada Lampiran 14-15 halaman 60-61.
Tabel 4.3. aAktivitas antibakteri ekstrak etanol, fraksi n-heksana, etilasetat, dan air daun beluntas terhadap bakteri Escherichia coli
Konsentrasi
Keterangan - : tidak terdapat daerah hambatan pertumbuhan bakteri * : rata-rata diameter daerah hambatan pertumbuhan bakteri Blanko : dimethyl sulfoxide (DMSO)
aktivitas antibakteri menunjukkan bahwa ekstrak etanol memberikan hasil efektif untuk bakteri Eschericia coli pada konsentrasi 400 mg/ml memberikan zona hambat 14,38 mm dan konsentrasi hambat minimum (KHM) 25 mg/ml (8mm). Pada fraksi etilasetat memberikan hasil efektif untuk bakteribakteri Eschericia coli pada konsentrasi 100 mg/ml memberikan zona hambat 15,42 mm dan konsentrasi hambat minimum (KHM) 25 mg/ml (8,83mm). Pada fraksi n-heksana dan fraksi air memberikan hasil yang kurang efektif, karena zona hambat di bawah 14 mm.
Tabel 4.4. aAktivitas antibakteri ekstrak etanol, fraksi n-heksana, etilasetat, dan air daun beluntas terhadap bakteri Bacillus subtilis
Konsentrasi
Keterangan - : tidak terdapat daerah hambatan pertumbuhan bakteri * : rata-rata diameter daerah hambatan pertumbuhan bakteri Blanko : dimethyl sulfoxide (DMSO)
mg/ml memberikan zona hambat 14,10 mm dan KHM 25 mg/ml (8,88 mm).Pada fraksi n-heksana dan fraksi air memberikan hasil yang kurang efektif, karena zona hambat di bawah 14 mm.
Berdasarkan hasil pengujian yang diperoleh dapat dikatakan bahwa efek aktivitas antibakteri ekstrak etanol serta fraksi-fraksi dari daun beluntas lebih efektif terhadap bakteri Eschericia coli (bakteri Gram negatif) dibandingkan dengan bakteri Bacillus subtilis (bakteri Gram positif).
Adanya perbedaan hasil uji daya hambat pada bakteri Gram positif dan Gram negatif dapat dihubungkan melalui perbedaan dinding sel bakteri. Data dari hasil uji menunjukkan bahwa hambatan terbesar untuk ekstrak etanaol adalah bakteri Bacillus substillis yang merupakan bakteri Gram positif. Umumnya bakteri Gram positif lebih peka terhadap senyawa antibakteri dibandingkan dengan bakteri Gram negatif karena dinding sel bakteri Gram positif tidak memiliki lapisan lipopolisakarida sehingga senyawa antimikroba yang bersifat hidrofilik maupun hidrofobik dapat melewati dinding sel bakteri Gram bakteri positif melalui mekanisme difusi pasif kemudian berinteraksi langsung dengan peptidoglikan pada sel bakteri yang sedang tumbuh dan menyebabkan kematian sel. Target kerja dari antibakteri tidak hanya merusak dinding sel, tapi juga dapat menyebabkan koagulasi DNA dan denaturasi protein bakteri (Manu, 2013).
golongan senyawa fenol yang diketahui memiliki aktivitas antimikroba yang bersifat bakterisida namun tidak bersifat sporisida (Pratiwi, 2008). Senyawa fenol bekerja dengan cara mendenaturasi protein sel dan merusak dinding sel bakteri sehingga bakteri mati (Horvath, 1981).
Senyawa steroid/triterpenoid menghambat pertumbuhan bakteri dengan mekanisme penghambatan terhadap sintesis protein karena terakumulasi dan menyebabkan perubahan komponen-komponen penyusun sel bakteri. Senyawa terpenoid mudah larut dalam lipid, sifat inilah yang mengakibatkan senyawa ini mudah menembus dinding sel bakteri Gram positif dan dinding sel bakteri Gram negatif (Ferawaty, dkk., 2012). Senyawa saponin termasuk dalam kelompok antibakteri yang dapat menurunkan tegangan permukaan sehingga mengganggu permeabilitas membran sel bakteri, yang mengakibatkan kerusakan membran sel dan menyebabkan keluarnya berbagai komponen penting dari dalam sel bakteri yaitu protein, asam nukleat dan nukleotida (Ganiswara, 1995).
BAB V
KESIMPULAN DAN SARAN
5.1. Kesimpulan
Berdasarkan hasil penelitian ini dapat disimpulkan bahwa:
a. Kadar air 7,33%, kadar abu total diperoleh 6,74%, kadar abu tidak larut asam diperoleh 1,01%, kadar sari larut air diperoleh 20,61, dan kadar sari larut dalam etanol diperoleh 16,30%.
b. Simplisia daun beluntas mengandung golongan senyawa kimia yaitu: steroid/triterpenoid, alkaloid, glikosida, flavonoid, saponin dan tanin.
c. Ekstrak etanol memberikan hasil efektif pada konsentrasi 400 mg/ml untuk bakteri Eschericia coli dan pada konsentrasi 300 mg/ml untuk bakteri Bacillus subtilis dengan KHM untuk kedua bakteri pada konsentrasi 25 mg/ml. Fraksi etilasetat memberikan hasil efektif pada konsentrasi 100 mg/ml untuk bakteri Eschericia coli dan bakteri Bacillus subtilis dengan KHM untuk kedua bakteri pada konsentrasi 25 mg/ml. Fraksi n-heksana dan fraksi air memberikan hasil yang kurang efektif, karena diameter hambat di bawah 14 mm.
5.2. Saran
BAB II
TINJAUAN PUSTAKA
2.1. Uraian Tumbuhan 2.1.1. Klasifikasi tumbuhan
Menurut Pujowati (2006) klasifikasi dari tumbuhan beluntas sebagai berikut: Kingdom : Plantae
Divisi : Spermatophyta Sub divisi : Angiospermae Kelas : Dycotyledonae Bangsa : Compositales Suku : Compositae Marga : Pluchea
Spesies : Pluchea indica(L.) Less 2.1.2. Morfologi tumbuhan
2.1.3. Habitat dan daerah tumbuhan
Pluchea indica (L.) Less pada umumnya di Indonesia dikenal dengan nama beluntas, khususnya bagi masyarakat Sumatra, Jawa dan Madura. Sulawesi disebut lamutasa dan di Timor disebut lenabou. Dalam pengobatan Cina dikenal dengan luan yi dan di Eropa dikenal dengan marsh heabane (Hariana, 2005). Beluntas umumnya tumbuh liar di daerah kering pada tanah yang keras atau berbatu atau ditanam sebagai tanaman pagar. Tumbuhan ini memerlukan cukup cahaya matahari atau sedikit naungan, banyak ditemukan pada daerah pantai dekat laut, terdapat sampai 1000 m di atas permukaan laut (Ardiansyah, 2005).
2.1.4. Kandungan kimia beluntas
Daun beluntas mengandung alkaloid, flavonoida, tanin, minyak atsiri, asam chlorogenik, kalium, aluminium, kalsium, magnesium dan fosfor. Akarnya mengandung flavonoida dan tanin (Dalimartha, 1999).
2.1.5. Manfaat tumbuhan
Tumbuhan Beluntas dapat digunakan untuk menghilangkan bau badan dan bau mulut, kurang nafsu makan, gangguan pencernaan pada anak, TBC kelenjar (skrofuloderma), nyeri pada rematik, nyeri tulang, sakit pinggang, demam, dating haid tidak teratur dan keputihan (Dalimartha, 1999).
2.2. Kandungan Senyawa Kimia 2.2.1. Alkaloid
2.2.2. Flavonoida
Flavonoida umumnya terdapat pada tumbuhan sebagai glikosida. Flavonoid berupa senyawa fenol dan telah diketahui memiliki respon terhadap mikroba (Robinson, 1995). Aktivitasnya dikarenakan kemampuannya membentuk kompleks dengan protein seluler dan dinding sel bakteri (Cowan, 1999).
2.2.3. Tanin
Tanin pada tanaman merupakan senyawa fenolik yang larut dalam air yang memiliki berat molekul antara 300-3000 dan menghasilkan reaksi warna biru
dengan besi (III) klorida. Tanin berasal dari bahasa Prancis ‘tanin’ yang
merupakan fenol alami (Khanbabaea, 2001). Secara kimia tanin tumbuhan terbagi dua, yaitu tanin terkondensasi (tanin katekin) dan tanin terhidrolisis (Robison, 1995).
Tanin memiliki kemampuan untuk mengendapkan protein, memiliki aktivitas sebagai antioksidan, antitumor (Robinson, 1995). Sifat antibakteri tanin berhubungan dengan kemampuannya membentuk komplek dengan protein bakteri (Cowan, 1999).
2.2.4. Glikosida
Glikosida adalah suatu golongan senyawa bila dihidrolisis akan terurai menjadi gula (glikon) dan senyawa lain (aglikon atau genin). Glikosida mudah terhidrolisis oleh asam mineral atau enzim. Hidrolisis oleh asam memerlukan panas, sedangkan hidrolisis oleh enzim tidak memerlukan panas (Sirait, 2007).
Berdasarkan ikatan antara glikon dan aglikon, glikosida dapat dibedakan menjadi:
b. Tipe C-glikosida, ikatan antara bagian glikon dengan aglikon melalui jembatan C, yakni gula melekat pada aglikon melalui ikatan karbon-karbon.
c. Tipe S-glikosida, ikatan antara bagian glikon dengan aglikon melalui jembatan S. Contoh: sinigrin(C10H16NS2K) yang termasuk ke dalam glikosida glukosinolat dari tumbuhan Brassicaceae.
d. Tipe N-glikosida, ikatan antara bagian dari glikon dengan aglikon melalui jembatan N. Contoh: nikleosidin, kronotosidin.
2.2.5. Saponin
Saponin tersebar luas diantara tanaman tingkat tinggi. Saponin merupakan senyawa berasa pahit, menusuk, menyebabkan bersin dan mengakibatkan iritasi terhadap selaput lendir. Saponin mula-mula diberi nama demikian karena sifatnya yang menyerupai sabun (bahasa Latin sapo berarti sabun). Saponin adalah senyawa aktif permukaan yang kuat dan menimbulkan busa jika dikocok dalam air dan pada konsentrasi yang rendah sering menyebabkan hemolisis sel darah merah. Saponin sangat beracun dalam larutan yang sangat encer, untuk ikan dan tumbuhan yang mengandung saponin telah digunakan oleh penduduk sebagai racun ikan selama beratus-ratus tahun. Beberapa saponin bekerja sebagai antimikroba (Robinson, 1995).
2.2.6. Steroid/triterpenoid
dengan kebanyakan triterpen dan sterol memberikan warna hijau-biru (Harborne, 1987). Steroid pada umumnya berupa alkohol dengan gugus hidroksil pada C3 sehingga steroid sering juga disebut sterol (Robinson, 1995). Gambar struktur dasar dapat dilihat pada Gambar 2.3.
Gambar 2.3Struktur dasarsteroid(Robinson, 1995)
2.3. Ekstraksi
Ekstraksi adalah penyarian komponen aktif dari suatu jaringan tumbuhan atau hewan dengan menggunakan pelarut yang cocok (Handa, 2008). Beberapa metode ekstraksi dengan menggunakan pelarut (Depkes, 2000) yaitu:
1. Cara dingin a. Maserasi
Maserasi adalah proses pengekstrakan simplisia dengan menggunakan pelarut dengan beberapa kalipengocokan atau pengadukan pada temperatur kamar. Maserasi kinetik berarti dilakukan pengadukan yang kontinu (terus menerus).Remaserasi berarti dilakukan penyarian berulang dan seterusnya.
b. Perkolasi
tahap perkolasi sebenarnya (penetesan/penampungan ekstrak), terus menerus sampai diperoleh ekstrak (perkolat) yang jumlahnya 1–5 kali bahan.
2. Cara panas a. Refluks
Refluks adalah ekstraksi dengan menggunakan pelarut pada temperatur titik didihnya, selama waktu tertentu dan jumlah pelarut terbatas yang relatif konstan dengan adanya pendingin balik.
b. Digesti
Digesti adalah maserasi kinetik (dengan pengadukan kontinu) pada temperatur lebih tinggi dari temperatur ruangan (kamar), yaitu secara umum dilakukan pada temperatur 40–50oC.
c. Sokletasi
Sokletasi adalah proses penyarian dengan menggunakan alat soklet dengan pelarut yang selalu baru sehingga terjadi ekstraksi kontinu dengan jumlah pelarut yang relatif konstan dengan adanya pendingin balik.
d. Infundasi
Infundasi adalah ekstraksi dengan pelarut air pada temperatur penangas air (bejana infus tercelup dalam penangas mendidih, temperatur terukur 96–98oC) selama waktu tertentu (15–20 menit).
e. Dekoktasi
Dekoktasi adalah infus pada waktu yang lebih lama (≥ 30 menit) dan temperatur sampai titik didih air.
2.4. Fraksinasi (Ekstaksi Cair-Cair)
organik), yang tidak tercampurkan. Pada proses ini terjadi pemisahan satu atau lebih zat terlarut (solute) kedalam pelarut yang kedua (Basset, 1994).
Pemisahan yang dilakukan bersifat sederhana, bersih, cepat dan mudah, yang dapat dilakukan dengan cara mengocok-ngocok dalam sebuah corong pisah selama beberapa menit (Basset, 1994). Analit-analit yang mudah terekstraksi dalam pelarut organik adalah molekul-molekul netral yang berikatan secara kovalen dengan substituent yang bersifat nonpolar atau agak polar. Senyawa-senyawa yang mudah mengalami ionisasi dan Senyawa-senyawa polar lainnya akan tertahan dalam fase air (Rohman, 2007).
Pelarut yang dipilih untuk ekstraksi pelarut ialah pelarut yang mempunyai kelarutan yang rendah dalam air, dapat menguap sehingga memudahkan penghilangan pelarut organik setelah dilakukan ekstraksi dan mempunyai kemurnian yang tinggi untuk meminimalkan adanya kontaminasi sampel (Rohman, 2007).
2.5. Bakteri
2.5.1. Uraian umum
Bakteri merupakan sekelompok mikroba atau mikroorganisme yang bersel satu, berkembangbiak dengan membelah diri, karena bentuknya sangat kecil sehingga hanya dapat dilihat dengan menggunakan mikroskop. Nama bakteri
berasal dari kata “bakterion” yang berarti tongkat atau batang
(Dwidjoseputro,1987). Bakteri pada umumnya terdiri dari tiga bentuk dasar, yaitu: bentuk bulat (kokus), batang (basilus) dan spiral (Fardiaz, 1992; Pratiwi, 2008).
a. Bakteri Gram positif, yaitu bakteri yang dapat mengikat zat warna utama (kristal violet)sehingga tampak berwarna ungu tua.
b. Bakteri Gram negatif, yaitu bakteri yang kehilangan warna utama (Kristal violet) ketika dicuci denngan alkohol dan menyerap zat warna kedua sewaktu pemberian safranin tampak berwarna merah (Suryanto, 2006).
2.5.2. Bakteri Escherichia coli
Eschericia coli merupakan bakteri Gram negatif, aerob atau anaerob fakulatif, berbentuk batang, tidak bergerak. Escherichia coli biasanya terdapat dalam saluran cerna sebagai flora normal (Dwidjoseputro, 1987). Bakteri ini tumbuh baik pada suhu 37oC, membentuk koloni yang bundar, halus dan tepi rata. Bakteri ini dapat menjadi patogen bila berada di luar usus atau di lokasi lain dalam jumlah yang banyak (Jawetz, et al., 2001). Sistematika bakteri Escherichia coli (Dwidjoseputro, 1987) adalah sebagai berikut:
Divisi : Schizophyta Kelas : Schizomycetes Ordo : Eubacterales Famili : Enterobacteriaceae Genus : Escherichia
Spesies : Escherichia coli
2.5.3. Bakteri Bacillus subtilis
Divisi : Firmicutes Kelas : Bacilli Ordo : Bacillales Famili : Bacillaceae Genus : Bacillus
Spesies : Bacillus subtilis
2.6. Fase Pertumbuhan Mikroorganisme
Fase pertumbuhan menurut (Pratiwi, 2008) terbagi menjadi empat macam, yaitu:
a. Fase lag (fase adaptasi)
Merupakan fase penyesuaian mikroorganisme pada suatu lingkungan baru dan bakteri belum mengadakan pembiakan. Ciri fase lag adalah tidak adanya peningkatan jumlah sel tetapi peningkatan ukuran sel.
b. Fase log
Merupakan fase dimana mikroorganisme tumbuh dan membelah pada kecepatan maksimum tergantung sifat media dan kondisi pertumbuhan. Sel baru terbentuk dengan laju konstan dan massa yang bertambah secara eksponensial. c. Fase stasioner (konstan)
Merupakan fase pertumbuhan mikroorganisme berhenti dan terjadi keseimbangan antara jumlah sel yang membelah dengan jumlah sel yang mati. d. Fase kematian
2.7. Faktor Pertumbuhan Mikroorganisme
Faktor yang dapat mempengaruhi pertumbuhan dapat dibedakan menjadi faktor fisik dan faktor kimia. Faktor fisik meliputi temperatur, pH dan tekanan osmosis. Faktor kimia meliputi karbon, oksigen, trace elementdan faktor-faktor pertumbuhan organik termasuk nutrisi yang ada dalam media pertumbuhan (Pratiwi, 2008).
2.8. Antibakteri
Antibakteri adalah senyawa yang digunakan untuk mengendalikan pertumbuhan bakteri yang bersifat merugikan. Antimikroba meliputi golongan antibakteri, antimikotik dan antiviral (Ganiswara, 1995). Senyawa antibakteri dapat bekerja secara bakteriostatik dan bakterisidal (Pelezar, 1988). Obat yang digunakan untuk membasmi bakteri penyebab infeksi pada manusia harus memiliki sifat toksisitas yang selektif yaitu toksis terhadap bakteri tetapi relatif tidak toksis terhadap hospes (Ganiswara, 1995). Target kerja antibakteri (antibiotik) berdasarkan spectrum atau kisaran kerjanya antibiotik dapat dibedakan menjadi berspektrum sempit (narrow spectrum) dan antibiotik berspektrum luas (broad spectrum). Antibiotik berspektrum sempit hanya mampu menghambat segolongan jenis bakteri saja, contohnya hanya mampu menghambat atau membunuh bakteri Gram negatif saja atau Gram positif saja. Sedangkan antibiotik Gram berspektrum luas dapat menghambat atau membunuh bakteri dari golongan Gram positif maupun Gram negatif (Pratiwi, 2008).
a. Antibiotik yang menghambat sintesis dinding sel
Antibiotik ini adalah antibiotik yang merusak lapisan peptidoglikan yang menyusun dinding sel bakteri Gram positif maupun Gram negatif, contohnya penisiln.
b. Antibiotik yang merusak membran plasma
Antibiotik yang bersifat merusak membrane plasma umum terdapat pada antibiotik golongan polipeptida yang bekerja dengan mengubah permeabilitas membrane plasma sel bakteri. Contohnya adalah polimiksin B yang melekat pada fosfolipid membran.
c. Antibiotik yang menghambat sintesis protein
Aminoglikosida merupakan kelompok antibiotik yang gula aminonya tergabung dalam ikatan glikosida. Antibiotic ini memiliki spektrum luas dan bersifat bakterisidal dengan mekanisme penghambatan pada sintesis protein. d. Antibiotik yang menghambat sintesis asam nukleat (DNA/RNA)
Penghambatan pada sintesis asam nukleat berupa penghambatan terhadap transkripsi dan replikasi mikroorganisme. Yang termasuk antibiotik penghambat sintesis asam nukleat ini adalah antibiotic golongan kuinolon dan rifampisin. e. Antibiotik yang menghambat sintesis metabolit esensial
Penghambatan terhadap sintesis metabolit esensial antara lain dengan adanya kompetitor berupa antimetobolit, yaitu substansi yang secara kompetitif menghambat metabolit mikroorganisme, karena memiliki struktur yang mirip dengan substrat normal bagi enzim metabolism. Contohnya adalah antimetabolit sulfanilamid dan Para Amino Benzoic Acid(PABA).
dan kadar bunuh minimal (KBM). Antimikroba tertentu aktivitasnya dapat meningkat dari bakteriostatik menjadi bakterisid bila kadar antimikrobanya ditingkatkan melebihi KHM (Ganiswara, 1995). Ada beberapa hal yang harus dipenuhi oleh suatu bahan antimikroba, seperti mampu mematikan mikroorganisme, mudah larut dan bersifat stabil, tidak bersifat racun bagi manusia dan hewan, efektif pada suhu kamar dan suhu tubuh, tidak menimbulkan karat dan warna, berkemapuan menghilangkan bau yang kurang sedap, murah dan mudah didapat (Pelezar, 1988).
2.9. Metode Pengujian Aktivitas Antimikroba
Pengujian aktivitas bahan antimiroba secara in vitro dapat dilakukan melalui dua cara, yaitu metode difusi dan metode dilusi. Pembagian metode difusi dan dilusi, yaitu (Pratiwi, 2008):
1. Metode difusi
a. Metode disc diffusion (tes Kirbydan Bauer)
Piringan yang berisi agen antimikroba diletakkan pada media agar yang telah ditanami mikroorganisme yang akan berdifusi pada media agar tersebut. Area jernih mengindikasikan adanya hambatan pertumbuhan mikroorganisme oleh agen antimikroba pada permukaan media agar.
b. E-test
c. Ditch-plate technique
Pada metode ini sampel uji berupa agen antimikroba yang telah diletakkan pada parit yang dibuat dengan cara memotong media agar dalam cawan petri pada bagian tengah secara membujur dan mikroba uji (maksimum 6 jenis) lalu digoreskan ke arah parit yang berisi agen antimikroba.
d. Cup-plate technique
Metode ini serupa dengan metode disc diffusion, dibuat sumur pada media agar yang telah ditanami dengan mikroorganisme dan pada sumur tersebut diberi agen antimikroba yang akan diuji.
2. Metode dilusi
Metode dilusi dibagi menjadi dua, yaitu dilusi padat (solid dilution) dan dilusi cair (broth dilution).
a. Metode dilusi cair/broth dilution test (serial dilution)
Metode ini untuk mengukur MIC atau KHM dan MBC atau KBM. Cara yang dilakukan adalah dengan membuat seri pengenceran agen antimikroba pada medium cair yang ditambahkan dengan mikroba uji.
b. Metode dilusi padat/solid dilution test
Metode ini serupa dengan metode dilusi cair namun menggunakan media padat (solid).
2.10. Sterilisasi
a. Sterilisasi panas basah
Strerilisasi panas basah dapat dilakukan pada suhu air mendidh 100oC selama 10 menit yang efektif untuk sel-sel vegetatif, namun tidak efektif untuk endospora bakteri. Sterilisasi panas basah menggunakan temperature di atas 100oC dilakukan dengan uap yaitu menggunakan autoklaf. Proses sterilisasi dengan cara mendenaturasi atau mengkoagulasi protein pada enzim dan membran sel mikroorganisme (Pratiwi, 2008), dengan suhu 121oC ( dengan tekanan 15 psi) selama 15-20 menit (Irianto, 2006).
b. Sterilisasi panas kering
BAB I PENDAHULUAN
1.1. Latar Belakang
Indonesia merupakan salah satu negara penghasil tanaman obat yang potensial, hasil alam yang paling banyak digunakan sebagai bahan obat adalah tanaman dan telah digunakan dalam kurun waktu cukup lama. Obat-obatan modern berkembang cukup pesat, namun potensi dari tanaman obat tetap tinggi karena dapat diperoleh tanpa resep dokter dan dapat diramu sendiri (Djauhariya dan Hermani, 2004).
Prospek pengembangantumbuhan obat semakin pesat saja mengingat perkembangan industri obat modern dan obat tradisional terus meningkat. Kondisi ini turut dipengaruhi oleh kesadaran masyarakat yang semakin meningkat tentang manfaat tumbuhan sebagai obat. Masyarakat semakin sadar akan pentingnya kembali ke alam (back to nature) dengan memanfaatkan obat-obat alami (Djauhariya dan Hermani, 2004).
Hasil komunikasi personal dengan masyarakat Desa Labuhan Deli, Kecamatan Medan Marelan, Kota Madya Medan, tumbuhan yang berkhasiat obat dikenal dan digunakan masyarakat salah satunya adalah tumbuhan beluntas (Pluchea indica (L.) Less.) dari sukuCompositae. Menurut pengalaman masyarakat,tumbuhan ini berkhasiat untuk meredakan asma dan batuk.
flavonoid (Hariana, 2006). Menurut Robinson (1995), senyawa flavonoid, saponin, tanin merupakan senyawa kimia yang memiliki potensi sebagai antibakteri dan antivirus. Karekteristik dari simplisia beluntas dilakukan sesuai denganyang tertera di Materia Medika Indonesia (MMI) edisi IV.Menurut Farmakope Indonesia edisi III (1979) penyarian simplisia menggunakan etanol 96%.
Bakteri yang digunakan adalah bakteri Bacillus subtilisyang merupakan salah satu bakteri penyebab batuk.Bakteri ini tersebar di udara dan termasuk dalam golongan bakteri Gram positif.Bakteri dari golongan Gram negatif digunakan bakteriEschericia colimerupakan bakteri yang dapat menyebabkan diare.
Berdasarkan hal di atas dilakukan penelitian uji aktivitas antibakteri ekstrak etanol dan fraksi-fraksi daun beluntas terhadap bakteri Eschericia coli dan Bacillus subtilis. Bahagian yang digunakan adalah simplisia daun beluntas. Penelitian meliputi karakterisasi simplisia, skrining fitokimia, pembuatan ekstrak, serta uji aktivitas antimikroba dari ekstak etanol dan fraksi-fraksi daun beluntas.
1.2. Perumusan Masalah
Berdasarkan latar belakang di atas dapat diambil perumusan masalah yaitu: a. Apakah karakteristik simplisia daun beluntas sesuai dengan yang tertera
diMMI edisi IV?
b. Apakah golongan senyawa kimia yang terdapat di dalam daun beluntas? c. Apakah ekstrak etanol dan fraksi-fraksidaun beluntas memiliki aktivitas
1.3. Hipotesis
Berdasarkan perumusan masalah di atas, maka hipotesis penelitian adalah: a. Karakteristik simplisia daun beluntas sesuai seprti yang tertera di MMI edisi
IV.
b. Golongan senyawa kimia yang terdapat di dalam adalah alkaloid dan flavonoid.
c. Ekstrak etanol dan fraksi-fraksidaun beluntas memiliki aktivitas antibakteri terhadap bakteri Gram negatifEscherichia colidan bakteri Gram positif Bacillus subtilis.
1.4. Tujuan Penelitian Tujuan penelitian adalah:
a. Untuk mengetahui karakteristik simplisia daun beluntas.
b. Untuk mengetahui golongan senyawa kimia yang terdapat di dalam daun beluntas.
c. Untuk mengetahui aktivitas antibakteri ekstrak etanol dan fraksi-fraksidaun beluntas terhadap bakteri Gram negatifEscherichia colidan bakteri Gram positif Bacillus subtilis.
1.5. Manfaat Penelitian
Uji Aktivitas Antibakteri Ekstrak Etanol Dan Fraksi-Fraksi Daun Beluntas (Pluchea indica (L.) Less.) Terhadap Bakteri Escherichia coliDan Bacillus
subtilis
Abstrak
Indonesia merupakan salah satu negara penghasil tumbuhan obat yang potensial, hasil alam yang paling banyak digunakan sebagai bahan obat adalah tumbuhan dan telah digunakan dalam kurun waktu cukup lama. Tumbuhan yang berkhasiat sebagai obat salah satunya adalah tumbuhan beluntas. Penelitian ini dilakukan untuk menguji aktivitas antibakteri daun beluntas.
Tahapan kerja meliputi karakterisasi simplisia, skrining fitokimia dan pembuatan ekstrak etanol daun beluntas secara maserasi kemudian difraksinasi secara berturut-turut dengan pelarut n-heksana, etilasetat dan air. Ekstrak etanol dan fraksi-fraksi selanjutnya diuji aktivitas antibakteri terhadap beberapa bakteri dengan metode difusi agar.
Antibacterial Activity Test of Extract Ethanol And Fractions of Leaves Beluntas (Pluchea indica (L.) Less.) Against Bacteria Escherichia coliAnd
Bacillus subtilis
Abstract
Indonesia is one of potential medicinal plants country, where natural products are most widely used as a medicinal ingeredient is a plant and it has been used in a long time. One of the plant that has medicinal properties is the plant beluntas. This research was conducted to test the antibacterial activity of leaves beluntas.
The processof the research includes sample collection, sample processing, characterization of crude drug, phytochemical screening and the manufacture of ethanol extract of leaves by maceration beluntas then fractionated successively with the solvent n-hexane and ethylacetate. Ethanol extract, fraction of n-hexane and ethylacetate were tested antibacterial activity against some bacteria by using agar diffusion method.
The result on research conducted of dried material leaves beluntashas showed that the water content 7.33%; the total ash 6.74%; the insoluble ash in acid 1.01%; the water soluble extract 20.61% and the ethanol soluble extract 16.30%. The phytochemical screening of dried matrial and ethanol extract hasgot the presence of steroid/triterpenoid, alkaloid, glycosides, flavonoid, saponine dan tannin.The result testgot that the antibacterial activity of ethanol extract provide effective result for Eschericia coli at a concentration of 400 mg/ml with inhibition zone 14.38 mm and Bacillus subtilis at a concentration of 300 mg/ml with inhibition zone 14.47 mm. The fraction ethylacetat provide effective result for Eschericia coli at a concentration of 100 mg/ml with inhibition zone 15.42 mm and Bacillus subtilis at a concentration of 100 mg/ml with inhibition zone 14.10 mm, while the n-hexane fraction and water fraction result are less effective because the inhibition zone under 14 mm. Effective antibacterial activity inhibit the bacteria Eschericia coli and Bacillus subtilis are ethanol extract and fraction ethylacetat compared the n-hexane fraction and water fraction.
UJI AKTIVITAS ANTIBAKTERI EKSTRAK
ETANOLDANFRAKSI-FRAKSIDAUN BELUNTAS(Pluchea indica
(L.) Less.)TERHADAP BAKTERI Escherichia coliDAN Bacillus
subtilis
SKRIPSI
OLEH: ALMUNADIA NIM121524168
PROGRAM EKSTENSI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
UJI AKTIVITAS ANTIBAKTERI EKSTRAK
ETANOLDANFRAKSI-FRAKSIDAUN BELUNTAS(Pluchea indica
(L.) Less.)TERHADAP BAKTERI Escherichia coliDAN Bacillus
subtilis
SKRIPSI
Diajukan sebagai salah satu syarat untuk mencapai gelar Sarjana Farmasi pada Fakultas Farmasi
Universitas Sumatera Utara OLEH:
ALMUNADIA NIM121524168
PROGRAM EKSTENSI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
PENGESAHAN SKRIPSI
UJI AKTIVITAS ANTIBAKTERI EKSTRAK ETANOLDAN
FRAKSI-FRAKSIDAUN BELUNTAS(Pluchea indica (L.)
Less.)TERHADAP BAKTERI Escherichia coliDANBacillus subtilis
OLEH : ALMUNADIA NIM 121524168
Dipertahankan di hadapan Panitia Penguji Fakultas Farmasi Universitas Sumatera Utara
Pada tanggal: 25 Januari 2016
Medan, Maret 2016 Fakultas Farmasi
Universitas Sumatera Utara Pejabat Dekan,
Dr. Masfria, M.S., Apt. NIP 195707231986012001 Disetujui Oleh:
Pembimbing I, Panitia Penguji,
Dra. Herawaty Ginting, M.Si., Apt. Dr. Masfria, M.S., Apt. NIP 195112231980032002 NIP 195707231986012001
Dra. Herawaty Ginting, M.Si., Apt.
Pembimbing II, NIP 195112231980032002
Dra. Erly Sitompul, M.Si., Apt. Dr. Panal Sitorus, M.Si., Apt. NIP 195006121980032001 NIP195310301980031002
KATA PENGANTAR
Skripsi ini disusun sebagai salah satu syarat mencapai gelar Sarjana Farmasi pada Fakultas Farmasi Universitas Sumatera Utara, dengan judul “Uji
Aktivitas Antibakteri Ekstrak Etanol dan Fraksi-Fraksi Daun Beluntas (Pluchea indica (L.) Less.) Terhadap Bakteri Escherichia colidan Bacillus subtilis.
Pada kesempatan ini dengan segala kerendahan hati penulis mengucapkan terima kasih yang sebesar-besarnya kepada Ibu Dr. Masfria, M.S., Apt.,selaku Pejabat Dekan yang telah memberikan fasilitas. Ucapan terima kasih kepada Ibu Dra. Herawaty Ginting, M.Si., Apt.,dan Ibu Dra. Erly Sitompul, M.Si., Apt., selaku pembimbing I dan II yang telah membimbing dan memberikan petunjuk serta saran-saran selama penelitian hingga selesainya skripsi ini.
Ucapan terima kasih kepada Ibu Dr. Masfria, M.S., Apt selaku ketua penguji, Bapak Panal Sitorus, M.Si., Apt., dan Bapak Popi Patilaya, M.Sc., Apt., selaku anggota penguji yang telah memberikan saran untuk menyempurnakan skripsi ini. Bapak dan Ibu staf pengajar Fakultas Farmasi USU Medan yang telah mendidik selama perkuliahan. Ibu Kepala Laboratorium Farmakognosi dan Mikrobiologi yangtelah memberikan fasilitas, petunjuk dan membantu selama penelitian.
Penulis menyadari sepenuhnya bahwa dalam penulisan skripsi ini masih jauh dari kesempurnaan, oleh karena itu penulis menerima kritik dan saran demi kesempurnaan skripsi ini. Penulis berharap semoga skripsi ini dapat memberikan manfaat bagi kita semua.
Medan, Maret 2016 Penulis
SURAT PERNYATAAN TIDAK PLAGIAT
Saya yang bertandatangan dibawah ini :
Nama : Almunadia
Nomor Induk Mahasiswa : 121524168 Program Studi : Ekstensi Farmasi
Judul Skripsi :eUji Aktivitas Antibakteri Ekstrak Etanol Dan Fraksi-Fraksi Daun Beluntas (Pluchea indica (L.) Less.) Terhadap Bakteri Escherichia coli Dan Bacillus subtilis
Dengan ini menyatakan bahwa skripsi ini ditulis berdasarkan data dari hasil pekerjaan yang saya lakukan sendiri, dan belum pernah diajukan oleh orang lain untuk memperoleh gelar kesarjanaan di perguruan tinggi lain, dan bukan plagiat karena kutipan yang ditulis telah disebutkan sumbernya di dalam daftar pustaka.
Apabila di kemudian hari ada pengaduan dari pihak lain karena di dalam skripsi ini ditemukan plagiat karena kesalahan saya sendiri, maka saya bersedia menerima sanksi apapun oleh Program Studi Farmasi Fakultas Farmasi Universitas Sumatera Utara, dan bukan menjadi tanggung jawab pembimbing.
Demikianlah surat pernyataan ini saya perbuat dengan sebenarnya untuk dapat digunakan jika diperlukan sebagaimana mestinya.
Medan, 18 Maret 2016 Yang membuat pernyataan,
Uji Aktivitas Antibakteri Ekstrak Etanol Dan Fraksi-Fraksi Daun Beluntas (Pluchea indica (L.) Less.) Terhadap Bakteri Escherichia coliDan Bacillus
subtilis
Abstrak
Indonesia merupakan salah satu negara penghasil tumbuhan obat yang potensial, hasil alam yang paling banyak digunakan sebagai bahan obat adalah tumbuhan dan telah digunakan dalam kurun waktu cukup lama. Tumbuhan yang berkhasiat sebagai obat salah satunya adalah tumbuhan beluntas. Penelitian ini dilakukan untuk menguji aktivitas antibakteri daun beluntas.
Tahapan kerja meliputi karakterisasi simplisia, skrining fitokimia dan pembuatan ekstrak etanol daun beluntas secara maserasi kemudian difraksinasi secara berturut-turut dengan pelarut n-heksana, etilasetat dan air. Ekstrak etanol dan fraksi-fraksi selanjutnya diuji aktivitas antibakteri terhadap beberapa bakteri dengan metode difusi agar.
Antibacterial Activity Test of Extract Ethanol And Fractions of Leaves Beluntas (Pluchea indica (L.) Less.) Against Bacteria Escherichia coliAnd
Bacillus subtilis
Abstract
Indonesia is one of potential medicinal plants country, where natural products are most widely used as a medicinal ingeredient is a plant and it has been used in a long time. One of the plant that has medicinal properties is the plant beluntas. This research was conducted to test the antibacterial activity of leaves beluntas.
The processof the research includes sample collection, sample processing, characterization of crude drug, phytochemical screening and the manufacture of ethanol extract of leaves by maceration beluntas then fractionated successively with the solvent n-hexane and ethylacetate. Ethanol extract, fraction of n-hexane and ethylacetate were tested antibacterial activity against some bacteria by using agar diffusion method.
The result on research conducted of dried material leaves beluntashas showed that the water content 7.33%; the total ash 6.74%; the insoluble ash in acid 1.01%; the water soluble extract 20.61% and the ethanol soluble extract 16.30%. The phytochemical screening of dried matrial and ethanol extract hasgot the presence of steroid/triterpenoid, alkaloid, glycosides, flavonoid, saponine dan tannin.The result testgot that the antibacterial activity of ethanol extract provide effective result for Eschericia coli at a concentration of 400 mg/ml with inhibition zone 14.38 mm and Bacillus subtilis at a concentration of 300 mg/ml with inhibition zone 14.47 mm. The fraction ethylacetat provide effective result for Eschericia coli at a concentration of 100 mg/ml with inhibition zone 15.42 mm and Bacillus subtilis at a concentration of 100 mg/ml with inhibition zone 14.10 mm, while the n-hexane fraction and water fraction result are less effective because the inhibition zone under 14 mm. Effective antibacterial activity inhibit the bacteria Eschericia coli and Bacillus subtilis are ethanol extract and fraction ethylacetat compared the n-hexane fraction and water fraction.
DAFTAR ISI
JUDUL ... i
HALAMAN PENGESAHAN ... ii
KATA PENGANTAR ... iii
SURAT PERNYATAAN TIDAK PLAGIAT ... v