UIN SYARIF HIDAYATULLAH JAKARTA
UJI EFEK ANTIINFLAMASI EKSTRAK n-heksan
LUMUT HATI Mastigophora diclados TERHADAP TIKUS
PUTIH JANTAN Strain Sprague Dawley
SKRIPSI
MIGI FEBRI ARINI
NIM: 109102000039
PROGRAM STUDI FARMASI
FAKULTAS KEDOKTERAN DAN ILMU KESEHATAN
UIN SYARIF HIDAYATULLAH JAKARTA
UJI EFEK ANTIINFLAMASI EKSTRAK n-heksan
LUMUT HATI Mastigophora diclados TERHADAP TIKUS
PUTIH JANTAN Strain Sprague Dawley
SKRIPSI
Diajukan sebagai salah satu syarat memperoleh gelar Sarjana Farmasi
MIGI FEBRI ARINI
NIM: 109102000039
PROGRAM STUDI FARMASI
FAKULTAS KEDOKTERAN DAN ILMU KESEHATAN
Nama
: Migi Febri Arini
Program Studi : Farmasi
Judul
: Uji Efek Antiinflamasi Ekstrak n-heksan Lumut
Hati Mastigophora diclados Terhadap Tikus Putih
Jantan Strain Sprague Dawley
Dari hasil penelitian sebelumnya diketahui bahwa ekstrak etanol lumut hati
Mastigophora diclados aktif sebagai antiinflamasi. Tujuan penelitian ini adalah untuk melanjutkan meneliti lumut hati Mastigophora diclados yang diekstraksi menggunakan metode maserasi dengan pelarut n-heksana. Penelitian dilakukan dengan menggunakan 30 ekor tikus Strain Sprague Dawley, yang dibagi dalam 5 kelompok perlakuan yaitu dosis 5 mg/KgBB, 10 mg/KgBB, dan 50 mg/KgBB serta kelompok kontrol negatif (Na CMC 0,5%) dan kelompok kontrol positif. Penelitian ini dilakukan dengan menggunakan metode pembentukan udem buatan pada telapak kaki tikus yang diinduksi karagenan 1% sebanyak 0,2 mL sebagai induktor radang. Sebagai kontrol positif digunakan asetosal dengan dosis 125 mg/KgBB. Hasil udem telapak kaki tikus diukur dengan menggunakan alat plestimometer setiap 1 jam selama 6 jam pengamatan pada setiap kelompok. Hasil penelitian menunjukan bahwa daya hambat terbesar yang dihasilkan pada ekstrak
n-heksan lumut hati Mastigophora diclados terjadi pada dosis 50 mg/KgBB dengan persentase inhibisi radang sebesar 82,04%, dosis 10 mg/KgBB sebesar 60,07% dan dosis 5 mg/KgBB sebesar 34,2%. Hasil uji ANOVA menunjukkan adanya perbedaan bermakna antara setiap dosis dengan kontrol negatif pada taraf
uji 0,05 (ρ≤0,05) dan semua dosis ekstrak terdapat perbedaan bermakna dengan
kontrol positif (ρ≤0,05) terkecuali pada dosis 10 mg/KgBB tidak terdapat perbedaan bermakna dengan kontrol positif pada taraf uji 0,05 (ρ≥0,05).
Name
: Migi Febri Arini
Program Study : Pharmacy
Title
: The Antiinflammatory Effect of n-hexane Extract
of Livermorts Mastigophora diclados on Sprague
Dawley white rats.
From the result of the previous study, it is known that the ethanol extract of liverworts Mastigophora diclados is active as anti inflammatory. The purpose of this study was to continue the research on liverworts Mastigophora diclados
which was extracted with maceration method using n-hexane. This research was conducted using 30 Sprague Dawley rats, which were divided in 5 dosage treatments; 5 mg/kgBW, 10 mg/KgBW, and 50mg/KgBW, along with negative control group (0,5% Na CMC) and positive control group. This research was carried out by using artificial edema formation method on the sole of 1% carrageenan-induced mice with the amount of 0,2 mL as an inflammation inductor. As positive control, acetosal was used with a dosage of 125 mg/KgBW. The production of edema on the rat sole foot was measured with plethysmometer every 1 hour for 6 hours under surveillance for each group. The result of the research showed that the strongest inhibition produced by n-hexane extract of Liverworts Mastigophora diclados occurred on the dosage of 50 mg/KgBW with the percentage of inflammation inhibition 82,04%, dosage of 10 mg/KgBB 60,07% and dosage of 5 mg/KgBB 34,2%. It was known from the result of ANOVA showed that there were significant differences between each dose of the extract with the negative control (ρ≤0.05) and all doses of the extract are significant differences with the positive control (ρ ≤ 0.05), except at a dose of 10 mg/Kg body weight there was no significant difference in the positive control
level test 0.05 (ρ ≥ 0.05).
Assalamu’alaikum Wr. Wb
Alhamdulillah, segala puji syukur ke hadirat Allah SWT yang telah
memberikan berkat dan rahmat-Nya, sehingga sehingga penulis dapat
menyelasaikan skripsi dengan judul “Uji Efek Antiinflamasi Ekstrak n-heksan Lumut Hati Mastigophora diclados Terhadap Tikus Putih Jantan Strain Sprague Dawley” Penulisan skripsi ini dilakukan dalam rangka untuk memenuhi tugas akhir sebagai salah satu syarat untuk memperoleh gelar Sarjana Farmasi
pada Fakultas Kedokteran dan Ilmu Kesehatan Program Studi Farmasi UIN
Syarif Hidayatullah, Jakarta.
Saya menyadari bahwa, tanpa bantuan dan bimbingan dari berbagai pihak, dari
masa perkuliahan sampai pada penyusunan skripsi ini sangatlah sulit bagi saya
untuk menyelesaikan skripsi ini. Oleh karena itu, saya mengucapkan terima
kasih kepada :
1. Ibu Ismiarni Komala, M.Sc., Ph.D, Apt selaku pembimbing pertama
dan Ibu Ofa Suzanti Betha, M.Si., Apt selaku pembimbing kedua, yang
memiliki andil besar dalam proses penelitian dan penyelesaian tugas akhir
saya ini, semoga segala bantuan dan bimbingan ibu mendapat imbalan
yang lebih baik di sisi-Nya
2. Bapak Prof. DR. (hc) dr. M.K Tadjudin Sp.And, selaku Dekan Fakultas
Kedokteran dan Ilmu Kesehatan UIN Syarif Hidayatullah Jakarta.
3. Bapak Drs.Umar Mansur selaku Ketua Jurusan Program Studi Farmasi
Fakultas Kedokteran dan Ilmu Kesehatan UIN Syarif Hidayatullah Jakarta.
4. Bapak dan Ibu staf pengajar dan karyawan yang telah memberikan
bimbingan dan bantuan selama saya menempuh pendidikan di Program
Studi Farmasi Fakultas Kedokteran dan Ilmu Kesehatan Universitar Islam
Negeri Syarif Hidayatullah Jakarta.
5. Kedua orang tua saya, ayahanda Purdjiman, SE panutan dalam keluarga
Nana Rohana, yang selalu memberikan doa, nasihat dan motivasi, hingga
selesainya skripsi ini.
6. Bapak H. M. Riko Rohim, Pak Purwo Priyanto yang selalu memberikan
doa, ilmu Allah SWT yang luar biasa dan energi positif pada penulis.
7. Untuk teman-teman Farmasi 2009 dan teman “GK” Nida Ghania Lidinilla,
Arestya Otary, Umu Aiman, Nda, Qory, Liza, Widya, Agung, Isti, Andy,
Ema yang selalu memberikan semangat kebersamaan dan bantuan kepada
penulis.
8. Untuk kakak senior Farmasi 2008 khususnya Endah Purnamasari yang
telah membantu penulis dalam memberikan pengarahan dan nasehat.
9. Dan kepada seluruh pihak yang telah membantu penulis selama
penyusunan skripsi ini yang tidak dapat disebutkan namanya satu persatu.
Saya menyadari sepenuhnya bahwa skripsi ini masih banyak
kekurangan dan jauh dari kesempurnaan. Oleh Karena itu, dengan segala
kerendahan hati, saya sangat mengharapkan kritik dan saran yang
membangun demi kesempurnaan skripsi ini.
Saya berharap semoga skripsi ini bermanfaat dan dapat member
sumbangan pengetahuan khususnya di Program Studi Farmasi Fakultas
Kedokteran dan Ilmu kesehatan, Universtas Islam Negeri Syarif
Hidayatullah Jakarta dan pembaca pada umumnya.
Wassalamu’alaikum Wr. Wb
Jakarta, 22 Januari 2014
Halaman
HALAMAN JUDUL ... ii
HALAMAN PERNYATAAN ORISINALITAS ... iii
HALAMAN PERSETUJUAN PEMBIMBING ... iv
HALAMAN PENGESAHAN ... v
ABSTRAK ... vi
ABTRACT ... vii
KATA PENGANTAR ... viii
HALAMAN PERSETUJUAN PUBLIKASI KARYA ILMIAH ... x
3.2.1 Alat ... 18
3.2.2 Bahan... 18
3.3 Prosedur Penelitian ... 19
3.3.1 Penyiapan Bahan ... 18
3.3.2 Penapisan Fitokimia ... 19
3.4 Uji Aktivitas Antiinflamasi ... 21
3.4.1 Pengelompokan Hewan Uji ... 21
3.4.2 Penyiapan Hewan Uji ... 21
3.5 Perencanaan Dosis dan Pembuatan Sediaan ... 21
3.5.1 Perhitungan Dosis ... 21
3.5.2 Pembuatan Asetosal... 22
3.5.4 Pembuatan Karagenan 1%... 22
3.5.4 Pembuatan Sediaan Ekstrak... 22
3.6 Prosedur Kerja Antiinflamasi... 23
3.6.1 Analisa Data... 24
BAB 4 HASIL PENELITIAN DAN PEMBAHASAN ... 25
4.1 Hasil Penelitian ... 25
4.1.1 Determinasi Tanaman ... 25
4.1.2 Pembuatan Ekstrak ... 25
4.1.3 Penapisan Fitokimia ... 26
4.1.4 Uji Antiinflamasi ... 27
4.1.5 Hasil Uji Antiinflamasi ... 29
BAB 5 KESIMPULAN DAN SARAN ... 37
5.1 Kesimpulan ... 37
5.2 Saran ... 37
DAFTAR PUSTAKA ... 38
Halaman
Tabel 3.1 Pembagian Kelompok Dosis ... 22
Tabel 4.1 Karakteristik Ekstrak ... 27
Tabel 4.2 Hasil Penapisan Fitokimia ... 28
Tabel 4.3 Rata-rata Volume Udem Kaki Tikus ... 30
Tabel 4.4 Rata-rata Persen Volume Udem Kaki Tikus ... 32
Halaman
Gambar 2.1 Gambar Struktur Asetosal ... 17
Gambar 4.2 Grafik Hubungan Rata-rata Volume Udem ... 31
Gambar 4.3 Grafik Hubungan Rata-rata Persen Udem... 32
Halaman
1. Tanaman Lumut Hati Mastigophora diclados ... 43
2. Determinasi tanaman lumut hati Mastigophora diclados ... 44
3. Hasil Penapisan Fitokimia ... 45
4. Perlakuan Pada Tikus Galur Sprague Dawley ... 47
5. Parameter Ekstrak ... 49
6. Rumus Perhitungan Dosis Hewan ... 50
7. Perhitungan Dosis Asam Asetil Salisilat (Asetosal) ... 51
8. Perhitungan Dosis Tikus ... 52
9. Hasil Volume Udem Telapak Kaki Tikus ... 53
10.Hasil Persen Udem Telapak Kaki Tikus ... 54
11.Hasil Persen inhibisi udem telapak kaki tikus... 55
12.Perhitungan Persen Udem dan Inhibisi Telapak Kaki Tikus ... 56
13.Aklimatisasi Hewan Uji Antiinflamasi ... 59
14.Alur Penelitian ... 60
15.Skema Kerja Ekstrak Kental Mastigophora diclados ... 61
16.Skema Kerja Uji Antiinflamasi ... 62
17.Analisis Data Statistik Uji Efek Antiinflamasi ... 63
1.1 Latar Belakang
Inflamasi adalah respon biologis dari jaringan vaskuler atas adanya
bahaya, seperti pathogen, kerusakan sel, atau iritasi. Ini adalah usaha perlindungan
diri organisme untuk menghilangkan rangsangan penyebab luka dan inisiasi
proses penyembuhan jaringan. Jika inflamasi tidak ada maka luka dan infeksi
tidak akan sembuh dan akan menggalami kerusakan yang lebih parah.
Inflamasi yang tidak terkontrol juga dapat menyebabkan penyakit, seperti
demam, atherosclerosis, dan reumathoid arthritis (Gard, 2001).
Saat ini ada bermacam-macam obat yang digunakan untuk mengatasi
peradangan. Antiinflamasi golongan steroid misalnya dapat menyebabkan
penurunan imunitas terhadap infeksi, osteoporosis, atropi otot dan jaringan
lemak, meningkatkan tekanan intra okular, serta bersifat diabetik. Sedangkan
pada gangguan fungsi ginjal, tukak lambung hingga perdarahan,
hipersensitivitas, bronkospasme merupakan efek samping dari obat antiinflamasi
golongan non steroid (Fajriani, 2005).
Tumbuhan herbal dapat menjadi salah satu sumber bahan obat alami yang
berasal dari senyawa kimia yang terkandung dalam tumbuhan. Senyawa kimia
yang berkhasiat sebagai obat tersebut merupakan hasil dari metabolisme sekunder,
seperti senyawa golongan terpen, alkaloid, fenol, poliketida, dan flavonoid
berserta turunannya (Solikin, 2007).
Lumut merupakan tumbuhan tingkat rendah yang termasuk ke dalam
divisi bryophyta. Pada umumnya tumbuhan lumut menyukai tempat-tempat
yang basah dan lembab didataran rendah sampai dataran tinggi. Tumbuhan
ini sering disebut sebagai tumbuhan pioneer atau tumbuhan perintis, karena
lumut dapat tumbuh dengan berbagai kondisi pertumbuhan dimana tumbuhan
tingkat tinggi tidak bisa tumbuh (Immanudin, 2006).
Lumut hati dibedakan dari kelas-kelas tumbuhan lumut lainnya karena
adanya minyak tubuh yang mampu mensintesis senyawa yang larut lemak
tidak. Lumut hati memiliki badan minyak (oil bodies) sebagai penanda yang
sangat penting untuk klasifikasi lumut hati tersebut. Beberapa kandungan
kimia dari lumut hati merupakan senyawa yang khas bagi kelas ini dan
menunjukkan berbagai aktivitas biologis yang menarik, seperti antimikroba,
sitotoksik, antioksidan dan sejumlah enzim yang bekerja sebagai inhibitor
serta memiliki aktivitas yang merangsang apoptosis (Komala, 2010).
Di Indonesia Mastigophora diclados banyak ditemukan di dataran
tinggi yang sejuk dan lembab seperti di hutan Gunung Slamet, Baturraden
Jawa Tengah Purwokerto Mastigophora hidup menempel pada batang pinus
dan agathis pada ketinggian 800 m blok 55. di hutan pegunungan Taman
Nasional Lore Lindu Sulawesi Tengah Mastigophora diclados hidup
diketinggian tinggi, Pada batang pohon palm sepanjang jalan menuju kawah
putih pada ketinggian 2050 m Gunung Patuha Bandung Jawa Barat (Haerida &
Gradstein, 2011 ; Gradstein &Culmsee, 2010).
Pada penelitian sebelumnya, Komala, et al (2010) telah melaporkan
bahwa tumbuhan lumut Mastigophora diclados yang tumbuh di Tahiti
mengandung senyawa-senyawa fenolik seskuiterpenoid herbertan.
Senyawa-senyawa golongan fenolik seskuiterpenoid herbertan dilaporkan memiliki
aktivitas sitotoksik, antioksidan, dan antimikrobial. Antioksidan dapat bekerja
menghambat radikal bebas yang diketahui sebagai mediator dari berbagai
penyakit antara lain karsinogenesis, jantung koroner, inflamasi, artitis, diabetes
dan penuaan (Ali et al, 2011).
Dari hasil penelitian lumut Mastigophora diclados dari Tahiti yang
menghasilkan aktivitas antioksidan maka lumut hati Mastigophora diclados
dimungkinkan memiliki aktivitas antiinflamasi, maka penelitian dilanjutkan
dengan mengamati aktivitas antiinflamasi pada lumut Mastigophora diclados
dengan pelarut etanol yang terdapat di Indonesia. Dari penelitian tersebut
diketahui bahwa Mastigophora diclados yang mengandung senyawa terpenoid,
fenolik, dan saponin yang ternyata memiliki aktivitas antiinflamasi (Purnamasari,
2013).
Berdasarkan penelitian terbaru yang dilakukan tersebut, maka perlu
Indonesia terhadap aktivitas antiinflamasi dengan metode ekstraksi bertingkat
yaitu dengan pelarut n-heksan, etil asetat, dan metanol. Pada penelitian ini akan
dilakukkan uji antiinflamasi dari ekstrak senyawa non polar yang terdapat dalam
pelarut n-heksan dari lumut hati Mastigophora diclados.
1.2 Rumusan Masalah
Apakah ekstrak n-heksan dari lumut Mastigophora diclados dapat
memberikan efek antiinflamasi pada tikus putih
1.3 Tujuan Penelitian
Untuk menguji aktivitas antiinflamasi dari ekstrak n-heksan lumut
Mastigophora diclados melalui penggukuran volume udem pada telapak kaki
tikus putih jantan Sprague Dawley secara in vivo.
1.4 Manfaat Penelitian
Penelitian ini diharapkan dapat memberikan informasi tentang
aktivitas lumut hati Mastigophora diclados, yang dapat digunakan sebagai
antiinflamasi sehingga dapat dijadikan salah satu alternatif pengobatan
2.1 Tanaman Lumut Hati (Mastigophora diclados)
2.1.1 Klasifikasi Tanaman
Klasifikasi Tanaman Mastigophora diclados adalah sebagai berikut:
Kingdom : Plantae
Phylum : Marchantiophyta
Class : Jungermanniopsida
Order : Jungermanniales
Suborder : Lophocoleineae
Family : Mastigophoraceae
Genus : Mastigophora Nees.
Species : M. diclados (Brid.) Nees
(Crandall-Stotler B; Stotler RE; Long DG, 2008)
2.1.2 Kandungan Kimia Mastigophora diclados
Berdasarkan kandungan kimianya, Mastigophoraceae dan herbertaceae
memiliki kesamaan, karena sama-sama menghasilkan senyawa seskuiterpenoid
herbertan sebagai komponen utamanya (Asakawa, 1995; 2004; Harinantenaina &
Asakawa, 2007).
Dari pemeriksaan GC / MS ekstrak eter M. diclados (Brid. Ex F. Weber)
dari borneo menunjukkan adanya senyawa herbertene, herbertenol,
herbertene-2,3-diol dan herbertene-1 ,2-diol. Dalam koleksi sebelumnya dari M. diclados
Malaysia Timur, selain herbertanes, herbertane dimer, juga ditemukan pada
Mastigophorenes A-D (Asakawa et al, 1991.). Namun, menurut Leong &
Harrison, 1997 spesies di Malaysia Barat tidak menghasilkan herbertanes,
melainkan jenis trachylobane diterpenoids dari hasil diisolasi.
Koleksi Jepang menjabarkan herbertene dan α-herbertenol dengan siklik
diklorinasi bis-bibenzyls, dimana tidak ada diterpenoids dan dimer herbertane
Data ini menunjukan bahwa setidaknya ada tiga ras geografis
Mastigophora diclados di Asia: tipe bis-bibenzyl di Jepang, jenis Mastigophorene
di borneo (Malaysia Timur), dan jenis pimarane serta turunan pimarane
trachylobane diterpenoid di Taiwan dan Malaysia Barat (Harinantenaina &
Asakawa, 2004) ( Agnieszka & Asakawa, 2010).
2.1.3 Aktivitas Biologi
Aktivitas yang dimiliki Mastigophora diclados adalah aktivitas sitotoksik
terhadap HL-60 dan sel KB, aktivitas antimikrobial, dan aktivitas antioksidan
(Komala, 2010 ; Komala, et al., 2010).
2.1.4 Habitat
Lumut Mastigophora diclados dapat tumbuh pada batang pohon pinus dan
agathis, batu-batuan, dan dinding lereng gunung (Ida Haerida, et al, 2011).
2.2. Simplisia
Simplisia adalah bahan alam yang digunakan sebagai bahan obat dan
belum mengalami pengolahan apapun juga, dan kecuali dinyatakan lain, berupa
bahan yang telah dikeringkan. Simplisia dapat berupa simplisia nabati, simplisia
hewani dan simplisia pelikan atau mineral (Depkes RI, 1979).
Simplisia nabati adalah simplisia yang berupa tumbuhan utuh, bagian
tumbuhan atau eksudat tumbuhan. Eksudat tumbuhan ialah isi sel yang secara
spontan keluar dari tumbuhan atau isi sel yang dengan cara tertentu dipisahkan
dari tumbuhannya dan belum berupa senyawa kimia murni (Depkes RI, 2000).
Simplisia Hewani adalah simplisia yang berupa hewan utuh, bagian dari
hewan atau zat-zat yang berguna yang dihasilkan oleh hewan dan belum berupa
zat kimia murni (Depkes RI, 1979).
Simplisia pelikan atau mineral adalah simplisia yang berupa bahan pelikan
atau mineral yang belum diolah atau telah diolah dengan cara sederhana dan
2.3. Ekstrak dan Ekstrasi
2.3.1 Pengertian Ekstrak dan Ekstraksi
Ekstrak adalah sediaan kering, kental atau cair, dibuat dengan menyari
simplisia nabati atau hewani menurut cara yang cocok, di luar pengaruh cahaya
matahari langsung. Ekstrak kering harus mudah digerus menjadi serbuk (Depkes
RI, 1979).
Faktor yang mempengaruhi ekstrak yaitu faktor biologi dan faktor kimia.
Adapun faktor biologi meliputi: spesies tumbuhan, lokasi tumbuh, waktu
pemanenan, penyimpanan bahan tumbuhan, umur tumbuhan dan bagian yang
digunakan. Sedangkan faktor kimia meliputi beberapa hal, yaitu: faktor internal
(Jenis senyawa aktif dalam bahan, komposisi kualitatif senyawa aktif, komposisi
kuantitatif senyawa aktif, kadar total rata-rata senyawa aktif) dan faktor eksternal
(metode ekstraksi, perbandingan ukuran alat ekstraksi, ukuran, kekerasan dan
kekeringan bahan, pelarut yang digunakan dalam ekstraksi, kandungan logam
berat, kandungan peptisida) ( Depkes RI, 2000).
Ekstraksi adalah penarikan zat pokok yang diinginkan dari bahan mentah
obat dengan menggunakan pelarut yang dipilih dimana zat yang diinginkan larut.
Simplisia yang akan diekstrak mengandung senyawa aktif yag dapat larut dan
senyawa aktif yang dapat larut dan senyawa yang tidak dapat larut. Struktur kimia
yang berbeda-beda akan mempengaruhi kelarutan serta stabilitas
senyawa-senyawa tersebut terhadap suhu, udara, cahaya, dan logam berat. Simplisia yang
lunak seperti rimpang, akar dan daun mudah diserap oleh pelarut, sehingga pada
proses ekstraksi tidak perlu diserbuk sampai halus. Sedangkan simplisia yang
keras seperti biji, kulit kayu, dan kulit akar susah diserap oleh pelarut, karena itu
perlu diserbuk sampai halus. Selain sifat fisik dan senyawa aktif dari simplisia,
senyawa-senyawa yang terdapat dalam simplisia seperti protein, karbohidrat,
lemak dan gula juga harus diperhatikan. Dengan diketahuinya akan
mempermudah pemilihan pelarut dan cara ekstraksi yang tepat. (Depkes, 2000).
Sistem pelarut yang digunakan dalam ekstraksi harus dipilih berdasarkan
kemampuannya dalam melarutkan jumlah maksimum dari zat aktif dan
Metode dasar ekstraksi adalah maserasi, perkolasi, dan sokletasi. Pemilihan
terhadap ketiga metode diatas disesuaikan dengan kepentingan dalam memperoleh
sari (Harborne, 1987).
2.3.2 Proses Pembuatan Ekstrak
Pembuatan ekstrak dapat dilakukkan melalui langkah-langkah sebagai
berikut:
a. Pembuatan Serbuk Simplisia
Zat aktif semula berada di dalam sel akan ditarik oleh cairan penyari
sehingga terjadi larutan zat aktif dalam cairan penyari tersebut. Pada
umumnya penyarian akan bertambah baik bila permukaan serbuk simplisia
yang bersentuhan dengan cairan penyari makin luas. Dengan demikian maka
makin halus serbuk simplisia seharusnya makin baik penyariannya. Tetapi
dalam pelaksanaannya tergantung pada sifar fisik dan sifat kimia simplisia
yang bersangkutan, serbuk yang terlalu halus membentuk suspensi yang sulit
dipisahkan dengan penyarian serta serbuk yang terlalu halus menyebabkan
banyak dinding sel yang pecah, sehingga zat yang tidak diinginkan pun ikut
ke dalam hasil penyarian (Depkes, 2000).
b. Pembasahan
Pembasahan serbuk dilakukan pada penyarian. Dimaksudkan memberikan
kesempatan sebesar-besarnya kepada cairan penyari memasuki pori-pori
dalam simplisia sehingga mempermudah penyarian selanjutnya (Depkes,
2000).
c. Penyari/Pelarut
Cairan peyari yang digunakan dalam proses pembuatan ekstrak adalah
penyari yang baik untuk senyawa kandungan yang berkhasiat atau aktif.
Penyari tersebut harus dapat dipisahkan dari bahan dan sari senyawa
kandungan lainnya, serta ekstrak hanya mengandung sebagian besar senyawa
kandungan yang diinginkan. Faktot utama yang menjadi pertimbangan dalam
pemilihan penyari adalah selektifitas, ekonomis, dan kemudahan bekerja
d. Pemisahan dan Pemurnian
Tujuan dari tahap ini adalah untuk menghilangkan (memisahkan) senyawa
yang tidak dikehendaki semaksimal mungkin tanpa berpengaruh pada
senyawa kandungan yang dikehendaki, sehingga diperoleh ekstrak yang lebih
murni. Proses-proses pada tahap ini adalah pengendapan, pemisahan dua
cairan tak campur, sentrifugasi, dekantasi, filtrasi, serta proses absorbsi, dan
penukaran ion (Depkes, 2000).
e. Pemekatan/Penguapan
Pemekatan berarti peningkatan jumlah partikel solute (senyawa terlarut)
dengan cara penguapan pelarut tanpa sampai menjadi kering tetapi ekstrak
hanya menjadi kental/pekat (Depkes, 2000).
f. Pengeringan Ekstrak
Pengeringan berarti menghilangkan pelarut dari bahan sehingga
menghasilkan serbuk, masa kering-rapuh, tergantung proses dan peralatan
yang digunakan, ada berbagai proses pengeringan ekstrak, yaitu dengan cara
pengeringan evaporasi, vaporasi, sublimasi, konveksi, kontak, radiasi,
dielektrik (Depkes, 2000).
g. Rendemen
Rendemen adalah perbandingan antara ekstrak yang diperoleh dengan
simplisia awal (Depkes, 2000).
2.3.3 Metode Ekstraksi
Metode ekstraksi dengan mengguakan pelarut terdiri dari dua cara yaitu
dengan cara dingin dan cara panas.
a. Cara Dingin
1. Maserasi
Maserasi adalah proses pengekstrakan simplisia dengan
menggunakan pelarut dengan beberapa kali pengocokan atau
pengadukan pada temperatur ruangan (kamar). Cairan penyari akan
menembus dinding sel dan masuk ke dalam rongga sel yang
mengandung zat aktif yang akan larut, karena adanya perbedaan
larutan terpekat didesak keluar. Proses ini berulang sehingga terjadi
keseimbangan konsentrasi antara larutan didalam dan diluar sel.
Remaserasi berarti dilakukan pengulangan penambahan pelarut
setelah dilakukan penyarian maserat pertama dan seterusnya
(Depkes, 2000).
2. Perkolasi
Perkolasi adalah ekstraksi dengan pelarut yang selalu baru
sampai sempurna yang umumnya dilakukan pada temperatur
ruangan. Proses terdiri dari tahapan pengembangan, tahap maserasi
antara, tahap perkolasi sebenarnya terus-menerus sampai diperoleh
ekstrak (perkolat) yang jumlahnya 1-5 kali bahan (Depkes, 2000).
b. Cara Panas
1. Refluks
Refluks adalah ekstraksi dengan pelarut pada temperatur titik
didihnya, selama waktu tertentu dan jumlah pelarut terbatas yang
relatif konstan dengan adanya pendingin balik. Umumnya
dilakukkan pengulangan proses pada residu pertama 3-5 kali
sehingga dapat termasuk pada proses ekstraksi sempurna (Depkes,
2000)
2. Sokletasi
Sokletasi adalah ekstraksi dengan menggunakan pelarut
yang selalu baru dan yang umumnya dilakukan dengan alat khusus
sehingga terjadi ekstrak kontinu dengan jumlah pelarut relatif
konstan dengan adanya pendingin balik (Depkes, 2000).
3. Digesti
Digesti adalah maserasi kinetik (dengan pengadukan
kontinu) pada temperatur yang lebih tinggi dari temperatur ruangan,
yaitu secara umum dilakukan pada temperatur 40-50 0C (Depkes,
2000).
4. Infundasi
Infundasi adalah proses penyarian yang umumnya
dari bahan-bahan nabati. Proses ini dilakukan pada suhu 90 0C
uap air berdasarkan peristiwa tekanan parsial senyawa kandungan
menguap dengan fase air dan kentel secara kontinu sampai sempurna
dan diakhiri dengan kondensasi fase uap campuran (senyawa
kandungan menguap ikut Terdestilasi) menjadi destilasi air bersama
senyawa kandungan yang memisah yang memisah sempurna atau
memisah sebagian (Depkes, 2000).
2.3.4 Parameter Ekstrak
1. Parameter Non spesifik Ekstrak ( Depkes RI, 2000).
a. Kadar Air
Kadar air adalah pengukuran kandungan air yang berada di
dalam bahan. Tujuannya adalah memberikan batasan maksimal
(rentang) tentang besarnya kandungan air di dalam bahan. Nilai
untuk kadar air sesuai dengan yang tertera dalam monografi
(Depkes, 2000).
b. Kadar Abu
Untuk penentuan kadar abu, bahan yang dipanaskan pada
temperatur dimana senyawa organik dan turunannya terdestruksi dan
menguap sehingga hanya tersisa unsur mineral dan anorganik.
Tujuannya adalah untuk memberikan gambaran tentang kandungan
mineral internal dan eksternal yang berasal dari proses awal sampai
terbenttuknya ekstrak. Nilai untuk kadar abu sesuai dengan yang
1. Parameter Spesifik
Parameter spesifik dilakukan dengan uji parameter organoleptik
ekstrak dengan menggunakan pancaindera mendeskripsikan bentuk,
warna, bau dan rasa.
2.4 Freeze Drying
Freeze drying atau pengeringan beku merupakan proses pengeringan yang
pelarut atau media suspensinya dikristalkan dengan suhu rendah dan selanjutnya
tersublimasi dari padatan menjadi ke fase uap. Pengeringan beku lebih sering
menggunakan air sebagai pelarutnya. Pengeringan mengubah es atau air dalam
fase amorf menjadi uap. Langkah ini relatif lebih mudah untuk prose pemurnian.
Jika didalam produk mengandung dua komponen atau lebih suspensi. Proses
tersebut bisa terjadi sehingga perlu disederhanakan dalam model pembuatanya
agar lebih mudah dan dimengerti. Pengeringan mengubah es atau air dalam fasa
amorf menjadi uap. Hal tersebut dapat terjadi karena tenakan uap es yang rendah,
volume uap menjadi besar. Pengeringan bertujuan untuk menghasilkan subtansi
dengan stabilitas yang baik dan yang tidak berubah setelah rekonstitusi dengan
air, meskipun hal ini tergantung sangat tergantung juga pada langkah terakhir
yaitu prose pengemasan dan kondisi penyimpanan.
Dalam pengeringan beku memiliki beberapa keuntungan diantaranya:
a. pengeringan pada suhu rendah dapat mengurangi produk sensitif-panas.
b. Produk cair dapat secara akurat terdosiskan.
c. Kadar air dari produk akhir dapat dikontrol selama proses.
d. Produk kering dapat memiliki bentuk fisik yang menarik.
e. Produk obat dengan luas permukaan spesifik yang tinggi dengan cepat
dibentuk kembali (Oetjen & Haseley, 2004).
2.5 Inflamasi
2.5.1 Definisi Inflamasi
Inflamasi merupakan respon kompleks dalam jaringan vaskular yang
terjadi akibat adanya rangsangan eksogen dan endogen. Peradangan adalah respon
bahaya bahan kimia atau mikrobiologis yang merupakan pertahanan dari tubuh.
Peradangan terjadi untuk menonaktifkan atau menghancurkan organisme asing,
menghilangkan iritasi merupakan tahap pertama perbaikan jaringan. Proses
inflamasi biasanya dapat sembuh pada proses pengobatan, tetapi dapat juga
menjadi lebih buruk menjadi radang yang parah yang dapat berakibat fatal (Sen et
al, 2010).
Tanda-tanda dari peradangan adalah kemerahan, suhu tubuh meningkat,
bengkak, nyeri, dan hilangnya fungsi. Peradangan dipicu oleh berbagai macam zat
berbahaya, benda asing, racun, infeksi, radang, dingin, bahan kimia, patogen,
antibodi, nekrosis, tumpul, reaksi kekebalan tubuh dan luka fisik. Mediator
inflamasi seperti histamin, serotonin, bradikin, neuropeptida, eikosanoid
(prostaglandin dan leukotrein B4, C4, D4, E4), oksida nitrat, oksidan biologis,
faktor mengaktifkan trombosit, faktor narkosis tumor, metabolit oksigen, protein
komplemen sitokin, faktor adhesi dan pencernaan yang memiliki peranan pentin
dalam patogenesis dari peradangan. Sel-sel seperti neutrofil, eosinofil, monosit,
limfosit, basofil, sel mast, fibroblas, jaringan ikat, makrofag juga terlibat dalam
patogenesis dari peradangan (Sen et al, 2010).
Peradangan atau inflamasi umumnya dibagi menjadi:
- Infalamasi akut : respon awal terhadap cedera jaringan, hal tersebut terjadi
melalui mediator respon inflamasi akut yang terlibat antara lain: histamin,
serotonin, bradikin, prostaglandin, leukotrin, dan pada umumnya didahului
oleh pembentukan respon imun. Respon imun terjadi ketikas sel yang
kompeten secara imunologis menjadi aktif sebagai respon terhadap organisme
atau zat antigenik asing yang dibebaskan selama respon peradangan akut atau
kronik. Dilain pihak, hasil akhir respon imun dapat bersifat merugikan jika
menyebabkan peradangan kronik, tanpa adanya resolusi dari poses cedera
yang mendasari.
- Inflamasi kronis melibatkan pelepasan sejumlah mediator yang tidak terlihat
jelas pada respon akut. Salah satu keadaan yang paling penting yang
meibatkan mediator-mediator ini adalah arthitis reumatoid; pada keadaan ini
tulang kartilago yang dapat menimbulkan cacat berat dan terjasi perubahan
sistemik yang dapat mengakibatkan pemendekan usia hidup (Katzung, 2010).
2.5.2 Mekanisme Inflamasi
Inflamasi terjadi dengan diawali adanya stimulus yang merusak jaringan,
mengakibatkan sel mast pecah dan terlepasnya mediator-mediator inflamasi.
Kemudian terjadi vasodilatasi dari seluruh pembuluh darah pada daerah inflamasi
sehingga aliran darah meningkat. Perubahan volume darah dalam kapiler dan
venula, yang menyebabkan sel-sel endotel pembuluh darah meregang dan
kemudian meningkatkan permeabilitas pembuluh darah, protein plasma keluar
dari pembuluh darah lalu menimbulkan edema. Infiltrasi leukosit ke tempat
inflamasi, pada tingkat awal infiltrasi oleh neutrofil, selanjutnya infiltrasi oleh sel
monosit. Sel monosit akan berubah menjadi makrofag. Baik neutrofil maupun
mkrofag dapat melepaskan enzim lisosom unttuk membantu mencerna eksudat
radang. Bila tidak terjadi resolusi, maka dapat meningkat menjadi inflamasi
kronik (Underwood, 1999).
2.5.3 Obat Inflamasi
1. Obat Antiinflamasi Golongan Non Steroid (AINS)
Obat golongan AINS yang mempunyai khasiat sebagai analgetik,
antipiretik, serta antiinflamasi merupakan suatu kelompok obat yang
heterogen, bahkan beberapa obat sangat berbeda secara kimia.
Walaupun demikian, obat-obat ini memiliki banyak persamaan dalam
efek terapi maupun efek samping berdasarkan mekanisme kerjanya,
yaitu menghambat biosintesis prostaglandin (Wilmana, 2007).
AINS mengambat siklooksigenase (COX) sehingga konversi asam
arakidonat menjadi prostaglandin, prostasiklin, dan tromboksan yang
berperan dalam menimbulkan reaksi peradangan terganggu. Tetapi
antiinflamasi nonsteroid tidak menghambat biosintesis leukotrein yang
diketahui ikut berperan dalam proses inflamasi. Obat anti infalamasi
non steroid adalah indometasin, Na. Diklofenak, Fenilbutazon dan
2. Obat Antiinflamasi Golongan Steroid
Golongan obat anti antiinflamasi golongan steroida
(glukokortikoid) berhubungan dengan kemampuannya untuk
merangsang biosintesis protein lipomodulin yang dapat menghambat
kerja enzimatik fosfolipase, suatu enzim yang bertanggung jawab
terhadap pelepasan asam arakhidonat dan metabolitnya seperti
prostaglandin, leukotrin, prostasiklin, dan tromboksan. Gukokortikoid
dapat memblok jalur siklooksigenase dan lipoksigenase. Obat-obatan
golongan steroida adalah prednisolon, betametason, triamsolon,
hidrokortison dan sebagainya (Katzung, 2010).
2.5.4 Beberapa Metode Uji Antiinflamasi 1. Metode Pembentukan Edema Buatan
Salah satu teknik yang paling umum digunakan berdasarkan
kemampuan agen tersebut untuk menghambat produksi edema di kaki
belakang tikus setelah injeksi agen radang yang kemudian diukur
volume radang. Volume edema diukur sebelum dan sesudah pemberian
zat yang diuji. Beberapa iritan yang dipakai sebagai penginduksi
edema antara lain formalin, kaolin, ragi, dan dekstran. Iritan yang
umum digunakan dan memiliki kepekaan yang tinggi adalah karagen
(Vogel, 2002).
2. Metode Pembentukan Eritema
Metode ini berdasarkan pengamatan secara visual terhadap eritema
pada kulit hewan yang telah dicukur bulunya. Marmot secara kimiawi
dihilangkan bulunya dengan suspense barium sulfat, 20 menit
kemudian dibersihkan dengan air hangat. Hari esoknya senyawa uji
disuspensikan dan setengah dosisnya diberikan 30 menit sebelum
pemaparan UV. Setengahnya lagi setelah 2 menit berjalan pemaparan
UV. Eritema dibentuk akibat iritasi sinar UV berjarak 20 cm diatas
3. Metode Iritasi dengan Panas
Metode ini berdasarkan pengukuran luas radang dan berat edema
yang terbentuk setelah diiritasi dengan panas. Mula-mula hewan diberi
zat warna tripan biru yang disuntik secara IV, dimana zat ini akan
berikatan dengan albumin plasma. Kemudian pada daerah penyuntikan
tersebut dirangsang dengan panas yang cukup tinggi. Panas
menyebabkan pembebasan histamine endrogen sehingga timbul
inflamasi. Zat warna akan keluar dari pembuluh darah yang mengalami
dilatasi bersama-sama dengan albumin plasma sehingga jaringan yang
meradang kelihatan berwarna. Penilaian derajat inflamasi diketahui
dengan mengukur luas radang akibat perembesan zat ke jaringan yang
meradang. Pengukuran juga dapat dilakukan dengan menimbang edema
yang terbentuk, dimana jaringan yang meradang dipotong kemudian
ditimbang (Vogel, 2002).
4. Metode Pembentukan Kantong Granuloma
Metode ini berdasarkan pengukuran volume eksudat yang
terbentuk di dalam kantong granuloma. Mula-mula benda terbentuk
pellet yang terbuat dari kapas yang ditanam di bawah kulit abdomen
tikus menembus lapisan linia alba. Respon yang terjadi berupa gejala
iritasi, migrasi leukosit dan makrofag ke tempat radang yang
mengakibatkan kerusakan jaringan dan timbul granuloma (Vogel,
2002).
5. Metode Iritasi Pleura
Metode ini berdasarkan pengukuran volume eksudat yang
terbentuk karena iritasi dengan inductor radang. Adanya aktivitas obat
yang diuji ditandai dengan berkurangnya volume eksudat. Obat
diberikan secara oral. Satu jam kemudian disuntik dengan inductor
radang seperti formalin secara intra pleura. Setelah 24 jam, hewan
dibunuh dengan eter lalu rongga pleura dibuka dan volume eksudat
6. Metode Induksi Oxazolon Edema Telinga Mencit.
Pada percobaan ini tikus telinga tikus diinduksi 0.01 ml 2% larutan
oxazolon ke dalam telinga kanan. Inflamasi terjadi dalam 24 jam.
Kemudian hewan dikorbankan dibawah anastesi lalu dibuat preparat
dengan 8 mm dan perbedaan berat preparat menjadi indicator inflamasi
udem (Vogel, 2002).
2.6 Karagenan
Karagenan dikenal juga dengan nama carragenan, carragenin,
carraghenates, chondrus extrax dan irish moss extrak. (Sweetman, 2009).
Karagenan merupakan polisakarida hasil ekstraksi rumput laut dari family
Euchema, Chondrus, dan Gigartina. Bentuknya berupa serbuk berwarna putih
hingga kuning kecokelatan, ada yang berbentuk butiran kasar hingga serbuk halus,
tidak berbau, serta memberi rasa berlendir di lidah. Berdasarkan kandungan sulfat
dan potensi pembentukan gelnya, karagenan dapat dibagi menjadi tiga jenis, yaitu
lamda karagenan, Iota karagenan, dan Kappa karagenan. Ketiga karagenan ini
memiliki sifat larut dalam air bersuhu 80 OC (Rowe et al, 2009).
Penggunaan karagenan sebagai penginduksi radang memiliki beberapa
keuntungan antara lain: tidak meninggalkan bekas, tidak menimbulkan kerusakan
jaringan dan memberikan respon yang lebih peka terhadap obat antiinflamasi
dibanding senyawa iritan lainnya (Siswanto dan Nurulita, 2005).
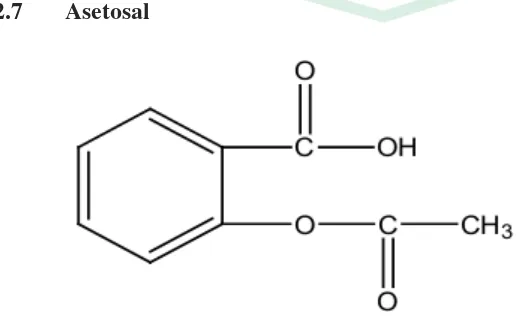
2.7 Asetosal
Rumus molekul : C9H8O4
Nama kimia : Asam Asetil Salisilat
Beratmolekul : 180,16
Pemerian : Hablur, tidak berwarna, atau serbuk hablur putih;
tidak berbau atau hampir tidak berbau; rasa asam.
Kelarutan : Agak sukar larut dalam air, mudah larut dalam
etanol, larut dalam kloroform, dan dalam eter
(Farmakope Indonesia, 1979).
Asam asetil salisilat yang lebih dikenal sebagai asetosal atau aspirin
merupakan salah satu senyawa yang secara luas digunakan, aspirin
digunakan sebagai obat analgetik, antipiretik, dan antiinflamasi yang
sangat luas digunakan (Wilmana,1995).
2.7.1 Mekanisme Kerja Asam Asetil Salisilat
Asam asetil salisilat bekerja menghambat enzim siklooksigenase secara
ireversibel (prostagladin sintetase), yang mengkatalisis perubahan asam
arakidonat menjadi senyawa endoperoksida ; pada dosis yang tepat obat ini akan
menurunkan pembentukan prostagladin maupun tronboksan A2, tetapi tidak
leukotrien (Gunawan, 2008 ; Katzung, 1998).
2.7.2 Efek Samping Asam Asetil Salisilat
Terjadi gangguan pada lambung (gastritis), pendarahan saluran cerna,
muntah, tinusitus, penurunan pendengaran, vertigo, meningkatkan kadar asam urat
3.1 Tempat dan Waktu Penelitian
Penelitian ini dilakukan di Laboratorium Farmakognosi dan Fitokimia,
Laboratorium Hewan (Animal house), dan Labolatorium Kimia Obat Fakultas
Kedokteran dan Ilmu Kesehatan Universitas Islam Negeri Syarif Hidayatullah
Jakarta. Mulai dari bulan April sampai Juli 2013.
3.2 Alat dan Bahan Penelitian 3.2.1 Alat
Peralatan yang digunakan dalam penelitian ini adalah : Neraca analitik
(wiggen hauser), blender, vacuum rotary evaporator, spatel, erlenmeyer, gelas
ukur, gelas becker, tabung reaksi, batang pengaduk, spatula, kaca arloji, pipet
tetes, almunium foil, lumpang dan satmfer, kertas saring, kapas, tisu gulung, lebel,
spuit injeksi suplantar dan peroral 1 mL dan 3 mL, stopwatch, timbangan hewan,
plestimometer, kandang tikus, sonde, sarung tangan, masker.
3.2.2 Bahan
Ekstrak n-heksan dari lumut hati Mastigophora diclados yang diperoleh
gunung slamet purwokerto. Bahan dalam uji antiinflamasi yaitu: n-heksan
(Bratako), kappa karagenan (Balitro bogor), Natrium Karboksimetilselulosa ( Na
CMC ), Etanol 70%, NaCl Fisiologis 0,9%, air raksa (Hg) (Bratako & Dwinika),
Asam asetil salisilat (Bratako), Aquadest, pereaksi Mayer, pereaksi Dragendroff,
amonia encer, HCl, FeCl3 0,1%, kloroform, H2SO4 1 M, NaOH, pereaksi
Lieberman-Buchard, HCl pekat, Tikus jantan putih galur Sprague Dawley (SD).
3.3 Prosedur Penelitian
3.3.1 Penyiapan Bahan dan Pembuatan Ekstrak Uji
Lumut hati Mastigophora diclaodos terlebih dahulu dipisahkan dari
pengotor yang menempel pada lumut, dan dibersihkan dengan air mengalir hingga
selama 2 hari, setelah benar-benar kering dilakukan kembali sortasi kering untuk
memastikan lumut hati Mastigophora diclados bebas dari pengotor, kemudian
ditimbang dan dihaluskan menggunakan blender hingga menjadi serbuk.
Sampel serbuk Mastigophora diclaodos sebanyak 2103 gram dimasukan
kedalam botol gelap 1 L, diekstraksi dengan metode maserasi bertingkat dengan
menggunakan pelarut non polar, semi polar, dan polar yaitu pelarut n-heksan, etil
asetat dan metanol sampai serbuk terendam oleh pelarut, disimpan di tempat yang
gelap dan sesekali digoyang-goyangkan. Pelarut diganti sampai diperoleh filtrat
yang bening, kemudian filtrat disaring, filtrat yang telah disaring, dipekatkan
menggunakan vacuum rotary evaporator sehingga diperoleh ekstrak kental,
kemudian dihitung hasil % rendemen ekstrak dengan rumus:
3.3.2 Penapisan Fitokimia
Penapisan fitokimia dilakukan dengan menguji adanya golongan senyawa
alkaloid, flavonoid, terpenoid, saponin, tanin dan fenolik. Prosedur pengujiannya
adalah sebagai berikut:
a. Identifikasi Golongan Alkaloid
Untuk mengidentifikasi alkaloid, ekstrak dilarutkan dengan etanol 96%
kemudian ditambahkan asam klorida encer 2N. Filtrat yang diperoleh
disaring kemudian diidentifikasi menggunakan pereaksi Mayer LP,
Bouchardat LP, Dragendorff LP. Pada penambahan Mayer LP, hasil
positif ditandai dengan terbentuknya endapan berwarna putih atau
kuning. Hasil positif Dragendorff LP ditunjukan dengan terbentuknya
endapan berwarna merah bata. Penambahan Bouchardat LP
memberikan hasil positif jika terbentuk endapan coklat sampai hitam
(Ayoola et al, 2008)
b. Identifikasi Golongan Flavonoid
Tiga metode yang digunakan untuk menguji flavonoid. Pertama,
kuning menunjukan adanya flavonoid. Kedua, beberapa tetes larutan
aluminium 1% ditambahkan ke sebagian dari filtrat, terbentuknya
warna kuning menunjukan adanya flavonoid. Ketiga, sebagian dari
ekstrak dipanaskan dengan 10 mL etil asetat yang telah diuapkan
selama 3 menit. Campuran kemudian disaring dan 4 mL filtrat dikocok
dengan penambahan 1 mL larutan amonia encer, terbentuknya warna
kuning menunjukan adanya flavonoid. (Ayoola et al, 2008).
c. Identifikasi Golongan Saponin
Ekstrak ditambahkan 5 ml aquadest panas, didinginkan kemudian
dikocok kuat-kuat selama 10 menit. Hasil positif ditunjukan dengan
terbentuknya buih yang stabil selama tidak kurang dari 10 menit
setinggi 1-10 cm dan pada penambahan 1 tetes asam klorida 2 N buih
tidak hilang (Ayoola et al, 2008).
d. Identifikasi golongan Terpenoid
Sejumlah 0,5 g ekstrak masing-masing ditambahkan dengan 2 mL
kloroform. Kemudian dengan hati-hati ditambahkan (3 mL) H2SO4
pekat sampai membentuk lapisan. Terbentuknya warna merah
kecoklatan pada permukaan menunjukan adanya terpenoid (Ayoola et
al, 2008).
e. Identifikasi Tanin
Sebanyak 0,5 g ekstrak dipanaskan dalam 10 ml air dalam tabung
reaksi dan kemudian disaring. Ditambahkan beberapa tetes FeCl3
0,1% dan diamati perubahan warna menjadi hijau kecoklatan atau biru
kehitaman. (Ayoola et al, 2008).
f. Identifikasi Fenolik
Sejumlah ekstrak ditambahkan 3-4 tetes larutan besi klorida,
terbentuknya warna biru-hitam menunjukan adanya fenolik (Tiwari et
3.4 Uji Aktivitas Antiinflamasi 3.4.1 Pengelompokan Hewan Uji
Jumah tikus yang digunakan sebanyak 30 ekor tikus putih jantan
Sprague Dawley yang dibagi menjadi 5 kelompok, masing- masing terdiri dari
6 ekor tikus.
Tabel 3.1. Pembagian Kelompok Dosis
Kelompok Jumlah tikus Perlakuan
1 6 Kontrol negatif diberikan larutan Na CMC 0,5%
2 6 Kontrol positif, diberikan asetosal 125 mg/KgBB dalam Na CMC 0,5%
3 6 Diberikan sediaan ekstrak n-heksan lumut hati
M.diclados dosis 5 mg/KgBB dalam Na CMC 0,5%
4 6 Diberikan sediaan ekstrak n-heksan lumut hati
M.diclados dosis 10 mg/KgBB dalam Na CMC 0,5%
5 6 Diberikan sediaan ekstrak n-heksan lumut hati
M.diclados dosis 50 mg/KgBB dalam Na CMC 0,5%
3.4.2 Penyiapan Hewan Uji
Hewan uji yang digunakan pada uji antiinflamasi ini adalah tikus jantan
putih strain Sprague Dawley (SD) yang diperoleh dari Model hewan UGM gamavet
yogyakarta yang berumur 2-3 bulan dengan berat badan 200-250 gram. Hewan uji
percobaan diaklimatisasi terlebih dahulu selama 3 minggu agar dapat beradaptasi
dengan lingkungan.
3.5 Perencanaan Dosis dan Pembuatan Sediaan 3.5.1 Perhitungan Dosis Asam asetil salisilat
Dosis lazim asam asetil salisilat untuk manusia adalah 325-650 mg untuk
sekali pakai. Dosis analgetik adalah 500 mg sekali pakai. Dosis asam asetil
Maka dosis untuk antiinflamasi (1000-1500) mg, sehingga dosis yang
dapat diberikan pada tikus (200 g) menggunakan rumus tabel konversi dosis
hewan (Reagan-Shaw, et al., 2007):
Dari hasil perhitungan tersebut, pada penelitian uji aktivitas antiinflamasi ekstrak
n-heksan lumut Mastigophora diclados akan digunakan asetosal dengan dosis 25
mg/200 g atau 125 mg/KgBB.
3.5.2 Pembuatan Suspensi Asam asetil salisilat (Asetosal)
Untuk dosis 125 mg/KgBB
Timbang asam asetil salisilat (asetosal) sebanyak 625 mg, digerus perlahan,
kemudian ditambahkan 5 mL suspensi Na CMC 0,5 % diaduk sampai
homogen di dalam lumpang, kemudian dipindahkan dalam labu ukur 25 mL
kemudian ditambahkan sampai tanda batas pada labu ukur dengan suspensi Na
CMC 0,5 %.
3.5.3 Pembuatan Karagenan 1%
Karagenan ditimbang sebanyak 100 mg kemudian dilarutkan dalam 10 mL
NaCl fisiologis diaduk hingga homogen (Annis Hidayati, 2008).
3.5.4 Pembuatan Sediaan Ekstrak n-heksan lumut Mastigophora diclados
Dosis yang digunakan pada ekstrak n-heksan Mastigophora diclados
adalah 5 mg/KgBB, 10 mg/KgBB, dan 50 mg/KgBB. masing-masing dosis uji
dihitung sesuai dengan berat badan tikus, kemudian ekstrak kental lumut hati
dipindahkan ke dalam lumpang dan ditambahkan dengan suspensi Na CMC 0,5%
aduk hingga homogen. Sediaan diberikan secara oral pada masing-masing tikus.
3.6 Prosedur Pengujian Aktivitas Antiinflamasi Ekstrak n-heksan Pada Lumut M.diclados
1. Tikus dipuasakan kurang lebih selama 18 jam sebelum percobaan dimulai (air minum tetap diberikan).
2. Tikus ditimbang dan dikelompokan secara acak yaitu: kelompok kontrol negatif, kelompok kontrol positif, dan kelompok uji ekstrak
n-heksan lumut hati Mastigophora diclados dengan jumlah tikus
masing-masing kelompok 6 ekor tikus.
3. Kaki belakang tikus yang akan diinduksi, diberi tanda pada mata
kaki tikus dengan menggunakan spidol, agar pemasukan kaki
dalam air raksa setiap kali pengukuran selalu sama. kemudian
volume kaki tikus diukur dengan mencelupkan kaki tikus ke dalam
raksa dan dicatat sebagai volume awal (V0) .
4. Pada kelompok kontrol negatif, setiap tikus diberi Na CMC 0,5% sesuai dengan dosis yang telah dihitung.
5. Pada kelompok kontrol positif, setiap tikus diberi suspensi obat asetosal dalam Na CMC 0,5% sesuai dengan dosis yang telah
dihitung.
6. Pada masing-masing kelompok uji dosis diberi ekstrak n-heksan lumut M. diclados dalam Na CMC 0,5% sesuai dosis yang telah
dihitung secara oral.
7. Setelah 1 jam diberikan sediaan uji, telapak kaki tikus disuntikan dengan larutan karagenan 1 % sebanyak 0,2 mL secara intrakutan.
8. Setelah 1 jam, volume kaki tikus diukur dengan menggunakan alat plestimometer hingga batas mata kaki lalu diukur setiap 1 jam
selama 6 jam pengamatan.
9. Ukur volume udem telapak kaki pada masing-masing telapak tikus. 10.Hitung persentase udem dan persentase inhibisi udem (Rustam et
3.6.1 Analisis Data
Data yang diperoleh dianalisis dengan uji kolmogorov smirnov untuk
melihat distrbusi data dan hasil data dengan uji levene untuk melihat homogenitas
data. Jika data terdistribusi normal dan homogenitas maka dilanjutkan dengan
pengujian uji analisis varian (ANOVA) satu arah dengan taraf kepercayaan 95 %
sehingga dapat diketahui perbedaan yang diperoleh bermakna atau tidak. Jika
terdapat perbedaan bermakna, maka dilanjutkan dengan uji nyata kecil (LSD)
(Satoso, 2008). Jika terdapat perbedaan bermakna, dilanjutkan dengan uji beda
nyata terkecil (LSD) dan setiap kelompok tikus dihitung presentasi penghambatan
udem rata-rata untuk setiap dosis zat uji dengan menggunakan rumus (Rustam et
al, 2010 ; Swathy et al, 2010):
Keterangan:
a = Volume udem kelompok kontrol negatif
b = Volume udem kelompok kelompok hewan uji
Keterangan :
Vt dan Vo adalah Volume udem telapak kaki tikus pada waktu t
4.1 Hasil Penelitian 4.1.1 Determinasi Tanaman
Tanaman lumut hati yang digunakan diperoleh dari Gunung Slamet
Purwokerto. Kemudian dilakukan determinasi di Herbarium Bogoriense, Bidang
Botani Pusat Penelitian Biologi-LIPI Bogor untuk mengetahui kebenaran tanaman
tersebut. Hasil determinasi tanaman lumut hati Mastigophora diclados
menunjukan bahwa tanaman yang digunakan dalam penelitian ini merupakan
tanaman lumut hati spesies Mastighopora diclados (Brid.) Nees.
4.1.2 Pembuatan Ekstrak
Tanaman lumut hati Mastigophora diclados diekstraksi dengan
menggunakan metode maserasi. Metode ini dipilih karena peralatan yang
digunakan sederhana, mudah dan dapat mencegah terjadinya degradasi pada
senyawa yang bersifat termolabil (Sarker, et al, 2006). Proses maserasi dilakukan
dengan menggunakan teknik maserasi bertingkat dengan pelarut yang memiliki
tingkat kepolaran yang berbeda yaitu n-heksan, etil asetat dan metanol. Teknik
maserasi bertingkat ini bertujuan untuk memaksimalkan proses ekstraksi dimana
senyawa akan terekstraksi berdasarkan tingkat kepolarannya.
Lumut hati Mastigophora diclados dibersihkan, kemudian dikeringkan
dengan cara diangin-anginkan, dan dihaluskan dengan menggunakan blender
hingga memperoleh serbuk halus, pembuatan serbuk bertujuan untuk
meningkatkan luas permukaan sampel sehingga diharapkan pelarut lebih mudah
masuk ke dalam sel dan menagkap komponen aktif yang larut keluar dari dalam
sel (Sarker, et al, 2006). Simplisia lumut hati Mastigophora diclados yang
digunakan untuk maserasi sebanyak 2103 gram. Hasil maserasi dengan pelarut n
-heksan di pekatkan dengan vacuum rotary evaporator sehingga diperoleh ekstrak
Karakteristik ekstrak dilakukan untuk mengetahui mutu dari ekstrak yang
akan digunakan sebagai bahan uji. Hasil karakteristik ekstrak dapat dilihat pada
tabel berikut:
Tabel 4.1. Tabel Karakteristik Ekstrak
No. Parameter Ekstrak n-heksan
1. Organoleptik :
a. Bentuk Gumpalan Kasar
b. Warna Hitam
c. Bau Jamu
2. Kadar air 0,048%
3. Kadar abu 0,636%
Pengujian kadar abu dilakukan untuk mengetahui kandungan mineral
internal dan eksternal yang berasal dari proses awal hingga terbentuk ekstrak
(Depkes RI, 2000). Hasil kadar abu menunjukan bahwa jumlah kandungan
mineral Ekstrak Mastigophora diclados masih dibawah ambang batas dari
peraturan (Depkes RI, 1980) yaitu tidak lebih dari 14%.
4.1.3 Penapisan Fitokimia
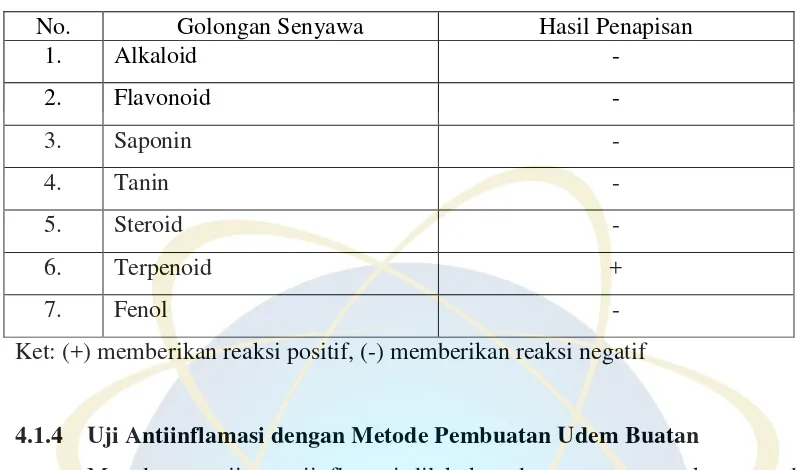
Hasil penapisan fitokimia ekstrak n-heksan lumut hati Mastigophora
diclados yang diuji hanya diperoleh senyawa terpenoid. Penapisan fitokimia
bertujuan untuk mengetahui berbagai macam zat yang terkandung dalam jaringan
tanaman (Depkes RI, 1987), sehingga memungkinkan untuk mengetahui
senyawa yang berpotensi sebagai antiinflamasi. Hasil uji penapisan fitokimia
ekstrak n-heksan tanaman lumut hati Mastigophora diclados dapat dilihat pada
Tabel 4.2. Tabel Penapisan Fitokimia
No. Golongan Senyawa Hasil Penapisan
1. Alkaloid -
2. Flavonoid -
3. Saponin -
4. Tanin -
5. Steroid -
6. Terpenoid +
7. Fenol -
Ket: (+) memberikan reaksi positif, (-) memberikan reaksi negatif
4.1.4 Uji Antiinflamasi dengan Metode Pembuatan Udem Buatan
Metode pengujian antiinflamasi dilakukan dengan menggunakan metoda
pembentukan udem buatan pada telapak kaki belakang tikus putih jantan yang
diinduksi dengan karagenan sebagai induktor udem. Metode ini dipilih karena
merupakan metode standar dalam penelitian uji antiinflamasi, dan sederhana
dalam pengerjaannya (Chakraborty et al., 2004).
Karagenan dipilih sebagai induktor udem karena memiliki kepekaan yang
tinggi dibandingkan dengan induktor lain pada metode pembentukan udem
buatan, selain itu pembentukan udem dengan karagenan tidak bersifat antigenik
dan tidak menimbulkan efek sistemik pada jaringan sekitar inflamasi
(Chakraborty et al., 2004).Karagenan akan menginduksi cedera sel sehingga sel
yang cedera melepaskan mediator yang mengawali proses inflamasi. Setelah
pelepasan mediator inflamasi, terjadi udem yang mampu bertahan selama 6 jam
dan berangsur-angsur berkurang dalam waktu 24 jam setelah injeksi. Pengukuran
daya antiinflamasi dilakukan dengan cara melihat kemampuan ekstrak n-heksan
lumut hati Mastigophora diclados dalam mengurangi pembengkakan telapak kaki
hewan percobaan akibat penyuntikan larutan karagenan 1%. Setelah disuntik
karagenan, hewan percobaan memperlihatkan adanya pembengkakan dan
kemerahan pada telapak kaki serta tidak dapat berjalan lincah seperti sebelum
diinjeksi. Dalam penelitian ini digunakan sebanyak 0,2 mL suspensi karagenan
volume udem dilakukan dengan menggunakan alat plestimometer dengan cara
mencelupkan telapak kaki kiri tikus hingga tanda batas pergelangan kaki tikus.
Hal yang perlu diperhatikan adalah volume air raksa harus sama pada setiap kali
pengukuran, tanda pada pergelangan kaki tikus harus jelas dan telapak kaki tikus
harus tercelup sempurna sampai tanda batas yang ditentukan dengan tujuan agar
mendapatkan data pengukuran yang konstan pada tiap waktu dan dalam kondisi
yang sama.
Hewan uji yang digunakan adalah tikus putih jantan galur Sprague Dawley
yang telah diaklimatisasi selama 3 minggu agar dapat memenuhi syarat berat
badan yaitu 200-250 gram serta dapat beradaptasi dan menyesuaikan diri dengan
lingkungan selama penelitian berlangsung. Pemilihan jenis kelamin tikus putih
jantan bertujuan agar hasil uji tidak dipengaruhi oleh hormon estrogen, karena
hormon ekstrogen lebih banyak terdapat pada tikus betina yang dapat
meningkatkan inflamasi melalui mediator kimia (bradikin) (Green, et al, 1999).
Tikus dikelompokan menjadi 5 kelompok, yaitu kelompok kontrol negatif (1
mL/200g Na CMC 0,5%), dosis rendah (5 mg/kgBB) , dosis sedang (10
mg/KgBB) dan dosis tinggi (50 mg/KgBB). Penentuan variasi dosis untuk
percobaan diperoleh setelah dilakukan uji pendahuluan pada dosis 10 mg/KgBB,
100 mg/KgBB, dan dosis 1000 mg/KgBB. Dari hasil persen ihhibisi ketiga dosis
uji pendahuluan tersebut menunjukan bahwa dosis 10 mg/KgBB memiliki persen
inhibisi sebesar 66,63% pada jam ke-5, dosis 100 mg/KgBB memiliki persen
inhibisi sebesar 42,58 pada jam ke-5,dan dosis 1000 mg/KgBB memiliki persen
inhibisi sebesar 55,36% pada jam ke-5. Dari hasil persen inhibisi udem yang
diperoleh dari uji pendahuluan tersebut didapatkan dosis 10 mg/KgBB memiliki
persen inhibisi yang baik, maka untuk penentuan dosis uji dilakukan pengecilan
dosis yaitu menjadi dosis 5 mg/KgBB, 10 mg/KgBB dan 50 mg/KgBB untuk
melihat aktivitas antiinflamasi yang lebih optimal.
Kontrol positif sebagai pembanding digunakan asam asetil salisilat
(asetosal) dengan dosis 125 mg/KgBB dalam Na CMC 0,5%. Pemilihan asam
asetil salisilat (asetosal) pada penelitian ini dikarenakan asetosal merupakan obat
yang paling banyak digunakan sebagai analgetik, antipiretik dan antiinflamasi
salisilat dapat diabsorpsi dengan cepat dalam bentuk utuh dilambung, tetapi
sebagian besar di usus halus bagian atas. Kadar tertinggi dicapai kira-kira 2 jam
setelah pemberian, asetosal memiliki mekanisme kerja dengan menghambat
enzime sikloooksigenase secara ireversibel (prostaglandin sintetase), yang
mengkatalis perubahan asam arakidonat menjadi prostaglandin, prostasiklin dan
tromboksan yang berperan mengganggu timbulnya reaksi peradangan (Wilmana,
2007; Gunawan, 2008).
Pengukuran volume udem dilakukan setiap 1 jam selama 6 jam
pengamatan pada telapak kaki kiri tikus yang telah diinduksi dengan karegenan.
Setelah mendapatkan hasil pengukuran kemudian dapat dihitung nilai rata-rata
dan standar deviasi dari volume udem telapak kaki tikus.
4.1.5 Hasil Uji Antiinflamasi Ekstrak n-heksan Lumut Hati Mastigophora diclados
Tabel 4.3 Tabel Rata-rata volume udem kaki tikus setelah diinduksi karagenan pada masing-masing kelompok perlakuan selama 6 jam.
No Perlakuan
Rata-rata Volume Udem (ml) ± SD Selama 6 jam Pengamatan
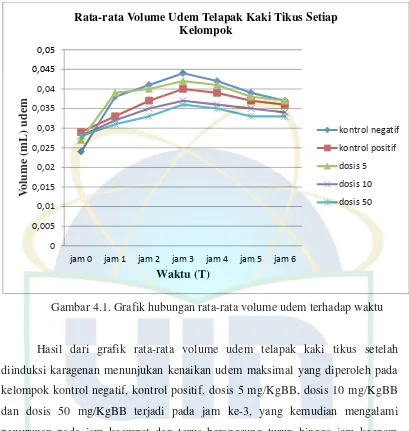
Gambar 4.1. Grafik hubungan rata-rata volume udem terhadap waktu
Hasil dari grafik rata-rata volume udem telapak kaki tikus setelah
diinduksi karagenan menunjukan kenaikan udem maksimal yang diperoleh pada
kelompok kontrol negatif, kontrol positif, dosis 5 mg/KgBB, dosis 10 mg/KgBB
dan dosis 50 mg/KgBB terjadi pada jam ke-3, yang kemudian mengalami
penurunan pada jam keempat dan terus berangsung turun hingga jam keenam
pengamatan.
Dari hasil data volume udem telapak kaki tikus yang diperoleh tersebut,
kemudian dihitung dengan menggunakan rumus (% udem) untuk mendapatkan
persentase udem yang dihasilkan pada masing-masing tikus dari setiap kelompok
perlakuan. Menghitung persen volume udem dilakukan dengan tujuan untuk
mengetahui besar udem dalam (%) yang dihasilkan masing-masing tikus pada
setiap kelompok perlakuan. Hasil rata-rata persen volume udem telapak kaki tikus
yang diperoleh dapat dilihat pada tabel berikut: 0
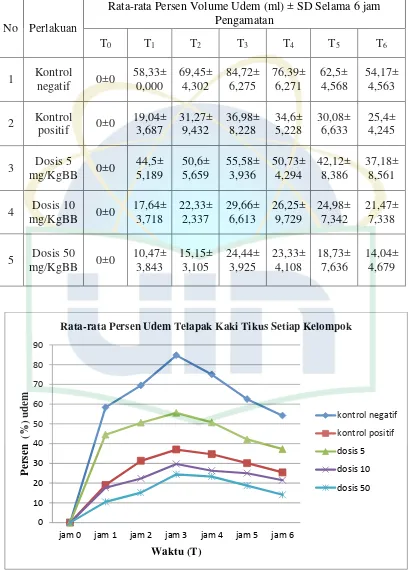
Tabel 4.4 Tabel Rata-rata persentase udem kaki tikus setelah diinduksi karagenan pada masing-masing kelompok perlakuan selama 6 jam.
No Perlakuan
Rata-rata Persen Volume Udem (ml) ± SD Selama 6 jam Pengamatan
Gambar 4.2. Grafik hubungan persen rata-rata udem terhadap waktu
0
Rata-rata Persen Udem Telapak Kaki Tikus Setiap Kelompok
kontrol negatif
kontrol positif
dosis 5
dosis 10
Hasil grafik rata-rata persentase udem pada telapak kaki tikus setiap
kelompok menunjukan bahwa pada kelompok kontrol negatif pembentukan udem
terbesar terjadi pada jam ketiga dengan persentase 84,72% kemudian berangsur
turun pada jam keenam dengan persentase sebesar 54,17%. Pada kontrol positif
persentase udem tertinggi 36,27% pada jam ketiga dan mengalami penurunan
udem pada jam keenam dengan presentase sebesar 25,4%. Sedangkan pada
kelompok dosis 5 mg/KgBB persentase udem tertinggi terjadi pada jam ketiga
sebesar 55,58% kemudian presentase terendah yang dihasilkan sebesar 37,18%
pada jam keenam. Pada dosis 10 mg/KgBB menunjukan udem tertinggi terjadi
pada jam ketiga dengan persentase 29,66% dan berangsur mengalami penurunan
udem pada jam keenam dengan persentase 21,47% dan hal yang sama tejadi pada
dosis 50 mg/KgBB persentase udem tertinggi sebesar 24,44% pada jam ketiga dan
persentase udem terendah dengan persentase 14,04% pada jam keenam. Dari
presentase tersebut dapat diketahui bahwa pembentukan udem optimal yang
terjadi pada telapak kaki tikus setiap kelompok perlakuan terjadi pada jam ketiga
yang kemudian mengalami penurunan persentase udem pada jam keenam.
Hasil persentase volume udem yang diperoleh tersebut dihitung kembali
untuk mendapatkan persen inhibisi udem pada masing-masing tikus dari setiap
kelompok perlakuan. Menghitung persentase inhibisi udem bertujuan untuk
mengetahui besar persentasi kemampuan ekstrak lumut hati Mastigophora
diclados dapat menghambat udem pada telapak kaki tikus. Persentase inhibisi
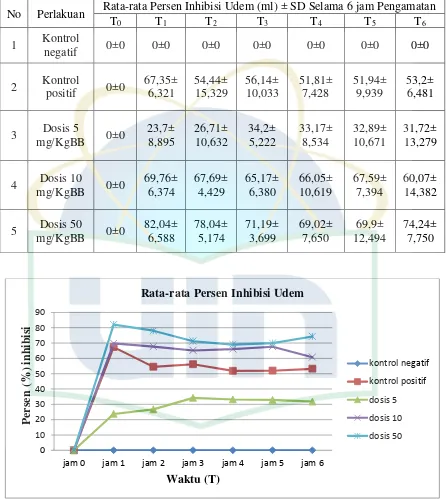
Tabel 4.5 Rata-rata persentase inhibisi udem kaki tikus setelah diinduksi karagenan pada masing-masing kelompok perlakuan selama 6 jam.
Gambar 4.3 Grafik hubungan persen rata-rata inhibisi udem terhadap waktu
Hasil garfik diatas menunjukan bahwa inhibisi radang terbesar terjadi pada
jam pertama. Pada kelompok kontrol positif menunjukan kemampuan
menghambat udem terbesar mencapai 67,35% pada jam pertama dan kemampuan
mengambat udem terkecil sebesar 51,81% pada jam keempat. Sedangkan pada
No Perlakuan Rata-rata Persen Inhibisi Udem (ml) ± SD Selama 6 jam Pengamatan