PENGARUH KONSENTRASI POLIVINIL ALKOHOL (PVA)
TERHADAP KARAKTERISTIK MEMBRAN KITOSAN-
KOLAGEN-PVA UNTUK APLIKASI
PEMBALUT LUKA BAKAR
SKRIPSI
DARMA SURBAKTI
130822032
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
UNIVERSITAS SUMATERA UTARA
PENGARUH KONSENTRASI POLIVINIL ALKOHOL (PVA)
TERHADAP KARAKTERISTIK MEMBRAN KITOSAN-
KOLAGEN-PVA UNTUK APLIKASI
PEMBALUT LUKA BAKAR
SKRIPSI
Diajukan untuk melengkapi tugas dan memenuhi syarat mencapai gelar Sarjana Sains
DARMA SURBAKTI
130822032
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
UNIVERSITAS SUMATERA UTARA
PERSETUJUAN
Judul : Pengaruh KonsentrasiPolivinil Alkohol (PVA) Terhadap Karakteristik Membran Kitosan- Kolagen-PVA untuk Aplikasi Pembalut Luka Bakar
Kategori : Skripsi
Nama : Darma Surbakti
Nomor Induk Mahasiswa : 130822032
Program Studi : Sarjana (S1) Kimia Departemen : Kimia
Fakultas : Matematika Dan Ilmu Pengetahuan Alam (FMIPA) Universitas Sumatera Utara
Disetujui di Medan, Juli 2015
Komisi Pembimbing :
Pembimbing 2, Pembimbing 1,
Prof. Dr. Thamrin, M.Sc. Dr. Amir Hamzah Siregar, M.Si. NIP. 19600741989031003 NIP. 196106114199131002
Departemen Kimia FMIPA USU Ketua,
PERNYATAAN
PENGARUH KONSENTRASI POLIVINIL ALKOHOL (PVA) TERHADAP KARAKTERISTIK MEMBRAN KITOSAN-
KOLAGEN-PVA UNTUK APLIKASI PEMBALUT LUKA BAKAR
SKRIPSI
Saya mengakui bahwa skripsi ini adalah hasil karya saya sendiri, kecuali beberapa kutipan dan ringkasan yang masing-masing disebutkan sumbernya.
Medan, Juli 2015
PENGHARGAAN
Puji dan syukur penulis panjatkan kepada Allah SWT Yang Maha Pengasih dan Maha Penyayang, dengan limpah karunia-Nya Penulis dapat menyelesaikan penyusunan skripsi ini dengan judul Pengaruh Konsentrasi Polivinil Alkohol (PVA) Terhadap Karakteristik Membran Kitosan-kolagen-PVA sebagai Pembalut Luka Primer pada Mencit (mus musculus) Secara In Vivo.
Selain itu, penulis juga mengucapkan terima kasih kepada Dr. Amir Hamzah Siregar, M.Si. selaku dosen pembimbing 1 yang telah memberikan judul dan tunjuk ajar serta bimbingan dan Prof. Dr. Thamrin, M.Sc. selaku dosen pembimbing 2 yang telah banyak memberikan pengarahan dan bimbingan hingga terselesaikannya skripsi ini. Terima kasih kepada Dr. Rumondang Bulan Nst, M.S selaku Ketua Departemen Kimia FMIPA USU dan Dr. Darwin Yunus, M.S selaku Koordianator Ekstensi Kimia FMIPA USU, Dekan dan Pembantu Dekan FMIPA USU, seluruh Staff dan Dosen Kimia FMIPA USU. Terima kasih kepada Ayahanda tercinta Nasib dan Ibunda tersayang Kusmida beserta adik-adik tersayang atas do’a, cinta, kasih sayang dan semangat yang telah diberikan kepada Penulis selama ini. Terima kasih kepada teman-teman Mahasiswa Kimia Ekstensi Angkatan 2013 atas dukungan dan semangat yang diberikan kepada Penulis. Serta segala pihak yang telah membantu Penulis menyelesaikan skripsi ini. Semoga Allah SWT membalasnya.
PENGARUH KONSENTRASI POLIVINIL ALKOHOL (PVA) TERHADAP KARAKTERISTIK MEMBRAN KITOSAN-
KOLAGEN-PVA UNTUK APLIKASI PEMBALUT LUKA BAKAR
ABSTRAK
Kerusakan jaringan seperti luka bakar membutuhkan penanganan yang khusus yang melibatkan penggunaan pembalut luka yang dapat merangsang pertumbuhan jaringan, melindungi luka serta tidak menyebabkan trauma baru ketika pelepasan bahan pembalut luka. Penelitian ini bertujuan untuk memperoleh pembalut luka dari membran kitosan-kolagen-poli(vinil alkohol) yang memenuhi kebutuhan perawatan luka bakar. Membran kitosan-kolagen-poli(vinil alkohol) dipreparasi dengan memvariasikan konsentrasi poli(vinil alkohol) yaitu 5, 10, dan 15%, kemudian semua bahan polimer dicampur dan diaduk secara mekanik hingga homogen pada suhu ruang. Selanjutnya ditambahkan gliserol sebagai plastisizer dan dituangkan ke atas plat kaca yang selanjutnya dikeringkan pada suhu 35 oC. Hasil penelitian menunjukan bahwa membran dengan konsentrasi poli(vinil alkohol) 10% dipilih sebagai membran terbaik dengan mempertimbangkan daya serap dan sifat mekaniknya yaitu 383% dan 1,44 Mpa. Selain itu membran tersebut memiliki rata-rata degradasi 86,6%/minggu, kadar air 29,5% dan dapat menyembukan luka bakar derajat II pada mencit (Mus musculus) dalam waktu 25 hari. Karakteristik dari membran tersebut telah memenuhi kebutuhan perawatan luka bakar.
THE EFFECT OF POLYVINYL ALCOHOL (PVA) CONCENTRATIAON TO CHITOSAN-COLLAGEN-PVA MEMBRANES
CHARACTERISTICSFOR BURN DRESSING APLICATION
ABSTRACT
Tissue damage such as burns requires special handling that involves the use of wound dressing that can stimulates tissue growth, protects the wound and does not cause a new trauma when the remove of the wound dressing material. This study aims to obtain a wound dressing of chitosan-collagen-poly (vinyl alcohol) membran which meet the needs of burn care. Chitosan-collagen-poly (vinyl alcohol) membrans were prepared by varying the concentration of poly (vinyl alcohol), ie 5, 10, and 15%, then all polymer materials were mixed and mechanically stirred until homogeneous at room temperature. Then added glycerol as a plasticizer and poured onto a glass plate and then dried at a temperature of 35 ° C. The results showed that the membrane with a concentration of poly (vinyl alcohol) 10% chosen as the best membrane by considering absorption and mechanical properties are 383% and 1.44 Mpa respectively. Besides the membrane has an average degradation of 86.6%/week, 29.5% moisture content and can heal II degree of burns of mice (Mus musculus) within 25 days. Characteristics of the membrane has been meeting the needs of burn care.
2.7. Hidrogel 23
2.10.1. Uji Gugus ujung ( Gugus Fungsi)
29 3.5.5. Uji Pre-Klinis (Khasiat) Kitosan-Kolagen-PVA
4.1.8. Uji Preklinis 55
BAB 5. Kesimpulan dan Saran 60
5.1 Kesimpulan 60
5.2 Saran 60
DAFTAR TABEL
Nomor Judul Halaman Tabel
2.1. Standar Kitosan 9
2.2. Aplikasi Kitosan dan Turunannya dalam Industri pangan 10
2.3. Komposisi Penyusun SBF 26
4.1. Hasil uji densitas ... 43 4.2. Hasil uji ketebalan membran 44 4.3. Hasil uji Biodegradasi Membran ... 46 4.4. Hasil Perbandingan Degradasi Membran Setelah 7 Hari 47
4.5. Hasil Uji Kadar Air Membran 48
4.6. Data Pengukuran Berat Serapan Air 50
4.7. Data Pengukuran Uji Tarik 51
4.8. Data Karakteristik Optimal 53
DAFTAR GAMBAR
Nomor Judul Halaman Gambar
2.1. Struktur Kitosan 6
2.2. Struktur Kolagen 11
2.3. Struktur Polivinil Alkohol 14 2.4. Aplikasi Membran Hidrogel 24 2.5. Skema Komponen Dasar FTIR 28 4.1. membran kitosan-kolagen-PVA Konsentrasi 5% (a), 10% (b)
dan 15% (c) ... 41 4.2. Hubungan Konsentrasi PVA terhadap Densitas 43 4.3. Hubungan Konsentrasi PVA terhadap Ketebalan Rata-rata 45 4.4. Hubungan Konsentrasi PVA terhadap Persen Degradasinya 47 4.5. Hubungan Konsentrasi PVA terhadap Persen Kadar Air 49 4.6. Hubungan Konsentrasi PVA terhadap Daya Serap ... 50 4.7. Hubungan Konsentrasi PVA terhadap Kekuatan Tarik ... 52 4.8. Hasil Uji FTIR ... 54 4.9 Perbandingan Hari Pengamatan dengan Persen penyembuhan
DAFTAR LAMPIRAN
Nomor
Lampiran Judul Halaman
1 Hasil uji densitas 66
2 Hasil uji daya serap membran 66
3 Hasil uji ketebalan membran 67
4 Hasil uji Biodegradasi membran 68
5 Hasil uji Biodegradasi membran 69
6 Data untuk mencari kekuatan tarik (N/mm2) dan
reganggan (%) dengan L0 = 1100 mm 70 7 Hasil pengukuran diameter luka mencit putih jantan
hari ke 1-36
72 8 Hasil pengamatan penyembuhan luka pada mencit 73 9 Uji FTIR terhadap membran kitosan-kolagen-polivinil
DAFTAR SINGKATAN
DD = Derajat Deasetilasi
FT-IR = Fourier Transform – Infra Red PVA = Polivinil Alkohol
PVC = Polivinil Clorida
BM = Berat Molekul
SBF = Simulated Body Fluid
FC = fosfatidil Cholin
PENGARUH KONSENTRASI POLIVINIL ALKOHOL (PVA) TERHADAP KARAKTERISTIK MEMBRAN KITOSAN-
KOLAGEN-PVA UNTUK APLIKASI PEMBALUT LUKA BAKAR
ABSTRAK
Kerusakan jaringan seperti luka bakar membutuhkan penanganan yang khusus yang melibatkan penggunaan pembalut luka yang dapat merangsang pertumbuhan jaringan, melindungi luka serta tidak menyebabkan trauma baru ketika pelepasan bahan pembalut luka. Penelitian ini bertujuan untuk memperoleh pembalut luka dari membran kitosan-kolagen-poli(vinil alkohol) yang memenuhi kebutuhan perawatan luka bakar. Membran kitosan-kolagen-poli(vinil alkohol) dipreparasi dengan memvariasikan konsentrasi poli(vinil alkohol) yaitu 5, 10, dan 15%, kemudian semua bahan polimer dicampur dan diaduk secara mekanik hingga homogen pada suhu ruang. Selanjutnya ditambahkan gliserol sebagai plastisizer dan dituangkan ke atas plat kaca yang selanjutnya dikeringkan pada suhu 35 oC. Hasil penelitian menunjukan bahwa membran dengan konsentrasi poli(vinil alkohol) 10% dipilih sebagai membran terbaik dengan mempertimbangkan daya serap dan sifat mekaniknya yaitu 383% dan 1,44 Mpa. Selain itu membran tersebut memiliki rata-rata degradasi 86,6%/minggu, kadar air 29,5% dan dapat menyembukan luka bakar derajat II pada mencit (Mus musculus) dalam waktu 25 hari. Karakteristik dari membran tersebut telah memenuhi kebutuhan perawatan luka bakar.
THE EFFECT OF POLYVINYL ALCOHOL (PVA) CONCENTRATIAON TO CHITOSAN-COLLAGEN-PVA MEMBRANES
CHARACTERISTICSFOR BURN DRESSING APLICATION
ABSTRACT
Tissue damage such as burns requires special handling that involves the use of wound dressing that can stimulates tissue growth, protects the wound and does not cause a new trauma when the remove of the wound dressing material. This study aims to obtain a wound dressing of chitosan-collagen-poly (vinyl alcohol) membran which meet the needs of burn care. Chitosan-collagen-poly (vinyl alcohol) membrans were prepared by varying the concentration of poly (vinyl alcohol), ie 5, 10, and 15%, then all polymer materials were mixed and mechanically stirred until homogeneous at room temperature. Then added glycerol as a plasticizer and poured onto a glass plate and then dried at a temperature of 35 ° C. The results showed that the membrane with a concentration of poly (vinyl alcohol) 10% chosen as the best membrane by considering absorption and mechanical properties are 383% and 1.44 Mpa respectively. Besides the membrane has an average degradation of 86.6%/week, 29.5% moisture content and can heal II degree of burns of mice (Mus musculus) within 25 days. Characteristics of the membrane has been meeting the needs of burn care.
BAB 1
PENDAHULUAN
1.1 Latar Belakang
Penelitian akhir-akhir ini dilakukan untuk menemukan cara agar luka dapat sembuh melalui regenerasi dan penggunaan berbagai macam bahan pembalut untuk memfasilitasi manajemen luka yang baik (Lim & Halim, 2010). Bahan pembalut yang banyak diteliti pada saat ini yaitu berasal dari polimer alam diantaranya adalah kitosan. Penggunaan kitosan pada pembalut luka memiliki banyak keuntungan karena sifat biokompatibilitas dan biodegradebilitas molekulnya yang tidak membahayakan kulit dan lingkungan (Lim & Halim, 2010). Sebagai pembalut luka, kitosan dapat dibuat dalam beberapa bentuk yang salah satunya adalah bentuk film/membran (Khan et.al, 2000).
Selain kitosan polimer alam lainnya yang dapat mempercepat penyembuhan luka adalah kolagen. Kolagen adalah protein berongga dan berserat yang banyak terdapat pada jaringan persendian, kulit, otot dan urat. Fibrosa alam ini menghubungkan dan mendukung jaringan tubuh lainnya, seperti tulang dan tendon (Hossein et al, 2007). Di bidang dermatologi kolagen digunakan sebagai peningkat pertumbuhan jaringan dan mempercepat penyembuhan luka (Ruszczak et.al, 1999).
Bahan baku kedua polimer diatas sangat melimpah di Indonesia yaitu dari limbah perikanan seperti kulit udang dan sisik ikan. Dengan demikian, apabila bahan bakunya berasal dari sumber daya alam yang ada, maka selain akan lebih ekonomis lagi, diharapkan terciptanya diversifikasi produk yang mempunyai nilai tambah.
membuat membran dari paduan kitosan dan kolagen yang memiliki sifat mekanik yang memadai. Lebih lanjut penelitian yang dilakukan oleh Dimas dkk. (in Press) dalam penelitianya “Pengolahan Limbah Perikanan Menjadi Biokomposit Kolagen-Kitosan sebagai Pembalut Primer pada Luka Infeksi” diketahui bahwa uji in vivo terhadap hewan mencit membuktikan bahwa penyebuhan luka yang cepat
tetapi membran tersebut memiliki kelemahan biodegradasi yang cepat, yaitu satu hari setelah pengaplikasian dan memiliki sifat mekanik yang rendah. Sehingga dibutuhkan penambahan suatu bahan polimer yang memiliki ketahanan biodegradasi yang tidak terlalu cepat, bersifat biocompatible dan memiliki sifat mekanik yang tinggi.
Polivinil alkohol merupakan salah satu polimer sintetik dengan keunggulan seperti hidrofilisitas dan kompatibilitas tidak toksis, kandungan air yang tinggi, sifat mekanik yang kuat, stabilitas kimia yang baik dibanding polimer sintetik lainnya dan biodegradabel. Oleh karena itu, PVA secara luas banyak digunakan di bidang biomedis (Jayasekarar, 2004).
Dari uraian diatas maka peneliti tertarik membuat membran dengan perpaduan kitosan-kolagen-polivinil alkohol. Adapun judul dari penelitian ini adalah pengaruh kosentrasi polivinil alkohol (PVA) terhadap membran kitosan-kolagen-PVA untuk aplikasi pembalut luka bakar.
1.2 Perumusahan Masalah
1.3 Pembatasan Masalah
Berdasarkan uraian diatas, penelitian ini dibatasi pada: 1. Kitosan, kolagen dan PVA yang diperoleh secara komersil 2. Konsentrasi PVA 5%, 10% dan 15%
3. Luka bakar derajat II dalam
1.4 Tujuan Penelitian
Berdasarkan latar belakang dan rumusan masalah yang diuraikan diatas, maka tujuan dari penelitian ini adalah untuk mengetahui pengaruh konsentrasi PVA terhadap karakteristik membran kitosan-kolagen-PVA dan untuk mengetahui kemampuan membran tersebut dalam mempercepat penyembuhan luka bakar.
1.5 Manfaat Penelitian
Hasil penelitian ini diharapkan dapat memberikan manfaat dan sumbangan pemikiran bagi pemerintah, perkuliahan dan dibidang medis yang ada dalam upaya pemanfaatan polimer alam sebagai pembalut luka dan bahan komposit lainnya. Selain itu juga bagi pengembangan ilmu khususnya ilmu kimia biopolimer atau biomaterial.
1.6. Metodologi Penelitian
• Variabel tetap : Larutan kitosan 3% Larutan kolagen 3%
Temperatur pengeringan membran 400C Gliserin 5%
• Variabel bebas : Variasi konsentrasi PVA 5%, 10%, 25% • Variabel terikat : Hasil analisa uji tarik, FTIR, Biodegradasi,
uji kadar air, uji ketebalan, daya serap, uji densitas, uji preklinis
1.7 Lokasi Penelitian
Penelitian ini dilakukan di beberapa laboratorium yaitu:
- Laboratorium Kimia Polimer Departemen Kimia FMIPA USU Medan sebagai tempat preparasi membran kitosan-kolagen-PVA
- LPPT UGM Yogyakarta sebagai tempat analisa FTIR.
- Laboratorium Fisiologis dan Anatomi Hewan Departemen Biologi FMIPA USU sebagai tempat adaptasi dan perlakuan terhadap hewan uji.
BAB 2
TINJAUAN PUSTAKA
2.1. Kitosan
Kitosan adalah padatan amorf putih kekuningan, tidak beracun dan baik sebagai flokulan dan koagulan serta mudah membentuk membran atau film (Meiratna, 2008), merupakan polimer rantai panjang yang disusun oleh monomer-monomer glukosamin (2-amino-2-deoksi-D-glikosa). Biopolimer ini disusun oleh 2 jenis amino yaitu glukosamin (2-amino-2-deoksi-D-glukosa, 70-80%) dan N-asetilglukosamin (2-asetamino-2-deoksi-D-glukosa, 20-30%). Semakin sedikit gugus asetil yang hilang dari polimer kitosan interaksi antar ion dan ikatan hidrogen dari kitosan akan semakin kuat (Astuti, 2008).
Sifat dari kitosan adalah tidak larut dalam air, memiliki ketahanan kimia cukup baik, larut dalam larutan asam tetapi tidak larut dalam basa dan ikatan silang kitosan memiliki sifat tidak larut dalam media campuran asam dan basa, memiliki reaktivitas kimia yang tinggi karena mengandung gugus OH dan gugus NH2 (Muzzarelli, 1997). Tetapi menurut (Kumar et al., 2000) kitosan mempunyai sifat yang lebih spesifik yaitu dengan adanya sifat bioaktif, biokomposit, pengkelat, antibakteria dan dapat terdegradasi.
Sandford dan Hutchins sebagaimana dikutip Meiratna (2008) menyatakan sifat kationik, biologi, dan sifat kimia kitosan adalah sebagai berikut :
1. Sifat kationik
flokulan yang baik: gugus NH3+ berinteraksi dengan muatan negatif dari polimer lain.
2. Sifat biologi
Dapat terdegradasi secara alami, polimer alami, non toksik. 3. Sifat kimia
Linier poliamin (poli D-glukosamin) yang memiliki gugus amino yang baik untuk reaksi kimia dan pembentukan garam dengan asam, gugus amino yang reaktif, gugus hidroksil yang reaktif (CH3-OH, C6-OH) yang dapat membentuk senyawa turunannya.
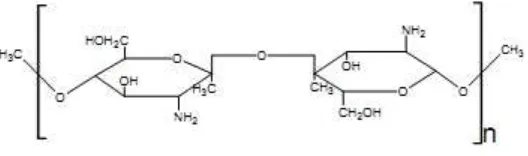
Proses deasetilasi menggunakan kombinasi perlakuan secara kimiawi dan enzimatis seperti penelitian yang dilakukan oleh Emmawati (2004) dan Rochima (2005) merupakan alternatif proses yang baik. Deasetilasi kitin akan menghilangkan gugus asetil dan menyisakan gugus amino yang bermuatan positif, sehingga kitosan bersifat polikationik. Rumus umum kitosan adalah (C6H11NO4)n atau disebut sebagai (1,4)-2-Amino-2-Deoksi-beta-D-Glukosa. Struktur kitosan dapat dilihat pada Gambar 2.2
Gambar 2.1 Struktur Kitosan
Kitosan atau poli-2-amino-2-deoksi-β-1,4-D-glukopiranosa dengan rumus molekul (C6H11O4)n yang dapat diperoleh dari deasetilasi kitin. Kitosan juga dijumpai secara alamiah di beberapa organisme. Kitosan adalah polisakarida linier tersusun atas residu : N- asetil glukosamin dan memiliki 2000-3000 monomer dengan ikatan 1.4-b-gliksida berupa molekul glukosa dengan cabang mengandung nitrogen (Gagne, 2000). Unit monomer pada chitosan mempunyai rumus molekul C8H12NO5 dengan kadar C, H, N, dan O masing-masing 47%, 6%, 7%, dan 40%. Sifat kitosan yang biodegradable ini mempunyai sifat lain diantaranya tidak larut dalam air, asam organik, encer dan alkalikat, akan tetapi larut dalam asam pekat seperti asam nitrit, asam sulfat, asam fosfat, dan asam formiat anhidros (Lee dan Tan, 2002). Chitosan mempunyai sifat penting untuk berbagai aplikasi, yaitu kemampuannya mengikat minyak dan air karena terdapat gugus hidrofilik dan hidrofobik, jumlah minyak dan air yang dapat diikat oleh chitosan masing-masing adalah 315% dan 385%. Berdasarkan sifat biologi dan kimianya maka chitosan mempunyai sifat yang khas yaitu mudah dibentuk menjadi spons, larutan gel, pasta, membran, dan serat yang sangat bermanfaat didalam aplikasinya (Irawan, 2007). Disamping itu telah terbukti pada beberapa penelitian bahwa chitosan dapat meminimalisasikan oksidasi, ditujukan oleh angka peroksida, perubahan warna dan jumlah mikroba dalam sampel (Yingyuad dkk., 2006).
2.1.1 Sifat Fisik dan Kimia Kitosan
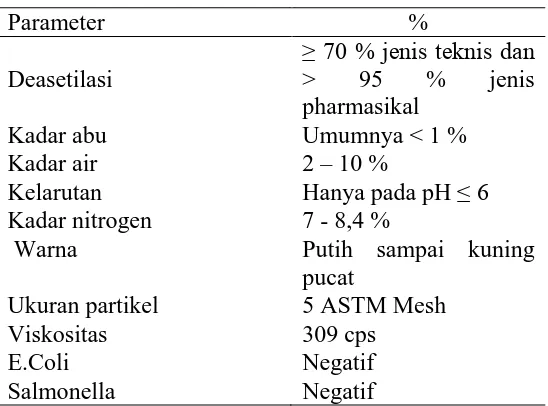
Tabel 2.1. Standard Kitosan
Parameter %
Deasetilasi
≥ 70 % jenis teknis dan
> 95 % jenis pharmasikal
Kadar abu Umumnya < 1 %
Kadar air 2 – 10 %
Kelarutan Hanya pada pH ≤ 6 Kadar nitrogen 7 - 8,4 %
Warna Putih sampai kuning
pucat
Ukuran partikel 5 ASTM Mesh Viskositas 309 cps
E.Coli Negatif
Salmonella Negatif
Sumber : Muzzarelli (1997) dan Austin (1988)
2.1.2. Manfaat Kitosan
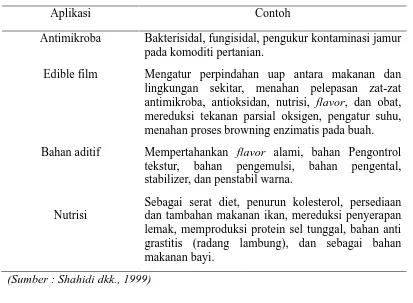
Tabel 2.2. Aplikasi kitosan dan turunannya dalam industri pangan
Aplikasi Contoh
Antimikroba Bakterisidal, fungisidal, pengukur kontaminasi jamur pada komoditi pertanian.
Edible film Mengatur perpindahan uap antara makanan dan lingkungan sekitar, menahan pelepasan zat-zat antimikroba, antioksidan, nutrisi, flavor, dan obat, mereduksi tekanan parsial oksigen, pengatur suhu, menahan proses browning enzimatis pada buah. Bahan aditif Mempertahankan flavor alami, bahan Pengontrol
tekstur, bahan pengemulsi, bahan pengental, stabilizer, dan penstabil warna.
Nutrisi
Sebagai serat diet, penurun kolesterol, persediaan dan tambahan makanan ikan, mereduksi penyerapan lemak, memproduksi protein sel tunggal, bahan anti grastitis (radang lambung), dan sebagai bahan makanan bayi.
(Sumber : Shahidi dkk., 1999)
2.2. Kolagen
Kolagen memegang peranan yang sangat penting pada setiap tahap proses penyembuhan luka. Kolagen mempunyai kemampuan antara lain hemostasis, interaksi dengan trombosit, interaksi dengan fibronektin, meningkatkan eksudasi cairan, meningkatkan komponen seluler, meningkatkan faktor pertumbuhan dan mendorong proses fibroplasia dan terkadang pada proliferasi epidermis (Triyono,2005). Manfaat kolagen dalam bidang medis adalah mempercepat tumbuhnya jaringan baru.
yang unik. Sekitar 30% dari tulang disusun oleh komponen – komponen organik dan 90-95 % diantaranya adalah kolagen , sisanya adalah protein bukan kolagen. Kolagen merupakan protein yang banyak terdapat dalam tubuh (Chi, et al, 2001).
Kolagen merupakan komponen serat utama dalam kulit, tulang, tendon, tulang rawan dan gigi. Kolagen merupakan material yang mempunyai kekuatan rentang dan struktur yang berbentuk serat. Protein jenis ini banyak terdapat dalam vertebrata tingkat tinggi. Hampir sepertiga protein dalam tubuh vertebrata berada sebagai kolagen. Semakin besar hewan, semakin besar pula bagian total protein yang merupakan kolagen. Kolagen juga merupakan komponen serat utama dalam tulang, gigi, tulang rawan, lapisan kulit dalam (dermis), tendon (urat daging) dan tulang rawan (Lehninger: 1993).
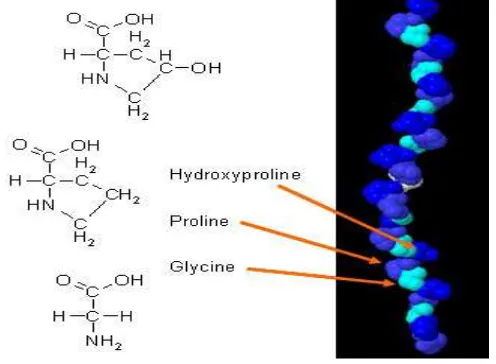
Gambar 2.2 Struktur kolagen
Dengan demikian kolagen termasuk sebagai jaringan pengikat. Jaringan pengikat berkolagen terdiri dari serat, struktur ini selanjutnya tersusun atas fibril kolagen, yang nampak seperti garis melintang. Fibril ini terorganisasi dengan cara yang berbeda-beda, tergantung pada fungsi biologi jaringan pengikatnya. Pada urat, fibril kolagen disusun dalam untaian paralel yang saling berhubungan silang dan berfungsi untuk menghasilkan struktur dengan kekuatan yang amat tinggi tanpa kemampuan meregang. Fibril kolagen dapat menyangga sedikit-nya 10.000 kali beratnya sendiri, dan dapat dikatakan mempunyai kekuatan lenting lebih besar dari penampang silang kawat tembaga dengan berat yang sama. Pada kulit, fibril kolagen membentuk suatu jaringan tidak teratur, terjalin dan amat liat. Kulit hampir seluruhnya merupakan kolagen murni (Page,1989).
Fibroblast bermigrasi ke tempat luka dari jaringan sekitarnya, mulai mensintesis kolagen dan berkembang biak. Respon PDGF, fibroblast sementara mensintesis matriks terdiri dari kolagen tipe III, glycosaminoglycans, dan fibronectin 1 yang menyediakan tempat untuk migrasi
keratinosit. Tipe lain dari fibroblasts "luka fibroblasts" yang sudah ada di luka. Jenis fibroblasts akan berubah menjadi myofibroblast yang memainkan peranan pada kontraksi luka (Broughton dkk., 2006).
2.2.1 Sifat Kolagen
Jika di didihkan di dalam air, kolagen akan mengalami transformasi, dari bentuk
untaian, tidak larut dan tidak tercerna menjadi gelatin, yaitu campuran polipetid
yang larut yang merupakan dasar pembentuk gelatin. Perubahan ini melibatkan
hidrolisis beberapa ikatan kovalen pada kolagen, karena kolagen pada jaringan
pengikat dan pembuluh yang menjadikan daging berbentuk liat. Kolagen
mengandung kira- kira 3-5 persen glisin dan kira-kira 11 persen alanin; persentasi
prolindan 4-hidroksiprolin yang tinggi, yaitu asam amino yang jarang ditemukan
pada protein selain pada kolagen dan elastin. Bersama-sama, prolin dan
hidroksiprolin mencapai kira-kira 21 persen dari residu asam amino pada kolagen
(Lehninger, 1993).
2.2.2 Peranan Kolagen dalam Penyembuhan Luka dan Pembentukan Jaringan
Penyembuhan luka merupakan proses yang kompleks dan berkesinambungan. Hemostatis atau penghentian pendarahan adalah proses pertama pada penyembuhan luka. Trombosit dan faktor-faktor pembekuan merupakan faktor hemostatik intravaskuler yang utama. Kolagen merupakan agen hemostatik yang sangat efesien, sebab trombosit melekat pada kolagen, kolagen akan membengkak dan selanjutnya melepaskan substansi yang memulai proses hemostatis. Interaksi kolagen–trombosit tergantung pada polimerisasi dari maturasi kolagen dan pengaruh positif pada molekul kolagen (www.pasteur. fr/aplications/euroconf/ tissuerepair-microba.pdf).
Kolagen dapat membantu agregasi trombosit karena kemampuannya mengikat fibronektin. Mekanisme yang pasti dari interaksi kolagen belum diketahui secara jelas, akan tetapi data yang pasti menunjukkan bahwa interaksi kolagen dan trombosit merupakan tahap pertama proses penyembuhan luka
2.3. Polivnil Akohol (PVA)
secara komersial dalam skala besar sebagai eksipien dalam berbagai produk farmasi seperti tablet salut, tetes mata, biofermentasi dan topikal. PVA bersifat kompatibel secara hayati dan sesuai untuk simulasi jaringan alami. Selain itu, PVA mempunyai permeabilitas oksigen yang baik, tidak bersifat imunogenik, dan memiliki sifat yang sangat baik dalam pembentukan film, pengemulsi dan dapat dilembabkan (Gessner, 1981). PVA berwarna putih, bentuk seperti serbuk, rasa hambar,tembus cahaya, tidak berbau dan larut dalam air. PVA salah satu polimer yang mempunyai sifat hidrofolik dan sebagai perekat. PVA dapat digunakan sebagai lapisan tipis yang sensitif. Struktur Polivinil alkohol dapat dilihat pada gambar 2.3.
Gambar 2.3 Struktur Polivinil Alkohol
Polivinil alkohol (PVA) merupakan salah satu jenis bahan polimer yang relatif murah dan tidak toksik. PVA dapat digunakan sebagai bahan dasar pembuatan hidrogel sebagai matriks untuk mengekang obat dan kemudian obat tersebut dilepaskan kembali (Zainuddin K.,1994). Menurut Doan Binh, hidrogel yang transparan, kuat secara mekanik dapat dihasilkan dari campuran PVA dan kitosan yang diiradiasi sehingga dapat digunakan untuk antibakteri, mencegah infeksi dan menstimulasi reepitelisasi (Binh,2001).
Polivinil alkohol dapat membentuk film yang sangat baik, pengemulsi dan sifat perekat. PVA juga tahan terhadap minyak, lemak dan pelarut. Memiliki kekuatan tarik tinggi dan fleksibilitas, serta tinggi oksigen. Namun sifat ini tergantung pada kelembaban, dengan kata lain, dengan kelembaban yang lebih tinggi maka lebih banyak yang air diserap, yang bertindak sebagai plasticizer, maka akan mengurangi kekuatan tarik, tetapi meningkatkan elongasi dan kekuatan sobek. PVA memiliki titik leleh 180-190°C (356-374 derajat Fahrenheit) untuk nilai sepenuhnya dihidrolisis dan sebagian dihidrolisis masing-masing. Ini terurai dengan cepat di atas 200° C karena dapat menjalani pirolisis pada suhu tinggi (Fromageau, J.,2003).
2.4. Luka
Luka didefenisikan sebagai cacat pada kulit yang disebabkan oleh kecelakaan
secara mekanik, terserang listrik, terbakar, terkena tumpahan bahan-bahan kimia
atau akibat tindakan operasi. Ketika luka timbul, beberapa efek akan muncul, yaitu
hilangnya seluruh atau sebagian fungsi organ, respon stres simpatis, pendarahan
dan pembekuan darah, kontaminasi bakteri dan kematian sel. Berdasarkan
kedalaman dan luasnya luka, maka luka dibagi menjadi :
Stadium I : luka yang terjadi pada lapisan epidermis kulit
Stadium II : hilangnya lapisan kulit pada lapisan epidermis dan bagian atas
dari dermis. Merupakan luka stadium I dan adanya tanda klinis
seperti abrasi, blister atau lubang yang dangkal.
Stadium III : hilangnya kulit keseluruhan meliputi kerusakan atau nekrosis
jaringan subkutan yang dapat meluas sampai bawah tetapi tidak
melewati jaringan yang mendasarinya. Lukanya sampai lapisan
epidermis, dermis dan fasia tetapi tidak mengenai otot. Luka
timbulsecara klinis sebagai suatu lubang yang dalam dengan atau
merusak jaringan sekitarnya.
Stadium IV : luka yang telah mencapai lapisan otot, tendon dan tulang dengan
adanya destruksi/kerusakan yang luas (Walker, V. 1999).
2.4.1 Luka Bakar
Luka bakar adalah suatu gangguan dari kondisi normal pada kulit (Oswari, 1993).
Luka bakar disebabkan oleh pengalihan energi dari suatu sumber panas kepada
tubuh. Panas dapat dipindahkan lewat hantaran atau radiasi elektromagnetik.
Ketika luka timbul, beberapa efek akan muncul :
a. Hilangnya seluruh atau sebagian fungsi organ
b. Respon stres simpatis
c. Pendarahan dan pembekuan darah
d. Kontaminasi bakteri
e. Kematian sel
Berat ringannya luka bakar tergantung dari lama dan banyaknya kulit
badan yang terbakar. Kerusakan paling ringan akibat terbakar yang timbul pada
kulit adalah warna merah pada kulit. Bila lebih berat, timbul gelembung. Pada
keadaan yang lebih berat lagi bila seluruh kulit terbakar sehingga dagingnya
tampak, sedangkan yang terberat adalah bila otot-otot ikut terbakar (Oswari,2003).
Berdasarkan penyebabnya, luka bakar dibedakan atas beberapa jenis, antara lain:
a. Luka bakar karena api
b. Luka bakar karena air panas
c. Luka bakar karena bahan kimia
d. Luka bakar karena listrik
e. Luka bakar karena logam panas (Djohansjah. 1991)
Berdasarkan kedalam kerusakan jaringan, luka bakar dibedakan atas beberapa jenis
yaitu:
1. Kerusakan terbatas pada epidermis
2. Kulit kering, tampak sebagai eritema
3. Penyembuhan terjadi secaraspontan dalam waktu 5-10 hari
b. Luka bakar derajat II:
1. Kerusakan meliputi dermis dan epidermis
2. Dasar luka berwarna merah, terletak lebih tinggi di atas kulit normal
Luka bakar derajat II dibedakan menjadi dua, yaitu:
a. Derajat II dangkal
Kerusakan mengenai bagian dermis. Penyembuhan terjadi
secara spontan dalam waktu 10-14 hari.
b. Derajat II dalam
Kerusakan hampir seluruh bagian dermis. Penyembuhan terjadi
lebih lama, biasanya penyembuhan terjadi dalam waktu lebih dari satu
bulan.
c. Luka bakar derajat III
1. Kerusakan meliputi seluruh ketebalan dermis dan lapisan yang lebih
dalam.
2. Kulit yang terbakar berwarna abu-abu.
3. Tidak dijumpai rasa nyeri, bahkan hilang sensasi karena ujung-ujung
saraf sensorik mengalami kerusakan / kematian.
4. Penyembuhan terjadi lama karena tidak ada proses epitelasi spontan
baik dari dasar luka, tepi luka maupun apendises kulit (Moenadjat,
2003).
2.4.2 Penyembuhan Luka
Tindakan yang dapat dilakukan pada luka bakar adalah dengan memberikan terapi
local dengan tujuan mendapatkan kesembuhan secepat mungkin, sehingga jumlah
jaringan fibrosis yang terbentuk akan sedikit dan dengan demikin mengurangi
jaringan parut. Diusahakan pula pencegahan terjadinya peradangan yang
Proses penyembuhan luka yang dibagi dalam tiga fase yaitu fase inflamasi,
proliferasi dan penyudahan jaringan.
1. Fase inflamasi
Fase inflamasi berlangsung sejak terjadinya luka sampai hari ketiga.
Pembuluh darah yang terputus pada luka menyebabkan pendarahan dan tubuh
akan berusaha menghentikannya dengan vasokontriksi. Hemostatis terjadi karena
trombosit yang keluar dari pembuluh darah saling melengket dan bersama dengan
fibrin yang terbentuk membekukan darah yang keluar dari pembuluh darah.
2. Fase proliferasi
Fase proliferasi disebut juga fibroplasias karena yang menonjol adalah proses
proliferasi fibroblast. Pada fase ini serat dibentuk dan dihancurkan kembali untuk
penyesuaian diri dengan tegangan pada luka yang cenderung mengerut. Sifat ini,
bersama dengan sifat kontraktil miofibroblast, menyebabkan tarikan pada tepi luka.
Pada akhir fase ini kekuatan regangan luka mencapai 25% jaringan normal.
Nantinya, dalam proses penyudahan kekuatan serat kolagen bertambah karena
ikatan intramolekul dan antar molekul. Pada fase fibroplasia ini, luka
dipenuhi fibroblast, dan kolagen, membentuk jaringan berwarna kemerahan
dengan permukaan yang berbenjol halus yang disebut jaringan granulasi. Epitel
tepi luka yang terdiri dari sel basal terlepas dari dasarnya dan berpindah mengisi
permukaan luka. Tempatnya kemudian diisi oleh sel baru yang terbentuk dari
proses mitosis.
Proses migrasi hanya bisa terjadi ke arah yang lebih rendah atau datar,
sebab epitel tak dapat bermigrasi ke arah yang lebih tinggi. Proses ini baru berhenti
setelah epitel saling menyentuh dan menutup seluruh permukaan luka. Dengan
tertutupnya permukaan luka, proses fibroplasia dengan pembentukan jaringan
granulasi juga akan berhenti dan mulailah proses pematangan dalam fase
3. Fase penyudahan
Pada fase ini terjadi proses pematangan yang terdiri dari penyerapan kembali
jaringan yang berlebih, pengerutan dan akhirnya terbentuk kembali jaringan yang
baru. Tubuh berusaha menormalkan kembali semua yang menjadi abnormal karena
proses penyembuhan. Selama proses ini dihasilkan jaringan parut yang pucat, tipis,
dan lemas serta mudah digerakkan dari dasar. Terlihat pengerutan maksimal pada
luka. Pada akhir fase ini, perupaan luka kulit mampu menahan regangan kira – kira
80% kemampuan kulit normal (Moenadjat, 2003).
2.5. Pembalut Luka
Pembalut luka adalah bahan yang digunakan untuk menutup luka. Berbagai jenis
luka dapat terjadi dalam kehidupan sehari-hari, misalnya luka akibat benturan
mekanik, seperti lecet-lecet, beragam luka bakar dan disebabkan oleh bahan kimia.
Sejak berabad-abad serat binatang maupun tumbuhan telah digunakan untuk
meneutupi luka guna menghentikan pendarahan, menyerap cairan yang keluar dari
luka/eksudat/nanah, mengurangi rasa sakit dan menyediakan perlindungan untuk
pembentukkan jaringan baru. Saat ini bermacam-macam pembalut luka telah
tersedia dipasaran untuk kepentingan medis atau paska operasi. Fungsi produk ini
antara lain adalah untuk memberikan perlindungan terhadap infeksi, menyerap
darah dan nanah, mempercepat penyembuhan luka dan beberapa diantaranya dapat
mengobati luka. Selain ituproduk tersebut harus mudah digunakan dan dilepaskan.
Pembalut luka dapat berupa produk tenun/woven (kain kasa, kain
pembalut/perban) atau produk nirtenun/nonwoven (membran/komposit).
Selain itu pembalut luka yang sering digunakan adalah berupa bahan
komposit atau nirtenun. Produk komposit adalah produk yang terdiri dari dua atau
lebih materialyang diikat satu sama lain baik secara kimia maupun secara mekanik.
antar muka dari masing-masing material yang digunakan, atau dengan bantuan
perekat (adhesive) dan tekanan. Adanya komposit akan menciptakan bahan baru
yang sifatnya dapat memperkaya jenis bahan yang telah ada di alam (Mutia, T.
2011).
2.5.1 Membran
Kata membran berasal dari bahasa latin yaitu ’membrane’ yang berarti potongan kain. Saat ini istilah membran didefenisikan sebagai lapisan tipis (film) yang fleksibel, pembatas antara fasa yang bersifat semipermiabel (Jones, 1987). Membran dapat berupa padatan ataupun cairan dan berfungsi sebagai media pemisahan yang selektif berdasarkan perbedaan koefisien difusivitas, muatan listrik atau kelarutan.
Sebenarnya membran sudah merupakan bagian integral dari kehidupan kita sehari-hari. Seluruh sel penyusun tubuh mahluk hidup, terutama penyusun sel-sel penyusun tubuh kita dibungkus dengan membran. Membran sel-sel sangat bersifat selektif sehingga hanya zat-zat tertentu saja yang dapat melaluinya. Pada tahun 1855 membran baru dikembangkan secara kecil-kecilan dalam skala laboratoriumnya oleh Fick. Pengelompokan membran dapat dilakukan atas dasar berbagai hal. Atas dasar material yang digunakan membran dapat dikelompokkan menjadi membran polimer, liquid membran, padatan (keramik) dan membran penukar ion. Berdasarkan konfigurasinya membran dapat dikelompokkan memnjadi lembaran, lilitan spiral (spiral warna), tubular dan emulsi (Mulder,1996)
pengaruh gugus fungsi yang dimilikinya bersifat polikationik maupun polielektrolit (Zhao, at al., 2002).
2.6. Biomaterial Medis
Biomaterial atau biomedical material dapat didefinisikan secara umum sebagai suatu material baik natural maupun buatan manusia (sintetis) yang digunakan sebagai peralatan medis (medical devices) dan berinteraksi dengan sistem biologis dengan tujuan untuk memperbaiki (repair), memulihkan (restore), mengoreksi ketidaknormalan, meningkatkan fungsi atau mengganti (replace) bagian tubuh yang mengalami kehilangan fungsi karena suatu penyakit atau trauma, atau sebagai
interface dengan lingkungan fisiologis (Guelcher,2006 dan Rosiak,2002). Adanya
interaksi dengan sistem biologis mengharuskan setiap bahan biomaterial memiliki sifat biokompatibilitas yaitu kemampuan suatu material untuk bekerja selaras dengan tubuh tanpa menimbulkan efek lain yang berbahaya.
Polimer dari bahan terbarukan (renewable matrial) menjadi objek penelitian yang menarik selama dua dekade akhir ini. Ada dua alasan yang mendasari polimer tersebut menjadi objek riset, yaitu konsen lingkungan dan realisasi dari sumber bahan bakar fosil yang terbatas. Diharapkan polimer dari bahan terbarukan adalah polimer biodegradable, yaitu polimer yang dapat mengalami degradasi secara alami. Biodegradasi merupakan peristiwa terurainya senyawa menjadi senyawa-senyawa lain yang lebih sederhana yang terjadi karena sebab-sebab alami, seperti proses fotodegradasi (degradasi yang melibatkan cahaya dan kalor), degradasi kimiawi (hidrolisis), degradasi oleh bakteri dan jamur, degradasi enzimatik, dan degradasi mekanik (disebabkan oleh angin, abarasi), atau gabungan dari beberapa sebab (Khoerudin, A., 2013).
biocompatible. Sifat biocompatible sangat penting dalam aplikasi ini karena
polimer yang digunakan dalam sistem pengantaran obat (DDS) nantinya akan dikonsumsi dan masuk kedalam tubuh sehingga tidak memberikan efek buruk terhadap tubuh. Polimer yang memiliki sifat tersebut banyak bersumber dari alam. Akan tetapi, sifat mekanik dari polimer biodegradable alami tidak begitu baik untuk diaplikasikan dalam media biologis. Oleh karena itu, biasanya dilakukan kombinasi dengan polimer biodegradable lain yang memiliki sifat mekanik baik sehingga menghasilkan sifat mekanik yang diinginkan dari suatu kombinasi (Edlund dan albertsson, 2002).
Dewasa ini biomaterials telah banyak digunakan dalam bidang medis seperti penutup luka (wound dressing), lensa kontak (contact lense), hemodialiser, kateter, artifical skin, artificial blood vessels, total artificial hearts, pacemakers, dental fillings, wires plates dan pins for bone repair, total artificial joint
replacements, scaffold in tissue engineering.
Membran didefinisikan suatu lapisan tipis semipermeabel yang berada di antara dua fasa. Teknologi membran banyak digunakan dalam industri sebagai alternatif dari teknologi pemisahan konvensional seperti penyulingan, ekstraksi dan kromatografi. Keuntungan dalam penggunaan teknologi membran adalah dapat berlangsung pada suhu kamar, tidak destruktif, pemisahan dapat berjalan secara sinambung dan tidak terlalu banyak membutuhkan energi.
2.7. Hidrogel
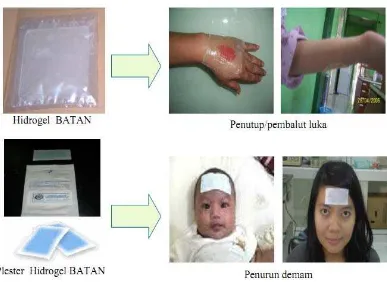
Hidrogel dapat didefinisikan sebagai sistem polimer yang tersusun atas network tiga dimensi antar rantai molekul polimer, bersifat tidak larut dalam air dan dapat mengabsorb air atau cairan tubuh dan mengembang ( Rosiak, J.M., 2002 dan . Peppas, N.A., 1996). Sejak beberapa tahun yang lalu, Darmawan dkk. (1993) telah berhasil mensintesis hidrogel dari polimer hidrofilik polivinil pirolidon (PVP) menggunakan radiasi gamma dan berkas elektron untuk digunakan sebagai pembalut luka dan plester penurun demam. Hidrogel yang dihasilkan mempunyai sifat yaitu memiliki kandungan air sekitar 80-90%, bersifat steril, dapat mengabsorbsi air, permeabel terhadap udara tetapi tidak dapat ditembus oleh mikroba, lunak, tidak toksis, mempunyai kemampuan untuk penyembuhan luka, kuat namun cukup elastik, nyaman dan terasa sejuk pada saat pemakaian, dapat melekat dengan baik pada daerah luka dan tidak menimbulkan jaringan parut pada bekas luka, sebagaimana diperlihatkan pada Gambar 2.3.
Adanya struktur network tiga dimensi dengan pori yang cukup halus serta mengandung air dalam hidrogel menyebabkannya mampu berfungsi untuk mempercepat proses penyembuhan dengan cara memberikan suasana humid pada daerah luka sehingga proses proliferasi sel dapat berjalan lebih sempurna. Selain itu pori yang ada pada hidrogel memberikan kesempatan terjadinya aerasi udara pada daerah luka. Dalam aplikasinya sebagai penurun demam, hidrogel yang mengandung air cukup tinggi dapat membantu menurunkan suhu tubuh pasien melalui mekanisme air yang terdapat pada hidrogel akan menyerap panas dari tubuh dan kemudian menurunkan suhu tubuh melalui evaporasi (Fever Cooling Pad, 2009).
2.8. Simulated Body Fluid (SBF)
Pada umumnya dilakukan pengujian terhadap biomaterial sintetik agar sesuai untuk diaplikasikan sebagai bahan implan. Metode pengujian secara in vivo atau in vitro dilakukan dengan media larutan simulated body fluid (SBF) (Vulelic,
2.8.1. Pembuatan Larutan Simulated Body Fluid (SBF)
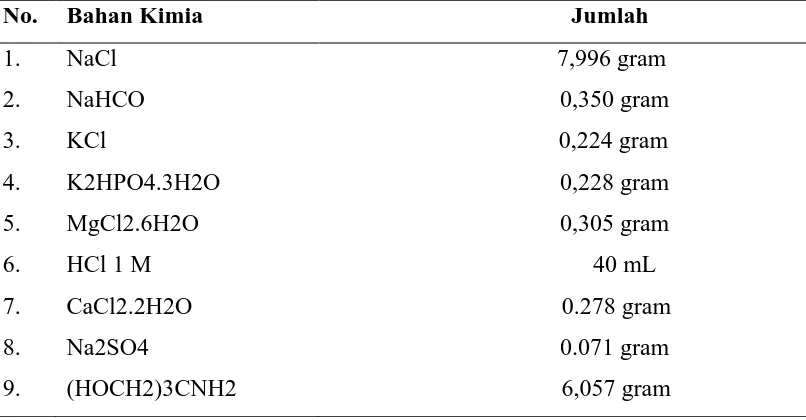
Metode yang digunakan untuk membuat larutan SBF adalah metode yang dipakai oleh Kokubo (Kokubo, T., Kushitani, H et al.,1990 ). Sebanyak 1 Liter aqua trides disiapkan untuk membuat larutan SBF dengan komposisi seperti pada Tabel 1. Aqua trides diaduk menggunaka magnetic stirrer, lalu bahan kimia dimasukkan satu persatu sesuai urutan seperti yang tertera pada Tabel 1 (satu bahan kimia diaduk sampai larut, baru ditambahkan dengan bahan kimia berikutnya). Suhu larutan diatur sampai 36,50C dan pH larutan disesuaikan sampai pH 7,4 dengan menggunakan larutan HCl 1 M.
Tabel 2.3. Komposisi bahan kimia penyusun larutan SBF (Simulated Body Fluid)
2.9 Kuat Tarik
yang dikaitkan pada alat uji dan beban penarik di pasang pada satuan beban kilo Newton (kN). Biofilm ditarik hingga putus. Besar beban penarik dan perubahan panjang biofilm pada saat putus dicatat (Wafiroh, dkk., 2010). Pengujian ini digunakan untuk meneliti keadaan cacat tetapi untuk memeriksa kualitas produk yang dihasilkan berdasarkan suatu standar spesifikasi.
Hasil pengukuran ini berhubungan erat dengan jumlah plasticizer yang ditambahkan pada proses pembuatan film. Plasticizer dapat mengurangi ikatan hidrogen internal molekul dan menyebabkan melemahnya gaya tarik intermolekul rantai polimer yang berdekatan sehingga mengurangi daya regang putus. Penambahan plasticizer lebih dari jumlah tertentu akan menghasilkan film dengan kuat tarik yang lebih rendah (Lai et al., 1997 sebagaimana dikutip Astuti, 2008). Panjang putus (elongation at break) atau proses pemanjangan merupakan perubahan panjang maksimum pada saat terjadi peregangan hingga sampel film terputus. Pada umumnya adanya penambahan plasticizer dalam jumlah lebih besar akan menghasilkan nilai persen pemanjangan suatu film semakin lebih besar (Widyaningsih, dkk. 2012).
2.9.1 Uji Kekuatan dan Persen Pemanjangan
Kuat tarik dan persen pemanjangan merupakan sifat mekanik yang berhubungan dengan struktur kimia biofilm. Kekuatan tarik menunjukkan ukuran ketahanan biofilm yaitu renggangan maksimal yang dapat diterima sampel, sedangkan persen pemanjangan merupakan perubahan panjang maksimum yang dialami plastik pada saat uji kuat tarik yaitu pada saat sampel sobek (Apriyanto, 2007). Adapun rumus dari kuat tarik dan persen elongasi diukur berdasarkan rumus:
Kuat Tarik = �
� kg/ cm 2
(2-1)
Dengan:
A = luas alas sampel (cm2) % Elongasi = �1−�0
�0 � 100% (2-2)
Dengan:
L1 = panjang setelah putus L0 = panjang awal
2.10 FT-IR (Fourier Transform Infrared)
Karakterisasi gugus ujung dapat dilakukan menggunakan IR. Spektroskopi FT-IR atau Fourier Transform Infrared dapat menganalisis gugus ujung suatu senyawa. Dalam penelitian Darni dan Utami (2010) uji FT-IR digunakan untuk mengidentifikasi bahan kimia yang terkandung dalam suatu polimer. Komponen dasar sebuah FT-IR ditunjukkan secara skematis pada Gambar 2.4
Gambar 2.5 Skema komponen dasar FT-IR
Kegunaan dari spektrum inframerah adalah memberikan keterangan mengenai molekul. Serapan tiap tipe ikatan (N-H, C-H, O-H, C-X, C=O, C-O, C=C, C-C, C=N, dan sebagainya) hanya dapat diperoleh dalam bagian-bagian kecil tertentu dari daerah vibrasi inframerah. Kisaran serapan yang kecil dapat digunakan untuk menentukan setiap tipe ikatan.
Cahaya infra merah terbagi menjadi 3 yakni, inframerah dekat, inframerah pertengahan, dan infra merah jauh. Hampir semua senyawa, termasuk senyawa organik menyerap dalam daerah inframerah. Agar senyawa bentuk padat dapat dianalisis pada daerah inframerah maka senyawa tersebut harus dibuat film,
Sumber Infra merah
Interferometer Sampel Detektor
dilebur, atau dilumatkan menjadi cairan yang kental (mull), didispersikan dalam senyawa halida organik menjadi bentuk cakram atau pellet, atau dilarutkan dalam berbagai pelarut. Polimer organik dapat dibuat film diantara dua lempengan garam setelah dilarutkan dalam pelarut yang cocok (Sastrohamidjojo, 1992).
Menurut Nisa (2005) pengukuran FT-IR kitosan-PVA dilakukan dengan cara sampel dijepit pada lempeng NaCl lalu diukur pada bilangan gelombang yang sama. Hasilnya di dapat berupa difraktogram hubungan antara bilangan gelombang dengan intensitas.
2.10.1 Uji Gugus Ujung (Gugus Fungsi)
BAB 3
METODE PENELITIAN
3.1 Alat-alat yang digunakan dalam penelitian ini
1. Timbangan Elektrik Mettler Toledo 2. Hot plate stirer Favorit HS 0707V2
3. Termometer Fischer
4. Alat-alat gelas Pyrex
5. Seperangkat alat uji tarik
6. Oven Memmert
7. Alu dan lumpang 8. Desikator
9. Seperangkat alat FTIR 10. Gunting
11. Bunsen 12. Pinset
13. Pencukur bulu 14. Plat bakar
3.2 Bahan yang digunakan dalam penelitian ini
- CH3COOH glacial p.a ( E. Merck ) - Akuades
- Fish collagen CV. Bio Kolagen Indonesia
- Chitosan CV. Bio Kolagen Indonesia
- PVA Merck
- Gliserol teknis (Bratachem)
- Sel fibroblast BHK-21
- Pembalut luka komersil Dermafix
- Plaster Hansaplast
- Kapas
- Alkohol 70% Brataco
- Mencit jantan - Ketamine - Pakan mencit
3.3 Prosedur Penelitian
3.3.1 Pembuatan Larutan Pereaksi
a. Larutan CH3COOH 1%
Sebanyak 10 mL CH3COOH glacial dilarutkan dengan 1000 ml aquades dalam labu takar 1000 mL sampai garis tanda, kemudian dihomogenkan.
b. Larutan kitosan 3%
Sebanyak 3 g kitosan dilarutkan dengan 100 ml CH3COOH 1% dalam labu takar 100 ml sampai garis tanda, kemudian dihomogenkan.
c. Larutan kolagen 3%
Sebanyak 3 g kolagen dilarutkan dengan 100 ml CH3COOH 1% dalam labu takar 100 ml sampai garis tanda, kemudian dihomogenkan.
d. Larutan PVA 5%
Sebanyak 5 gram PVA dilarutkan dengan 100 ml akuades dalam beaker glass pada suhu 80oC, kemudian dihomogenkan dengan stirer
Sebanyak 10 gram PVA dilarutkan dengan 100 ml akuades dalam beaker glass pada suhu 80oC, kemudian dihomogenkan dengan stirer
f. Larutan PVA 15%
Sebanyak 15 gram PVA dilarutkan dengan 100 ml akuades dalam beaker glass pada suhu 80oC, kemudian dihomogenkan dengan stirer
g. Larutan SBF
Sebanyak 1 Liter aquatrides disiapkan untuk membuat larutan SBF dengan komposisi seperti pada Tabel 3.1. Aquatrides diaduk menggunakan magnetic stirrer, lalu bahan kimia dimasukkan satu persatu sesuai urutan
seperti yang tertera pada Tabel 3.1. (satu bahan kimia diaduk sampai larut, baru ditambahkan dengan bahan kimia berikutnya). Suhu larutan diatur sampai 36,50C dan pH larutan disesuaikan sampai pH 7,4 dengan menggunakan larutan HCl 1 M.
Tabel 3.1. Komposisi bahan kimia penyusun larutan SBF (Simulated Body Fluid)
Sumber: Kokubo 1990
3.3.2 Pembuatan Membran Kitosan-Kolagen-PVA
kembali selama 2 jam hingga homogen. Setelah homogen campuran tersebut dimasukkan kedalam cetakan dan dimasukkan kedalam oven pada suhu 400C selama 24 jam. Kemudian hasil dikarakteristik dengan uji tarik, analisa gugus fungsi dengan FTIR, uji kadar air, uji tarik, uji daya serap, uji ketebalan, uji degradasi SBF dan uji preklinis pada mencit.
3.3.3 Karakteristik Membran Kitosan-Kolagen-PVA
3.3.3.1 Uji Kadar Air
Analisis kadar air dilakukan dengan menggunakan metode oven. Prinsipnya adalah menguapkan molekul air (H2O) bebas yang ada dalam sampel. Cawan dioven terlebih dahulu selama 30 menit pada suhu 100-1050C, kemudian didinginkan dalam desikator untuk menghilangkan uap air dan ditimbang. Selanjutnya sampel ditimbang sebanyak 2g dalam cawan yang sudah dikeringkan, lalu sampel tersebut dioven pada suhu 100-1050C selama 6 jam, kemudian didinginkan dalam desikator selama 30 menit dan ditimbang. Tahap ini diulangi hingga dicapai bobot yang konstan. Kemudian kadar air dihitung dengan persamaan:
b – c
% Kadar air = x 100% (3-1) b – a
Keterangan:
a = berat cawan kosong (g)
b = berat cawan berisi sampel sebelum dioven (g) c = berat cawan berisi sampel sesudah dioven (g)
3.3.3.2 Uji Daya Serap Air
selama 24 jam. Selanjutnya dihitung berat basahnya dan ditentukan daya serap menggunakan persamaan:
mb-mk
DS % = x 100% (3-2) mk
Keterangan:
DS = daya serap (%) mk = massa kering (g) mb = massa basah (g)
3.3.3.3 Uji Ketebalan
Uji ketebalan pada sampel uji dilakukan menggunakan mikrometer sekrup. Ketebalan sampel diukur pada tiga posisi yaitu bagian atas, bagian tengah, dan bagian bawah membran, kemudian hasilnya dirata-rata. Pengukuran ini bertujuan untuk mengetahui keseragaman dan kontrol kualitas dari membran.
3.3.3.4 Uji Tarik
Membran berbentuk dumbbell ukuran standar, ke dua ujungnya dijepit pada posisi atas-bawah pada mesin. Kemudian salah satu ujung membran ditarik ke atas dengan mesin. Setelah bagian tengah dari membran putus, jarak awal (Lo) hingga putusnya (L1) membran diukur dengan penggaris. Pengujian dilakukan 5 kali ulangan dengan kecepatan penarikan 30mm/menit pada suhu kamar. Data hasil pengujian tegangan putus dicatat.
Perpanjangan putus = (�1−��)
�� � 100 % (3-3) Dimana :
L1= Ukuran panjang bahan yang ditarik hingga saat putus Tegangan putus = �
� kg/cm 2
(3-4)
Dimana :
F = Beban pada alat hingga saat bahan putus (kg) A = Luas penampang bahan (cm2)
3.3.3.5 Uji Spektroskopi FTIR
Sampel dijepit pada tempat sampel kemudian diletakkan pada alat ke arah sinar inframerah. Hasilnya akan direkam berupa aliran kurva bilangan gelombang terhadap intensitas sinar atau grafik spektrum.
3.3.3.6 Uji Biodegredasi perendaman dalam larutan SBF (simulated body
fluid)
Membran poliblend direndaman dalam larutan SBF (simulated body Fluid) dengan perbandingan 1:10 (b/v) selama 7-14 hari dengan pergantian larutan SBF setiap 24 jam. Kemudian diangkat dari larutan SBF kemudian dikeringkan dan ditimbang.
D0-D1
% Degradasi = x 100% (3-5) D0
Keterangan
D0 = perlakuan sebelum didegradasi
3.3.3.7 Uji Densitas
Pengujian densitas dilakukan dengan menimbang piknometer kosong, piknometer berisi aquadest dan piknometer berisi aquadest dan sampel membran dengan variasi konsentrasi PVA yang berbeda-beda. Setelah itu dihitung densitasnnya menggunakan persamaan (6).
Densitas (ρ) = m/v m/cm3 (3-6)
Keterangan:
ρ = densitas (g/cm3) m = massa (g) v = volume (cm3)
3.3.3.8 Uji Pre-Klinis (Khasiat) Kitosan-Kolagen-PVA Pada Mencit
a. Analisa Data
Analisa data dilakukan dengan metode analisis varian (ANOVA) dan untuk pengukuran luas luka atau persentase penyembuhan luka, yaitu dengan cara mengukur rata-rata diameter luka pada arah vertikal, horisontal, dan kedua diagonal (Morton, 1972). Persentase penyembuhan luka dihitung dengan rumus sebagai berikut:
% Penyembuhan luka = d1² – d2²
d1² x 100% (3-7)
Keterangan:
d1= diameter sehari setelah pembuatan luka (cm)
3.4 Bagan Penelitian
3.4.1 Pembuatan Membran Kitosan-Kolagen-PVA
Dihomogenkan selama 5 menit dengan strirer
Ditambahkan 6% gliserol dari volume keseluruhan larutan poliblend
Dihomogenkan kembali selama 2 jam dengan stirer
Dicetak pada plat kaca
Dioven pada suhu 40OC selama 24 jam
20 ml Larutan Kitosan 3% 20 ml Larutan PVA 5%, 10%, 15%
Larutan Poliblend
Karakteristik: 1. Uji FTIR 2. Uji Kadar air 3. Uji Daya Serap 4. Uji Ketebalan 5. Uji Tarik 6. Uji Densitas 7. Uji Biodegradasi 8. Uji Preklinis
20 ml Larutan Kolagen 3%
3.5 UJI Karakteristik Membran Kitosan-Kolagen-PVA
3.5.1 Uji Kadar Air
Dimasukkan kedalam cawan porselin Dioven pada suhu 100-105OC selama 6 jam Didinginkan didalam desikator selama 30menit Ditimbang hingga mendapat berat konstan
3.5.2 Uji Tarik
Dicetak membran berbentuk dumbbell
Dijepit kedua ujung pada posisi atas dan bawah dengan mesin Ditarik salah satu ujung kearah atas dengan mesin hingga bagian tengah terputus
Dihitung jarak awal (L0) hingga jarak putusnya (L1) dengan penggaris
Membran
Hasil
Membran
3.5.3 Uji Daya Serap
Dikeringkan didalam oven dengan suhu 105oC hingga berat konstan Direndam didalam aquadest selama 24 jam
Dihitung berat basahnya
Ditentukan persentase daya serapnya
3.5.4 Uji biodegradasi
Direndam dalam larutan SBF dengan perbandingan 1:10 (b:v) Selama 1-7 hari
Dilakukan pergantian larutan SBF setiap @$ jam Dikeluarkan dari larutan SBF
Dikeringkan Ditimbang Membran
Hasil
Membran
3.5.5 Uji Pre-Klinis (Khasiat) Kitosan-Kolagen-PVA Pada Mencit
diaklimatisasi dahulu selama 4 hari diberi makan dan minum
ditimbang berat badan masing-masing dibagi menjadi tiga kelompok perlakuan
pembuatan luka luka bakar dipilih bagian punggung mencit
dicukur bulu sekitar 3 cm menggunakan krim cukur
didesinfeksi dengan alkohol 70% dipanaskan logam selama 5 menit ditempelkan selama 5 detik pada punggung tikus
KO tanpa perlakuan
P1 ditutup dengan membran P2 ditutup dengan plaster komersil diukur diameter luka setiap hari sampai sembuh
dihitung persentase diameter luka 9 ekor mencit
P2
KO P1
Terbentuk luka bakar derajat II
BAB IV
HASIL DAN PEMBAHASAN
4.1 Preparasi Membran Kitosan-Kolagen-Polivinil Alkohol
Preparasi membran kitosan-kolagen-polivinil alkohol dibuat dengan pengeringan pelarut, sehingga terbentuk lapisan tipis membran yang padat seperti yang ditunjukkan pada gambar 4.1. Membran tersebut memiliki permukaan lembut yang nyaman pada kulit
(a) (b) (c)
Gambar 4.1 membran kitosan-kolagen-PVA konsentrasi 5% (a), 10% (b) dan 15% (c).
4.1.1. Uji Densitas
Hasil yang diperoleh dari pengukuran densitas berupa data massa dan volume membran dalam piknometer 5ml, kemudian data yang diperoleh dihitung densitasnya menggunakan persamaa (3-6). Hasil perhitungan uji densitas ditunjukkan pada tabel 4.1.
Tabel 4.1 Hasil uji densitas
Sampel
Sampel I : membran Kitosan-Kolagen-PVA 3:3:5% Sampel II : membran Kitosan-Kolagen-PVA 3:3:10% Sampel III : membran Kitosan-Kolagen-PVA 3:3:15%
Dari gambar 4.2 dapat dilihat hubungan antara konsentrasi polivinil alkohol dan densitas, dimana semakin bertambahnya konsentrasi polivinil alkohol menyebabkan terjadinya peningkatan densitas. Hal ini dikarenakan polivinil alkohol memiliki densitas lebih tinggi dari pada kitosan dan kolagen, dimana densitas dari polivinil yaitu 1,2000-1,3030 g/ml, densitas kitosan yaitu 0,166-0,178 g/ml dan densitas dari kolagen yaitu 1,0439 g/ml. Selain itu poliovinil alkohol memiliki sifat daya lekat antar partikel yang kuat sehingga menyebabkan membran yang terbentuk memiliki kerapatan molekul yang semakin tinggi.
4.1.2. Uji Ketebalan Membran
Uji ketebalan dilakukan untuk mengetahui pengaruh variasi penambahan komposisi PVA pada membran. Uji ketebalan inidilakukan dengan menggunakan mikrometer sekrup dengan skala ketelitian 0,01 mm. pengukuran ini dilakukan dengan mengambil sampel membran kitosan-kolagen-PVA dari berbagai sisi berbeda, yaitu sisi atas, tengah, dan bawah. Nilai yang didapat dihitung rata-ratanya. Hasil perhitungan uji ketebala membran ditunjukan pada tabel 4.2.
Tabel 4.2 Hasil uji ketebalan membran
Sampel Atas Tengah Bawah
I 0,25 0,25 0,15
II 0,25 0,15 1,6
III 1,15 1,45 1,35
Keterangan
Sampel I : membran Kitosan-Kolagen-PVA 3:3:5% Sampel II : membran Kitosan-Kolagen-PVA 3:3:10% Sampel III : membran Kitosan-Kolagen-PVA 3:3:15%
tersebut menunjukkan perbedaan nilai ketebalan membran seiring dengan penambahan variasi polivinil alkohol (PVA). Hal ini terjadi karena saat penambahan polivinil alkohol (PVA) semakin tinggi konsentrasinya menyebabkan larutan semakin pekat, sehingga ketebalan membran kitosan-kolagen-polivinil alkohol (PVA) pun ikut meningkat. Menurut Krisna (2011), ketebalan membran akan mempengaruhi karakteristik mekanik membran yang dihasilkan diantaranya sifat kuat tarik (tensile strength). Pada penambahan PVA yang terlalu tinggi akan menghasilkan membran dengan sifat yang kaku.
Gambar 4.3 Grafik hubungan konsentrasi PVA terhadap ketebalan rata-rata membran kitosan-kolagen-polivini alkohol
4.1.3 Uji Biodegradasi Membran
Hasil pengujian yang diperoleh berupa data berat awal membran dengan berat degradasi dari hari ke-1 hingga ke-7. Hasi uji biodegradasi ditunjukan pada tabel 4.3 dan Gambar 4.4. Tabel dan Gambar tersebut menunjukkan bahwa semua variasi membran dapat terbiodegradasi secara perlahan. Namun laju degradasi yang
sangat cepat terjadi pada tahap awal degradasi untuk semua variasi membran dikarenakan kitosan dan kolagen merupakan senyawa biopolimer yang memiliki laju biodegradasi yang lebih cepat dibandingkan dengan senyawa-senyawa sintetis (Indrani, 2012). Sehingga dapat diperkirakan pengurangan bobot membran yang drastis pada hari pertama disebabkan karena terdegradasinya komponen biopolimer.
Tabel 4.3 Hasil uji Biodegradasi membran Hari Pengamatan Sampel I
(g)
Hasil pengukuran diatas dapat ditunjukkan pada grafik dibawah ini.
Gambar 4.4 Grafik hubungan konsentrasi PVA terhadap persentase degradasinya
Selain itu, juga terdapat perbedaan laju degradasi pada setiap membran, yang mana laju degradasi menurun seiring bertambah konsentrasi PVA seperti yang ditunjukkan pada . Hal itu dikarenakan polivinil alkohol merupakan senyawa sintetis yang memiliki ketahanan degradasi yang lebih tinggi dibandingkan biopolimer. Sehingga semakin tinggi konsentrasi PVA menyebabkan penurunan laju degradasi.
Tabel 4.4 Hasil perbandingan degradasi membran setelah 7 hari
Sampel Degradasi Setelah 7 Hari (%/24 jam)
I 92,2%
II 86,6%
III 84,2%
Keterangan
Sampel I : membran Kitosan-Kolagen-PVA 3:3:5% Sampel II : membran Kitosan-Kolagen-PVA 3:3:10% Sampel III : membran Kitosan-Kolagen-PVA 3:3:15%
4.1.4 Uji Kadar Air Membran
Analisis kadar air dilakukan dengan menggunakan metode oven. Prinsipnya adalah menguapkan molekul air (H2O) bebas yang ada dalam sampel. Data yang diperoleh persentase kadar airnya menggunakan Persamaan (3-1). Hasil perhitungan persentase degradasi ditunjukan pada Tabel 4.5 dan Gambar 4.5.
Tabel 4.5 Hasil Uji Kadar Air Membran No. Sampel
(%)
a (g)
b (g)
c (g)
Kadar Air %
1 I 22,20 24,25 23,60 31,7
2 II 41,39 43,39 42,80 29,5
3 III 21,82 23,97 23,29 26,9
Keterangan :
Sampel I : membran Kitosan-Kolagen-PVA 3:3:5% Sampel II : membran Kitosan-Kolagen-PVA 3:3:10% Sampel III : membran Kitosan-Kolagen-PVA 3:3:15% a : berat cawan kosong (g)
Gambar 4.5 Grafik hubungan konsentrasi PVA terhadap persen kadar air membran
Dari hasil uji hasil kadar tersebut memiliki kelembaban yang dibutuhkan untuk memdukung regenerasi sel dalam penyebuhan luka. Sesuai yang dikatakan Teresia Mutia, 2009. Semua variasi membran memiliki kadar air yang dapat memberi suasana kelembaban pada luka. Keseimbangan kelembaban pada permukaan balutan luka adalah faktor kunci dalam mengoptimalkan perbaikan jaringan; mengeliminasi eksudat dari luka yang berlebihan pada luka kronik yang merupakan bagian penting untuk permukaan luka. Untuk itu dikembangkan suatu metode perawatan luka dengan cara mempertahankan isolasi lingkungan luka agar tetap lembab dengan menggunakan balutan penahan kelembaban, yang dikenal dengan Moist Wound Healing (Tarigan, 2007).
4.1.5 Uji Daya Serap Air
Uji ketahanan terhadap air (swelling) dilakukan untuk mengetahui pengaruh variasi polivinil alkohol (PVA) pada membran yang terdiri dari kitosan-kolagen-PVA terhadap persen air yang diserap oleh membran. Hasil pengujian yang diperoleh berupa data berat sampel sebelum dan sesudah perendaman dalam akuades selama
24 jam. Data yang diperoleh dihitung nilai daya serapnya menggunakan persamaan (3-2). Hasil pengujian daya serap ditunjukkan Tabel 4.6.
Tabel 4.6 Data pengukuran berat serapan air
Sampel
Sampel I : membran Kitosan-Kolagen-PVA 3:3:5% Sampel II : membran Kitosan-Kolagen-PVA 3:3:10% Sampel III : membran Kitosan-Kolagen-PVA 3:3:15%
Gambar 4.6 menunjukkan bahwa menurunnya daya serap membran seiring dengan bertambahnya konsentrasi polivinil alkohol. Hal ini dikarenakan penambahan polivinil alkohol dapat mengakibatkan densitas membran semakin besar. Densitas yang besar menunjukkan pori-pori yang dimiliki oleh membran berukuran kecil sehingga daya absorpsinya menurun.
Gambar 4.6 Grafik hubungan konsentrasi polivinil alkohol terhadap daya serap membran
Menurut Saarai (2011), nilai swelling yang dapat digunakan untuk aplikasi pembalut luka yaitu antara 200-500%. Sehingga dari hasil penelitian yang didapat menunjukkan bahwa membran dengan konsentrasi PVA 5% dan 10% memiliki nilai swelling yang memenuhi syarat untuk aplikasi pembalut luka.
4.1.6. Uji Tarik Membran
Karakterisasi sifat mekanik perlu dilakukan untuk mengetahui kekuatan membran terhadap gaya yang berasal dari luar, yang dapat merusak membran. Data yang diperoleh dihitung nilai kekuatan tarik dan regangan menggunakan persamaan (3-3) dan (3-4). Hasil dari uji tarik dapat dilihat pada Tabel 4.7 dan Gambar 4.7
Tabel. 4.7. Data untuk mencari kekuatan tarik (N/mm2) dan reganggan (%) dengan L0 = 1100 mm
Sampel Load (kgf/mm2) Extention (mm-2
)
Kekuatan tarik (N/mm2)
Regangan (%)
I 0,02 40,086 0,196 3,64
II 0,30 55,353 1,44 5,03
III 0.51 65,802 5,292 6,89
Keterangan
L0 : panjang awal membran
Gambar 4.7 Grafik perbandingan antara konsentrasi polivinil alkohol dengan kekuatan tarik membran.
Kekuatan tarik pada saat putus (tegangan) meningkat dengan bertambah tingginya konsentrasi membran ki-ko-PVA.Membran dengan konsentrasi polivinil alkohol memiliki kekuatan tarik yang besar yaitu berkisar antara 0,1 hingga 5,2 N/mm2. Hal tersebut dikarenakan strukturnya yang rapat menyebabkan jarak antara molekul dalam membran semakin rapat sehingga mempunyai kekuatan tarik yang besar.Ini menunjukkan bahwa hydrogel memiliki kekuatan mekanik yang cukup dan bersifat fleksibel sehingga apabila digunakan pada bagian persendian tubuh tidak mengalami putus saat tubuh melakukan aktifitas (Darwis, D., 2005).
Suatu polimer yang dihasilkan semakin kuat dan kuat tarik intermolekulnya menjadi tinggi sehingga kemampuan merenggang dari film juga meningkat. Kekuatan tarik dan persen elongasi semakin tinggi dengan bertambahnya massa PVA dan konsentrasi pati. Peningkatan kekuatan tarik disebabkan pembentukan ikatan hidrogen antar molekul NH3+ pada stuktur kitosan dan OH- pada PVA. Gugus amino (NH2) akandiprotonasi menjadi NH3 dalam larutan asam asetat dan gugus OH- pada polivinil alkohol akan berikatan dengan NH3 membentuk ikatan hidrogen. Semakin tinggi konsentrasi polivinil alkohol yang ditambahkan menyebabkan larutan menjadi sangat kental dan rantai menjadi panjang, hal ini terkait dalam penelitian (Abu-Aid et all sebagaimana dikutip Riyanto, 2010) semakin panjang rantai polimer pada sampel menyebabkan pelepasan rantai monomer yang tidak mudah sehingga mempunyai elastisitas yang tinggi. Penambahan plasticizer mampu mengurangi kerapuhan (meningkatkan nilai kuat tarik) dan meningkatkan elastisitas film karena ikatan hidrogen antara molekul polimer yang berdekatan sehingga kekuatan tarik menarik intermolekul rantai polimer menjadi bertambah.
Dari uji yang telah dilakukan dapat diketahui membran yang memiliki karakteristik optimal berdasarkan perbandingan dari hasil uji-uji tersebut. Seperti yang ditunjukkan pada tabel 4.8
Tabel 4.8 Data karakteristik optimal
No. Uji Membran
Dari tabel 4.8 menunjukkan variasi membran yang terbaik terdapat pada sampel II. Hal itu terkait dengan nilai daya serap dan kekuatan mekanik yang didapat sesuai standar dan memadai sebagai aplikasi pembalut luka.
4.1.7. Uji FTIR terhadap membran kitosan-kolagen-polivinil alkohol
Tabel4.9 Hasil analisa gugus fungsi menggunakan FTIR
Gugus Fungsi Panjang Gelombang (cm-1) OH tumpang tindih dengan N-H stretching
C-H stretching N-H vibrasi
Amida NH2 (stretching) dari glukosamin amida NH asetilglukosamin
Vibrasi tekuk OH dan vibrasi ulur CN Vibrasi ulur C-O
Hasil analisa FTIR membran kitosan-kolagen-PVA 10% ditunjukkan pada Gambar 4.8 dan daftar gugus fungsi serta serapan gelombangnya secara lengkap ditunjukkan pada Tabel 4.9 . Dari spektrum IR tersebut terdapat puncak yang khas pada gugus OH tumpang tindih dengan N-H stretching pada daerah gelombang 3425,58 cm-1.. Mondal et al. (2012) menyatakan bahwa gugus OH- terdeteksi pada kisaran bilangan gelombang 3497 cm-1.Sedangkan spektrum IR NH vibrasi dari kitosan dicirikan dengan puncak pada daerah gelombang 1635,64 cm-1. Data ini sesuai dengan penelitian Nugroho et al. (2014) bahwas erapan khas kitosan terlihat pada bilangan gelombang 1635,64 cm-1 yang merupakan tekuk N-H yang menunjukkan keberadaan amina (-NH2) gugus amida NH2 pada panjang gelombang 2931,8 cm-1, pada pita serapan 1381,03 cm-1 menunjukkan adanya vibrasi tekuk –OH dan vibrasi ulur C-Ndan pita serapan pada 1041,56 cm-1 menunjukkan adanya vibrasi ulur C-O.
4.1.8 Hasil Uji Pre-Klinis
Tabel 4.10 Hasil pengukuran diameter luka mencit putih jantan hari ke 1-36
Hari ke Diameter Luka (cm)
Kontrol (K0) Perlakuan 1 (P1) Perlakuan 2 (P2)
0 1,75 1,95 1,87