PENCARIAN VARIAN GEN MIOSTATIN
PADA DOMBA KOMPOSIT SUMATERA
ANDALUSIA
DEPARTEMEN BIOLOGI
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
2
ABSTRAK
ANDALUSIA. Pencarian Varian Gen Miostatin Pada Domba Komposit Sumatera. Dibimbing oleh ACHMAD FARAJALLAH dan BESS TIESNAMURTI.
Domba komposit sumatera merupakan bentuk silangan domba lokal ekor tipis Sumatera (DETS) dengan domba St. Croix (SC) dan Barbados Blackbelly (BB) dengan komposisi 50% DETS: 25% SC: 25%BB (Subandriyo et al. 2000). Miostatin atau growth differentiations factor 8
(GDF 8) merupakan anggota dari superfamili transforming growth factor-β (TGF-β) berfungsi sebagai pengontrol negatif pertumbuhan otot (McPherron et al.1997). Mutasi gen miostatin dapat mengganggu ekspresi dan aktifitasnya sehingga otot kerangka akan mengalami hipertropi ataupun hiperplasia (pertumbuhan otot yang melebihi normal), hal ini dikenal dengan fenomena double muscling. Mutasi pada makhluk hidup dapat terjadi secara alami dalam jangka waktu yang panjang, sehingga menghasilkan varian-varian baru dari makhluk hidup tersebut. Hasil pencarian varian gen miostatin pada domba komposit sumatera menggunakan dengan metode PCR-RFLP dengan enzim restriksi Hae III dan Mbo I tidak menunjukkan adanya keragaman. Metode PCR-SSCP menunjukkan adanya varian gen miostatin ekson 3 pada domba komposit dalam penelitian ini yaitu W, X, Y, dan Z dengan frekuensi berturut-turut 3.62 %, 37.35 %, 37.35 %, dan 21.69 %. Berdasarkan hasil penelitian ini dapat disimpulkan bahwa tipe SSCP gen miostatin ekson 3 tidak nyata mempengaruhi tipe kelahiran, bobot lahir, bobot sapih, dan pertambahan bobot badan pada domba komposit sumatera.
Kata-kata kunci: Domba komposit sumatera, miostatin, PCR-RFLP, PCR-SSCP
ABSTRACT
ANDALUSIA. Exploring Myostatin Gene in Sumatera Composite Sheep. Under supervising of ACHMAD FARAJALLAH and BESS TIESNAMURTI.
Sumatera composite sheep is a synthetic breed of Sumatera thin tail (STT) sheep with St. Croix (SC) and Barbados Blackbelly (BB) with genetic constituent of 50% STT : 25% SC: 25%BB (Subandriyo et al. 2000). Myostatin or growth differentiations factor 8 (GDF 8) is a member from super family transforming growth factor-β (TGF-β) act as a feedback negative that controlling muscle growth (McPherron et al.1997). Mutation in myostatin gene interact with the expression and activity of muscle growth. It can cause hypertrophy or hyperplasia (abnormally muscle growth), known as double muscling. Naturally, mutation can occur in a long and slow process that produce new variants. The result from exploring the myostatin gene in Sumatera composite sheep by PCR-RFLP using Hae III and Mbo I restriction enzyme showed no differences among the samples. PCR-SSCP methods showed four variants in myostatin gene reside at exon 3 of Sumatera composite sheep which are W, X, Y,and Z (3.62 %, 37.35 %, 37.35 %, and 21.69 %, respectively). SSCP types of myostatin gene exon 3 were not significantly influencing birth type. It can be concluded that SSCP technique of myostatin gene at exon 3 did not significantly affect (P>0.05) litter size, birth weight as well as average daily gain of Sumatera Composite Sheep.
3
PENCARIAN VARIAN GEN MIOSTATIN
PADA DOMBA KOMPOSIT SUMATERA
ANDALUSIA
Skripsi
Sebagai salah satu syarat untuk memperoleh gelar
Sarjana Sains pada Departemen Biologi
DEPARTEMEN BIOLOGI
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
4
Judul Skripsi: Pencarian Varian Gen Miostatin Pada Domba Komposit Sumatera
Nama :
Andalusia
NRP
: G 34103059
Menyetujui:
Pembimbing I
Pembimbing II
Dr. Ir. Achmad Farajallah, M.Si
Dr. Ir. BessTiesnamurti
NIP 131878947
NIP 080063117
Mengetahui:
Dekan Fakultas Matematika dan Ilmu Pengetahuan Alam
Institut Pertanian Bogor
Prof. Dr. Ir. Yonny Koesmaryono, MS
NIP 131473999
5
PRAKATA
Puji dan syukur penulis panjatkan kepada Allah SWT yang telah melimpahkan rahmat, karunia, dan ridho-Nya sehingga penulis dapat menyelesaikan karya ilmiah dengan judul
Pencarian Varian Gen Miostatin Pada Domba Komposit Sumatera.
Terima kasih penulis ucapkan kepada Bapak Dr. Ir. Achmad Farajallah, M.Si dan Ibu Dr. Ir. Bess Tiesnamurti selaku pembimbing serta seluruh staf Departemen Biologi, khususnya Staf Zoologi yang telah bersedia memberikan bimbingan, fasilitas, saran dan masukkan dalam penyelesaian karya ilmiah ini.
Ucapan terimakasih juga penulis sampaikan kepada Mama, Daddy, dan Adik-adik: Cordova dan Sevilla atas curahan doa, cinta, kasih sayang, dukungan dan pengertiannya yang tulus selama ini. Tak lupa penulis ucapkan terimakasih kepada keluarga besar Agus MB dan Moechidin serta teman-teman di Biologi 39, 40, 41, 42, Zoologiers, Malabar 8, SMU 6 Jakarta, FOSMA, Teens, dan FKA ESQ 165 Bogor Raya, Bunda Gina, Bunda Wiwi, Bunda Noortje, Mba Fina dan sahabat-sahabatku yang tak dapat disebutkan satu persatu. Terima kasih untuk hari-hari indah, nasihat, spirit, motivasi dan perhatian yang selalu terjalin indah hingga saat ini.
Penulis menyadari bahwa karya tulis ini mungkin masih jauh dari sempurna. Oleh karena itu saran dan kritik yang membangun sangat diharapkan. Semoga karya ilmiah ini dapat memberikan tambahan informasi dan bermanfaat bagi masyarakat pertanian, khususnya peternakan.
Bogor, September 2007
6
RIWAYAT HIDUP
Penulis dilahirkan di Jakarta pada tanggal 12 Januari 1986 dari ayah Helmi Agus, SE dan ibu Muji Lestari. Penulis merupakan putri pertama dari tiga bersaudara.
Tahun 2003 penulis lulus dari SMU Negeri 6 Jakarta dan pada tahun yang sama lulus seleksi masuk IPB melalui jalur Undangan Seleksi Masuk IPB. Penulis memilih Program Studi Biologi Jurusan biologi, Fakultas Matematika dan Ilmu Pengetahuan Alam.
7
DAFTAR ISI
Halaman
DAFTAR TABEL... vii
DAFTAR GAMBAR... vii
PENDAHULUAN Latar Belakang ... 1
Tujuan ... 1
BAHAN DAN METODE Lokasi dan Waktu ... 1
Sampel DNA... 1
Amplifikasi DNA... 1
Elektroforesis dan Visualisasi DNA ... 2
PCR-RFLP ... 2
PCR-SSCP ... 2
Analisa Statistik ... 2
HASIL Amplifikasi DNA... 2
PCR-RFLP ... 2
PCR-SSCP ... 3
Respon Bobot Lahir, Bobot Sapih, Pertambahan Bobot Badan dan Tipe Kelahiran Terhadap Tipe SSCP Gen Miostatin Ekson 3 ... 3
PEMBAHASAN Amplifikasi DNA... 3
PCR-RFLP ... 4
PCR-SSCP ... 4
Respon Bobot Lahir, Bobot Sapih, Pertambahan Bobot Badan dan Tipe Kelahiran Terhadap Tipe SSCP Gen Miostatin Ekson 3 ... 4
SIMPULAN... 5
SARAN... 5
8
DAFTAR TABEL
Halaman
1 Tampilan Ternak Domba Komposit BALITNAK Bogor ... 3 2 Hasil Analisis Respon Tipe Kelahiran, Bobot Lahir, Bobot Sapih, Dan Pertambahan Bobot Badan Terhadap Tipe SSCP... ... 4
DAFTAR GAMBAR
Halaman
1 Hasil Amplifikasi Gen Miostatin Ekson 3. ... ... 2 2 Hasil Pemotongan Gen Miostatin Ekson 3 dengan Enzim Restriksi Hae III (A)Dan
Mbo I (B)... ... 2 3 Hasil Elektroforesis Produk PCR-SSCP Sampel Domba Komposit Sumatera, (B)
Interpretasi Migrasi Untai Tunggal Pita DNA Hasil Elektroforesis Produk
PCR-SSCP ... ... 3 4 Sekuen Gen Miostatin Ekson 3 Gabungan dari Ovis Aries (Domba) Dan
PENDAHULUAN
Latar Belakang
Domba merupakan salah satu hewan ternak populer di Indonesia setelah ayam, sapi dan kambing. Domba lokal di Indonesia dapat dibedakan menjadi beberapa jenis, antara lain domba ekor tipis, domba ekor gemuk, domba garut (Utoyo et al. 1996) dan domba sumatera (Priyanto et al. 1999). Beberapa hasil silangan antar jenis domba-domba tersebut banyak ditemukan dalam rangka meningkatkan kualitas produksi domba, misalnya laju pertumbuhan yang cepat, kualitas karkas, tahan penyakit dan sifat prolifik (kemampuan beranak lebih banyak). Salah satu domba hasil persilangan yang sengaja dirakit untuk meningkatkan laju pertumbuhan adalah domba komposit sumatera. Domba komposit sumatera merupakan hasil silangan domba lokal ekor tipis Sumatera (DETS) dengan domba St. Croix (SC) dan Barbados Blackbelly (BB) dengan komposisi 50% DETS: 25% SC: 25%BB (Subandriyo et al. 2000).
Miostatin atau growth differentiations factor 8 (GDF 8) merupakan anggota dari superfamili transforming growth factor-β (TGF-β) yang mengontrol pertumbuhan dan diferensiasi otot kerangka. Cara kerja miostatin dalam mengontrol pertumbuhan dan diferensiasi otot adalah dengan menghambat aktifitas miogenin. Miogenin yang tidak bekerja menyebabkan mioblas tidak dapat berdiferensiasi menjadi miotube. Miotube ini nantinya akan berkembang menjadi serabut otot. Dengan kata lain, miostatin berfungsi sebagai pengontrol negatif pertumbuhan otot. Miostatin diekspresikan oleh gen miostatin yang pada sapi terdapat pada kromosom No. 2 (McPherron et al.1997). Pada sebagian besar vertebrata, ekspresi gen miostatin terjadi pascanatal (McNally 2004). Jika gen miostatin mengalami mutasi yang mengganggu ekspresi dan/atau aktifitasnya, maka otot kerangka akan mengalami hipertropi (serabut otot bertambah besar) ataupun hiperplasia (jumlah serabut otot bertambah banyak). Fenomena
double muscling pada sapi Belgian Blue dan Piedmontese adalah salah satu contoh mutasi pada ekson ketiga gen miostatin sehingga otot mengalami pertumbuhan yang melebihi normal (McPherron et al.1997, Oldham et al.
2001). Walaupun jenis mutasi pada kedua sapi diatas berbeda, mutasi keduanya ternyata sama-sama mengganggu proses ekspresi gen akibat bergesernya kodon stop.
Mutasi pada makhluk hidup dapat terjadi secara alami dalam setiap gen dan dapat menyebabkan perubahan fisiologis atau morfologis yang semakin baik, semakin buruk, bahkan tidak menyebabkan perubahan sama sekali. Makhluk hidup yang mengalami mutasi ini disebut mutan. Mutan yang dapat bertahan hidup ini tentunya memiliki perbedaan dalam susunan nukleotida basa suatu gen sehingga di dalam populasi akan ada banyak keragaman (varian) dari makhluk hidup tersebut.
Tujuan
Penelitian ini bertujuan mencari varian gen miostatin pada domba komposit sumatera.
BAHAN DAN METODE
Lokasi dan Waktu
Penelitian ini dilaksanakan mulai bulan Januari sampai Juni 2007 di Laboratorium Zoologi, Departemen Biologi Fakultas Matematika dan Ilmu Pengetahuan Alam Institut Pertanian Bogor (FMIPA IPB).
Sampel DNA
Sampel DNA domba yang digunakan dalam penelitian ini merupakan koleksi DNA dalam EtOH yang diekstraksi dari darah domba komposit sumatera yang laju pertumbuhannya sudah dikarakterisasi dengan baik (koleksi Dr. Bess Tiesnamurti BALITNAK Bogor yang disimpan di Laboratorium Zoologi, Departemen Biologi FMIPA IPB). Sampel yang tersedia berjumlah 89 sampel yang terdiri dari jenis M (komposit sumatera) hasil persilangan antara DETS, SC dan BB.
Amplifikasi DNA
Amplifikasi DNA secara in vitro
menggunakan mesin TaKaRa Thermal Cycler. Sepasang primer yang digunakan untuk mengamplifikasi ruas ekson ketiga gen miostatin sebesar 610 pb mengikuti Tellgren
2
predenaturasi 92 oC selama 10 menit, denaturasi 94 oC selama 4 menit, penempelan primer pada suhu 51 oC selama 1 menit, pemanjangan ruas target pada suhu 72 oC selama 2 menit, dan pemanjangan akhir pada 72 oC selama 7 menit .
yij = Variabel terikat (tipe kelahiran,
bobot lahir, bobot sapih, dan pertambahan bobot badan.)
μ = Rataan umum
ai = Variabel bebas (tipe pita DNA) εi j = Galat eror
Elektroforesis dan Visualisasi DNA
Produk PCR diuji menggunakan PAGE 6% (polyacrylamide gel electrophoresis) yang dilanjutkan dengan pewarnaan perak mengikuti Tegelstrom (1986) yang dimodifikasi oleh Farajallah et al. (1998).
HASIL
Amplifikasi DNA
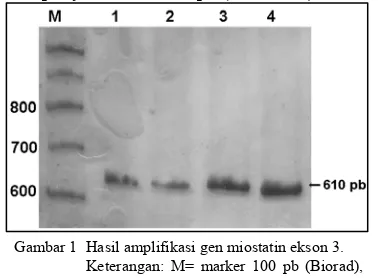
Produk PCR hasil amplifikasi menggunakan primer M03-30 dan M03-33 mempunyai ukuran 610 pb (Gambar 1).
PCR-RFLP
Gambar 1 Hasil amplifikasi gen miostatin ekson 3. Keterangan: M= marker 100 pb (Biorad), kolom 1 – 4: produk PCR
Produk PCR kemudian dipotong menggunakan enzim restriksi HaeIII dan
MboI mengikuti petunjuk produsen (NewEngland Biolabs). Pola pita hasil pemotongan enzim restriksi diuji menggunakan PAGE 6% yang dilanjutkan dengan pewarnaan perak.
PCR-SSCP
Produk PCR dimurnikan dengan metode pengendapan alkohol. Sebanyak 20 μl produk PCR ditambah dengan 5M NaCl 2 μl dan alkohol absolut 200 μl kemudian diinkubasi semalaman dalam suhu -20 oC. Molekul DNA diendapkan dengan sentrifuse selama 5 menit pada kecepatan 8000 rpm. Endapan DNA kemudian disuspensikan dengan larutan formamida 25 μl (formamida solution 80%, EDTA 10 mM bromtimol blue 1 mg/mL, dan xylene cyanol 1mg/mL) dan direndam dalam
water bath bersuhu 94 oC selama ± 10 menit agar untai ganda DNA terpisah menjadi untai tunggal (single strand). Setelah 10 menit sampel dipindahkan dengan cepat ke dalam
ice bath selama ± 5 menit untuk mencegah kedua untai yang sudah terpisah menyatu kembali. Konformasi untai tunggal kemudian diuji dengan PAGE 12% (akrilamid:bis akrilamid = 59:1). Elektroforesis dijalankan dengan kekuatan listrik sebesar 150 volt selama 240 menit pada suhu konstan 4 oC. Visualisasi dilakukan dengan pewarnaan perak seperti pada visualisasi produk PCR.
PCR-RFLP
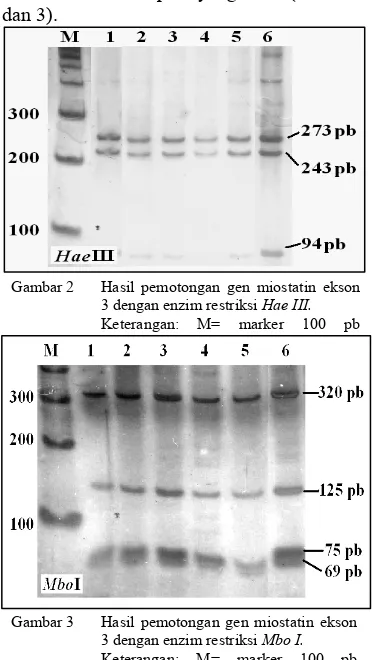
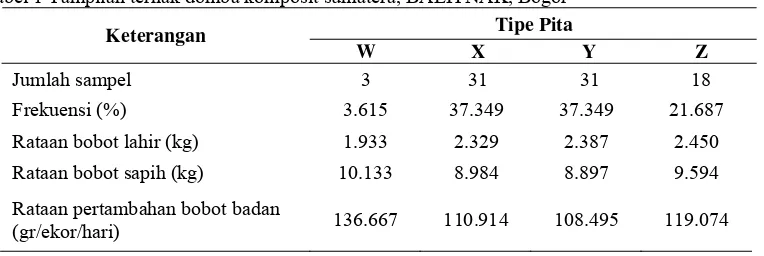
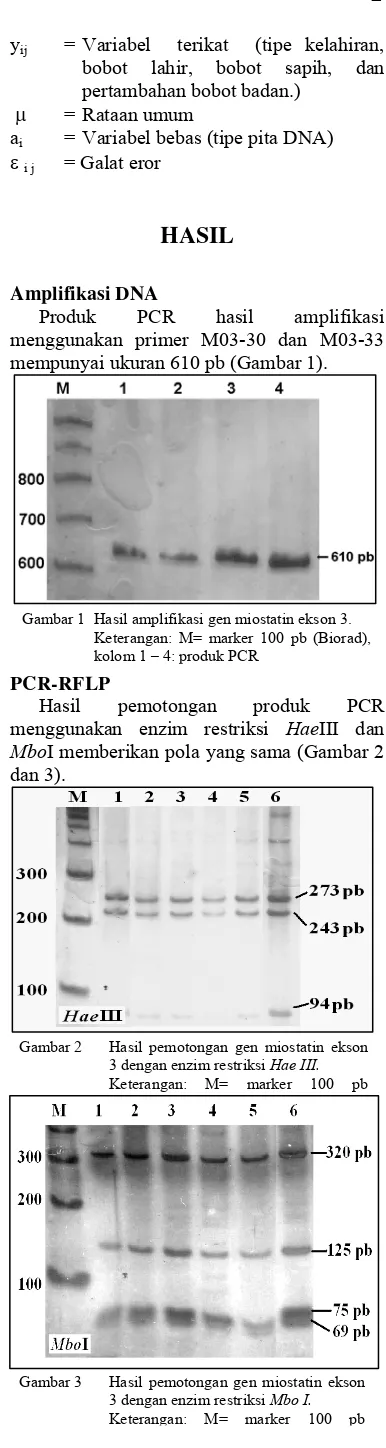
Hasil pemotongan produk PCR menggunakan enzim restriksi HaeIII dan
MboI memberikan pola yang sama (Gambar 2
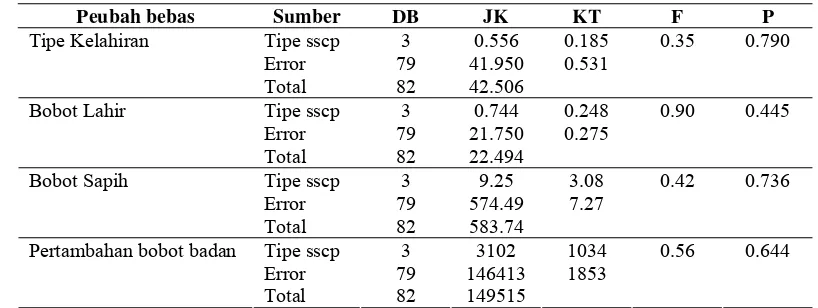
Gambar 2 Hasil pemotongan gen miostatin ekson 3 dengan enzim restriksi Hae III. Keterangan: M= marker 100 pb dan 3).
Gambar 3 Hasil pemotongan gen miostatin ekson 3 dengan enzim restriksi Mbo I. Keterangan: M= marker 100 pb
Analisa statistik
Uji statistik dilakukan untuk melihat keterpautan tipe gen dengan beberapa karakter ternak dengan model linier umum menggunakan program Minitab 14.
Model matematis yang diajukan adalah: yij = μ + ai + εi j
3
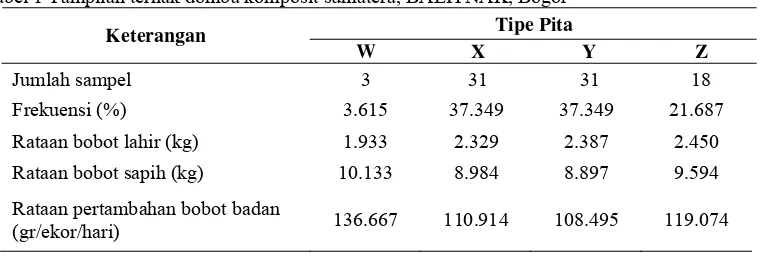
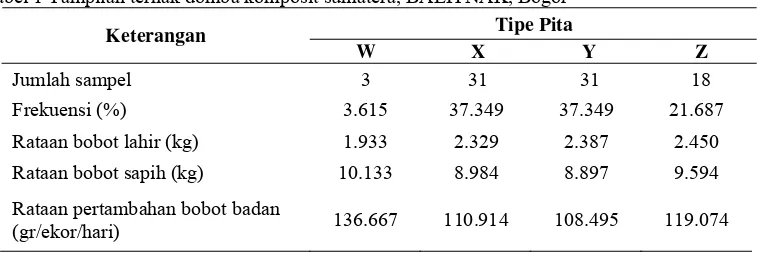
Tabel 1 T
Gambar 5 Sekuen gen miostatin ekson 3 gabungan dari Ovis aries (domba) dan Bos taurus (sapi). Sumber: www.ncbi.nlm.nih.gov
ampilan ternak domba komposit sumatera, BALITNAK, Bogor
Tipe Pita Keterangan
W X Y Z
Jumlah sampel 3 31 31 18
Frekuensi (%) 3.615 37 37 21
hir (kg)
t badan
136.667 110.914 108.495 119.074
.349 .349 .687
Rataan bobot la 1.933 2.329 2.387 2.450
Rataan bobot sapih (kg) 10.133 8.984 8.897 9.594
Rataan pertambahan bobo (gr/ekor/hari)
CR-SSCP
i DNA hasil SSCP dari 88 sam
Analisis SSCP memberikan hasil adanya var
Jenis kelam ibu, dan b
semua tipe kelamin betina. Selain u, jika ditelusuri menurut induknya bapak dan ibu berbangsa BC (Barbados x Croix) memiliki anak yang semuanya bertipe Z.
Re
ahan obot badan sebagai peubah terikat. Hasil
AHASAN
P
Visualisas
pel domba komposit menunjukkan adanya keragaman tipe DNA (polimorfik). Tipe-tipe DNA ini kemudian dikelompokkan menjadi empat tipe berdasarkan bentuk pemisahan rantai DNAnya yaitu W,X,Y, dan Z (Gambar 4).
ian/keragaman pola tipe pada gen miostatin ekson 3 (polimorfik), keempat tipe tersebut yaitu W=3 sampel, X=31 sampel, Y=31 sampel, dan Z=18 sampel. Frekuensi keempat pola tipe pita hasil SSCP tersebut adalah 3.615 % (W), 37.349 % (X), 37.349 % (Y), dan 21.687% (Z) (Tabel 1).
Perbandingan hasil SSCP ini dengan data sekunder milik BALITNAK Bogor (Jenis,
in, jenis domba komposit, bangsa angsa bapak). Menunjukkan bahwa
W berjenis it
spon Bobot lahir, Bobot Sapih, Pertambahan Bobot Badan dan Tipe Kelahiran Terhadap Tipe SSCP Gen Miostatin Ekson 3.
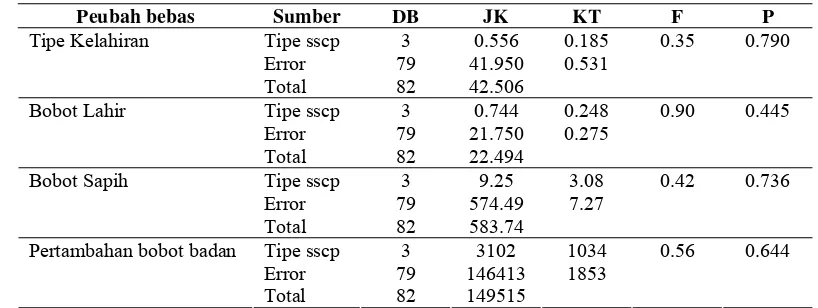
Analisis dilakukan dengan uji statistik model linier umum yaitu dengan tipe SSCP sebagai peubah bebas serta tipe kelahiran, bobot lahir, bobot sapih, dan pertamb b
analisis disajikan dalam Tabel 2.
PEMB
Amplifikasi DNA
Ukuran produk PCR sepanjang 610 pb sesuai dengan sekuen DNA miostatin domba dan sapi yang disimpan dalam GenBank
.ncbi.nlm.gov
(www no. acc. AF266758 dan B076403).
A Gambar 4 (A) Hasil elektroforesis produk PCR-SSCP
4
Tabel 2 is respo ahira bot la obot s dan p mbahan bot terhadap tip
Peubah bebas er KT
Hasil analis n tipe kel n, bo hir, b apih, erta bo badan e SSCP
Sumb DB JK F P
Tipe sscp 3 0.556 0.185 0.35 0.790
Error 79 41.950 0.531
Tipe Kelahiran
Total 82 42.506
Tipe sscp 3 0.744 0.248 0.90 0.445
Error 79 21.750 0.275
Bobot Lahir
Total 82 22.494
Tipe sscp 3 9.25 3.08 0.42 0.736
Error 79 574.49 7.27
Bobot Sapih
Total 82 583.74
Tipe sscp 3 3102 1034 0.56 0.644 Error 79
Pertambahan bobot badan
146413 1853
149515
Total 82
PCR-RFLP
Pola yang sama pada hasil pemotongan produk PCR menggunakan enzim restriksi
HaeIII dan MboI memberikan arti bahwa sek
a selain sapi lebih terjaga dan sta l. Untuk mencari varian gen miostatin lakuan dengan metode deteksi PC ariasi sek pada gen miost (Jenis, Jenis kel min, jenis domba komposit, bangsa
erasal dari bapak dan ibu ber
bahwa mutasi ini tidak emiliki pengaruh pada fungsi protein miostatin dalam miogenesis. Walaupun begitu, usaha-usaha pencarian varian gen tetap harus bisa mencakup keseluruhan gen target uen DNA yang menjadi pengenal kedua
enzim tersebut sama pada semua sampel domba yang dianalisis.
Eksplorasi berbagai situs enzim retsriksi lain yang dilakukan dengan analisis homologi dari berbagai sekuen gen miostatin yang disimpan dalam Gen Bank tidak berpeluang untuk bisa menemukan keragaman gen miostatin lebih lanjut (data tidak diperlihatkan). Selain itu, Cieslak et al. (2003) melaporkan bahwa bagian ekson gen miostatin pad
bi
lebih lanjut di R-SSCP.
PCR-SSCP
Single-Strand Conformation Polymorphisms (SSCPs) adalah metode
elektroforesis yang populer untuk mengidentifikasi mutasi sekuen karena mudah, murah dan memiliki sensitifitas tinggi walau hanya satu nukleotida saja (Nataraj 1999) dapat mendeteksi polimorfisme dan mutasi titik pada berbagai posisi dalam fragmen DNA, meskipun mutasi yag terjadi hanya pada satu basa. (Orita et al.1998). Kesensitifitasan dari analsis SSCP merupakan hal yang cukup sulit dalam teknik karena sangat peka seperti kondisi elektroforesis, sensitifitas dipengaruhi beberapa faktor termasuk didalamnya tipe subtitusi basa, panjang fragmen, sekuen basa, kandungan G dan C dalam fragmen dan lokasi v
uen, tidak ada teori yang tepat memprediksi apakah SSCP dapat mendeteksi mutasi tertentu (Highsmith et al. 1999).
Analisis SSCP memberikan hasil adanya varian/keragaman pola tipe
atin ekson 3 (polimorfik), keempat tipe tersebut yaitu W=3 sampel, X=31 sampel, Y=31 sampel, dan Z=18 sampel. Frekuensi keempat pola tipe pita hasil SSCP tersebut adalah 3.62 % (W), 37.35 % (X), 37.35 % (Y), dan 21.69 % (Z) (Tabel 1).
Perbandingan hasil SSCP ini dengan data sekunder milik BALITNAK Bogor
a
ibu, dan bangsa bapak) menunjukkan bahwa semua tipe Z dan W berjenis kelamin betina. Selain itu, semua tipe Z jika ditelusuri menurut induknya b
bangsa BC (Barbados x St.Croix).
Respon Bobot Lahir, Bobot Sapih, Pertambahan Bobot Badan dan Tipe Kelahiran Terhadap Tipe SSCP Gen Miostatin Ekson 3
Hasil analisis menunjukkan bahwa tipe-tipe SSCP gen miostatin ekson 3 yang ditemukan dalam penelitian ini tidak terpaut dengan tipe kelahiran, bobot lahir, bobot sapih, dan pertambahan bobot badan. Sebagaimana telah disampaikan oleh Cockett
et al. (2001) bahwa fenomena hipertropi otot pada domba Texel terpaut dengan mutasi gen miostatin dibagian promotor. Hal yang sama juga ditemukan pada fenomena hipertropi pada babi (Cieslak et al. 2003). Kelebihan otot pada babi ditemukan sebagai konsekuensi dari hipertropi otot, khususnya pada babi jenis Pietrain dan Belgian Landrace, namun perbedaan ciri-ciri karkas dan genotip mengindikasikan
5
mulai dari p dan ekson
(Dunner 2003).
bahwa tipe SSCP gen miostatin ekson 3 tidak nyata mempengaruhi tipe kelahiran, bobot lahir, bobot sapih, dan an bobot badan pada domba komposi ra.
miostatin yang lebih lua
yang diperoleh dari penelitian tersebut bisa diguna n untuk mendeteksi keterpautannya
dengan t bobot
sapih, dan pertambaha obot badan.
Cies harsi T, Kapelanski W,
h J anim Sci
Coc
ted review].
Dun
Fara
Air Tawar (Reptilia: Testudines) di Indonesia Sebagai Dasar Pelestarian dan
litian dan
Hig
f
McN s –
McP
due to mutations in the
Nata
analysis for gel-based
Old Orit ingle-strand Priy domba Sub omba rambut Teg riation based Tell ants predates Uto
Animal Diversity in Indonesia. Jakarta: Ministry of Ari
romotor, intron
SIMPULAN
Varian gen miostatin ekson 3 dengan menggunakan metode PCR-RFLP dengan enzim restriksi Hae III dan Mbo I tidak menunjukkan adanya keragaman. Metode PCR-SSCP menunjukkan adanya varian gen miostatin ekson 3 pada domba komposit dalam penelitian ini yaitu W, X, Y, dan Z dengan frekuensi berturut-turut 3.62 %, 37.35 %, 37.35 %, dan 21.69 %. Berdasarkan hasil penelitian ini dapat disimpulkan
pertambah t sumate
SARAN
Pencarian varian gen
s perlu dilakukan pada populasi domba-domba lokal Indonesia sebagai manifestasi dari proses adaptasi domba-omba tersebut di wilayah tropis Indnesia.
Penelitian lebih lanjut terhadap varian gen miostatin ekson 3 yang ditemukan dalam penelitian ini perlu diverifikasi dengan sekuensing. Selain itu, tipe-tipe
ka
ipe kelahiran, bobot lahir, n b
DAFTAR PUSTAKA
lak D, Blic
Pierzchala M. 2003. Investigation of polymorphisms in the porcine myostatin (GDF8; MSTN) gene. Czec
48(2):69-75.
kett NE, Shay TL, Smit M. 2001. Analysis of the sheep genome [invi
Physiol Genomics 7:69-78.
ner et al. 2003. Haplotype diversity of the myostatin gene among beef cattle breeds.
Genet Sel Evol 35: 103-118.
jallah A, Suryobroto B, Puntorini T. 1998. Analisis Keragaman Genetik dan Filogeni Molekular Bangsa Kura-Kura
Pemanfaatannya. Laporan Pelaksanaan RUT V/1. Lembaga Pene
Pengabdian Pada Masyarakat Institut Pertanian Bogor. Bogor: IPB.
hsmith et al. 1999. Use of DNA toolbox for the characterization of mutation scanning methods. II: Evaluation o single-strand conformation polymorphism analysis. Electrophoresis 20:1195-1203.
ally EM. 2004. Powerful gene myostatin regulation of human muscle mass. N Engl J Med 350:2642-2644. herron AC, Lee SJ. 1997. Double muscling in cattle
myostatin gene. Proc Natl Acad Sci USA
94:12457-12461.
raj AJ, Glander IO, Kusukawa N. Highsmith WE. 1999. Single-strand conformation polymorphism and heteroduplex
mutation detection. Electrophoresis
20:117-1185.
ham et al. 2001. Molecular expression of myostatin and MyoD is greater in double-muscled than normal-double-muscled cattle fetuses. Am J Physiol Regulatory Integrative Comp Physiol 280:1488-1493. a M, Iwahana A, Kanazawa H, Hayashi K,
Sekiya T. 1998. Detection of polymorphisms of human DNA by gel electrophoresis as s
conformation polymorphisms. Proc Natl Acad Sci USA 86:2766-2770.
anto D, Siregar AR, Handiwirawan E, Subandriyo. 1999. Karakter domba introduksi dan pola konservasi
lokal sumatera di Sumatera Utara. Ilmu Ternak dan Veteriner 5(1):12-22.
andriyo, Setiadi B, Handiwirawan E, Suparyanto A. 2000. Performa domba komposit hasil persilangan antara domba lokal sumatera dengan d
pada kondisi dikandangkan. Ilmu Ternak dan Veteriner 5(2):73-83.
elstrom H. 1986. Mitokondrial DNA in natural population: an improved routine for screening of genetic va
on sensitive silver staining.
Electrophoresis 7:226-229.
gren A, Berglund A, Savolainen P, Janis CM, Liberles DA. 2004. Myostatin rapid sequence evolution in rumin
domestication. Molecular Phylogenetics and Evolution 33:782-790.
yo DP, Djarsanto, Nasution SN. 1996. Animal Genetic Resources and Domestic
PENCARIAN VARIAN GEN MIOSTATIN
PADA DOMBA KOMPOSIT SUMATERA
ANDALUSIA
DEPARTEMEN BIOLOGI
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
2
ABSTRAK
ANDALUSIA. Pencarian Varian Gen Miostatin Pada Domba Komposit Sumatera. Dibimbing oleh ACHMAD FARAJALLAH dan BESS TIESNAMURTI.
Domba komposit sumatera merupakan bentuk silangan domba lokal ekor tipis Sumatera (DETS) dengan domba St. Croix (SC) dan Barbados Blackbelly (BB) dengan komposisi 50% DETS: 25% SC: 25%BB (Subandriyo et al. 2000). Miostatin atau growth differentiations factor 8 (GDF 8) merupakan anggota dari superfamili transforming growth factor-ȕ (TGF-ȕ) berfungsi sebagai pengontrol negatif pertumbuhan otot (McPherron et al.1997). Mutasi gen miostatin dapat mengganggu ekspresi dan aktifitasnya sehingga otot kerangka akan mengalami hipertropi ataupun hiperplasia (pertumbuhan otot yang melebihi normal), hal ini dikenal dengan fenomena double muscling. Mutasi pada makhluk hidup dapat terjadi secara alami dalam jangka waktu yang panjang, sehingga menghasilkan varian-varian baru dari makhluk hidup tersebut. Hasil pencarian varian gen miostatin pada domba komposit sumatera menggunakan dengan metode PCR-RFLP dengan enzim restriksi Hae III dan Mbo I tidak menunjukkan adanya keragaman. Metode PCR-SSCP menunjukkan adanya varian gen miostatin ekson 3 pada domba komposit dalam penelitian ini yaitu W, X, Y, dan Z dengan frekuensi berturut-turut 3.62 %, 37.35 %, 37.35 %, dan 21.69 %. Berdasarkan hasil penelitian ini dapat disimpulkan bahwa tipe SSCP gen miostatin ekson 3 tidak nyata mempengaruhi tipe kelahiran, bobot lahir, bobot sapih, dan pertambahan bobot badan pada domba komposit sumatera.
Kata-kata kunci: Domba komposit sumatera, miostatin, PCR-RFLP, PCR-SSCP
ABSTRACT
ANDALUSIA. Exploring Myostatin Gene in Sumatera Composite Sheep. Under supervising of ACHMAD FARAJALLAH and BESS TIESNAMURTI.
Sumatera composite sheep is a synthetic breed of Sumatera thin tail (STT) sheep with St. Croix (SC) and Barbados Blackbelly (BB) with genetic constituent of 50% STT : 25% SC: 25%BB (Subandriyo et al. 2000). Myostatin or growth differentiations factor 8 (GDF 8) is a member from super family transforming growth factor-ȕ (TGF-ȕ) act as a feedback negative that controlling muscle growth (McPherron et al.1997). Mutation in myostatin gene interact with the expression and activity of muscle growth. It can cause hypertrophy or hyperplasia (abnormally muscle growth), known as double muscling. Naturally, mutation can occur in a long and slow process that produce new variants. The result from exploring the myostatin gene in Sumatera composite sheep by PCR-RFLP using Hae III and Mbo I restriction enzyme showed no differences among the samples. PCR-SSCP methods showed four variants in myostatin gene reside at exon 3 of Sumatera composite sheep which are W, X, Y,and Z (3.62 %, 37.35 %, 37.35 %, and 21.69 %, respectively). SSCP types of myostatin gene exon 3 were not significantly influencing birth type. It can be concluded that SSCP technique of myostatin gene at exon 3 did not significantly affect (P>0.05) litter size, birth weight as well as average daily gain of Sumatera Composite Sheep.
PENDAHULUAN
Latar Belakang
Domba merupakan salah satu hewan ternak populer di Indonesia setelah ayam, sapi dan kambing. Domba lokal di Indonesia dapat dibedakan menjadi beberapa jenis, antara lain domba ekor tipis, domba ekor gemuk, domba garut (Utoyo et al. 1996) dan domba sumatera (Priyanto et al. 1999). Beberapa hasil silangan antar jenis domba-domba tersebut banyak ditemukan dalam rangka meningkatkan kualitas produksi domba, misalnya laju pertumbuhan yang cepat, kualitas karkas, tahan penyakit dan sifat prolifik (kemampuan beranak lebih banyak). Salah satu domba hasil persilangan yang sengaja dirakit untuk meningkatkan laju pertumbuhan adalah domba komposit sumatera. Domba komposit sumatera merupakan hasil silangan domba lokal ekor tipis Sumatera (DETS) dengan domba St. Croix (SC) dan Barbados Blackbelly (BB) dengan komposisi 50% DETS: 25% SC: 25%BB (Subandriyo et al. 2000).
Miostatin atau growth differentiations factor 8 (GDF 8) merupakan anggota dari superfamili transforming growth factor-β (TGF-β) yang mengontrol pertumbuhan dan diferensiasi otot kerangka. Cara kerja miostatin dalam mengontrol pertumbuhan dan diferensiasi otot adalah dengan menghambat aktifitas miogenin. Miogenin yang tidak bekerja menyebabkan mioblas tidak dapat berdiferensiasi menjadi miotube. Miotube ini nantinya akan berkembang menjadi serabut otot. Dengan kata lain, miostatin berfungsi sebagai pengontrol negatif pertumbuhan otot. Miostatin diekspresikan oleh gen miostatin yang pada sapi terdapat pada kromosom No. 2 (McPherron et al.1997). Pada sebagian besar vertebrata, ekspresi gen miostatin terjadi pascanatal (McNally 2004). Jika gen miostatin mengalami mutasi yang mengganggu ekspresi dan/atau aktifitasnya, maka otot kerangka akan mengalami hipertropi (serabut otot bertambah besar) ataupun hiperplasia (jumlah serabut otot bertambah banyak). Fenomena
double muscling pada sapi Belgian Blue dan Piedmontese adalah salah satu contoh mutasi pada ekson ketiga gen miostatin sehingga otot mengalami pertumbuhan yang melebihi normal (McPherron et al.1997, Oldham et al.
2001). Walaupun jenis mutasi pada kedua sapi diatas berbeda, mutasi keduanya ternyata sama-sama mengganggu proses ekspresi gen akibat bergesernya kodon stop.
Mutasi pada makhluk hidup dapat terjadi secara alami dalam setiap gen dan dapat menyebabkan perubahan fisiologis atau morfologis yang semakin baik, semakin buruk, bahkan tidak menyebabkan perubahan sama sekali. Makhluk hidup yang mengalami mutasi ini disebut mutan. Mutan yang dapat bertahan hidup ini tentunya memiliki perbedaan dalam susunan nukleotida basa suatu gen sehingga di dalam populasi akan ada banyak keragaman (varian) dari makhluk hidup tersebut.
Tujuan
Penelitian ini bertujuan mencari varian gen miostatin pada domba komposit sumatera.
BAHAN DAN METODE
Lokasi dan Waktu
Penelitian ini dilaksanakan mulai bulan Januari sampai Juni 2007 di Laboratorium Zoologi, Departemen Biologi Fakultas Matematika dan Ilmu Pengetahuan Alam Institut Pertanian Bogor (FMIPA IPB).
Sampel DNA
Sampel DNA domba yang digunakan dalam penelitian ini merupakan koleksi DNA dalam EtOH yang diekstraksi dari darah domba komposit sumatera yang laju pertumbuhannya sudah dikarakterisasi dengan baik (koleksi Dr. Bess Tiesnamurti BALITNAK Bogor yang disimpan di Laboratorium Zoologi, Departemen Biologi FMIPA IPB). Sampel yang tersedia berjumlah 89 sampel yang terdiri dari jenis M (komposit sumatera) hasil persilangan antara DETS, SC dan BB.
Amplifikasi DNA
Amplifikasi DNA secara in vitro
menggunakan mesin TaKaRa Thermal Cycler. Sepasang primer yang digunakan untuk mengamplifikasi ruas ekson ketiga gen miostatin sebesar 610 pb mengikuti Tellgren
PENDAHULUAN
Latar Belakang
Domba merupakan salah satu hewan ternak populer di Indonesia setelah ayam, sapi dan kambing. Domba lokal di Indonesia dapat dibedakan menjadi beberapa jenis, antara lain domba ekor tipis, domba ekor gemuk, domba garut (Utoyo et al. 1996) dan domba sumatera (Priyanto et al. 1999). Beberapa hasil silangan antar jenis domba-domba tersebut banyak ditemukan dalam rangka meningkatkan kualitas produksi domba, misalnya laju pertumbuhan yang cepat, kualitas karkas, tahan penyakit dan sifat prolifik (kemampuan beranak lebih banyak). Salah satu domba hasil persilangan yang sengaja dirakit untuk meningkatkan laju pertumbuhan adalah domba komposit sumatera. Domba komposit sumatera merupakan hasil silangan domba lokal ekor tipis Sumatera (DETS) dengan domba St. Croix (SC) dan Barbados Blackbelly (BB) dengan komposisi 50% DETS: 25% SC: 25%BB (Subandriyo et al. 2000).
Miostatin atau growth differentiations factor 8 (GDF 8) merupakan anggota dari superfamili transforming growth factor-β (TGF-β) yang mengontrol pertumbuhan dan diferensiasi otot kerangka. Cara kerja miostatin dalam mengontrol pertumbuhan dan diferensiasi otot adalah dengan menghambat aktifitas miogenin. Miogenin yang tidak bekerja menyebabkan mioblas tidak dapat berdiferensiasi menjadi miotube. Miotube ini nantinya akan berkembang menjadi serabut otot. Dengan kata lain, miostatin berfungsi sebagai pengontrol negatif pertumbuhan otot. Miostatin diekspresikan oleh gen miostatin yang pada sapi terdapat pada kromosom No. 2 (McPherron et al.1997). Pada sebagian besar vertebrata, ekspresi gen miostatin terjadi pascanatal (McNally 2004). Jika gen miostatin mengalami mutasi yang mengganggu ekspresi dan/atau aktifitasnya, maka otot kerangka akan mengalami hipertropi (serabut otot bertambah besar) ataupun hiperplasia (jumlah serabut otot bertambah banyak). Fenomena
double muscling pada sapi Belgian Blue dan Piedmontese adalah salah satu contoh mutasi pada ekson ketiga gen miostatin sehingga otot mengalami pertumbuhan yang melebihi normal (McPherron et al.1997, Oldham et al.
2001). Walaupun jenis mutasi pada kedua sapi diatas berbeda, mutasi keduanya ternyata sama-sama mengganggu proses ekspresi gen akibat bergesernya kodon stop.
Mutasi pada makhluk hidup dapat terjadi secara alami dalam setiap gen dan dapat menyebabkan perubahan fisiologis atau morfologis yang semakin baik, semakin buruk, bahkan tidak menyebabkan perubahan sama sekali. Makhluk hidup yang mengalami mutasi ini disebut mutan. Mutan yang dapat bertahan hidup ini tentunya memiliki perbedaan dalam susunan nukleotida basa suatu gen sehingga di dalam populasi akan ada banyak keragaman (varian) dari makhluk hidup tersebut.
Tujuan
Penelitian ini bertujuan mencari varian gen miostatin pada domba komposit sumatera.
BAHAN DAN METODE
Lokasi dan Waktu
Penelitian ini dilaksanakan mulai bulan Januari sampai Juni 2007 di Laboratorium Zoologi, Departemen Biologi Fakultas Matematika dan Ilmu Pengetahuan Alam Institut Pertanian Bogor (FMIPA IPB).
Sampel DNA
Sampel DNA domba yang digunakan dalam penelitian ini merupakan koleksi DNA dalam EtOH yang diekstraksi dari darah domba komposit sumatera yang laju pertumbuhannya sudah dikarakterisasi dengan baik (koleksi Dr. Bess Tiesnamurti BALITNAK Bogor yang disimpan di Laboratorium Zoologi, Departemen Biologi FMIPA IPB). Sampel yang tersedia berjumlah 89 sampel yang terdiri dari jenis M (komposit sumatera) hasil persilangan antara DETS, SC dan BB.
Amplifikasi DNA
Amplifikasi DNA secara in vitro
menggunakan mesin TaKaRa Thermal Cycler. Sepasang primer yang digunakan untuk mengamplifikasi ruas ekson ketiga gen miostatin sebesar 610 pb mengikuti Tellgren
2
predenaturasi 92 oC selama 10 menit, denaturasi 94 oC selama 4 menit, penempelan primer pada suhu 51 oC selama 1 menit, pemanjangan ruas target pada suhu 72 oC selama 2 menit, dan pemanjangan akhir pada 72 oC selama 7 menit .
yij = Variabel terikat (tipe kelahiran,
bobot lahir, bobot sapih, dan pertambahan bobot badan.)
μ = Rataan umum
ai = Variabel bebas (tipe pita DNA) εi j = Galat eror
Elektroforesis dan Visualisasi DNA
Produk PCR diuji menggunakan PAGE 6% (polyacrylamide gel electrophoresis) yang dilanjutkan dengan pewarnaan perak mengikuti Tegelstrom (1986) yang dimodifikasi oleh Farajallah et al. (1998).
HASIL
Amplifikasi DNA
Produk PCR hasil amplifikasi menggunakan primer M03-30 dan M03-33 mempunyai ukuran 610 pb (Gambar 1).
PCR-RFLP
Gambar 1 Hasil amplifikasi gen miostatin ekson 3. Keterangan: M= marker 100 pb (Biorad), kolom 1 – 4: produk PCR
Produk PCR kemudian dipotong menggunakan enzim restriksi HaeIII dan
MboI mengikuti petunjuk produsen (NewEngland Biolabs). Pola pita hasil pemotongan enzim restriksi diuji menggunakan PAGE 6% yang dilanjutkan dengan pewarnaan perak.
PCR-SSCP
Produk PCR dimurnikan dengan metode pengendapan alkohol. Sebanyak 20 μl produk PCR ditambah dengan 5M NaCl 2 μl dan alkohol absolut 200 μl kemudian diinkubasi semalaman dalam suhu -20 oC. Molekul DNA diendapkan dengan sentrifuse selama 5 menit pada kecepatan 8000 rpm. Endapan DNA kemudian disuspensikan dengan larutan formamida 25 μl (formamida solution 80%, EDTA 10 mM bromtimol blue 1 mg/mL, dan xylene cyanol 1mg/mL) dan direndam dalam
water bath bersuhu 94 oC selama ± 10 menit agar untai ganda DNA terpisah menjadi untai tunggal (single strand). Setelah 10 menit sampel dipindahkan dengan cepat ke dalam
ice bath selama ± 5 menit untuk mencegah kedua untai yang sudah terpisah menyatu kembali. Konformasi untai tunggal kemudian diuji dengan PAGE 12% (akrilamid:bis akrilamid = 59:1). Elektroforesis dijalankan dengan kekuatan listrik sebesar 150 volt selama 240 menit pada suhu konstan 4 oC. Visualisasi dilakukan dengan pewarnaan perak seperti pada visualisasi produk PCR.
PCR-RFLP
Hasil pemotongan produk PCR menggunakan enzim restriksi HaeIII dan
MboI memberikan pola yang sama (Gambar 2
Gambar 2 Hasil pemotongan gen miostatin ekson 3 dengan enzim restriksi Hae III. Keterangan: M= marker 100 pb dan 3).
Gambar 3 Hasil pemotongan gen miostatin ekson 3 dengan enzim restriksi Mbo I. Keterangan: M= marker 100 pb
Analisa statistik
Uji statistik dilakukan untuk melihat keterpautan tipe gen dengan beberapa karakter ternak dengan model linier umum menggunakan program Minitab 14.
Model matematis yang diajukan adalah: yij = μ + ai + εi j
2
predenaturasi 92 oC selama 10 menit, denaturasi 94 oC selama 4 menit, penempelan primer pada suhu 51 oC selama 1 menit, pemanjangan ruas target pada suhu 72 oC selama 2 menit, dan pemanjangan akhir pada 72 oC selama 7 menit .
yij = Variabel terikat (tipe kelahiran,
bobot lahir, bobot sapih, dan pertambahan bobot badan.)
μ = Rataan umum
ai = Variabel bebas (tipe pita DNA) εi j = Galat eror
Elektroforesis dan Visualisasi DNA
Produk PCR diuji menggunakan PAGE 6% (polyacrylamide gel electrophoresis) yang dilanjutkan dengan pewarnaan perak mengikuti Tegelstrom (1986) yang dimodifikasi oleh Farajallah et al. (1998).
HASIL
Amplifikasi DNA
Produk PCR hasil amplifikasi menggunakan primer M03-30 dan M03-33 mempunyai ukuran 610 pb (Gambar 1).
PCR-RFLP
Gambar 1 Hasil amplifikasi gen miostatin ekson 3. Keterangan: M= marker 100 pb (Biorad), kolom 1 – 4: produk PCR
Produk PCR kemudian dipotong menggunakan enzim restriksi HaeIII dan
MboI mengikuti petunjuk produsen (NewEngland Biolabs). Pola pita hasil pemotongan enzim restriksi diuji menggunakan PAGE 6% yang dilanjutkan dengan pewarnaan perak.
PCR-SSCP
Produk PCR dimurnikan dengan metode pengendapan alkohol. Sebanyak 20 μl produk PCR ditambah dengan 5M NaCl 2 μl dan alkohol absolut 200 μl kemudian diinkubasi semalaman dalam suhu -20 oC. Molekul DNA diendapkan dengan sentrifuse selama 5 menit pada kecepatan 8000 rpm. Endapan DNA kemudian disuspensikan dengan larutan formamida 25 μl (formamida solution 80%, EDTA 10 mM bromtimol blue 1 mg/mL, dan xylene cyanol 1mg/mL) dan direndam dalam
water bath bersuhu 94 oC selama ± 10 menit agar untai ganda DNA terpisah menjadi untai tunggal (single strand). Setelah 10 menit sampel dipindahkan dengan cepat ke dalam
ice bath selama ± 5 menit untuk mencegah kedua untai yang sudah terpisah menyatu kembali. Konformasi untai tunggal kemudian diuji dengan PAGE 12% (akrilamid:bis akrilamid = 59:1). Elektroforesis dijalankan dengan kekuatan listrik sebesar 150 volt selama 240 menit pada suhu konstan 4 oC. Visualisasi dilakukan dengan pewarnaan perak seperti pada visualisasi produk PCR.
PCR-RFLP
Hasil pemotongan produk PCR menggunakan enzim restriksi HaeIII dan
MboI memberikan pola yang sama (Gambar 2
Gambar 2 Hasil pemotongan gen miostatin ekson 3 dengan enzim restriksi Hae III. Keterangan: M= marker 100 pb dan 3).
Gambar 3 Hasil pemotongan gen miostatin ekson 3 dengan enzim restriksi Mbo I. Keterangan: M= marker 100 pb
Analisa statistik
Uji statistik dilakukan untuk melihat keterpautan tipe gen dengan beberapa karakter ternak dengan model linier umum menggunakan program Minitab 14.
Model matematis yang diajukan adalah: yij = μ + ai + εi j
3
Tabel 1 T
Gambar 5 Sekuen gen miostatin ekson 3 gabungan dari Ovis aries (domba) dan Bos taurus (sapi). Sumber: www.ncbi.nlm.nih.gov
ampilan ternak domba komposit sumatera, BALITNAK, Bogor
Tipe Pita Keterangan
W X Y Z
Jumlah sampel 3 31 31 18
Frekuensi (%) 3.615 37 37 21
hir (kg)
t badan
136.667 110.914 108.495 119.074
.349 .349 .687
Rataan bobot la 1.933 2.329 2.387 2.450
Rataan bobot sapih (kg) 10.133 8.984 8.897 9.594
Rataan pertambahan bobo (gr/ekor/hari)
CR-SSCP
i DNA hasil SSCP dari 88 sam
Analisis SSCP memberikan hasil adanya var
Jenis kelam ibu, dan b
semua tipe kelamin betina. Selain u, jika ditelusuri menurut induknya bapak dan ibu berbangsa BC (Barbados x Croix) memiliki anak yang semuanya bertipe Z.
Re
ahan obot badan sebagai peubah terikat. Hasil
AHASAN
P
Visualisas
pel domba komposit menunjukkan adanya keragaman tipe DNA (polimorfik). Tipe-tipe DNA ini kemudian dikelompokkan menjadi empat tipe berdasarkan bentuk pemisahan rantai DNAnya yaitu W,X,Y, dan Z (Gambar 4).
ian/keragaman pola tipe pada gen miostatin ekson 3 (polimorfik), keempat tipe tersebut yaitu W=3 sampel, X=31 sampel, Y=31 sampel, dan Z=18 sampel. Frekuensi keempat pola tipe pita hasil SSCP tersebut adalah 3.615 % (W), 37.349 % (X), 37.349 % (Y), dan 21.687% (Z) (Tabel 1).
Perbandingan hasil SSCP ini dengan data sekunder milik BALITNAK Bogor (Jenis,
in, jenis domba komposit, bangsa angsa bapak). Menunjukkan bahwa
W berjenis it
spon Bobot lahir, Bobot Sapih, Pertambahan Bobot Badan dan Tipe Kelahiran Terhadap Tipe SSCP Gen Miostatin Ekson 3.
Analisis dilakukan dengan uji statistik model linier umum yaitu dengan tipe SSCP sebagai peubah bebas serta tipe kelahiran, bobot lahir, bobot sapih, dan pertamb b
analisis disajikan dalam Tabel 2.
PEMB
Amplifikasi DNA
Ukuran produk PCR sepanjang 610 pb sesuai dengan sekuen DNA miostatin domba dan sapi yang disimpan dalam GenBank
.ncbi.nlm.gov
(www no. acc. AF266758 dan B076403).
A Gambar 4 (A) Hasil elektroforesis produk PCR-SSCP
3
Tabel 1 T
Gambar 5 Sekuen gen miostatin ekson 3 gabungan dari Ovis aries (domba) dan Bos taurus (sapi). Sumber: www.ncbi.nlm.nih.gov
ampilan ternak domba komposit sumatera, BALITNAK, Bogor
Tipe Pita Keterangan
W X Y Z
Jumlah sampel 3 31 31 18
Frekuensi (%) 3.615 37 37 21
hir (kg)
t badan
136.667 110.914 108.495 119.074
.349 .349 .687
Rataan bobot la 1.933 2.329 2.387 2.450
Rataan bobot sapih (kg) 10.133 8.984 8.897 9.594
Rataan pertambahan bobo (gr/ekor/hari)
CR-SSCP
i DNA hasil SSCP dari 88 sam
Analisis SSCP memberikan hasil adanya var
Jenis kelam ibu, dan b
semua tipe kelamin betina. Selain u, jika ditelusuri menurut induknya bapak dan ibu berbangsa BC (Barbados x Croix) memiliki anak yang semuanya bertipe Z.
Re
ahan obot badan sebagai peubah terikat. Hasil
AHASAN
P
Visualisas
pel domba komposit menunjukkan adanya keragaman tipe DNA (polimorfik). Tipe-tipe DNA ini kemudian dikelompokkan menjadi empat tipe berdasarkan bentuk pemisahan rantai DNAnya yaitu W,X,Y, dan Z (Gambar 4).
ian/keragaman pola tipe pada gen miostatin ekson 3 (polimorfik), keempat tipe tersebut yaitu W=3 sampel, X=31 sampel, Y=31 sampel, dan Z=18 sampel. Frekuensi keempat pola tipe pita hasil SSCP tersebut adalah 3.615 % (W), 37.349 % (X), 37.349 % (Y), dan 21.687% (Z) (Tabel 1).
Perbandingan hasil SSCP ini dengan data sekunder milik BALITNAK Bogor (Jenis,
in, jenis domba komposit, bangsa angsa bapak). Menunjukkan bahwa
W berjenis it
spon Bobot lahir, Bobot Sapih, Pertambahan Bobot Badan dan Tipe Kelahiran Terhadap Tipe SSCP Gen Miostatin Ekson 3.
Analisis dilakukan dengan uji statistik model linier umum yaitu dengan tipe SSCP sebagai peubah bebas serta tipe kelahiran, bobot lahir, bobot sapih, dan pertamb b
analisis disajikan dalam Tabel 2.
PEMB
Amplifikasi DNA
Ukuran produk PCR sepanjang 610 pb sesuai dengan sekuen DNA miostatin domba dan sapi yang disimpan dalam GenBank
.ncbi.nlm.gov
(www no. acc. AF266758 dan B076403).
A Gambar 4 (A) Hasil elektroforesis produk PCR-SSCP
4
Tabel 2 is respo ahira bot la obot s dan p mbahan bot terhadap tip
Peubah bebas er KT
Hasil analis n tipe kel n, bo hir, b apih, erta bo badan e SSCP
Sumb DB JK F P
Tipe sscp 3 0.556 0.185 0.35 0.790
Error 79 41.950 0.531
Tipe Kelahiran
Total 82 42.506
Tipe sscp 3 0.744 0.248 0.90 0.445
Error 79 21.750 0.275
Bobot Lahir
Total 82 22.494
Tipe sscp 3 9.25 3.08 0.42 0.736
Error 79 574.49 7.27
Bobot Sapih
Total 82 583.74
Tipe sscp 3 3102 1034 0.56 0.644 Error 79
Pertambahan bobot badan
146413 1853
149515
Total 82
PCR-RFLP
Pola yang sama pada hasil pemotongan produk PCR menggunakan enzim restriksi
HaeIII dan MboI memberikan arti bahwa sek
a selain sapi lebih terjaga dan sta l. Untuk mencari varian gen miostatin lakuan dengan metode deteksi PC ariasi sek pada gen miost (Jenis, Jenis kel min, jenis domba komposit, bangsa
erasal dari bapak dan ibu ber
bahwa mutasi ini tidak emiliki pengaruh pada fungsi protein miostatin dalam miogenesis. Walaupun begitu, usaha-usaha pencarian varian gen tetap harus bisa mencakup keseluruhan gen target uen DNA yang menjadi pengenal kedua
enzim tersebut sama pada semua sampel domba yang dianalisis.
Eksplorasi berbagai situs enzim retsriksi lain yang dilakukan dengan analisis homologi dari berbagai sekuen gen miostatin yang disimpan dalam Gen Bank tidak berpeluang untuk bisa menemukan keragaman gen miostatin lebih lanjut (data tidak diperlihatkan). Selain itu, Cieslak et al. (2003) melaporkan bahwa bagian ekson gen miostatin pad
bi
lebih lanjut di R-SSCP.
PCR-SSCP
Single-Strand Conformation Polymorphisms (SSCPs) adalah metode
elektroforesis yang populer untuk mengidentifikasi mutasi sekuen karena mudah, murah dan memiliki sensitifitas tinggi walau hanya satu nukleotida saja (Nataraj 1999) dapat mendeteksi polimorfisme dan mutasi titik pada berbagai posisi dalam fragmen DNA, meskipun mutasi yag terjadi hanya pada satu basa. (Orita et al.1998). Kesensitifitasan dari analsis SSCP merupakan hal yang cukup sulit dalam teknik karena sangat peka seperti kondisi elektroforesis, sensitifitas dipengaruhi beberapa faktor termasuk didalamnya tipe subtitusi basa, panjang fragmen, sekuen basa, kandungan G dan C dalam fragmen dan lokasi v
uen, tidak ada teori yang tepat memprediksi apakah SSCP dapat mendeteksi mutasi tertentu (Highsmith et al. 1999).
Analisis SSCP memberikan hasil adanya varian/keragaman pola tipe
atin ekson 3 (polimorfik), keempat tipe tersebut yaitu W=3 sampel, X=31 sampel, Y=31 sampel, dan Z=18 sampel. Frekuensi keempat pola tipe pita hasil SSCP tersebut adalah 3.62 % (W), 37.35 % (X), 37.35 % (Y), dan 21.69 % (Z) (Tabel 1).
Perbandingan hasil SSCP ini dengan data sekunder milik BALITNAK Bogor
a
ibu, dan bangsa bapak) menunjukkan bahwa semua tipe Z dan W berjenis kelamin betina. Selain itu, semua tipe Z jika ditelusuri menurut induknya b
bangsa BC (Barbados x St.Croix).
Respon Bobot Lahir, Bobot Sapih, Pertambahan Bobot Badan dan Tipe Kelahiran Terhadap Tipe SSCP Gen Miostatin Ekson 3
Hasil analisis menunjukkan bahwa tipe-tipe SSCP gen miostatin ekson 3 yang ditemukan dalam penelitian ini tidak terpaut dengan tipe kelahiran, bobot lahir, bobot sapih, dan pertambahan bobot badan. Sebagaimana telah disampaikan oleh Cockett
et al. (2001) bahwa fenomena hipertropi otot pada domba Texel terpaut dengan mutasi gen miostatin dibagian promotor. Hal yang sama juga ditemukan pada fenomena hipertropi pada babi (Cieslak et al. 2003). Kelebihan otot pada babi ditemukan sebagai konsekuensi dari hipertropi otot, khususnya pada babi jenis Pietrain dan Belgian Landrace, namun perbedaan ciri-ciri karkas dan genotip mengindikasikan
5
mulai dari p dan ekson
(Dunner 2003).
bahwa tipe SSCP gen miostatin ekson 3 tidak nyata mempengaruhi tipe kelahiran, bobot lahir, bobot sapih, dan an bobot badan pada domba komposi ra.
miostatin yang lebih lua
yang diperoleh dari penelitian tersebut bisa diguna n untuk mendeteksi keterpautannya
dengan t bobot
sapih, dan pertambaha obot badan.
Cies harsi T, Kapelanski W,
h J anim Sci
Coc
ted review].
Dun
Fara
Air Tawar (Reptilia: Testudines) di Indonesia Sebagai Dasar Pelestarian dan
litian dan
Hig
f
McN s –
McP
due to mutations in the
Nata
analysis for gel-based
Old Orit ingle-strand Priy domba Sub omba rambut Teg riation based Tell ants predates Uto
Animal Diversity in Indonesia. Jakarta: Ministry of Ari
romotor, intron
SIMPULAN
Varian gen miostatin ekson 3 dengan menggunakan metode PCR-RFLP dengan enzim restriksi Hae III dan Mbo I tidak menunjukkan adanya keragaman. Metode PCR-SSCP menunjukkan adanya varian gen miostatin ekson 3 pada domba komposit dalam penelitian ini yaitu W, X, Y, dan Z dengan frekuensi berturut-turut 3.62 %, 37.35 %, 37.35 %, dan 21.69 %. Berdasarkan hasil penelitian ini dapat disimpulkan
pertambah t sumate
SARAN
Pencarian varian gen
s perlu dilakukan pada populasi domba-domba lokal Indonesia sebagai manifestasi dari proses adaptasi domba-omba tersebut di wilayah tropis Indnesia.
Penelitian lebih lanjut terhadap varian gen miostatin ekson 3 yang ditemukan dalam penelitian ini perlu diverifikasi dengan sekuensing. Selain itu, tipe-tipe
ka
ipe kelahiran, bobot lahir, n b
DAFTAR PUSTAKA
lak D, Blic
Pierzchala M. 2003. Investigation of polymorphisms in the porcine myostatin (GDF8; MSTN) gene. Czec
48(2):69-75.
kett NE, Shay TL, Smit M. 2001. Analysis of the sheep genome [invi
Physiol Genomics 7:69-78.
ner et al. 2003. Haplotype diversity of the myostatin gene among beef cattle breeds.
Genet Sel Evol 35: 103-118.
jallah A, Suryobroto B, Puntorini T. 1998. Analisis Keragaman Genetik dan Filogeni Molekular Bangsa Kura-Kura
Pemanfaatannya. Laporan Pelaksanaan RUT V/1. Lembaga Pene
Pengabdian Pada Masyarakat Institut Pertanian Bogor. Bogor: IPB.
hsmith et al. 1999. Use of DNA toolbox for the characterization of mutation scanning methods. II: Evaluation o single-strand conformation polymorphism analysis. Electrophoresis 20:1195-1203.
ally EM. 2004. Powerful gene myostatin regulation of human muscle mass. N Engl J Med 350:2642-2644. herron AC, Lee SJ. 1997. Double muscling in cattle
myostatin gene. Proc Natl Acad Sci USA
94:12457-12461.
raj AJ, Glander IO, Kusukawa N. Highsmith WE. 1999. Single-strand conformation polymorphism and heteroduplex
mutation detection. Electrophoresis
20:117-1185.
ham et al. 2001. Molecular expression of myostatin and MyoD is greater in double-muscled than normal-double-muscled cattle fetuses. Am J Physiol Regulatory Integrative Comp Physiol 280:1488-1493. a M, Iwahana A, Kanazawa H, Hayashi K,
Sekiya T. 1998. Detection of polymorphisms of human DNA by gel electrophoresis as s
conformation polymorphisms. Proc Natl Acad Sci USA 86:2766-2770.
anto D, Siregar AR, Handiwirawan E, Subandriyo. 1999. Karakter domba introduksi dan pola konservasi
lokal sumatera di Sumatera Utara. Ilmu Ternak dan Veteriner 5(1):12-22.
andriyo, Setiadi B, Handiwirawan E, Suparyanto A. 2000. Performa domba komposit hasil persilangan antara domba lokal sumatera dengan d
pada kondisi dikandangkan. Ilmu Ternak dan Veteriner 5(2):73-83.
elstrom H. 1986. Mitokondrial DNA in natural population: an improved routine for screening of genetic va
on sensitive silver staining.
Electrophoresis 7:226-229.
gren A, Berglund A, Savolainen P, Janis CM, Liberles DA. 2004. Myostatin rapid sequence evolution in rumin
domestication. Molecular Phylogenetics and Evolution 33:782-790.
yo DP, Djarsanto, Nasution SN. 1996. Animal Genetic Resources and Domestic
5
mulai dari p dan ekson
(Dunner 2003).
bahwa tipe SSCP gen miostatin ekson 3 tidak nyata mempengaruhi tipe kelahiran, bobot lahir, bobot sapih, dan an bobot badan pada domba komposi ra.
miostatin yang lebih lua
yang diperoleh dari penelitian tersebut bisa diguna n untuk mendeteksi keterpautannya
dengan t bobot
sapih, dan pertambaha obot badan.
Cies harsi T, Kapelanski W,
h J anim Sci
Coc
ted review].
Dun
Fara
Air Tawar (Reptilia: Testudines) di Indonesia Sebagai Dasar Pelestarian dan
litian dan
Hig
f
McN s –
McP
due to mutations in the
Nata
analysis for gel-based
Old Orit ingle-strand Priy domba Sub omba rambut Teg riation based Tell ants predates Uto
Animal Diversity in Indonesia. Jakarta: Ministry of Ari
romotor, intron
SIMPULAN
Varian gen miostatin ekson 3 dengan menggunakan metode PCR-RFLP dengan enzim restriksi Hae III dan Mbo I tidak menunjukkan adanya keragaman. Metode PCR-SSCP menunjukkan adanya varian gen miostatin ekson 3 pada domba komposit dalam penelitian ini yaitu W, X, Y, dan Z dengan frekuensi berturut-turut 3.62 %, 37.35 %, 37.35 %, dan 21.69 %. Berdasarkan hasil penelitian ini dapat disimpulkan
pertambah t sumate
SARAN
Pencarian varian gen
s perlu dilakukan pada populasi domba-domba lokal Indonesia sebagai manifestasi dari proses adaptasi domba-omba tersebut di wilayah tropis Indnesia.
Penelitian lebih lanjut terhadap varian gen miostatin ekson 3 yang ditemukan dalam penelitian ini perlu diverifikasi dengan sekuensing. Selain itu, tipe-tipe
ka
ipe kelahiran, bobot lahir, n b
DAFTAR PUSTAKA
lak D, Blic
Pierzchala M. 2003. Investigation of polymorphisms in the porcine myostatin (GDF8; MSTN) gene. Czec
48(2):69-75.
kett NE, Shay TL, Smit M. 2001. Analysis of the sheep genome [invi
Physiol Genomics 7:69-78.
ner et al. 2003. Haplotype diversity of the myostatin gene among beef cattle breeds.
Genet Sel Evol 35: 103-118.
jallah A, Suryobroto B, Puntorini T. 1998. Analisis Keragaman Genetik dan Filogeni Molekular Bangsa Kura-Kura
Pemanfaatannya. Laporan Pelaksanaan RUT V/1. Lembaga Pene
Pengabdian Pada Masyarakat Institut Pertanian Bogor. Bogor: IPB.
hsmith et al. 1999. Use of DNA toolbox for the characterization of mutation scanning methods. II: Evaluation o single-strand conformation polymorphism analysis. Electrophoresis 20:1195-1203.
ally EM. 2004. Powerful gene myostatin regulation of human muscle mass. N Engl J Med 350:2642-2644. herron AC, Lee SJ. 1997. Double muscling in cattle
myostatin gene. Proc Natl Acad Sci USA
94:12457-12461.
raj AJ, Glander IO, Kusukawa N. Highsmith WE. 1999. Single-strand conformation polymorphism and heteroduplex
mutation detection. Electrophoresis
20:117-1185.
ham et al. 2001. Molecular expression of myostatin and MyoD is greater in double-muscled than normal-double-muscled cattle fetuses. Am J Physiol Regulatory Integrative Comp Physiol 280:1488-1493. a M, Iwahana A, Kanazawa H, Hayashi K,
Sekiya T. 1998. Detection of polymorphisms of human DNA by gel electrophoresis as s
conformation polymorphisms. Proc Natl Acad Sci USA 86:2766-2770.
anto D, Siregar AR, Handiwirawan E, Subandriyo. 1999. Karakter domba introduksi dan pola konservasi
lokal sumatera di Sumatera Utara. Ilmu Ternak dan Veteriner 5(1):12-22.
andriyo, Setiadi B, Handiwirawan E, Suparyanto A. 2000. Performa domba komposit hasil persilangan antara domba lokal sumatera dengan d
pada kondisi dikandangkan. Ilmu Ternak dan Veteriner 5(2):73-83.
elstrom H. 1986. Mitokondrial DNA in natural population: an improved routine for screening of genetic va
on sensitive silver staining.
Electrophoresis 7:226-229.
gren A, Berglund A, Savolainen P, Janis CM, Liberles DA. 2004. Myostatin rapid sequence evolution in rumin
domestication. Molecular Phylogenetics and Evolution 33:782-790.
yo DP, Djarsanto, Nasution SN. 1996. Animal Genetic Resources and Domestic
5
mulai dari p dan ekson
(Dunner 2003).
bahwa tipe SSCP gen miostatin ekson 3 tidak nyata mempengaruhi tipe kelahiran, bobot lahir, bobot sapih, dan an bobot badan pada domba komposi ra.
miostatin yang lebih lua
yang diperoleh dari penelitian tersebut bisa diguna n untuk mendeteksi keterpautannya
dengan t bobot
sapih, dan pertambaha obot badan.
Cies harsi T, Kapelanski W,
h J anim Sci
Coc
ted review].
Dun
Fara
Air Tawar (Reptilia: Testudines) di Indonesia Sebagai Dasar Pelestarian dan
litian dan
Hig
f
McN s –
McP
due to mutations in the
Nata
analysis for gel-based
Old Orit ingle-strand Priy domba Sub omba rambut Teg riation based Tell ants predates Uto
Animal Diversity in Indonesia. Jakarta: Ministry of Ari
romotor, intron
SIMPULAN
Varian gen miostatin ekson 3 dengan menggunakan metode PCR-RFLP dengan enzim restriksi Hae III dan Mbo I tidak menunjukkan adanya keragaman. Metode PCR-SSCP menunjukkan adanya varian gen miostatin ekson 3 pada domba komposit dalam penelitian ini yaitu W, X, Y, dan Z dengan frekuensi berturut-turut 3.62 %, 37.35 %, 37.35 %, dan 21.69 %. Berdasarkan hasil penelitian ini dapat disimpulkan
pertambah t sumate
SARAN
Pencarian varian gen
s perlu dilakukan pada populasi domba-domba lokal Indonesia sebagai manifestasi dari proses adaptasi domba-omba tersebut di wilayah tropis Indnesia.
Penelitian lebih lanjut terhadap varian gen miostatin ekson 3 yang ditemukan dalam penelitian ini perlu diverifikasi dengan sekuensing. Selain itu, tipe-tipe
ka
ipe kelahiran, bobot lahir, n b
DAFTAR PUSTAKA
lak D, Blic
Pierzchala M. 2003. Investigation of polymorphisms in the porcine myostatin (GDF8; MSTN) gene. Czec
48(2):69-75.
kett NE, Shay TL, Smit M. 2001. Analysis of the sheep genome [invi
Physiol Genomics 7:69-78.
ner et al. 2003. Haplotype diversity of the myostatin gene among beef cattle breeds.
Genet Sel Evol 35: 103-118.
jallah A, Suryobroto B, Puntorini T. 1998. Analisis Keragaman Genetik dan Filogeni Molekular Bangsa Kura-Kura
Pemanfaatannya. Laporan Pelaksanaan RUT V/1. Lembaga Pene
Pengabdian Pada Masyarakat Institut Pertanian Bogor. Bogor: IPB.
hsmith et al. 1999. Use of DNA toolbox for the characterization of mutation scanning methods. II: Evaluation o single-strand conformation polymorphism analysis. Electrophoresis 20:1195-1203.
ally EM. 2004. Powerful gene myostatin regulation of human muscle mass. N Engl J Med 350:2642-2644. herron AC, Lee SJ. 1997. Double muscling in cattle
myostatin gene. Proc Natl Acad Sci USA
94:12457-12461.
raj AJ, Glander IO, Kusukawa N. Highsmith WE. 1999. Single-strand conformation polymorphism and heteroduplex
mutation detection. Electrophoresis
20:117-1185.
ham et al. 2001. Molecular expression of myostatin and MyoD is greater in double-muscled than normal-double-muscled cattle fetuses. Am J Physiol Regulatory Integrative Comp Physiol 280:1488-1493. a M, Iwahana A, Kanazawa H, Hayashi K,
Sekiya T. 1998. Detection of polymorphisms of human DNA by gel electrophoresis as s
conformation polymorphisms. Proc Natl Acad Sci USA 86:2766-2770.
anto D, Siregar AR, Handiwirawan E, Subandriyo. 1999. Karakter domba introduksi dan pola konservasi
lokal sumatera di Sumatera Utara. Ilmu Ternak dan Veteriner 5(1):12-22.
andriyo, Setiadi B, Handiwirawan E, Suparyanto A. 2000. Performa domba komposit hasil persilangan antara domba lokal sumatera dengan d
pada kondisi dikandangkan. Ilmu Ternak dan Veteriner 5(2):73-83.
elstrom H. 1986. Mitokondrial DNA in natural population: an improved routine for screening of genetic va
on sensitive silver staining.
Electrophoresis 7:226-229.
gren A, Berglund A, Savolainen P, Janis CM, Liberles DA. 2004. Myostatin rapid sequence evolution in rumin
domestication. Molecular Phylogenetics and Evolution 33:782-790.
yo DP, Djarsanto, Nasution SN. 1996. Animal Genetic Resources and Domestic