ABSTRAK
PENGARUH KONSENTRASI PUTIH TELUR TERHADAP SIFAT FISIK, KADAR ANTOSIANIN DAN AKTIVITAS ANTIOKSIDAN BUBUK INSTAN EKSTRAK KULIT MANGGIS (Garcinia mangostana. L.)
DENGAN METODE FOAM MAT DRYING
Oleh
BAMBANG HARYANTO
Buah manggis (Garcinia mangostana. L.) merupakan buah yang mempunyai banyak manfaat bagi kesehatan dibanding buah lainnya. Bagian kulit buah manggis yang mengandung antosianin dapat dimanfaatkan sebagai pewarna alami dan berperan sebagai antioksidan. Penelitian ini bertujuan untuk mengetahui pengaruh konsentrasi putih telur terhadap sifat fisik, kadar antosianin dan aktivitas antioksidan bubuk instan kulit manggis dan mendapatkan konsentrasi putih telur terbaik sebagai foam agent yang menghasilkan bubuk instan dengan metode foam mat drying.
Penelitian berupa perlakuan tunggal disusun dalam Rancangan Acak Kelompok Lengkap dengan enam perlakuan dan empat ulangan. Perlakuan tunggal adalah konsentrasi putih telur sebagai foam agen yang terdiri dari 6 taraf yaitu P0 (tanpa putih telur), P1 (konsentrasi putih telur 5%), P2 (konsentrasi putih telur 10%), P3 (konsentrasi putih telur 15%), P4 (konsentrasi putih telur 20%) dan P5 (konsentrasi putih telur 25%). Data dianalisis kesamaan ragam dengan uji Bartlet dan kemenambahan data dengan uji Tukey. Selanjutnya dilakukan analisis ragam untuk mengetahui pengaruh perlakuan. Apabila terdapat pengaruh yang nyata, data dianalisis lebih lanjut dengan uji Beda Nyata Terkecil (BNT) pada taraf nyata 5 %. Pengamatan dilakukan terhadap rendemen, tingkat kelarutan, kecepatan larut, kadar antosianin, aktivitas antioksidan, derajad kecerahan dan derajad kemerahan bubuk instan ekstrak kulit manggis yang dihasilkan.
ABSTRACT
EFFECT OF CONCENTRATION OF EGG WHITE ON THE PHYSICAL PROPERTIES, ANTHOCYANINS CONTENT, ACTIVITIES
ANTIOXIDANTS EXTRACT POWDER INSTANT SKIN MANGOSTEEN (Garcinia mangostana. L.) WITH FOAM MAT DRYING METHOD
By
BAMBANG HARYANTO
Mangosteen fruit (Garcinia mangostana. L.) is a fruit that has many health benefits compared to other fruits. The skin of the mangosteen fruit that contains anthocyanins can be used as natural dyes and acts as an antioxidant. This study aimed to determine the effect of concentration of egg white on the physical properties, anthocyanin content and antioxidant activity of instant powder mangosteen skin and get the best concentration of egg white as foam agent that produces instant powder with foam mat drying method.
Research in the form of a single treatment arranged in a randomized block design with six treatments complete and four replications. Single treatment is the concentration of egg white as foam agent which consists of 6 levels P0 ( without egg whites), P1 (5 % concentration of egg white), P2 (10 % concentration of egg white ), P3 (concentration of egg white 15 %), P4 (concentration of egg whites 20 %) and P5 (concentration of egg whites 25 %). Data were analyzed in common variance with Bartlet and kemenambahan test data by Tukey test. Further analysis of variance to determine the effect of treatment. If there is a real effect, the data were analyzed further to test the Least Significant Difference ( LSD ) at the 5% significance level. Observations were made to the yield, solubility, soluble speed, levels of anthocyanins, antioxidant activity, the degree of brightness and degree of redness instant powder wish mangosteen peel extract .
RIWAYAT HIDUP
Penulis dilahirkan di Desa Tanggungharjo, Kecamatan Kedungjati, Kabupaten Purwodadi Grobogan Jawa Tengah pada tanggal 12 September 1962 merupakan anak pertama dari pasangan bapak Suparman dan ibu Suhartini. Pendidikan Sekolah Dasar di SD Negeri I Tanggungharjo, Grobogan Jawa Tengah lulus tahun 1975. Pendidikan Sekolah Menengah Pertama (SMP) Budiluhur Tanggung di Grobogan Jawa Tengah lulus pada tahun 1979, dan Pendidikan Sekolah Perkebunan Menengah Atas (SpbMA MM 52) Yogyakarta lulus tahun 1983, Sarjana Pertanian pada Sekolah Tinggi Pertanian (STIPER) SURYADHARMA Bandar Lampung lulus tahun 1996.
MOTTO
TAK AKAN ADA LOMPATAN BESAR DALAM
KEHIDUPAN TANPA DILALUI DARI
SANWACANA
Puji dan syukur penulis panjatkan ke hadirat Tuhan Yang Maha Esa, karena penulis dapat menyelesaikan penelitian dan penulisan tesis dengan judul “Pengaruh Konsentrasi Putih Telur terhadap Sifat Fisik, Kadar Antosianin dan Aktivitas Antioksidan Bubuk Instan Ekstrak Kulit Manggis (Garcinia Mangostana. L.) dengan Metode Foam Mat Drying”.
Penulis menyadari bahwa dalam penelitian dan penulisan tesis ini tidak terlepas dari partisipasi dan bantuan dari berbagai pihak. Oleh karena itu, dalam kesempatan ini penulis mengucapkan terima kasih kepada :
1. Ibu Dr. Ir. Sussi Astuti, M.Si. selaku pembimbing pertama yang dengan penuh kesabaran membimbing dan memotivasi penulis selama proses penyelesaian tesis ini.
2. Bapak Dr. Ir. Murhadi, M.Si. selaku pembimbing kedua yang telah memberikan saran dan bimbingannya petunjuk dan arahan kepada penulis demi kesempurnaan tesis ini.
3. Bapak Dr. Ir. Subeki, M.Si., M.Sc. selaku pembahas yang telah memberikan masukan dan saran perbaikan.
5. Bapak dan Ibu dosen dan seluruh staf pengajar Jurusan Magister Teknologi Industri Pertanian Universitas Lampung atas segala bantuan dan motivasinya. 6. Istri dan anak-anakku yang telah mendukung baik secara moril maupun material
serta doa yang tulus sehingga saya dapat menyelesaikan tesis ini.
7. Teman-teman seperjuangan yang tidak bisa saya sebutkan satu persatu namanya yang telah memberikan bantuan dan selalu kompak selama studi di Jurusan Magister Teknologi Industri Pertanian Universitas Lampung.
Akhirnya, penulis berdoa semoga Tuhan Yang Maha Esa memberi balasan kepada mereka yang telah membantu selama penelitian dan penulisan tesis ini, dan semoga karya ini bermanfaat bagi para pembaca sekalian. Amiin.
Bandar Lampung, Januari 2015
Bambang Haryanto
DAFTAR ISI
Halaman
KATA PENGANTAR ... i
DAFTAR ISI ... ii
DAFTAR GAMBAR ... iii
DAFTAR TABEL ... iv
I. PENDAHULUAN ... 1
A. Latar Belakang dan Masalah ... 1
B. Tujuan Penelitian ... 4
C. Kerangka Pemikiran ... 4
D. Hipotesis ... 7
II. TINJAUAN PUSTAKA ... 8
A. Buah Manggis ... 8
B. Aktivitas Antioksidan ... 10
C. Antosianin ... 12
D. Putih Telur ... 14
1 Daya Stabilitas Buih ... 14
2 Komposisi Protein Putih Telur yang Berperan dalam Pembentukan Buih ... 16
3 Pembentukan Buih ... 17
E. Dekstrin ... 20
F. Pengeringan ... 22
DAFTAR TABEL
Tabel Halaman 1. Komposisi protein putih telur yang berperan dalam
pembentukan buih ... 16 2. Perhitungan nilai Hue ... 39 3. Rendemen bubuk instan kulit buah manggis dengan penambahan putih telur sebagai foam agent ... 41 4. Aktivitas antioksidan bubuk instan kulit manggis dengan penambahan
DAFTAR LAMPIRAN
Lampiran Hal 1 Data rendemen bubuk instan kulit manggis dengan metode foam
mat drying ... 67
2. Uji homogenitas Bartlet rendemen bubuk intans kulit manggis ... 67
3. Uji aditifitas rendemen bubuk instan kulit manggis ... 68
4. Analisis ragam rendemen bubuk instan kulit manggis ... 68
5. Data tingkat kelarutan bubuk instan kulit manggis ... 69
6. Uji homogenitas Bartlet tingkat kelarutan bubuk instan kulit manggis . 69 7. Uji aditivitas tingkat kelarutan bubuk instan kulit manggis... 70
8. Analisis ragam tingkat kelarutan bubuk instan kulit manggis ... 70
9. Data kecepatan larut bubuk instan kulit manggis ... 71
10. Uji homogenitas Bartlet kecepatan larut bubuk instan kulit manggis.. 71
11. Uji aditivitas kecepatan larut bubuk instan kulit manggis ... 72
12. Analisis ragam kecepatan larut bubuk instan kulit manggis ... 72
13. Data kadar antosianin bubuk instan kulit manggis ... 73
14. Uji homogenitas Bartlet kadar antosianin bubuk instan kulit manggis 73 15. Uji aditivitas kadar antosianin bubuk instan kulit manggis ... 74
16. Analisis ragam kadar antosianin bubuk instan kulit manggis ... 74
17. Data aktivitas antioksidan bubuk instan kulit manggis ... 75
18. Uji homogenitas Bartlet aktivitas antioksidan bubuk kulit manggis ... 75
19. Uji aditivitas aktivitas antioksidan bubuk instan kulit manggis... 76
21. Data derajad kecerahan (L*) bubuk instan kulit manggis ... 77 22. Uji homogenitas Bartlet derajad kecerahan (L*) bubuk kulit manggis 77 23. Uji aditivitas derajad kecerahan (L*) bubuk instan kulit manggis ... 78 24. Analisis ragam derajad kecerahan (L*) bubuk instan kulit manggis ... 78 25. Data derajad kemerahan (a*) bubuk instan kulit manggis ... 79 26. Uji homogenitas Bartlet derajad kemerahan (a*) bubuk kulit
DAFTAR GAMBAR
Gambar Halaman
1. Mekanisme pembentukan buih ... 19
2. Struktur dekstrin ... 21
3. Pembuatan Tepung kulit manggis ... 31
4. Diagram alir proses pembuatan sari kulit manggis ... 32
5. Diagram alir pembuatan bubuk instan kulit manggis ... 34
6. Tingkat kelarutan bubuk instan kulit manggis akibat pemberian putih telur dengan metode foam mat drying ... 44
7. Kecepatan larut bubuk instan kulit manggis akibat pemberian putih telur dengan metode foam mat drying ... 46
8. Kadar antosianin bubuk instan kulit manggis akibat pemberian putih telur dengan metode foam mat drying ... 49
1
I. PENDAHULUAN
A. Latar Belakang dan Masalah
Tananam manggis (Garcinia Mangostana L) merupakan salah satu buah asli negara tropika yang mempunyai prospek cerah untuk dikembangkan di berbagai daerah dengan ekologi yang cocok untuk pertumbuhan manggis. Saat ini manggis merupakan salah satu komoditas ekspor yang menjadi andalan Indonesia untuk meningkatkan penerimaan devisa negara, karena manggis digemari di luar negeri. Buah manggis mempunyai rasa asam-manis lezat dan menyegarkan sehingga dijuluki sebagai Ratu Buah (Queen of Fruits).
Buah manggis merupakan buah yang mempunyai banyak manfaat bagi kesehatan dibandingkan buah lainnya. Bagian kulit buah manggis dapat dimanfaatkan sebagai penghasil zat warna alami yang dapat digunakan sebagai pewarna makanan, juga dimanfaatkan sebagai antioksidan. Penampilan kulit buah manggis yang berwarna ungu menunjukkan adanya pewarna alami yang terkandung didalamnya. Salah satu senyawa flavonoid yang terkandung dalam kulit buah manggis adalah antosianin.
Kulit buah manggis mengandung antosianin seperti cyanidin-3-sophoroside dan
cyanidin-3-glucoside yang merupakan antioksidan dan berperan penting pada
pewarnaan kulit manggis, selain itu kulit buahnya mengandung senyawa pektin,
2
tanin, dan resin yang dimanfaatkan untuk menyamak kulit dan sebagai zat pewarna hitam untuk makanan dan industri tekstil, sedangkan getah kuning dimanfaatkan sebagai bahan baku cat dan insektisida (Qosim, 2007).
Antosianin merupakan salah satu zat pewarna alami berwarna kemerah-merahan yang larut dalam air dan tersebar luas di dunia tumbuh-tumbuhan. Antosianin tergolong senyawa flavonoid yang memiliki fungsi sebagai antioksidan alami (Madhavi, 1996 dalam Nuciferani, 2004). Antosianin mampu menghentikan reaksi radikal bebas dengan menyumbangkan hidrogen atau elektron pada radikal bebas dan menstabilkannya. Menurut Francis (1985) dan Markakis (1982) dalam Nuciferani (2004), sifat antosianin sebagai antioksidan dikarenakan terdapatnya dua cincin benzena yang dihubungkan dengan tiga atom C dan dirapatkan oleh satu atom O sehingga terbentuk cincin di antara dua cincin benzena pada antosianin.
Antosianin adalah pigmen yang bisa larut dalam air. Secara kimiawi antosianin dikelompokkan dalam golongan flavonoid dan fenolik. Zat tersebut berperan dalam pemberian warna terhadap bunga atau bagian tanaman lain dari mulai merah, biru sampai ungu termasuk juga kuning (Samsudin dan Khoirudin, 2008).
Antioksidan adalah zat yang dapat menangkal atau mencegah reaksi oksidasi dari radikal bebas (Chang et al. 2002). Oksidasi merupakan suatu reaksi kimia yang menstranfer elektron dari suatu zat ke oksidator. Reaksi oksidasi dapat menghasilkan radikal bebas dan memicu reaksi berantai yang menyebabkan kerusakan sel dalam tubuh. Radikal bebas sangat berbahaya karena dapat
3
menyebabkan penyakit degeneratif seperti kanker, tekanan darah tinggi, jantung koroner, diabetes militus, katarak, proses penuaan dini dan lain-lain (Hailla, 1999 dalam Wiwin et al., 2010).
Produk pangan yang dikehendaki oleh masyarakat modern tidak hanya mempertimbangkan unsur pemenuhan gizi, akan tetapi juga harus praktis, cepat saji, tahan lama dan tidak memerlukan tempat atau ruang penyimpanan yang lebih besar. Oleh karena itu, kecenderungan konsumen saat ini mengarah pada produk siap saji (instan), di samping nilai gizi yang diinginkan. Produk pangan bubuk siap saji (instan) merupakan produk pangan yang berbentuk bubuk, berstruktur remah, mudah dilarutkan dengan air dingin maupun air panas, mudah dalam penyajian, mudah terdispersi dan tidak mengendap di bagian bawah wadah (Desrosier, 1988; Wirakartakusuma et al., 1992).
Permasalahan dalam pembuatan bubuk instan adalah kerusakan akibat proses pengeringan yang umumnya memerlukan suhu pemanasan tinggi (lebih 60oC) sehingga mengakibatkan kerusakan flavour atau terjadi pengendapan pada saat bubuk dilarutkan dalam air. Salah satu metode pengeringan yang digunakan untuk membuat bubuk instan adalah metode foam mat yang merupakan metode pengeringan bahan cair yang sebelumnya dijadikan buih terlebih dahulu dengan penambahan zat pembusa dan zat tahan panas dengan tujuan memperluas permukaan, menurunkan tegangan permukaan, meningkatkan rongga, mengembangkan bahan, mempercepat penguapan air, serta menjaga mutu bahan.
4
B. Tujuan Penelitian
Penelitian ini bertujuan untuk
1. Mengetahui pengaruh konsentrasi putih telur terhadap sifat fisik, kadar antosianin dan aktivitas antioksidan bubuk instan kulit manggis (Garcinia mangostana. L) dengan metode foam mat drying.
2. Mendapatkan konsentrasi putih telur terbaik sebagai foam agent yang menghasilkan bubuk instan dengan metode foam mat drying.
C. Kerangka Pemikiran
Pemanfaatan kulit buah manggis sebenarnya sudah dilakukan sejak dahulu. Kulit buah manggis secara tradisional digunakan pada berbagai pengobatan di negara India, Myanmar Sri langka, dan Thailand (Mahabusarakam et al., 1987). Secara luas, masyarakat Thailand memanfaatkan kulit buah manggis untuk pengobatan penyakit sariawan, disentri, cystitis, diare, gonorea, dan eksim. Di era modern, pemanfaatankulit buah manggis secara luas di negara tersebut memicu minat para ilmuwan untuk meneliti dan mengembangkan lebih lanjut aspek ilmiah khasiat kulit manggis.
Produk pangan yang dikehendaki oleh masyarakat modern tidak hanya mempertimbangkan unsur pemenuhan gizi, akan tetapi juga harus praktis, cepat saji, tahan lama dan tidak memerlukan tempat atau ruang penyimpanan yang lebih besar. Oleh karena itu, kecenderungan konsumen saat ini mengarah pada produk-produk yang menonjolkan sifat siap saji (instan), disamping nilai gizi yang diinginkan. Produk pangan bubuk siap saji (instan) merupakan produk pangan
5
yang berbentuk bubuk, berstruktur remah, mudah dilarutkan dengan air dingin maupun air panas, mudah dalam penyajian, mudah terdispersi dan tidak mengendap di bagian bawah wadah (Desrosier, 1988; Wirakartakusuma et al., 1992). Bentuk bubuk memiliki kelebihan yaitu lebih awet, ringan dan volumenya lebih kecil sehingga dapat mempermudah dalam pengemasan dan pengangkutan.
Pembuatan bubuk siap saji (bubuk instant) dapat dilakukan dengan teknologi tinggi menggunakan alat canggih seperti freeze dryer dan spray dryer, namun alat ini cukup mahal dan tidak terjangkau oleh kelompok tani atau industri rumah tangga. Salah satu metode yang dapat menggantikan spray dryer adalah metode
foam mat drying. Metode foam mat drying lebih sederhana dan dapat
diaplikasikan di tingkat industri rumah tangga. Foam mat drying adalah teknik pengeringan produk berbentuk cair dan peka terhadap panas melalui teknik pembusaan dengan menambahkan zat pembuih (Kumalaningsih et al., 2005). Pengeringan dengan oven tanpa pembuih (foam) memerlukan suhu yang tinggi, sehingga akan merusak mutu produk pangan yang dikeringkan (Desrosier, 1988).
Menurut Murtala (1999), metode foam mat drying memerlukan bahan pengisi yang berfungsi membentuk foam dan melapisi komponen flavour, mencegah kerusakan akibat panas, meningkatkan total padatan dan rendemen serta mempercepat pengeringan. Tranggono et al. (1990) mengemukakan bahwa monogliserida atau protein kedelai yang dimodifikasi dengan metil selulosa, ester-ester, tween 80 dan protein putih telur merupakan bahan yang berperan dalam pembentukan foam. Putih telur memiliki harga yang relatif murah dan mudah diperoleh. Menurut Pulungan et al. (2003), pembuatan kunyit sinom instan
6
menggunakan 2,5 % putih telur sebagai bahan pembentuk foam menghasilkan produk dengan kelarutan 99,94%. Pembentukan buih dari bagian putih telur dilakukan dengan pengocokan. Pengocokan dapat menggunakan tenaga tangan atau dengan bantuan mesin pengocok telur (Sirait, 1986). Saat putih telur dikocok, gelembung udara terperangkap dalam cairan albumen dan membentuk buih. Salah satu kesulitan yang telah dilaporkan dalam proses ini adalah kurangnya kestabilan “foam” (busa) selama proses pemanasan. Jika busa tidak cukup stabil, terjadi kerusakan seluler yang menyebabkan kerusakan selama proses pengeringan.
Menurut Tari (2007), perlakuan konsentrasi putih telur 7,5% dan maltodekstrin 15% merupakan perlakuan terbaik terhadap karakteristik bubuk instan secang. Sedangkan menurut Theresia (2011) konsentrasi putih telur 20 % memberikan karakteristik bubuk tomat terbaik bila dibandingkan dengan konsentrasi putih telur 10 % dan 15 %. Fadilah et al. (2006) melaporkan bahwa penambahan putih telur 2,5% dan dekstrin 12,5 % memberikan karakteristik yang baik terhadap bubuk buah nangka. Penelitian lainnya yaitu Olubunmi et al. (2012) melaporkan bahwa konsentrasi putih telur 15% terhadap nektar pepaya memberikan hasil terbaik sesuai dengan karakteristik nektar pepaya.
Menurut Desrosier (1988) konsentrasi busa yang semakin banyak akan meningkatkan luas permukaan dan memberi struktur berpori pada bahan sehingga akan meningkatkan kecepatan pengeringan. Zubaidah (2009) menyatakan bahwa lapisan pada pengeringan busa lebih cepat kering daripada lapisan tanpa busa pada kondisi yang sama. Hal ini disebabkan cairan lebih mudah bergerak melalui
7
struktur busa daripada melalui lapisan padat pada bahan yang sama. Keuntungan lain pengeringan metode foam mat drying adalah mempercepat proses pengeringan.
D. Hipotesis
Hipotesis yang diajukan dalam penelitian adalah :
1. Konsentrasi putih telur sebagai foam agent berpengaruh terhadap sifat fisik, kadar antosianin dan aktivitas antioksidan bubuk instan kulit manggis dengan metode foam mat drying.
2. Terdapat konsentrasi putih telur sebagai foam agent yang menghasilkan bubuk instan kulit manggis terbaik dengan metode foam mat drying.
8
II.TINJAUAN PUSTAKA
A. Buah Manggis
Manggis tergolong famili Guttiferae, diduga hybrid allotetraploid dari G.
hombroniana dan G. malaccensis. Pohon manggis termasuk pohon dioecious
dengan tinggi 6-25 meter, tegak lurus dengan percabangan simetri membentuk tajuk pyramid. Semua bagian tanaman mengeluarkan latex kuning jika saluran latex rusak (Rukmana, 2003).
Daun manggis tunggal, berpasangan di sisi ranting, helai daun berbentuk oblong atau elips dengan ukuran 15-25 cm x 7-13 cm. Permukaan atas daun berwarna hijau tua, bagian bawah hijau kekuningan. Bunga tunggal atau berpasangan dengan tangkai bunga pendek dan gemuk dengan diameter 5.5 cm; sepal 4, tersusun 2 pasang, petal 4 tebal dan fleshy. Benang sari jumlahnya banyak, panjang 0.5 cm tersusun dalam 2 seri; ovary melekat di dasar bunga, hampir bulat dengan 4-8 ruang. Stigma menonjol dan tebal melekat dan terbentuk dengan jumlah yang sama dengan jumlah ruang dalam ovary (Rukmana, 2003).
Buah berbentuk bulat atau agak pipih, berat bervariasi 75-150 g, diameter 3.5-8 cm. Perikarp atau kulit buah halus dengan tebal 4-8 mm, keras, berwarna ungu. Kulit membungkus daging buah terdiri dari 4-8 segmen, dengan beberapa diantaranya mengandung biji (2-3 biji). Biji berbentuk pipih berwarna ungu gelap
9
atau coklat ( Rukmana, 2003). Buah dipanen ketika telah berwarna ungu muda sampai ungu tua dengan tangkai buah masih melekat. Indeks panen didasarkan pada perkembangan intensitas warna ungu pada pericarp. Umumnya buah yang dipanen dengan perkembangan warna yang kurang akan mempunyai lateks yang banyak pada tangkai buah dan mempunyai aroma yang kurang baik dibandingkan stadia ungu penuh. Jumlah lateks akan berkurang seiring dengan kematangan buah, padatan terlarut meningkat dan keasaman konstan (Nakasone dan Paul, 1998). Menurut Sosrodiharjo dalam Yaacob dan Tindall (1995) perkembangan fisik maksimum 103 hari dari pembungaan, sedangkan Verheij (1992) menyatakan bahwa buah masak terjadi pada periode 6-12 minggu. Apresiasi yang beragam memungkinkan petani panen pada umur buah bervariasi tergantung tujuan pemasarannya.
Getah yang berwarna kuning atau gamboge sering dijumpai pada permukaan kulit buah maupun dalam daging buah. Getah yang berwarna kuning merupakan eksudat resin yang banyak terdapat pada berbagai tanaman yang termasuk famili Guttiferae dan eksudat ini berasal dari saluran resin yang rusak (Asano et al., 1996; Pankasemsuk et al.,1996). Apabila saluran resin rusak maka getah mengucur dari saluran getah dan menembus ke dalam segmen buah yang akan menyebabkan daging buah menjadi bening dan rasanya pahit. Gamboge juga bisa dijumpai pada kulit buah dengan bentuk bintik kuning pada kulit manggis. Buah yang terserang getah kuning digolongkan buah yang tidak layak jual. Kerusakan saluran resin pada kulit buah dapat disebabkan faktor lingkungan misalnya angin
10
dan hujan berlebihan, penanganan yang tidak hati-hati yang menyebabkan kerusakan kulit buah, dan juga serangan hama (Yaacob dan Tindall, 1995).
B. Aktivitas Antioksidan
Antioksidan merupakan senyawa yang dapat menunda atau mencegah terjadinya reaksi oksidasi radikal bebas dalam oksidasi lipid dalam konsentrasi yang lebih rendah dari substrat yang dapat dioksidasi. Antioksidan bereaksi dengan radikal bebas sehingga mengurangi kapasitas radikal bebas untuk menimbulkan kerusakan. Dalam bahan pangan, antioksidan banyak terdapat dalam sayur dan buah-buahan seperti jeruk, apel, kol merah, bit, manggis dan sebagainya. Antioksidan alami yang terdapat dalam bahan pangan tersebut anatara lain adalah vitamin C, vitamin E, antosianin, klorofil dan senyawa flavonoid.
Antioksidan alami pada umumnya berbentuk cairan pekat dan sensitif terhadap pemanasan (DeMan, 1997). Radikal bebas adalah molekul yang sangat reaktif karena memiliki elektron tidak berpasangan pada orbital luarnya sehingga dapat bereaksi dengan molekul sel tubuh dengan cara mengikat elektron sel tersebut, dan mengakibatkan reaksi berantai yang menghasilkan radikal bebas baru (Ketaren, 1986).
Antioksidan bereaksi dengan radikal bebas dengan cara mengurangi konsentrasi oksigen, mencegah pembentukan singlet oksigen yang reaktif, mencegah inisiasi rantai pertama dengan menangkap radikal primer seperti radikal hidroksil, mengikat katalis ion logam, mendekomposisi produk-produk primer radikal
11
menjadi senyawa non-radikal, dan memutus rantai hidroperoksida. Antioksidan berdasarkan mekanisme kerjanya dikelompokan menjadi :
1. Antioksidan Primer yaitu antioksidan yang bereaksi dengan radikal lipid berenergi tinggi untuk menghasilkan produk yang memiliki kestabilan termodinamis lebih baik. Antioksidan golongan fenol seperti Isoflavon termasuk dalam antioksidan yang memiliki mekanisme ini.
2. Antioksidan sekunder yang juga dikenal dengan antioksidan pencegah (Preventive Antioxidant) yang dapat memperlambat reaksi inisiasi dengan cara memutus rantai (chain-breaking antioxidant) hidroperoksida. Contoh antioksidan ini yaitu dilauril thiodipropionate dan asam thiodipropionic. Antioksidan golongan ini adalah antioksidan yang berikatan dengan gugus thiol.
Mekanisme kerja antioksidan senyawa fenolik adalah sebagai berikut :
Senyawa antioksidan (AH) dapat memberikan atom hidrogen secara cepat ke radikal lipida (ROO , RO , R , OH ) dan mengubahnya menjadi bentuk yang lebih stabil. Sementara turunan radikal antioksidan (A) yang dihasilkan lebih stabil dibandingkan radikal lipida karena akan terjadi delokalisasi perbaikan elektron dari ikatan rangkap pada cincin benzen sebagai indikasi oleh ikatan isomer valensi. Peningkatan jumlah gugus hidroksil (alkil hidrogen pada struktur
12
kimianya) pada posisi para atau ortho seperti pada genistein dapat meningkatkan aktivitas antioksidan isoflavon. Reaksi radikal bebas dengan komponen sel baik komponen struktural (molekul penyusun membran) maupun komponen fungsional yaitu enzim dan DNA dapat merusak sel melalui oksidasi lemak tidak jenuh dan protein sel. Kerusakan lebih lanjut pada organel sel dapat mencapai kerusakan DNA dan membran sel. Berdasarkan mekanisme tersebut, radikal bebas tentunya akan turut mempengaruhi akan timbulnya berbagai jenis penyakit degeneratif seperti aterosklerosis (pengendapan lemak yang mengeras dalam pembuluh darah arteri). Antioksidan digolongkan menjadi tiga berdasarkan prinsip kerja dalam mencegah proses oksidasi yaitu :
1. Antioksida gugus fenol dan amin aromatic yang bereaksi dengan radikal bebas dari system membentuk produk substrat non radikal dan radikal antioksidan
2. Antioksidan yang dapat menghilangkan molekul-moleku hidroperoksida dan substrat tetapi tanpa melibatkan radikal bebas
3. Antioksidan yang dapat menginaktifkan logam untuk mempercepat reaksi oksidasi
C. Antosianin
Antosianin adalah glikosida antosianidin, yang merupakan garam polihidroksiflavilium (2-arilbenzopirilium). Sebagian besar antosianin berasal dari 3,5,7-trihidroksiflavilium klorida dan bagian gula biasanya terikat pada gugus hidroksil pada atom karbon ketiga. Telaah akhir-akhir ini menunjukkan bahwa
13
beberapa antosianin mengandung komponen tambahan seperti asam organik dan logam (Fe, Al, Mg).
Antosianin tergolong pigmen yang disebut flavonoid yang pada umumnya larut dalam air. Warna pigmen antosianin merah, biru, violet, dan biasanya dijumpai pada bunga, buah-buahan, dan sayur-sayuran. Dalam tanaman terdapat dalam bentuk glikosida yaitu membentuk ester dengan monosakarida (glukosa, galaktosa, ramnosa, dan kadang-kadang pentosa). Sewaktu pemanasan dalam asam mineral pekat, antosianin pecah menjadi antosianin dan gula. Konsentrasi pigmen juga sangat berperan dalam menentukan warna. Pada konsentrasi yang encer antosianin berwarna biru, sebaliknya pada konsentrasi pekat berwarna merah, dan konsentrasi biasa berwarna ungu. Dalam pengolahan sayur-sayuran adanya antosianin dan keasaman larutan banyak menentukan warna produk tersebut (Winarno, 2002).
Menurut Winarno (2002) antosianin tergolong pigmen disebut flavonoid yang pada umumnya larut dalam air. Sewaktu pemanasan dalam asam mineral pekat, antosianin pecah menjadi antosianin dan gula. Konsentrasi pigmen juga sangat berperan dalam menentukan warna, berkurangnya kadar antosianin disebabkan proses steam (pemanasan dengan uap air), akibat kerusakan secara enzimatis dan perlakuan pemanasan. Degradasi antosianin selama proses akibat enzim sangat terbatas dan retensinya tergantung pada proses dan bahan bakunya, penurunan warna antosianin disebabkan oleh berbagai bahan kimia dan sistem enzimatik. Antosianin sangat sensitif terhadap penurunan intensitas warnanya oleh berbagai agen, karena defisiensi elektron.
14
D. Putih Telur
Putih telur atau albumen tersusun oleh lapisan encer luar, lapisan kental luar, lapisan encer dalam dan lapisan kalaza atau lapisan kental dalam. Air merupakan komponen utama albumen. Kandungan padatan dalam putih telur berkisar antara 13% (Stadelman dan Cotterill, 1977).
1. Daya Stabilitas Buih
Buih merupakan dispersi koloid dari suatu fase gas yang terdispersi dalam fase cair (Stadelman dan Cotterill, 1977). Pembentukan buih dari bagian putih telur dilakukan dengan pengocokan. Pengocokan dapat menggunakan tenaga tangan atau dengan bantuan mesin pengocok telur (Sirait, 1986). Saat putih telur dikocok, gelembung udara terperangkap dalam cairan albumen dan membentuk buih. Buih yang terbentuk dari pengocokan putih telur merupakan komponen yang penting dalam pembuatan berbagai produk makanan seperti cake. Daya dan kestabilan buih yang tinggi akan berperan penting dalam pembentukan film yang stabil untuk mengikat gas dalam pembuatan angel food cake (Winarno dan Koswara, 2002). Dalam proses pembuatan cake, udara dalam gelembung buih akan memuai ketika dipanaskan dan putih telur yang menyelubunginya meregang kemudian membentuk struktur pori pada cake. Daya buih yang tinggi memiliki ukuran buih yang besar sehingga saat dipanggang ukuran remah cake yang dihasilkan juga besar.
Buih yang baik adalah yang memiliki kemampuan dan kestabilan buih yang baik. Stadelman dan Cotterill (1977) menyatakan bahwa daya buih merupakan ukuran
15
kemampuan putih telur dalam membentuk buih jika dikocok dan biasanya dinyatakan dalam presentase terhadap putih telur. Berdasarkan pernyataan tersebut, maka daya buih dapat dinyatakan dengan rumus:
volume buih (ml)
Daya Buih = --- x 100% Volume putih telur (ml)
Dasar pembentukan buih yang stabil adalah cairan dengan kekuatan regangan atau elastisitas tinggi. Kestabilan buih putih telur dapat diukur berdasarkan banyaknya air yang terlepas dari buih dalam waktu tertentu dan biasanya dinyatakan dalam bobot, volume atau derajat pencairan (Stadelman dan Cotterill, 1977).
Menurut Stadelman dan Cotterill (1977), faktor-faktor yang mempengaruhi daya dan kestabilan buih putih telur antara lain lama pengocokan, pH, suhu, serta penambahan bahan kimia atau bahan tambahan lainnya. Volume buih putih telur akan meningkat seiring lamanya waktu pengocokkan namun setelah lama pengocokan 6 menit, tidak ada lagi kenaikan volume buih. Kestabilan buih tertinggi didapat setelah lama pengocokkan 2 menit, sehingga untuk mendapatkan kestabilan buih yang diinginkan, putih telur sebaiknya tidak dikocok hingga mencapai volume maksimum.
Menurut Stadelman dan Cotterill (1977) menyatakan bahwa volume dari putih telur yang dikocok akan meningkat seiring kenaikan nilai pH. Selanjutnya disebutkan bahwa putih telur dengan nilai pH di bawah 8 memerlukan waktu pengocokan yang lebih lama untuk memperoleh buih yang stabil. Pemanasan putih telur pada suhu di atas 50 0 C dapat menyebabkan penurunan kestabilan buih
16
dan volume buih putih telur yang dihasilkan juga akan menurun sekitar 30% lebih rendah dari umumnya.
2. Komposisi Protein Putih Telur yang Berperan Dalam Pembentukan
Buih.
Menurut Winarno dan Koswara (2002) komposisi putih telur ayam dapat dilihat pada Tabel 1.
Tabel 1. Kandungan putih telur ayam
No Komposisi Jumlah (%)
1 Air 88,57
2 Protein 10,30
3 Lemak 0,03
4 Karbohidrat 0,65
5 Abu 0,55
Sumber : Winarno dan Koswara (2002)
Menurut Stadelman dan Cotterill (1977), protein putih telur yang berperan dalam pembentukan buih yaitu ovomucin, globulin serta ovalbumin. Ovomucin, globulin serta conalbumin mempunyai kemampuan membuih yang tinggi, dan lysozyme, ovomucoid serta ovalbumin menunjukkan karakteristik membuih yang rendah.
Ovomucin merupakan glikoprotein, dicirikan oleh sifat kekentalan yang tinggi. Pada proses pembentukan buih, ovomucin berperan membentuk film dari materi tak terlarut dan menstabilkan buih (Stadelman dan Cotterill, 1977).
Ovalbumin adalah salah satu jenis protein dalam putih telur yang terbanyak (54% dari total protein putih telur) yang mempunyai kemampuan membentuk buih (Alleoni dan Antunes, 2004). Protein ini pada pembuatan kue akan menggumpal
17
saat dipanaskan dan akan mempengaruhi struktur dan tekstur kue yang dihasilkan.
Ovalbumin tidak akan hilang akibat pengocokan dan jumlahnya tetap sama
dengan kandungan telur segar (Stadelman dan Cotterill, 1977).
Globulin berperan dalam kekentalan putih telur dan mencegah mencairnya
gelembung udara. Globulin mempunyai tegangan permukaan yang rendah sehingga membantu tahapan pembentukan buih. Tegangan permukaan yang rendah cenderung memperkecil ukuran gelembung dan meratakan tekstur buih. Kandungan globulin serta ovomucin yang rendah, membutuhkan waktu pengocokan yang lebih lama dalam pembentukan buih putih telur dan bila digunakan dalam pembuatan cake dapat menyebabkan pembentukan volume yang kurang baik (Stadelman dan Cotterill, 1977).
3. Pembentukan Buih
Buih dapat didefinisikan sebagai dua fase yang terdiri atas fase gas dalam fase cair. Buih merupakan dispersi koloid dari fase gas yang terdispersi di dalam fase cair atau fase padat. Daya buih merupakan ukuran kemampuan putih telur untuk membentuk buih jika dikocok dan biasanya dinyatakan dalam persen terhadap putih telur (Stadelman dan Cotterill, 1977).
Perubahan putih telur menjadi buih disebabkan denaturasi protein, yaitu proses yang mengubah struktur molekul protein tanpa memutuskan ikatan kovalen. Pemekaran atau pengembangan molekul protein yang terdenaturasi akan membuka gugus reaktif yang ada pada rantai polipeptida (Belitz dan Grosch, 1999). Denaturasi protein dapat disebabkan bukan hanya karena panas tetapi juga
18
oleh pH ekstrim (terlalu asam atau terlalu basa), beberapa pelarut organik seperti alkohol atau aseton, zat terlarut tertentu seperti urea, detergen atau hanya dengan pengguncangan intensif (mekanik) larutan protein yang bersinggungan dengan udara sehingga terbentuk buih.
Mekanisme terbentuknya buih diawali dengan terbukanya ikatan-ikatan dalam molekul protein sehingga rantainya menjadi lebih panjang. Tahap selanjutnya adalah proses adsorpsi yaitu pembentukan monolayer atau film dari protein yang terdenaturasi. Udara ditangkap dan dikelilingi oleh film dan membentuk gelembung. Pembentukan lapisan monolayer kedua dilanjutkan di sekitar gelembung untuk mengganti bagian film yang terkoagulasi. Film protein dari gelembung yang berdekatan akan berhubungan dan mencegah keluarnya cairan. Terjadinya peningkatan kekuatan interaksi antara polipeptida akan menyebabkan agregasi (pengumpulan) protein dan melemahnya permukaan film dan diikuti dengan pecahnya gelembung buih (Chairungsriled et.al., 1996).
Perubahan tersebut menyebabkan hilangnya daya larut atau sifat koagulasi putih telur, dan absorpsi buih penting untuk kestabilan buih (Stadelman dan Cotterill, 1977). Semakin lama ikatan yang terbentuk tersebut akan semakin melemah dan tirisan akan keluar dari lamela yang terdapat diantara gelembung, pada akhirnya ini dapat menyebabkan rusaknya film buih. Volume buih yang tinggi diperoleh dari putih telur dengan elastisitas rendah, sebaliknya struktur buih yang stabil pada umumnya akan dihasilkan dari putih telur yang memiliki elastisitas yang tinggi. Jika putih telur terlalu banyak dikocok atau direnggangkan seluas mungkin akan menyebabkan hilangnya elastisitas (Stadelman dan Cotterill, 1977).
19
Kestabilan buih merupakan ukuran kemampuan struktur buih untuk bertahan kokoh atau tidak mencair selama waktu tertentu. Indikator kestabilan buih adalah besarnya tirisan buih selama waktu tertentu dan dinyatakan dalam bobot, volume atau derajat pencairan buih (Stadelman dan Cotterill, 1977). Tirisan buih terjadi karena ikatan antara udara dengan protein putih telur yang kurang kokoh, sehingga setelah didiamkan beberapa saat akan terbentuk tirisan buih. Mekanisme pembentukan buih dapat dilihat pada Gambar 2.
Gambar 1 : Mekanisme Pembentukan Buih
Sumber : Cherry and Mc. Waters (1981)
20
E. Desktrin
Telah dilakukan usaha pengembangan teknologi pembuatan dekstrin (pati termodifikasi) dari pati berasal dari umbi suweg dengan proses hidrolisa cara enzimatis. Dekstrin (dengan nama lain : Anylin) merupakan polimer D-glukosa yang merupakan hasil antara hidrolisis pati (Ruqoiyah, 2002). Dekstrin adalah produk hidrolisa zat pati, berbentuk zat amorf berwarna putih sampai kekuning-kuningan. Dekstrin merupakan produk degradasi pati sebagai hasil hidrolisis tidak sempurna pati dengan katalis asam atau enzim pada kondisi yang di kontrol. Dekstrin umumnya berbentuk bubuk dan berwarna putih sampai kuning keputihan (Anonimous, 2009).
Dekstrin merupakan produk degradasi pati yang dapat dihasilkan dengan beberapa cara yaitu memperlakukan suspensi pati dalam air dengan asam atau enzim pada kondisi tertentu, atau degradasi / pirolisis pati dalam bentuk kering dengan menggunakan perlakuan panas atau kombinasi antara panas dan asam atau katalis lain. Dekstrin mempunyai rumus kimia (C
6H10O5)n dan memiliki struktur serta karakteristik intermediate antara pati dan dextrose seperti pada Gambar 3.
21
Gambar 2. Struktur Dekstrin (Anonimous, 2009).
Berdasarkan reaksi warnanya dengan iodium, dekstrin dapat diklasifikasikan atas amilodekstrin, eritrodekstrin dan akrodekstrin. Pada tahap awal hidrolisa, akan dihasilkan amilodekstrin yang masih memberikan warna biru bila direaksikan dengan yodium. Bila hidrolisa dilanjutkan akan dihasilkan eritrodekstrin yang akan memberikan warna merah kecoklatan bila direaksikan dengan iodium. Sedangkan pada tahap akhir hidrolisa, akan dihasilkan akrodekstrin yang tidak memberikan warna bila direaksikan dengan iodium (Anonimous, 2009).
Dekstrin larut dalam air dingin dan larutannya bila direaksikan dengan alkohol atau Ca / BaOH akan menghasilkan endapan dekstrin yang bentuknya tidak beraturan. Dekstrin merupakan produk degradasi pati sebagai hasil hidrolisis tidak sempurna pati dengan katalis asam atau enzim pada kondisi yang di kontrol. Dekstrin umumnya berbentuk bubuk dan berwarna putih sampai kuning keputihan (Anonimous, 2009).
22
F. Pengeringan
Pengeringan mempunyai pengertian yaitu aplikasi pemanasan melalui kondisi yang teratur, sehingga dapat menghilangkan sebagian besar air dalam bahan makanan dengan cara diuapkan. Penghilangan air dalam bahan pangan dengan cara pengeringan mempunyai satuan operasi yang berbeda dengan dehidrasi. Dehidrasi akan menurunkan aktivitas air yang terkandung dalam bahan pangan dengan cara mengeluarkan air dalam jumlah lebih banyak, sehingga umur simpan bahan pangan menjadi lebih panjang atau lebih lama. Pengurangan air tersebut dapat menghambat tumbuhnya mikroba dan aktivitas enzim, namun tidak dapat melakukan inaktivasi. Hal ini dikarenakan suhu selama proses tidak mencukupi untuk melakukannya.
Pengeringan sering juga digunakan dalam pengawetan makanan, sehingga dapat variasi makanan menjadi bertambah dan membuat makanan lebih bergizi dan terasa enak. Proses pengeringan juga dapat digunakan untuk mengurangi berat dan besar suatu bahan pangan. Hal ini dapat mendatangkan keuntungan, karena proses pengemasan dan distribusi bahan pangan menjadi lebih mudah. Kerugian dari dilakukannya proses pengeringan adalah kualitas dan nilai gizi yang terdapat pada bahan pangan menjadi turun.
Pengeringan merupakan suatu cara untuk mengeluarkan atau menghilangkan sebagian besar air dari suatu bahan dengan menggunakan energy panas. Keuntungan pengeringan adalah bahan menjadi lebih tahan lama disimpan dan volume bahan menjadi lebih kecil sehingga mempermudah dan menghemat ruang
23
pengangkutan dan pengepakan. Di sisi lain, pengeringan menyebabkan sifat asli bahan mengalami perubahan, penurunan mutu dan memerlukan penanganan tambahan sebelum digunakan yaitu rehidrasi.
Pengeringan juga didefinisikan sebagai suatu proses pengeluaran air dari bahan sehingga tercipta kondisi dimana kapang, jamur, dan bakteri yang menyebabkan pembusukan tidak dapat tumbuh. Pengeringan adalah suatu proses pengeluaran kadar air untuk memperoleh kadar air yang aman untuk penyimpanan. Tujuan pengeringan adalah mengurangi kadar air bahan sampai batas perkembangan mikroorganisme dan kegiatan enzim yang dapat menyebabkan pembusukan terhambat atau terhenti.
Proses pengeringan yang umumnya digunakan pada bahan pangan ada dua cara, yaitu pengeringan dengan penjemuran dan pengeringan dengan alat pengering. Kelemahan dari penjemuran adalah waktu pengeringan lebih lama dan lebih mudah terkontaminasi oleh kotoran atau debu sehingga dapat mengurangi mutu akhir produk yang dikeringkan. Di sisi lain, pengeringan yang dilakukan menggunakan alat pengering biasanya lebih mahal, tetapi mempunyai kelebihan yaitu kondisi sanitasi lebih terkontrol sehingga kontaminasi dari debu, serangga, burung dan tikus dapat dihindari. Selain itu pula dehidrasi dapat memperbaiki kualitas produk yang dihasilkan.
Pemilihan jenis alat dan kondisi pengering yang akan digunakan tergantung dari jenis bahan yang dikeringkan, mutu hasil akhir yang dikeringkan dan pertimbangan ekonomi, misalnya untuk bahan yang berbentuk pasta atau pure
24
maka alat pengering yang sesuai adalah alat pengering drum, sedangkan untuk bahan yang berbentuk lempengan atau jenis bahan padatan dapat menggunakan pengering kabinet. Jenis alat pengering lainnya yang dapat digunakan untuk bahan pangan adalah pengeringan terowongan, pengering semprot, pengering fluidized bed, pengering beku dan lain-lain.
Efisiensi sistem dan alat pengeringan merupakan salah satu faktor yang perlu dipertimbangkan dalam aplikasi pengeringan dan optimasinya. Efisiensi operasi pengeringan dapat dinyatakan sebagai perbandingan panas yang secara teoritis diperlukan untuk menguapkan air dengan penggunaan panas yang sebenarnya di dalam alat pengering. Efisiensi tersebut berguna untuk mempelajari pendugaan atau konstruksi alat pengering dan studi perbandingan antar berbagai alat pengering yang digunakan untuk alternative.
Proses pengeringan pada bahan dimana udara panas dialirkan dapat dianggap sebagai salah satu proses adiabatik. Hal ini berarti panas yang diberikan untuk penguapan air dari bahan hanya disuplai oleh udara pengering secara konduksi atau radiasi tanpa tambahan energi dari luar.
Proses perpindahan panas terjadi karena suhu bahan lebih rendah dari suhu udara yang dialirkan disekeliling bahan. Panas yang diberikan ini akan menaikkan suhu bahan dan akan menyebabkan tekanan uap air di udara sehingga terjadi perpindahan uap air dari bahan ke udara. Peristiwa perpindahan uap air ke udara ini disebut peristiwa pindah massa.
Faktor-faktor yang mempengaruhi pengeringan ada dua golongan, yaitu ;
25
1. Faktor yang berhubungan dengan udara pengering (suhu, kecepatan volumetrik aliran udara pengering, dan kelembaban udara.
2. Faktor yang berhubungan dengan sifat bahan (ukuran bahan, kadar air awal, dan tekanan parsial dalam bahan)
Bahan pangan yang dihasilkan dari produk-produk pertanian pada umumnya mengandung kadar air tinggi. Kadar air tersebut apabila masih tersimpan dan tidak dihilangkan, maka akan dapat mempengaruhi kondisi fisik bahan pangan.
Metode pengeringan pangan maupun non-pangan yang umum dilakukan antara lain adalah pengeringan matahari (Sun drying), rumah kaca (Greenhouse), oven, iradiasi surya (Solar Drying), pengeringan beku (Freeze drying) dan yang berkembang saat ini pengeringan menggunakan sinar infra merah. Pangan dapat dikeringkan dengan beberapa cara yaitu menggunakan matahari, oven atau microwave. Pengeringan merupakan metode pengawetan yang membutuhkan energy dan biaya yang cukup tinggi, kecuali pengeringan matahari (Sun Drying).
G.
Foam Mat DryingSalah satu metode yang sering digunakan pada pembuatan produk pangan siap saji adalah metode foam mat drying. Foam mat drying (pengeringan busa) tergolong dalam atmospheric drying. Metode pengeringan busa digunakan untuk mengeringkan bahan berbentuk cair (Anonimous, 2001).
Foam menyangkut campuran cair dan gas. Pembentukan busa memerlukan bahan
aktif permukaan dan penting dalam bebagai produk pangan (Tranggono, et al., 1990). Menurut Baniel, et al. (1997), foam (busa) dapat didefinisikan sebagai
26
suatu sistem yang terbentuk oleh dua fase, yaitu udara sebagai fase terdispersi dan air sebagai fase kontinyu. Salah satu metode yang telah digunakan untuk membentuk foam adalah dengan pengocokan dengan menggunakan mixer. Foam
mat drying adalah cara pengeringan bahan berbentuk cair yang sebelumnya
dijadikan foam terlebih dahulu dengan menambahkan zat pembuih (Desrosier, 1988).
Karim dan Wai (1997), melaporkan bahwa metode pengeringan busa diaplikasikan pada bahan pangan yang sensitif terhadap panas. Dalam proses pengeringan busa, bahan makanan yang berbentuk cair atau semi cair dikocok hingga berbentuk busa yang stabil dan selanjutnya dikeringkan dengan pemanasan. Setelah dilakukan pemanasan, bahan dihancurkan menjadi bentuk bubuk. Menurut Woodrof dan Luh (1975), makanan yang dikeringan dengan metode foam mat drying mempunyai struktur yang mudah menyerap air, sehingga makanan tersebut mudah untuk dilarutkan dalam air dingin. Keuntungan pengeringan menggunakan metode foam mat drying menurut Karim dan Wai (1997) dan Kumalaningsih (2005), antara lain :
1. Bentuk busa maka penyerapan air lebih mudah dalam proses pengocokan dan pencampuran sebelum dikeringkan.
2. Suhu pengeringan tidak terlalu tinggi sebab dengan adanya busa maka akan mempercepat proses penguapan air walaupun tanpa suhu yang terlalu tinggi, suhu yang digunakan sekitar 50ºC - 80ºC dan dapat menghasilkan kadar air hingga 3%, produk yang dikeringkan menggunakan busa pada suhu 71ºC dapat menghasilkan kadar air 2%.
27
3. Bubuk yang dihasilkan dengan metode foam mat drying mempunyai kualitas warna dan rasa yang bagus, sebab hal tersebut dipengaruhi oleh suhu penguapan yang tidak terlalu tinggi sehingga warna produk tidak rusak dan rasa tidak banyak yang terbuang.
4. Biaya pembuatan bubuk dengan menggunakan metode foam mat drying lebih murah dibandingkan dengan metode vakum atau freeze drying sebab tidak terlalu rumit dan cepat dalam proses pengeringan sehingga energi yang dibutuhkan untuk pengeringan lebih kecil dan waktunya lebih singkat.
5. Bubuk yang dihasilkan mempunyai densitas yang rendah (ringan), dengan banyak gelembung gas yang terkandung pada produk kering sehingga mudah dilarutkan dalam air.
6. Foam mat drying baik digunakan karena strukturnya mudah menyerap air, dan relatif stabil selama penyimpanan.
Keberhasilan teknik pengeringan busa sangat ditentukan oleh kecepatan pengeringan yang dapat dilakukan dengan cara pengaturan suhu dan konsentrasi bahan pengisi yang tepat. Suhu yang terlalu tinggi akan menyebabkan hilangnya senyawa-senyawa volatil atau yang mudah menguap seperti aroma dan mempercepat reaksi pencoklatan dalam bahan pangan, sedangkan suhu yang terlalu rendah akan menyebabkan proses pengeringan kurang efisien dan juga akan mendorong kerusakan selama proses (Kumalaningsih et al., 2005).
Pengeringan bahan pangan sampai kadar airnya dibawah 5% akan dapat mengawetkan rasa dan nutrisi serta dapat disimpan untuk jangka waktu yang
28
lama. Sedangkan karakteristik bahan pangan bubuk memiliki kadar air 2-4% (Kumalaningsih et al., 2005).
29
III. METODOLOGI PENELITIAN
A. Waktu Dan Tempat Penelitian
Penelitian dilaksanakan di Laboratorium Pengolahan Hasil Pertanian, Jurusan Teknologi Hasil Pertanian Universitas Lampung, Laboratorium Jasa Analisis Universitas Brawijaya Malang dan Politeknik Negeri Lampung. Penelitian dilaksanakan pada bulan Oktober 2013 sampai Februari 2014.
B. Bahan dan Alat
Bahan utama yang digunakan dalam penelitian adalah kulit buah manggis dengan tingkat kematangan 5 yaitu berumur 114 hari yang diperoleh dari Kabupaten Tanggamus Provinsi Lampung dan putih telur. Bahan pembantu yang digunakan adalah dekstrin yang diperoleh dari CV Yona Kimia Bandar Lampung dan air.
Alat-alat yang digunakan dalam penelitian antara lain timbangan analitik dua digit (Mettler PJ 3000), pisau stainless stell kiwi, panci email (bima), kompor gas (Rinai), blender merek Phillips, Mixer merek Phillips, sendok, baskom plastik, loyang alumunium, panci, kain saring (Hero), oven vakum, pH meter, refraktometer, spektrofotometer dan colorimeter.
30
C. Metode Penelitian
Penelitian berupa perlakuan tunggal disusun dalam Rancangan Acak Kelompok Lengkap dengan enam perlakuan dan empat ulangan. Perlakuan tunggal adalah konsentrasi putih telur sebagai foam agen yang terdiri dari 6 taraf yaitu P0 (tanpa putih telur), P1 (konsentrasi putih telur 5%), P2 (konsentrasi putih telur 10%), P3 (konsentrasi putih telur 15%), P4 (konsentrasi putih telur 20%) dan P5 (konsentrasi putih telur 25%). Data dianalisis kesamaan ragam dengan uji Bartlet dan kemenambahan data dengan uji Tukey. Selanjutnya dilakukan analisis ragam untuk mengetahui pengaruh perlakuan. Apabila terdapat pengaruh yang nyata, data dianalisis lebih lanjut dengan uji Beda Nyata Terkecil (BNT) pada taraf nyata 5 %.
D. Pelaksanaan Penelitian
Penelitian dilakukan dalam tiga tahap. Tahapan pertama adalah pembuatan tepung kulit manggis, pada tahap kedua dilakukan pembuatan sari kulit manggis, sedangkan pada tahap ketiga dilakukan pembuatan bubuk instan kulit manggis. Setiap ulangan pada proses pembuatan bubuk instan kulit manggis terdiri dari enam satuan percobaan yang berasal dari banyaknya perlakuan. Setelah diperoleh enam satuan percobaan dilakukan pengamatan sifat fisik, kadar antosianin dan aktivitas antioksidan bubuk instan kulit manggis. Ulangan kedua, ketiga dan keempat dilakukan dengan cara yang sama seperti ulangan pertama tetapi dilakukan pada hari yang berbeda.
31
1. Pembuatan Serbuk Kulit Manggis
Proses pembuatan serbuk kulit manggis adalah dengan cara memisahkan daging buah manggis dengan kulit manggis menggunakan pisau stainles sebanyak 20 kg. Selanjutnya kulit buah manggis tersebut dikerok dengan sendok untuk memisahkan daging kulit dengan lapisan luar kulit buah manggis yang keras. Setelah dikerok selanjutnya dilakukan pengecilan ukuran dan dilakukan penghancuran menggunakan cuper selama 3 menit dengan kecepatan tinggi (skala 3). Sehingga diperoleh serbuk kulit manggis sebanyak 2,4 kg dengan kadar air 76,2%. Proses pembuatan serbuk kulit manggis dapat dilihat pada Gambar 3.
Gambar 3. Pembuatan serbuk kulit manggis
2. Pembuatan Filtrat Kulit Manggis
Proses pembuatan filtrat kulit manggis dimulai dengan penambahan air sebanyak 300% dari bahan berupa serbuk kulit manggis dan direbus selama 30 menit selanjutnya disaring sehingga diperoleh filtrat sebasar 50%. Ampas kulit
Pembelahan kulit manggist
Buah Manggisbu
Pengerokan kulit manggis dengan sendok Daging Buah
Pengecilan ukuran dengan blender kering
Serbuk Kulit ManggisT Daging kulit manggis
32
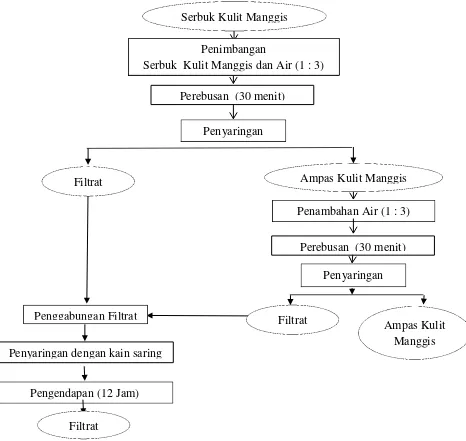
manggis selanjutnya ditambah air sebanyak 300% kemudian direbus kembali selama 30 menit sehingga diperoleh filtrat kulit manggis. Filtrat kulit manggis perebusan pertama dan kedua digabung kemudian diendapkan selama 12 jam lalu disaring hasilnya adalah filtrat kulit manggis yang siap untuk dibuat bubuk ekstrak kulit manggis. Diagram alir proses pembuatan sari kulit manggis dapat dilihat pada Gambar 4.
Gambar 4. Diagram alir proses pembuatan filtrat kulit manggis Sumber : Tari (2007) yang telah dimodifikasi
Perebusan (30 menit) Penyaringan
Penambahan Air (1 : 3)
Perebusan (30 menit) Penyaringan Penimbangan Serbuk Kulit Manggis dan Air (1 : 3)
Penggabungan Filtrat
Penyaringan dengan kain saring
Pengendapan (12 Jam)
Serbuk Kulit Manggis
Filtrat
Filtrat Ampas Kulit
Manggis
Filtrat
Ampas Kulit Manggis
33
3. Pembuatan Bubuk Instan Ekstrak Kulit Manggis
Penelitian disusun dalam Rancangan Acak Kelompok Lengkap (RAKL) dengan 4 ulangan (kelompok). Setiap ulangan pada proses pembuatan bubuk instan ekstrak kulit manggis terdiri dari 6 taraf yaitu konsentrasi putih telur sebagai foam agen. Setelah diperoleh 6 satuan percobaan, selanjutnya dilakukan pengamatan terhadap parameter yang diuji pada ke 6 satuan percobaan tersebut. Ulangan kedua, ketiga dan keempat dilakukan dengan cara yang sama seperti ulangan pertama, namun perlakuan perlakuan percobaan dilakukan pada hari yang berbeda.
Proses pembuatan bubuk instan ekstrak kulit manggis adalah sebagai berikut : Memisahkan putih telur dan kuning telur, selanjutnya menimbang filtrat kulit buah manggis dan putih telur dengan perbandingan (1) 230 g : 0 % ; (2) 230 g : 5% ; (3) 230 : 10% ; (4) 230 g : 15%; (5) 230 g : 20%; dan (6) 230 g : 25% dan menimbang dekstrin sebanyak 10 % dari berat bahan atau sebesar 23 g. Setelah bahan ditimbang sesuai dengan perlakuan selanjutnya mencampur filtrat kulit manggis, dekstrin, dan putih telur dengan menggunakan mixer selama 7 menit. Setelah semua bahan tercampur dan membentuk busa kemudian dituangkan pada loyang pengering dengan ketebalan 3 mm kemudian dikeringkan pada oven dengan suhu 55o C selama 7 jam hingga diperoleh ekstrak kulit manggis. Selanjutnya dilakukan penghancuran ekstrak kulit manggis dengan blender kering selama 30 detik, kemudian dilakukan pengayakan dengan ayakan 60 mesh. Diagram alir proses pembuatan bubuk instan kulit manggis dapat dilihat pada Gambar 5.
34
Gambar 5. Diagram alir pembuatan bubuk instan kulit manggis Sumber : Tari (2007) yang telah dimodifikasi.
Putih telur 0%, 5%, 10 %, 15 %, 20%, 25%
Pengeringan dengan oven (T 55 OC , t 7 jam) )UAH
Bubuk Instan Kulit Manggis
Filtrat Kulit Manggis (230 g)
Pemasukan ke dalam Loyang
Pengocokan dengan mixer (7 menit)
Pemasukan ke loyang stainles dengan ketebalan 3 mm
Penghancuran (blender kering 30 detik) Ekstrak Kulit Manggis Kering
Pengayakan 60 mesh
Dekstrin 10 %
35
E. Pengamatan
1. Rendemen
Pengamatan terhadap rendemen bubuk sari kulit buah manggis dengan metode (AOAC, 1996) adalah dengan membandingkan antara berat bahan baku dibagi dengan berat hasil ekstrasi dikalikan 100 % sehingga diperoleh hitungan dengan menggunakan rumus:
Berat bubuk ekstrak kulit manggis
Rendemen % = --- x 100 %. Berat filtrat kulit manggis
2. Tingkat Kelarutan
Pengujian tingkat kelarutan menggunakan metode Yuwono dan Santoso (1988). Pengujian tingkat kelarutan didasarkan pada prinsip mengukur jumlah sampel yang tidak larut dalam waktu dan kondisi yang telah ditentukan. Kertas saring whatman 41 di oven pada suhu 1050C selama 10 menit, didinginkan dalam desikator dan ditimbang sampai konstan (a), sampel produk sebanyak 3,5 g (berat awal) ditimbang dan dimasukkan ke dalam 150 ml air bersuhu 250C. Setelah itu disaring dengan kertas saring yang telah diketahui beratnya, kemudian kertas saring tersebut dioven kembali pada suhu 1050C selama 3 jam. Selanjutnya didinginkan dalam desikator dan ditimbang sampai didapatkan berat konstan (b)
Perhitungan : Berat akhir = (b-a)
(berat awal – berat akhir)
Kelarutan = --- x 100 % Berat awal
36
3. Kecepatan Larut
Penentuan kecepatan larut digunakan metode Yuwono dan Susanto (1998). Penentuan kecepatan larut dilakukan dengan menyiapkan 100 ml air dingin dengan suhu kurang lebih 250C. Sampel yang sudah ditimbang dimasukkan ke dalam 100 ml air tersebut. Waktu yang dibutuhkan untuk melarutkan seluruh sampel dihitung dengan menggunakan stopwatch. Kemudian kecepatan larut ditentukan dengan rumus sebagai berikut :
Berat sampel (g) Kecepatan larut = --- Waktu larut (dtk)
4. Kadar antosianin
Pengujian kadar antosianin dilakukan menggunakan metode Giusti dan Wrolstad (2000).
• Persiapan bahan:
- Dibuat larutan buffer pH 1 dengan cara mencampurkan KCl 0,2 M 14,9 g diencerkan dalam 1000 ml dalam labu ukur (larutan A) dan HCl 0,2 M (larutan B), buffer pH 1 (50 ml larutan A + 97 ml larutan B diencerkan sampai 200 ml) diukur pH sampai mencapai pH 1
- Dibuat larutan buffer pH 4,5 dengan cara mencampurkan asam asetat 0,2 M 11,55 ml asetat dalam 1000 ml (larutan A) dan larutan Na-asetat 0,2 M 16,49 g dalam 1000 ml (larutan B), buffer pH 4,5 (28 ml larutan A + 22 ml larutan B diencerkan sampai 100 ml) diukur pH sampai mencapai pH 4,5
37
• Preparasi sampel padat :
- Sampel dihancurkan kemudian ditimbang sebanyak 20 g
- Dimasukkan dalam labu ukur 100 ml, kemudian diekstrak dengan menambahkan pelarut HCl 1% dalam metanol sampai tanda batas
- Diekstrak dan dihomogenkan, kemudian dimaserasi selama 4 jam dan disaring dengan menggunakan kertas saring wathmant no 1 ekstrak kembali sampai antosianin tersekstrak semua
- Filtrat disentrifuse selama 10 menit pada putaran angka 7 (4000 rpm) - Jika sampel mengandung lemak tinggi maka diekstrak terlebih dahulu
dengan petroleum ether
- Dan jika mengandung gula tinggi maka tambahkan serbuk bentonit pada saat sampel disaring
• Preparasi sampel cair :
- Hasil preparasi sampel (filtrat) dipipet sebanyak 1 ml dan dimasukkan dalam labu ukur 10 ml, kemudian diencerkan dengan menggunakan larutan buffer pH 1,0 sampai tanda batas
- Diambil 1 ml larutan hasil preparasi dan dimasukkan dalam labu ukur 10 ml, kemudian diencerkan dengan menggunakan larutan buffer pH 4,5 sampai tanda batas
- Diukur absorbansi tiap sampel pada λ maks dan λ 700 nm
• Dihitung absorbansi sampel dengan rumus :
A = (A λmax – A λ700 nm)pH 1,0 – (A λmax – A λ700 nm)pH 4,5
38
ε = koefisien absorbsivitas antosianin (Peonidin-3-5-diglusida = 36654
L/mol)BM = Berat Molekul antosianin (Peonidin-3-5-diglusida = 463,2)
FP = Faktor Pengenceran V = Volume larutan W = Berat sampel awal
λmax = menunjukkan serapan paling tinggi pada sampel λ700 nm = menunjukkan serapan Peonidin-3-5-diglusida
5. Aktivitas antioksidan
Uji aktivitas antioksidan dilakukan dengan metode DPPH (Kubo et al, 1963 ( 1,1-diphenyl-2-picrylhydrazil radical-scavenging).
a. Absorbansi kontrol
Larutan DPPH dengan konsentrasi 0,07mM dalam etanol 96 % diambil 10 ml, kemudian diinkubasi pada suhu 37º C selama 30 menit. Setelah itu diukur absobansinya pada panjang gelombang 517 nm.
b. Absobansi Sampel
Masing – masing sampel dicentrifuge dengan kecepatan 3500 rpm selama 15 menit. Setelah terpisah sampel cair dengan padatan diambil sampel cair sebanyak 7,5 ml dan ditambahkan larutan DPPH 0,07 mM dalam etanol 96 % v/v sebanyak 2,5 ml. Setelah itu diinkubasi pada suhu 37º C selama 30 menit, kemudian dimasukan kedalam duvet untuk diukur absorbansinya pada panjang gelombang 517 nm. Nilai % aktivitas antioksidan diperoleh dengan rumus (Molyneux, 2004)
39
(Ak-As)
% Aktivitas Antioksidan =--- x 100 % Ak
Keterangan :
Ak = Absorbansi Kontrol As = Absorbansi Sampel
6. Warna (Pomeranz, et al., 1978)
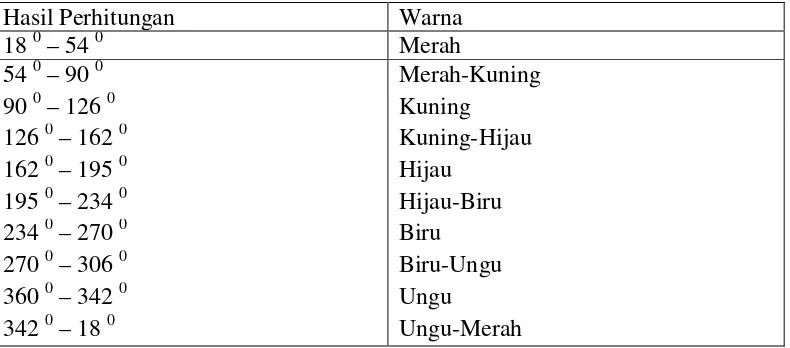
Intensitas warna diukur dengan menggunakan kromameter CR-200 merek “Minolta”. Pada kromameter ini digunakan sistem warna x, y, Y. Kemudian dari koordinat warna x, y, Y diubah menjadi L, a, b. L menunjukkan kecerahan, a dan b adalah koordinat-koordinat kromatis dimana a untuk warna hijau (a negative) ke merah (a positif) dan b untuk biru (b negatif) sampai kuning (b positif). Semakin tinggi nilai L, maka semakin tinggi tingkat kecerahan warnanya. Selanjutnya dari nilai a dan b dapat dihitung 0 Hue dengan rumus: 0 Hue = tan-1 b/a
Tabel 2. Perhitungan nilai Hue
Hasil Perhitungan Warna
Sebelum dilakukan pengukuran terhadap bubuk instan kulit manggis, kromameter CR-200 dikalibrasi terlebih dahulu dengan menggunakan Calibration Plate dengan Y = 94.1 ; x = 0.3134 ; y = 0.3211. Setelah alat dikalibrasi, bubuk instan
40
kulit manggis dianalisis dengan diukur tingkat kecerahannya serta intensitas warna merah dan kuning dari masing-masing produk dengan nilai Y, x, dan y. Pengukuran tiap produk dilakukan sebanyak 3 kali.
59
V. SIMPULAN DAN SARAN
A. Simpulan
Berdasarkan hasil penelitian maka dapat disimpulkan sebagai berikut :
1. Konsentrasi putih telur sebagai foam agent berpengaruh nyata terhadap rendemen, aktivitas antioksidan, derajad kecerahan dan derajad kemerahan bubuk instan ekstrak kulit manggis.
2. Konsentrasi putih telur sebagai foam agent yang menghasilkan bubuk instan ekstrak kulit manggis terbaik diperoleh pada perlakuan konsentrasi putih telur 15% (P3) dengan rendemen sebesar 20,48%, tingkat kelarutan sebesar 73,39%, kecepatan larut sebesar 0,0055/detik, kadar antosianin sebesar 2,12%, aktivitas antioksidan sebesar 56,00%, derajad kecerahan (L*) sebesar 56,33, serta derajad kemerahan (a*) sebesar 17,83.
B. Saran
60
DAFTAR PUSTAKA
Anonimous. 2009. Metode Pengeringan Busa, Manfaat dan Permasalahannya. Departemen Perindustrian. Jakarta.
Anonimous. 2011. Tanaman Pangan : Singkong. Badan Pusat Statistik. http://www.bps.go.id/tnmn_pgn.php?kat=3 (diakses pada 25 Juni 2014) Alkoni dan A.J. Antunes. 2004. Albumen Foam Stability and Ovalbumin
Contents In Eggs Corted with Whey Protein Concentrate. Journal Revista Brasileira de Ciencia Avicola. 6(2):105–110.
AOAC. 1996. Official Methods of Analysis of Official Analitical Chemist. Washington.
Asano J., K. Chiba, M. Tada, dan T. Yoshii. 1996. Cytotoxic Xanthones From Garcinia Hanburyi. JournalPhytochemistry. 41(3):815-820.
Baniel, A., A. Fains dan Y. Poineau. 1997. Foaming Properties of Egg Albumen with a Bubbling Apparatus Compared with Whipping. Journal of Food Sciences. 62:377-378.
Belitz, H. D. dan Grosch 1987. Food Chemistry. Springer Verlag Berlin. Heidelberg.
Buckle, K.A., R.A. Edward, G.H. Fleet dan M. Wootton. 1978. Ilmu Pangan. Diterjemahkan oleh Hari Poernomo dan Andiono. UI Press. Jakarta.
Chairungsrilerd N., K. Furukawa, T. Ohta, S. Nozoe, dan Y. Ohizumi. 1996a. Histaminergic and Serotonergic Receptor Blocking Substances From The Medical Plant Garcinia mangosta. Planta Media 62(5): 471-472.
Chairungsrilerd N., K. Furukawa, T. Ohta, S. Nozoe, dan Y. Ohizumi. 1996b, Pharmacological Properties of Alpha-mangostin, a Novel Histamin HI Receptor Antagonist. Europa Journal Pharmacol 314(3):351-356.
Cherry, J. P. dan Mc Waters. 1981. Protein Functionality in Foods. American Chemical Soviety, Washington
61
Dalimartha dan Soedibyo. 1999. Pengaruh Pengolahan Terhadap Kandungan Antioksidan pada Biji Kedelai. (Skripsi) Universitas Jember.
Desrosier, NW. 1988. Teknologi Pengawetan Pangan. Penterjemah M. Muljoharjo. Penerbit UI-Press. Jakarta 614 Hal.
De Mann, J. 1989. Kimia Makanan. Terjemahan Oleh Kosasih Padmawinata. Penerbit ITB Bandung. Bandung
Endang S.S. dan Prasetyastuti. 2010. Pengaruh Pemberian Juice Lidah Buaya
(Aloevera L) terhadap Kadar Lipid Peroksida (MDA) pada Tikus Putih
Jantan Hyperlipidemia. Jurnal Farmasi Kedokteran 3(1):353-362.
Estiasih dan Sofiah. 2009. Pembuatan Tepung dengan Metode Foam Mat Drying. (Skripsi). Universitas Muhamadiyah Malang.
Effendi, R. 2006. Pengaruh Konsentrasi Putih Telur Terhadap Kualitas Fisik dan Kimia Susu Bubuk Metode Foam Mat Drying. (Tesis). Fakultas Peternakan Universitas Muhamadiyah Malang.
Fardias, S. 1987. Penuntun Praktikum Mikrobiologi Pangan. PAU Pangan Gizi.
Institut Pertanian Bogor, Bogor.
Fadilah, E.R. Dyartanti, dan E.K. Artati. 2006. Pengeringan Buah Nangka dengan Metode Foam Mat Drying untuk Pembuatan Bubuk Buah Nangka. (Skripsi). Jurusan Teknik Kimia Institut Teknologi Bandung.
Fennema O.R. 1996. Food Chemistry 3rd edition. New York : Marcel Dekker Institut.
Geankoplis, dan J. Christie. 1983. Transport Processes and Unit Operation 3rd edition. Prentice Hall International, inc., Boston.
Giusti, M. M., dan R.E. Wrolstad. 2000. Anthocyanins. Characterization and measurement with UV- visiblespectroscopy. In R.E.Wrolstad(Ed.). Current Protocols in Food Analytical Chemistry. NewYork:Wiley
Hartati, S. 2001. Potensi Pengembangan Genus Garcinia Sumber Bahan Baku Farmasi. Prosiding Seminar Nasional Tumbuhan Obat Indonesia. Puslitbang Kimia Terapan LIPI. Bogor. Halaman 27-33.
Ho, C.K., Y.L. Huang dan C.C. Chen. 2002. Garcinone E,a Xanthone Derivative, Has Potent Cytotoxic Effect Against Hepatocellular Carcinoma Cell Lines. JournalPlanta Media. 68(11):975-979.
62
Kahkonen, P. Marja dan M. Heinonen. 2003. Antioksidan Activity of Anthocyanins and Their Aglicons. Journal Agriculture Food Chemical 51:628-633.
Kamsiati, E. 2006. Pembuatan Bubuk Sari Buah Tomat Dengan Metode Foam Mat Drying. Balai Pengkajian Teknologi Pertanian Kalimantan Tengah. Kalimantan Tengah. Jurnal Teknologi Pertanian 7(2):113 – 119.
Karim, A.A. dan C.C. Wai. 1997. Foam Mat Drying Starfruit (Averrhoa Carambola L.) Purre. Stability and Air Drying Characteristic. Journal Food Chemistry. 64(3) : 337 – 343.
Kenyon, M. 1992. Modified Starch, Maltodekstrin and Corn Syrup Solid as well
Material For Food For Encapsulation Dalam Reinccuss, G.A (ed).
Encapsulation and Controlled Released Of Food Ingredient. Edward Brother Inc. New York.
Kumalaningsih, S., Suprayogi, dan B. Yuda. 2005. Membuat Makanan Siap Saji. Trubus Agrisarana, Surabaya.
Koswara, S. 2009. Teknologi Modifikasi Pati. http:/ebookpangan.com; 30 Agustus 2009.
Kubo, L., M. Tamguchi, A. Chapya, dan K. Tsujimoto. 1980. An Insect Antifeedant and Antimicrobial Agent from Plumbago Capenensis. Journal of Medicinal PlantReseach, Suplement 185-187.
Lastriningsing. 1997. Mempelajari Pembuatan Bubuk Konsentrat Kunyit
(Curcumae Domestice var) dengan Menggunakan Pengering Semprot
(Skripsi) IPB, Bogor.
Limei Y., M. Zhao, B. Yang, Q. Zhao, dan Y. Jiang. 2007. Phenolics from Hull of Garcinia mangostana Fruit and Their Antioxidant Activities. Journal Food Chemestry. 104(1):176-181.
Mahabusarakam W, P. Iriyachitra, dan WC. Taylor. 1987. Chemical Constituents of Garcinia mangostana. Journal National Production 50:474-478.
Mariana, S dan Suwondo. 2009. Ramuan dan Kasiat Kulit Manggis. Penebar Swadaya. Jakarta.
Moongkardi, P, N. Kosem, S. Kaslungka, O. Luanratana, P. Pongpan, dan N. Neungton. 2004. Antiproliferation, Antioxidan and Induction of apoptosis
by Garcinia mangostana (mangosteen) on SKBR3 Human Breast Cancer
Cell Line. Journal Ethnopharmacol 90(1):161-166.
Mujumdar, A. S. 1995. Hand Book of Industrial Drying Second Edition Revised and Expanded. Marcel Dekker, Inc. New York