PRODUKTIVITAS PRIMER PERIFITON
DI SUNGAI CIAMPEA, DESA CIAMPEA UDIK, BOGOR
PADA MUSIM KEMARAU 2010
RINI WIDDYASTUTI
SKRIPSI
DEPARTEMEN MANAJEMEN SUMBERDAYA PERAIRAN FAKULTAS PERIKANAN DAN ILMU KELAUTAN
INSTITUT PERTANIAN BOGOR BOGOR
RINGKASAN
Rini Widdyastuti. C24061877. Produktivitas Primer Perifiton di Sungai Ciampea, Desa Ciampea Udik, Bogor pada Musim Kemarau 2010. Di bawah bimbingan Niken TM Pratiwi dan Enan M Adiwilaga
Perifiton adalah salah satu komunitas di sungai Sungai Ciampea yang berperan sebagai produsen primer, penghasilkan oksigen, dan menjadi sumber penghasil bahan organik di sungai. Keberadaan bahan organik tersebut dapat diduga dari produktivitas perifiton. Oleh karena itu, penelitian ini dilakukan dengan tujuan untuk mengkaji keberadaan bahan organik yang dihasilkan oleh perifiton yang didekati melalui produktivitas primer yang terjadi. Penelitian ini merupakan eksperimen di lapang dengan rancangan percobaan acak lengkap. Objek yang digunakan adalah perifiton yang melekat pada substrat buatan. Penelitian dilaksanakan pada bulan April-Agustus 2010. Penelitian ini terdiri dari dua tahap, yaitu penelitian di lapang dan analisis di laboratorium.
Stasiun pengamatan terdiri dari dua stasiun, yaitu yang terkena sinar matahari langsung (24.630-114.500 Lux) dan yang tidak terkena sinar matahari langsung (11.120-98.360 Lux). Substrat buatan yang digunakan pada penelitian utama adalah tali rafia. Pengamatan dilakukan sebanyak tiga kali, yaitu hari 7, 12, dan ke-17. Nilai produktivitas primer diukur melalui dua pendekatan, yaitu oksigen dan klorofil. Data yang dikumpulkan meliputi data perifiton (kelimpahan dan indeks biologi), produktivitas primer (pendekatan oksigen dan klorofil), dan bahan organik yang dihasilkan (pendekatan oksigen dan klorofil). Analisis data dilakukan menggunakan ANOVA RAL dan regresi.
PRODUKTIVITAS PRIMER PERIFITON
DI SUNGAI CIAMPEA, DESA CIAMPEA UDIK, BOGOR
PADA MUSIM KEMARAU 2010
RINI WIDDYASTUTI C24061877
Skripsi
sebagai salah satu syarat untuk memperoleh
gelar Sarjana Perikanan pada Fakultas Perikanan dan Ilmu Kelautan
DEPARTEMEN MANAJEMEN SUMBERDAYA PERAIRAN FAKULTAS PERIKANAN DAN ILMU KELAUTAN
INSTITUT PERTANIAN BOGOR BOGOR
PERNYATAAN MENGENAI SKRIPSI
DAN SUMBER INFORMASI
Dengan ini saya menyatakan bahwa skripsi yang berjudul :
Produktivitas Primer Perifiton di Sungai Ciampea, Desa Ciampea Udik, Bogor pada Musim Kemarau 2010
adalah benar merupakan hasil karya saya sendiri dan belum diajukan dalam bentuk apapun kepada perguruan tinggi manapun. Semua sumber data dan informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir skripsi ini.
Bogor, Januari 2011
LEMBAR PENGESAHAN
Judul : Produktivitas Primer Perifiton di Sungai Ciampea, Desa Ciampea Udik, Bogor pada Musim Kemarau 2010
Nama : Rini Widdyastuti NIM : C24061877
Program Studi : Manajemen Sumberdaya Perairan
Menyetujui, Komisi Pembimbing
Pembimbing I, Pembimbing II,
Dr. Ir. Niken T.M. Pratiwi, M.Si. Dr. Ir. Enan M. Adiwilaga NIP. 19680111 199203 2 002 NIP. 19481207 198012 1 001
Mengetahui,
Ketua Departemen Manajemen Sumberdaya Perairan
Dr. Ir. Yusli Wardiatno, M.Sc. NIP. 19660728 199103 1 002
UCAPAN TERIMA KASIH
Pada kesempatan ini penulis mengucapkan terima kasih kepada :
1. Dr. Ir. Niken T.M. Pratiwi, M.Si selaku dan Dr. Ir. Enan M.Adiwilaga, selaku ketua dan anggota komisi pembimbing skripsi yang telah memberikan bimbingan, masukan dan arahan sehingga penulis dapat menyelesaikan skripsi ini.
2. Dr. Ir. Hefni Effendi, M.Phil selaku dosen penguji dan Ir. Agustinus M. Samosir, M.Phil selaku ketua komisi pendidikan program S1, atas saran, perbaikan dan nasihat yang telah diberikan.
3. Dr. Ario Damar selaku pembimbing akademik yang telah memberikan nasihat dan bimbingan.
4. Keluarga tercinta, Ibu Estu Iratnowati, Bapak Syahrul Halimi, Kakek H. Sahlani, Irwansyah P., Tri W., Teguh M., dan Mas Nosesa H yang bertemu setelah dewasa atas dukungan, doa, kasih sayang, dan motivasinya.
5. Ibu Siti N, Ibu Ana, Mas Budi, Pak Tony, Pak Heri, dan Mba Widar, yang telah banyak membantu selama penyusunan skripsi ini.
6. Teman-teman MSP 43 yang telah bersama-sama menjalani suka dan duka selama kurang lebih tiga tahun.
7. Keluarga kedua penulis, Pondok Putri Rahmah (Dwi H., Sakinah I., Sari R., Muthmainah, Irfina F., Sri R., Tri U., Fitriani A., Dian, Rina G., Yulia P., dan Kartika P.) atas kebersamaan yang dilalui selama di IPB hingga saat ini. Serta seluruh pihak yang telah berkontribusi dalam membantu penulis menyelesaikan skripsi ini yang tidak dapat disebutkan satu per satu.
RIWAYAT HIDUP
Penulis dilahirkan di Jakarta, pada tanggal 19 Oktober 1988 dari Pasangan Bapak Syahrul Halimi dan Ibu Estu Iratnowati. Penulis merupakan putri pertama dari empat bersaudara. Pendidikan formal ditempuh di SDS Muhammadiyah 41 Jakarta (2000), SLTPN 99 Jakarta (2003), dan SMUN 21 Jakarta (2006). Pada tahun 2006 penulis lulus seleksi masuk Institut Pertanian Bogor melalui jalur Undangan Seleksi Masuk IPB (USMI) di Departemen Manajemen Sumberdaya Perairan, Fakultas Perikanan dan Ilmu Kelautan.
Selama mengikuti perkuliahan penulis berkesempatan menjadi anggota Divisi Kewirausahaan pengurus Himpunan Mahasiswa Manajemen Sumberdaya Perairan (HIMASPER) pada tahun 2007/2008 dan Sekretaris Umum pengurus Himpunan Mahasiswa Manajemen Sumberdaya Perairan (HIMASPER) pada tahun 2008/2009.
Untuk menyelesaikan studi di Fakultas Perikanan dan Ilmu Kelautan, penulis melaksanakan penelitian yang berjudul “Produktivitas Primer Perifiton di Sungai Ciampea, Desa Ciampea Udik, Bogor pada Musim Kemarau 2010”.
PRAKATA
Syukur Alhamdulillah dipanjatkan kehadirat Allah SWT atas rahmat dan karunia-Nya penulis dapat menyusun skripsi ini dengan baik. Adapun skripsi ini berjudul “Produktivitas Primer Perifiton di Sungai Ciampea, Desa Ciampea Udik, Bogor pada Musim Kemarau 2010” disusun berdasarkan penelitian yang dilaksanakan pada bulan April 2010. Skripsi ini disusun sebagai salah satu syarat untuk memperoleh gelar sarjana perikanan pada Fakultas Perikanan dan Ilmu Kelautan, Institut Pertanian Bogor.
Pada kesempatan ini penulis mengucapkan terima kasih kepada Dr. Ir. Niken T.M. Pratiwi, M.Si. dan Dr. Ir. Enan M Adiwilaga, serta kepada seluruh pihak yang telah memberikan bimbingan, arahan, dan kontribusi sehingga penulis dapat menyelesaikan skripsi ini.
Penulis menyadari skripsi ini masih jauh dari sempurna sehingga besar harapan adanya saran dan kritik yang membangun untuk memperbaiki penulisan selanjutnya.
Bogor, Januari 2011
vi
2. TINJAUAN PUSTAKA 2.1. Ekosistem Sungai ... 4
3. METODE PENELITIAN 3.1. Rancangan Penelitian ... 10
b. Indeks keanekaragaman, indeks keseragaman, dan indeks dominansi ... 13
3.3.4.2. Kualitas air ... 14
3.3.4.3. Produktivitas primer ... 15
vii
4. HASIL DAN PEMBAHASAN
4.1. Hasil ... 18
4.1.1. Kelimpahan perifiton ... 18
4.1.2. Kondisi komunitas perifiton ... 18
4.1.3. Kondisi fisika dan kimia perairan ... 19
4.1.4. Bahan organik yang dihasilkan oleh perifiton ... 19
4.1.4.1. Pendekatan oksigen ... 19
4.1.4.2. Pendekatan klorofil ... 20
4.1.5. Analisis statistik ... 20
4.1.5.1. Rancangan Acak Lengkap ... 20
4.1.5.2. Regresi ... 20
4.2. Pembahasan ... 22
5. KESIMPULAN 5.1. Kesimpulan ... 27
DAFTAR PUSTAKA ... 28
viii
DAFTAR TABEL
Halaman 1. Penentuan stasiun pengamatan perifiton di sungai ... 11 2. Parameter, alat, dan metode yang digunakan dalam pengambilan data
kualitas air (APHA, 1995) ... 14 3. Tabel Sidik Ragam (TSR) ... 17 4. ANOVA ... 17 5. Nilai Indeks keanekaragaman, keseragaman, dan dominansi perifiton
pada stasiun 1 dan stasiun 2 ... 18 6. Kondisi fisika dan kimia perairan pada stasiun 1 dan stasiun 2... 19 7. Hasil analisis statistik menggunakan ANOVA RAL ... 20
ix
DAFTAR GAMBAR
Halaman 1. Bagan Alir Penentuan Produktivitas Primer Perifiton
di Sungai Ciampea ... 2 2. Peta Lokasi Penelitian ... 10 3. Kelimpahan perifiton pada stasiun 1 dan stasiun 2 ... 18 4. Bahan organik yang dihasilkan oleh perifiton (gC/m2/hari) melalui
pendekatan oksigen pada stasiun 1 dan stasiun 2 ... 19 5. Bahan organik yang dihasilkan oleh perifiton (gC/m2) melalui
pendekatan klorofil pada stasiun 1 dan stasiun 2 ... 19 6. Hubungan antara cahaya (Lux) dengan kelimpahan perifiton
(ind/cm2) ... 21 7. Hubungan antara cahaya (Lux) dengan bahan organik
yang dihasilkan oleh perifiton (gC/m2/hari)
melalui pendekatan oksigen ... 21 8. Hubungan antara cahaya (Lux) dengan bahan organik
yang dihasilkan oleh perifiton (gC/m2)
x
DAFTAR LAMPIRAN
Halaman 1. Prosedur analisis parameter yang diamati (APHA, 1995) ... 31 2. Contoh organisme yang ditemukan selama pengamatan ... 33 3. Kelimpahan perifiton pada stasiun 1 dan stasiun 2 selama pengamatan .... 34 4. Bahan organik yang dihasilkan oleh perifiton selama pengamatan
melalui pendekatan oksigen dan klorofil ... 35 6. Analisis ANOVA RAL antara pengaruh cahaya
terhadap bahan organik yang dihasilkan oleh perifiton
1. PENDAHULUAN
1.1.Latar Belakang
Sungai Ciampea merupakan salah satu perairan mengalir yang terdapat di Desa Ciampea Udik, Kabupaten Ciampea, Bogor Barat. Daerah di sekitar sungai terdiri atas pemukiman penduduk, dan areal pertanian. Sungai Ciampea dimanfaatkan oleh penduduk sekitar untuk kehidupan sehari-hari dan menjadi kawasan wisata lokal. Selain itu, beberapa penduduk sekitar mendapatkan penghasilan dari sungai tersebut melalui kegiatan penambangan batu kali.
Sungai Ciampea merupakan salah satu ekosistem yang memiliki berbagai bentuk komunitas. Salah satu komunitas tersebut adalah perifiton. Perifiton merupakan organisme yang tumbuh pada permukaan substrat di wilayah perairan. Perifiton berperan sebagai produsen primer dengan menghasilkan oksigen dan menjadi salah satu penghasil bahan organik yang ada di sungai. Keberadaan bahan organik tersebut dapat diduga dari produktivitas perifiton. Oleh karena itu, dilakukanlah penelitian ini yang bertujuan untuk mengetahui keberadaan dari bahan organik yang dihasilkan oleh perifiton yang didekati melalui produktivitas primer yang terjadi.
1.2. Pendekatan Masalah
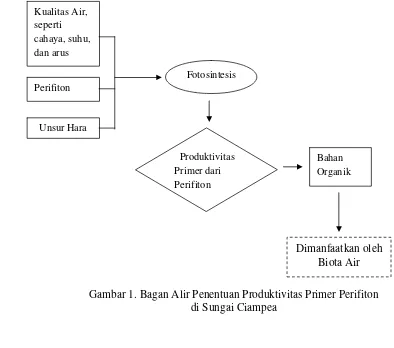
Keberadaan perifiton di perairan dipengaruhi oleh kualitas air dari perairan tersebut. Kualitas air akan berpengaruh terhadap produktivitas primer perifiton sehingga bahan organik yang dihasilkan oleh perifiton juga dapat berbeda. Pada ekosistem perairan mengalir, perifiton memiliki peran yang lebih besar dalam menentukan produktivitas primer dibandingkan dengan fitoplankton. Hal ini dapat terjadi karena perifiton hidup menempel pada substrat sehingga pengaruh kondisi lingkungan akan lebih nyata dibanding fitoplankton yang terbawa arus (Gambar 1).
2
fisiologis organisme. Menurut Whitton (1975) dalam Wijaya (2009), kecepatan arus yang besar (> 5 m/detik) dapat mengurangi jenis flora yang tinggal sehingga hanya jenis-jenis yang melekat saja yang tahan terhadap arus dan tidak mengalami kerusakan fisik
Pada penelitian ini, telah dikaji produktivitas primer perifiton pada musim kemarau tahun 2010 di Sungai Ciampea, Bogor. Perifiton yang diamati adalah perifiton yang tumbuh pada substrat buatan. Penumbuhan perifiton dilakukan pada kondisi perairan yang berbeda, yaitu pada perairan yang tidak terlindung oleh pohon, serta perairan yang terlindung oleh pohon.
Gambar 1. Bagan Alir Penentuan Produktivitas Primer Perifiton di Sungai Ciampea
Bahan Organik Perifiton
Kualitas Air, seperti cahaya, suhu, dan arus
Produktivitas Primer dari Perifiton
Dimanfaatkan oleh Biota Air
Unsur Hara
3
1.3. Tujuan dan Manfaat
2. TINJAUAN PUSTAKA
2.1. Ekosistem Sungai
Sungai adalah ekosistem perairan mengalir yang membawa berbagai kebutuhan hidup manusia dan makhluk lainnya. Salah satu contohnya adalah Sungai Ciampea yang terletak pada titik koordinat 6°32'59"LS dan 106°41'23"BT di desa Ciampea Udik, Kabupaten Ciampea, Bogor Barat. Pada umumnya, perbedaan antara perairan mengalir dengan perairan tergenang terkait dengan tiga kondisi yaitu (1) arus (2) pertukaran tanah-air, dan (3) oksigen (Odum 1993). Ada dua zona utama pada aliran air (sungai), yaitu:
• Zona air deras merupakan daerah yang dangkal dimana kecepatan arus cukup tinggi dan menyebabkan dasar sungai bersih dari endapan dan materi lain yang lepas, sehingga dasarnya padat. Zona ini dihuni oleh bentos yang beradaptasi khusus atau organisme perifitik yang dapat melekat atau berpegang dengan kuat pada dasar yang padat, dan ikan yang kuat berenang. Zona ini umumnya terdapat pada hulu sungai di daerah pegunungan.
• Zona air tenang merupakan bagian sungai yang dalam dimana kecepatan arus sudah berkurang, maka lumpur dan materi lepas cenderung mengendap di dasar, sehingga dasarnya lunak, tidak sesuai untuk bentos permukaan tetapi cocok untuk penggali, nekton dan plankton. Zona ini banyak dijumpai pada daerah landai.
Arus merupakan faktor pembatas utama pada aliran deras, tetapi dasar yang keras, terutama batu, dapat menyediakan permukaan yang cocok bagi organisme untuk menempel dan melekat. Menurut Odum (1993), beberapa bentuk adaptasi dari organisme komunitas air deras untuk mempertahankan posisi pada air yang mengalir adalah sebagai berikut.
• Melekat permanen pada substrat yang kokoh, seperti batu, kayu, atau daun.
• Mempunyai kaitan atau penghisap yang memungkinkan mereka untuk berpegang pada permukaan yang tampak halus.
5
2.2. Perifiton
Perifiton mencakup semua organisme tanaman, kecuali makrofita berakar, yang tumbuh pada material di bawah permukaan air. Material tersebut meliputi semua substrat, seperti sedimen, batu, puing-puing, dan organisme hidup. (Wetzel and Westlake 1974). Menurut Cooke (1956) in Weitzel (1979), perifiton merupakan kumpulan dari mikroorganisme yang tumbuh pada permukaan benda yang diletakkan dalam air. Young (1945) in Weitzel (1979) mendefinisikan perifiton sebagai kumpulan organisme yang tumbuh pada permukaan benda yang terdapat di bawah permukaan air dan menutupi mereka dengan lapisan tipis. Lapisan ini berwarna coklat atau hijau yang umumnya ditemukan melekat pada permukaan tanaman air, kayu, batu, atau benda lainnya dan dapat berkembang secara bertahap. Definisi trersebut menunjukkan bahwa perifiton dapat tumbuh pada substrat alami dan buatan. Odum (1971) dalam Weitzel (1979) memasukkan tumbuhan dan hewan yang melekat pada benda di bawah permukaan air sebagai definisi dari perifiton.
Dalam bahasa Jerman, istilah perifiton dikenal dengan nama ‘Aufwuchs’. Istilah ini pertama kali digunakan untuk mendeskripsikan organisme yang tumbuh di atas atau melekat pada substrat, tetapi tidak tumbuh ke dalam atau menembus substrat (Cooke 1956 and Young 1945 in Weitzel, 1979). Berdasarkan substrat penempelannya, perifiton dibedakan atas epilithic (perifiton yang tumbuh pada batu), epipelic (perifiton yang tumbuh pada permukaan sedimen), epiphytic (perifiton yang tumbuh pada batang dan daun tumbuhan), dan epizoic (perifiton yang tumbuh pada hewan) (Cole 1988). Selain itu, terdapat pula epipsammic (perifiton yang tumbuh pada permukaan pasir) dan epidendric (perifiton yang tumbuh pada kayu) (Weitzel 1979). Faktor-faktor yang umumnya dipertimbangkan sebagai pembatas, hal-hal yang diperlukan, serta penting untuk perkembangan perifiton, meliputi tipe perairan, ketersediaan cahaya, tipe substrat, perpindahan air, pH, alkalinitas, nutrien, bahan terlarut lainnya, suhu, salinitas, dan oksigen (Weitzel 1979).
6
2.3. Produktivitas Primer
Produktivitas sebagai pertumbuhan dan perkembangan maksimum dari organisme pada kondisi optimal (Thienemann 1931 in Wetzel 2001), dan produksi potensial organisme atau bahan organik per unit volume atau luas permukaan per unit waktu (Dussart 1966 in Wetzel 2001). Produktivitas primer didefinisikan sebagai tingkat pembentukan bahan organik dari karbon anorganik melalui fotosintesis yang menggambarkan konversi energi matahari menjadi energi kimia (Bott 1996). Tumbuhan air dan perifiton dianggap sebagai sumber penting dari oksigen dan produksi primer pada perairan mengalir (Weitzel 1979). Pada sungai berukuran kecil hingga sedang, biomassa bentos lebih besar daripada organisme kolom perairan dan metabolisme didominasi oleh hewan-hewan dasar perairan. Pada sungai besar dan waduk, produktivitas primer dan respirasi plankton lebih besar daripada bentos (Bott 1996). Perkiraan produkivitas dapat diketahui melalui pengukuran dari pertukaran oksigen, pH, karbon, dan konduktivitas selama periode tertentu (Wetzel 2001).
Teknik botol gelap-terang untuk memperkirakan produksi primer telah banyak digunakan. Pada metode oksigen, sampel fitoplankton diinkubasi pada botol terang dan gelap (tidak tembus cahaya) pada kedalaman yang diinginkan. Konsentasi awal oksigen terlarut diharapkan menjadi berkurang karena respirasi pada botol gelap dan bertambah pada botol terang, disebabkan oleh produksi fotosintesis dan konsumsi untuk respirasi. Jumlah dari aktivitas respirasi dengan aktivitas fotosintesis bersih sama dengan aktivitas fotosintesis kotor (Wetzel 2001).
7
1979). Produktivitas merupakan jumlah karbon yang terdapat di dalam material hidup dan secara umum dinyatakan sebagai jumlah gram karbon yang dihasilkan dalam satu meter kuadrat kolom air per hari (gC/m2/hari) atau jumlah gram karbon yang dihasilkan dalam satu meter kubik per hari (gC/m3/hari).
2.4. Parameter Fisika-Kimia Perairan 2.4.1. Suhu
Sumber terbesar dari panas pada perairan tawar adalah radiasi sinar matahari. Hal ini berlaku untuk danau, sungai besar, atau sungai kecil yang sebagian besar permukaan perairannya terkena sinar matahari langsung. Pada sungai kecil yang sangat teduh, pemindahan panas dari udara dan aliran dari air tanah lebih penting daripada radiasi sinar matahari dalam mengatur suhu. Fluktuasi pada suhu harian lebih dari 5oC merupakan hal yang biasa. Fluktuasi suhu tahunan pada sungai kecil sangat penting bagi organisme sungai tersebut. Reproduksi dan pertumbuhan dari organisme perairan mengalir diatur oleh suhu (Hauer and Hill 1996).
2.4.2. Kekeruhan
Kekeruhan merupakan gambaran sifat optik dari suatu perairan yang ditentukan dari jumlah cahaya yang dipancarkan dan diserap oleh partikel-partikel yang berada di dalam air (APHA 1995). Pada perairan, kekeruhan berasal dari bahan-bahan tersuspensi seperti lumpur, dan pasir. Kekeruhan yang tinggi dapat menghalangi cahaya matahari yang masuk ke dalam perairan sehingga dapat mengganggu proses fotosintesis organisme autotrof. Sungai-sungai di dataran tinggi dengan substrat batuan besar memiliki kekeruhan yang rendah sedangkan sungai-sungai di dataran rendah memiliki kekeruhan yang tinggi (Welch 1952).
2.4.3. Cahaya
8
Sungai sebagai salah satu lingkungan perairan, membutuhkan sinar matahari untuk proses fotosintesis oleh alga. Kisaran panjang gelombang antara 400-700 nm digunakan oleh autrotof seperti alga atau lumut untuk fotosintesis (Hauer and Hill 1996). Jumlah radiasi yang mencapai permukaan perairan dipengaruhi oleh awan, ketinggian dari permukaan laut, letak geografis, dan musim. Di sisi lain, penetrasi cahaya ke dalam air dipengaruhi oleh intensitas dan sudut datang cahaya, kondisi permukaan perairan, dan bahan-bahan yang terlarut dan tersuspensi di dalam air (Boyd 1988; Welch 1952 in Effendi 2003).
2.4.4. Arus
Arus dapat mempengaruhi pertumbuhan dan produksi perifiton. Pengaruh ini dapat menguntungkan atau merugikan, tergantung pada kekuatan dan arah pergerakan (arus). Arus secara terus menerus dapat memperbarui bahan yang dibutuhkan dan menghilangkan hasil sampingan proses metabolisme (Weitzel 1979). Douglas (1958) in Weitzel (1979) menemukan bahwa kepadatan perifiton pada jenis substrat berbeda, bervariasi sebagai fungsi dari mutu dan kecepatan air. Pada sungai dan perairan mengalir lainnya, oksigen dan biomassa yang dihasilkan dari tempat produksi banyak yang hilang karena adanya arus (Weitzel 1979). Menurut Welch (1980) in Muharram (2006), arus dibagi kedalam 5 kategori yaitu arus sangat cepat (> 1m/s), cepat (0,5-1 m/s), sedang (0,25-0,5 m/s), lambat (0,10-0,25 m/s), dan sangat lambat (< 0,10 m/s). Kecepatan arus dipengaruhi oleh ketinggian antara hulu dan hilir sungai. Jika perbedaan ketinggiannya cukup besar, maka arus akan semakin deras (Wijaya 2009).
2.4.5. Oksigen terlarut (Dissolved Oxigen)
9
2.5. Unsur Hara
Unsur hara dibutuhkan oleh perifiton untuk pertumbuhannya. Unsur hara tersebut meliputi nitrogen dalam bentuk nitrat, nitrit, dan amonia dan fosfor dalam bentuk ortofosfat.
2.5.1. Nitrogen
Nitrogen merupakan salah satu unsur penting dalam pembentukan protein dan pertumbuhan organisme (Wetzel 2001). Nitrogen di perairan terdapat dalam bentuk senyawa anorganik dan organik. Senyawa anorganik meliputi nitrit (NO2), nitrat (NO3), dan amonia (NH3) (Goldman and Horne 1983). Nitrat merupakan nutrien utama bagi pertumbuhan tanaman dan alga. Nitrat bersifat stabil dan mudah larut. Nitrat umumnya terdapat dalam jumlah yang banyak di perairan. Kisaran nitrat yang baik untuk pertumbuhan perifiton antara 0,01-5 mg/L (Parson and Takeshi 1987 in Nuraeni 1996). Batas toleransi perifiton terhadap kandungan amonia di perairan adalah < 0,200 mg/L (Pescod 1973).
2.5.2. Fosfor
3. METODE PENELITIAN
3.1. Rancangan Penelitian
Penelitian ini merupakan penelitian eksperimen di lapang dengan rancangan
percobaan acak lengkap. Objek yang digunakan pada penelitian ini adalah perifiton
yang melekat pada substrat buatan yang diletakkan pada daerah berarus dengan
pemaparan sinar matahari yang berbeda. Kegiatan ini dilakukan untuk mendapatkan
informasi mengenai bahan organik yang dihasilkan oleh perifiton melalui
pendekatan oksigen dan klorofil.
3.2. Waktu dan Lokasi Penelitian
Penelitian dilaksanakan pada bulan April-Agustus 2010. Penelitian ini terdiri
dari dua tahap, yaitu penelitian di lapang meliputi pengukuran suhu, cahaya, oksigen
terlarut, dan kecepatan arus serta analisis di laboratorium meliputi kelimpahan
perifiton, pengukuran klorofil-a, dan unsur hara (nitrit, nitrat, amonia, dan
ortofosfat). Penelitian di lapang dilaksanakan di Sungai Ciampea, Desa Ciampea
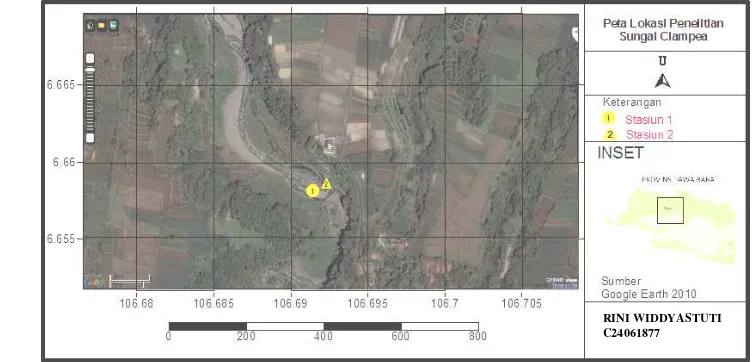
Udik, Kabupaten Ciampea, Bogor Barat, Jawa Barat (Gambar 2). Analisis di
laboratorium dilakukan pada Laboratorium Biologi Mikro 1 dan Laboratorium
Fisika dan Kimia Lingkungan, Bagian Produktivitas dan Lingkungan Perairan,
Departemen Manajemen Sumberdaya Perairan, Fakultas Perikanan dan Ilmu
Kelautan, Institut Pertanian Bogor.
Gambar 2. Peta Lokasi Penelitian
11
3.3. Pelaksanaan Penelitian 3.3.1. Penentuan stasiun
Stasiun pengamatan terdiri dari dua stasiun, yaitu tempat yang terkena sinar
matahari langsung (stasiun 1) dan tempat yang tidak terkena sinar matahari langsung
(stasiun 2) (Tabel 1). Salah satu faktor yang mempengaruhi pertumbuhan dan
fotosintesis pada perifiton adalah sinar matahari. Oleh karena itu, penentuan stasiun
berdasarkan perbedaan pemaparan sinar matahari dilakukan untuk mengetahui ada
tidaknya perbedaan bahan organik yang dihasilkan oleh perifiton pada kedua stasiun,
Kedua stasiun tersebut memiliki kondisi lingkungan yang hampir sama, seperti
kecepatan arus, kedalaman rata-rata sungai, lebar sungai, dan lebar badan sungai.
Tabel 1. Penentuan stasiun pengamatan perifiton di sungai
Stasiun Lintang Selatan Bujur Timur Keterangan
1 06o39'44,6" LS 106o41'39,2" BT Kondisi : Terkena Sinar Matahari Langsung
2 06o39'43,8" LS 106o41'39,4" BT Kondisi : Tidak Terkena Sinar Matahari Langsung
3.3.2. Penelitian pendahuluan
Penelitian pendahuluan dilakukan untuk menentukan substrat buatan sebagai
media tumbuh perifiton. Komposisi perifiton pada substrat tersebut diharapkan
mendekati komposisi perifiton pada substrat di alam (batu). Substrat buatan yang
digunakan pada percobaan pendahuluan meliputi kaca, fiber glass, tali rafia, dan
paralon. Substrat buatan tersebut diletakkan tegak lurus dengan arus sungai pada
daerah yang terkena sinar matahari langsung dan daerah yang tidak terkena sinar
matahari langsung. Pengamatan terhadap komposisi perifiton pada substrat tersebut
dilakukan setelah lebih kurang 2 minggu dari waktu peletakkan. Setelah dilakukan
pengamatan, diperoleh hasil bahwa jenis dan kelimpahan pada tali rafia mendekati
dengan yang ada di batu sehingga tali rafia dijadikan sebagai substrat buatan untuk
media tumbuh perifiton.
3.3.3. Penelitian utama
Pada substrat buatan yang telah terpilih (tali rafia), kemudian dilakukan
pengamatan. Pengamatan dilakukan sebanyak tiga kali, yaitu hari ke-7, ke-12, dan
12
meliputi kecepatan arus, cahaya, dan suhu sedangkan pengukuran terhadap unsur
hara, dan kelimpahan perifiton dilakukan di laboratorium. Nilai produktivitas
primer diukur melalui dua pendekatan, yaitu pendekatan oksigen dan pendekatan
klorofil. Pengukuran mengggunakan pendekatan oksigen lebih cepat dan mudah
dilakukan serta biaya yang dikeluarkan lebih murah bila dibandingkan dengan
pendekatan klorofil.
Pada pengukuran dengan menggunakan pendekatan oksigen, botol BOD yang
digunakan sebanyak 3 buah untuk setiap stasiun. Satu botol terang, satu botol gelap,
dan satu botol inisial. Substrat buatan yang berukuran 5x1 cm2 dimasukkan ke
dalam botol BOD yang telah berisi air sungai yang sebelumnya telah disaring
dengan plankton net untuk mengurangi fitoplankton dan zooplankton. Botol BOD
terang dan gelap yang telah berisi substrat buatan kemudian diletakkan di dalam air
sungai untuk diinkubasi selama empat jam sedangkan botol inisial langsung diukur
kandungan oksigen terlarutnya dengan menggunakan metode modifikasi Winkler.
Pada pengukuran dengan pendekatan klorofil, substrat buatan yang berukuran
5x1 cm2 dikerik pada salah satu sisinya dan hasil kerikan tersebut dimasukkan ke
dalam botol sampel berukuran 250 ml yang berisi air akuades sebanyak 100 ml.
Setelah itu, diberikan larutan MgCO3 sebanyak 2 tetes. Selanjutnya, pengukuran
untuk mengetahui kandungan klorofil dari perifiton tersebut dilakukan di
laboratorium.
Hasil yang didapat dari pengukuran dengan menggunakan kedua pendekatan
tersebut kemudian dikonversi ke dalam bentuk karbon. Konversi ini dilakukan
untuk mengetahui besarnya bahan organik yang dihasilkan oleh perifiton.
3.3.4. Pengumpulan data 3.3.4.1. Perifiton
Pengambilan contoh perifiton dilakukan dengan mengerik permukaan substrat
dengan menggunakan kuas. Hasil kerikan dimasukkan ke dalam botol sampel yang
telah berisi aquades. Hasil kerikan untuk pengamatan komposisi perifiton diawetkan
13
a. Kelimpahan perifiton
Sampel perifiton dianalisis untuk mendapatkan data jenis dan kelimpahan
perifiton. Kelimpahan perifiton dihitung dengan menggunakan rumus APHA (1995)
sebagai berikut.
Keterangan :
K = Kelimpahan perifiton (ind/cm2) N = Jumlah perifiton yang diamati
As = Luas substrat yang dikerik untuk perhitungan perifiton At = Luas penampang permukaan cover glass (mm2) Ac = Luas amatan (mm2)
Vt = Volume botol sampel (30 ml) Vs = Volume sampel/1 tetes (ml)
b. Indeks keanekaragaman, indeks keseragaman, dan indeks dominansi
Indeks keanekaragaman menunjukkan keseimbangan dalam pembagian jumlah
individu tiap jenis dan menggambarkan kekayaan jenis dalam suatu komunitas.
Rumus yang digunakan untuk menghitung indeks keanekaragaman adalah rumus
Shannon dan Wiener (Brower dan Zar, 1990) :
Keterangan :
H’ = Indeks Keanekaragaman pi = ni/N
ni = Jumlah individu jenis ke-i N = Jumlah total individu
Indeks keseragaman digunakan untuk mengetahui tingkat penyebaran jumlah
individu pada tiap jenis organism. Rumus yang digunakan yaitu rumus Indeks
Keseragaman (Brower dan Zar, 1990) :
Keterangan :
E = Indeks keseragaman H’ = Indeks keanekaragaman Hmaks = ln S
14
Indeks dominansi digunakan untuk mengetahui ada tidaknya organisme
tertentu yang mendominasi pada suatu komunitas. Untuk mengetahui nilai
dominansi digunakan rumus Indeks Dominansi Simpson (Odum, 1993) :
Keterangan :
C = Indeks Dominansi Simpson pi = ni/N
ni = Jumlah individu jenis ke-i N = Jumlah total individu
3.3.4.2. Kualitas air
Kualitas air yang diukur meliputi suhu, cahaya, kecepatan arus, dan unsur
hara (nitrat, nitrit, amonia, dan ortofosfat) (Tabel 2). Alat yang digunakan untuk
mengukur kualitas air tersebut antara lain termometer untuk mengukur suhu dan
luxmeter untuk mengukur cahaya. Kecepatan arus diukur dengan menggunakan
transek kuadrat. Transek tersebut diletakkan pada permukaan perairan yang di
dalamnya terdapat bola pingpong yang diikat dengan tali serta dibiarkan terbawa
arus. Pengukuran unsur hara (nitrat, nitrit, amonia, dan ortofosfat) dilakukan di
laboratorium.
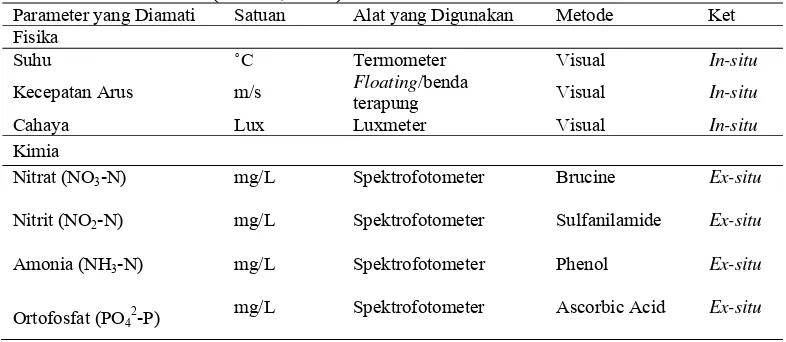
Tabel 2. Parameter, alat, dan metode yang digunakan dalam pengambilan data kualitas air (APHA, 1995)
Parameter yang Diamati Satuan Alat yang Digunakan Metode Ket
Fisika
Suhu ˚C Termometer Visual In-situ
Kecepatan Arus m/s Floating/benda
terapung Visual In-situ
Cahaya Lux Luxmeter Visual In-situ
Kimia
Nitrat (NO3-N) mg/L Spektrofotometer Brucine Ex-situ
Nitrit (NO2-N) mg/L Spektrofotometer Sulfanilamide Ex-situ
Amonia (NH3-N) mg/L Spektrofotometer Phenol Ex-situ
Ortofosfat (PO42-P)
15
3.3.4.3. Produktivitas primer a. Pendekatan oksigen
Setelah diperoleh kadar oksigen pada botol inisial, botol terang, dan botol
gelap, selanjutnya dianalisis nilai produksi primer bersih dari perifiton. Produksi
primer bersih atau Net Primary Production (NPP) merupakan kelebihan bahan
organik yang disimpan dalam jaringan setelah dikurangi dengan jumlah yang
terpakai untuk respirasi. Rumus yang digunakan untuk menghitung produksi primer
bersih adalah
Keterangan :
NPP = Produksi primer bersih atau Net Primary Production I = Kadar oksigen pada botol inisial (mgO2/L/waktu inkubasi) L = Kadar oksigen pada botol terang (mgO2/L/ waktu inkubasi)
b. Pendekatan klorofil
Pengukuran klorofil pada perifiton digunakan untuk mengetahui biomassa
yang terkandung di dalamnya. Kadar klorofil yang telah diekstrak dapat dihitung
dengan rumus APHA (1995) :
Keterangan :
Ca = Klorofil-a (mg/L)
A664 = Absorbance pada panjang gelombang 664 nm A647 = Absorbance pada panjang gelombang 647 nm A664 = Absorbance pada panjang gelombang 630 nm V = Volume aseton (ml)
L = Panjang garis sinar pada spektro (1) S = Volume air contoh (ml)
3.3.4.4. Kandungan bahan organik
Kandungan bahan organik dari perifiton dapat dihitung dengan
mengkonversikan nilai produksi primer bersih dan klorofil-a yang telah diperoleh ke
16
a. Pendekatan oksigen
gC/m2/hari
Keterangan :
NPP = Produksi primer bersih atau Net Primary Production (mgC/L/ waktu inkubasi)
C = Kandungan bahan organik (gC/m2/hari)
I = Kadar oksigen pada botol inisial (mgO2/L/ waktu inkubasi) L = Kadar oksigen pada botol terang (mgO2/L/ waktu inkubasi)
PQ = 1,2 (dengan asumsi hasil metabolisme sebagian besar disebabkan oleh fitoplankton/perifiton (Strickland dan Parson 1965))
Vb = Volume botol BOD yang dipakai (L) BM Chl-a = Berat molekul klorofil-a
Chl-a = Nilai klorofil-a yang diperoleh (mg/L) Vs = Volume air akuades (L)
Ls = Luas permukaan tali rafia yang dikerik (m2)
3.3.5. Analisis data
Penelitian ini menggunakan Rancangan Acak Lengkap (RAL) dan regresi.
Pada analisis dengan menggunakan Rancangan Acak Lengkap (RAL), perlakuan
pertama merupakan daerah yang terkena sinar matahari langsung dan perlakuan
kedua merupakan daerah yang tidak terkena sinar matahari langsung. Ulangan yang
dilakukan sebanyak tiga kali. Data penelitian dianalisis dengan ANOVA RAL.
Rancangan Acak Lengkap dilakukan untuk mengetahui pengaruh dari kedua
17
dengan kelimpahan dan cahaya dengan bahan organik yang dihasilkan oleh
perifiton.
Hipotesis yang digunakan :
H0 : τ1 = τ2 = . . . = τt = 0 atau tidak ada pengaruh perlakuan terhadap respon yang
diamati
H1 : minimal ada satu τi ≠ 0, untuk i = 1, 2, … ,t atau paling sedikit ada sepasang τi
yang tidak sama
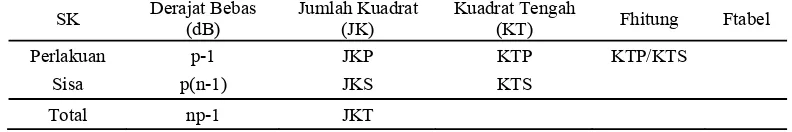
Tabel 3. Tabel Sidik Ragam (TSR)
4. HASIL DAN PEMBAHASAN
4.1. Hasil
Hasil yang diperoleh selama pengamatan meliputi kelimpahan perifiton, kondisi komunitas perifiton, kondisi fisika dan kimia perairan, serta bahan organik yang dihasilkan oleh perifiton. Hasil pengamatan dan pengukuran disajikan dalam bentuk tabel dan grafik.
4.1.1. Kelimpahan perifiton
Perifiton yang terdapat pada substrat buatan selama pengamatan terdiri dari empat genus, yaitu Thallasiotrhix, Melosira, Stauroneis, dan Navicula. Kelimpahan perifiton pada stasiun 1 dan 2 mencapai nilai tertinggi pada hari ke-12, yaitu 2640 ind/cm2 dan 2040 ind/cm2 (Gambar 3 dan Lampiran 3).
Gambar 3. Kelimpahan perifiton pada stasiun 1 dan stasiun 2; stasiun 1, dan stasiun 2.
4.1.2. Kondisi komunitas perifiton
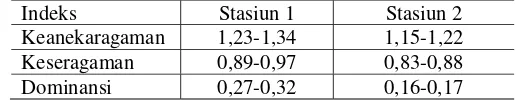
Kondisi komunitas perifiton dapat digambarkan dengan nilai indeks keanekaragaman, keseragaman, dan dominansi (Tabel 5). Nilai indeks keanekaragaman dan dominansi dari kedua stasiun tergolong rendah, sedangkan indeks keseragaman pada kedua stasiun tergolong tinggi.
Tabel 5. Nilai Indeks keanekaragaman, keseragaman, dan dominansi perifiton pada stasiun 1 dan stasiun 2
Indeks Stasiun 1 Stasiun 2 Keanekaragaman 1,23-1,34 1,15-1,22
19
4.1.3. Kondisi fisika dan kimia perairan
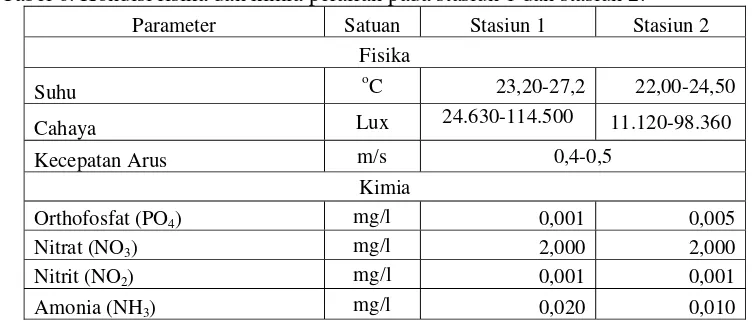
Kondisi fisika dan kimia perairan pada kedua stasiun yang diukur selama pengamatan meliputi suhu, cahaya, dan unsur hara (Tabel 6). Unsur hara yang diukur adalah ortofosfat, nitrat, nitrit, dan amonia.
Tabel 6. Kondisi fisika dan kimia perairan pada stasiun 1 dan stasiun 2.
Parameter Satuan Stasiun 1 Stasiun 2 Fisika
Suhu oC 23,20-27,2 22,00-24,50 Cahaya Lux 24.630-114.500 11.120-98.360
Kecepatan Arus m/s 0,4-0,5
Kimia
Orthofosfat (PO4) mg/l 0,001 0,005
Nitrat (NO3) mg/l 2,000 2,000
Nitrit (NO2) mg/l 0,001 0,001
Amonia (NH3) mg/l 0,020 0,010
4.1.4. Bahan organik yang dihasilkan oleh perifiton 4.1.4.1. Pendekatan oksigen
Jumlah bahan organik yang dihasilkan pada stasiun 1 dan 2 yang diukur dengan pendekatan oksigen memiliki nilai tertinggi pada hari ke-12. Nilai tersebut berturut-turut adalah 2,44 gC/m2/hari dan 2,26 gC/m2/hari (Gambar 4 dan Lampiran 4).
Gambar 4. Bahan organik yang dihasilkan oleh perifiton (gC/m2/hari) melalui pendekatan oksigen pada stasiun 1 dan stasiun 2;
20
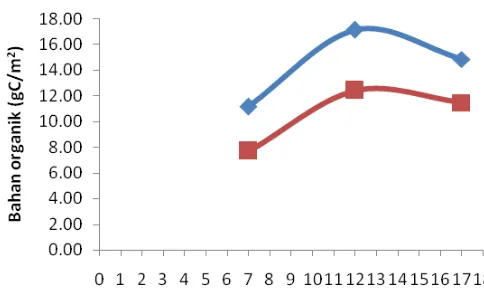
4.1.4.2. Pendekatan klorofil
Pada kedua stasiun, kandungan bahan organik tertinggi terdapat pada hari ke-12. Bahan organik tersebut bernilai 17,14 gC/m2 untuk stasiun1 dan 12,40 gC/m2 untuk stasiun 2 (Gambar 5 dan Lampiran 4).
Gambar 5. Bahan organik yang dihasilkan oleh perifiton (gC/m2) melalui pendekatan klorofil pada stasiun 1 dan stasiun 2;
stasiun 1, dan stasiun 2.
4.1.5. Analisis statistik
4.1.5.1. Rancangan Acak Lengkap
Data yang dianalisis dengan menggunakan ANOVA RAL meliputi data bahan organik yang dihasilkan oleh perifiton pada stasiun 1 dan stasiun 2 (Tabel 7 dan Lampiran 5). Pendekatan yang digunakan pada kedua stasiun meliputi pendekatan oksigen maupun klorofil. Bila nilai P <0,05 maka tidak ada perbedaan yang signifikan pada kedua perlakuan, serta sebaliknya.
Tabel 7. Hasil analisis statistik menggunakan ANOVA RAL Pendekatan yang Digunakan Nilai P Pendekatan Oksigen 0,8007 Pendekatan Klorofil 0,1623
4.1.5.2. Regresi
21
Gambar 6. Hubungan antara cahaya (Lux) dengan kelimpahan perifiton (ind/cm2). Hasil regresi antara cahaya dengan bahan organik yang dihasilkan oleh perifiton melalui pendekatan oksigen memperoleh nilai koefisien determinasi dan koefisien korelasi sebesar 0,361 dan 0,601 (Gambar 7). Nilai ini menunjukkan hubungan yang erat antara cahaya dengan bahan organik yang dihasilkan melalui pendekatan oksigen.
Gambar 7. Hubungan antara cahaya (Lux) dengan bahan organik yang dihasilkan oleh perifiton (gC/m2/hari) melalui pendekatan oksigen.
22
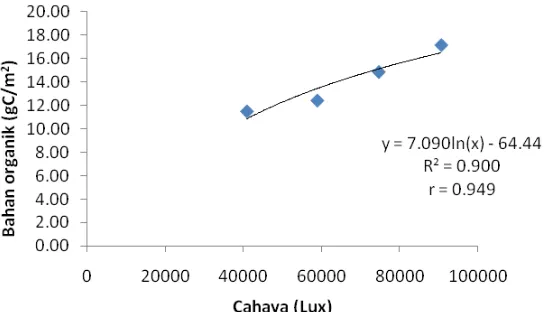
Gambar 8. Hubungan antara cahaya (Lux) dengan bahan organik yang dihasilkan oleh perifiton (gC/m2) melalui pendekatan klorofil.
4.2. Pembahasan
Selama pengamatan, perifiton yang ditemukan berasal dari satu kelas, yaitu Bacillariophyceae yang terdiri dari empat genus, yaitu Thallasiotrhix, Melosira, Stauroneis, dan Navicula. Perifiton sudah ditemukan mulai dari hari ke-7 hingga hari ke-17. Perifiton mengalami kenaikan pertumbuhan sejak hari ke-7 hingga hari ke-12. Setelah itu pertumbuhan menurun hingga hari ke-17. Hal ini menunjukkan bahwa perifiton pada substrat buatan tersebut telah mengalami kestabilan. Menurut Uehlinnger (2000), kelimpahan perifiton yang berfluktasi secara tidak teratur pada skala hari dan minggu terlihat bersatu di titik keseimbangan dalam skala waktu yang lebih lama. Pertumbuhan organisme tersebut antara lain dipengaruhi oleh cahaya matahari, unsur hara, dan suhu.
Cahaya pada stasiun 1 berkisar antara 24.630-114.500 Lux dan 11.120-98.360 Lux pada stasiun 2. Cahaya merupakan salah satu faktor yang mempengaruhi pertumbuhan perifiton (Weitzel, 1979). Hal ini dapat terlihat dari kelimpahan perifiton pada stasiun 1 di setiap pengamatan yang lebih besar daripada stasiun 2. Hal ini terjadi karena stasiun 1 terkena sinar matahari langsung sehingga cahaya yang masuk ke stasiun 1 lebih besar dan cocok daripada yang masuk ke stasiun 2.
23
berturut-turut adalah 0,005 mg/L dan 0,01 mg/L. Kondisi unsur hara pada kedua stasiun didasarkan pada nilai N dan P yang tersedia pada kedua stasiun. Berdasarkan kadar ortofosfat, kedua stasiun termasuk perairan oligotrofik (Vollenweinder 1969 in Wetzel 1975). Nitrat yang terdapat pada kedua stasiun baik untuk pertumbuhan perifiton (Parson dan Takeshi 1987 in Nuraeni 1996), dan kadar amonia yang terdapat di kedua stasiun masih bisa ditoleransi oleh perifiton (Pescod 1973). Unsur hara pada perairan tersebut masih mencukupi bagi pertumbuhan perifiton.
Selama pengamatan, suhu perairan pada stasiun 1 berkisar antara 23,20-27,2 oC, sedangkan pada stasiun 2 berkisar antara 22,00-24,50 oC. Berdasarkan data tersebut, dapat terlihat bahwa stasiun 1 memiliki rentang suhu lebih luas dan lebih tinggi dibandingkan dengan stasiun 2. Hal ini diduga karena stasiun 1 merupakan tempat yang terkena sinar matahari langsung sedangkan stasiun 2 tidak terkena sinar matahari langsung. Cahaya matahari yang masuk ke stasiun 1 lebih besar daripada stasiun 2 sehingga menjadikan suhu pada stasiun 1 lebih tinggi dibandingkan dengan stasiun 2.
Kecepatan arus selama pengamatan berkisar antara 0,4-0,5 m/s. Hal ini menunjukkan bahwa arus pada daerah tersebut tergolong sedang sampai cepat (Welch 1980 in Muharram 2006). Hal ini diduga karena adanya perbedaan ketinggian di sekitar kedua stasiun yang cukup besar. Selain itu, pergantian unsur hara akan berlangsung lebih cepat pada perairan dengan arus sedang hingga cepat. Hal ini mengakibatkan unsur hara pada perairan tersebut lebih berflukuasi. Organisme yang mampu hidup pada perairan tersebut merupakan organisme yang melekat dan tahan terhadap arus. Substrat dasar perairan berupa batuan.
24
dari nilai indeks dominansi, kedua stasiun memiliki nilai indeks dominansi rendah yang menggambarkan bahwa tidak ada genus yang mendominansi dalam komunitas tersebut. Hal ini menunjukkan bahwa komunitas tersebut berada dalam keadaan stabil.
Bahan organik pada kedua stasiun yang diukur baik dengan pendekatan oksigen maupun pedekatan klorofil mencapai nilai tertinggi pada hari ke-12. Hal ini diduga terjadi karena perifiton sebagai penghasil bahan organik di kedua stasiun memiliki kelimpahan tertinggi pada hari ke-12. Menurut Kevern et.al (1966), tingkat pertumbuhan dalam waktu singkat pada perifiton dapat dijadikan sebagai perkiraan dari produktivitas perifiton. Selain itu, menurut Larned and Santos (2000), klorofil pada daerah yang terang memiliki nilai yang lebih besar daripada daerah yang teduh. Hal ini mengakibatkan bahan organik yang dihasilkan pada daerah yang terang lebih besar daripada daerah yang teduh. Berdasarkan hasil yang diperoleh dari pengukuran, stasiun 1 menghasilkan bahan organik yang lebih besar dibandingkan dengan stasiun 2 pada setiap waktu pengamatan. Hal ini dapat terjadi karena ketersediaan cahaya matahari pada stasiun 1 lebih besar daripada stasiun 2. Cahaya matahari diperlukan bagi produktivitas dan pertumbuhan perifiton. Dengan produktivitas dan kelimpahan perifiton yang lebih besar, maka stasiun 1 dapat menghasilkan bahan organik yang lebih besar pula.
Berdasarkan hasil analisis menggunakan ANOVA RAL pada kedua pendekatan, nilai P yang diperoleh lebih besar dari 0,05. Hal ini menunjukkan bahwa tidak ada perbedaan yang signifikan terhadap bahan organik yang dihasilkan antara perlakuan pada stasiun 1 (terkena sinar matahari lansung) dengan stasiun 2 (tidak terkena sinar matahari langsung).
25
dengan bahan organik yang dihasilkan oleh perifiton menggunakan pendekatan klorofil memiliki nilai koefisien korelasi dan determinasi yang tinggi. Hal ini juga menunjukkan bahwa cahaya memiliki hubungan yang erat terhadap bahan organik yang dihasilkan oleh perifiton melalui pendekatan klorofil. Pada regresi antara cahaya dengan bahan organik yang dihasilkan oleh perifiton melalui pendekatan oksigen, koefisien korelasi dan koefisien determinasi yang diperoleh tidak terlalu tinggi. Hal ini menunjukkan adanya hubungan yang tidak erat antara cahaya dengan bahan organik yang dihasilkan oleh perifiton melalui pendekatan oksigen.
Bahan organik yang dihasilkan oleh perifiton dapat dimanfaatkan sebagai pakan alami oleh organisme lainnya, di antaranya adalah bentos. Beberapa kelompok bentos yang memanfaatkan perifiton adalah gastropoda dan larva insekta. Larva insekta tersebut berasal dari Ordo Ephemeroptera (famili Heptageniidae, Baetidae, Ephemerellidae, Caenidae, Leptophlebiidae), Tricoptera (famili Glossosomatidae, Helicopsychidae, Molannidae, Odontoceridae, Goreridae, Leptoceridae), Lepidoptera, Coleoptera (famili Elmidae, Psephenidae), Diptera (famili Chironomidae, Tabanidae, Simuliidae), dan Hemiptera (famili Corixidae) (Wetzel 2001).
Gambaran mengenai potensi pemanfaatan perifiton sebagai pakan alami akan dijelaskan dengan penjabaran sebagai berikut. Akan tetapi, panjabaran tersebut menggunakan data bentos pada hulu Sungai Cisadane disebabkan belum adanya data bentos pada hulu Sungai Ciampea dengan pertimbangan bahwa karakteristik hulu Sungai Cisadane hampir serupa dengan hulu Sungai Ciampea.
Pada bagian hulu Sungai Cisadane tersebut terdapat lima famili bentos, yaitu Elmidae, Simuliidae, Tabanidae, Baetidae, Heptageniidae, dan Pyralidae, dengan kepadatan total 449 individu/m2 (Andriana 2008). Kelima famili tersebut tergolong sebagai bentos yang memanfaatkan perifiton sebagai pakan alami (Otemin 2002).
26
pertumbuhan perifiton, serta dengan tingkat pemanfaatan perifiton sebesar 10% dari bobot bentos (0,00055 gram). Jumlah bahan organik yang dihasilkan oleh perifiton masih mencukupi untuk dimanfaatkan oleh bentos pemakan perifiton di Sungai Cisadane. Uraian tersebut dapat dijadikan sebagai gambaran bagi potensi sediaan bahan organik oleh perifiton yang dapat dimanfaatkan oleh bentos di Sungai Ciampea.
5. KESIMPULAN
5.1. Kesimpulan
Bahan organik yang dihasilkan oleh perifiton pada substrat buatan (tali rafia) di perairan mengalir melalui pendekatan oksigen berkisar antara 0,79-2,44 gC/m2/hari pada stasiun tanpa naungan dan 0,44-2,26 gC/m2/hari pada stasiun dengan naungan. Pada pendekatan klorofil, bahan organik yang dihasilkan berkisar antara 11,17-17,14 gC/m2 pada stasiun tanpa naungan dan 7,71-12,40 gC/m2 pada stasiun dengan naungan.
DAFTAR PUSTAKA
Andriana W. 2008. Keterkaitan Struktur Komunitas Makrozoobentos sebagai Indikator Keberadaan Bahan Organik di Perairan Hulu Sungai Cisadane Bogor, Jawa Barat [Skripsi]. Fakultas Perikanan dan Ilmu Kelautan, Institut Pertanian Bogor. Bogor.
[APHA] American Public Health Association. 1995. Standard Methods for the Examination of Water and Wastewater. 19th Edition. American Public Health Association, Washington, American Water Works Association, Water Enviroment Federation. United Book Press, Inc. Maryland. The United State of America.
Bott T L. 1996. Primary Productiviy and Community Respiration. Hauer F R dan Lamberti G A [editor], Stream Ecology. Academic Press. San Diego.
Brower J E and Zar J H. 1990. Field and Laboratory Methods for General Ecology. 3rd Edition. Wm. C. Brown Publisher. Dubuque, Iowa.
Cole G A. 1988. Textbook of Limnology. 3rd Edition. Waveland Press Inc. USA. Effendi H. 2003. Telaah Kualitas Air. Kanisius. Yogyakarta.
Goldman G R and A J Horne. 1983. Limnology. McGraw-Hill International Book Company. Tokyo.
Hauer F R and Hill W R. 1996. Temperature, Light, and Oxigen. Hauer F R dan Lamberti G A [editor], Stream Ecology. Academic Press. San Diego.
Kevern N R, Wilhm J L, and Van Dyne G M. 1966. Use of Artificial Substrata to Estimate the Productivity of Periphyton. Limnol. 11(4): 499-502.
Larned S T and Santos S R. 2000. Light-and Nutrient-Limited Periphyton in Lower Order Stream of Oahu, Hawaii. Hydrobiologia. 432: 101-111.
Muharram N. 2006. Struktur Komunitas perifiton dan Fitoplankton di Bagian Hulu Sungai Ciliwung, Jawa Barat [Skripsi]. Fakultas Perikanan dan Ilmu Kelautan, Institut Pertanian Bogor. Bogor.
Nuraeni H. 1996. Struktur Komunitas Perifiton pada Ekosistem Padang Lamun di Perairan Pesisir Pulau Kapoposang, Sulawesi Selatan [Skripsi]. Fakultas Perikanan dan Ilmu Kelautan, Institut Pertanian Bogor. Bogor.
29
29 Otermin A, Basaguren A, and Pozo J. 2002. Re-colonization by the
Macroinvertebrate Community after a Drought Period in a First-Order Stream (Agüera Basin, Northern Spain). Limnetica. 21(1-2):117-128.
Pescod M B. 1973. Investigation of Rational Effluent and Stream Standard for Tropical Countries. AIT. Bangkok.
Strickland J D H and Parsons T R. 1965. A Manual of Sea Water Analysis. Fisheries Research of Canada. Ottawa.
Uehlinger U. 2000. Periphyton Biomass in Unpredictable in an Environtment : Exploring the Temporal Variability with a Dynamic Model. Limnol. 27 :3162-3165.
Weitzel R L. 1979. Methods and Measurements of Periphyton Communities : A Review. American Society for testing and Materials. Baltimore.
Welch P S. 1952. Limnologi. 2nd Edition. McGraw-Hill Book Company, Inc. New York.
Wetzel R G. 1975. Limnology. W B Saunders Co Philadelphia. Pennsylvania.
Wetzel R G. 2001. Limnology : Lake and River Ecosystems. 3rd Edition. Academic Press. San Diego.
Wetzel R G and Westlake D F. 1974. Periphyton. Vollenweider R A, Talling J F, Westlake D F [editor], A Manual on Methods Primary Production in Aquatic Environtments. Burgess and Son (Abingdon) Limited. Great Britain.
31
31 Lampiran 1. Prosedur analisis parameter yang diamati (APHA, 1995)
Nitrat (Metode Brucine)
1. Air sampel disaring dengan menggunakan kertas saring.
2. Air sampel yang telah disaring kemudian diambil sebanyak 5 ml dan dimasukkan ke dalam tabung reaksi.
3. Kemudian ditambahkan 0,5 ml Brucine, lalu diaduk.
4. Ditambahkan 5 ml H2SO4 pekat (gunakan ruang asam), kemudian diaduk dengan menggunakan vibrofix. Setelah itu, dipanaskan pada hot plate selama 30 menit. Kemudian didiamkan hingga dingin.
5. Untuk pengukuran blanko, 5 ml aquades dimasukkan ke dalam tabung reaksi, kemudian dilakukan prosedur seperti di atas.
6. Absorban diukur dengan spektrofotometer pada panjang gelombang 410 nm.
Nitrit (Metode Sulfanilamide)
1. Air sampel disaring dengan menggunakan kertas saring berukuran 0,45 µm. 2. Jika pH tidak berada antara 5 sampai 9, ditambahkan HCL 1N atau NH4OH
sampai pada kisaran tertentu.
3. 10 ml air contoh yang telah disaring, ditambahkan color reagen sebanyak 0,4 ml, kemudian diaduk dan didiamkan selama 10 menit.
4. Ukur absorban dengan spektrofotometer pada panjang gelombang 543 nm.
Amonia (Metode Phenol)
1. 25 ml air sampel yang telah disaring kemudian dimasukkan ke dalam Erlenmeyer 125 ml.
2. Ditambahkan 1 ml Phenol solution, kemudian diaduk.
3 Ditambahkan 1 ml larutan Soddium Nitroposside, kemudian diaduk. 4. Kemudian ditutup dengan alumunium foil dan didiamkan selama 1 jam. 5. Absorban diukur dengan spektrofotometer pada panjang gelombang 640 nm.
Ortofosfat (Metode Ascorbic Acid)
1. Air sampel disaring dengan milliopore 0,45 µm dengan vacuum pump.
2. Air sampel yang telah disaring kemudian diambil sebanyak 25 ml dan dimasukkan ke dalam Erlenmeyer berukuran 125 ml.
3. Kemudian ditambahkan 0,05 ml (1 tetes) indikator Phenolphthalein. Jika berubah warna merah muda, ditambahkan kembali dengan larutan H2SO4 1 N 4. Ditambahkan 4 ml mix reagen, kemudian diaduk, lalu didiamkan selama 10
menit.
5. Absorban diukur pada panjang gelombang 880 nm.
Oksigen (Metode Modifikasi Winkler)
1. Botol BOD berukuran 300 ml disiapkan sebanyak 3 buah pada tiap stasiun. Satu untuk botol terang, satu untuk botol gelap, dan satu untuk botol inisisal. Botol gelap dilapisi dengan plastik hitam sehingga cahaya tidak masuk ke dalam botol. 2. Air sungai disaring dengan menggunakan plankton net dan hasil saringannya
32
32 3. Botol terang dan gelap dibenamkan dalam air sungai untuk diinkubasi selama 4
jam. Sedangkan botol inisial langsung diukur oksigen terlarutnya dengan metode modifikasi Winkler.
4. Setelah 4 jam, botol terang dan botol gelap diangkat kemudian diukur oksigen terlarutnya dengan metode modifikasi Winkler.
Klorofil-a (Metode Ekstrak Aseton)
1. Akuades sebanyak 100 ml dimasukkan ke dalam botol sampel berukuran 250 ml. 2. Perifiton pada substrat buatan dengan luasan 5x1 cm2 dikerik, kemudian hasil
kerikan dimasukkan ke dalam botol sampel tersebut. 3. Ditambahkan MgCO3 sebanyak 2 tetes.
4. Air sampel disaring dengan kertas membrane filter menggunakan vacuum pump. 5. Kertas saring dibungkus dengan alumunium foil, kemudian diletakkan di dalam
freezer.
6. Kertas saring dari dalam freezer diambil kemudian dimasukkan ke dalam tabung reaksi yang ditutup alumunium foil.
7. Aseton 90% dimasukkan ke dalam tabung reaksi tersebut dan dibiarkan hingga kertas saring menjadi larut.
8. Disimpan kembali ke dalam lemari es selama 15 menit.
33
33 Lampiran 2. Contoh organisme yang ditemukan selama pengamatan
Melosira sp. Stauroneis sp.
34
34 Lampiran 3. Kelimpahan perifiton pada stasiun 1 dan stasiun 2 selama pengamatan
Stasiun Organisme
Kelimpahan Perifiton (ind/cm2)
pada Pengamatan Ke-
1 2 3
Bacillariophyceae
Thallasiotrhix 600 1080 840
1 (Terkena sinar matahari langsung)
Melosira 480 600 720
Stauroneis 480 720 480
Navicula 240 240 120
Total 1800 2640 2160
Bacillariophyceae
Thallasiotrhix 480 720 600
Melosira 360 600 480
2 (Tidak terkena sinar matahari langsung)
Stauroneis 360 480 360
Navicula 120 240 120
35
35 Lampiran 4. Bahan organik yang dihasilkan oleh perifiton selama pengamatan
melalui pendekatan oksigen dan klorofil
Hari ke-
NPP Bahan Organik
mgO2/L/4 jam mgC/L/4 jam mgC/L/hr mgC/m
Klorofil-a Bahan Organik
mgChl-a/L mgC/L mgC/cm2 gC/m2
Stasiun 1 Stasiun 2 Stasiun 1 Stasiun 2 Stasiun 1 Stasiun 2 Stasiun 1 Stasiun 2
7 75,49 52,09 55,85 38,54 11170,60 7708,05 11,17 7,71
12 115,85 83,82 85,72 62,02 17143,55 12403,35 17,14 12,40
36
36 Lampiran 5. Analisis ANOVA RAL antara pengaruh cahaya terhadap bahan organik
yang dihasilkan oleh perifiton melalui pendekatan oksigen dan klorofil
Pendekatan Oksigen
Anova: Single Factor
SUMMARY
Groups Count Sum Average Variance
Column 1 3 4.587694 1.529231 0.704571
Column 2 3 4.010018 1.336673 0.824371
ANOVA
Source of Variation SS df MS F P-value F crit
Between Groups 0.055618 1 0.055618 0.072754 0.800712 7.708647
Within Groups 3.057884 4 0.764471
Total 3.113502 5
Pendekatan Klorofil
Anova: Single Factor
SUMMARY
Groups Count Sum Average Variance
Column 1 3 43.15887 14.38629 9.076646
Column 2 3 31.58454 10.52818 6.181182
ANOVA
Source of Variation SS df MS F P-value F crit
Between Groups 22.32752 1 22.32752 2.926697 0.162296 7.708647
Within Groups 30.51566 4 7.628914
37
37 Lampiran 6. Contoh perhitungan
1. Kelimpahan perifiton Diketahui :
N (jumlah perifiton yang diamati) = 7 ind As (luas substrat yang dikerik untuk perhitungan perifiton) = 5 cm2 At (luas penampang permukaan cover glass) = 400 mm2
Ac (luas amatan) = 400 mm2
Vt (volume botol sampel) = 30 ml
Vs (volume sampel/1 tetes) = 0,05 ml Ditanya :
Kelimpahan perifiton (ind/cm2) ? Jawab :
Jadi, kelimpahan perifiton yang diperoleh yaitu sebesar 840 ind/cm2
2. Bahan organik yang dihasilkan oleh perifiton melalui pendekatan klorofil Diketahui :
Bobot molekul karbon pada klorofil-a (BM C) = 660 Bobot molekul klorofil-a (BM Chl-a) = 892
Nilai klorofil-a yang diperoleh = 74,2236 mg/L
Volume air sampel (Vs) = 0,1 L
Luas substrat yang dikerik (As) = 5 cm2 (0,00002 m2) Ditanya :
Bahan organik yang dihasilkan (gC/m2) ? Jawab :
38
38 Jadi, bahan organik yang dihasilkan oleh perifiton melalui pendekatan klorofil yaitu sebesar 14,84 gC/m2.
2. Bahan organik yang dihasilkan oleh perifiton melalui pendekatan oksigen Diketahui :
Oksigen terlarut pada botol BOD inisial (I) = 14,09 mgO2/L Oksigen terlarut pada botol BOD terang (L) = 8,07 mgO2/L Volume botol BOD = 300 mL Luas substrat yang dikerik = 10 cm2 Ditanya :
39
40
40 Lampiran 7. Dokumentasi selama penelitian
Pengukuran oksigen terlarut dengan modifikasi Winkler
Tempat untuk meletakkan substrat buatan
Luxmeter DO meter
Gambar GPS map 60 CSx Lokasi pengamatan pada stasiun 2