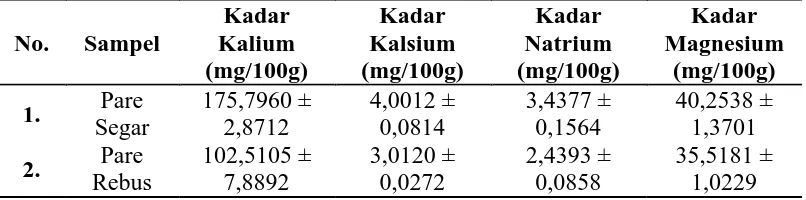
Lampiran 1. Gambar Buah Pare Putih (Momordica charantia L.)
Gambar 1. BuahPare Putih
Lampiran 1. (Lanjutan)
Gambar 3. Buah Pare yang Telah Selesai Dipotong Kecil-Kecil
Gambar 4. BuahPare yang Telah Selesai Direbus
Lampiran 3. Bagan Alir Proses Destruksi Kering
1. Buah Pare Putih Segar Buah Pare Putih Segar
Dicuci bersih dan dibilas dengan akua demineralisata
Dicabut tangkainya dari buah pare
Dipotong tipis-tipis buah pare dan dibuang bijinya
Sampel yang telah dipotong kecil-kecil
Ditimbang sebanyak 20 gram di atas krus Diarangkan di atas hot plate pada suhu 100o C-120oC
Diabukan dalam tanur dengan temperatur awal 100oC dan perlahan-lahan temperatur dinaikkan hingga suhu 500oC dengan interval 25oC setiap 5 menit
Dilakukan selama 24 jam dan dibiarkan hingga dingin pada desikator
Abu putih
Lampiran 3. (Lanjutan)
2. Buah Pare Putih Rebus Buah Pare Putih Segar
Dicuci bersih, dibilas dengan akua demineralisata
Dicabut tangkainya dari buah pare
Dipotong tipis-tipis buah pare dan dibuang bijinya
Direbus dengan menggunakan air mendidih 500 ml pada suhu 95oC selama 15 menit lalu ditiriskan
Ditimbang sebanyak 20 gram di atas krus Diarangkan di atas hot plate pada suhu 100o C-120oC
Diabukan dalam tanur dengan temperatur awal 100oC dan perlahan-lahan temperatur dinaikkan hingga suhu 500oC dengan interval 25oC setiap 5 menit
Dilakukan selama 24 jam dan dibiarkan hingga dingin pada desikator
Abu putih Sampel yang telah dipotong kecil-kecil
Lampiran 4. Bagan Alir Pembuatan Larutan Sampel
Abu putih hasil destruksi
Dilarutkan dalam 5 ml HNO3 (1:1)
Dipindahkan ke dalam labu tentukur 100 ml
Dibilas krus porselen sebanyak tiga kali dengan akua demineralisata. Dicukupkan dengan akua demineralisata hingga garis tanda
Disaring dengan kertas saring Whatman No. 42 Filtrat
Dimasukkan ke dalam botol Larutan sampel
Dilakukan analisis kuantitatif dengan Spektrofotometer Serapan Atom pada λ 766,5 nm untuk kadar kalium, pada λ 422,7 nm untuk kadar kalsium, pada λ 589,0 nm untuk kadar natrium dan pada λ 285,2 nm untuk kadar magnesium
Lampiran 5. Data Kalibrasi Kalium dengan Spektrofotometer Serapan Atom,
Perhitungan Persamaan Garis Regresi dan Koefisien Korelasi (r) No. Konsentrasi (µg/ml)
(X)
Absorbansi (Y)
1. 0,0000 -0,0020
2. 2,0000 0,0853
3. 4,0000 0,1711
4. 6,0000 0,2437
5. 8,0000 0,3267
6. 10,0000 0,4036
No. X Y X2 Y2 XY
1. 0,0000 -0,0020 0,0000 0,00000400 0,0000
2. 2,0000 0,0853 4,0000 0,00727609 0,1706
3. 4,0000 0,1711 16,0000 0,02927521 0,6844
4. 6,0000 0,2437 36,0000 0,05938969 1,4622
5. 8,0000 0,3267 64,0000 0,10673289 2,6136
6. 10,0000 0,4036 100,0000 0,16289296 4,0360 ∑ 30,0000
X = 5
1,2284 Y = 0,20473
220,0000 0,36557084 8,9668
a =
( )
X nX n Y X XY / / 2 2
∑
∑
∑
∑ ∑
− − =( )(
)
( )
30 /6 220 6 / 2284 , 1 30 9668 , 8 2 − − = 0,040354 Y = a X + b b = Y− aX= 0,20473 – (0,040354)(5) = 0,002962
Maka persamaan garis regresinya adalah: Y = 0,040354X+0,002962
=
( )(
)
( )
Lampiran 6. Data Kalibrasi Kalsium dengan Spektrofotometer Serapan Atom,
Perhitungan Persamaan Garis Regresi dan Koefisien Korelasi (r) No. Konsentrasi (µg/ml)
(X)
Absorbansi (Y)
1. 0,0000 -0,0002
2. 2,0000 0,0812
3. 4,0000 0,1472
4. 6,0000 0,2121
5. 8,0000 0,2879
6. 10,0000 0,3552
No. X Y X2 Y2 XY
1. 0,0000 -0,0002 0,0000 0,00000004 0,0000
2. 2,0000 0,0812 4,0000 0,00659344 0,1624
3. 4,0000 0,1472 16,0000 0,02166784 0,5888
4. 6,0000 0,2121 36,0000 0,04498641 1,2726
5. 8,0000 0,2879 64,0000 0,08288641 2,3032
6. 10,0000 0,3552 100,0000 0,12616704 3,5520 ∑ 30,0000
X = 5
1,0834 Y = 0,180567
220,0000 0,28230118 7,8790
a =
( )
X nX n Y X XY / / 2 2
∑
∑
∑
∑ ∑
− − =( )(
)
( )
30 /6 220 6 / 0834 , 1 30 8790 , 7 2 − − = 0,035171 Y = a X + b b = Y− aX= 0,180567 – (0,035171)(5) = 0,0047095
Maka persamaan garis regresinya adalah: Y = 0,035171X + 0,004710
=
( )(
)
( )
Lampiran 7. Data Kalibrasi Natrium dengan Spektrofotometer Serapan Atom,
Perhitungan Persamaan Garis Regresi dan Koefisien Korelasi (r) No. Konsentrasi (µg/ml)
(X)
Absorbansi (Y)
1. 0,0000 -0,0001
2. 0,2000 0,0265
3. 0,4000 0,0489
4. 0,6000 0,0715
5. 0,8000 0,0932
6. 1,0000 0,1186
No. X Y X2 Y2 XY
1. 0,0000 -0,0001 0,0000 0,00000001 0,0000
2. 0,2000 0,0265 0,0400 0,00070225 0,0053
3. 0,4000 0,0489 0,1600 0,00239121 0,01956
4. 0,6000 0,0715 0,3600 0,00511225 0,0429
5. 0,8000 0,0932 0,6400 0,00868624 0,07456
6. 1,0000 0,1186 1,0000 0,01406596 0,1186
∑ 3,0000
X = 0,5
0,3586 Y= 0,059767
2,2000 0,03095792 0,26092
a =
( )
X nX n Y X XY / / 2 2
∑
∑
∑
∑ ∑
− − =( )(
)
( )
3 /6 2 , 2 6 / 3586 , 0 3 26092 , 0 2 − − = 0,116600 Y = a X + b b = Y− aX= 0,059767 – (0,116600)(0,5) = 0,001467
Maka persamaan garis regresinya adalah: Y = 0,116600X + 0,001467
=
( )
( )
Lampiran 8. Data Kalibrasi Magnesium dengan Spektrofotometer Serapan
Atom, Perhitungan Persamaan Garis Regresi dan Koefisien Korelasi (r)
No. Konsentrasi (µg/ml) (X)
Absorbansi (Y)
1. 0,0000 -0,0001
2. 0,2000 0,0801
3. 0,4000 0,1611
4. 0,6000 0,2369
5. 0,8000 0,3163
6. 1,0000 0,3848
No. X Y X2 Y2 XY
1. 0,0000 -0,0001 0,0000 0,00000001 0,0000
2. 0,2000 0,0801 0,0400 0,00641601 0,01602
3. 0,4000 0,1611 0,1600 0,02595321 0,06444
4. 0,6000 0,2369 0,3600 0,05612161 0,14214
5. 0,8000 0,3163 0,6400 0,10004569 0,25304
6. 1,0000 0,3848 1,0000 0,14807104 0,3848
∑ 3,0000 X = 0,5
1,1791 Y = 0,196517
2,2000 0,33660757 0,86044
a =
( )
X nX n Y X XY / / 2 2
∑
∑
∑
∑ ∑
− − =( )
( )
3 /6 2 , 2 6 / 1791 , 1 3 86044 , 0 2 − − = 0,386986 Y = a X + b b = Y− aX= 0,196517 – (0,386986)(0,5) = 0,003024
Maka persamaan garis regresinya adalah: Y = 0,386986X + 0,003024
=
( )
( )
Lampiran 9. Perhitungan Batas Deteksi dan Batas Kuantitasi
1. Perhitungan Batas Deteksi dan Batas Kuantitasi Kalium Y = 0,040354X+0,002962
Slope = 0,040354
No
Konsentrasi (µg/ml)
(X)
Absorbansi
(Y) Yi Y-Yi (Y-Yi)
2
x10-6
1 0,0000 -0,0020 0,002962 -0,004962 24,62
2 2,0000 0,0853 0,083670 0,001630 2,66
3 4,0000 0,1711 0,164378 0,006722 45,19
4 6,0000 0,2437 0,245086 -0,001386 1,92
5 8,0000 0,3267 0,325794 0,000906 0,82
6 10,0000 0,4036 0,406502 -0,002902 8,42
Ʃ 83,63
( )
2 -nY -Yi /
2
∑
= x Sy
=
2 6
10 x 83,63 -6
− = 0,00457247
LOD =
Slope x Sy x( / ) 3
= 3 x 0,00457247 0,040354
= 0,3399 µg/ml
LOQ =
Slope x Sy x( / ) 10
= 10 x 0,00457247
0,040354
= 1,1331 µg/ml
2. Perhitungan Batas Deteksi dan Batas Kuantitasi Kalsium Y = 0,035171X+0,004710
Slope = 0,035171
No
Konsentrasi (µg/ml)
(X)
Absorbansi
(Y) Yi Y-Yi (Y-Yi)
2
x10-6
1 0,0000 -0,0002 0,004710 -0,004910 24,11
2 2,0000 0,0812 0,075052 0,006148 37,8
3 4,0000 0,1472 0,145394 0,001806 3,26
4 6,0000 0,2121 0,215736 -0,003636 13,22
5 8,0000 0,2879 0,286078 0,001822 3,32
6 10,0000 0,3552 0,356420 -0,001220 1,49
Ʃ 83,2
( )
2 -nY -Yi /
2
∑
= x Sy
=
2 6
10 x 83,2 -6
− = 0,00456070
LOD =
Slope x Sy x( / ) 3
= 3 x 0,00456070 0,035171
= 0,3890 µg/ml
LOQ =
Slope x Sy x( / ) 10
= 10 x 0,00456070
0,035171
= 1,2967 µg/ml
3. Perhitungan Batas Deteksi dan Batas Kuantitasi Natrium Y = 0,116600X+0,001467
Slope = 0,1166
No
Konsentrasi (µg/ml)
(X)
Absorbansi
(Y) Yi Y-Yi (Y-Yi)
2
x10-6
1 0,0000 -0,0001 0,001467 -0,001567 2,455
2 0,2000 0,0265 0,024787 0,001713 2,934
3 0,4000 0,0489 0,048107 0,000793 0,629
4 0,6000 0,0715 0,071427 0,000073 0,005
5 0,8000 0,0932 0,094747 -0,001547 2,393
6 1,0000 0,1186 0,118067 0,000533 0,284
Ʃ 8,7
( )
2 -nY -Yi /
2
∑
= x Sy
=
2 6
10 x 8,7 -6
− = 0,00147479
LOD =
Slope x Sy x( / ) 3
= 3 x 0,00147479 0,1166
= 0,0379 µg/ml
LOQ =
Slope x Sy x( / ) 10
= 10 x 0,00147479
0,1166
= 0,1265 µg/ml
4. Perhitungan Batas Deteksi dan Batas Kuantitasi Magnesium Y = 0,386986X+0,003024
Slope = 0,386986
No
Konsentrasi (µg/ml)
(X)
Absorbansi
(Y) Yi Y-Yi (Y-Yi)
2
x10-6 1 0,0000 -0,0001 0,0030240 -0,0031240 9,76
2 0,2000 0,0801 0,0804212 -0,0003212 0,1
3 0,4000 0,1611 0,1578184 0,0032816 10,77
4 0,6000 0,2369 0,2352156 0,0016844 2,84
5 0,8000 0,3163 0,3126128 0,0036872 13,6
6 1,0000 0,3848 0,3900100 -0,0052100 27,14
Ʃ 64,21
( )
2 -nY -Yi /
2
∑
= x Sy
=
2 6
10 x 64,21 -6
− = 0,00400656
LOD =
Slope x Sy x( / ) 3
= 3 x 0,00400656 0,386986
= 0,0311 µg/ml
LOQ =
Slope x Sy x( / ) 10
= 10 x 0,00400656
0,386986
Lampiran 10. Hasil Analisis Kadar Kalium, Kalsium, Natrium, dan Magnesium
dalam Pare Segar 1. Hasil Analisis Kadar Kalium
Sampel Berat Sampel (g) Absorbansi (A) Konsentrasi (µg/ml) Kadar (mg/100g)
1 20,0150 0,2851 6,9915 174,6565
2 20,0800 0,2836 6,9544 173,1673
3 20,0250 0,2898 7,1080 177,4782
4 20,0350 0,2899 7,1105 177,4519
5 20,0500 0,2891 7,0906 176,8304
6 20,0600 0,2866 7,0287 175,1919
2. Hasil Analisis Kadar Kalsium Sampel Berat Sampel
(g) Absorbansi (A) Konsentrasi (µg/ml) Kadar (mg/100g)
1 20,0150 0,2826 7,9011 3,9476
2 20,0800 0,2824 7,8954 3,9320
3 20,0250 0,2890 8,0830 4,0365
4 20,0350 0,2889 8,0802 4,0330
5 20,0500 0,2902 8,1172 4,0485
6 20,0600 0,2876 8,0433 4,0096
3. Hasil Analisis Kadar Natrium Sampel Berat Sampel
(g) Absorbansi (A) Konsentrasi (µg/ml) Kadar (mg/100g)
1 20,0150 0,0809 0,6812 3,4034
2 20,0800 0,0791 0,6658 3,3157
3 20,0250 0,0833 0,7018 3,5046
4 20,0350 0,0799 0,6726 3,3571
5 20,0500 0,0828 0,6975 3,4788
6 20,0600 0,0849 0,7155 3,5667
4. Hasil Analisis Kadar Magnesium Sampel Berat Sampel
(g) Absorbansi (A) Konsentrasi (µg/ml) Kadar (mg/100g)
1 20,0150 0,3254 0,8330 41,6187
2 20,0800 0,3136 0,8025 39,9651
3 20,0250 0,3141 0,8038 40,1398
4 20,0350 0,3063 0,7836 39,1115
5 20,0500 0,3137 0,8028 40,0399
Lampiran 11. Hasil Analisis Kadar Kalium, Kalsium, Natrium, dan Magnesium
dalam Pare Rebus 1. Hasil Analisis Kadar Kalium
Sampel Berat Sampel (g) Absorbansi (A) Konsentrasi (µg/ml) Kadar (mg/100g)
1 20,0550 0,1788 4,3574 108,6362
2 20,0850 0,1658 4,0352 100,4531
3 20,0350 0,1598 3,8865 96,9927
4 20,0250 0,1733 4,2211 105,3957
5 20,0750 0,1745 4,2508 105,8729
6 20,0400 0,1610 3,9163 97,7121
2. Hasil Analisis Kadar Kalsium Sampel Berat Sampel
(g) Absorbansi (A) Konsentrasi (µg/ml) Kadar (mg/100g)
1 20,0550 0,2187 6,0843 3,0338
2 20,0850 0,2173 6,0445 3,0095
3 20,0350 0,2170 6,0359 3,0127
4 20,0250 0,2162 6,0132 3,0029
5 20,0750 0,2166 6,0246 3,0011
6 20,0400 0,2207 6,1411 3,0644
3. Hasil Analisis Kadar Natrium Sampel Berat Sampel
(g) Absorbansi (A) Konsentrasi (µg/ml) Kadar (mg/100g)
1 20,0550 0,0596 0,4986 2,4862
2 20,0850 0,0572 0,4780 2,3798
3 20,0350 0,0579 0,4840 2,4157
4 20,0250 0,0598 0,5003 2,4984
5 20,0750 0,0573 0,4788 2,3851
6 20,0400 0,0592 0,4951 2,4705
4. Hasil Analisis Kadar Magnesium Sampel Berat Sampel
(g) Absorbansi (A) Konsentrasi (µg/ml) Kadar (mg/100g)
1 20,0550 0,2812 0,7188 35,8414
2 20,0850 0,2740 0,7002 34,8618
3 20,0350 0,2773 0,7088 35,3781
4 20,0250 0,2855 0,7299 36,4494
5 20,0750 0,2737 0,6994 34,8393
Lampiran 12. Contoh Perhitungan Kadar Kalium, Kalsium, Natrium, dan
Magnesium dalam Pare Segar 1. Contoh Perhitungan Kadar Kalium
Berat Sampel yang ditimbang = 20,0150 gram Absorbansi (Y) = 0,2851
Persamaan Regresi: Y= 0,040354X + 0,002962 X = 040354 , 0 002962 , 0 2851 , 0 −
= 6,9915 µg/ml Konsentrasi Kadar Kalium = 6,9915 µg/ml
Kadar logam(µg/g) = Konsentrasi(µg/ml) x Volume (ml) x Faktor Pengenceran Berat Sampel (g)
= g mlx mlx g 0150 , 20 ) 5 , 0 / 25 ( 100 / 9915 , 6 µ
= 1746,5651 µg/g = 174,6565 mg/100g
2. Contoh Perhitungan Kadar Kalsium
Berat Sampel yang ditimbang = 20,0150 gram Absorbansi (Y) = 0,2826
Persamaan Regresi: Y= 0,035171X + 0,004710 X = 035171 , 0 004710 , 0 2826 , 0 −
= 7,9011 µg/ml Konsentrasi Kadar Kalsium = 7,9011 µg/ml
Kadar logam(µg/g) = Konsentrasi(µg/ml) x Volume (ml) x Faktor Pengenceran Berat Sampel (g)
= g mlx mlx g 0150 , 20 ) 100 / 100 ( 100 / 9011 , 7 µ
Lampiran 12. (Lanjutan)
3. Contoh Perhitungan Kadar Natrium
Berat Sampel yang ditimbang = 20,0150 gram Absorbansi (Y) = 0,0809
Persamaan Regresi: Y= 0,116600X + 0,001467 X = 116600 , 0 001467 , 0 0809 , 0 −
= 0,6812 µg/ml Konsentrasi Kadar Natrium = 0,6812 µg/ml
Kadar logam(µg/g) = Konsentrasi(µg/ml) x Volume (ml) x Faktor Pengenceran Berat Sampel (g)
= g mlx mlx g 0150 , 20 ) 5 , 2 / 25 ( 100 / 6812 , 0 µ
= 34,0344 µg/g = 3,4034 mg/100g
4. Contoh Perhitungan Kadar Magnesium Berat Sampel yang ditimbang = 20,0150 gram Absorbansi (Y) = 0,3254
Persamaan Regresi: Y= 0,386986X + 0,003024 X = 386986 , 0 003024 , 0 3254 , 0 −
= 0,8330 µg/ml
Konsentrasi Kadar Magnesium = 0,8330 µg/ml
Kadar logam(µg/g) = Konsentrasi(µg/ml) x Volume (ml) x Faktor Pengenceran Berat Sampel (g)
= g mlx mlx g 0150 , 20 ) 25 , 0 / 25 ( 100 / 8330 , 0 µ
Lampiran 13. Contoh Perhitungan Kadar Kalium, Kalsium, Natrium, dan
Magnesium dalam Pare Rebus 1. Contoh Perhitungan Kadar Kalium
Berat Sampel yang ditimbang = 20,0550 gram Absorbansi (Y) = 0,1788
Persamaan Regresi: Y= 0,040354X + 0,002962 X = 040354 , 0 002962 , 0 1788 , 0 −
= 4,3574 µg/ml Konsentrasi Kadar Kalium = 4,3574 µg/ml
Kadar logam(µg/g) = Konsentrasi(µg/ml) x Volume (ml) x Faktor Pengenceran Berat Sampel (g)
= g mlx mlx g 0550 , 20 ) 5 , 0 / 25 ( 100 / 3574 , 4 µ
= 1086,3625 µg/g = 108,6362 mg/100g
2. Contoh Perhitungan Kadar Kalsium
Berat Sampel yang ditimbang = 20,0550 gram Absorbansi (Y) = 0,2187
Persamaan Regresi: Y= 0,035171X + 0,004710 X = 035171 , 0 004710 , 0 2187 , 0 −
= 6,0843 µg/ml Konsentrasi Kadar Kalsium = 6,0843 µg/ml
Kadar logam(µg/g) = Konsentrasi(µg/ml) x Volume (ml) x Faktor Pengenceran Berat Sampel (g)
= g mlx mlx g 0550 , 20 ) 100 / 100 ( 100 / 0843 , 6 µ
Lampiran 13. (Lanjutan)
3. Contoh Perhitungan Kadar Natrium
Berat Sampel yang ditimbang = 20,0550 gram Absorbansi (Y) = 0,0596
Persamaan Regresi: Y= 0,116600X + 0,001467 X = 116600 , 0 001467 , 0 0596 , 0 −
= 0,4986 µg/ml Konsentrasi Kadar Natrium = 0,4986 µg/ml
Kadar logam(µg/g) = Konsentrasi(µg/ml) x Volume (ml) x Faktor Pengenceran Berat Sampel (g)
= g mlx mlx g 0550 , 20 ) 5 , 2 / 25 ( 100 / 4986 , 0 µ
= 24,8616 µg/g = 2,4862 mg/100g
4. Contoh Perhitungan Kadar Magnesium Berat Sampel yang ditimbang = 20,0550 gram Absorbansi (Y) = 0,2812
Persamaan Regresi: Y= 0,386986X + 0,003024 X = 386986 , 0 003024 , 0 2812 , 0 −
= 0,7188 µg/ml
Konsentrasi Kadar Magnesium = 0,7188 µg/ml
Kadar logam(µg/g) = Konsentrasi(µg/ml) x Volume (ml) x Faktor Pengenceran Berat Sampel (g)
= g mlx mlx g 0550 , 20 ) 25 , 0 / 25 ( 100 / 7188 , 0 µ
Lampiran 14.Perhitungan Statistik Kadar Kalium dalam Sampel
1. Perhitungan Statistik Kadar Kalium dalam Pare Segar
No.
Xi
Kadar (mg/100g) (Xi-X ) (Xi-X)2
1. 174,6565 -1,1395 1,29846025
2. 173,7547 -2,6287 6,91006369
3. 177,4782 1,6822 2,82979684
4. 177,4519 1,6559 2,74200481
5. 176,8304 1,0344 1,06998336
6. 175,1919 -0,6041 0,36493681
∑ 1054,7762
X = 175,7960
15,21524576
SD =
( )
1 -n X -Xi 2
∑
= 1 -6 21524576 , 15 = 1,7444Pada interval kepercayaan 99%, dengan nilai α = 0.01 n = 6 dk = 5, diperoleh nilai t tabel = α/2, dk = 4,0321.
Data diterima jika t hitung < t tabel
t hitung =
n SD X Xi / −
t hitung 1 =
6 / 7444 , 1 1395 , 1 − = 1,6002
t hitung 2 =
6 / 7444 , 1 6287 , 2
− = 3,6914
t hitung 3 =
6 / 7444 , 1 6822 , 1 = 2,3623
t hitung 4 =
6 / 7444 , 1 6559 , 1 = 2,3253
t hitung 5 =
Lampiran 14. (Lanjutan)
t hitung 6 =
6 / 7444 , 1 6041 , 0 − = 0,8483
Dari hasil perhitungan di atas, didapat semua t hitung < t tabel , maka semua data
diterima.
Kadar Kalium dalam Pare Segar adalah µ = X ± t (α/2, dk) x SD / √n
= 175,7960 ± (4,0321 x 1,7444 / √6 ) = (175,7960 ± 2,8712) mg/100g
2. Perhitungan Statistik Kadar Kalium dalam Pare Rebus
No.
Xi
Kadar (mg/100g) (Xi-X ) (Xi-X )2
1. 108,6362 6,1257 37,52420049
2. 100,4531 -2,0574 4,23289476
3. 96,9927 -5,5178 30,44611684
4. 105,3957 2,8852 8,32437904
5. 105,8729 3,3624 11,30573376
6. 97,7121 -4,7984 23,02464256
∑ 615,0627
X = 102,5105
114,8579675
SD =
( )
1 -n X -Xi 2
∑
= 1 -6 8579675 , 114 = 4,7928Pada interval kepercayaan 99%, dengan nilai α = 0.01 n = 6 dk = 5, diperoleh nilai t tabel = α/2, dk = 4,0321.
Data diterima jika t hitung < t tabel
t hitung =
n SD X Xi / −
t hitung 1 =
Lampiran 14. (Lanjutan)
t hitung 2 =
6 / 7928 , 4
0574 , 2 −
= 1,0515
t hitung 3 =
6 / 7928 , 4
5178 , 5 −
= 2,8201
t hitung 4 =
6 / 7928 , 4
8852 , 2
= 1,4745
t hitung 5 =
6 / 7928 , 4
3624 , 3
= 1,7185
t hitung 6 =
6 / 7928 , 4
7984 , 4
− = 2,4524
Dari hasil perhitungan di atas, didapat semua t hitung < t tabel , maka semua data
diterima.
Kadar Kalium dalam Pare Rebus adalah µ = X ± t (α/2, dk) x SD / √n
Lampiran 15. Perhitungan Statistik Kadar Kalsium dalam Sampel
1. Perhitungan Statistik Kadar Kalsium dalam Pare Segar
No.
Xi
Kadar (mg/100g) (Xi-X ) (Xi-X )2
1. 3,9476 -0,0536 0,00287296
2. 3,9320 -0.0692 0,00478864
3. 4,0365 0,0353 0,00124609
4. 4,0330 0,0318 0,00101124
5. 4,0485 0,0473 0,00223729
6. 4,0096 0,0084 0,00007056
∑ 24,0072
X = 4,0012
0,01222678
SD =
( )
1 -n X -Xi 2
∑
= 1 -6 01222678 , 0 = 0,0495Pada interval kepercayaan 99%, dengan nilai α = 0.01 n = 6 dk = 5, diperoleh nilai t tabel = α/2, dk = 4,0321.
Data diterima jika t hitung < t tabel
t hitung =
n SD X Xi / −
t hitung 1 =
6 / 0495 , 0 0536 , 0
− = 1,0828
t hitung 2 =
6 / 0495 , 0 0692 , 0
− = 3,4257
t hitung 3 =
6 / 0495 , 0 0353 , 0 = 1,7475
t hitung 4 =
6 / 0495 , 0 0318 , 0 = 1,5743
t hitung 5 =
Lampiran 15. (Lanjutan)
t hitung 6 =
6 / 0495 , 0 0084 , 0 = 0,4158
Dari hasil perhitungan di atas, didapat semua t hitung < t tabel , maka semua data
diterima.
Kadar Kalsium dalam Pare Segar adalah µ = X ± t (α/2, dk) x SD / √n
= 4,0012 ± (4,0321 x 0,0495 / √6 ) = (4,0012 ± 0,0814) mg/100g
2. Perhitungan Statistik Kadar Kalsium dalam Pare Rebus
No.
Xi
Kadar (mg/100g) (Xi-X ) (Xi-X )2
1. 3,0338 0,0131 0,00017161
2. 3,0095 -0,0112 0,00012544
3. 3,0127 -0,0080 0,00006400
4. 3,0029 -0,0178 0,00031684
5. 3,0011 -0,0196 0,00038416
6. 3,0644 0,0437 0,00190969
∑ 18,1244
X = 3,0207
0,00297174
SD=
( )
1 -n X -Xi 2
∑
= 1 -6 00297174 , 0 = 0,0244Pada interval kepercayaan 99%, dengan nilai α = 0.01 n = 6 dk = 5, diperoleh nilai t tabel = α/2, dk = 4,0321.
Data diterima jika t hitung < t tabel
t hitung =
n SD X Xi / −
t hitung 1 =
Lampiran 15. (Lanjutan)
t hitung 2 =
6 / 0244 , 0 0112 , 0 − = 1,1313
t hitung 3 =
6 / 0244 , 0 0080 , 0 − = 0,8081
t hitung 4 =
6 / 0244 , 0 0178 , 0 − = 1,7979
t hitung 5 =
6 / 0244 , 0 0196 , 0 − = 1,9797
t hitung 6 =
6 / 0244 , 0 0437 , 0 = 4,4141
Dari hasil perhitungan di atas, data ke-6 tidak memenuhi, sehingga perhitungan diulangi dengan cara yang sama tanpa mengikutsertakan data ke-6.
No.
Xi
Kadar (mg/100g) (Xi-X ) (Xi-X )2
1. 3,0338 0,0218 0,00047524
2. 3,0095 -0,0025 0,00000625
3. 3,0127 0,0007 0,00000049
4. 3,0029 -0,0091 0,00008281
5. 3,0011 -0,0109 0,00011881
∑ 15,0600
X = 3,0120
0,0006836
SD =
( )
1 -n X -Xi 2
∑
= 1 -5 0006836 , 0 = 0,0131Pada interval kepercayaan 99%, dengan nilai α = 0.01 n = 5 dk = 4, diperoleh nilai t tabel = α/2, dk = 4,6041.
Data diterima jika t hitung < t tabel
t hitung =
Lampiran 15. (Lanjutan)
t hitung 1 =
5 / 0131 , 0
0218 , 0
= 3,6949
t hitung 2 =
5 `/ 0131 , 0
0025 , 0 −
= 0,4237
t hitung 3 =
5 / 0131 , 0
0007 , 0
= 0,1186
t hitung 4 =
5 / 0131 , 0
0091 , 0 −
= 1,5423
t hitung 5 =
5 / 0131 , 0
0109 , 0
− = 1,8475
Dari hasil perhitungan di atas, didapat semua t hitung < t tabel , maka semua data
diterima.
Kadar Kalsium dalam Pare Rebus adalah µ = X ± t (α/2, dk) x SD / √n
Lampiran 16. Perhitungan Statistik Kadar Natrium Sampel
1. Perhitungan Statistik Kadar Natrium dalam Pare Segar
No.
Xi
Kadar (mg/100g) (Xi-X ) (Xi-X )2
1. 3,4034 -0,0343 0,00117649
2. 3,3157 -0,1220 0,01488400
3. 3,5046 0,0669 0,00447561
4. 3,3571 -0,0806 0,00649636
5. 3,4788 0,0411 0,00168921
6. 3,5667 0,1290 0,01664100
∑ 20,6263
X = 3,4377
0,04536267
SD =
( )
1 -n X -Xi 2
∑
= 1 -6 04536267 , 0 = 0,0952Pada interval kepercayaan 99%, dengan nilai α = 0.01 n = 6 dk = 5, diperoleh nilai t tabel = α/2, dk = 4,0321.
Data diterima jika t hitung < t tabel
t hitung =
n SD X Xi / −
t hitung 1 =
6 / 0952 , 0 0343 , 0
− = 0,8840
t hitung 2 =
6 / 0952 , 0 1220 , 0
− = 3,1443
t hitung 3 =
6 / 0952 , 0 0669 , 0 = 1,7242
t hitung 4 =
6 / 0952 , 0 0806 , 0
− = 2,0773
t hitung 5 =
Lampiran 16. (Lanjutan)
t hitung 6 =
6 / 0952 , 0 1290 , 0 = 3,3247
Dari hasil perhitungan di atas, didapat semua t hitung < t tabel , maka semua data
diterima.
Kadar Natrium dalam Pare Segar adalah µ = X ± t (α/2, dk) x SD / √n
= 3,4377 ± (4,0321 x 0,0952 / √6 ) = (3,4377 ± 0,1564) mg/100g
2. Perhitungan Statistik Kadar Natrium dalam Pare Rebus
No.
Xi
Kadar (mg/100g) (Xi-X ) (Xi-X )2
1. 2,4862 0,0469 0,00219961
2. 2,3798 -0,0595 0,00354025
3. 2,4157 -0,0236 0,00055696
4. 2,4984 0,0591 0,00349281
5. 2,3851 -0,0542 0,00293764
6. 2,4705 0,0312 0,00097344
∑ 14,6357
X = 2,4393
0,01370071
SD =
( )
1 -n X -Xi 2
∑
= 1 -6 01370071 , 0 = 0,0523Pada interval kepercayaan 99%, dengan nilai α = 0.01 n = 6 dk = 5, diperoleh nilai t tabel = α/2, dk = 4,0321.
Data diterima jika t hitung < t tabel
t hitung =
n SD X Xi / −
t hitung 1 =
Lampiran 16. (Lanjutan)
t hitung 2 =
6 / 0523 , 0
0595 , 0 −
= 2,7934
t hitung 3 =
6 / 0523 , 0
0236 , 0 −
= 1,1079
t hitung 4 =
6 / 0523 , 0
0591 , 0
= 2,7746
t hitung 5 =
6 / 0523 , 0
0542 , 0 −
= 2,5446
t hitung 6 =
6 / 0523 , 0
0312 , 0
= 1,4647
Dari hasil perhitungan di atas, didapat semua t hitung < t tabel , maka semua data
diterima.
Kadar Natrium dalam Pare Rebus adalah µ = X ± t (α/2, dk) x SD / √n
Lampiran 17. Perhitungan Statistik Kadar Magnesium dalam Sampel
1. Perhitungan Statistik Kadar Magnesium dalam Pare Segar
No.
Xi
Kadar (mg/100g) (Xi-X ) (Xi-X )2
1. 41,6710 1,3649 1,86295201
2. 39,6500 -0,2887 0,08334769
3. 40,7770 -0,1140 0,01299600
4. 39,6088 -1,1423 1,30484929
5. 40,5896 -0,2139 0,04575321
6. 40,8279 0,3942 0,15539364
∑ 241,5230
X = 40,2538
3,46529184
SD =
( )
1 -n X -Xi 2
∑
= 1 -6 46529184 , 3 = 0,8325Pada interval kepercayaan 99%, dengan nilai α = 0.01 n = 6 dk = 5, diperoleh nilai t tabel = α/2, dk = 4,0321.
Data diterima jika t hitung < ttabel
t hitung =
n SD X Xi / −
t hitung 1 =
6 / 8325 , 0 3649 , 1 = 4,0167
t hitung 2 =
6 / 8325 , 0 2887 , 0
− = 0,8496
t hitung 3 =
6 / 8325 , 0 1140 , 0
− = 0,3354
t hitung 4 =
6 / 8325 , 0 1423 , 1
− = 3,3616
t hitung 5 =
6 / 8325 , 0 2139 , 0
Lampiran 17. (Lanjutan)
t hitung 6 =
6 / 8325 , 0 3942 , 0 = 1,1600
Dari hasil perhitungan di atas, didapat semua t hitung < t tabel , maka semua data
diterima.
Kadar Magnesium dalam Pare Segar adalah µ = X ± t (α/2, dk) x SD / √n
= 40,2538 ± (4,0321 x 0,8325 / √6 ) = (40,2538 ± 1,3701) mg/100g
2. Perhitungan Statistik Kadar Magnesium dalam Pare Rebus
No.
Xi
Kadar (mg/100g) (Xi-X ) (Xi-X )2
1. 35,7259 0,3233 0,10452289
2. 34,6860 -0,6563 0,43072969
3. 35,7054 -0,1400 0,01960000
4. 36,6745 0,9313 0,86731969
5. 34,7458 -0,6788 0,46076944
6. 35,7856 0,2204 0,04857616
∑ 213,1085
X = 35,5181
1,93151787
SD =
( )
1 -n X -Xi 2
∑
= 1 -6 93151787 , 1 = 0,6215Pada interval kepercayaan 99%, dengan nilai α = 0.01 n = 6 dk = 5, diperoleh nilai t tabel = α/2, dk = 4,0321.
Data diterima jika t hitung < t tabel
t hitung =
n SD X Xi / −
t hitung 1 =
Lampiran 17. (Lanjutan)
t hitung 2 =
6 / 6215 , 0
6563 , 0 −
= 2,5869
t hitung 3 =
6 / 6215 , 0
1400 , 0 −
= 0,5518
t hitung 4 =
6 / 6215 , 0
9313 , 0
= 3,6708
t hitung 5 =
6 / 6215 , 0
6788 , 0 −
= 2,6756
t hitung 6 =
6 / 6215 , 0
2204 , 0
= 0,8687
Dari hasil perhitungan di atas, didapat semua t hitung < t tabel , maka semua data
diterima.
Kadar Magnesium dalam Pare Rebus adalah µ = X ± t (α/2, dk) x SD / √n
Lampiran 18. Persentase Penurunan Kadar Kalium, Kalsium, Natrium, dan
Magnesium dalam Pare Segar dan Rebus 1. Kalium
Kadar Kalium Pare Segar adalah 175,7960 mg/100g Kadar Kalium Pare Rebus adalah 102,5105 mg/100g Persentase Penurunan Kadar Kalium pada Pare adalah :
Kadar rata−rata logam dalam Pare segar – Kadar rata−rata logam dalam Pare rebus
Kadar rata−rata logam dalam Pare segar x 100%
(175,7960 − 102,5105) mg/100g
175,7960 mg/100g x 100% = 41,69%
2. Kalsium
Kadar Kalsium Pare Segar adalah 4,0012 mg/100g Kadar Kalsium Pare Rebus adalah 3,0120 mg/100g Persentase Penurunan Kadar Kalsium pada Pare adalah :
Kadar rata−rata logam dalam Pare segar – Kadar rata−rata logam dalam Pare rebus
Kadar rata−rata logam dalam Pare segar x 100%
(4,0012 − 3,0120) mg/100g
4,0012 mg/100g x 100% = 24,72%
3. Natrium
Kadar Natrium Pare Segar adalah 3,4377 mg/100g Kadar Natrium Pare Rebus adalah 2,4393 mg/100g Persentase Penurunan Kadar Natrium pada Pare adalah :
Kadar rata−rata logam dalam Pare segar – Kadar rata−rata logam dalam Pare rebus
Kadar rata−rata logam dalam Pare segar x 100%
(3,4377 – 2,4393) mg/100g
Lampiran 18. (Lanjutan)
4. Magnesium
Kadar Magnesium Pare Segar adalah 40,2538 mg/100g Kadar Magnesium Pare Rebus adalah 35,5181 mg/100g Persentase Penurunan Kadar Magnesium pada Pare adalah :
Kadar rata−rata logam dalam Pare segar – Kadar rata−rata logam dalam Pare rebus
Kadar rata−rata logam dalam Pare segar x 100%
(40,2538 – 35,5181) mg/100g
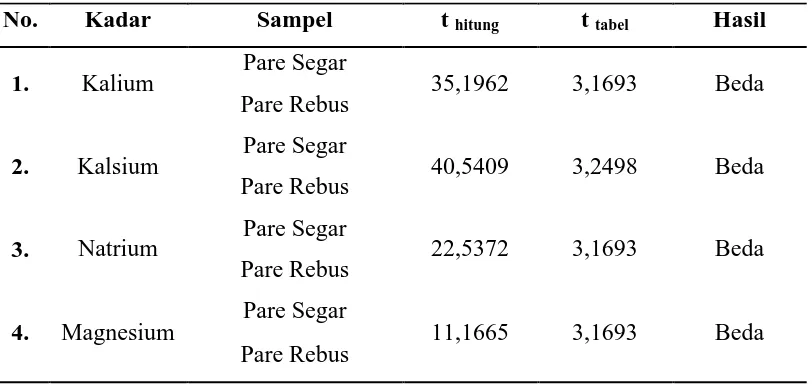
Lampiran 19. Hasil Pengujian Beda Nilai Rata-Rata Kadar Kalium dalam Pare
Segar dan Pare Rebus
No. Pare Segar Pare Rebus
1. X1 = 175,7960 mg/100g X2 = 102,5105 mg/100g
2. S1 = 1,7444 S2 = 4,7928
Dilakukan uji F dengan taraf kepercayaan 99% untuk mengetahui apakah variasi kedua populasi sama (σ1 = σ2) atau berbeda (σ1 ≠ σ2 ).
− Ho : σ1 = σ2
H1 : σ1 ≠ σ2
− Nilai kritis F yang diperoleh dari tabel (F0,01/2 (5,5)) adalah = 14,94
Daerah kritis penerimaan : Jika Fo ≤ 14,94 Daerah kritis penolakan : jika Fo ≥ 14,94
Fo = 2 2 2 1 S S
Fo = 2
2
7928 , 4 1,7444
Fo = 0,1325
− Dari hasil ini menunjukkan bahwa Ho diterima dan H1 ditolak sehingga
disimpulkan bahwa σ1 = σ2, simpangan bakunya adalah:
Sp =
2 1 1 2 1 2 2 2 2 1 1 − − − n + n )S (n + )S (n = 2 6 6 4,7928 1 6 7444 , 1 1
6 2 2
Lampiran 19. (Lanjutan)
− Ho : µ1 = µ2
H1 : µ1 ≠ µ2
− Dengan menggunakan taraf kepercayaan 99% dengan nilai α = 1 % → t0,01/2 = 3,1693 untuk df = 6+6-2 = 10
− Daerah kritis penerimaan : -3,1693 ≤ to≤ 3,1693
Daerah kritis penolakan : to< -3,1693 dan to> 3,1693
to =
(
)
2 1
2 1
/ 1 / 1
x -x
n n
Sp +
=
(
)
6 1 6 1 3,6065
102,5105
-175,7960 +
= 35,1962
− Karena to = 35,1962 > 3,1693 maka hipotesis ditolak. Berarti terdapat
Lampiran 20. Hasil Pengujian Beda Nilai Rata-Rata Kadar Kalsium dalam Pare
Segar dan Pare Rebus
No. Pare Segar Pare Rebus
1. X1 = 4,0012 mg/100g X2 = 3,0120 mg/100g
2. S1 = 0,0495 S2 = 0,0244
Dilakukan uji F dengan taraf kepercayaan 99% untuk mengetahui apakah variasi kedua populasi sama (σ1 = σ2) atau berbeda (σ1 ≠ σ2 ).
− Ho : σ1 = σ2
H1 : σ1 ≠ σ2
− Nilai kritis F yang diperoleh dari tabel (F0,01/2 (5,4)) adalah = 22,46
Daerah kritis penerimaan : Jika Fo ≤ 22,46 Daerah kritis penolakan : jika Fo ≥ 22,46
Fo = 2 2 2 1 S S
Fo = 2
2
0244 , 0 0,0495
Fo = 4,1148
− Dari hasil ini menunjukkan bahwa Ho diterima dan H1 ditolak sehingga
disimpulkan bahwa σ1 = σ2, simpangan bakunya adalah:
Sp =
2 1 1 2 1 2 2 2 2 1 1 − − − n + n )S (n + )S (n = 2 5 6 0,0244 1 5 0495 , 0 1
6 2 2
Lampiran 20. (Lanjutan)
− Ho : µ1 = µ2
H1 : µ1 ≠ µ2
− Dengan menggunakan taraf kepercayaan 99% dengan nilai α = 1 % → t0,01/2 = 3,2498 untuk df = 6+5-2 = 9
− Daerah kritis penerimaan : -3,2498 ≤ to≤ 3,2498
Daerah kritis penolakan : to< -3,2498 dan to> 3,2498
to =
(
)
2 1
2 1
/ 1 / 1
x -x
n n
Sp +
=
(
)
5 1 6 1 0,0403
3,0120
-4,0012 +
= 40,5409
− Karena to = 40,5409 > 3,2498 maka hipotesis ditolak. Berarti terdapat
Lampiran 21. Hasil Pengujian Beda Nilai Rata-Rata Kadar Natrium dalam Pare
Segar dan Pare Rebus
No. Pare Segar Pare Rebus
1. X1 = 3,4377 mg/100g X2 = 2,4393 mg/100g
2. S1 = 0,0952 S2 = 0,0523
Dilakukan uji F dengan taraf kepercayaan 99% untuk mengetahui apakah variasi kedua populasi sama (σ1 = σ2) atau berbeda (σ1 ≠ σ2 ).
− Ho : σ1 = σ2
H1 : σ1 ≠ σ2
− Nilai kritis F yang diperoleh dari tabel (F0,01/2 (5,5)) adalah = 14,94
Daerah kritis penerimaan : Jika Fo ≤ 14,94 Daerah kritis penolakan : jika Fo ≥ 14,94
Fo = 2 2 2 1 S S
Fo = 2
2
0523 , 0 0,0952
Fo = 3,3137
− Dari hasil ini menunjukkan bahwa Ho diterima dan H1 ditolak sehingga
disimpulkan bahwa σ1 = σ2, simpangan bakunya adalah:
Sp =
2 1 1 2 1 2 2 2 2 1 1 − − − n + n )S (n + )S (n = 2 6 6 0,0523 1 6 0952 , 0 1
6 2 2
Lampiran 21. (Lanjutan)
− Ho : µ1 = µ2
H1 : µ1 ≠ µ2
− Dengan menggunakan taraf kepercayaan 99% dengan nilai α = 1 % → t0,01/2 = 3,1693 untuk df = 6+6-2 = 10
− Daerah kritis penerimaan : -3,1693 ≤ to≤ 3,1693
Daerah kritis penolakan : to< -3,1693 dan to> 3,1693
to =
(
)
2 1
2 1
/ 1 / 1
x -x
n n
Sp +
=
(
)
6 1 6 1 0,0767
2,4393
-3,4377 +
= 22,5372
− Karena to = 22,5372 > 3,1693 maka hipotesis ditolak. Berarti terdapat
Lampiran 22. Hasil Pengujian Beda Nilai Rata-Rata Kadar Magnesium dalam
Pare Segar dan Pare Rebus
No. Pare Segar Pare Rebus
1. X1 = 40,2538 mg/100g X2 = 35,5181 mg/100g
2. S1 = 0,8325 S2 = 0,6215
Dilakukan uji F dengan taraf kepercayaan 99% untuk mengetahui apakah variasi kedua populasi sama (σ1 = σ2) atau berbeda (σ1 ≠ σ2 ).
− Ho : σ1 = σ2
H1 : σ1 ≠ σ2
− Nilai kritis F yang diperoleh dari tabel (F0,01/2 (5,5)) adalah = 14,94
Daerah kritis penerimaan : Jika Fo ≤ 14,94 Daerah kritis penolakan : jika Fo ≥ 14,94
Fo = 2 2 2 1 S S
Fo = 2
2
6215 , 0 0,8325
Fo = 1,7942
− Dari hasil ini menunjukkan bahwa Ho diterima dan H1 ditolak sehingga
disimpulkan bahwa σ1 = σ2, simpangan bakunya adalah:
Sp =
2 1 1 2 1 2 2 2 2 1 1 − − − n + n )S (n + )S (n = 2 6 6 0,6215 1 6 8325 , 0 1
6 2 2
Lampiran 22. (Lanjutan)
− Ho : µ1 = µ2
H1 : µ1 ≠ µ2
− Dengan menggunakan taraf kepercayaan 99% dengan nilai α = 1 % → t0,01/2 = 3,1693 untuk df = 6+6-2 = 10
− Daerah kritis penerimaan : -3,1693 ≤ to≤ 3,1693
Daerah kritis penolakan : to< -3,1693 dan to> 3,1693
to =
(
)
2 1
2 1
/ 1 / 1
x -x
n n
Sp +
=
(
)
6 1 6 1 0,7346
35,5181
-40,2538 +
= 11,1665
− Karena to = 11,1665 > 3,1693 maka hipotesis ditolak. Berarti terdapat
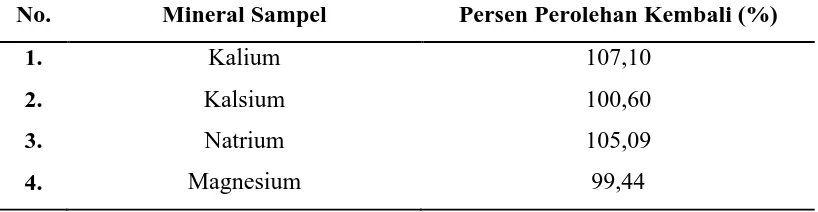
Lampiran 23. Hasil Uji Recovery Kalium, Kalsium, Natrium, dan Magnesium
Setelah Penambahan Masing-masing Larutan Baku dalam Pare Segar
1. Hasil Uji Recovery Kalium Setelah Ditambahkan Larutan Baku Kalium Sampel Berat
Sampel (g) Absorbansi (A) Konsentrasi (µg/ml) Kadar (mg/100g) Persen Perolehan Kembali (%)
1 20,0250 0,3171 7,7845 194,3695 106,33
2 20,0350 0,3172 7,7870 194,3349 106,13
3 20,0500 0,3182 7,8118 194,8080 108,84
∑ 321,30
X 107,10
2. Hasil Uji Recovery Kalsium Setelah Ditambahkan Larutan Baku Kalsium Sampel Berat
Sampel (g) Absorbansi (A) Konsentrasi (µg/ml) Kadar (mg/100g) Persen Perolehan Kembali (%)
1 20,0250 0,3220 9,0213 4,5050 100,94
2 20,0350 0,3228 9,0440 4,5141 102,76
3 20,0500 0,3214 9,0042 4,4909 98,12
∑ 301,82
X 100,60
3. Hasil Uji Recovery Natrium Setelah Ditambahkan Larutan Baku Natrium Sampel Berat
Sampel (g) Absorbansi (A) Konsentrasi (µg/ml) Kadar (mg/100g) Persen Perolehan Kembali (%)
1 20,0250 0,0942 0,7953 3,9715 106,95
2 20,0350 0,0938 0,7919 3,9526 103,16
3 20,0500 0,0941 0,7945 3,9626 105,17
∑ 315,28
X 105,09
4. Hasil Uji Recovery Magnesium Setelah Ditambahkan Larutan Baku Magnesium
Sampel Berat Sampel (g) Absorbansi (A) Konsentrasi (µg/ml) Kadar (mg/100g) Persen Perolehan Kembali (%)
2 20,0350 0,3535 0,9057 45,2059 99,22
3 20,0500 0,3536 0,9059 45,1820 98,74
∑ 298,33
X 99,44
Lampiran 24.Perhitungan Penambahan Larutan Baku Kalium, Kalsium, Natrium,
dan Magnesium dalam Pare Segar 1. Penambahan Larutan Baku Kalium pada Sampel
Kadar Kalium = 175,7960 ± 2,8712 mg/100g = 176 mg/100 g
Penambahan baku 10% dari baku 1000 µg/ml = 176mg
100g × 10g
100ml= 176µg/ml
Volume penambahan baku kalium yang diambil dari larutan baku kalium dengan konsentrasi 1000 µg/ml =
Kadar baku standar = konsentrasi logam yang ditambah
berat sampel rata-rata × volpenambahan baku 176µg/ml =
g ml g 20
Y × / 1000µ
Y =
ml g ml g
/ 1000
20g × / 176
µ µ
= 3,5 ml
2. Penambahan Larutan Baku Kalsium pada Sampel Kadar Kalsium = 4,0012 ± 0,0814 mg/100g
= 4,0 mg/100 g
Penambahan baku 10% dari baku 1000 µg/ml = 4,0 mg
100g × 10g
Lampiran 24.(Lanjutan)
Volume penambahan baku kalsium yang diambil dari larutan baku kalsium dengan konsentrasi 100 µg/ml =
Kadar baku standar = konsentrasi logam yang ditambah
berat sampel rata-rata × volpenambahan baku 4,0 µg/ml =
g ml g 20 Y × / 100µ Y = ml g ml g / 100 20g × / 0 , 4 µ µ
= 1 ml
3. Penambahan Larutan Baku Natrium pada Sampel Kadar Natrium = 3,4377 ± 0,1564 mg/100g
= 3,4 mg/100 g
Penambahan baku 10% dari baku 1000 µg/ml = 3,4 mg
100g × 10g
100ml= 3,4 µg/ml
Volume penambahan baku natrium yang diambil dari larutan baku natrium dengan konsentrasi 100 µg/ml =
Kadar baku standar = konsentrasi logam yang ditambah
berat sampel rata-rata × volpenambahan baku 3,4 µg/ml =
g ml g 20 Y × / 100µ Y = ml g ml g / 100 20g × / 4 , 3 µ µ
Lampiran 24.(Lanjutan)
4. Penambahan Larutan Baku Magnesium pada Sampel Kadar Magnesium = 40,2538 ± 1,3701 mg/100g
= 40,3 mg/100g
Penambahan baku 10% dari baku 1000 µg/ml = 40,3 mg
100g × 10g
100ml= 40,3 µg/ml
Volume penambahan baku magnesium yang diambil dari larutan baku magnesium dengan konsentrasi 1000 µg/ml =
Kadar baku standar = konsentrasi logam yang ditambah
berat sampel rata-rata × volpenambahan baku 40,3 µg/ml =
g ml g 20
Y × / 1000µ
Y =
ml g ml g
/ 1000
20g × / 3 , 40
µ µ
Lampiran 25. Contoh Perhitungan Uji Perolehan Kembali Kalium, Kalsium,
Natrium, dan Magnesium dalam Pare Segar 1. Contoh Perhitungan Uji Perolehan Kembali Kadar Kalium Persamaan regresi: Y= 0,040354X + 0,002962
Absorbansi (Y) = 0,3171 X = 040354 , 0 002962 , 0 3171 , 0 −
= 7,7845 µg/ml
Konsentrasi setelah ditambahkan larutan baku = 7,7845 µg/ml Kadar sampel setelah ditambah larutan baku (CF)
CF = Konsentrasi(µg/ml) x Volume (ml) x Faktor Pengenceran
Berat Sampel (g) = g mlx mlx g 0250 , 20 ) 5 , 0 / 25 ( 100 / 7845 , 7 µ
= 1943,6954 µg/g = 194,3695 mg/100g
Kadar sampel setelah ditambah larutan baku (CF) = 194,3695 mg/100g
Kadar rata-rata sampel sebelum ditambah larutan baku (CA) = 175,7960 mg/100g
Berat sampel rata-rata uji recovery = 20,0367 g Kadar larutan standar yang ditambahkan (C*A)
C*A = Konsentrasi logam yang ditambahkan x ml yang ditambah
Berat sampel rata-rata = g ml g 0367 , 20 / 1000µ
x 3,5 ml = 174,6794 µg/g = 17,4679 mg/100g
Lampiran 25. (Lanjutan)
2. Contoh Perhitungan Uji Perolehan Kembali Kadar Kalsium Persamaan regresi: Y= 0,035171X + 0,004710
Absorbansi (Y) = 0,3220 X = 035171 , 0 004710 , 0 3220 , 0 −
= 9,0213 µg/ml
Konsentrasi setelah ditambahkan larutan baku = 9,0213 µg/ml Kadar sampel setelah ditambah larutan baku (CF)
CF = Konsentrasi(µg/ml) x Volume (ml) x Faktor Pengenceran
Berat Sampel (g) = g mlx mlx g 0250 , 20 ) 100 / 100 ( 100 / 0213 , 9 µ
= 45,0502 µg/g = 4,5050 mg/100g
Kadar sampel setelah ditambah larutan baku (CF) = 4,5050 mg/100g
Kadar rata-rata sampel sebelum ditambah larutan baku (CA) = 4,0012 mg/100g
Berat sampel rata-rata uji recovery = 20,0367 g Kadar larutan standar yang ditambahkan (C*A)
C*A = Konsentrasi logam yang ditambahkan x ml yang ditambah
Berat sampel rata-rata = g ml g 0367 , 20 / 100µ
x 1 ml = 4,9908 µg/g = 0,4991 mg/100g
Lampiran 25. (Lanjutan)
3. Contoh Perhitungan Uji Perolehan Kembali Kadar Natrium Persamaan regresi: Y= 0,116600X + 0,001467
Absorbansi (Y) = 0,0942 X = 01166 , 0 001467 , 0 0942 , 0 −
= 0,7953 µg/ml
Konsentrasi setelah ditambahkan larutan baku = 0,7953 µg/ml Kadar sampel setelah ditambah larutan baku (CF)
CF = Konsentrasi(µg/ml) x Volume (ml) x Faktor Pengenceran
Berat Sampel (g) = g mlx mlx g 0250 , 20 ) 5 , 2 / 25 ( 100 / 7953 , 0 µ
= 39,7153 µg/g = 3,9715 mg/100g
Kadar sampel setelah ditambah larutan baku (CF) = 3,9715 mg/100g
Kadar rata-rata sampel sebelum ditambah larutan baku (CA) = 3,4377 mg/100g
Berat sampel rata-rata uji recovery = 20,0367 g Kadar larutan standar yang ditambahkan (C*A)
C*A = Konsentrasi logam yang ditambahkan x ml yang ditambah
Berat sampel rata-rata = g ml g 0367 , 20 / 100µ
x 1 ml = 4,9908 µg/g = 0,4991 mg/100g
Lampiran 25. (Lanjutan)
4. Contoh Perhitungan Uji Perolehan Kembali Kadar Magnesium Persamaan regresi: Y= 0,386986X + 0,003024
Absorbansi (Y) = 0,3538 X = 386986 , 0 003024 , 0 3538 , 0 −
= 0,9064 µg/ml
Konsentrasi setelah ditambahkan larutan baku = 0,9064 µg/ml Kadar sampel setelah ditambah larutan baku (CF)
CF = Konsentrasi(µg/ml) x Volume (ml) x Faktor Pengenceran
Berat Sampel (g) = g mlx mlx g 0250 , 20 ) 25 , 0 / 25 ( 100 / 9064 , 0 µ
= 452,6342 µg/g = 45,2634 mg/100g
Kadar sampel setelah ditambah larutan baku (CF) = 45,2634 mg/100g
Kadar rata-rata sampel sebelum ditambah larutan baku (CA) = 40,2538 mg/100g
Berat sampel rata-rata uji recovery = 20,0367 g Kadar larutan standar yang ditambahkan (C*A)
C*A = Konsentrasi logam yang ditambahkan x ml yang ditambah
Berat sampel rata-rata = g ml g 0367 , 20 / 1000µ
x 1 ml = 49,9084 µg/g = 4,9910 mg/100g
Lampiran 26. Perhitungan Simpangan Baku Relatif (RSD) Kadar Kalium,
Kalsium, Natrium, dan Magnesium dalam Pare Segar 1. Perhitungan Simpangan Baku Relatif (RSD) Kadar Kalium
No. % Perolehan Kembali (Xi) (%) (Xi-X ) (Xi-X )2
1. 106,33 -0,77 0,5929
2. 106,13 -0,97 0,9409
3. 108,84 1,74 3,0276
∑ 321,30 4,5614
X 107,10
SD =
( )
1 -n
X -Xi 2
∑
=
1 -3 5614 , 4
= 1,51
RSD = X SD
x 100%
= 1 , 107
51 , 1
Lampiran 26. (Lanjutan)
2. Perhitungan Simpangan Baku Relatif (RSD) Kadar Kalsium
No. % Perolehan Kembali (Xi) (%) (Xi-X ) (Xi-X )2
1. 100,94 0,34 0,1156
2. 102,76 2,16 4,6656
3. 98,12 -2,48 6,1504
∑ 301,82 10,9316
X 100,60
SD =
( )
1 -n
X -Xi 2
∑
=
1 -3
9316 , 10
= 2,33
RSD = X SD
x 100%
=
60 , 100
33 , 2
Lampiran 26. (Lanjutan)
3. Perhitungan Simpangan Baku Relatif (RSD) Kadar Natrium
No. % Perolehan Kembali (Xi) (%) (Xi-X ) (Xi-X )2
1. 106,95 1,86 3,4596
2. 103,16 -1,93 3,7249
3. 105,17 0,08 0,0064
∑ 315,28 7,1909
X 105,09
SD =
( )
1 -n
X -Xi 2
∑
=
1 -3 1909 , 7
= 1,89
RSD = X SD
x 100%
=
09 , 105
89 , 1
Lampiran 26. (Lanjutan)
4. Perhitungan Simpangan Baku Relatif (RSD) Kadar Magnesium
No. % Perolehan Kembali (Xi) (%) (Xi-X ) (Xi-X )2
1. 100,37 0,93 0,8649
2. 99,22 -0,22 0,0484
3. 98,74 -0,70 0,4900
∑ 298,33 1,4033
X 99,44
SD =
( )
1 -n
X -Xi 2
∑
=
1 -3 4033 , 1
= 0,84
RSD = X SD
x 100%
= 44 , 99
84 , 0
Lampiran 27. Gambar Alat-Alat yang Digunakan
Gambar 6. Spektrofotometer Serapan Atom (HITACHI Seri Z-2000)
Lampiran 27. (Lanjutan)
Gambar 8. Neraca Analitik (BOECO)
Gambar 9. Purelab UHQ (Elga)
[image:58.595.205.418.387.609.2]Gambar 10. Hot plate (BOECO)
Lampiran 28. Tabel Kandungan Nutrisi Buah Pare /100 g
Air 93,8 %
Energi 20 KJ
Karbohidrat 0,20 g
Serat 3,30 g
Asam organik 0,11 g
Abu 0,60 g
Kalsium 22 mg
Kalium 260 mg
Magnesium 16 mg
Besi 0,9 mg
Natrium 3,0 mg
Seng 0,1 mg
Vitamin A 0,04 mg
Thiamin 0,05 mg
Riboflavin 0,03 mg
Niacin 0,40 mg
Vitamin C 50,00 mg
Protein 0,90 g
Lemak 0,10 g
(Islam, dkk., 2011).
DAFTAR PUSTAKA
Almatsier, S. (2013). Prinsip Dasar Ilmu Gizi. Cetakan Kesembilan. Jakarta: PT. Gramedia Pustaka Utama. Halaman 228-238, 241-243, 247-250.
Anonim. (2014).Flame Atomic Absorption Spectroscopy.Diakses pada tanggal 1 September
Dalimartha, S. (2008). Atlas Tumbuhan Obat Indonesia Jilid 5. Cetakan Pertama. Jakarta: Pustaka Bunda. Halaman 131-132.
Ermer, J. dan McB. Miller, J. H. (2005). Method Validation in Pharmaceutical Analysis. A Guide to Best Practice. Weinheim: Wiley-Vch Verlag GmBH & Co. KGaA. Halaman 171.
Gandjar, I. G. dan Rohman, A. (2007).Kimia Farmasi Analisis. Cetakan Kedua. Yogyakarta: Pustaka Pelajar. Halaman 298-321.
Gemede, H. F. DanRatta, N. (2014). Antinutritional Factors in Plant Foods: Potential Health Benefits and Adverse Effects. International Journal of Nutrition and Food Sciences. 3(4): 284-289.
Harmita. (2004). Petunjuk Pelaksanaan Validasi Metode dan Cara Perhitungannya. Review Artikel Majalah Ilmu Kefarmasian. 1(3): 117-135. Isaac, R.A. (1988). Metal in Plants: Atomic Absorption Spectrophotometric
Method. Disunting Oleh: Helrich, K. (1990). Official Method of Analysis of the Association of Official of Chemist. Edisi Kelima belas. Virginia: AOAC Internasional. Halaman 42.
Islam, S., Mohammad, J., dan Navam, S.H. (2011). Bio-Active Compounds of Bitter Melon Genotypes (Momordica charantia L.) in Relation to Their Physiological Functions. Functional Foods in Heals and Disease. 2(1): 61-74.
Khomsan, A. (2009). Rahasia Sehat dengan Makanan Berkhasiat.Jakarta: PT Kompas Media Nusantara. Halaman 128, 132-135.
Khopkar, S. M. (1985). Basic Concepts of Analytical Chemistry. Penerjemah: A. Saptorahajo (1990). Konsep Dasar Kimia Analitik. Jakarta: UI Press. Halaman 275.
Koplik, R. (2014). Atomic Spectrometry. Diunduh dari http://web.vscht. cz/~poustkaj/en%20asfa%20au%20koplik%20atomic%20spectrometry.pdf.
Rizki, F. (2013). The Miracle of Vegetables.Jakarta: PT Agro Media Pustaka. Halaman 153.
Rohman, A., Harsojo, Raharjo, T. J., Sismindari, Triyana, K., dan Astuti, P. (2012). Analisis Makanan Dan Lingkungan Secara Fisika-Kimia. Cetakan Pertama. Yogyakarta: Pustaka Pelajar. Halaman 14-15.
Saparinto, C. (2013). Grow Your Own Vegetables. Panduan Praktis Menanam 14 Sayuran Konsumsi Populer di Pekarangan. Yogyakarta: Lily Publisher. Halaman 126.
Sudjana. (2005). Metode Statistika. Edisi Keenam. Bandung: Tarsito. Halaman 168-254.
Syamsuhidayat, S.S dan Hutapea, J.R. (1991). Inventaris Tanaman Obat Indonesia. Jakarta: Departemen Kesehatan RI. Halaman 388.
United States Department of Agriculture. (2015). Bitter Melon. Diunduh
dari
BAB III
METODE PENELITIAN
3.1 Tempat dan Waktu Penelitian
Penelitian ini dilakukan di Laboratorium Penelitian Fakultas Farmasi Universitas Sumatera Utara pada bulan Maret 2015 – Juni 2015.
3.2 Bahan-Bahan
3.2.1 Sampel
Sampel yang digunakan dalam penelitian ini adalah buah pare putih yang berasal dari Pasar Pancurbatu, Kabupaten Deli Serdang, Sumatera Utara. Gambar dapat dilihat pada Lampiran 1 halaman 39.
3.2.2 Pereaksi
Bahan-bahan yang digunakan dalam penelitian ini berkualitas pro analisa keluaran E. Merck yaitu asam nitrat 65% b/v, larutan baku kalium nitrat 1000 µg/ml, larutan baku kalsium nitrat 1000 µg/ml, larutan baku natrium nitrat 1000 µg/ml dan larutan baku magnesium nitrat 1000 µg/ml kecuali akua demineralisata.
3.3 Alat-Alat
Alat-alat yang digunakan dalam penelitian ini adalah spektrofotometer serapan atom (Hitachi Zeeman-2000) dengan nyala udara-asetilen lengkap dengan lampu katoda K, Ca, Na, dan Mg, neraca analitik (BOECO), tanur (Stuart), hot plate (BOECO), purelab UHQ (Elga), kertas saring Whatman no. 42, krus
3.4 Pembuatan Pereaksi
3.4.1 Larutan HNO3 (1:1)
Larutan HNO3 65% b/v sebanyak 500 ml diencerkan dengan 500 ml akua
demineralisata (Isaac, 1988).
3.5 Prosedur Penelitian
3.5.1 Pengambilan Sampel
Metode pengambilan sampel secara purposif ini ditentukan atas dasar pertimbangan bahwa sampel yang tidak terambil mempunyai karakteristik yang sama dengan sampel yang diteliti dan dianggap sebagai sampel yang representatif (Sudjana, 2005).
3.5.2 Penyiapan Sampel
Pare dicuci bersih, dibilas dengan akua demineralisata, dicabut tangkainya dan buah pare yang segardibagi menjadi dua bagian, masing-masing ± 500 g, dipotong tipis-tipis lalu dibuang bijinya. Bagian pertama dipotong kecil-kecildan bagian keduadirebus dengan menggunakan air mendidih 500 ml pada suhu 95oCselama 15 menit lalu ditiriskan dan dipotong kecil-kecil.
3.5.3 Proses Destruksi Kering
dingin lalu dipindahkan kedesikator.Bagan alir proses destruksi kering dapat dilihat pada Lampiran 3 halaman 42.
3.5.4 Pembuatan Larutan Sampel
Abu hasil destruksi yang telah dingin dilarutkan dengan 5 ml HNO3 (1:1)
lalu dipindahkan ke dalam labu tentukur 100 ml dan krus porselen dibilas sebanyak 3 kali dengan akua demineralisata. Hasil pembilasan dimasukkan ke dalam labu tentukur, kemudian larutan dicukupkan volumenya dengan akua demineralisata hingga garis tanda dan disaring dengan kertas saring Whatman No. 42, filtrat pertama dibuang sebanyak 5 ml untuk menjenuhkan kertas saring kemudian filtrat selanjutnya ditampung dalam botol. Filtrat ini digunakan sebagai larutan sampel untuk analisa kuantitatif logam kalium, kalsium, natrium, dan magnesium. Perlakuan yang sama diulang sebanyak enam kali untuk masing-masing sampel. Bagan alir proses pembuatan larutan sampel dapat dilihat pada Lampiran4halaman 44.
3.5.5Analisa Kuantitatif
3.5.5.1 Pembuatan Kurva Kalibrasi Kalium
Larutan baku kalium (1000 µg/ml) dipipet sebanyak 5 ml, dimasukkan ke dalam labu tentukur 100 ml dan dicukupkan hingga garis tanda dengan akua demineralisata (konsentrasi 50 µg/ml).
3.5.5.2 Pembuatan Kurva Kalibrasi Kalsium
Larutan baku kalsium (1000 µg/ml) dipipet sebanyak 5 ml, dimasukkan ke dalam labu tentukur 100 ml dan dicukupkan hingga garis tanda dengan akua demineralisata (konsentrasi 50 µg/ml).
Larutan untuk kurva kalibrasi kalsium dibuat dengan memipet (2; 4; 6; 8; dan 10) ml larutan baku 50 µg/ml, masing-masing dimasukkan ke dalam labu tentukur 50 ml dan dicukupkan hingga garis tanda dengan akua demineralisata(larutan ini mengandung (2; 4; 6; 8; dan 10) µg/ml) dan diukur pada panjang gelombang 422,7 nm dengan nyala udara-asetilen.
3.5.5.3 Pembuatan Kurva Kalibrasi Natrium
Larutan baku natrium (1000 µg/ml) dipipet sebanyak 1 ml, dimasukkan ke dalam labu tentukur 100 ml dan dicukupkan hingga garis tanda dengan akua demineralisata (konsentrasi 10 µg/ml).
Larutan untuk kurva kalibrasi natrium dibuat dengan memipet (1; 2; 3; 4; dan 5) ml larutan baku 10 µg/ml, masing-masing dimasukkan ke dalam labu tentukur 50 ml dan dicukupkan hingga garis tanda dengan akua demineralisata (larutan ini mengandung (0,2; 0,4; 0,6; 0,8; dan 1,0) µg/ml) dan diukur absorbansinya pada panjang gelombang 589,0 nm dengan nyala udara-asetilen.
3.5.5.4 Pembuatan Kurva Kalibrasi Magnesium
Larutan baku magnesium (1000 µg/ml) dipipet sebanyak 1 ml, dimasukkan ke dalam labu tentukur 100 ml dan dicukupkan hingga garis tanda dengan akua demineralisata (konsentrasi 10 µg/ml).
tentukur 50 ml dan dicukupkan hingga garis tanda dengan akua demineralisata (larutan ini mengandung (0,2; 0,4; 0,6; 0,8; dan 1,0) µg/ml) dan diukur absorbansinya pada panjang gelombang 285,2 nm dengan nyala udara-asetilen.
3.5.6 Penetapan Kadar Mineral dalam Sampel
3.5.6.1 Penetapan Kadar Kalium
Larutan sampel pare segar hasil destruksi sebanyak 0,5 ml dimasukkan ke dalam labu tentukur 25 ml dan dicukupkan dengan akua demineralisata hingga garis tanda.
Larutan sampel parerebus hasil destruksi sebanyak 0,5 ml dimasukkan ke dalam labu tentukur 25 ml dan dicukupkan dengan akua demineralisata hingga garis tanda.
Diukur absorbansinya dengan menggunakan spektrofotometer serapan atom pada panjang gelombang 766,5 nm dengan nyala udara-asetilen. Nilai absorbansi yang diperoleh harus berada dalam rentang kurva kalibrasi larutan baku kalium. Konsentrasi kalium dalam sampel ditentukan berdasarkan persamaan garis regresi dari kurva kalibrasi.
3.5.6.2 Penetapan Kadar Kalsium
Larutan sampel pare segar dari larutan induk baku hasil destruksi dan larutan sampel parerebus dari larutan induk baku hasil destruksi.
3.5.6.3 Penetapan Kadar Natrium
Larutan sampel pare segar hasil destruksi sebanyak 2,5 ml dimasukkan ke dalam labu tentukur 25ml dan dicukupkan dengan akua demineralisata hingga garis tanda.
Larutan sampel parerebus hasil destruksi sebanyak 2,5 ml dimasukkan ke dalam labu tentukur 25ml dan dicukupkan dengan akua demineralisata hingga garis tanda.
Diukur absorbansinya dengan menggunakan spektrofotometer serapan atom pada panjang gelombang 589,0 nm dengan nyala udara-asetilen. Nilai absorbansi yang diperoleh harus berada dalam rentang kurva kalibrasi larutan baku natrium. Konsentrasi natrium dalam sampel ditentukan berdasarkan persamaan garis regresi dari kurva kalibrasi.
3.5.6.4 Penetapan Kadar Magnesium
Larutan sampel pare segar hasil destruksi sebanyak 0,25 ml dimasukkan ke dalam labu tentukur 25ml dan dicukupkan dengan akua demineralisata hingga garis tanda.
Larutan sampel parerebus hasil destruksi sebanyak 0,25 ml dimasukkan ke dalam labu tentukur 25ml dan dicukupkan dengan akua demineralisata hingga garis tanda.
3.5.6.5 Perhitungan Kadar Mineral dalam Sampel
Kadar kalium, kalsium, magnesium dan natrium dalam sampel dapat dihitung dengan cara berikut:
Kadar logam(µg/g) = Konsentrasi(µg/ml) x Volume (ml) x Faktor Pengenceran Berat Sampel (g)
3.5.7 Analisa Data Secara Statistik
3.5.7.1 Penolakan Hasil Pengamatan
Kadar kalium, kalsium, natrium, dan magnesium yang diperoleh dari hasil pengukuran masing-masing larutan sampel dianalisis secara statistik. Menurut Sudjana (2005), standar deviasi dapat dihitung dengan menggunakan rumus:
SD =
( )
1 -n
X
-Xi 2
∑
Keterangan: Xi = Kadar sampel
X = Kadar rata-rata sampel n = Jumlah perlakuan Untuk mencari t hitung digunakan rumus:
t hitung =
n SD
X Xi
/
−
dan untuk menentukan kadar mineral di dalam sampel dengan interval kepercayaan 99%, dengan nilai α = 0.01, dk= n-1, dapat digunakan rumus:
µ = X± t (α/2, dk) x SD / √n
Keterangan: SD = standar deviasi µ = interval kepercayaan
X = kadar rata-rata sampel
t = harga t tabel sesuai dengan dk= n – 1 n = jumlah pengulangan
� = tingkat kepercayaan
3.5.7.2 Pengujian Beda Nilai Rata-Rata Antar Sampel
Menurut Sudjana (2005), sampel yang dibandingkan adalah independen dan jumlah pengamatan masing-masing lebih kecil dari 30 dan variansi (�) tidak diketahui sehingga dilakukan uji F untuk mengetahui apakah variansi kedua populasi sama (�1 = �2) atau berbeda (�1≠�2) dengan menggunakan rumus:
Fo=
2 2
2 1 S
S
Keterangan: Fo = Beda nilai yang dihitung
S1 = Standar deviasi sampel 1
[image:72.595.160.394.422.561.2]S2 = Standar deviasi sampel 2
Tabel distribusi F dapat dilihat pada Lampiran 29 halaman 85
Apabila dari hasilnya diperoleh Fo tidak melewati nilai kritis F, maka dilanjutkan
uji dengan distribusi t dengan rumus:
to =
(
)
2 1
2 1
/ 1 / 1
X -X
n n
Sp +
Keterangan: X1 = kadar rata-rata sampel 1 2
X = kadar rata-rata sampel 2 Sp = simpangan baku
n1 = jumlah perlakuan sampel 1
n2 = jumlah perlakuan sampel 2
Kedua sampel dinyatakan berbeda apabila to yang diperoleh melewati nilai
kritis t dan sebaliknya jika Fo melewati nilai kritis F, maka dilanjutkan uji dengan
distribusi t dengan rumus :
to =
(
)
2 2 2 1 2 1
2 1
/ /
X -X
n S n
Keterangan: X1 = kadar rata-rata sampel 1 1
X = kadar rata-rata sampel 2 S1 = Standar deviasi sampel 1
S2 = Standar deviasi sampel 2
n1 = jumlah perlakuan sampel 1
n2 = jumlah perlakuan sampel 2
Kedua sampel dinyatakan berbeda apabila to yang diperoleh melewati nilai
kritis t, dan sebaliknya.
3.5.8 Uji Perolehan Kembali (Recovery)
Uji perolehan kembali atau recovery dilakukan dengan metode penambahan larutan standar (Standard addition method). Dalam metode ini, kadar mineral dalam sampel ditentukan terlebih dahulu, selanjutnya dilakukan penentuan kadar mineral dalam sampel setelah penambahan larutan baku dengan konsentrasi tertentu. Larutan baku yang ditambahkan yaitu, 3,5 ml larutan baku kalium (konsentrasi 1000 µg/ml), 1 ml larutan baku kalsium (konsentrasi 100µg/ml), 1 ml larutan baku natrium (konsentrasi 100 µg/ml) dan1 ml larutan baku magnesium (konsentrasi 1000 µg/ml).
Menurut Harmita (2004), persen perolehan kembali dapat dihitung dengan rumus berikut:
% Perolehan Kembali = CF- CA
C*A x 100% Keterangan:
CA = kadar logam dalam sampel sebelum penambahan baku
CF = kadar logam dalam sampel setelah penambahan baku
C*A = kadar larutan baku yang ditambahkan
3.5.9 Simpangan Baku Relatif
Keseksamaan atau presisi diukur sebagai simpangan baku relatif atau koefisien variasi. Keseksamaan atau presisi merupakan ukuran yang menunjukkan derajat kesesuaian antara hasil individual ketika suatu metode dilakukan secara berulang untuk sampel yang homogen. Nilai simpangan baku relatif yang memenuhi persyaratan menunjukkan adanya keseksamaan metode yang dilakukan (Harmita, 2004).
Menurut Harmita (2004), rumus untuk menghitung simpangan baku relatif adalah sebagai berikut:
RSD = X SD
x 100% Keterangan:
X = Kadar rata-rata sampel SD = Standar Deviasi
3.5.10 Penentuan Batas Deteksi (Limit of Detection) dan Batas Kuantitasi
(Limit of Quantitation)
Batas deteksi adalah jumlah terkecil analit dalam sampel yang dapat dideteksi yang masih memberikan respon signifikan. Batas kuantitasi merupakan kuantitas terkecil analit dalam sampel yang masih dapat memenuhi kriteris cermat dan seksama (Harmita, 2004).
Menurut Harmita (2004), batas deteksi dan batas kuantitasi ini dapat dihitung dengan rumus sebagai berikut:
Simpangan Baku Residual
( )
2 -n
Y -Yi )
/ (
2
∑
=
x Sy
Batas Deteksi (LOD) =
Slope x Sy x( / ) 3
Batas Kuantitasi (LOQ) =
BAB IV
HASIL DAN PEMBAHASAN
4.1 Identifikasi Sampel
Hasil identifikasi sampel yang dilakukan oleh bagian Herbarium Bogoriense Bidang Botani Pusat Penelitian LIPI Bogor terhadap tumbuhan pare adalah jenis Momordica charantia L. suku Cucurbitaceae. Hasil identifikasi sampel dapat dilihat pada Lampiran 2 halaman 41.
4.2 Analisa Kuantitatif
4.2.1 Kurva Kalibrasi Kalium, Kalsium, Natrium, dan Magnesium
Kurva kalibrasi dalam spektrofotometri serapan atom dibuat dalam berbagai konsentrasi dengan konsentrasi yang meningkat. Dari pengukuran kurva kalibrasi diperoleh persamaan garis regresi yaitu Y= 0,040354X + 0,002962 untuk kalium, Y= 0,035171X + 0,004710 untuk kalsium, Y= 0,116600X + 0,001467 untuk natrium, dan Y= 0,386986X + 0,003024 untuk magnesium.
Gambar 4.1 Kurva Kalibrasi Larutan Baku Kalium
[image:77.595.155.422.536.704.2]Gambar 4.2 Kurva Kalibrasi Larutan Baku Kalsium
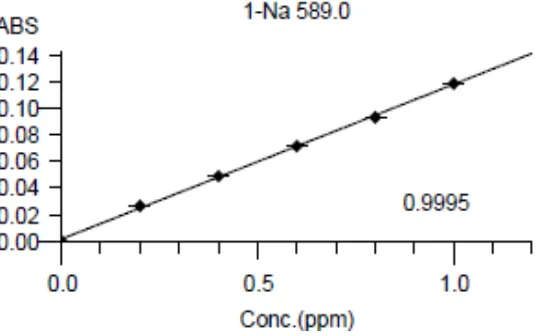
Gambar 4.3 Kurva Kalibrasi Larutan Baku Natrium
Berdasarkan kurva di atas diperoleh hubungan yang linier antara konsentrasi dengan absorbansi, dengan koefisien korelasi (r) kalium sebesar 0,9996, kalsium sebesar 0,9995, natrium sebesar 0,9995, dan magnesium sebesar 0,9997. Nilai r≥0,97 menunjukkan adanya korelasi linier yang menyatakan adanya hubungan antara X (Konsentrasi) dan Y (Absorbansi) (Ermer dan McB. Miller, 2005). Data hasil pengukuran absorbansi larutan baku kalium, kalsium, natrium, dan magnesium dan perhitungan persamaan garis regresi dapat dilihat pada Lampiran 5 sampai dengan Lampiran 8, halaman 45 sampai dengan halaman 48.
4.2.2 Analisis Kadar Kalium, Kalsium, Natrium, dan Magnesium pada Pare
Segar dan Pare Rebus
Penentuan kadar kalium, kalsium, natrium, dan magnesium dilakukan secara spektrofotometri serapan atom. Konsentrasi mineral kalium, kalsium, natrium, dan magnesium dalam sampel ditentukan berdasarkan persamaan regresi kurva kalibrasi larutan baku masing-masing mineral. Agar konsentrasi mineral kalium, kalsium, natrium, dan magne