SKRIPSI
PRODUKSI BAHAN BAKU SPREADS KAYA β-KAROTEN BERBASIS MINYAK SAWIT MERAH MELALUI INTERESTERIFIKASI
ENZIMATIK MENGGUNAKAN REAKTOR BATCH
Oleh :
MARIO WIBOWO F24060850
2010
FAKULTAS TEKNOLOGI PERTANIAN INSTITUT PERTANIAN BOGOR
PRODUKSI BAHAN BAKU SPREADS KAYA β-KAROTEN BERBASIS MINYAK SAWIT MERAH MELALUI INTERESTERIFIKASI
ENZIMATIK MENGGUNAKAN REAKTOR BATCH
Oleh :
MARIO WIBOWO F24060850
SKRIPSI
Sebagai salah satu syarat untuk memperoleh gelar
SARJANA TEKNOLOGI PERTANIAN
pada Departemen Ilmu dan Teknologi Pangan Fakultas Teknologi Pertanian
Institut Pertanian Bogor
2010
FAKULTAS TEKNOLOGI PERTANIAN INSTITUT PERTANIAN BOGOR
Judul Skripsi : Produksi Bahan Baku Spreads Kaya β-karoten Berbasis Minyak Sawit Merah Melalui Interesterifikasi Enzimatik Menggunakan Reaktor Batch
Nama : Mario Wibowo
NRP : F24060850
Menyetujui:
Mengetahui:
Ketua Departemen Ilmu dan Teknologi Pangan,
(Dr. Ir. Dahrul Syah) NIP: 19650814 199022 1 001
Tanggal Lulus:
Pembimbing I,
(Dr. Ir. Sugiyono, M.App.Sc.) NIP. 19650729 199002 1 002
Pembimbing II,
RIWAYAT HIDUP
Penulis dilahirkan di Jakarta pada tanggal 18 Maret 1989. Penulis adalah anak keempat dari empat bersaudara, pasangan Ng Pak Lim dan Tan Gan May. Penulis menyelesaikan pendidikan dasar pada tahun 2000 di SD Suci Hati, Jakarta kemudian melanjutkan pendidikan menengah pertama di SLTP Kristen Ketapang I, Jakarta hingga tahun 2003. Penulis menamatkan pendidikan menengah atas di SMA Negeri 2 Jakarta pada tahun 2006. Penulis melanjutkan pendidikan tinggi di Institut Pertanian Bogor (IPB) pada Departemen Ilmu dan Teknologi Pangan, Fakultas Teknologi Pertanian melalui jalur USMI (Undangan Seleksi Masuk IPB) pada tahun 2006.
Mario Wibowo. F24060850. Produksi Bahan Baku Spreads Kaya β-Karoten Berbasis Minyak Sawit Merah Melalui Interesterifikasi Enzimatik Menggunakan Reaktor Batch. Di bawah bimbingan: Sugiyono dan Soenar Soekopitojo. 2010.
RINGKASAN
Kelapa sawit merupakan salah satu komoditas hasil perkebunan utama Indonesia. Berbagai bahan pangan dapat diolah menggunakan minyak kelapa sawit sebagai bahan baku. Selain itu minyak sawit adalah salah satu sumber karotenoid terbesar, hanya saja pada kebanyakan bahan pangan olahan sawit kandungan karoten sudah banyak hilang akibat proses produksi. Salah satu produk turunan minyak kelapa sawit adalah produk spreads. Minyak sawit merah dapat digunakan untuk membuat bahan baku spreads kaya β-karoten. Untuk mencapai karakteristik bahan baku spreads yang diinginkan, maka ditambahkan minyak kelapa. Minyak kelapa mengandung banyak asam laurat.
Penelitian ini merupakan aplikasi penggunaan reaktor batch dalam produksi bahan baku spreads melalui proses interesterifikasi enzimatik untuk mempermudah proses scalling up di industri pangan. Bahan baku spreads dibuat melalui reaksi interesterifikasi enzimatik menggunakan 10% Novozyme 435 (lipase Candida antartica). Penggunaan reaksi interesterifikasi enzimatik ini memungkinkan reaksi berjalan pada suhu yang tidak terlalu tinggi sehingga kandungan karoten dalam minyak sawit merah dapat dipertahankan. Penelitian ini bertujuan untuk mempelajari pengaruh penggunaan reaktor batch pada beberapa lama reaksi terhadap karakteristik bahan baku spreads berbasis minyak sawit merah yang meliputi total karoten, slip melting point (SMP), solid fat content
(SFC), kadar air, dan kadar asam lemak bebas.
Berdasarkan hasil penelitian, diketahui bahwa campuran minyak sawit merah dan minyak kelapa dengan formula red palm stearin/red palm olein (1:1) dan minyak kelapa dengan perbandingan 77,5:22,5 dan 82,5:17,5 yang diinteresterifikasi selama 2,4, dan 6 jam pada suhu 60oC dan kecepatan agitasi 200 rpm dapat menghasilkan bahan baku spreads yang memiliki nilai SMP dan profil SFC yang mendekati profil margarin komersial. Nilai SMP dan SFC menurun sesudah interesterifikasi enzimatik, akan tetapi meningkat dengan peningkatan lama reaksi. Nilai SMP bahan baku spreads yang dihasilkan dalam penelitian ini adalah 30,8-34,9oC. Total karoten, kadar air dan kadar asam lemak bebas juga meningkat sesudah interesterifikasi enzimatik. Retensi karoten setelah interesterifikasi enzimatik berkisar antara 74,80-81,08%. Selain itu bahan baku
Mario Wibowo. F24060850. Production of Red Palm Oil Based Spread Base Rich in Carotene through Enzymatic Interesterification in Batch-type Reactor. Supervised by Sugiyono and Soenar Soekopitojo. 2010.
ABSTRACT
Interesterification of red palm oil (red palm olein/RPO and red palm stearin/RPS) and coconut oil (CNO) blends of varying proportions using a non-specific immobilized Candida antartica lipase (Novozyme 435) was studied for the production of spread base. The interesterification reaction was held in a batch-type reactor. Two substrate blends were chosen for the production of spread base: 77,5:22,5 and 82,5:17,5 (RPO/RPS:CNO, by weight) through enzymatic interesterification in three different reaction times (2, 4, and 6 hours). RPO/RPS ratio was 1:1. Interesterification reactions were studied at 60oC at constant weight ratio (10%) of Novozyme 435. The reaction was carried out at steady agitation (200 rpm). The interesterified blends were evaluated for their physical characteristics (solid fat content/SFC and slip melting point/SMP) and chemical characteristics (moisture content, free fatty acid/FFA content and carotene retention). The results showed that all of the interesterified mixtures have a lower SFC and SMP values compared with the initial mixtures. SMP values and SFC increased in a longer reaction. SMP values were ranging from 30,8oC to 34,9oC. The moisture content and FFA content increased in a longer reaction. Carotene retentions were ranging from 74,80% to 81,08%. This study indicated that interesterified products have desirable physical properties for possible use as spread base rich in carotene.
i
KATA PENGANTAR
Puji dan syukur yang tak terhingga penulis ucapkan kepada Tuhan Yesus Kristus, Tuhan yang luar biasa yang telah memberikan berkat pertolongan, kesempatan dan karunia sehingga penulis dapat menyelesaikan skripsi ini. Skripsi ini disusun sebagai salah satu syarat untuk memperoleh gelar Sarjana Teknologi Pertanian pada Departemen Ilmu dan Teknologi Pangan, Fakultas Teknologi Pertanian, Institut Pertanian Bogor.
Penulisan skripsi yang berjudul “PRODUKSI BAHAN BAKU SPREADS
KAYA β-KAROTEN BERBASIS MINYAK SAWIT MERAH MELALUI
INTERESTERIFIKASI MENGGUNAKAN REAKTOR BATCH” ini didasarkan pada penelitian yang telah dilaksanakan sejak Oktober 2009 sampai Mei 2010 di Laboratorium SEAFAST Center IPB dan Laboratorium Departemen Ilmu dan Teknologi Pangan IPB.
Penghargaan dan ucapan terima kasih penulis sampaikan kepada:
1. Orang tua penulis, Papa dan Mama (the world’s #1 parents) atas cinta kasih, doa, nasihat, dan dukungan yang tiada berhenti kepada penulis. Thank you.
2. Dr.Ir. Sugiyono, M.App.Sc. selaku dosen pembimbing pertama atas waktu, arahan, kesabaran, dan masukan yang diberikan selama penulis menjadi mahasiswa ITP.
3. Ir. Soenar Soekopitojo, M.Si. selaku dosen pembimbing kedua yang dengan senang hati selalu menyempatkan diri mendengarkan masalah yang penulis hadapi dan atas semua masukan, nasihat, dan arahan yang diberikan.
4. Nur Wulandari, S.TP., M.Si. atas kesediannya menjadi dosen penguji dan atas masuka yang diberikan.
5. Kementerian Pendidikan Nasional yang telah membiayai penelitian ini melalui Hibah Kompetitif Strategis Nasional.
6. Saudara-saudara penulis: Titin, Yanuar, dan Marisa atas motivasi, dan nasihat yang diberikan.
ii 8. Teman seperjuangan penulis: Taufik dan Pales atas kerja sama, kebersamaan dan bantuan yang diberikan selama melakukan penelitian. Without you guys, it’s kind of difficult to finish this research.
9. Teman-teman satu Lab: Adit, Dzikri, Kak Ayusta, Victor, dan Winnie.
10. Seluruh staf dan laboran SEAFAST Center, especially for Mba Ria, Abah, Kak Arif, Mas Marto, Mba Desty dan Mba Dilla untuk bantuan yang sudah diberikan selama penulis melaksanakan penelitian.
11. Laboran Lab ITP dan LJA, terutama Mba Yane untuk kesediaannya membantu penulis dalam menggunakan NMR, Ibu Antin untuk peminjaman loker, dan Pak Rojak.
12. Teman-teman perwira: Richie, Syenny, Stefanus, Feli, Stephanie GH, Stephanie, Daisy, Nina, Stella, Federika, Nina, Prima, Jessica, Erin, Yurin, Feri, Peni, Margaret, Dyas dan Andrew.
13. Mas Iman, Mba Yuli, dan Pak Ade untuk bantuan yang diberikan. 14. Teman-teman ITP 43 untuk bantuan dan support yang diberikan.
15. Kakak-kakak 42: Kak Dina untuk pinjaman buku dan bahan kuliah, Kak Marcel thanks sudah mencarikan jurnal, Kak Esther untuk bantuannya, Kak Irene untuk jadi kakak kelas bersama yang luar biasa baiknya.
16. Semua pihak yang telah membantu penulis dalam menyelesaikan skripsi ini.
Thanks to all the persons that I couldn’t mention.
Penulis sangat mengharapkan saran dari berbagai pihak untuk memperbaiki dan menyempurnakan penulisan skripsi ini. Penulis juga berharap semoga skripsi ini dapat berguna dan bermanfaat bagi semua yang membaca.
Bogor, Juli 2010
iii
DAFTAR ISI
Halaman
KATA PENGANTAR ... i
DAFTAR ISI ... iii
DAFTAR TABEL ... v
DAFTAR GAMBAR ... vii
DAFTAR LAMPIRAN ... viii
I. PENDAHULUAN ... 1
A. LATAR BELAKANG ... 1
B. TUJUAN PENELITIAN... 3
C. MANFAAT PENELITIAN ... 3
II. TINJAUAN PUSTAKA ... 4
A. MINYAK KELAPA SAWIT ... 4
B. MINYAK SAWIT MERAH ... 5
C. KAROTENOID ... 6
D. MINYAK KELAPA ... 8
E. INTERESTERIFIKASI ENZIMATIK ... 10
F. ENZIM LIPASE ... 12
G. SPREADS ... 14
H. REAKTOR BATCH... 15
III. BAHAN DAN METODE ... 17
A. BAHAN DAN ALAT ... 17
B. METODE PENELITIAN ... 17
1. Penelitian Tahap Pertama: Karakterisasi Bahan Baku ... 17
2. Penelitian Tahap Kedua: Pemilihan Formula Bahan Baku ... 18
3. Penelitian Tahap Ketiga: Interesterifikasi Enzimatik Menggunakan Reaktor Batch... 20
C. METODE ANALISIS ... 22
1. Total Karoten ... 22
2. Slip Melting Point (SMP) ... 23
3. Solid Fat Content (SFC) ... 23
iv
5. Kadar Asam Lemak Bebas ... 24
6. Analisis Data ... 25
IV. HASIL DAN PEMBAHASAN ... 26
A. Penelitian Tahap Pertama: Karakterisasi Bahan Baku ... 26
1. Total Karoten ... 26
2. Slip Melting Point (SMP) dan Solid Fat Content (SFC) ... 28
3. Kadar Air dan Kadar Asam Lemak Bebas (ALB) ... 29
B. Penelitian Tahap Kedua : Pemilihan Formula Bahan baku ... 30
1. Total Karoten ... 31
2. Slip Melting Point (SMP) dan Solid Fat Content (SFC) ... 32
C. Penelitian Tahap Ketiga: Interesterifikasi Enzimatik Menggunakan Reaktor Batch ... 37
1. Total karoten ... 37
2. Slip Melting Point (SMP) dan Solid Fat Content (SFC) ... 40
3. Kadar Air dan Kadar Asam Lemak Bebas (ALB) ... 44
V. KESIMPULAN DAN SARAN ... 48
A. KESIMPULAN ... 48
B. SARAN ... 49
DAFTAR PUSTAKA ... 50
v
DAFTAR TABEL
Halaman
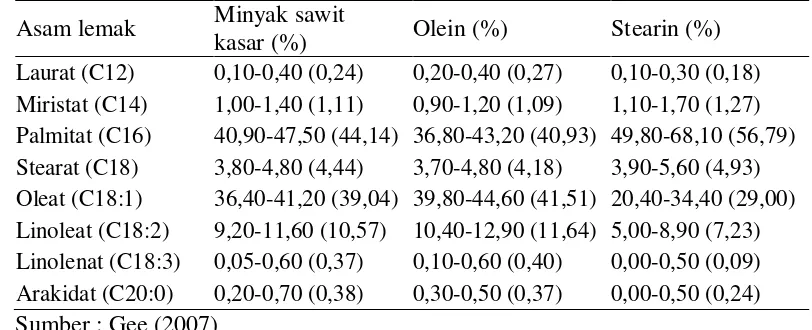
Tabel 1. Komposisi asam lemak minyak sawit ... 5
Tabel 2. Komposisi triasilgliserol pada minyak sawit ... 5
Tabel 3. Karakteristik olein minyak sawit merah ... 6
Tabel 4. Sifat fisikokimia minyak kelapa ... 8
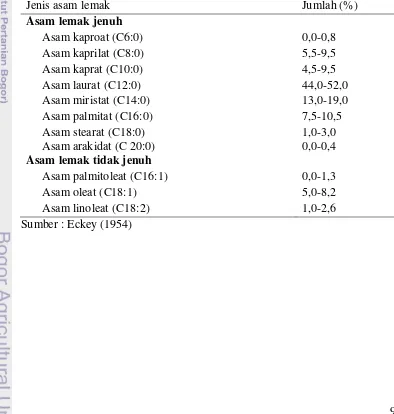
Tabel 5. Komposisi asam lemak minyak kelapa ... 9
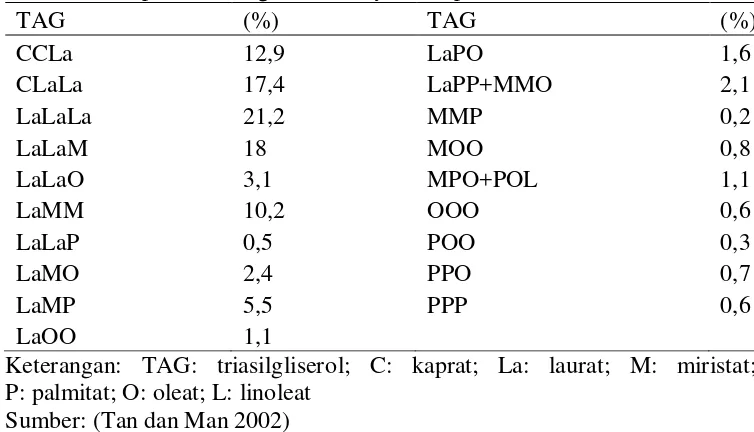
Tabel 6. Komposisi triasilgliserol minyak kelapa ... 10
Tabel 7. Kandungan karoten bahan baku... 26
Tabel 8. Kandungan karoten bahan baku yang telah diformulasi ... 27
Tabel 9. Kandungan karoten hasil penelitian Widarta (2008), Hasrini (2008), dan Riyadi (2009) ... 27
Tabel 10. Nilai SFC dan SMP formula bahan baku ... 28
Tabel 11. Nilai SFC dan SMP bahan baku pada penelitian Hasrini (2008) ... 29
Tabel 12. Kadar air dan kadar ALB bahan baku ... 30
Tabel 13. Kadar air dan kadar asam lemak bebas bahan baku penelitian Widarta (2008), Hasrini (2008), dan Riyadi (2009) ... 30
Tabel 14. Perbandingan total karoten sebelum dan sesudah interesterifikasi enzimatik (IE) penelitian tahap kedua ... 32
Tabel 15. Perbandingan total karoten sebelum dan sesudah interesterifikasi enzimatik (IE) hasil penelitian Hasrini (2008) ... 32
Tabel 16. Perbandingan SMP sebelum dan sesudah interesterifikasi enzimatik (IE) penelitian tahap kedua dibandingkan dengan SMP margarin komersial dan margarin target (Fattahi-far et al., 2006) ... 34
Tabel 17. Perbandingan SMP sebelum dan sesudah interesterifikasi enzimatik (IE) penelitian Hasrini (2008) ... 34
Tabel 18. Total karoten campuran sebelum dan sesudah interesterifikasi enzimatik (IE) menggunakan reaktor batch ... 38
vi
Tabel 20. Perbandingan SMP sebelum dan sesudah interesterifikasi enzimatik (IE) menggunakan reaktor batch dibandingkan dengan SMP margarin komersial dan margarin target (Fattahi-far et al. 2006) ... 40
Tabel 21. Kadar air sampel sebelum dan sesudah interesterifikasi enzimatik (IE) menggunakan reaktor batch ... 45
Tabel 22. Kadar ALB sampel sebelum dan sesudah interesterifikasi enzimatik (IE) menggunakan reaktor batch ... 45
vii
DAFTAR GAMBAR
Halaman
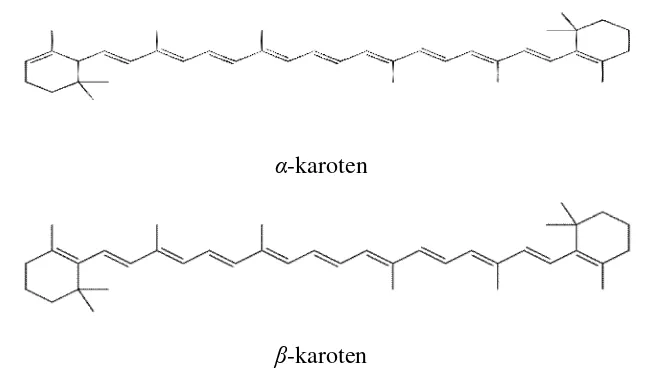
Gambar 1. Struktur α-karoten dan β-karoten (Fennema 1996) ... 7
Gambar 2. Prinsip reaksi interesterifikasi (Huyghebaert et al. 1994) ... 12
Gambar 3. Desain reaktor batch (Nurcahyo 2001) ... 16
Gambar 4. Diagram proses fraksinasi (modifikasi Aini et al. 2005) ... 18
Gambar 5. Prosedur interesterifikasi enzimatik ... 20
Gambar 6. Diagram alir prosedur interesterifikasi enzimatik mengunakan reaktor batch ... 21
Gambar 7. Rangkaian reaktor batch, dengan (A) water bath, (B) reaktor batch, dan (C) agitator ... 22
Gambar 8. Profil SFC hasil interesterifikasi enzimatik Hasrini (2008) ... 35
Gambar 9. Profil SFC dari campuran sebelum dan sesudah interesterifikasi enzimatik (IE) penelitian tahap kedua pada sampel (a) M75, (b) M77, dan (c) M82 yang dibandingkan dengan profil SFC margarin komersial A, margarin komersial B, dan margarin target ... 36
viii
DAFTAR LAMPIRAN
Halaman Lampiran 1. Karakteristik bahan baku interesterifikasi enzimatik ... 56
Lampiran 2. Karakteristik hasil interesterifikasi enzimatik pada penelitian tahap kedua ... 59
Lampiran 3. Hasil ANOVA dan uji lanjut Duncan pada karakter total karoten dari hasil interesterifikasi enzimatik penelitian tahap kedua ... 60
Lampiran 4. Hasil ANOVA dan uji lanjut Duncan pada karakter SMP dari hasil interesterifikasi enzimatik penelitian tahap kedua ... 61
Lampiran5. Karakteristik hasil interesterifikasi enzimatik menggunakan reaktor batch... 62
Lampiran 6. Hasil ANOVA dan uji lanjut Duncan pada karakter total karoten dari hasil interesterifikasi enzimatik menggunakan reaktor
batch ... 65
Lampiran 7. Hasil ANOVA dan uji lanjut Duncan pada karakter SMP dari hasil interesterifikasi enzimatik dalam reaktor batch ... 66
Lampiran 8. Hasil ANOVA dan uji lanjut Duncan pada karakter kadar air dari hasil interesterifikasi enzimatik menggunakan reaktor
batch ... 67
Lampiran 9. Hasil ANOVA dan uji lanjut Duncan pada karakter kadar asam lemak bebas dari hasil interesterifikasi enzimatik menggunakan reaktor batch... 68
1
I. PENDAHULUAN
A. LATAR BELAKANG
Indonesia adalah negara penghasil minyak sawit terbesar di dunia. Produksi minyak sawit Indonesia meningkat setiap tahunnya. Produksi minyak sawit kasar (CPO/crude palm oil) Indonesia dari tahun 2006 sampai tahun 2008 yaitu 16,05 juta ton pada tahun 2006, 17,10 juta ton pada tahun 2007, dan 19,33 juta ton pada tahun 2008 (Pusat Penelitian Kelapa Sawit 2010).
Beragam bahan pangan menggunakan minyak sawit sebagai bahan bakunya, di antaranya adalah minyak goreng, shortening, vanaspati,
mayonnaise, dan saladdressing. Akan tetapi pada kebanyakan olahan minyak sawit tersebut, kandungan β-karoten sudah banyak hilang akibat proses produksi. Salah satu bahan pangan olahan minyak sawit yang mempertahankan kandungan β-karoten di dalamnya adalah minyak sawit merah (red palm oil). Menurut Rossi et al. (2001) kandungan karotenoid dalam minyak sawit merah berkisar antara 500-700 ppm, terutama α- dan β -karoten.
Karoten memiliki banyak kegunaan dalam tubuh manusia. Karoten dapat berfungsi sebagai prekursor vitamin A, selain itu karoten dapat meningkatkan pengaruh anti kanker dan tumor, baik bagi kekebalan tubuh dan melawan infeksi, serta berfungsi sebagai antioksidan (Packer et al. 2005). Akan tetapi karoten sangat rentan terhadap suhu tinggi. Oleh karena itu diperlukan upaya untuk mempertahankan kandungan β-karoten agar dapat dimanfaatkan sebanyak-banyaknya.
Minyak sawit merah dapat dijadikan sebagai bahan baku produk spreads.
2 ruang yang cenderung mengandung triasilgliserol bertitik leleh tinggi (fraksi stearin) (Lida et al. 2002). Selain itu, kandungan karoten dalam minyak sawit merah diharapkan dapat bertahan sampai menjadi produk
spreads sehingga dapat meningkatkan nilai gizi spreads yang dihasilkan. Salah satu karakteristik penting dalam produk spreads adalah kandungan padatan lemak (solid fat content) di dalamnya. Untuk memperbaiki kandungan lemak padat dalam bahan baku spreads berbasis minyak sawit merah, maka dapat ditambahkan minyak kelapa. Kandungan asam lemak utama dalam minyak kelapa adalah asam laurat.
Interesterifikasi enzimatik adalah pertukaran asam lemak antar triasilgliserol. Interesterifikasi terbagi menjadi tiga macam reaksi, yaitu asidolisis (perpindahan gugus asil antara asam dan ester), alkoholisis (reaksi antara lemak dan alkohol untuk menghasilkan ester), dan transesterifikasi (pertukaran gugus asil antara dua ester). Pada penelitian ini reaksi yang digunakan adalah transesterifikasi. Interesterifikasi enzimatik minyak sawit merah dengan minyak kelapa diharapkan dapat menghasilkan bahan baku
spreads yang memiliki sifat plastis sehingga mempunyai kemampuan untuk dioles (spreadable) dan membentuk krim. Komposisi asam lemak pada triasilgliserol dalam minyak sawit didominasi oleh susunan palmitat-oleat-palmitat (POP) yang cenderung membentuk granula kristal yang rapuh. Oleh karena itu, perlu dilakukan interesterifikasi minyak sawit dengan minyak lain yang mengandung asam lemak berantai lebih pendek. Salah satu sumber minyak tersebut adalah minyak kelapa (coconut oil/CNO) yang mengandung asam lemak berantai panjang dan pendek (Lida et al. 2002).
3 sebesar 75:25, 77,5:12,5, dan 82,5:17,5 (b/b) telah diteliti oleh Hasrini (2008) memiliki karakter fisik yang paling mendekati bahan baku margarin interesterifikasi enzimatik ritel dan industri. Interesterifikasi enzimatik ini diharapkan mampu menghasilkan bahan baku produk spreads yang kaya dengan β-karoten. Penggunaan reaktor batch pada penelitian ini diharapkan dapat menjadi acuan dalam proses scalling up produksi bahan baku spreads
berbasis minyak sawit merah di industri pangan.
B. TUJUAN PENELITIAN
Penelitian ini merupakan aplikasi proses interesterifikasi enzimatik menggunakan reaktor batch dalam produksi bahan baku spreads untuk mempermudah proses scalling up di industri pangan. Penelitian ini bertujuan untuk mempelajari pengaruh reaksi interesterifikasi enzimatik menggunakan reaktor batch pada beberapa lama reaksi terhadap karakteristik bahan baku
spreads berbasis minyak sawit merah, yang meliputi total karoten, slip melting point (SMP), solid fat content (SFC), kadar air, dan kadar asam lemak bebas.
C. MANFAAT PENELITIAN
Hasil penelitian ini dapat memberikan informasi proses produksi bahan baku spreads melalui proses interesterifikasi enzimatik menggunakan reaktor
4
II. TINJAUAN PUSTAKA
A. MINYAK KELAPA SAWIT
Kelapa sawit terdiri dari 80% bagian perikarp (epikarp dan mesokarp) dan 20% biji (endokarp dan endosperm). Dari minyak sawit, dapat diperoleh dua jenis minyak yang berbeda sifatnya, yaitu minyak dari inti (endosperm) sawit disebut minyak inti atau PKO (palm kernel oil) dan minyak dari sabut (mesokarp) sawit disebut minyak sawit kasar atau CPO (crude palm oil) (Ketaren 2005). Minyak sawit kasar adalah minyak yang diperoleh dari bagian mesokarp buah sawit dengan cara ekstraksi, yang dapat dilakukan dengan bermacam cara, di antaranya dengan rendering, pengepresan mekanik (hydraulic atau expeller), ekstraksi dengan pelarut ataupun menggunakan
supercritical fluid extraction (Muchtadi 1992).
Pengolahan minyak sawit dari sabut kelapa sawit menjadi minyak goreng secara umum melalui beberapa tahap, yaitu ekstraksi, pemurnian, dan fraksinasi. Ekstraksi adalah suatu cara untuk mendapatkan minyak dari bahan yang diduga mengandung minyak atau lemak. Pemurnian (refining) minyak goreng meliputi tahapan netralisasi atau pemisahan asam lemak bebas (deasidifikasi), pemucatan (bleaching), dan penghilangan bau (deodorisasi). Tahap terakhir yaitu fraksinasi, yang merupakan proses pemisahan fraksi cair (olein) dan fraksi padat (stearin). Fraksi padat tersusun dari asam-asam lemak jenuh, sedangkan fraksi cair tersusun dari asam-asam lemak tidak jenuh.
5
Tabel 1. Komposisi asam lemak minyak sawit
Asam lemak Minyak sawit
kasar (%) Olein (%) Stearin (%)
Laurat (C12) 0,10-0,40 (0,24) 0,20-0,40 (0,27) 0,10-0,30 (0,18) Miristat (C14) 1,00-1,40 (1,11) 0,90-1,20 (1,09) 1,10-1,70 (1,27) Palmitat (C16) 40,90-47,50 (44,14) 36,80-43,20 (40,93) 49,80-68,10 (56,79) Stearat (C18) 3,80-4,80 (4,44) 3,70-4,80 (4,18) 3,90-5,60 (4,93) Oleat (C18:1) 36,40-41,20 (39,04) 39,80-44,60 (41,51) 20,40-34,40 (29,00) Linoleat (C18:2) 9,20-11,60 (10,57) 10,40-12,90 (11,64) 5,00-8,90 (7,23) Linolenat (C18:3) 0,05-0,60 (0,37) 0,10-0,60 (0,40) 0,00-0,50 (0,09) Arakidat (C20:0) 0,20-0,70 (0,38) 0,30-0,50 (0,37) 0,00-0,50 (0,24) Sumber : Gee (2007)
Tabel 2. Komposisi triasilgliserol pada minyak sawit Jenuh
Keterangan: M: miristat; P: palmitat; S: stearat; O: oleat; L: linoleat Sumber: (Gee 2007)
B. MINYAK SAWIT MERAH
6 (cair) dan fraksi stearin (padat). Pemisahan dilakukan dengan cara peningkatan suhu sampai 70oC dan penurunan suhu secara perlahan-lahan hingga tercapai suhu kamar sambil diagitasi. Pada suhu kamar terjadi kristalisasi fraksi stearin sehingga fraksi olein yang masih bersifat cair dapat dipisahkan dengan penyaringan vakum (Weiss 1983).
Menurut Naibaho (1990), MSM mengandung karotenoid sebesar 600-1000 ppm dengan persentase α-karoten 36,2%, β-karoten 54,4%, δ-karoten 3,3%, likopen 3,8%, dan xantofil 2,2%. Kandungan karoten ini menyebabkan MSM berwarna kemerahan. MSM tidak dianjurkan digunakan sebagai minyak goreng, karena karotenoid yang terkandung di dalamnya dapat rusak pada suhu tinggi. MSM biasa digunakan dalam pembuatan minyak salad, serta dapat digunakan sebagai bahan fortifikan makanan untuk produk pangan berbasis minyak/lemak, seperti margarin, selai kacang, dan produk spreads
lainnya.
Menurut Choo et al. (1993), MSM fraksi olein memiliki kandungan karotenoid sebesar 680-760 ppm dan MSM fraksi stearin masih memiliki kandungan karotenoid yang cukup tinggi, yaitu sebesar 380-540 ppm. Karakteristik olein MSM dapat dilihat pada Tabel 3.
Tabel 3. Karakteristik olein minyak sawit merah
Parameter Jumlah
Asam lemak bebas 0,04%
Bilangan peroksida 0,10 mekv/kg
Karoten 513 ppm
Tokoferol 707 ppm
Sumber : Choo et al. (1993)
C. KAROTENOID
7 merah, yaitu dengan aktivitas vitamin A sebesar 30000 µg retinol ekuivalen/100g porsi yang dapat dimakan (Patterson 1983).
Provitamin A yang memiliki aktivitas vitamin A yang paling tinggi adalah β-karoten. Aktivitas provitamin A dinyatakan dalam retinol ekuivalen
(RE, 1 RE = 1µg retinol = 6 µg β-karoten = 12 µg karotenoid (Winarno 1992)). β-karoten mempunyai beberapa aktivitas biologis yang bermanfaat bagi tubuh, antara lain untuk menanggulangi kebutaan karena xeroftalmia, meningkatkan imunitas tubuh, membantu diferensiasi sel epitel, pertumbuhan dan reproduksi. Selain itu karoten juga memiliki aktivitas antioksidan untuk mencegah timbulnya penyakit kanker, mencegah proses penuaan dini, dan mengurangi terjadinya penyakit degeneratif. Provitamin A dikonversi menjadi vitamin A di dalam tubuh. Persentase β-karoten yang dikonversi menjadi vitamin A sekitar 60-70% (Bender 2006). Struktur α -karoten dan β-karoten dapat dilihat pada Gambar1.
Gambar 1. Struktur α-karoten dan β-karoten (Fennema 1996)
Karotenoid memberikan warna merah jingga pada minyak sawit. Pigmen ini bersifat labil terhadap panas dan jumlahnya menurun secara drastis pada suhu sekitar 180-220oC. Karotenoid akan stabil selama ± 9 bulan di dalam minyak sawit merah jika disimpan pada suhu 30oC dan akan stabil lebih dari 1 tahun jika disimpan pada suhu 10oC (Choo 1993).
Karotenoid sangat mudah teroksidasi, hal ini karena adanya ikatan ganda pada karotenoid menyebabkan percepatan laju oksidasi karena sinar dan
α-karoten
8 katalis logam seperti tembaga, besi, dan mangan (Wafford 1980), selain itu reaksi oksidasi dapat dipicu oleh suhu yang relatif tinggi. β-karoten dapat mengalami auto-oksidasi menghasilkan produk degradasi oksidatif, yaitu retinal dan beta apo-8’-karotenal (Woggon 2002). Menurut Combs (1992), karotenoid dalam minyak sawit kasar terdapat dalam bentuk bebas dan dalam minyak yang merupakan medium pelarutnya. Sedangkan di dalam sayuran dan buah-buahan, karotenoid biasanya membentuk kompleks dengan protein atau teresterifikasi dengan asam lemak sehingga bersifat lebih stabil dibandingkan dengan karotenoid dalam minyak sawit kasar, sehingga karotenoid dalam minyak sawit merah lebih mudah diserap tubuh.
D. MINYAK KELAPA
Minyak kelapa atau coconutoil (CNO) diperoleh dari kopra, yaitu daging buah kelapa yang telah dikeringkan. Minyak kelapa dapat digunakan sebagai bahan baku untuk industri pangan seperti minyak goreng, shortening,
emulsifier, dan lain-lain. Secara umum, deskripsi minyak kelapa dapat dijelaskan sebagai lemak yang berwarna putih sampai putih kekuningan, tergantung kepada metode ekstraksi minyak dan kualitas minyak. Pada saat meleleh, minyak kelapa berubah wujud menjadi minyak jernih sampai coklat kekuningan. Minyak kelapa relatif tahan terhadap kemungkinan terjadinya ketengikan karena derajat ketidakjenuhannya rendah (bilangan iodnya 7,5-10,5) Sifat fisikokimia minyak kelapa dapat dilihat pada Tabel 4.
Tabel 4. Sifat fisikokimia minyak kelapa
Sifat fisiko kimia Selang
Bilangan iod ( g I2/100 g CNO) 7,5-10,5 Bilangan asam (mg NaOH/g CNO) 0,01
Bobot jenis (25oC) 0,919
Titik cair (oC) 24-27
Sumber : Swern (1979)
9 dari gugus karbonil (dari pemecahan peroksida) dengan asam amino (dari protein) dan suhu sangat berpengaruh pada reaksi tersebut (Djatmiko et al.
1976).
Minyak kelapa mengandung 84% triasilgliserol yang ketiga asam lemak tidak jenuh, 12% triasilgliserol dengan dua asam lemak jenuh dan satu asam lemak tidak jenuh, dan 4% triasilgliserol yang mempunyai satu asam lemak jenuh dan dua asam lemak tidak jenuh (Swern 1979). Minyak kelapa disebut juga minyak asam laurat, karena kandungan asam lauratnya paling tinggi dibandingkan dengan kandungan asam lemak lainnya, yaitu 44-52%. Komposisi asam lemak dan triasilgliserol minyak kelapa dapat dilihat pada
Tabel 5 dan Tabel 6.
Tabel 5. Komposisi asam lemak minyak kelapa
Jenis asam lemak Jumlah (%)
Asam lemak jenuh
Asam kaproat (C6:0) 0,0-0,8
Asam kaprilat (C8:0) 5,5-9,5
Asam kaprat (C10:0) 4,5-9,5
Asam laurat (C12:0) 44,0-52,0
Asam miristat (C14:0) 13,0-19,0
Asam palmitat (C16:0) 7,5-10,5
Asam stearat (C18:0) Asam arakidat (C 20:0)
1,0-3,0 0,0-0,4
Asam lemak tidak jenuh
Asam palmitoleat (C16:1) 0,0-1,3
Asam oleat (C18:1) 5,0-8,2
Asam linoleat (C18:2) 1,0-2,6
10
Tabel 6. Komposisi triasilgliserol minyak kelapa
TAG (%) TAG (%) P: palmitat; O: oleat; L: linoleat
Sumber: (Tan dan Man 2002)
E. INTERESTERIFIKASI ENZIMATIK
Reaksi interesterifikasi adalah reaksi penyusunan kembali asam-asam lemak ke dalam molekul triasilgriserol. Interesterifikasi tidak memengaruhi derajat kejenuhan asam lemak ataupun mengisomerasi asam lemak tidak jenuh (mempunyai ikatan rangkap). Reaksi interesterifikasi tidak mengubah sifat dan profil asam lemak yang ada, akan tetapi mengubah profil lemak atau minyak karena mengubah susunan triasilgliserol (Tombs 1995).
12 1.Asidolisis
2.Alkoholisis
3.Transesterifikasi
Gambar 2. Prinsip reaksi interesterifikasi (Huyghebaert et al. 1994)
F. ENZIM LIPASE
Lipase adalah enzim yang mengkatalisis hidrolisis ikatan karboksil ester dalam asilgliserol. Keunggulan enzim lipase dalam interesterifikasi enzimatik dibandingkan dengan interesterifikasi kimiawi adalah kespesifikannya. Lipase akan mengkatalisis hidrolisis substrat yang terdapat dalam bentuk misel, agregat kecil atau partikel emulsi. Cara kerjanya berbeda-beda, tergantung dari jenis mikroorganisme dan sumber penghasilnya. Spesifitas kerjanya tergantung pada posisi atau lokasi ester, asam lemak dan asilgliserol (Macrae 1983).
13 meningkatkan penggunaan enzim (reusability), penghentian yang cepat dari reaksi, pembentukan produk yang lebih terkontrol, menekan biaya, dan memudahkan pemisahan enzim dari reaktan dan produk. Imobilisasi juga menyediakan kemungkinan mendapatkan lipase murni dari ekstrak kotor dan imobilisasi secara simultan. Lipozyme TL IM merupakan enzim komersial terimobilisasi yang berasal dari lipase mikrobial Thermomyces lanuginosa
yang mempunyai spesifitas posisional molekul triasilgliserol pada posisi primer (sn-1 dan atau sn-3). Lipozyme TL IM ini terimobilisasi dalam bentuk metode penjebakan, yaitu enzim dijebak di dalam matriks silica gel atau di “bungkus” di dalam membran semipermiabel dengan erat sehingga enzim menjadi tidak bebas dalam menjalankan fungsi katalitiknya di dalam kisi-kisi polimer tersebut (Suhartono 1989). Lypozyme TL IM biasa digunakan dalam reaksi interesterifikasi untuk pembuatan bahan baku shortening dan margarin (Novozyme 2010).
Novozyme 435 merupakan enzim lipase terimobilisasi komersial non-spesifik dari Candida antartica. Enzim ini dapat digunakan untuk berbagai macam substrat dan sangat stabil terhadap kenaikan suhu (termostabil). Novozyme 435 dapat digunakan dalam reaktor batch maupun reaktor kolom, akan tetapi paling baik digunakan dalam fixed-bed reactors.
Novozyme 435 biasa digunakan dalam reaksi esterase untuk memproduksi ester-ester tertentu pada suhu proses yang rendah (60-70oC). Enzim ini juga dapat digunakan untuk meresintesis lemak (triasilgliserol) dari gliserol dan asam-asam lemak bebas. Suhu proses untuk Novozyme 435 yang relatif rendah dapat mencegah pembentukan hasil sampingan sehingga dapat menurunkan biaya purifikasi produk akhir (Novozyme 2010). Novozyme 435 memiliki aktivitas katalitik sebesar 7000 PLU/g (propyl laurate units per gram) dengan carrier akrilik resin dan kadar air 1-2% (b/b) (Chang et al. 2005).
14 optimum untuk lipase adalah antara 0,04-11% (b/v), walaupun kebanyakan reaksi interesterifikasi membutuhkan kadar air kurang dari 1% (Willis dan Marangoni 2002).
G. SPREADS
Spreads adalah produk yang menyerupai margarin, tetapi mengandung lemak kurang dari 80% (Chrysam 1996). Produk olesan rendah lemak (reduced spreads) bukan merupakan margarin, tetapi dibuat dengan cara yang sama dengan margarin, mengandung lemak lebih rendah (±40%) dan mengandung kadar air lebih tinggi (±60%).
Menurut Codex (2007), spreads adalah produk olahan lemak untuk olesan yang memiliki kadar lemak lebih dari 10% dan tidak melebihi 90%.
Spreads dikategorikan dalam standar Codex menjadi dua kelompok, yaitu fat spreads yang memiliki kadar lemak kurang dari 80%, dan margarin yang memiliki kadar lemak lebih dari atau sama dengan 80%.
Banyak tipe spreads yang tersedia secara komersial, yaitu terdiri dari campuran lemak hewani dan lemak nabati, produk dengan kandungan lemak bervariasi lebih dari 80% sampai kurang dari 5%, spreads dari fase air kontinyu air alami, hingga produk mengandung protein susu dan agen penstabil emulsi hidrokoloid.
Sebagian besar spreads adalah emulsi air dalam minyak, seperti margarin dan table spreads. Spreads harus bersifat plastis, sehingga mempunyai kemampuan untuk dioles dan membentuk krim. Untuk memperoleh sifat
spreadable umumnya digunakan lemak nabati. Menurut Gaman dan Sherrington (1992), plastisitas lemak disebabkan karena lemak merupakan campuran triasilgliserol yang masing-masing mempunyai titik leleh tersendiri, hal ini berarti pada suhu tertentu sebagian lemak mencair dan sebagian lagi dalam bentuk kristal padat.
15 sebagai sumber asam lemak esensial, pembentuk tekstur produk, dan berperan pada sensasi dingin (coolness effect)ketika dimakan.
Karakter penting dari produk spreads adalah solid fat content (SFC) dan
slip melting point (SMP). SFC menunjukkan jumlah kristal lemak dalam campuran, berperan pada banyak karakteristik produk seperti penampilan umum, memudahkan pengemasan, sifat organoleptik, memudahkan penyebaran (spreading), dan pengeluaran minyak. SFC antara 4-10oC menentukan kemudahan penyebaran pada suhu refrigerator. SFC pada suhu 10oC yang baik adalah sekitar 32% untuk mendapatkan daya oles yang baik pada suhu refrigerator. SFC pada suhu 20 dan 22oC menentukan stabilitas produk dan daya tahan terhadap pengeluaran minyak pada suhu kamar. SFC antara 35-37oC menentukan kekentalan dan sifat pelepasan flavor spreads
dalam mulut (Lida dan Ali 1998). Menurut Timms (1994), SMP adalah suhu pada saat lemak dalam pipa kapiler yang berada dalam air menjadi cukup leleh untuk naik dalam pipa kapiler.
H. REAKTOR BATCH
Reaktor kimia adalah sebuah alat industri kimia, dimana terjadi reaksi bahan mentah menjadi hasil jadi (produk) yang bernilai lebih. Penggunaan reaktor bergantung dari proses yang dijalankan. Pada proses produksi batch, digunakan reaktor batch. Reaktor batch adalah tempat terjadinya suatu reaksi kimia tunggal, yaitu reaksi yang berlangsung dengan hanya satu persamaan laju reaksi. Reaktor jenis ini biasanya sangat cocok digunakan untuk produksi berkapasitas kecil misalnya dalam proses pelarutan padatan, pencampuran produk, reaksi kimia, batch distillation, kristalisasi, ekstraksi cair-cair, polimerisasi, farmasi, dan fermentasi.
Dalam proses batch, seluruh bahan reaksi dicampur pada awal proses. Reaksi dihentikan dan hasil reaksi dikeluarkan apabila mencapai ke tahap yang diinginkan (Masyitah 2004). Reaktor batch bisa tersusun oleh sebuah tangki dengan pengaduk serta sistem pendingin atau pemanas yang menyatu
16
batch biasanya terbuat dari baja, stainless steel, atau baja berlapis kaca. Padatan dan cairan yang akan masuk reaktor biasanya melalui sambungan yang terdapat pada tutup atas reaktor. Untuk uap dan gas yang keluar reaktor biasanya juga melalui bagian atas, sedangkan untuk cairan keluar melalui bagian bawah (Coulson dan Ricardson 1983). Desain reaktor batch yang digunakan dalam penelitian ini dapat dilihat pada Gambar 3.
Gambar 3. Desain reaktor batch (Nurcahyo 2001)
17
III. BAHAN DAN METODE
A. BAHAN DAN ALAT
Bahan-bahan yang digunakan adalah minyak sawit merah netral
(neutralized deodorized red palm oil/NDRPO) dari SEAFAST Center IPB, minyak kelapa (CNO) merk Barco, Lipozyme TL IM (lipase Thermomyces lanuginosa terimobilisasi spesifik sn-1,3) dan Novozyme 435 (lipase Candida antartica terimobilisasi non-spesifik) yang merupakan produk Novo Nordisk Bioindustrial Ltd., Denmark. Bahan-bahan untuk analisis kimia adalah heksana p.a., etanol 95% netral, indikator fenoftalein, NaOH 0,25 N, gas N2, dan air destilata.
Alat-alat yang digunakan pada penelitian ini adalah spektrofotometer, erlenmeyer, oven, desikator, timbangan analitik, labu takar, corong gelas, hot plate, termometer, peralatan titrasi, water bath, refrigerator, reaktor batch, Bruker Minispec PC 100 Nuclear Magnetic Resonance Analyzer, cawan aluminium, hot plate, magnetic stirer, pipa kapiler (milipore), buret, label kertas, kertas tissue, kertas saring, termometer, rotary shaker bath, sentrifus, dan tabung sentrifus. Selain itu juga digunakan alat-alat gelas untuk analisis.
B. METODE PENELITIAN
Penelitian ini dibagi menjadi tiga tahap. Penelitian tahap pertama adalah karakterisasi bahan baku. Penelitian tahap kedua yaitu pemilihan formula bahan baku kemudian dilanjutkan dengan penelitian tahap ketiga yaitu interesterifikasi enzimatik dalam reaktor batch.
1. Penelitian Tahap Pertama: Karakterisasi Bahan Baku
18 fraksinasi pada penelitian ini menggunakan metode Aini et al. (2005) yang dimodifikasi Hasrini (2008). Proses fraksinasi dapat dilihat pada
Gambar 4.
Gambar 4. Diagram proses fraksinasi (modifikasi Aini et al. 2005)
NDRPO (neutralized deodorized red palm oil) dipanaskan pada suhu 60℃ selama 30 menit, lalu NDRPO tersebut dipindahkan ke dalam tabung sentrifus 50 ml dan didiamkan semalam (±16 jam). Pemisahan RPO dan RPS dilakukan dengan sentrifus pada kecepatan 2500 rpm selama 25 menit. Setelah proses fraksinasi, dilakukan proses formulasi terhadap RPO, RPS, dan CNO (coconut oil). Proses formulasi dilakukan dengan cara mencampurkan RPO/RPS (1:1) dan CNO dengan perbandingan 75:25, 77,25:22,5, dan 82,5:17,5. Karakteristik yang dianalisis pada penelitian tahap ini adalah total karoten, slip melting point (SMP), solid fat content
(SFC), kadar air, dan kadar asam lemak bebas.
2. Penelitian Tahap Kedua: Pemilihan Formula Bahan Baku
Penelitian tahap kedua bertujuan untuk memilih dua formula terbaik. Pemilihan formula campuran bahan baku dilakukan terhadap tiga formula hasil penelitian Hasrini (2008) yang menghasilkan karakter fisik paling
NDRPO
Sentrifugasi (V=2500 rpm, 25 menit) Pemindahan ke tabung sentrifus 50 ml
RPO RPS
Pemanasan (T= 60oC, 30 menit)
Penyimpanan di tempat gelap semalam, T ruang NDRPO
Pemanasan (T= 60oC, 30 menit) NDRPO
Pemindahan ke tabung sentrifus 50 ml Pemanasan (T= 60oC, 30 menit)
NDRPO
Penyimpanan di tempat gelap semalam, T ruang Pemindahan ke tabung sentrifus 50 ml
Pemanasan (T= 60oC, 30 menit) NDRPO
Penyimpanan di tempat gelap semalam, T ruang Pemindahan ke tabung sentrifus 50 ml
Pemanasan (T= 60oC, 30 menit) NDRPO
Sentrifugasi (V=2500 rpm, 25 menit) Penyimpanan di tempat gelap semalam, T ruang
Pemindahan ke tabung sentrifus 50 ml Pemanasan (T= 60oC, 30 menit)
NDRPO
Sentrifugasi (V=2500 rpm, 25 menit) Penyimpanan di tempat gelap semalam, T ruang
Pemindahan ke tabung sentrifus 50 ml Pemanasan (T= 60oC, 30 menit)
NDRPO
Sentrifugasi (V=2500 rpm, 25 menit) Penyimpanan di tempat gelap semalam, T ruang
Pemindahan ke tabung sentrifus 50 ml Pemanasan (T= 60oC, 30 menit)
19 mendekati margarin ritel dan industri, yaitu formula (RPO/RPS)/CNO dengan rasio 75:25, 77,5:12,5, dan 82,5:17,5. Rasio RPO/RPS yang digunakan adalah 1:1. Prosedur interesterifikasi enzimatik yang dilakukan adalah dengan metode Zhang et al. (2001) yang dimodifikasi Hasrini (2008), di mana modifikasi Hasrini (2008) adalah dengan melakukan interesterifikasi enzimatik menggunakan rotary shaker bath (shaker
inkubator), kecepatan agitasi 200 rpm, dosis enzim 10% (b/b), dan lama reaksi 4 jam.
20
Gambar 5. Prosedur interesterifikasi enzimatik (modifikasi Zhang et al.
2001)
3. Penelitian Tahap Ketiga: Interesterifikasi Enzimatik Menggunakan Reaktor Batch
Penelitian tahap ketiga bertujuan untuk menghasilkan bahan baku
spreads melalui proses interesterifikasi enzimatik menggunakan reaktor
batch. Enzim yang digunakan pada penelitian tahap ketiga adalah enzim Novozyme 435. Selain itu penelitian tahap ketiga ini juga bertujuan untuk mendapatkan karakter bahan baku spreads yang diproduksi dalam reaktor
batch. Penelitian yang dilakukan adalah pembuatan bahan baku spreads
dari dua formulasi terbaik penelitian Hasrini (2008) menggunakan reaktor
batch dengan perlakuan perbedaan lama reaksi. Lama reaksi yang dilakukan adalah 2 jam, 4 jam, dan 6 jam. Reaktor batch yang digunakan dalam penelitian ini memiliki kapasitas maksimum 100 g.
RPO/RPS ditambahkan CNO masing-masing dengan rasio sesuai perlakuan sebanyak 50 g kemudian dimasukkan ke dalam reaktor batch
dan diagitasi dengan agitator pada kecepatan 200 rpm dan suhu 60oC. Setelah mencapai suhu 60oC dan sampel telah meleleh sempurna,
Hasil interesterifikasi enzimatik Agitasi selama 4 jam (V=200 rpm, T=60 ºC)
Penyaringan enzim
Penambahan 10% (b/b) enzim Lipozyme TL IM Agitasi sampai suhu mencapai 60 ºC (V=200 rpm)
Pemasukan ke dalam erlenmeyer Penambahan CNO sesuai perlakuan
21 kemudian dimasukkan Novozyme 435 sebanyak 10% (b/b) dan diagitasi kembali selama 2, 4, dan 6 jam. Hasil interesterifikasi tersebut diambil dan Novozyme 435 disaring. Sampel kemudian disimpan dalam botol kaca gelap, dihembus N2, dan disimpan dalam refrigerator. Tahapan kerja interesterifikasi enzimatik menggunakan reaktor batch dapat dilihat pada
Gambar 6. Gambar rangkaian reaktor batch disajikan pada Gambar 7. Analisis yang dilakukan meliputi total karoten, SMP, SFC, kadar air, dan kadar asam lemak bebas terhadap sampel hasil interesterifikasi enzimatik menggunakan reaktor batch dari dua formula yang telah ditentukan.
Gambar 6. Diagram alir prosedur interesterifikasi enzimatik mengunakan reaktor batch
Hasil interesterifikasi enzimatik
Agitasi (V=200 rpm, T=60 ºC selama 2, 4, 6 jam)
Penyaringan enzim
Penambahan 10% (b/b) enzim Novozyme 435 Agitasi sampai suhu mencapai 60 ºC (V=200 rpm)
Pemasukan ke dalam reaktor batch
22
Gambar 7. Rangkaian reaktor batch, dengan (A) water bath, (B) reaktor
batch, dan (C) agitator
C. METODE ANALISIS
Metode analisis yang digunakan dalam penelitian ini meliputi total karoten, slip melting point, solid fat content, kadar air, dan kadar asam lemak bebas. Data yang didapat kemudian dianalisis secara statistik.
1. Total Karoten (PORIM p2.6 1995)
Analisis total karoten dalam penelitian ini didasarkan pada PORIM
test method (1995) yang mengukur nilai absorbansi menggunakan spektrofotometer. Hasil analisis menggunakan metode ini sudah dinyatakan dalam ppm β-karoten.
Sampel dilelehkan dan dihomogenasi. Kemudian sampel sebanyak 0,1 g dilarutkan dengan heksana p.a. ke dalam labu takar 25 ml sampai tanda tera, lalu dikocok hingga benar-benar homogen. Selanjutnya absorbansi diukur dengan spektrofotometer pada panjang gelombang 446 nm. Total karotenoid dihitung dengan menggunakan rumus:
Total karoten (ppm) =
A
B
C
23
2. Slip Melting Point (SMP) (AOCS Official Method Cc 3-25 1990)
Pipa kapiler yang berdiameter 1 mm dan panjang 10 cm dicelupkan dalam sampel minyak yang sudah dipanaskan setinggi ± 1 cm, lalu bagian luar pipa kapiler dibersihkan dengan kertas tissue. Pipa kapiler disimpan dalam refrigerator (suhu 4-10 ºC) selama 16 jam (semalam). Kemudian dipasangkan pada termometer dengan diikat karet sejajar dengan ujung termometer. Termometer dicelupkan ke dalam gelas piala di atas hot plate
berisi air dengan suhu 8-10℃di bawah SMP sampel. Hot plate dinyalakan dengan kenaikan suhu 1℃ per menit. Air dalam gelas piala naik suhunya, pada suhu tertentu sampel minyak dalam kapiler mencair yang ditandai dengan naiknya sampel tersebut. Selang suhu termometer saat sampel minyak mulai naik sampai sampel minyak berada di atas batas 1 cm dicatat.
3. Solid Fat Content (SFC) (IUPAC 2.150 ex 2.323 1987)
Pengukuran SFC dilakukan menggunakan alat nuclear magnetic resonance (NMR) Brucker Minispec PC 100 NMR Analyzer. Pre-treatment atau prosedur stabilisasi sangat menentukan jumlah dan tipe kristal lemak yang terbentuk, dan konsekuensinya terhadap kandungan padatan (solid content) yang diukur dengan NMR. Prosedur stabilisasi dan tempering untuk pengukuran SFC margarin, sesuai dengan yang dikeluarkan oleh Bruker (Typical Applications for Industry: Minispec Application Note 8).
24 c-(a-b)
c
M x V x T 10m
4. Kadar Air (AOAC 1995)
Sejumlah ± 5.0 g sampel dimasukkan ke dalam cawan yang telah dikeringkan terlebih dulu dalam oven dan yang telah diketahui beratnya. Kemudian cawan dimasukkan ke dalam oven bersuhu 105oC hingga diperoleh berat yang konstan. Perhitungan kadar air dilakukan dengan menggunaan rumus:
Kadar air (%) = x 100%
Keterangan : a = berat cawan dan sampel awal (g) b = berat cawan dan sampel akhir (g) c = berat sampel awal (g)
5. Kadar Asam Lemak Bebas (AOCS Official Method Ca 5a-40 1990)
Sampel sebanyak 7,05 ± 0.05 g dilarutkan dalam 75 ml alkohol 95% netral, dipanaskan selama 10 menit dalam hot plate sambil diaduk, lalu ditambahkan 3-5 tetes indikator fenoftalein 1%. Setelah itu sampel tersebut dititrasi dengan larutan standar NaOH 0,25 N hingga warna merah muda tetap. Asam lemak bebas dinyatakan sebagai persen asam lemak, dihitung sampai dua desimal dengan menggunakan rumus :
Kadar asam lemak bebas (%) = %
Keterangan : M = Bobot molekul asam lemak (269,74 untuk NDRPO, 270,54 untuk olein sawit, 266,38 untuk stearin sawit, dan 212,23 untuk minyak kelapa)
V = Volume NaOH yang diperlukan dalam peniteran (ml) T = Normalitas NaOH (N)
25
6. Analisis Data
Data yang diperoleh dari hasil pengukuran terhadap karakteristik produk selanjutnya diuji secara statistik. Pengolahan data untuk uji statistik menggunakan program SPSS 15.0. Data yang diperoleh terlebih dahulu dilakukan analisis ragam dengan one-way ANOVA (analysis of variance) untuk mengetahui perbedaan pada karakteristik produk yang diuji. Setelah diketahui bahwa karakteristik produk berbeda nyata, selanjutnya dilakukan uji lanjut Duncan. Hasil uji lanjut Duncan menunjukkan apakah terdapat perbedaan nyata pada tiap sampe (Lea et al.
26
IV. HASIL DAN PEMBAHASAN
A. Penelitian Tahap Pertama: Karakterisasi Bahan Baku
Karakter yang dianalisis dari bahan baku minyak sawit merah adalah total karoten, nilai slip melting point (SMP), profil solid fat content (SFC), kadar air, dan kadar asam lemak bebas. Karakterisasi bahan baku dilakukan untuk mengetahui kondisi awal minyak sawit merah dan formula bahan baku sehingga dapat diketahui peluangnya untuk proses interesterifikasi enzimatik. Karakteristik bahan baku dapat dilihat pada Lampiran 1.
1. Total Karoten
Gee (2007) menyebutkan bahwa kandungan karoten dalam minyak sawit kasar (CPO) sekitar 500-700 ppm. Tabel 7 memperlihatkan data total karoten dari bahan baku minyak sawit merah yang digunakan dalam penelitian ini. RPO memiliki kandungan karoten yang lebih tinggi dibanding RPO/RPS. Fraksi stearin sawit mengandung karoten yang lebih sedikit dibandingkan dengan fraksi olein. Stearin sawit lebih banyak mengandung monoasilgliserol, sterol, dan fosfolipid (Gee 2007). Hal ini yang menyebabkan RPO mengandung karoten yang lebih tinggi daripada RPO/RPS. Kandungan karoten dalam NDRPO lebih tinggi dibandingkan dengan RPO dan RPO/RPS. Hal ini diduga karena adanya pemanasan sebelum tahap fraksinasi.
Tabel 7. Kandungan karoten bahan baku
Sampel Total karoten (ppm)
NDRPO 376,47 ± 3,65
RPO 351,36 ± 12,07
RPO/RPS (1:1) 343,27 ± 7,89
Keterangan: NDRPO = neutralized deodorized red palm oil; RPO = red palm olein; RPS
= red palm stearin.
27 karotennya juga semakin tinggi. Pada Tabel 8 terlihat bahwa semakin tinggi jumlah RPO/RPS maka kandungan karotennya juga semakin tinggi.
Tabel 8. Kandungan karoten bahan baku yang telah diformulasi
Sampel (RPO/RPS:CNO) Kode Sampel Total karoten (ppm)
75:25 M75 262,42 ± 6,80
77,5:22,5 M77 265,01 ± 12,65
82,5:17,5 M82 269,02 ± 8,73
Keterangan: RPO = red palm olein; RPS = red palm stearin; CNO = coconut oil.
Penelitian ini merupakan tahap lanjutan dari serangkaian penelitian pemanfaatan minyak sawit merah. Penelitian terdahulu merupakan kendali proses deasidifikasi dengan menggunakan CPO sebagai bahan baku (Widarta 2008). Produk deasidifikasi adalah minyak sawit merah netral atau neutralized red palm oil (NRPO). Setelah dilakukan deasidifikasi kemudian NRPO dideodorisasi oleh Riyadi (2009) untuk mendapatkan
neutralized deodorized red palm oil (NDRPO). NDRPO yang dihasilkan Riyadi (2009) ini yang dipakai sebagai bahan baku interesterifikasi enzimatik dalam penelitian ini. Hasrini (2008) menggunakan NRPO yang diformulasi dengan minyak kelapa. Tabel 9 menunjukkan data kandungan karoten hasil penelitian Widarta (2008), Hasrini (2008), dan Riyadi (2009). Terlihat bahwa kandungan karoten dalam NDRPO yang digunakan dalam penelitian ini mendekati hasil analisis yang dilakukan Riyadi (2009).
Tabel 9. Kandungan karoten hasil penelitian Widarta (2008), Hasrini (2008), dan Riyadi (2009)
Sampel Total karoten (ppm)
Widarta (2008) Hasrini (2008) Riyadi (2009)
NRPO 464,96 511,31 -
NDRPO - - 375,33
RPO - 529,74 -
RPO/RPS - 465,43 -
Keterangan: NRPO = neutralized red palm oil; NDRPO= neutralized deodorized red
28
2. Slip Melting Point (SMP) dan Solid Fat Content (SFC)
Karakteristik leleh dari minyak sawit dapat terlihat dari nilai slip melting point (SMP). SMP didefinisikan sebagai suhu saat lemak atau minyak memiliki padatan lemak sebesar 5% (Lida et al. 1998). SMP dari lemak atau minyak berubah dengan adanya perubahan panjang asam lemak, rasio ketidakjenuhan, kandungan asam lemak trans dan posisi asam lemak pada struktur triasilgliserol (Karabulut et al. 2004).
Nilai SMP meningkat secara berurutan pada sampel M75, M77, dan M82 (Tabel 10). Hal ini diduga disebabkan oleh adanya peningkatan konsentrasi RPS yang memiliki titik leleh lebih tinggi daripada RPO dan CNO. Menurut Reshma et al. (2007) stearin sawit memiliki titik leleh sebesar 45-55oC (di atas suhu ruang).
SFC adalah jumlah kristal lemak yang terkandung dalam campuran lemak/minyak. Nilai SFC diukur pada suhu 10-40oC. Tabel 10
menunjukkan nilai SFC dan SMP dari sampel bahan baku. Nilai SFC juga bertambah dengan adanya peningkatan komposisi RPO/RPS. Adhikari et al. (2010) menyatakan bahwa penambahan stearin sawit dapat meningkatkan SFC campuran lemak/minyak.
Tabel 10. Nilai SFC dan SMP formula bahan baku
Sampel SFC (%) SMP (oC)
Keterangan: M75= Rasio (RPO/RPS):CNO sebesar 75:25; M77= Rasio (RPO/RPS):CNO sebesar 77,5:22,5; M82= Rasio (RPO/RPS):CNO sebesar 82,5:17,5.
29 sedangkan SMP hasil penelitian Hasrini (2008) lebih rendah dibandingkan dengan SMP bahan baku pada penelititan ini. Perbedaan ini dapat disebabkan oleh perbedaan bahan baku yang digunakan. Hasrini (2008) menggunakan NRPO, sedangkan penelitian ini menggunakan NDRPO. Menurut Riyadi (2009) selama proses deodorisasi, asam-asam lemak bebas dan komponen-komponen odor dihilangkan untuk mendapatkan minyak yang tidak berbau. Oleh karena itu komposisi NRPO dan NDRPO juga berbeda.
Tabel 11. Nilai SFC dan SMP bahan baku pada penelitian Hasrini (2008)
Sampel SFC (%) SMP (℃)
10 oC 20 oC 25 oC 30 oC 35 oC 40 oC
M75 45,78 23,52 20,13 14,11 11,23 8,12 31,15±0,23 M77 46,47 23,46 20,46 14,18 11,28 8,29 33,34±0,78 M82 46,90 41,37 22,62 16,14 12,59 9,63 36,19±0,28
Keterangan: M75= Rasio (RPO/RPS):CNO sebesar 75:25; M77= Rasio (RPO/RPS):CNO sebesar 77,5:22,5; M82= Rasio (RPO/RPS):CNO sebesar 82,5:17,5.
3. Kadar Air dan Kadar Asam Lemak Bebas (ALB)
Kadarair dan kadar asam lemak bebas (ALB) merupakan karakteristik yang penting dalam reaksi interesterifikasi enzimatik. Kadar air dapat memengaruhi kadar ALB dalam produk minyak sawit. Minyak yang ideal untuk interesterifikasi enzimatik mengandung kadar air dan kadar ALB kurang dari 0,1% (Cowan 2009). Berdasarkan Tabel 12, kadar air bahan baku sudah memenuhi syarat, sedangkan kadar ALB sedikit melewati batas ideal untuk reaksi interesterifikasi enzimatik. Walaupun demikian, menurut PORIM test method (1995) batas penerimaan kadar ALB untuk minyak sawit dan produk turunannya adalah sekitar 0,5-1%.
30
Tabel 12. Kadar air dan kadar ALB bahan baku
Sampel Kadar air (%) Kadar ALB (%)
Keterangan: NDRPO = neutralized deodorized red palm oil; RPO = red palm olein; RPS
= red palm stearin; CNO= coconut oil; M75= Rasio (RPO/RPS):CNO sebesar 75:25; M77= Rasio (RPO/RPS):CNO sebesar 77,5:22,5; M82= Rasio (RPO/RPS):CNO sebesar 82,5:17,5.
Kadar air NDRPO yang digunakan dalam penelitian ini sebesar 0,065%. Riyadi (2009) melaporkan kadar air NDRPO adalah sebesar 0% (Tabel 13). Berdasarkan data yang diperoleh dalam penelitian ini, telah terjadi peningkatan kadar air dalam NDRPO yang digunakan. Peningkatan kadar air ini diduga oleh karena masuknya air selama penyimpanan NDRPO. Kadar air yang tinggi dapat memicu terjadinya kerusakan minyak melalui hidrolisis sehingga meningkatkan kadar asam lemak bebas.
Tabel 13. Kadar air dan kadar asam lemak bebas bahan baku penelitian Widarta (2008), Hasrini (2008), dan Riyadi (2009)
Sampel
B. Penelitian Tahap Kedua : Pemilihan Formula Bahan baku
31 ritel dan industri (Hasrini 2008). Ketiga formula ini diinteresterifikasi menggunakan Lypozyme TL IM dalam erlenmeyer menggunakan shaker
inkubator. Hasil interesterifikasi dianalisis total karoten, nilai SMP, dan profil SFC untuk mengetahui formula mana yang karakternya paling mendekati karakter margarin target (Fattahi-far et al. 2006) dan yang memiliki kandungan karoten yang cukup tinggi. Karakteristik hasil interesterifikasi enzimatik pada penelitian tahap kedua dapat dilihat pada Lampiran 2.
1. Total Karoten
Hasil analisis total karoten pada sampel sebelum dan sesudah interesterifikasi enzimatik disajikan pada Tabel 14. Hasil ANOVA memperlihatkan bahwa total karoten berbeda nyata (p<0,05) (Lampiran 3). Uji lanjut Duncan menunjukkan bahwa total karoten sampel sebelum dan sesudah interesterifikasi enzimatik berbeda nyata. Total karoten pada sampel M75, M77, dan M82 tidak berbeda nyata. Hal ini diduga karena komposisi RPO/RPS dalam M75, M77, dan M82 tidak berbeda jauh, sehingga kandungan karoten di dalamnya juga tidak banyak berbeda. Pada
Tabel 14 terlihat bahwa total karoten sesudah interesterifikasi enzimatik lebih rendah daripada sebelum total karoten interesterifikasi enzimatik. Penurunan karoten yang terjadi relatif rendah (retensi karoten cukup tinggi) karena interesterifikasi dilakukan pada suhu yang relatif rendah pula, yaitu 60oC. Karoten banyak terdapat pada RPO/RPS. Oleh karena itu semakin banyak komposisi RPO/RPS maka total karoten dalam sampel juga semakin tinggi. Sampel M77 dan M82 adalah dua sampel dengan kandungan karoten terbesar.
Retensi karoten berkisar antara 79,98-84,38%. Retensi karoten dihitung berdasarkan perbandingan total karoten yang tersisa sesudah interesterifikasi enzimatik terhadap jumlah karoten awal. Data pada
32 sawit merah, temperatur/suhu pemanasan, dan lama pemanasan minyak sawit merah.
Tabel 14. Perbandingan total karoten sebelum dan sesudah interesterifikasi enzimatik (IE) penelitian tahap kedua
Sampel Total karoten (ppm) Retensi karoten (%)
Sebelum IE Sesudah IE
M75 262,42 ± 6,80b 209,88 ± 0,28a 79,98
M77 265,01 ± 12,65b 212,92 ± 4,84a 80,34
M82 269,02 ± 8,73b 227,00 ± 0,83a 84,38
Keterangan: Data ± standar deviasi. Angka yang diikuti huruf yang sama tidak berbeda nyata dengan ANOVA dan uji lanjut Duncan pada taraf uji 5%.
M75= Rasio (RPO/RPS):CNO sebesar 75:25; M77= Rasio (RPO/RPS):CNO sebesar 77,5:22,5; M82= Rasio (RPO/RPS):CNO sebesar 82,5:17,5.
Tabel 15 menunjukkan perbandingan total karoten sebelum dan sesudah interesterifikasi enzimatik hasil penelitian Hasrini (2008). Hasrini (2008) melaporkan data retensi karoten yang lebih tinggi dibandingkan retensi karoten pada tahap ini. Hal ini diduga karena perbedaan komposisi bahan baku, sehingga dihasilkan retensi karoten yang berbeda pula.
Tabel 15. Perbandingan total karoten sebelum dan sesudah interesterifikasi enzimatik (IE) hasil penelitian Hasrini (2008)
Sampel Total karoten (ppm) Retensi karoten
(%)
Sebelum IE Sesudah IE
M75 363,13 ± 3,35 356 43 ± 2,39 98,15
M77 378,21 ± 3,03 366,72 ± 4,06 96,96
M82 392,81 ± 2,86 381,32 ± 3,72 97,07
Keterangan: M75= Rasio (RPO/RPS):CNO sebesar 75:25; M77= Rasio (RPO/RPS):CNO sebesar 77,5:22,5; M82= Rasio (RPO/RPS):CNO sebesar 82,5:17,5.
2. Slip Melting Point (SMP) dan Solid Fat Content (SFC)
33
Tabel 16. Sampel sesudah interesterifikasi enzimatik memiliki SMP yang lebih rendah (30,1-32,5oC) dibandingkan sampel sebelum interesterifikasi enzimatik (34,1-36,5oC) pada semua formula. Hal ini disebabkan karena perubahan profil triasilgliserol akibat interesterifikasi enzimatik. Diduga triasilgliserol yang terbentuk memiliki titik leleh yang lebih rendah sehingga SMP sesudah interesterifikasi enzimatik menjadi lebih rendah. Titik leleh lemak bergantung pada berbagai faktor, seperti sifat asam lemak penyusunnya. Sifat asam lemak tersebut antara lain adalah panjang rantai atom C, jumlah ikatan rangkap, dan bentuk cis atau trans pada asam lemak tidak jenuh. Makin panjang rantai atom C, titik leleh semakin tinggi dan sebaliknya. Titik leleh akan menurun dengan semakin banyaknya ikatan rangkap. Asam lemak jenuh memiliki titik leleh yang lebih tinggi daripada asam lemak tak jenuh. Bentuk trans pada asam lemak menyebabkan lemak memiliki titik leleh lebih tinggi (Barus 2006). Setiap sampel sesudah interesterifikasi enzimatik memiliki SMP di bawah suhu tubuh, yang artinya tidak menimbulkan tekstur seperti lilin (waxy flavor) ketika dikonsumsi.
34
Tabel 16. Perbandingan SMP sebelum dan sesudah interesterifikasi enzimatik (IE) penelitian tahap kedua dibandingkan dengan SMP margarin komersial dan margarin target (Fattahi-far et al., 2006) nyata dengan ANOVA dan uji lanjut Duncan pada taraf uji 5%.
M75= Rasio (RPO/RPS):CNO sebesar 75:25; M77= Rasio (RPO/RPS):CNO sebesar 77,5:22,5; M82= Rasio (RPO/RPS):CNO sebesar 82,5:17,5.
Tabel 17 menunjukkan data analisis SMP sebelum dan sesudah interesterifikasi enzimatik pada penelitian Hasrini (2008). Hasil analisis SMP pada penelitian Hasrini (2008) berbeda dengan hasil analisis SMP pada penelitian ini. Hal ini diduga disebabkan oleh perbedaan bahan baku yang digunakan.
Tabel 17. Perbandingan SMP sebelum dan sesudah interesterifikasi enzimatik (IE) penelitian Hasrini (2008)
Keterangan: M75= Rasio (RPO/RPS):CNO sebesar 75:25; M77= Rasio (RPO/RPS):CNO sebesar 77,5:22,5; M82= Rasio (RPO/RPS):CNO sebesar 82,5:17,5.
35
Keterangan: M75= Rasio (RPO/RPS):CNO sebesar 75:25; M77= Rasio (RPO/RPS):CNO sebesar 77,5:22,5; M82= Rasio (RPO/RPS):CNO sebesar 82,5:17,5.
Gambar 8. Profil SFC hasil interesterifikasi enzimatik Hasrini (2008) SFC memengaruhi karakter fisik dari produk spreads, seperti kekerasan, mouthfeel, dan spreadability. Oleh karena itu nilai SFC diperlukan untuk mengetahui karakter fisik dari spreads. Perubahan profil triasilgliserol akibat interesterifikasi enzimatik juga diikuti dengan perubahan SFC. Gambar 9 menunjukkan profil SFC sampel sebelum dan sesudah interesterifikasi enzimatik yang dibandingkan dengan profil SFC margarin komersial A, margarin komersial B, dan margarin target (Fattahi-far et al. 2006). SFC pada suhu 10oC lebih tinggi dibandingkan dengan SFC pada suhu pengukuran lainnya. Hal ini menunjukkan bahwa SFC berbanding terbalik dengan suhu. Semakin tinggi suhu, maka SFC semakin rendah (Maulina 2004). Setiap sampel memiliki profil SFC yang mirip dan SFC-nya meningkat dengan peningkatan komposisi RPO/RPS. RPS mengandung banyak trisaturated triacylglycerol bertitik leleh tinggi, sehingga semakin tinggi komposisi RPS maka SFC juga semakin tinggi.
36 (a)
(b)
(c)
Keterangan: M75= Rasio (RPO/RPS):CNO sebesar 75:25; M77= Rasio (RPO/RPS):CNO sebesar 77,5:22,5; M82= Rasio (RPO/RPS):CNO sebesar 82,5:17,5.
37
C. Penelitian Tahap Ketiga: Interesterifikasi Enzimatik Menggunakan Reaktor Batch
Sampel yang digunakan dalam penelitian tahap ketiga adalah M77 dan M82. Sampel M77 dan M82 dipilih dengan pertimbangan SMP yang paling mendekati SMP margarin komersial dan retensi karoten yang cukup tinggi. Karakter hasil interesterifikasi enzimatik menggunakan reaktor batch dapat dilihat pada Lampiran 5.
Bahan baku dalam penelitian ini adalah campuran antara RPS, RPO, dan CNO. RPS adalah fraksi padatan dari minyak sawit merah yang diperoleh setelah fraksinasi. RPS tidak dapat dikonsumsi secara langsung karena titik lelehnya tinggi (45-55oC). RPS dipakai sebagai sumber lemak jenuh. RPO adalah fraksi cair dari minyak sawit merah, digunakan sebagai sumber karoten. CNO digunakan sebagai sumber asam lemak berantai pendek. Produksi bahan baku spreads membutuhkan campuran antara minyak dan lemak yang mempunyai titik leleh tinggi dengan minyak yang mempunyai titik leleh rendah, atau antara minyak yang mengandung asam lemak berantai panjang dengan minyak yang mengandung asam lemak berantai pendek sehingga dihasilkan campuran minyak/lemak sesudah interesterifikasi enzimatik yang plastis. Lemak yang plastis adalah ketika lemak tersebut mudah dibentuk dan tidak terlalu lunak maupun terlalu keras (Jennings dan Akoh 2009).
1. Total karoten
38 menunjukkan bahwa terjadi penurunan total karoten sesudah interesterifikasi enzimatik menggunakan reaktor batch.
Hasil analisis juga menunjukkan bahwa semakin lama reaksi, maka retensi karoten semakin menurun. Retensi karoten berkisar antara 74,80-81.08%. Retensi karoten pada interesterifikasi enzimatik menggunakan reaktor batch lebih rendah dibandingkan dengan interesterifikasi enzimatik pada penelitian tahap kedua. Penurunan karoten ini diduga karena adanya oksigen dan panas yang mengkatalisis oksidasi karoten dalam minyak selama reaksi. Selain itu cahaya juga berpengaruh dalam penurunan karoten. Wafford (1980) menyatakan bahwa oksidasi karoten dipercepat dengan adanya cahaya dan katalis logam.
Sampel M822 memiliki kandungan karoten tertinggi, sedangkan M776 adalah sampel dengan kandungan karoten terendah. Berdasarkan data pada Tabel 18 hasil interesterifikasi enzimatik dapat dijadikan bahan baku pembuatan produk spreads kaya β-karoten karena mengandung karoten yang cukup tinggi.
Tabel 18. Total karoten campuran sebelum dan sesudah interesterifikasi enzimatik (IE) menggunakan reaktor batch
Bahan Lama nyata dengan ANOVA dan uji lanjut Duncan pada taraf uji 5%.
39 6 µg β-karoten setara dengan 1 RE vitamin A. Diasumsikan bahan baku
spreads hasil interesterifikasi enzimatik menggunakan reaktor batch yang digunakan sebanyak 80% untuk memproduksi spreads siap konsumsi dengan berat per takaran sajinya sebesar 10 g, maka hasil interesterifikasi enzimatik sampel M772 dapat memenuhi 47,61% AKG vitamin A per takaran saji.
Contoh perhitungan:
β-karoten dalam sampel M772= 212,24 ppm (µg/g);
β-karoten dalam spreads berbahan baku M772 per takaran saji= 80% x
212,24 µg/g x 10 g = 1697,92 µg β-karoten;
Dalam RE = 1697,92 µg β-karoten: 6 µg β-karoten/RE= 282,99 RE;
AKG vitamin A pria dewasa= 600 RE, maka dengan mengkonsumsi
spreads berbahan baku M772 per takaran saji dapat memenuhi (282,99:600) x 100%= 47,16% AKG vitamin A pria dewasa.
Tabel 19 menunjukkan jumlah AKG yang dipenuhi oleh 1 takaran saji