KAJIAN KANDUNGAN MINERAL KALIUM, NATRIUM DAN
KALSIUM PADA SAYURAN KUBIS (Brassica oleracea L.)
YANG DIPEROLEH DARI LAHAN HASIL PERTANIAN
PASCA LETUSAN GUNUNG SINABUNG
SKRIPSI
]OLEH:
SUPARLAN
NIM 121524126
PROGRAM EKSTENSI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
KAJIAN KANDUNGAN MINERAL KALIUM, NATRIUM DAN
KALSIUM PADA SAYURAN KUBIS (Brassica oleracea L.)
YANG DIPEROLEH DARI LAHAN HASIL PERTANIAN
PASCA LETUSAN GUNUNG SINABUNG
SKRIPSI
Diajukan untuk melengkapi salah satu syarat memperoleh gelar Sarjana Farmasi pada Fakultas Farmasi
Universitas Sumatera Utara
OLEH:
SUPARLAN
NIM 121524126
PROGRAM EKSTENSI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
PENGESAHAN SKRIPSI
KAJIAN KANDUNGAN MINERAL KALIUM, NATRIUM DAN
KALSIUM PADA SAYURAN KUBIS (Brassica oleracea L.)
YANG DIPEROLEH DARI LAHAN HASIL PERTANIAN
PASCA LETUSAN GUNUNG SINABUNG
OLEH:
SUPARLAN
NIM 121524126
Dipertahankan di Hadapan Panitia Penguji Skripsi Fakultas Farmasi Universitas Sumatera Utara
Pada Tanggal: 28 November 2014
Pembimbing I,
Drs. Fathur Rahman Harun, M.Si., Apt. NIP 195201041980031002
Pembimbing II,
Dr. Muchlisyam, M.Si., Apt. NIP 195006221980021001
Panitia Penguji,
Prof. Dr. Ginda Haro, M.Sc., Apt. NIP 195108161980031002
Drs. Fathur Rahman Harun, M.Si., Apt. NIP 195201041980031002
Drs. Nahitma Ginting, M.Si., Apt. NIP 195406281983031002
Dra. Sudarmi, M.Si., Apt. NIP 195409101983032001
Medan, Desember 2014 Fakultas Farmasi
Universitas Sumatera Utara Dekan,
KATA PENGANTAR
Bismillahirrahmanirrahiim,
Puji dan syukur penulis panjatkan kepada Allah SWT, karena berkat
limpahan rahmat dan karuniaNya, sehingga penulis dapat menyelasikan penelitian
dan penyusunan skripsi ini, serta Shalawat dan Salam kepada Nabi Allah SWT:
Rasulullah Muhammad SAW sebagai suri teladan dalam kehidupan.
Skripsi ini disusun untuk melengkapi salah satu syarat mencapai gelar
Sarjana Farmasi pada Fakultas Farmasi Universitas Sumatra Utara, dengan judul:
“Kajian Kandungan Mineral Kalium, Natrium Dan Kalsium Pada Sayuran Kubis
(Brassica Oleracea L.) Yang Diperolah Dari Lahan Hasil Pertanian Pasca Letusan
Gunung Sinabung”.
Pada kesempatan ini dengan segala kerendahan hati penulis mengucapkan
terima kasih yang sebesar-besarnya kepada Bapak Prof. Dr. Sumadio
Hadisahputra, Apt., selaku Dekan Fakultas Farmasi Universitas Sumatera Utara
Medan, yang telah memberikan fasilitas sehingga penulis dapat menyelesaikan
pendidikan. Bapak Drs. Fathur Rahman Harun, M.Si.,Apt., dan Bapak Dr.
Muchlisyam, M.Si., Apt., yang telah membimbing dan memberikan petunjuk serta
saran-saran selama penelitian hingga selesainya skripsi ini. Bapak Prof. Dr. Ginda
Haro, M.Sc., Apt., Bapak Drs. Nahitma Ginting, M.Si., Apt., dan Ibu Dra.
Sudarmi, M.Si., Apt., selaku dosen penguji yang telah memberikan kritik, saran
dan arahan kepada penulis dalam menyelesaikan skripsi ini. Bapak Prof. Dr. rer.
nat. Effendy De Lux Putra, S.U., Apt., selaku Koordinator Laboratorium
penulis sehingga dapat mengerjakan dan menyelesaikan penelitian. Bapak dan Ibu
staff pengajar Fakultas Farmasi USU Medan yang telah mendidik selama
perkuliahan dan Ibu Dra. Aswita Hafni Lubis, M.Si., Apt., selaku penasehat
akademik yang selalu memberikan bimbingan kepada penulis selama perkuliahan.
Penulis mengucapkan terima kasih dan penghargaan yang tiada terhingga
kepada Ayahanda Nurman dan Ibunda Patmawati yang telah memberikan cinta
kasih yang tidak ternilai dengan apapun, doa yang tulus, serta pengorbanan baik
materi maupun non materi. Adikku Sukarniati dan Diky Candra serta seluruh
keluarga yang selalu mendoakan dan memberikan semangat.
Penulis menyadari bahwa dalam penulisan skripsi ini masih jauh dari
kesempurnaan, oleh karena itu dengan segala kerendahan hati, penulis menerima
kritik dan saran yang bersifat membangun sangat penulis harapkan, mengingat
keterbatasan pengetahuan dan pengalaman.
Akhirnya, penulis berharap semoga skripsi ini dapat memberi manfaat
bagi kita semua.
Medan, November 2014 Penulis
KAJIAN KANDUNGAN MINERAL KALIUM, NATRIUM DAN KALSIUM PADA SAYURAN KUBIS (Brassica oleracea L.)
YANG DIPEROLEH DARI LAHAN HASIL PERTANIAN PASCA LETUSAN GUNUNG SINABUNG
ABSTRAK
Kubis merupakan salah satu sayuran yang terdapat di mineral pada tanaman, terutama sayuran kubis. Tujuan dari penelitian ini adalah untuk mengetahui kandungan serta perbedaan kandungan mineral kalium, natrium dan kalsium pada sayuran kubis yang diperoleh dari lahan pertanian pasca letusan Gunung Sinabung.
Metode penelitian yang dilakukan adalah pengambilan sampel secara purposif terhadap sayuran kubis yang terdapat di empat desa. Penelitian ini meliputi proses destruksi kering, analisis kuantitatif dilakukan dengan menggunakan metode spektrofotometri serapan atom (SSA) yaitu kalium pada panjang gelombang 766,5 nm, natrium pada panjang gelombang 589,0 nm dan kalsium pada panjang gelombang 422,7 nm dengan nyala udara-asetilen.
Hasil penelitian menunjukkan kadar mineral dari empat desa (Suka Ndebi, Suka Tepu, Ndeskati dan Raya) berturut-turut diperoleh yaitu kalium (332,9800 ± 2,3430 mg/100g; 341,5055 ± 6,8799 mg/100g; 303,5585 ± 13,8707 mg/100g; dan 266,1727 ± 6,9771 mg/100g), natrium (10,1384 ± 0,0488 mg/100g; 10,9081 ± 0,1326 mg/100g; 9,5502 ± 0,1210 mg/100g; dan 8,9698 ± 0,0653 mg/100g) dan kalsium (18,1748 ± 0,6786 mg/100g; 22,0825 ± 0,4088 mg/100g; 17,0041 ± 07277 mg/100g dan 16,0342 ± 0,4399 mg/100g).
Dari hasil penelitian di atas dapat disimpulkan bahwa sayuran kubis yang berasal dari daerah Gunung Sinabung mengandung mineral kalium, natrium dan kalsium. Kadar mineral kalium, natrium dan kalsium di desa yang lebih dekat yakni di kecamatan Naman Teran (Desa Suka Tepu > Desa Suka Ndebi > Desa Ndeskati) lebih tinggi dari desa Raya di kecamatan Brastagi yang lebih jauh dari daerah Gunung Sinabung.
THE MINERAL CONTENT STADY OF POTASSIUM, SODIUM AND CALCIUM IN CABBAGE (Brassica oleracea L.) OBTAINED FROM
AGRICULTURAL LAND AFTER THE SINABUNG ERUPTION
ABSTRACT
Cabbage is one of vegetables in the Karo Highlands. Mount Sinabung eruption would affect the mineral content in plants, especially cabbages. The purpose of this study is to determine the content and mineral content differences of potassium, sodium and calcium in cabbage from agricultural land after the eruption of Sinabung.
The research methodology was purposively sampling the cabbage in the four villages. This study includes the dry destruction process followed by quantitative analysis of potassium, sodium and calcium using atomic absorption spectrophotometry (AAS), which was wavelength potassium metal at 766.5 nm, wavelength sodium metal at 589.0 nm and wavelength calcium metal at 422.7 nm with air-acetylene flame.
The results showed levels of minerals from four villages (Suka Ndebi, Suka Tepu, Ndeskati and Raya) obtained were potassium (332.9800 ± 2.3430 mg / 100g; 341.5055 ± 6.8799 mg / 100g; 303.5585 ± 13.8707 mg / 100g, and 266.1727 ± 6.9771 mg / 100g), sodium (10.1384 ± 0.0488 mg / 100g; 10.9081 ± 0.1326 mg / 100g; 9.5502 ± 0.1210 mg / 100g, and 8.9698 ± 0.0653 mg / 100g) and calcium (18.1748 ± 0.6786 mg / 100g; 22.0825 ± 0.4088 mg / 100g; 17.0041 ± 07 277 mg / 100g and 16.0342 ± 0.4399 mg / 100g).
From the above results it can be concluded that cabbage from the Mount Sinabung contains minerals potassium, sodium and calcium. Mineral content of potassium, sodium and calcium in villages closer to that in the subdistrict Naman Teran (Suka Tepu Village > Suka Ndebi Village > Ndeskati Village) higher than the Raya Village in the subdistrict Brastagi more distant from the area of Mount Sinabung.
DAFTAR ISI
Halaman
JUDUL ... i
HALAMAN PENGESAHAN ... iii
KATA PENGANTAR ... iv
ABSTRAK ... vi
ABSTRACT ... vii
DAFTAR ISI ... viii
DAFTAR TABEL ... xi
DAFTAR GAMBAR ... xii
DAFTAR LAMPIRAN ... xiii
BAB I PENDAHULUAN ... 1
1.1 Latar Belakang ... 1
1.2 Perumusan Masalah ... 3
1.3 Hipotesis ... 3
1.4 Tujuan Penelitian ... 3
1.5 Manfaat Penelitian ... 4
BAB II TINJAUAN PUSTAKA ... 5
2.1 Gunung Berapi ... 5
2.1.1 Jenis Gunung Berapi Berdasarkan Bentuknya ... 5
2.1.2 Klasifikasi Gunung Berapi di Indonesia ... 6
2.1.3 Gunung Berapi Meletus ... 7
2.1.4 Ciri – Ciri Gunung Berapi Meletus ... 7
2.2 Gunung Sinabung ... 9
2.3 Kubis …………. ... 10
2.3.1 Klasifikasi ... 11
2.3.2 Varietas dan Jenis ... 12
2.3.3 Kandungan Gizi ... 13
2.4 Mineral ... 13
2.4.1 Kalium ... 14
2.4.2 Kalsium ... 14
2.4.3 Natrium ... 15
2.5 Spektrofotometri Serapan Atom ... 15
2.5.1 Instrumentasi Spektrofotometri Serapan Atom ... 16
2.5.2 Gangguan-gangguan pada Spektrofotometri Serapan atom ... 18
2.6 Validasi Metode Analisis ... 19
BAB III METODE PENELITIAN ... 22
3.1 Tempat dan Waktu Penelitian ... 22
3.2 Alat dan Bahan ... 22
3.2.1 Alat ... 22
3.2.2 Bahan ... 22
3.3 Pembuatan Pereaksi ... 23
3.5.1 Larutan HNO3 (1:1) ... 23
3.4 Prosedur Penelitian ... 23
3.4.1 Pengambilan Sampel ... 23
3.4.3 Proses Destruksi Kering ... 24
3.4.4 Pembuatan Larutan Sampel ... 24
3.4.5 Pemeriksaan Kualitatif dan Kuantatif ... 25
3.4.5.1 Pembuatan Kurva Kalibrasi dan Penetapan Kadar Kalium ... 25
3.4.5.2 Pembuatan Kurva Kalibrasi dan Penetapan Kadar Natrium ... 25
3.4.5.2 Pembuatan Kurva Kalibrasi dan Penetapan Kadar Kalsium ... 26
3.5 Analisis Data Secara Statistik ... 27
3.5.1 Penolakan Hasil Pengamatan ... 27
3.5.2 Pengujian Beda Nilai Rata-rata ... 28
3.5.3 Uji Perolehan Kembali (Recovery) ... 28
3.5.4 Simpangan Baku Relatif ... 29
3.5.5 Penentuan Batas Deteksi (Limit of Detection) dan Batas Kuantitasi (Limit of Quantitation) ... 30
BAB IV HASIL DAN PEMBAHASAN ... 31
4.1 Pengambilan Sampel ... 31
4.2 Identifikasi Sampel ... 32
4.3 Analisis Kualitatif ... 32
4.4 Analisis Kuantitatif ... 33
4.4.1 Kurva Kalibrasi Kalium, Natrium dan Kalsium ... 33
4.4.2 Pengukuran Kadar Kalium, Natrium dan Kalsium dalam Sampel ... 34
4.5 Pengujian Beda Nilai Rata-rata ... 36
4.6 Uji Perolehan Kembali ... 37
4.8 Batas Deteksi dan Batas Kuantitasi ... 39
BAB V KESIMPULAN DAN SARAN ... 41
5.1 KESIMPULAN ... 41
5.1 SARAN ... 41
DAFTAR PUSTAKA ... 43
DAFTAR TABEL
Halaman
Tabel 4.1 Hasil Analisis Kadar Kalium, Natrium dan Kalsium
dalam Sampel ... 35
Tabel 4.2 Hasil Uji Beda Nilai Rata-rata Kadar Kalium, Natrium
Kalsium Antarsampel ... 36
Tabel 4.3 Persen uji Perolehan Kembali (recovery) Kalium,
Natrium Kalsium ... 38
Tabel 4.4 Nilai Simpangan Baku dan Simpangan Baku Relatif
Kalium, Natrium dan Kalsium ... 38
Tabel 4.5 Batas Deteksi dan Batas Kuantitasi Kalium, Natrium dan
DAFTAR GAMBAR
Halaman
Gambar 2.1 Gunung Sinabung ... 10
Gambar 2.2 Sistem Peralatan Spektrofotometri Serapan Atom ... 17
Gambar 4.1 Kurva Kalibrasi Kalium ... 33
Gambar 4.2 Kurva Kalibrasi Natrium ... 33
DAFTAR LAMPIRAN
Halaman
Lampiran 1. Hasil Identifikasi Tanaman ... 46
Lampiran 2. Foto Letusan Gunung Sinabung ... 47
Lampiran 3. Foto Sampel yang Digunakan ... 48
Lampiran 4. Foto Sampel Setelah di Hotplate dan Setelah di Tanur .. 49
Lampiran 5. Bagan Alur Proses Dekstruksi Kering ... 50
Lampiran 6. Bagan Alur Proses Pembutan Larutan Sampel ... 51
Lampiran 7. Data Kalibrasi Kalium dengan Spektrofotometer Serapan Atom, Perhitungan Persamaan Garis Regresi dan Koefisien Korelasi ... 52
Lampiran 8. Data Kalibrasi Natrium dengan Spektrofotometer Serapan Atom, Perhitungan Persamaan Garis Regresi dan Koefisien Korelasi ... 54
Lampiran 9. Data Kalibrasi Kalsium dengan Spektrofotometer Serapan Atom, Perhitungan Persamaan Garis Regresi dan Koefisien Korelasi ... 56
Lampiran 10. Hasil Analisis Kadar Kalium, Natrium dan Kalsium dalam Sampel ... 58
Lampiran 11. Contoh Perhitungan Kadar Kalium, Natrium Dan Kalsium dalam Sampel ... 64
Lampiran 12. Perhitungan Statistik Kadar Kalium dalam Sampel ... 66
Lampiran 13. Perhitungan Statistik Kadar Natrium dalam Sampel ... 75
Lampiran 14. Perhitungan Statistik Kadar Kalsium dalam Sampel ... 86
Lampiran 15. Pengujian Beda Nilai Rata-Rata Kalium dalam Sampel 95
Lampiran 17. Pengujian Beda Nilai Rata-Rata Kalsium dalam
Sampel ... 97
Lampiran 18. Hasil Analisis Kadar Kalium, Natrium dan Kalsium Sebelum Penambahan Masing-Masing Larutan Baku dalam Kubis ... 99
Lampiran 19. Hasil Analisis Kadar Kalium, Natrium dan Kalsium Setelah Penambahan Masing-Masing Larutan Baku dalam Kubis ... 101
Lampiran 20. Perhitungan Uji Perolehan Kembali Kalium, Natrium dan Kalsium ... 103
Lampiran 21. Perhitungan Simpangan Baku Relatif (RSD) Kalium, Natrium dan Kalsium dalam Sampel ... 121
Lampiran 22. Perhitungan Batas Deteksi dan Batas Kuantitasi ... 124
Lampiran 23. Gambar Alat yang Digunakan ... 127
Lampiran 24. Tabel Distribusi t ... 128
BAB I
PENDAHULUAN
1.1 Latar Belakang
Indonesia adalah negara yang kaya akan gunung api dan merupakan salah
satu negara yang terpenting dalam menghadapi masalah gunung api aktif. Tidak
kurang dari 30 gunung api aktif terdapat di Indonesia dengan lereng-lerengnya di
padati oleh pemukiman penduduk (Lucas, 1991). Salah satu gunung berapi yang
ada di Indonesia adalah Gunung Sinabung yang terletak di
2.460 m dari permukaan laut dan masih terdapat desa-desa di lerengnya. Gunung
Sinabung tidak pernah tercatat meletus sejak tahun 1.600 tetapi mendadak aktif
kembali pada bulan september 2013 (Anonim, 2014).
Hasil dari erupsi Gunung Sinabung tersebut mengeluarkan kabut asap
yang tebal berwarna hitam disertai hujan abu dan debu vulkanik yang menutupi
ribuan hektar lahan para petani. Debu vulkanik mengakibatkan tanaman petani
yang berada dilereng gunung banyak yang mati dan rusak. Debu vulkanik
berdampak pada beberapa desa yang ada disekitar Gunung Sinabung yaitu desa
Bekerah, desa Simacem, desa Beras Tepu, desa Suka Nalu, desa Suka Tepu, desa
Suka Ndebi, desa Ndeskati (BPTP Sumatera Utara, 2014).
Abu vulkanik adalah material vulkanik yang disemburkan ke udara saat
terjadi suatu letusan gunung berapi. Abu vulkanik terdiri dari batuan berukuran
besar sampai berukuran halus. Abu Vulkanik yang berukuran besar biasanya jatuh
pada jarak mencapai ratusan hingga ribuan kilometer (Sudaryo dan Sutjipto,
2009). Menurut Balai Teknik Kesehatan Lingkungan (BTKL) (1994), komposisi
kimia tanah abu vulkanik gunung merapi terdiri dari: SiO2 (54,56%), Al2O3
(18,37%), Fe2O3 (18,59%), CaO (8,33%), MgO (2,45%), Na2O (3,62%), K2O
(2,32%), MnO (0,17%), TiO2 (0,92%), P2O6 (0,32%), dan H2O (0,11).
Kimia tanah abu vulkanik K2O, Na2O, dan CaO akan mempengaruhi
perkembangan sektor pertanian terutama tanaman yang ada di sekitar gunung
tersebut. Salah satu tanaman yang banyak terdapat adalah sayuran kubis atau kol
yang merupakan sayuran yang termasuk jenis Brassica olaracea, yang dapat
membentuk telur seperti kepala. Sayuran kubis mempunyai peranan yang penting
untuk kesehatan manusia karena cukup banyak mengandung vitamin dan mineral
yang sangat diperlukan tubuh manusia (Pracaya, 1992).
Mineral merupakan salah satu unsur yang memegang peranan penting
dalam pemeliharaan fungsi tubuh, baik pada tingkat sel, jaringan, organ maupun
fungsi tubuh secara keseluruhan. Mineral digolongkan ke dalam mineral makro
dan mineral mikro. Mineral makro adalah mineral yang dibutuhkan tubuh dalam
jumlah lebih dari 100 mg sehari. Termasuk kedalam mineral makro adalah
natrium, klorida, kalium, kalsium, fosfor, magnesium dan sulfur. (Almatsier,
2004; Budiyanto, 2001).
Berdasarkan uraian di atas, maka penulis tertarik untuk meneliti kajian
kandungan mineral kalium, natrium dan kalsium pada sayuran kubis yang
diperoleh dari lahan hasil pertanian pasca letusan Gunung Sinabung secara
1.2 Perumusan Masalah
Berdasarkan uraian di atas, maka permasalahan pada penelitian ini adalah
1. Berapa kandungan mineral kalium, natrium dan kalsium pada sayuran
kubis yang diperoleh dari lahan hasil pertanian pasca letusan Gunung
Sinabung
2. Apakah ada perbedaan kandungan mineral kalium, natrium dan kalsium
pada sayuran kubis yang diperoleh dari lahan hasil pertanian pasca letusan
Gunung Sinabung yang terdapat di beberapa desa.
1.3 Hipotesis
Hipotesis dalam penelitian ini adalah
1. Sayuran kubis mengandung mineral kalium, natrium dan kalsium dalam
jumlah tertentu.
2. Terdapat perbedaan kandungan mineral kalium, natrium dan kalsium pada
sayuran kubis yang diperoleh dari lahan hasil pertanian pasca letusan
Gunung Sinabung yang terdapat di beberapa desa.
1.4 Tujuan Penelitian
Tujuan penelitian ini adalah
1. Untuk mengetahui kandungan mineral kalium, natrium dan kalsium pada
sayuran kubis yang diperoleh dari lahan hasil pertanian pasca letusan
2. Mengetahui perbedaan kandungan mineral kalium, natrium dan kalsium
pada sayuran kubis yang diperoleh dari lahan hasil pertanian pasca letusan
Gunung Sinabung yang terdapat di beberapa desa.
1.5 Manfaat Penelitian
1. Memberikan informasi kepada masyarakat tentang kandungan mineral
kalium, natrium dan kalsium pada sayuran kubis yang diperoleh dari
lahan hasil pertanian pasca letusan Gunung Sinabung yang terdapat di
BAB II
TINJAUAN PUSTAKA
2.1 Gunung Berapi
Bentuk permukaan bumi tidaklah merata. Hal ini disebabkan karena
adanya pengaruh dari luar dan dalam bumi itu sendiri. Pengaruh dari dalam bumi
berupa tenaga yang sangat besar sehingga dapat membentuk muka bumi beraneka
ragam. Tenaga yang berasal dari dalam bumi ini disebut endogen, contoh
tektonisme, vulkanisme, dan seisme. Sedangkan tenaga yang berasal dari luar
bumi disebut eksogen, conroh pelapukan dan erosi pengikisan. Karena tenaga
endogen inilah, akhirnya terbentuk sebuah gunung. Gunung merupakan tonjolan
pada kulit bumi yang terdiri dari lereng dan puncak (Hartuti, 2009).
Rangkaian dari gunung-gunung akan membentuk pegunungan. Gunung
dan pegunungan terbentuk karena adanya tenaga endogen. Apabila suatu tempat
di permukaan bumi pernah atau masih mengeluarkan magma, maka terbentuklah
gunung berapi. Gunung berapi atau gunung api secara umum adalah istilah yang
didefinisikan sebagai suatu saluran fluida panas (batuan dalam wujud cair atau
lava) yang memanjang dari kedalaman sekitar 10 km di bawah permukaan bumi
sampai ke permukaan bumi, termasuk endapan hasil akumulasi material yang
dikeluarkan saat meletus. Secara singkat, gunung berapi adalah gunung yang
masih aktif dalam mengeluarkan material di dalamnya (Hartuti, 2009).
2.1.1 Jenis Gunung Berapi Berdasarkan Bentuknya
Tersusun dari batuan hasil letusan dengan tipe letusan berubah – ubah
sehingga dapat menghasilkan susunan yang berlapis – lapis dari beberapa jenis
batuan, sehingga membentuk suatu kerucut besar (raksasa), kadang – kadang
bentuknya tidak beraturan, karena letusan terjadi sudah beberapa ratus kali.
b. Gunung berapi perisai (Shieldvolcano)
Tersusun dari batuan aliran lava yang pada saat diendapkan masih cair,
sehingga tidak sempat membentuk suatu kerucut yang tinggi (curam),
bentuknya akan berlereng landai, dan susunannya terdiri dari batuan yang
bersifat basaltik. Contoh bentuk gunung berapi ini terdapat di kepulauan
Hawai.
c. Cinder Cone
Merupakan gunung berapi yang abu dan pecahan kecil batuan vulkanik
menyebar di sekeliling gunung. Sebagian besar gunung jenis ini membentuk
mangkuk di puncaknya. Jarang yang tingginya diatas 500 meter dari tanah di
sekitarnya.
d. Kaldera
Gunung berapi jenis ini terbentuk dari ledakan yang sangat kuat yang
melempar ujung atas gunung sehingga membentuk cekungan. Gunung Bromo
merupakan jenis ini.
2.1.2 Klasifikasi Gunung Berapi di Indonesia
a. Gunung Berapi Tipe A
Gunung berapi yang pernah mengalami erupsi magmatik
b. Gunung Berapi Tipe B
Gunung berapi yang sesudah tahun 1600 belum lagi mengadakan erupsi
magmetik, namun masih memperlihatkan gejala kegiatan seperti kegiatan
solfatara.
c. Gunung Berapi Tipe C
Gunung berapi yang erupsinya tidak diketahui dalam sejarah manusia,
namun masih terdapat tanda-tanda kegiatan masa lampau berupa lapangan
solfatara/fumarola pada tingkat lemah.
2.1.3 Gunung Berapi Meletus
Gunung berapi meletus merupakan peristiwa yang terjadi akibat endapan
magma di dalam perut bumi yang didorong keluar oleh gas yang bertekanan
tinggi. Magma adalah cairan pijar yang terdapat di dalam lapisan bumi dengan
suhu yang sangat tinggi, yakni diperkirakan lebih dari 1000 0C. Cairan magma
yang keluar dari dalam bumi disebut lava. Suhu lava yang dikeluarkan bisa
mencapai 700-1200 0C. Letusan gunung berapi yang membawa batu dan abu
dapat menyembur sampai sejauh radius 18 km atau lebih, sedangkan lavanya bisa
membanjiri sampai sejauh radius 90 km. Tidak semua gunung merapi sering
meletus. Gunung berapi yang sering meletus disebut gunung berapi aktif (Hartuti,
2009).
2.1.4 Ciri – Ciri Gunung Berapi Meletus
Menurut Hartuti (2009), Gunung berapi yang meletus dapat diketahui
melalui beberapa tanda, antara lain
a. Suhu di sekitar gunung naik.
c. Sering mengeluarkan suara gemuruh, kadang disertai getaran (gempa)
d. Tumbuhan di sekitar gunung layu
e. Binatang di sekitar gunung bermigrasi.
2.1.5 Status Gunung Berapi
Gunung berapi biasanya akan diberi status oleh para pengamat
kegunungapian. Hal ini dilakukan untuk mengetahui sejauh mana suatu gunung
sedang berproses.
Berikut beberapa status dari gunung berapi yang digunakan sebagai isyarat
keadaan suatu gunung.
Status Makna Tindakan
AWAS • Menandakan gunung berapi
akan segera atau sedang meletus atau dalam keadaan kritis yang menimbulkan bencana.
• Letusan pembukaan dimulai dengan keluarnya abu dan asap.
• Letusan berpeluang terjadi dalam waktu 24 jam.
• Wilayah yang terancam bahaya direkomendasikan untuk dikosongkan.
• Koordinasi dilakukan secara harian.
• Diadakan piket penuh dan terus-menerus.
SIAGA • Menandakan gunung berapi yang sedang bergerak menuju letusan.
• Peningkatan intensif kegiatan seismik.
• Semua data menunjukkan bahwa aktivitas dapat segera berlanjut ke letusan atau menuju pada keadaan yang dapat menimbulkan bencana.
• Jika terjadi peningkatan berlanjut, letusan dapat terjadi dalam waktu 2 minggu.
• Sosialisasi di wilayah terancam.
• Penyiapan sarana darurat.
• Koordinasi harian.
WASPADA • Gunung selalu melakukan aktivitas dalam bentuk apa pun.
• Terdapat kenaikan aktivitas di atas level normal.
• Peningkatan aktivitas vulkanis.
• Sedikit perubahan aktivitas yang diaki- batkan oleh aktivitas magma, tektonik, dan hidrotermal.
• Penyuluhan/sosialis asi.
• Penilaian bahaya.
• Pengecekan sarana.
• Pelaksanaan Piket terbatas.
NORMAL • Tidak ada gejala adanya aktivitas tekanan magma.
• Level aktivitas masih pada posisi dasar.
• Pengamatan rutin.
• Survei dan Penyelidikan
(Hartuti, 2009)
2.2 Gunung Sinabung
Gunung Sinabung merupakan salah satu gunung di dataran tinggi
Kabupaten Karo, Sumatera Utara, Indonesia. Koordinat puncak Gunung Sinabung
adalah 03o 10’ LU dan 98o 23’ BT dengan puncak tertinggi gunung ini adalah
2.460 meter dari permukaan laut yang menjadi puncak tertinggi di Sumatera
Utara. Gunung ini belum pernah tercatat meletus sejak tahun 1600 (Anonim,
2014).
Abu vulkanik atau pasir vulkanik merupakan bahan material vulkanik
jatuhan yang disemburkan ke udara saat terjadi letusan. Abu vulkanik maupun
pasir vulkanik terdiri dari batuan berukuran besar sampai berukuran halus, yang
berukuran besar biasanya jatuh disekitar kawah sampai radius 5-7 km dari kawah,
kilometer dari kawah disebabkan oleh adanya hembusan angin (Sudaryo dan
Sutjipto, 2009).
Gambar 1. Letusan Gunung Sinabung (Tanggal 1 Februari 2014)
Menurut Balai Teknik Kesehatan Lingkungan (BTKL), (1994) komposisi
kimia tanah abu vulkanik gunung merapi yaitu SiO2 (54,56%), Al2O3 (18,37%),
Fe2O3 (18,59%), CaO (8,33%), MgO (2,45%), Na2O (3,62%), K2O (2,32%), MnO
(0,17%), TiO2 (0,92%), P2O6 (0,32%), dan H2O (0,11%).
2.3 Kubis
Tanaman kubis berasal dari Eropa dan Asia, terutama tumbuh di daerah
Great Britain dan Mediteranean. Asal usul tanaman kubis dibudidaya berawal dari
kubis liar (Brassica oleracea var. sylvestris) yang tumbuh di sepanjang pantai laut
tengah, Inggris, Denmark dan sebelah utara Perancis barat serta pantai Glamorgan
(Rukmana, 1994).
Yang dimaksud kubis disini ialah kubis yang dapat membentuk telur yang
hipokotil yang berwarna merah, panjang beberapa centimeter, dua keping, akar
tunggang. Daun pertama mempunyai tungkai yang panjang dan tangkai-tangkai
daun selanjutnya makin memendek, kemudian daun mementuk roset dan daun
kubis tidak berbulu tapi tertutup lapisan lilin. Daun-daun yang pertama akan
membengkok dapat mencapai panjang lebih kurang 30 cm. Daun-daun yang
berikutnya mulai membengkok dan membungkus atau menutupi daun-daun muda
yang terbentuk kemudian, makin lama dan makin banyak daun muda yang
terbantuk maka akan kelihatan seakan-akan membentuk telur atau kepala. Bentuk
kepala atau telur bermacam-macam, dari bentuk bulat, bulat pipih sampai bulat
meruncing, dan garis tengah dapat mencapai lebih dari 20 cm (Pracaya, 1992).
Kubis termasuk tanaman sayuran semusim yang dipanen sekaligus dan
dikonsumsi dari bagian tamanan yang berupa daun yang berumur kurang dari 1
tahun dan pemanenannya dilakukan sekali kemudian dibongkar untuk diganti
dengan tanaman baru (Vincent, 1998).
2.3.1 Klasifikasi
Menurut Pracaya (1992), klasifikasi tumbuhan kubis (Brassica oleracea
var. capitata) secara sistematik adalah sebagai berikut:
Nama Lokal : Kubis
Dunia (kingdom) : Plantae
Superdivisi (Superdivisi) : Spermatophyta
Divisi (divisi) : Magnoliophyta
Kelas (classis) : Magnoliopsida
Bangsa (ordo) : Capparales
Marga (genus) :
Jenis (Spesies) : Brassica oleracea var. capitata L.
2.3.2 Varietas dan Jenis
Menurut Novery (1999), Kubis merupakan tanaman sayur yang terdiri dari
banyak varietas. Namun, secara umum kubis terbagi dalam 3 kelompok besar
yaitu kubis putih, kubis merah, dan kubis savoy.
1. Kubis putih (B.oleracea. var. capitata L. f. alba DC)
Kubis dari kelompok ini daunya berwarna putih. Dalam kelompok ini
terdiri dari kubis kepala bulat atau kol bulat, kubis kepala bulat datar, dan
kubis kepala bulat runcing.
2. Kubis merah (B.oleracea. var. capitata L.f. rubra)
Sesuai dengan namanya, daun kubis merah berwarna merah keunguan. Di
bagian daun sebelah luar terdapat lapisan lilin. Pada umumnya kubis
merah mempunyai bentuk kepala bulat.
3. Kubis savoy (B.oleracea. var. sabauda L.)
Kubis savoy mempunyai daun yang khas, yaitu kriting. Oleh karena itu,
sebutan lain dari kubis savoy adalah kubis keriting atau kubis babat.
Namun, kubis jenis ini belum popular dan belum terlalu disukai
konsumen, mungkin karena rasanya belum cocok dengan lidah.
Beberapa waktu terakhir muncul jenis kubis baru, yaitu kubis brussel atau
kol brussel (Brassica oleracea var. gemnifera). Kubis jenis ini sering disebut juga
kubis tunas. Bentuknya sama persis dengan kubis kepala, tetapi ukurannya lebih
kecil dan lebih padat. Tanaman kubis jenis ini pertama diusahakan di Belgia,
2.3.3 Kandungan Gizi
Kubis putih mengandung: kalori, karbohidrat, lemak, protein, serat makanan,
vitamin-vitamin; A, B1, B2, B3 dan C, mineral; besi, khlor, fosfor, kalsium,
Kalium, natrium dan zat besi. Dalam 100 g bahan mentah kubis terdapat 24 kalori
(Novery, 1999; Soehardi, 2004).
Menurut Calvin dan Donald (1983) dalam 100 g kubis putih memiliki
kandungan gizi, yaitu: Air (92,4%); Energi (24 kalori); Protein (1,3 g); Lemak
(0,2 g); Karbohidrat (5,4 g); Serat (0,8 g); Kalsium (49 mg); Fosfor (29 mg); Besi
(0,4 mg); Natrium (20 mg); Kalium (233 mg); Vitamin A (130 IU); Vitamin B1
(0,05 mg); Vitamin B2 (0,05 mg); Vitamin B3 (0,3 mg), Vitamin C (47 mg).
2.4 Mineral
Menurut Budiyanto (2004), mineral merupakan salah satu komponen yang
sangat diperlukan oleh mahluk hidup di samping karbohidrat, lemak, protein, dan
vitamin, juga dikenal sebagai zat anorganik atau kadar abu. Berdasarkan jenisnya,
mineral dibagi 2 macam, yaitu:
a) Makromineral (kalsium, Alluminium, Magnesium, fosfor, kalium, natrium
dan sulfur)
b) Mikromineral (besi, iodium, flour, Mangan, zink, kuprum, kobalt dan
kromium).
Menurut almatsier, mineral adalah unsur atau senyawa kimia yang ada
yang dibutuhkan tubuh untuk menjaga kesehatan. Mineral adalah bagian dari
tubuh yang memegang peranan penting dalam pemeliharaan fungsi tubuh, baik
pada tingkat sel, jaringan, organ maupun fungsi tubuh secara keseluruhan. Di
samping itu, mineral berperan dalam berbagai tahap metabolisme, terutama
sebagai kofaktor dalam aktivitas enzim-enzim (Almatsier, 2004).
Mineral digolongkan kedalam mineral makro dan mineral mikro. Mineral
makro adalah mineral yang ada di dalam tubuh lebih dari 0,01% berat badan dan
mineral yang dibutuhkan tubuh dalam jumlah lebih dari 100 mg/hari, sedangkan
mineral mikro terdapat dalam tubuh kurang dari 0,01% berat badan dan mineral
yang dibutuhkan kurang dari 100 mg/hari. Yang termasuk mineral makro adalah
natrium, kalium, kalsium, fosfor, magnesium, dan sulfur. Adapun yang termasuk
mineral mikro adalah besi, seng, mangan, dan tembaga (Almatsier, 2004).
2.4.1 Kalium
Kalium merupakan salah satu mineral makro yang berperan dalam
pengaturan keseimbangan cairan dan elektrolit serta keseimbangan asam basa
tubuh. Sebanyak 95% kalium berada di dalam cairan intraseluler. Sumber utama
kalium adalah sayuran, buah dan kacang-kacangan. Kekurangan kalium karena
makanan jarang terjadi, sepanjang seseorang cukup makan sayuran dan buah segar
(Almatsier, 2004).
2.4.2 Natrium
Natrium adalah kation utama dalam darah dan cairan ekstraselular. Fungsi
natrium di dalam tubuh bersama-sama dengan kalium menjaga keseimbangan
cairan di dalam tubuh dan sebagai penghantar impuls dalam serabut syaraf.
sedangkan di dalam cairan ekstraseluler 28:1. Sumber utama natrium adalah
garam dapur (Almatsier,2004).
2.4.3 Kalsium
Kalsium merupakan mineral yang paling banyak terdapat di dalam tubuh,
yaitu 1,5 - 2% dari berat badan orang dewasa atau kurang lebih sebanyak 1 kg.
Dari jumlah ini, sebanyak 99% berada di dalam jaringan keras, yaitu tulang dan
gigi, selebihnya tersebar luas didalam tubuh. Didalam cairan ekstraselular dan
intraselular, kalsium memegang peranan penting dalam mengatur fungsi sel,
seperti untuk transmisi saraf, kontraksi otot, penggumpalan darah, dan menjaga
permeabilitas membran sel (Almatsier, 2004).
Sumber kalsium utama adalah susu dan hasil olahan susu seperti keju. Ikan
yang dimakan dengan tulang, termasuk ikan kering merupakan sumber kalsium
yang baik. Kacang-kacangan dan hasil kacang-kacangan, tahu, tempe, serta
sayuran hijau merupakan sumber kalsium yang baik (Almatsier, 2004).
2.5 Spektrofotometer Serapan Atom
Spektrofotometri serapan atom digunakan untuk analisis kuantitatif
unsur-unsur logam dalam jumlah kecil (trace) dan sangat kecil (ultratrace). Cara
analisis ini memberikan kadar total unsur logam dalam suatu sampel dan tidak
tergantung pada bentuk molekul dari logam dalam sampel tersebut. Cara ini cocok
untuk analisis kecil logam karena mempunyai kepekaan yang tinggi (batas deteksi
kurang dari 1 ppm), pelaksanaannya relatif sederhana, dan interferensinya sedikit
Spektrofotometri serapan atom didasarkan pada penyerapan energi sinar
oleh atom-atom netral atau absorbsi cahaya oleh atom. Atom-atom akan menyerap
cahaya pada panjang gelombang tertentu, tergantung pada sifat. Jika suatu larutan
yang mengandung suatu garam logam (atau suatu senyawa logam) dihembuskan
kedalam suatu nyala (misalnya asetilena yang terbakar di udara) maka terbentuk
uap yang mengandung atom-atom logam itu. Atom logam bentuk gas tersebut
tetap berada dalam keadaan tak tereksitasi atau dengan perkataan lain, dalam
keadaan dasar. Jadi jika cahaya dengan panjang gelombang yang khas dengan
logam tersebut dilewatkan nyala yang mengandung atom-atom yang
bersangkutan, maka cahaya tersebut akan diserap dan jauhnya penyerapan akan
berbanding lurus dengan banyaknya atom keadaan dasar yang berada dalam nyala
(Gandjar dan Rohman, 2009).
Dengan menyerap energi, maka atom akan memperoleh energi sehingga
suatu atom dalam keadaan dasar dapat ditingkatkan menjadi ke tingkat eksitasi
dan garis-garis spektrum serapan atom yang timbul karena serapan sinar yang
menyebabkan eksitasi atom dari keadaan azas ke salah satu tingkat energi yang
lebih tinggi disebut garis-garis resonansi (resonance line). Garis-garis ini akan
dibaca dalam bentuk angka oleh Readout. (Gandjar dan Rohman, 2009; Bassett,
dkk., 1994).
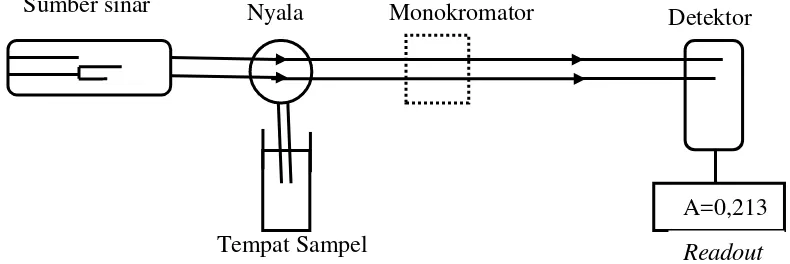
2.5.1 Instrument Spektrofotometer Serapan Atom
Sistem peralatan spektrofotometer serapan atom dapat dilihat pada gambar
Gambar 2. Sistem Peralatan Spektrofotometer Serapan Atom (sumber: Watson,1999)
a. Sumber sinar
Sumber sinar yang lazim dipakai adalah lampu katoda berongga (hollow
catodhe lamp). Lampu ini terdiri atas tabung kaca tertutup yang mengandung
suatu katoda dan anoda. Katoda sendiri berbentuk silinder berongga yang terbuat
dari logam atau dilapisi dengan logam tertentu.
b. Tempat sampel
Dalam analisis dengan spektrofotometri serapan atom, sampel yang akan
dianalisis harus diuraikan menjadi atom-atom netral yang masih dalam keadaan
dasar.
c. Monokromator
Pada spektrofotometri serapan atom, monokromator dimaksudkan untuk
memisahkan dan memilih panjang gelombang yang digunakan untuk analisis.
Sumber sinar Nyala Monokromator
Detektor
Readout
Tempat Sampel
d. Detektor
Detektor digunakan untuk mengukur intensitas cahaya yang melalui tempat
pengatoman.
e. Readout
Readout merupakan suatu sistem pencatatan hasil yang berupa hasil
pembacaan. Hasil pembacaan dapat berupa angka atau kurva.
2.5.2 Gangguan-gangguan pada Spektrofotometri Serapan Atom
Gangguan-ganguan pada SSA adalah peristiwa-peristiwa yang
menyebabkan pembacaan absorbansi unsur yang dianalisis menjadi lebih kecil
atau lebih besar dari nilai yang sesuai dengan konsentrasinya dalam sampel.
Gangguan-gangguan yang dapat terjadi dalam SSA adalah sebagai berikut
(Gandjar dan Rohman, 2009):
a. Gangguan yang berasal dari matriks sampel yang dapat mempengaruhi
banyaknya sampel yang mencapai nyala.
Sifat-sifat tertentu matriks sampel dapat mengganggu analisis yakni matriks
tersebut dapat berpengaruh terhadap laju aliran bahan bakar gas pengoksidasi.
Sifat-sifat tersebut adalah viskositas, tegangan permukaan, berat jenis dan
tekanan uap. Gangguan matriks yang lain adalah pengendapan unsur yang
dianalisis sehingga jumlah atom yang mencapai nyala menjadi lebih sedikit
dari konsentrasi yang seharusnya yang terdapat dalam sampel.
b. Gangguan kimia yang dapat mempengaruhi jumlah/banyaknya atom yang
terjadi di dalam nyala.
Terbentuknya atom-atom netral yang masih dalam keadaan dasar di dalam
senyawa-senyawa yang tidak sempurna dan ionisasi atom-atom di dalam nyala. Terjadi
disosiasi yang tidak sempurna disebabkam oleh terbentuknya senyawa-
senyawa yang bersifat refraktorik (sukar diuraiakan di dalam nyala api).
Contoh senyawa refraktorik adalah garam-garam fosfat, silikat, aluminat dari
logam alkali tanah. Dengan terbentuknya senyawa ini, maka akan mengurangi
jumlah atom netral yang ada di dalam nyala. Ionisasi atom-atom di dalam
nyala dapat terjadi jika suhu yang digunakan untuk atomisasi terlalu tinggi.
Prinsip analisis dengan SSA adalah mengukur absorbansi atom-atom netral
yang berada dalam keadaan dasar. Jika terbentuk ion maka akan mengganggu
pengukuan absorbansi atom netral karena atom-atom yang mengalami
ionisasi tidak sama spektrum atom dalam keadaan netral.
c. Gangguan oleh absorbansi yang disebabkan bukan oleh absorbansi atom yang
dianalisis yakni; absorbansi oleh molekul-molekul yang tidak terionisasi di
dalam nyala.
d. Gangguan oleh penyerapan non-atomik (non atomic absorption) Gangguan
jenis ini berarti terjadinya penyerapan cahaya dari sumber sinar yang bukan
berasal dari atom-atom yang akan dianalisis. Penyerapan non atomik dapat
disebabkan oleh adanya penyerapan cahaya oleh partikel-partikel padat yang
berada di dalam nyala.
2.6 Vaidasi Metode Analisis
Menurut Harmita (2004), validasi metode analisis adalah suatu tindakan
penilaian terhadap parameter tertentu berdasarkan percobaan laboratorium untuk
penggunaannya. Beberapa parameter analisis yang harus dipertimbangkan dalam
validasi metode analisis adalah sebagai berikut:
a. Kecermatan
Menurut Harmita (2004), kecermatan adalah ukuran yang menunjukkan
derajat kedekatan hasil analisis dengan kadar analit yang sebenarnya. Kecermatan
dinyatakan sebagai persen perolehan kembali (recovery) analit yang
ditambahkan. Kecermatan ditentukan dengan dua cara, yaitu:
- Metode simulasi
Metode simulasi (Spiked-placebo recovery) merupakan metode yang
dilakukan dengan cara menambahkan sejumlah analit bahan murni ke dalam
suatu bahan pembawa sediaan farmasi (plasebo), lalu campuran tersebut
dianalisis dan hasilnya dibandingkan dengan kadar analit yang ditambahkan
(kadar yang sebenarnya) (Harmita, 2004).
- Metode penambahan baku
Metode penambahan baku (standard addition method) merupakan metode
yang dilakukan dengan cara menambahkan sejumlah analit dengan konsentrasi
tertentu pada sampel yang diperiksa, lalu dianalisis dengan metode yang akan
divalidasi. Hasilnya dibandingkan dengan sampel yang dianalisis tanpa
penambahan sejumlah analit. Persen perolehan kembali ditentukan dengan
menentukan berapa persen analit yang ditambahkan ke dalam sampel dapat
ditemukan kembali.
Keseksamaan atau presisi diukur sebagai simpangan baku relatif atau
koefisien variasi. Keseksamaan atau presisi merupakan ukuran yang menunjukkan
derajat kesesuaian antara hasil uji individual ketika suatu metode dilakukan secara
berulang untuk sampel yang homogen.
c. Selektivitas (Spesifisitas)
Selektivitas atau spesifisitas suatu metode adalah kemampuannya yang hanya
mengukur zat tertentu secara cermat dan seksama dengan adanya komponen lain
yang ada di dalam sampel.
d. Linearitas dan rentang
Linearitas adalah kemampuan metode analisis yang memberikan respon baik
secara langsung maupun dengan bantuan transformasi matematika, menghasilkan
suatu hubungan yang proporsional terhadap konsentrasi analit dalam sampel.
Rentang merupakan batas terendah dan batas tertinggi analit yang dapat
ditetapkan secara cermat, seksama dan dalam linearias yang dapat diterima.
e. Batas deteksi (Limit of detection) dan batas kuantitasi (Limit of quantitation)
Batas deteksi merupakan jumlah terkecil analit dalam sampel yang dapat
dideteksi yang masih memberikan respon signifikan, sedangkan batas kuantitasi
merupakan kuantitas terkecil analit dalam sampel yang masih dapat memenuhi
BAB III
METODE PENELITIAN
3.1 Tempat dan Waktu Penelitian
Penelitian ini dilakukan di Laboratorium Penelitian Fakultas Farmasi
Universitas Sumatera Utara Medan pada bulan Maret – Juli 2014.
3.2 Alat dan Bahan
3.2.1 Alat
Alat yang digunakan adalah Spektrofotometer Serapan Atom (Hitachi
Z-2000) lengkap dengan Lampu katoda kalium, natrium dan kalsium, neraca analitik
(BOECO Germany), hot plate 0 oC – 450 oC (MSH 420 BOECO Germany), alat
tanur (Nabertherm), blender, kertas saring Whatman No.42, krus porselen dan
alat-alat gelas (Pyrex).
3.2.2 Bahan
3.2.2.1 Sampel
Sampel yang digunakan dalam penelitian ini adalah sayuran kubis
(Brassica oleracea L.) dari lahan hasil pertanian pasca letusan gunung sinabung
yang di ambil di empat desa yaitu desa Suka Ndebi, desa Suka Tepu, desa
Ndeskati kecamatan Naman Teran, Kabupaten Karo, Sumatra Utara, Indonesia
dan Desa Raya, kecamatan Brastagi, Kabupaten Karo, Sumatra Utara.
3.2.2.2 Identifikasi Sampel
Identifikasi tanaman kubis (Brassica oleracea L.) dilakukan di Pusat
3.2.2.3 Pereaksi
Semua bahan yang digunakan dalam penelitian ini yaitu akua
demineralisata, asam nitrat (HNO3) 65% b/v, larutan baku kalium 1000 µg/ml,
larutan baku natium 1000 µg/ml, dan larutan baku kalsium 1000 µg/ml
(Laboratorium Penelitian Fakultas Farmasi USU).
3.3 Pembuatan Pereaksi
3.3.1 Larutan HNO3 (1:1)
Sebanyak 250 ml larutan HNO3 65% b/v diencerkan dengan 250 ml
akuademineralisata.
3.4 Prosedur Penelitian
3.4.1 Pengambilan Sampel
Metode pengambilan sampel dilakukan dengan cara sampling purposif
yang dikenal juga sebagai sampling pertimbangan. Metode sampling ini
ditentukan atas dasar pertimbangan bahwa sampel yang diambil dapat mewakili
populasi (Budiarto, 2004).
3.4.2 Penyiapan Sampel
Kubis sebanyak ± 1 kg ( yang tidak ditentukan kadar airnya ) dicuci bersih
dengan air mengalir untuk membarsihkannya dari pengotoran dan dicuci lagi
dengan aquades, ditiriskan sampai air cuciannya kering. Sampel dibelah menjadi
dua bagian dan diblender sampai halus. Perlakuan yang sama juga dilakukan
3.4.3 Proses Dekstruksi
Proses destruksi sampel dilakukan dengan cara destruksi kering dimana
sampel yang telah dihaluskan, ditimbang sebanyak 25 gram dalam kurs porselen,
diarangkan di atas hot plate (MSH 420 BOECO Germany), lalu diabukan dalam
tanur dengan temperatur awal 100ºC dan perlahan-lahan temperatur dinaikkan
hingga suhu 500 ºC dengan interval 25 ºC setiap 5 menit. Pengabuan dilakukan
selama 48 jam (dihitung saat suhu sudah 500 ºC), lalu setelah suhu tanur ± 27 ºC,
krus porselen dikeluarkan dan dibiarkan hingga dingin pada desikator. Abu
ditambahkan 5 ml HNO3 (1 : 1), kemudian diuapkan pada hot plate (MSH 420
BOECO Germany) sampai kering. Kurs porselen dimasukkan kembali ke dalam
tanur dengan temperatur awal 100 ºC dan perlahan-lahan temperatur dinaikkan
hingga 500 ºC dengan interval 25 ºC setiap 5 menit. Pengabuan dilakukan selama
1 jam dan dibiarkan hingga dingin pada desikator (Howirtz, 2000).
3.4.4 Pembuatan Larutan Sampel
Sampel hasil dekstruksi dilarutkan dalam 5 ml HNO3 (1 : 1), lalu
dipindahkan ke dalam labu tentukur 50 ml, dibilas kurs porselen dengan 10 ml
akua demineralisata sebanyak 3 kali dan dicukupkan dengan akua demineralisata
hingga garis tanda. Kemudian disaring dengan kertas saring Whatman No.42
dimana 5 ml filtrat pertama dibuang untuk menjenuhkan kertas saring kemudian
filtrat selanjutnya ditampung ke dalam botol (Howirtz, 2000). Larutan ini
digunakan untuk analisis kualitatif dan kuantitatif terhadap mineral kalium,
3.4.5 Pemeriksaan Kualitatif dan Kuantitatif 3.4.5.1 Kalium
3.4.5.1.1 Pembuatan Kurva Kalibrasi Kalium
Larutan baku kalium (1000 µg/ml) sebanyak 1 ml dimasukan ke dalam
labu tentukur 100 ml lalu dicukupkan hingga garis tanda dengan akua
demineralisata. Dari konsentrasi 10 µg/ml dipipet masing-masing 5 ml; 10 ml; 15
ml; 20 ml; dan 25 ml, dimasukkan ke dalam labu tentukur 25 ml dan dicukupkan
hingga garis tanda dengan akua demineralisata sehingga diperoleh larutan dengan
konsentrasi 2,0 µg/ml; 4,0 µg/ml; 6,0 µg/ml; 8,0 µg/ml; dan 10,0 µg/ml. Diukur
absorbansi pada panjang gelombang 766,5 nm dengan tipe nyala udara-asetilen.
3.4.5.1.2 Penetapan Kadar Kalium dalam Sampel
Larutan sampel kubis hasil dekstruksi dipipet sebanyak 1 ml dimasukkan
ke dalam labu tentukur 50 ml dan dicukupkan dengan akua demineralisata hingga
garis tanda. Kemudian dari 50 ml dipipet 2,5 ml dimasukkan ke dalam labu
tentukur 25 ml. (Faktor Pengenceran = 50 ml/1 ml x 25 ml/2,5 ml = 500 kali).
Lalu diukur absorbansinya dengan menggunakan spektrofotometer serapan atom
pada panjang gelombang 766,5 nm dengan nyala udara-asetilen. Nilai absorbansi
yang diperoleh harus berada dalam rentang kurva kalibrasi larutan baku kalium.
Konsentrasi kalium dalam sampel dihitung berdasarkan persamaan garis regresi
dari kurva kalibrasi.
3.4.5.2 Natrium
3.4.5.2.1 Pembuatan Kurva Kalibrasi Natrium
Larutan baku Natrium (1000 µg/ml) sebanyak 0,5 ml dimasukan ke dalam
labu tentukur 50 ml lalu dicukupkan hingga garis tanda dengan akua
1,5 ml; 2,0 ml; dan 2,5 ml, dimasukkan ke dalam labu tentukur 25 ml dan
dicukupkan hingga garis tanda dengan akua demineralisata sehingga diperoleh
larutan dengan konsentrasi 0,2 µg/ml; 0,4 µg/ml; 0,6 µg/ml; 0,8 µg/ml; dan 1,0
µg/ml. Diukur absorbansi pada panjang gelombang 589,0 nm dengan tipe nyala
udara-asetilen.
3.4.5.2.2 Penetapan Kadar Natrium dalam Sampel
Larutan sampel kubis hasil dekstruksi dipipet sebanyak 0,5 ml dimasukkan
ke dalam labu tentukur 50 ml dan dicukupkan dengan akua demineralisata hingga
garis tanda (Faktor Pengenceran = 50 ml/0,5 ml = 100 kali). Lalu diukur
absorbansinya dengan menggunakan spektrofotometer serapan atom pada panjang
gelombang 589,0 nm dengan nyala udara-asetilen. Nilai absorbansi yang
diperoleh harus berada dalam rentang kurva kalibrasi larutan baku natrium.
Konsentrasi natrium dalam sampel dihitung berdasarkan persamaan garis regresi
dari kurva kalibrasi.
3.4.5.3 Kalsium
3.4.5.3.1 Pembuatan Kurva Kalibrasi Kalsium
Larutan baku kalsium (1000 µg/ml) sebanyak 1 ml dimasukan ke dalam
labu tentukur 100 ml lalu dicukupkan hingga garis tanda dengan akua
demineralisata. Dari konsentrasi 10 µg/ml dipipet masing-masing 5 ml; 10 ml; 15
ml; 20 ml; dan 25 ml, dimasukkan ke dalam labu tentukur 25 ml dan dicukupkan
hingga garis tanda dengan akua demineralisata sehingga diperoleh larutan dengan
konsentrasi 2,0 µg/ml; 4,0 µg/ml; 6,0 µg/ml; 8,0 µg/ml; dan 10,0 µg/ml. Diukur
3.4.5.3.2 Penetapan Kadar Kalsium dalam Sampel
Larutan sampel kubis hasil dekstruksi dipipet sebanyak 2,5 ml dimasukkan
ke dalam labu tentukur 50 ml dan dicukupkan dengan akua demineralisata hingga
garis tanda (Faktor Pengenceran = 50 ml/2,5 ml = 20 kali). Lalu diukur
absorbansinya dengan menggunakan spektrofotometer serapan atom pada panjang
gelombang 589,0 nm dengan nyala udara-asetilen. Nilai absorbansi yang
diperoleh harus berada dalam rentang kurva kalibrasi larutan baku kalsium.
Konsentrasi kalsium dalam sampel dihitung berdasarkan persamaan garis regresi
dari kurva kalibrasi.
Menurut Gandjardan Rohman (2007), kadar logam kalsium, kalium dan
natrium dalam sampel dapat dihitung dengan cara sebagai berikut:
Kadar logam (µg/g) =
konsentrasi µg
ml x Volume (ml )x Faktor Pengenceran
�
Berat sampel (g)
3.5 Analisis Data Secara Statistik
3.5.1 Penolakan Hasil Pengamatan
Kadar kalsium, kalium dan natrium yang diperoleh dari hasil pengukuran
masing-masing larutan sampel dianalisis secara statistik. Menurut Sudjana (2005)
standar deviasi dapat dihitung dengan menggunakan rumus:
SD =
�
∑(Xi−X)2
n−1
Keterangan : Xi = Kadar sampel
X = Kadar rata-rata sampel
Untuk mencari t hitung digunakan rumus:
t hitung =
n SD
X Xi
/
−
Menurut Harris (1982), untuk menghitung kadar mineral di dalam sampel
dengan interval kepercayaan 99%, dk = n-1, dapat digunakan rumus:
Kadar mineral : µ = X ± (tα/2, dk) x SD / √n)
Keterangan : X = Kadar rata-rata sampel SD= Standar Deviasi
dk= Derajat kebebasan (dk = n-1) α = Interval kepercayaan
n = jumlah perlakuan
3.5.2 Pengujian Beda Nilai Rata-Rata Antar Sampel
Menurut Singgih (2012), secara dasar metode statistik ANOVA bisa
digunakan untuk menguji apakah rata-rata lebih dari dua sampel berbeda secara
signifikan ataukah tidak.
Uji statistik parametrik analisis varian (ANOVA) satu jalan menggunakan
Post Hoc Test pilihan Boferroni dan Tukey.
3.5.3 Uji Perolehan Kembali (Recovery)
Menurut Harmita (2004), uji perolehan kembali (recovery) dilakukan
dengan metode penambahan larutan standar (standard addition method). Dalam
metode ini, kadar mineral dalam sampel ditentukan terlebih dahulu, selanjutnya
ditentukan penentuan kadar mineral dalam sampel setelah penambahan larutan
standar dengan konsentrasi tertentu. Larutan baku yang ditambahkan yaitu 8,5 ml
(konsentrasi 1000 µg/ml) dan 0,5 ml larutan baku kalsium (konsentrasi 1000
µg/ml).
Kubis yang telah dihaluskan ditimbang sebanyak 25 gram di dalam krus
porselen, lalu ditambahkan 8,5 ml larutan baku kalium (konsentrasi 1000 µg/ml);
0,5 ml larutan baku natrium (konsentrasi 1000 µg/ml) dan 0,5 ml larutan baku
kalsium (konsentrasi 1000 µg/ml), kemudian dilanjutkan dengan prosedur
dekstruksi seperti yang telah dilakukan sebelumnya.
Menurut Harmita (2004), persen perolehan kembali dapat dihitung dengan
rumus dibawah ini:
% Perolehan Kembali = ��−��
�∗� x 100%
Keterangan:
CA = Kadar logam dalam sampel sebelum penambahan baku
CF = Kadar logam dalam sampel setelah penambahan baku
C*A = Kadar larutan baku yang ditambahkan
3.5.4 Simpangan Baku Relatif
Menurut Harmita (2004), keseksamaan atau presisi diukur sebagai
simpangan baku relatif atau koefisien variasi. Keseksamaan atau presisi
merupakan ukuran yang menunjukkan derajat kesesuaian antara hasil uji
individual ketika suatu metode dilakukan secara berulang untuk sampel yang
homogen. Nilai simpangan baku relatif yang memenuhi persyaratan menunjukkan
adanya keseksamaan metode yang dilakukan.
Menurut Harmita (2004), rumus untuk menghitung simpangan baku relatif
adalah:
Keterangan : X = Kadar rata-rata sampel SD = Standar Deviasi
RSD = Relative Standard Deviation
3.5.5 Penentuan Batas Deteksi (Limit of Detection) dan Batas Kuantitasi (Limit of Quantitation)
Batas deteksi merupakan jumlah terkecil analit dalam sampel yang dapat
dideteksi yang masih memberikan respon signifikan. Sedangkan batas kuantitasi
merupakan kuantitas terkecil analit dalam sampel yang masih dapat memenuhi
kriteria cermat dan seksama (Harmita, 2004).
Menurut Harmita (2004), batas deteksi dan batas kuantitasi ini dapat
dihitung dengan rumus sebagai berikut:
Simpangan Baku (���� ) =
�
∑(Y−Yi )2
n−2
Deteksi (LOD) = 3 x SY X�
slope
Batas kuantitasi (LOQ) = 10 x SY X�
BAB IV
HASIL DAN PEMBAHASAN
4.1 Pengambilan Sampel
Pengambilan sampel dilakukan pasca letusan Gunung Sinabung bulan
September 2013-Februari 2014, sampel di ambil pada bulan 28 Maret 2014.
Sampel di ambil di empat desa yakni desa Suka Ndebi, desa Suka Tepu desa
Ndeskati yang berada di kecamatan Naman Teran dekat daerah Gunung Sinabung
yakni berjarak 6 kilometer dari gunung, dan desa Raya yang berada di kecamatan
Brastagi yang agak jauh dari daerah Gunung Sinabung yakni berjarak 11
kilometer. Peta situasi Gunung Sinabung, Kab. Karo. Prov. Sumatera Utara dapat
Gambar 1 Peta situasi Gunung Sinabung, Kab. Karo. Prov. Sumatera Utara
4.2 Identifikasi Sampel
Hasil identifikasi sampel yang dilakukan oleh bagian Herbarium
Bogoriense Bidang Botani Pusat Penelitian Biologi LIPI-Bogor terhadap sayuran
kubis adalah jenis (Brassica oleracea, L.). suku Brassicaceae. Hasil identifikasi
sampel dapat dilihat pada Lampiran 1, halaman 46.
4.3 Analisis Kualitatif
Analisis kualitatif dilakukan sebagai analisis pendahuluan untuk
mengetahui ada atau tidaknya mineral kalium, natrium dan kalsium dalam
sampel. Ada atau tidaknya mineral kalium, natrium dan kalsium dengan cara
mengukur serapan dari larutan sampel hasil destruksi pada panjang gelombang
tertentu yang sesuai dengan jenis mineral yaitu kalium diukur pada panjang
gelombang 766,5 nm, natrium diukur pada panjang gelombang 589,0 nm, dan
kalsium pada panjang gelombang 422,7 nm. Dari hasil pengkuran ini bahwa
larutan sampel hasil destruksi membuktikan sampel kubis (Brassica oleraceae
L.) mengandung mineral kalium, natirum dan kalsium karena memiliki serapan
4.4 Analisis Kuantitatif
4.4.1 Kurva kalibrasi Kalium, Natrium dan Kalsium
Kurva kalibrasi kalium, natrium dan kalsium diperoleh dengan cara
mengukur serapan dari larutan baku ketiganya pada panjang gelombang
masing-masing. Hasil pengukuran kurva kalibrasi untuk ketiganya diperoleh persamaan
garis regresi yaitu Y = 0,035054X − 0,006171429 dengan R2 = 0,9994 untuk
kalium, Y = 0,171886X + 0,00362381 R2 = 0,9992 untuk natrium dan Y =
0,044259X + 0,000957143 R2 = 0,9995 untuk kalsium.
Kurva kalibrasi larutan baku kalium, natrium dan kalsium dapat dilihat
[image:48.595.146.506.347.832.2]pada Gambar 3 sampai dengan Gambar 5.
Gambar 3 Kurva Kalibrasi Kalium
[image:48.595.146.480.352.525.2]Gambar 5 Kurva Kalibrasi Kalsium
Berdasarkan kurva di atas diperoleh koefisien korelasi (r) mendekati satu
yang berarti adanya hubungan yang linear antara konsentrasi dengan serapan
(Shargel dan Andrew, 1999).
Data hasil pengukuran serapan larutan baku kalium, natrium dan kalsium
dan perhitungan persamaan garis regresi dapat dilihat pada Lampiran 7 sampai
dengan Lampiran 9, halaman 52 sampai halaman 57.
4.4.2 Pengukuran Kadar Kalium, Natrium dan Kalsium dalam Sampel
Penentuan kadar mineral kalium, natrium dan kalsium dilakukan secara
spektrofotometri serapan atom. Pada pengukuran sampel yang dilakukan secara
spektrofotometri serapan atom, terlebih dahulu dikondisikan alat dengan baik dan
benar. Konsentrasi mineral kalium, natrium dan kalsium dalam sampel ditentukan
berdasarkan persamaan garis regresi kurva kalibrasi larutan baku masing-masing
mineral. Agar konsentrasi mineral kalium, natrium dan kalsium dalam sampel
berada pada rentang kurva kalibrasi maka masing-masing sampel diencerkan
terlebih dahulu dengan faktor pengencaran yang berbeda-beda Faktor
pengenceran untuk penentuan kadar kalium pada kubis di empat desa (Suka
Ndebi, Suka Tepu, Ndeskati dan Raya) yaitu sebesar 500 kali (50/1 x 25/2,5),
faktor pengenceran untuk penentuan kadar natrium pada kubis di empat desa
(Suka Ndebi, Suka Tepu, Ndeskati dan Raya) yaitu sebesar 100 kali (50/0.5) dan
faktor pengenceran untuk penentuan kadar kalsium pada kubis di empat desa
dan contoh perhitungan dapat dilihat pada Lampiran 10 sampai dengan Lampiran
11, halaman 58 sampai halaman 65.
Analisis dilanjutkan dengan perhitungan statistik (Perhitungan dapat
dilihat pada Lampiran 12 sampai dengan Lampiran 14, halaman 66 sampai
halaman 94. Hasil analisis kuantitatif mineral kalium, natrium dan kalsium pada
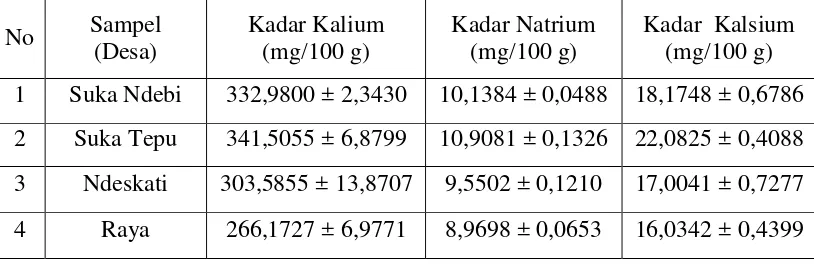
[image:50.595.109.516.280.412.2]sampel dapat dilihat pada Tabel 1 berikut ini:
Tabel 1. Hasil Analisis Kadar Kalium, Natrium dan Kalsium dalam Sampel
No Sampel
(Desa)
Kadar Kalium (mg/100 g)
Kadar Natrium (mg/100 g)
Kadar Kalsium (mg/100 g) 1 Suka Ndebi 332,9800 ± 2,3430 10,1384 ± 0,0488 18,1748 ± 0,6786 2 Suka Tepu 341,5055 ± 6,8799 10,9081 ± 0,1326 22,0825 ± 0,4088 3 Ndeskati 303,5855 ± 13,8707 9,5502 ± 0,1210 17,0041 ± 0,7277 4 Raya 266,1727 ± 6,9771 8,9698 ± 0,0653 16,0342 ± 0,4399
Berdasarkan Tabel 1 di atas dapat diketahui bahwa terdapat perbedaan
kadar kalium, natrium dan kalsium pada sayuran kubis di keempat desa (Suka
Ndebi, Suka Tepu, Ndeskati dan Raya) yang diperoleh dari hasil analisis. Dari
tabel tersebut dapat diketahui bahwa kadar kalium pada kubis di desa Suka
Tepu>Suka Ndebi>Ndeskati>Raya. Hal ini disebabkan karena jarak desa dengan
gunung Sinabung dan arah angin serta kecepatan angin pada saat terjadi letusan
yang memberikan hasil dari dampak letusan Gunung Sinabung terhadap kadar
mineral kalium, natrium dan kalsium di desa yang lebih dekat yakni di kecamatan
Naman Teran (Desa Suka Tepu > Desa Suka Ndebi > Desa Ndeskati) lebih tinggi
dari desa Raya di kecamatan Brastagi yang lebih jauh dari daerah Gunung
4.5 Pengujian Beda Nilai Rata-Rata
Data yang di dapat di uji kembali secara statistik parametrik analisis varian
(ANOVA) satu jalan untuk mengetahui beda nilai rata-rata ketiga mineral
(kalium, natrim dan kalsium) pada keempat desa (Suka Ndebi, Suka Tepu,
Ndeskati dan Raya) dengan rata-rata antarkeempat desa (perhitungan dapat
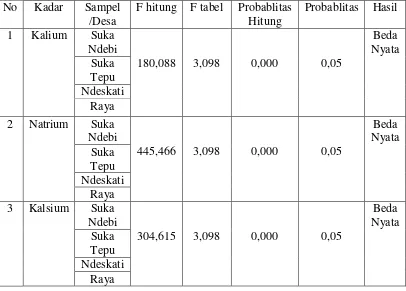
[image:51.595.107.513.292.583.2]dilihat pada Lampiran 15 sampai Lampiran 17, halaman 95 samapi halaman 97.
Tabel 2. Hasil Uji Beda nilai rata-rata kadar kalium, natrium dan kalsium antarsampel
No Kadar Sampel /Desa
F hitung F tabel Probablitas Hitung
Probablitas Hasil
1 Kalium Suka
Ndebi
180,088 3,098 0,000 0,05
Beda Nyata Suka
Tepu Ndeskati
Raya 2 Natrium Suka Ndebi
445,466 3,098 0,000 0,05
Beda Nyata Suka
Tepu Ndeskati
Raya 3 Kalsium Suka Ndebi
304,615 3,098 0,000 0,05
Beda Nyata Suka
Tepu Ndeskati
Raya
Berdasarkan Tabel 2 di atas dapat diketahui bahwa t hitung > dari t tabel
dengan taraf kepercayaan 95% dan kadar mineral kalium, natrium dan kalsium
pada sayuaran kubis di desa (Suka Ndebi, Suka Tepu, Ndeskati dan Raya) maka
kadar rata-rata kalium, natrium dan kalsium dari keempat desa yakni desa Suka
Hal ini kemungkinan terjadi karena penyebaran abu vulkanik yang berbeda-beda
sehingga dampak pengaruh abu terhadap kadar rata-rata dari ketiga mineral
kalium, natrium dan kalsium berbeda nyata.
Data hasil analisis kadar mineral kalium, natrium, dan kalsium pada
sampel desa Suka Ndebi, desa Suka Tepu, desa Ndeskati dan desa Raya
menunjukkan perbedaan yang terlihat nyata, sehingga tidak perlu dilakukan
pengujian beda nilai rata-rata (uji ANOVA). Namun untuk melengkapi data dan
memastikan seberapa jauh perbedaan kadar mineral kalium, natrium, dan kalsium
pada sampel desa Suka Ndebi, desa Suka Tepu, desa Ndeskati dan desa Raya.
4.6 Uji Perolehan Kembali (Recovery)
Hasil uji perolehan kembali (recovery) kadar kalium, natrium dan kalsium
setelah penambahan masing-masing larutan baku dapat dilihat pada Lampiran 18
sampai Lampiran 19, halaman 98 sampai halaman 102. Contoh perhitungannya
pada Lampiran 20, halaman 103 smpai halaman 120.
Persen perolehan kembali (recovery) kadar mineral kalium, natrium dan
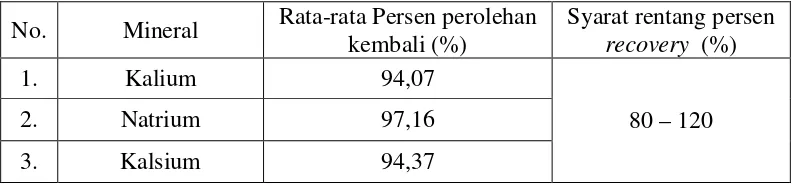
[image:52.595.122.518.636.729.2]kalsium dalam sampel dapat dilihat pada Tabel 3.
Tabel 3. Persen Uji Perolehan Kembali (recovery) Kalium, Natrium dan Kalsium dalam Sampel (kubis)
No. Mineral Rata-rata Persen perolehan kembali (%)
Syarat rentang persen
recovery (%)
1. Kalium 94,07
80 – 120
2. Natrium 97,16
Berdasarkan Tabel 3 di atas, dapat dilihat bahwa rata-rata hasil uji
perolehan kembali (recovery) kalium adalah 94,07%, untuk natrium adalah
97,16% dan untuk kalsium adalah 94,37%. Persen perolehan kembali (recovery)
tersebut menunjukkan kecermatan kerja yang memuaskan pada saat pemeriksaan
kadar kalium, natrium dan kalsium dalam sampel. Hasil yang diperoleh dari uji
perolehan kembali memberikan ketepatan pada pemeriksaan kadar mineral dalam
sampel. Menurut Harmita (2004), suatu metode dikatakan teliti jika nilai
perolehan kembalinya antara 80-120%.
4.7 Simpangan Baku Relatif
Nilai simpangan baku dan simpangan baku relatif untuk kalium, natrium
dan kalsium pada sampel (kubis) dapat dilihat pada Tabel 4, sedangkan
perhitungannya dapat dilihat pada Lampiran 21, halaman 121 sampai dengan
[image:53.595.110.504.486.577.2]halaman 123.
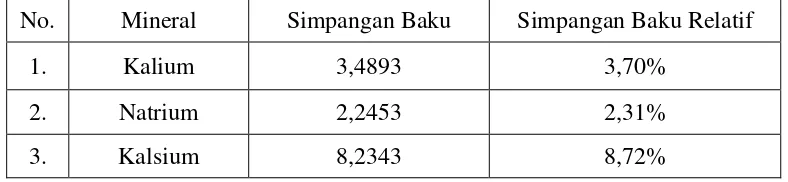
Tabel 4. Nilai Simpangan Baku dan Simpangan Baku Relatif Kalium, Nalium dan Kalsium dalam Sampel (kubis)
No. Mineral Simpangan Baku Simpangan Baku Relatif
1. Kalium 3,4893 3,70%
2. Natrium 2,2453 2,31%
3. Kalsium 8,2343 8,72%
Berdasarkan Tabel 4 di atas, dapat dilihat nilai simpangan baku (SD)
untuk mineral kalium 3,4893, untuk mineral natrium 2,453 dan untuk mineral
kalsium 8,2343, sedangkan nilai simpangan baku relatif (RSD) yang diperoleh
sebesar 3,70% untuk mineral kalium; 2,31% untuk mineral natrium; 8,72% untuk
untuk analit dengan kadar part per billion (ppb) RSDnya adalah tidak lebih dari
32%. Dari hasil yang diperoleh menunjukkan bahwa metode yang dilakukan
memiliki presisi yang baik.
4.8 Batas Deteksi dan Batas Kuantitasi
Berdasarkan data kurva kalibrasi kalium, natrium dan kalsium diperoleh
batas deteksi dan batas kuantitasi untuk ketiga mineral tersebut pada sampel
(kubis) dapat dilihat pada Tabel 5, sedangkan perhitungannya dapat dilihat pada
Lampiran 22, halaman 124 sampai dengan halaman 127.
Batas deteksi dan batas kuantitasi kalium, natrium dan kalsium dapat
dilihat pada Tabel 5.
Tabel 5. Batas Deteksi dan Batas Kuantitasi Kalium, Natrium dan Kalsium No. Mineral Batas Deteksi (µg/ml) Batas Kuantitasi (µg/ml)
1. Kalium 0,3428 1,1428
2. Natrium 0,0366 0,1222
3. Kalsium 0,3800 1,2669
Dari hasil perhitungan diperoleh batas deteksi untuk pengukuran kalium,
nalium dan kalsium masing-masing sebesar 0,3428 µg/ml, 0,0366 µg/ml dan
0,3800 µg/ml, sedangkan batas kuantitasinya sebesar 1,1428 µg/ml, 0,1222
µg/ml dan 1,2669 µg/ml.
Dari hasil perhitungan dapat dilihat bahwa semua hasil yang diperoleh
pada pengukuran sampel berada diatas batas deteksi dan batas kuantitasi sehingga
BAB V
KESIMPULAN DAN SARAN
5.1Kesimpulan
a. Hasil penetapan kadar mineral kalium, natrium dan kalsium secara
spektrofotometri serapan atom menunjukkan adanya perbedaan pada
sayuran kubis di keempat desa (Suka Ndebi, Suka Tepu, Ndeskati dan
Raya) diperoleh masing-masing yaitu untuk kalium (332,9800 ± 2,3430
mg/100g; 341,5055 ± 6,8799 mg/100g; 303,5585 ± 13,8707 mg/100g; dan
266,1727 ± 6,9771 mg/100g), untuk natrium (10,1384 ± 0,0488 mg/100g;
10,9081 ± 0,1326 mg/100g; 9,5502 ± 0,1210 mg/100g; dan 8,9698 ±
0,0653 mg/100g) dan untuk kalsium (18,1748 ± 0,6786 mg/100g; 22,0825
± 0,4088 mg/100g; 17,0041 ± 07277 mg/100g dan 16,0342 ± 0,4399
mg/100g).
b. Hasil pemeriksaan kadar mineral kalium, natrium dan kalsium di desa
yang lebih dekat Gunung Sinabung yakni Desa Suka Ndebi, Desa Suka
Tepu, Desa Ndeskati lebih tinggi dari desa Raya yang lebih jauh dari
Gunung Sinabung.
5.2Saran
a. Disarankan kepada peneliti selanjutnya untuk meneliti mineral lain seperti
b. Disarankan kepada peneliti selanjutnya untuk meneliti tanaman lain seperti
cabe, jeruk, tomat yang tedapat di daerah gunung untuk diteliti dampak
DAFTAR PUSTAKA
Almatsier, S. (2004). Prinsip Dasar Ilmu Gizi. Jakarta: PT. Gramedia pustaka Utama. Halaman 228-276.
Anonim. (2014). Gunung Sinabung.
Januari 2014.
BPTP Sumatera Utara. (2014). Rekomendasi Kebijakan Mitigasi Dampak Erupsi Gunung Sinabung Terhadap Sector Pertanian.
iKebijakanMitigasiErupsiSinabung.pdf. Tanggal akses 28 Februari 2014.
Budiarto, E. (2004). Metodologi Penelitian Kedokteran. Jakarta: Kedokteran EGC. Halaman 1-57.
Budiyanto, M.A.K. (2001). Dasar Dasar Ilmu Gizi Edisi Kedua. Cetakan I. Malang: UMM Press. Halman 59.
Calvin, C.L., dan Donald M. (1983). Modern Home Gardening. United States of America: John Wiley & Sons. Halaman 532.
Ermer, J., dan McB. Miller. J.H. (2005). Method Validation in Pharmaceutical Analysis. Weinheim: Wiley-Vch Verlag GmbH & Co. KGaA. Halaman 250-253.
Gandjar, I.G., dan Rohman, A. (2009). Kimia Farmasi Analisis. Cetakan II. Yogyakarta: Pustaka Pelajar. Halaman 298-322.
Harmita. (2004). Petunjuk Pelaksanaan Validasi Metode dan Cara Perhitungannya. Review Artikel. Majalah Ilmu Kefarmasian. 1(3): 117-135.
Hartuti, E. R. (2009). Buku Pintar Gempa : Mengenali Seluk Beluk Gempa, Jenis-Jenisnya, Penyebab-penyebabnya dan Dampak-dampaknya.
Jogjakarta: Diva Press. Halaman 49-72.
Helrich, K. (1990). Official Methods of the Association of Official Analytical Chemist. Fifteenth Edition. Virginia: AOAC International. Page 658
Horwitz, K. (2000). Official Methods of the Association of official Anaytical Chemist. Seventeenth Edition. Arlington. ACOAC International. Halaman 42.
Novary, E. W. 1999. Penanganan dan pengolahan sayuran segar. Cetakan II. Jakarta: Penebar Swadaya. Halaman 119-123.
Pracaya, IR. (1992). Kol alias kubis. Cetakan VII. Jakarta: penebar swadaya. Halaman 1-44.
Shargel, L., and Andrew, B. C. (1999). Applied Biopharmaceutics and Pharmacokinetics. USA: Prentice-hall international, INC. Page 15.
Santoso, S. (2012). Aplikasi SPSS Pada Statistik Parametrik. Jakarta: PT. Elex Media Komputindo. Halaman 167-186.
Soehardi, S. (2004). Memelihara Kesehatan Jasmani Melalui Makanan. Bandung: ITB. Hal. 206-207.
Sudaryo dan Sutjipto. (2009). Identifikasi Dan Penentuan Logm Berat Pada Tanah Vulkanik Di Daerah Cangkringan, Kabupaten Sleman Dengan Metode Analisis Aktivasi Neutron Cepat. Seminar Nasional V SDM Teknologi Nuklir ISSN 1978-0176, Yogyakarta.
Susila, Anas D. (2006). PanduanBudi Daya Tanaman Sayur. Bogor: Departemen Agronomi dan Hortikultura, Fakultas Pertanian IPB. Halaman 65-69.
Suta