KORELASI SKOR CHILD PUGH DENGAN
KADAR GLUKOSA DARAH PADA PENDERITA SIROSIS HATI
PENELITIAN POTONG LINTANG DI BAGIAN /SMF ILMU PENYAKIT DALAM FAKULTAS KEDOKTERAN USU/ RS H ADAM MALIK MEDAN
FEBRUARI 2008 – NOVEMBER 2008
TESIS
OLEH
JANNUS SITORUS
DEPARTEMEN ILMU PENYAKIT DALAM
FAKULTAS KEDOKTERAN UNIVERSITAS SUMATERA UTARA RSUP H ADAM MALIK/ RSUD DR PIRNGADI
DIAJUKAN DAN DIPERTAHANKAN DIDEPAN SIDANG LENGKAP DEWAN PENILAI BAGIAN ILMU PENYAKIT DALAM
FAKULTAS KEDOKTERAN UNIVERSITAS SUMATERA UTARA
DAN DITERIMA SEBAGAL SALAH SATU SYARAT UNTUK MENDAPATKAN KEAHLIAN DALAM BIDANG PENYAKIT DALAM
PEMBIMBING TESIS
Dr. Betthin Marpaung, SpPD KGEH Dr. Dharma Lindarto, SpPD KEMD
Disahkan oleh
KEPALA DEPARTEMEN KETUA PROGRAM STUDI PPDS ILMU PENYAKIT DALAM ILMU PENYAKIT DALAM FAKULTAS KEDOKTERAN USU FAKULTAS KEDOKTERAN USU
DEWAN PENILAI
1. Prof. Dr. Harun Rasyid Lubis, SpPD KGH 2. Dr. Mabel Sihombing, SpPD KGEH
KATA PENGANTAR
Puji dan syukur saya panjatkan ke hadirat Tuhan Yang Maha Kuasa yang telah
memberikan berkat dan kasihNya, sehingga saya dapat menyelesaikan tesis ini yang
berjudul: “KORELASI SKOR CHILD PUGH DENGAN KADAR GLUKOSA DARAH
PADA PENDERITA SIROSIS HATI”, yang berlangsung sejak Februari 2008 hingga
November 2008. Tulisan ini dibuat sebagai salah satu syarat dalam menyelesaikan
pendidikan dokter spesialis dibidang Ilmu Penyakit Dalam Fakultas Kedokteran
Universitas Sumatera Utara.
Dengan selesainya karya tulis ini, maka penulis ingin menyampaikan terima
kasih dan rasa hormat serta penghargaan yang setinggi-tingginya kepada:
1. Dr Salli Rossefi Nasution SpPD-KGH, selaku Kepala Departemen Ilmu Penyakit
Dalam FK USU/ RSUP H. Adam Malik Medan dan Prof. Dr. Lukman Hakim Zein
SpPD-KGEH, selaku Kepala Divisi Gastroentero-Hepatologi Ilmu Penyakit Dalam
FK USU/ RSUP H. Adam Malik Medan dimana penulis memulai pendidikan pada
Januari 2004, yang telah memberikan kemudahan dan perhatian yang besar
terhadap pendidikan penulis.
2. Ketua Program Studi Ilmu Penyakit Dalam Dr Zulhelmi Bustami SpPD-KGH dan
Sekretaris Program Studi Ilmu Penyakit Dalam Dr Dharma Lindarto SpPD-KEMD
dengan sungguh-sungguh telah membantu dan membentuk penulis menjadi ahli
penyakit dalam yang berkualitas, handal dan berbudi luhur serta siap untuk
3. Khusus untuk karya tulis ini, penulis mengucapkan terima kasih yang
sebesar-besarnya kepada Dr. Betthin Marpaung SpPD KGEH selaku pembimbing I dan
Dr. Dharma Lindarto SpPD KEMD sebagai pembimbing II yang penulis rasakan
benar-benar dengan tulus membantu dan membimbing penulis menyelesaikan
penelitian dan karya tulis ini, hanya doa yang dapat penulis berikan kiranya
berkat berlimpah dari Yang Maha Kuasa selalu beserta beliau dan keluarga.
4. Seluruh staf Departemen Ilmu Penyakit Dalam FK USU/ RSUD Dr Pirngadi/
RSUP H. Adam Malik Medan, Prof Dr Harun Rasyid Lubis SpPD-KGH, Prof Dr T
Renardi Haroen SpPD-KKV, MPH, Prof Dr Bachtiar Fanani Lubis SpPD-KHOM,
Prof Dr Habibah Hanum SpPD-Kpsi, Prof Dr Sutomo Kasiman SpPD-KKV, Prof
Dr Azhar Tanjung KP-KAI-SpMK, Prof Dr Pengarapen Tarigan
KGEH, Prof Dr OK Moehad Sjah KR, Prof Dr Lukman Hakim Zain
SpPD-KGEH, Prof Dr M Yusuf Nasution SpPD-KGH, Prof Dr Azmi S Kar SpPD-KHOM,
Prof Dr Gontar A Siregar SpPD-KGEH, Prof Dr Harris Hasan SpPD-SpJP(K), Dr
Nur Aisyah KEMD, Dr A Adin St Bagindo KKV, Dr Lufti Latief
SpPD-KKV, Dr Syafii Piliang SpPD-KEMD, Dr T Bachtiar Panjaitan SpPD, Dr Betthin
Marpaung SpPD-KGEH, Dr Sri M Sutadi SpPD-KGEH, Dr Mabel Sihombing
SpPD-KGEH, Dr Salli R Nasution SpPD-KGH, Dr Abdurrahim Rasyid Lubis
KGH, Dr Abiran Nababan KGEH, Dr Juwita Sembiring
SpPD-KGEH, Dr Alwinsyah Abidin SpPD-KP, Dr Dharma Lindarto SpPD-KEMD, Dr
Umar Zein SpPD-KPTI-DTM&H-MHA, Dr Josia Ginting SpPD-KPTI, Dr Refli
Hasan SpJP, Dr R Tunggul Ch Sukendar KGH, Dr EN Keliat
merupakan guru-guru saya yang telah banyak memberikan arahan dan petunjuk
kepada saya selama mengikuti pendidikan.
5. Dr Armon Rahimi, SpPD, Dr Heriyanto Yoesoef SpPD, Dr Daud Ginting SpPD,
Dr Tambar Kembaren SpPD, Dr Saut Marpaung SpPD, Dr Mardianto SpPD, Dr
Zuhrial SpPD, Dr Dasril Efendi SpPD, Dr Rustam Efendi YS SpPD, Dr Ilhamd
SpPD, Dr Calvin Damanik SpPD, Dr Zainal Safri SpPD, Dr Rahmat Isnanta
SpPD, Dr Santi Safril SpPD, Dr Dairion Gatot SpPD, Dr Jerahim Tarigan SpPD,
Dr Endang Sembiring SpPD, Dr Abraham SpPD, Dr Soegiarto Gani SpPD, Dr
Savita Handayani SpPD, Dr Franciscus Ginting SpPD, Dr Syafrizal Nasution
SpPD, Dr Deske SpPD sebagai dokter kepala ruangan/ senior yang telah amat
banyak membimbing saya selama mengikuti pendidikan ini.
6. Direktur RSUP H Adam Malik Medan dan RSUD Dr Pirngadi Medan yang telah
memberikan begitu banyak kemudahan dan izin dalam menggunakan fasilitas
dan sarana Rumah Sakit untuk menunjang pendidikan keahlian ini.
7. Kepada Direktur Rumah Sakit Panyabungan Kabupaten Mandailing Natal dr.
Sakdiah Lubis, yang telah memberikan kesempatan dan bimbingan kepada
penulis selama ditugaskan sebagai Konsultan Penyakit Dalam RS Panyabungan
dalam rangka pendidikan ini.
8. Kepada Kepala Dinas Kesehatan Kabupaten Bengkulu Utara, Rektor Universitas
Sumatera Utara, Dekan Fakultas Kedokteran Universitas Sumatera Utara yang
telah memberikan izin dan menerima saya, sehingga dapat mengikuti pendidikan
9. Para pasien yang telah dengan ikhlas menjadi “guru” sehingga memungkinkan
saya mencapai gelar dokter spesialis dibidang Ilmu Penyakit Dalam.
10. Kepada Drs Abdul Jalil Amri Arma, M.Kes yang telah memberikan bantuan dan
bimbingan yang tulus dalam menyelesaikan penelitian ini.
11. Para sejawat PPDS-Interna, perawat serta paramedis dan seluruh
karyawan/karyawati di lingkungan SMF/Bagian Ilmu Penyakit Dalam RSUD Dr
Pirngadi / RSUP H Adam Malik Medan atas segala kerjasamanya yang baik
selama ini.
12. Buat teman-temanku yang penuh kesetiakawanan dan kebersamaan memberi
bantuan, dorongan dan pengorbanan selama menjalani pendidikan sehingga
terjalin rasa persaudaraan yang erat.
Kepada kedua orang tua saya, Ayahanda Samo Sitorus dan Ibunda Toman
Butar-butar yang saya kasihi dan sayangi, tiada kata-kata yang paling tepat untuk
mengungkapkan perasaan hati, rasa terima kasih atas segala jasa-jasa ayahanda dan
ibunda yang tiada mungkin terucapkan dan terbalaskan. Demikian juga kepada Bapak
dan Ibu Mertua, Junias Sitanggang dan Tormauli Sinurat, penulis ucapkan terima kasih
yang tak terhingga dan sebagian amanahmu sudah penulis selesaikan serta yang
dengan ikhlas memberikan “bahunya” sebagai tempat sandaran penulis disaat suka
duka, serta memberi dorongan dan semangat kepada penulis dalam menyelesai
pendidikan ini.
Kepada istriku tercinta Liburiah Sitanggang, tiada kata yang paling tepat selain
pendorong dan teman paling setia dalam suka maupun duka, selalu mendengarkan dan
memberikan solusi yang baik dalam berbagai masalah yang dihadapi penulis.
Sebenarnya masih banyak lagi kata ucapan terima kasih yang ingin penulis
sampaikan buat berbagai pihak yang tidaklah mungkin disebutkan satu persatu, pada
kesempatan ini izinkanlah penulis menyampaikan rasa terima kasih yang tulus secara
menyeluruh.
Medan, Februari 2009
Penulis
DAFTAR ISI
Halaman
Kata Pengantar ... i
Daftar Isi ... vi
Lampiran ... ix
Daftar Tabel dan Gambar ... x
Daftar Singkatan ... xii
Abstrak ... xiii
BAB I PENDAHULUAN ... 1
BAB II TINJAUAN PUSTAKA 2.1 Hepatogenous diabetes ... 4
2.2 Skor Child Pugh ... 12
2.3 Serum bilirubin ... 12
2.4 Serum albumin ... 13
2.5 Waktu protrombin ... 14
2.6 TTGO ... 15
2.7 Glucometer ... 16
2.8 Retinopati diabetik ... 18
BAB III PENELITIAN SENDIRI 3.1 Latar belakang ... 21
3.2 Perumusan masalah ... 24
3.4 Tujuan penelitian ... 24
3.5 Manfaat penelitian ... 24
3.6 Kerangka konsepsional ... 25
3.7 Bahan dan cara 3.7.1 Desain penelitian ... 25
3.7.2 Waktu dan tempat peneltian ... 25
3.7.3 Populasi terjangkau ... 25
3.7.4 Kriteria inklusi ... 26
3.7.5 Kriteria eksklusi ... 26
3.7.6 Besar sampel ... 26
3.7.7 Cara penelitian ... 27
3.7.8 Analisa data ... 28
3.7.9 Defenisi operasional ... 29
3.7.10 Kerangka operasional ... 30
BAB IV HASIL PENELITIAN DAN PEMBAHASAN 4.1 Hasil penelitian 4.1.1 Karakteristik dasar penderita sirosis hati ... 31
4.1.2 Gambaran gangguan metabolisma glukosa pada penderita sirosis hati ... 33
4.1.3 Korelasi skor Child Pugh dengan kadar glukosa darah ... 34
4.2 Pembahasan ... 38
BAB V KESIMPULAN DAN SARAN... 41.
LAMPIRAN
1. Master Tabel ... 47
2. Lembaran penjelasan kepada calon subjek penelitian ... 48
3. Formulir Persetujuan Subjek Penjelasan ... 49
4. Profil Peserta Studi ... 50
5. Persetujuan Komite Etik Kedokteran ... 51
DAFTAR TABEL
Halaman
Tabel 1. Skor Child Pugh ... 12
Tabel 2. Nilai TTGO dari plasma vena atau kapiler ... 16
Tabel 3. Stadium retinopati diabetik ... 20
DAFTAR TABEL Tabel 1. Rerata umur penderita sirosis hati ... 31
Tabel 2. Karakteristik demografi dan klinis penderita sirosis hati ... 32
Tabel 3. Rerata nilai laboratorium penderita sirosis hati ... 33
Tabel 4. Rerata variabel laboratorium berdasarkan gangguan metabolisma glukosa ... 34
Tabel 5. Rerata variabel laboratorium berdasarkan Child Pugh ... 35
Tabel 6. Korelasi skor Child Pugh dengan kadar glukosa darah ... 36
Tabel 7. Korelasi antara kadar glukosa darah dengan bilirubin, albumin dan waktu protrombin... 37
DAFTAR GAMBAR Halaman Gambar 1. Mekanisme terjadinya DM pada hepatitis C ... 5
Gambar 2. Hubungan IL-6 dengan Child Pugh ... 6
Gambar 3. Korelasi keparahan sirosis hati dengan resistin ... 7
Gambar 5. Kumulatif angka survival pada penderita sirosis hati ... 11
Gambar 6. Glucometer ... 17
Gambar 7. Analisa Error grid glucometer ... 18
Gambar 8. Retinopati diabetik nonproliferatif dan proliferatif ... 20
DAFTAR GAMBAR
Gambar 1. Patogenese terjadinya DM pada hepatitis C ... 8
Gambar 2. Prevalensi gangguan metabolisma glukosa
berdasarkan kriteria Child Pugh ... 33
DAFTAR SINGKATAN
CP : Child Pugh
DM : Diabetes Melitus
TTGO : Tes Toleransi Glukosa Oral
KGD : Kadar glukosa darah
OR : Odds Ratio
Cl : Confidence interval
GAD : Glutamic Acid Dehidrogenase
HCV : Hepatitis C Virus
TNF- : Tumor necrosis factor-
IL : Interleukin
WHO : Word Health Organization
ADA : American Diabetes Association
HCV : Hepatitis C Virus
IRS : Insulin Receptor Substrate
Th : T helper
Glut 4 : Glucose transporter 4
TNFR : Tumor necrose factor receptor
HGP : Hepatic Glucose Production
Abstrak
Korelasi skor Child Pugh dengan kadar glukosa darah pada penderita sirosis hati
Latar belakang
Gangguan metabolisma glukosa sering dijumpai pada sirosis hati ditandai dengan terganggunya kadar glukosa darah puasa dan 2 jam beban glukosa saat dilakukan Tes Toleransi Glukosa Oral (TTGO). Pada banyak kasus, diabetes kelihatannya sering terjadi pada sirosis hati dan ini disebut hepatogenous diabetes. Klasifikasi Child Pugh merupakan model yang sering digunakan untuk menilai keparahan pasien sirosis hati.
Metode
Ada 36 pasien sirosis hati yang memenuhi syarat ikut dalam studi cross sectional ini. Skor Child Pugh dinilai untuk setiap pasien. Kemudian dilakukan penilaian toleransi glukosa dengan melakukan TTGO dengan meminum 75 gram glukosa sesuai dengan kriteria World Health Organization (WHO). Kadar glukosa darah semua pasien diperiksa melalui darah kapiler dengan alat glucometer. Korelasi skor Child Pugh dan kadar glukosa darah dinilai dengan analisa Pearson.
Hasil
Diabetes melitus (DM) dijumpai pada 15 subjek (42%), intoleransi glukosa pada 14 subjek (39%) dan toleransi glukosa normal pada 7 subjek (19%). Dengan analisa Pearson didapati bahwa skor Child Pugh berkorelasi dengan kadar glukosa darah puasa (r=0,67 p=0,000) dan 2 jam beban glukosa darah (r=0,73 p=0,000).
Kesimpulan
Skor Child Pugh berkorelasi positif bermakna dengan kadar glukosa darah
Key words : Sirosis hati, skor Child Pugh, hepatogenous diabetes, glucometer, kadar
Abstract
Correlation between Child Pugh score and blood glucose level in liver cirrhosis patients
Background
Alterations in carbohydrate metabolism are frequently observed in liver cirrhosis, both in fasting plasma glucose and 2 hours postload plasma glucose during Oral Glucose Tolerance Test (OGTT). In plenty of cases, diabetes seems to occur frequently in cirrhosis, and it is called hepatogenous diabetes. The Child Pugh classification is the most widely used model to determined severity in patients with liver cirrhosis.
Methods
Thirty-six patients with liver cirrhosis were enrolled in this cross-sectionally study. The Child Pugh score was calculated from each patient. In all cases, glucose tolerance was diagnosed by a 75 gram OGTT according to World Health Organization (WHO) criteria. And patients underwent venous plasma glucose with glucometer testing of capillary blood. The correlation of Child Pugh score with glucose blood level was investigated using Pearson analysis.
Results
Diabetes mellitus (DM) was diagnosed in 15 subjects (42%), glucose intolerance in 14 subjects (39%) and normal glucose tolerance in 7 subjects (19%). Pearsons analysis showed that Child Pugh score were correlated with fasting glucose (r=0,67 p=0,000) and 2 hours postload glucose (r=0,73 p=0,000).
Conclusions
Child Pugh score has a significance correlation with blood glucose level
BAB I
PENDAHULUAN
Skor Child Pugh merupakan suatu skor untuk menilai cadangan fungsi hati pada
penderita sirosis hati, yang dipublikasikan oleh Child (1964).
Pada awalnya skor ini direncanakan untuk menstratifikasi pasien yang masuk
kedalam kelompok resiko sebelum menjalani operasi pemintasan. Dan sekarang ini
digunakan sebagai kriteria baku menilai keparahan penyakit hati, prognosa sirosis hati
dan pembuatan daftar pasien yang akan menjalani transplantasi hati (Child Pugh B).
Variabel penting yang digunakan, ada 5 jenis yaitu kadar serum bilirubin, serum
albumin, ascites, gangguan neurologis dan status nutrisi. Kemudian Pugh dkk (1973)
memodifikasi kriteria Child, dimana variabel status nutrisi pada kriteria sebelumnya
digantikan dengan waktu protrombin. Untuk kadar albumin, Pugh memberikan batasan
terendah 2,8 mg/dL dimana pada kriteria Child batasan terendahnya 3 mg/dL.
Selanjutnya kriteria tersebut dikenal dengan modifikasi Child Pugh (CP). Kelima
variabel masing-masing diberi skor 1, 2 dan 3 berturut-turut sehingga jumlah skor
antara 5-15 dan jumlah skor ini dibagi menjadi 3 kelompok yaitu A, B dan C, yakni CP A
dengan skor 5-6, CP B dengan skor 7-9 dan CP C dengan skor total 10-15.1,2
Sirosis hati adalah merupakan penyakit hati menahun yang ditandai dengan
adanya kegagalan hepatoseluler dan hipertensi portal. Pada keadaan ini sering
dijumpai gangguan metabolisma glukosa, dapat berupa intoleransi glukosa dengan
angka kejadian 60-80% dan Diabetes Melitus (DM) tipe 2 berkisar 15-30%. DM pada
Banyak studi telah melaporkan angka kejadian DM pada penderita sirosis hati.
Holstein dkk (2002), menyatakan bahwa dari 52 orang penderita sirosis hati terdapat
25% penderita sirosis hati dengan intoleransi glukosa dan 71% dengan DM.5 Alavian dkk (2004), mendapatkan dari 41 orang penderita sirosis hati terdapat 54% penderita
sirosis hati yang DM.6 Lecube dkk (2006), melaporkan prevalensi DM pada penderita sirosis oleh karena virus hepatits C berkisar 19,6%-50%.
Patogenese terjadinya DM pada penderita sirosis hati sangat kompleks dan
belum sepenuhnya dimengerti, tetapi diduga hal ini terjadi melalui proses autoimun,
kerusakan langsung di sel pankreas dan peranan proinflamasi sitokin.7
Adanya DM pada penderita sirosis hati ternyata lebih memperburuk angka
survivalnya dibandingkan dengan penderita sirosis hati yang kadar glukosanya normal.
Kwon dkk (2004), melaporkan bahwa pada penderita sirosis hati virus B dan C dengan
hiperglikemia memiliki angka survival yang lebih rendah dibandingkan yang
normoglikemia.8 Nishida dkk (2006), mendapatkan bahwa survival 5 tahun pada penderita hepatogenous diabetes lebih rendah dibandingkan dengan penderita sirosis
hati yang glukosa normal. Kematian yang terjadi disebabkan oleh koma hepatik, infeksi
dan perdarahan varises. Ini berarti penderita hepatogenous diabetes lebih
berkemungkinan untuk terjadi koma hepatik, infeksi dan perdarahan varises
dibandingkan yang tidak diabetes.9 Diaz J dkk (2006), mendapatkan infeksi lebih sering terjadi pada hepatogenous diabetes dibandingkan yang tidak diabetes (OR=5,90, 95%
Cl: 2,47-14,18).10
Untuk menilai adanya intoleransi glukosa yang terjadi dapat dilakukan dengan
Health Organization (WHO) 1999 dengan melakukan pemeriksaan kadar glukosa darah
puasa, ½ jam, 1 jam, 1½ jam dan 2 jam setelah beban glukosa 75 gram. Pengambilan
sampel darah dapat berasal dari vena ataupun dari kapiler.11,12,13
Letiexhe dkk (1993), dengan Tes Toleransi Glukosa Intravena didapatkan bahwa
pada penderita sirosis hati memiliki kadar glukosa darah yang lebih tinggi dibandingkan
dengan kontrol (p<0,05).14
Beberapa studi mencoba menghubungkan antara kriteria Child Pugh dengan
kadar glukosa darah pada penderita sirosis hati. Holstein dkk (2002), mendapatkan
bahwa pada Child Pugh A memiliki kadar glukosa darah yang lebih rendah
dibandingkan Child Pugh B dan C walaupun secara statistik tidak ada perbedaan
bermakna.5 Alavian dkk (2004), mendapatkan bahwa 9,6 kali lebih mungkin untuk kejadian DM pada skor Child Pugh yang lebih tinggi (OR = 9,6, 95% Cl: 1,0 – 88,4).6
Dari data tersebut maka kami ingin menilai apakah ada korelasi skor Child Pugh
BAB II
TINJAUAN PUSTAKA
2.1 Hepatogenous diabetes
Pada sirosis hati sering dijumpai gangguan metabolisma glukosa dimana angka
kejadian intoleransi glukosa 60-80% dan Diabetes Melitus (DM) tipe 2 sekitar 15-30%.
Hepatogenous diabetes merupakan istilah adanya DM pada penderita sirosis hati.3,4 Patogenese DM pada penderita sirosis hati sangat kompleks dan belum
sepenuhnya dimengerti, tetapi diduga terjadinya diabetes melalui proses autoimun,
kerusakan langsung di sel pancreas dan proinflamasi sitokin.
Pada proses autoimun ternyata terjadi fenomena molecular mimicry yang
mengakibatkan kerusakan pada sel pankreas akibat reaksi autoantigen dan
autoantibodi. Hal ini disebabkan karena virus hepatitis C dapat membentuk asam amino
yang homolog dengan GAD (Glutamic Acid Dehidrogenase) sehingga merangsang
terbentuknya GAD antibodi di sel pancreas. Mason dkk (1999), mendeteksi GAD
autoantibodi pada 2 dari 25 penderita hepatogenous diabetes.
Selain itu juga ternyata virus hepatitis C ini dapat juga secara langsung
menyebabkan kerusakan pada sel pankreas. Laskus dkk (1998), menemukan adanya
HCV RNA di sel acinar pankreas dan sel epitel duktus pankreas. Masini dkk (2005),
mendapatkan adanya HVC pada sel pankreas dan menimbulkan perubahan morfologi
pada pankreas dan menurunkan sekresi insulinnya. Tetapi adanya proses autoimune
dan kerusakan langsung pada sel pankreas ini tidak membuat menurunnya fungsi sel
Peranan proinflamasi sitokin pada penderita sirosis hati kaitannya dengan
resistensi insulin belumlah sepenuhnya dimengerti. Lecube dkk (2006), menyebutkan
bahwa protein HCV core menginduksi terjadinya respon imun yang dimediasi sel
limfosit Th1 dan steatosis hati. Limfosit mensekresikan interferon sebagai predominan
sitokinin, yang dapat meningkatkan produksi TNF- oleh makrofag. Aktivasi TNF- ini
melalui reseptor TNFR1 dan TNFR2 mengakibatkan terjadinya resistensi insulin dimana
terjadi hambatan pada proses fosforilasi pada Insulin Receptor Substrate (IRS-1) yang
bertanggung jawab untuk translokasi Glut-4 (Glucose Transporter 4) di hati sehingga
terjadi gangguan uptake glukosa sedangkan sisi lain aktivasi TNF- juga berperan pada
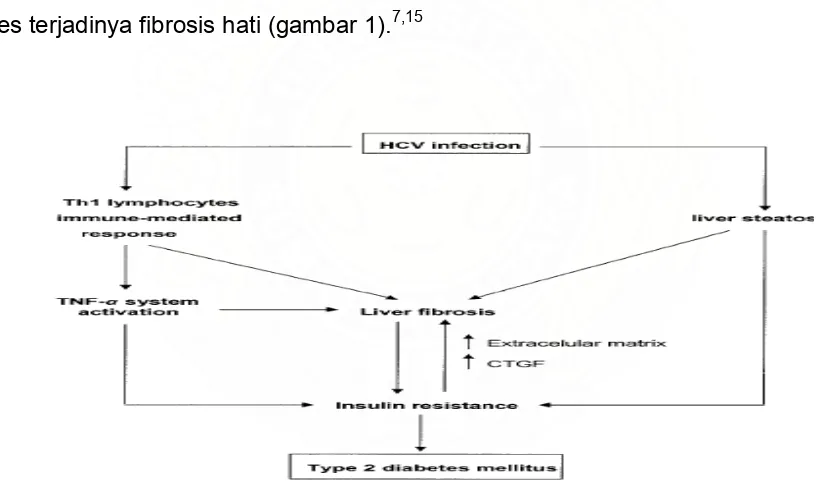
proses terjadinya fibrosis hati (gambar 1).7,15
Gambar 1. Mekanisme terjadinya DM pada hepatitis C dikutip dari 7
Tilg dkk (1992) dan Streetz dkk (2003), menyatakan bahwa selain peningkatan
TNF didapati juga peningkatan interleukin (IL) dan resistin pada penderita sirosis
penderita sirosis hati Child Pugh A dengan Child Pugh C (p<0,01) dan antara penderita
sirosis hati Child Pugh B dengan Child Pugh C (p<0,05). IL-6 ini merupakan salah satu
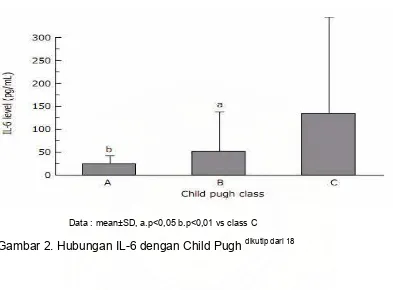
sitokin yang dijumpai pada penderita sirosis dengan hipertensi portal (gambar 2).18
Data : mean±SD, a.p<0,05 b.p<0,01 vs class C
Gambar 2. Hubungan IL-6 dengan Child Pugh dikutip dari 18
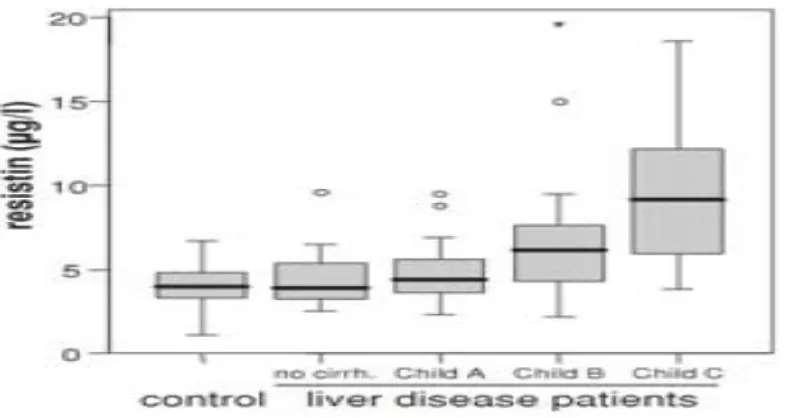
Sedangkan Yagmur dkk (2006) dan Kakizaki dkk (2008), mendapatkan adanya
korelasi peningkatan resistin dengan tingkat keparahan penderita sirosis hati yang
dinilai dengan skor Child Pugh (r=0,391 dan p=0,001). Ini berarti bahwa resistin lebih
tinggi dijumpai pada penderita sirosis hati dengan Child Pugh C dibandingkan Child
Pugh B dan A (gambar 3). Resistin ini merupakan polipeptida dengan ukuran 12,5 kDa
yang dihasilkan sel adiposit yang memiliki kemampuan untuk menurunkan sensitivitas
Gambar 3. Korelasi keparahan sirosis hati dengan resistin dikutip dari 19
Akibat sitokin ini, mengakibatkan adanya gangguan transport glukosa maka
terjadi gangguan uptake glukosa di reseptor sehingga terjadi peningkatan kadar
glukosa darah (hiperglikemia post prandial) dan terjadinya penurunan sensitivitas
insulin. Keadaan ini akan merangsang pengeluaran insulin dari sel pankreas sehingga
terjadi keadaan hiperinsulinemia. Tetapi studi lainnya mendapatkan hal yang berbeda,
bahwa pada penderita sirosis hati tidak dijumpai over produksi insulin.9 Letiexhe dkk (1993), menyatakan hiperinsulinemia pada sirosis hati bukanlah disebabkan karena
hipersekresi pankreas tetapi karena menurunnya klirens insulin hepatik.14 Greco dkk (2002), mendapatkan bahwa hiperinsulinemia terjadi paling tidak pada penderita sirosis
hati Child Pugh B.21
Hiperinsulinemia ini akan mengakibatkan fenomena down regulation dimana
meningkatnya kadar insulin menyebabkan jumlah reseptor insulin berkurang. Hal ini
respon insulin). Cavalio dkk (1985), menyebutkan menurunnya sensitivitas insulin
dengan defek reseptor dan respon insulin yang menurun dengan defek post reseptor.22 Adanya defek pada insulin mengakibatkan insulin tidak mampu bekerja dengan
baik di reseptor insulin. Hal ini disebut dengan resistensi insulin.7,9
Di sisi lain, perubahan struktur hati yang mengalami fibrosis, adanya nodul
disertai resistensi insulin yang terjadi menyebabkan kegagalan reseptor di hati, otot dan
lemak untuk mengkontrol hepatic glucose production (HGP). Petersen dkk (1999) dan
Changani (2001), menyatakan bahwa pada penderita sirosis hati terjadi penurunan
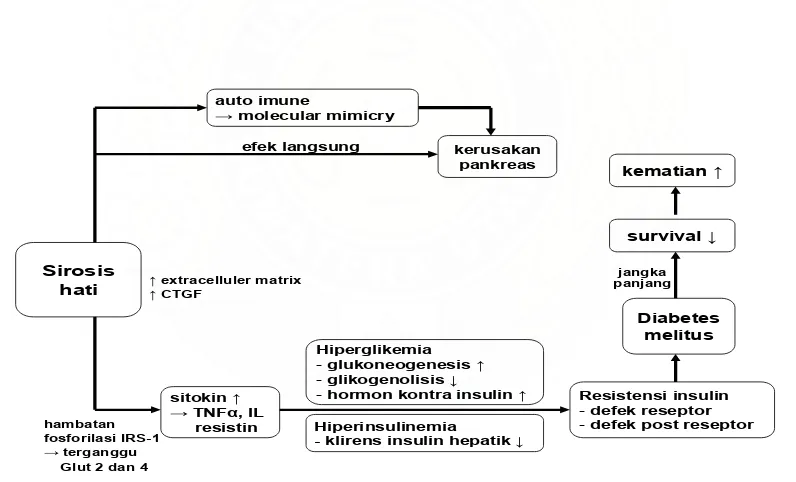
glikogenolisis, peningkatan glukoneogenesis dan hormon kontra insulin.23,24 Secara keseluruhan patogenesa hepatogenous diabetes disederhanakan seperti gambar 1.
Sirosis
Resistensi insulin yang terjadi ini dapat dipastikan dengan melakukan
lalu pada lengan yang lain diberi infus insulin (insulin drips) dan kadar glukosa darah
dipertahankan konstan. Semakin banyak jumlah insulin yang diberikan untuk
mempertahankan kadar glukosa darah tetap konstan berarti semakin rendah
sensitivitas terhadap insulin atau semakin berat resistensi insulin. Namun pemeriksaan
ini sulit dikerjakan dan biayanya mahal maka kini ada cara lain yang dikenal
Homeostatic Model Assesment (HOMA) dengan cara mengukur kadar glukosa darah
dan insulin puasa kemudian dimasukkan ke rumus : HOMA = insulin puasa (µU/ml)x
KGD puasa (mmol/L)/22,5 dengan nilai normal di USA 2,7±0,1. Semakin tinggi nilai
HOMA semakin berat resistensi insulin yang terjadi dan semakin menurun sensitivitas
dan respon insulin.25
Kakizaki dkk (2008), menyatakan bahwa pada penderita sirosis hati dijumpai nilai
HOMA yang lebih tinggi dibandingkan kontrol sehat (4,44±8,2 versus 1,23±0,70 dengan
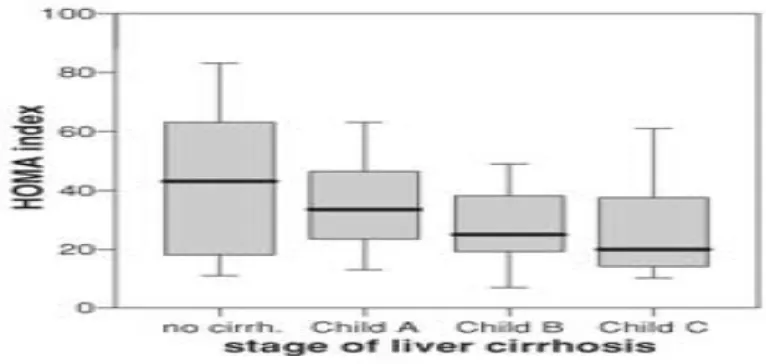
p<0,05).20 Yagmur dkk (2006), mendapatkan bahwa indeks HOMA berkorelasi negatif dengan tingkat keparahan pada penderita sirosis hati. Ini berarti bahwa semakin berat
keparahan penyakit hatinya ternyata sensitivitas insulin semakin rendah (gambar 4).19 Dari hal tersebut diatas, maka semakin tinggi tingkat keparahan sirosis hati maka
kemungkinan didapati kadar glukosa darah yang semakin meningkat. Holstein dkk
(2002), mendapatkan bahwa pada Child Pugh A memiliki kadar glukosa darah yang
lebih rendah dibandingkan Child Pugh B dan C walaupun secara statistik tidak ada
perbedaan bermakna.5 Alavian dkk (2004) mendapatkan bahwa 9,6 kali lebih mungkin untuk kejadian DM pada skor Child Pugh yang lebih tinggi (OR = 9,6, 95% Cl: 1,0 –
Gambar 4. Hubungan indeks HOMA dengan Child Pugh dikutip dari 19
Dan adanya diabetes ini ternyata meningkatkan kejadian resiko infeksi dan
kematian pada jangka panjang. Pada jangka pendek dan menengah, kematian
biasanya disebabkan oleh penyakit hati dan komplikasinya.9 Diaz dkk (2006), mendapatkan bahwa infeksi saluran kemih, pneumoni, selulitis dan spontaneus
bakterial peritonitis merupakan infeksi yang terbanyak pada penderita hepatogenous
diabetes di Peru.10
Komplikasi yang terjadi lebih sering dijumpai pada hepatogenous diabetes
dibandingkan dengan penderita sirosis hati yang tidak diabetes, yang akhirnya
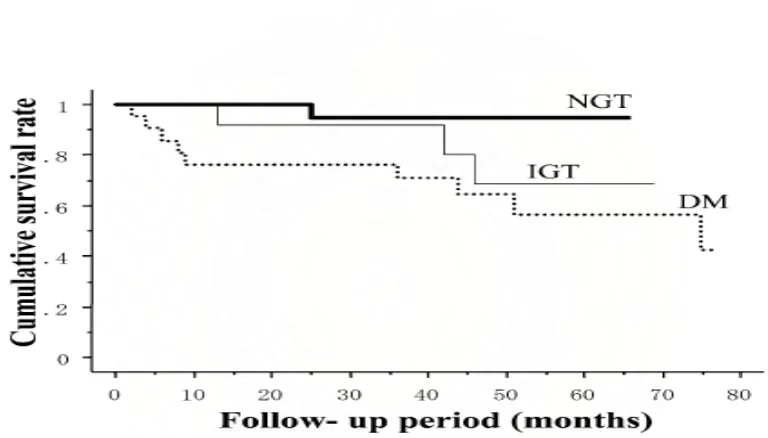
menurunkan angka survival pada jangka panjang.9 Kwon dkk (2004), melaporkan bahwa pada penderita sirosis hati virus B dan C dengan hiperglikemia memiliki angka
survival yang lebih rendah dibandingkan yang normoglikemi.8 Nishida dkk (2006), mendapatkan bahwa survival 5 tahun pada penderita hepatogenous diabetes lebih
rendah dibandingkan dengan normal glukosa dengan kematian terbanyak disebabkan
Oleh sebab itu, perlu dilakukan usaha untuk mengatasi diabetes yang terjadi
pada penderita sirosis hati. Prinsip penatalaksanaan hepatogenous diabetes ini sama
dengan penatalaksanaan DM yang sebenarnya hanya yang perlu diingat adalah bahwa
pada hepatogenous diabetes telah terjadi kerusakan hati sehingga perlu dihindari
obat-obat yang bersifat hepatotoksik. Obat-obat-obat sulfonilurea, repaglinide, biguanide dan
thiazolidine dimetabolisma di hati oleh sebab itu pilihan terbaik dengan menggunakan
insulin.26
Gambar 5. Kumulatif angka survival pada penderita sirosis hati dikutip dari 9
Namun memang tidak ada tes spesifik yang dapat membedakan antara
hepatogenous diabetes dengan diabetes dulu baru kemudian menderita sirosis hati.
Holstein dkk (2002), menyatakan bahwa pada hepatogenous diabetes tidak ada
riwayat keluarga diabetes dan jarang timbul komplikasi makro serta mikro angiopati.
Dan American Diabetes Association (ADA) dan World Health Organization (WHO) tidak
2.2 Skor Child Pugh
Pada tahun 1964, Child dan Turcotte mempublikasikan tentang kriteria empiris
yang mereka temukan untuk menilai cadangan fungsi hati pada penderita sirosis hati.
Variabel penting yang mereka ajukan ada 5 jenis yaitu kadar serum bilirubin, serum
albumin, ascites, gangguan neurologis dan status nutrisi. Kemudian pada tahun 1973,
Pugh dkk memodifikasi kriteria Child, dimana variabel status nutrisi pada kriteria
sebelumnya digantikan dengan waktu protrombin. Untuk kadar albumin, Pugh
memberikan batasan terendah 2,8 mg/dL dimana pada kriteria Child batasan
terendahnya 3 mg/dL. Selanjutnya kriteria tersebut dikenal dengan modifikasi Child
Pugh. Kelima variabel masing-masing dibagi menjadi 3 kelompok yaitu A, B dan C,
yang diberi skor 1, 2 dan 3 secara berturut-turut, sehingga berdasarkan nilai total dari
kriteria ini dapat diklasifikasikan dalam 3 tingkatan yakni tingkat Child Pugh A dengan
skor 5-6, tingkat Child Pugh B dengan skor 7-9 dan Child Pugh C dengan skor total
10-15 (tabel 1).1,2
Tabel 1. Skor Child Pugh dikutip dari 1
Skor 1 2 3
Serum bilirubin (mg/dL) < 2 2 – 3 > 3
Serum albumin (mg/dL) > 3,5 2,8 – 3,5 < 2,8
Ascites tidak ada mudah sulit
dikontrol dikontrol
Gangguan neurologi tidak ada minimal koma
lanjut
Waktu protrombin (detik) < 4 4 – 6 >6
≠: selisih waktu protrombin dengan kontrol (detik)
Sampai saat ini kriteria yang dipakai sebagai parameter dalam upaya
menentukan prognostik sirosis hati adalah skor modifikasi Child Pugh. Kriteria ini juga
dapat dipakai untuk menilai keberhasilan terapi konservatif.2
Prognosis sirosis hati berdasarkan skor kriteria Child Pugh yang dihubungkan
dengan angka mortalitas terhadap tindakan operasi adalah Child Pugh A 10-15%, Child
Pugh B ± 30% dan Child Pugh C > 60%.1,2
2.3 Serum bilirubin
Bilirubin adalah suatu pigmen kuning dengan struktur tetrapirol yang tidak larut
dalam air, berasal dari destruksi sel darah merah (75%), katabolisma protein hem
(22%) dan inaktivasi eritropoesis sum-sum tulang (3%). Bilirubin yang tidak
terkonyugasi, di hati akan mengalami konyugasi dengan enzim glukoronil transferase.
Selanjutnya bilirubin terkonyugasi akan dikonversi menjadi urobilinogen di colon dan
sebagian direabsorpsi dan diekskresikan ginjal dalam bentuk urobilinogen dan
dikeluarkan bersama dengan feses sebagai sterkobilin.
Pemeriksaan bilirubin ini dapat dengan menggunakan metode van den Bergh
assay, dimana dapat ditentukan tingkat bilirubin total dalam serum dan jumlah bilirubin
terkonyugasi ataupun tak terkonyugasi. Pada sirosis hati akan dijumpai peningkatan
produksi bilirubin.1,28
2.4 Serum albumin
Albumin merupakan protein plasma terbanyak dalam tubuh manusia. Kadarnya
albumin darah merupakan hasil kecepatan sintesis hati dikurangi kecepatan degradasi
dan distribusi albumin kedalam ruang intra dan ekstra vaskuler.
Sintesa albumin terutama dihati yaitu sebanyak 9-12 g/hari pada orang dewasa
normal dan merupakan 25% dari total protein yang hati setiap hari. Katabolisma
albumin terjadi di sel hati, dimana sebanyak ± 15% albumin yang sudah tua usianya
akan diurai kembali menjadi berbagai komponen asam amino yang kemudian siap
digunakan untuk berbagai sintesis protein yang dibutuhkan tubuh. Sisanya sebanyak
40-60% di sel otot dan kulit. Distribusi albumin terjadi di dalam pembuluh darah maupun
di luar pembuluh darah (cairan intertitial). Pada sirosis hati akan dijumpai rendahnya
produksi albumin.1,29
2.5 Waktu protrombin
Protrombin (faktor II), faktor VII, IX dan X merupakan faktor koagulasi yang
dihasilkan oleh hati dimana dalam pembentukannya memerlukan vitamin K. Vitamin K
ini pun dihasilkan di hati. Adapun peranan vitamin K pada tahap karboksilasi gugus
gamma glutamil.
Waktu protrombin pertama kali diperkenalkan oleh Quick tahun 1935 dimana
prinsip pemeriksaan ini, mengukur lamanya waktu yang dibutuhkan dalam detik untuk
pembentukan fibrin dari plasma sitrat, setelah penambahan tromboplastin jaringan dan
ion kalsium dalam jumlah optimal. Hasil pemeriksaan waktu protrombin tergantung dari
beberapa hal seperti pengambilan bahan, penanganan bahan pemeriksaan, macam
reagen yang dipakai dan teknik pemeriksaan. Waktu protrombin merupakan ukuran
2.6 Tes Toleransi Glukosa Oral (TTGO)
Pada tahun 1960, TTGO termasuk salah satu pemeriksaan rutin dalam
membantu menegakkan diagnosa DM. Tetapi kemudian Marvin dkk (1975),
menyebutkan bahwa TTGO bukan merupakan rutin karena panjangnya langkah
menegakkan diagnosa DM dan ini menjadi kontroversi selama 35 tahun saat itu. Dan
akhirnya tahun 1997, American Diabetes Association (ADA) mengeluarkan TTGO dari
pemeriksaan rutin untuk penegakkan diagnosa DM.
Tetapi kemudian timbul pertanyaan, kadar glukosa darah berapa dapat
memprediksikan peningkatan resiko terjadinya diabetes. Kemudian Qiano dkk,
mempublikasikan kembali pemeriksaan TTGO untuk menjawab pertanyaan tersebut.
Dan WHO pada tahun 1999, kemudian merekomendasikan kembali TTGO sebagai
pemeriksaan skreening untuk intoleransi glukosa dengan meminum 75 gram glukosa
dengan 250 ml air dan kemudian dilakukan pemeriksaan kadar glukosa darah vena
puasa, ½ jam, 1 jam, 1½ jam dan 2 jam beban glukosa.
Tetapi tahun 2002, World Health Organization (WHO) merekomendasikan bahwa
pada TTGO merupakan pemeriksaan kadar glukosa darah cukup hanya dengan kadar
glukosa darah puasa dan 2 jam setelah beban glukosa.11,12 Schianca dkk (2003), menyatakan bahwa pada TTGO, kadar glukosa darah puasa menggambarkan
sensitivitas insulin dan kadar glukosa darah 2 jam setelah beban glukosa
menggambarkan sekresi insulin.30 Sampel darah dapat menggunakan darah dari vena atau kapiler. Bila menggunakan darah kapiler maka kadar glukosa darah dapat
Penggunaan glucometer dengan sampel darah kapiler telah banyak dilakukan
karena mudah melakukan, tidak menyakitkan bagi penderita dan biayanya lebih murah
dibandingkan plasma vena serta memiliki keakuratan yang cukup baik. Rolka dkk
(2001), mendapatkan bahwa kadar glukosa darah kapiler yang diukur dengan alat
glucometer ternyata memiliki sensitivitas 70% dan spesifisitas 90% untuk menegakkan
kriteria sesuai kriteria WHO 2002.33
Beberapa studi telah mencoba membandingkan antara hasil kadar glukosa
kapiler dengan plasma vena (tabel 2). Hasil kadar glukosa darah dapat dinyatakan
dengan mg/dl atau mmol/l. Konversi mmol/l ke mg/dl dikalikan 18 dan konversi mg/dl ke
mmol/l dibagi 18 atau kali 0,055.31,32
Tabel 2. Nilai TTGO dari plasma vena atau kapiler dikutip dari 31
Tes Toleransi Glukosa Oral (TTGO) Plasma vena Kapiler mmol/l mg/dl mmol/l mg/dl KGD puasa
- DM ≥7,0 ≥126 ≥7,0 ≥126 - Glukosa Darah Puasa Terganggu ≥6,0 ≥110 ≥6,0 ≥110
(GDPT)
KGD 2 jam beban glukosa
- DM ≥11,0 ≥200 ≥12,2 ≥220 - Toleransi Glukosa Terganggu (TGT) ≥7,8 ≥140 ≥8,9 ≥160
2.7 Glucometer
Glucometer merupakan alat untuk melakukan pemeriksaan kadar glukosa darah
kapiler (gambar 6). Alat ini pertama kali diperkenalkan tahun 1980 di Amerika Utara
Pembacaan nilai kadar glukosa darah dilakukan dari perubahan warna yang terjadi
pada strip. Kemudian seiring perkembangan teknologi ditemukan berbagai alat yang
semakin kecil, pembacaan nilai kadar glukosa darah secara digital dan harga yang
semakin murah untuk strip yang digunakan.31,32
Gambar 6. Glucometer dikutip dari 32
Volume darah yang dibutuhkan ± 0,3-10 µl dari ujung jari, dengan pembacaan
dalam satuan mg/dl atau mmol/l tergantung alat yang digunakan.
Glucometer ini menggunakan metode electrochemical dimana pada strip
terdapat elektroda enzim mengandung glucose oxidase. Elektroda ini akan mengukur
kadar konsentrasi glukosa darah yang melaluinya.
Beberapa penelitian telah menilai keakuratan pemeriksaan kadar glukosa darah
kapiler dengan menggunakan glucometer. Pemeriksaan ini ternyata cukup baik dengan
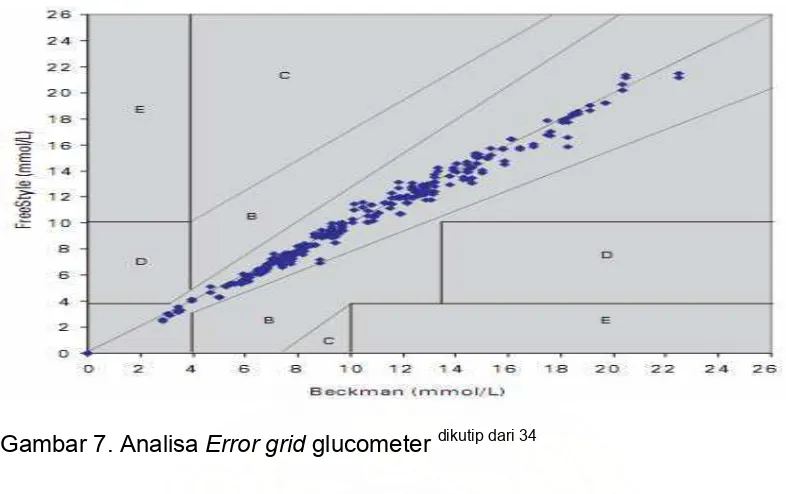
sensitivitas 70% dan spesifisitas 90%.32 Weitgasser dkk (2007), mendapatkan bahwa glucometer memiliki keakuratan yang cukup baik, dimana pada analisa error grid
berada pada zona A (gambar 7). Pada zona A merupakan daerah klinis yang akurat,
zona B ada deviasi > 20%, zone C tidak diperlukan kemungkinan over koreksi, zone D
Gambar 7. Analisa Error grid glucometer dikutip dari 34
Dan beberapa studi telah menggunakan glucometer untuk pemeriksaan kadar
glukosa darah sebagai salah satu cara pemeriksaan kadar glukosa darah. Shah dkk
(2005), menggunakan glucometer untuk monitoring kadar glukosa darah pada penderita
DM yang menerima transplantasi ginjal.35 Gupta dkk (2006), melakukan skrening DM gestational untuk grup resiko tinggi dengan pemeriksaan kadar glukosa darah kapiler.36 Vinita dkk (2006), menggunakan glucometer untuk skrening DM gestational.37
2.8 Retinopati diabetik
Retinopati diabetik merupakan salah satu komplikasi kronik mikroangiopati dari
DM tipe 2 yang sering mengganggu arteri kapiler retina, arteriole dan vena. Kerusakan
pada barier inner blood retina dan oklusi mikrovaskuler.
Retinopati diabetik merupakan penyebab utama kebutaan. Lamanya penderita
12% kasus ini timbul setiap tahunnya. Pada penderita DM tipe 1, kurang lebih dalam 14
tahun akan terjadi sekitar 12,7% gangguan penglihatan dan 2,4% menjadi buta.38,39 Pada hepatogenous diabetes kejadian retinopati diabetik dapat juga terjadi tetapi
lebih jarang dibandingkan pada DM tipe 2. Fujiwara dkk (2005), mendapatkan bahwa
kejadian komplikasi retinopati diabetik dan kardiovaskuler lebih rendah pada
hepatogenous diabetes dibandingkan DM tipe 2 (p<0,05 dan p<0,01).40
Makular edema diabetik merupakan salah satu manifestasi retinopati diabetik
dan berperan penyebab kebutaan pada DM tipe 2. Terjadinya makular edema diabetik
biasanya lebih dari 10 tahun semenjak DM terjadi.
Hiperglikemia kronik memegang peranan patogenesis terjadinya retinopati
diabetik disertai adanya hipertensi dan hiperlipidemia. Dijumpainya perubahan
komposisi struktur dan seluler mikrovaskular dengan peningkatkan permeabilitas
vaskular dan selanjutnya barier blood retina akan rusak dan mengakibatkan akumulasi
cairan ekstraseluler di makula. Perisit yang merupakan komposisi seluler esensial yang
berperanan pada perfusi kapiler retina akan rusak sehingga mengganggu hemodinamik
retina termasuk autoregulasi aliran darah retina dan akhirnya menimbulkan
pembentukan formasi mikroaneurisma. Dan selanjutnya terjadi penebalan membran
basalis kapiler dan peningkatan deposisi komponen matrik ekstraseluler. Darah dari
retinopati diabetik nonproliferatif retinopati diabetik proliferatif
Gambar 8. Retinopati diabetik nonproliferatif dan proliferatif dikutip dari 39
Stadium retinopati diabetik dibedakan atas beberapa stadium no apparent
retinopathy, mild, moderate dan severe nonproliferative diabetic retinopathy (tabel 3).38
BAB III
PENELITIAN SENDIRI
3.1. Latar Belakang
Sirosis hati merupakan penyakit utama di negara-negara Asia yang dapat
menyebabkan morbiditas dan mortalitas. Kejadian di Indonesia menunjukkan bahwa
pria lebih banyak dari wanita (2,4-5:1), dimana kelompok terbanyak didapati pada
dekade kelima. Sedangkan angka kejadian sirosis hati dari hasil otopsi sekitar 2,4% di
negara Barat.
Penyebab terbanyak sirosis hati di Asia Tenggara adalah virus hepatitis B dan C.
Di Indonesia, para penderita sirosis hati memiliki prevalensi virus hepatitis B
21,2-46,9% dan virus hepatitis C 38,7-73,9%.1,2
Pada sirosis hati sering dijumpai gangguan metabolisma glukosa dimana sekitar
60-80% terjadi intoleransi glukosa dan dalam 5 tahun kemudian 15-30% diantaranya
dapat menjadi Diabetes Melitus (DM) tipe 2. Dan Nauryn (1906), pertama kali
menyebutkannya dengan hepatogenous diabetes, sebagai istilah DM yang terjadi pada
penderita sirosis hati.3,4
Patogenese hepatogenous diabetes sangat kompleks dan belum sepenuhnya
dimengerti, tetapi diduga berkaitan dengan proses autoimune, kerusakan langsung
pada sel pankreas dan peranan proinflamasi sitokin yang mengakibatkan keadaan
hiperglikemia post prandial dan hiperinsulinemia.7 Dengan melakukan Tes Toleransi Glukosa Oral (TTGO) akan dijumpai peningkatan kadar glukosa darah puasa dan 2 jam
Pada beberapa studi juga didapatkan bahwa hepatogenous diabetes ternyata
memiliki harapan hidup yang lebih rendah dibandingkan penderita sirosis hati yang
glukosa normal dalam pengamatan jangka panjang. Kwon dkk (2004), melaporkan
bahwa pada penderita sirosis hati viral B dan C dengan hiperglikemia memiliki angka
harapan hidup yang lebih rendah dibandingkan penderita sirosis hati yang
normoglikemia.8 Nishida dkk (2006), mendapatkan bahwa angka harapan hidup 5 tahun pada penderita hepatogenous diabetes sekitar 56,6% sedangkan bila penderita sirosis
hati yang glukosa normal sekitar 94,7%. Kematian penderita hepatogenous diabetes
pada studi ini disebabkan oleh koma hepatik, infeksi dan perdarahan varises.9 Ini berarti penderita hepatogenous diabetes lebih berkemungkinan untuk lebih sering terjadi koma
hepatik, infeksi dan perdarahan varises dibandingkan penderita sirosis hati yang normal
glukosa.5 Diaz dkk (2006), mendapatkan infeksi lebih sering terjadi pada hepatogenous diabetes dibandingkan penderita sirosis yang tidak diabetes (OR=5,90, 95% Cl:
2,47-14,18).10 Oleh karena itu untuk meningkatkan angka harapan hidup pada hepatogenous diabetes diperlukan juga penatalaksanaan terhadap diabetesnya melengkapi
penatalaksanaan utama lainnya pada penderita sirosis hati.26
Untuk menilai adanya intoleransi glukosa yang terjadi dapat dilakukan dengan
pemeriksaan TTGO. Tes ini dilakukan menurut cara World Health Organization (WHO)
1999 dengan melakukan pemeriksaan kadar glukosa darah vena puasa, ½ jam, 1 jam,
1½ jam dan 2 jam setelah beban glukosa 75 gram. Tetapi pengambilan sampel darah
yang berasal dari vena menyakitkan bagi penderita, lebih mahal dan lebih sulit
dilakukan maka sampel darah dari kapiler dapat dilakukan. Bila menggunakan dari
Indeks untuk menilai keparahan penyakit hati yang sering digunakan adalah
kriteria Child Pugh. Kriteria ini telah menjadi dasar indeks keparahan penyakit hati sejak
formulasinya digunakan untuk menghitung stratifikasi resiko pasien yang akan
menjalani operasi pemintasan dan saat ini digunakan sebagai prognostik pada
penderita sirosis hati. Kriteria ini terdiri dari 5 parameter yang dinilai dimana
masing-masing diberi skor dan jumlah skor dibedakan atas gradasi A, B dan C dimana gradasi
C menunjukkan tingkat keparahan yang lebih berat. Ini berarti bahwa penderita sirosis
hati dengan Child Pugh C memiliki mortalitas yang lebih besar dibandingkan penderita
sirosis hati dengan Child Pugh A dan B.1,2
Saat ini, beberapa studi mencoba menghubungkan antara kriteria Child Pugh
dengan kadar glukosa darah pada penderita sirosis hati. Holstein dkk (2002),
mendapatkan bahwa pada Child Pugh A ternyata memiliki kadar glukosa darah yang
lebih rendah dibandingkan Child Pugh B dan C walaupun secara statistik tidak ada
perbedaan bermakna.5 Alavian dkk (2004), mendapatkan 9,6 kali lebih mungkin untuk kejadian DM pada skor Child Pugh yang lebih tinggi (OR = 9,6, 95% Cl: 1,0 – 88,4).6 Nishida dkk (2006), menganjurkan TTGO dapat dilakukan turut sebagai pemeriksaan
rutin pada penderita sirosis hati untuk penatalaksanaan yang menyeluruh sehingga
lebih dapat meningkatkan angka harapan hidupnya.9
Dari data tersebut maka kami hanya ingin menilai apakah ada korelasi skor Child
Pugh dengan kadar glukosa darah penderita sirosis hati yang sepengetahuan kami
3. 2. Perumusan masalah
Apakah ada korelasi skor Child Pugh dengan kadar glukosa darah pada
penderita sirosis hati
3. 3. Hipotesa
Ada korelasi skor Child Pugh dengan kadar glukosa darah pada penderita
sirosis hati
3. 4. Tujuan penelitian
Untuk mengetahui korelasi skor Child Pugh dengan kadar glukosa darah pada
penderita sirosis hati
3. 5. Manfaat penelitian
- Dengan penelitian ini diharapkan kadar glukosa darah yang diperiksa dengan
TTGO dapat turut digunakan sebagai salah satu parameter lain untuk menilai
keparahan penyakit hati bersama dengan kriteria Child Pugh
- TTGO turut sebagai pemeriksaan rutin pada penderita sirosis hati
- Sebagai data dasar bagaimana gambaran gangguan metabolisma glukosa pada
3. 6. Kerangka konsepsional
Penelitian ini dilakukan secara studi potong lintang
3.7.2 Waktu dan tempat penelitian
Penelitian dilakukan mulai bulan Februari s/d November 2008 di RSUP H. Adam
Malik Medan dan RSUD Pirngadi Medan.
3.7.3 Populasi terjangkau
Penderita sirosis hati yang rawat jalan poliklinik ataupun rawat inap di
3.7.4 Kriteria inklusi :
- Penderita sirosis hati
- Bersedia ikut dalam penelitian (informed consent)
3.7.5 Kriteria eksklusi
- Penderita DM sebelumnya
- Riwayat keluarga DM
- KGD sewaktu ≥ 200 mg/dl - Penderita retinopati diabetik
- Penderita memakai OAD atau insulin atau kortikosteroid
3.7.6 Besar sampel
Untuk menentukan besar sampel digunakan rumus41,42 : N = Z 2P.Q
d2
dimana Z = nilai baku normal berdasarkan = 0,05 Z = 1,96
P = proporsi penderita sirosis hati diasumsikan 70% 0,70
d = presisi (besarnya penyimpangan yang dapat ditolerir), 15%
Q = (1-P) = (1,0-0,70) =0,30
N = (1,96)2 x 0,70 x 0,30 = 36 (0,15)2
3.7.7 Cara penelitian
Setiap penderita sirosis hati yang datang berobat jalan di poliklinik
Gastroenterohepatologi Penyakit Dalam, maupun yang dirawat inap, dianamnesis
serta dilakukan pemeriksaan fisik, laboratorium (bilirubin, albumin, waktu
protrombin, SPE, viral marker), ultrasonografi abdomen atas dan funduskopi.
Pemeriksaan funduskopi dilakukan di poliklinik mata. Setelah memenuhi kriteria
penelitian, diberikan penjelasan kepada pasien ataupun keluarga dekat yang
mewakilinya untuk mengisi formulir (informed consent), kemudian dinilai skor
Child Pughnya dan penderita sirosis hati tersebut dikelompokkan berdasarkan
Child Pugh A, Child Pugh B dan Child Pugh C.
Kadar glukosa darah penderita sirosis hati dinilai dengan melakukan
pemeriksaan Tes Toleransi Glukosa Oral (TTGO). Tes ini dilakukan menurut cara
WHO tahun 1999, dengan cara sebagai berikut :
-3 hari sebelum pemeriksaan tetap makan seperti kebiasaan sehari-hari
dan tetap melakukan kegiatan jasmani seperti biasa
-berpuasa paling sedikit 8 jam (mulai malam hari) sebelum pemeriksaan
-minum air putih tanpa gula tetap diperbolehkan, kemudian diperiksa
kadar glukosa darah puasa dari kapiler dengan glucometer
-diberikan glukosa 75 gram yang dilarutkan dalam air 250 ml dan diminum
dalam waktu 5 menit
-berpuasa kembali sampai pengambilan sampel darah untuk pemeriksaan
kadar glukosa darah ½ jam, 1 jam, 1½ jam dan 2 jam setelah beban
Berdasarkan hasil kadar glukosa darah puasa, ½ jam, 1 jam, 1½ jam dan
2 jam beban glukosa tersebut, penderita sirosis dikelompokkan pada kelompok
Diabetes Melitus, intoleransi glukosa dan glukosa normal.
3.7.8 Analisa data
Semua data yang diperlukan dimasukkan kedalam tabel induk dengan
menggunakan bantuan program komputer. Kemudian data diolah dan dianalisis
dengan bantuan program SPSS 11,5. Data deskriptif disajikan dalam bentuk teks,
tabel dan gambar untuk dianalisis. Hasil penelitian dituangkan berupa rerata,
simpang baku.
Untuk menilai perbedaan rerata bilirubin, albumin dan waktu protrombin
pada kelompok penderita sirosis hati DM, intoleransi glukosa dan glukosa normal
digunakan uji Anova jika data terdistribusi normal dan uji Kruskal Wallis jika data
tidak terdistribusi normal. Dan untuk menilai perbedaan rerata albumin ada pada
kelompok mana diantara ke-3 kelompok penderita sirosis hati berdasarkan
gangguan metabolisma glukosa digunakan uji Post Hoc dengan Least Significant
Difference test.
Untuk menilai perbedaan rerata kadar glukosa darah puasa, ½ jam, 1 jam,
1½ jam dan 2 jam beban glukosa pada kelompok penderita sirosis Child Pugh A,
Child Pugh B dan Child Pugh C digunakan uji Anova jika data terdistribusi normal
dan uji Kruskal Wallis jika data tidak terdistribusi normal. Dan untuk menilai
kelompok mana diantara ke-3 kelompok penderita sirosis hati berdasarkan Child
Pugh digunakan uji Post Hoc dengan Least Significant Difference test.
Untuk mengetahui korelasi antara skor Child Pugh dengan kadar glukosa
darah puasa, ½ jam, 1 jam, 1½ jam dan 2 jam digunakan uji Pearson.
Untuk mengetahui korelasi antara kadar glukosa darah puasa, ½ jam, 1
jam, 1½ jam dan 2 jam dengan bilirubin, albumin dan waktu protrombin digunakan
uji Pearson.
Hasil analisis dianggap bermakna apabila p < 0,05.41,42
3.7.9. Defenisi operasional
a. Sirosis hati :
diagnosis penyakit hati ditegakkan dengan anamnesis, pemeriksaan fisik,
laboratorium dan ultrasonografi abdomen atas.
b. Kadar glukosa darah dinilai dengan Tes Toleransi Glukosa Oral (TTGO)
dimana diperoleh nilai kadar glukosa darah puasa, ½ jam, 1 jam, 1½ jam dan
2 jam beban glukosa.
c. Diabetes Melitus (DM) bila hasil TTGO :
- KGD puasa ≥126 mg/dL atau
- KGD 2 jam beban glukosa ≥ 220 mg/dL d. Intoleransi glukosa (IG) bila hasil TTGO :
- KGD puasa 110-125 mg/dL dan
e. Glukosa normal (GN) bila hasil TTGO :
- KGD puasa <110 mg/dL dan
- KGD 2 jam beban glukosa <160 mg/dL
f. Skor Child Pugh :
skor untuk menilai keparahan penyakit hati pada penderita sirosis hati (tabel 1)
BAB IV
HASIL PENELITIAN DAN PEMBAHASAN
4.1 Hasil penelitian
4.1.1. Karateristik dasar penderita sirosis hati
Kami melakukan penelitian terhadap 36 orang subjek di unit Rawat Jalan dan
Rawat Inap RSUP H. Adam Malik dan RSUD Dr. Pirngadi Medan, Departemen
Penyakit Dalam FK USU. Subjek penelitian adalah penderita sirosis hati yang diambil
datanya dari Februari 2008 sampai dengan November 2008.
Kisaran usia subjek peneltian berada diantara 28 – 71 tahun dengan rerata usia
51,17±10,96 tahun (tabel 1).
Tabel 1. Rerata umur penderita sirosis hati
Parameter Rerata ± SB Kisaran
Umur (tahun) 51,17 ± 10,96 28 - 71
Ket : SB = Simpang Baku
Dari seluruh subjek penelitian ada 24 orang (67%) berjenis kelamin laki-laki dan
12 orang (33%) wanita. Etiologi sirosis hati terbanyak penderita dengan petanda virus
HbsAg positif (72%). Ada 12 orang (33%) penderita sirosis hati dengan riwayat
ensefalopati dan 24 orang (61%) dengan ascites. Dan dengan menilai Child Pugh ada
16 orang (44%) penderita sirosis dengan Child Pugh B dan dengan TTGO ada 15 orang
Tabel 2. Karakteristik demografi dan klinis penderita sirosis hati
Rerata nilai variabel laboratorium dan simpang baku seluruh subjek penelitian
Tabel 3. Rerata nilai laboratorium penderita sirosis hati
Parameter Rerata ± SB Kisaran
Bilirubin total (mg/dl) 2,99 ± 2,52 0,79 - 11,59
4.1.2. Gambaran gangguan metabolisma glukosa pada penderita sirosis hati
Child Pugh
Gambar 2. Prevalensi gangguan metabolisma glukosa berdasarkan Child Pugh
Setelah dilakukan TTGO, diperoleh nilai kadar glukosa darah puasa dan 2 jam
36 orang subjek penelitian, ada 29 orang (81%) penderita sirosis hati mengalami
gangguan metabolisma glukosa dimana 15 orang (42%) penderita sirosis hati DM, 14
orang (39%) penderita sirosis hati intoleransi glukosa sedangkan 7 orang (18%)
penderita sirosis hati glukosa normal (gambar 2).
Studi kami ini juga menunjukkan adanya perbedaan rerata bermakna variabel
albumin antara ke-3 kelompok penderita sirosis hati berdasarkan gangguan
metabolisma glukosa (tabel 4).
Tabel 4. Rerata variabel laboratorium berdasarkan gangguan metabolisma glukosa
Parameter Glukosa
Normal
(n=7)
Intoleransi
Glukosa
(n=14)
DM
(n=15)
Billirubin total (mg/dl) 1,67±0,21 3,02±3,22* 3,58±2,24**
Albumin (mg/dl) 4,17±0,88 3,06±0,90 2,70±0,43
Waktu protrombin (det) 15,34±2,15 17,18±3,03 20,10±5,94
Ket : Rerata±SB, *p=0,003 **p=0,000 banding Glukosa Normal
Dengan analisis Post Hoc, ternyata didapati bahwa perbedaan rerata albumin
ada antara kelompok penderita sirosis hati DM dengan glukosa normal (p=0,000),
antara penderita sirosis hati intoleransi glukosa dengan glukosa normal (p=0,003)
sedangkan antara penderita sirosis hati DM dengan intoleransi glukosa tidak dijumpai
4.1.3 Korelasi skor Child Pugh dengan kadar glukosa darah
Pada penelitian ini juga dijumpai adanya perbedaan rerata kadar glukosa darah
puasa dan 2 jam beban glukosa antara ke-3 kelompok penderita sirosis hati
berdasarkan Child Pugh (tabel 5).
Tabel 5. Rerata variabel laboratorium berdasarkan Child Pugh
Parameter CP A
KGD puasa (mg/dl) 98,88±2,74 116,13±22,04* 186,33±75,50**a
KGD ½ jam beban (mg/dl) 217,63±31,91 187,75±45,95 199,83±75,71
KGD 1 jam beban (mg/dl) 199,25±30,26 203,81±44,07 186,75±41,30
KGD 1½ jam beban (mg/dl) 181,38±44,96 206,00±51,62 185,58±41,41
KGD 2 jam beban (mg/dl) 145,13±13,90 180,50±35,44† 237,67±40,84††b
Ket : Rerata ± SB, *p=0,000 **p=0,003 banding CP A, a p=0,008 banding CP B
†p=0,032 ††p=0,000 banding CP A, b p=0,001 banding CP B
Dengan analisis Post Hoc, ternyata didapati bahwa perbedaan rerata kadar
glukosa darah puasa dan 2 jam beban glukosa ada antara kelompok penderita sirosis
hati Child Pugh A dengan Child Pugh B (p=0,000 dan p=0,032), antara penderita sirosis
hati Child Pugh A dengan Child Pugh C (p=0,003 dan p=0,000) dan antara penderita
sirosis hati Child Pugh B dengan Child Pugh C (p=0,008 dan p=0,001).
Dilakukan uji korelasi dan didapati bahwa ada korelasi positif antara skor Child
Pugh dengan kadar glukosa darah puasa (r=0,671 dengan p=0,000) dan 2 jam beban
glukosa darah ½ jam, 1 jam dan 1½ jam beban glukosa berkorelasi tetapi tidak
bermakna secara statistik (tabel 6).
Tabel 6. Korelasi antara Skor Child Pugh dengan kadar glukosa darah
KGD
Ket : r : kekuatan korelasi, p= tingkat kemaknaan, bermakna p<0,05
Gambar 3. Korelasi skor Child Pugh dengan kadar glukosa darah
A. kadar glukosa darah puasa (r=0,67 , p=0,000)
B. kadar glukosa darah 2 jam beban glukosa (r=0,73, p=0,000)
Pada gambar 3 ini, terlihat bahwa semakin tinggi skor Child Pugh maka semakin
4.1.4 Korelasi antara kadar glukosa darah dengan bilirubin, albumin dan waktu
protrombin
Untuk mengetahui korelasi antara kadar glukosa darah dengan bilirubin, albumin
dan waktu protrombin dilakukan uji korelasi (tabel 7).
Tabel 7. Korelasi antara kadar glukosa darah dengan bilirubin, albumin dan waktu
protrombin
Ket : r : kekuatan korelasi, p= tingkat kemaknaan, bermakna p<0,05
Dari tabel 10 ini, dapat dilihat bahwa kadar glukosa darah puasa berkorelasi
positif bermakna dengan bilirubin dan waktu protrombin (r=0,374 , p=0,025 dan r=0,462
p=0,005). Dan kadar glukosa darah 2 jam beban glukosa berkorelasi positif bermakna
dengan bilirubin dan waktu protrombin (r=0,455 , p=0,005 dan r=0,338 , p=0,044).
Sedangkan kadar glukosa darah puasa dan kadar glukosa darah 2 jam beban glukosa
berkorelasi negatif bermakna dengan albumin (r=-0,374, p=0,025 dan r=-0,539 ,
p=0,001). Sedangkan kadar glukosa darah ½ jam, 1 jam dan 1½ jam berkorelasi
4.2. Pembahasan
Sirosis hati paling sering dijumpai pada usia dekade kelima dimana
perbandingan jenis kelamin pria dan wanita berkisar antara 2,5-4:1 dengan etilogi
tersering virus hepatitis C.1,2 Studi kami memperlihatkan hal yang sama dimana penderita sirosis hati dijumpai pada usia rerata 51,17±10,97 dimana perbandingan pria
dan wanita 2:1 dengan etiologi terbanyak oleh karena virus hepatitis B.
Pada sirosis hati sering dijumpai intoleransi glukosa dengan angka kejadian
60-80% dan diabetes sekitar 15-30%.3,4 Diabetes yang terjadi pada penderita sirosis hati dikenal dengan hepatogenous diabetes. Studi ini kami mendapatkan hal yang tidak
berbeda dimana angka kejadian diabetes sekitar 42 % dan intoleransi glukosa sekitar
39%. Ini menunjukkan bahwa sebahagian besar penderita sirosis hati (81%) telah
terjadi gangguan fungsi hati yang berkaitan dengan metabolisma glukosa dimana terjadi
peningkatan proses glukoneogenesis dan penurunan proses glikogenolisis.22,23
Pada hepatogenous diabetes dijumpai penurunan rerata albumin, peningkatan
kadar glukosa darah puasa dan 2 jam beban glukosa. Holstein dkk (2002),
mendapatkan bahwa ada perbedaan rerata albumin antara penderita sirosis hati yang
diabetes dengan intoleransi glukosa (p<0,0001). Yagmur dkk (2006), mendapatkan
adanya korelasi negatif (r=-0,477) antara albumin dengan tingkat keparahan penderita
sirosis hati (Child Pugh). Studi kami mendapatkan adanya perbedaan rerata albumin
antara kelompok penderita sirosis hati diabetes dengan glukosa normal (p<0,000) dan
antara penderita sirosis hati intoleransi glukosa dengan glukosa normal (p<0,003).
Untuk menilai kadar glukosa ini dapat dilakukan dengan Tes Toleransi Glukosa
termasuk pemeriksaan rutin untuk menegakkan DM tetapi saat ini tidak lagi merupakan
penilaian rutin tetapi untuk skrening intoleransi glukosa. WHO tahun 1999
merekomendasi 75 gram glukosa dalam 250 ml air dan yang diperiksa kadar glukosa
darah puasa, ½ jam, 1 jam, 1½ jam dan 2 jam beban glukosa. Pengambilan sampel dari
darah plasma vena. Tetapi kemudian pada tahun 2002, WHO merekomendasi
pemeriksaan kadar glukosa darah dengan kadar glukosa darah puasa dan 2 jam beban
glukosa saja serta pengambilan sampel darah dapat dari vena atau kapiler.
Pengambilan darah kapiler lebih disukai dari pada darah vena karena tidak terlalu
menyakitkan bagi penderita, lebih murah dan mudah. Pemeriksaan kadar glukosa
darah kapiler dengan menggunakan alat glucometer memiliki ketepatan yang cukup
akurat.11,12 Weitgasser dkk (2007), menyatakan glucometer memiliki keakuratan yang cukup baik. Dan saat ini, banyak studi telah menggunakan alat glucometer untuk
pemeriksaan kadar glukosa darah diantaranya Shah dkk (2005), Gupta dkk (2006) serta
Vinita dkk (2006).37,38,39 Studi kami juga menggunakan cara TTGO sesuai WHO 1999 dengan sampel darah kapiler yang diperiksa dengan alat glucometer.
Beberapa studi mencoba mencari hubungan antara skor Child Pugh dengan
kadar glukosa darah. Holstein dkk (2002), mendapatkan bahwa pada Child Pugh A
memiliki kadar glukosa darah yang lebih rendah dibandingkan Child Pugh B dan C
walaupun secara statistik tidak ada perbedaan bermakna.5 Alavian dkk (2004), mendapatkan bahwa 9,6 kali lebih mungkin untuk kejadian diabetes pada skor Child
Pugh yang lebih tinggi (OR = 9,6, 95% Cl: 1,0 – 88,4).6 Studi kami ini mendapatkan bahwa ada perbedaan rerata kadar glukosa darah puasa dan 2 jam beban glukosa
ada korelasi positif bermakna antara skor Child Pugh dengan kadar glukosa darah
puasa (r=0,671 , p=0,000) dan kadar glukosa darah 2 jam beban glukosa (r=0,730 ,
p=0,000). Ini berarti semakin tinggi nilai skor Child Pugh semakin tinggi kadar glukosa
darah puasa dan 2 jam beban glukosa. Kami juga mendapatkan adanya korelasi positif
bermakna antara kadar glukosa darah puasa dan 2 jam beban glukosa dengan bilirubin
dan waktu protrombin. Didapat juga adanya korelasi negatif bermakna antara kadar
glukosa darah puasa dan 2 jam beban glukosa dengan albumin.
Keterbatasan studi ini, bahwa merupakan studi potong lintang dengan
pengukuran variabel hanya dilakukan satu kali, sehingga hasilnya tidak dapat dipakai
untuk menilai perkembangan dan mortalitas subjek selanjutnya, tidak ada alat ukur
standar untuk membedakan apakah penderita ini merupakan murni hepatogenous
diabetes atau diabetes dulu baru kemudian menderita sirosis hati serta penilaian
funduskopi tidak dilakukan oleh dokter spesialis mata yang sama di poliklinik mata.
Untuk melengkapi penelitian ini perlu dilakukan penelitian serupa yang menggunakan
BAB V
KESIMPULAN DAN SARAN
5.1 Kesimpulan
5.1.1 Skor Child Pugh berkorelasi positif bermakna dengan kadar glukosa darah pada
penderita sirosis hati
5.2.2 Kadar glukosa darah puasa dan 2 jam beban glukosa berkorelasi positif
bermakna dengan bilirubin dan waktu protrombin serta berkorelasi negatif
bermakna dengan albumin
5.2 Saran
5.2.1. Hasil penelitian ini menunjukkan perlunya untuk pemeriksaan kadar glukosa
darah yang diperiksa dengan TTGO sebagai pemeriksaan rutin pada penderita
sirosis hati
5.2.2. Perlu untuk dilakukan penelitian yang melibatkan subjek lebih banyak dan
dengan rancangan serta cara yang lebih baik untuk memperoleh bukti adanya
korelasi skor Child Pugh dengan kadar glukosa darah dan mortalitas pada
penderita sirosis hati
BAB VI
DAFTAR PUSTAKA
1. Nurdjanah S. Sirosis hati. Dalam: Sudoyo AW, Setiyohadi B, Alwi I, Simadibrata M,
Setiati S (ed). Buku Ajar Ilmu Penyakit Dalam. Edisi ke-4. Jakarta. Balai Penerbit FK
UI. 2007: 443-51
2. Sherlock S, Dooley J. Anatomy and function. In: Disease of the liver and biliary
system. 10th Ed. Blackwell scine. Nalden 1997: 1-16
3. Petrides AS, Stanley T, Matthews DE, Vogt C, Bush AJ, Lambeth H. Insulin
Resistance in Cirrhosis: Prolonged Reduction of Hyperinsulinemia Normalizes
Insulin Sensitivity. Hepatology 1996; 28: 141-9
4. Perseghin G, Mazzaferro V, Sereni LP, Regalia E, Benedini S, Bazzigaluppi E, et al.
Contribution of reduced insulin sensitivity and secretion to the phatogenesis of
hepatogenous diabetes; Effect of the Liver Transplantion. Hepatology 2000; 31 (3):
684-703
5. Holstein A. Hinze S, Thiesen E, Plaschke A, Egberts EH. Hepatogenous Diabetes in
Liver Cirrhosis. Clinical implications of hepatogenous diabetes in liver cirrhosis.
Journal of Gastroentrology and Hepatology 2002; 17: 677-81
6. Alavian SM, Hajarizadeh B, Nematizadeh F, Larijani B. Prevalance and
determinants of diabetes mellitus among Iranian patients with chronic liver disease.
BMC Endocrine Disorder 2004; 4 (4); 1-7
7. Lecube A, Hernandez C, Genesca J, Simo R. Glucose abnormalities in patients with
8. Kwon SY, Kim SS, Kwon OS, Kwon KA, Chung MG, Park DK, et al. Prognostic
significance of glycaemic control in patients with HBV and HCV related cirrhosis and
diabetes mellitus. Diabetic Medicine 2004; 22: 1530-35
9. Nishida T, Tsuji S, Tsujii M, Aritmisu S, Haruna Y, Imano E, et al. Oral glucose
tolerance test predicts prognosis of patients with liver cirrhosis. American Journal of
Gastroenterology 2006; 101: 70-5
10. Diaz J, Monge E, Roman R, Ulloa V. Diabetes as a risk factor for infection in
cirrhosis. American Journal of Gastroenterology 2008; 248: 1-2
11. World Health Organization. Laboratory Diagnosis and Monitoring of Diabetes
Mellitus 2002
12. Genuth S, Alberti KG, Bennett P, Buse J, DeFronzo R, Katin R, et al. Follow up
report on the diagnosis of diabetes mellitus. Diabetes Care 2003; 26: 3160-7
13. Konsensus Pengelolaan dan Pencegahan Diabetes Melitus tipe 2 di Indonesia 2006
14. Letiexhe MR, Schreen AJ, Gerard PL, Basten BH, Pirotte J, Belaiche J, et al. Insulin
secreation, clearance and action on glucose metabolism in cirrhosis patients.
Journal of Clinical Endocrinology and Metabolism 1993; 1263-6
15. Gomez MR. Insulin resistance and hepatitis C. World J Gastroenterol 2006; 12 (44):
7075-80
16. Tilg H, Wilmer A, Vogel W. Serum levels of cytokines in chronic liver disease
(abstract). Gastroenterology 1992: 103; 264-74
17. Streetz KL, Tacke F, Leifeld L. Interleukin 6/gp 130-dependent pathways are
18. Elsing C, Harenberg S, Stremmel W, Herrman T. Serum levels of soluable fas, nitric
oxide and cytokines in acute decompensated cirrhotic patients. World J
Gastroenterol 2007: 13 (3): 421-25
19. Yagmur E, Trautwein C, Gressner AM, Tacke F. Resistin serum levels are
associated with insulin resistance, disease severity, clinical complication and
prognosis in patients with chronic liver disease. American Journal of Gatroenterology
2006: 101; 1244-52
20. Kakizaki S, Sohara N, Yamazaki Y, Horiguchi N, Kanda D, Kabeya K, et al. Elevated
plasma resistin concentration in patients with liver cirrhosis. Journal of
Gastroenterology and Hepatology 2008: 23; 73-7
21. Greco AV, Mingrone G, Mari A, Capristo E, Manco M, Gasbarrini G. Mechanism of
hyperinsulinemia in Child’s disease grade B liver cirrhosis investigated in free living
conditions. Gut 2002: 51; 870-75
22. Cavalio P, Cassader M, Bozzo C, Bruno A, Nuccio P, Daliomo AM, et al. Mechanism
of insulin resitance in human liver cirrhosis Evidance of a combined receptor and
postreceptor defect. J. Clin. Invest 1985: 75; 1659-65
23. Peterson KF, Krssak M, Navarro V, Chandramouli V, Hundal R, Schumann WC, et
al. Contributions of net hepatic glycogenolysis and gluconeogenesis to glucose
production in cirrhosis. Endocrinol Metab 1999: 39; E529-35
24. Changani KK, Jalan R, Cox IJ, Korpela MA, Bhakoo K, Robinson SDT, et al.
Evidance for altered hepatic gluconeogenesis in patients with cirrhosis using in vivo
25. Karam JH, German MS. Pancreatic Hormone and Diabetes Mellitus. In: Greenspan
FS, Gardner DG. Basic and clinical endocrinology. 7th ed New York : Mc Graw Hill 2004. p658-46
26. MCNeely M. Case study : Diabetes in patient with cirrhosis. Clinical Diabetes 2004:
22 (1); 42-3
27. Tolman K, Dalpiaz A, Fonseca V, Tan MH. Spectrum of liver disease in type 2
diabetes and management of patients wity diabetes and liver disease. Diabetes
Care 2007: 30 (3); 734-43
28. Amirudin R. Fisiologi dan biokimia hati. Dalam: Sudoyo AW, Setiyohadi B, Alwi I,
Simadibrata M, Setiati S (ed). Buku Ajar Ilmu Penyakit Dalam. Edisi ke-4. Jakarta.
Balai Penerbit FK UI. 2007: 415-9
29. Pemberian albumin pada sirosis hati. Konsensus FKUI-PPHI 4 Juli 2003; 1-2
30. Schianca GP, Rossi A, Sainaghi PP, Maduli E, Bartoli E. The significance of
impaired fasting glucose versus impaired glucose tolerance. Diabetes Care 2003; 26
(5); 1333-7
31. Diabetes Guidelines Health-care Europe Type 2. Available from : http://www.
.staff.ncl.ac.uk/philip.home/t2dgch1a.htm. Cited et November 2007
32. Glucosemeter. Available from : http://www.en.wikipedia.org/wiki/Glucose-meter.
Cited et November 2007
33. Rolka DB, Narayan KMV, Thompson TJ, Goldman D, Lindenmayer J, Alich K, et al.
Performance of recommended screening test for undiagnosed diabetes and