ABSTRAK
PENGARUH AMNION LIOFILISASI STERIL-RADIASI (ALS-R) TERHADAP PENYEMBUHAN FRAKTUR FEMUR YANG DILAKUKAN OPEN REDUCTION INTERNAL FIXATION (ORIF) PADA TIKUS PUTIH
SPRAGUE DAWLEY
Oleh
Suci Widya Primadhani
Penatalaksanaan fraktur dengan metode Open Reduction Internal Fixation (ORIF) memiliki kekurangan berupa risiko tinggi infeksi, non union, kegagalan implantasi dan refraktur. Amnion Liofilisasi Steril-Radiasi (ALS-R) telah diketahui memiliki growth factor dan cell scaffold yang dapat berperan dalam penyembuhan fraktur. Penelitian ini dilakukan untuk mengetahui pengaruh penambahan ALS-R pada ORIF secara histopatologi pada proses penyembuhan fraktur femur pada tikus. Penelitian ini melibatkan 30 tikus Sprague Dawley. Sampel dibagi menjadi 3 kelompok yakni fraktur (K), fraktur yang dilakukan ORIF (P1) dan fraktur yang dilakukan ORIF dengan penambahan ALS-R (P2). Setelah 28 hari tikus diterminasi dan diambil jaringan tulang femur yang diamati secara histopatologi dengan menggunakan skoring Salked. Penelitian ini menggunakan analisis non-parametrik Kruskal-Wallis dan post hoc
Mann-Whitney. Terdapat perbedaan yang bermakna secara statistik skor histopatologi
penyembuhan fraktur antara ketiga kelompok penelitian (p<0,05). Perbandingan rata-rata skor histopatologi pada kelompok P2 dan P1 menunjukkan tidak terdapat perbedaan yang signifikan (p>0,05), namun rata-rata skor histopatologi lebih tinggi pada kelompok P2 dibandingkan dengan kelompok P1. ALS-R memberikan pengaruh positif terhadap penyembuhan fraktur femur tikus putih
Sprague Dawley.
ABSTRACT
ROLE OF LYOPHILIZED RADIATION STERILIZED AMNIOTIC MEMBRANE TOWARD BONE HEALING OF FRACTURE FEMUR IN
OPEN REDUCTION INTERNAL FIXATION (ORIF) IN SPRAGUE DAWLEY RATS
By
Suci Widya Primadhani
Fracture treatment with Open Reduction Internal Fixation (ORIF) method has some weaknesses such as high risk infection, non union, implantation failed, and refracture. Lyophilized Radiation Sterilized Amnion Membrane (ALS-R) known that has some growth factors and cells scaffold which play role in fracture healing. This study aims to know the role of giving ALS-R in ORIF histopathologically in fracture femur healing process in rats.This study is involving 30 Sprague Dawley rats. Samples divided into three groups, whic is fracturized (K), fracturized and immobilized with ORIF (P1), and fracturized then immobilized with ORIF and given ALS-R (P2). After 28 days samples were terminated and took for its femur and analized histopathologically using Salked score. Data were analized with Kruskal-Wallis test and post hoc Mann-Whitney. This study results a statistically different histopathologic fracture healing between three groups (p<0,05). Comparison the means of P2 and P1 showed there was no significance difference, how ever the means of P2 is higher than P1. ALS-R has a positive impact toward fracture femur healing in Sprague Dawley rats.
PENGARUH AMNION LIOFILISASI STERIL-RADIASI (ALS-R) TERHADAP PENYEMBUHAN FRAKTUR FEMUR YANG DILAKUKAN OPEN REDUCTION INTERNAL FIXATION (ORIF)
PADA TIKUS PUTIH SPRAGUE DAWLEY
Oleh:
SUCI WIDYA PRIMADHANI
SKRIPSI
Sebagai Salah Satu Syarat untuk Mencapai Gelar SARJANA KEDOKTERAN
Pada
Program Studi Pendidikan Dokter Fakultas Kedokteran Universitas Lampung
FAKULTAS KEDOKTERAN UNIVERSITAS LAMPUNG
RIWAYAT HIDUP
Penulis dilahirkan di Bandung 18 Febuari 1994, sebagai anak kedua dari tiga
bersaudara, dari Bapak Yansari dan Ibu Erwina.
Pendidikan Taman Kanak-kanak (TK) diselesaikan di TK Cahaya, Bekasi pada
tahun 2000, Sekolah Dasar (SD) diselesaikan di SDS Angkasa IV, Jakarta pada
tahun 2006, Sekolah Menengah Pertama (SMP) di SMPN 109 Jakarta diselesaikan
pada tahun 2009, dan Sekolah Menengah Atas (SMA) di SMAN 71 Jakarta
diselesaikan pada tahun 2012.
Pada tahun 2012, penulis terdaftar sebagai mahasiswa pada Fakultas Kedokteran
Universitas Lampung (FK Unila) melalui jalur Seleksi Nasional Masuk Perguruan
Tinggi Negeri (SNMPTN) Tertulis. Selama menjadi mahasiswa penulis pernah
aktif menjadi Wakil Gubernur Badan Eksekutif Mahasiswa (BEM) Fakultas
Kedokteran Universitas Lampung periode 2014/2015 dan aktif dibeberapa
organisasi lainnya seperti PMPATD PAKIS Rescue Team dan Forum Studi Islam
SANWACANA
Alhamdulillah. Puji dan syukur penulis haturkan kehadirat Allah SWT yang atas
rahmat dan karunia serta ridho-Nya penulis dapat menyelesaikan serangkaian
proses penyusunan skripsi ini. Shalawat beserta salam semoga senantiasa
tercurahkan kepada Nabi Muhammad SAW, para keluarga dan sahabatnya hingga
akhir zaman.
Skripsi dengan judul ”Pengaruh Amnion Liofilisasi Steril-Radiasi (ALS-R)
terhadap Penyembuhan Fraktur Femur yang Dilakukan Open Reduction Internal
Fixation (ORIF) pada Tikus Putih Sprague Dawley” adalah salah satu syarat untuk
memperoleh gelar Sarjana Kedokteran di Fakultas Kedokteran Universitas
Lampung.
Dalam kesempatan ini penulis mengucapkan terima kasih kepada:
1. Prof. Dr. Ir. Hasriadi Mat Akin, M.P, selaku Rektor Universitas Lampung.
2. Dr. dr. Muhartono, M.Kes., Sp.PA selaku Dekan Fakultas Kedokteran
sekaligus sebagai pembahas atas saran dan masukan yang sangat konstruktif
3. Prof. Dr. dr. Efrida Warganegara, M.Kes, Sp. MK, selaku Guru Besar
Fakultas Kedokteran Universitas Lampung.
4. dr. Hanna Mutiara, M.Kes selaku pembimbing satu atas kesediaan waktu,
tenaga serta pikiran dalam memberikan bimbingan, motivasi, saran dan
pengarahan dalam penyusunan skripsi ini.
5. dr. Ahmad Fauzi, M. Epid., Sp.OT, selaku pembimbing dua atas kesediaan
waktu, tenaga, serta pikiran ditengah kesibukannya dalam memberikan
bimbingan, motivasi, saran dan pengarahan pada penyusunan skripsi ini.
Terima kasih penulis ucapkan telah mengajarkan banyak hal terkait
serangkaian proses penelitian ini.
6. dr. Indri Windarti, Sp.PA, atas dukungan motivasi, dana, tenaga dan pikiran
ditengah kesibukan beliau kepada penulis hingga penulis dapat
menyelesaikan penyusunan skripsi ini.
7. dr. Mukhlis Imanto, M.Kes., Sp.THT, selaku pembimbing akademik atas
kesediaan waktu, tenaga serta pikiran dalam memberikan bimbingan,
motivasi, saran dan pengarahan dalam penyusunan skripsi ini.
8. Bapak Ir. Basril Abbas, M.Si, atas kesediaan waktu, tenaga serta pikiran
yang telah membantu dalam pembuatan ALS-R dan Bapak Ir. Ismanto
Jumadi yang telah menjembatani penelitian ini dengan Badan Tenaga
Nuklir Nasional (BATAN). Terima kasih kepada segenap pihak BATAN
yang telah membantu.
9. Dokter dan Staff Pengajar, Staff Administrasi serta seluruh civitas
akademica Fakultas Kedokteran Universitas Lampung atas keramahan dan
tercinta, Ir. Erwina atas kiriman doa, kasih sayang, kesabaran, semangat,
motivasi dan nilai-nilai kehidupan yang berharga kepada penulis. Papa
tercinta Ir. Yansari, MM, yang juga tiada henti memberikan doa, kasih
sayang, dukungan finansial, arahan dan semangat juang kepada penulis.
Abang Muhammad Arief Akbar dan adik Nadya Nurmadina yang
merupakan anggota keluarga kecil ku yang berbahagia. Keluarga Besar
Nawawi Aziz, sepupuku yang tergabung dalam Big Five, terimakasih atas
doa, motivasi dan keceriaan yang telah diberikan selama ini.
11.Kepada pihak-pihak yang telah memberikan dukungan motivasi, tenaga,
waktu dan pikiran dalam menyelesaikan penyusunan skripsi ini. Dina
Ikrama Putri selaku mitraku dalam penelitian ini. Tim Help: Andika Yusuf
Ramadhan, Desti Nurul Qomariah, Ferina Nur Haqiqi, Fairuz Rabbaniyah,
Indriasari Nurul Putri, Radita Dewi Prasetyani, Alyssa Fairudz, Gheavani
Legowo, Restiko Maleo F, Fetiara Nurannisa, Idzni Mardhiyah, Farida
Hakim, Ratna Agustina, Airi Firdausia, Ade Marantika, Nico Aldrin, dan
kawan seperjuangan yang tidak dapat penulis sampaikan satu persatu.
Terima kasih tim help yang tak kenal lelah sepanjang hari hingga malam
menemani dan membantu dalam menyelesaikan penelitian ini, mulai dari
melakukan operasi frakturisasi, memberikan obat untuk tikus, hingga
terminasi tikus penelitian penulis. Kepada teman sekamar dalam mengelola
Airi, Nico, Fetiara, Ade dan Dyah Kartika. Terima kasih kepada Ferina Nur
Haqiqi atas kesediaan rumahnya menjadi sebagai rumah kedua ku.
12.Kepada Klub Belajar Babons: Aulia Rahma, Indriasari NP, Seffia Riandini,
Ratu Balqis Anasa, Silvia Marischa, Radita Dewi Prasetyani, Zahra Zettira,
Nani Indah dan Yvonne Yolanda, terima kasih atas segalanya yang telah
kita lalui bersama.
13. Kepada tetangga Kosan Lumbok Seminung, Aulia Kauri dan Astrid Wendi
atas dukungan, tempat bercerita, berkeluh kesah serta berbagi keceriaan
setiap harinya.
14.Kepada Keluarga FK UNILA 2012 terima kasih atas momen serta pelajaran
hidup yang berharga setelah 3,5 tahun mengenyam pendidikan di Fakultas
Kedokteran Universitas Lampung.
15.Kepada Keluarga Besar BEM FK Unila yang telah memberikan amanah,
pelajaran serta pengalaman berharga yang tidak dapat tergantikan oleh
apapun.
16.Kepada Keluarga Besar PMPATD PAKIS Rescue Team, FSI Ibnu Sina
serta Lunar FK Unila atas pelajaran dan pengalaman yang diberikan kepada
penulis.
17.Kepada Keluarga Besar Jokam Rajabasa (KEJORA) yang telah
mengingatkan untuk terus taat dalam menjalani ibadah dan mencari ridho
Allah SWT. Alhamdulillahi Jaza Kumullahu Khoiro.
18.Kepada guru-guru ku sedari TK hingga SMA. Guru SD ku Ibu Suharti yang
telah memberikan pecutan dikala kecil hingga aku dapat membuktikan
langsung.
20.Kepada kamu yang telah tertuliskan di Lauhul Mahfudz, yang
memotivasiku untuk menjadi pribadi yang lebih baik lagi.
Penulis berdoa semoga segala kebaikan dan keikhlasan segenap pihak yang telah
membantu mendapatkan balasan dari Allah SWT. Aamiin.
Akhirussalam, Wassalamualaikum Wr. Wb.
Bandar Lampung, Januari 2016
UNTUKMU KU PERSEMBAHKAN MAMA, PAPA, ABANG, ADIK DAN GURU-GURU KU
“BESERTA KESULITAN ITU ADA
KEMUDAHAN” QS: Al Insyirah 5
-6
“Keep moving forward”
DAFTAR TABEL
Tabel Halaman
Tabel 1. Derajat Fraktur Terbuka Menurut Gustillo ... 7
Tabel 2. Waktu dan Aktivitas Molekuler pada Penyembuhan Fraktur ... 23
Tabel 3. Definisi Operasional ... 30
Tabel 4. Skoring Salked pada Fraktur Healing yang Telah Dimodifikasi .. 36
Tabel 5. Analisis Skor Histopatologi Penyembuhan Tulang Femur pada Masing-Masing Kelompok ... 42
Tabel 6. Hasil Uji Normalitas Data pada Masing-Masing Kelompok ... 44
Tabel 7. Uji Non-Parametrik Kruskal-Wallis ... 45
vi
DAFTAR LAMPIRAN
Lampiran Halaman
Lampiran 1. Hasil Uji Statistik... 56
Lampiran 2. Dokumentasi Penelitian ... 60
Lampiran 3. Surat Keterangan Lolos Kaji Etik ... 64
DAFTAR GAMBAR
Gambar Halaman
Gambar 1. Variasi Fraktur ... 8
Gambar 2. Proses Penyembuhan Fraktur ... 11
Gambar 3. Potongan Longitudinal Proses Penyembuhan Fraktur ... 13
Gambar 4. Bagian External Callus pada Fraktur ... 13
Gambar 5. Pembentukkan Periosteum Tulang Baru ... 14
Gambar 6. Maturasi dari Permulaan Sintesis Periosteum Tulang Anyaman ... 15
Gambar 7. Gap Telah Terisi dengan Tulang Baru Setelah 6 Minggu ... 15
Gambar 8. Variasi Open Reduction Internal Fixation ... 18
Gambar 9. Kerangka Teori ... 26
Gambar 10. Kerangka Konsep ... 27
Gambar 11. Histopatologi Penyembuhan Fraktur Tulang Femur dengan Pewarnaan HE pada Kelompok Kontrol ... 41
Gambar 12. Histopatologi Penyembuhan Fraktur Tulang Femur dengan Pewarnaan HE pada Kelompok Perlakuan 1 ... 42
Gambar 13. Histopatologi Penyembuhan Fraktur Tulang Femur dengan Pewanraan HE pada Kelompok Perlakuan 2 ... 42
i
2.1.3.2 Penyembuhan dengan Penyatuan Langsung (direct union) ... 11
2.2 Penilaian Proses Penyembuhan Fraktur secara Histopatologi ... 12
2.3 Open Reduction Internal Fixation ... 15
2.4 Amnion Liofilisasi Steril Radiasi (ALS-R) ... 18
2.6 Kerangka Konsep ... 27
2.7 Hipotesis ... 27
III. METODE PENELITIAN 3.1 Desain Penelitian ... 29
3.2 Waktu dan Tempat ... 29
3.3 Identifikasi Variabel Penelitian dan Definisi Operasional 3.3.1 Variabel Bebas ... 29
3.3.2 Variabel Terikat ... 30
3.3.3 Definisi Operasional ... 30
3.4 Populasi dan Sampel Penelitian 3.4.1 Kriteria Inklusi ... 31
3.4.2 Kriteria Ekslusi ... 31
3.4.3 Besar Sampel ... 31
iii
3.9 Etika Penelitian ... 38
IV. HASIL DAN PEMBAHASAN 4.1 Hasil Penelitian ... 39
4.1.1 Gambaran Histopatologi Tulang Tikus ... 39
4.1.2 Analisis Gambaran Histopatologi Tulang Tikus ... 41
4.2 Pembahasan ... 46
4.3 Keterbatasan Penelitian ... 49
V. KESIMPULAN DAN SARAN 5.1 Kesimpulan ... 51
5.2 Saran ... 51
DAFTAR SINGKATAN
ALS-R : Amnion Liofilisasi Steril Radiasi
BATAN : Badan Tenaga Nuklir Nasional (BATAN)
bFGF : Fibroblast Growth Factor Basic
BMSC : Bone Marrow Mesenchymal Cell
BMP : Bone Morphogenetic Protein
BJRB : Bank Jaringan Riset Batan
DCPs : Dynamic Compression Plates
FGF : Fibroblast Growth Factor
GDF : Growth Differentiation Factor
HAAM : Human Acellular Amniotic Membranes
HAM : Human Amniotic Membranes
HE : Hematoksilin Eosin
IGF : Insuline-like Growth Factor
IGFBP : Insuline-like Growth Factor Binding Protein PDGF-AB
IL : Interleukin
K-wires : Kirschner wires
viii
MSC : Mesenchymal Stem Cell
M-SCF-R : Mesenchymal Stem Cell Factor-R
ORIF : Open Reduction Internal Fixation
PDGF : Platelet-Derived Growth Factor
TGF- 1 : Transforming Growth Factor- 1
TNF : Tumor Necrosis Factor
I. PENDAHULUAN
1.1 Latar Belakang
Fraktur adalah rusaknya kontinuitas struktur tulang, tulang rawan dan
lempeng pertumbuhan yang disebabkan oleh trauma maupun non trauma.
Kejadian fraktur dapat diakibatkan oleh kecelakaan, tekanan yang berulang,
atau kelemahan tulang yang abnormal (fraktur patologis) (Solomon et al.,
2010). Prinsip penanganan fraktur adalah mengembalikan posisi patahan
tulang ke posisi semula (reposisi) dan mempertahankan posisi itu selama
masa penyembuhan fraktur (Sjamsuhidajat & Jong, 2010).
Penatalaksanaan fraktur dapat dilakukan secara operatif dan non operatif.
Penatalaksanaan non‒operatif antara lain dengan cara proteksi tanpa
reposisi dan imobilisasi, imobilisasi luar tanpa reposisi (seperti
pembidaian), reposisi dengan cara manipulasi yang diikuti dengan
imobilisasi, dan reposisi dengan traksi terus menerus selama masa tertentu
pada beberapa minggu, lalu diikuti dengan imobilisasi (seperti pemasangan
gips). Penatalaksanaan operatif berupa reposisi yang diikuti dengan
2
diikuti dengan pemasangan fiksator tulang secara operatif dan reposisi
secara operatif diikuti dengan fiksasi interna (Sjamsuhidajat & Jong, 2010).
Penatalaksanaan fraktur dapat dilakukan dengan berbagai macam cara,
salah satunya dengan fiksasi internal atau dikenal juga Open Reduction
Internal Fixation (ORIF). Metode ORIF telah banyak digunakan. Pada
umumnya metode ini digunakan plate, screw dan kawat atau intramedullary
(IM) wire untuk menstabilkan tulang (Lakatos, 2014). Metode ini memiliki
kekurangan berupa risiko tinggi infeksi (Sjamsuhidajat & Jong, 2010).
Selain itu, komplikasi dari ORIF adalah non union, kegagalan implantasi
dan refraktur (Solomon et al., 2010). Oleh karena itu dibutuhkan metode
lain yang dapat meningkatkan kesembuhan fraktur, salah satunya dengan
penambahan Amnion Liofilisasi Steril Radiasi (ALS‒R) pada fraktur.
Amnion Liofilisasi Steril‒Radiasi merupakan suatu penemuan yang telah
dikembangkan oleh Badan Tenaga Nuklir Nasional (BATAN) yang
disimpan dalam Bank Jaringan Riset Batan (BJRB). Amnion diproses
dengan metode liofilisasi untuk dikeringkan dan dilakukan sterilisasi
dengan radiasi sinar sehingga dapat menghambat aktifitas
mikroorganisme. Metode ini juga dapat meminimalisasi kerusakan jaringan
(Suryani, 2013) sehingga tidak merusak senyawa organik seperti growth
factor yang terkandung dalam amnion. Growth factor diperlukan dalam
Penelitian Winanto et al. membuktikan bahwa implantasi dengan membran
amnion memberikan efek stimulasi yang positif terhadap penyembuhan
fraktur (Winanto et al., 2013). Oleh karena itu, peneliti tertarik untuk
mengetahui apakah dengan penambahan ALS‒R pada ORIF lebih baik
secara histopatologi pada proses penyembuhan fraktur femur pada tikus
Sprague Dawley.
1.2 Rumusan Masalah
Penanganan fraktur umumnya dengan dilakukan ORIF, namun ORIF
memiliki banyak kekurangan seperti rentan terjadi infeksi, kejadian non‒
union, kegagalan implantasi dan kejadian refraktur. Sehingga dibutuhkan
suatu metode untuk meningkatkan kesembuhan ORIF dengan penambahan
ALS‒R. Rumusan masalah pada penelitian ini adalah sebagai berikut:
1. Apakah terdapat pengaruh ORIF terhadap penyembuhan fraktur
femur pada tikus Sprague Dawley secara histopatologi?
2. Apakah terdapat pengaruh penambahan ALS-R pada ORIF
terhadap penyembuhan fraktur femur pada tikus Sprague Dawley
secara histopatologi?
3. Apakah terdapat pengaruh penambahan ALS-R pada ORIF
terhadap penyembuhan fraktur femur yang dilakukan ORIF pada
4
1.3 Tujuan Penelitian
Tujuan penelitian ini adalah :
1. Tujuan Umum
Untuk mengetahui pengaruh ALS-R terhadap kesembuhan fraktur
femur yang dilakukan ORIF pada tikus Sprague Dawley secara
histopatologi.
2. Tujuan Khusus
a. Mengetahui pengaruh ORIF terhadap penyembuhan fraktur
femur pada tikus Sprague Dawley secara histopatologi
b. Mengetahui pengaruh penambahan ALS-R pada ORIF terhadap
penyembuhan fraktur femur pada tikus Sprague Dawley secara
histopatologi
c. Mengetahui pengaruh penambahan ALS-R pada ORIF terhadap
penyembuhan fraktur femur yang dilakukan ORIF pada tikus
Sprague Dawley secara histopatologi
1.4 Manfaat Penelitian a. Bagi Penulis
Penelitian ini dapat menjawab pertanyaan penulis akan kegunaan ALS‒
R bagi kesembuhan fraktur.
b. Bagi Institusi Pendidikan
Penelitian ini dapat berkontribusi dalam pengembangan pengetahuan
c. Bagi Masyarakat
a) Penelitian ini dapat memberikan informasi mengenai manfaat ALS‒
R bagi kesembuhan fraktur.
b) Penelitian ini dapat sebagai acuan untuk mengaplikasikan ALS‒R
dalam penggunaan klinis.
c) Penelitian ini dapat menambah pengetahuan mengenai kegunaan
ALS‒R terhadap kesembuhan fraktur pada ORIF.
d. Bagi Peneliti Lain
Penelitian ini dapat digunakan sebagai tambahan sumber referensi untuk
II. TINJAUAN PUSTAKA
2.1 Fraktur
2.1.1 Definisi dan Klasifikasi Fraktur
Fraktur adalah rusaknya kontinuitas dari struktur tulang, tulang rawan dan
lempeng pertumbuhan yang disebabkan oleh trauma dan non trauma. Tidak
hanya keretakan atau terpisahnya korteks, kejadian fraktur lebih sering
mengakibatkan kerusakan yang komplit dan fragmen tulang terpisah. Tulang
relatif rapuh, namun memiliki kekuatan dan kelenturan untuk menahan
tekanan. Fraktur dapat diakibatkan oleh cedera, stres yang berulang,
kelemahan tulang yang abnormal atau disebut juga fraktur patologis
(Solomon et al., 2010).
2.1.2 Klasifikasi Fraktur
Secara klinis, fraktur dibagi menurut ada tidaknya hubungan patahan tulang
dengan dunia luar, yaitu fraktur terbuka dan fraktur tertutup. Fraktur tulang
terbuka dibagi menjadi tiga derajat yang ditentukan oleh berat ringannya luka
Tabel 1. Derajat fraktur terbuka menurut Gustillo
Derajat Luka Fraktur
I Laserasi <1 cm kerusakan
jaringan tidak berarti relatif bersih
II Laserasi >1cm tidak ada
kerusakan jaringan yang hebat atau avulsi, ada kontaminasi
III Luka lebar dan rusak hebat
atau hilangnya jaringan disekitarnya. Kontaminasi hebat
(Sumber: Sjamsuhidajat & Jong, 2010)
Sederhana, dislokasi
Fraktur sangat bervariasi dari segi klinis, namun untuk alasan praktis, fraktur
dibagi menjadi beberapa kelompok, yaitu :
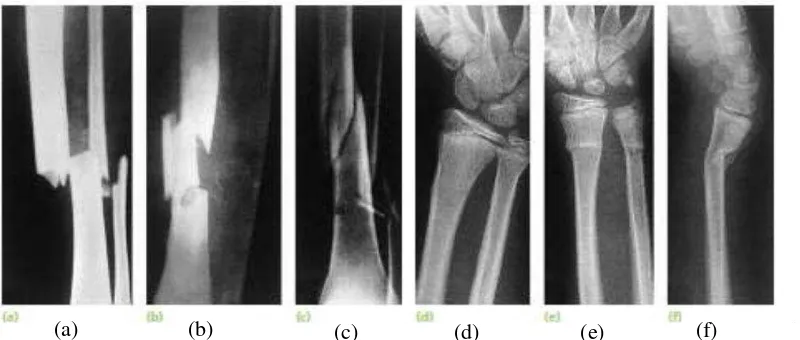
a. Complete fractures
Tulang terbagi menjadi dua atau lebih fragmen. Patahan fraktur yang
dilihat secara radiologi dapat membantu untuk memprediksi tindakan
yang harus dilakukan setelah melakukan reduksi. Pada fraktur
transversal (gambar 1a), fragmen tetap pada tempatnya setelah reduksi,
sedangkan pada oblik atau spiral (gambar 1c) lebih cenderung
memendek dan terjadi pergeseran meskipun tulang telah dibidai. Fraktur
segmental (gambar 1b) membagi tulang menjadi 3 bagian. Pada fraktur
impaksi fragmen menumpuk saling tumpang tindih dan garis fraktur
tidak jelas. Pada raktur kominutif terdapat lebih dari dua fragmen,
karena kurang menyatunya permukaan fraktur yang membuat tidak
8
b. Incomplete fractures
Pada fraktur ini, tulang tidak terbagi seutuhnya dan terdapat kontinuitas
periosteum. Pada fraktur buckle, bagian yang mengalami fraktur
hampir tidak terlihat (gambar 1d). Pada fraktur greenstick (gambar 1e
dan 1f), tulang melengkung atau bengkok seperti ranting yang retak.
Hal ini dapat terlihat pada anak‒anak, yang tulangnya lebih elastis
daripada orang dewasa. Pada fraktur kompresi terlihat tulang spongiosa
tertekan kedalam (Solomon et al., 2010).
(a) (b) (c) (d) (e) (f)
Gambar 1. Variasi fraktur. Keterangan : Complete fractures: (a) transversal; (b) segmental; (c) spiral. Incomplete fractures: (d) fraktur buckle; (e, f) fraktur greenstick (Solomon et al., 2010).
2.1.3 Proses Penyembuhan Fraktur
Penyembuhan fraktur umumnya dilakukan dengan cara imobilisasi. Akan
tetapi, penyembuhan fraktur alamiah dengan kalus dan pembentukan kalus
berespon terhadap pergerakan bukan terhadap pembidaian. Pada umumnya
fraktur dilakukan pembidaian hal ini dilakukan tidak untuk menjamin
tulang pada posisi yang benar dan mempercepat pergerakan tubuh dan
pengembalian fungsi (Solomon et al., 2010).
Fraktur disembuhkan dengan proses perkembangan yang melibatkan
pembentukan fibrokartilago dan aktivitas osteogenik dari sel tulang utama.
Fraktur merusak pembuluh darah yang menyebabkan sel tulang terdekat mati.
Pembekuan darah dibuang bersamaan dengan debris jaringan oleh makrofag
dan matriks yang rusak, tulang yang bebas dari sel di resorpsi oleh osteoklas
(Mescher, 2013).
2.1.3.1 Penyembuhan dengan kalus
Proses ini adalah bentuk alamiah dari penyembuhan fraktur pada tulang
tubular tanpa fiksasi, proses ini terdiri dari lima fase, yaitu (Solomon et
al., 2010) :
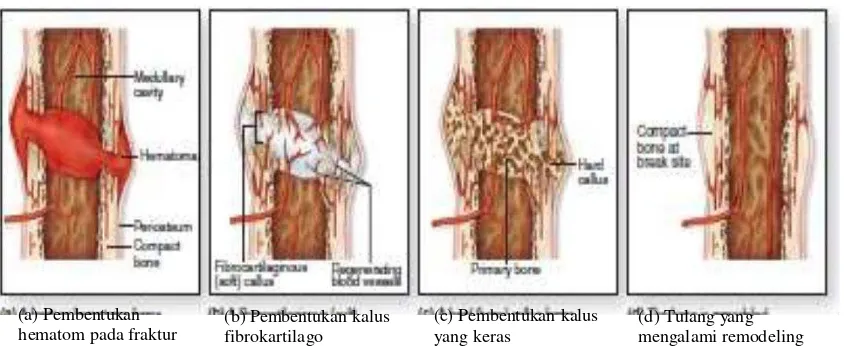
1. Destruksi jaringan dan pembentukan hematom
Pembuluh darah robek dan terjadi pembentukan hematom disekitar
fraktur. Tulang pada permukaan yang patah, kehilangan asupan darah,
dan mati (gambar 2a).
2. Inflamasi dan proliferasi selular
Dalam 8 jam, fraktur mengalami reaksi inflamasi akut dengan migrasi
sel inflamatorik dan inisiasi proliferasi dan diferensiasi dari stem sel
10
Sejumlah besar mediator inflamasi seperti sitokin dan beberapa faktor
pertumbuhan dilibatkan. Selanjutnya bekuan darah hematom diabsorbsi
perlahan dan membentuk kapiler baru pada area tersebut.
3. Pembentukan kalus
Diferensiasi stem sel menyediakan sejumlah sel kondrogenik dan
osteogenik. Pada kondisi yang tepat mereka akan mulai membentuk
tulang dan pada beberapa kasus, juga membentuk kartilago (gambar
2b). Di sejumlah sel ini terdapat osteoklas yang siap membersihkan
tulang yang mati. Massa seluler yang tebal bersama pulau‒pulau tulang
imatur dan kartilago, membentuk kalus atau rangka pada permukaan
periosteum dan endosteum. Saat anyaman tulang yang imatur
termineralisasi menjadi lebih keras (gambar 2c), pergerakan pada lokasi
fraktur menurunkan progresivitas dan fraktur menyatu dalam 4 minggu
setelah cidera.
4. Konsolidasi
Tulang anyaman terbentuk menjadi tulang lamelar dengan aktivitas
osteoklas dan osteoblas yang kontinyu. Osteoklas pada proses ini
melakukan pelubangan melalui debris pada garis fraktur, dan menutup
kembali jaringan tersebut. Osteoblas mengisi ruang yang tersisa antara
fragmen dan tulang baru. Proses ini berjalan lambat sebelum tulang
5. Remodeling
Fraktur telah dijembatani dengan lapisan tulang yang solid. Pada
beberapa bulan atau bahkan tahun, dilakukan pembentukkan ulang atau
reshaped dengan proses yang kontinu dari resorpsi dan pembentukan
tulang (gambar 2d).
Gambar 2. Proses penyembuhan fraktur (Mescher, 2013).
2.1.3.2 Penyembuhan dengan penyatuan langsung (direct union)
Proses penyatuan langsung tidak lagi melibatkan proses pembentukan
kalus. Jika lokasi fraktur benar‒benar dilakukan imobilisasi dengan
menggunakan plate, tidak dapat memicu kalus. Namun, pembentukan
tulang baru dengan osteoblas timbul secara langsung diantara fragmen.
Gap antar permukaan fraktur diselubungi oleh kapiler baru dan sel
osteoprogenitor tumbuh dimulai dari pangkal dan tulang baru terdapat
pada permukaan luar (gap healing). Saat celah atau gap sangat kecil,
12
tama akan diisi dengan tulang anyaman, yang selanjutnya dilakukan
remodeling untuk menjadi tulang lamelar. Setelah 3‒4 minggu, fraktur
sudah cukup kuat untuk melakukan penetrasi dan bridging mungkin
kadang ditemukan tanpa adanya fase pertengahan atau contact healing
(Solomon et al., 2010).
Penyembuhan dengan kalus, meskipun tidak langsung (indirect) memiliki
keuntungan antara lain dapat menjamin kekuatan tulang di akhir penyembuhan
tulang, dengan peningkatan stres kalus berkembang lebih kuat sebagai contoh
dari hukum Wolff. Dengan penggunaan fiksasi metal, disisi lain, tidak
terdapatnya kalus berarti tulang akan bergantung pada implan metal dalam
jangka waktu yang cukup lama. Karena, implan akan mengurangi stress, yang
mungkin dapat menyebabkan osteoporotik dan tidak sembuh total sampai
implan dilepas (Solomon et al., 2010).
2.2 Penilaian Proses Penyembuhan Fraktur secara Histopatologi
Proses perbaikan tulang dimulai dari korteks perifer beberapa sentimeter dari
lokasi fraktur. Meskipun terdapat perubahan pada perbaikan lingkungan dan
jaringan hipoksia akibat dari kerusakan suplai darah, hal ini mengawali
pembentukan oleh lapisan dalam periosteum dan sel mesenkimal yang belum
berdiferensiasi dari massa kartilago baik di luar korteks disebut external callus
Kalus diawali dengan kartilago dan fibrokartilago untuk menstabilisasi lokasi
fraktur. Kemudian melalui peran vaskuler, kalus bertambah dari lapisan korteks
paling jauh dari lokasi fraktur dan dari periosteum yang terletak pada batas luar
external callus. Terlihat fase awal pembentukkan tulang endokondral, terdapat
external dan internal callus (gambar 3).
E
I
Gambar 3. Potongan longitudinal proses penyembuhan fraktur mid diafisis os femur (Shapiro, 2008). Keterangan : E : external callus, I : internal callus
External callus (gambar 4), terlihat jaringan fibrosa pada bagian atas dan awal
perbaikan kartilago pada bagian bawah gambar. Secara keseluruhan external
callus yang baru terbentuk ini dikatakan terdapat jaringan fibrokartilago.
14
Setelah satu minggu terlihat pembentukkan periosteum tulang baru pada
sebelah kanan dari korteks dan pembentukkan kartilago pada sebelah kiri
korteks yang lebih mobile dan kurang stabil pada lokasi fraktur (gambar 5).
Dengan cara seperti ini tulang anyaman disintesis pada kartilago yang
terkalsifikasi dari kalus hingga perbaikan kartilago telah diubah dengan
sempurna oleh tulang melalui mekanisme endokondral (Shapiro, 2008).
Gambar 5. Pembentukkan periosteum tulang baru (Shapiro, 2008).
Proses selanjutnya adalah dengan melibatkan transformasi tulang anyaman
menjadi tulang kompak. Proses ini melalui resorbsi external callus yang tidak
lagi dibutuhkan sejak ujung patahan tulang telah mengalami bridging dan stabil
dengan pemulihan jaringan dan remodeling korteks tulang Havers. Pada fase
ini, external callus yang digambarkan secara mikroskopis terdapat tulang
anyaman yang telah dilapisi dengan proses sintesis tulang lamelar. Tulang
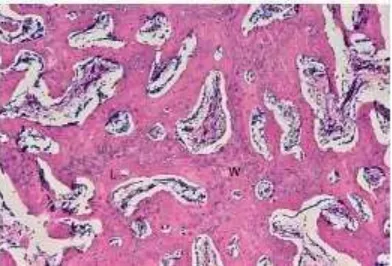
Gambar 6. Tulang anyaman (W) dan tulang lamelar (L) (Shapiro, 2008)
Setelah 6 minggu gap telah terisi dengan tulang baru. Terlihat (gambar 7) tulang
anyaman berwarna ungu gelap, dikelilingi dengan tulang lamelar berwarna
ungu terang dan osteoblas yang mengisi rongga kosong. Jaringan ini disebut
juga woven bone atau tulang anyaman (Shapiro, 2008)
Gambar 7. Tulang anyaman (ungu gelap), tulang lamelar (ungu terang) dan osteoblas (Shapiro, 2008).
2.3 Open Reduction Internal Fixation (ORIF)
Meskipun konsep teknik internal fiksasi telah dikemukakan pada pertengahan
16
Penggunaan plate, screw dan kawat pertama kali dilakukan pada tahun 1880
dan 1890. Awal mula dilakukan pembedahan fiksasi internal mengalami
berbagai macam rintangan seperti infeksi, sedikit pengetahuan tentang implant
dan tekniknya, metal allergic dan keterbatasan pengetahuan tentang proses
penyembuhan fraktur secara biologis. Pada tahun 1950, Dannis dan Muller
menetapkan prinsip dan teknik fiksasi internal. Setelah 40 tahun kemudian,
kemajuan ilmu biologi dan mekanikal saat ini telah mempermudah teori dan
teknik fiksasi (Lakatos, 2014).
ORIF merupakan reposisi secara operatif yang diikuti dengan fiksasi interna.
Fiksasi interna yang dipakai biasanya berupa plate and screw. Keuntungan
ORIF adalah tercapainya reposisi yang sempurna dan fiksasi yang kokoh
sehingga pascaoperasi tidak perlu lagi dipasang gips dan mobilisasi segera bisa
dilakukan. Kerugiannya adalah adanya risiko infeksi tulang (Sjamsuhidajat &
Jong, 2010). Indikasi tindakan ORIF pada fraktur femur bagian distal antara
lain fraktur terbuka, fraktur yang dihubungkan dengan neurovascular
compromise, seluruh displaced fractures, fraktur ipsilateral ekstrimitas bawah,
irreducible fractures, dan fraktur patologis (Thomson & Jonna, 2014).
Prinsip umum dari fiksasi interna antara lain dengan menggunakan pin and
wire, plate and screw, tension‒band principle, intramedullary nails dan
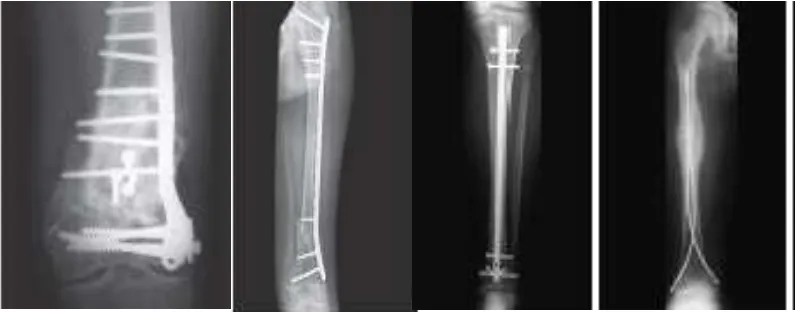
biodegradable fixation (gambar 8). Pin and wires menggunakan metode
Kirschner wires (K‒wires) dan Steinmann pins memiliki beberapa kegunaan,
Metode ini juga memberikan fiksasi sementara untuk rekonstruksi dari fraktur
yang melibatkan kerusakan tulang dan soft tissue yang minimal (Lakatos,
2014).
Bone screw adalah bagian dasar dari metode fiksasi interna modern dan dapat
digunakan baik secara independen atau dengan kombinasi dengan tipe
implantasi lain. Kekuatan dipengaruhi oleh pemasangan pengencangan screw.
Seiring berjalannya waktu, sejumlah kekuatan kompresif menurun secara
lambat saat tulang mengalami remodeling terhadap tekanan. Namun, waktu
penyembuhan fraktur biasanya lebih singkat dibandingkan waktu yang
dibutuhkan dari substansi yang hilang akibat kompresi dan fiksasi (Lakatos,
2014). Metode lain dengan menggunakan plate memiliki berbagai macam
ukuran dan bentuk untuk tulang dan lokasi yang berbeda. Dynamic
compression plates (DCPs) tersedia dalam ukuran 3,5 mm dan 4,5 mm. Lubang
screw pada DCP membentuk sudut kemiringan pada satu sisi berlawanan dari
bagian tengah plate (Lakatos, 2014).
Pada tahun 1930 an, Küntscher memperbaiki nailing technique, sehingga
intramedullary (IM) nails menjadi teknik fiksasi standar untuk tulang femur.
IM nails memiliki keuntungan dari plate dan fiksasi eksternal karena lokasi
intramedular memungkinkan penjajaran sumbu aksis dan pengurangan beban.
Implantasi IM nails memberikan fiksasi yang stabil, akan tetapi penyembuhan
berlangsung secara primer melalui pembentukan dari kalus periosteum
18
Gambar 8. Variasi ORIF (Solomon et al., 2010)
2.4 Amnion Liofilisasi Steril Radiasi (ALS‒R)
Amnion liofilisasi steril radiasi (ALS‒R) adalah amnion yang dikeringkan
dengan cara liofilisasi kemudian dilakukan sterilisasi dengan mengggunakan
radiasi sinar γ. Proses pengeringan amnion di Bank Jaringan Riset Batan
dilakukan dengan dua metode yaitu dengan liofilisasi dan suhu ruangan (air
dried), liofilisasi adalah penghilangan air melalui sublimasi yakni perubahan
wujud padat (es) langsung menjadi wujud gas (uap) sehingga menghambat
aktifitas mikroorganisme dan enzim secara normal dapat mendegradasi
senyawa di dalam bahan biologi. Sehingga pengeringan dengan cara ini dapat
mengurangi kerusakan jaringan secara minimal (Suryani, 2013).
Proses pengawetan jaringan agar jaringan biologi dapat disimpan dalam waktu
lama, BJRB melakukan beberapa cara proses pengawetan, antara lain (Abbas,
2010) :
Liofilisasi, yaitu suatu proses pengeringan dari bahan biologi
tanpa melalui fase cair. Dengan cara ini tidak mengalami perubahan
kimia dan fisika.
Pembekuan pada suhu ‒80°C, dilakukan untuk menjaga keamanan
dari jaringan alograf agar tetap awet sebelum diproses. Disamping
itu juga digunakan untuk menyimpan jaringan autograf untuk
dipakai kembali oleh pasien yang sama di kemudian hari.
Penyimpanan jaringan pada suhu ‒80°C dapat digunakan sebelum 5
tahun.
Sterilisasi Radiasi, untuk menjaga keamanan dari jaringan biologi,
jaringan disterilkan dengan cara radiasi dengan sinar γ atau partikel
elektron. Sterilisasi radiasi sangat cocok untuk jaringan biologi,
karena prosesnya dingin sehingga tidak mengubah struktur jaringan,
tidak meninggalkan residu beracun, sangat ampuh membunuh
mikroorganisme dan juga virus sampai batas tertentu, sehingga
aman digunakan untuk implantasi pada manusia.
Jaringan yang telah diproses dengan cara liofilisasi hingga kadar air 5‒7%,
dikemas dalam kantung plastik poli etilen, dan diiradiasi dengan dosis 25kGγ.
Jaringan tersebut dapat disimpan pada suhu 4‒10°C dan terhindar dari cahaya
matahari langsung. Cara penyimpanan ini direkomendasikan hanya untuk 2‒5
tahun, tergantung dari jenis jaringannya. Untuk menjaga kualitas dan sterilitas
jaringan, kemasan yang rusak atau terbuka akibat pemakaian (jaringan sisa)
20
Proses liofilisasi tetap menjaga morfologi membran amnion seperti struktur
epitel yang terlihat kuboid selapis, beberapa lapisan stratifikasi dan stroma
edematosa yang diamati secara makroskopis. Perwarnaan dengan PAS
mengindikasikan terdapat membran dasar yang terlihat seperti pembatas
dibawah stroma pada membran amnion terliofilisasi (Rodriguez et al., 2009).
Kolagen IV terlihat pada membran amnion terliofilisasi membentuk selapis tipis
yang memmanjang pada membran dasar yang ditunjukkan secara
imunohistokimia.
Selain kandungan kolagen, membran amnion terliofilisasi tetap menjaga
kandungan growth factor yang berperan dalam bone healing antara lain
transforming growth factor‒ 1 (TGF‒ 1), fibroblast growth factor basic
(bFGF) (Rodriguez et al., 2009). Penelitian Grzywocz et al. (2014),
menunjukkan beberapa growth factor dari membran sel amnion manusia,
seperti FGF‒6, VEGF‒R3, M‒SCF‒R, IGFBP‒4, IGFBP‒6 dan PDGF‒AB
(Grzywocz et al., 2014). Membran sel amnion mengekspresikan bone
morphogenetic protein (BMP)‒2 dan ‒4 dan juga kolagen tipe 2 yang memiliki
potensi terapeutik sebagai terapi dari kerusakan atau penyakit kartilago (Toda
et al., 2007).
Growth factor adalah protein yang disekresikan oleh sel yang aktif pada sel
target atau sel yang memiliki aksi yang spesifik. Growth factor memiliki
mempercepat penyembuhan tulang, tatalaksana kejadian nonunion, dan juga
sebagai salah satu elemen dari strategi tissue‒engineering yang komprehensif
yang termasuk dalam terapi gen untuk tatalaksana permasalahan bone loss
dalam jumlah besar (Lieberman et al., 2002).
Transforming growth factor‒beta (TGF‒ ) memiliki super family yang
termasuk kedalamnya adalah bone morphogenetic protein (BMPs), growth
differentiation factor (GDF), activins, inhibins dan Mullerian inhibiting
substance. Pada proses penyembuhan fraktur, TGF‒ berperan sebagai
mitogenik dan kemotaktik poten bagi sel pembentuk tulang, faktor kemotaktik
bagi makrofag. Sedangkan BMPs berperan dalam diferensiasi pada
undifferentiated mesenchymal cell menjadi kondrosit dan osteoblas, dan
osteoprogenitor menjadi osteoblas (Dimitriou et al., 2005).
Selain TGF‒ dan BMPs, growth factor lain yang terkandung dalam ALS‒R
adalah fibroblast growth factor (FGFs) berperan dalam angiogenetik dan
mitogenik pada sel mesenkimal dan epitel, osteoblas dan kondrosit. α‒FGF
memiliki efek terhadap proliferasi kondrosit, ‒FGF (lebih poten)
mempengaruhi maturasi kondrosit dan resorpsi tulang. Insulin‒like growth
factor‒I (IGF‒I) berperan dalam proliferasi dan melibatkan sel mesenkimal dan
osteoprogenitor yang diekspresikan pada penyembuhan fraktur. IGF‒I
mempromosikan pembentukkan matriks tulang (kolagen tipe‒1 dan matriks
protein non‒kolagen) oleh osteoblas yang telah berdiferensiasi. Sedangkan
22
menstimulasi produksi kolagen tipe‒1, matriks kartilago dan proliferasi seluler.
Platelet‒derived growth factor (PDGF) memiliki peran yang sama seperti
TGF‒ dalam mitogenik bagi sel mesenkimal dan osteoblas, kemotaktik bagi
sel inflamatorik dan mesenkimal (Dimitriou et al., 2005).
Vascular endothelial growth factor (VEGF) diproduksi oleh sel endotel,
makrofag, fibroblas, sel otot polos, osteoblas dan kondrosit hipertrofik. VEGF
berperan dalam angiogenesis pada proses penyembuhan fraktur. Selain itu
secara tidak langsung VEGF menginduksi proliferasi dan diferensiasi dari sel
prekursor osteoblas. Hal ini dihasilkan dari sekresi faktor osteoanabolik seperti
endotelin‒I dan IGF‒I oleh sel endotel yang distimulasi VEGF (Beamer et al.,
2009).
Baik secara seluler, atau aseluler membran amnion memiliki fungsi dalam
penyembuhan fraktur. Penelitian menunjukkan human acellular amniotic
membran (HAAM) dapat memuat bone marrow mesechymal stem cell
(BMSCs) yang dapat memperbaiki jaringan kartilago sendi pada kelinci
percobaan pada lingkungan in vitro. Komponen utama dari tissue‒engineered
kartilago adalah seed cell, scaffold, dan growth factors. Seed cells adalah
elemen dasar dari perbaikan jaringan dan menjadi kandungan utama dalam
perbaikan defek kartilago. Sebagai sel pemicu (cell scaffold), human amniotic
membranes (HAM) memiliki komposisi sel yang mempromosikan proliferasi
dan diferensiasi dengan lebih banyak substansi adhesi (seperti kolagen dan
Growth factor memiliki peran dalam aktivitas molekuler masing‒masing
berdasarkan waktu dan proses penyembuhan seperti yang dijelaskan pada tabel
2.
Tabel 2. Waktu dan aktivitas molekuler pada penyembuhan fraktur
Hari Proses Aktivitas molekuler
Hari ke‒1 Pembentukan hematom, inflamasi
Perekrutan sel mesenkimal Diferensiasi osteogenik MSCs dari sumsum tulang
Sitokin: IL‒1, IL‒6, TNF‒
α
PDGF, TGF‒ BMP‒2
Hari ke‒3 Proliferasi MSCs dimulai Proliferasi dan diferensiasi dari preosteoblast dan osteoblas di lokasi oleh osifikasi intramembranosa
Proses angiogenesis dimulai Hari ke‒7 Puncak proliferasi sel pada
osifikasi intramembranosa antara hari ke‒7 dan 10
Kondrogenesis dan osifikasi endokondral dimulai (maturasi kondrosit hari ke 9‒14)
Hari ke‒14 Penghentian proliferasi sel
pada osifikasi
intramembranosa, namun aktivitas osteoblas tetap berlangsung
Mineralisasi soft callus, resorpsi kartilago dan pembentukkan tulang anyaman Neo‒angiogenesis yang diinfiltrasi bersamaan dengan sel mesenkimal
Penurunan ekspresi TGF‒ 2, GDF‒5 dan mungkin GDF‒1
Ekspresi dari BMP‒3, ‒4,
‒7 dan ‒8
Ekspresi dari VEGFs
24
Winanto et al., telah melakukan penelitian pada tikus Sprague Dawley yang
mengalami fraktur femur yang diberikan ALS‒R dan xenograf. Hasil yang
didapatkan meliputi ALS‒R memiliki skor radiologi yang sama dibandingkan
dengan kelompok kontrol, namun secara skor histopatologi lebih baik daripada
kelompok kontrol. Xenograf memiliki hasil yang sama dengan kelompok
kontrol baik secara radiologi maupun histopatologi. Kombinasi antara
pemberian membran amnion dengan xenograf lebih baik secara histopatologi
dibandingkan kelompok kontrol, dengan hasil yang sama pada skor radiologi
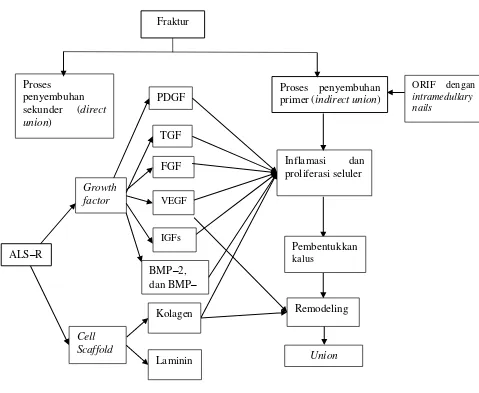
2.5 Kerangka Teori
Penyembuhan fraktur dibagi menjadi direct union dan indirect union.
Penanganan operatif pada fraktur dilakukan ORIF dengan menggunakan
intramedullary nails akan melibatkan proses penyembuhan indirect union.
Terdapat beberapa tahapan proses penyembuhan fraktur indirect union seperti
inflamasi dan proliferasi seluler, pembentukan kalus, dan remodeling (Solomon
et al., 2010). Dengan penambahan ALS‒R yang mengandung beberapa growth
factor seperti PDGF, TGF, FGF, VEGF, IGFs, BMP‒2, BMP‒4 dan cell
scaffold seperti kolagen dan laminin diharapkan dapat mempercepat penyatuan
tulang atau union. Pengaruh growth factor dan cell scaffold tersaji pada gambar
26
primer (indirect union)
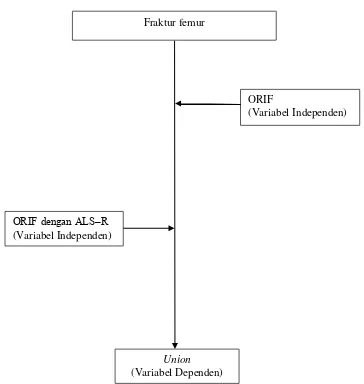
2.6Kerangka Konsep
Gambar 10. Kerangka konsep perbandingan penyembuhan fraktur femur yang dilakukan ORIF dan ALS‒R dengan tanpa ALS‒R
2.7Hipotesa Penelitian
Hipotesis penelitian ini adalah sebagai berikut:
a. Terdapat pengaruh ORIF terhadap penyembuhan fraktur femur
pada tikus Sprague Dawley secara histopatologi
b. Terdapat pengaruh penambahan ALS-R pada ORIF terhadap
penyembuhan fraktur femur pada tikus Sprague Dawley secara
histopatologi
ORIF dengan ALS‒R
(Variabel Independen)
Fraktur femur
ORIF
(Variabel Independen)
Union
28
c. Terdapat pengaruh penambahan ALS-R pada ORIF terhadap
penyembuhan fraktur femur yang dilakukan ORIF pada tikus
III. METODE PENELITIAN
3.1 Desain Penelitian
Jenis penelitian ini adalah penelitian eksperimental menggunakan post test only
control group design yang menggunakan evaluasi secara histopatologi.
Penelitian ini menggunakan penilaian histopatologi Salked score (Winanto et
al., 2013).
3.2 Waktu dan Tempat Penelitian
Penelitian ini dilakukan pada bulan Oktober‒Desember 2015 dengan tempat
penelitian di animal house Fakultas Kedokteran Universitas Lampung.
Pembuatan dan pengawetan bahan jaringan ALS‒R dilakukan oleh Bank
Jaringan Riset Batan (BJRB), Pasar Jumat, Jakarta. Pembuatan dan pengamatan
preparat secara mikroskopis dilakukan di Laboratorium Patologi Anatomi
Fakultas Kedokteran Universitas Lampung.
3.3 Identifikasi Variabel Penelitian dan Definisi Operasional 3.3.1 Variabel Bebas
30
3.3.2 Variabel Terikat
Variabel terikat pada penelitian ini adalah penyatuan (union) fraktur femur
tikus Sprague Dawley
3.3.3 Definisi Operasional
Definisi operasional pada penelitian ini terdiri dari fraktur femur, ALS‒R,
ORIF, penilaian histopatologi seperti yang dijelaskan pada tabel 3.
Tabel 3. Definisi operasional
No Variabel Definisi Operasional Alat Ukur Hasil Ukur Skala Ukur
Tidak ada Tidak ada Kategorik
Tidak ada Tidak ada Kategorik
Tidak ada Tidak ada Kategorik
3.4 Populasi dan Sampel Penelitian
Populasi penelitian ini adalah tikus putih jantan (Rattus novergicus) galur
Sprague Dawley yang telah dewasa berumur 2‒3 bulan, berat badan 200‒300
gram yang diperoleh dari Laboratorium Hewan Coba Pusat Biomedis dan
Teknologi Dasar Kesehatan, Badan Litbangkes.
3.4.1 Kriteria Inklusi a Tikus jantan
b Sehat
c Berumur 2‒3 bulan
d Berat badan 200‒300 gram
3.4.2 Kriteria Eksklusi a Mati
b Tampak sakit (gerakan tidak aktif, tidak mau makan, rambut kusam atau
rontok)
3.4.3 Besar Sampel
Sampel penelitian sebanyak 30 ekor dipilih secara acak dan dibagi ke dalam
3 kelompok perlakuan sesuai dengan rumus Frederer. Rumus Federer yaitu :
(t − 1)(n − 1) > 15
Dengan t adalah jumlah kelompok perlakuan dan n adalah besar sampel tiap
kelompok, sehingga didapatkan jumlah sampel dengan rumus Frederer
32
(3‒1) (n‒1) > 15
2n ‒2 > 15
n > 8,5
sampel yang digunakan tiap kelompok percobaan sebanyak 9 ekor (n>8,5)
dan jumlah kelompok yang akan digunakan adalah 3 kelompok. Penambahan
sampel untuk mencegah drop out sebesar 10%. Sehingga penelitian ini akan
menggunakan 30 ekor tikus Sprague Dawley dari populasi yang ada.
Pada penelitian ini sampel dibagi dalam tiga kelompok, yakni kelompok K,
P1, dan P2. Pada kelompok kontrol (K) tikus akan diberikan pakan standar
dan dibuat fraktur tanpa perlakuan khusus. Pada kelompok kedua (P1) tikus
diberikan pakan standar, dibuat fraktur dan diberikan perlakuan khusus
dengan dilakukan ORIF tanpa ALS‒R. Pada kelompok ketiga (P2) tikus
diberikan pakan standar, dibuat fraktur dan diberikan perlakuan khusus
dengan dilakukan ORIF dengan ALS‒R.
3.5 Alat dan Bahan Penelitian 3.5.1 Alat Penelitian
Alat yang digunakan dalam penelitian ini adalah :
a. Kandang hewan
b. Tempat pakan hewan
c. Tempat minum hewan
e. Handscoen
f. Spuit
g. Gergaji kecil (small saw)
h. Alat bedah minor
i. Mikroskop
j. Object glass
3.5.2 Bahan Penelitian
Bahan yang digunakan dalam penelitian ini adalah
a. Hewan coba berupa tikus Sprague Dawley dengan berat badan 200‒300
g, berumur 2‒3 bulan. Hewan coba diberi pakan standar dan minum
secara ad libitum
b. Bahan Perlakuan
i. ORIF
ii. ALS‒R
c. Bahan untuk tindakan anasthesia berupa :
i. Ketamine 75 mg/kgBB
ii. Xylaxine 5 mg/kgBB
d. Bahan pembuatan preparat
i. Formalin 10%
ii. Paraffin block
34
3.6 Prosedur Penelitian 3.6.1 Persiapan
Persiapan sebelum penelitian dilakukan pemilihan sampel tikus Sprague
Dawley yang didapatkan dari Laboratorium Hewan Coba Pusat Biomedis
dan Teknologi Dasar Kesehatan, Badan Litbangkes. Pembuatan ALS‒R
dilakukan di Bank Jaringan Riset Batan (BRJB), Pasar Jumat, Jakarta.
3.6.2 Adaptasi Tikus
Adaptasi tikus dilakukan bertujuan untuk memgurangi stres dan kematian.
Tikus sebanyak 30 ekor dibagi kedalam 3 kandang dan diadaptasi selama
3 hari sebelum perlakuan dimulai di animal house Fakultas Kedokteran
Universitas Lampung. Selama masa adaptasi tikus diberi makan berupa
pelet dan air secara ad libitum.
3.6.3 Prosedur Frakturisasi
Mengacu pada penelitian sebelumnya, proses frakturisasi tikus dengan
menggunakan gergaji kecil (small saw). Tikus di anastesi subkutan
dengan ketamin 75 mg/kgBB dan xylazine 5 mg/kgBB. Selanjutnya
dilakukan fraktur transversal pada mid diafisis os femur hingga
menunjukkan garis patahan pada periosteum.
3.6.4 Pembedahan
Setelah dilakukan frakturisasi, dilakukan fiksasi interna dengan
dengan implantasi pada bagian fraktur femur dengan ukuran 15x5 mm.
Pembedahan ini dilakukan dengan alat bedah minor steril.
3.6.5 Perawatan Pasca Pembedahan
Tikus diberikan gentamicin salep setelah pembedahan untuk
meminimalisir infeksi. Selama 5 hari pasca operasi tikus diberikan asam
mefenamat dan amoksisilin peroral. Luka operasi diobati dengan
menggunakan larutan betadine.
3.6.6 Pengambilan Jaringan dan Pembuatan Preparat
Proses penyembuhan fraktur terjadi selama 28 hari, selanjutnya dilakukan
euthanasia untuk diambil jaringan tulang femur. Pengambilan jaringan
dilakukan dengan menggunakan alat bedah minor steril. Jaringan
kemudian dimasukkan ke dalam pot sampel yang berisi formalin 10%.
Jaringan dikirimkan ke tempat pembuatan preparat di bagian Departemen
Patologi Anatomi Fakultas Kedokteran Universitass Lampung.
3.6.7 Pembuatan Preparat
Pembuatan preparat dilakukan dengan menggunakan paraffin block
selanjutnya dilakukan pewarnaan Hematoxyillin Eosin. Pembuatan
preparat dilakukan di Laboratorium Patologi Anatomi Fakultas
36
3.6.8 Pengamatan Preparat
Pengamatan preparat dilakukan dengan melihat jaringan tulang, fibrosis,
kalus, kartilago tulang dan bone union. Pengamatan dilakukan dengan
menggunakan mikroskop dengan perbesaran 100x dan 400x di
Laboratorium Patologi Anatomi Fakultas Kedokteran Universitas
Lampung.
3.6.9 Penilaian Histopatologi
Berdasarkan Salked score penilaian histopatologi proses penyembuhan
tulang yang telah dimodifikasi dapat dilihat pada tabel 4.
Tabel 4. Penilaian Salked score pada fraktur healing yang telah dimodifikasi
Kualitas dari penyatuan (union) Skor
Tidak ada tanda‒tanda fibrosis atau penyatuan lainnya 0
Penyatuan fibosis 1
Fibrokartilaginosa atau penyatuan kartilago <25% 2 Fibrokartilaginosa atau penyatuan kartilago 26‒50% 3 Fibrokartilaginosa atau penyatuan kartilago 51‒75% 4 Fibrokartilaginosa atau penyatuan kartilago >75% 5 Kartilago termineralisasi dan penyatuan tulang 6
Woven bone (tulang anyaman) 7
Tulang matur 8
3.7Alur Penelitian
Pengambilan jaringan dan pembuatan preparat
Pengamatan dan penilaian secara histopatologi
Pada minggu keempat, tikus dieuthanasia menggunakan katemine 75‒100 mg/kgBB
xylazine 25‒50 mg/kgBB secara intraperitoneal dan terminasi Fraktur Femur dengan
gergaji kecil pada mid diafisis os femur
Kelompok K Kelompok P1 Kelompok P2
Adaptasi tikus selama 3 hari
Pengelompokkan tikus menjadi 3 kelompok,
masing‒masing berisi 10 tikus
38
3.8 Analisis Data
Data dianalisis dengan menggunakan uji statistik dengan program komputer.
Uji normalitas dilakukan dengan uji Shapiro‒Wilk dan uji homogenitas
dilakukan dengan uji levene. Selanjutnya dilakukan, uji analisis non‒parametrik
Kruskal‒Wallis dan post hoc Mann‒Whitney.
3.9 Etika Penelitian
Penelitian ini telah dilakukan kaji etik dan disetujui oleh komite etik penelitian
Fakultas Kedokteran Universitas Lampung dengan nomor
V. KESIMPULAN DAN SARAN
5.1 Kesimpulan
1. Terdapat pengaruh positif ORIF (P1) terhadap penyembuhan
fraktur femur (K) pada tikus Sprague Dawley secara histopatologi.
2. Terdapat pengaruh positif ORIF dan diberikan penambahan ALS-
R (P2) terhadap penyembuhan fraktur femur (K) pada tikus
Sprague Dawley secara histopatologi.
3. Tidak terdapat perbedaan yang signifikan secara statistik antara
penyembuhan fraktur femur yang dilakukan ORIF dan diberikan
penambahan ALS-R (P2) dibandingkan dengan kelompok yang
dilakukan ORIF (P1) pada tikus Sprague Dawley secara
histopatologi. Namun rata-rata skor histopatologi P2 lebih tinggi
dibandingkan dengan P1.
5.2 Saran
1. Peneliti lain perlu melakukan penelitian lebih lanjut mengenai
pengaruh perbandingan luas permukaan ALS-R terhadap proses
52
2. Perlu dilakukan penelitian lebih lanjut mengenai ALS-R terhadap
penambahan sel tulang yang ditinjau secara in vitro.
3. Perlu dilakukan penelitian lebih lanjut mengenai efek
antiangiogenesis dan reaksi inflamasi yang ditimbulkan oleh ALS-
DAFTAR PUSTAKA
Abbas B. 2010. Bank jaringan riset batan: Batan Research. Jakarta: Pusat Diseminasi Iptek Nuklir.
Angle SR, Sena K, Sumner DR, Virkus WW, & Virdi AS. 2012. Healing of rat femoral segmental defect with bone morphogenetic protein-2 : A dose response study. J Musculoskelet Neuronal Interact. 12(1):28–37.
Beamer B, Hettrich C, Lane J. 2009. Vascular endothelial growth factor : an essential component of angiogenesis and fracture healing. HSS J. 6(1):85–94.
Dimitriou R, Tsiridis E, Giannoudis PV. 2005. Current concepts of molecular aspects of bone healing. Injury Journal. 36(12):1392–404.
Grzywocz Z, Pius-sadowska E, Klos P, Gryzik M, Wasilewska D, Aleksandrowicz B, et al. 2014. Growth factors and their receptors derived from human amniotic cells in vitro. Folia Histochem Cytobiol. 52(3):163–70.
Lakatos R. 2014. General principles of internal fixation. Diakses pada tanggal 13
Agustus 2015. Tersedia dari:
http://emedicine.medscape.com/article/1269987-overview#aw2aab6b2
Lappas M, Permezel M, Georgiou HM, Rice GE. 2002. Nuclear Factor Kappa B Regulation of Proinflammatory Cytokines in Human Gestational Tissues In Vitro 1. Biol Reprod. 67(2):668–73.
Lieberman JR, Daluiski A, Einhorn TA. 2002. The role of growth factors in the repair of bone. J Bone Joint Surg. 84(6):1032–43.
Liu P, Guo L, Zhao D, Zhang Z, Kang K, Zhu R. 2014. Study of human acellular amniotic membrane loading bone marrow mesenchymal stem cells in repair of articular cartilage defect in rabbits. Genet Mol Res. 13(3):7992–8001.
Mescher AL. 2013. Junqueira’s Basic Histology: Text & Atlas 13th ed. New York: Mc Graw Hill.
Ridwan E. 2013. Etika pemanfaatan hewan percobaan dalam penelitiaan kesehatan. J Indon Med Assoc. 63(3):112-6.
Rodriguez AMT, Gude F, Valladares MJL, Tourino R, Vietes B, Silva MT, et al. 2009. Effects of lyophilization on human amniotic membrane. Acta
Ophthalmol. 87(4):396–403.
Shapiro F. 2008. Bone development and its relation to fracture repair. The role of mesencymal osteoblast and surface osteoblast. Eur Cell Mater. 15(1):53–76.
Sjamsuhidajat R, Jong WD. 2010. Buku Ajar Bedah Edisi Ke-3. Jakarta: Penerbit Buku Kedokteran EGC.
Solomon L, Warwick D, Nayagam S. 2010. Apley's System of Orthopaedics and
Fractures 9th ed. Liverpool: The Royal Liverpool University.
Sulistiyani A. 2013. Jumlah Osteoblas Pada Tulang Femur Tikus Sprague dawley Pasca Imobilisasi Dengan Metode Pin Intramedular [Skripsi]. Yogyakarta: Universitas Gadjah Mada.
Suryani N. 2013. Perbandingan metode pengeringan terhadap resorbsi amnion dalam larutan simulated body fluid (SBF). Majalah Ilmiah Aplikasi Isotop
Dan Radiasi. 4(2):53–8.
Thomson JD, Jonna K. 2014. Open reduction and internal fixation of distal femoral fractures in adult. Diakses pada tanggal 13 Agustus 2015. Tersedia dari: http://emedicine.medscape.com/article/2000429-overview
Toda A, Okabe M, Yoshida T, Nikaido T. 2007. Critical review the potential of amniotic membrane / amnion-derived cells for regeneration of various tissues. J Pharmacol Sci. 105(3):215–28.
Winanto ID, Kamal AF, Prabowo Y, Jusuf AA, Prasetyo M. 2013. Role of sterile
lyophilized amniotic membrane in treatment of fracture with bone defect : an