i
PEMBENTUKAN TUNAS ADVENTIF PISANG BARANGAN
(
Musa acuminata
L.) DENGAN KONSENTRASI BAP DAN POSISI BONGGOL
EKSPLAN YANG BEBEDA SECARA IN VITRO
SKRIPSI
Oleh:
NURNAWIYAH KARTIKA SARI
070301008
DEPARTEMEN BUDIDAYA PERTANIAN
FAKULTAS PERTANIAN
UNIVERSITAS SUMATERA UTARA
MEDAN
PEMBENTUKAN TUNAS ADVENTIF PISANG BARANGAN
(
Musa acuminata
L.) DENGAN KONSENTRASI BAP DAN POSISI BONGGOL
EKSPLAN
YANG BEBEDA SECARA IN VITRO
SKRIPSI
Oleh:
NURNAWIYAH KARTIKA SARI
070301008
Skripsi sebagai salah satu syarat untuk memperoleh
gelar sarjana di Fakultas Pertanian
Universitas Sumatera Utara
DEPARTEMEN BUDIDAYA PERTANIAN
FAKULTAS PERTANIAN
UNIVERSITAS SUMATERA UTARA
M E D A N
iii
Judul Skripsi : Pembentukan Tunas Adventif Pisang Barangan(Musa accuminata
L.) dengan Posisi Potongan dan Konsentrasi BAP yang Berbeda
Nama : Nurnawiyah Kartika Sari
NIM : 070301008
Departemen : Budidaya Pertanian
Program Studi : Agronomi
Disetujui oleh
Komisi Pembimbing
Ir. Mariati, M.Sc. Ir. Jonis Ginting, MS.
Ketua Anggota
ABSTRAK
NURNAWIYAH KARTIKA SARI. : Pembentukan Tunas Adventif Pisang
Barangan (Musa accuminata L.). Penelitian ini dilakukan di bawah bimbingan
Ir. Mariati, Msc dan Ir. Jonis Ginting, Ms.
Perbanyakan pisang barangan secara generatif hanya menggunakan anakan pada
umumnya menghasilkan 2-3 anakan saja. Namun, kebutuhan bibit tidak terpenuhi maka
digunakan teknik kultur jaringan dengan menggunakan BAP dan posisi bonggol eksplan
agar dapat menghasilkan bibit pisang barangan lebih banyak dalam waktu yang relatif
singkat. Penelitian ini mengkaji tanggap pertumbuhan tunas adventif pisang barangan
terhadap konsentrasi BAP dan posisi bonggol eksplan yang berbeda secara in-vitro yang
telah dilaksanakan di laboratorium kultur jaringan Dinas Pertanian Gedung Johor Medan
Polonia pada Maret-Mei 2011 menggunakan Rancangan Acak Lengkap
faktorial.Parameter yang diamati adalah Jumlah akar (buah), Panjang akar (cm), Waktu
inisiasi akar (hari), Jumlah tunas (buah), Panjang tunas(cm), Waktu inisiasi tunas (hari).
Hasil penelitian menunjukkan bahwa penggunaan BAP dan Posisi bonggol
eksplan tidak berbeda nyata terhadap semua parameter
v
RIWAYAT HIDUP
Nurnawiyah Kartika.Sari dilahirkan di Medan, Sumatera Utara pada
tanggal 19 november 1989 anak dari Ayahanda Syamsul Bahri dan Ibu Siti
Fauziah. sebagai putri pertama dari tiga bersaudara.
Pendidikan formal yang pernah ditempuh adalah SD Kemala Bhayangkari I
Medan lulus pada tahun 2001, SLTP Kemala Bhayangkari I Medan lulus
tahun 2004 dan SMA Kemala Bhayangkari I Medan lulus tahun 2007. Tahun
2007 diterima sebagai mahasiswa Universitas Sumatera Utara, Fakultas Pertanian
pada Departemen Budidaya Pertanian Program Studi Agronomi.
Selama mengikuti perkuliahan penulis pernah asisten laboratorium
Perbanyakan Vegetatif Tanaman (2011). Selain itu penulis aktif dalam organisasi
ekstra kampus HMI Komisariat FP USU (2007-2009) dan pengalaman di bidang
kemasyarakatan, penulis peroleh saat mengikuti Praktek Kerja Lapangan (PKL) di
Sumatera Bakrie Plantations Tbk, Kisaran pada bulan Juli sampai Agustus
tahun 2010.
KATA PENGANTAR
Puji dan syukur penulis panjatkan kehadirat Allah SWT. karena atas berkat
dan rahmat-Nya penulis dapat menyelesaikan penulisan skripsi yang berjudul
”Pembentukan Tunas adventif Pisang Barangan ( Musa accuminata L.)”.
Pada kesempatan ini penulis menghaturkan ucapan terima kasih yang
sebesar-besarnya kepada Ayahanda Syamsul Bahri dan Ibunda Siti Fauziah. yang
telah membesarkan dan mendidik penulis selama ini. Penulis menyampaikan
ucapan terima kasih kepada Ibu Ir. Mariati, Msc dan Bapak Ir. Jonis Ginting, MS
selaku ketua dan anggota komisi pembimbing yang telah membimbing dan
memberikan berbagai masukan, mulai dari penetapan judul, melakukan penelitian,
sampai pada ujian akhir.
Terima kasih kepada kedua orang tua saya yang telah membesarkan
penulis dengan kasih sayang dan kesabaran, adik-adikku Levita Indriani dan
Rizky Muhamadi yang telah menjadi penyemangat bagi penulis dalam
menyelesaikan perkuliahan. Selain itu, penulis juga mengucapkan terima kasih
kepada kak Asni SP, dan sahabat-sahabat terbaikku Agus Salim, Rofikoh A.
Siregar, Ahmad Fadli Arbian, Wulan Devita Sari, Mazidah Ulfa,Meilisya Dwi
Arga, Subarianto, Dedi Irawan sari dan sahabat-sahabat angkatan 2007 yang telah
vii
Penulis menyadari bahwa skripsi ini masih jauh dari kesempurnaan, oleh
sebab itu penulis mengharapkan kritik dan saran yang bersifat membangun demi
kesempurnaan skripsi ini. Akhir kata, penulis mengucapkan terima kasih.
DAFTAR ISI
ABSTRAK ... i
ABSTRACT ... i
RIWAYAT HIDUP ... ii
KATA PENGANTAR ... iii
DAFTAR TABEL ... vi
DAFTAR GAMBAR . ... vii
DAFTAR LAMPIRAN ... viii
PENDAHULUAN Latar Belakang ... 1
Tujuan Penelitian ... 3
Hipotesa Penelitian ... 3
Kegunaan Penelitian ... 3
TINJAUAN PUSTAKA Biologi Jamur Merang ... 4
Siklus Hidup Jamur Merang ... 5
Syarat Tumbuh Jamur Merang ... 7
ix
Media tumbuh ... 8
METODE PENELITIAN Lokasi dan Waktu ... 12
Bahan dan Alat ... 12
Metode Penelitian ... 12
Peubah Amatan ... 14
Umur mulai panen (hari) ... 14
Panjang badan buah (cm) ... 15
Diameter Tudung (cm) ... 15
Jumlah badan buah (buah) ... 15
Bobot basah/plot (g) ... 15
Lamanya periode panen (hari) ... 15
Pelaksanaan Penelitian ... 16
Sanitasi rumah kaca ... 16
Persiapan media ... 16
Fermentasi pengomposan ... 16
Sterilisasi media ... 17
Sterilisasi rumah kaca dan kotak ... 17
Inkubasi ... 18
Penyiraman ... 18
Pengendalian kontaminan ... 18
HASIL DAN PEMBAHASAN Hasil ... 19
Pembahasan ... 25
KESIMPULAN DAN SARAN Kesimpulan ... 29
Saran ... 29
DAFTAR PUSTAKA ... 30
xi
DAFTAR TABEL
No. Hal.
1. Tabel 1. Rataan Jumlah Akar ...20
2. Tabel 2. Rataan Panjang Akar...21
3. Tabel 3. Rataan Waktu Inisiasi Akar...21
4. Tabel 4. Rataan Jumlah Tunas...22
.
5. Tabel 5. Rataan Panjang Tunas...24
6. Tabel 6. Rataan Waktu Inisiasi Tunas...24
DAFTAR LAMPIRAN
No. Hal.
1. Bagan Penelitian...34
2. Tabel Kegiatan Penelitian...35
3. Komposisi Media Murashige dan Skoog...36
4. Data Pengamatan Jumlah Akar (buah)...37
5. Data Transformasi Jumlah Akar √X+0.5...37
6. Sidik Ragam Jumlah Akar...38
7. Data Pengamatan Panjang Akar (cm)...39
8. Data Transformasi Panjang Akar √X+0.5...39
9. Sidik Ragam Panjang Akar...40
10.Data Pengamatan Waktu Inisiasi Akar (hari)...41
11.Data Transformasi Waktu Inisiasi Akar √X+0.5...41
12.Sidik Ragam Waktu Inisiasi Tunas...42
13.Data Pengamatan Jumlah Tunas (buah)...43
14. Data Transformasi Jumlah Tunas √X+0.5...43
xiii
16. Data Pengamatan Panjang Tunas (cm)...45
17. Data Transformasi Panjang Tunas √X+0.5...45
18. Sidik Ragam Panjang Tunas...46
19. Data Pengamatan Waktu Inisiasi Tunas (hari)...47
20. Data Transformasi Waktu Inisiasi Tunas √X+0.5...47
PENDAHULUAN
Latar Belakang
Berdasarkan Sensus Pertanian Tahun 2003 (SP 2003, BPS 2004), rumah
tangga tani yang terlibat dalam budidaya pisang di Indonesia sebanyak 16 juta
atau 30% dari rumah tangga pertanian secara keseluruhan yang berjumlah
52,9 juta rumah tangga pertanian. Hal ini menggambarkan bahwa setiap 10 orang
petani 3 diantaranya menanam pisang baik sebagai tanaman perkarangan maupun
sebagai tanaman kebun/ladang. Potensi yang besar ini bila dikelola dengan baik
akan dapat meningkatkan pendapatan petani secara signifikan.
Data Badan Pusat Statistik Sumatera Utara (2010) menunjukkan produksi
pisang barangan terjadi peningkatan mencapai angka 15793 ton dengan luas areal
13787 ha, dimana produksi/ha 11.46 kw/ha. Jika dibandingkan dengan produksi
tahun 2008 yang hanya mencapai 7043 ton dengan luas areal 6311 ha, dimana
produksi/ha 11.66 kw/ha. Diantara sekian banyak jenis pisang, jenis pisang
barangan termasuk jenis pisang yang sangat digemari oleh masyarakat, selain
pisang barangan memiliki rasa yang manis pisang barangan juga memiliki nilai
gizi yang lebih tinggi dibandingkan dengan pisang lainnya.
Permintaan buah pisang barangan terus meningkat dari tahun ke tahun,
tetapi belum diikuti dengan peningkatan produktivitas. Beberapa kendala dalam
budidayanya adalah bibit/anakan yang sangat terbatas. Dari 1 tanaman induk
2
2
anakan saja, padahal kebutuhan bibit untuk pengembangan budidaya ini sangat
banyak. Pengembangan kebun seluas 6000 ha untuk memenuhi kebutuhan pasar
eksport dan 2500 ha untuk industri membutuhkan benih kultivar canvendish dan
non cavendish sebanyak- banyaknya 10 juta tanaman. Kebutuhan benih tersebut
diharapkan dapat membuka peluang investasi usaha bisnis benih sumber kultivar
unggul . Salah satu cara mengatasi masalah kekurangan bibit tersebut dengan cara
menggunakan teknik perbanyakan secara kultur jaringan (Fiani, 1994).
Dengan teknik perbanyakan tanaman secara kultur jaringan dapat
diperbanyak bibit tanaman pisang barangan dalam jumlah yang banyak dan dalam
waktu yang relatif singkat. Abdany (2001) dari hasil penelitiannya dengan
perlakuan ZPT BAP pada beberapa tingkat konsentrasi, melaporkan bahwa
konsentrasi BAP 5 mg/l mampu membentuk tunas adventif dari daun pisang
barangan, sementara itu Wahyudi (2004) melaporkan dari hasil penelitiannya
yang menggunakan Eksplan bonggol pisang barangan dengan konsentrasi
BAP 3,6, 9, 12 mg/l pada semua perlakuan menghasilkan tunas adventif.
Dari beberapa laporan penelitian tentang pembentukan tunas adventif dari
pisang barangan secara kultur jaringan belum ada yang menggunakan posissi
bonggol eksplan dengan konsentrasi BAP yang lebih rendah dari 3 mg/l, oleh
karena itu penulis tertarik untuk melakukan penelitian tentang pengeruh
pemberian BAP terhadap pembentukan tunas adventif pisang barangan dengan
Tujuan Penelitian
Untuk mengetahui tanggap pertumbuhan tunas adventif pisang barangan
terhadap konsentrasi BAP dan Posisi bonggol eksplan yang berbeda secara
in vitro
Hipotesis Penelitian
1. Konsentrasi BAP yang berbeda berpegaruh nyata terhadap pertumbuhan
tunas adventif dan akar pisang barangan.
2. Posisi bonggol eksplan yang berbeda berpengaruh nyata terhadap
pertumbuhan tunas adventif dan akar pisang barangan.
3. Ada Interaksi antara posisi bonggol eksplan dengan konsentrasi BAP
terhadap pertumbuhan tunas adventif dan akar pisang barangan.
Kegunaan Penelitian
1. Sebagai bahan dalam penyusunan skripsi yang merupakan salah satu syarat
untuk dapat memperoleh gelar sarjana di Fakultas Pertanian Universitas
Sumatera Utara, Medan.
2. Sebagai bahan informasi bagi pihak yang membutuhkan.
TINJAUAN PUSTAKA
Pisang Barangan
Suhadirman (1997) menyebutkan bahwa Musa acuminata ini berdasarkan
klasifikasi tumbuhan ini sebagai berikut : Kingdom : Plantae;
Filum : Magnoliophyta; Kelas : Magnoliopsida; Ordo : Zingiberales;
Famili : Zingiberraceae; Genus : Musa; Spesies :Musa acuminata L.
Tanaman pisang termasuk kedalam family Zingiberraceae dan golongan
herba. Pisang yang dapat dimakan berasal dari dua spesies yaitu Musa acuminata
dan musa balbisiana, dengan jumlah kromosom dasar n= 11. Pada umumnya
kultivar- kultivar pisang bersifat diploid dengan jumlah kromosom 22
(Satuhu dan Supriadi, 2000).
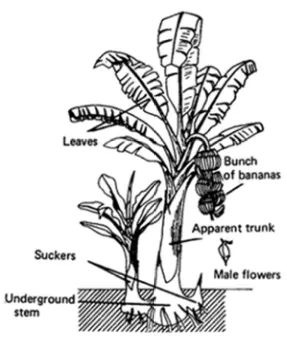
Batang pisang berakar rimpang dan tidak mempunyai akar tunggang. Akar
ini berpangkal pada umbi batang. Akar terbanyak berada dibagian bawah sampai
kedalaman 75-150 cm. Sedangkan akar yang bearada dibagian samping umbi
batang tumbuh kesamping dan mendatar, panjangnya dapat mencapai 4-5 meter.
Ada dua macam perakaran yaitu perakaran utama, akar batang yang menempel
pada bonggol batang dan perakaran sekunder, akar tumbuh dari perakaran utama
sepanjang 5 cm dari pangkal akar (Satuhu dan Supriadi, 2000).
Batang pisang sebenarnya terletak dalam tanah berupa umbi batang.
Dibagian atas umbi batang terdapat titik tumbuh yang menghasilkan daun dan
pada suatu saat akan tumbuh bunga pisang ( jantung) . Sedang yang berdiri tegak
ini terbentuk dari pelepah daun pisang yang saling menelungkup dan menutupi
dengan kuat dan kompak sehingga bisa berdiri tegak seperti batang tanaman.
Tinggi batang semu ini berkisar 3,5 – 7,5 meter tergantung jenisnya
(Cahyono, 1995).
Bonggol adalah batang pisang yang terdapat didalam tanah. Pada sepertiga
bagian bonggol sebelah atas terdapat mata calon tumbuh tunas anakan
(Gunawan, 1987; Smith, 1992)
Lembaran daun (lamina) pisang lebar dengan urat daun utama menonjol
berukuran besar sebagai pengembangan morfologis lapisan batang semu
(gedebong). Urat daun utama ini sering disebut sebagai pelepah daun. Lembaran
daun yang lebar berurat sejajar dan tegak lurus pada pelepah daun. Urat daun ini
tidak ada ikatan daun yang kuat ditepinya sehingga daun mudah sobek akibat
terkena angin kencang (Suhardiman, 1997).
Bunga pisang berupa tongkol yang sering disebut jantung. Bunga ini
muncul dari primodia yang terbentuk pada bonggolnya. Perkembangan primodia
bunga memanjang keatas hingga menembus inti batang semu dan keluar inti
batang semu. Bunga jantan dan bunga betina terjalin dalam satu rangkaian yang
terdiri dari 5-20 bunga. Rangkaian bunga ini nantinya membentuk buah, yang
disebut satu sisir. Satu bunga jantung dapat pula terdiri dari 1-2 rangkaian bunga
sehingga deretan sisirnya sangat panjang, misalnya pisang seribu
(Gunawan, 1987; Smith, 1992)
Kulit buah kuning kemerahan dengan bintik- bintik coklat. Daging buah
agak orange. Satu tandan terdiri dari 8-12 sisir. Dalam setiap sisir terdiri dari
6
6
jenis tanaman pisang. Adapun pembentukan buah pisang sesudah keluar, maka
akan terbentuk sisir pertama, kemudian memanjang lagi dan terbentuk sisir kedua
dan ketiga dan seterusnya. Jantungnya perlu dipotong sebab sudah tidak bisa
menghasilkan sisir lagi (Wattimena, 1992).
Wahyudi (2000) dari penelitiannya melaporkan bahwa dengan
penggunaan konsentrasi NAA 0,5 mg/l memberikan hasil terbaik untuk persentase
pertumbuhan yaitu 100%, jumlah tunas 3,35 buah, panjang tunas yaitu 4,7 mm
dan jumlah eksplan yang membentuk tunas yaitu 80%.
Amri (1998) dari hasil penelitian melaporkan bahwa perlakuan tingkat
konsentrasi arang aktif dengan taraf 0,02 gram berpengaruh nyata terhadap
peubah amatan panjang tunas pada 9 MSt, jumlah akar serta panjang akar.
Sedangkan terhadap peubah amatan : saat muncul tunas 6,7 dan 8 MST, jumlah
tunas serta saat muncul akar 6 MST, 7MST, dan 8 MST berpengaruh tidak nyata.
Kultur Jaringan
Kultur jaringan itu sendiri dapat diartikan suatu metode untuk mengisolasi
bagian tanaman serta menumbuhkannya dalam kondisi yang aseptik secara
in-vitro Sehingga bagian tersebut dapat memperbanyak diri dan beregenerasi
menjadi tanaman lengkap (Hartman, dkk, 2002).
Berbeda dengan teknik perbanyakan vegetatif konvensional, kultur
jaringan melibatkan pemisahan komponen-komponen biologis dan tingkat
pengendalian yang tinggi dalam memacu proses regenerasi dan perkembangan
jaringan. Setiap urutan proses dapat dimanipulasi melalui seleksi bahan tanaman,
seperti jamur dan bakteri. Semua itu dimaksudkan untuk memaksimalkan produk
akhir dalam bentuk kuantitas dan kualitas propagula berdasarkan prinsip
totipotensi sel (Zulkarnain, 2009).
Menurut Yusnita (2003) dibanding dengan perbanyakan tanaman secara
konvensional, perbanyakan tanaman secara kultur jaringan mempunyai beberapa
kelebihan sebagai berikut:
1. Untuk memperbanyak tanaman tertentu yang sulit atau sangat lambat
diperbanyak secara konvensional. Perbanyakan tanaman secara kultur
jaringan menawarkan peluang besar untuk menghasilkan jumlah bibit
tanaman yang banyak dalam waktu relatif singkat sehingga lebih ekonomis.
2. Perbanyakan tanaman secara kultur jaringan tidak memerlukan tempat yang
luas.
3. Teknik perbanyakan tanaman secara kultur jaringan dapat dilakukan
sepanjang tahun tanpa bergantung pada musim.
4. Bibit yang dihasilkan lebih sehat.
5. Memungkinkan dilakukannya manipulasi genetik.
Kultur jaringan akan lebih besar persentase keberhasilannya bila
menggunakan jaringan meristem. Jaringan meristem adalah jaringan muda, yaitu
jaringan yang terdiri dari sel-el yang selalu membelah, dindingnya tipis, belum
mempunyai penebalan dari zat pektin, plasmanya penuh, dan vakuolanya
kecil-kecil. Kebanyakan orang menggunakan jaringan ini untuk tissue culture.
Sebab, jaringan meristem keadaannya selalu membelah, sehingga
diperkirakan mempunyai zat hormone yang mengatur pembelahan
8
8 Eksplan
Eksplan artinya jaringan tanaman yang digunakan sebagai bahan tanam di
dalam botol. Eksplan dipilih dari jaringan yang masih muda karena jaringan
tersebut tersusun atas sel-sel yang masih muda dan selalu membelah. Dengan
demikian diharapkan nantinya bisa menghasilkan tanaman yang sempurna.
Sebagai eksplan (Purwanto, 2007).
Ukuran eksplan juga menentukan keberhasilan kultur jaringan. Eksplan
yang berukuran besar sangat dikhawatirkan bannyak mengan dung kontaminan,
tetapi ukuran eksplan yang terlalu kecilpun dianggap kurang efektif karena
kemampuan perkembangannya dalam media sangat lambat. Ukuran eksplan yang
paling baik adalah 0,5-1 cm, namun ukuran ini dapat bervariasi tergantung
materialtanaman yang dipakai dan jenis tanamannya (Gunawan, 1995)
Nisa (2009) melaporkandari hasil penelitiannnya bahwa campuran NAA
dan Kinetin dengan kultivar pisang berpengaruh nyata terhadap semua peubah
pengamatan. Perlakuan NAA 0,4 mg l-1 + kinetin 6 mg l-1 kultivar pisang mauli
memberikan hasil yang tertinggi terhadap persentase hidup eksplan yaitu 87,5%
dan persentase kontaminasi terendah yaitu < 5% sedangkan pemberian NAA 0,8
mg l-1 + kinetin 9 mg l-1 kultivar pisang kepok memberikan saat pertumbuhan
Media Kultur
Media kultur merupakan salah satu faktor penentu keberhasilan
perbanyakan tanaman secara kultur jaringan. Berbagai komposisi media kultur
telah diformulasikan untuk mengoptimalkan pertumbuhan dan perkembangan
tanaman yang dikulturkan (Yusnita, 2003).
Sebelum membuat medium, maka terlebih dahulu kita harus menentukan
medium apa yang akan kita buat. Jenis medium dengan komposisi unsur kimia
yang berbeda dapat digunakan untuk media tumbuh dari jaringan tanaman yang
berbeda pula (Hendaryono dan Wijayani, 1994).
Medium yang digunakan untuk kultur in vitro tanaman dapat berupa
medium padat atau cair. Medium padat digunakan untuk menghasilkan kalus yang
selanjutnya diinduksi membentuk tanaman yang lengkap (disebut sebagai planlet),
sedangkan medium cair biasanya digunakan untuk kultur sel. Medium yang
digunakan mengandung lima komponen utama yaitu senyawa anorganik, sumber
karbon, vitamin, zat pengatur tumbuh dan suplemen organik (Yuwono, 2008).
Media yang digunakan secara luas adalah media MS yang dikembangkan
pada tahun 1962. Dari berbagai komposisi dasar ini kadang-kadang dibuat
modifikasi, misalnya hanya menggunakan ½ dari konsentrasi dari garam-garam
makro yang digunakan (1/2 MS) atau menggunakan komposisi garam makro
10
10
pengatur tumbuh yang akan digunakan disesuaikan dengan tujuan inisiasi kultur
(Gunawan, 1995).
Lingkungan In Vitro
Lingkungan kultur merupakan hasil interaksi antara bahan tanaman,
wadah kultur, dan lingkungan eksternal ruang kultur, memiliki pengaruh yang
sangat besar terhadap suatu sistem kultur jaringan. Secara teoritis, semua variabel
di dalam setiap wadah kultur pada ruang kultur yang sama adalah seragam.
Sebagai konsekuensinya, hal yang sama terjadi pula di wadah-wadah kultur pada
ruang kultur yang lain. Agar pertumbuhan kultur seragam maka keseragaman
faktor lingkungan harus diupayakan, tidak hanya di dalam ruang kultur, tetapi
juga di dalam semua wadah kultur dengan cara menggunakan wadah yang
seragam (Zulkarnain, 2009).
Menurut Gunawan (1995) lingkungan tumbuh yang dapat mempengaruhi
regenerasi tanaman meliputi:
Temperatur
Penyinaran: panjang penyinaran, intensitas penyinaran, dan kualitas sinar,
serta
Ukuran wadah kultur
Dalam teknik kultur jaringan tanaman, cahaya dinyatakan dengan dimensi
lama penyinaran, intensitas dan kualitasnya. Prof. Murashige menyarankan untuk
merupakan pencerminan dari kebutuhan periodisitas tanaman yang bersangkutan
dilapangan. Kualitas cahaya mempengaruhi arah diferensiasi jaringan
(Yusnita, 2003).
Pengaruh intensitas cahaya terhadap pembentukan akar bergantung pada
cara pemberian cahaya tersebut. Protokorm Cymbidium yang berwarna hijau akan
membentuk akar dan tunas bila diberi intensitas cahaya 2200 sampai 2500 lux.
Namun, bila disimpan dalam gelap hanya membentuk tunas. Pembentukan akar
disini diduga ada kaitannya dengan metabolisme nitrogen yang terjadi dengan
adanya cahaya. Untuk keperluan kultur jaringan cahaya putih dari lampu
flourscent dengan intensitas 1000 lux untuk fase inisiasi dan subkultur, sedangkan
untuk fase pengakaran dan persiapan planlet sebelum dilakukan aklimatisasi
menggunakan intensitas 5000 sampai 6000 lux. Intensitas yang lebih rendah akan
menghasilkan planlet yang mengalami etiolasi dengan daun yang berwarna pucuk.
Lama penyinaran yang dianjurkan adalah 16 jam per hari (Wattimena, dkk, 1992).
Zat Pengatur Tumbuh
Zat pengatur tumbuh memegang peranan penting dalam pertumbuhan dan
perkembangan kultur. Faktor yang perlu mendapat perhatian dalam penggunaan
zat pengatur tumbuh antara lain jenis zat pengatur tumbuh yang akan digunakan,
konsentrasi, urutan penggunaan, dan periode masa induksi dalam kultur tertentu
(Gunawan, 1995).
Terdapat kisaran interaksi yang luas antara kelompok auksin dengan pula
dengan senyawa-senyawa kimia lainnya dan dipengaruhi oleh faktor-faktor
12
12
menyerupai sitokinin atau sebaliknya. Meskipun demikian, baik auksin maupun
sitokinin, keduanya seringkali diberikan secara bersamaan pada medium kultur
untuk menginduksi pola morfogenesis tertentu, walaupun rasio yang dibutuhkan
untuk induksi perakaran maupun pucuk tidak selalu sama. Terdapat keragaman
yang tinggi antargenus, antarspesies, bahkan antar kultivar dalam hal jenis serta
takaran auksin dan sitokinin yang dibutuhkan untuk menginduksi terjadinya
morfogenesis (Wilkins, 1989).
Benzil aminopurin (BAP)
Sifat paling karakteristik yang berkaitan dengan sitokinin adalah
perangsangan mereka terhadap pembelahan sel pada kultur jaringan tanaman. Satu
dari reaksi yang benar-benar dramatis terhadap sitokinin adalah pembentukan
organ-organ yang terjadi di bawah kondisi yang tepat dalam berbagai kultur
jaringan. Heide (1965) menemukan bahwa sitokinin-sitokinin tertentu beberapa
kali lebih efektif daripada kinetin itu sendiri pada penginduksian pembentukan
tunas dan lebih jauh bahwa spesies atau kultivar tertentu Begonia yang biasanya
tidak membentuk tunas-tunas kebetulan didaun atau berbuat demikian hanya
kadang-kadang saja, dengan pemprosesan sitokinin mengeluarkan pembentukan
tunas yang melimpah (Wilkins, 1989).
Sitokinin biasanya tidak digunakan untuk tahap pengakaran pada
mikropropogasi karena aktivitasnya yang dapat menghambat pembentukan akar,
menghalangi pertumbuhan akar, dan menghambat pengaruh auksin terhadap
inisiasi akar pada kultur jaringan sejumlah spesies tertentu. apabila ketersediaan
jaringan yang dikulturkan akan terhambat. Akan tetapi, apabila jaringan tersebut
disubkulturkan pada medium dengan kandungan sitokinin yang memadai maka
pembelahan sel akan berlangung secara sinkron (George dan Sherrington, 1984).
Zat pengatur tumbuh yang diberikan harus dapat diabsorbsi dan
ditranslokasikan ke jaringan target. Hal ini tentu tergantung dari formulasi dan
konsentrasi zat pengatur tumbuh sehingga dapat dikatakan bahwa pada
konsentrasi tersebut belum dapat diabsorbsi dan ditranslokasikan oleh tanaman
untuk pertumbuhan dan perkembangan (Wattimena, dkk, 1992).
Catrina (2009) melaporkan dari hasil penelitiannya melaporkan bahwa
BAP dan interaksi keduanya tidak berpengaruh nyata terhadap peubah waktu
munculnya tunas pertama. Tunas pertama muncul pada minggu ke-1 dan ke-2.
Semua eksplan mampu bertunas 100% dalam waktu empat minggu, namun tunas
yang tercepat muncul diperoleh dari media MS + BAP 13.32 μM yaitu pada 6.6
HST. Media yang optimum untuk multiplikasi anthurium wave of love adalah MS
+ BAP 6.66 μM dan ½MS + BAP 13.32 μM. Komposisi media MS + BAP 6.66
μM menghasilkan tunas yang banyak dengan menggunakan BAP yang lebih
sedikit, sedangkan ½MS + BAP 13.32 μM menghasilkan tunas yang sama banyak
dengan hanya menggunakan media setengah MS, namun BAP yang digunakan
harus lebih banyak. Sedangkan menurut Andriana (2005) melaporkan hasil
penelitiannya bahwa multiplikasi menunjukkan bahwa perlakuan
BAP (1, 2, 3, 4 ppm) tidak memberikan pengaruh yang nyata terhadap peubah
jumlah tunas besar, jumlah tunas kecil, jumlah primordia, jumlah nodul, total
jumlah tunas, dan panjang tunas pisang FHIA-17. Rata-rata total jumlah tunas
14
14
antara beberapa periode subkultur. Perlakuan BAP memberikan pengaruh yang
nyata pada peubah jumlah akar, panjang akar dan panjang daun. Rata-rata jumlah
akar pisang FHIA-17 terbanyak didapatkan pada perlakuan BAP 1 ppm pada
subkultur 7, yaitu 11.8. Sedangkan untuk peubah ratarata panjang akar, BAP
memberikan pengaruh yang nyata pada subkultur 5 dan subkultur 7. Pada
subkultur 5, akar pisang terpanjang didapatkan dengan perlakuan BAP 1 ppm,
yaitu sebesar 8 cm. Sedangkan pada subkultur 7, akar pisang terpanjang
didapatkan dengan perlakuan BAP 2 ppm, yaitu sebesar 4.4 cm. Perlakuan BAP
memberikan pengaruh nyata terhadap peubah rata-rata panjang daun pisang
FHIA-17 pada subkultur 5 dan subkultur 7. Pada subkultur 5, daun pisang
terpanjang didapatkan dengan perlakuan BAP 1 ppm, yaitu sebesar 4.8 cm.
Sedangkan pada subkultur 7, daun pisang terpanjang didapatkan dengan perlakuan
BAP 2 ppm, yaitu sebesar 3.8 cm.
Hasil percobaan perlakuan giberelin terhadap kualitas tunas didapatkan
bahwa tinggi tanaman, panjang batang semu, panjang pelepah, lebar daun dan
panjang akar dipengaruhi oleh jenis tunas. Perlakuan giberelin berpengaruh nyata
pada tinggi tanaman, jumlah akar, panjang batang semu dan lebar daun.
Sedangkan konsentrasi BAP pada media asal berpengaruh nyata hanya pada
peubah panjang pelepah pada minggu keempat. Pertambahan tinggi tanaman
terbesar, jumlah akar terbanyak, batang semu, pelepah, dan akar terpanjang, serta
daun terlebar dihasilkan pada perlakuan asal media BAP 3 ppm dan pada jenis
tunas tinggi. Pemberian giberelin 20 ppm dapat menghasilkan panjang batang
jumlah akar terbanyak, daun terlebar dan akar terpanjang dihasilkan oleh giberelin
0 ppm.
16
16
BAHAN DAN METODE
Tempat dan Waktu Penelitian
Penelitian dilaksanakan di Laboratorium Kultur Jaringan Dinas Pertanian
Gedung Johor Medan Polonia dengan ketinggian ± 25 meter diatas permukaan
laut, yang dimulai pada bulan Maret sampai dengan Mei 2011.
Bahan dan Alat Penelitian
Bahan tanaman yang digunakan dalam penelitian ini adalah bonggol
tanaman pisang yang berumur 3 bulan . Bahan untuk media meliputi larutan stok
media MS, BAP, agar-agar, NaOH 1 N, HCl, pH meter, aluminium foil dan
aquades. Bahan sterilisasi yang digunakan dalam penelitian ini adalah alkohol
70% dan betadine.
Alat-alat yang digunakan adalah autoklaf, Laminar Air Flow (LAF), botol
kultur, erlenmeyer, pipet skala, gelas ukur, petridis, skalpel, gunting, bunsen,
timbangan analitik, hot plate, batang pengaduk, lemari es, kertas milimeter, pinset,
oven, dan alat-alat lainnya yang mendukung penelitian ini.
Metode Penelitian
Percobaan ini menggunakan Rancangan Acak Lengkap (RAL) Faktorial
dengan dua perlakuan, yaitu:
Faktor I : Tingkat konsentrasi Pemberian BAP dengan 6 taraf :
B0 = 0
B2 = 1 mg/l
B3 = 1,5 mg/l.
B4 = 2 mg/l
B5 = 2,5 mg/l
Faktor II : Posisi Eksplan
P1 = Posisi eksplan bagian kiri bawah
P2 = Posisi eksplan bagian kanan bawah
P3 = Posisi eksplan bagian kiri atas
P4 = Posisi eksplan bagian kanan bawah
Kombinasi perlakuan ada 16, yaitu:
B0P1 B1P1 B2P1 B3P1 B4P1 B5P1
B0P2 B1P2 B2P2 B3P2 B4P2 B5P2
B0P3 B1P3 B2P3 B3P3 B4P3 B5P3
B0P4 B1P4 B2P4 B3P4 B4P4 B5P4
Jumlah ulangan : 4 ulangan
Jumlah Tanaman/botol : 1 tanaman
18
18
Data hasil penelitian dianalisis dengan sidik ragam model linier sebagai
berikut:
Yij = µ + αi + βj + (αβ)ij + εij
i = 1,2,3,4 j = 1,2,3
Dimana:
Yij = Hasil pengamatan dari konsentrasi BAP pada taraf ke-i dan varietas pada
taraf ke-j
µ = Nilai tengah
αi = Efek dari konsentrasi BAP pada taraf ke-i
βj = Efek Varietas pada taraf ke-j
(αβ)ij = Interaksi antara konsentrasi BAP pada taraf ke-i dengan varietas pada
taraf ke-j
εijk = Galat dan konsentrasi BAP pada taraf ke-i dengan varietas pada taraf
ke-j
Jika perlakuan berpengaruh nyata maka dilanjutkan dengan DMRT
Sterilisasi Alat dan Bahan
Adapun alat yang disterilisasi adalah botol kultur, erlenmeyer, pipet skala,
gelas ukur, petridis, skalpel, gunting, pinset dan aquadest dan selanjutnya
alat-alat tersebut terlebih dahulu dicuci dengan deterjen, kemudian dibilas dengan
air, setelah itu dikeringkan. Kemudian alat seperti skalpel, pipa skala, pinset dan
cawan petri dibungkus dengan kertas, sedang untuk erlenmeyer dan gelas ukur
permukaannya ditutup dengan aluminium foil. Setelah itu, semua botol kultur,
alat-alat dan aquadest dimasukkan ke dalam autoklaf pada tekanan 17,5 psi,
dengan suhu 1210C selama 60 menit. Kemudian alat-alat tersebut dimasukkan ke
dalam oven kecuali botol kultur.
Persiapan Media
Media yang digunakan dalam penelitian ini adalah Murashige dan Skoog
(1962), komposisi dapat dilihat pada Lampiran 3. Media yang telah dicampur
diatas hot plate diukur pH sampai 5,8 kemudian disterilkan didalam autoklaf
dengan suhu 1210C, tekanan 17.5 psi selama 30 menit setelah itu dibagikan
kedalam 6 erlenmeyer lalu diberi BAP pada setiap erlenmeyer sesuai perlakuan
BAP. Dibagikan kedalam 4 botol kultur untuk setiap perlakuan dan diberi label
sesuai perlakuan masing-masing.
Persiapan Eksplan
Eksplan yang digunakan adalah bonggol yang diambil dari anakan pisang
22
22 Parameter Pengamatan
Jumlah Tunas (buah)
Dihitung pada akhir penelitian dengan menghitung tunas yang muncul
yang memiliki kriteria panjang tunas lebih dari 0,5 cm.
Panjang tunas (cm)
Diukur pada akhir penelitian dengan menggunakan kertas milimeter mulai
dari tempat munculnya tunas (pangkal) sampai ujung tunas tertinggi
Waktu inisiasi tunas (hari)
Diamati setiap hari dengan melihat tunas yang muncul.
Jumlah akar (buah)
Dihitung pada akhir penelitian dengan menghitung akar yang muncul yang
memiliki kriteria panjang akar lebih dari 0,05 cm
Panjang akar (cm)
Diukur pada akhir penelitian dengan menggunakan kertas milimeter mulai
dari tempat munculnya akar (pangkal) sampai ujung akar tertinggi dengan kriteria
pada bonggol terlihat muncul radikula yang berwarna putih.
Waktu inisiasi akar (hari)
HASIL DAN PEMBAHASAN
Hasil
Jumlah akar (buah)
Data hasil pengamatan jumlah akar 12 MST dapat dilihat pada
Lampiran 4 sedangkan daftar sidik ragam dapat dilihat pada Lampiran 5.
Perlakuan BAP dan perlakuan Posisi bonggol eksplan. Rataan jumlah akar dari
perlakuan BAP dan Posisi bonggol eksplan dapat dilihat pada Tabel 1.
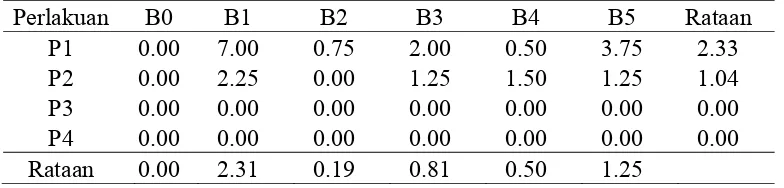
Tabel 1. Pengaruh Konsentrasi BAP dan Posisi bonggol eksplan terhadap jumlah akar (buah) pada umur 12 MST
Perlakuan B0 B1 B2 B3 B4 B5 Rataan
P1 0.00 7.00 0.75 2.00 0.50 3.75 2.33
P2 0.00 2.25 0.00 1.25 1.50 1.25 1.04
P3 0.00 0.00 0.00 0.00 0.00 0.00 0.00
P4 0.00 0.00 0.00 0.00 0.00 0.00 0.00
Rataan 0.00 2.31 0.19 0.81 0.50 1.25
Tabel 1 menunjukkan bahwa rataan jumlah akar tertinggi dihasilkan oleh
B1(BAP 0,5mg/l) yaitu sebesar 2.31 buah dan terendah terdapat pada B0 yaitu
sebesar 0.00 buah.
Pada perlakuan Posisi bonggol eksplan rataan jumlah akar tertinggi
dihasilkan oleh P1(posisi eksplan bagian kiri bawah) yaitu 2.33 buah dan
terendah terdapat pada P3 dan P4 yaitu sebesar 0.00.
Panjang akar (cm)
Data hasil pengamatan panjang akar 12 MST dapat dilihat pada
24
24
Perlakuan BAP dan perlakuan Posisi bonggol eksplan. Rataan panjang akar dari
perlakuan BAP dan Posisi bonggol eksplan dapat dilihat pada Tabel 2.
Tabel 2. Pengaruh konsentrasi BAP dan Posisi bonggol eksplan terhadap panjang
Tabel 1 menunjukkan bahwa rataan jumlah akar tertinggi dihasilkan oleh
B1(BAP 0,5mg/l) yaitu sebesar 4.20 buah dan terendah terdapat pada B0 yaitu
sebesar 0.00 buah.
Pada perlakuan Posisi bonggol eksplan rataan jumlah akar tertinggi
dihasilkan oleh P1(posisi eksplan bagian kiri bawah) yaitu 2.22 buah dan
terendah terdapat pada P4 yaitu sebesar 0.69.
Waktu inisiasi akar (hari)
Data hasil pengamatan waktu inisiasi akar 12 MST dapat dilihat pada
Lampiran 8 sedangkan daftar sidik ragam dapat dilihat pada Lampiran 9.
Perlakuan BAP dan perlakuan Posisi bonggol eksplan. Rataan waktu inisiasi akar
dari perlakuan BAP dan Posisi bonggol eksplan dapat dilihat pada Tabel 3.
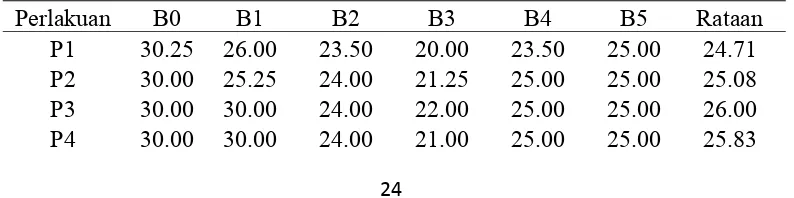
Tabel 3. Pengaruh konsentrasi BAP dan Posisi bonggol eksplan terhadap waktu inisiasi akar (hari) pada umur 12MST
Perlakuan B0 B1 B2 B3 B4 B5 Rataan
P1 30.25 26.00 23.50 20.00 23.50 25.00 24.71
P2 30.00 25.25 24.00 21.25 25.00 25.00 25.08
P3 30.00 30.00 24.00 22.00 25.00 25.00 26.00
Rataan 30.06 27.81 23.88 21.06 24.63 25.00
Tabel 3 menunjukkan bahwa rataan waktu inisiasi akar tertinggi dihasilkan
oleh B0(BAP 0 mg/l) yaitu sebesar 30.06 hari dan terendah terdapat pada B3 yaitu
sebesar 21.06 hari.
Pada perlakuan Posisi bonggol eksplan rataan waktu inisiasi akar tertinggi
dihasilkan oleh P3(potongan eksplan bagian kiri atas) yaitu 26.00 dan terendah
terdapat pada P1 yaitu sebesar 24.71.
Jumlah tunas (buah)
Data hasil pengamatan jumlah tunas 12 MST dapat dilihat pada
Lampiran 10 sedangkan daftar sidik ragam dapat dilihat pada Lampiran 11.
Perlakuan BAP dan perlakuan Posisi bonggol eksplan. Rataan jumlah tunas dari
perlakuan BAP dan Posisi bonggol eksplan dapat dilihat pada Tabel 4.
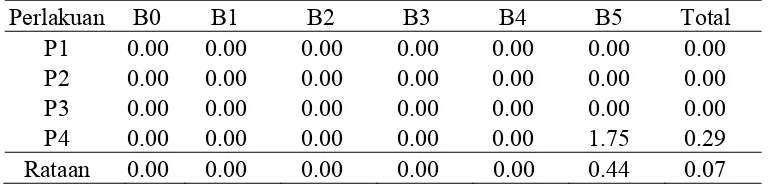
Tabel 4. Pengaruh konsentrasi BAP dan Posisi bonggol eksplan terhadap waktu Jumlah tunas (buah) pada umur 12MST
Perlakuan B0 B1 B2 B3 B4 B5 Total
P1 0.00 0.00 0.00 0.00 0.00 0.00 0.00
P2 0.00 0.00 0.00 0.00 0.00 0.00 0.00
P3 0.00 0.00 0.00 0.00 0.00 0.00 0.00
P4 0.00 0.00 0.00 0.00 0.00 1.75 0.29
Rataan 0.00 0.00 0.00 0.00 0.00 0.44 0.07
Tabel 4 menunjukkan bahwa perlakuan BAP dan perlakuan Posisi
bonggol eksplan, tunas hanya dihasilkan oleh B5 (BAP 2,5 mg/l) yaitu sebesar
1.75 buah Pada perlakuan Posisi bonggol eksplan jumlah tunas dihasilkan oleh
26
26 Panjang tunas (cm)
Data hasil pengamatan panjang tunas 12 MST dapat dilihat pada
Lampiran 12 sedangkan daftar sidik ragam dapat dilihat pada Lampiran 13.
Perlakuan BAP dan perlakuan Posisi bonggol eksplan. Rataan panjang tunas dari
perlakuan BAP dan Posisi bonggol eksplan dapat dilihat pada Tabel 5.
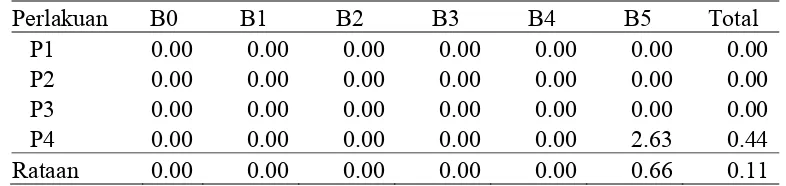
Tabel 5. Pengaruh konsentrasi BAP dan Posisi bonggol eksplan terhadap waktu Panjang tunas (cm) pada umur 12MST
Perlakuan B0 B1 B2 B3 B4 B5 Total
P1 0.00 0.00 0.00 0.00 0.00 0.00 0.00
P2 0.00 0.00 0.00 0.00 0.00 0.00 0.00
P3 0.00 0.00 0.00 0.00 0.00 0.00 0.00
P4 0.00 0.00 0.00 0.00 0.00 2.63 0.44
Rataan 0.00 0.00 0.00 0.00 0.00 0.66 0.11
Tabel 5 menunjukkan bahwa perlakuan BAP dan perlakuan Posisi bonggol
eksplan, panjang tunas hanya dihasilkan oleh B5 (BAP 2,5 mg/l) yaitu
sebesar 0.66 cm. Pada perlakuan Posisi bonggol eksplan panjang tunas hanya
dihasilkan oleh P4(potongan eksplan bagian kanan atas) yaitu 0.44 cm.
Waktu inisiasi tunas (hari)
Data hasil pengamatan waktu inisiasi tunas 12 MST dapat dilihat pada
Lampiran 15 sedangkan daftar sidik ragam dapat dilihat pada Lampiran 16.
Perlakuan BAP dan perlakuan Posisi bonggol eksplan. Rataan waktu inisiasi tunas
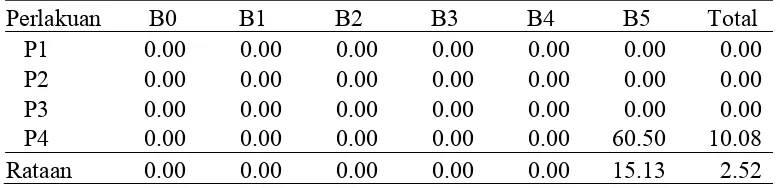
Tabel 6. Pengaruh konsentrasi BAP dan Posisi bonggol eksplan terhadap waktu Waktu inisiasi tunas (cm) pada umur 12MST
Perlakuan B0 B1 B2 B3 B4 B5 Total
P1 0.00 0.00 0.00 0.00 0.00 0.00 0.00
P2 0.00 0.00 0.00 0.00 0.00 0.00 0.00
P3 0.00 0.00 0.00 0.00 0.00 0.00 0.00
P4 0.00 0.00 0.00 0.00 0.00 60.50 10.08
Rataan 0.00 0.00 0.00 0.00 0.00 15.13 2.52
Tabel 6 menunjukkan bahwa inisiasi tunas hanya dihasilkan oleh
B5 (BAP 2,5 mg/l) yaitu sebesar 60.50 hari Pada perlakuan Posisi bonggol
eksplan waktu inisasi tunas hanya dihasilkan oleh
P4 (potongan eksplan bagian kanan atas) yaitu 10.08 hari.
Pembahasan
Hasil analisis sidik ragam diketahui bahwa pemberian BAP tidak
berpengaruh nyata terhadap semua perlakuan Dari data dapat dilihat ada
kecendrungan semakin tinggi konsentrasi BAP yang diberikan maka jumlah tunas
yang dihasilkan akan semakin tinggi.karena pemberian konsentrasi BAP yang
tertinggi pada perlakuan ini masih bisa direspon oleh tanaman sehingga tanaman
terdorong untuk melakukan pembelahan sel secara aktif.
Gunawan (1992) menyatakan bahwa sitokinin meningkatkan baik sitokinesis
maupun pembesaran sel,tetapi sitokenesis tidak meningkatkan pertumbuhan
organnya sendiri, sebab sitokenesis hanya merupakan proses pembelahan saja.
Dari hasil analisis sidik ragam diketahui bahwa pemberian BAP tidak
berpengaruh nyata terhadap pembentukan akar, panjang akar dan jumlah akar. Hal
28
28
berkesinambungan dengan auksin yang ada pada tanaman pisang barangan. Pada
dasarnya setiap tanaman telah memiliki hormon auksin dan sitokinin yang
berbeda- beda, maka pada pemberian BAP yang rendah maka terbentuk akar
adventif pada tanaman pisang barangan,karena pada bagian bawah bonggol pisang
barangan banyak terdapat hormon auksin.
Dari hasil analisis sidik ragam diketahui bahwa potongan tidak
berpengaruh nyata terhadap jumlah tunas yang terdapat pada semua perlakuan.
Dari data dapat dilihat bahwa ada kecendrungan ketelitian membelah bonggol
pisang barangan tersebut. Hal ini diduga karena posisi dari titik tumbuh dari setiap
bonggol pisang letak nya berbeda- beda . Gunawan (1992) menyatakan faktor dari
setiap fisiologis setiap tanaman berbeda- beda dan dari setiap tanaman memiliki
auksin dan sitokinin yang berbeda priode dari masa inkubasi dari setiap tanaman
juga berbeda.
Dari hasil analisis sidik ragam diketahui bahwa potongan tidak
berpengaruh nyata terhadap jumlah tunas hal ini juga diduga karena keberhasilan
morfogenesis suatu kultur in-vitro sangat dipengaruhi oleh eksplan yang
dikulturkan dan ukuran eksplan yang digunakan. Wattimena (1992) ukuran yang
terlampau kecil akan kurang daya tahannya bila dikulturkan sementara bila
terlampau besar akan sulit mendapatkan eksplan yang steril. Setiap jenis tanaman
maupun organ memiliki ukuran eksplan yang optimum untuk di kulturkan.
Dari hasil analisis sidik ragam diketahui bahwa interaksi BAP dan
Potongan tidak berpengaruh nyata terhadap semua peubah amatan seperti jumlah
akar, panjang akar, waktu inisiasi akar, panjang tunas, jumlah tunas dan waktu
diberikan telah mampu mencapai taraf keseimbangan untuk pertumbuhan dan
morfogenesis tanaman, Wattimena, dkk (1992) menyatakan kultur jaringan
morfogenesis dari eksplan selalu tergantung dari interaksi antara konsentrasi BAP
dan Potongan. Perlu diperhatikan bahwa apa saja yang digambarkan tentang
pengaruh interaksi anatara konsentrasi BAP dan Posisi merupakan gambaran
kasar. Interaksi yang ditemukan dalam praktek umumnya lebih kompleks.
Konsentrasi yang di perlukan dari masing- masing ZPT tersebut (sitokinin)
tergantung dari jenis eksplan, genotipe, kondisi kultur serta jenis sitokinin yang
dipergunakan. Selain itu, pada keadaan tertentu BAP dapat mendukung auksin
terhadap eksplan. Didukung oleh Hendaryono dan wijayani (1994) menyatakan
dalam pertumbuhan jaringan, sitokinin berpengaruh terutama pada proses
pembelahan sel. Bersama- sama dengan sitokinin dengan kadar yang relatif
rendah, diferensiasi cendrung kearah pembentukan akar adventif. Sedangkan pada
pemberian sitokinin dengan kadar yang relatif tinggi, diferensissi akan cenderung
30
30
KESIMPULAN DAN SARAN
Kesimpulan
1. Perlakuan konsentrasi BAP berpengaruh nyata terhadap semua
parameter perlakuan.
2. Perlakuan konsentrasi BAP 2,5 mg/l merangsang munculnya tunas
lebih cepat di bandingkan dengan perlakuan lain.
3. Interaksi antara konsentrasi BAP dan Posisi eksplan berpengaruh nyata
terhadap semua parameter perlakuan.
Saran
Perlu dilakukan penelitian lanjutan dengan meningkatkan konsentrasi BAP
yang di gunakan dalam usaha meningkatkan pembentukan tunas adventif pisang
Bakhtiar, A. 1991. Manfaat Tanaman Pisang.Makalah Penataran Petani dan Pedagang Pengumpul Pisang di Kabupaten Simalungun , Sumatera Utara.
Cahyono, A. 1995.Potensi Pengembangan Budaya dan Peluang Agribisnis Pisang. Prodising. Seminar Nasional. Ketahanan Pangan dan Agribisnis. PSE. Sumatera Utara 21 – 22 November 2000 : 110 – 116.
Fiani, A. dan A. Denian. 1994. Teknologi Budidaya Pisang. Dalam: Proseding Seminar Penelitian Tanaman Pangan no 05 – 1994 Balai Penelitian dan Pengembangan Tanaman Pertanian Sub Balai Penelitian Tanaman Pangan Solok Hal 65 - 67.
George, E.F and P.D. Sherrington. 1984. Plant Propagation by Tissue Culture, Handbook and Directory of Comercial Laboratoryes. Easter Press, England.
Gunawan, L.W. 1995. Teknik Kultur Jaringan In Vitro dalam Hortikultura. Penebar Swadaya: Jakarta.
Hartmann, H.T., D.E. Kester, F.T. Davies and R.L. Geneve. 2002. Plant Propagation Principles and Practiese, 6th Ed. New Delhi: Prentice Hall of Insia Private Limited.
Hendaryono dan Wijayani. 1994. Pengetahuan Dasar Biologi Bunga dan Teknik Penyerbukan Silang Buatan. PT. Gramedia: Jakarta.
Nazir, N. 2000. Pisang Budidaya Pengolahan dan Prospek Diserfikasinya . Okada. Yayasan Hutanku : Padang.
Purwanto, W. A. 2007. Budi Daya Pisang. Kanisius: Yogyakarta.
Reni ,W. 2005. Variasi Morfologi dan Sistem Polinasi Pisang yang Terdapat di Kurai, Kecamatan Suliki Kabupaten Limapuluh Kota Skripsi Fakultas FMIPA Universitas Andalas Padang: Padang.
Satuhu, S. dan A. Supriadi ., 1990. Pisang Budidaya Pengolahan dan Prospek Pasar. Penebar Swadaya: Jakarta.
Suhardiman, P ., 1997 Budidaya pisamng Cavendish. Kanisius : Yogyakarta.
32
32
Wilkins, M.B., 1992. Fisiologi Tanaman. Penerjemah Sutedjo M.M dan Kartasapoetra A.G. penerbit Bumi Aksara: Jakarta.
Yusnita, 2003. Kultur Jaringan. Cara Memperbanyak Tanaman Secara Efisien. Agromedia Pustaka: Jakarta.
Yuwono, T. 2008. Bioteknologi Pertanian. Gadjah Mada University Press: Yogyakarta.
34
34 Lampiran 2. Tabel kegiatan penelitian
Lampiran 3. Komposisi media murashige dan skoog (MS)