SINTESIS GALAKTOMANAN IKAT SILANG FOSFAT DARI
GALAKTOMANAN KOLANG-KALING (Arenga pinnata)
DENGAN TRINATRIUM TRIMETAFOSFAT
SKRIPSI
HOTNIDA NOVALIA
NIM : 100802021
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
UNIVERSITAS SUMATERA UTARA
SINTESIS GALAKTOMANAN IKAT SILANG FOSFAT DARI
GALAKTOMANAN KOLANG-KALING (Arenga pinnata)
DENGAN TRINATRIUM TRIMETAFOSFAT
SKRIPSI
Diajukan untuk melengkapi tugas dan memenuhi syarat mencapai gelar Sarjana Sains
HOTNIDA NOVALIA
100802021
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
UNIVERSITAS SUMATERA UTARA
PERSETUJUAN
Judul : Sintesis Galaktomanan Ikat Silang Fosfat Dari Galaktomanan Kolang-Kaling (Arenga pinnata) dan Trinatrium Trimetafosfat
Kategori : Skripsi
Nama : Hotnida Novalia Nomor Induk Mahasiswa : 100802021
Program : Sarjana (S1) Kimia Departemen : Kimia
Fakultas : Matematika dan Ilmu Pengetahuan Alam Universitas Sumatera Utara
Disetujui di
Medan, Januari 2014
Komisi Pembimbing :
Pembimbing II Pembimbing I
Dr. Mimpin Ginting, MS Dr.Juliati Br Tarigan, M.Si NIP: 195510131986011001 NIP: 197205031999032001
Diketahui/ Disetujui oleh
Departemen Kimia FMIPA USU Ketua,
PERNYATAAN
SINTESIS GALAKTOMANAN IKAT SILANG FOSFAT DARI GALAKTOMANAN KOLANG-KALING (Arenga pinnata)
DENGAN TRINATRIUM TRIMETAFOSFAT
SKRIPSI
Saya mengakui bahwa skripsi ini adalah hasil karya sendiri, kecuali beberapa kutipan dan ringkasan yang masing-masing disebutkan sumbernya.
Medan, Januari 2015
PENGHARGAAN
Puji dan syukur penulis penjatkan kepada Tuhan Yang Maha Esa, yang telah selalu memberkati semua apa yang saya kerjakan, dan penulis menyadari sepenuhnya bahwa oleh karena kasih dan anugerahNya penulis dapat menyelesaikan skripsi ini sebagai salah satu syarat untuk menyelasaikan pendidikan sarjana sains di Fakultas MIPA USU.
Penulis mengucap terima kasih kepada :
1. Ibu Dr. Juliati Br. Tarigan, M.Si, selaku pembimbing I dan Bapak Dr. Mimpin Ginting, MS, selaku pembimbing II yang telah banyak meluangkan waktu dan
setia membimbing penulis selama melakukan penelitian dan penyusunan skripsi ini hingga selesai.
2. Ibu Dr. Rumondang Bulan, MS dan Bapak Drs.Albert Pasaribu, M,Sc selaku Ketua dan Sekretaris Departemen Kimia FMIPA USU.
3. Bapak Drs. Minto Supeno, MS selaku dosen wali serta seluruh staf pengajar yang telah membimbing penulis selama mengikuti perkuliahan.
4. Bapak Prof. Dr. Jamaran Kaban, M.Sc selaku ketua bidang Kimia Organik FMIPA USU.
5. Bapak Dr. Mimpin Ginting, MS selaku Kepala Laboratorium KIMIA Organik MIPA USU beserta Dosen dan Staff Laboratorium Kimia Organik FMIPA USU.
6. Orang yang penulis kasihi, Thamrin Pakpahan, dan teman-teman 2010, terkhususnya, kepada Dela, Dorkas, Gusti, Roympus, Dedi M, Dedi, Dewi, dan Berkat yang telah banyak membantu, menghibur, dan memberi semangat kepada penulis selama perkuliahan hingga saat ini.
7. Asisten Kimia Organik, Asisten Kimia Organik Bahan Alam, Asisten Pusat Penelitian USU, Asisten Kimia Analitik dan adik-adik stambuk 2011-2014, terima kasih karena telah banyak membantu dan memotivasi penulis.
8. Kelompok Kecil Eunike yang penulis kasihi, yaitu Adelina Sidabutar, Doni, Zulfanri, Dian, Yabes, dan Rahel, terima kasih buat setiap doa, motivasi, saran, waktu, yang telah kalian berikan kepada penulis selama perkuliahan hingga saat ini hingga penulis dapat menyelesaikan skripsi ini.
Akhirnya penulis mengucapkan terima kasih yang sebesar-besarnya kepada Paian Bonar Lbn.Tobing dan Lilis Suryani Tompul selaku orang tua penulis yang telah memberikan seluruh dukungan sarana dan prasarana, dan setia mendidik, mendoakan, dan memberi semangat kepada penulis, serta kepada adik penulis, Leonardo Tobing, yang telah banyak mendukung, mendoakan, dan membantu penulis hingga menyelesaikan skripsi ini.
Penulis menyadari bahwa skripsi ini masih jauh dari sempurna karena keterbatasan penulis. Semoga skripsi ini dapat bermanfaat bagi penelitian dan ilmu pengetahuan .
SINTESIS GALAKTOMANAN IKAT SILANG FOSFAT DARI GALAKTOMANAN KOLANG-KALING (Arenga pinnata)
DENGAN TRINATRIUM TRIMETAFOSFAT
ABSTRAK
Hasil modifikasi galaktomanan “kolang-kaling” (GKK) melalui proses pembentukan ikat silang, dapat diaplikasikan sebagai matriks pembawa obat. Dalam penelitian ini dilakukan ekstraksi galaktomanan dari 700 gram kolang-kaling menggunakan pelarut etanol diperoleh 9,9013 gram (1,4%). Ikat silang galaktomanan dengan Trinatrium Trimetafosfat dilakukan dengan dua metode yaitu ikat silang tanpa proses pemanasan dan ikat silang dengan proses pemanasan pada suhu 50oC. Analisis gugus fungsi galaktomanan ikat silang fosfat dengan spektrofotometer FT-IR menghasilkan pita serapan pada daerah bilangan gelombang 1280-1260 cm-1 yang menunjukan adanya gugus P=O alifatik yang didukung oleh pita serapan pada daerah bilangan gelombang 1050-950 cm-1 yang menunjukkan adanya gugus P-O-C asimetrik. Hasil analisis SEM (Scanning electron Microscopic) menunjukkan morfologi permukaan galaktomanan ikat silang fosfat menjadi kasar dan berlubang. Hasil pengukuran ketebalan menghasilkan tebal film 0,05-0,22 mm. Hasil uji kuat tarik yang diperoleh sebesar 0,268-9,714 MPa, kemuluran yang diperoleh sebesar 0,751 - 14,35 %, hasil pengukuran derajat swelling galaktomanan ikat silang fosfat yang diperoleh dari metode perendaman didalam NaCl 0,9 % lebih kecil dibandingkan derajat
swelling didalam air suling dan derajat swelling galaktomanan ikat silang fosfat tanpa pemanasan lebih besar dibandingkan galaktomanan ikat silang fosfat dengan pemanasan.
SYNTHESIS OF PHOSPHATE CROSSLINKED GALACTOMANAN FROM GALACTOMANNAN OF SUGAR PALM FRUIT (Arenga
pinnata) WITH TRISODIUM TRIMETAPHOSPATE
ABSTRACT
Modification of galactomannan of sugar palm fruit (GKK) by the process of crosslinked can be used as a drug carrier matrix. Phosphate crosslinked galactomannan can be used as a drug carrier matrix. Extraction of galactomannan from 700 grams sugar palm fruit used ethanol that resulted 9.9013 grams (1,4%). The crosslinked of galactomannan with Trisodium Trimetaphosphate has done by two methods, crosslinked without heating process and crosslinked with the heating process in the temperature of 50oC. The analysis of functional groups phosphate crosslinked galactomannan with the spectrophotometer of FT-IR which appeared the absorption band in wave number 1280-1260 cm-1 which shows the group of P = O aliphatic that supported by an absorption band in wave number 1050-950 cm-1 which shows the group of P-O-C asymmetric. The result of SEM (Scanning electron Microscopic) appeared that morphology of surface have showed that phosphate crosslinked galactomanan was rough and perforated. The measurement of thickness appeared that thick of film have obtained was 0.05-0.22 mm. The test results of tensile strength was 0,268-9,714 MPa, percentage of elongation was 0,751 - 14,35 %, the measurement degree of swelling phosphate crosslinked galactomanan in NaCl 0,9% was smaller than the degree of swelling phosphate crosslinked galactomannan without heating process in water, and the degree of swelling was larger than phosphate crosslinked galactomannan with the heating process.
DAFTAR ISI
Bab 1. Pendahuluan
1.1 Latar Belakang 1.2 Permasalahan
1.3 Pembatasan Masalah 1.4 Tujuan Penelitian 1.5 Manfaat Penelitian 1.6 Lokasi Penelitian 1.7 Metodologi Penelitian
1
Bab 2. Tinjauan Pustaka 2.1 Aren
2.2 Kolang-kaling
2.3 Polisakarida 2.3.1 Manan 2.4 Galaktomanan
2.5 Galaktomanan dari Kolang-Kaling 2.6 Ikat Silang
2.7 Galaktomanan Ikat Silang
5
Bab 3. Metodologi Percobaan 3.1 Alat-alat
3.2 Bahan-bahan 3.3 Prosedur Penelitian
3.3.1 Ekstraksi Galaktomanan dari Kolang-Kaling 3.3.2 Pembuatan Larutan Trinatrium Trimetafosfat 3.3.3 Pembuatan Galaktomanan Ikat Silang Fosfat
3.3.3.1 Pembuatan Galaktomanan Ikat Silang Fosfat dengan Waktu Reaksi 8 Jam
3.3.3.2 Pembuatan Galaktomanan Ikat Silang Fosfat dengan Waktu Reaksi 8 Jam dan Pemanasan dengan Suhu 50oC
3.3.4 Uji Sifat Mengembang (Swelling)
3.3.6 Pengukuran Kekuatan Tarik dan Kemuluran dengan Uji Kuat Tarik
3.4 Bagan Penelitian
3.4.1 Ekstraksi Galaktomanan dari Kolang-Kaling 3.4.2 Pembuatan Larutan Trinatrium Trimetafosfat 3.4.3 Pembuatan Galaktomanan Ikat Silang Fosfat
3.4.3.1 Pembuatan Galaktomanan Ikat Silang Fosfat dengan Waktu Reaksi 8 Jam
3.4.3.2 Pembuatan Galaktomanan Ikat Silang Fosfat dengan Waktu Reaksi 8 Jam dan Pemanasan dengan Suhu 50oC
3.3.4 Uji Sifat Mengembang (Swelling)
3.3.5 Uji Ketebalan Film Galaktomanan Ikat Silang Fosfat
3.3.6 Pengukuran Kekuatan Tarik dan Kemuluran dengan Uji Kuat Tarik
22
Bab 4. Hasil Dan Pembahasan 4.1 Hasil
4.1.1 Hasil Ekstraksi Dari Kolang-Kaling 4.1.2 Hasil dari Spektroskopi Inframerah
Galaktomanan
4.1.2.1 Hasil Analisis Gugus Fungsi
Galaktomanan dengan Spektrofotometer FT-IR
4.1.2.2 Hasil Analisis Gugus Fungsi
Galaktomanan Ikat Silang Fosfat (GIF) dari Spektrofotometer FT-IR dengan Waktu Reaksi 8 Jam
4.1.2.3 Hasil Analisis Gugus Fungsi dari
Galaktomanan Ikat Silang Fosfat (GIF) dengan Spektrofotometer FT-IR dalam Pemanasan dengan Suhu 50oC
4.1.3 Hasil Analisis Morfologi Permukaan GKK dan GIF dengan SEM (Scanning Electron
Microscope)
4.1.4 Hasil Uji Sifat Mengembang (Swelling) 4.1.5 Hasil Pengukuran Ketebalan Film
4.1.6 Hasil Uji Kekuatan Tarik dan Kemuluran Film 4.2 Pembahasan
4.2.1 Hasil Ekstraksi Galaktomanan dari Kolang- Kaling
4.2.2 Ikat Silang Galaktomanan dengan Trinatrium Trimetafosfat
4.2.3 Hasil Analisis GKK dan GIF dengan Spektrofotometer FT-IR
4.2.4 Hasil Uji Morfologi Permukaan dengan SEM (Scanning Electron Microscope)
4.2.5 Hasil Uji Sifat Mengembang (Swelling) 4.2.6 Hasil Pengukuran Ketebalan Film
4.2.7 Hasil Uji Kekuatan Tarik dan Kemuluran Film
Bab 5. Kesimpulan Dan Saran 5.1 Kesimpulan 5.2 Saran
Daftar Pustaka
39 40 40
42 43
DAFTAR TABEL
Nomor Judul
Tabel
Tabel 2.1 Jenis Galaktomanan Komersial
Tabel 4.1 Hasil Analisis Gugus Fungsi Galaktomanan dengan Spektrofotometer FT-IR
Tabel 4.2 Hasil Analisis Gugus Fungsi GIF dengan Spektrofotometer FT-IR
Tabel 4.3 Hasil Analisis Gugus Fungsi GIF dengan Spektrofotometer FT-IR
Tabel 4.4 Hasil Pengukuran Ketebalan Film
Tabel 4.5 Hasil Uji Kekuatan Tarik dan Kemuluran Film
Halaman
12 28
28
29
DAFTAR GAMBAR
Nomor Judul
Gambar
Gambar 2.1 Pohon Aren Gambar 2.2 Kolang-kaling Gambar 2.3 Manan
Gambar 2.4 Glukomannan Gambar 2.5 Galaktomannan Gambar 2.6 Galaktoglukomannan
Gambar 2.7 Reaksi Galaktomanan Ikat Silang Gambar 2.8 Reaksi Galaktomanan dan Ion Borat
Gambar 2.9 Proses Isomerisasi Glutaraldehida dalam Suasana Asam dan Reaksi antara Gluteraldehida dan Gugus Hidroksil Gambar 4.1 Hasil SEM dari A. Galaktomanan; B. Galaktomanan
Ikat Silang Fosfat
Gambar 4.2 Histogram Derajat Swelling Galaktomanan dan Galaktomanan Ikat Silang Fosfat Tanpa Pemanasan di dalam Air
Gambar 4.3 Histogram Derajat Swelling Galaktomanan Ikat Silang Fosfat dengan Pemanasan dengan Suhu 50oC di dalam Air
Gambar 4.4 Histogram Derajat Swelling Galaktomanan Ikat Silang Fosfat Tanpa Pemanasan di dalam NaCl 0,9 %
Gambar 4.5 Histogram Derajat Swelling Galaktomanan dan Galaktomanan Ikat Silang Fosfat dengan Pemanasan dengan Suhu 50oC di dalam NaCl 0,9%
Gambar 4.6 Reaksi Ikat Silang Galaktomanan dan Trinatrium Trimetafosfat
Gambar 4.7 Spektrum FT-IR dari Galaktomanan
Gambar 4.8 Spektrum FT-IR Galaktomanan Ikat Silang Fosfat Gambar 4.9 Spektrum FT-IR Galaktomanan Ikat Silang Fosfat
DAFTAR LAMPIRAN
Nomor Judul
Lampiran
Lampiran 1. Film Galaktomanan dan Galaktomanan Ikat Silang Fosfat yang dihasilkan
Lampiran 2. Uji Derajat Swelling
Lampiran 3. Hasil Analisis FT-IR GIF 1A Lampiran 4. Hasil Analisis FT-IR GIF 2A Lampiran 5. Hasil Analisis FT-IR GIF 3A Lampiran 6. Hasil Analisis FT-IR GIF 4A Lampiran 7. Hasil Analisis FT-IR GKK Lampiran 8. Hasil Analisis FT-IR GIF 3B
Lampiran 9. Perhitungan Uji Kekutan Tarik (σT) dan Kemuluran (�) Film
Halaman
49
DAFTAR ISTILAH
Galaktomanan Ikat Silang Fosfat dengan pebandingan GKK : TMP = 1:1 tanpa pemanasan.
Galaktomanan Ikat Silang Fosfat dengan pebandingan GKK : TMP = 1:2 tanpa pemanasan.
Galaktomanan Ikat Silang Fosfat dengan pebandingan GKK : TMP = 1:3 tanpa pemanasan.
Galaktomanan Ikat Silang Fosfat dengan pebandingan GKK : TMP = 1:4 tanpa pemanasan.
SINTESIS GALAKTOMANAN IKAT SILANG FOSFAT DARI GALAKTOMANAN KOLANG-KALING (Arenga pinnata)
DENGAN TRINATRIUM TRIMETAFOSFAT
ABSTRAK
Hasil modifikasi galaktomanan “kolang-kaling” (GKK) melalui proses pembentukan ikat silang, dapat diaplikasikan sebagai matriks pembawa obat. Dalam penelitian ini dilakukan ekstraksi galaktomanan dari 700 gram kolang-kaling menggunakan pelarut etanol diperoleh 9,9013 gram (1,4%). Ikat silang galaktomanan dengan Trinatrium Trimetafosfat dilakukan dengan dua metode yaitu ikat silang tanpa proses pemanasan dan ikat silang dengan proses pemanasan pada suhu 50oC. Analisis gugus fungsi galaktomanan ikat silang fosfat dengan spektrofotometer FT-IR menghasilkan pita serapan pada daerah bilangan gelombang 1280-1260 cm-1 yang menunjukan adanya gugus P=O alifatik yang didukung oleh pita serapan pada daerah bilangan gelombang 1050-950 cm-1 yang menunjukkan adanya gugus P-O-C asimetrik. Hasil analisis SEM (Scanning electron Microscopic) menunjukkan morfologi permukaan galaktomanan ikat silang fosfat menjadi kasar dan berlubang. Hasil pengukuran ketebalan menghasilkan tebal film 0,05-0,22 mm. Hasil uji kuat tarik yang diperoleh sebesar 0,268-9,714 MPa, kemuluran yang diperoleh sebesar 0,751 - 14,35 %, hasil pengukuran derajat swelling galaktomanan ikat silang fosfat yang diperoleh dari metode perendaman didalam NaCl 0,9 % lebih kecil dibandingkan derajat
swelling didalam air suling dan derajat swelling galaktomanan ikat silang fosfat tanpa pemanasan lebih besar dibandingkan galaktomanan ikat silang fosfat dengan pemanasan.
SYNTHESIS OF PHOSPHATE CROSSLINKED GALACTOMANAN FROM GALACTOMANNAN OF SUGAR PALM FRUIT (Arenga
pinnata) WITH TRISODIUM TRIMETAPHOSPATE
ABSTRACT
Modification of galactomannan of sugar palm fruit (GKK) by the process of crosslinked can be used as a drug carrier matrix. Phosphate crosslinked galactomannan can be used as a drug carrier matrix. Extraction of galactomannan from 700 grams sugar palm fruit used ethanol that resulted 9.9013 grams (1,4%). The crosslinked of galactomannan with Trisodium Trimetaphosphate has done by two methods, crosslinked without heating process and crosslinked with the heating process in the temperature of 50oC. The analysis of functional groups phosphate crosslinked galactomannan with the spectrophotometer of FT-IR which appeared the absorption band in wave number 1280-1260 cm-1 which shows the group of P = O aliphatic that supported by an absorption band in wave number 1050-950 cm-1 which shows the group of P-O-C asymmetric. The result of SEM (Scanning electron Microscopic) appeared that morphology of surface have showed that phosphate crosslinked galactomanan was rough and perforated. The measurement of thickness appeared that thick of film have obtained was 0.05-0.22 mm. The test results of tensile strength was 0,268-9,714 MPa, percentage of elongation was 0,751 - 14,35 %, the measurement degree of swelling phosphate crosslinked galactomanan in NaCl 0,9% was smaller than the degree of swelling phosphate crosslinked galactomannan without heating process in water, and the degree of swelling was larger than phosphate crosslinked galactomannan with the heating process.
BAB 1
PENDAHULUAN
1.1 Latar Belakang
Polisakarida merupakan suatu biopolimer yang pertama terbentuk di bumi. Galaktomanan merupakan suatu kelompok polisakarida, yang secara khusus diproduksi dari kacang-kacangan (Mathur, 2012). Galaktomanan umumnya terdapat pada bagian endosperma biji-bijian yang termasuk keluarga Leguminosae, dan juga terdapat pada biji kelapa sawit, kelapa, dan kapas. Polisakarida ini hampir seluruhnya larut dalam air membentuk larutan kental dan membentuk gel jika ditambahkan garam anorganik, serta akan membentuk kompleks dengan pereaksi Fehling (Rozana, 2013). Seperti namanya, galaktomanan terdiri dari dua jenis unit monomer gula, yaitu mannosa dan galaktosa. Mannosa merupakan komponen utama dan galaktosa merupakan komponen pelengkap (minor). Jumlah unit galaktosa pada polisakarida selalu lebih kecil dari mannosa (Mathur, 2012). Mannosa membentuk suatu rantai linier yang terdiri dari (1→4)-β-D-mannopiranosil, dan terikat (1→6) dengan α -D-galaktopiranosil pada jarak yang berbeda-beda, sesuai sumber tanamannya (Anonim, 2008).
Salah satu sumber galaktomanan melimpah di alam adalah kolang-kaling. Kolang-kaling merupakan endosperm biji buah aren yang berumur setengah masak setelah melalui proses pengolahan (Sunanto, 1993).
pengemulsi, dan pengental (Vargas et al, 2008). Galaktomanan telah diisolasi dari kolang-kaling menggunakan air suling dan pemisahan dilakukan dengan cara sentrifugasi sehingga diperoleh kadar galaktomanan sebesar 4,58 % (Tarigan, 2012).
Trinatrium Trimetafosfat merupakan senyawa pengikat silang yang tidak bersifat racun, sehingga sering digunakan dalam industri makanan. Trinatrium Trimetafosfat digunakan untuk mereduksi indeks kemampuan mengembang galaktomanan didalam larutan (Kabir et al., 2000).
Saat ini, telah dilakukan beberapa penelitian dengan menggunakan bahan baku galaktomanan seperti pembuatan edible film dan coating dari galaktomanan yang diaplikasikan sebagai edible packing sebagai pengganti plastik (Cerqueira et al., 2011), penggunakan polisakarida dan galaktomannan sebagai zat pembentuk gel untuk pembentukan suatu kapsul makanan buatan (Sorvari et al, 1997).
Gowda et al, 2012 dan Kabir et al., 2000, menjelaskan pengembangan dan evaluasi dari galaktomanan yang diikat silang dengan menggunakan bahan Trinatrium Trimetafosfat yang diaplikasikan sebagai zat penghantar obat. Gupta, 2012, menjelaskan karakterisasi film guar gum, salah satu galaktomanan yang dikomersilkan, yang diikat silang dengan glutaraldehida selama pencampuran dengan penambahan zat additif berupa asam sitrat dan poli vinil alkohol (PVA). Selain itu, Kabir et al, 1998, menjelaskan proses ikat silang guar gum dengan menggunakan glutaraldehida untuk mencapai derajat swelling yang rendah hingga berpotensial untuk digunakan sebagai penghantar obat yang spesifik sampai ke usus.
1.2 Permasalahan
1. Bagaimanakah sintesis galaktomanan ikat silang fosfat dari galaktomanan kolang-kaling (Arenga pinnata) dengan Trinatrium Trimetafosfat.
2. Bagaimanakah karakteristik galaktomanan ikat silang fosfat tanpa proses pemanasan dan dengan proses pemananasan pada suhu 50oC.
1.3 Pembatasan Masalah
Penelitian ini dibatasi pada sintesis galaktomanan ikat silang fosfat yang disintesis dari galaktomanan “kolang-kaling” dengan Trinatrium Trimetafosfat sebagai bahan pengikat silang dengan proses pemanasan pada suhu 50oC dan tanpa pemanasan.
1.4 Tujuan Penelitian
1. Untuk mensintesis galaktomanan ikat silang fosfat dari galaktomanan kolang- kaling (Arenga pinnata) dengan Trinatrium Trimetafosfat.
2. Untuk mengetahui karakteristik galaktomanan ikat silang fosfat tanpa proses pemanasan dan dengan proses pemananasan pada suhu 50oC.
1.5 Manfaat Penelitian
1.6 Lokasi Penelitian
Penelitian ini dilakukan di Laboratorium Kimia Organik FMIPA-USU Medan. Proses sentrifugasi dilakukan di Laboratorium Anorganik FMIPA-USU, Laboratorium Kimia Organik Bahan Alam FMIPA-USU, dan Laboratorium Penelitian Fakultas Farmasi USU. Analisis morfologi permukaan dengan SEM
(Scanning Electron Microscopic) dan perubahan gugus fungsi dengan
spektrofotometer FT-IR dilakukan di Laboratorium Terpadu USU. Uji kuat tarik dilakukan di Laboratorium Penelitian Teknik Kimia USU.
1.7 Metodologi Penelitian
Penelitian ini bersifat eksperimen laboratorium dimana pada tahap pertama dilakukan ekstraksi galaktomanan menggunakan pelarut air suling dengan perbandingan kolang-kaling dan 1:12 air suling, kemudian disentrifugasi pada kecepatan 9500 rpm selama 15 menit. Endapan dibentuk dengan etanol dengan perbandingan 1:2, kemudian disaring dan endapan ditambahkan dengan reagen Fehling kemudian dihidrolisis dengan HCl 5% dalam etanol. Kemudian disaring dan dimasukkan kedalam desikator. Pada tahap berikutnya, galaktomanan yang diperoleh diikat silang dengan menggunakan Trinatrium Trimetafosfat dalam kondisi pH 12 dengan pemanasan pada suhu 50oC dan tanpa pemanasan. Galaktomanan ikat silang fosfat yang diperoleh diukur ketebalan filmnya, indeks
BAB 2
TINJAUAN PUSTAKA
2.1 Aren
Aren (Arenga pinnata) merupakan salah satu sumber daya alam di daerah tropis, distribusinya tersebar luas, sangat diperlukan dan mudah didapatkan untuk keperluan sehari-hari oleh masyarakat setempat sebagai sumber daya yang berkesinambungan. Di Indonesia pohon aren (Gambar 2.1) sebagian besar secara nyata digunakan untuk melengkapi kebutuhan sehari-hari (Irawan et al, 2009).
Pohon aren (Arenga pinnata) dapat tumbuh dengan baik di daerah beriklim sedang pada ketinggian 500 hingga 800 meter di atas permukaan dengan kondisi tanah yang beragam jika tidak terlalu asam dengan curah hujan 1200 mm per tahun (Iswanto, 2009).
Aren termasuk suku Arecaceae (pinang-pinangan). Sistematika tanaman aren adalah sebagai berikut :
Kingdom : Plantae (tumbuhan)
Subkingdom : Tracheobionta (tumbuhan berpembuluh) Super Divisi : Spermatophyta (menghasilkan biji) Divisi : Magnoliophyta (tumbuhan berbunga) Kelas : Liliopsida (berkeping satu/ monokotil) Sub Kelas : Arecidae
Ordo : Arecales
Famili : Arecaceae (suku pinang-pinangan) Genus : Arenga
Spesies : Arenga pinnata Merr
Aren merupakan tumbuhan biji tertutup karena biji buahnya terbungkus dengan daging buah. Daun aren majemuk menyirip seperti daun kelapa dengan panjang pelepah mencapai 5 meter dan tangkai daun mencapai 1,5 meter dengan warna hijau gelap di atas dan di sisi bawahnya berwarna keputih-putihan oleh karena adanya lapisan lilin di sisi bawahnya. Tanaman aren berkeping satu, dimana bunga jantan terpisah dari bunga-bunga betina dalam tongkol yang berbeda yang muncul di ketiak daun. Panjang tongkol dapat mencapai 2,5 meter. Buah aren berbentuk bulat peluru, dengan diameter sekitar 4 sentimeter, mempunyai tiga ruang dan memiliki tiga biji, tersusun dalam untaian seperti rantai. Setiap tandan mempunyai 10 tangkai atau lebih, dan setiap tangkai memiliki lebih kurang 50 butir buah berwarna hijau sampai cokelat kekuningan (Sunanto, 1993).
Aren merupakan tumbuhan serbaguna, dimana setiap bagian pohon aren tersebut dapat diambil manfaatnya, mulai dari akar untuk obat tradisional, batang untuk berbagai macam peralatan dan bangunan, daun muda/janur untuk pembungkus kertas rokok. Hasil produksinya juga dapat dimanfaatkan, misalnya buah aren muda diolah menjadi kolang-kaling, air nira untuk bahan pembuatan gula merah/ cuka dan pati/ tepung dalam batang untuk bahan pembuatan berbagai macam makanan (Irawan et al, 2009).
Setiap pohon dapat menghasilkan 15 liter nira per hari dengan rendemen gula 12%. Selain itu, aren juga menghasilkan ijuk rata-rata 2 kg/pohon/tahun,
kolang-kaling 100 kg/pohon/tahun, dan tepung 40 kg/pohon bila tanaman tidak
disadap niranya. Kayu aren dapat diolah menjadi mebel atau kerajinan tangan,
seperti kayu kelapa (Anonim, 2009).
2.2 Kolang-kaling
(Gambar 2.2) yang dalam bahasa Belanda biasa disebut aren palm ini, dibuat dari biji pohon aren (Arenga pinnata) yang berbentuk pipih dan bergetah
Buah aren yang masih muda besifat keras dan melekat sangat erat pada untaian buah, sedangkan buah yang sudah masak daging buahnya agak lunak. Daging buah aren yang masih muda mengandung lendir yang sangat gatal jika mengenai kulit karena lendir tersebut mengandung asam oksalat. Kolang- kaling merupakan endosperm biji buah aren yang berumur setengah masak setelah melalui proses pengolahan (Sunanto, 1993).
Untuk membuat kolang-kaling, biasanya dengan membakar buah aren sampai hangus, kemudian diambil bijinya untuk direbus selama beberapa jam. Biji yang sudah direbus tersebut kemudian direndam dengan larutan air kapur selama beberapa hari sehingga terfermentasi
menjadi lunak, kenyal, dan berwarna putih agak bening (Sunanto, 1993).
Gambar 2.1 Kolang-kaling
Selain memiliki rasa yang menyegarkan, mengkonsumsi kolang kaling juga membantu memperlancar kerja saluran cerna manusia. Kandungan karbohidrat yang dimiliki kolang kaling bisa memberikan rasa kenyang bagi orang yang mengkonsumsinya, selain itu juga menghentikan nafsu makan dan mengakibatkan konsumsi makanan jadi menurun, sehingga cocok dikonsumsi sebagai makanan diet
2.3 Polisakarida
Suatu polisakarida adalah senyawa yang mana molekul-molekulnya mengandung banyak satuan monosakarida yang dipersatukan dengan ikatan glikosida. Hidrolisis akan mengubah suatu polisakarida menjadi monosakarida (Fessenden, 1986).
Polisakarida semakin banyak diperhatikan untuk keperluan dalam industri makanan, farmasi dan kosmetik. Secara konvensional digunakan sebagai pengental dan pembuat gel. Karena struktur polihidroksi (poliol) sedemikian maka bahan ini mudah dikonsumsi oleh bakteri. Karena itu perlu modifikasi dari struktur sehingga dihasilkan suatu derivat yang dimungkinkan dengan mengurangi jumlah OH dari poliol dengan gugus organik (Kok, et al, 1999)
Susunan dan fungsi suatu polisakarida ditentukan oleh jumlah monomer gula dan posisi ikatan glikosidiknya. Polisakarida bukan pati (Non Starch Polysaccharides), terdiri atas 3 kelompok besar yakni selulosa, polimer non selulosa, dan pektik polisakarida. Polimer non selulosa ini terdiri dari arabinoxylan, glukan, mannan, galaktan, dan xyloglukan (Anonim, 2008).
2.3.1 Manan
diklasifikasikan menjadi 4 subfamili: manan, glukomanan, galaktomanan, galaktoglukomanan. Masing-masing polisakarida tersebut tersusun atas ikatan β -1-4 yang terdiri dari manosa atau kombinasi glukosa dan galaktosa. Manan dapat dihidrolisis menjadi manosa maupun manooligosakarida. Senyawa manan merupakan komponen utama dari endosperma kelapa sawit, kelapa, locust bean gum (Ceratonia siliqua) biji kopi, akar konjak (Amorphophallus konjak) (Sigres dan Sutrisno, 2013)
O
Gambar 2.3 Manan (Manosa : Manosa)
O
Gambar 2.4 Glukomannan (Glukosa : Manosa)
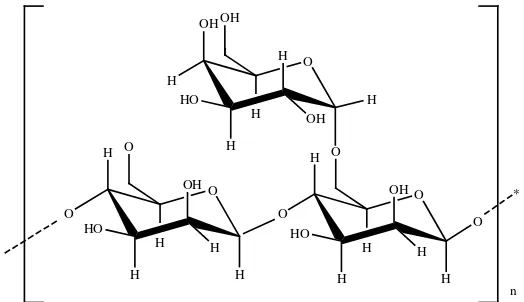
Gambar 2.5 Galaktomannan (Galaktosa : Manosa)
Gambar 2.6 Galaktoglukomannan (Glukosa : Galaktosa : Manosa)
2.4 Galaktomanan
Galaktomanan salah satu bagian dari polisakarida, yang secara khusus dihasilkan dari tanaman jenis Leguminaceae. Butiran benih, yang menghasilkan galaktomanan pada umumnya tumbuh dari tanaman legume di daerah yang semi kering di dunia. Biosintesis galaktomanan adalah proses fotosintesis yang terjadi pada banyak tanaman legum. Proses ini in vitro dikatalisis oleh enzim tertentu (Mathur, 2012). Struktur dasar yang membangun galaktomanan adalah galaktosa dan manosa (Srivastava dan Kapoor, 2005).
Polisakarida galaktomanan (Gambar 2.5) memiliki struktur umum yang linear, yang mana unit polimer (1→4)-β-D-mannopiranosa, terikat (1→6) dengan
α-D-galaktosa (Mathur, 2012). Galaktomanan dari tumbuhan yang berbeda akan menghasilkan berat molekul, rasio penyusun polisakarida (M:G), dan fungsi yang berbeda juga (Mathur, 2012).
Galaktomanan merupakan cadangan karbohidrat serta pengatur banyaknya air dalam biji selama perkecambahan. Galaktomanan juga bersifat pengental dan penstabil emulsi yang baik serta dapat mengurangi resiko masuknya racun jika digunakan sebagai bahan farmasi dan industri makanan (Stephen et al, 2006).
Galaktomanan dari masing-masing tanaman berbeda-beda pada rasio manosa dan galaktosa, distribusi galaktosa pada rantai manosa dan berat molekulnya. Rasio rantai manosa dan galaktosa pada umumnya berkisar pada 1,1-5,0 (Srivastava dan Kapoor, 2005). Sifat fisikokimia galaktomanan dapat dikarakterisasi dengan menggunakan beberapa peralatan dan teknik yang berbeda. Parameter-parameter yang penting dalam karakterisasi galaktomanan adalah perbandingan manosa dan galaktosa, rata-rata berat molekul, bentuk struktur, dan viskositas intrinsiknya (Cerqueira et al, 2009).
Galaktomanan dengan rasio galaktosa yang besar umumnya mudah larut dalam air dan kecenderungannya untuk membentuk gel sangat rendah dibandingkan galaktomanan dengan rasio galaktosa yang rendah. Kelarutan yang sangat tinggi tersebut disebabkan oleh banyaknya rantai cabang sehingga rantai manosa menjadi sukar untuk berinteraksi secara intermolekuler (Srivastava dan Kapoor, 2005).
Tabel 2.1 menunjukkan beberapa jenis galaktomanan komersial dari beberapa tanaman dan rasio antara manosa dan galaktosa.
Tabel 2.1 Jenis Galaktomanan Komersial
Galaktomanan Sumber Tanaman Rasio M:G
Guar Gum Guar Plant 2 : 1 Fenugreek Gum Fenugreek Plant 1 : 1 Locust bean gum Carob Tree 4 : 1 Tara gum Tara shrub 3 : 1 Cassia tora gum Cassia tora 5 : 1 Daincha gum Sesbania bisipinosa 2 : 1
Galaktomanan yang diperoleh dari masing-masing tanaman yang berbeda memiliki kadar yang berbeda, misalnya galaktomanan yang diperoleh dari ampas kelapa sebesar 20% (Zultiniar dan Casoni, 2009), pada kolang-kaling 4,58% (Tarigan, 2012), sedangkan pada Fenugreek kadar galaktomanan yang diperoleh berkisar 25-30% (Mathur dan Mathur, 2005).
Kelebihan dari galaktomanan jika dibandingkan dengan jenis polisakarida yang lain adalah kemampuannnya untuk membentuk suatu larutan yang kental dalam kondisi konsentrasi yang sangat rendah, dan hanya sedikit dipengaruhi pH, kekuatan ionik dan pemanasan. (Anonim, 2008). Viskositas galaktomanan sangat konstan sekali pada kisaran pH 1-10,5 yang kemungkinan disebabkan oleh karakter molekulnya yang bersifat netral (Cerqueira et al, 2009). Namun dengan suhu yang tinggi, dan kondisi yang sangat asam atau basa, galaktomanan dapat terdegradasi (Anonim, 2008).
Saat ini konsumsi galaktomanan sangat bervariasi tergantung pada penggunaannya. Menurut salah satu estimasi sekitar 90-100 ribu ton dipakai pertahun. Pemakaian terbesar adalah guar gum dengan 70-80 ribu ton, locust bean gum dengan 12-14 ribu ton. Pemakaian galaktomanan bermanfaat untuk pembentukan viskositas yang sangat baik dan juga penggunaannya untuk penyerapan air atau pembentukan ikatan hidrogen membentuk formasi gel (Kok et al, 1999).
Pada industri makanan, galaktomanan biasa dipakai sebagai penggumpal. Pada industri es krim, galaktomanan juga digunakan untuk membuat es agar tidak cepat mencair (Zultiniar dan Casoni, 2009). Selain itu, galaktomanan juga digunakan oleh industri pembuatan keju (Cerqueira et al, 2010), kalengan, dan bumbu salad (Zultiniar dan Casoni, 2009).
2.5 Galaktomanan dari Kolang-Kaling
Salah satu sumber galaktomanan adalah kolang kaling, dimana saat ini pemanfaatannya masih sangat terbatas. Galaktomanan merupakan polisakarida terbesar di dalam kolang-kaling. Kolang-kaling yang digunakan untuk ekstraksi galaktomanan berbentuk lonjong agak pipih, berwarna putih agak bening, dan kenyal.
Galaktomanan dari kolang-kaling memiliki aktivitas antioksidan sehingga dapat digunakan dalam aplikasi kehidupan manusia. Sifat antioksidan galaktomanan kolang-kaling ditentukan dengan menggunakan metoda DPPH dan menggunakan spektrofotometer ultra violet, pada bilangan gelombang maksimum 515 nm. Galaktomanan dari kolang-kaling diperoleh sebesar 4,58 % melalui proses ekstraksi pada kondisi netral dengan mengunakan pelarut etanol. Perbandingan galaktosa dan mannosa pada galaktomanan dari kolang-kaling adalah 1 : 1,331.
Komponen kimia yang terdapat pada hasil ekstraksi kolang-kaling adalah protein 0,261%, galaktomanan 90,57 %, serat kasar 8,05%, dan lemak 0,101 %. Galaktomanan dari kolang-kaling berbentuk serbuk putih, memiliki sifat viskositas yang cukup besar dalam konsentrasi yang rendah (Tarigan, 2012).
2.6 Ikat Silang
Ikat silang merupakan metode lain yang dapat digunakan untuk memodifikasi polisakarida selain asetilasi. Prinsip dengan menggunakan metode ikat silang hampir sama dengan metode asetilasi yaitu sama-sama mengganti gugus OH- dengan gugus fungsi yang lain. Pada metode ikat silang gugus OH- diganti dengan gugus eter, gugus ester, atau gugus fosfat.
Raina et al, 2006, menjelaskan keuntungan dari penggunaan metode ikat silang adalah dapat menghasilkan suatu pati dengan kemampuan mengembang yang rendah dimana hal ini akan memperkuat granula pati dan menjadikan pati lebih tahan terhadap medium asam dan panas sehingga tidak mudah pecah pada saat pemanasan. Selain itu metode ikat silang dapat meningkatkan tekstur, viskositas, kejernihan pasta (paste clarity), kekuatan gel (gel strength), dan sifat adhesif pati. Disisi lain, metode ini memiliki kekurangan yaitu dapt menurunkan
solubility, sediment volume, gel elasticity, dan freeze-thaw stability dari polisakarida.
Beberapa jenis zat pengikat silang yang dapat dipakai adalah Mononatrium Fosfat, Natrium Trimetafosfat, Natrium Tripolifosfat, Epichlorohydrin, dan
Phosphoryl Cloride (Mao Gui-Jie, 2006).
Reaksi ikat silang pada umumnya dipengaruhi oleh ukuran bahan pengikat silang. Jika ukuran molekul pengikat silang semakin kecil, maka reaksi ikat silang akan semakin cepat, karena proses difusi dalam larutan semakin mudah.
Interaksi antara grup yang bermuatan positif dari bahan pengikat silang dan grup yang bermuatan negatif dari galaktomanan menunjukan adanya interaksi yang bersifat ionik. Sifat dari hasil ikat silang tergantung dari sifat pengikat silang (Rana et al, 2011).
2.7 Galaktomanan Ikat Silang
peningkatan sifat fisika seperti kelarutannya didalam air, viskositas dan kemurniannya dibanding dengan yang aslinya (Kok et al, 1999).
Modifikasi kimia pada galaktomanan pada umumnya untuk mengurangi sifat mengembangnya (swelling). Modifikasi galaktomanan, seperti guar gum, masih dikembangkan dengan mereaksikan guar gum dengan senyawa fosfat,
borax, glutaraldehida, dan enzim pendegradasi (Kabir et al., 2000).
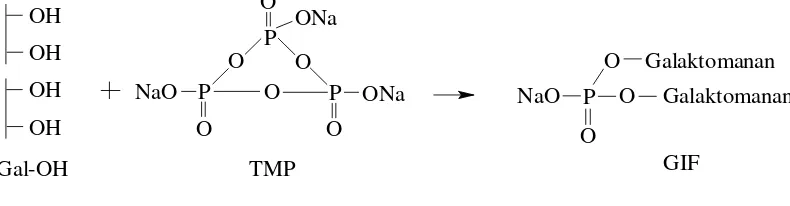
Salah satu pengikat silang dari senyawa fosfat adalah Trinatrium Trimetafosfat yang digunakan untuk mereduksi sifat mengembang guar gum. Trinatrium Trimetafosfat merupakan suatu pengikat silang yang tidak bersifat racun. Pada pH basa, senyawa kompleks ester di-polimer fosfat dibentuk dari
guar gum dan Trinatrium Trimetafosfat yang mengalami reaksi ikat silang (Gambar 2.7). Sifat mengembang pada polimer yang terikat silang menurun secara jelas (29-35 kali lipat) (Gowda et al, 2012).
Gambar 2.7 Reaksi Galaktomanan Ikat Silang
C
Guar Borate Ion Guar Cross-linked
Gambar 2.8 Reaksi galaktomanan dan ion borat
Pada reaksi ini, akan terbentuk gel dengan penambahan senyawa borat pada galaktomanan dan larutan alkali untuk membentuk suasana alkali, dengan pH optimum diantara 7,5-10,5. Sifat dari gel yang terbentuk berdasarkan jenis galaktomanan dan konsentarasi senyawa borax yang digunakan (Chudzikowski, 1971).
Glutaraldehida juga telah digunakan secara luas untuk proses ikat silang polimer yang mengandung gugus hidroksil. Telah diketahui bahwa dengan peningkatan konsentrasi glutaraldehida maka terjadi peningkatan densitas hasil ikat silang dan penurunan kemampuan mengembang pada larutan penyangga. Jika jumlah glutaraldehida yang digunakan untuk reaksi ikat silang makin tinggi maka efisiensi ikat silang rendah. Glutaraldehida merupakan pengikat silang yang bersifat racun, tetapi sifat racun itu dapat direduksi secara signfikan setelah proses ikat silang (Kabir et al,1998).
Sifat dari galaktomanan ikat silang tergantung dari densitas pengikat silang yang digunakan, yaitu perbandingan mol bahan pengikat silang dan mol dari unit polimer yang berulang. Selain itu, nilai kritis dari ikat silang yang terjadi per rantai diperlukan untuk membentuk suatu jaringan polimer.
Galaktomanan ikat silang saat ini semakin dikembangkan sebagai bahan yang digunakan untuk membawa obat ke bagian usus yang bermasalah. Kemampuan mengembang dari suatu galaktomanan di dalam cairan gastrointestinal menurun dari 100-200 kali menjadi 10-35 kali tergantung jumlah bahan pengikat silang yang digunakan. Galaktomanan akan kehilangan sifat non-ioniknya disebabkan oleh proses ikat silang dan menjadi bermuatan negatif (Rana
BAB 3
METODOLOGI PENELITIAN
3.1 Alat-alat
Alat-alat yang digunakan dalam penelitian ini adalah :
- Gelas Erlenmeyer 1000 ml Pyrex - Gelas Erlenmeyer 250 ml Pyrex
- Corong Pyrex
- Gelas Beaker 1000 ml Pyrex - Gelas Beaker 500 ml Pyrex - Gelas Ukur 100 ml Pyrex - Gelas Ukur 25 ml Pyrex - Neraca Analitis Shimadzu
- Blender National Super
- Magnetik Bar - Kain Kasa - Botol Akuades
- Sentrifugator Hitachi
- Tabung Reaksi Pyrex
- Batang Pengaduk
- Hotpate Stirer Ika
- Termometer 360oC Fissons - Plat Kaca 13x13 cm
- Spektrofotometer FT-IR Perkin Elmer - Scanning Electron Microscope Hitachi
- Oven Blower Memmert
- Alat uji kuat tarik Gotech AI-7000 M - Desikator
- Spatula - Pipet Tetes - Teflon - Gunting
- Indikator Universal p.a E’ Merck
3.2 Bahan-bahan
- Kolang-kaling - Air Suling
- Etanol p.a E’ Merck
- Air Terde-ionisasi Hach
- Fehling A p.a E’ Merck
- Fehling B p.a E’ Merck
- HCl 37% p.a E’ Merck
- Trinatrium Trimetafosfat Aldrich
- NaOH p.a E’ Merck
3.3 Prosedur Penelitian
3.3.1 Ekstraksi Galaktomanan dari Kolang-Kaling
Sebanyak 20 gram kaling dibersihkan dan di rajang. Kemudian kolang-kaling dihaluskan dengan blender selama ± 3-5 menit dengan penambahan air suling sebanyak 250 ml, dan disimpan dalam lemari pendingin selama 24 jam. Kemudian disentrifugasi pada kecepatan rata-rata 9500 rpm selama 15 menit. Supernatan ditambahkan etanol 96% dengan perbandingan volume 1:2, kemudian disimpan dalam lemari pendingin selama 24 jam. Disaring endapan kemudian ditambahkan reagen Fehling A dan Fehling B. Endapan disaring kembali, dilarutkan dengan air suling dan dihidrolisis dengan HCl 5% dalam etanol. Endapan yang terbentuk disaring dan dicuci dengan air suling dan etanol 96% kemudian disaring dan direndam dengan etanol p.a. Endapan disaring dan dikeringkan didalam desikator.
3.3.2 Pembuatan Larutan Trinatrium Trimetafosfat
3.3.3 Pembuatan Galaktomanan Ikat Silang Fosfat (GIF)
3.3.3.1 Pembuatan Galaktomanan Ikat Silang Fosfat (GIF) Tanpa Pemanasan
Sebanyak 100 ml air suling dimasukkan kedalam gelas Erlenmeyer. Kemudian ditambahkan 0,75 gram galaktomanan secara perlahan selanjutnya ditambahkan NaOH 2M secara perlahan-lahan hingga pH 12. Campuran diaduk hingga galaktomanan larut. Ditambahkan larutan 0,75 gram Trinatrium Trimetafosfat secara perlahan-lahan (perbandingan galaktomanan : Trinatrium Trimetafosfat = 1:1 (GIF 1A)). Kemudian diaduk selama 8 jam. Dituang kedalam plat kaca yang berukuran 13 x 13 cm. Dikeringkan di dalam oven blower pada suhu 45oC selama 18 jam. Selanjutnya film dicuci dengan air suling dan dikeringkan kembali. Film dilepaskan dari plat secara perlahan-lahan kemudian dimasukkan kedalam wadah tertutup hingga digunakan selanjutnya. Dengan prosedur yang sama dilakukan untuk perbandingan galaktomanan : Trinatrium Trimetafosfat = 1:2 (GIF 2A); 1:3 (GIF 3A); dan 1:4 (GIF 4A). Galaktomanan ikat silang fosfat yang terbentuk diukur ketebalan, kuat tarik dan kemulurannya, dianalisis perubahan gugus fungsi dengan spektrofotometer FT-IR dan morfologi permukaan dengan SEM (Scanning Electron Microscopic).
3.3.3.2 Pembuatan Galaktomanan Ikat Silang Fosfat (GIF) dengan Pemanasan pada Suhu 50oC
suhu 45oC selama 18 jam. Kemudian film dicuci dengan air suling dan dikeringkan kembali. Film dilepaskan dari plat kaca secara perlahan-lahan kemudian dimasukkan kedalam wadah tertutup hingga digunakan selanjutnya. Dengan prosedur yang sama dilakukan untuk perbandingan galaktomanan : Trinatrium Trimetafosfat = 1:2 (GIF 2B); 1:3 (GIF 3B); dan 1:4 (GIF 4B). Galaktomanan ikat silang fosfat yang terbentuk diukur ketebalan, kuat tarik dan kemulurannya, kemudian dianalisis perubahan gugus fungsi dengan spektrofotometer FT-IR.
3.3.4 Uji Sifat Mengembang (Swelling)
Galaktomanan ikat silang fosfat digunting dengan ukuran 3 x 3 cm. Kemudian ditimbang beratnya dan dimasukkan kedalam gelas Beaker yang telah berisi 20 ml NaCl 0,9%. Dihitung waktunya selama 30 menit hingga film mengalami pengembangan. Diangkat film yang masih basah dan ditimbang dalam keadaan basah. Dengan prosedur yang sama dilakukan uji sifat mengembang (swelling) didalam 20 ml air suling.
3.3.5 Uji Ketebalan Film Galaktomanan Ikat Silang Fosfat
Ketebalan film diukur dengan mikrometer sekrup digital. Lima bagian yang berbeda diukur ketebalannya masing- masing. Nilai ketebalan film diperoleh dari perhitungan rata-rata 5 data pengukuran tersebut.
3.3.6 Pengukuran Kekuatan Tarik dan Kemuluran Dengan Uji Kuat Tarik
3.4 Bagan Penelitian
3.4.1 Ekstraksi Galaktomanan dari Kolang-Kaling
20 gram Kolang-Kaling
dicuci hingga bersih dirajang
dihaluskan dengan blender selama 3-5 menit dengan penambahan air suling sebanyak 250 ml
disimpan didalam lemari pendingin selama 24 jam
disentrifugasi dengan kecepatan rata-rata 9500 rpm selama 15 menit
Endapan Supernatan
ditambahkan etanol 96% dengan perbandigan 1:2 disimpan didalam lemari pendingin selama 24 jam disaring
Endapan
ditambahkan reagen Fehling A dan Fehling B disaring
Filtrat Endapan
dilarutkan dengan air suling
dihidrolisis dengan HCl 5% dalam etanol disaring
Endapan
3.4.2 Pembuatan Larutan Trinatrium Trimetafosfat
0,75 gram Trinatrium Trimetafosfat
dimasukkan kedalam beaker Glass
diaduk hingga homogen
Hasil
ditambahkan 10 ml air terde-ionisasi
Dilakukan prosedur yang sama dengan variasi jumlah Trinatrium Trimetafosfat 1,5 gram; 2,25 gram; dan 3,0 gram.
3.4.3 Pembuatan Galaktomanan Ikat Silang Fosfat (GIF)
3.4.3.1 Pembuatan Galaktomanan Ikat Silang Fosfat (GIF 1A) Tanpa Pemanasan
0,75 gram Galaktomanan
dimasukkan kedalam gelas Erlenmeyer dimasukkan 100 ml air suling
ditambahkan NaOH 2M secara perlahan-lahan hingga pH 12 diaduk hingga homogen
ditambahkan larutan 0,75 gram Trinatrium Trimetafosfat diaduk selama 8 jam
dituang kedalam plat kaca yang berukuran 13x13 cm
dikeringkan didalam oven blower pada suhu 45oC selama 18 jam dicuci dengan air suling
dikeringkan
dilepaskan dari plat secara perlahan-lahan Hasil
SEM FT-IR
3.4.3.2 Pembuatan Galaktomanan Ikat Silang Fosfat (GIF 1B) dengan Pemanasan pada Suhu 50oC
0,75 gram Galaktomanan
dimasukkan kedalam Erlenmeyer
dimasukkan 100 ml air suling
ditambahkan NaOH 2M secara perlahan-lahan hingga pH 12
diaduk hingga homogen
ditambahkan larutan 0,75 gram Trinatrium Trimetafosfat
diaduk selama 8 jam
dituang kedalam plat kaca yang berukuran 13x13 cm
dikeringkan didalam oven blower pada suhu 45oC selama 18 jam
dicuci dengan air suling
dikeringkan
dilepaskan dari plat secara perlahan-lahan
Hasil
dipanaskan pada suhu 50oC dipanaskan pada suhu 50oC
FT-IR
Dengan prosedur yang sama dilakukan untuk perbandingan galaktomanan : Trinatrium Trimetafosfat = 1:2 (GIF 2B); 1:3 (GIF 3B); dan 1:4 (GIF 4B).
3.3.4 Uji Ketebalan Film Galaktomanan Ikat Silang Fosfat
Galaktomanan Ikat Silang Fosfat
diukur ketebalan pada lima bagian yang berbeda dengan mikrometer sekrup digital
dihitung rata-rata ketebalan
3.3.5 Uji Sifat Mengembang (Swelling)
Dengan prosedur yang sama dilakukan uji sifat mengembang (swelling) di dalam air suling.
3.3.6 Pengukuran Kekuatan Tarik dan Kemuluran Dengan Uji Kuat Tarik
Galaktomanan Ikat Silang Fosfat
digunting dengan ukuran 5,2 x 1,6 cm
diuji kuat tarik dan kemuluran dengan alat kuat tarik Gotech AI-7000M
dihitung nilai kuat tarik dan kemuluran
Hasil
Galaktomanan Ikat Silang Fosfat
digunting dengan ukuran 3 x 3 cm ditimbang
dimasukkan kedalam Beaker gelas yang telah berisi 20 ml NaCl 0,9% dihitung waktunya selama 30 menit hingga film mengalami pengembangan (swelling)
diangkat film yang masih basah ditimbang dalam keadaan basah
BAB 4
HASIL DAN PEMBAHASAN
4.1 Hasil
4.1.1 Hasil Ekstraksi Dari Kolang-Kaling
Dari 700 gram kolang-kaling setelah diekstraksi dan dimurnikan, endapannya sampai diperoleh padatan berwarna putih dan dikeringkan maka didapat hasilnya sebanyak 9,9013 gram.
% Galaktomanan = 9,9013
700 x 100% = 1,4 %
4.1.2 Hasil Dari Spektroskopi Inframerah
4.1.2.1 Hasil Analisis Gugus Fungsi Galaktomanan dengan Spektrofotometer FT-IR
Tabel 4.1 Hasil Analisis Gugus Fungsi Galaktomanan dengan Spektrofotometer FT-IR
Gugus Fungsi Frkuensi (cm-1)
(a) vibrasi streching O-H 3234,54
(b) vibrasi streching -CH sp3 2917,49
(c) vibrasi bending O-H 1646,86
(d) vibrasi bending -CH sp3 1348,58
(e) vibrasi streching -CO dari C-OH 1053,39
4.1.2.2 Hasil Analisis Gugus Fungsi Galaktomanan Ikat Silang Fosfat (GIF) Tanpa Pemanasan dengan Spektrofotometer FT-IR
Hasil analisis galaktomanan ikat silang fosfat dari senyawa galaktomanan yang telah diikat silang dengan Trinatrium Trimetafosfat dengan waktu reaksi 8 jam, pada bilangan gelombang 4000-650 cm-1 ditunjukan pada Tabel 4.2.
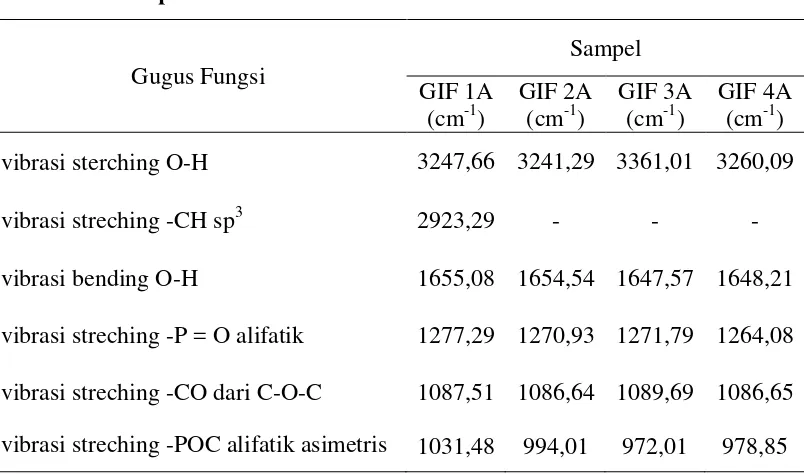
Tabel 4.2 Hasil Analisis Gugus Fungsi GIF (Tanpa Pemanasan) dengan Spektrofotometer FT-IR
Gugus Fungsi
Sampel GIF 1A
(cm-1)
GIF 2A (cm-1)
GIF 3A (cm-1)
GIF 4A (cm-1) vibrasi sterching O-H 3247,66 3241,29 3361,01 3260,09
vibrasi streching -CH sp3 2923,29 - - -
vibrasi bending O-H 1655,08 1654,54 1647,57 1648,21
vibrasi streching -P = O alifatik 1277,29 1270,93 1271,79 1264,08
vibrasi streching -CO dari C-O-C 1087,51 1086,64 1089,69 1086,65
4.1.2.3 Hasil Analisis Gugus Fungsi Galaktomanan Ikat Silang Fosfat (GIF) (Pemanasan pada Suhu 50oC ) dengan Spektrofotometer FT-IR
Hasil analisis gugus fungsi senyawa galaktomanan yang telah diikat silang dengan Trinatrium Trimetafosfat dengan perbandingan galaktomanan dan Trinatrium Trimetafosfat 1:3 (GIF 3B) selama 8 jam, dengan kecepatan 1000 rpm dan dalam pemanasan pada suhu 50oC pada bilangan gelombang 4000-650 cm-1 ditunjukkan pada Tabel 4.3.
Tabel 4.3 Hasil Analisis Gugus Fungsi GIF (Pemanasan pada Suhu 50oC) dengan Spektrofotometer FT-IR
Gugus Fungsi
Sampel
GIF 3A (cm-1)
GIF 3B (cm-1) vibrasi sterching O-H 3361,01 3309,46
vibrasi bending O-H 1647,57 1556,11
vibrasi streching -P = O alifatik 1271,79 1277,91
vibrasi streching -CO dari C-O-C 1089,69 1098,82 vibrasi streching -POC alifatik asimetris 972,01 950,79
4.1.3 Hasil Analisis Morfologi Permukaan GKK dan GIF dengan SEM (Scanning Electron Microscopic)
A B
Gambar 4.1 Hasil SEM dari A. Galaktomanan; B. Galaktomanan Ikat Silang Fosfat (1:3)
4.1.4 Hasil Uji Sifat Mengembang (Swelling)
Uji sifat mengembang (swelling) dilakukan pada galaktomanan dan galaktomanan ikat silang fosfat dengan waktu 30 menit. Pengukuran derajat swelling dapat dihitung melalui rumus :
� = Wg−Wo
Wo � 100 %
dimana :
Wg = Berat sampel yang konstan didalam medium Wo = Berat sampel awal
Gambar 4.2 Histogram Derajat Swelling Galaktomanan dan Galaktomanan Ikat Silang Pospat Tanpa Pemanasan
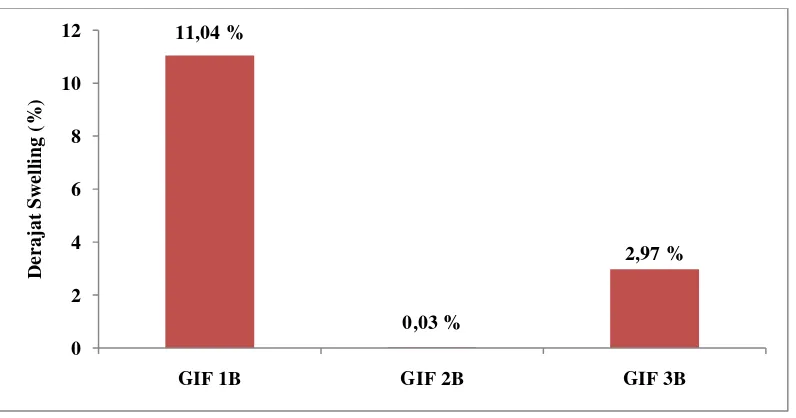
Gambar 4.3 Histogram Derajat Swelling Galaktomanan Ikat Silang Fosfat dengan Pemanasan dalam Suhu 50oC
0 %
Galaktomanan GIF 1A GIF 2A GIF 3A GIF 4A
Hasil pengukuran derajat swelling di dalam NaCl 0,9 % dapat dilihat pada Gambar 4.4 dan Gambar 4.5.
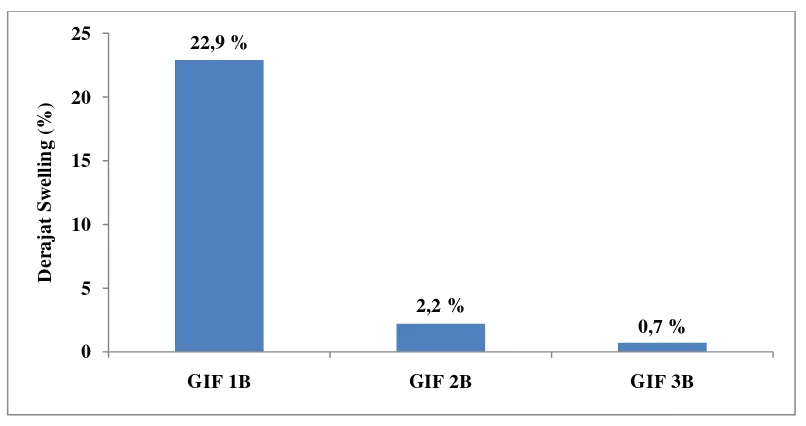
Gambar 4.4 Histogram Derajat Swelling Galaktomanan dan Galaktomanan Ikat Silang Fosfat Tanpa Pemanasan
Gambar 4.5 Histogram Derajat Swelling Galaktomanan Ikat Silang Fosfat dengan Pemanasan dalam Suhu 50oC
Galaktomanan GIF 1A GIF 2A GIF 3A GIF 4A
4.1.5 Hasil Pengukuran Ketebalan Film
Pengukuran ketebalan film dilakukan pada lima titik yang diukur secara acak dan dihitung rata-rata ketebalan film. Hasilnya dapat dilihat pada Tabel 4.4.
Tabel 4.4 Hasil Pengukuran Ketebalan Film
Parameter
Sampel
GKK GIF 1A
GIF 2A
GIF 3A
GIF 4A
GIF 1B
GIF 2B
GIF 3B
Ketebalan 0,05 0,08 0,1 0,12 0,41 0,09 0,22 0,15
4.1.6 Hasil Uji Kekuatan Tarik dan Kemuluran Film
Tabel 4.5 Hasil Uji Kekuatan Tarik dan Kemuluran Film
Sampel
Parameter
Max Load (Kgf)
Stroke (mm)
Kekuatan Tarik (Mpa)
Kemuluran (%)
GKK 0,11 0,391 1,347 0,751
GIF 1A 0,22 6,229 1,684 11,97
GIF 2A 1,59 4,593 9,714 8,83
GIF 3A 1,78 5,410 9,080 10,40
GIF 4A 0,18 1,875 0,268 3,61
GIF 1B 0,28 7,463 1,095 14,35
GIF 2B 0,30 2,509 0,835 4,825
GIF 3B 0,37 1,062 1,510 2,642
4.2 Pembahasan
4.2.1 Hasil Ekstraksi Galaktomanan dari Kolang-Kaling
Ekstraksi galaktomanan dari 700 gram galaktomanan diperlukan sekitar 9,9013 gram (1,4%). Pada ekstraksi ini, galaktomanan dimurnikan dengan menggunakan reagen Fehling, dimana galaktomanan akan mengendap dalam bentuk senyawa kompleks Cu2+ yang berwarna biru dan kemudian dihidrolisis dengan menggunakan HCl 5% dalam etanol yang membuat galaktomanan terbentuk kembali.
Hal ini disebabkan tahapan proses ekstraksi yang dilakukan lebih banyak yakni adanya penambahan reagen Fehling yang memungkinkan adanya galaktomanan yang larut pada tahapan tersebut.
4.2.2 Ikat Silang Galaktomanan dengan Trinatrium Trimetafosfat
Hasil ikat silang galaktomanan dengan Trinatrium Trimetafosfat berupa lapisan tipis (film) galaktomanan ikat silang fosfat yang disintesis selama 8 jam dalam pemanasan pada suhu 50oC dan tanpa pemanasan. Reaksi ikat silang antara galaktomanan dan Trinatrium Trimetafosfat secara sederhana dapat dilihat pada Gambar 4.6.
4.2.3 Hasil Analisis GKK dan GIF dengan Spektrofotometer FT-IR
Galaktomanan yang dianalisis dengan spektrofotometer FT-IR (Gambar 4.7) menghasilkan pita serapan pada bilangan gelombang cm-1 yang menunjukkan adanya vibrasi streching gugus O-H yang didukung oleh pita serapan pada bilangan gelombang 1646,86 cm-1 yang menunjukan vibrasi bending O-H atau gugus O-H yang terikat dengan air. Pita serapan pada bilangan gelombang 2917,49 cm-1 menunjukan adanya vibrasi streching C-H sp3 yang didukung oleh pita serapan pada bilangan gelombang 1348,58 cm-1 yang menunjukan adanya vibrasi bending C-H sp3. Pita serapan pada bilangan gelombang 1053,39 cm-1 menunjukan adanya vibrasi streching C-O pada ikatan C-OH (Stuart, 2004).
Gambar 4.7 Spektrum FT-IR dari Galaktomanan
Untuk membuktikan ikat silang fosfat pada galaktomanan, pada spektrum FT-IR (Gambar 4.8) muncul pita serapan pada bilangan gelombang 1280-1260 cm-1 yang menunjukan adanya gugus P = O alifatik yang didukung oleh pita serapan pada bilangan gelombang 1050-950 cm-1 yang menunjukkan adanya gugus P-O-C asimetrik (Stuart, 2004). Hal ini juga dapat dilihat dari hasil spektrum FT-IR galaktomanan (Gambar 4.7) dan hasil spektrum FT-IR galaktomanan ikat silang fosfat (GIF) (Gambar 4.8), menunjukkan terjadinya
1646,86
3234,54
2917,49
1348,58
perubahan nilai absorbansi pada masing-masing spektrum, dimana makin besar jumlah Trinatrium Trimetafosfat yang ditambahkan, maka nilai absorbansi akan semakin kecil dan persen (%) transmitansi makin besar. Ini menunjukkan bahwa proses ikat silang galaktomanan dengan senyawa Trinatrium Trimetafosfat telah terbentuk.
Gambar 4.8 Spektrum FT-IR Galaktomanan Ikat Silang Fosfat
Keterangan : Waktu reaksi = 8 jam
Perbandingan Galaktomanan dan Trinatrium Trimetafosfat = 1:1 Perbandingan Galaktomanan dan Trinatrium Trimetafosfat = 1:2 Perbandingan Galaktomanan dan Trinatrium Trimetafosfat = 1:3 Perbandingan Galaktomanan dan Trinatrium Trimetafosfat = 1:4
4000 3500 3000 2500 2000 1500 1000
Bila dibandingkan hasil spektrum FT-IR galaktomanan ikat silang fosfat tanpa pemanasan dan galaktomanan ikat silang fosfat dengan pemanasan pada suhu 50oC, menunjukkan bahwa nilai absorbansi gugus OH tidak jauh berbeda, sehingga faktor pemanasan tidak cukup potensial untuk meningkatkan ikat silang fosfat.
Gambar 4.9 Spektrum FT-IR Galaktomanan Ikat Silang Fosfat
Keterangan : Waktu reaksi = 8 jam Kecepatan pengadukan = 1000 rpm
GIF 3A
GIF 3B :
:
Perbandingan Galaktomanan dan Trinatrium Trimetafosfat = 1:3 tanpa pemanasan.
Perbandingan Galaktomanan dan Trinatrium Trimetafosfat = 1:3 dengan pemanasan pada suhu 50oC.
4000 3500 3000 2500 2000 1500 1000
950,79 1098,82
1277,91 1556,11
972,01 1089,69
1271,79 1647,57 3361,01
3309,46
GIF 3B GIF 3A
%T
4.2.4 Hasil Uji Morfologi Permukaan GKK dan GIF dengan SEM (Scanning Electron Microscopic)
Berdasarkan hasil uji SEM (Scanning Electron Microscpic), galaktomanan (Gambar 4.4 A) dan galaktomanan ikat silang fosfat (Gambar 4.4 B) menunjukkan telah terjadi perubahan morfologi permukaan.Pada GKK bentuk permukaan halus sedangkan bentuk permukaan galaktomanan ikat silang fosfat kasar dan bergelombang. Ini menunjukkan perubahan morfologi yang mendukung telah terjadinya ikat silang fosfat antara galaktomanan dan Trinatrium Trimetafosfat.
4.2.5 Hasil Uji Sifat Mengembang (Swelling)
Pengukuran derajat kemampuan mengembang (swelling), masing-masing dilakukan dengan perendaman selama 30 menit di dalam 20 ml air suling dan 20 ml larutan NaCl isotonik atau NaCl 0,9 %. Hasil pengukuran derajat swelling
yang diperoleh dapat dilihat pada Gambar 4.2, Gambar 4.3, Gambar 4.4 dan Gambar 4.5.
NaCl isotonik merupakan cairan yang memiliki kepekatan (osmolaritas) yang mendekati dengan komponen cairan di dalam darah. Dapat dilihat bahwa hasil derajat swelling yang dilakukan dalam air suling lebih besar dibandingkan dengan hasil derajat swelling yang dilakukan di dalam NaCl isotonik. Hal ini dikarenakan kekuatan ionik dari larutan NaCl isotonik akan menurunkan tekanan osmotik dalam film galatomanan dan galaktomanan ikat silang fosfat (Kabir et al, 2000), sehingga waktu untuk mengembang dalam larutan NaCl isotonik lebih lama dibandingkan di dalam air suling.
GIF 2A dan GIF 2B-GIF 3B di dalam air suling; galaktomanan-GIF 2A di dalam NaCl 0,9 %, memiliki derajat swelling yang semakin meningkat. Hal ini disebabkan oleh rantai lurus dalam polimer galaktomanan yang meningkatkan masuknya air ke dalam jaringan polimer. Derajat swelling meningkat sampai konsentrasi Trinatrium Trimetafosfat cukup tinggi menyebabkan jaringan rusak oleh proses ikat silang (Kabir et al, 2000).
4.2.6 Hasil Pengukuran Ketebalan Film
Hasil pengukuran ketebalan film diperoleh dari 0,05-0,22 mm. Dari hasil pengukuran ketebalan film yang telah dilakukan dapat diketahui bahwa semakin banyak jumlah Trinatrium Trimetafosfat yang dicampur dengan galaktomanan yang berjumlah sama, maka ketebalan film akan semakin meningkat. Hal ini disebabkan karena volume campuran semakin meningkat.
4.2.7 Hasil Uji Kekuatan Tarik dan Kemuluran Film
Kekutan tarik/ daya rengang adalah kemampuan suatu bahan untuk tahan dibawah suatu gaya tekanan hingga putus. Kemuluran/ elongasi adalah peningkatan persentasi perpanjangan yang terjadi pada suatu bahan dibawah tekanan hingga putus (Sperling, 2006).
Hasil uji kekuatan tarik dan kemuluran dapat dilihat pada Tabel 4.5 dan perhitungannya dapat dilihat pada lampiran 2. Dari hasil yang diperoleh dapat dilihat bahwa dengan peningkatan jumlah Trinatrium Trimetafosfat yang dicampur dengan galaktomanan, maka kekuatan tarik akan semakin meningkat dan persentase kemuluran akan semakin kecil.
Trinatrium Trimetafosfat, maka nilai kekuatan tarik akan semakin meningkat dan persentase kemuluran akan semakin menurun.
Namun pada pada film GIF 2A-GIF 4A dan GIF 1B-GIF 2B terjadi penurunan kekuatan tarik dan persentase kemuluran yang naik-turun. Hal ini disebabkan proses ikat silang yang tidak sempurna antara galaktomanan dan Trinatrium Trimetafosfat, dimana rantai polimer linier galaktomanan tidak berinteraksi secara merata dengan peningkatan jumlah Trinatrium Trimetafosfat dalam proses ikat silang. Berbeda dengan yang diteliti oleh Kabir et al, 2000., yang menggunakan guar gum sebagai bahan dasar film dan Trinatrium Trimetafosfat sebagai bahan pengikat silang. Kabir et al, 2000., menyatakan semakin meningkatnya konsentrasi Trinatrium Trimetafosfat, maka kekuatan tarik akan semakin meningkat dan kemuluran akan semakin menurun.
BAB 5
KESIMPULAN DAN SARAN
5.1 Kesimpulan
1. Galaktomanan ikat silang fosfat disintesis melalui reaksi antara galaktomanan dengan Trinatrium Trimetafosfat sebagai bahan pengikat silang tanpa pemanasan dan dengan pemanasan pada suhu 50oC dalam kondisi pH 12 dengan penambahan NaOH 2M.
2. Terbentuknya ikat silang fosfat dengan pemanasan pada suhu 50oC dan tanpa pemanasan didukung oleh :
a. hasil analisis spektrofotometer FT-IR yang menunjukkan munculnya gugus fungsi P=O alifatik pada daerah bilangan gelombang 1280-1260 cm-1 dan gugus fungsi P-O-C asimetrik pada daerah bilangan gelombang 1050-950 cm-1,
b. hasil analisis SEM (Scanning Electron Microscopic) yang menunjukkan perubahan morfologi permukaan yang kasar dan bergelombang,
c. hasil analisis sifat mekanik yang menunjukkan peningkatan ketebalan film
dari 0,05 (GKK), menjadi 0,08-0,41 mm (GIF A) dan 0,09-0,15 mm (GIF B), kekuatan tarik yang diperoleh sebesar 1,347 Mpa GKK;
1,684-0,268 Mpa GIF A; 1,095-1,510 Mpa GIF B, kemuluran yang diperoleh 0,751% GKK, 11,97-3,61% GIF A; 14,35-2,642% GIF B,
5.2 Saran
Diharapkan peneliti selanjutnya meneliti sifat swelling dari setiap film galaktomanan ikat silang fosfat karena waktu untuk swelling dalam penelitian ini
DAFTAR PUSTAKA
Anonim, 2009, Aren Sumber Alternatif, Warta Penelitian dan Pengembangan Pertanian,31, 2.
Anonim, 2008, A Glimpse of Galactomannans, Science Tech Entrepreneur, 1-2.
Cerqueira, M.A., Bourbon, A.I., Pinheiro, A.C., Martins, J.T., Souza, B.W.S., Teixeria, A.J., and Vicente, A.A., 2011, Galactomannans Use in The Development of The Edible Films/ Coatings for Food Applications, Food Science and Technology, 22: 662-671.
Cerqueira, M.A., Gallagher, M.J.S., Macedo, I., Souza, B.W.S., Aguilera, Rodriguez, R., Teixerira, A.J., and Vicente, A.A., 2010, Use of Galactomannan Edible Coating Application and Storage Temperature for Prolonging Shelf-Life of ‘‘Regional” Cheese, Journal of Food Engineering, 97: 87-94.
Cerqueira, M.A., Souza, B.W.S., Pinheiro, A.C., Lima, A.M.P., Ribeiro, A.C., Miranda, C., Teixeria, A.J., Morira, R.A., Coimbra, M.A., and Goncalves., M.P., 2009, Extraction, Purification and Characterization of Galactomannans from Non-Traditional Source, Carbohydrate Polymers, 75: 408-414. Didalam Tarigan, R., 2013, Sintesa Karboksi Metil Galaktomanan Melalui Reaksi Antara Chloro Asetat dengan Galaktomanan yang Diekstraksi dari Pelepah Lidah Buaya, FMIPA, Universitas Sumatra Utara, Medan.
Chudzikowski, R.J., 1971, Guar Gum and Its Applications, Society of Cosmetic Chemists of Great Britain, 22: 43-60.
Dakia, P.A., Blecker, C., Roberta, C., Watheleta, B., and Paquota, M., 20s08.
Composition and Physicochemical Properties of Locust Bean Gum Extracted from Whole Seeds by Acid or Water Dehulling Pre-treatment. Food Hydrocolloids, 22: 807-818.
Faessenden, R.J., and Fessenden J.S., 1986, Kimia Organik, Jilid 2, Jakarta, Penerbit Erlangga.
Gowda D.V., Khan, M.S and Vineela S., 2012, Development and Evaluation Cross-Linked Guar Gum Microspheres for Improved Delivery of Anticancer to Colon, Taylor & Francis Group, LLC, 51: 1395-1404.
Hermansson, A.M., and Svegmark, K., 1996, Developments in The Understanding of Starch Functionality, Trends in Food Science & Technology, 7: 345-353. Didalam Teja, A., Sindi, P., Ayucitra A., Setiawan, L.E.K., 2008,
Karakterisasi Pati Sagu dengan Metode Modifikasi Asetilasi dan Cross-linking, Jurnal Teknik Kimia Indonesia, 7: 836-843.
http://upload.wikimedia.org/wikipedia/id/3/3d/Kolangkaling_mentah.jpg
Irawan, B., Rahmayani, E., and Iskandar, J., 2009, Studi Variasi, Pemmanfaatan, Pengolahan dan Pengolahan Aren di Desa Rancakalong, Kecamatan
Rancakalong, Kabupaten Sumedang, Jawa Barat, Jurusan Biologi
Fakultas Matematika dan Ilmu Pengetahuan Alam, Universitas Padjadjaran.
Kabir, G.I., K., Yagen B., Penhasi A and Rubinstein A., 2000, Phosphated Crosslinked Guar for Colon-Specific Drug Delivery, 1. Preparation and Physicochemical Characterization, Journal Controlled Release, 63: 121-127.
Kabir, G.I., Yagen B., Penhasi A and Rubinstein A., 1998, Low Swelling, Crosslinked Guar and Its Potential Use as Colon-Specific Drug Carrier,
Pharmaceutical Research, 15 (7): 1091-1025.
Kok, M.S., Hill, S.E., and Mitchell, J.R., 1999, Viscosity of Galactomannan During High Temperature Processing, Influence of Degradation and Solubilisation, Food Hydrocoloids, 13: 535-542. Didalam Tarigan, R., 2013, Sintesa Karboksi Metil Galaktomanan Melalui Reaksi Antara Chloro Asetat dengan Galaktomanan yang Diekstraksi dari Pelepah Lidah Buaya, FMIPA, Universitas Sumatra Utara, Medan.
Kooiman, P., 1971, Stuctures of The Galactomannan Seeds of Annona muricata, Arenga saccharifera, Cocos nucifera, Convolvulus tricolor, and Sophora Japonica, Carbohid. Res, 20: 329-337. Didalam Tarigan, J., 2012,
Mao Gui-Jie, Peng, W., Xing, Z., Tong, Z., 2006, Crosslinking of Corn Starch with Sodium Trimetaphosphate in Solid State by Microwave Irradiation, Journal of Applied Polymer Science, 102: 5854-5860. Didalam Teja, A., Sindi, P., Ayucitra A., Setiawan, L.E.K., 2008, Karakterisasi Pati Sagu dengan Metode Modifikasi Asetilasi dan Cross-linking, Jurnal Teknik Kimia Indonesia, 7: 836-843.
Mathur, N.K., 2012, Indutrial Galactomannan Polysaccharides, CRC Press, Boca Raton, Florida.
Mathur, V., and Mathur, N.K., 2005, Fenugreek and Other Lesser Known Legume Galactomannan-Polysaccharides : Scope For Developments, Journal of Scientific & Industrial Research, 64: 475-481.
Nisa, C.T., 1996, Masalah Dorminasi pada Biji Aren (Arenga pinnata merr) serta
Pemecahannya untusk Meningkatkan Perkecambahan, Pidato
Pengukuhan Guru Besar USU, Medan. Didalam Tarigan, J., 2012,
Karakterisasi Edible Film yang Bersifat Antioksidan dan Antimikroba dari Galaktomanan Biji Aren (Arenga pinnata) yang Diinkoporasi dengan Minyak Atsiri Daun Kemangi (Ocimum basilicum L.), FMIPA, USU, Medan.
Ophardt, C.E., 2003, Protein and Its Properties, Marcel Dekker Inc. New York.
Rana, V., Rai, P., Tiwary, A.K., Singh, R.S., Kennedy, J.F., and Charles, 2011,
Modified gums: Approaches and Applications in Drug Delivery,
Carbohydrate Polymers, 83: 1031-1047.
Raina, C., Singh, S., Bawa, A., and Saxena, D., 2006, Some Characteristics of Acetylated, Cross-linked and Dual Modified Indian Rice Starches, European Food Research and Technology, 223 : 561-570. Didalam Teja, A., Sindi, P., Ayucitra A., Setiawan, L.E.K., 2008, Karakterisasi Pati Sagu dengan Metode Modifikasi Asetilasi dan Cross-linking, Jurnal Teknik Kimia Indonesia, 7: 836-843.
Rozana, 2013, Kesesuaian Galaktomanan Sebagai Edible Coating Untuk Buah
Tropis, Makalah Review Jurnal, Departemen Teknik Mesin dan
Biosistem, Fakultas Pertanian, Institut Pertanian Bogor, Bogor.
Sigres, D.P., dan Sutrisno, A., 2013, Enzim Mananase dan Aplikasi di Bidang Industri, Jurnal Pangan dan Agroindustri, Vol. 3.
Sorvary, S., Toldi, O., Hakonen, T., Tahvonen, R., Ahanen, K., and Viinamaki, T., 1997, Using Polysaccharides and Galactomannans as Gelling Agents in Capsule Formation of Artificial Seeds, J. Amer. Soc. Hort. Sci., 122(6): 878-883.
Sperling, L.H., 2006, Introduction to Physical Polymer Science, John Wiley & Sons, New Jersey.
Srivastava, M., and Kapoor, V. P., 2005, Seed Galactomannans, An Overview in Chemistry and Biodiversity, 2 : 295-217.
Stuart, B., 2004, Infrared Spectroscopy : Fundamentals and Applications, Analytical Techniques in The Science, John Wiley and Sons, Page 84.
Sunanto, 2009, Aren : Budidaya dan Multigunanya, Kanisius-Jakarta.
Tarigan, J., 2012, Karakterisasi Edible Film yang Bersifat Antioksidan dan Antimikroba dari Galaktomanan Biji Aren (Arenga pinnata) yang Diinkoporasi dengan Minyak Atsiri Daun Kemangi (Ocimum basilicum L.), FMIPA, USU, Medan.
Torio, M.A.O., Saez, J., and Merca, E., 2006, Physicochemical Characterization of Galactomannan from Sugar Palm (Arenga saccharifera Labill.) Endosperm at Different Stages of Nut Maturity, Philippine Journal of Science, 135(1): 19-30.
Vargas, M., Pastor, C., Chiralt, A., McClements, D. J., and Gonzalez-Martınez, C., 2008, Recent Advances in Edible Coatings for Fresh and Minimally Processed Fruits, Critical Reviews in Food Science and Nutrition, 48: 496-511.
Lampiran 1. Film Galaktomanan dan Galaktomanan Ikat Silang Fosfat yang dihasilkan
GKK GIF 1A
GIF 2A GIF 3A
GIF 4A GIF 1B