Modul 3
Spektrofotometri Infrared (IR)
A. Kompetensi Dasar
Kompetensi dasar yang harus dicapai mahasiswa dalam modul ini adalah menjelaskan metode analisis spektrofotometri IR dan menginterpretasikan data hasil pengukurannya.
Spektroskopi IR adalah studi mengenai interaksi antara energi cahaya dan materi, dimana energi yang dipancarkan berasal dari radiasi inframerah dengan panjang gelombang yang lebih panjang dari cahaya tampak, tetapi lebih pendek dari radiasi gelombang mikro. Spektrofotometri IR adalah salah satu teknik analisis yang penting karena dapat mempelajari berbagai jenis sampel, baik identifikasi senyawa organik maupun anorganik.
Interaksi Energi IR
Materi (Prinsip Dasar & Teori)
Atom-atom di dalam suatu molekul tidak diam melainkan bervibrasi atau berosilasi bila molekul menyerap radiasi IR. Tipe ikatan dalam molekul yang berlainan menyerap radiasi IR pada panjang gelombang dengan karakteristik tertentu. Kebanyakan gugus seperti C-H, O-H, C=O dan CN, menimbulkan absorpsi IR yang hanya sedikit berubah dari satu molekul ke molekul lain bergantung pada substituen-substituen lain. Hampir semua senyawa dapat menyerap radiasi IR kecuali yang berinti sama, misalnya O2, N2, dan lain-lain.
Absorbansi radiasi IR sesuai dengan tingkat energi vibrasi dan rotasi pada ikatan kovalen yang mengalami perubahan momen dipol dalam suatu molekul. Vibrasi molekul hanya akan terjadi bila suatu molekul terdiri dari dua atom atau lebih. Untuk dapat menyerap radiasi IR (aktif IR), vibrasi suatu molekul harus menghasilkan perubahan momen dipol. Molekul yang tidak mempunyai momen dipol (μ = 0) atau selama bervibrasi ikatannya tidak menghasilkan perubahan momen dipol, maka rotasi ataupun vibrasi molekulnya tidak menyerap radiasi IR (tidak aktif IR). Suatu ikatan dalam suatu molekul dapat menyerap energi lebih dari satu bilangan gelombang, disebabkan oleh sebagian perubahan dalam momen ikatan pada saat energi diserap. Dengan demikian, prinsip dasar spektrofotometer IR adalah interaksi energi IR terhadap materi yang menyebabkan terjadinya transisi diantara tingkat vibrasi dasar dan tingkat vibrasi tereksitasi.
Jenis-Jenis Vibrasi Molekul Jenis-jenis vibrasi molekul ada 2:
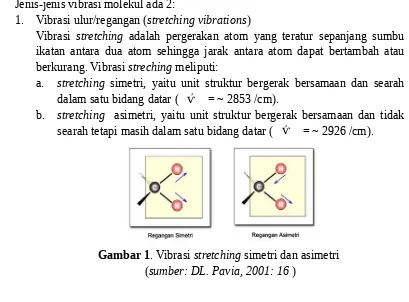
1. Vibrasi ulur/regangan (stretching vibrations)
Vibrasi stretching adalah pergerakan atom yang teratur sepanjang sumbu ikatan antara dua atom sehingga jarak antara atom dapat bertambah atau berkurang. Vibrasi streching meliputi:
a. stretching simetri, yaitu unit struktur bergerak bersamaan dan searah dalam satu bidang datar ( ѵ´ = ~ 2853 /cm).
b. stretching asimetri, yaitu unit struktur bergerak bersamaan dan tidak searah tetapi masih dalam satu bidang datar ( ѵ´ = ~ 2926 /cm).
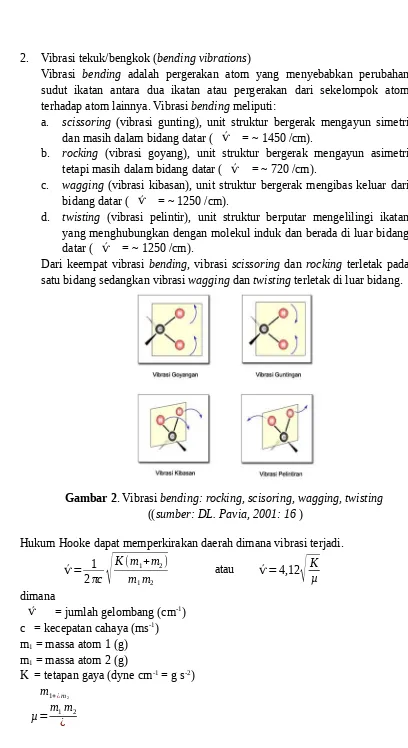
2. Vibrasi tekuk/bengkok (bending vibrations)
Vibrasi bending adalah pergerakan atom yang menyebabkan perubahan sudut ikatan antara dua ikatan atau pergerakan dari sekelompok atom terhadap atom lainnya. Vibrasi bending meliputi:
a. scissoring (vibrasi gunting), unit struktur bergerak mengayun simetri dan masih dalam bidang datar ( ѵ´ = ~ 1450 /cm).
b. rocking (vibrasi goyang), unit struktur bergerak mengayun asimetri tetapi masih dalam bidang datar ( ѵ´ = ~ 720 /cm).
c. wagging (vibrasi kibasan), unit struktur bergerak mengibas keluar dari bidang datar ( ѵ´ = ~ 1250 /cm).
d. twisting (vibrasi pelintir), unit struktur berputar mengelilingi ikatan yang menghubungkan dengan molekul induk dan berada di luar bidang datar ( ѵ´ = ~ 1250 /cm).
Dari keempat vibrasi bending, vibrasi scissoring dan rocking terletak pada satu bidang sedangkan vibrasi wagging dan twisting terletak di luar bidang.
Gambar 2. Vibrasi bending: rocking, scisoring, wagging, twisting ((sumber: DL. Pavia, 2001: 16 )
Hukum Hooke dapat memperkirakan daerah dimana vibrasi terjadi.
´ ѵ= 1
2πc
√
K(m1+m2) m1m2
atau ѵ´=4,12
√
K µ dimana´
ѵ = jumlah gelombang (cm-1) c = kecepatan cahaya (ms-1) m1 = massa atom 1 (g) m1 = massa atom 2 (g)
K = tetapan gaya (dyne cm-1 = g s-2) m1+¿m2
Posisi relatif suatu atom dengan atom lainnya dalam suatu molekul selalu berubah-ubah akibat dari gerakan vibrasi. Untuk molekul dwiatom atau tri-atom, vibrasi berhubungan dengan energi absorpsi, namun untuk poliatom vibrasi tidak mudah diperkirakan karena banyaknya pusat vibrasi yang berinteraksi. Adapun cara vibrasi untuk molekul poliatom dapat dikelompokkan untuk molekul linier dan molekul non linier. Vibrasi fundamental untuk molekul linier = 3n – 5, sedangkan untuk molekul non linier = 3n – 6, dengan n = banyaknya atom.
Instrumentasi Spektrofotometer IR
Instrumentasi spektrofotometer IR memiliki sistem optik yang serupa dengan spektrofotometer UV-Vis. Perbedaan utama terletak pada sumber energi, dan sel. Sumber radiasi bisa berupa laser, dan selnya lebih tipis daripada sel pada UV-Vis karena energi IR lebih rendah dari UV-Vis. Umumnya alat IR menggunakan berkas ganda yang dirancang lebih sederhana daripada berkas tunggal.
Prinsip kerja spektrofotometer IR yaitu radiasi dari sumber radiasi IR dipecah oleh pencacah sinar menjadi dua bagian yang sama dengan arah yang saling tegak lurus. Kemudian kedua radiasi tersebut dipantulkan kembali ke dua cermin sehingga bertemu kembali di pencacah sinar untuk saling berinteraksi. Dari sini sinar dipancarkan ke cuplikan yang dapat menyerap energi, setelah itu terjadilah transisi diantara tingkat energi vibrasi dasar dan tingkat vibrasi tereksitasi berupa berkas radiasi IR yang ditangkap oleh detektor, kemudian signal yang dihasilkan dari detektor direkam sebagai spektrum IR yang berbentuk puncak-puncak absorpsi berupa grafik. Sebagian sinar dari pencacah akan dibalikan ke sumber gerak. Maju mundur cermin akan menyebabkan sinar mencapai ke detektor berfluktuasi tetapi terkendali.
Interpretasi Spektrofotometer IR
Spektrum IR diperoleh dengan melewatkan radiasi IR melalui sampel dan menentukan fraksi radiasi yang diserap pada energi tertentu. Energi pada puncak spektrum absorbsi memperlihatkan hubungan antara frekuensi vibrasi dari bagian molekul sampel. Dengan kata lain, Spektrum IR menggambarkan hubungan intensitas absorbsi (% T) dengan bilangan gelombang (cm-1). Pita-pita IR dalam sebuah spektrum dapat dikelompokkan menurut intensitasnya yaitu kuat (strong = S), sedang (medium = M) dan lemah (weak = W). Interpretasi spektrum IR dapat dilakukan dengan menggunakan bagan korelasi dan tabel, sehingga peak-peak yang ada dapat dianalisis.
Analisis Kualitatif dengan Spektrofotometer IR
absorpsinya dalam suatu spektrum. Pita absorpsi C-H ( ѵ´ = ± 3000 cm-1) tidak perlu dianalisis secara mendalam karena hampir semua senyawa memiliki absorbsi ini. Selain itu, hal-hal kecil di sekeliling gugus fungsional yang didapatkan juga tidak perlu dihiraukan dulu. Tidak ada molekul yang berbeda strukturnya memiliki pola absorpsi-IR atau spektrum-IR yang sama (fingerprint spectrum).
Adapun urutan daftar penelusuran terhadap spektra IR gugus yang penting adalah memeriksa ada tidaknya gugus karbonil (C=O), jika ada cek asam, amida, ester, anhidrida, aldehid, dan keton, sedangkan jika tidak ada gugus karbonil cek alkohol, fenol, amina, dan eter. Selanjutnya memerika ikatan rangkap dan cincin aromatik, ikatan rangkap tiga, gugus nitro, dan hidrokarbon.
Membedakan IR Konvensional dan FTIR
Spektrofotometer Fourier Trasform Infra Red (FTIR) adalah spektrofotometer dengan sistem optik yang berupa inferometer. Pada dasarnya spektrofotometer FTIR sama dengan spektrofotometer IR Dispersi (konvensional). Perbedaannya terletak pada pengembangan sistem optiknya sebelum berkas sinar IR melewati contoh. Sensitifitas dari metoda Spektrofotometri FTIR lebih besar daripada cara dispersi, sebab radiasi yang masuk ke sistim detektor lebih banyak karena tanpa harus melalui celah (slitless). Dengan demikian, keuntungan FTIR dibandingkan IR dapat disimpulkan sebagai berikut:
FTIR tidak menggunakan celah sehingga total output sumber dapat melewati sampel terus menerus, menyebabkan detektor dapat menerjemahkan signal lebih tinggi.
FTIR lebih cepat daripada IR karena adanya cermin pada inferometernya.
D. Rangkuman
E. Latihan/Tugas
Kerjakan latihan berikut untuk memperdalam pemahaman Anda mengenai materi spektrofotometri IR.
1. Berapakah vibrasi fundamental dari CO2?
2. Perkirakan ѵ´ vibrasi stretching untuk tipe ikatan C-H dengan menggunakan hukum Hooke (K = 5105 dyne/cm)
3. Identifikasi gugus fungsi dari spektra IR berikut ini.
Petunjuk Jawaban Latihan!
1. CO2à O = C = O (molekul linier)
vibrasi: 3n - 5 = (3 x 3) - 5 = 4 jenis vibrasi
2. ѵ´=4,12
√
Kµ
dengan
µ= m1m2 m1+m2=(12)(1)
12+1 =0,923
´
ѵ=4,12
√
5 1050,923=3032cm
−1
3. Berdasarkan spektra IR tersebut, maka gugus fungsi yang ada adalah:
C-H stretch (3000 cm-1) -CH2- bend (1465 cm-1) -CH3 bend (1375 cm-1)
C-H (stretch)
-CH2-
(bend) -CH3
F. Tes Mandiri
1. Berapakah vibrasi fundamental dari CHCl3?
2. Perkirakan ѵ´ vibrasi stretching untuk masing-masing tipe ikatan O-H, C=O, CC dengan menggunakan hukum Hooke (Tetapan gaya untuk O-H: 7,0105 dyne/cm; C=O: 12,1105 dyne/cm; CC: 15,6105 dyne/cm) 3. Identifikasi gugus fungsi dari spektra IR berikut ini.
4. Perhatikan spektra IR berikut ini.
Manakah senyawa yang diperlihatkan oleh spektra tersebut? Jelaskan!
GLOSARIUM Spektrofotometri Vibrasi
DAFTA PUSTAKA
DL Pavia, GM Lampman, GS Kriz Jr. 2001. Introduction to Spectroscopy. Philadelphia: Saunders.
Harvey D. 2000. Modern Anayitical Chemistry. USA: McGraw-Hill Companies, Inc.
Hendayana, S., et.al. 1994. Kimia Analitik Instrumen. Semarang: Penerbit IKIP Semarang.
Silverstein RM & Bassler GC. 2000. Spectrometric Identification of Organic Compounds 5ed. New York : John Wiley and Sons, Inc.
Skoog DA, West DM, Holler FJ, Crouch SR. 2004. Fundamentals of Analytical Chemistry. Eighth Edition. USA: Thomson Learning, Inc. Skoog, Holler & Nieman. 1998. Principles of Instrumental Analysis 5ed.