KERANG BULU (Anadara inflata) SEBAGAI BIOINDIKATOR
PENCEMARAN LOGAM BERAT TIMBAL (Pb) DAN
CADMIUM (Cd) DI MUARA
SUNGAI ASAHAN
T E S I S
Oleh
ERNAWATI
087030007
PROGRAM STUDI MAGISTER BIOLOGI
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
UNIVERSITAS SUMATERA UTARA
KERANG BULU (Anadara inflata) SEBAGAI BIOINDIKATOR
PENCEMARAN LOGAM BERAT TIMBAL (Pb) DAN
CADMIUM (Cd) DI MUARA
SUNGAI ASAHAN
T E S I S
Diajukan sebagai salah satu syarat untuk memperoleh gelar
Magister Sains Biologi Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Sumatera Utara
Oleh
ERNAWATI
087030007
PROGRAM STUDI MAGISTER BIOLOGI
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
UNIVERSITAS SUMATERA UTARA
Judul Penelitian : KERANG BULU (Anadara inflata) SEBAGAI
BIOINDIKATOR PENCEMARAN LOGAM BERAT TIMBAL (Pb) DAN CADMIUM (Cd) DI MUARA SUNGAI ASAHAN
Nama : ERNAWATI
NIM : 087030007
Program Studi : PASCASARJANA BIOLOGI
Mengetahui Komisi Pembimbing
Prof. Dr. Ing. Ternala A. Barus M.Sc Prof.Dr. Syafruddin Ilyas M.BioMed
Ketua Anggota
Ketua Program Studi Dekan FMIPA
Prof.Dr.Dwi Suryanto, MSc Dr.Sutarman, M.Sc
Telah diuji pada
Tanggal : 14 Agustus 2010
PANITIA PENGUJI TESIS
Ketua : Prof. Dr. Ing. Ternala A. Barus M.Sc
Anggota : 1. Prof. Dr. Syafruddin Ilyas M.BioMed
PERNYATAAN
KERANG BULU (Anadara inflata) SEBAGAI BIOINDIKATOR PENCEMARAN LOGAM BERAT TIMBAL (Pb) DAN
CADMIUM (Cd) DI MUARA SUNGAI ASAHAN
TESIS
Dengan ini saya menyatakan bahwa dalam tesis ini tidak terdapat karya yang pernah diajukan untuk memperoleh gelar kesarjanaan di suatu perguruan tinggi dan sepanjang pengetahuan saya juga tidak terdapat karya atau pendapat yang pernah ditulis atau diterbitkan oleh orang lain kecuali secara tertulis diacu dalam naskah ini dan disebutkan dalam daftar pustaka.
Medan, Agustus 2010 Penulis
Ernawati
PENGHARGAAN
Syukur Alhamdulillah penulis panjatkan kehadirat Allah SWT, yang telah
melimpahkan rahmat dan karuniaNya sehingga penulis dapat menyelesaikan
penelitian yang berjudul “Kerang Bulu (Anadara Inflata) Bioindikator
Pencemaran Logam Berat Timbal (Pb) Dan Cadmium (Cd) Di Perairan Muara
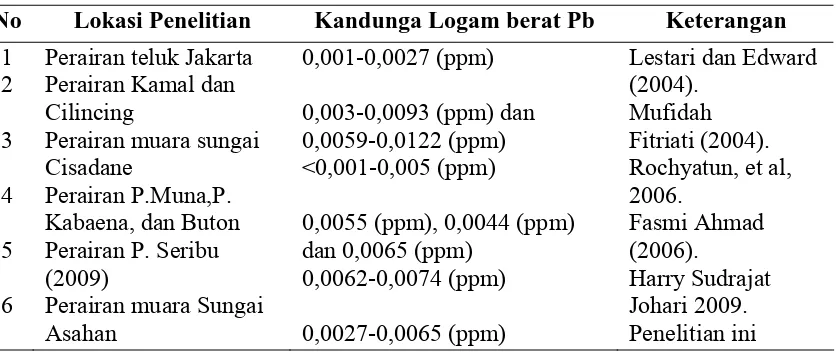
Asahan”. Dibuat sebagai salah satu syarat untuk menyelesaikan pendidikan pada
Program Studi Magister Biologi Sekolah Pascasarjana Universitas Sumatera Utara
Medan.
Penulis menyampaikan terima kasih kepada Bapak Prof. Dr. Ing. Ternala
Alexander Barus, M.Sc sebagai Dosen Pembimbing I dan Prof. Dr. Syafruddin Ilyas
M.Bio.Med selaku Dosen Pembimbing II Penulis yang telah banyak memberikan
arahan dan bimbingan selama penulis melaksanakan penelitian sampai selesainya
penyusunan hasil penelitian ini.
Dalam kesempatan ini penulis mengucapkan terima kasih kepada :
1. Prof.Dr.Retno Widhiastuti, M.Si, sebagai Dosen Penguji yang telah memberikan
arahan dan masukan dalam penyempurnaan penyusunan hasil penelitian ini.
2. Dr.Suci Rahayu, M.Sc, sebagai Dosen Penguji yang telah memberikan arahan
dan masukan dalam penyempurnaan penyusunan hasil penelitian ini.
3. Prof.Dr.Dwi Suryanto, M.Sc., sebagai Ketua Program Studi Magister Biologi
4. Gubernur Provinsi Sumatera Utara dan Kepala Bapeda Sumatera Utara yang telah
memberikan beasiswa S2 kepada penulis sehingga penulis dapat menyelesaikan
Studi S2.
5. Bapak Drs. Agus Ismadi Kuncoro, sebagai Kepala SMAN 5 Binjai yang telah
memberikan dukungannya bagi penulis.
6. Suamiku (Mukhlizar Mukhtar), Ayahanda dan Ibunda terkasih (Imran Hadi dan
Almh.Dahwiah Alwi) dan anak-anakku tercinta (Hilman, Yudha, dan Luthfi)
serta saudara-saudaraku tersayang (Danial, Alisan, Iwan, Eli, Juhri, Fitri dan
Minah) yang telah memberiku doa dan dukungannya.
7. Teman-teman dalam tim penelitian yang telah banyak memberikan motivasi dan
dukungannya dalam penyelesaian tesis ini.
Akhir kata semoga Allah SWT memberikan rahmatNya dalam kita mengejar
ilmu dan semoga penelitian ini bermanfaat bagi kita semua.
Medan, Agustus 2010
RIWAYAT HIDUP
Penulis lahir di Teluk Nibung Tanjung Balai Asahan pada tanggal 25 Maret
1969. Anak Kedua dari Tujuh bersaudara dari pasangan Ayahanda Imran Hadi dan
Ibunda Dahwiah Alwi. Menikah pada tanggal 9 Februari 1992 dengan Drs.
Mukhlizardi Mukhtar, anak keempat dari enam bersaudara dari pasangan Bapak
Mukhtar (Alm.) dan Ibu Nursilam (Alm.). Telah dikaruniai 3 orang putra-putri :
M.Hilman Zarkasih, M.Yudha, dan Luthfi Lizardi.
Adapun riwayat pendidikan penulis :
1. SD Negeri Pematang Pasir Tanjung Balai Asahan Tahun 1983
2. SMP Negeri 1 Tanjung Balai Asahan Tahun 1986
3. SMA Negeri 1 Tanjung Balai Asahan Tahun 1989
4. D3 Jurusan Kependidikan Biologi FMIPA USU Tahun 1992.
5. S1 Jurusan Biologi FMIPA UNIMED Pada tahun 1997
6. S2 Tahun 2008 mendapat kesempatan melanjutkan pendidikan Program Magister
(S2) di Program Studi Biologi Sekolah Pascasarjana Universitas Sumatera Utara
dengan beasiswa dari Pemerintah Provinsi Sumatera Utara.
Riwayat Pekerjaan
1. Tahun 1993 diangkat sebagai Pegawai Negeri Sipil di SMA Negeri 1 Gebang
Kabupaten Langkat.
2. Tahun 2000 pindah tugas ke SMA Negeri 5 Binjai dan bertugas di sekolah
ABSTRAK
KERANG BULU (Anadara inflata) SEBAGAI BIOINDIKATOR
PENCEMARAN LOGAM BERAT TIMBAL (Pb) DAN CADMIUM
(Cd) DI MUARA SUNGAI ASAHAN
Muara Sungai Asahan adalah kawasan yang mendapat pengaruh langsung
aliran massa air dari Sungai Asahan yang berasal dari Danau Toba dan perairan Laut Selat Malaka. Berbagai aktivitas masyarakat di perairan tersebut dapat mempengaruhi kualitas perairan termasuk logam beratnya.
Tujuan penelitian ini untuk mengetahui kandungan logam berat Pb dan Cd pada daging kerang bulu (Anadara inflata), air dan sedimen. Penelitian ini dilakukan pada bulan Agustus 2009 di muara Sungai Asahan. Pengamatan dilakukan pada 3 stasiun dengan masing-masing 3 ulangan. Stasiun 1 lokasinya di mulut muara, stasiun II 4 mil lepas pantai, dan stasiun III 5 mil lepas pantai. Metode yang digunakan untuk pengambilan sampel adalah ”Purpossive Random Sampling”.
Analisa kandungan logam berat Timbal (Pb) dan Cadmium (Cd) dilakukan di
Laboratorium Bapedalda Sumatera Utara dengan menggunakan alat AAS (Atomic
Absorption Spectrophotometer) tipe Shimadzu, series AA.6200 dengan batas deteksi Cd≥0,004 ppm, Pb≥0,01 ppm.
Hasil pengukuran kandungan logam berat Pb daging kerang bulu (Anadara inflata) rata-rata 0,0021-0,0187 ppm, kandungan logam berat Cd daging kerang bulu (Anadara inflata) rata-rata 0,0049-0,0146 ppm. Nilai konsentrasi logam berat Pb dan Cd daging kerang bulu belum melebihi batas baku mutu yang ditetapkan oleh Keputusan Dirjen Pom No.03725/B/SK/VII/1989 sebesar 2 ppm Pb dan 0,2 ppm Cd.
Nilai konsentrasi Pb dalam badan air rata-rata 0,0027-0,0065 ppm, kandungan Cd dalam badan air rata-rata 0,0076-0,0264 ppm. Nilai konsentrasi logam berat Pb dalam badan air belum melebihi batas baku mutu air air laut untuk biota laut yang ditetapkan Kep.Men LH No.51/2004 sebesar 0,008 ppm Pb dan 0,001 ppm Cd. Nilai konsentrasi Pb pada sedimen rata-rata 0,0403-0,0569 ppm sedangkan nilai konsentrasi logam Cd pada sedimen rata-rata 0,0120-0,0384 ppm. Nilai konsentrasi kandungan logam berat Pb dan Cd dalam sedimen masih dibawah batas alamiah yang telah direkomendasikan oleh Reseau National d’Observation (RNO, 1981 dalam
Ahmad, 2009) sebesar 10-70 ppm Pb dan 0,1-2 ppm Cd.
ABSTRACT
COCKLE SHELL (ANADARA INFLATE) AS BIO-INDICATOR
IN POLLUTED HEAVY METAL (PB) AND
CADMIUM (CD) ON MOUTH RIVER OFASAHAN
The Asahan river’s mouth is an area got directly influence in massive flowing of water from Asahan River sourced from Danau Toba and Malacca Strait’s sea waters. Variously activities of community on that waters can influence the quality of waters including its heavy metal.
The objective of this study is to know the content of heavy metal Pb and Cd on the flesh of cockle shell (Anadara inflate), water and sediment. This study was conducted on August 2009 on Asahan River’s mouth. The survey was done on 3 stations with 3 repetitions of each. Station I located on the end of mouth, station II 4 miles seashore, and station III of 5 miles seashore. The method used in taking the sample known as purposive random sampling.
To analyze the content of its heavy metal (Pb) and Cadmium (Cd) was completed on Laboratory of Bapedalda Sumatera Utara adopting the Atomic Absorption Spectrophotometer type Shimadzu, series AA.6200 with detection limit Cd ≥ 0.004 ppm, Pb ≥ 0.01 ppm.
The assessment to the content of heavy metal Pb on flesh of cockle shell (Anadara inflate) resulted average 0.0021-0.0187 ppm, content of heavy metal Cd on the flesh is average 0.0049-0.0146 ppm. The concentrated rate of heavy metal Pb and Cd the flesh do not exceed yet limit of quality standard as defined by government decree Dirjen POM No.03725/B/SK/VII/1989 with 2 ppm Pb and 0.2 ppm Cd.
The concentrated rate Pb within water body average 0.0027-0.0065 ppm, the content CD within water body average 0.0076-0.0264 ppm. The concentrated rate of heavy metal Pb within water body do not exceed limit of quality standard on sea water for marine biota as defined by government decree Kep.Men LH No.51/2004 of 0.008 ppm Pb and 0.001 ppm Cd. The concentrated rate of Pb on sediment average 0.0403-0.0569 ppm whereas the concentrated rate of Cd metal on sediment average of 0.0120-0.0384 ppm. The concentrated rate of content heavy metal Pb and Cd in
sediment is still underestimate as has been recommended by Reseau National
d’Observation (RNO, 1981 in Ahmad, 2009) of 10-70 ppm Pb and 0.1-2 ppm Cd.
DAFTAR ISI
2.1.1 Pengertian Logam Berat... 9
2.1.2 Karakteristik Logam berat... 10
2.1.3 Dampak Negatif Logam Berat Bagi Manusia... 13
2.2 Kasus Pencemaran Logam Berat Di Indonesia... 15
2.3 Pencemaran Logam Berat Pada Wilayah Pesisir ... 16
2.4 Sumber Logam Berat Pb dan Cd di Perairan ... 20
2.5 Bioindikator Pencemaran Logam Berat ... 22
2.6 Biologi Kerang Bulu (Anadara inflata) ... 24
2.7 Spektroskopi Serapan Atom (SSA)... 27
2.8 Faktor Fisik Kimia Perairan ... 28
3.5 Metode Pengambilan Sampel... 34
3.5.1 Kerang Bulu (Anadara inflata) ... 34
3.5.2 Air ... 35
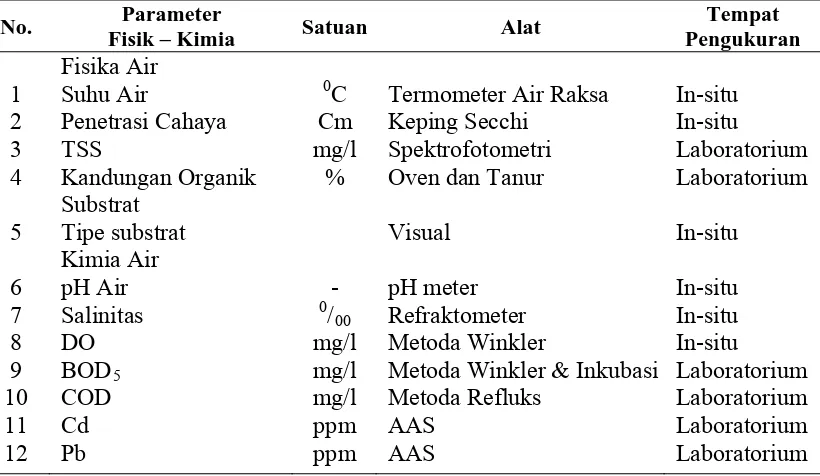
3.6 Pengukuran Faktor Fisika, Kimia, dan Biologi Perairan ... 36
3.7 Analisis data ... 39
BAB IV HASIL DAN PEMBAHASAN ... 41
4.1 Kandungan Logam Berat pada Daging Anadara inflata ... 41
4.1.1 Timbal (Pb) ... 41
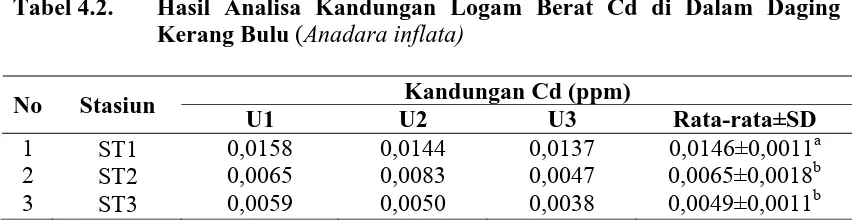
4.1.2 Cadmium (Cd)... 45
4.2 Kandungan Logam Berat Dalam Badan Air ... 48
4.2.1 Timbal (Pb) ... 48
4.2.2 Cadmium (Cd)... 52
4.3 Kandungan Logam Berat Dalam Sedimen Di Perairan Muara Sungai Asahan ... 57
4.3.1 Timbal (Pb) ... 57
4.3.2 Cadmium (Cd)... 60
4.4 Korelasi Antara Pb atau Cd Daging Kerang dengan Pb atau Cd Air dan Sedimen pada Stasiun I, II, dan III ... 64
4.4.1 Korelasi Antara Pb atau Cd Daging Kerang dengan Pb atau Cd Air dan Sedimen pada Stasiun I ... 64
4.4.2 Korelasi Antara Pb atau Cd Daging Kerang dengan Pb atau Cd Air dan Sedimen pada Stasiun II ... 66
4.4.3 Korelasi Antara Pb atau Cd Daging Kerang dengan Pb atau Cd Air dan Sedimen pada Stasiun III... 69
4.4.4 Korelasi Antara Pb atau Cd Daging Kerang dengan Pb atau Cd Air dan Sedimen pada Stasiun I, II Dan III... 71
4.5 Faktor Fisika Kimia Perairan Muara Sungai Asahan ... 72
4.5.1 Temperatur (Suhu) ... 73
4.5.2 Kecerahan (Penetrasi Cahaya) ... 74
4.5.3 Padatan Tersuspensi Total (TSS) ... 75
4.5.4 Kandungan Organik Substrat (KO Substrat) ... 76
4.5.5 Tipe Substra ... 77
4.5.6 Derajat Keasaman (pH) atau Konsentrasi ion Hidrogen... 78
4.5.7 Salinitas ... 79
4.5.8 Kebutuhan Oksigen Kimia (COD)... 80
DAFTAR TABEL
No. Judul Halaman
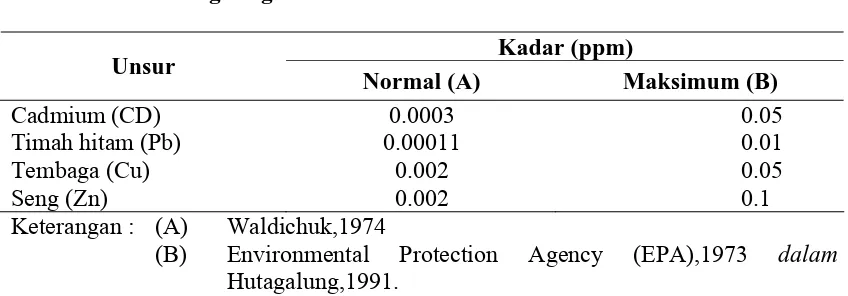
2.1. Kadar Normal dan Kadar Maksimum Logam Berat yang Masuk
ke Lingkungan Laut ... 19 2.2 Indikator Biologi dan Jenis-jenis Indikator... 24 3.1. Alat dan Bahan yang Digunakan dalam Penelitian... 34 3.2. Alat dan Satuan yang dipergunakan dalam Pengukuran Faktor
Fisika/Kimia dan Biologi Perairan ... 39
4.1. Hasil Analisa Kandungan Logam Pb pada Daging Kerang Bulu
(Anadara inflata)... 41 4.2. Hasil Analisa Kandungan Logam Berat Cd di Dalam Daging
Kerang Bulu (Anadara inflata) ... 45 4.3 Kandungan Kadmium (Cd) dalam Beberapa Jenis Air Buangan... 48 4.4. Hasil Analisa Konsentrasi Logam Pb (ppm) dalam Badan Air di
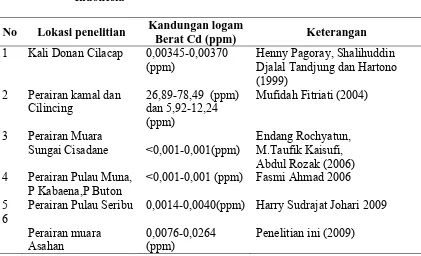
Perairan Muara Sungai Asahan ... 49 4.5. Perbandingan Logam Berat Timbal (Pb) ppm Dalam Perairan
Muara Sungai Asahan dan Perairan lain di Indonesia ... 51 4.6. Hasil Analisa Konsentrasi Logam Cd (ppm) dalam Badan Air di
Perairan Muara Sungai Asahan... 52 4.7. Persentase Kandungan Cd yang Masuk ke Teluk New York ... 53 4.8. Perbandingan Kadar Logam Berat Cadmium dalam Air Laut di
Perairan Muara Sungai Asahan dan Perairan lain di Indonesia ... 54 4.9 Hasil Pengukuran Kadar Logam Berat Pb dalam Sedimen di
Perairan Muara Sungai Asahan... 57 4.10 Perbandingan Kadar Logam Berat Timbal (Pb) ppm dalam
Sedimen di Perairan Muara Sungai Asahan dengan Perairan lain
di Indonesia ... 60 4.11 Hasil Pengukuran Kadar Logam Berat Cd dalam Sedimen di
Perairan Muara Sungai Asahan... 61 4.12 Perbandingan Kadar Cd di Perairan Muara Sungai Asahan
dengan Perairan di Indonesia lainnya ... 63 4.13 Korelasi Antara Pb atau Cd Daging Kerang Dengan Pb atau Cd
Air dan Sedimen pada Stasiun I ... 64 4.14 Korelasi Antara Pb atau Cd Daging Kerang Dengan Pb atau Cd
Air dan Sedimen pada Stasiun II... 67 4.15 Korelasi Antara Pb atau Cd Daging Kerang Dengan Pb atau Cd
Air dan Sedimen pada Stasiun III ... 69 4.16. Nilai Rata-rata Parameter Fisika Kimia Perairan pada Masing-
DAFTAR GAMBAR
No. Judul Halaman
DAFTAR LAMPIRAN
No. Judul Halaman
A. Prosedur Analisa Logam Berat Pb dan Cd Dalam Kerang Bulu
(Anadara inflata)... 93
B. Prosedur Analisa Logam Berat (Terlarut) Pb dan Cd dalam Contoh Air 94 C. Prosedur Analisa Pb dan Cd dalam sedimen... 95
D. Surat Hasil Uji dan Analisis Logam Pb, Cd pada kerang, Air dan Sedimen dengan Uji AAS dari Laboratorium Bapedalda Sumatera Utara ... 96
E. Surat Hasil Analisis Substrat Organik, COD, TDS, dan TSS Puslit Sumatera Utara ... 97
F. Kepmen KLH No.51 Tahun 2004 tentang Baku Mutu Air Laut ... 98
G. Bagan Kerja Metode Winkler Untuk Mengukur Kelarutan Oksigen (DO) ... 100
H. Bagan Kerja Metode Winkler Untuk Mengukur BOD5... 101
I. Bagan Kerja Pengukuran COD dengan Metode Refluks ... 102
J. Bagan Kerja Untuk Mengukur Kadar Organik Substrat ... 103
K. Peta Lokasi Penelitian ... 104
L. Foto Stasiun Penelitian... 105
M. Alat Penangkap Kerang... 107
N. Foto Alat AAS (Atomic Absorbtion Spectrophotometer) Tipe Shimadzu, Series AA 6200 ... 108
O. Foto Alat Eeckman Grab ... 109
ABSTRAK
KERANG BULU (Anadara inflata) SEBAGAI BIOINDIKATOR
PENCEMARAN LOGAM BERAT TIMBAL (Pb) DAN CADMIUM
(Cd) DI MUARA SUNGAI ASAHAN
Muara Sungai Asahan adalah kawasan yang mendapat pengaruh langsung
aliran massa air dari Sungai Asahan yang berasal dari Danau Toba dan perairan Laut Selat Malaka. Berbagai aktivitas masyarakat di perairan tersebut dapat mempengaruhi kualitas perairan termasuk logam beratnya.
Tujuan penelitian ini untuk mengetahui kandungan logam berat Pb dan Cd pada daging kerang bulu (Anadara inflata), air dan sedimen. Penelitian ini dilakukan pada bulan Agustus 2009 di muara Sungai Asahan. Pengamatan dilakukan pada 3 stasiun dengan masing-masing 3 ulangan. Stasiun 1 lokasinya di mulut muara, stasiun II 4 mil lepas pantai, dan stasiun III 5 mil lepas pantai. Metode yang digunakan untuk pengambilan sampel adalah ”Purpossive Random Sampling”.
Analisa kandungan logam berat Timbal (Pb) dan Cadmium (Cd) dilakukan di
Laboratorium Bapedalda Sumatera Utara dengan menggunakan alat AAS (Atomic
Absorption Spectrophotometer) tipe Shimadzu, series AA.6200 dengan batas deteksi Cd≥0,004 ppm, Pb≥0,01 ppm.
Hasil pengukuran kandungan logam berat Pb daging kerang bulu (Anadara inflata) rata-rata 0,0021-0,0187 ppm, kandungan logam berat Cd daging kerang bulu (Anadara inflata) rata-rata 0,0049-0,0146 ppm. Nilai konsentrasi logam berat Pb dan Cd daging kerang bulu belum melebihi batas baku mutu yang ditetapkan oleh Keputusan Dirjen Pom No.03725/B/SK/VII/1989 sebesar 2 ppm Pb dan 0,2 ppm Cd.
Nilai konsentrasi Pb dalam badan air rata-rata 0,0027-0,0065 ppm, kandungan Cd dalam badan air rata-rata 0,0076-0,0264 ppm. Nilai konsentrasi logam berat Pb dalam badan air belum melebihi batas baku mutu air air laut untuk biota laut yang ditetapkan Kep.Men LH No.51/2004 sebesar 0,008 ppm Pb dan 0,001 ppm Cd. Nilai konsentrasi Pb pada sedimen rata-rata 0,0403-0,0569 ppm sedangkan nilai konsentrasi logam Cd pada sedimen rata-rata 0,0120-0,0384 ppm. Nilai konsentrasi kandungan logam berat Pb dan Cd dalam sedimen masih dibawah batas alamiah yang telah direkomendasikan oleh Reseau National d’Observation (RNO, 1981 dalam
Ahmad, 2009) sebesar 10-70 ppm Pb dan 0,1-2 ppm Cd.
ABSTRACT
COCKLE SHELL (ANADARA INFLATE) AS BIO-INDICATOR
IN POLLUTED HEAVY METAL (PB) AND
CADMIUM (CD) ON MOUTH RIVER OFASAHAN
The Asahan river’s mouth is an area got directly influence in massive flowing of water from Asahan River sourced from Danau Toba and Malacca Strait’s sea waters. Variously activities of community on that waters can influence the quality of waters including its heavy metal.
The objective of this study is to know the content of heavy metal Pb and Cd on the flesh of cockle shell (Anadara inflate), water and sediment. This study was conducted on August 2009 on Asahan River’s mouth. The survey was done on 3 stations with 3 repetitions of each. Station I located on the end of mouth, station II 4 miles seashore, and station III of 5 miles seashore. The method used in taking the sample known as purposive random sampling.
To analyze the content of its heavy metal (Pb) and Cadmium (Cd) was completed on Laboratory of Bapedalda Sumatera Utara adopting the Atomic Absorption Spectrophotometer type Shimadzu, series AA.6200 with detection limit Cd ≥ 0.004 ppm, Pb ≥ 0.01 ppm.
The assessment to the content of heavy metal Pb on flesh of cockle shell (Anadara inflate) resulted average 0.0021-0.0187 ppm, content of heavy metal Cd on the flesh is average 0.0049-0.0146 ppm. The concentrated rate of heavy metal Pb and Cd the flesh do not exceed yet limit of quality standard as defined by government decree Dirjen POM No.03725/B/SK/VII/1989 with 2 ppm Pb and 0.2 ppm Cd.
The concentrated rate Pb within water body average 0.0027-0.0065 ppm, the content CD within water body average 0.0076-0.0264 ppm. The concentrated rate of heavy metal Pb within water body do not exceed limit of quality standard on sea water for marine biota as defined by government decree Kep.Men LH No.51/2004 of 0.008 ppm Pb and 0.001 ppm Cd. The concentrated rate of Pb on sediment average 0.0403-0.0569 ppm whereas the concentrated rate of Cd metal on sediment average of 0.0120-0.0384 ppm. The concentrated rate of content heavy metal Pb and Cd in
sediment is still underestimate as has been recommended by Reseau National
d’Observation (RNO, 1981 in Ahmad, 2009) of 10-70 ppm Pb and 0.1-2 ppm Cd.
BAB I
PENDAHULUAN
1.1Latar Belakang
Perairan Bagan Asahan yang terletak pada koordinat 03° 01' 00” LU dan 99°
51' 30” BT perairan tersebut penting di Sumatera Utara. Selain terletak di bibir Selat
Malaka, Bagan Asahan adalah kawasan muara Sungai Asahan, sungai yang berhulu
dari Danau Toba. Sungai Asahan mengalir melewati Kabupaten Tapanuli Utara,
Kabupaten Asahan dan Kota Tanjung Balai. Sejumlah sungai kecil bermuara ke
Sungai Asahan, sehingga semakin mendekati muaranya, debit air Sungai Asahan
makin besar. Lebar Sungai Asahan di kawasan muara sekitar 1 kilometer.
Secara kasat mata, terutama yang terlihat di bagian sungai yang melewati
Kota Tanjung Balai, Sungai Asahan telah tercemar. Air sungai selalu keruh dan
sering pula terlihat tumpahan sisa minyak pelumas tergenang di sungai. Sejumlah
industri di Asahan dan Tanjung Balai, terutama yang terdapat di sepanjang Sungai
Asahan sekitar 10 kilometer sebelum muara, atau persisnya sejak pusat Kota Tanjung
Balai, sisi kiri sungai merupakan tangkahan (pelabuhan pendaratan kapal ikan) yang
setiap hari disinggahi sekitar 1.500 kapal, boat dan sampan nelayan (PT. Pelabuhan
Indonesia 1, 2010).
Di pinggir Sungai Asahan terdapat Pelabuhan Teluk Nibung, yakni pelabuhan
ekspor impor barang dan penumpang tujuan dalam dan luar negeri. Kemudian, di
letaknya berhadapan langsung dengan pelabuhan negara tetangga Malaysia atau Port
Klang. Pelabuhan tersebut dimanfaatkan untuk pendaratan perahu maupun kapal
nelayan, diantaranya adalah kapal nelayan penangkap kerang.
Tanjung Balai memang dikenal sebagai penghasil kerang bulu (Anadara
inflata) utama di Sumatera Utara, sehingga dikenal dengan sebutan sebagai kota
kerang. Penangkapan kerang dilakukan secara tradisional maupun dengan peralatan
tangkap modern. Hasilnya dijual ke berbagai kota di Sumatera Utara, seperti Medan,
Binjai, Tanah Karo, Pematang Siantar, Kisaran, Rantau Prapat dan Padang
Sidempuan.
Muara Sungai Asahan mendapat pengaruh langsung aliran massa air dari
Sungai Asahan yang berasal dari Danau Toba dan perairan laut Selat Malaka. Di
sepanjang Sungai Asahan banyak terdapat aktivitas manusia antara lain Pembangkit
Listrik Tenaga Uap (PLTU) Asahan, pariwisata, pemukiman, rumah sakit, pabrik es
(cold storange), pabrik kapur, industri tapioka, gudang-gudang penyimpanan barang,
gudang-gudang ikan, tambak udang dan lalu lintas kapal mempunyai potensi
membuang limbah khususnya logam berat ke Sungai Asahan. Perilaku masyarakat
yang cendrung membuang limbah industri, limbah rumah tangga dan minyak sisa
kapal ke Sungai Asahan akan dapat menyebabkan perairan muara Sungai Asahan
tercemar logam berat seperti Kadmium (Cd), Plumbum (Pb).
Menurut Kementrian Negara Kependudukan dan Lingkungan Hidup (1990)
sifat toksisitas logam berat dapat dikelompokan ke dalam 3 kelompok, yaitu bersifat
toksik sedang terdiri dari unsur-unsur Cr, Ni, dan Co, sedangkan bersifat tosik rendah
terdiri atas unsur Mn dan Fe (PPLH-IPB,1997; Sutamihardja et al., 1982, dalam
Marganof, 2003).
Logam berat berbahaya karena umumnya memiliki rapat massa tinggi dan
sejumlah konsentrasi kecil dapat bersifat racun dan berbahaya, yang termasuk
golongan logam berat adalah seluruh elemen logam kimia. Merkuri atau raksa (Hg),
kadmium (Cd), arsen (As), kromium (Cr), talium (Tl), dan timbal (Pb) adalah
beberapa contoh logam berat berbahaya. Logam berat merupakan komponen alami
tanah. Elemen ini tidak dapat didegradasi maupun dihancurkan (Supriharyono, 2006).
Logam berat memiliki beberapa sifat, diantaranya yang pertama sulit
didegradasi, sehingga mudah terakumulasi dalam lingkungan dan keberadaannya
secara alami sulit terurai (dihilangkan). Kedua, dapat terakumulasi dalam organisme
termasuk kerang dan ikan, dan akan membahayakan kesehatan manusia yang
mengkonsumsi organisme tersebut. Ketiga, mudah terakumulasi di sedimen, sehingga
konsentrasinya selalu lebih tinggi dari konsentrasi logam dalam air (PPLH, IPB,
1997; Sutamiharjda et al., 1982 dalam Marganof, 2003).
Berdasarkan Surat Keputusan Direktur Jenderal Pengawasan Obat dan
Makanan (Dirjen POM) Nomor. 03725/B/SK/VII/1989 tentang batas Maksimum
Cemaran Logam dalam makanan untuk biota laut dan hasil olahan sebesar 2 mg/kg
(ppm). Oleh karena itu perlu dilakukan penelitian mengenai kandungan logam berat
1.2Perumusan Masalah
Perairan muara Sungai Asahan dikenal sebagai penghasil kerang bulu
(Anadara inflata) utama di Sumatera Utara. Kawasan tersebut juga muara dari limbah
industri, kapal, rumah tangga dan minyak pelumas sisa kapal ke Sungai Asahan,
terutama dari kawasan sepanjang 10 kilometer yakni dari Kota Tanjung Balai hingga
ke perairan muara Sungai Asahan.
Melihat tingginya aktivitas masyarakat di sepanjang perairan muara Sungai
Asahan seperti pembuangan limbah industri, rumah tangga, transportasi serta sisa
pelumas dari kapal-kapal nelayan dapat menyebabkan terjadinya pencemaran logam
berat pada perairan muara Sungai Asahan seperti cadmium (Cd) dan Plumbum (Pb).
Berdasarkan Surat Keputusan Direktur Jenderal Pengawasan Obat dan Makanan
No.03725/B/SK/VII/1989 tentang batas Maksimum Cemaran Logam dalam makanan
untuk Biota laut dan hasil olahan sebesar 2 mg/kg(ppm).
Dampak negatif pencemaran di perairan muara Sungai Asahan menyebabkan
perubahan populasi biota laut, khususnya kerang bulu (Anadara inflata). Untuk
mengetahui sejauh mana kandungan logam berat Cd dan Pb pada kerang, sedimen
dan air yang terdapat di perairan muara Sungai Asahan perlu dilakukan penelitian. Ini
dilakukan karena kerang bulu (Anadara inflata) adalah salah satu spesies biota laut
yang merupakan bioindikator pencemaran (Palar, 2004).
1.3Tujuan Penelitian
1. Untuk mengetahui kadar logam berat Pb dan Cd pada daging kerang bulu
2. Untuk mengetahui kandungan logam berat Pb dan Cd di beberapa lokasi
perairan muara Sungai Asahan.
3. Untuk mengetahui kandungan logam berat Pb dan Cd pada sedimen di
beberapa lokasi perairan muara Sungai Asahan.
4. Untuk menganalisa korelasi kadar Pb dan Cd daging kerang bulu (Anadara
inflata) terhadap kandungan Pb dan Cd di beberapa lokasi perairan muara
Sungai Asahan (sedimen dan air).
1.4Hipotesis
1. Adanya perbedaan kandungan logam berat Pb dan Cd daging kerang bulu
(Anadara inflata) yang hidup pada beberapa lokasi di perairan muara Sungai
Asahan.
2. Adanya perbedaan kandungan logam berat Pb dan Cd pada beberapa lokasi
perairan muara Sungai Asahan.
3. Adanya perbedaan kandungan logam berat Pb dan Cd pada sedimen di
beberapa lokasi perairan muara Sungai Asahan.
4. Adanya korelasi kadar Pb dan Cd daging kerang bulu (Anadara inflata)
terhadap kandungan Pb dan Cd di beberapa lokasi perairan muara Sungai
Asahan (sedimen dan air).
1.5Manfaat Penelitian
1. Sebagai informasi bagi masyarakat mengenai kelayakan kerang bulu
2. Untuk mengetahui tingkat kontaminasi logam berat dalam air, sedimen dan
kerang bulu sebagai informasi bagi Pemkab Asahan, Kodya Tanjung Balai
dan Departemen Perikanan dan Kelautan dalam kaitanya dengan usaha
pemanfaatan sumberdaya perikanan daerah tersebut.
3. Sebagai informasi bagi Bapeldalda dalam kaitanya dalam masalah
penyusunan AMDAL dan ANDAL bagi industri yang menghasilkan limbah
BAB II
TINJAUAN PUSTAKA
2.1Pencemaran Laut
Laut Indonesia memiliki luas lebih kurang 5,6 juta km2 dengan garis pantai
sepanjang 81.000 km, dengan potensi sumberdaya, terutama perikanan laut yang
cukup besar, baik dari segi kuantitas maupun diversitasnya. Di sisi lain,
perkembangan ilmu pengetahuan dan teknologi memacu terjadinya pencemaran
lingkungan baik pencemaran air, tanah dan udara. Pencemaran air yang diakibatkan
oleh dampak perkembangan industri harus dapat dikendalikan, karena bila tidak
dilakukan sejak dini akan menimbulkan permasalahan yang serius bagi kelangsungan
hidup manusia maupun alam sekitarnya. Salah satu hal yang perlu dilakukan dalam
pengendalian dan pemantauan dampak lingkungan adalah melakukan analisis
unsur-unsur dalam ikan air laut, terutama kadmium (Cd) dan timbal (Pb).
Pencemaran logam-logam tersebut dapat mempengaruhi dan menyebabkan
penyakit pada konsumen, karena di dalam tubuh unsur yang berlebihan akan
mengalami detoksifikasi sehingga membahayakan manusia. Logam berat umumnya
bersifat racun terhadap makhluk hidup walaupun beberapa diantaranya diperlukan
dalam jumlah kecil. Melalui berbagai perantara, seperti udara, makanan, maupun air
yang terkontaminasi oleh logam berat, logam tersebut dapat terdistribusi ke bagian
tubuh manusia dan sebagian akan terakumulasikan. Jika keadaan ini berlangsung
terus menerus, dalam jangka waktu lama dapat mencapai jumlah yang
Pencemaran logam berat merupakan permasalahan yang sangat serius untuk
ditangani, karena merugikan lingkungan dan ekosistem secara umum. Sejak kasus
merkuri di Minamata Jepang pada 1953, pencemaran logam berat semakin sering
terjadi dan semakin banyak dilaporkan. Agen Lingkungan Amerika Serikat (EPA)
melaporkan, terdapat 13 elemen logam berat yang diketahui berbahaya bagi
lingkungan. Diantaranya arsenik (As), timbal (Pb), merkuri (Hg), dan kadmium (Cd).
Logam merupakan unsur esensial yang sangat dibutuhkan setiap makhluk
hidup, namun beberapa diantaranya (dalam kadar tertentu) bersifat racun. Di alam,
unsur ini biasanya terdapat dalam bentuk terlarut atau tersuspensi (terikat dengan zat
padat) serta terdapat sebagai bentuk ionik. Dampak dari pencemaran logam berat ini
sering dilaporkan.
Logam berat yang masuk ke sistem perairan, baik di sungai maupun lautan
akan dipindahkan dari badan airnya melalui tiga proses yaitu pengendapan, adsorbsi,
dan absorbsi oleh organisme-organisme perairan (Bryan, 1976 dalam Purnomo,
2008). Pada saat buangan limbah industri masuk ke dalam suatu perairan maka akan
terjadi proses pengendapan dalam sedimen. Hal ini menyebabkan konsentrasi bahan
pencemar dalam sedimen meningkat.
Logam berat yang masuk ke dalam lingkungan perairan akan mengalami
pengendapan, pengenceran dan dispersi, kemudian diserap oleh organisme yang
hidup di perairan tersebut. Pengendapan logam berat di suatu perairan terjadi karena
adanya anion karbonat hidroksil dan klorida (Hutagalung, 1984 dalam Purnomo,
mengendap di dasar perairan dan bersatu dengan sedimen sehingga kadar logam berat
dalam sedimen lebih tinggi dibanding dalam air (Hutagalung, 1991 dalam Purnomo,
2008).
2.1.1 Pengertian Logam Berat
Logam merupakan bahan pertama yang dikenal oleh manusia dan digunakan
sebagai alat-alat yang berperan penting dalam sejarah peradaban manusia (Darmono,
1995 dalam Purnomo, 2008). Logam berat masih termasuk golongan logam dengan
kriteria-kriteria yang sama dengan logam lain. Perbedaannya terletak dari pengaruh
yang dihasilkan bila logam berat ini berikatan dan atau masuk ke dalam organisme
hidup. Berbeda dengan logam biasa, logam berat biasanya menimbulkan efek-efek
khusus pada mahluk hidup (Palar, 2008).
Dapat dikatakan semua logam berat dapat menjadi tahan racun yang akan
meracuni tubuh mahluk hidup. Sebagai contoh adalah logam air raksa (Hg), cadmium
(Cd), timah hitam (Pb) dan khrom (Cr). Meskipun semua logam berat dapat
mengakibatkan keracunan atas mahluk hidup, sebagian dari logam berat tersebut tetap
dibutuhkan oleh mahluk hidup. Kebutuhan tersebut berada dalam jumlah yang
sedikit, tetapi bila kebutuhan dalam jumlah yang sangat kecil itu tidak terpenuhi,
maka dapat berakibat fatal terhadap kelangsungan hidup dari setiap mahluk hidup.
Karena dibutuhkan dalam tubuh maka disebut logam esensial, logam beresensial ini
Logam berat adalah unsur-unsur kimia dengan bobot jenis lebih besar dari 5
gr/cm3, terletak di sudut kanan bawah sistem periodik, mempunyai afinitas yang
tinggi terhadap unsur S dan biasanya bernomor atom 22 sampai 92 dari perioda 4
sampai 7 (Miettinen, 1977 dalam Purnomo, 2008). Sebagian logam berat seperti
timbal (Pb), kadmium (Cd), dan merkuri (Hg) merupakan zat pencemar yang
berbahaya. Afinitas yang tinggi terhadap unsur S menyebabkan logam ini menyerang
ikatan belerang dalam enzim, sehingga enzim bersangkutan menjadi tak aktif. Gugus
karboksilat (-COOH) dan amina (-NH2) juga bereaksi dengan logam berat.
Kadmium, timbal, dan tembaga terikat pada sel-sel membran yang menghambat
proses transpormasi melalui dinding sel. Logam berat juga mengendapkan senyawa
fosfat biologis atau mengkatalis penguraiannya (Manahan, 1977 dalam Marganof
2003).
2.1.2 Karakteristik Logam berat
Berdasarkan daya hantar panas dan listriknya, semua unsur kimia yang
terdapat dalam susunan berkala unsur-unsur dapat dibagi atas dua golongan yaitu
logam dan non logam. Golongan logam mempunyai daya hantar panas dan listrik
yang tinggi, sedangkan golongan non logam mempunyai daya hantar panas dan listrik
yang rendah. Berdasarkan densitasnya, golongan logam di bagi atas dua golongan,
yaitu golongan logam ringan dan logam berat. Golongan logam ringan (light metals)
mempunyai densitas <5, sedangkan logam berat (heavy metal) mempunyai densitas
Menurut Palar (2008) karakteristik dari logam berat adalah sebagai berikut:
1. Memiliki spesifikasi gravitasi yang sangat besar (>4).
2. Mempunyai nomor atom 22-34 dan 40-50 serta unsur lantinada dan aktanida.
3. Mempunyai respon biokimia (spesifik)pada organisme hidup.
Berbeda dengan logam biasa,logam berat biasanya menimbulkan efek-efek
khusus pada mahkluk hidup. Dapat dikatakan bahwa semua logam berat dapat
menjadi racun yang akan meracuni tubuh mahkluk hidup. Namun demikian sebagi
logam-logam berat tersebut tetap dibutuhkan dalam jumlah yang sedikit, tetapi
apabila tidak terpenuhi berakibat fatal terhadap kelangsungan hidup dari setiap
mahkluk hidup.
Salah satu polutan yang paling berbahaya bagi kesehatan manusia adalah
logam berat. WHO (World Health Organization) atau Organisasi Kesehatan Dunia
dan FAO (Food Agriculture Organization) atau Organisasi Pangan Dunia
merekomendasikan untuk tidak mengkomsumsi makanan laut (seafood) yang
tercemar logam berat. Logam berat telah lama dikenal sebagai suatu elemen yang
mempunyai daya racun yang sangat potensil dan memiliki kemampuan terakumulasi
dalam organ tubuh manusia. Bahkan tidak sedikit yang menyebabkan kematian. Di
antara logam berat yang berbahaya Cadmium (Cd) dan Timbal atau Plumbum (Pb).
1. Kadmium
Kadmium (Cd) menjadi populer sebagai logam berat yang berbahaya setelah
timbulnya pencemaran sungai di wilayah Kumamoto Jepang yang menyebabkan
menyebabkan penyakit “itai-itai”. Gejalanya ditandai dengan ketidak-normalan
tulang dan beberapa organ tubuh menjadi mati. Keracunan kronis yang
disebabkan oleh Cd adalah kerusakan sistem fisiologis tubuh seperti pada
pernapasan, sirkulasi darah, penciuman, serta merusak kelenjar reproduksi
jantung dan kerapuhan tulang (Friberg, et al, 1974 dalam Palar, 2008).
Kadmium telah digunakan secara meluas pada berbagai industri antara lain
pelapisan logam, peleburan logam, pewarnaan, baterai, minyak pelumas, bahan
bakar. Bahan bakar dan minyak pelumas mengandung Cd sampai 0,5 ppm,
batubara mengandung Cd sampai 2 ppm, pupuk superpospat juga mengandung Cd
bahkan ada yang sampai 170 ppm.
Limbah cair dari industri dan pembuangan minyak pelumas bekas yang
mengandung Cd masuk ke dalam perairan laut serta sisa-sisa pembakaran bahan
bakar yang terlepas ke atmosfir dan selanjutnya jatuh masuk ke laut. Konsentrasi
Cd pada air laut yang tidak tercemar adalah kurang dari 1 mg/l atau kurang dari 1
mg/kg sedimen laut. Konsentrasi Cd maksimum dalam air minum yang
diperbolehkan oleh Depkes RI dan WHO adalah 0,01,mg/l. Sementara batas
maksimum konsentrasi atau kandungan Cd pada daging makanan laut mg/kg.
Sebaliknya Dirjen Pengawasan Obat dan Makanan merekomendasikan tidak lebih
dari 2,0 mg/kg.
3 Timbal (Pb)
Timah hitam (Pb) adalah jenis logam yang lunak dan berwarna coklat
sulfide logam (Pbs) yang sering disebut galena (Darmono, 1995, dalam Afrizal
2000). Timbal masuk keperairan melalui pengendapan, jatuhan debu yang
mengandung Pb yaitu dari hasil pembakaran bensin yang mengandung tetra etil,
erosi dan limbah industri (Saeni, 1989, dalam Afrizal 2000). Pada hewan dan
manusia timbal dapat masuk ke dalam tubuh melalui makanan dan minuman yang
di komsumsi serta melalui pernafasan dan penetrasi pada kulit. Di dalam tubuh
manusia, di dalam tubuh manusia, dapat menghambat aktivitas enzim yang
terlibat dalam pembentukan haemoglobin yang dapat menyebabkan anemia.
Gejala yang di akaibatkan dari keracunan logam timbal adalah kurangya nafsu
makan, kejang-kejang, muntah dan pusing-pusing. Timbal dapat juga menyerang
susunan saraf dan mengganggu system reproduksi, kelainan ginjal dankelainan
jiwa (Palar, 2008).
2.1.3 Dampak Negatif Logam Berat Bagi Manusia
Masing-masing logam berat memiliki dampak negatif terhadap manusia jika
dikonsumsi dalam jumlah yang besar dan waktu yang lama. Dampak tersebut antar
lain :
1. Timbal (Pb)
Dalam peredaran darah dan otak dapat menyebabkan gangguan sintesis
hemoglobin darah, gangguan neurologi (susunan syaraf), gangguan pada ginjal,
sistem reproduksi, penyakit akut atau kronik sistem syaraf, dan gangguan fungsi
beberapa tanda yang mendahului efek keracunan sebelum terjadinya koma,
kemudian kematian (Palar, 2008)
2. Kadmium (Cd)
Jika berakumulasi dalam jangka waktu yang lama dapat menghambat kerja
paru-paru, bahkan mengakibatkan kanker paru-paru, mual, muntah, diare, kram,
anemia, dermatitis, pertumbuhan lambat, kerusakan ginjal dan hati, dan gangguan
kardiovaskuler. Kadmium dapat pula merusak tulang (osteomalacia,
osteoporosis) dan meningkatkan tekanan darah. Gejala umum keracunan
Kadmium adalah sakit di dada, nafas sesak (pendek), batuk – batuk, dan lemah
(Palar, 2008)
3. Merkuri (Hg)
Dapat berakumulasi dan terbawa ke organ-organ tubuh lainnya, menyebabkan
bronchitis, sampai rusaknya paru-paru. Gejala keracunan Merkuri tingkat awal,
pasien merasa mulutnya kebal sehingga tidak peka terhadap rasa dan suhu, hidung
tidak peka bau, mudah lelah, gangguan psikologi (rasa cemas dan sifat agresif),
dan sering sakit kepala. Jika terjadi akumulasi yang tinggi mengakibatkan
kerusakan sel-sel saraf di otak kecil, gangguan pada luas pandang, kerusakan
sarung selaput saraf dan bagian dari otak kecil. Gejala lain kesulitan menelan,
buta tuli, lumpuh kelainan fungsi ginjal, cacat lahir dan membawa kematian
2.2Kasus Pencemaran Logam Berat Di Indonesia
Teluk Buyat, terletak di Kabupaten Minahasa, Sulawesi Utara, adalah lokasi
pembuangan limbah tailing (lumpur sisa penghancuran batu tambang) milik PT.
Newmont Minahasa Raya (NMR). Sejak tahun 1996, perusahaan asal Denver, AS,
tersebut membuang sebanyak 2.000 ton limbah tailing ke dasar perairan Teluk Buyat
setiap harinya. Sejumlah ikan ditemui memiliki benjolan semacam tumor dan
mengandung cairan kental berwarna hitam dan lendir berwarna kuning keemasan.
Fenomena serupa ditemukan pula pada sejumlah penduduk Buyat, dimana mereka
memiliki benjol-benjol di leher, payudara, betis, pergelangan, pantat dan kepala.
Sejumlah laporan penelitian telah dikeluarkan oleh berbagai pihak sejak 1999
hingga 2004. Penelitian-penelitian ini dilakukan sebagai respon atas pengaduan
masyarakat nelayan setempat yang menyaksikan sejumlah ikan mati mendadak,
menghilangnya beberapa jenis ikan, serta keluhan kesehatan pada masyarakat. Dari
laporan-laporan penelitian tersebut, ditemukan kesamaan pola penyebaran
logam-logam berat seperti Arsen (As), Antimon (Sb), dan Merkuri (Hg) dan Mangan (Mn),
dimana konsentrasi tertinggi logam berbahaya tersebut ditemukan di sekitar lokasi
pembuangan tailing Newmont.
Hal ini mengindikasikan bahwa pembuangan tailing Newmont di Teluk Buyat
merupakan sumber pencemaran sejumlah logam berbahaya. Namun demikian,
sejumlah Menteri, diantaranya Menteri Lingkungan Hidup Nabiel Makarim,
mengeluarkan pernyataan bahwa Teluk Buyat tidak tercemar. Menteri Kesehatan
Achmad Sujudi bahkan mengatakan seolah-olah penyakit yang diderita oleh
2.3Pencemaran Logam Berat Pada Wilayah Pesisir
Wilayah pesisir daerah pertemuan antara darat dan laut, ke arah darat meliputi
bagian daratan, baik kering mapun terendam air yang masih dipengaruhi sifat-sifat
laut seperti pasang surut,dan pembebasan air asin sedangkan ke arah laut meliputi
bagian laut yang masih dipengaruhi oleh proses-proses alami yang terjadi di darat
seperti sedimentasi dan aliran air tawar maupun yang disebabkan oleh kegiatan
manusia seperti sedimentasi dan aliran air tawar maupun yang disebabkan oleh
kegiatan manusia seperti pencemaran (Dahuri et al,.1996). Jadi wilayah pesisir
merupan ekosistem yang paling rawan terkena dampak kegiatan manusia. Menurut
Sutamiharja et al, (1982), dalam Zubayr (2009), faktor-faktor penyebab pencemaran
adalah :
1. Erosi dan sedimentasi yang disebabkan oleh rusaknya hutan di daerah hulu
sungai yang bermuara ke laut serta penggalian pasir dan kerikil di sungai-sungai
tersebut.
2. Limbah pertanian berupa sisa pestisida dan pupuk yang digunakan dalam usaha
peningkatan produksi pertanian yang masuk ke dalam sistem perairan dan
akhirnya sampai keperairan laut.
3. Air selokan dari kota yang mengandung berbagai bahan, yang kemudian masuk
melalui sungai dan bermuara keperairan.
4. Permasalahan yang pokok dari aktivitas perminyakan yang dapat menimbulkan
a. Masalah operasional berupa ceceran minyak dan buangan secara kontinyu;
pembuangan air bekas pencucian tanki dan kapal.
b. Masalah kecelakaan berupa gangguan transortasi seperti pecahnya pipa-pipa
penyalur tanki penimbunan, kandasnya kapal tanki, dan tumpahan minyak
yang berasal dari kegiatan di pelabuhan.
5. Pembangkit listrik tenaga uap (PLTU), berupa air panas yang berasal dari air
pendingin yang dibuang ke perairan sehingga akan meningkatkan suhu perairan,
akibat pembuangan air panas tersebut akan menimbulkan masalah lingkungan
terutama bagi organisme akuatik yang hidup di sekitar perairan tersebut.
6. Industri, peningkatan jumlah industri yang pesat disamping memberi dampak
positif terhadap peningkatan perekonomian penduduk, juga menimbulkan
masalah terhadap lingkungan, akibat limbah yang di hasilkan oleh industri.
Logam berat masuk kedalam perairan melalui air hujan, aliran air permukaan,
erosi korofikasi batuan mineral, dan berbagai kegiatan manusia seperti aktivitas
industri, pertambangan, pengolahan atau penggunaan logam dan bahan yang
mengandung logam. Kelarutan logam berat dalam air bisa berubah menjadi lebih
tinggi atau lebih rendah, tergantung kondisi lingkungan perairan. Pada perairan yang
kekurangan oksigen akibat tingginya konsentrasi bahan organik, kelarutan beberapa
jenis logam, seperti Zn, Cd, Pb dan Hg, semakin rendah dan lebih mudah mengendap.
Logam berat yang masuk ke sistem perairan baik di sungai maupun lautan akan
dipindahkan dari badan airnya melalui tiga proses yaitu pengendapan, adsorbsi, dan
Dalam perairan, logam berat dapat ditemukan dalam bentuk terlarut dan tidak
terlarut. Logam berat terlarut adalah logam yang membentuk komplek dengan
senyawa organik dan anorganik, sedangkan logam berat yang tidak terlarut
merupakan partikel-partikel yang berbentuk koloid dan senyawa kelompok metal
yang teradsorbsi pada partikel-partikel yang tersuspensi (Razak, 1980 dalam Zubayr
2009). Masuknya logam berat ke dalam tubuh organisme perairan dapat melalui
rantai makanan dan difusi melalui kulit dan insang selanjutnya di dalam tubuh biota
perairan akanterjadi bioakumulasi dan biomagnifikasi logam berat hal ini
mengakibatkan “factor concentrate” (rasio konsentrasi logam berat dalam tubuh
organisme dan konsentrasi dalam badan air semakin meningkat) (Hutagalung et al.,
1999 dalam Zubayr, 2009).
Secara alamiah logam berat terdapat dalam laut namun kadarnya sangat rendah,
yaitu berkisar 10-5-10-2 ppm. Dalam kondisi alamiah ini logam berat dibutuhkan
organisme hidup untuk pertumbuhan dan perkembangan hidupnya (Philips, 1980
dalam Hutagalung, 1997). Bahkan kadar logam berat yang rendah dalam suatu
perairan dapat menyababkan berbagai organisme yang hidup didalamnya menderita
defisiensi (Bryan, 1976 dalam Hutagalung, 1991). Pencemaran logam berat terhadap
alam lingkungan estuaria merupakan suatu proses yang erat hubunganya dengan
penggunaan logam tersebut oleh manusia. Pada air laut di lautan lepas kontaminasi
logam berat biasanya terjadi secara langsung dari atmosfer atau karena tumpahan
minyak dari kapal tanker yang melaluinya. Sedangkan di daerah sekitar pantai
kontaminasi logam kebanyakan berasal dari mulut sungai yang terkontaminasi oleh
Tabel 2.1. Kadar Normal dan Kadar Maksimum Logam Berat yang Masuk
(B) Environmental Protection Agency (EPA),1973 dalam
Hutagalung,1991.
Menurut Lhacher dan Goldstein (1996 dalam Bahri 2003), logam berat secara
alami berasal dari proses geologi secara alami, pertambangan dan aktivitas industri.
Selanjutnya Clark (1986 dalam Bahri 2003) membagi logam untuk kepentingan
Biologi dalam tiga kelompok yaitu :
1. Logam ringan (seperti natrium, kalium, kalsium dan sebagainya), biasanya di
angkut sebagai kation aktif di dalam larutan encer.
2. Logam transisi (seperti besi, tembaga, kobal dan mangan), diperlukan dalam
konsentrasi yang tinggi
3. Logam berat dan metalloid (raksa, timah hitam, selenium dan arsen) umumnya
tidak diperlukan dalam kegiatan metabolism dan dapat menjadi bahan yang
beracun pada sel dan organisme tertentu walaupun pada konsentrasi rendah.
Logam berat adalah unsur yang mempunyai densitas, lebih besar dari
5 gram cm-3 mempunyai nomor atom lebih besar dari 21 dan terdapat pada bagian
tengah dari faktor unsur-unsur periodik (Bahri, 2003). Diketahui ada 18 logam berat
organisme, misalnya Cu dan Zn tetapi dalam jumlah berlebih dapat bersifat racun
bagi organisme (Bryan, 1976;Valke dan Walker, 1970 dalam Afrizal 2000). Dalam
kenyataannya logam berat Cd dan Pb juga sangat berbahaya bagi kehidupan
organisme walaupun dalam konsentrasi yang sangat rendah.
Logam berat ini mempunyai sifat “Biomagnifikasi” artinya dapat berakumulasi
dalam jaringan organisme dan melalui rantai makanan akhirnya membahayakan
kehidupan manusia (Dahuri, 2003). Logam yang berbahaya dapat menyebabkan
toksin dan bersifat agak permanen dan mempunyai waktu paruh yang lama adalah
Cadmium(Cd), Plumbum(Pb) dan air raksa (Palar, 2008).
2.4 Sumber Logam Berat Pb dan Cd di Perairan
Timbal (Pb) dan persenyawaan dapat berada di dalam badan perairan secara
alamiah dan sebagai dampak dari aktivitas manusia. Menurut Palar, (2008) Pb dapat
masuk ke badan perairan melalui penkristalan Pb di udara dengan bantuan air hujan,
di samping itu proses porosifikasi dalam bantuan mineral akibat hempasan ombak
dan angin, juga merupakan salah satu jalur sumber Pb yang akan masuk kedalam
badan perairan. Timbal (Pb) yang masuk kedalam perairan sebagai dampak dari
aktifitas kehidupan manusia ada berbagai macam bentuk, diantaranya adalah air
buangan (limbah) dari industri yang berkaitan dengan Pb, air buangan dari
pertambangan biji timah hitam dan buangan sisa industri baterai. Buangan-buangan
tersebut akan jatuh pada jalur-jalur perairan seperti anak-anak sungai dan kemdian
perindustrian yang menggunakan Pb akan merusak tata lingkungan perairan yang di
masukinya menjadikan sungai dan alurnya tercemar.
Logam kadmium (Cd) mempunyai penyebaran yang sangat luas di alam.
Penggunaan Cd yang paling utama adalah sebagai stabiliser (penyeimbang) dan
pewarna plastik dan elektroplating (penyepuh/pelapisan logam). Selain itu di gunakan
pula penyolderan dan pencampuran logam serta indusri baterai. Akumulasinya dalam
air tanah antara lain diakibatkan oleh kegiatan elektroplating (pelapisan emas dan
perak), pengerjaan bahan-bahan dengan menggunakan pigmen/zat warna lainnya,
tekstil dan industri kimia (Darmono, 1995). Selanjutnya Palar, (2008) logam
cadmium dan bermacam-macam bentuk persenyawaan dapat masuk kelingkungan,
terutama seali merupakan efek samping dari aktivitas yang dilakukan manusia. Boleh
dikatakan bahwa semua industri yang melibatkan Cd dalam proses opreasional
industrinya menjadi sumber pencemaran Cd. Logam Cd membawa sifat racun yang
sangat merugikan bagi bagi semua organisme hidup, bahkan juga sangat berbahaya
untuk manusia.
Dalam badan perairan, kelarutan Cd dalam konsentrasi tertentu dapat
membunuh biota perairan. Secara sederhana dapat diketahui bahwa kandungan logam
Cd akan dapat dijumpai di daerah-daerah penimbunan sampah dan aliran air hujan,
selain dalam air buangan. Penelitian yang pernah dilakukan untuk mengetahui sumber
dari beberapa logam berat Cd dalam perairan Teluk New York, dimana hasil yang
diperoleh menunjukkan bahwa sumber Cd dalam badan perairan yang dikontribusi
Jumlah yang paling besar dikontribusi oleh limbah padat yaitu 82% (Palar, 2008).
Selanjutnya Warlina, (2004) bahan buangan padat adalah bahan buangan yang
berbentuk padat, baik yang kasar atau yang halus, misalnya sampah, buangan tersebut
bila dibuang ke air menjadi pencemaran dan akan menimbulkan pelarutan,
pengendapan ataupun pembentukan koloidal.
2.5 Bioindikator Pencemaran Logam Berat
Dalam lingkungan perairan ada tiga media yang dapat dipakai sebagai
indikator pencemaran logam berat, yaitu air, sedimen dan organisme hidup.
Pemakaian organisme hidup sebagai indikator pencemaran inilah yang disebut
bioindikator (Fitriati, 2004).
Setiap lingkungan perairan alami dihuni oleh berbagai organisme hidup dan
semua organisme hidup ini berada dalam suatu sistem trofik (trophic level).
Masuknya bahan cemaran ke dalam perairan akan membunuh organisme yang paling
sensitif. Bila bahan cemaran terus masuk, maka organisme yang paling sensitif
berikutnya akan terbunuh. Demikian seterusnya, dan penambahan bahan cemaran
terakhir akanm membunuh moluska kelompok “filter feeder” pemakan serasah.
Pemasukan bahan cemaran ke lingkungan perairan dapat juga mengganggu daur
pakan (food cycle) (Fitriati, 2004)
Dalam penelitian pencemaran perairan laut, agar didapatkan data yang
betul-betul mewakili perairan yang diteliti, maka dari semua organisme hidup yang ada
menggambarkan kondisi lingkungan sebenarnya. Sebagai contoh, fitoplankton
walaupun memiliki kemampuan yang besar untuk mengakumulasi logam berat,
namun pemakaian fitoplankton sebagai bio-indikator kurang menggambarkan kondisi
lingkungan yang sebenarnya. Hal ini disebabkan gerakan fitoplankton sangat
dipengaruhi oleh arus dan gelombang laut. Pemakaian jenis-jenis ikan juga kurang
tepat karena gerakannya sangat luas. Kecuali kalau ikan tersebut tetap berada dalam
lingkungan perairan tertentu (tidak bermigrasi) seperti ikan baji-baji, Platycephalus
bassensis, atau Platycephalus indicus (Philips, 1980 dalam Fitriati, 2004).
Dalam pemilihan organisme laut sebagai bioindikator pencemaran, (Philips,
1980 dalam Fitriati, 2004) memberikan beberapa kriteria sebagai berikut:
1. Harus dapat mengakumulasi bahan cemaran tanpa dia sendiri mati terbunuh.
2. Harus terdapat dalam jumlah yang banyak di seluruh daerah penelitian.
3. Terikat pada suatu tempat yang keras agar bisa mewakili daerah yang diteliti.
4. Hidup dalam waktu yang lama untuk memungkinkan sampling lebih dari satu
tahun jika dibutuhkan.
5. Mudah diambil dan tidak mudah rusak. Philips (1980 dalam Fitriati, 2004)
menambah pedoman tersebut dengan hal-hal sebagai berikut:
Mempunyai toleransi terhadap air payau untuk memungkinkan penelitian di
daerah estuaria. Harus ada korelasi antara kadar bahan cemaran dalam air dan
organisme. Philips (1980 dalam Fitriati, 2004) menyatakan bahwa jenis kerang
(molusca, bivalvia) dan makro-algae merupakan bioindikator yang paling tepat dan
(Mytilus edulis). Kerang biru menjadi pilihan pertama karena disamping memenuhi
kriteria di atas, juga merupakan “highly specialized filterfeeder” dan mempunyai
toleransi yang besar terhadap perubahan lingkungan.
Pilihan kedua adalah tiram raksasa (Crassostrea gigas), karena merupakan
“filter feeder” dan makanannya terutama serasah yang berasal dari tumbuh-tumbuhan
dan hewan. Kerang biru (Mytilus edulis) telah dipakai sebagai bioindikator
pencemaran logam berat di negara-negara Eropa dan Amerika (Philip, 1980 dalam
Fitriati).
Tabel 2.2 Indikator Biologi dan Jenis-jenis Indikator
Indikator Biologi Jenis-Jenis Indikator
Phytoplanton (jenis plankton tanaman)
Besi (Fe), Kobal (Co), Nikel (Ni), Plutonium (Pu), Cesium (Cs), Ytrum (Y), Tritum (H3)
Zooplankton (jenis plankton hewan)
Ytrium (Y), Kobalt (Co), Besi (Fe), Mangan (Mn), Srontium (Sr), Nikel (Ni), Zirkonium (Zr)
Mollusca (jenis kerang-kerangan)
Seng (Zn), Nikel (Ni), Tembaga (Cu), Kadmium (Kd), Cromium (Cr), Mangan (Mn), Cesium (Cs), Kobal (Co), Timbal (Pb).
Crustacea (udang-udangan)
Strintium (Sr), Tritium (H3), Ytrium (Y), Cesium (Cs), Kobal (Co), Seng (Zn), Mangan (Mn)
Ikan dan jenisnya Kadmium (Kd), Kromium (Cr), Mangan (Mn), Cesium (Cs),
Seng (Zn), Besi (Fe), Kobalt (CO)
2.6 Biologi Kerang Bulu (Anadara inflata)
Sistimatika kerang Anadara menurut Olsson (1961) adalah sebagai berikut:
Filum : Mollusca
Kelas : Pelecypoda (Lamellibranchiata)
Ordo : Eutaxodontida
Super famili : Arcacea
Famili : Arcidae
Sub famili : Anadarinae
Genus : Anadara
Spesies : Anadara inflata
Gambar. 2.1. Kerang bulu (Anadara inflata)
Ciri-ciri kelas Pelecypoda adalah mempunyai dua belah cangkang yang
simetris, mempunyai engsel dan ligamen pada bagian dorsal, mempunyai satu atau
dua pasang otot aduktor dan memiliki kaki berbentuk kapak. Ciri-ciri super famili
Arcacea pada umumnya mempunyai cangkang yang lonjong hampir pipih, menempel
Reinhard (1935) dalam Dody (1998) menerangkan bahwa ciri-ciri famili
Arcidae ialah memiliki dua otot aduktor yang hampir sama dalam ukuran, siphon
tidak ada palial-line biasanya ada dan lenkap engsel terletak pada bagian dorsal dan
dilengkapi dengan gigi yang melintang serta mempunyai insang. Tekstur cangkang
seperti porselen dan pada beberapa bagian sangat halus seperti mutiara. Pada
sebagian besar pustaka genus Anadara disebut cockle, mangrove-cockle atau
bloodv-cockle.
Menurut Hanada (1975), dalam Dody (1998), bivalvia bentik umumnya
melekat pada substrat dengan bysus pada stasiun larva, sedangkan yang dewasa
bergerak hampir bebas tanpa menempel pada substrat. Anadara (Scarpharca)
mengikuti pola dan oleh karena itu spatnya dapat dikumpulkan dengan kolektor.
Selanjutnya menurut Nishikawa (1977) Anadara dapat melekatkan dirinya pada
segala benda yang tersedia karena mempunyai byssus. Larva Anadara mulai hidup
sesil pada waktu juncture-nya 230 sampai 300 mikron atau 190 mikron ukuran
panjang cangkang (Dody, 1998).
Menurut Kira (1975), dalam Dody (1998) ciri-ciri Anadara sp adalah
memiliki cangkang setangkup kokoh dengan bentuk memanjang arah
posterior-ventral. Lapisan luar cangkang berbulu dan memiliki 38 lekukan (radial ribs).
Anadara biasanya ditemukan di sepanjang pantai yang ditumbuhi pohon bakau, itu
sendiri maupun diluarnya. Anadara hidup di daerah tropic pada lumpur halus atau
kadang-kadang pasir berlumpur dan terlindung atau berasosiasi dengan pohon-pohon
2.7 Spektroskopi Serapan Atom (SSA)
Metode spektroskopi serapan atom (SSA) pertama kali diperkenalkan oleh
Wals pada tahun 1953. Alat ini kemudian dikembangkan di Exhibition Melbourne of
Physical Institute dan dipublikasi pada tahun 1954. Wals menyatakan bahwa unsur
logam lebih mudah dan akurat ditentukan kadarnya dengan proses atomik
dibandingkan dengan proses emisi. Metode ini dapat menentukan 67 unsur logam.
Spektroskopi Serapan Atom (SSA) dan Flame Emision Spectrophotometer
(FES) adalah dua instrumen yang sangat potensial untuk menganalisa mineral.
Meskipun kegunaannya sama, masing-masing instrumen bekerja dengan prinsip yang
berbeda dan dengan kepekaan yang berbeda pula. Di dalam penetapan mineral suatu
bahan pangan dengan instrumen ini, terlebih dahulu bahan pangan harus diabukan
kemudian mineralnya diekstrak dengan asam. Larutan sampel yang mengandung
mineral kemudian dapat dianalisa langsung dengan SSA maupun FES (Vesilin et al.
1994)
Dalam analisis logam dengan menggunakan sistem flame, sampel diatomisasi
pada alat atomizer melalui nyala api dengan bahan bakar asetilen murni. Biasanya
logam yang dianalisis dengan flame AAS adalah Ca, Cd, Cu, dan Cr. Sedangkan
untuk analisis Hg dilakukan tanpa nyala, tetapi larutan sampel harus direduksi lebih
dahulu dengan SnCl. Uap hasil reduksi ditampung dalam tabung bercendela yang
Metode spektroskopi serapan atom berprinsip pada absorpsi cahaya oleh
atom. Atom-atom menyerap cahaya tersebut pada panjang gelombang tertentu,
tergantung pada unsurnya (Hutabarat, 1987).
2.8 Faktor Fisik Kimia Perairan
Faktor fisik dan kimia merupakan dua faktor pembatas distribusi populasi
selain faktor tingkah laku dan interaksi antara organisme. Setiap organisme
mempunyai kisaran toleransi faktor fisik dan kimia tertentu dalam menunjang
kehidupannya tergantung spesies dan lingkungannya serta keterkaitan antara
keduanya. Beberapa faktor fisik dan kimia antara lain:
1. Suhu
Suhu air di daerah estuaria biasanya memperlihatkan fluktuasi annual dan diurnal
yang lebih besar daripada di laut, terutama apabila estuaria tersebut dangkal dan
air yang masuk (pada saat pasang naik) ke perairan estuaria tersebut kontak
dengan daerah yang subtratnya terekspos (Supriharyono, 2006). Suhu merupakan
salah satu parameter penting dalam pertumbuhan dan perkembangan bivalvia.
Kerang Anodonta woodiana menyukai lingkungan dengan temperatur 24 – 29 °C.
(Thana, 1976 dalam Suwignyo, 1981). Selanjutnya menurut Winanto (2004) suhu
yang baik untuk kelangsungan hidup mutiara berkisar 25 – 30 °C. Suhu air pada
kisaran 27 – 31 °C juga dianggap cukup layak untuk kehidupan tiran mutiara
2. Kecerahan
Kejernihan air sangat ditentukan oleh partikel-partikel terlarut. Semakin banyak
partikel atau bahan organik terlarut maka kekeruhan akan meningkat. Kekeruhan
atau konsentrasi bahan tersuspensi dalam perairan akan menurunkan efisiensi
makan dari organisme pemakan suspensi (Levinton, 1982). Selanjutnya menurut
Romimohtarto (1991), kekeruhan tidak hanya membahayakan ikan tetapi juga
menyebabkan air tidak produktif karena menghalangi masuknya sinar matahari
untuk fotosintesa.
3. Biological Oxygen Demand (BOD)
Nilai BOD menyatakan jumlah oksigen yang dibutuhkan oleh mikroorganisme
aerobik dalam proses penguraian senyawa organik yang diukur pada temperatur
20 °C. Pengukuran yang umum dilakukan adalah pengukuran selama 5 hari atau
BOD5 (Forstner, 1990 dalam Barus, 2004). Angka BOD tinggi menunjukkan
terjadinya pencemaran organik di perairan. Brower et al (1990) menyatakan nilai
konsentrasi BOD5 menunjukkan kualitas suatu perairan masih tergolong baik
apabila konsumsi O2 selama 5 hari berkisar sampai 5 mg/l.
4. Chemical Oxygen Demand (COD)
Yaitu kebutuhan oksigen kimia untuk reaksi oksidasi terhadap bahan buangan di
dalam air, atau jumlah oksigen yang diperlukan agar bahan buangan yang ada di
5. Salinitas
Salinitas merupakan nilai yang menunjukkan jumlah garam-garam terlarut dalam
satuan volum air biasanya dinyatakan dalam satuan per mil ‰. Berdasarkan nilai
salinitas air diklasifikasikan sebagai berikut: air tawar <0,5 ‰, air payau (0,5 – 30
‰) laut (30 – 40 ‰) dan hiperhialin (>40 ‰) (Barus, 2004). Selanjutnya
komponen fauna di estuaria berdasarkan salinitasnya dikelompokkan menjadi 3
(tiga) yakni fauna air tawar, payau dan laut (Dahuri, 2003). Menurut
Romimohtarto, (1985) menyatakan pada salinitas 18‰ keberhasilan menempel
kerang darah (Anadara granosa) lebih tinggi. Tiram dapat hidup dalam perairan
dengan salinitas yang lebih rendah daripada salinitas untuk kerang hijau dan
kerang darah.
6. pH
Nilai pH menyatakan konsentrasi ion hydrogen dalam suatu larutan. pH sangat
penting sabagai parameter kualitas air karena mengontrol tipe dan laju kecepatan
reaksi di dalam air. Nilai pH yang ideal bagi kehidupan organisme pada umumnya
antara 7-8,5. Kodisi perairan yang sangat asam maupun sangat basa akan
membahayakan kelangsungan hidup organisme karena akan menyebabkan
terjadinya gangguan metabolisme dan respirasi (Barus, 2004). Menurut
Romimohtarto (1985), pH permukaan laut Indonesia pada umumnya antara 6,0–
7. Substrat
Hewan bivalvia sebagai makrozobentos umumnya hidup pada dasar perairan.
Substrat yang disukai, berpasir dan berlumpur. Pennak (1989) dalam Prihatini
(1999) menyatakan bahwa lingkungan yang disukai kerang famili Anodontidae
adalah substrat pasir atau campuran dengan material lain, namun beberapa jenis
Anodonta menyukai lumpur.
8. Oksigen terlarut (Disolved Oxigen)
Distribusi oksigen terlarut di laut dikendalikan oleh 1) pertukaran dengan atmosfir
secara difusi, 2) proses fotosintesis oleh fitoplankton oleh tumbuhan air, 3)
respirasi oleh organisme autotrof dan heterotrof serta proses perombakan bahan
BAB III
BAHAN DAN METODE
3.1 Waktu dan Tempat
Penelitian ini dilaksanakan pada bulan Agustus 2009 di Muara Sungai
Asahan, Tanjung Balai, Kabupaten Asahan, yang secara geografis terletak pada
03o01’00”LU dan 99o51’30” BT.
3.2 Metoda Penelitian
Metode yang digunakan dalam penentuan lokasi sampling untuk pengambilan
sampel ikan adalah ”Purposive Random Sampling” pada 3 (tiga) stasiun pengamatan.
Pada masing-masing stasiun dilakukan 3 kali ulangan pengambilan sampel.
3.3 Deskripsi Area
Di perairan Muara Sungai Asahan ini banyak terdapat aktivitas, seperti
pelabuhan, pemukiman, daerah mangrove, dan berbagai aktivitas lain yang dapat
berpengaruh terhadap perairan.
3.3.1 Stasiun 1
Stasiun ini secara geografis terletak pada 0,3o3,33,8”LU dan 99o51’22,3” BT,
daerah ini merupakan muara berjarak 3 mil dari pantai. Denah dan lokasi penelitian
3.3.2 Stasiun 2
Stasiun ini secara geografis terletak pada 3o5’00,3”LU dan 99o50’18,1” BT
Daerah ini berjarak 4 mil dari pantai. Denah dan lokasi penelitian dapat dilihat pada
Lampiran H.
3.3.3 Stasiun 3
Stasiun ini secara geografis terletak pada 3o4’15’7”LU dan 99o50’2,6” BT.
Daerah ini berjarak 5 mil dari pantai. Denah dan lokasi penelitian dapat dilihat pada
Lampiran H.
3.4 Alat dan Bahan
Bahan yang digunakan dalam penelitian ini adalah kerang bulu (Anadara
inflata),contoh air dan lumpur dari setiap stasiun dan bahan-bahan kimia untuk
analisa dan pengawet sampel. Alat penelitian yang digunakan mencakup alat-alat
lapangan dan laboratorium, untuk mengambil sedimen digunakan Birge-Ekman Grab.
Adapun alat dan bahan yang digunakan untuk penelitian ini dapat dilihat pada Tabel
Tabel 3.1. Alat dan Bahan yang Digunakan dalam Penelitian
No Alat dan Bahan Dosis (%) Kegunaan Keterangan 1. Mengukur massa kerang Pemanas sampel
3.5 Metode Pengambilan Sampel
3.5.1 Kerang Bulu (Anadara inflata)
Pengambilan sampel kerang bulu dilakukan masing-masing 3 kali ulangan dan
menggunakan alat penangkap kerang (garuk), alat ini biasa digunakan oleh nelayan.
Pada setiap stasiun sebanyak 3 kali ulangan. Alat penangkap kerang (garuk)
dimasukkan ke dasar perairan, kemudian diseret sedemikian rupa, lalu ditarik ke atas
permukaan lalu disaring. Sampel kerang yang didapatkan dibersihkan dan disortir,
kemudian dimasukkan ke plastik dan diberi label. Sampel dibawa ke laboratorium
Bappedalda Sumatera Utara.
Pengukuran Cd dan Pb dalam daging kerang dilakukan di laboratorium
Bapedalda (Sumut). Kerang Bulu dicuci dan dipisahkan daging dari kulitnya. Setelah
itu ke dalam sampel daging kerang bulu ditambahkan 25 ml aqua dan 10 ml HNO3
menit atau sampai volume menjadi 10 ml dan didinginkan. Kemudian ditambahkan
HNO3 (p) sebanyak 5 ml dan HClO4 sebanyak 3 ml sampai timbul asap putih dan
filtrate jernih. Setelah asap putih timbul, teruskan pemanasan lebih kurang 30 menit,
lalu didinginkan dan disaring. Kemudian masukkan ke dalam labu ukur 50 ml sampai
tanda tera (tanda batas). Selanjutnya diukur kadar Cd dan Pb dengan AAS (Atomic
Absorption Spectrophotometer).
3.5.2 Air
Untuk pengambilan sampel air pada permukaan dilakukan dengan
menggunakan ember, sedangkan untuk pengambilan sampel air pada kedalaman 1,2
m, 1,5 m dilakukan dengan menggunakan lamnot. Panjang tali lamnot disesuaikan
dengan kedalaman yang diinginkan kemudian dimasukkan ke dalam badan air untuk
mendapatkan sampel air. Sampel air yang diperoleh dituang ke dalam botol alkohol.
Kemudian botol alkohol ditutup dan diberi label. Sampel air di bawa ke laboratorium.
Pengukuran Cd dan Pb air dilakukan di laboratorium Bapedalda (Sumut).
Pengukuran logam berat digunakan dengan metoda AAS (Atomic Absorbtion
Spectrophotometer) tipe Shimadzu, series AA-6200. Alat ini dapat mendeteksi
kandungan logam berat dalam contoh dengan batas deteksi untuk masing-masing
logam berat adalah: Cd ≥ 0.004 ppm,Pb ≥ 0,01 ppm.
3.5.3 Sedimen
Sampel lumpur/sedimen diambil dengan menggunakan eckman grabb. Alat