PEMANFAATAN LIMBAH PADAT
NATA DE COCO
UNTUK
PRODUKSI BIOETANOL MENGGUNAKAN
Zymomonas mobilis
SITI PUSPITASARI
DEPARTEMEN TEKNOLOGI INDUSTRI PERTANIAN FAKULTAS TEKNOLOGI PERTANIAN
INSTITUT PERTANIAN BOGOR BOGOR
PERNYATAAN MENGENAI SKRIPSI DAN
SUMBER INFORMASI SERTA PELIMPAHAN HAK CIPTA
Dengan ini saya menyatakan bahwa skripsi berjudul Pemanfaatan Limbah Padat Nata de Coco untuk Produksi Bioetanol Menggunakan Zymomonas mobilis
adalah benar karya saya dengan arahan komisi pembimbing dan belum diajukan dalam bentuk apa pun kepada perguruan tinggi mana pun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir skripsi ini.
Dengan ini saya melimpahkan hak cipta dari karya tulis saya kepada Institut Pertanian Bogor.
Bogor, Agustus 2014
Siti Puspitasari
ABSTRAK
SITI PUSPITASARI. Pemanfaatan Limbah Padat Nata de Coco untuk Produksi Bioetanol Menggunakan Zymomonas mobilis. Dibimbing oleh MUHAMMAD ROMLI.
Dalam proses hilir produksi nata de coco dihasilkan limbah produk berupa kulit ari, sisa potongan, dan yang tidak lolos sortasi berkisar 10% dari total produksi. Limbah tersebut mengandung selulosa yang dapat dimanfaatkan menjadi bioetanol sebagai energi alternatif. Penelitian ini bertujuan untuk mengevaluasi potensi pemanfaatan limbah nata de coco untuk produksi bioetanol. Praperlakuan bahan dilakukan dengan menghidrolisis nata de coco menggunakan enzim selulase. Proses fermentasi dilakukan dengan menggunakan Zymomonas mobilis pada suhu kamar selama 72 jam. Analisis produk dilakukan setiap 12 jam. Dalam penelitian ini dievaluasi pengaruh tingkat penggunaan konsentrasi inokulum Zymomonas mobilis, yaitu 10% dan 15% (v/v) dan pengaruh penambahan urea sebagai nutrisi. Hidrolisis dengan enzim selulase sebesar 30IU/g serat kasar menghasilkan hidrolisat sebesar 1.77 L/kg bahan dan meningkatkan gula pereduksi 0.08 g/L menjadi 6.8 g/L. Pemakaian 15% inokulum menghasilkan kadar etanol yang lebih tinggi yaitu 0.27% (v/v) dibandingkan dengan 10% inokulum yaitu 0.2% (v/v). Penambahan urea sebesar 2.9 g/L substrat meningkatkan kadar etanol dari 0.2% menjadi 0.25% pada tingkat 10% inokulum dan dari 0.27% menjadi 0.3% pada tingkat 15%. Kadar etanol tertinggi dihasilkan oleh inokulum 15% (v/v) dengan penambahan nutrisi dan yield (p/s) yang dihasilkan adalah 0.49±0.02 (g/g). Waktu optimum fermentasi adalah 48 jam dan kadar gula tersisa 22.4±0.8%. Hasil analisis kelayakan finansial menunjukkan nilai R-C ratio sebesar 0.3.
ABSTRACT
SITI PUSPITASARI. Utilization of Nata de Coco Solid Waste for Bioethanol Production by Zymomonas mobilis. Supervised by MUHAMMAD ROMLI.
Production of nata de coco generates waste in the forms of skin, the residual and the pieces of nata that do not meet spesification as product and it can reach to 10% of the total production. The waste contains cellulose that can be utilized for bioethanol production as an energy alternative. This research aims to evaluate the potential utilization of nata de coco waste for bioethanol production. Pretreatment of material was done by hydrolyzing nata de coco using the enzyme cellulase. The fermentation process was done using Zymomonas mobilis at room temperature for 72 hours. Analysis of the products was carried out every 12 hours. This research evaluated the influence of the concentration level of Zymomonas mobilis inoculum, i.e. 10% and 15% (v/v) and the influence of the addition of urea as nutrients. Concentration of enzyme cellulose that used to hydrolyze was 30IU/g fibers produces hydrolizate as much 1.77 L/kg of materials and increased reducing sugar from 0.08 g/L to 6.8 g/l. The use of 15% inoculums produces higher ethanol levels of 0.27% (v/v) compared to 10% inoculums, which is 0.2% (v/v). The addition of 2.9 g/L urea increases the levels of ethanol from 0.2% to 0.25% on 10% inoculums and from 0.27% to 0.3% on 15% inoculums. The highest bioethanol concentration was produced by 15% inoculums with addition of nutrition and the yield (p/s) achieved 0.49±0.02 (g/g). Optimum fermentation time is 48 hours with residuce 22.4±0.8% sugar levels. The result of financial visibility analyze show that R-C ratio value is 0.3.
PEMANFAATAN LIMBAH PADAT
NATA DE COCO
UNTUK
PRODUKSI BIOETANOL MENGGUNAKAN
Zymomonas mobilis
SITI PUSPITASARI
Skripsi
Sebagai salah satu syarat untuk memperoleh gelar Sarjana Teknologi Pertanian
pada
Departemen Teknologi Industri Pertanian
DEPARTEMEN TEKNOLOGI INDUSTRI PERTANIAN FAKULTAS TEKNOLOGI PERTANIAN
INSTITUT PERTANIAN BOGOR BOGOR
Judul Skripsi : Pemanfaatan Limbah Padat Nata de Coco untuk Produksi Bioetanol Menggunakan Zymomonas mobilis
Nama : Siti Puspitasari
NIM : F34100077
Disetujui oleh
Prof. Dr. Ir. Muhammad Romli, M.Sc. Pembimbing
Diketahui oleh
Prof. Dr. Ir. Nastiti Siswi Indrasti Ketua Departemen
PRAKATA
Puji dan syukur peneliti panjatkan kepada Allah SWT atas segala karunia-Nya sehingga karya ilmiah ini berhasil diselesaikan. Tema yang dipilih dalam penelitian yang dilaksanakan sejak bulan Februari 2014 sampai Mei 2014 ialah bioenergi, dengan judul Pemanfaatan Limbah Padat Nata de Coco untuk Produksi Bioetanol Menggunakan Zymomonas mobilis.
Terima kasih penulis ucapkan kepada Prof. Dr. Ir. H Muhammad Romli, M.Sc. selaku pembimbing. Di samping itu, penghargaan penulis sampaikan kepada segenap dosen Teknologi Industri Pertanian, dan Departemen Teknologi Industri Pertanian, serta Beasiswa Lippo atas rekomendasi dari Direktorat Kemahasiswaan IPB yang telah memberi dukungan kepada penulis sehingga penelitian dapat dilaksanakan dengan lancar. Ungkapan terima kasih juga disampaikan kepada Alm. Bapak dan Ibu yang selalu memberikan dorongan untuk selalu menghasilkan yang terbaik.
Semoga karya ilmiah ini bermanfaat
Bogor, Agustus 2014
DAFTAR ISI
DAFTAR TABEL
DAFTAR GAMBAR
DAFTAR LAMPIRAN
PENDAHULUAN 1
Latar Belakang 1
Perumusan Masalah 2
Tujuan Penelitian 2
Lingkup Penelitian 2
METODOLOGI PENELITIAN 3
Bahan dan Peralatan 3
Metode Penelitian 3
HASIL DAN PEMBAHASAN 6
Karakteristik Nata de Coco 6
Hidrolisis 7
Penentuan Persentase Penambahan Nutrisi pada Media Fermentasi 10
Hasil Fermentasi 11
Kadar etanol 11
Penggunaan Gula Pereduksi 13
Pertumbuhan Biomassa 14
Hasil Fermentasi Kondisi Media Terpilih 16
Kinetika Fermentasi 17
Analisis Kelayakan Finansial 18
Keuntungan 20
SIMPULAN DAN SARAN 22
Simpulan 22
Saran 22
DAFTAR PUSTAKA 22
LAMPIRAN 25
DAFTAR TABEL
1 Veriabel perlakuan 5
2 Komposisi kimia nata de coco (pada 100 g berat basah) 6
3 Karakteristik limbah padat nata de coco 6
4 Kadar gula hasil hidrolisis 9
5 Hasil analisis perbandingan gula pereduksi pada dosis enzim 30 IU/g serat 10 6 Penghitungan kebutuhan urea (gram) dalam 100 ml substrat 10
7 Rincian penerimaan 18
8 Rincian biaya investasi 19
9 Rincian biaya tetap 20
10 Rincian biaya variabel 20
11 Hasil keuntungan dan R-C ratio bioetanol 21
DAFTAR GAMBAR
1 Diagram alir tahapan penelitian 4
2 Konsentrasi etanol selama proses fermentasi 72 jam 12 3 Kadar gula pereduksi selama proses fermentasi 72 jam 13 4 Konsentrasi biomassa sel selama proses fermentasi 72 jam 15 5 Grafik hubungan antara kadar etanol, biomassa sel, dan kadar gula sisa 16
6 Kurva standar fenol sulfat 26
7 Kurva standar DNS 27
8 Kurva standar aktivitas enzim 28
DAFTAR LAMPIRAN
1 Analisis karakterisasi bahan 25
2 Uji aktivitas enzim 27
3 Analisis hasil fermentasi 28
4 Analisis hasil hidrolisis 28
5 Neraca massa proses hidrolisis 29
6 Data hasil fermentasi 29
PENDAHULUAN
yang luas dan bernilai jual tinggi (AgroTekno 2013).PT Daya Agro Mitra Mandiri merupakan perusahan yang bergerak sebagai
supplier nata de coco antara para petani dan perusahaan besar minuman nata de coco. Perusahaan tersebut melakukan proses pengupasan kulit ari, sortasi, pencetakan, dan pencucian nata de coco. Dalam proses tersebut, terdapat nata yang tidak dapat dijadikan sebagai produk sehingga menghasilkan limbah padat yang menumpuk dan menimbulkan dampak estetika seperti bau yang tidak enak yang sering menjadi masalah bagi masyarakat sekitar. Dalam sehari limbah padat yang dihasilkan sebanyak lebih kurang 10% dari total nata yang diproses, yaitu sekitar 500-700 kilogram dari 7 ton. Limbah tersebut masih memiliki nilai yang dapat dimanfaatkan karena kandungannya, seperti selulosa yang merupakan sumber gula yang dapat dimanfaatkan kembali menjadi bioetanol yang memiliki nilai jual tinggi.
Ketersediaan bahan bakar fosil kini mulai menipis dan merupakan sumber energi yang tidak dapat diperbaharui. Kebutuhan energi nasional dipenuhi oleh minyak bumi sekitar 51.66%, gas alam 28.57% dan batubara 15.34%. Sedangkan diperkirakan bahwa cadangan minyak bumi akan habis sekitar 12 tahun lagi, gas 30 tahun lagi, dan batu bara masih bisa dimanfaatkan hingga 70 tahun ke depan. Pemerintah mengeluarkan peraturan dalam Peraturan Presiden (Perpres) No. 5 Tahun 2006 tentang kebijakan energi nasional untuk mendorong pengembangan sumber energi alternatif sebagai pengganti bahan bakar minyak. Peneliti Pusat Penelitian Kimia Lembaga Ilmu Pengetahuan Indonesia (P2 Kimia-LIPI), yang dikutip dari Agus Haryono bahwa pada tahun 2025 diharapkan 17% dari pemenuhan energi Indonesia berasal dari energi terbarukan, salah satunya memanfaatkan etanol sebagai energi alternatif, khususnya bioetanol berbasis lignoselulosa (Badan Ristek 2012).
Proses utama pembuatan bioetanol adalah mengubah gula menjadi senyawa etanol secara anaerob oleh mikroorganisme tertentu yang memenuhi syarat untuk dapat memproduksi etanol. Mikroorganisme yang digunakan dalam penelitian ini adalah bakteri Zymomonas mobilis. Bakteri tersebut memiliki keunggulan dalam memproduksi etanol, diantaranya memiliki kestabilan biokimia (karakteristiknya konstan dan uniform), mempunyai bentuk stabil bila disimpan pada suhu normal, mampu dan cepat terurai dalam air, dapat melakukan fermentasi dalam sumber karbohidrat yang digunakan, dapat berkembang biak dengan baik dan memberikan hasil yang baik dalam medium pembiakan, serta tahan terhadap kadar etanol tinggi dan suhu tinggi pada proses fermentasi dibandingkan
2
mampu menghasilkan etanol dengan produktivitas 2.5 kali lebih tinggi dari
Saccharomycess cereviseae (Zhang et al. 1995 dan Dien et al. 2003).
Sementara itu, dikarenakan bahan utama yang digunakan adalah limbah padat nata de coco yang memiliki kandungan utama selulosa maka diperlukan proses pendukung untuk mengubah polimer selulosa menjadi gula sebagai substrat fermentasi. Proses hidrolisis tersebut menggunakan enzim selulase. Hidrolisis menggunakan enzim akan bekerja secara spesifik dan tidak menimbulkan limbah baru.Selulase spesifik terhadap substrat selulosa, terdiri atas kompleks protein enzim yang akan menghidrolisis ikatan glikosidik (Rabinovich
et al. 2002).
Perumusan Masalah
Mengacu pada konteks dan fokus penelitian, masalah penelitian yang dapat dirumuskan adalah limbah padat nata de coco memiliki kandungan selulosa yang dominan selain air. Selulosa dapat dimanfaatkan sebagai bioetanol yang terlebih dahulu diubah menjadi gula sederhana melalui proses hidrolisis menggunakan enzim. Analisis komposisi substrat perlu dilakukan untuk mendapatkan kinerja fermentasi terbaik dengan melakukan percobaan yang terdiri dari dua variabel yaitu konsentrasi inokulum dan pemberian nutrisi. Produksi bioetanol dari hasil penelitian dianalisis secara ekonomi bila diaplikasikan dalam bentuk usaha sehingga dilakukan analisis kelayakan finansial.
Tujuan Penelitian
Tujuan dari penelitian ini diantaranya : 1. Memanfaatkan sisa nata de coco sebagai limbah
2. Mengetahui potensi limbah tersebut menjadi bioetanol, serta mengetahui kadar bioetanol yang dihasilkan melalui fermentasi yang dilakukan oleh Zymomonas mobilis
3. Membandingkan kadar bioetanol yang dihasilkan antara substrat dengan konsentrasi starter Zymomonas mobilis berbeda dan substrat yang diberi tambahan nutrisi.
4. Mengetahui kinerja fermentasi Zymomonas mobilis terhadap substrat limbah
nata de coco
5. Menganalisis kelayakan finansial produksi bioetanol dari limbah padat nata de coco menggunakan Zymomonas mobilis.
Lingkup Penelitian
METODOLOGI PENELITIAN
Bahan dan Peralatan
Bahan Baku
Bahan baku utama yang digunakan dalam penelitian ini adalah limbah padat nata de coco, kemudian enzim yang digunakan untuk keperluan hidrolisis nata de coco adalah enzim selulase, serta mikroorganisme yang digunakan untuk fermentasi adalah Zymomonas mobilis yang diperoleh dari Laboratorium Bioindustri, Teknologi Industri Pertanian, IPB.
Bahan Kimia
Bahan kimia/nutrien yang digunakan untuk pertumbuhan antara lain
nutrient agar (NA), yeast extract, amonium sulfat, magnesium sulfat, dan urea. Sedangkan bahan kimia yang digunakan untuk analisis antara lain, H2SO4 pekat, fenol 5%, NaOH 0.1 N, indikator fenolftalein, larutan DNS, larutan glukosa standar, alkohol 70%, etanol 95%, Ca(OH), HCl 0.01 N, H2SO4 0.32 N, NaOH 1.25 N, NaOH 0.02 N, alkohol 70%, Na – K Tartarat, dan Na – metabisulfit.
Peralatan
Peralatan yang digunakan dalam penelitian ini diantaranya : fermentor skala 300 ml (Erlenmeyer 300 ml dan leher angsa), erlenmeyer 500 ml, erlenmeyer 100 ml, shaker (inkubator goyang), gelas piala 2000 ml, gelas ukur, blender, oven,
tray, tabung reaksi, jarum ose, kapas, dan kertas saring inkubator goyang, autoklaf, termometer, cawan alumunium, desikator, pipet, penangas air, spektrofotometer, timbangan, pH meter, alat titrasi, distilator dan piknometer.
Metode Penelitian
Tahapan Penelitian
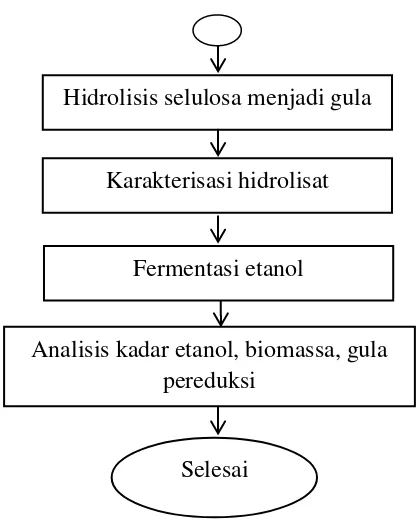
Tahapan penelitian diilustrasikan pada Gambar 1 berikut :
\\ Mulai
Karakterisasi limbah nata de coco
4
Gambar 1 Diagram alir tahapan penelitian
Karakterisasi Limbah Padat Nata de Coco
Kandungan nata de coco terbesar selain air adalah selulosa. Selulosa merupakan senyawa yang utama dalam produksi bioetanol pada penelitian ini. Dengan demikian untuk mengetahui kadar selulosa yang terdapat dalam limbah
nata de coco yang telah disediakan dilakukan uji kadar serat kasar, beserta uji karakterisasi lainnya seperti kadar air, kadar protein, kadar abu, kadar total gula dan dilakukan penghitungan C/N ratio dengan prosedur yang terdapat pada Lampiran 1.
Persiapan Bahan
Bahan baku utama yang digunakan adalah limbah padat nata de coco
sebagai substrat untuk menghasilkan gula. Substrat dibuat dengan cara nata de coco dicuci terlebih dahulu dengan air agar asam asetat yang terkandung hilang. Kemudian digiling menggunakan blender.
Hidrolisis Selulosa
Proses hidrolisis yang digunakan adalah hidrolisis enzimatis menggunakan enzim selulase komersial. Sebelum enzim digunakan, diuji nilai aktivitas enzim. Prosedur pengujian aktivitas enzim disajikan pada Lampiran 1.
Besar konsentrasi enzim yang digunakan merupakan salah satu faktor dari penelitian ini, yaitu menentukan konsentrasi enzim optimum untuk menghasilkan gula yang maksimum. Enzim yang ditambahkan sebanyak 10, 20, 30,40, dan 50 IU/g substrat (serat kasar) dan diinkubasi selama 3 hari. Bahan dicampurkan bersama enzim dalam kondisi pH 5 menggunakan buffer fosfat sitrat pH 5 dan diinkubasi pada suhu 60°C (Derosya 2010).
Hidrolisis selulosa menjadi gula
Fermentasi etanol
Selesai
Karakterisasi hidrolisat
Karakterisasi Hidrolisat
Pada tahap ini dilakukan pengukuran konsentrasi total gula dan gula pereduksi hasil hidrolisis. Analisis total gula ditetapkan berdasarkan metode fenol sulfat (Dubois et al 1956) sedangkan gula pereduksi menggunakan metode DNS (Miller 1959). Prosedur penetapan total gula dan gula pereduksi disajikan pada Lampiran 2.
Fermentasi
1. Persiapan Media
Media fermentasi berasal dari substrat glukosa hasil hidrolisis limbah nata de coco menggunakan enzim selulase. Fermentasi dilakukan pada labu erlenmeyer 300 ml dengan volume media yang digunakan adalah 100 ml v/v.
2. Persiapan Kultur
Zymomonas mobilis dapat ditumbuhkan pada media padat dengan kandungan 5 g/l yeast extract, 20 g/l glukosa, dan 20 g/l agar (Nutrient Agar) pada pH 6.8 (Obire 2005). Inkubasi dilakukan pada suhu 30°C selama 24-48 jam. Pembuatan starter dilakukan dengan membuat medium yang terdiri atas 20 g/l glukosa, 10 g/l yeast extract, 1 g/l pottasium dihydrogen orthophosphate, 1 g/l ammonium sulfat, dan 1 g/l magnesium sulfat. Kemudian diinkubasi goyang 100 rpm pada suhu 30°C selama 24 jam (Pannesar et al. 2007).
3. Proses Fermentasi
Substrat fermentasi yang digunakan adalah gula hasil hidrolisis nata de coco
secara enzimatis. Pada tahap ini terdapat dua faktor yang diamati yaitu konsentrasi starter dan penambahan nutrisi. Starter yang ditambahkan yaitu 10, dan 15% (v/v) media. Terdapat dua jenis media yaitu satu tidak menggunakan sumber nutrien lain dan satu lainnya menggunakan sumber nutrien lain. Sumber nutrien lain yang digunakan adalah urea (Thomsen et al. 2008). Urea yang ditambahkan berdasarkan rasio C/N untuk produksi etanol. pH media diatur 4-5 dengan menggunakan Ca(OH2). Fermentasi dilakukan secara anaerobik dengan suhu ruang (30°C) secara batch dengan waktu 72 jam dan dilakukan analisis setiap 12 jam. Labu ditutup dengan sumbat dan leher angsa. Hasil fermentasi kemudian dianalisa terlebih dahulu dengan dipasteurisasi pada suhu 80°C selama 10 menit untuk menginaktifkan mikroorganisme.
6
HASIL DAN PEMBAHASAN
Karakteristik Nata de Coco
Nata merupakan produk hasil fermentasi oleh mikroba Acetobacter xylinum
yang dapat mengubah glukosa menjadi selulosa. Nata adalah biomassa yang sebagian besar terdiri dari selulosa, berbentuk agar, dan berwarna putih. Nata berasal dari substrat yang mengandung gula dan protein hingga terbentuk massa. Komponen utama nata adalah selulosa yang mampu mengikat air sebesar 95% dalam bentuk gel nata sehingga bersifat empuk (Enie A.B. 1998). Nata de coco
adalah nata yang dibuat dengan bahan baku air kelapa. Air kelapa mengandung gula yang terdiri dari sukrosa, glukosa, dan fruktosa. Berdasarkan penelitian yang dilakukan oleh Mayasti (2009), kandungan nata de coco terdiri dari berikut ini,
Tabel 2 Komposisi kimia nata de coco (pada 100 g berat basah)
Komposisi Nata de coco (dalam %)
Air 94.44
Abu 0.3
Protein 0.04
Lemak 0
Serat Kasar 1.63
Sumber : Mayasti (2009)
Bahan yang digunakan pada penelitian ini sebagai substrat fermentasi adalah limbah padat nata de coco. Yang dimaksud hal tersebut adalah nata de coco yang tidak memenuhi syarat untuk dijual, seperti kulit ari dan sisa potongan. Meskipun demikian limbah tersebut tetap memiliki kandungan yang sama dengan
nata de coco aslinya, seperti hasil uji yang telah dilakukan, dapat dilihat pada Tabel 3 berikut.
Tabel 3 Karakteristik limbah padat nata de coco
Komponen % Bobot basah
Kadar air 97±1
Kadar abu 0.14±0.05
Kadar protein 0.040±0.014
Kadar serat kasar 1.4±0.1
Kadar karbohidrat dan lemak (by different)
2.7±0.9
Analisis kadar air dilakukan untuk mengetahui kandungan air di dalam nata de coco sebagai basis perbandingan antara total padatan dan air. Baik hasil pengujian dan penelitian terlebih dahulu oleh Mayasti (2009) menunjukkan bahwa
nata de coco memiliki kandungan air yang sangat tinggi dibandingkan dengan padatannya.
tersebut memperlihatkan perbedaan dari segi bahan yang digunakan, bahwa bahan yang digunakan kandungannya tidak sebaik nata de coco segar namun masih memiliki potensi serat yang cukup sebagai pemanfaatan substrat gula.
Kadar protein adalah banyaknya protein yang terdapat dalam nata. Kadar protein ini menjadi basis penentuan kadar nitrogen. Sedangkan kadar karbon dapat diketahui dari hasil pengurangan antara kadar air, kadar abu, dan kadar nitrogen. Setelah diketahui kadar nitrogen dan kadar karbon maka dapat diketahui rasio C/N yang digunakan sebagai basis dalam penentuan jumlah nutrisi yang akan ditambahkan untuk memenuhi kriteria rasio C/N produksi bioetanol.
Karbohidrat terdiri dari kandungan pati, gula, dan selulosa. Berdasarkan hasil penelitian dari Mayasti (2009) bahwa nata de coco tidak memiliki kandungan lemak maka dalam penelitian ini pun diasumsikan bahwa nata de coco
yang digunakan tidak memiliki kandungan lemak. Dengan demikian hasil perhitungan by different untuk karbohidrat dapat diindikasikan sebagai kandungan gula dan selulosa.
Hidrolisis
Selulosa merupakan polisakarida linier dari residu glukosa yang
dihubungkan oleh ikatan β-1,4 glikosidik, terdiri dari daerah kristalis (85%) dan daerah amorf (non kristalin) (15%) yang membentuk mikrofibril yaitu struktur dengan kekuatan tegang tinggi (Howard et al. 2003) dan Tsao et al (1978). Selulosa dapat dimanfaatkan menjadi bioetanol karena dari proses hidrolisis akan menghasilkan monomer yang dapat dimanfaatkan sebagai substrat fermentasi. Selulosa memiliki gula disakarida yaitu selobiosa dan dapat terhidrolisis menjadi monosakarida yaitu glukosa.
Untuk dapat dijadikan sebagai substrat fermentasi maka bahan nata de coco
yang digunakan terlebih dahulu dihirolisis menjadi gula sederhana. Bahan tidak memerlukan perlakuan pendahuluan seperti pemecahan lignin ataupun hemiselulosa karena nata de coco tidak memiliki struktur seperti sumber selulosa pada tumbuhan. Selulosa pada nata de coco merupakan selulosa bakterial, yaitu selulosa yang terbentuk akibat aktivitas mikroorganisme, dalam hal ini yaitu
Acetobacter xylinum akan memproduksi enzim extraseluler yang akan membentuk glukosa menjadi ribuan rantai selulosa (Sri 1992). Phillips G.O dan Williams P.A (2000) dalam Sulistiyana dan Ita (2011) menyatakan bahwa selulosa bakterial memiliki struktur kimia yang sama dengan selulosa pada sel tumbuhan, dan merupakan polisakarida berantai lurus yang tersusun oleh molekul D-glukosa
melalui ikatan β-1.4 glikosidik. Pembentukan selulosa bakterial terjadi di luar sel bakteri, sedangkan selulosa tanaman terbentuk di dalam dinding sel (Sri 1992). Dengan demikian selulosa bakterial tidak membutuhkan perlakuan awal untuk memecah lignin dan atau hemiselulosa karena selulosa tidak dilindungi oleh bagian tersebut.
8
pada percabangan tertentu sehingga produk yang dihasilkan sesuai dengan keinginan dan dengan jumlah yang sedikit dapat mengencerkan sejumlah besar substrat (Pomeranz 1991).
Metode hidrolisis yang digunakan adalah hidrolisis enzimatis menggunakan enzim selulase. Selulase adalah enzim yang dapat mengkatalis proses pemecahan selulosa menjadi glukosa. Selulase spesifik terhadap substrat selulosa, terdiri atas
kompleks protein enzim yang akan memutuskan ikatan β-1,4 glikosidik dalam selulosa, selodekstrin, dan selobiosa, serta turunan selulosa lainnya. Hidrolisis selulosa menggunakan enzim selulase merupakan sebuah rangkaian proses enzimatis yang sinergis antara endoglukonase, eksoglukonase/selobiohidrolase, dan β-glukosidase. Ketiga enzim ini disebut selulase atau enzim selulolitik (Rabinovich et al. 2002). β-glukosidase dapat menghidrolisis selubiosa dan selo-oligosakrida menjadi glukosa yang dapat dimetabolisme mikroba di dalam sel.
Proses konversi selulosa menjadi glukosa pada hidrolisis dengan enzim berlangsung secara bertahap. Tahap pertama adalah proses konversi selulosa menjadi selobiosa, dan tahap berikutnya adalah proses konversi selobiosa menjadi glukosa. Hidrolisis sempurna akan menghasilkan monomer selulosa yaitu glukosa dan hidrolisis tidak sempurna akan menghasilkan disakarida dari selulosa yang disebut selobiosa. Faktor kinerja enzim yaitu praperlakuan substrat, konsentrasi enzim, dan pengadukan. Pengecilan ukuran substrat membantu untuk adsorpsi enzim pada substrat, namun proses penghancuran bahan atau pengecilan ukuran yang terlalu halus dapat merusak sturktur kristal dan memutus ikatan kimia dari rantai panjang molekulnya pada selulosa sehingga enzim selobiohidrolase tidak akan bekerja maksimum atau menguraikan selulosa dalam jumlah yang sebenarnya (Chang et al. 1981)
Pada penelitian ini menggunakan enzim selulase yang terlebih dahulu diuji aktivitasnya agar dapat menentukan konsentrasi enzim yang dapat digunakan untuk hidrolsis. Aktivitas enzim disebut sebagai kinetik enzim, yaitu kemampuan enzim dalam membantu reaksi kimia yang dapat dipengaruhi oleh beberapa faktor, seperti suhu, pH, kadar substrat, kadar enzim, inhibitor, dan aktivator. Tiap enzim memerlukan suhu dan pH optimum yang berbeda-beda karena enzim adalah protein yang dapat mengalami perubahan bentuk jika suhu dan keasaman berubah. Suhu dan pH yang di luar optimum dapat menurunkan atau menghilangkan kinerja enzim karena enzim dapat mengalami kerusakan.
Suhu optimum untuk aktivitas enzim selulase pada umumnya optimum di suhu 50 - 60ºC (Mandels et al. 1976). Dalam penentuan aktivitas selulase, kondisi kerja enzim yang digunakan yaitu pada suhu 60ºC dan pH 5 menggunakan buffer fosfat sitrat yang didasarkan atas penelitian terdahulu yang dilakukan oleh Derosya (2010). Aktivitas enzim selulase didefinisikan sebagai jumlah gula pereduksi yang dihasilkan dari hidrolisis selulosa oleh enzim per menit per milimeter filtrat enzim dengan satuan IU/menit.ml, dimana 1 IU sama dengan 1 mikromol glukosa (Darwis et al. 1995). Hasil pengujian menunjukkan aktivitas enzim sebesar 414.35 IU/ml yang berarti hidrolisis yang dilakukan oleh enzim tersebut per ml dan menit menghasilkan 414.35 mikromol glukosa dari substrat. Dengan demikian, dapat ditentukan volume enzim yang akan digunakan untuk hidrolisis per gram serat kasar bahan.
IU/g serat kasar. Enzim yang ditambahkan pada substrat sangat berpengaruh terhadap kecepatan proses hidrolisis yang terjadi dan hasil yang diperoleh akan semakin banyak ((Taherzadeh dan Karimi 2007).
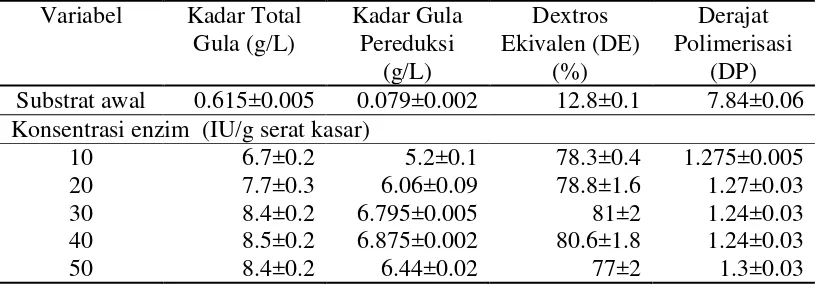
Tabel 4 Kadar gula hasil hidrolisis
Variabel Kadar Total Substrat awal 0.615±0.005 0.079±0.002 12.8±0.1 7.84±0.06 Konsentrasi enzim (IU/g serat kasar)
10 6.7±0.2 5.2±0.1 78.3±0.4 1.275±0.005
20 7.7±0.3 6.06±0.09 78.8±1.6 1.27±0.03
30 8.4±0.2 6.795±0.005 81±2 1.24±0.03
40 8.5±0.2 6.875±0.002 80.6±1.8 1.24±0.03
50 8.4±0.2 6.44±0.02 77±2 1.3±0.03
Penetapan konsentrasi enzim yang digunakan didasarkan dari nilai DP dan DE. DE adalah derajat konversi polimer selulosa menjadi dekstrosa (gula sederhana) secara enzimatis. Semakin tinggi nilai DE maka semakin tinggi pula derajat konversinya. Konversi sempurna berindex DE = 100 dan jika tidak terjadi hidrolisis DE = 0 (Tjokrodikoesoemo 1986). Sebaliknya pada nilai DP dimana semakin mendekati nilai 1 maka semakin baik derajat konversinya. Hal tersebut dikarenakan perbandingan gula pereduksi yang mendekati jumlah total gula. Pada tabel di atas dapat dilihat bahwa konsentrasi enzim 30 IU/g serat kasar memiliki nilai DE yang paling tinggi dibandingkan konsentrasi lainnya, meskipun tidak berbeda signifikan dengan konsentrasi enzim 40 IU/g serat kasar. Namun pemilihan 30 IU/g dinilai lebih efisien karena menggunakan volume enzim yang lebih sedikit dibandingkan 40 IU/g. Semakin banyak jumlah enzim yang ditambahkan akan semakin meningkatkan konversi gula namun akan semakin tinggi pula biaya yang akan dikeluarkan. Menurut Taberzadeh dan Karim (2007) banyaknya enzim yang ditambahkan pada substrat umumnya 5-35 IU/g substrat. Pada konsentrasi enzim 50 IU/g mengalami penurunan tingkat konversi gula. Hal ini dapat disebabkan perbandingan antara jumlah enzim dan substrat yang tidak seimbang. Terjadinya penghambatan oleh substrat tergantung pada rasio enzim terhadap substrat.
10
Tabel 5 Hasil analisis perbandingan gula pereduksi pada dosis enzim 30 IU/g serat kasar
Percobaan ke- Gula pereduksi sebelum hidrolisis kadar gula bahan awal berbeda. Hal ini mengartikan bahwa kondisi limbah padat
nata de coco tersebut dapat berbeda setiap waktu sehingga gula yang dihasilkan setelah proses hidrolisis dapat tidak konstan.
Penentuan Persentase Penambahan Nutrisi pada Media Fermentasi
Fermentasi etanol pada dasarnya adalah proses pengubahan gula menjadi etanol oleh mikroorganisme sebagai jalur metabolismenya. Namun untuk memaksimalkan etanol yang dihasilkan maka selain gula sebagai sumber karbon, mikroorganisme tersebut membutuhkan nitrogen sebagai nutrisinya. Maka pada penelitian ini dilakukan penghitungan rasio karbon dan nitrogen yang tersedia di dalam bahan. Penghitungan rasio C/N ini didasarkan dari karakteristik nata de coco. Total nitrogen didasarkan dari kadar protein sehingga didapatkan nilai sebesar 0.0064%, sedangkan total karbon dihitung secara by difference yaitu sebesar 1.45%.
Menurut Syamsu et al (2002) dalam Haryani 2008 rasio C/N yang dibutuhkan dalam media fermentasi etanol adalah sebesar 10. Sementara itu, rasio C/N dalam bahan sebesar 226.96 sehingga masih membutuhkan nitrogen yang diperoleh dari sumber bahan lain. Bahan sumber nitrogen yang dipilih adalah urea. Hal ini dikarenakan kandungan urea yang spesifik terhadap nitrogen dan harga yang murah sehingga diharapkan mudah dalam pengaplikasiannya. Cara penghitungan jumlah kebutuhan urea disajikan pada Tabel 6.
Tabel 6 Penghitungan kebutuhan urea (gram) dalam 100 ml substrat
Parameter Jumlah
Hasil Fermentasi
Fermentasi adalah proses perubahan kimia pada substrat organik, baik karbohidrat, protein, lemak, atau lainnya melalui kegiatan katalis biokimia yang disebut enzim dan dihasilkan oleh jenis mikroba spesifik (Prescott dan Dunn 1959). Bioetanol merupakan salah satu produk yang dihasilkan dari proses fermentasi bahan yang mengandung gula oleh khamir seperti Saccharomyces sp. ataupun oleh bakteri seperti Zymomonas mobilis. Pada penelitian ini mikroba yang digunakan adalah Zymomonas mobilis.
Zymomonas mobilis merupakan bakteri gram negatif dan yang dapat ditemukan pada tumbuh-tumbuhan yang kaya gula. Bakteri ini memiliki metabolisme anaerob fakultatif. Pemakaian bakteri ini di industri pembuatan etanol memiliki beberapa keuntungan, antara lain kemampuan untuk tumbuh secara anaerob, hasil produksi lebih tinggi, dan kemampuan fermentasi lebih spesifik dibandingkan dengan yeast (Ismail et al. 2009). Selain itu mampu tumbuh lebih cepat daripada yeast dan toleran terhadap kadar etanol tinggi sampai 10% (Wijono 1988). Zymomonas mobilis memfermentasikan glukosa, fruktosa, dan sukrosa melalui jalur Entner Doudoroff (Doelle 1990) menjadi etanol sebagai produk utama dan beberapa produk samping seperti asam asetat, gliserol, sorbitol dan levan (Gunasekaran dan Raj, 1999). Bakteri ini menghasilkan enzim piruvat dekarboksilase yang mengubah pituvat menjadi acetaldehyde, kemudian diubah menjadi enzim alcohol dehydrogenase.
Fermentasi dilakukan sebanyak tiga kali percobaan, dimana pada percobaan 1 dan 2 bertujuan untuk melihat perbandingan kinerja fermentasi antar variabel penelitian, sedangkan pada percobaan ketiga dilakukan untuk melihat konsistensi kinerja fermentasi dari variabel penelitian terbaik serta menentukan waktu optimum fermentasi. Pada percobaan 1 dan 2 didapatkan bahwa kadar gula pereduksi awal pada substrat memiliki jumlah yang berbeda, yaitu berturut-turut sebesar 3.56 g/l dan 6.51 g/l, sehingga masing-masing percobaan tersebut tidak dapat dinyatakan sebagai pengulangan, namun dapat dievaluasi mengenai konsistensi trend produksi etanol, konsumsi gula, dan pertumbuhan sel.
Kadar etanol
Etanol merupakan hasil samping pemecahan glukosa oleh mikroba seperti
12
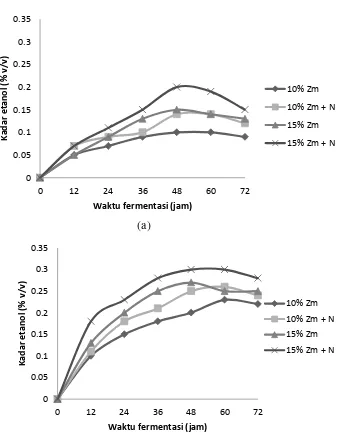
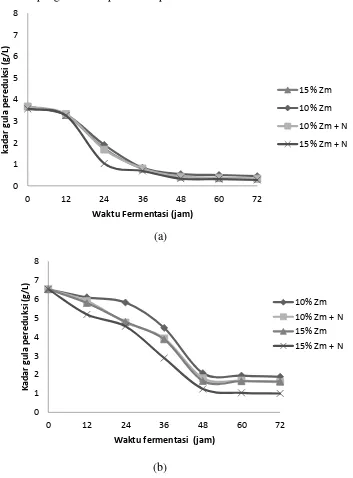
Gambar 2 Konsentrasi etanol selama proses fermentasi 72 jam (a: percobaan 1, b: percobaan 2)
Hasil percobaan 1 dan 2 menunjukkan konsentrasi etanol optimum pada waktu 48 jam. Konsentrasi Zymomonas mobilis (inokulum) 10% memiliki kadar etanol yang lebih rendah sebesar 0.1-0.2% (v/v) (0.71-1.58 g/l) dibandingkan inokulum 15% sebesar 0.15-0.27% (1.03-2.13 g/l). Pada substrat yang diberi penambahan nutrisi memiliki kadar etanol yang lebih tinggi yaitu 0.14-0.25% (1.11 -1.97 g/l) pada inokulum 10% dan 0.2-0.3% (1.58-2.37 g/l) pada inokulum 15%. Sehingga dapat dinyatakan bahwa media fermentasi dengan perlakuan 15% inokulum dan ditambahkan nutrisi urea menghasilkan kadar etanol yang lebih tinggi.
Pada waktu fermentasi jam ke-60 dan 72 mengalami penurunan kadar etanol. Penurunan kadar etanol dapat disebabkan oleh menurunnya juga jumlah sel akibat pengaruh produk. Menurut Mc Lellan (1999), produksi etanol mengalami penurunan ketika biomassa sel mulai turun. Dapat juga dikarenakan
produksi asam yang terjadi karena proses fermentasi etanol melalui produk-produk seperti asam piruvat dan asetaldehid. Selain itu juga terbentuk produk-produk samping yaitu asam-asam organik seperti asam laktat, asam asetat, dan gliserol.
Penggunaan Gula Pereduksi
Gula pereduksi adalah gula yang mempunyai kemampuan untuk mereduksi yang dikarenakan adanya gugus keton dan aldehid. Gula pereduksi yang terdapat di dalam polimer selulosa adalah glukosa. Glukosa ini menjadi basis pengukuran penggunaan gula yang dikonsumsi oleh Zymomonas mobilis untuk fermentasi etanol. Hasil pengukuran dapat dilihat pada Gambar 3 berikut.
14
Hasil kedua percobaan menunjukkan terjadinya penurunan kadar gula pereduksi selama waktu fermentasi. Terlihat pada grafik bahwa kadar gula pereduksi sisa yang terendah adalah pada media fermentasi inokulum 15% beserta ditambahkan nutrisi. Tingkat penggunaan gula yang paling optimum yaitu pada waktu fermentasi 48 jam, setelah itu konsumsi gula tidak mengalami peningkatan yang signifikan. Hal ini dapat dikarenakan Zymomonas mobilis yang tidak dapat mengonsumsi substrat dengan baik dikarenakan kondisi substrat yang sudah tidak cocok untuk pertumbuhan Zymomonas mobilis, hal ini pula yang menyebabkan kadar etanol menurun. Selama proses fermentasi kondisi substrat akan berubah karena pembentukan produk.
Pada percobaan 1 (P1) kadar gula awal adalah 3.56 g/l dan pada percobaan 2 (P2) kadar gula awal adalah 6.51 g/l. Tingkat penggunaan substrat pada fermentasi yang berbeda sehingga pada percobaan kedua jumlah gula masih banyak tersisa. Seharusnya semakin tinggi kadar gula pada substrat maka mikroorganisme dapat lebih memanfaatkannya menjadi produk yang bernilai lebih tinggi sehingga tingkat penggunaan substrat dapat konsisten. Tingginya kadar gula yang tersisa dapat dikarenakan kondisi substrat fermentasi yang sudah tidak baik untuk pertumbuhan Zymomonas mobilis.
Pertumbuhan Biomassa
Biomassa yang dihitung merupakan biomassa sel kering yang terdapat di dalam media fermentasi. Hasil pengamatan pertumbuhan sel Zymomonas mobilis
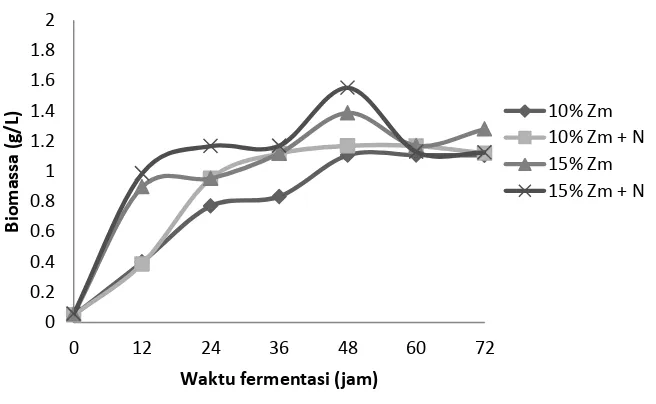
pada setiap variabel penelitian dapat dilihat pada Gambar 4.
Gambar 4 Konsentrasi biomassa sel selama proses fermentasi 72 jam ( a: percobaan 1, b: percobaan 2)
Kinetika pertumbuhan dan pertumbuhan produk menggambarkan kemampuan sel dalam merespon lingkungan (Wang et al 2006). Biomassa merupakan bobot biomassa kering yang terdapat dalam cairan hasil fermentasi.
Pada saat fermentasi, pertumbuhan mikroba secara umum terdiri atas fase lag, fase log (eksponensial), stasioner, dan kematian. Fase lag adalah masa penyesuaian mikroba sejak inokulum diinokulasikan ke dalam media fermentasi. Pada fase lag terjadi pertumbuhan yang lambat dimana sel mempersiapkan diri melakukan pembelahan sehingga peningkatan jumlah sel berjalan lambat karena pada fase ini tidak ada pertambahan jumlah sel yang banyak, meskipun metabolit sel dalam keadaan aktif (Hogg 2005) Cepat atau lambatnya fase lag tergantung kepada kualitas, kuantitas, dan umur biakan yang diinokulasikan (Moat 1979). Pada fase log terjadi pertumbuhan cepat dimana jumlah sel bertambah secara eksponensial terhadap waktu. Pada fase ini kondisi lingkungan berubah karena substrat dan nutrien dikonsumsi sementara metabolik dilakukan (Reed dan Rhem 1983). Pada fase stasioner konsentrasi biomassa mencapai maksimum, setelah fase tersebut terjadi fase kematian yang ditandai dengan penurunan jumlah sel (Bailey dan Olis 1991).
Baik pada percobaan 1 dan 2 dapat dilihat bahwa Zymomonas mobilis
mengalami fase lag pada waktu kurang dari 12 jam, fase log pada waktu 12-48 jam, fase stasioner pada waktu antara 60 jam, dan fase kematian pada waktu 60 jam hingga seterusnya karena mengalami penurunan jumlah sel. Penurunan laju pertumbuhan dikarenakan substrat yang mulai habis dan semakin meningkatnya produk-produk yang dihasilkan.
Laju pertumbuhan mikroba dapat menurun dan akhirnya terhenti pada waktu tertentu dikarenakan pertumbuhan berlangsung dengan mengonsumsi nutrien sekaligus mengeluarkan produk. Pertumbuhan dapat berhenti disebabkan terdapat beberapa nutrien esensial dalam medium atau karena terjadi akumulasi autotoksin dalam medium atau kombinasi keduanya (Hutkins 2006).
16
Hasil Fermentasi Kondisi Media Terpilih
Hasil percobaan 1 dan 2 menunjukkan bahwa media fermentasi yang menghasilkan produk etanol tertinggi adalah pada kondisi substrat dengan inokulum 15% yang ditambahkan nutrisi. Maka dilakukan kembali percobaan ketiga dengan dua kali pengulangan.
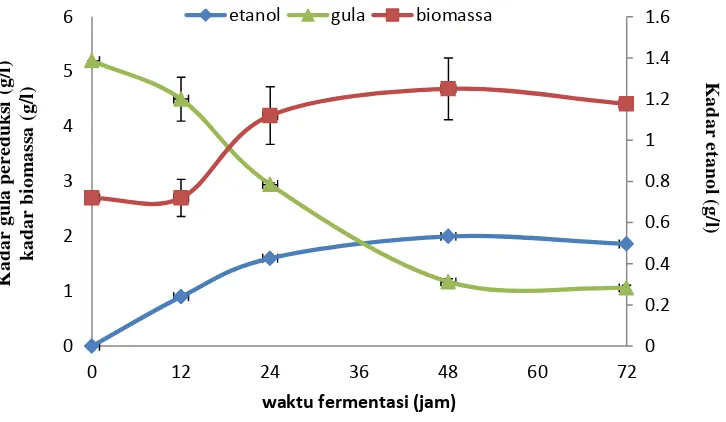
Hasil percobaan ditunjukkan pada Gambar 5. Kadar etanol optimum pada waktu fermentasi 48 jam sebesar 0.25±0.014 % (v/v) (1.97 ± 0.11 g/l) dengan tingkat penggunaan gula sebesar 77.6 ± 0.8 %. Kadar gula pereduksi awal sebesar 5.21 g/l dan tersisa menjadi 1.71 ± 0.06 g/l. Pada pengukuran konsentrasi biomassa, fase lag ditunjukkan pada waktu fermentasi 0-12 jam dikarenakan tidak terjadi pertambahan jumlah sel yang signifikan. Fase log terjadi pada waktu fermentasi 12-24 jam yang ditunjukkan oleh grafik. Waktu fermentasi 36 jam tidak dilakukan dikarenakan pada percobaan sebelumnya kadar etanol yang didapatkan tidak berbeda jauh dengan 48 jam. Dengan demikian waktu fermentasi 36 jam masih bisa masuk ke dalam fase log. Fase stasioner terjadi pada waktu fermentasi 48 jam dikarenakan konsentrasi biomassa mencapai maksimum. Sementara itu, fase kematian dapat terjadi pada waktu fermentasi 60-72 jam karena mengalami penurunan jumlah sel dan penurunan jumlah etanol. Berdasarkan semua hasil pengukuran tersebut maka terdapat konsistensi antara percobaan sebelumnya meskipun kondisi substrat yang berbeda kadar gula awalnya.
Gambar 5 Grafik hubungan antara kadar etanol, biomassa sel, dan kadar gula sisa
Grafik di atas menunjukkan pula hubungan antara produksi etanol dan pertumbuhan sel di mana keduanya saling berasosiasi. Artinya pembentukan produk sejalan dengan pertumbuhan sel. Kedua parameter tersebut menunjukkan pula jumlah yang optimum pada waktu fermentasi 48 jam dan terjadi penurunan baik kadar etanol dan biomassa pada waktu 72 jam. Menurut Mc Lellan (1999) bahwa produksi etanol dapat menurun ketika jumlah sel menurun. Berdasarkan grafik tersebut, gula dalam substrat belum habis namun sudah terjadi penurunan
jumlah sel. Hal ini dapat disebabkan oleh kondisi substrat yang sudah tidak memenuhi kondisi untuk pertumbuhan sel. Pembentukan produk yang berasosiasi dengan pertumbuhan sel maka disebut dengan metabolisme primer. Menurut Shuler dan Kargi (1992), salah satu contoh produk yang dimana pembentukannya berasosiasi dengan pertumbuhan sel adalah etanol, dimana terjadi ketika laju pertumbuhan spesifik produk berbanding lurus dengan laju spesifik pertumbuhan sel.
Berdasarkan hasil analisis Anova didapatkan bahwa waktu fermentasi memiliki respon yang berbeda terhadap kadar etanol yang dihasilkan. Maka analisis dilanjutkan pada uji Duncan. Hasil perhitungan menunjukkan bahwa hasil etanol berbeda signifikan antara waktu 12, 24, dan 48 jam. Sedangkan waktu fermentasi 48 jam dan 72 jam tidak berbeda signifikan sehingga dapat dinyatakan bahwa waktu optimum fermentasi untuk menghasilkan etanol adalah 48 jam.
Kinetika Fermentasi
Kinetika fermentasi menunjukkan perkembangbiakkan mikroba yang ditunjukkan oleh meningkatnya konsentrasi biomassa pada media fermentasi karena konsumsi substrat. Kinetika fermentasi juga menunjukkan kecepatan pertumbuhan sel yang dipengaruhi oleh lingkungan fisik dan kimianya (Reed dan Rehm 1983). Kinetika fermentasi dilihat dari parameter laju pertumbuhan spesifik (µ), waktu penggandaan sel (doubling time tg), koefisien antara hasil sel hidup terhadap sumber karbon yang dikonsumsi (Yx/s), koefisien konversi nutrien dalam substrat menjadi produk pada periode tertentu (Yp/s), dan koefisien produk terhadap jumlah sel hidup (Yp/x).
Laju pertumbuhan spesifik (µ) bersifat tidak konstan tergantung pada kondisi lingkungan fisik dan kimianya. Nilai maksimum (µmaks) dicapai pada kondisi ketersediaan substrat dan nutrien masih berlebih serta konsentrasi zat-zat metabolik yang menghambat pertumbuhan masih rendah. Hasil fermentasi pada media fermentasi dengan inokulum 15% dan ditambahkan nutrisi menunjukkan bahwa laju pertumbuhan spesifiknya (µmaks) sebesar 0.018 jam-1 dengan waktu penggandaan sel (doubling time) 37 jam, artinya Zymomonas mobilis
membutuhkan waktu 37 jam untuk memperbanyak diri dua kali jumlah semula. Hasil Penelitian menunjukkan waktu optimum fermentasi adalah 48 jam. Parameter kinetika pertumbuhan lainnya pada penelitian ini menghasilkan nilai Yp/s = 0.49 ± 0.02 g etanol/g substrat, Yx/s = 0.13 ± 0.03 g sel/ g substrat, Yp/x = 3.7 ± 0.9 g etanol/ g sel.
Secara teoritis konversi molekul gula menjadi 2 molekul etanol dan 2 molekul CO2 mengikuti persamaan Gay Lussac :
C6H12O6 2 C2H5OH + 2 CO2
18
Analisis Kelayakan Finansial
Analisis kelayakan finansial ini dilakukan untuk mengestimasi penerimaan dan pengeluaran dari kegiatan produksi dan investasi usaha produksi bioetanol dari limbah padat nata de coco berdasarkan penelitian yang telah dilakukan. Parameter kelayakan finansial yang digunakan adalah rasio penerimaan dan biaya (R-C ratio). Untuk menghitung parameter tersebut maka ditentukan pula mengenai hal berikut :
a. Arus manfaat (inflow)
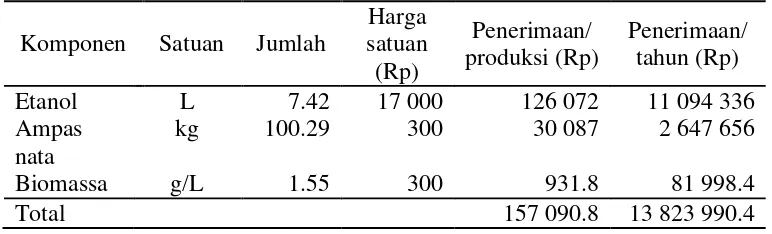
Arus manfaat atau inflow dalam hal ini adalah arus pemasukan dari hasil penjualan bioetanol. Dalam satu kali produksi bioetanol yang dihasilkan adalah 7.42 L/ton limbah nata de coco. Harga jual per liternya adalah Rp 17 000. Dalam 1 kali produksi akan menghasilkan pendapatan sebesar Rp 126 072. Selain itu penerimaan juga diperoleh dari hasil penjualan ampas nata de coco dari hasil penyaringan cairan hidrolisis dan biomassa dari hasil samping fermentasi untuk dimanfaatkan sebagai bahan baku pupuk yang dihargai Rp 300/kg. Rincian penerimaan disajikan pada Tabel 7.
Tabel 7 Rincian penerimaan
Komponen Satuan Jumlah
Harga
Merupakan biaya-biaya yang dikeluarkan selama usaha berlangsung. Biaya tersebut terdiri dari investasi dan biaya operasional. Sebelum dihitung biaya-biaya yang akan dikeluarkan maka beberapa asumsi ditetapkan terlebih dahulu.
1. Asumsi perhitungan
Analisis perhitungan dilakukan dengan menentukan total investasi, biaya tetap dan tidak tetap, dan pemasukan. Produksi bioetanol dilakukan dua kali setiap minggunya dan 11 bulan dalam setahun, sehingga produksi dilakukan sebanyak 88 kali. Dalam 1 kali produksi etanol yang dihasilkan sebesar 7.42 L dengan mengansumsikan kadar gula pereduksi sebesar 6.51 g/L dalam 2000 liter hidrolisat nata de coco sehingga perhitungan jumlah etanol yang dihasilkan berdasarkan (Yp/s) yang didapat dari penelitian yang sudah dilakukan yaitu 0.45 g etanol/g substrat gula. Dalam satu kali produksi nata de coco yang diproses sebesar 1 ton. Etanol diproses hingga kemurnian 90%.
2. Biaya investasi
pengadaan peralatan proses produksi serta kultur Zymomonas mobilis. Hal tersebut dikarenakan pembelian Zymomonas mobilis dilakukan hanya sekali karena seterusnya akan dilakukan perbanyakan sel dengan menggunakan media pertumbuhan, Rincian biaya investasi disajikan pada Tabel 8 berikut.
Tabel 8 Rincian biaya investasi
Uraian Kapasitas Jumlah Satuan Harga (Rp) Total Harga (Rp)
Biaya operasional merupakan seluruh biaya yang berhubungan dengan kegiatan produksi dari usaha bioetanol. Biaya ini terbagi menjadi dua, yaitu biaya tetap dan biaya variabel atau tidak tetap.
20
Tabel 9 Rincian biaya tetap
Biaya variabel yaitu biaya yang jumlahnya tidak tetap karena bergantung pada kegiatan produksi. Biaya ini meliputi biaya pembelian bahan proses produksi dan biaya utilitas seperti konsumsi air, listrik, dan gas. Total biaya yang dikeluarkan setiap 1 kali proses produksi sebesar Rp 154 148 dan per tahunnya yaitu Rp 13 565 398. Rincian biaya terdapat pada Tabel 10.
Tabel 10 Rincian biaya variabel
Uraian Jumlah Satuan Harga tahun yang dihitung dari perjumlahan biaya tetap dan biaya variabel.
Keuntungan
Keuntungan merupakan selisih dari pendapatan dari hasil penjualan bioetanol dan pengeluaran dari biaya operasional produksi. Perhitungan keuntungan dilakukan dengan menggunakan analisis Revenue Cost Ratio (R-C
R-C ratio =
Adapun hasil keuntungan dan R--C ratio disajikan pada Tabel 11.
Tabel 11 Hasil keuntungan dan R-C ratio bioetanol
Uraian Nilai/tahun (Rp)
Jumlah biaya produksi 46 494 108
Hasil penjualan 13 823 990.4
Keuntungan -32 670 117
R-C ratio 0.3
Dari hasil perhitungan didapatkan nilai R-C ratio < 1 maka usaha produksi bioetanol dari limbah padat nata de coco ini tidak menguntungkan. Nilai kerugian yang besar dikarenakan produksi bioetanol yang sangat kecil. Hal ini dikarenakan
nata de coco yang memiliki karakteristik mengandung banyak air melebihi 95% dibandingkan dengan kadar seratnya hanya 1.42% yang menjadikan kadar gulanya pun rendah sehingga etanol yang dihasilkan pun sangat rendah dibandingkan proses produksi yang sudah dilakukan. Selain itu, biaya perbanyakan sel kultur Zymomonas mobilis menimbulkan biaya investasi yang besar dan biaya untuk media pertumbuhan. Apabila terdapat kultur Zymomonas mobilis yang secara mudah diaplikasikan untuk industri, hal ini dapat meminimumkan biaya produksi yang dikeluarkan.
PT. Daya Agro Mitra Mandiri dalam mengatasi limbah padat nata de coco
yaitu dengan membuangnya secara percuma ke TPA, namun hal tersebut menimbulkan dampak sosial yaitu terganggunya masyarakat oleh keberadaan limbah tersebut. Hal ini dikarenakan kapasitas limbah yang cukup tinggi per harinya yaitu dapat mencapai 1 ton. Biaya yang dikeluarkan untuk pembuangan limbah tersebut sebesar Rp 700 000/bulan. Maka dilakukan alternatif penanganan limbah tersebut dengan mengadakan usaha produksi bioetanol. Hasil analisis yang sudah dilakukan menyatakan bahwa usaha produksi bioetanol dari limbah padat
22
SIMPULAN DAN SARAN
Simpulan
Hasil penelitian menunjukkan bahwa limbah padat nata de coco dapat dimanfaatkan menjadi bioetanol. Potensi menjadi bietanol ditunjukkan dengan kadar gula pereduksi yang dapat mencapai 6.51 g/L hidrolisat.
Perlakuan fermentasi terbaik yaitu pada 15% inokulum Zymomonas mobilis
dari volume substrat yang ditambahkan nutrisi urea. Hasil fermentasi menunjukkan nilai yield (p/s) 0.49±0.02 g etanol/g substrat dan konsumsi gula pereduksi sebesar 77.6 ± 0.8 %. Persentase konsumsi gula yang tidak mendekati 100% menyiratkan bahwa Zymomonas mobilis belum optimum dalam mengonsumsi substrat sehingga konversi menjadi etanol tidak maksimum.
Hasil analisis kelayakan finansial menunjukkan bahwa produksi bioetanol dari limbah nata de coco menggunakan Zymomonas mobilis tidak menguntungkan karena nilai R-C ratio yang kurang dari 1, yaitu sebesar 0.3.
Saran
Ketidalayakkan usaha produksi bioetanol ini dikarenakan volume etanol yang tidak sebanding dengan biaya produksi. Selain itu pada analisis ekonomi ini menggunakan kultur murni sehingga membutuhkan biaya investasi yang tinggi dan setiap produksinya memerlukan proses propagasi untuk memperoleh starter. Maka diperlukan kajian mengenai penggunaan Zymomonas mobilis yang secara praktis dan murah untuk dapat menekan biaya.
Usaha produksi bioetanol dari limbah padat nata de coco ini tidak potensial karena kandungan selulosa yang tidak banyak untuk menghasilkan gula yang tinggi sehingga volume etanol yang dihasilkan pun rendah. Alternatif lain pemanfaatan limbah dapat dilakukan seperti penggunaan kembali limbah menjadi produk minuman nata de coco namun hambatan yang dialami adalah belum terciptanya pasar untuk minuman dengan nata de coco yang berbentuk tidak beraturan seperti sisa-sisa potongan.
DAFTAR PUSTAKA
AgroTekno. 2013. Nata de coco industri unggulan [Internet]. [diunduh 2013 Desember 13]. Tersedia pada http://www.agrotekno.net/2013/07/nata-de-coco-industri-unggulan.html.
concentration on etanol production. Bioresource Technology. 98: 2824-2828.
Chang MM, TYC Chou, dan GT Tsao. 1981. Structure, preatreatment, and hidrolysis of cellulose. Di dalam: A Fiechter, editor. Advance in Biochemistry Engineering. Volume (20).
Darwis AA, I Sailah, TT Irawadi, dan Safriani. 1995. Kajian kondisi fermentasi produksi selulase dari limbah kelapa sawit (tandan kosong dan sabut) oleh
Neurospora sitophila. J Teknol. Ind. Pert 5(3): 199-207.
Derosya V. 2010. Sakarifikasi empulur sagu (Metroxylon sagu) dengan konsorsium enzim amilolitik dan holoselulolitik untuk produksi bioetanol [skripsi]. Bogor: Institut Pertanian Bogor.
Dien BS, MA Cotta, TW Jeffries. 2003. Bacteria engineered for fuel ethanol production: current status. Appl. Microbial Biothecnol. 63: 258-266.
Doelle, H.W. 1990. Zymomonas Ethanol Process Laboratory to Commercial Evaluation. In Yu, P.L. editor. Fermentation Technologies Industrial Aplication. New York: Elsevier Applied Science.
Dubois M. KA Gilles, JK Hamilton, PA Rebers, F Smith. 1956. Colorimetic method for determination of sugar and related substance. Analitical Chemist. 28: 350-356.
Enie A.B. 1998. Kajian Pengembangan Industri Nata de Soya dari Air Tahu. Seminar Pengembangan Pengolahan dan Penggunaan Kedele selain Tempe. Di dalam: Intan N.T, Catur B.H, dan Sri H. 2013. Pembuatan Nata de coco: Tinjauan Sumber Nitrogen terhadap Sifat Fisiko-Kimianya [Jurnal]. Sukoharjo: Fakultas Pertanian Universitas Veteran Bangun Nusantara. Fardiaz S. 1988. Fisiologi Fermentasi. Bogor: Pusat Antar Universitas, Institut
Pertanian Bogor.
Gong CS dan GT Tsao. 1979. Cellulase and Biosynthesis Regulation. Di dalam D. Perlman, editor. Annual Report of Fermentation Process. New York: batatas L.) Menggunakan Saccharomyces cerevisiae [Skripsi]. Bogor: Institut Pertanian Bogor.
Hogg, S. 2005. Essential Microbiology. England: John Wiley & Sons Ltd.
Husnan S. dan Suwarsono M. 2000. Studi Kelayakan Proyek. Edisi ke-4. Yogyakarta : Unit Penerbit dan Percetakan.
Hutkins, R.W. 2006. Microbiology and Technology of Fermented Food. USA: Blackwell Publishing Ltd.
Ismail T, L Iksanti, ND Jayanti. 2009. Etanol dari molases menggunakan
Zymomonas mobilis yang diamobolisasi dengan karaginan pada reaktor kontinyu. Makalah pada Seminar Nasional Teknik Kimia Indonesia, 19-20 Oktober 2009, Bandung.
Lee W and C Huang, 2000. Modelling of ethanol fermentation using Zymomonas mobilis ATCC 10988 grown on the media containing glucose and fructose.
24
Mandels M, R. Andreotti and C. Rochie. 1976. Measurement of saccharifying cellulose. Biotechnol.Bioeng. Symp. 6: 21-33.
Mayasti Nur. K. I. 2009. Analisis kelayakan pasar, teknis dan finansial produksi
nata de cassava dari hasil samping industri pati tapioka, Pundong Bantul [skripsi]. Yogyakarta: Universitas Gadjah Mada.
Mc Lellan, PJ, AJ Daugulis, and J Li, 1999. The incidence of oscillatory behavior in the continous fermentations of Z. mobilis. Biotechnology Progress 15 (4): 667-680.
Moat A. G. 1979. Microbiology Physiology. New York: John Willey and Sons Inc.
Miller GC. 1959. Use of dinitrosalicylic acid reagent for the determination of reducing sugar. Analitical Chemist. 31: 420-428.
Obire O. 2005. Activity of Zymomonas sp in palm-sap obtained in there areas in edo state, nigeria. J Appl Sci Environ Manage. 9(1): 25-30
Pannesar PS, SS Marwaha, JF Kenedy. 2007. Comparison of ethanol and temperature tolerance of Zymomonas mobilis strain in glucose and mollases medium. J Biothecnol. 6: 74-77.
Philip GO and Williams PA. 2000. Handbook of Hydrocolloids, Woodhead Publishing limited, Cambridge. Di dalam: Sulistyana dan Ita Ulfin. 2011. Studi Pendahuluan Adsorpsi Kation Ca dan Mg (Penyebab Kesadahan) Menggunakan Selulosa Bakterial Nata de Coco dengan Metode Batch
[skripsi]. Surabaya : Institut Teknologi Sepuluh Nopember.
Pomeranz Y. 1991. Functional Properties of Food Components. San Diego: Academic Press Inc.
Prescott SG and CG. Dunn. 1959. Industrial Microbiology. New York: McGraw-Hill BookCompany.
Purba Elida. 2009. Hidrolisis pati ubi kayu (Manihot esculenta) dan pati ubi jalar (Impomonea batatas) menjadi glukosa secara cold process dengan acid fungal amilase dan glukoamilase [skripsi]. Lampung: Universitas Lampung. Rabinovich ML, Melnik MS, Bolobova AV. 2002. Microbial Cellulases.
Microbiol. 38(4): 305-321.
Reed G, HJ Rehm. 1983. Biotechnology Vol III. Industrial Biotechnology.
Wstport, Connecticut: AVI Publishing Company Inc.
Shuler ML, Kargi F. 1992. Bioprocess Engineering, Basic concept. New Jessey: Prentice Hall International Inc.
Sri RS. 1992. Faktor-faktor yang mempengaruhi nata sari buah tomat [skripsi]. Bogor : Fakultas Teknologi Pertanian, Institut Pertanian Bogor.
Taherzadeh M J dan Karimi K. 2007. Acid-Based hydrolysis processes for ethanol from lignocellulosic material: a Review, J Biores 2(3): 472-499.
Thomsen MH, JB Holm-Nilsen, P Oleskowiez-Popiel, AB Thomsen. 2008. Pretreatment of whole crop harvested, ensiled maize for ethanol production.
Appl Biochem Biothecnol. 148: 23-33.
Tjokroadikoesoemo S. 1986. HFS dan Industri Ubi Kayu Lainnya. Jakarta: Gramedia Pustaka Utama.
Wang D, X Wu, S Bean, JP Wilson. 2006. Ethanol production from pearl millet using Saccharomycess cereviseae. Cereal Chem. 83 (2): 127-131.
Wijono D. 1988. Evaluasi kinetika fermentasi etanol oleh Zymomonas mobilis ZM 4. FTP UGM dalam Bioproses dalam Industri Pangan. Yogyakarta: PAU Pangan dan Gizi UGM.
Zhang M, C Eddy, K Dedana, M Finkelstein dan S Pictaggio. 1995. Metabolic engineering of a pentose metabolism pathway in ethanologenic Zymomonas mobilis. Science. 267: 240-243.
Zhao Xueyan, El-Zahab, Bilal, Brosnahan, Ryan, Perry, Justin, Wang, Ping. 2007. An organic soluble lipase for water-freesynthesis of biodiesel. Appl Biochem Biotechnol. 143:236–243
LAMPIRAN
Lampiran 1 Analisis karakterisasi bahan Kadar Air (AOAC 1995)
Cawan alumunium yang telah dikeringkan dan diketahui bobotnya, diisi sebanyak 2-3 gram sampel lalu ditimbang (W1) kemudian dimasukkan kedalam oven suhu 105oC selama 1-2 jam. Cawan alumunium dan sampel yang telah dikeringkan dimasukkan ke dalam desikator kemudian ditimbang. Ulangi pemanasan sampai dihasilkan bobot konstan (W2). Sisa contoh dihitung sebagai total padatan dan air yang hilang sebagai kadar air.
Kadar air (%) =
Kadar Serat Kasar (AOAC 1984)
Contoh sebanyak 5 g dimasukkan ke dalam Erlenmeyer 500 ml kemudian ditambahkan 100 ml H2SO4 0,325 N dan dididihkan selama kurang lebih 30 menit. Ditambahkan lagi 50 ml NaOH 1,25 N dan dididihkan selama 30 menit. Dalam keadaan panas disaring dengan kertas Whatman No.40 setelah diketahui bobot keringnya. Kertas saring yang digunakan dicuci berturut-turut dengan air panas, 25 ml H2SO4 dan etanol 95%. Kemudian dikeringkan di dalam oven bersuhu 100-110°C sampai bobotnya konstan. Kertas saring didinginkan dalam desikator dan ditimbang.
Kadar serat kasar (%) =
Kandungan nitrogen (N) dengan metode Kjedahl
26
tetes. Setelah itu larutan sampel dimasukkan ke dalam labu destilasi. Destilasi dihentikan apabila tidak ada lagi terbentuk gelembung-gelembung yang keluar pada larutan penampung. Hasil destilasi kemudian dititrasi dengan H2SO4 0.02 N.
% N =
Kandungan karbon (C) (JICA 1978)
Perhitungan kadar karbon didefinisikan sebagai kadar abu dalam bahan. Penentuan kadar abu berdasar pada prinsip sisa mineral hasil pembakaran bahan organik pada suhu 550oC. Cawan porselen dikeringkan terlebih dahulu di dalam oven pada suhu 105oC selama 1 jam, kemudian didinginkan selama 30 menit didalam desikator dan ditimbang hingga diperoleh berat konstan (A). Lalu ditimbang contoh sebanyak 2 gam (B), dan dimasukkan ke dalam cawan porselin dan dipijarkan menggunakan pembakar Bunsen sampai tidak membentuk asap lagi. Kemudian dimasukkan ke dalam tanur listrik (furnace) pada suhu 550oC selama ± 12 jam. Selanjutnya cawan didinginkan selama 30 menit pada desikator, dan ditimbang hingga didapatkan berat konstan (C).
Kadar abu (%) =
Kadar C (%) =
Penetapan Total Gula Metode Fenol H2SO4 (Dubois et al., 1956)
Sebelum dilakukan pengukuran total gula pada sampel, maka perlu diketahui kurva standar fenol yang digunakan. Tahapan pembuatan kurva fenol antara lain adalah 2 ml larutan yang mengadung 0, 10, 20, 30, 40 dan 60 g glukosa masing-masing dimasukan ke dalam tabung reaksi. Setelah itu, ditambahkan 1 ml larutan fenol 5 % dan dikocok. Kemudian 5 ml asam sulfat pekat ditambahkan dengan cepat. Setelah itu ditunggu selama 10 menit. Kemudian, sampel dikocok dan ditempatkan dalam penangas air selama 15 menit. Selanjutnya, diukur absorbansinya pada panjang gelombang 490 nm.
Pengukuran sampel hasil hidrolisat sama dengan metode pembuatan kurva fenol. Pada pengujian, larutan glukosa diganti dengan larutan hasil hidrolisis. Kurva standar fenol dapat dilihat pada Gambar 9 berikut.
Gambar 6 Kurva standar fenol sulfat
Penetapan Total Gula Pereduksi Metode DNS (Miller, 1959)
Prinsip uji suasana alkali gula pereduksi akan mereduksi asam 3,5 – dinitrosolisilat (DNS) membentuk senyawa yang dapat diukur absorbansinya pada panjang gelombang 550 nm.
Tahapan prosesnya terdiri dari penyiapan pereaski DNS, penentuan kurva standar, dan penetapan total gula pereduksi. Pereaksi DNS dibuat dengan melarutkan 10,6 g asam 3,5 dinitrosalisilat dan 19,8 g NaOH ke dalam 1416 ml air. Setelah itu, ditambahkan 306 g Na – K Tartarat, 7,6 g fenol yang dicairkan pada suhu 50 oC, dan 8,3 g Na – Metebisulfit. Larutan ini diaduk rata. Kemudian, sebanyak 3 ml larutan ini dititrasi dengan HCl 0,1 N dengan indikator fenolftalein. Banyaknya titran berkisar 5 – 6 ml. Jika kurang dari itu harus ditambahkan 2 g NaOH untuk setiap ml kekurangan HCl 0,1 N.
Penentuan kurva standar dibuat dengan mengukur untuk mengetahui nilai gula pereduksi pada glukosa pada selang 0,2 – 0,5 mg/l. Kemudian nilai gula pereduksi dicari dengan metode DNS. Hasil yang didapatkan diplotkan dalam gafik secara linier. Kurva standar gula pereduksi metode DNS dapat dilihat pada Gambar 10 berikut.
Gambar 7 Kurva standar DNS
Pengujian gula pereduksi menggunakan kurva standar DNS adalah 1 ml sampel dimasukkan ke dalam tabung reaksi. Kemudian, ditambahkan 3 ml pereaksi DNS. Larutan tersebut ditempatkan dalam air mendidih selama 5 menit. Biarkan sampai dingin pada suhu ruang. Selanjutnya, diukur absorbansinya pada panjang gelombang 550 nm.
Lampiran 2 Uji aktivitas enzim (Derosya 2010)
Substrat CMC dibuat menjadi larutan 0.5% dalam buffer fosfat sitrat pada pH yang akan diujikan. Enzim juga diencerkan dengan buffer fosfat sitrat pada pH yang akan diujikan. Larutan substrat dan enzim kemudian dicampurkan dan diinkubasi pada suhu yang akan diujikan selama 30 menit. Tiap 10 menit, larutan dipipet sebanyak 2 ml kemudian ditambahkan pelarut DNS (dinitrosalisilat) sebanyak 6 ml untuk diukur gula pereduksi yang terbentuk. Sebagai kontrol, larutan substrat dan enzim pada waktu ke-0 juga diukur gula pereduksinya. Aktivitas enzim diperoleh dengan rumus berikut.
28
Aktivitas enzim (IU/ml) =
⁄
Penentuan kadar gula sampel maupun kontrol diketahui dengan terlebih dahulu menghubungkan nilai absorbansi substrat CMC pada berbagai konsentrasi sehingga diperoleh kurva standar menggunakan metode DNS pada panjang gelombang 550 nm. Kurva standar aktivitas enzim ditunjukkan pada Gambar 11 berikut.
Gambar 8 Kurva standar aktivitas enzim
Lampiran 3 Analisis hasil fermentasi
Kadar Etanol metode specific gravity (AOAC 1995)
Sebanyak 25 ml contoh dimasukkan ke dalam labu distilasi sambil diukur suhunya, kemudian ditambahkan akuades dengan volume yang sama. Distilasi dihentikan setelah diperoleh distilat ±23 ml dan diatur suhunya agar sama dengan suhu pada saat pemipetan. Destilat tersebut kemudian dimasukkan ke dalam piknometer 25 ml yang telah diketahui bobotnya (P), selanjutnya ditepatkan hingga tanda tera dengan menambahkan akuades dan ditutup. Dinding piknometer dikeringkan kemudian ditimbang (D).
Piknometer dicuci dengan aseton, kemudian dikeringkan dan dibiarkan hingga mencapai suhu kamar. Dengan menggunakan piknometer yang sama, ditentukan pula bobot air suling (W). Kadar etanol ditentukan dengan bantuan tabel hubungan antara bobot jenis dengan kadar etanol pada berbagai suhu. Rumus perhitungan bobot jenis adalah sebagai berikut.
Biomassa kering
Sebanyak 1 ml sampel di sentrifuse dengan kecepatan 4000 rpm selama 30 menit. Selanjutnya sampel dikeringkan menggunakan oven pada suhu 50oC selama 24 jam. Sebelum ditimbang, biomassa disimpan terlebih dahulu di dalam desikator selama 1 jam.
Lampiran 4 Analisis hasil hidrolisis
Ekuivalen Dekstrosa (Dextrose Equivalent/DE)
Ekuivalen dekstrosa (DE) diperoleh melalui rasio antara nilai gula pereduksi dengan nilai total gula.
Derajat Polimerisasi (DP)
Derajat polimerisasi diperoleh dengan membagi nilai total gula dengan nilai gula pereduksi contoh.
Lampiran 5 Neraca massa proses hidrolisis
Lampiran 6 Data hasil fermentasi Keterangan :
10% Zm : 10% inokulum Zymomonas mobilis dari volume substrat
10% Zm+N : 10% inokulum Zymomonas mobilis dari volume substrat dan ditambahkan nutrisi
15% Zm : 15% inokulum Zymomonas mobilis dari volume substrat
15% Zm+N : 15% inokulum Zymomonas mobilis dari volume substrat dan ditambahkan nutrisi
Limbah nata de coco
Pencucian
Pengecilan ukuran
Hidrolisis Enzim
selulase
Penyaringan Ampas
Hidrolisat nata de coco
Larutan
buffer pH 5 6.78 kg
kg
7 ml 3435 ml
680 g
30
1. Kadar Etanol
Hasil uji kadar etanol (% v/v) selama fermentasi 72 jam (percobaan 1) Faktor
Hasil uji kadar etanol (g/l) selama fermentasi 72 jam (percobaan 1)
Hasil uji kadar etanol (% v/v) selama fermentasi 72 jam (percobaan 2) Faktor
Hasil uji kadar etanol (g/l) selama fermentasi 72 jam (percobaan 2) Faktor
2. Kadar Gula Pereduksi Sisa
Hasil uji kadar gula pereduksi (g/l) selama fermentasi 72 jam (percobaan 2)
Faktor pengamatan
Pengamatan jam ke-
0 12 24 36 48 60 72
10% Zm 6.51 6.09 5.81 4.46 2.07 1.94 1.88
10% Zm + N 6.51 5.89 4.75 3.91 1.8 1.68 1.6
15% Zm 6.51 5.88 4.79 3.86 1.65 1.64 1.63
15% Zm + N 6.51 5.17 4.55 2.87 1.23 1.03 0.99
3. Konsentrasi Biomassa sel
Konsentrasi biomassa sel (g/l) selama fermentasi 72 jam (percobaan 1) Faktor
Pengamatan
Pengamatan jam ke-
0 12 24 36 48 60 72
10% Zm 0.048 0.26 0.526 0.67 1.269 0.62 0.753
10% Zm + N 0.05 0.32 0.646 0.655 1.22 0.68 0.68
15% Zm 0.056 0.4 0.473 0.647 1.073 0.624 1.073
15% Zm + N 0.058 0.543 0.813 1.086 1.896 1.473 1.473
Konsentrasi biomassa sel (g/l) selama fermentasi 72 jam (percobaan 2) Faktor
pengamatan
Pengamatan jam ke-
0 12 24 36 48 60 72
10% Zm 0,048 0,4 0,771 0,833 1,107 1,107 1,106
10% Zm + N 0,05 0,387 0,953 1,118 1,169 1,168 1,12
15% Zm 0,056 0,897 0,953 1,118 1,387 1,169 1,28
15% Zm + N 0,058 0,987 1,167 1,169 1,553 1,129 1,125
4. Hasil Uji Fermentasi Perlakuan Media Terbaik (inokulum 15% + nutrisi) a. Kadar etanol
Hasil uji kadar etanol (% v/v) selama fermentasi 72 jam
Percobaan Pengamatan jam ke-
12 24 48 72
Ulangan 1 0.09 0.2 0.24 0.22
Ulangan 2 0.13 0.22 0.26 0.25
mean 0.11 0.21 0.25 0.24
32
Hasil uji kadar etanol (g/l) selama fermentasi 72 jam
Percobaan Pengamatan jam ke-
12 24 48 72
Ulangan 1 0.711 1.58 1.896 1.738
Ulangan 2 1.027 1.738 2.054 1.975
mean 0.9 1.6 2.0 1.8
SD 0.2 0.1 0.1 0.2
b. Kadar gula pereduksi sisa
Hasil uji kadar gula pereduksi sisa (g/l) selama fermentasi 72 jam
Percobaan Pengamatan jam ke-
0 12 24 48 72
Hasil uji konsentrasi biomassa sel (g/l) selama fermentasi 72 jam
Percobaan Pengamatan jam ke-
0 12 24 48 72
Ulangan 1 0.72 0.661 1.018 1.145 1.187 Ulangan 2 0.72 0.788 1.224 1.353 1.167
mean 0.72 0.72 1.12 1.25 1.18
SD 0 0.09 0.14 0.14 0.01
5. Penentuan waktu fermentasi optimum
Menggunakan analisis Anova Faktor Tunggal Perlakuan
(jam) Ulangan Jumlah Rata-rata Varian
0 2 0 0 0
12 2 0,22 0,11 0,0008
24 2 0,42 0,21 0,0002
48 2 0,5 0,25 0,0002
72 2 0,47 0,235 0,00045