SINTESIS HIDROTERMAL DAN KARAKTERISASI
KRISTAL TITANIUM DIOKSIDA (TiO
2)
MARLIA SUGIARTI
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
ABSTRAK
MARLIA SUGIARTI. Sintesis Hidrotermal dan Karakterisasi Kristal Titanium
Dioksida (TiO
2). Dibimbing oleh SRI MULIJANI dan ARMI WULANAWATI.
Penelitian ini bertujuan untuk mempelajari pengaruh suhu dan metode
terhadap ukuran dan fase kristal titanium dioksida (TiO
2). Kristal TiO
2disintesis
melalui metode hidrotermal dengan mencampurkan TiO
2(Rutil, Merck) dan
NaOH pekat dalam tabung reaktor hidrotermal selama 48 jam, pada suhu 180 °C.
Setelah proses hidrotermal, satu sampel tidak dikasinasi (a) dan sampel yang lain
dikalsinasi selama 2 jam pada suhu 500 °C (a) dan 800 °C (c). Kristal TiO
2yang
dihasilkan dianalisis menggunakan XRD dan SEM. Pada perlakuan (a), belum
terbentuk fase anatase maupun rutil dengan jelas, dihasilkan kristal dengan ukuran
rerata 0,147 nm dan kristalinitas sebesar 37,84 %. Pada perlakuan (b) dihasilkan
kristal fase anatase dengan ukuran rerata 34,507 nm dan kristalinitas sebesar
70,38 %. Kristal yang lebih homogen dihasilkan pada perlakuan (c) dengan
ukuran rerata 45,168 nm dan kristalinitas sebesar 90,47 %. Kristal pada perlakuan
(c) bertransformasi dari fase anatase menuju rutil.
ABSTRACT
MARLIA SUGIARTI. Hydrothermal Synthesis and Characterization of Titanium
dioxide (TiO
2) Crystal. Supervised by SRI MULIJANI and ARMI
WULANAWATI.
The aim of this research is studied about methode and temperature effect to
phase and size of titanium dioxide (TiO
2) crystal. Titanium dioxide (TiO
2) crystal
was synthesized by hydrothermal method with mixed of TiO
2powder (Rutile,
SINTESIS HIDROTERMAL DAN KARAKTERISASI
KRISTAL TITANIUM DIOKSIDA (TiO
2)
MARLIA SUGIARTI
Skripsi
Sebagai salah satu syarat untuk memperoleh gelar
Sarjana Sains pada
Departemen Kimia
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
Judul Skripsi : Sintesis Hidrotermal dan Karakterisasi Kristal Titanium Dioksida
(TiO
2)
Nama
: Marlia Sugiarti
NIM : G44052015
Disetujui oleh
Pembimbing I
Pembimbing II
Dr. Sri Mulijani, M.S. Armi Wulanawati, S.Si., M.Si.
NIP. 196304011991032001 NIP. 196907252000032001
Diketahui oleh
Ketua Departemen Kimia
Prof Dr Ir Tun Tedja Irawadi, MS
NIP 19501227 197603 2 002
PRAKATA
Puji syukur penulis panjatkan kepada Allah SWT atas rahmat dan pertolongan-Nya
penulis dapat menyelesaikan karya ilmiah dengan judul Sintesis hidrotermal dan karakterisasi
kristal titanium dioksida (TiO
2). Shalawat dan salam semoga senantiasa tercurah pada
Rasulullah SAW dan kita semua sebagai umatnya.
Penulis mengucapkan terima kasih banyak kepada Ibu Dr. Sri Mulijani, M.S. dan Ibu
Armi Wulanawati, S.Si., M.Si. selaku pembimbing yang senantiasa memberikan saran,
motivasi dan bimbingannya kepada penulis. Penulis juga mengucapkan terima kasih kepada
Bapak Budi Arifin, S.Si., M.Si. yang telah memberikan motivasi dan arahan kepada penulis.
Penulis juga mengucapkan terima kasih kepada Ibu ‘Ai, Pak Yani, Pak Syawal, Pak Mail,
Pak Mul, Pak Caca dan Teh Nurul atas bantuannya selama penelitian.
Terima kasih yang tak terhingga penulis ucapkan kepada Ayah, Mamah, Anona, Teh
Wiwi, Didit dan Eneng tercinta atas kesabaran, doa, kasih sayang dan dukungannya. Juga
ucapan terima kasih kepada Dartiawati, Laras, Guslina, Ade, Syaeful Fahmi, Novi dan semua
teman-teman kimia angkatan 41 sampai 45 atas bantuan, doa, motivasi dan saran yang
diberikan kepada penulis.
Semoga karya ilmiah ini dapat bermanfaat bagi perkembangan ilmu pengetahuan.
Bogor, Juni 2012
RIWAYAT HIDUP
Penulis dilahirkan di Bogor pada tanggal 9 Maret 1987 dari pasangan Bapak M. Sibli
Santibi dan Ibu Maryamah, S.Ag. Penulis merupakan anak ketiga dari lima bersaudara.
Tahun 2005 penulis lulus dari SMAN 5 Bogor dan pada tahun yang sama lulus seleksi masuk
IPB melalui jalur Undangan Seleksi Masuk IPB (USMI IPB).
DAFTAR ISI
Halaman
DAFTAR GAMBAR ... vi
DAFTAR LAMPIRAN ... vii
PENDAHULUAN ... 1
BAHAN DAN METODE
Bahan dan alat ... 1
Sintesis kristal TiO
2dengan metode hidrotermal ... 2
Kalsinasi kristal TiO
2... 2
Karakterisasi kristal TiO
2... 2
HASIL DAN PEMBAHASAN
Karakterisasi dengan XRD ... 2
Karakterisasi dengan SEM ... 4
SIMPULAN DAN SARAN ... 5
DAFTAR PUSTAKA ... 5
DAFTAR
GAMBAR
Halaman
1 Pola difraksi kristal TiO
2tanpa kalsinasi ... 2
2 Pola difraksi kristal TiO
2dengan kalsinasi selama 2 jam, 500 °C ... 3
3 Pola difraksi kristal TiO
2dengan kalsinasi selama 2 jam, 800 °C ... 3
4 Perbandingan pola difraksi kristal TiO
2pada ketiga perlakuan ... 4
DAFTAR LAMPIRAN
Halaman
1 Diagram alir penelitian ... 7
2 Data JCPDS TiO
2fase anatase dan rutil ... 8
3 Data karakteristik TiO
2(Rutil, Merck) ... 9
4 Data puncak dan intensitas relatif (
IR
) kristal TiO
2hasil sintesis ... 10
5 Pola difraksi kristal TiO
2hasil sintesis dan pola difraksi standar ... 11
6 Data ukuran kristal TiO
2hasil analisis XRD ... 12
7 Contoh perhitungan ukuran kristal pada bidang hkl ... 15
1
PENDAHULUAN
Titanium dioksida (TiO2) merupakan bahan kimia bersifat semikonduktor dan fotokatalis yang dapat disintesis melalui proses sulfat dari TiOSO4 dan kalsinasi pada suhu 800-1000 °C menghasilkan TiO2 anatase maupun melalui proses klorida dari distilasi TiCl4 dan direaksikan dengan O2 pada suhu 1000 sampai dengan 1400 °C menghasilkan TiO2 rutil (Wilberg 2001). TiO2 sering digunakan di berbagai industri diantaranya industri pemurnian air, sensor gas, pewarna atau cat, dan kosmetik (Yuan 2004). Aplikasi TiO2 bergantung pada fase kristal, dimensi dan morfologi TiO2. Struktur TiO2 telah banyak dimodifikasi menjadi ukuran nano. Istilah nanopartikel digunakan dalam ilmu bahan yang menunjukkan partikel dengan ukuran lebih kecil dari 100 nm. Nanopartikel diketahui memiliki berbagai keunggulan antara lain yaitu ketahanan partikelnya terhadap perubahan sifat kimia dan fisik lingkungan, kekerasan mekanik, ketahanan kejut termal, dan elastisitas yang tinggi (Kartohardjono 2009).
Nanopartikel TiO2 dapat dimodifikasi menjadi beberapa bentuk antara lain
nanotube, nanoflakes, nanosheet, dan
nanowire bergantung pada metode sintesis dan variasi suhu yang digunakan. Penelitian mengenai modifikasi nanopartikel TiO2 dan aplikasinya sudah dikembangkan dengan berbagai metode, salah satunya metode sol-gel alumina berpori dan pelapisan titanium pada larutan tetrabutil amonium (TBA) hidroksida menghasilkan nanoflakes dan nanosheet TiO2 dengan ukuran kristal sebesar 5 nm (Yuan 2004).
TiO2 memiliki tiga fase kristal, yaitu anatase, rutil, dan brukit. Metode sintesis TiO2 dipilih berdasarkan aplikasi yang akan digunakan. Pada sintesis dengan suhu rendah biasanya dihasilkan kristal TiO2 fase anatase. Anatase merupakan bentuk yang paling sering digunakan karena memiliki luas permukaan serbuk yang lebih besar serta ukuran partikel yang lebih kecil dibandingkan rutil.
Fase anatase mulai muncul pada rentang suhu 400-650 °C dan cenderung bertransformasi menjadi rutil pada suhu 915 °C (Afrozi 2010). Fase rutil dipreparasi dengan kalsinasi anatase pada suhu tinggi. Fase rutil TiO2 menunjukkan fotoaktivitas yang lebih rendah daripada fase anatase. Selain itu, bandgap energi anatase lebih besar daripada rutil sehingga memiliki aktivitas fotokatalitik yang tinggi (Afrozi 2010).
Namun, beberapa sumber melaporkan bahwa preparasi rutil pada suhu rendah telah berkembang dan menghasilkan fotoaktivitas cukup tinggi (Palmisano 2007). Sementara itu, fase brukit kristal sulit untuk dipreparasi sehingga biasanya hanya kristal pada fase rutil dan anatase yang umum digunakan pada untuk berbagai aplikasi industri.
Kristal TiO2 pada bentuk nanotube dan pada fase anatase diketahui memiliki luas permukaan dan efek listrik yang besar, serta efisiensi fotokatalis yang tinggi sehingga sesuai jika digunakan untuk aplikasi semikonduktor dan membran keramik (Zhang 2008).
Pada penelitian ini dipelajari pengaruh metode hidrotermal dan suhu kalsinasi terhadap karakteristik kristal TiO2. Karakteristik tersebut meliputi ukuran dan fase kristal yang dihasilkan. Metode hidrotermal dipilih karena diketahui telah berhasil menyintesis kristal berukuran nano. Penelitian sebelumnya yang dilakukan oleh Retnantiti (2010) berhasil menyintesis BaTiO3 dengan ukuran butiran kristal sebesar 100 nm menggunakan metode hidrotermal. Keuntungan lain metode hidrotermal adalah dapat dilakukan pada suhu rendah dan juga dapat menghasilkan produk kristal yang homogen, tidak membutuhkan waktu banyak dan menjaga kemurnian bahan karena sampel dimasukkan ke dalam teflon dan bejana baja (reaktor hidrotermal) yang tertutup rapat sehingga terjaga dari kontaminasi luar.
BAHAN DAN METODE
Bahan dan Alat
Bahan-bahan yang digunakan adalah serbuk TiO2 (Sampel, Merck), NaOH 10 M, HCl pH 2, air destilata. Alat-alat yang digunakan adalah reaktor hidrotermal, teflon, corong Buchner, pengaduk magnetik, oven automatis, tanur, sentrifuse, indikator pH universal, alat-alat gelas, difraktometer sinar X (SHIMADZU XRD 7000) dan SEM (BRUKER ZEISS EVO 50).
Metode Penelitian
Sintesis kristal TiO2 dengan metode
hidrotermal (Zhang 2008)
2
hidrotermal). Proses hidrotermal dilakukan di dalam oven yang telah dikalibrasi pada suhu 180 °C selama 48 jam.
Hasil proses hidrotermal berupa suspensi berwarna putih terbentuk akibat reaksi antara NaOH dan TiO2. Setelah suspensi mencapai suhu ruang kemudian dicuci dengan air destilata dan disaring vacum setelah itu dikeringkan dalam suhu ruang kemudian dimasukkan ke dalam 500 mL HCl pH 2 dan distirer selama 24 jam dengan kecepatan 800 rpm (pada metode ini dilakukan pengulangan sebanyak tiga kali) untuk menghilangkan Na+ dan larutan menjadi netral (Yoshida et al
2005). Setelah itu dilakukan pemusingan atau sentrifugasi pada larutan dengan kecepatan 1500 rpm agar terpisah dengan cepat antara suspensi dan larutan HCl encer. Setelah didapatkan suspensi titanium dioksida, lalu dikeringkan dengan pemanasan selama 10 jam di dalam oven pada suhu 70 °C (Djaeni 2010). Setelah 10 jam maka terbentuklah kristal titanium dioksida tanpa residu ion Na+.
Kalsinasi terhadap kristal TiO2
Kristal TiO2 yang terbentuk melalui proses hidrotermal kemudian dikalsinasi di dalam tanur pada variasi suhu 500 °C dan 800 °C selama masing-masing 2 jam. Setelah itu didiamkan hingga tanur mencapai suhu ruang lalu sampel dikeluarkan dari tanur dan dibiarkan mendingin sampai suhu ruang.
Karakterisasi kristal TiO2
Kristal TiO2 hasil sintesis dengan metode hidrotermal pada suhu 180 °C tanpa kalsinasi dan kristal TiO2 yang dikalsinasi dengan dua variasi suhu (500 °C dan 800 °C). Variasi suhu tersebut dipilih karena diketahui pada kedua suhu tersebut fase kristal TiO2 bertransformasi (Yoshida et al 2005). Kristal TiO2 kemudian dikarakterisasi dengan XRD dan SEM. Karakterisasi XRD dapat memberi informasi secara umum baik kuantitatif maupun kualitatif untuk mengetahui fasa yang terdapat dalam sampel, menentukan ukuran kristal dan kristalinitas. Kristal hasil sintesis dikarakterisasi menggunakan alat XRD. Untuk mengetahui morfologi kristal yaitu tampilan permukaan dan keseragaman bentuknya, kristal TiO2 hasil sintesis dikarakterisasi dengan SEM. Diagram alir penelitian dapat dilihat pada Lampiran 1.
HASIL DAN PEMBAHASAN
Karakterisasi dengan XRD
Bahan utama yang digunakan adalah serbuk TiO2 (Merck). Pola difraksi TiO2 tersebut menunjukkan bahwa kristal TiO2 memiliki fase rutil dengan ukuran rerata kristal pada bidang hkl sebesar 0.156 nm (Lampiran 2 dan 3).
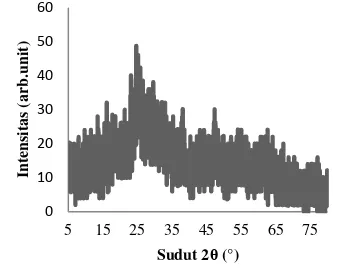
Pada proses awal, TiO2 (Rutil, Merck) direaksikan dengan NaOH 10 M, selama proses hidrotermal 48 jam pada suhu 180 °C, ikatan Ti-O-Ti terurai dan ikatan Ti-OH dan Ti-O-Na terbentuk dengan adanya penambahan NaOH. Setelah proses hidrotermal, suspensi TiO2 yang masih mengandung Na+ dimasukkan ke dalam larutan HCl pH 2 selama 24 jam dengan 3 kali ulangan untuk menghilangkan residu Na+ tersebut (Zhang 2008). Sampel dibedakan atas 3 perlakuan (tanpa kalsinasi, kalsinasi 2 jam 500 °C dan 800 °C). Ketiga perlakuan tersebut dilakukan untuk melihat pengaruh suhu terhadap perubahan fase dan ukuran kristal. Kristal TiO2 hasil sintesis dikarakterisasi dengan XRD. Pola difraksi yang dihasilkan dicocokkan dengan data joint cristal powder difraction standard (JCPDS) (Lampiran 2). Pola difraksi kristal TiO2 tanpa kalsinasi ditunjukkan pada Gambar 1.
Gambar 1 Pola difraksi kristal TiO2 tanpa kalsinasi.
Pola difraksi kristal TiO2 tanpa kalsinasi menunjukkan bahwa puncak-puncak yang tinggi terbentuk pada sudut sekitar 25°. Hanya ada satu puncak yang mirip dengan pola difraksi dan data JCPDS anatase (Lampiran 2), yaitu puncak pada sudut 25.20° dengan intensitas relatif (IR) 95.83% sementara IR
tertinggi 100 % dimiliki puncak dengan nilai sudut 24.66° (Lampiran 4). Kristal TiO2 pada
0 10 20 30 40 50 60
5 15 25 35 45 55 65 75
In te n si ta s (a r b. uni t)
3
perlakuan tanpa kalsinasi masih berbentuk amorf atau belum terbentuk fase kristal, tetapi kemunculan puncak pada rentang sudut 25° memperlihatkan bahwa kristal cenderung akan membentuk fase anatase pada suhu lebih tinggi. Hal ini menunjukkan bahwa metode hidrotermal selama 48 jam pada suhu 180 °C dapat mengubah kristal TiO2 rutil menjadi amorf dan selanjutnya dapat berubah menjadi anatase dengan pemberian suhu lebih tinggi. Nilai kristalinitas TiO2 tanpa kalsinasi masih rendah, yaitu sebesar 37.84%. Pengukuran ukuran kristal pada bidang hkl menggunakan formula Scherrer, dengan persamaan (Shinoda 2011):
L(h,k,l) = �0���.9��
dengan L adalah ukuran kristal (nm) pada bidang hkl, λ adalah panjang gelombang sinar-x (nm), � adalah Full Width at Half Maximum
(FWHM) dalam radian, dan θ adalah setengah sudut difraksi. Bidang yang lazim digunakan untuk menghitung ukuran kristal adalah bidang yang memiliki puncak yang cukup tinggi. Ukuran kristal berbanding terbalik dengan nilai FWHM. Semakin kecil nilai FWHM maka ukuran kristal semakin besar. Ukuran rerata kristal TiO2 sebesar 0.147 nm (Lampiran 6).
Pada perlakuan berikutnya, TiO2 dikalsinasi pada variasi suhu 500 °C dan 800 °C. Perlakuan ini dimaksudkan untuk mengamati pengaruh suhu terhadap perubahan karakteristik kristal. Pola difraksi kristal TiO2 hasil kalsinasi selama 2 jam pada suhu 500 °C ditunjukkan oleh Gambar 2.
Gambar 2 Pola difraksi kristal TiO2, kalsinasi 2 jam, 500 °C.
Fase anatase kristal TiO2 mulai terbentuk pada suhu 500 °C. Hal ini dapat dilihat dengan adanya puncak-puncak yang sejajar dengan puncak standar anatase (Lampiran 5). Puncak-puncak tersebut memiliki nilai sudut yang mendekati JCPDS (Lampiran 2), yaitu 25.32°;
47.96°; 37.90°; 55.10°; 53.94°; 62.66° dan 75.12° (Lampiran 4). Puncak tertinggi terdapat pada sudut 25.32° dengan nilai IR
100%. Fase anatase merupakan fase yang diharapkan terbentuk karena pada fase ini kristal TiO2 memiliki luas permukaan dan
bandgap energi yang lebih besar (Afrozi 2010), serta ukuran kristal yang lebih kecil daripada fase rutil sehingga TiO2 sering digunakan untuk aplikasi semikonduktor. Kristalinitas kristal TiO2 dengan kalsinasi 2 jam pada suhu 500 °C sebesar 70.38%. Ukuran rerata kristal sebesar 34.507 nm (Lampiran 6). Berdasarkan hasil yang diperoleh dapat diketahui bahwa suhu mampu meningkatkan kristalinitas sehingga ukuran kristal menjadi lebih besar.
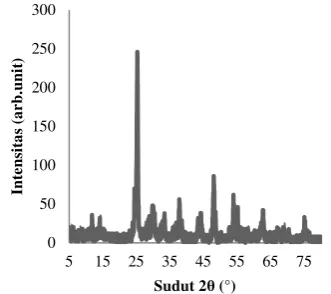
Pola difraksi sampel TiO2 yang dikalsinasi selama 2 jam pada suhu 800 °C dapat dilihat pada Gambar 3.
Gambar 3 Pola difraksi kristal TiO2, kalsinasi 2 jam, 800 °C.
Pada pola difraksi kristal TiO2 dengan kalsinasi 2 jam pada suhu 800 °C terdapat beberapa puncak yang nilai sudutnya mendekati JCPDS fase anatase (Lampiran 2), yaitu pada sudut 25.32°; 48.08°; 53.96°; 37.82°; 55.12°; 68.76°; 74.06° (Lampiran 4). Puncak tertinggi pada sudut 25.32° dengan IR
100%. Pada suhu 800 °C ini terjadi transformasi fase dari anatase menuju rutil. Hal ini diperlihatkan dengan munculnya puncak-puncak yang nilai sudutnya mendekati JCPDS fase rutil (Lampiran 2), yaitu pada sudut 27.42°; 36.90° dan 62.72° (Lampiran 4). Namun pada sudut-sudut ini nilai IR masih
rendah dibandingkan dengan nilai IR fase
anatase. Hal ini dikarenakan untuk membentuk fase rutil dibutuhkan suhu pemanasan yang lebih tinggi, yaitu sekitar 915 °C (Afrozi 2010).
Pada sudut sekitar 11° dan 14° muncul puncak yang tidak sesuai dengan data JCPDS
0 50 100 150 200 250 300
5 15 25 35 45 55 65 75
In te n si ta s (a r b. uni t )
Sudut 2θ (°)
0 50 100 150 200 250 300
5 15 25 35 45 55 65 75
Int e ns it a s ( a r b. uni t)
4
yang diduga sebagai pengotor yang berasal dari teflon yang digunakan atau bisa juga merupakan serpihan dekomposisi dari ion titanat (Yoshida et al 2005). Perbandingan pola difraksi kristal TiO2 hasil sintesis pada suhu 800 °C dan pola difraksi standar kristal TiO2 fase anatase dan rutil dapat dilihat pada Lampiran 5. Contoh perhitungan IR dapat
dilihat pada Lampiran 5.
Pada sampel dengan kalsinasi 800 °C diperoleh nilai kristalinitas terbesar yaitu 90.47%. Hal ini dikarenakan pada suhu tinggi dihasilkan puncak X-ray yang lebih tajam dan sempit sehingga meningkatkan kristalinitas. Kenaikan suhu mengakibatkan meningkatnya energi getaran termal yang kemudian mempercepat difusi atom melalui batas butir, dari butiran kecil menuju butiran yang lebih besar (Shinoda 2011). Ukuran rerata kristal TiO2 pada perlakuan kalsinasi 800 °C adalah sebesar 45.168 nm (Lampiran 6). Contoh perhitungan ukuran kristal dapat dilihat pada Lampiran 7.
Perbandingan pola difraksi kristal TiO2 hasil sintesis dengan tiga perlakuan (tanpa kalsinasi, kalsinasi 2 jam pada suhu 500 °C dan 800 °C) dapat dilihat pada Gambar 4.
Gambar 4 Perbandingan pola difraksi kristal TiO2 hasil sintesis dengan tiga perlakuan: tanpa kalsinasi ( ), kalsinasi 2 jam pada suhu 500 °C ( ) dan 800 °C ( )
Karakterisasi dengan SEM
Analisis SEM bertujuan untuk melihat pengaruh pemanasan terhadap morfologi kristal. Hasil analisis sampel menggunakan SEM dapat dilihat dalam Gambar 5.
Analisis sampel tanpa kalsinasi (a) dilakukan pada perbesaran 5000x. Hasil analisis sampel menunjukkan kristal mengalami penggumpalan hal ini dikarenakan TiO2 bersifat menggumpal jika terkena udara. Penggumpalan juga disebabkan tidak adanya pengadukan saat proses hidrotermal dan tidak dilakukan proses kalsinasi pada sampel.
Kristal pada sampel tanpa kalsinasi memiliki ukuran panjang dan lebar sebesar 565.7 nm dan 401.9 nm. Sementara itu untuk sampel dengan kalsinasi 500 °C (b) dilakukan pada perbesaran 10000x. Morfologi kristal nampak lebih baik, butiran yang nampak lebih besar. Satu butir kristal terukur dengan panjang dan lebar sebesar 446.6 nm dan 256.8 nm. Pada sampel dengan kalsinasi 800 °C (c) analisis SEM dilakukan pada perbesaran 5000x terlihat butiran lebih menyebar dan homogen. Ukuran panjang dan lebar kristal sebesar 379.6 nm dan 312.6 nm. Berdasarkan hasil analisis SEM dari ketiga sampel terlihat bahwa butiran kristal lebih homogen seiring bertambahnya suhu kalsinasi. Morfologi dari ketiga sampel hampir sama dengan morfologi TiO2 (Rutil, Merck) yang digunakan sebagai bahan dasar, hanya ada beberapa yang berbentuk bulat-panjang pada kristal TiO2 hasil sintesis hidrotermal. Morfologi kristal TiO2 yang digunakan sebagai bahan awal dapat dilihat pada Lampiran 8.
Gambar 4 Mikrograf SEM kristal TiO2 hasil sintesis: tanpa kalsinasi, perbesaran 5000 x (a); kalsinasi 2 jam, 500°C, perbesaran 10000 x (b); kalsinasi 2 jam, 800°C, perbesaran 5000 x (c).
a
b
5
SIMPULAN DAN SARAN
Simpulan
Kristal nanopartikel TiO2 fase anatase dapat disintesis dari TiO2 fase rutil dengan metode hidrotermal selama 48 jam pada suhu 180 °C dan kalsinasi pada suhu 500 °C. Fase transformasi dari anatase menuju rutil terjadi pada suhu 800 °C. Perubahan kristalinitas dan ukuran kristal TiO2 pada bidang hkl sangat dipengaruhi oleh suhu kalsinasi. Semakin tinggi suhu yang diberikan maka kristalinitas dan ukuran kristal pada bidang hkl semakin besar. Berdasarkan hasil analisis SEM, ukuran butiran kristal TiO2 secara berturut-turut sebesar, 565.7 nm dan 401.9 nm (kristal TiO2, tanpa kalsinasi), 446.6 nm dan 256.8 nm (kalsinasi 2 jam, 500 °C), dan 379.6 nm dan 312.6 nm (kalsinasi 2 jam, 800 °C).
Saran
Berdasarkan hasil penelitian, diperlukan optimasi suhu dan waktu saat proses hidrotermal dan optimasi suhu kalsinasi untuk menghasilkan puncak- puncak dan fase kristal TiO2 yang sesuai dengan JCPDS.
DAFTAR PUSTAKA
Afrozi. 2010. Pengembangan Sensor Analisis [skripsi]. Jakarta: Fakultas Teknik, Universitas Indonesia.
Djaeni. 2010. Multistage Zeolite Drying to Enhance Energy Efficiency of Food Drying.
Drying Technology 25 (6): 1053-1067.
Kartohardjono. 2009. Pengaruh Ukuran Nano Terhadap Sifat Mekanik Partikel. Bandung: ITB Press.
Palmisano. 2007. Optical Properties of TiO2 Suspensions: Influence of pH and Powder Concentration on Mean Particle Size. Ind. Eng. Chem. Res46: 7620-7626.
Retnantiti MD. 2010. Sintesis Hidrotermal dan Karakterisasi Barium Titanat (BaTiO3) [skripsi]. Bogor: Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor.
Samosir N. 2005. Karakterisasi struktur mikro pelat elemen baker (PEB) U3Si2Al dengan menggunakan scanning electron microscope
(SEM). Presentasi Peneliti Muda Bidang Metalurgi. Tangerang: PTBN Batan.
Shinoda. 2011. X-Ray Diffraction Crystallography: Introduction, Examples
and Solved Problems. Department of
Materials Science and Engineering. Kyoto University. Kyoto; 2011.
Tilmant JB, Pommier C, Chhor K. 2000. Synthesis of supported TiO2 membrane by using supercritical alcohol. Materials Chemistry and Physics 64: 156-165.
Wilberg. 2001. Inorganic Chemistry. Munchen: Academic Press.
Will George. Powder Difraction: The Rietveld Method and The Two Stage Methode Determine and Refine Crystal Structure from Powder Diffraction Data. Berlin: Springer-verlag Berlin Heidelberg. 2006.
Yoshida R, Suzuki Y, Yoshikawa S. 2005. Syntheses of TiO2(B) nanowires and TiO2 anatase nanowires by hydrothermal and post-heat treatment. J Solid State Chem 178: 2179-2185.
Yuan. 2004. Titanium oxide nanotubes, nanofibers and nanowires. Colloids and Surfaces A: Physicochem. Eng. Aspects 241:
173–183 [terhubung berkala].
http://www.elsevier.com/locate/collsurface [25 Mei 2004].
Lampiran 1 Diagram alir penelitian
2 g serbuk TiO
2(Rutil, Merck)
NaOH 10 M (aq), 25 mL
Sintesis kristal TiO
2dengan
metode hidrotermal pada suhu
180 °C selama 48 jam
Pencucian dengan air destilata
dan penyaringan dengan corong
buchner
Pencucian suspensi dengan larutan
HCl pH 2, 500 mL (3x ulangan)
Sentrifugasi suspensi TiO
2dan
larutan HCl pH 2
Pengeringan dengan pemanasan
pada suhu 70 °C selama 10 jam
Karakterisasi kristal TiO
2XRD
(SHIMADZU XRD 7000)
SEM
(BRUKER ZEISS EVO 50)
Kalsinasi selama 2 jam
8
Lampiran 2 Data JCPDS TiO
2Fase Anatase
9
Lampiran 3 Pola difraksi dan data kristal TiO
2sampel (Rutil, Merck) berdasarkan
analisis XRD
2θ (°) β (°) 2θ (rad) θ (rad) cos θ β (rad) L (nm)
10
Lampiran 4 Data puncak dan intensitas relatif (
IR
) kristal TiO
2hasil sintesis
No 2θ (°) IR (%)
180 °C 500 °C 800 °C 180 °C 500 °C 800 °C
1 24.66 25.32 25.32 100 100 100
2 25.22 47.96 48.08 95.83 25.95 35.00
3 37.96 37.90 53.96 58.33 23.66 25.20
4 62.68 55.10 37.82 50.00 20.61 22.76
5 55.08 53.94 55.12 50.00 16.03 17.07
6 68.76 62.66 68.76 33.33 13.74 8,.3
7 75.24 75.12 74.06 29.17 12.98 5,.9
8 27.42 10.56
9 62.72 17.07
10 36.90 10.57
Contoh perhitungan intensitas relatif (
I
R), kalsinasi 2 jam, 500 °C.
IR
= x 100%
=
x 100%
= 25.95%
Keterangan:
IR
= intensitas relatif
Ia
= intensitas puncak tertinggi
11
Lampiran 5 Perbandingan pola difraksi kristal TiO
2hasil analisis dan standar
Kalsinasi 2 jam, 500 °C (biru) dan standar anatase (merah).
Kalsinasi 2 jam, 800 °C (biru), dan standar anatase (merah).
12
Lampiran 6 Data kristal TiO
2hasil sintesis
Tanpa kalsinasi (180 °C)
13
Lanjutan Lampiran 6
Kalsinasi 2 jam, 500 °C.
2θ (°) β (°) 2θ (rad) θ (rad) cos θ β (rad) L (nm)
14
Lanjutan Lampiran 6
Kalsinasi 2 jam, 800 °C.
2θ (°) β (°) 2θ (rad) θ (rad) cos θ β (rad) L (nm)
15
Lampiran 7 Contoh perhitungan ukuran kristal TiO
2Ukuran satu butir kristal pada sampel dengan kalsinasi 2 jam 800 °C
Data yang diketahui:
λ
= 0,15404 nm
Ukuran kristal dihitung menggunakan formula Scherrer, dengan persamaan:
L
(h,k,l)=
0.9 � �����
=
0.9 . 0.15404nm 0.007 . 0.976= 21.613 nm
Keterangan:
L
= ukuran kristal (nm) pada bidang hkl
λ
= panjang gelombang sinar-x (nm)
�
= Full Width at Half Maximum / FWHM (radian)
θ
= setengah sudut difraksi.
2θ (o)
β (o)
2θ (rad)
θ (rad)
cos θ
β (rad)
D(nm)16