ANALISA UNSUR HARA Mg DALAM DAUN KELAPA SAWIT DENGAN METODE SPEKTROFOTOMETRI SERAPAN ATOM (SSA) UNTUK MENINGKATKAN PRODUKSI BUAH PADA TANAMAN KELAPA SAWIT
(Elaeis guineensis Jacq.)
KARYA ILMIAH
XERRA FAZARIYANI 092401008
PROGRAM STUDI DIPLOMA III KIMIA DAPERTEMEN KIMIA
FAKULTAS ATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS SUMATRA UTARA
ANALISA UNSUR HARA Mg DALAM DAUN KELAPA SAWIT DENGAN METODE SPEKTROFOTOMETRI SERAPAN ATOM (SSA) UNTUK MENINGKATKAN PRODUKSI BUAH PADA TANAMAN KELAPA SAWIT
(Elaeis guineensis Jacq.)
KARYA ILMIAH
Diajukan untuk melengkapi tugas dan memenuhi syarat memperoleh Ahli Madya
XERRA FAZARIYANI 092401008
PROGRAM STUDI DIPLOMA III KIMIA DAPERTEMEN KIMIA
FAKULTAS ATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS SUMATRA UTARA
PERSETUJUAN
Judul : ANALISA UNSUR HARA Mg DALAM
DAUNKELAPA SAWIT DENGAN METODE SPEKTROFOTOMETRISERAPAN ATOM (SSA) UNTUK MENINGKATKAN PRODUKSI BUAH PADA TANAMAN KELAPA SAWIT
(Elaeis guineensis Jacq.)
Katagori : KARYA ILMIAH
Nama : XERRA FAZARIYANI
Nomor Induk Mahasiswa : 092401008
Program Studi : DIPLOMA III KIMIA
Departemen : KIMIA
Fakultas : MATEMATIKA DAN ILMU PENGETAHUAN
ALAM
(FMIPA) UNIVERSITAS SUMATRA UTARA
Diluluskan di Medan, April 2012
Disetujui
Program studi Kimia Analis Dosen Pembimbing
FMIPA USU Ketua,
Dra. Emma Zaidar Nst, M.si Prof.Dr Harry
Agusnar,M.Sc
NIP. 195512181987012001 NIP.
195308171983031002
Diketahui :
Dr. Rumondang Bulan, MS NIP. 195408301985032001
PERNYATAAN
ANALISA UNSUR HARA Mg DALAM DAUN KELAPA SAWIT DENGAN METODE SPEKTROFOTOMETRI SERAPAN ATOM (SSA) UNTUK
MENINGKATKAN
PRODUKSI BUAH PADA TANAMAN KELAPA SAWIT (Elaeis guineensis Jacq.)
KARYA ILMIAH
Saya mengakui bahwa karya ilmiah ini adalah hasil kerja saya sendiri, kecuali beberapa kutipan dan ringkasan yang masing – masing telah disebutkan sumbernya.
Medan, April 2012
PENGHARGAAN
Puji syukur penulis ucapkan kehadirat ALLAH SWT, yang telah memberikan rahmat dan karunia-Nya sehingga penulis dapat menyelesaikan karya ilmiah ini yang diberi judul “ANALISA UNSUR HARA Mg DALAM DAUN KELAPA SAWIT DENGAN METODE SPEKTROFOTOMETRI SERAPAN ATOM (SSA) UNTUK MENINGKATKAN PRODUKSI BUAH PADA TANAMAN KELAPA SAWIT (Elaeis guineensis Jacq.)”karya ilmiah ini disusun untuk melengkapi salah satu persyaratan agar dapat menyelesaikan pendidikan Diploma III Kimia Analis.
Penulis menyadari sepenuhnya bahwa penulisan karya ilmiah ini tidak akan pernah selesai tanpa bantuan dan dorongan dari berbagai pihak. Oleh karena itu, dalam kesempatan ini penulis mengucapkan rasa terima kasih yang setulus – tulusnyakepada:
• Ayah dan ibu tercinta yaitu Bapak Irwansyah,S.pd dan Ibu Siti Muliana yang telah bersusah payah, dan tanpa pamrih berbuat yang baik untuk anak – anaknya, sehingga penulis bisa bersekolah, mendukung dan memberi dorongan serta semangat kepada penulis, sehingga penulis dapat menyelesaikan semua masalah yang penulis hadapi.
• Adik – adik tersayang yaitu Regia Achmad Wicaksana, Aulia Akbar, dan Dekna Mutiara Ramadhani yang selalu memberi semangat dan memberi keceriaan, sehingga penulis tidak mudah putus asa.
• Bapak Prof.Dr Harry Agusnar,M.Sc , selaku dosen pembimbing yang telah memberikan bimbingan dan pengarahan yang tak henti – henti selama penulisan karya ilmia ini.
• Ibu Dr. Rumondang Bulan, MS , Selaku ketua Departemen Kimia FMIPA USU.
• Ibu Dra. Emma Zaidar Nst, M.Si, Selaku ketua program studi D3 Kimia Analis.
• Bapak dan Ibu dosen yang telah memberikan ilmu yang bermanfaat selama saya kuliah.
• Bapak Dr. Ir. Witjaksana Darmosarkoro selaku Direktur PPKS.
• Bapak Dr.Tjahjono Herawan selaku pembimbing lapangan (PKL).
• Saudara Mhd.Refnaldi R yang selalu memberi bantuan, masukan, semangat, dan dukungan kepada penulis.
• Seluruh rekan – rekan Kimia Analis Khususnya angkatan 2009 yang namanya tidak dapat disebutkan satu persatu.
Atas segala bantuan, penulis hanya dapat berdoa dengan memohon semoga ALLAH SWT memberikan balasan atas kebaikan dari berbagai pihak yang telah banyak membantu dalam penulisan karya ilmiah ini, untuk itu dengan segala kerendahan hati penulis mengharapkan kritik dan saran dari berbagai pihak.
Akhir kata, penulis berharap semoga karya ilmiah ini dapat bermanfaat bagi pembaca.
Medan, April 2012
ABSTRAK
ANALYSIS OF MAGNESIUM ELEMENT (Mg) IN PALM LEAF THE METHOD ATOMIC ABSORPTION SPECTROPHOTOMETRI (AAS) TO
INCREASE PRODUCTION OF OIL PALMFRUITS ON THE PLANT (Elaeis guineensis Jacq.)
ABSTRACT
DAFTAR ISI
Halaman
PERSETUUAN i
PERNYATAAN ii
PENGHARGAAN iii
ABSTRAK vi
1.2 Permasalahan 2
1.3 Tujuan 3
1.4 Manfaat 3
BAB II TINJAUAN PUSTAKA 4
2.1 Daun Kelapa Sawit 4
2.1.1 Susunan Letak Daun 5
2.1.2 Pengambilan Contoh Anak Daun 6
2.2 Metode Analisa Unsur Hara Daun 7
2.3 Unsur Hara Magnesium (Mg) Pada Daun 7
2.4 Analisa Laboratorium dengan Spektrofotometri Serapan Atom (SSA) 9
2.4.1 Prinsip Dasar 10
2.4.2 Instrumen SSA 10
2.4.3 Analisa Kuantitatif dengan SSA 13
BAB III METODOLOGI PERCOBAAN 14
3.1 Persiapan Sampel Daun 14
3.1.1 Membersihkan Contoh Daun Kelapa Sawit 14 3.1.2 Mengeringkan dan Menggiling Sampel Daun 14
3.2 Proses Anasila Sapel Daun 15
3.2.1 Destruksi Basah (H2SO4 + H2O2) 15
3.2.2 Penetapan Magnesium (Mg) 16
3.3 Cara Kerja SSA 18
3.3.1 Cara Penggunaan SSA 18
3.3.2 Cara mematikan SSA 19
BAB IV Hasil Dan Pembahasan 21
4.1 Hasil 21
4.1.1 Hasil Analisa Magnesium (Mg) Daun 21
4.1.2 Menghitung Konsentrasi Sampel 24
4.1.3. Penentuan Kadar Logam Mg Pada Daun Kelapa Sawit 25
BAB V Kesimpulan Dan Saran 29
5.1 Kesimpulan 29
5.2 Saran 29
DAFTAR TABEL
Halaman Tabel 2.4. Temperatur nyala dengan berbagai pembakar 12
Tabel 4.1 Larutan Standart Mg 21
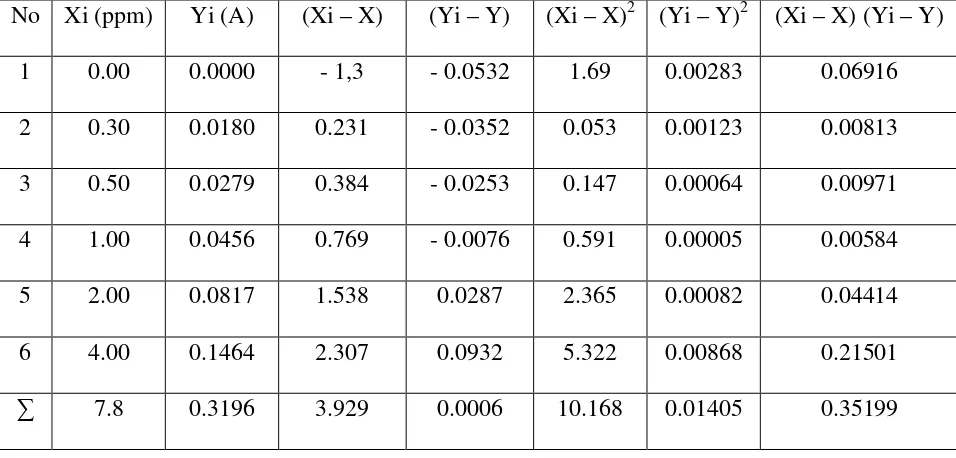
Tabel 4.2. Data Hasil Penurunan Garis Regresi untuk Logam Mg 22
DAFTAR GAMBAR
Halaman Gambar 2.4 : Sistem perelatan Spektrofotometer Serapan Atom 11
Gambar Lampiran II : Kurva Larutan Standart 32
ABSTRAK
ANALYSIS OF MAGNESIUM ELEMENT (Mg) IN PALM LEAF THE METHOD ATOMIC ABSORPTION SPECTROPHOTOMETRI (AAS) TO
INCREASE PRODUCTION OF OIL PALMFRUITS ON THE PLANT (Elaeis guineensis Jacq.)
ABSTRACT
BAB I
PENDAHULUAN
1.1. Latar Belakang
Dalam pertumbuhannya tanaman kelapa sawit membutuhkan adanya
ketersediaan unsur hara. Kandungan unsur hara didalam jaringan tanaman
memberikan informasi tentang status tanaman yang dapat dipercaya pada saat
dilakukan pengambilan sampel. Dengan melihat status unsur hara dapat diperoleh
gambaran jumlah pupuk yang harus ditambahakan dimasa yang akan datang
(umumnya dalam priode 1 tahun). Unsur hara yang dibutuhkan terdiri dari 16 jenis.
Unsur tersebut adalah karbon (C), hidrogen (H), Oksigen (O), nitrogen (N), belerang
(S), fosfor (P), klor (Cl), besi (Fe), mangan (Mn), tembaga (Cu), kalium (K), kalsium
(Ca), magnesium (Mg), seng (Zn), borium (Bo), dan molibdum (Mo).
Unsur C, H, dan O diperoleh tanaman dari udara dan air, sedangkan ketiga belas
unsur yang lainnya diperoleh dari lahan pertanaman. Ketiga belas unsur hara tanaman
ini digolongkan kedalam unsur hara makro yaitu N, P, K, Ca, Mg, dan S dan unsur
hara mikro yaitu Cl, Fe, Mn, Cu, Zn, Bo, dan Mo. Unsur hara makro dibutuhkan
tanaman dalam jumlah banyak, sedangkan unsur hara mikro dibutuhkan dalam jumlah
sedikit.
Tanaman kelapa sawit dilapangan tidak luput dari serangan penyakit, mulai dari
saat pindah tanam dari pembibitan kelapangan. Penyakit – penyakit yang sering
muncul dapat di sebabkan oleh adanya gangguan – gangguan fisiologis tanaman
karena faktor lingkungan yang biasanya disebabkan oleh virus atau jamur. Dan juga
Ada bermacam unsur hara yang apabila kekurangan maupun kelebihan dapat
menimbulkan gejala pada tanaman. Ada dua kelompok unsur hara yang essensial bagi
tanaman, kelompok pertama disebut unsur makro dan yang kedua adalah unsur hara
mikro. Unsur hara makro relatif lebih banyak diperlukan oleh tanaman, sedangkan
unsur hara mikro juga sama pentingnya dengan unsur hara makro, hanya dalam hal
kebutuhan akan zat – zat ini hanya sedikit.
Kekurangan unsur Mg dapat mengakibatkan daun tampak kusam, tidak berkilat
dan pudar. Gejala yang lebih jelas berkembang pada daun – daun yang lebih tua
dengan warna yang hijau-kuning pudar, sedangkan bagian ujung dan tengah daun
dekat tulang daun hijau pucat. Selanjutnya semua daun menjadi hijau pucat (klorosis
berat), dan ujung – ujung daun mengering mulai dari daun tua.
Penyebab kekeurangan unsur Mg karena selama masa perkembangan awal bibit
menggunakan cadangan hara yang ada dalam benih pada tahap selanjutnya bibit
memerlukan hara dari tanah. Gejala – gejala yang ditunjukkan diatas menunjukkan
bahwa cadangan Mg tanah tidak mampu mendukung pertumbuhan bibit yang normal.
1.2. Permasalahan
Dalam perkembangannya, perkebunan kelapa sawit adalah salah satu faktor
penting bagi perekonomian indonesia. Untuk mendapatkan kelapa sawit yang
berkualitas tinggi diperlukan berbagai faktor kesuburan, salahnya satunya yaitu
tingkat kesuburan pada daun. Dengan melakukan analisa laboratorium terhadap unsur
– unsur hara yang ada pada daun, sehingga dapat memberikan informasi tentang
1.3.Tujuan
Untuk mengetahui unsur hara Mg yang terkandung dalam daun kelapa sawit
dengan metode Spektrofotometer Serapan Atom. Sehingga dapat meningkatkan
kualitas produksi buah pada tanaman kelapa sawit.
1.4.Manfaat
Analisa ini digunakan untuk mengetahui apakah daun kelapa sawit kekurangan
unsur hara dan mempersiapkan beberapa banyak unsur hara yang dibutuhkan pada
BAB II
TINJAUAN PUSTAKA
2.1 Daun Kelapa Sawit
Daun kelapa sawit mirip daun kelapa yaitu membentuk susunan daun
majemuk, bersirip genap, dan bertulang belakang sejajar. Daun – daun membentuk
satu pelepah yang panjangnya mencapai lebih dari 7,5 – 9 m. Jumlah anak daun di
setiap pelepah berkisar antara 250 – 400 helai. Daun muda yang masih kuncup
berwarna kuning pucat. Pada tanah yang subur, daun cepat membuka sehingga makin
efektif melakukan fungsinya sebagai tempat berlangsungnya fotosintesis dan sebagai
alat respirasi. Semakin lama proses fotosintesis berlangsung, semakin banyak bahan
makanan yang dibentuk sehingga produksi akan meningkat. Produksi daun tergantung
iklim setempat. Di Sumatera Utara, misalnya produksi daun mencapai 20 – 24
helai/tahun. Umur daun mulai terbentuk sampai tua sekitar 6 – 7 tahun. Daun kelapa
sawit yang sehat dan segar berwarna hijau tua. Jumlah pelepah, panjang pelepah, dan
jumlah anak daun tergantung pada umur tanaman.
Tanaman yang berumur tua, jumlah pelepah dan anak daun lebih banyak.
Begitu pula pelepahnya akan lebih panjang dibandingkan dengan tanaman yang masih
muda. Berat kering satu pelepah dapat mencapai 4,5 kg. Pada tanaman dewasa
ditemukan sekitar 40 – 50 pelepah. Saat tanaman berumur 10 – 13 tahun dapat
ditemukan daun yang luas permukaannya mencapai 10 -15 m2 . Luas permukaan daun
akan berinteraksi dengan tingkat produktivitas tanaman. Semakin luas permukaan atau
Jumlah kedudukan pelepah daun pada batang kelapa awit disebut juga
phyllotaxis yang dapat ditentukan berdasarkan perhitungan susunan duduk daun, yaitu
dengan menggunakan rumus duduk daun 1/8. Artinya, setiap satu kali berputar
melingkari batang, terdaat duduk daun (pelepah) sebanyak 8 helai. Pertumbuhan
melingkar duduk daun mengarah ke kanan atau ke kiri menyerupai spiral. Pada
tanaman yang normal, dapat dilihat 2 set spiral berselang 8 daun yang mengarah ke
kanan dan berselang 13 daun mengarah ke kiri.
Arah duduk daun sangat berguna untuk menentukan letak duduk daun ke – 9
dan ke – 7 saat pengambilan contoh daun. Disamping itu, duduk daun juga berguna
untuk menentukan jumlah daun yang harus tetap ada di bawah buah terendah yang
disebut songgoh. (Fauzi, Y. 2006)
2.1.1 Susunan Letak Daun
Daun ke-9 maupun ke-17 ditentukan dengan memperhatikan susunan letak daun dapat
ditentukan dengan pedoman sabagai berikut :
o Daun ke-1 adalah daun termuda yang helai daunnya telah mekar seluruhnya
dan jarak antara helai daun yang lain sudah jelas tampak pada pangkal
pelepah.
o Daun ke-3 letaknya 274o dari daun pertama. Derajat sudut ini dihitung dari
daun pertama kearah kiri pada tanaman yang mempunyai pusingan spiral ke
kanan ( righ handed palm) dan dihitung kearah kanan pada tanaman yang
mempunyai pusingan spiral ke kiri ( left handed palm ).
o Daun ke-9 letaknya dibawah daun ke-1 agak sebelah kiri pada pusingan kanan
dan agak kesebelah kanan pada pusingan spiral kiri.
o Daun ke-17 letaknya dibawah daun ke-1 agak kesebelah kiri pada pusingan
2.1.2 Pengambilan Contoh anak daun
Anak daun diambil setelah daun contoh diturunkan dari pohon.dari daun
contoh tersebut diambil sebanyak 8 atau 12 helai anak daun ( 4 atau 6 helai dari
sebelah kiri dan 4 atau 6 helai dari sebelah kanan). Anak daun diambil dari bagian
tengah daun. Helai anak daun tersebut diambil dengan menggunakan sabit (egrek)
yang tajam.
Rangkaian penyimpanan anak daun untuk analisis dilaboratorium adalah
sebagai berikut :
o Bagian ujung dan pangkal anak – anak daun dibuang. Sehingga tinggal bagian
tengah sepanjang 10 – 20 cm.
o Setiap helaian daun dibersihkan dengan menggunakan kapas/kain lap yang
telah dicelupkan dengan air aquadest, tidak boleh membersihkan helai daun
tersebut dengan cara merendam dalam air karena hara kalium dapat tercuci.
o Tulang anak daun (lidi) dibuang.
o Contoh daun yang telah dibersihkan kemudian dimasukkan kedalam kantong –
kantong yang terbuat dari kain kelambu.
o Kantong – kantong kelambu yang telah berisi contoh daun kemudian diberi
lebel dengan menggunakan kertas lebel yang telah dipersiapkan. Lebel tersebut
terdiri lebel yang diletakkan dalam kantong dan label yang diikat pada leher
kantong (di luar).
o Contoh daun dalam kantong selanjutnya dikeringkan dalam oven pada
o Setelah dilakukan pengeringan, contoh daun dikirim ke laboratorium untuk
dilakukan analisa daun. Salah satu lembaga yang melayani jasa analisa daun
adalah pusat penelitian kelapa sawit (PPKS). Sebelum contoh daun dikirim ke
laboratorium, agar dibuat daftar contoh keseluruhan yang telah diambil dengan
mengisi formulir.
(Suhardjo,H.
1996).
2.2. Metode Analisa Unsur Hara Daun
Analisa kimia unsur hara tanaman biasanya dilakukan terhadap contoh daun
tanaman yang bersangkutan. Bahan – bahan organik penyusun daun terlebih dahulu
dirombak (destroyed). Dalam ilmu kimia analis tanaman, pekerjaan merombak bahan
organik disebut destruksi.
Filtrat destruksi kering dan destruksi basah dan campuran asam nitrat asam
perklorat dan asam sulfat dipergunakan untuk penetapan unsur hara makro dan mikro
adapun unsur hara makro yang terdapat pada kelapa sawit yaitu N, P, K, Ca, Mg dan
unuk unsur hara mikro dalam kelepa sawit redapat unsur hara Mn, Fe, S, Cu, Zn, B,
Mo, dan Cl. Pada analisa harus dilakukan dua cara destruksi yaitu destruksi kering dan
destruksi basah dengan asam sulfat, atau destruksi basah campuran asam dan basa
dengan asam sulfat. (Anwar,N dan Kosasih. 1972)
2.3 Unsur Hara Magnesium (Mg) dan Kalsium (Ca) Pada Daun Untuk unsur Mg
Unsur Magnesium (Mg) di serap kedalam tanaman dalam bentuk Mg++, dimana
1. Magnesium merupakan bagian tanaman dari klorofil
2. Merupakan salah satu bagian enzim yang disebut organic pyrophosphatse
dan carboxy peptisida.
3. Sangat berperan dalam pembentukan daging buah
Unsur Mg sangat berpengaruh di dalam daun kelapa sawit, sebagai penyusun
klorofil, berperan dalam respirasi tanaman, dan pengaktifan enzim.
Sumber – sumber magnesium ialah :
a) Batuan kapur ( Dolomit Limestone) CaCO3MgCo3
b) Garam Epsom (Epsom salt) MgSO4, 7H2O
c) Kleserit MgSO4.H2O
d) Magnesia MgO
e) Zat ini berasal dari laut yang telah mengalami proses sedemikian :
Mg Cl2 + Ca(OH)2 Mg (OH)2 + Ca Cl2
Mg (OH)2 panas MgO + (OH)4
f) Terpentin Mg3SIO2 (OH)4
g) Magnesit MgCO3
h) Karnalit MgCl2KCl.6H2O
i) Basic slag
j) Kalium magnesium sulfat
(http://bertanimandiri.blogspot.com/2010/11/fungsi-unsur-hara.html)
Kekurangan unsur Mg dapat mengakibatkan daun yang tua berwarna hijau
kekuningan pada sisi yang terkena sinar matahari. Selanjutnya akan kuning kecoklatan
lalu kering.
Gejala kekurangan Mg yaitu :
o Pada gejala awal yang ringan daun tampak kusam, tidak berkilat dan pudar.
o Gejala yang lebih jelas berkembang pada daun – daun yang lebih tua dengan
warna yang hijau kuning pudar, sedangkan bagian ujung dan tengah daun
dekat tulang daun hijau pucat.
o Selanjutnya semua daun menjadi kuning pucat (klorosis berat), dan ujung –
ujung daun mengering mulai dari daun tua.
Penyebab defisi unsur Mg di dalam tanah yaitu seperti :
o Defisiensi Mg terutama mulai terlihat pada bibit berumur 2 – 3 bulan.
o Mengaplikasikan Mg yang kurang dan tidak berimbang.
o Keberadaan unsur Mg dalam kation lain dalam keadaan tidak seimbang.
o Lahan tempat tumbuh ber tekstur pasir dengan top soil tipis, dan CH yang
sangat berlebihan (>3,500mm/th).
Antisipasi untuk kekurangan Mg dapat dilakukan dengan mengunakan :
o Aplikasi tandan kelapa sawit.
o Menggunakan Dolomit jika kemasan tinggi aplikasi pemupukan dengan
ditabur pada dindin piringan, dan
o Menjaga rasio Ca/ Mg dan Mg/K tanah agar tidak melebihi 5 dan 12.
2.4. Analisa Laboratorium dengan Spektrofotometri Serapan Atom (SSA)
SSA merupakan alat instrumentasi yang paling banyak digunakan untuk
mengukur kadar unsur – unsur. Bila suatu larutan analit di aspirasikan kedalam nyala
api maka akan terjadi suatu larutan berbentuk gas yang disebut plasma. Plasma ini
berisi suatu partikel – partikel atom yang telah teratomisasi (telah direduksi menjadi
atom – atomnya). Pada SSA, radiasi dari suatu sumber radiasi yang sesuai (lampu
katoda cekung) dilewatkan kedalam nyala api yang telah teratomisasi maka radiasi
tersebut akan diabsorbsi oleh atom yang telah teratomisasi. Besarnya radiasi yang
diabsorbsi diketahui dari selisih radiasi diketahui dari selisih radiasi asal dengan
radiasi yang diteruskan ( yang tidak diabsorbsi). Konsentrasi unsur diperoleh
berdasarkan besarnya radiasi yang di absorbansi, sesuai dengan hukum beer, bahwa
hubungan antara absorben dengan konsentrasi berbanding lurus atau linier. Untuk
menentukan konsentrasi suatu unsur dapat diketahui dengan menggunakan larutan
standar untuk mendapatkan kurva kalibrasi. Analisis daun tanaman yang pengukuran
analitnya menggunakan SSA adalah analisis K, Ca, Mg, Fe, Cu, Zn, Mn, dan beberapa
logam – logam lainnya.
2.4.1 Prinsip Dasar
Metode spektrofotometri serapan atom berprinsip pada absorpsi cahaya oleh
atom. Atom – atom menyerap cahaya tersebut pada panjang gelombang tertentu,
tergantung pada sifat unsurnya. Cahaya pada panjang gelombang ini mempunyai
cukup energi untuk mengubah tingkat elektronik suatu atom. Transisi elektronik suatu
Instrumen SSA, dapat dibagi menjadi tiga komponen yaitu :
1. Sumber cahaya atau sumber energi
2. Ruang contoh
3. Pengukuran cahaya
sumber cahaya Ruang contoh Pengukuran cahaya
elektronik
sumber sinar monokromator detektor Read Out
nyala
Gambar 2.4 : Sistem perelatan Spektrofotometer Serapan Atom
I. Sumber Sinar
Sumber sinar yang utama digunakan untuk SSA adalah lampu katoda (hollow
cathode lamp, HCL) . Lampu hollow katoda ini berupa tabung yang didalamnya
terdapat anoda dan katoda yang cekung dan silindrik yang diisi dengan gas neon atau
argon pada tekanan rendah (10 – 15 torr). Tabungnya dioperasikan dengan sumber
tenaga beberapa ratus volt. Atom – atom gas terionisasikan didalam loncatan listrik,
dan benturan ion – ion berenergi dengan permukaan katoda menggeser atom – atom
yang telah tereksitasikan sehingga menghasilkan spektrum garis / garis resonansi yang
digunakan untuk analisis suatu unsur .
Pada komponen ini terdapat sistem pembakar, dimana larutan sampel harus di
atomisasikan menggunakan nyala api atau busur api listrik.
Ada berbagai macam alat yang dapat digunakan untuk mengubah suatu sampel
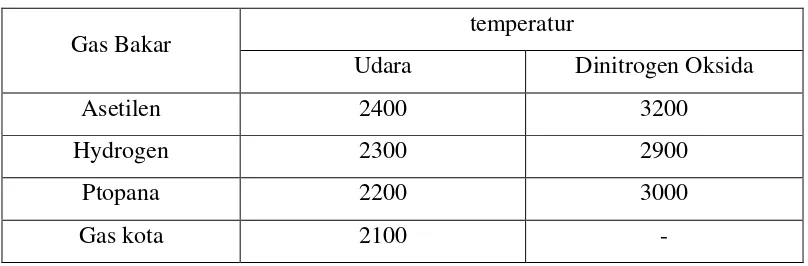
Tabel 2.4. Temperatur nyala dengan berbagai pembakar
Gas Bakar temperatur
Udara Dinitrogen Oksida
Asetilen 2400 3200
Hydrogen 2300 2900
Ptopana 2200 3000
Gas kota 2100 -
Sumber : Anwar, N. 2000 Instrumen SSA dan Kimia Analis
2. Monokromator
Pada SSA, monokromator dimasukkan untuk memisahkan dan memilih
panjang gelombang yang digunakan dalam analisis. Misalnya untuk unsur kalium (K)
diukur dengan panjang gelombang 766,5 nm, untuk unsur kalsium (Ca) diukur dengan
panjang gelombang 422,7 nm, dan untuk unsur magnesium (Mg) diukur dengan
panjang gelombang285,2 nm. Disamping sistem optik, dalam monokromator juga
terdapat suatu alat yang digunakan untuk memisahkan radiasi resonansi dan kontiniu
yang disebut chopper.
3. Detektor
Detektor biasanya digunakan untuk mengukur intensitas cahaya yang melalui
tempat pengatoman. Biasanya digunakan tabung penggandaan foton. Ada 2 cara yang
dapat digunakan dalam sistem deteksi, yaitu :
a) Yang memberikan respon terhadap radiasi resonansi dan radiasi kontiniu.
Pada cara pertama, output yang dihasilkan dari radiasi resonansi dan radiasi
kontiniu disalurkan pada sistem galvanometer dan setiap perubahan yang disebabkan
oleh radiasi resonan dan radiasi kontiniu yang dipisahkan. Dalam hal ini, sistem
penguat harus cukup selektif untuk dapat membedakan radiasi. Cara terbaik adalah
dengan menggunakan detektor yang hanya peka terhadap radiasi resonan yang
termodulasi.
4. Read Out
Readout merupakan suatu alat petunjuk atau dapat juga diartikan sebagai
sistem pencatat hasil. Pencatatan hasil dilakukan dengan suatu alat yang telah
terkalibrasi untuk pembacaan suatu transmisi atau absorbansi. Hasil pembacaan dapat
berupa angka atau berupa kurva dari suatu rekorder yang menggambarkan absorbansi
atau intensitas emisi.
2.4.3. Analisa Kuantitatif dengan SSA
Untuk keperluan analisa kuantitatif dengan SSA, maka sampel harus dalam bentuk
larutan. Untuk menyiapkan larutan, sampel harus diperlakukan sedemikian rupa yang
pelaksanaanya tergantung dari macam dan jenis sampel. Yang penting untuk diingat
adalah bahwa larutan yang akan dianalisa haruslah sangat encer.
Ada beberapa cara melarutkan sampel yaitu :
a) Langsung dilarutkan dengan pelarut yang sesuai
b) Sampel dilarutkan dengan suatu asam
c) Sampel dilarutkan dengan suatu basa atau dilebur dahulu dengan basa
kemudian hasil leburan dilarutkan dalam pelarut yang sesuai.
BAB III
METODOLOGI PERCOBAAN
3.1 Persiapan Sapel Daun
3.1.1 Membersihkan Contoh Daun Kelapa Sawit
Contoh daun yang ada dilaboratorium terlebih dahulu dicatat dan diberi nomor
Laboratorium secara beraturan. Contoh segera dibersihkan dengan kapas yang telah
dibasahi dengan air destilasi. Bagian tulang yang kasar (lidinya) dibuang dengan
gunting, begitu juga bagian pinggir daun terutama daun yang agak lebar digunting dan
dibuang. Kemudian contoh daun dimasukkan kedalam kain kelambu ukuran 50 x 30
cm dan disertai nomor contoh / nomor laboratorium.
3.1.2 Mengeringkan dan Menggiling Sampel Daun
Contoh daun yang sudah bersih didalam kantongan kelambu dikeringkan
didalam oven pengering pada suhu 60oC – 70oC terus menerus sampai contoh daun
menjadi kering dengan indikasi terasa rapuh bila diremas dengan tangan. Contoh daun
kering digiling dengan mesin giling listrik dengan menggunakan saringan kehalusan <
1 mm. Contoh daun yang telah halus kemudian dimasukkan kedalam mangkuk
plastik memakai tutup disertakan nomor contoh, kemudian contoh daun yang telah
halus dan sudah di beri nomor pada mangkuk plastik di masukkan kedalam botol kaca
secukupnya dengan penomoran yang sama dan kemudian siap untuk di analisa. Sisa
daun yang ada botol plastik keudian disusun kedalam rak – rak lemari penyimpanan,
3.2 Proses Analisa Sapel Daun
3.2.1 Destruksi Basah (H2SO4 + H2O2)
Prinsip
Bahan organik dapat didestruksi oleh peroksida dengan suhu yang relatif
rendah. Destruksi disempurnakan lebih lanjut oleh asam sulfat pekat pada suhu yang
lebih tinggi.
Bahan – bahan - H2SO4 (p)
- H2O2 30%
- Kertas saring whatman No 40
- Aquadest
Alat – alat
- Tabung reaksi 20 mL
- Timbangan analitik.
- Penangas listrik khusus untuk tabung reaksi ukuran 20 mL.
- Labu ukur 100 mL.
- Botol aquadest
- Corong plastik
1. Ditimbang 0,1 gr contoh kering mutlak 105oC, lalu dimasukkan kedalam
tabung reaksi 20 mL (apabila yang ditimbang adalah contoh kering udara,
maka dilakukan juga penimbangan untuk penetapan kadar air)
2. Ditambahkan 1 mL H2SO4 pekat dan 0,5 mL H2O2 30%, digoyang berlahan –
lahan, larutan contoh didestruksi menggunakan penangas listrik khusus untuk
tabung reaksi, suhu dinaikkan berlahan – lahan sampai dengan ± 160oC,
contoh akan menjadi agak lebih hitam dan agak berbuih. Bila larutan contoh
sudah tidak berbuih lagi, tabung diangkat dan didinginkan.
3. Setelah dingin kemudian ditambahkan 0,5 mL H2O2 30% dan didestruksi
kembali. Penambahan H2O2 30 % diulangi sampai larutan contoh menjadi
bening dan suhu disempurnakan pada suhu 280oC selama ± 15 menit sampai
sampel berwarna hitam. Kemudian ditambahkan dengan H2O2 30% kembali
dan di destruksi kembali sehingga terjadi perubahan berwarna bening. Tabung
reaksi diangkat dan didinginkan.
4. Larutan disaring kedalam labu ukur 100 mL sambil dibilas dengan air destilasi.
Penuhkan labu ukur 100 mL hingga garis batas.
5. Filtrat digunakan untuk penetapan N,P,K,Ca, dan Mg.
3.2.2 Penetapan Magnesium (Mg)
Prinsip
Contoh diuapkan dengan nyala api udara asetilen. Senyawa ,Mg mengalami
proses atomisasi dan penyerapan radiasi dari lampu katoda oleh atom – atom unsur
tersebut.
Bahan – bahan
- Larutan H2SO4 0,36 N
- 1 mL H2SO4(P) diencerkan dengan air destilasi hingga 100 mL
- Larutan standart baku Mg 1000 ppm
- Larutan standart 100 ppm Mg dalam H2O
Dipipet 10 ml larutan standart baku 1000 ppm Mg ke dalam labu ukur 100 ml,
kemudian ditarakan dengan menggunakan air destilat sampai tanda batas.
- Larutan seri standart 0-1-2-4-6-8-10 ppm Mg dalam H2SO4 0,36 N
dipipet 1 ml H2SO4(P) kedalam labu ukur 100 ml, lalu ditambahkan air destilat
± 30 ml, kemudian ditambahkan larutan seri standart 0-1-2-4-6-8-10 ppm
dalam H2O, kemudian ditarakan hingga garis tanda.
Alat – alat
- Atomic Absorption spectrophotometer (AAS), Perkin Elmen
- GBC Avanta ∑
Cara kerja
- Filtrat hasil destruksi contoh daun dalam H2SO4 p.a dan H2O2 30 % (destruksi
basah) langsung diukur dengan menggunakan Atomic absorption
spectrophotometer (AAS) yang mana sebelumnya alat dikalibrasi dengan
larutan seri standart (0-10) ppm larutan seri standart (0-10) ppm Mg dengan
C
3.3.1 Cara Penggunaan SSA
1. Isi buku pengendali penggunaan alat.
2. Hidupkan kompresor udara, tekanan 70 psi dan blower.
3. Buka gas acytilene ( tekanan minimal 70 psi), tekanan ke SSA 10 – 15 psi.
Ingat : gas dibuka hanya sesaat akan dinyalakan.
4. Periksa drainase trap harus berisi air dan tanki diisi air sekitar 1/3 dari
volume.
5. Power ON
6. Pasang lampu H.C yang dikehendaki
7. Sesuaikan atau pilih panjang gelombang, slit (0,2 atau 0,7) dan high atau
low.
8. Tekan param entry, param entry hidup.
8.1LAMP CUR (0.5 MA)
---(isikan, sesuai dengan kontinu masing – masing lampu)
8.2INT. TIME (0.5 – 60 sec)
---(isikan 1,2 atau 3 detik)
8.3REPLICATION (1-99)
---(isikan 1, 2 atau 3 detik)
8.4CAL : NON LIN (1), LIN (2) ADD (3)
8.5FLAME (1), PK AREA (2)
---(isikan pilih nomor 1 ,2 atau 3)
8.6STD : 1. ---), 2. ---),3. ---)
---( isikan konsentrasi masing – masing standar nomor 1,2 dan
seterusnya)
8.7RESLOPE (0,0001 – 99), salah satu dari nomor standar yang
diinginkan
9. Tekanan ENERGY. AA CTS : ... EN
9.1 atur kecepatan
9.1.1 Panjang gelombang s/d CTS... max.
9.1.2 Panjang lampu maju mundur s/d CTs ... max.
9.1.3 Posisi lampu vertikal s/d CTS ... max.
9.1.4 Posisi lampu horizontal s/d CTS ... max.
10.Tekan GAIN
11.Tekan CONTINOUS
12.Tekan DATA
12.1 Ukuran blanko sampel, tekan A/Z – 0,000
12.2 Calibrasi s. b. b.
- Tekanan konsentrasi STD 1, tekan Calib
- Tekanan konsentrasi STD 2, tekan Calib
- Tekanan konsentrasi STD 3, tekan Calib
13.Baca konsentrasi sampel s. b. b
1. Aspirasi H2O beberapa menit.
2. OFF-kan oxidant (nyala api mati)
3. Tekan “Param Entry” ketik 0 untuk Lamp cur.
4. Tutup gas acytiline. Bila menggunakan gas nitrous, maka gas nitrous
terlebih dahulu dimatikan.
5. Matikan kompresor udara.
6. Buang gas yang tersisa pada tubing – tubing selang.
7. Tutup tangki gas acytiline.
8. Putar tombol oxidant pada posisi AIR sampai Fuel-0
9. Putar tombol oxidant pasa posisi AIR sampai Oxidant-0
BAB IV
HASIL DAN PEMBAHASAN
4.1 HASIL
4.1.1 Hasil Analisa Magnesium (Mg) Daun Absorbansi Larutan Mg-standart
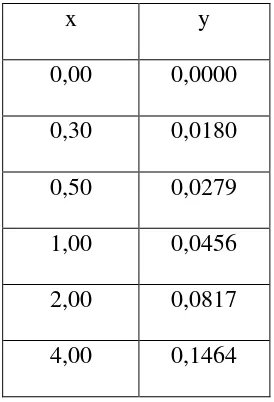
Tabel 4.1 Larutan Standart Mg
Keterangan : x = Konsentrasi (ppm)
y = Absorbansi
x y
0,00 0,0000
0,30 0,0180
0,50 0,0279
1,00 0,0456
2,00 0,0817
Penentuan garis regresi untuk kurva kalibrasi dapat diturunkan dari persamaan garis :
Y = ax + b
Dimana : a = Slop
b = Intersept
Selanjutnya harga Slope dapat ditentukan dengan menggunakan metode Least Squere
sebagai berikut :
∑
dengan menggunakan substansi hara – harga yang tercantum pada tabel 4.2 diatas
pada persanaan ini maka diperoleh :
- Untuk harga a (Slope)
10.168 0.35199 a=
= 0.0346
- Untuk harga b (intersept)
b = 0.0532 – 0.0346 (1,3)
= 0.0532 – 0.0426
= 0.008
4.1.2 Menghitung Konsentrasi Sampel
Dengan mensubstitusikan harga – harga x yang ada kedalam persamaan garis
regresi diatas maka diperoleh :
Unuk Nomor Lab 17
Untuk Nomor Lab 18
Slope
Untuk Nomor Lab 19
Slope
Slope
Untuk Nomor Lab 22
Slope
4.1.3. Penentuan Kadar Logam Magnesium Pada Daun Kelapa Sawit
C
Untuk Nomor Lab 17
0.01 x 1.777
Untuk Nomor Lab 18
Untuk Nomor Lab 19
0.1
Untuk Nomor Lab 20
0.1
Untuk Nomor Lab 22
4.2 Pembahasan
Unsur Magnesium (Mg) diserap oleh tanaman dalam bentuk Mg++, dimana
unsur hara Mg yang telah di analisa didalam Daun Kelapa Sawit diperoleh % Mg
sebesar :
o 0,18 % pada no Lab 17
o 0,22 % pada no Lab 18
o 0,15 % pada no Lab 19
o 0,32 % pada no Lab 20
o 0,24 % pada no Lab 21
o 0,20 % pada no Lab 22
Dari hasil analisa yang diperoleh, unsur Mg yang di analisa pada daun kelapa sawit,
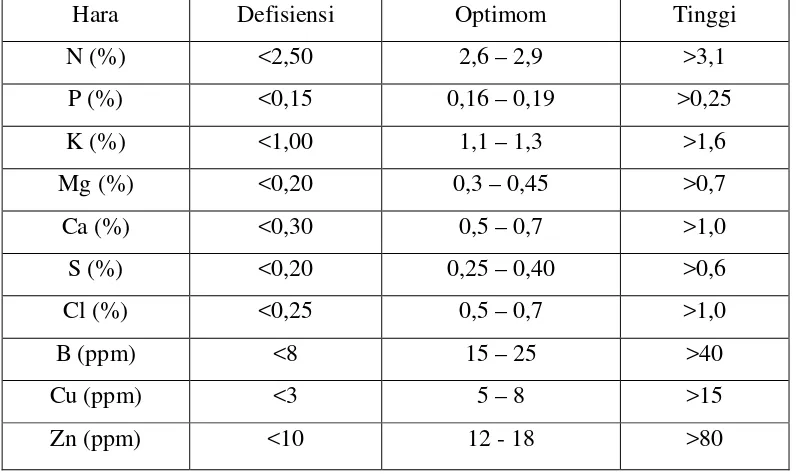
dapat dibandingkan dengan tabel kriteria hasil analisa sebagai berikut :
Tabel 4.2.1 Kadar Hara Daun Kelapa Sawit
Hara Defisiensi Optimom Tinggi
N (%) <2,50 2,6 – 2,9 >3,1
P (%) <0,15 0,16 – 0,19 >0,25
K (%) <1,00 1,1 – 1,3 >1,6
Mg (%) <0,20 0,3 – 0,45 >0,7
Ca (%) <0,30 0,5 – 0,7 >1,0
S (%) <0,20 0,25 – 0,40 >0,6
Cl (%) <0,25 0,5 – 0,7 >1,0
B (ppm) <8 15 – 25 >40
Cu (ppm) <3 5 – 8 >15
Jadi dari perbandingan hasil analisa dengan kriteria hasil analisa dapat
diperoleh hasil analisa daun pada Nomor Lab 17 dan 19 adalah sangat rendah, karena
tidak termasuk kedalam keriteria manapun.
Kekurangan unsur Mg dapat menyebabkan daun tampak kusam, tidak berkilat dan
pudar. Sehingga daun yang lebih tua dapat berubah warna menjadi hijau kuning
pudar, sedangkan bagian ujung dan tengah daun dekat tulang daun berwarna hijau
pucat.
Selanjutnya semua daun menjadi kuning pucat (klorosis berat), dan ujung – ujung
daun mengering mulai dari daun tua pembentukan daging buahnya tidak stabil . selain
itu juga pembentukan daging buahnya juga tidak akan berkembang, karena fungsi
utama Mg adalah membentuk pertumbuhan daging buah.
Sedangkan pada No Lab 18, 20, 21,22, 23 hasil analisa menunjukkan batas
defesiensi optimum unsur hara Mg, sehingga daun kelapa sawit pada nomor tersebut
termasuk kedalam golongan kelapa sawit yang subur dan sehat.
Karena fungsi dari Magnesium itu sendiri adalah sebagai penyusun klorofil,
dan sangat berperan dalam respirasi tanaman, dimana untuk membantu peningkatkan
cara kerja enzim dalam daun, sehingga menyebabkan tanaman Kelapa Sawit menjadi
BAB 5
KESIMPULAN DAN SARAN
5. 1 . Kesimpulan
Dari hasil analisa daun yang di lakukan dengan metode Spektrofotometer
Serapan Atom di pusat penelitian kelapa sawit (PPKS) Medan, di peroleh
kadar Mg sebesar :
o Sampel pada No. Lab 17 adalah sebesar 0,18 % kadar Mg dalam daun
Kelapa sawit, dan termasuk kriteria defisiensi.
o Sampel pada No. Lab 18 adalah sebesar 0,22 % kadar Mg dalam daun
kelapa sawit, dan memiliki kriteria defisiensi.
o Sampel pada No. Lab 19 adalah sebesar 0,15 % kadar Mg dalam daun
kelapa sawit, dan memiliki kriteria defisiensi
o Sampel pada No. Lab 20 adalah sebesar 0,32 % kadar Mg dalam daun
kelapa sawit, dan memiliki kriteria optimum.
o Sampel pada No. Lab 21 adalah sebesar 0,24 % kadar Mg dalam daun
kelapa sawit, dan memiliki kriteria defisiensi.
o Sampel pada No. Lab 22 adalah sebesar 0,20 % kadar Mg dalam daun
kelapa sawit, dan memiliki kriteria defisiensi.
5. 2. Saran
DAFTAR PUSTAKA
Anwar, N.2000. Instrumen AAS Dan Kimia Analis. Depertemen Perindustrian Dan
Perdagangan. Jakarta.
Anwar, M, dan Kosasih. 1972. Metode Analisa Daun. Balai Penelitian Perkebunan
Medan.
Baharuddin,A.R. 2005. Prosedur Analis Pengujian Kimia Daun Laboratorium Tanah
Dan Daun. PPKS Medan.
Fauzi, Y. 2002. Kelapa Sawit . Edisi Revisi. Penebar Swadaya. Jakarta.
di akses
tanggal 03 Maret 2012.
Purba, R. 2009. Penyakit – Penyakit Kelapa Sawit ( Elaesis guineensis jacq) Di
Indonesia. PPKS Medan.
Soeharjo, H. 1996. Bidang Tanaman Vadecium Kelapa Sawit. Pt. Perkebunan
LAMPIRAN I
KADAR HARA DAUN KELAPA SAWIT
Tanaman Sawit Muda (<6 Tahun ) Daun ke 17
Hara Defisiensi Optimom Tinggi
N (%) <2,50 2,6 – 2,9 >3,1
Sumber : Van Uexkull,H.R and Fairhurst,T.H(1991) IPI Bulletin 12. The OilPalm,
LAMPIRAN II Kurva LarutanStandar Mg
y = 0,0346x + 0,008 R² = 0,9938
0.0000 0.0200 0.0400 0.0600 0.0800 0.1000 0.1200 0.1400 0.1600
0.00 1.00 2.00 3.00 4.00 5.00
A
bs
orba
ns
i
LAMPIRAN III
Prosedur Kerja Analisa Mg Pada Daun
dimasukkan kedalam tabung reaksi
ditambahkan 1 mL H2SO4(P) dan 0.5 mL H2O2 30 %
didestruksi menggunakan penangas listrik khusus untuk
tabung reaksi
dinaikkan suhu berlahan – lahan sampai dengan ± 160oC
didinginkan
ditambahkan 1 mL H2SO4(p) dan didestruksi kembali
ditambahkan H2O2 30 %
didestruksi pada suhu 280oC selama ± 15 menit
diangkat dan didinginkan
disaring dengan kertas saring whatman No 40
diencerkan dengan air destilasi pada labu ukur
100 mL pada garis tanda
diukur absorbansinya dengan alat SSA pada panjang
gelombang 285,2 nm untuk analisa Mg 0.1 g Contoh DaunKering
Larutan
Larutan Bening
Filtrat Residu